Mivacron TM 10 mg Enjektabl Steril, apirojen
|
|
|
- Erdem Bilgili
- 7 yıl önce
- İzleme sayısı:
Transkript
1 Mivacron Enjektabl Mivacron TM Enjektabl Steril, apirojen Formülü Mivacron enjektabl, cam ampul içinde, berrak, soluk sarı, steril, sulu, 2mg/ml mivakuryuma eşdeğer mivakuryum klorür içeren bir çözeltidir. Her 5ml lik ampul 10mg mivakuryuma eşdeğerde mivakuryum klorür içerir. Yardımcı maddeler: ph ayarı için (ph= ) yeterli miktarda hidroklorik asit çözeltisi, 5ml ye tamamlanacak miktarda enjeksiyonluk su. Bu formülasyonda antimikrobiyal hiçbir koruyucu madde bulunmaz ve tek hastada kullanım için hazırlanmıştır. Farmakolojik Özellikleri Farmakodinamik özellikleri: Mivakuryum, kısa etki süreli, geriye dönüş profili hızlı, seçiciliği yüksek, non-depolarizan nöromüsküler blokerdir. Farmakokinetik özellikleri: Mivakuryum üç stereoizomerin bir karışımıdır. Transtrans ve cis-trans stereoizomerleri mivakuryum klorürün % sını oluşturur. Yapılan araştırmalarda bunların nöromüsküler blok oluşturma gücü birbirinden veya mivakuryum klorürünkinden önemli ölçüde farklı bulunmamıştır. Çalışmalarda cis-cis izomerinin nöromüsküler blok oluşturma gücünün, diğer iki stereoizomerin onda biri kadar olduğu hesaplanmıştır. Plazma kolinesterazıyla enzimatik hidroliz mivakuryumun inaktive edilmesi için primer mekanizmadır ve bir kuaterner alkol ve bir kuaterner monoester metabolit oluşur. Mivakuryumun nöromüsküler bloker aktivitesinin sonlanması esas olarak insan plazmasında yüksek seviyelerde bulunan plazma psödokolinesteraz ile hidrolizine bağlıdır. Mivakuryumun (örn. karaciğer esterazları ile hidroliz, safra içinde eliminasyon ve böbrek yoluyla atılım gibi) çeşitli eliminasyon yollarının olduğu görülmektedir. Endikasyonları Mivacron, genel anesteziye ek olarak iskelet kaslarını gevşetmek, trakeal entübasyonu sağlamak ve mekanik ventilasyonu kolaylaştırmak amacıyla uygulanır. Kontrendikasyonları Mivacron, mivakuryuma duyarlı olduğu bilinen hastalara uygulanmamalıdır. Mivacron atipik plazma kolinesteraz için homozigot olduğu bilinen hastalarda kontrendikedir (Uyarılar/Önlemler e bakınız). Uyarılar/Önlemler Bütün diğer nöromüsküler blokerleri gibi, Mivacron da diğer iskelet kasları ile birlikte solunum kaslarında da felç oluşturur, ancak şuur üzerinde herhangi bir etkisi yoktur. Mivacron, sadece uygun genel anestezi ile birlikte ve deneyimli bir anestezist tarafından veya onun yakın denetimi altında, endotrakeal entübasyon ve yapay solunum için uygun olanakların mevcudiyetinde uygulanmalıdır. Atipik plazma kolinesteraz geni için homozigot olan hastalar (2500 hastada 1 hasta) süksametonyum/süksinilkoline olduğu gibi mivakuryumun TM: Mivacron GlaxoSmithKline şirketler grubunun tescilli markasıdır. W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 1KUBLER\PROSPEKTÜS\WORD\Mivacron
2 Mivacron Enjektabl nöromüsküler bloke edici etkisine de fazla duyarlıdırlar. Böyle üç hastada 0.03mg/kg lık küçük bir Mivacron dozu (genotipik bakımdan normal hastalarda yaklaşık ED10-20) dakikalık tam nöromüsküler blok oluşturmuştur. Bu hastalarda bir kez spontan düzelme başladığında nöromüsküler blok neostigminin konvansiyonel dozlarıyla antagonize edilmiştir. Histamine duyarlılığı akla getiren bazı durumlarda (örn. astımlılar gibi) Mivacron uygulanmasında dikkatli olunmalıdır. Bu gruptaki hastalarda Mivacron kullanılırsa uygulama süresi 60 saniye olmalıdır. Hipovolemik hastalar gibi arteriyel kan basıncı düşmelerine fazla duyarlı hastalarda Mivacron 60 saniyelik bir sürede uygulanmalıdır. Yetişkinlerde, Mivacron > 0.2mg/kg (> 3xED 95 ) dozlarında hızlı bolus enjeksiyon şeklinde verildiğinde histamin salıverilmesi olabilir. Ancak, 0.2mg/kg Mivacron un daha yavaş uygulanması ve 0.25mg/kg Mivacron dozunun bölünmüş dozlarda verilmesi (Bkz. Kullanım Şekli ve Dozu) bu dozlardaki kardiyovasküler etkileri en aza indirir. Klinik çalışmalarda 0.2mg/kg lık hızlı bolus doz ile çocuklarda kardiyovasküler güvenilirliğin tehlikeye girdiği görülmemiştir. Önerilen dozlarda Mivacron önemli vagal veya ganglion bloke edici özellikler göstermez. Önerilen dozlarda Mivacron un kalp atış hızı üzerinde önemli hiçbir etkisi yoktur ve birçok anestezik ilaç veya ameliyat sırasında vagal stimülasyonla meydana gelen bradikardiye karşı etkili olmaz. Diğer non-depolarizan nöromüsküler blokerlerle olduğu gibi miyastenia gravis hastalarında, diğer nöromüsküler hastalıkları olan hastalarda ve kaşektik hastalarda mivakuryuma karşı duyarlılığın artması beklenebilir. Ciddi asit-baz veya elektrolit anormallikleri, mivakuryuma duyarlılığı artırabilir veya azaltabilir. Mivacron solüsyonu asidiktir (ph yaklaşık 4.5) ve yüksek alkali solüsyonlarla (Örn. barbiturat solüsyonları) aynı enjektörde karıştırılmamalı veya aynı iğneden birlikte uygulanmamalıdır. Yaygın şekilde kullanılan bazı asidik perioperatif solüsyonlarla (Örn. fentanil, alfentanil, sufentanil, droperidol ve midazolam) geçimli olduğu gösterilmiştir. Mivacron için kullanılan yerleşik iğne veya kanül diğer anestezik ajanların uygulanması için kullanılacaksa ve geçimlilikleri kanıtlanmamışsa her ilacın serum fizyolojik ile tamamen yıkanması önerilir. Yanıklı hastalarda non-depolarizan nöromüsküler blokerlere direnç gelişebilir ve nöromüsküler bloker dozunun artırılması gerekebilir. Bununla beraber, bu hastalarda dozun azaltılmasını gerektiren plazma kolinesteraz aktivitesi düşüklüğü de olabilir. Bu nedenle, yanıklı hastalara mg/kg lık bir Mivacron test dozunun arkasından bir periferik sinir stimulanıyla blokun izlenmesine göre ayarlanan uygun dozlama yapılır. Mivacron, malign hipertermiye duyarlı insanlarda araştırılmamıştır. Nöromusküler bloğun geri dönmesi: Diğer nöromusküler bloker ajanlarda olduğu gibi geri döndürücü bir ajanın (neostigmin gibi) verilmesinden önce spontan düzelme belirtileri gözlenmelidir. Nöromuskuler bloğun geri dönüşünü değerlendirmek için, öncesinde ve düzelmeyi takiben periferik sinir stimülasyonu kullanılması kuvvetle önerilmektedir. Yoğun bakım ünitesinde mekanik ventilasyon uygulanan hastalarda Mivacron un uzun süreli kullanımı üzerinde veri mevcut değildir. Gebelik ve emzirme döneminde kullanımı: Gebelik Kategorisi : C. Gebelik sırasında plazma kolin esteraz düzeyleri azalır. Mivacron sezaryende nöromüsküler blokajı sürdürmek için kullanılmıştır. Fakat plazma kolin esteraz W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 2KUBLER\PROSPEKTÜS\WORD\Mivacron
3 Mivacron Enjektabl düzeylerindeki azalma nedeniyle infüzyon hızında doz ayarlaması gerekmiştir. Sezaryen sırasında önceden MgSO 4 ile tedavi edilen hastalarda Mg un potansiyalize edici etkisi nedeniyle infüzyon hızında daha da azaltma gerekebilir. Mivacron gebelikte anneye sağlaması beklenen potansiyel yararları fetüs üzerinde olası risklerinden fazla ise kullanılabilir. Sezaryen sırasında Mivacron kullanımıyla ilgili bir tecrübe yoktur. Mivakuryumun anne sütüyle atılıp atılmadığı bilinmemektedir. Araç ve makine kullanımı üzerine etkisi: Bildirilmemiştir. Yan Etkiler/Advers Etkiler Mivacron uygulaması ile ilgili olarak deride kızarıklık, eritem, ürtiker, hafif geçici hipotansiyon, geçici taşikardi veya bronkospazm görüldüğü bildirilmiş ve bu histamin serbestlenmesine bağlanmıştır. Bu etkiler doza bağlıdır ve 0.2mg/kg veya daha yüksek başlangıç dozları hızlı verildiğinde daha sık görülür. Eğer Mivacron saniyede verilirse veya 30 saniyede bölünmüş dozlarda verilirse bu etkiler azalır. Mivacron u bir ya da daha fazla anestezik ajanla birlikte kullanan hastalarda çok nadir olarak ciddi anafilaksi veya anafilaktoid reaksiyonlar rapor edilmiştir. İlaç Etkileşmeleri Mivakuryum tarafından oluşturulan nöromüsküler blok, enfluran, izofluran ve halotan gibi inhalasyon anestezikleriyle birlikte verildiğinde uzatılabilir. Mivacron, süksametonyumla kolaylaştırılan trakeal entübasyon sonrasında emniyetli şekilde uygulanmıştır. Mivacron uygulamasından önce süksametonyumdan spontan düzelme görüldüğü mutlaka gözlenmelidir. Bütün non-depolarizan nöromüsküler blokerlerle olduğu gibi non-depolarizan nöromüsküler blokun şiddet ve/veya süresi aşağıdakilerle etkileşim nedeniyle artabilir ve infüzyon gereksinimleri azalabilir: Antibiyotikler: Anti-aritmik ilaçlar: Diüretikler: Magnezyum tuzları Ketamin Lityum tuzları Ganglion blokeri ilaçlar: Aminoglikozidler, polimiksinler, spektinomisin, tetrasiklinler, linkomisin ve klindamisin Propranolol, kalsiyum kanal blokerleri, lignokain, prokainamid ve kinidin Frusemid ve muhtemelen tiazidler, mannitol ve asetazolamid Trimetafan, heksametonyum Plazma kolinesteraz aktivitesini azaltabilen ilaçlar aynı zamanda Mivacron un nöromüsküler bloker aktivitesini de uzatabilir. Bu ilaçlar arasında antimitotik ilaçlar, monoamin oksidaz inhibitörleri, ekotiyopat iyodür, pankuronyum, organofosfatlar, antikolinesterazlar, bazı hormonlar, bambuterol bulunur. Nadiren bazı ilaçlar miyastenia gravisi şiddetlendirebilir veya gizli miyastenia gravisi ortaya çıkarabilir veya gerçekten bir miyastenik sendromu endükleyebilir; böyle bir gelişme sonrasında Mivacron a karşı artmış duyarlılık görülebilir. Bu gibi ilaçların arasında antibiyotikler, beta-blokerler (propranolol, osprenolol), antiaritmik ilaçlar (prokainamid, kinidin), anti-romatizmal ilaçlar (klorokin, D-penisilamin), trimetafan, klorpromazin, steroidler, fenitoin ve lityum bulunur. Mivacron diğer non depolarizan nöromusküler blokerlerle kombinasyon halinde verildiğinde, W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 3KUBLER\PROSPEKTÜS\WORD\Mivacron
4 Mivacron Enjektabl nöromusküler blokaj etkisinde artma görülür. Bu artış, mivacron un total dozundan beklenen etki gücünden daha fazladır. Değişik ilaç kombinasyonlarında bu sinerjik etki çeşitlilik gösterir. Süksametonyum klorür gibi depolarizan bir kas gevşeticinin birlikte uygulanması uzun ve antikolinesteraz ilaçlarla tersine çevrilmesi güç, kompleks bir bloğa neden olabileceği için non-depolarizan nöromüsküler blokerlerin nöromüsküler blok etkilerini uzatmak için bu gibi depolarizan kas gevşetici ilaçlar uygulanmamalıdır. Kullanım Şekli ve Dozu Erişkinler: Enjeksiyon şeklinde: Mivacron intravenöz enjeksiyon yoluyla uygulanır. Narkotik anestezi uygulanan erişkinlerde ulnar sinir stimülasyonuna adductor pollicis tek seğirme cevabında %95 supresyon (ED95) meydana getirecek ortalama doz 0.07mg/kg dır ( mg/kg). Trakeal entübasyon için aşağıdaki dozlar önerilir: I. 0.2mg/kg lık bir doz, 30 saniyede verildiğinde, dakikada trakeal entübasyon için iyi veya mükemmel koşulları sağlar. II. 0.25mg/kg lık bir doz, bölünmüş dozlar şeklinde verildiğinde (0.15mg/kg takiben 30 saniye sonra 0.1mg/kg), ilk doz kısmının verilmesinin bitişini takiben dakika içinde trakeal entübasyon için iyi veya mükemmel koşulları sağlar. Sağlıklı yetişkinlerde önerilen bolus dozu mg/kg dır. Nöromüsküler blok süresi doza bağlıdır. 0.07, 0.15, 0.20 ve 0.25mg/kg lık dozlar sırasıyla yaklaşık 13, 16, 20 ve 23 dakika süreyle, klinik olarak etkili blok sağlar. 0.15mg/kg a kadar olan dozlar 5-15 saniyede verilebilir. Daha yüksek dozlar, kardiyovasküler etkilerin oluşma olasılığını en aza indirmek için 30 saniyenin üzerinde verilmelidir. Tam blok süresi Mivacron un idame dozlarıyla uzatılabilir. Narkotik anestezi sırasında uygulanan 0.1mg/kg lık dozların her biri yaklaşık 15 dakikalık ilave klinik olarak etkili blok etkisi sağlar. Ardarda uygulanan ek dozlar nöromüsküler blok etkisinde birikmeye neden olmaz. Mivakuryumun nöromüsküler bloker etkisi izofluran veya enfluran anestezisiyle kuvvetlendirilir. İzofluran veya enfluran ile kararlı durum anestezisi sağlanmışsa önerilen Mivacron başlangıç dozu %25 azaltılmalıdır. Halotan mivakuryumun etkisini sadece minimum ölçüde kuvvetlendirdiği için dozda herhangi bir azaltma gerekli olmayabilir. Spontan düzelme bir kez başlayınca yaklaşık 15 dakikada tamamlanır ve uygulanan doza bağlı değildir. Mivakuryumla oluşturulan nöromüsküler blok, antikolinesteraz ajanların standart dozlarıyla geriye çevrilebilir. Bununla beraber, mivakuryum sonrasında düzelme hızlı olduğu ve geriye çevrilme (düzelme) süresini sadece 5-6 dakika kısalttığı için rutin olarak antikolinesteraz ilaçlar gerekli olmayabilir. Mivacron kesinlikle intramüsküler uygulanmamalıdır. BU İLAÇ SADECE HASTANEDE VE BİR ANESTEZİ UZMANI DENETİMİNDE KULLANILMALIDIR. İnfüzyon şeklinde: Nöromüsküler bloğun idame ettirilmesi için sürekli Mivacron infüzyonu uygulanabilir. Başlangıç Mivacron dozundan sonra erken bir spontan düzelme belirtisinde 8-10 mikrogram/kg/dak. lık ( mg/kg/saat) bir infüzyon hızı önerilir. Başlangıç infüzyon hızı, hastanın periferik sinir stimülasyonuna cevabı ve klinik kriterlere göre ayarlanmalıdır. İnfüzyon hızı ayarlamaları yaklaşık 1mcg/kg/dak lık (0.06mg/kg/saat) artışlarla yapılmalıdır. Genellikle, bir hız değişikliği yapılmadan önce belli bir hız en az 3 dakika idame ettirilmelidir. Narkotik anestezi uygulanan erişkinlerde ortalama olarak 6-7mcg/kg/dak lık bir infüzyon hızı, uzatılan anestezi sürelerinde nöromüsküler bloğu %89-99 aralığında idame W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 4KUBLER\PROSPEKTÜS\WORD\Mivacron
5 Mivacron Enjektabl ettirecektir. Kararlı durum izofluran veya enfluran anestezisi sırasında infüzyon hızının %40 kadar düşürülmesi düşünülmelidir. Halotan anestezisinde infüzyon hızında daha küçük azaltmalar gerekebilir. Yapılan bir çalışmada sevofluran ile birlikte Mivacron verildiğinde, Mivacron infüzyon hızında %50 ye kadar azaltma gerektiği gösterilmiştir. Mivacron infüzyonundan sonra spontan düzelme infüzyon süresine bağımlı değildir ve tek doz uygulaması sonrasında bildirilen düzelme ile karşılaştırılabilir. Mivacron un sürekli infüzyonuna bağlı olarak taşiflaksi veya kümülatif nöromüsküler blok gelişimi görülmemektedir. Enjeksiyonluk Mivacron (2mg/ml) infüzyon için seyreltilmeden kullanılabilir. Enjeksiyonluk Mivacron aşağıdaki infüzyon sıvılarıyla geçimlidir: Sodyum Klorür İntravenöz İnfüzyon (%0.9 a/h) Glukoz İntravenöz İnfüzyon (%5 a/h) Sodyum Klorür (%0.18 a/h) ve Glukoz (%4 a/h) İntravenöz İnfüzyon Laktatlı Ringer Solüsyonu, USP Yukarıdaki infüzyon solüsyonlarıyla 1 e 3 oranıyla (Örn. 0.5mg/ml elde edilecek şekilde) seyreltildiğinde Mivacron enjeksiyonun 30 o C de en az 48 saat kimyasal ve fiziksel olarak stabil kaldığı gösterilmiştir. Bununla beraber ürün hiçbir antimikrobiyal koruyucu madde içermediği için seyreltme hemen kullanım öncesinde yapılmalı ve uygulamaya mümkün olduğu kadar erken başlanmalı ve artan solüsyon atılmalıdır. 7 ay-12 yaş arası çocuklarda doz: Mivacron un yetişkinlere nazaran 7 ay-12 yaş bebek ve çocuklarda ED 95 değeri daha yüksek (yaklaşık 0.1mg/kg), etkinin başlaması hızlı, klinik etkinlik olarak etki süresi daha kısa ve spontan düzelme daha hızlıdır. Önerilen bolus dozu 7 ay-12 yaş arası bebek ve çocuklarda 5-15 saniyede uygulanan mg/kg dır. Stabil narkotik ve halotan anestezisi altında uygulandığında 0.2mg/kg ortalama 9 dakika içinde klinik olarak etkin blok oluşturur. 7 ay - 12 yaş arası bebek ve çocuklarda trakeal entübasyon için 0.2mg/kg lık Mivacron dozu önerilir. Bu dozun uygulanmasından 2 dakika sonra maksimum bloğa ulaşılır ve bu süre içinde entübasyon yapılması mümkün olabilir. Çocuklarda ve bebeklerde genellikle erişkinlerde olduğundan daha sık idame dozları gereklidir. Mevcut veriler 0.1mg/kg lık idame dozlarının narkotik veya halotan anestezisi sırasında yaklaşık 6-9 dakikalık, klinik olarak etkili ek blok sağlayabileceğini göstermektedir. Çocuklarda ve bebeklerde genellikle erişkinlerdekinden daha yüksek infüzyon hızları gerekir. Halotan anestezisi sırasında 7-23 aylık hastalarda %89-99 nöromüsküler bloğun idame ettirilmesi için gereken infüzyon hızı ortalama 11mcg/kg/dakikadır (Yaklaşık 0.7mg/kg/saat) [Yayılım 3-26 mcg/kg/dakika (yaklaşık mg/kg/saat)] yaşındaki çocuklarda halotan veya narkotik anestezi altında eşdeğer ortalama infüzyon hızı 13-14mcg/kg/dakikadır (yaklaşık 0.8mg/kg/saat) [yayılım 5-31mcg/kg/dakika (yaklaşık mg/kg/saat)]. Mivacron un nöromusküler bloker etkisi inhalasyon ajanlarla kuvvetlendirilir. Yapılan bir çalışmada 2-12 yaş arasındaki çocuklarda sevofluran ile kullanıldığında infüzyon hızında %70 kadar azaltma gerektiği gösterilmiştir. Spontan düzelme bir kez başlayınca yaklaşık 10 dakikada tamamlanır. W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 5KUBLER\PROSPEKTÜS\WORD\Mivacron
6 Mivacron Enjektabl 2-6 aylık bebeklerde dozaj: 2-6 aylık bebeklerde Mivacron ED 95 değeri yetişkinlerdekine benzer (0.07mg/kg), fakat etki başlaması daha hızlıdır ve klinik olarak etkili süre daha kısadır ve spontan düzelme daha hızlıdır. Önerilen bolus doz yayılımı 2-6 aylık bebek ve çocuklarda 5-15 saniyede uygulanan mg/kg dır. Stabil halotan anestezisi sırasında uygulandığında 0.15mg/kg lık doz ortalama 9 dakikalık klinik olarak etkili blok oluşturur. 2-5 aylık bebeklerde intratrakeal entübasyon için 0.15mg/kg lık bir Mivacron dozu önerilir. Bu dozun uygulanmasını takiben yaklaşık 1.4 dakikada maksimum bloka ulaşılır ve bu süre için entübasyon mümkün olabilir. 2-6 aylık bebeklerde yetişkinlere nazaran daha sık idame dozları gerekebilir. Mevcut veriler, halotan anestezisi sırasında 0.1mg/kg lık bir idame dozunun yaklaşık 7 dakikalık ilave klinik olarak etkili blok vereceğini göstermektedir. 2-6 aylık bebeklerde genellikle erişkinlerden daha yüksek infüzyon hızları gerekir. Halotan anestezisi sırasında %89-99 nöromüsküler blok için gerekli ortalama infüzyon hızı 11 mcg/kg/dakikadır (yaklaşık olarak 0.7 mg/kg/saat(yayılım 4-24 mcg/kg/dakika-yaklaşık mg/kg/saat). Spontan düzelme bir kez başlayınca, yaklaşık 10 dakikada tamamlanır. Neonatlar ve 2 ayın altındaki bebeklerde doz: Yeterli klinik bilgi elde edilinceye kadar neonatlar ve 2 ayın altındaki bebeklerde herhangi bir doz önerilmemektedir. Yaşlı hastalar: Mivacron un tek bolus dozları uygulanan yaşlı hastalarda etki başlangıç süresi, etkinin devam süresi ve düzelme hızı genç hastalara nazaran %20-%30 daha uzayabilir. Yaşlı hastalarda infüzyon hızının azaltılması veya daha küçük veya daha seyrek uygulanan idame bolus dozları gerekebilir. Kardiyovasküler rahatsızlığı olanlar: Klinik bakımdan önemli kardiyovasküler hastalığı olan hastalarda Mivacron un başlangıç dozu 60 saniye içinde uygulanmalıdır. Bu şekilde Mivacron, kalp cerrahisi uygulanmakta olan hastalara minimal hemodinamik etkiyle uygulanmaktadır. Böbrek fonksiyonu azalmış hastalar: Son dönem böbrek yetersizliği görülen hastalarda 0.15mg/kg lık dozla meydana gelen klinik etkili blok süresi böbrek fonksiyonu normal olan hastalara nazaran yaklaşık 1.5 kez daha uzundur. Bu nedenle doz hastaların bireysel klinik cevaplarına göre ayarlanmalıdır. Hepatik fonksiyonu azalmış hastalar: Son dönem hepatik yetersizlik görülen hastalarda 0.15mg/kg lık dozla meydana gelen klinik etkili blok süresi hepatik fonksiyonu normal olan hastalara nazaran yaklaşık 3 kez daha uzundur. Bu uzama bu hastalarda görülen azalmış plazma kolinesteraz aktivitesine bağlıdır. Bu nedenle doz hastaların bireysel klinik cevaplarına göre ayarlanmalıdır. Plazma kolinesteraz aktivitesi azalmış hastalar: Mivakuryum, plazma kolinesterazı tarafından metabolize edilir. Plazma kolinesteraz aktivitesi, plazma kolinesterazın genetik anormallikleri mevcudiyetinde (örn., atipik plazma kolinesteraz geni için heterozigot veya homozigot hastalarda) ve çeşitli patolojik durumlarda (Bkz. Kullanım Şekli ve Dozu: Hepatik fonksiyonu azalmış hastalarda doz) ve bazı ilaçlarla birlikte uygulanması (Bkz. İlaç Etkileşmeleri) durumunda azalabilir. Plazma kolinesteraz aktivitesi azalmış hastalarda Mivacron uygulamasını takiben nöromüsküler blokta uzama gözönüne alınmalıdır. Plazma kolinesteraz aktivitesinde hafif azalmalara (Örn. normal aralığın alt limitinin %20 si içinde) bağlı olarak etki süresinde klinik önemi olan etkiler görülmez. Atipik plazma kolinesteraz geni için heterozigot hastalarda 0.15 mg/kg lık Mivacron la sağlanan klinik bakımdan etkili blok süresi kontrol grubu hastalara göre yaklaşık 10 dakika daha uzundur. W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 6KUBLER\PROSPEKTÜS\WORD\Mivacron
7 Mivacron Enjektabl Şişman hastalar: Obez hastalarda (boylarına göre ideal vücut ağırlıkları %30 veya daha fazla olanlar) Mivacron başlangıç dozu için gerçek ağırlık değil ideal ağırlık esas alınmalıdır. İzleme: Tüm nöromüsküler blokerlerde olduğu gibi, Mivacron uygulaması sırasında bireysel doz ihtiyacını belirlemek için nöromüsküler fonksiyonun izlenmesi önerilir. Mivacron ile başlangıç sırasında anlamlı bir dörtlü uyarının sönmesi (trainof-four-fade) görülmez. Genellikle, adductor pollicis kasının dörtlü uyarı cevabı (train-of-four-response) tamamen kalkmadan trakeanın entübasyonu mümkündür. Aşırı Dozaj Bulgular: Uzun süreli kas paralizisi ve buna bağlı olarak görülen olaylar nöromüsküler blokerler için temel doz aşımı bulgularıdır. Bununla beraber, özellikle kan basıncının düşmesi olmak üzere hemodinamik yan etkiler riski de artabilir. Tedavi: Spontan solunum yeterli olana kadar hava yolunun açık tutulması ve pozitif basınçlı ventilasyon uygulanması zorunludur. Bilinç yerinde olduğu için tam sedasyon gerekir. Düzelme, spontan düzelme bulgularının görülmesi üzerine atropin veya glikopirolat ile birlikte antikolinesteraz ilaçların uygulanmasıyla hızlandırılabilir. Hastanın pozisyonunun uygun şekilde ayarlanması ve sıvı uygulanması veya gereğine göre, vazopresör ilaçların uygulanmasıyla kardiyovasküler destek sağlanabilir. Farmasötik Önlemler ve Saklama Koşulları 25 C nin altındaki oda sıcaklığında saklayınız. Işıktan koruyunuz. Dondurmayınız. Hiçbir koruyucu madde içermediği için Mivacron tam aseptik koşullarda kullanılmalı ve seyreltme hemen kullanım öncesinde yapılmalıdır. Açık ampullerde kalan kullanılmamış solüsyon atılmalıdır. Mivacron enjeksiyonun, asidik solüsyonlar şeklinde yaygın şekilde kullanılan peri-operatif ilaçlarla geçimli olduğu kanıtlanmıştır. Bu gibi ilaçlar Mivacron için kullanılan yerleşik iğne veya kanülle uygulanacaksa ve geçimlilikleri kanıtlanmamışsa her ilacın serum fizyolojik ile tamamen yıkanması önerilir. Ticari Takdim Şekli ve Ambalaj Muhtevası Mivacron 10mg enjektabl, 5ml lik 5 adet ampul içeren karton kutularda satılmaktadır. Piyasada Mevcut Diğer Farmasötik Dozaj Şekilleri Mivacron 20mg enjektabl, 10ml, 5 adet ampul. Ruhsat Sahibinin İsim ve Adresi: GlaxoSmithKline İlaçları San. ve Tic. A.Ş., Levent - İstanbul. Ruhsat Tarih ve Numarası: /92 Üretim Yeri İsim ve Adresi: GlaxoSmithKline S.p.A, İtalya. Reçete ile satılır. W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 7KUBLER\PROSPEKTÜS\WORD\Mivacron
8 Mivacron Enjektabl GlaxoSmithKline İlaçları Sanayi ve Ticaret A.Ş. 06/ /06/C AMPUL AÇMA TALİMATLARI Ampuller OPC (Tek Kırma Noktası) açma sistemi ile donatılmışlardır ve aşağıdaki talimatlar doğrultusunda açılmalıdırlar : Ampul, Şekil 1 de gösterildiği gibi alt kısmından tutulur Şekil 2 de gösterildiği gibi diğer elinizin başparmağı ampuldeki renkli noktaya bastırılır. Şekil 1 Şekil 2 W:\RegulatoryAffairs\SON ONAYLI PROSPEKTUS VE 8KUBLER\PROSPEKTÜS\WORD\Mivacron
Tracrium 25 mg Steril Ampul IV
 Tracrium TM 25 mg Steril Ampul i.v. Formülü Bir ampul 25 mg (10 mg/ml) atrakuryum besilat içerir. Tracrium, berrak cam ampul içinde soluk sarı, steril bir solüsyondur. Yardımcı maddeler: ph ayarı için
Tracrium TM 25 mg Steril Ampul i.v. Formülü Bir ampul 25 mg (10 mg/ml) atrakuryum besilat içerir. Tracrium, berrak cam ampul içinde soluk sarı, steril bir solüsyondur. Yardımcı maddeler: ph ayarı için
K U L L A N M A T A L İ M A T I
 K U L L A N M A T A L İ M A T I TRACRİUM TM 50 mg steril ampul i.v. Damar içine uygulanır. Etkin madde: 50 mg atrakuryum besilat içerir. Yardımcı maddeler: ph ayarı için benzen sülfonik asit çözeltisi,
K U L L A N M A T A L İ M A T I TRACRİUM TM 50 mg steril ampul i.v. Damar içine uygulanır. Etkin madde: 50 mg atrakuryum besilat içerir. Yardımcı maddeler: ph ayarı için benzen sülfonik asit çözeltisi,
KULLANMA TALİMATI NEUCURİUM
 KULLANMA TALİMATI NEUCURİUM 50mg/5mL İ.V. İnfüzyon ve Enjeksiyon İçin Çözelti İçeren Ampul Damar içine uygulanır. Etkin madde: 50 mg atrakuryum besilat içerir. Yardımcı madde(ler): Benzensülfonik asit
KULLANMA TALİMATI NEUCURİUM 50mg/5mL İ.V. İnfüzyon ve Enjeksiyon İçin Çözelti İçeren Ampul Damar içine uygulanır. Etkin madde: 50 mg atrakuryum besilat içerir. Yardımcı madde(ler): Benzensülfonik asit
KULLANMA T A L İ M A T I. ATRASYL 25 mg/2.5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul Damar içine uygulanır.
 KULLANMA T A L İ M A T I ATRASYL 25 mg/2.5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul Damar içine uygulanır. Etkin madde: 25 mg atrakuryum besilat içerir. Yardımcı maddeler: ph ayarı için
KULLANMA T A L İ M A T I ATRASYL 25 mg/2.5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul Damar içine uygulanır. Etkin madde: 25 mg atrakuryum besilat içerir. Yardımcı maddeler: ph ayarı için
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TRACRİUM TM 50 mg steril ampul i.v.
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TRACRİUM TM 50 mg steril ampul i.v. 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Bir ampulde; Atrakuryum besilat 50 mg (10 mg/ml) Yardımcı maddeler: Yardımcı
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TRACRİUM TM 50 mg steril ampul i.v. 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Bir ampulde; Atrakuryum besilat 50 mg (10 mg/ml) Yardımcı maddeler: Yardımcı
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ATRASYL 50 mg/5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ATRASYL 50 mg/5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Bir ampulde; Atrakuryum besilat 50
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ATRASYL 50 mg/5 ml i.v. enjeksiyon ve infüzyon için çözelti içeren ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Bir ampulde; Atrakuryum besilat 50
Dematrac (Atrakuryum besilat) 25mg 2,5ml 10 ampul FORMÜL
 Dematrac (Atrakuryum besilat) 25mg 2,5ml 10 ampul FORMÜL Bir ampul, 2.5 ml enjeksiyon solüsyonunda 25 mg atrakuryum besilat içerir. Yardımcı madde olarak; ph ayarı için benzensülfonik asit ve enjeksiyonluk
Dematrac (Atrakuryum besilat) 25mg 2,5ml 10 ampul FORMÜL Bir ampul, 2.5 ml enjeksiyon solüsyonunda 25 mg atrakuryum besilat içerir. Yardımcı madde olarak; ph ayarı için benzensülfonik asit ve enjeksiyonluk
K U L L A N M A T A L Đ M A T I
 K U L L A N M A T A L Đ M A T I MIVACRON 20 mg Enjektabl Damar içine uygulanır. Etkin madde: Her ampulde, 20 mg mivakuryuma eşdeğer mivakuryum klorür içerir. Yardımcı maddeler: ph ayarı için yeterli miktarda
K U L L A N M A T A L Đ M A T I MIVACRON 20 mg Enjektabl Damar içine uygulanır. Etkin madde: Her ampulde, 20 mg mivakuryuma eşdeğer mivakuryum klorür içerir. Yardımcı maddeler: ph ayarı için yeterli miktarda
KISA ÜRÜN BİLGİSİ. Etkin madde: 1 ampul 1 ml içinde 4 mg veküronyum bromür olacak şekilde 4 mg veküronyum bromür içerir.
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI KISA ÜRÜN BİLGİSİ NORCURON 4 mg IV liyofilize toz içeren ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 1 ampul 1 ml içinde 4 mg veküronyum bromür olacak şekilde 4 mg
1. BEŞERİ TIBBİ ÜRÜNÜN ADI KISA ÜRÜN BİLGİSİ NORCURON 4 mg IV liyofilize toz içeren ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 1 ampul 1 ml içinde 4 mg veküronyum bromür olacak şekilde 4 mg
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI SERUM FİZYOLOJİK İZOTONİK % 0.9 5 ml Ampul Damar içine uygulanır. - Etkin madde: 1 ml si 9 mg sodyum klorür içerir. - Yardımcı madde (ler): Enjeksiyonluk su. Bu ilacı kullanmaya başlamadan
KULLANMA TALİMATI SERUM FİZYOLOJİK İZOTONİK % 0.9 5 ml Ampul Damar içine uygulanır. - Etkin madde: 1 ml si 9 mg sodyum klorür içerir. - Yardımcı madde (ler): Enjeksiyonluk su. Bu ilacı kullanmaya başlamadan
KULLANMA TALİMATI. RESCUE FLOW 250 ml enfüzyon çözeltisi Damar içine uygulanır.
 RESCUE FLOW 250 ml enfüzyon çözeltisi Damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her 1000 ml çözelti; 60 g enjeksiyonluk dekstran 70, 75 g sodyum klorür içerir. Yardımcı maddeler: Hidroklorik
RESCUE FLOW 250 ml enfüzyon çözeltisi Damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her 1000 ml çözelti; 60 g enjeksiyonluk dekstran 70, 75 g sodyum klorür içerir. Yardımcı maddeler: Hidroklorik
KULLANMA TALİMATI. ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır.
 KULLANMA TALİMATI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
KULLANMA TALİMATI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
KULLANMA TALİMATI. DONA, kutuda 6 adet 2 ml lik kahverengi ampul (A) ve 6 adet 1 ml lik şeffaf ampul (B) den oluşmaktadır.
 KULLANMA TALİMATI DONA 400 mg ampul Kas içine uygulanır. Etkin Madde: Her bir 2 ml lik kahverengi ampulde kristalize glukozamin sülfat 502.5 mg (Glukozamin sülfat 400.0 mg Sodyum klorür 102.5 mg a eşdeğer.)
KULLANMA TALİMATI DONA 400 mg ampul Kas içine uygulanır. Etkin Madde: Her bir 2 ml lik kahverengi ampulde kristalize glukozamin sülfat 502.5 mg (Glukozamin sülfat 400.0 mg Sodyum klorür 102.5 mg a eşdeğer.)
Kas Gevşeticiler ve Etki Mekanizmaları. Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O.
 Kas Gevşeticiler ve Etki Mekanizmaları Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O. Kas Gevşeticiler N ö r o m u s k u l e r b l o k e r l e r diye de isimlendirilirler. Analjezik, anestezik
Kas Gevşeticiler ve Etki Mekanizmaları Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O. Kas Gevşeticiler N ö r o m u s k u l e r b l o k e r l e r diye de isimlendirilirler. Analjezik, anestezik
KULLANMA TALİMATI NEOFLEKS HİPERTONİK
 KULLANMA TALİMATI NEOFLEKS HİPERTONİK % 3 sodyum klorür sudaki çözeltisi 50 ml, 100 ml, 150 ml ve 250 ml Damar içine (intravenöz) uygulanır. Etkin madde : Her 100 ml çözelti 3.0 gr sodyum klorür Yardımcı
KULLANMA TALİMATI NEOFLEKS HİPERTONİK % 3 sodyum klorür sudaki çözeltisi 50 ml, 100 ml, 150 ml ve 250 ml Damar içine (intravenöz) uygulanır. Etkin madde : Her 100 ml çözelti 3.0 gr sodyum klorür Yardımcı
KULLANMA TALĐMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALĐMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALĐMATI DROGSAN SODYUM BĐKARBONAT % 8.4 Ampul Sadece damar içi kullanım içindir. Etkin madde Yardımcı maddeler : 10 ml lik ampul de 0.84 g sodyum bikarbonat içerir. : Enjeksiyonluk su Bu ilacı
KULLANMA TALĐMATI DROGSAN SODYUM BĐKARBONAT % 8.4 Ampul Sadece damar içi kullanım içindir. Etkin madde Yardımcı maddeler : 10 ml lik ampul de 0.84 g sodyum bikarbonat içerir. : Enjeksiyonluk su Bu ilacı
KULLANMA TALİMATI. COLİSTİMCİN İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir.
 KULLANMA TALİMATI COLİSTİMCİN İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir. Etkin madde: Her bir flakon 150 mg kolistin bazına eşdeğer
KULLANMA TALİMATI COLİSTİMCİN İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir. Etkin madde: Her bir flakon 150 mg kolistin bazına eşdeğer
Yardımcı maddeler: Sodyum klorür, hidroklorik asit, enjeksiyonluk su
 KULLANMA TALİMATI KEPLERON 4 mg / 2 ml IM Enjektabl Çözelti İçeren Ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, hidroklorik asit, enjeksiyonluk
KULLANMA TALİMATI KEPLERON 4 mg / 2 ml IM Enjektabl Çözelti İçeren Ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, hidroklorik asit, enjeksiyonluk
1- TIBBİ ÜRÜNÜN ADI. SPAZMOL Ampul, 1 ml 2- KALİTATİF VE KANTİTATİF BİLEŞİMİ. Her bir ampul; 20 mg Skopolamin N-Butil Bromür içermektedir.
 1- TIBBİ ÜRÜNÜN ADI SPAZMOL Ampul, 1 ml 2- KALİTATİF VE KANTİTATİF BİLEŞİMİ Her bir ampul; 20 mg Skopolamin N-Butil Bromür içermektedir. Yardımcı maddeler için, Bkz. 6.1 3 FARMASÖTİK FORMU 1 ml lik ampul
1- TIBBİ ÜRÜNÜN ADI SPAZMOL Ampul, 1 ml 2- KALİTATİF VE KANTİTATİF BİLEŞİMİ Her bir ampul; 20 mg Skopolamin N-Butil Bromür içermektedir. Yardımcı maddeler için, Bkz. 6.1 3 FARMASÖTİK FORMU 1 ml lik ampul
KULLANMA TALİMATI. NORCURON, kas gevşeticiler olarak bilinen bir ilaç grubuna dahildir.
 KULLANMA TALİMATI NORCURON 10 mg IV liyofilize toz içeren flakon İntravenöz olarak kullanılır. Etkin madde: Veküronyum bromür 10 mg Yardımcı maddeler: Sitrik asit monohidrat, disodyum hidrojen fosfat dihidrat,
KULLANMA TALİMATI NORCURON 10 mg IV liyofilize toz içeren flakon İntravenöz olarak kullanılır. Etkin madde: Veküronyum bromür 10 mg Yardımcı maddeler: Sitrik asit monohidrat, disodyum hidrojen fosfat dihidrat,
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI MUSCOFLEX 4 mg/2 ml I.M. enjeksiyon için solüsyon içeren ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, enjeksiyonluk su
KULLANMA TALİMATI MUSCOFLEX 4 mg/2 ml I.M. enjeksiyon için solüsyon içeren ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, enjeksiyonluk su
ANTİBİYOTİK HAZIRLAMA VE SAKLAMA KOŞULLARI
 TOTMDSD46 4.2.216 Antibiyotik ADI HAZIRLANIŞI Saklama koşulu TAZOCIN G IV infüzyon (Piperasilin + Tazobaktam 5 ml ila 15 ml lik: %.9 NACL %5 Dekstroz Ringer Laktat solüsyonu Sıvılarla ile en az 3 dakikada
TOTMDSD46 4.2.216 Antibiyotik ADI HAZIRLANIŞI Saklama koşulu TAZOCIN G IV infüzyon (Piperasilin + Tazobaktam 5 ml ila 15 ml lik: %.9 NACL %5 Dekstroz Ringer Laktat solüsyonu Sıvılarla ile en az 3 dakikada
KULLANMA TALİMATI. ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır.
 KULLANMA TALİMATI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
KULLANMA TALİMATI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
Esmeron 100 mg / 10 ml IV Flakon Steril, apirojen
 Esmeron 100 mg / 10 ml IV Flakon Steril, apirojen BİRİM FORMÜLÜ Roküronyum bromür 100 mg Sodyum asetat 20 mg Sodyum klorid 33 mg Asetik asid (ph: 4) 60-100 mg Enjeksiyonluk su 10 ml. Sadece hastane şartlarında
Esmeron 100 mg / 10 ml IV Flakon Steril, apirojen BİRİM FORMÜLÜ Roküronyum bromür 100 mg Sodyum asetat 20 mg Sodyum klorid 33 mg Asetik asid (ph: 4) 60-100 mg Enjeksiyonluk su 10 ml. Sadece hastane şartlarında
Zoladex LA 10.8 mg Depot (Subkütan Implant)
 1 Zoladex LA 10.8 mg Depot (Subkütan Implant) 2 Prospektüs 3 Zoladex LA 10.8 mg Depot (Subkütan Implant) Steril,apirojen Formülü Beher Zoladex LA Subkütan implant, enjektör içinde, uygulamaya hazır, beyaz
1 Zoladex LA 10.8 mg Depot (Subkütan Implant) 2 Prospektüs 3 Zoladex LA 10.8 mg Depot (Subkütan Implant) Steril,apirojen Formülü Beher Zoladex LA Subkütan implant, enjektör içinde, uygulamaya hazır, beyaz
KULLANMA TALİMATI. DOPAMINE DBL 200 mg/ 5 ml IV İnfüzyon İçin Solüsyon İçeren Ampul 5 Ampul İlaç damar içine yavaşça damla damla uygulanır.
 KULLANMA TALİMATI DOPAMINE DBL 200 mg/ 5 ml IV İnfüzyon İçin Solüsyon İçeren Ampul 5 Ampul İlaç damar içine yavaşça damla damla uygulanır. - Etkin madde: Dopamin hidroklorür 5 ml lik solüsyon içeren 1
KULLANMA TALİMATI DOPAMINE DBL 200 mg/ 5 ml IV İnfüzyon İçin Solüsyon İçeren Ampul 5 Ampul İlaç damar içine yavaşça damla damla uygulanır. - Etkin madde: Dopamin hidroklorür 5 ml lik solüsyon içeren 1
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI MYODİN 4mg/2ml IM ampul Kas üzerine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, hidroklorik asit, sitrik asit monohidrat, susuz sodyum
KULLANMA TALİMATI MYODİN 4mg/2ml IM ampul Kas üzerine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, hidroklorik asit, sitrik asit monohidrat, susuz sodyum
KULLANMA TALĐMATI. KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Damar içine veya kas içine uygulanır.
 KULLANMA TALĐMATI KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Damar içine veya kas içine uygulanır. Etkin madde: Her bir ampul (2 ml) 4 mg Ondansetron a eşdeğer Ondansetron hidroklorür
KULLANMA TALĐMATI KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Damar içine veya kas içine uygulanır. Etkin madde: Her bir ampul (2 ml) 4 mg Ondansetron a eşdeğer Ondansetron hidroklorür
2. KALİTATİF VE KANTİTATİF BİLEŞİM ESMERON un bir ml si 10 mg roküronyum bromür ihtiva etmektedir. Yardımcı maddeler için 6.1 e bakınız.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM ESMERON un bir ml si 10 mg roküronyum bromür ihtiva etmektedir.
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM ESMERON un bir ml si 10 mg roküronyum bromür ihtiva etmektedir.
Ultracain % 2 Ampul Steril ampul
 Ultracain % 2 Ampul Steril ampul FORMÜLÜ 1 ml enjeksiyon solüsyonu 20 mg artikain hidroklorür, 5mg sodyum klorür ve ad. 1 ml enjeksiyonluk distile su içerir. FARMAKOLOJİK ÖZELLİKLERİ Ultracain, amid tipi
Ultracain % 2 Ampul Steril ampul FORMÜLÜ 1 ml enjeksiyon solüsyonu 20 mg artikain hidroklorür, 5mg sodyum klorür ve ad. 1 ml enjeksiyonluk distile su içerir. FARMAKOLOJİK ÖZELLİKLERİ Ultracain, amid tipi
KULLANMA TALİMATI. Etkin Madde: 100 mg sugammadeks Yardımcı Maddeler: Hidroklorik asit, sodyum hidroksit, enjeksiyonluk su
 KULLANMA TALİMATI BRIDION 500 mg/5ml IV Enjeksiyonluk Çözelti İçeren Flakon Damardan uygulanır. Etkin Madde: 100 mg sugammadeks Yardımcı Maddeler: Hidroklorik asit, sodyum hidroksit, enjeksiyonluk su Bu
KULLANMA TALİMATI BRIDION 500 mg/5ml IV Enjeksiyonluk Çözelti İçeren Flakon Damardan uygulanır. Etkin Madde: 100 mg sugammadeks Yardımcı Maddeler: Hidroklorik asit, sodyum hidroksit, enjeksiyonluk su Bu
İNNOHEP 10 000 IU / ml KULLANIMA HAZIR ENJEKTÖR 0.45 ml PROSPEKTÜS
 PROSPEKTÜS FORMÜLÜ : 0.45 ml lik enjektör içinde; Tinzaparin sodyum 4 500 IU Anti-Xa Sodyum asetat, 3H2O 2.25 mg Enjeksiyonluk su k.m. 0.45 ml FARMAKOLOJİK ÖZELLİKLERİ: Farmakodinamik Özellikler: Tinzaparin
PROSPEKTÜS FORMÜLÜ : 0.45 ml lik enjektör içinde; Tinzaparin sodyum 4 500 IU Anti-Xa Sodyum asetat, 3H2O 2.25 mg Enjeksiyonluk su k.m. 0.45 ml FARMAKOLOJİK ÖZELLİKLERİ: Farmakodinamik Özellikler: Tinzaparin
KULLANMA TALİMATI. HAEMACCEL, 500 ml renksiz ve berrak çözelti içeren plastik şişe olarak ambalajlanmıştır.
 KULLANMA TALİMATI HAEMACCEL infüzyon solüsyonu 500 ml Damar içine yavaş olarak uygulanır. Etkin madde: Çözeltinin 1000 ml sinde: Poligelin (6.3 g azot a eşdeğer) Sodyum klorür Potasyum klorür Kalsiyum
KULLANMA TALİMATI HAEMACCEL infüzyon solüsyonu 500 ml Damar içine yavaş olarak uygulanır. Etkin madde: Çözeltinin 1000 ml sinde: Poligelin (6.3 g azot a eşdeğer) Sodyum klorür Potasyum klorür Kalsiyum
KISA ÜRÜN BİLGİLERİ Pozoloji ve uygulama şekli Sadece berrak ve partikül içermeyen ampuller kullanılmalıdır.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI SERUM FİZYOLOJİK İZOTONİK % 0.9 10 ml Ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Sodyum klorür 9 mg/ml Yardımcı maddeler: Yardımcı maddeler için
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI SERUM FİZYOLOJİK İZOTONİK % 0.9 10 ml Ampul 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Sodyum klorür 9 mg/ml Yardımcı maddeler: Yardımcı maddeler için
KULLANMA TALİMATI. ZONTRON 8 mg/4ml I.V. enjektabl solüsyon içeren ampul Kasa veya damar içine uygulanır.
 KULLANMA TALİMATI ZONTRON 8 mg/4ml I.V. enjektabl solüsyon içeren ampul Kasa veya damar içine uygulanır. Etkin madde: Her ampulde (4ml); 8 mg ondansetron (hidroklorür dihidrat olarak) içerir. Yardımcı
KULLANMA TALİMATI ZONTRON 8 mg/4ml I.V. enjektabl solüsyon içeren ampul Kasa veya damar içine uygulanır. Etkin madde: Her ampulde (4ml); 8 mg ondansetron (hidroklorür dihidrat olarak) içerir. Yardımcı
KULLANMA TALİMATI MYOCRON
 KULLANMA TALİMATI MYOCRON 50mg/5ml I.V. Enjeksiyonluk Çözelti İçeren Flakon İntravenöz olarak kullanılır. Etkin madde: Her bir flakon (5 ml) etkin madde olarak 50 mg roküronyum bromür içermektedir. Yardımcı
KULLANMA TALİMATI MYOCRON 50mg/5ml I.V. Enjeksiyonluk Çözelti İçeren Flakon İntravenöz olarak kullanılır. Etkin madde: Her bir flakon (5 ml) etkin madde olarak 50 mg roküronyum bromür içermektedir. Yardımcı
KULLANMA TALİMATI. COLİMYCİN 75 mg İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir.
 KULLANMA TALİMATI COLİMYCİN 75 mg İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir. Etkin madde: Her bir flakon 75 mg kolistin bazına eşdeğer
KULLANMA TALİMATI COLİMYCİN 75 mg İ.M./İ.V. Enjeksiyon İçin Liyofilize Toz İçeren Flakon Steril-Apirojen Kas içine ya da damar içine enjekte edilir. Etkin madde: Her bir flakon 75 mg kolistin bazına eşdeğer
KISA ÜRÜN BİLGİLERİ. Etkin madde: Her ml PAVULON 2 mg panküronyum bromür içerir. Yardımcı maddeler için 6.1 e bakınız.
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI PAVULON 4 mg/2 ml IV ampul. KISA ÜRÜN BİLGİLERİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her ml PAVULON 2 mg panküronyum bromür içerir. Yardımcı maddeler için 6.1 e bakınız.
1. BEŞERİ TIBBİ ÜRÜNÜN ADI PAVULON 4 mg/2 ml IV ampul. KISA ÜRÜN BİLGİLERİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her ml PAVULON 2 mg panküronyum bromür içerir. Yardımcı maddeler için 6.1 e bakınız.
KULLANMA TALİMATI. Etkin Madde: Mepiramin maleat, lidokain hidroklorür, dekspantenol.
 KULLANMA TALİMATI STİDERM jel Cilde uygulanır. Etkin Madde: Mepiramin maleat, lidokain hidroklorür, dekspantenol. Yardımcı Maddeler: Benzalkonyum klorür, mentol kristali, karbomer 980, disodyum EDTA, sodyum
KULLANMA TALİMATI STİDERM jel Cilde uygulanır. Etkin Madde: Mepiramin maleat, lidokain hidroklorür, dekspantenol. Yardımcı Maddeler: Benzalkonyum klorür, mentol kristali, karbomer 980, disodyum EDTA, sodyum
B. KISA ÜRÜN BİLGİLERİ
 B. KISA ÜRÜN BİLGİLERİ 1. Tıbbi farmasötik ürünün adı BETOPTIC Steril Oftalmik Solüsyon 2. Kalitatif ve kantitatif formülü mg/ml Betaksolol hidroklorür (5.0mg betaksolol baza eşdeğer), Ph. Eur 5.6 mg*
B. KISA ÜRÜN BİLGİLERİ 1. Tıbbi farmasötik ürünün adı BETOPTIC Steril Oftalmik Solüsyon 2. Kalitatif ve kantitatif formülü mg/ml Betaksolol hidroklorür (5.0mg betaksolol baza eşdeğer), Ph. Eur 5.6 mg*
KULLANMA TAL MATI MAXTH O 4 mg/2 ml M Enjeksiyon çin Çözelti çeren Ampul Kas içine uygulanır. Etkin madde Yardımcı maddeler : Bu ilacı kullanmaya ba
 KULLANMA TALİMATI MAXTHİO 4 mg/2 ml İM Enjeksiyon İçin Çözelti İçeren Ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, sitrik asit monohidrat,
KULLANMA TALİMATI MAXTHİO 4 mg/2 ml İM Enjeksiyon İçin Çözelti İçeren Ampul Kas içine uygulanır. Etkin madde: Her bir ampulde 4 mg Tiyokolşikosid Yardımcı maddeler: Sodyum klorür, sitrik asit monohidrat,
Ultiva 2 mg Enjektabl toz içeren flakon. Steril, Apirojen
 Ultiva TM 2mg Enjektabl Toz içeren Flakon (iv) Steril, Apirojen Formülü Ultiva steril, endotoksin ve koruyucu madde içermeyen, beyaz-kırık beyaz renkte liyofilize bir tozdur. Kullanılmadan önce sulandırılması
Ultiva TM 2mg Enjektabl Toz içeren Flakon (iv) Steril, Apirojen Formülü Ultiva steril, endotoksin ve koruyucu madde içermeyen, beyaz-kırık beyaz renkte liyofilize bir tozdur. Kullanılmadan önce sulandırılması
KULLANMA TALİMATI. FENTANYL 0,05 mg/ml 2 ml Enjeksiyon için Solüsyon İçeren Ampul Damar içine uygulanır.
 KULLANMA TALİMATI FENTANYL 0,05 mg/ml 2 ml Enjeksiyon için Solüsyon İçeren Ampul Damar içine uygulanır. Etkin madde: Her 1 ml solüsyon 0.05 miligram fentanile eşdeğer fentanil sitrat içerir. Yardımcı Maddeler:
KULLANMA TALİMATI FENTANYL 0,05 mg/ml 2 ml Enjeksiyon için Solüsyon İçeren Ampul Damar içine uygulanır. Etkin madde: Her 1 ml solüsyon 0.05 miligram fentanile eşdeğer fentanil sitrat içerir. Yardımcı Maddeler:
KISA ÜRÜN BİLGİSİ. 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Tek dozluk (0.4 ml) flakon, 5.60 mg polivinil alkol ve 2.40 mg povidon içerir.
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NOVAQUA tek dozluk göz damlası KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Tek dozluk (0.4 ml) flakon, 5.60 mg polivinil alkol ve 2.40 mg povidon içerir.
1. BEŞERİ TIBBİ ÜRÜNÜN ADI NOVAQUA tek dozluk göz damlası KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Tek dozluk (0.4 ml) flakon, 5.60 mg polivinil alkol ve 2.40 mg povidon içerir.
KULLANMA TALİMATI. MON.TALYUM-201 berrak ve renksiz bir çözeltidir. 1 ml enjeksiyonluk çözelti içinde 37 MBq Talyum-201 ( 201 Tl) radyonüklidi içerir.
 KULLANMA TALİMATI MON.TALYUM-201 I.V. enjeksiyonluk çözelti içeren flakon Her bir flakondaki talyum klorür ( 201 Tl) aktivitesi kalibrasyon tarih ve saatinde 37 MBq/mL dir. Damar içine uygulanır. Etkin
KULLANMA TALİMATI MON.TALYUM-201 I.V. enjeksiyonluk çözelti içeren flakon Her bir flakondaki talyum klorür ( 201 Tl) aktivitesi kalibrasyon tarih ve saatinde 37 MBq/mL dir. Damar içine uygulanır. Etkin
Ultracain % 2-Suprarenin Ampul Steril ampul
 Ultracain % 2-Suprarenin Ampul Steril ampul FORMÜLÜ 1 ml enjeksiyon solüsyonu 20 mg artikainhidroklorür, 0.006 mg epinefrin hidroklorür (adrenalin hidroklorür), 0.5 mg sodyum disülfit, 5 mg sodyum klorür
Ultracain % 2-Suprarenin Ampul Steril ampul FORMÜLÜ 1 ml enjeksiyon solüsyonu 20 mg artikainhidroklorür, 0.006 mg epinefrin hidroklorür (adrenalin hidroklorür), 0.5 mg sodyum disülfit, 5 mg sodyum klorür
KULLANMA TALİMATI MUSCURON
 KULLANMA TALİMATI MUSCURON 100 mg/ 10 ml enjeksiyon için çözelti içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
KULLANMA TALİMATI MUSCURON 100 mg/ 10 ml enjeksiyon için çözelti içeren flakon İntravenöz olarak kullanılır. Etkin madde: Roküronyum bromür. Yardımcı maddeler: Sodyum asetat, sodyum klorür, asetik asit,
KULLANMA TALİMATI. Cabral Ampul Kas içine uygulanır.
 KULLANMA TALİMATI Cabral Ampul Kas içine uygulanır. Etkin madde: Her bir ampul (3 ml), 800 mg feniramidol HCl içerir. Yardımcı maddeler: Sodyum hidroksit, deiyonize su Bu ilacı kullanmaya başlamadan önce
KULLANMA TALİMATI Cabral Ampul Kas içine uygulanır. Etkin madde: Her bir ampul (3 ml), 800 mg feniramidol HCl içerir. Yardımcı maddeler: Sodyum hidroksit, deiyonize su Bu ilacı kullanmaya başlamadan önce
EXELDERM KREM KISA ÜRÜN BİLGİLERİ. : % 1 Sulkonazol nitrat
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI EXELDERM krem 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde : % 1 Sulkonazol nitrat Yardımcı maddeler : Propilen Glikol Stearil alkol Setil alkol 5.000
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI EXELDERM krem 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde : % 1 Sulkonazol nitrat Yardımcı maddeler : Propilen Glikol Stearil alkol Setil alkol 5.000
SODYUM BİKARBONAT %8.4 IV İnfüzyon İçin Çözelti İçeren Ampul Sadece damar içi kullanım içindir.
 SODYUM BİKARBONAT %8.4 IV İnfüzyon İçin Çözelti İçeren Ampul Sadece damar içi kullanım içindir. Etkin madde : 10 mloik amputde 0.84 g sodyum bikarbonat içerir. * Yardımcı maddeler : Enjeksiyonluk su Bu
SODYUM BİKARBONAT %8.4 IV İnfüzyon İçin Çözelti İçeren Ampul Sadece damar içi kullanım içindir. Etkin madde : 10 mloik amputde 0.84 g sodyum bikarbonat içerir. * Yardımcı maddeler : Enjeksiyonluk su Bu
CONTRAMAL RETARD 100 mg TABLET PROSPEKTÜS
 PROSPEKTÜS FORMÜLÜ : Contramal Retard 100 mg Tablet; 100 mg tramadol hidroklorür ve boyar madde olarak titanyum dioksit (E 171) içerir. FARMAKOLOJİK ÖZELLİKLERİ : Farmakodinamik Özellikleri : Contramal
PROSPEKTÜS FORMÜLÜ : Contramal Retard 100 mg Tablet; 100 mg tramadol hidroklorür ve boyar madde olarak titanyum dioksit (E 171) içerir. FARMAKOLOJİK ÖZELLİKLERİ : Farmakodinamik Özellikleri : Contramal
KULLANMA TALİMATI. PRESLON 1000 mg/4 ml İ.M./İ.V. Ampul Kas içine veya damar içine uygulanır.
 PRESLON 1000 mg/4 ml İ.M./İ.V. Ampul Kas içine veya damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her bir ampul 1000 mg sitikoline eşdeğer 1045.05 mg sitikolin sodyum içerir. Yardımcı maddeler:
PRESLON 1000 mg/4 ml İ.M./İ.V. Ampul Kas içine veya damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her bir ampul 1000 mg sitikoline eşdeğer 1045.05 mg sitikolin sodyum içerir. Yardımcı maddeler:
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI Droser Burun Damlası. 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde:
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI Droser Burun Damlası KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Sodyum klorür % 0.9 (a/h) Yardımcı maddeler: Yardımcı maddeler için Bölüm 6.1 e bakınız.
1. BEŞERİ TIBBİ ÜRÜNÜN ADI Droser Burun Damlası KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Sodyum klorür % 0.9 (a/h) Yardımcı maddeler: Yardımcı maddeler için Bölüm 6.1 e bakınız.
KULLANMA TALİMATI. KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Kasa veya damar içine uygulanır.
 KULLANMA TALİMATI KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Kasa veya damar içine uygulanır. Etkin madde: Her ampulde (2 ml); 4 mg ondansetron (hidroklorür dihidrat olarak) içerir. Yardımcı
KULLANMA TALİMATI KEMOSET 4 mg / 2 ml im/iv enjeksiyonluk çözelti içeren ampul Kasa veya damar içine uygulanır. Etkin madde: Her ampulde (2 ml); 4 mg ondansetron (hidroklorür dihidrat olarak) içerir. Yardımcı
FUCITHALMIC VISKOZ GÖZ DAMLASI %1
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI FUCİTHALMİC viskoz göz damlası % 1 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : %1 anhidr maddeye ekivalan fusidik asit hemihidrat içerir. Yardımcı maddeler
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI FUCİTHALMİC viskoz göz damlası % 1 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : %1 anhidr maddeye ekivalan fusidik asit hemihidrat içerir. Yardımcı maddeler
KULLANMA TALİMATI. Protamin ICN 5000 IU/5 ml IV Kullanım İçin Enjeksiyonluk Solüsyon İçeren Ampul
 KULLANMA TALİMATI Protamin ICN 5000 IU/5 ml IV Kullanım İçin Enjeksiyonluk Solüsyon İçeren Ampul Damar içine uygulanır. Etkin madde: Protamin Hidroklorür Yardımcı maddeler: Metil paraben, propil paraben,
KULLANMA TALİMATI Protamin ICN 5000 IU/5 ml IV Kullanım İçin Enjeksiyonluk Solüsyon İçeren Ampul Damar içine uygulanır. Etkin madde: Protamin Hidroklorür Yardımcı maddeler: Metil paraben, propil paraben,
2. DROSER i kullanmadan önce dikkat edilmesi gerekenler 3. DROSER nasıl kullanılır? 4. Olası yan etkiler nelerdir? 5. DROSER in saklanması
 KULLANMA TALİMATI DROSER burun damlası Yalnızca burun içine uygulanır. Etkin madde : Sodyum klorür Yardımcı maddeler : Deiyonize su. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice
KULLANMA TALİMATI DROSER burun damlası Yalnızca burun içine uygulanır. Etkin madde : Sodyum klorür Yardımcı maddeler : Deiyonize su. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice
KULLANMA TALİMATI. Etkin madde: Her bir ampulde (5ml); 100.0 mg (20 mg/ml) demir (III) e eşdeğer demir hidroksit sükroz kompleksi içerir
 EMFER 100 mg/5 ml i.v. Ampul Damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her bir ampulde (5ml); 100.0 mg (20 mg/ml) demir (III) e eşdeğer demir hidroksit sükroz kompleksi içerir Yardımcı maddeler:
EMFER 100 mg/5 ml i.v. Ampul Damar içine uygulanır. KULLANMA TALİMATI Etkin madde: Her bir ampulde (5ml); 100.0 mg (20 mg/ml) demir (III) e eşdeğer demir hidroksit sükroz kompleksi içerir Yardımcı maddeler:
2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: MUSCURON'un bir ml'si 10 mg roküronyum bromür ihtiva etmektedir.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI MUSCURON 100 mg/ 10 ml enjeksiyon için çözelti içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: MUSCURON'un bir ml'si 10 mg roküronyum bromür
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI MUSCURON 100 mg/ 10 ml enjeksiyon için çözelti içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: MUSCURON'un bir ml'si 10 mg roküronyum bromür
KULLANMA TALİMATI. Uygulanmadan önce uygun infüzyon çözeltisi içinde seyreltilen bir konsantredir.
 KULLANMA TALİMATI TRACUTİL Konsantre infüzyon çözeltisi Damar içine uygulanır. Etkin madde: 10 ml lik herbir ampul Demir (II) klorür tetrahidrat 6.958 mg, Çinko klorür 6.815 mg, Mangan (II) klorür tetrahidrat
KULLANMA TALİMATI TRACUTİL Konsantre infüzyon çözeltisi Damar içine uygulanır. Etkin madde: 10 ml lik herbir ampul Demir (II) klorür tetrahidrat 6.958 mg, Çinko klorür 6.815 mg, Mangan (II) klorür tetrahidrat
KULLANMA TALİMATI. İSOFLUDEM 250 ml inhalasyon çözeltisi İnhalasyon (soluma) yoluyla uygulanır.
 KULLANMA TALİMATI İSOFLUDEM 250 ml inhalasyon çözeltisi İnhalasyon (soluma) yoluyla uygulanır. Etkin madde: Her şişe % 99.9 oranında isofluran içerir. Yardımcı madde: Bulunmamaktadır. Bu ilacı kullanmaya
KULLANMA TALİMATI İSOFLUDEM 250 ml inhalasyon çözeltisi İnhalasyon (soluma) yoluyla uygulanır. Etkin madde: Her şişe % 99.9 oranında isofluran içerir. Yardımcı madde: Bulunmamaktadır. Bu ilacı kullanmaya
PROCTOLOG hemoroid krizleri sırasında ağrılı ve kaşıntılı anal semptomların ve fissürlerin semptomatik tedavisinde endikedir.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI PROCTOLOG rektal krem 2. KALİTATİF VE KANTİTATİF BİLEŞİM 100 g. kremde, Etkin madde: Ruskogenin Trimebutin Yardımcı maddeler: Setostearil alkol Propilen glikol
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI PROCTOLOG rektal krem 2. KALİTATİF VE KANTİTATİF BİLEŞİM 100 g. kremde, Etkin madde: Ruskogenin Trimebutin Yardımcı maddeler: Setostearil alkol Propilen glikol
Flixonase TM Nazal Damla
 Flixonase TM Nazal Damla Formülü Flixonase Nazal Damla, flutikazon propiyonatın sulu süspansiyonudur. Her tek kullanımlık nazal damlalık, 0.4 ml sulu süspansiyon içinde 400 mikrogram flutikazon propiyonat,
Flixonase TM Nazal Damla Formülü Flixonase Nazal Damla, flutikazon propiyonatın sulu süspansiyonudur. Her tek kullanımlık nazal damlalık, 0.4 ml sulu süspansiyon içinde 400 mikrogram flutikazon propiyonat,
Netilmisin sülfat. Her tek dozluk kap (0.3 ml) mg netilmisin sülfat (0.900 mg Netilmisin e eşdeğer) içerir.
 KULLANMA TALİMATI NETİRA tek doz göz damlası Göze uygulanır. Etkin madde : Netilmisin sülfat. Her tek dozluk kap (0.3 ml) 1.365 mg netilmisin sülfat (0.900 mg Netilmisin e eşdeğer) içerir. Yardımcı Maddeler
KULLANMA TALİMATI NETİRA tek doz göz damlası Göze uygulanır. Etkin madde : Netilmisin sülfat. Her tek dozluk kap (0.3 ml) 1.365 mg netilmisin sülfat (0.900 mg Netilmisin e eşdeğer) içerir. Yardımcı Maddeler
KULLANMA TALİMATI. ASİST 200 mg kapsül Ağızdan alınır.
 KULLANMA TALİMATI ASİST 200 mg kapsül Ağızdan alınır. Etkin madde: Her kapsülde 200 mg asetilsistein Yardımcı maddeler: Magnezyum stearat, kolloidal anhidrus silika, sodyum lauril sülfat, etil selüloz,
KULLANMA TALİMATI ASİST 200 mg kapsül Ağızdan alınır. Etkin madde: Her kapsülde 200 mg asetilsistein Yardımcı maddeler: Magnezyum stearat, kolloidal anhidrus silika, sodyum lauril sülfat, etil selüloz,
Uygulama şekli : Sadece ağızdan kullanım içindir. Yemeklerden önce ya da sonra veya yemeklerle birlikte ölçek vasıtasıyla kullanılabilir.
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TUSİBRON 7.5 mg / 5 ml Şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : Butamirat sitrat Yardımcı maddeler : Sorbitol % 70 non-kristalin Gliserin Sodyum
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TUSİBRON 7.5 mg / 5 ml Şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : Butamirat sitrat Yardımcı maddeler : Sorbitol % 70 non-kristalin Gliserin Sodyum
SEDASYON-ANALJEZİ KAS GEVŞETİCİLER
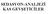 SEDASYON-ANALJEZİ KAS GEVŞETİCİLER MİDAZOLAMIN ÖNERİLEN DOZLARI ORAL 0.5-0.7 mgr/kg Max dox 20 mgr REKTAL 1.0 mgr/kg Max doz 20 mgr NAZAL 0.2-0.4 mgr/kg Max doz 10 mgr SUBLİNGUAL 0.2 mgr/kg * Max doz 2
SEDASYON-ANALJEZİ KAS GEVŞETİCİLER MİDAZOLAMIN ÖNERİLEN DOZLARI ORAL 0.5-0.7 mgr/kg Max dox 20 mgr REKTAL 1.0 mgr/kg Max doz 20 mgr NAZAL 0.2-0.4 mgr/kg Max doz 10 mgr SUBLİNGUAL 0.2 mgr/kg * Max doz 2
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 TIENAM 500 mg I.V. enjektabl flakon Damar içine uygulanır. KULLANMA TALİMATI Etkin madde(ler): Her bir flakon steril olarak 500 mg imipenem (imipenem monohidrat olarak) ve 500 mg silastatin (silastatin
TIENAM 500 mg I.V. enjektabl flakon Damar içine uygulanır. KULLANMA TALİMATI Etkin madde(ler): Her bir flakon steril olarak 500 mg imipenem (imipenem monohidrat olarak) ve 500 mg silastatin (silastatin
KULLANMA TALİMATI. METACARTİN 1 g/5 ml İ.M/İ.V. enjeksiyonluk çözelti içeren ampul Steril, apirojen Kas içine veya damar içine uygulanır.
 KULLANMA TALİMATI METACARTİN 1 g/5 ml İ.M/İ.V. enjeksiyonluk çözelti içeren ampul Steril, apirojen Kas içine veya damar içine uygulanır. Etkin madde: Her bir 5 ml lik ampul 1 g Levokarnitin içerir. Yardımcı
KULLANMA TALİMATI METACARTİN 1 g/5 ml İ.M/İ.V. enjeksiyonluk çözelti içeren ampul Steril, apirojen Kas içine veya damar içine uygulanır. Etkin madde: Her bir 5 ml lik ampul 1 g Levokarnitin içerir. Yardımcı
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI. STİLEX jel 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI STİLEX jel 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde : 1 g STİLEX, etkin madde olarak 15 mg Mepiramin maleat, 15 mg Lidokain hidroklorür ve 50 mg Dekspantenol
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI STİLEX jel 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde : 1 g STİLEX, etkin madde olarak 15 mg Mepiramin maleat, 15 mg Lidokain hidroklorür ve 50 mg Dekspantenol
Farmakokinetik özellikler Trimetobenzamid hidroklorürün etkinliği oral yoldan alındıktan 10-40 dakika sonra başlar ve yaklaşık 3-4 saat devam eder.
 Emedur Draje FORMÜLÜ Bir drajede: Trimetobenzamid HCl 200 mg (Şeker, kinolin sarısı, indigo karmin ve titan dioksit içerir.) FARMAKOLOJİK ÖZELLİKLERİ Farmakodinamik özellikler Trimetobenzamid hidroklorür,
Emedur Draje FORMÜLÜ Bir drajede: Trimetobenzamid HCl 200 mg (Şeker, kinolin sarısı, indigo karmin ve titan dioksit içerir.) FARMAKOLOJİK ÖZELLİKLERİ Farmakodinamik özellikler Trimetobenzamid hidroklorür,
KULLANMA TALİMATI. NETİRA göz damlası 5 ml Göze uygulanır. Etkin madde :
 KULLANMA TALİMATI NETİRA göz damlası 5 ml Göze uygulanır. Etkin madde : Netilmisin sülfat. 100 ml de, 0.300 g Netilmisin e eşdeğer 0.455 g Netilmisin sülfat içerir. Yardımcı Maddeler : Sodyum klorür, Benzalkonyum
KULLANMA TALİMATI NETİRA göz damlası 5 ml Göze uygulanır. Etkin madde : Netilmisin sülfat. 100 ml de, 0.300 g Netilmisin e eşdeğer 0.455 g Netilmisin sülfat içerir. Yardımcı Maddeler : Sodyum klorür, Benzalkonyum
Uygulama şekli : Sadece ağızdan kullanım içindir. Yemeklerden önce ya da sonra veya yemeklerle birlikte ölçek vasıtasıyla kullanılabilir.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NOTUSS FORT şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : Butamirat sitrat Yardımcı maddeler : Sodyum sitrat dihidrat Sodyum benzoat Sorbitol % 70
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NOTUSS FORT şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde : Butamirat sitrat Yardımcı maddeler : Sodyum sitrat dihidrat Sodyum benzoat Sorbitol % 70
KULLANMA TALİMATI. VENORUTON FORTE 500 mg tablet Ağız yoluyla alınır.
 KULLANMA TALİMATI VENORUTON FORTE 500 mg tablet Ağız yoluyla alınır. Etkin madde: Her bir tablet 500 mg okserutin içerir. Yardımcı maddeler: Makrogol, magnezyum stearat Bu ilacı kullanmaya başlamadan önce
KULLANMA TALİMATI VENORUTON FORTE 500 mg tablet Ağız yoluyla alınır. Etkin madde: Her bir tablet 500 mg okserutin içerir. Yardımcı maddeler: Makrogol, magnezyum stearat Bu ilacı kullanmaya başlamadan önce
KISA ÜRÜN BİLGİLERİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM ESMERON un bir ml si 10 mg roküronyum bromür ihtiva etmektedir.
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI ESMERON 50 mg/ 5 ml enjeksiyon için solüsyon içeren flakon 2. KALİTATİF VE KANTİTATİF BİLEŞİM ESMERON un bir ml si 10 mg roküronyum bromür ihtiva etmektedir.
KULLANMA TALĐMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALĐMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALĐMATI ZĐNCOBEST 15 mg / 5 ml şurup Ağızdan alınır. Etkin madde: Her 5 ml şurupta 15 mg çinkoya eşdeğer 66 mg çinko sülfat heptahidrat Yardımcı maddeler: Metil paraben sodyum, sükroz, portakal
KULLANMA TALĐMATI ZĐNCOBEST 15 mg / 5 ml şurup Ağızdan alınır. Etkin madde: Her 5 ml şurupta 15 mg çinkoya eşdeğer 66 mg çinko sülfat heptahidrat Yardımcı maddeler: Metil paraben sodyum, sükroz, portakal
Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI GRİZİNC 15 mg / 5 ml şurup Ağızdan alınır. Etkin madde: Her 5 ml şurupta 15 mg çinkoya eşdeğer 66 mg çinko sülfat heptahidrat bulunur. Yardımcı maddeler: Şeker (sükroz), gliserin, nipajin
KULLANMA TALİMATI GRİZİNC 15 mg / 5 ml şurup Ağızdan alınır. Etkin madde: Her 5 ml şurupta 15 mg çinkoya eşdeğer 66 mg çinko sülfat heptahidrat bulunur. Yardımcı maddeler: Şeker (sükroz), gliserin, nipajin
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI. FENİSTİL Jel 2. KALİTATİF VE KANTİTATİF BİLEŞİM
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI FENİSTİL Jel 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 1 g jel, 1 mg dimetinden maleat içerir. Yardımcı maddeler: Propilen glikol, benzalkonyum klorür
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI FENİSTİL Jel 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 1 g jel, 1 mg dimetinden maleat içerir. Yardımcı maddeler: Propilen glikol, benzalkonyum klorür
KULLANMA TALİMATI. PREDOPAM 50 mg/ 5 ml i.v. infüzyon için konsantre çözelti içeren ampul
 KULLANMA TALİMATI PREDOPAM 50 mg/ 5 ml i.v. infüzyon için konsantre çözelti içeren ampul Damar içine ve yavaşça damla damla olarak uygulanır. Etkin madde: Her ampul 50 mg dopamin hidroklorür içerir. Yardımcı
KULLANMA TALİMATI PREDOPAM 50 mg/ 5 ml i.v. infüzyon için konsantre çözelti içeren ampul Damar içine ve yavaşça damla damla olarak uygulanır. Etkin madde: Her ampul 50 mg dopamin hidroklorür içerir. Yardımcı
KULLANMA TALİMATI. OXXA ŞURUP ( %4 Asetilsistein içeren Şurup hazırlamak için Granül ) Ağız yoluyla uygulanır.
 KULLANMA TALİMATI OXXA ŞURUP ( %4 Asetilsistein içeren Şurup hazırlamak için Granül ) Ağız yoluyla uygulanır. Etkin madde: Her 5 ml şurup 200 mg (%4) asetilsistein içerir Yardımcı maddeler: Metil paraben
KULLANMA TALİMATI OXXA ŞURUP ( %4 Asetilsistein içeren Şurup hazırlamak için Granül ) Ağız yoluyla uygulanır. Etkin madde: Her 5 ml şurup 200 mg (%4) asetilsistein içerir Yardımcı maddeler: Metil paraben
KULLANMA TALİMATI. ROBİSİD 500 mg film tablet Ağızdan alınır. Etkin madde: Bir film kaplı tablet 500 mg sodyum fusidat içerir.
 KULLANMA TALİMATI ROBİSİD 500 mg film tablet Ağızdan alınır. Etkin madde: Bir film kaplı tablet 500 mg sodyum fusidat içerir. Yardımcı maddeler: DL-alfa tokoferol, mikrokristalin selüloz, laktoz monohidrat,
KULLANMA TALİMATI ROBİSİD 500 mg film tablet Ağızdan alınır. Etkin madde: Bir film kaplı tablet 500 mg sodyum fusidat içerir. Yardımcı maddeler: DL-alfa tokoferol, mikrokristalin selüloz, laktoz monohidrat,
ÜRÜN BİLGİSİ. ETACİD, erişkinler, 12 yaş ve üzerindeki adolesanlarda mevsimsel alerjik rinitin profilaksisinde endikedir.
 ÜRÜN BİLGİSİ 1. ÜRÜN ADI ETACİD % 0,05 Nazal Sprey 2. BİLEŞİM Etkin madde: Mometazon furoat 50 mikrogram/püskürtme 3. TERAPÖTİK ENDİKASYONLAR ETACİD erişkinler, adolesanlar ve 6-11 yaş arasındaki çocuklarda
ÜRÜN BİLGİSİ 1. ÜRÜN ADI ETACİD % 0,05 Nazal Sprey 2. BİLEŞİM Etkin madde: Mometazon furoat 50 mikrogram/püskürtme 3. TERAPÖTİK ENDİKASYONLAR ETACİD erişkinler, adolesanlar ve 6-11 yaş arasındaki çocuklarda
KULLANMA TALİMATI SERUM FİZYOLOJİK İZOTONİK (%0.9) AMPUL;
 KULLANMA TALİMATI SERUM FİZYOLOJİK İZOTONİK (%0.9) AMPUL Kas içine, deri altına, damara ya da benzeri bölgelere uygulanır. Steril - Apirojen Etkin madde: Her 10 ml lik ampul 0.09 g sodyum klorür içerir.
KULLANMA TALİMATI SERUM FİZYOLOJİK İZOTONİK (%0.9) AMPUL Kas içine, deri altına, damara ya da benzeri bölgelere uygulanır. Steril - Apirojen Etkin madde: Her 10 ml lik ampul 0.09 g sodyum klorür içerir.
KULLANMA TALİMATI. TALİNAT 0.5 mg/10ml İ.V./İ.M. enjeksiyonluk çözelti içeren ampul Kas içine ve damar içine uygulanır.
 KULLANMA TALİMATI TALİNAT 0.5 mg/10ml İ.V./İ.M. enjeksiyonluk çözelti içeren ampul Kas içine ve damar içine uygulanır. Etkin madde: Her 1 ml çözelti 0,05 miligram fentanile eşdeğer fentanil sitrat içerir.
KULLANMA TALİMATI TALİNAT 0.5 mg/10ml İ.V./İ.M. enjeksiyonluk çözelti içeren ampul Kas içine ve damar içine uygulanır. Etkin madde: Her 1 ml çözelti 0,05 miligram fentanile eşdeğer fentanil sitrat içerir.
KULLANMA TALİMATI. Etkin madde: 1 ampul, 3 ml izotonik tuz çözeltisi içinde 3 mg granisetrona eşdeğer granisetron hidroklorür içerir.
 KULLANMA TALİMATI GRATRYL 3 mg/ 3 ml i.v. infüzyon için çözelti içeren ampul Damar içine uygulanır. Etkin madde: 1 ampul, 3 ml izotonik tuz çözeltisi içinde 3 mg granisetrona eşdeğer granisetron hidroklorür
KULLANMA TALİMATI GRATRYL 3 mg/ 3 ml i.v. infüzyon için çözelti içeren ampul Damar içine uygulanır. Etkin madde: 1 ampul, 3 ml izotonik tuz çözeltisi içinde 3 mg granisetrona eşdeğer granisetron hidroklorür
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI DRYEX % 0.15 göz damlası Göze uygulanır. Etkin madde: 1.5 mg/ml Sodyum Hiyalüronat içerir. Yardımcı maddeler: Benzalkonyum klorür %50, disodyum hidrojen fosfat dodekahidrat, sodyum dihidrojen
KULLANMA TALİMATI DRYEX % 0.15 göz damlası Göze uygulanır. Etkin madde: 1.5 mg/ml Sodyum Hiyalüronat içerir. Yardımcı maddeler: Benzalkonyum klorür %50, disodyum hidrojen fosfat dodekahidrat, sodyum dihidrojen
KULLANMA TALİMATI. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
 KULLANMA TALİMATI MIOSTAT %0.01 steril intraoküler solüsyon Göz içine (intraoküler) enjeksiyon olarak uygulanır. Etkin madde: 0.10 mg/ml karbakol içerir. Yardımcı maddeler: Sodyum klorür, potasyum klorür
KULLANMA TALİMATI MIOSTAT %0.01 steril intraoküler solüsyon Göz içine (intraoküler) enjeksiyon olarak uygulanır. Etkin madde: 0.10 mg/ml karbakol içerir. Yardımcı maddeler: Sodyum klorür, potasyum klorür
KULLANMA TALİMATI. Etkin madde: Her saşe1200 mg asetilsistein içerir. Yardımcı maddeler: Beta karoten, aspartam, sorbitol ve portakal aroması içerir.
 KULLANMA TALİMATI MUCOCURE 1200 mg toz içeren saşe Ağızdan alınır. Etkin madde: Her saşe1200 mg asetilsistein içerir. Yardımcı maddeler: Beta karoten, aspartam, sorbitol ve portakal aroması içerir. Bu
KULLANMA TALİMATI MUCOCURE 1200 mg toz içeren saşe Ağızdan alınır. Etkin madde: Her saşe1200 mg asetilsistein içerir. Yardımcı maddeler: Beta karoten, aspartam, sorbitol ve portakal aroması içerir. Bu
KISA ÜRÜN BİLGİSİ. 1.BEŞERİ TIBBİ ÜRÜNÜN ADI BEMİKS kompoze ampul 2.KALİTATİF VE KANTİTATİF BİLEŞİM
 1.BEŞERİ TIBBİ ÜRÜNÜN ADI BEMİKS kompoze ampul KISA ÜRÜN BİLGİSİ 2.KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her 2 ml lik ampulde, Tiamin (B 1 ).. 25 mg Riboflavin (B 2 ).. 2 mg Piridoksin (B 6 )..
1.BEŞERİ TIBBİ ÜRÜNÜN ADI BEMİKS kompoze ampul KISA ÜRÜN BİLGİSİ 2.KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her 2 ml lik ampulde, Tiamin (B 1 ).. 25 mg Riboflavin (B 2 ).. 2 mg Piridoksin (B 6 )..
KULLANMA TALİMATI ASİST
 KULLANMA TALİMATI ASİST 300 mg/3 ml (% 10) solüsyon içeren ampul Toplardamar içine (intravenöz), kas içine (intramüsküler), solunum yoluna (inhalasyon) veya soluk borusu içine (intratrakeal) uygulanır.
KULLANMA TALİMATI ASİST 300 mg/3 ml (% 10) solüsyon içeren ampul Toplardamar içine (intravenöz), kas içine (intramüsküler), solunum yoluna (inhalasyon) veya soluk borusu içine (intratrakeal) uygulanır.
KULLANMA TALİMATI. Etkin madde: Her bir ampul, 10 ml çözelti içinde 50 mg midazolam içerir.
 KULLANMA TALİMATI MİDOLAM 50 mg/10 ml IM/IV/rektal çözelti içeren ampul Damar veya kas içine ya da rektal olarak uygulanır. Etkin madde: Her bir ampul, 10 ml çözelti içinde 50 mg midazolam içerir. Yardımcı
KULLANMA TALİMATI MİDOLAM 50 mg/10 ml IM/IV/rektal çözelti içeren ampul Damar veya kas içine ya da rektal olarak uygulanır. Etkin madde: Her bir ampul, 10 ml çözelti içinde 50 mg midazolam içerir. Yardımcı
Tabletler çiğnenmeden yeterli miktarda sıvı, örneğin bir bardak su ile yutulmalıdır.
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DEBRİDAT tablet 100 mg 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir tablet 100 mg Trimebutin Maleat içerir. Yardımcı maddeler: Laktoz monohidrat
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DEBRİDAT tablet 100 mg 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir tablet 100 mg Trimebutin Maleat içerir. Yardımcı maddeler: Laktoz monohidrat
Pazoloji ve Kullanım Şekli Çocuklar ve erişkinlerde kullanımı aşağıdaki tabloda verilmiştir;
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NAC 200 mg efervesan tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Asetilsistein 200 mg Yardımcı madde(ler): Aspartam (E 951) Sodyum hidrojen karbonat
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NAC 200 mg efervesan tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Asetilsistein 200 mg Yardımcı madde(ler): Aspartam (E 951) Sodyum hidrojen karbonat
II. YIL ASİSTANLARININ SORUMLU OLDUĞU KONULAR:
 II. YIL ASİSTANLARININ SORUMLU OLDUĞU KONULAR: I- TEMEL BİLİMLER Anesteziye Giriş: Anestezide Fizik Kurallar Temel Monitörizasyon Medikal Gaz Sistemleri Anestezi Cihazı Vaporizatörler Soluma sistemleri,
II. YIL ASİSTANLARININ SORUMLU OLDUĞU KONULAR: I- TEMEL BİLİMLER Anesteziye Giriş: Anestezide Fizik Kurallar Temel Monitörizasyon Medikal Gaz Sistemleri Anestezi Cihazı Vaporizatörler Soluma sistemleri,
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI HEPA-MERZ İnfüzyon Konsantresi
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI HEPA-MERZ İnfüzyon Konsantresi KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde: 1 ampul (10 ml), 5,0 g L-ornitin L-aspartat içermektedir. Yardımcı maddeler:
1. BEŞERİ TIBBİ ÜRÜNÜN ADI HEPA-MERZ İnfüzyon Konsantresi KISA ÜRÜN BİLGİSİ 2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde: 1 ampul (10 ml), 5,0 g L-ornitin L-aspartat içermektedir. Yardımcı maddeler:
KULLANMA TALİMATI DOPADREN
 KULLANMA TALİMATI DOPADREN 200 mg/5 ml İ.V. infüzyon için konsantre solüsyon içeren ampul İlaç damar içine yavaşça damla damla uygulanır. Etkin madde: Dopamin hidroklorür 5 ml lik solüsyon içeren 1 ampulde
KULLANMA TALİMATI DOPADREN 200 mg/5 ml İ.V. infüzyon için konsantre solüsyon içeren ampul İlaç damar içine yavaşça damla damla uygulanır. Etkin madde: Dopamin hidroklorür 5 ml lik solüsyon içeren 1 ampulde
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TUSAMOL 7.5 mg / 5 ml şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM. Etkin madde: Butamirat sitrat
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TUSAMOL 7.5 mg / 5 ml şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Butamirat sitrat 7.5 mg Yardımcı maddeler: Sorbitol Gliserin Sodyum Sakarin 2.5
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI TUSAMOL 7.5 mg / 5 ml şurup 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Butamirat sitrat 7.5 mg Yardımcı maddeler: Sorbitol Gliserin Sodyum Sakarin 2.5
KULLANMA TALİMATI. INFEROSE I.V. 100 mg/5 ml İnfüzyonluk Konsantre Çözelti İçeren Ampul. Damar içine (intravenöz) uygulanır.
 KULLANMA TALİMATI INFEROSE I.V. 100 mg/5 ml İnfüzyonluk Konsantre Çözelti İçeren Ampul Damar içine (intravenöz) uygulanır. Etkin madde: Her 5 ml lik ampul, 100 mg Demir(III) e eşdeğer 2700 mg Demir III-
KULLANMA TALİMATI INFEROSE I.V. 100 mg/5 ml İnfüzyonluk Konsantre Çözelti İçeren Ampul Damar içine (intravenöz) uygulanır. Etkin madde: Her 5 ml lik ampul, 100 mg Demir(III) e eşdeğer 2700 mg Demir III-
KULLANMA TALİMATI. Etkin madde: Palivizumab (Her bir flakon 50 mg palivizumab içerir).
 KULLANMA TALİMATI SYNAGIS 50 mg I.M. Enjeksiyon İçin Liyofilize Toz İçeren Flakon İntramüsküler yoldan alınır. Etkin madde: Palivizumab (Her bir flakon 50 mg palivizumab içerir). Yardımcı maddeler: Histidin,
KULLANMA TALİMATI SYNAGIS 50 mg I.M. Enjeksiyon İçin Liyofilize Toz İçeren Flakon İntramüsküler yoldan alınır. Etkin madde: Palivizumab (Her bir flakon 50 mg palivizumab içerir). Yardımcı maddeler: Histidin,
KULLANMA TALİMATI. BİTERAL 500 mg/3 ml i.v infüzyon için çözelti içeren ampul Damar içine (intravenöz) uygulanır.
 KULLANMA TALİMATI BİTERAL 500 mg/3 ml i.v infüzyon için çözelti içeren ampul Damar içine (intravenöz) uygulanır. Etkin madde: Her bir ampulde 500 mg Ornidazol. Yardımcı maddeler: Alkol absolü (etanol),
KULLANMA TALİMATI BİTERAL 500 mg/3 ml i.v infüzyon için çözelti içeren ampul Damar içine (intravenöz) uygulanır. Etkin madde: Her bir ampulde 500 mg Ornidazol. Yardımcı maddeler: Alkol absolü (etanol),
