ĐÇ YAPISI Doç. Dr. Halit YAZICI
|
|
|
- Hazan Aysel Bozer
- 7 yıl önce
- İzleme sayısı:
Transkript
1 Dokuz Eylül Üniversitesi Đnşaat Mühendisliği Bölümü YAPI MALZEMESĐ I DERSĐ KATI ÇĐSĐMLERĐN ĐÇ YAPISI Doç. Dr. Halit YAZICI
2 Đnşaat Mühendisliğinde, cisimlerin yükler altındaki davranışını saptayabilmek çok önemlidir. Yapının tasarımı, boyutlandırma ve kesin hesapları açısından malzemenin "mekanik özelliklerini" bilmek gereklidir.
3 Malzemenin mekanik özellikleri cismin iç yapısına bağlı olduğundan önce bunun incelenmesi gerekir. Ayrıca, metallerin korozyonu gibi malzeme açısından önemli olayları atom yapısına dayanmadan açıklamak olanaksızdır. Bu nedenle bu bölümde, bir yapı mühendisinin hatırlaması gereken kimya bilgilerini özetlemekte yarar vardır.
4 Atom Yapısı Atomlar, çevrelerinde negatif yüklü elektronların devinimler yaptığı pozitif yüklü proton ve yüksüz nötronlardan oluşur. Nötronu olmayan atom, yalnız hidrojen atomudur. Bir atom çekirdeğinde, elektron sayısı kadar proton vardır. Elektronlar, çekirdek kütlesi yanında çok küçüktür (1/1850 oranında) ve bu değer kütle hesabında göz önüne alınmaz.
5 Atom elektronlar, protonlar ve nötronlardan n oluşur. ur. Atom numarası: atomdaki protonların n toplam sayısı Kütle numarası: atomdaki proton ve nötronlarn tronların toplam sayısı Denge durumundaki bir atomda elektronların n (-)( sayısı protonların n (+) sayısına eşittir. e Bir atom gramda; örneğin 55,85 gram demirde 6, (Avagadro sayısı ) kadar atom vardır. r.
6 ELEMENTLER VE ATOM YAPISI Atom numarasına na bağlı olarak atom çekirdeğinin inin yarıçap apı mm aralığı ığında, atom yarıçap apı ise yaklaşı şık k 10-7 mm civarındad ndadır. Hidrojenin atom yarıçap apı 0, mm, toryumun atom yarıçap apı 1, mm dir
7 Atomların çapları çok küçük üçüktür. Örneğin, hidrojen atomunun çapı 10-8 cm dir dir.. Atomun en önemli özelliği, i, çeşitli bağ kuvvetlerinin meydana gelmesine yol açan a an elektron sayısıdır. Atom numarası da elektron sayısına eşittir. e Örneğin, atom numarası 92 olan uranyumun 92 elektronu vardır. r. Buna göre, g uranyum atomunun çekirdeğinde inde 92 proton ve 146 nötron n vardır. r. Böylece uranyumun kütle k ağıa ğırlığı 238 olur.
8 ELEMENTLER VE ATOM YAPISI Elementler, Kabaca; metaller, ametaller ve yarı metaller olmak üzere üçe e ayrılabilir.
9 İZOTOP ELEMENTLER VE ATOM YAPISI Aynı atomun protonları sabit kalmakla beraber nötronları değişik ik olabilir ki bunlara izotop denilir. Örneğin; 26 Atom numarasına na sahip demirin izotopları: 54Fe (26 p, 28 n) 55Fe (26 p, 29 n) 56Fe (26 p, 30 n) 57Fe (26 p, 31 n) 58Fe (26 p, 32 n)
10 İZOTOP ELEMENTLER VE ATOM YAPISI HİDROJENİN İZOTOPLARI Hidrojen Protium 1 p + 0 n Ağır r Hidrojen Deuterium 1 p + 1 n Radyoaktif Hidrojen Tritium 1 p + 2 n
11 ELEMENTLER VE ATOM YAPISI İZOTOP Elementlerin kimyasal özelliklerini o elementin elektron ve proton sayısı belirler. Bir elementin tüm t m izotoplarında kimyasal özellikleri aynıdır. İzotoplarda yalnızca fark nötron n sayısıdır. İzotoplarda bazı fiziksel özellikler birbirinden farklı olabilir. Örneğin bazı izotoplar radyoaktif olmalarına karşı şın n diğerleri değildir.
12 İZOBAR ELEMENTLER VE ATOM YAPISI Atom numaraları birbirlerine yakın elementlerin bazı izotopların n kütle k sayılar ları birbirlerine eşit e olabilir. Proton adedi farklı,, kütle k sayılar ları farklı atomlara izobar denir.
13 ELEMENTLER VE ATOM YAPISI ATOM MODELLERİ Lewis-Langmuir Langmuir Başlang langıçta küp k şeklinde ve elektronların n hareket etmediği i tahmin edilen model Bohr çekirdek etrafında güneş sistemine benzer belirli yörüngelerde dönen d elektronlar dalga mekaniği son olarak elektronların dalga hareketi yaptığı ve belirli bir bölgede b bulunması ihtimali olduğu u yörüngelery
14 ATOMLAR ARASI BAĞLAR
15 ATOMLAR ARASI BAĞLAR Atomların n son yörüngelerinde y en çok sekiz elektron bulunabilir (tek yörüngeli y atomlarda iki elektron). Tüm m atomlar son yörüngelerindeki y elektronları 8 yaparak soy gazlar gibi kararlı hale geçme eğilimindedirler. e
16 Atom Bağları Cisimlerin en küçük yapı birimi olan atomları, atomlar arası bağ kuvvetleri birarada tutar. Bu bağ kuvvetleri cismin mukavemetinin esasını oluşturur. Ayrıca elektriksel ve ısıl özellikleri belirler. Genellikle atomlar arası bağ kuvvetli ise şekil değiştirme direnci büyük, ergime sıcaklığı yüksek ve ısıl genleşme düşük olur. Atom bağları zayıf (fiziksel) veya kuvvetli (kimyasal) olabilir. Kimyasal bağlar üç şekilde olur.
17 ATOMLAR ARASI BAĞLAR BAĞ ÇE İTLERİ 1. İyonik Bağ 2. Kovalent Bağ 3. Metalik Bağ 4. Van Der Waals Bağı
18 ATOMLAR ARASI BAĞLAR Atomların n son yörüngelerinde y en çok sekiz elektron bulunabilir (tek yörüngeli y atomlarda iki elektron). İyonik bağ metaller ile ametaller arasında oluşur. ur.
19 ATOMLAR ARASI BAĞLAR İYONİK K BAĞ Son yörüngedeki y eksiklikler elektron alış ışverişi i ile sekize tamamlanır. Elektron kaybeder Na + Cl - Na (0) yüksüz Cl (0) yüksüz Elektron alır Na + (+) Katyon Cl - (-) Anyon + -
20 ATOMLAR ARASI BAĞLAR İYONİK K BAĞ İyonik bağ metaller ile ametaller arasında oluşur. ur.
21 ATOMLAR ARASI BAĞLAR KOVALENT BAĞ Elektronlar çekirdek etrafında döndd ndükleri gibi kendi eksenleri etrafında da dönerler. d Bu dönme d hareketi neticesinde elektromagnetik kuvvetler oluşur. ur
22 ATOMLAR ARASI BAĞLAR KOVALENT BAĞ Ametaller ile Ametaller arasında olur. Valans elektronlarının n ortak kullanımı söz z konusudur. Paylaşı şılan elektron ile pozitif çekirdek arasında çekim kuvveti oluşur. ur.
23 ATOMLAR ARASI BAĞLAR KOVALENT BAĞ Bu bağ genellikle gazlarda meydana gelir (H 2, NH 3, O 2, CH 4 ).
24 ATOMLAR ARASI BAĞLAR KOVALENT BAĞ Buzda her su molek Buzda her su molekülü diğer 4 molekül l tarafından sarılarak tetrahedronşeklinde eklinde bağlanm lanmıştır. Üç boyutta da hidrojen bağlar ları mevcuttur. Buz 0 o C de eriyince hidrojen bağlar larının n kabaca %15 i i kırılır. k r. Sonuç olarak tetrahedral yapı bozulur, her su molekülü komşu u 4 molekülden lden daha fazla moleküle bağlan lanır. Böylece yoğunluk den 1 e 1 çıkar.
25 ATOMLAR ARASI BAĞLAR KOVALENT BAĞ Katılardaki en güzel g örneği i ise kübik k yapıdaki elmastır. Silisyum, Germanyum, Karbon gibi elementler dört d kovalent bağ ile tetrahedron bağ oluştururlar. Bu tetrahedron gruplar birleşerek erek elmas kübik k yapı meydana getirirler.
26 ATOMLAR ARASI BAĞLAR METALİK K BAĞ Metaller son yörüngelerindeki y valans elektronlarını serbest bırakarak iyon haline gelirler. Serbest kalan elektronların metal çekirdeği i ile bağlar ları çok zayıft ftır r ve hiçbir atoma bağlı kalmadan metal çekirdekleri etrafında serbestçe e dolaşı şırlar.
27 ATOMLAR ARASI BAĞLAR METALİK K BAĞ Metal atomları birbirine yaklaştığı ığında son yörüngelerindeki enerji bantları birbirinin içine i ine girer ve serbest elektronlar bu bantlarda hareket edebilirler.
28 ATOMLAR ARASI BAĞLAR METALİK K BAĞ Metallerin valans elektronlarını serbest bırakmalarb rakmaları özelliği, i, iyi elektrik iletimi sağlamalar lamalarına sebep olur. Bu bantlar içinde i inde hareket eden negatif yükly klü elektronlar ile pozitif yükly klü çekirdek arasındaki çekim metalik bağı oluşturur
29 ATOMLAR ARASI BAĞLAR METALİK K BAĞ Metal atomları arasındaki bağ belirli atomlar ve elektronlara bağlı olmadığı için, in, atomların n birbirine göre hareket etmesi ile bu bağ kopmaz. Bu özellik metallerin şekillendirilebilmelerini sağlar.
30 ATOMLAR ARASI BAĞLAR VAN DER WAALS BAĞLARI Bu bağlar, elektron alış verişini ini tamamlamış moleküller ller veya son yörüngesindeki elektron sayısı sekiz olan inert gaz atomları arasında oluşan zayıf f bağlard lardır r ve üçşekilde olabilir: 1. Molekül l Kutuplaşmas ması 2. Ani Kutuplaşma 3. Hidrojen KöprK prüsü
31 ATOMLAR ARASI BAĞLAR VAN DER WAALS BAĞLARI MOLEKÜL L KUTUPLA MASI Kovalent bağ ile kurulmuş bir molekülde, lde, mesela hidrojen florür molekülünde paylaşı şılan elektronların çoğu florür atomu etrafında olacağı ğından, molekül içinde inde bir elektrik yüküy dengesizliği vardır. r. Molekülün n hidrojen tarafı + + H H Florür - H H Dipol + oluşumu umu Florür - + pozitif florür tarafı negatif olur ve bu iki yük y k farkı moleküller ller arası çekim kuvvetini oluşturur.
32 ATOMLAR ARASI MESAFE itme + + çekme + - itme itme - - itme
33 ATOMLAR ARASI MESAFE Metal atomları arasında oluşan itme ve çekme kuvvetlerinin kuvvetin Kuvvet Çekme Net kuvvet dengelendiği i durumdaki atomlar arasındaki uzaklığ ığa a atomlar arası İtme Atomlar arası mesafe mesafe denilir. Bu konumda içi enerji en r R a = R + r azdır; yani atomlar en a kararlı durumdadırlar. rlar.
34 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı Atomlar 3 boyutta belirli bir düzendedir. d Tüm T m malzeme boyunca süreklilis rekliliğini ini korur.
35 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı 2. Amorf Yapı Atomların n dizilişinde inde bir düzensizlik d vardır. r.
36 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı 2. Amorf Yapı 3. Bileşik ik Yapı Çok küçük üçük k kristal parçalar alarının n gelişig igüzel bir yığıy ığını vardır. r.
37 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı 2. Amorf Yapı 3. Bileşik ik Yapı 4. Kolloidal Yapı Çok küçük üçük k elemanlar halinde bazı cisimler, birbirlerinden ayrı olarak, ayrı faz veya aynı faz halinde bulunan başka bir cisim içinde i inde dağı ğılmıştır. Örneğin, dumanın n içinde i inde oldukça a küçük üçük çaplı yanmamış kömür r zerreciklerinin bulunması veya bir sıvının s n diğer bir sıvı içinde inde yayılmas lması bu tip yapılard lardır. r. Yol malzemelerinden bitüml mlü emülsiyonlar bu yapıdad dadır.
38 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı 2. Amorf Yapı 3. Bileşik ik Yapı 4. Kolloidal Yapı 5. Seramik Yapı Bir metal veya iki metal ile bir ametal atomun belirli steokimetrik oranlarda birleşmesiyle oluşurlar. urlar. Seramiklerde metal olmayan atom çoğunlukla oksijendir. Seramiklerde metaller katyon, ametaller ise anyon oluşumuna umuna neden olurlar. Böylece B seramiklerde iyonsal bağlar oldukça a yaygınd ndır. Ancak seramiklerde kovalan bağlara, kristal yapıya, ya, hatta amorf yapıya da rastlanır. r.
39 ATOMSAL YAPI TÜRLERT RLERĐ 1. Kristal (Metalik) Yapı Atomlar 3 boyutta belirli bir düzendedir. d Tüm T m malzeme boyunca süreklilis rekliliğini ini korur. 2. Amorf Yapı Atomların n dizilişinde inde bir düzensizlik d vardır. r. 3. Bileşik ik Yapı Çok küçük üçük k kristal parçalar alarının n gelişig igüzel bir yığıy ığını vardır. r. 4. Kolloidal Yapı Çok küçük üçük k elemanlar halinde bazı cisimler, birbirlerinden ayrı olarak, ayrı faz veya aynı faz halinde bulunan başka bir cisim içinde i inde dağı ğılmıştır. 5. Seramik Yapı Bir metal veya iki metal ile bir ametal atomun belirli steokimetrik oranlarda birleşmesiyle oluşurlar. urlar.
40 ATOMSAL YAPI TÜRLERT RLERĐ Kristal (Metalik) Yapı Amorf Yapı
41 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Metal atomları üç boyutlu olarak düzenli d bir diziliş meydana getirirler ki buna uzay kafesi denilir. Üç boyutlu olarak tekrarlanan en küçük üçük yapıya birim hücre h (kafes) denilir.
42 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi uzunlukları Açıları kübik a = b = c α = β = γ = 90
43 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi hekzagonal uzunlukları a = b c Açıları γ = β = 90, α = 120
44 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi tetragonal uzunlukları Açıları a = b c α = β = γ = 90
45 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi rombohedral uzunlukları Açıları a = b = c α = β = γ 90
46 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi uzunlukları Açıları ortorombik a b c α = β = γ = 90
47 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi monoklinik uzunlukları a b c Açıları α = β = 90, γ 90
48 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Kristal sistemi uzunlukları Açıları triklinik a b c α β γ 90
49 ATOMSAL YAPI TÜRLERT RLERĐ KRİSTAL (METALİK) YAPI Yapı Malzemesi olarak kullanılan lan metallerin kristal yapılar ları daha çok kübik k ve hekzagonal sisteme uymaktadır. Hacim Merkezli Kübik (hmk) Yüzey Merkezli Kübik (ymk) Sıkı dizilmiş hekzogonal (sdk)
50 ATOMSAL YAPI TÜRLERT RLERĐ Hacim Merkezli Kübik K (hmk( hmk) Küpün n tam merkezine bir atom ve köşelere k de birer atom yerleşmi miştir. Küp K p hacminin içinde inde kalan atom hacmi:
51 ATOMSAL YAPI TÜRLERT RLERĐ Yüzey Merkezli Kübik K (ymk( ymk): Küpün n her köşesine k birer atom ve her bir yüzeye de birer atom yerleşmi miştir. Küp K içinde inde kalan atom hacmi:
52 ATOMSAL YAPI TÜRLERT RLERĐ Sıkı Dizilmiş Hegzagonal (sdh): Atomlar taban düzlemde d altıgenin köşelerine ve bir tane de altıgenin tam ortasına yerleşmi miştir. İki taban düzlemi arasında taban düzlemindeki d üç atoma teğet et olacak şekilde üç tane atom yerleşmi miştir.
53 ATOMSAL YAPI TÜRLERT RLERĐ
54 ATOMSAL YAPI TÜRLERT RLERĐ Tipik bir metal kristali birim hücresinin h düzgün n bir blok şeklinde düzenlenmesinden oluşabilir. Kusursuz bir kristal yapının n herhangi iki hücresinin h karşı şılıklı yüzleri her iki hücre h için i in de ortak olur.
55 ATOMSAL YAPI TÜRLERT RLERĐ Metalik malzemelerin çoğu küçük k kristal kümeciklerinden oluştu tuğundan undan polikristal adını alırlar. Bu kristal kümeciklerinin kristal yapısı da kendi içinde i inde düzenlidir. d Kristal kümeciklerinin k ayrımını,, bunların n birim hücrelerinin değişik ik yönlerde dizilişinden inden anlayabiliriz.
56 ATOMSAL YAPI TÜRLERT RLERĐ Birleşen en kristal kümecikleri k arasında tane sınırıs adı verilen atomik bir boşluk vardır. r. Bu bölgede b belirli bir düzensizlik görülür. g r. İnce yapılı bir metalik cismin kristal kümecikleri k daha küçük k yapılıdır. Bu nedenle kaba tane yapılı kristale kıyasla daha çok tane sınırıs bulunmaktadır.
57 ATOMSAL YAPI TÜRLERT RLERĐ ALLOTROPİK K DEĞİ İ Ğİ İM Isı ve basınc ncın n etkisiyle bazı cisimlerin kristal yapılar larında değişimler imler olabilir. Örneğin, demirin C C de hacim merkezli kübik k kristal yapısı var iken, 910 C C C arasında kristal yapısı yüzey merkezli kübik k olur. Bu tip kristal yapı değişimine imine allotropik değişim im denir.
58 ATOMSAL YAPI TÜRLERT RLERĐ ANİZOTROP ZOTROPİ Tekil kristal kümeciklerinin k (monokristal( monokristal) özellikleri kristal eksenlerine göre g farklılıklar klar gösterir. g Monokristallerin yönlere göre g farklı davranış göstermesi nedeniyle; mekanik, fiziksel, kimyasal özellikleri, dışd etkilerin, uygulama doğrultusuna bağlı olarak, farklı değerler erler alabilir. Özelliklerin yönlere y göre g farklılık k göstermesine g anizotropi denir.
59 METALLERDE ERGĐME ve KRĐSTALLE STALLEŞME
60 METALLERDE ERGĐME ve KRĐSTALLE STALLEŞME Her bir maddenin atomları devamlı titreşim im yapar. Bu titreşim im o maddenin sıcakls caklığını belirler. Sıcaklık k yükseldiky kseldikçe e titreşim im artar, düştükçe d e azalır. Mutlak sıfır s sıcaklığında (-273( 273ºC) bütün b n atomların n titreşimleri imleri durur. Metallerin sıcakls caklığı arttıkça, a, atomların n titreşimleri imleri artar ve bu titreşimler imler atomlar arasındaki bağı zayıflat flatır. Titreşimlerin imlerin meydana getirdiği i enerji, metal atomlarını birbirine bağlayan enerjiyi geçince ergime dediğimiz imiz olay meydana gelir; yani metal sıvıs hale geçer. er.
61 METALLERDE ERGĐME ve KRĐSTALLE STALLEŞME Ergimiş bir metalin sıvıdan s katıya geçişinde inde meydana gelen kristalleşme iki safhada oluşur: ur: 1. Çekirdek oluşumu umu 2. Kristal büyümesi. b
62 TANE SINIRLARI METALLERDE ERGĐME ve KRĐSTALLE STALLEŞME Katıla laşma sırass rasında belirli düzlem grupları farklı yönlerde dizilir. Bu dizilme gruplarına tane sınırları denir. Tek kristalli yapılarda tane grupları aynı yönde gelişir ir ve tane sınırlars rları oluşmaz. Tane sınırlars rları yüksek enerjilidir. (Yüzey gerilimi) Tane sınırlars rları kimyasal reaksiyona girebildiği i için i in üzerine dökülen d kimyasallar ile tespit edilir.
63 METALLERDE ERGĐME ve KRĐSTALLE STALLEŞME KRİSTAL HATALARI Nokta Hataları Çizgi Hataları Yüzeysel Hatalar Segregasyon
64 KRĐSTAL HATALARI Nokta Hataları Boş Yer Boşyer yer: : (Porozite) Katıla laşma sırass rasında büzülme, b yeterli sıvıs olmaması veya içeride gaz hapsolması nedenleri ile oluşur. ur. Boş yer Süreksizlik Kesitte daralma Mukavemet kaybı nedenidir.
65 KRĐSTAL HATALARI Nokta Hataları Boş Yer Boşluklar atomların n kristal içerisinde i hareketlerini kolaylaştırır. r.
66 KRĐSTAL HATALARI Nokta Hataları Ara yer Ara Yer hataları Ara yer: Her hangi bir kristalde esas atomların n aralarındakilere daha küçük çaplı atomların n yerleşmesi ile oluşur. ur. Yer alan Yer alan: Her hangi bir kristalde esas atomların n yerine başka atomların yerleşmesi ile oluşur. ur.
67 KRĐSTAL HATALARI Çizgi Hataları Atomların n hatalı dizilişleri leri bir çizgi boyunca devam ederse çizgi hatası oluşur. ur. Çizgi hataları kenar dislokasyonu ve vida dislokasyonu olarak bilinir.
68 KRĐSTAL HATALARI Çizgi Hataları Kenar Dislokasyonu Kenar dislokasyonu,, kristal içinde i inde sona eren bir düzlemin kenarıdır. r. İşareti şeklindedir.
69 KRĐSTAL HATALARI Çizgi Hataları Vida Dislokasyonu Vida dislokasyonunda ise, çizgi etrafındaki atomların n dizilişi i vidanın n helisi gibidir. İşareti şeklindedir.
70 KRĐSTAL HATALARI Çizgi Hataları Vida Dislokasyonu
71 KRĐSTAL HATALARI Çizgi Hataları Kenar ve vida dislokasyonları çoğu zaman beraber bulunurlar ki; buna karışı ışık dislokasyon denilir. Dislokasyonlar,, atomların n denge mesafesini bozduğu u için i in kristalin enerjisini artırır. r.
72 KRĐSTAL HATALARI Çizgi Hataları Dislokasyon yoğunlu unluğu Birim hacimdeki dislokasyon çizgilerinin uzunluğu u olarak verilir. (mm / mm 2 )
73 KRĐSTAL HATALARI Yüzeysel hatalar Dış Yüzey: İç kısımdaki atomlar kendini çevreleyen atomlar ile denge durumunda olduğu u halde, metalin dışd yüzeye açılan a atomlarında denge durumu bozulmuştur. Küçük k AçılıA Tane Sınırı: S Kenar dislokasyonları biri birinin üzerine sıralanmass ralanması ile küçük üçük açılı tane sınırlars rları oluşur. ur. İki boyutlu olan bu sınırlarda s atomlar düzensiz yerleşirler Tane SınırlarS rları: Metal sıvıs halden katı hale geçerken erken genellikle çok sayıda kristal tanesi oluşur. ur. Katıla laşma tamamlandığı ığında tanelerin birleşti tiği yerlerde atom kalınl nlığında düzensiz d yerleşme oluşur ur
74 KRĐSTAL HATALARI Segregasyon Katıla laşma sırass rasında belirli malzemeler, belirli fazların, belirli bir yerde toplanması. Makro ya da mikro olabilir.
75 Metalik Yapı Kontrolü ve Bozuklukları Bir metalik malzemenin yapısı gerekli kesme, parlatma gibi hazırlıklar yapıldıktan sonra mikroskobik olarak incelenebilir. Bu çalışmalar şu açılardan çok yararlıdır: 1) Metalik göçmelerin nedenini açıklayabilirler, 2) Metalin geçmişini öğrenerek uygun fabrikasyon işlemini ortaya çıkarırlar, 3) Isıl işlemlerin yeterlilik derecesini saptarlar, 4) Alaşımların geliştirilmesine yardımcı olabilirler, 5) Metal bileşenleri ve özellikleri kestirilebilir.
76 Metalik kristal kümelerindeki kusurlar şöylece sıralanabilir : Tane sınırı bölgeleri bozuklukları, Yabancı iyonların varlığı, Mikroskobik yapı kontrolü işlemleri (kesme, parlatma) sonucu meydana gelen bozukluklar, Fazla sıcaklık nedeniyle ortaya çıkan bazı iyonların konum bozuklukları, Dislokasyonlar (Bazı iyon sıra ve düzlemlerinin yanlış yerlerde bulunabilmesi), Mozaik yapı çarpıklıkları.
77 Dokuz Eylül Üniversitesi Đnşaat Mühendisliği Bölümü YAPI MALZEMESĐ I DERSĐ KATI ÇĐSĐMLERĐN ĐÇ YAPISI Doç. Dr. Halit YAZICI
Dokuz Eylül Üniversitesi Đnşaat Mühendisliği Bölümü YAPI MALZEMESĐ I DERSĐ ĐÇ YAPISI YRD.DOÇ.DR. KAMĐLE TOSUN GÜZ YY.
 Dokuz Eylül Üniversitesi Đnşaat Mühendisliği Bölümü YAPI MALZEMESĐ I DERSĐ KATI ÇĐSĐMLERĐN ĐÇ YAPISI YRD.DOÇ.DR. KAMĐLE TOSUN 2010-2011-GÜZ YY. KATI ÇĐSĐMLERĐN ĐÇ YAPISI Đnşaat Mühendisliğinde, cisimlerin
Dokuz Eylül Üniversitesi Đnşaat Mühendisliği Bölümü YAPI MALZEMESĐ I DERSĐ KATI ÇĐSĐMLERĐN ĐÇ YAPISI YRD.DOÇ.DR. KAMĐLE TOSUN 2010-2011-GÜZ YY. KATI ÇĐSĐMLERĐN ĐÇ YAPISI Đnşaat Mühendisliğinde, cisimlerin
ATOMLAR ARASI BAĞLAR
 MALZEME 2. HAFTA 1 ATOMSAL BAĞ ATOMLAR ARASI BAĞLAR Atomlar, atomlar arası bağ kuvvetleri ile bir araya gelirler. Malzemenin en küçük yapı taşı olan atomları bağ kuvvetleri bir arada tutar. Atomsal bağların
MALZEME 2. HAFTA 1 ATOMSAL BAĞ ATOMLAR ARASI BAĞLAR Atomlar, atomlar arası bağ kuvvetleri ile bir araya gelirler. Malzemenin en küçük yapı taşı olan atomları bağ kuvvetleri bir arada tutar. Atomsal bağların
MALZEME BİLGB ATOM YAPISI. Yrd. Doç. Dr. Hayri ÜN. Pamukkale Üniversitesi 2007 - BAHAR
 2 MALZEME BİLGB LGİSİ ATOM YAPISI Yrd. Doç. Dr. Hayri ÜN Pamukkale Üniversitesi 2007 - BAHAR GİRİŞİŞ Herhangi bir yapının projelendirmesi ve inşaatı aşamasında, inşaat mühendisinin görevi ve amacı, aşağıda
2 MALZEME BİLGB LGİSİ ATOM YAPISI Yrd. Doç. Dr. Hayri ÜN Pamukkale Üniversitesi 2007 - BAHAR GİRİŞİŞ Herhangi bir yapının projelendirmesi ve inşaatı aşamasında, inşaat mühendisinin görevi ve amacı, aşağıda
Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I
 Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I 2. Katı Cisimlerin İç Yapısı 2.1. Atom Yapısı 2.2. Atom Bağları 2.3. Atomsal Yapı Türleri 2.3.1. Metalik (Kristal) Yapı 2.3.2. Amorf
Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I 2. Katı Cisimlerin İç Yapısı 2.1. Atom Yapısı 2.2. Atom Bağları 2.3. Atomsal Yapı Türleri 2.3.1. Metalik (Kristal) Yapı 2.3.2. Amorf
Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I
 Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I 2. Katı Cisimlerin İç Yapısı 2.1. Atom Yapısı 2.2. Atom Bağları 2.3. Atomsal Yapı Türleri 2.3.1. Metalik (Kristal) Yapı 2.3.2. Amorf
Dokuz Eylül Üniversitesi İnşaat Mühendisliği Bölümü YAPI MALZEMESİ -I 2. Katı Cisimlerin İç Yapısı 2.1. Atom Yapısı 2.2. Atom Bağları 2.3. Atomsal Yapı Türleri 2.3.1. Metalik (Kristal) Yapı 2.3.2. Amorf
ATOMSAL YAPI TÜRLERİ Metalik malzemelerin çoğu küçük kristal kümeciklerinden oluştuğundan polikristal adını alırlar. Bu kristal kümeciklerinin
 ATOMSAL YAPI TÜRLERİ Metalik malzemelerin çoğu küçük kristal kümeciklerinden oluştuğundan polikristal adını alırlar. Bu kristal kümeciklerinin kristal yapısıda kendi içinde düzenlidir. Kristal kümeciklerinin
ATOMSAL YAPI TÜRLERİ Metalik malzemelerin çoğu küçük kristal kümeciklerinden oluştuğundan polikristal adını alırlar. Bu kristal kümeciklerinin kristal yapısıda kendi içinde düzenlidir. Kristal kümeciklerinin
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
MALZEME BİLGİSİ. Katı Eriyikler
 MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Katı Eriyikler 1 Giriş Endüstriyel metaller çoğunlukla birden fazla tür eleman içerirler, çok azı arı halde kullanılır. Arı metallerin yüksek iletkenlik, korozyona
MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Katı Eriyikler 1 Giriş Endüstriyel metaller çoğunlukla birden fazla tür eleman içerirler, çok azı arı halde kullanılır. Arı metallerin yüksek iletkenlik, korozyona
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ
 ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
BÖLÜM 2 ATOMİK YAPI İÇERİK. Atom yapısı. Bağ tipleri. Chapter 2-1
 BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
BÖLÜM 2 ATOMİK YAPI İÇERİK. Atom yapısı. Bağ tipleri. Chapter 2-1
 BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
KRİSTAL KAFES SİSTEMLERİ
 KRİSTAL KAFES SİSTEMLERİ Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA 1 Giriş 2 Kristal Yapısı ve Birim Hücreler
KRİSTAL KAFES SİSTEMLERİ Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA 1 Giriş 2 Kristal Yapısı ve Birim Hücreler
BİYOLOJİK MOLEKÜLLERDEKİ
 BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
FZM 220. Malzeme Bilimine Giriş
 FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Atomsal Yapı ve Atomlararası Bağ1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin
FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Atomsal Yapı ve Atomlararası Bağ1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin
MALZEME BİLGİSİ DERS 4 DR. FATİH AY.
 MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.
 ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR. Aytekin Hitit
 ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
1. Düzensiz yapı : Atom veya moleküllerin rastgele dizilmesi. Argon gibi asal gazlarda görülür.
 Malzemeler atomların bir araya gelmesi ile oluşur. Bu yapı içerisinde atomları bir arada tutan kuvvete atomlar arası bağ denir. Yapı içerisinde bir arada bulunan atomlar farklı düzenlerde bulunabilir.
Malzemeler atomların bir araya gelmesi ile oluşur. Bu yapı içerisinde atomları bir arada tutan kuvvete atomlar arası bağ denir. Yapı içerisinde bir arada bulunan atomlar farklı düzenlerde bulunabilir.
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN. Temel kavramlar Atomsal yapı
 Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Temel kavramlar Atomsal yapı İçerik Temel kavramlar Atom modeli Elektron düzeni Periyodik sistem 2 Temel kavramlar Bütün maddeler kimyasal elementlerden oluşur.
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Temel kavramlar Atomsal yapı İçerik Temel kavramlar Atom modeli Elektron düzeni Periyodik sistem 2 Temel kavramlar Bütün maddeler kimyasal elementlerden oluşur.
MALZEMENİN İÇ YAPISI: Katılarda Atomsal Bağ
 MALZEMENİN İÇ YAPISI: Katılarda Atomsal Bağ Bölüm İçeriği Bağ Enerjisi ve Kuvveti Atomlar arası mesafe, Kuvvet ve Enerji İlişkisi Atomlar arası Mesafeyi Etkileyen Faktörler. Sıcaklık, Iyonsallik derecesi,
MALZEMENİN İÇ YAPISI: Katılarda Atomsal Bağ Bölüm İçeriği Bağ Enerjisi ve Kuvveti Atomlar arası mesafe, Kuvvet ve Enerji İlişkisi Atomlar arası Mesafeyi Etkileyen Faktörler. Sıcaklık, Iyonsallik derecesi,
KATILARIN ATOMİK DÜZENİ KRİSTAL YAPILAR
 KATILARIN ATOMİK DÜZENİ KRİSTAL YAPILAR KRİSTAL YAPILAR Mühendislik açısından önemli olan katı malzemelerin fiziksel özelikleri; katı malzemeleri meydana getiren atom, iyon veya moleküllerin dizilişine
KATILARIN ATOMİK DÜZENİ KRİSTAL YAPILAR KRİSTAL YAPILAR Mühendislik açısından önemli olan katı malzemelerin fiziksel özelikleri; katı malzemeleri meydana getiren atom, iyon veya moleküllerin dizilişine
Katılar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN. Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 2006
 Katılar Tüm maddeler, yeteri kadar soğutulduğunda katıları oluştururlar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Oluşan katıların doğası atom, iyon veya molekülleri birarada tutan kuvvetlere
Katılar Tüm maddeler, yeteri kadar soğutulduğunda katıları oluştururlar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Oluşan katıların doğası atom, iyon veya molekülleri birarada tutan kuvvetlere
ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur.
 DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır.
 14 DENEY KATI HAL 1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır. 2. Giriş Atomlar arası (veya moleküller arası) çekim kuvvetleri
14 DENEY KATI HAL 1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır. 2. Giriş Atomlar arası (veya moleküller arası) çekim kuvvetleri
BMM 205 Malzeme Biliminin Temelleri
 BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
INSA 283 MALZEME BİLİMİ. Giriş
 INSA 283 MALZEME BİLİMİ Giriş Malzeme Gereksinimi Bütün mühendislik bilim dallari malzeme ile yakindan iliskilidir. Mühendisler kullanacaklari malzemeyi çok iyi tanıyarak ve genis malzeme tayfi içinde
INSA 283 MALZEME BİLİMİ Giriş Malzeme Gereksinimi Bütün mühendislik bilim dallari malzeme ile yakindan iliskilidir. Mühendisler kullanacaklari malzemeyi çok iyi tanıyarak ve genis malzeme tayfi içinde
ATOM BİLGİSİ Atom Modelleri
 1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
Gelin bugün bu yazıda ilkokul sıralarından beri bize öğretilen bilgilerden yeni bir şey keşfedelim, ya da ne demek istediğini daha iyi anlayalım.
 Kristal Yapılar Gelin bugün bu yazıda ilkokul sıralarından beri bize öğretilen bilgilerden yeni bir şey keşfedelim, ya da ne demek istediğini daha iyi anlayalım. Evrende, kimyasal özellik barındıran maddelerin
Kristal Yapılar Gelin bugün bu yazıda ilkokul sıralarından beri bize öğretilen bilgilerden yeni bir şey keşfedelim, ya da ne demek istediğini daha iyi anlayalım. Evrende, kimyasal özellik barındıran maddelerin
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ
 KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
Soygazların bileşik oluşturamamasının sebebi bütün orbitallerinin dolu olmasındandır.
 KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
Prof. Dr. İRFAN AY / Öğr. Gör. FAHRETTİN KAPUSUZ 1
 MAKİNE PROGRAMI MALZEME TEKNOLOJİSİ-I- (DERS NOTLARI) Prof.Dr.İrfan AY Öğr. Gör. Fahrettin Kapusuz 2008-20092009 BALIKESİR Prof. Dr. İRFAN AY / Öğr. Gör. FAHRETTİN KAPUSUZ 1 ATOMİK YAPI VE BAĞ KUVVETLERİ
MAKİNE PROGRAMI MALZEME TEKNOLOJİSİ-I- (DERS NOTLARI) Prof.Dr.İrfan AY Öğr. Gör. Fahrettin Kapusuz 2008-20092009 BALIKESİR Prof. Dr. İRFAN AY / Öğr. Gör. FAHRETTİN KAPUSUZ 1 ATOMİK YAPI VE BAĞ KUVVETLERİ
KRİSTAL YAPISI VE KRİSTAL SİSTEMLERİ
 KRİSTAL YAPISI VE KRİSTAL SİSTEMLERİ Kristal Yapı: Atomların, üç boyutlu uzayda düzenli (kendini tekrar eden) bir şekilde dizilmesiyle oluşan yapıya kristal yapı denir. Bir kristal yapı birim hücresiyle
KRİSTAL YAPISI VE KRİSTAL SİSTEMLERİ Kristal Yapı: Atomların, üç boyutlu uzayda düzenli (kendini tekrar eden) bir şekilde dizilmesiyle oluşan yapıya kristal yapı denir. Bir kristal yapı birim hücresiyle
Element atomlarının atom ve kütle numaraları element sembolleri üzerinde gösterilebilir. Element atom numarası sembolün sol alt köşesine yazılır.
 Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
FZM 220. Malzeme Bilimine Giriş
 FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin amacı, fizik mühendisliği öğrencilerine,
FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin amacı, fizik mühendisliği öğrencilerine,
TEKNOLOJİSİ--ITEKNOLOJİSİ. Prof. Dr. İRFAN AY / Öğr. Gör. FAHRETTİN KAPUSUZ
 MAKİNE PROGRAMI MALZEME TEKNOLOJİSİ--ITEKNOLOJİSİ (DERS NOTLARI) Prof.Dr.İrfan AY Öğr. Gör. Fahrettin Kapusuz 2008-2009 2008BALIKESİR 1 ATOMİK YAPI VE BAĞ KUVVETLERİ 2 MALZEMLERİN ATOMİK YAPISI Her element
MAKİNE PROGRAMI MALZEME TEKNOLOJİSİ--ITEKNOLOJİSİ (DERS NOTLARI) Prof.Dr.İrfan AY Öğr. Gör. Fahrettin Kapusuz 2008-2009 2008BALIKESİR 1 ATOMİK YAPI VE BAĞ KUVVETLERİ 2 MALZEMLERİN ATOMİK YAPISI Her element
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır:
 Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
BÖLÜM 2. Kristal Yapılar ve Kusurlar
 BÖLÜM 2 Kristal Yapılar ve Kusurlar 1- ATOMİK VE İYONİK DÜZENLER Kısa Mesafeli Düzenler-Uzun Mesafeli Düzenler Kısa Mesafeli Düzenler (SRO): Kısa mesafede atomların tahmin edilebilir düzenlilikleridir.
BÖLÜM 2 Kristal Yapılar ve Kusurlar 1- ATOMİK VE İYONİK DÜZENLER Kısa Mesafeli Düzenler-Uzun Mesafeli Düzenler Kısa Mesafeli Düzenler (SRO): Kısa mesafede atomların tahmin edilebilir düzenlilikleridir.
Katılar & Kristal Yapı
 Katılar & Kristal Yapı Katılar Kristal katılar Amorf katılar Belli bir geometrik şekle sahip olan katılardır, tanecikleri belli bir düzene göre istiflenir. Belli bir geometrik şekli olmayan katılardır,
Katılar & Kristal Yapı Katılar Kristal katılar Amorf katılar Belli bir geometrik şekle sahip olan katılardır, tanecikleri belli bir düzene göre istiflenir. Belli bir geometrik şekli olmayan katılardır,
CALLİSTER - SERAMİKLER
 CALLİSTER - SERAMİKLER Atomik bağı ağırlıklı olarak iyonik olan seramik malzemeler için, kristal yapılarının atomların yerine elektrikle yüklü iyonlardan oluştuğu düşünülebilir. Metal iyonları veya katyonlar
CALLİSTER - SERAMİKLER Atomik bağı ağırlıklı olarak iyonik olan seramik malzemeler için, kristal yapılarının atomların yerine elektrikle yüklü iyonlardan oluştuğu düşünülebilir. Metal iyonları veya katyonlar
Aşağıda verilen özet bilginin ayrıntısını, ders kitabı. olarak önerilen, Erdik ve Sarıkaya nın Temel. Üniversitesi Kimyası" Kitabı ndan okuyunuz.
 KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN. Atom ve moleküller arası Atomsal bağlar
 Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Atom ve moleküller arası Atomsal bağlar İçerik Atomlararası denge mesafesi Elastisite modülü Atomlar niçin bağ yapmak ister? İyonik bağ Kovalent bağ Metalik bağ
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Atom ve moleküller arası Atomsal bağlar İçerik Atomlararası denge mesafesi Elastisite modülü Atomlar niçin bağ yapmak ister? İyonik bağ Kovalent bağ Metalik bağ
Bazı atomlarda proton sayısı aynı olduğu halde nötron sayısı değişiktir. Bunlara izotop denir. Şekil II.1. Bir atomun parçaları
 8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010
 METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010 WEBSİTE www2.aku.edu.tr/~hitit Dersler İÇERİK Metalik Malzemelerin Genel Karakteristiklerİ Denge diyagramları Ergitme ve döküm Dökme demir ve çelikler
METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010 WEBSİTE www2.aku.edu.tr/~hitit Dersler İÇERİK Metalik Malzemelerin Genel Karakteristiklerİ Denge diyagramları Ergitme ve döküm Dökme demir ve çelikler
Atomların bir arada tutulmalarını sağlayan kuvvetlerdir Atomlar daha düşük enerjili duruma erişmek (daha kararlı olmak) için bir araya gelirler
 Kimyasal Bağlar; Atomların bir arada tutulmalarını sağlayan kuvvetlerdir Atomlar daha düşük enerjili duruma erişmek (daha kararlı olmak) için bir araya gelirler İki ana gruba ayrılır Kuvvetli (birincil,
Kimyasal Bağlar; Atomların bir arada tutulmalarını sağlayan kuvvetlerdir Atomlar daha düşük enerjili duruma erişmek (daha kararlı olmak) için bir araya gelirler İki ana gruba ayrılır Kuvvetli (birincil,
MMT407 Plastik Şekillendirme Yöntemleri
 K O C A E L İ ÜNİVERSİTESİ Metalurji ve Malzeme Mühendisliği Bölümü MMT407 Plastik Şekillendirme Yöntemleri 3 Şekillendirmenin Metalurjik Esasları Yrd. Doç. Dr. Ersoy Erişir 2012-2013 Güz Yarıyılı 3. Şekillendirmenin
K O C A E L İ ÜNİVERSİTESİ Metalurji ve Malzeme Mühendisliği Bölümü MMT407 Plastik Şekillendirme Yöntemleri 3 Şekillendirmenin Metalurjik Esasları Yrd. Doç. Dr. Ersoy Erişir 2012-2013 Güz Yarıyılı 3. Şekillendirmenin
izotop MALZEME BILGISI B2
 1. Giriş 2. Temel Kavramlar 3. Atomlarda Elektronlar 4. Periyodik Tablo 5. Bağ Kuvvetleri ve Enerjileri 6. Atomlararası Birincil Bağlar 7. İkincil bağlar veya Van Der Waals Bağları 8. Moleküller Bu özelliklerinden
1. Giriş 2. Temel Kavramlar 3. Atomlarda Elektronlar 4. Periyodik Tablo 5. Bağ Kuvvetleri ve Enerjileri 6. Atomlararası Birincil Bağlar 7. İkincil bağlar veya Van Der Waals Bağları 8. Moleküller Bu özelliklerinden
KATILARDA KRİSTAL YAPI. Hekzagonal a b c 90 o, 120. Tetragonal a b c 90 o. Rombohedral (Trigonal) Ortorombik a b c 90 o. Monoklinik a b c 90 o
 KATILARDA KRİSTAL YAPI Kristal yapı atomun bir üst seviyesinde incelenen ve atomların katı halde oluşturduğu düzeni ifade eden birim hücre (kafes) geometrik parametreleri ve atom dizilimi ile tarif edilen
KATILARDA KRİSTAL YAPI Kristal yapı atomun bir üst seviyesinde incelenen ve atomların katı halde oluşturduğu düzeni ifade eden birim hücre (kafes) geometrik parametreleri ve atom dizilimi ile tarif edilen
İmal Usulleri 1. Fatih ALİBEYOĞLU -1-
 1 Fatih ALİBEYOĞLU -1- İMALATA GİRİŞ ve GENEL BAKIŞ Öğretim Görevlisi Fatih Alibeyoğlu Dersin İçeriği nin İlkeleri ve Sınıflandırılması Döküm Plastik Şekil Verme Esasları Plastik Şekil Verme Yöntemleri
1 Fatih ALİBEYOĞLU -1- İMALATA GİRİŞ ve GENEL BAKIŞ Öğretim Görevlisi Fatih Alibeyoğlu Dersin İçeriği nin İlkeleri ve Sınıflandırılması Döküm Plastik Şekil Verme Esasları Plastik Şekil Verme Yöntemleri
MALZEME BİLGİSİ. Kristal Yapılar ve Kristal Geometrisi
 MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Kristal Yapılar ve Kristal Geometrisi 1 KRİSTAL YAPILAR Malzemelerin iç yapısı atomların diziliş biçimine bağlıdır. Kristal yapı Kristal yapılarda atomlar düzenli
MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Kristal Yapılar ve Kristal Geometrisi 1 KRİSTAL YAPILAR Malzemelerin iç yapısı atomların diziliş biçimine bağlıdır. Kristal yapı Kristal yapılarda atomlar düzenli
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Periyodik Tablo(sistem)
 Periyodik Tablo(sistem) Geçmişten Günümüze Periyodik Tablo Bilim adamları elementlerin sayısı arttıkça bunları benzer özelliklerine göre sıralamaya çalışmışlardır.(bunu süpermarketlerdeki ürünlerin dizilişlerine
Periyodik Tablo(sistem) Geçmişten Günümüze Periyodik Tablo Bilim adamları elementlerin sayısı arttıkça bunları benzer özelliklerine göre sıralamaya çalışmışlardır.(bunu süpermarketlerdeki ürünlerin dizilişlerine
Bölüm 3 - Kristal Yapılar
 Bölüm 3 - Kristal Yapılar Katı malzemeler, atomların veya iyonların oluşturdukları düzene göre sınıflandırılır. Kristal malzemede uzun-aralıkta atomsal ölçekte tekrarlayan bir düzen mevcuttur. Katılaşma
Bölüm 3 - Kristal Yapılar Katı malzemeler, atomların veya iyonların oluşturdukları düzene göre sınıflandırılır. Kristal malzemede uzun-aralıkta atomsal ölçekte tekrarlayan bir düzen mevcuttur. Katılaşma
ATOM BİLGİSİ I ÖRNEK 1
 ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
ATOMUN YAPISI ATOMUN ÖZELLİKLERİ
 ATOM Elementlerin özelliğini taşıyan, en küçük yapı taşına, atom diyoruz. veya, fiziksel ve kimyasal yöntemlerle daha basit birimlerine ayrıştırılamayan, maddenin en küçük birimine atom denir. Helyum un
ATOM Elementlerin özelliğini taşıyan, en küçük yapı taşına, atom diyoruz. veya, fiziksel ve kimyasal yöntemlerle daha basit birimlerine ayrıştırılamayan, maddenin en küçük birimine atom denir. Helyum un
Bir kristal malzemede uzun-aralıkta düzen mevcu4ur.
 Bir kristal malzemede uzun-aralıkta düzen mevcu4ur. Kristal ka8ların bazı özellikleri, malzemelerin kristal yapılarına, yani atomların, iyonların ya da moleküllerin üç boyutlu olarak meydana ge@rdikleri
Bir kristal malzemede uzun-aralıkta düzen mevcu4ur. Kristal ka8ların bazı özellikleri, malzemelerin kristal yapılarına, yani atomların, iyonların ya da moleküllerin üç boyutlu olarak meydana ge@rdikleri
FZM 220. Malzeme Bilimine Giriş
 FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin amacı, fizik mühendisliği öğrencilerine,
FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin amacı, fizik mühendisliği öğrencilerine,
MALZEME BILIMI DERS NOTU
 MALZEME BILIMI DERS NOTU Bölüm 2. Malzemelerin Yapısı ve Atomik ve İyonik Düzenler Doç. Dr. Özkan ÖZDEMİR HEDEFLER: Yapının bağlı olduğu fiziksel kavramları tanımlamak, Atomların yapısı- bağlar-mühendislik
MALZEME BILIMI DERS NOTU Bölüm 2. Malzemelerin Yapısı ve Atomik ve İyonik Düzenler Doç. Dr. Özkan ÖZDEMİR HEDEFLER: Yapının bağlı olduğu fiziksel kavramları tanımlamak, Atomların yapısı- bağlar-mühendislik
Bölüm 4: Kusurlar. Kusurlar
 Bölüm 4: Kusurlar Malzemelerin bazı özellikleri kusurların varlığıyla önemli derecede etkilenir. Kusurların türleri ve malzeme davranışı üzerindeki etkileri hakkında bilgi sahibi olmak önemlidir. Saf metallerin
Bölüm 4: Kusurlar Malzemelerin bazı özellikleri kusurların varlığıyla önemli derecede etkilenir. Kusurların türleri ve malzeme davranışı üzerindeki etkileri hakkında bilgi sahibi olmak önemlidir. Saf metallerin
A. ATOMUN TEMEL TANECİKLERİ
 ÜNİTE 3 MADDENİN YAPISI VE ÖZELLİKLERİ 1. BÖLÜM MADDENİN TANECİKLİ YAPISI 1- ATOMUN YAPISI Maddenin taneciklerden oluştuğu fikri yani atom kavramı ilk defa demokritus tarafından ortaya atılmıştır. Örneğin;
ÜNİTE 3 MADDENİN YAPISI VE ÖZELLİKLERİ 1. BÖLÜM MADDENİN TANECİKLİ YAPISI 1- ATOMUN YAPISI Maddenin taneciklerden oluştuğu fikri yani atom kavramı ilk defa demokritus tarafından ortaya atılmıştır. Örneğin;
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar.
 Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6
 PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
Bir atomdan diğer bir atoma elektron aktarılmasıyla
 kimyasal bağlar Kimyasal bağ, moleküllerde atomları bir arada tutan kuvvettir. Atomlar daha düşük enerjili duruma erişmek için bir araya gelirler. Bir bağın oluşabilmesi için atomlar tek başına bulundukları
kimyasal bağlar Kimyasal bağ, moleküllerde atomları bir arada tutan kuvvettir. Atomlar daha düşük enerjili duruma erişmek için bir araya gelirler. Bir bağın oluşabilmesi için atomlar tek başına bulundukları
Malzemelerin Deformasyonu
 Malzemelerin Deformasyonu Malzemelerin deformasyonu Kristal, etkiyen kuvvete deformasyon ile cevap verir. Bir malzemeye yük uygulandığında malzeme üzerinde çeşitli yönlerde ve çeşitli şekillerde yükler
Malzemelerin Deformasyonu Malzemelerin deformasyonu Kristal, etkiyen kuvvete deformasyon ile cevap verir. Bir malzemeye yük uygulandığında malzeme üzerinde çeşitli yönlerde ve çeşitli şekillerde yükler
Malzemeler yapılarının içerisinde, belli oranlarda farklı atomları çözebilirler. Bu durum katı çözeltiler olarak adlandırılır.
 KATI ÇÖZELTİ Malzemeler yapılarının içerisinde, belli oranlarda farklı atomları çözebilirler. Bu durum katı çözeltiler olarak adlandırılır. Katı çözeltilerin diğer bir ismi katı eriyiktir. Bir çözelti
KATI ÇÖZELTİ Malzemeler yapılarının içerisinde, belli oranlarda farklı atomları çözebilirler. Bu durum katı çözeltiler olarak adlandırılır. Katı çözeltilerin diğer bir ismi katı eriyiktir. Bir çözelti
FİZ 427 KRİSTAL FİZİĞİ
 FİZ 427 KRİSTAL FİZİĞİ 1. Madde nedir? Kaça ayrılır? Fiziksel Özellikler Kimyasal Özellikler Ortak ve Ayırtedici özellikler 2. Katı nedir? Katı maddenin özellikleri Katı cisimler kaça ayrılır? 3. Mükemmel
FİZ 427 KRİSTAL FİZİĞİ 1. Madde nedir? Kaça ayrılır? Fiziksel Özellikler Kimyasal Özellikler Ortak ve Ayırtedici özellikler 2. Katı nedir? Katı maddenin özellikleri Katı cisimler kaça ayrılır? 3. Mükemmel
Malzeme Bilimi I Metalurji ve Malzeme Mühendisliği
 I Metalurji ve Malzeme Mühendisliği Doç. Dr. Rıdvan YAMANOĞLU 2017-2018 Metaller katılaşırken kendilerine has, elektron düzenlerinin neden olduğu belli bir kafes sisteminde kristalleşirler. Aluminyum,
I Metalurji ve Malzeme Mühendisliği Doç. Dr. Rıdvan YAMANOĞLU 2017-2018 Metaller katılaşırken kendilerine has, elektron düzenlerinin neden olduğu belli bir kafes sisteminde kristalleşirler. Aluminyum,
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA MOLEKÜLLER ARASI KUVVETLER Moleküller Arası Kuvvetler Yüksek basınç ve düşük sıcaklıklarda moleküller arası kuvvetler gazları ideallikten saptırır. Moleküller arası kuvvetler molekülde kalıcı
GENEL KİMYA MOLEKÜLLER ARASI KUVVETLER Moleküller Arası Kuvvetler Yüksek basınç ve düşük sıcaklıklarda moleküller arası kuvvetler gazları ideallikten saptırır. Moleküller arası kuvvetler molekülde kalıcı
ATOMUN YAPISI. Özhan ÇALIŞ. Bilgi İletişim ve Teknolojileri
 ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
MMM291 MALZEME BİLİMİ
 MMM291 MALZEME BİLİMİ Ofis Saatleri: Perşembe 14:00 16:00 ayse.kalemtas@btu.edu.tr, akalemtas@gmail.com Bursa Teknik Üniversitesi, Doğa Bilimleri, Mimarlık ve Mühendislik Fakültesi, Metalurji ve Malzeme
MMM291 MALZEME BİLİMİ Ofis Saatleri: Perşembe 14:00 16:00 ayse.kalemtas@btu.edu.tr, akalemtas@gmail.com Bursa Teknik Üniversitesi, Doğa Bilimleri, Mimarlık ve Mühendislik Fakültesi, Metalurji ve Malzeme
ELEKTRONLARIN DĠZĠLĠMĠ
 ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
CANLILARIN KİMYASAL İÇERİĞİ
 CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
BÖLÜM 3. Katı malzemeler yapılarındaki atom ve iyonların birbirlerine göre düzenlerine bağlı olarak sınıflandırılırlar.
 KRİSTAL YAPISI ve KRİSTAL KUSURLARI Katı malzemeler yapılarındaki atom ve iyonların birbirlerine göre düzenlerine bağlı olarak sınıflandırılırlar. Kristal yapı içinde atomlar büyük atomik mesafeler boyunca
KRİSTAL YAPISI ve KRİSTAL KUSURLARI Katı malzemeler yapılarındaki atom ve iyonların birbirlerine göre düzenlerine bağlı olarak sınıflandırılırlar. Kristal yapı içinde atomlar büyük atomik mesafeler boyunca
2. KATI CİSİMLERİN İÇ YAPISI
 2. KATI CİSİMLERİN İÇ YAPISI İnşaat Mühendisliğinde, cisimlerin yükler altındaki davranışını saptayabilmek çok önemlidir. Yapının tasarımı, boyutlandırma ve kesin hesapları açısından malzemenin "mekanik
2. KATI CİSİMLERİN İÇ YAPISI İnşaat Mühendisliğinde, cisimlerin yükler altındaki davranışını saptayabilmek çok önemlidir. Yapının tasarımı, boyutlandırma ve kesin hesapları açısından malzemenin "mekanik
KĠMYASAL ÖZELLĠKLER VE KĠMYASAL BAĞ
 Elektronların Dizilimi ve Kimyasal Özellikler Atomların katmanlarında belirli sayılarda elektron bulunmaktadır. Ancak bir atom, tek katmanlıysa ve bu katmanda iki elektronu varsa kararlıdır. Atomun iki
Elektronların Dizilimi ve Kimyasal Özellikler Atomların katmanlarında belirli sayılarda elektron bulunmaktadır. Ancak bir atom, tek katmanlıysa ve bu katmanda iki elektronu varsa kararlıdır. Atomun iki
 2007-2008 GÜZ YARIYILI MALZEME I Malzeme Bilimi ve Mühendisliğine Giriş Malzemelerin İç Yapısı 01.10.2007 1 ÖĞRETİM ÜYELERİ ve KAYNAKLAR Yrd.Doç.Dr. Şeyda POLAT Yrd.Doç.Dr. Ömer YILDIZ Ders Kitabı : Malzeme
2007-2008 GÜZ YARIYILI MALZEME I Malzeme Bilimi ve Mühendisliğine Giriş Malzemelerin İç Yapısı 01.10.2007 1 ÖĞRETİM ÜYELERİ ve KAYNAKLAR Yrd.Doç.Dr. Şeyda POLAT Yrd.Doç.Dr. Ömer YILDIZ Ders Kitabı : Malzeme
Boya eklenmesi Kısmen karışma Homojenleşme
 DİFÜZYON 1 Katı içerisindeki atomların hareketi yüksek konsantrasyon bölgelerinden düşük konsantrasyon bölgelerine doğrudur. Kayma olayından farklıdır. Kaymada hareketli atom düzlemlerindeki bütün atomlar
DİFÜZYON 1 Katı içerisindeki atomların hareketi yüksek konsantrasyon bölgelerinden düşük konsantrasyon bölgelerine doğrudur. Kayma olayından farklıdır. Kaymada hareketli atom düzlemlerindeki bütün atomlar
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
MALZEME BİLİMİ (DERS NOTLARI)
 MALZEME BİLİMİ (DERS NOTLARI) Bölüm 4. Malzemelerde Atom ve İyon Hareketleri Doç.Dr. Özkan ÖZDEMİR Doç. Dr. Özkan ÖZDEMİR Hedefler Malzemelerde difüzyon uygulamalarını ve prensipleri incelemek. Difüzyonun
MALZEME BİLİMİ (DERS NOTLARI) Bölüm 4. Malzemelerde Atom ve İyon Hareketleri Doç.Dr. Özkan ÖZDEMİR Doç. Dr. Özkan ÖZDEMİR Hedefler Malzemelerde difüzyon uygulamalarını ve prensipleri incelemek. Difüzyonun
Dielektrik malzeme DİELEKTRİK ÖZELLİKLER. Elektriksel Kutuplaşma. Dielektrik malzemeler. Kutuplaşma Türleri 15.4.2015. Elektronik kutuplaşma
 Dielektrik malzeme DİELEKTRİK ÖZELLİKLER Dielektrik malzemeler; serbest elektron yoktur, yalıtkan malzemelerdir, uygulanan elektriksel alandan etkilenebilirler. 1 2 Dielektrik malzemeler Elektriksel alan
Dielektrik malzeme DİELEKTRİK ÖZELLİKLER Dielektrik malzemeler; serbest elektron yoktur, yalıtkan malzemelerdir, uygulanan elektriksel alandan etkilenebilirler. 1 2 Dielektrik malzemeler Elektriksel alan
MALZEME BİLGB METALLERDE STALLEŞME. Yrd. Doç. Dr. Hayri ÜN. Pamukkale Üniversitesi 2007 - BAHAR
 3 MALZEME BİLGB LGİSİ METALLERDE ERGİME ve KRİSTALLE STALLEŞME Yrd. Doç. Dr. Hayri ÜN Pamukkale Üniversitesi 2007 - BAHAR METALLERDE ERGİME ve KRİSTALLE STALLEŞME Her bir maddenin atomları devamlı titreşim
3 MALZEME BİLGB LGİSİ METALLERDE ERGİME ve KRİSTALLE STALLEŞME Yrd. Doç. Dr. Hayri ÜN Pamukkale Üniversitesi 2007 - BAHAR METALLERDE ERGİME ve KRİSTALLE STALLEŞME Her bir maddenin atomları devamlı titreşim
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN. Kristalleşme ve kusurlar Kristal Yapılar
 Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Kristalleşme ve kusurlar Kristal Yapılar İçerik Kristalleşme Kristal yapı kusurları Noktasal kusurlar Çizgisel kusurlar Düzlemsel kusurlar Kütlesel kusurlar Katı
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Kristalleşme ve kusurlar Kristal Yapılar İçerik Kristalleşme Kristal yapı kusurları Noktasal kusurlar Çizgisel kusurlar Düzlemsel kusurlar Kütlesel kusurlar Katı
İNTERMETALİK MALZEMELER (DERS NOTLARI-2) DOÇ. DR. ÖZKAN ÖZDEMİR
 İNTERMETALİK MALZEMELER (DERS NOTLARI-2) DOÇ. DR. ÖZKAN ÖZDEMİR KRİSTAL YAPILAR Ayrı ayrı birbirine benzemeyen veya birbirine güçlü afiniteleri olan 2 veya daha fazla elementin birleşmesiyle intermetalik
İNTERMETALİK MALZEMELER (DERS NOTLARI-2) DOÇ. DR. ÖZKAN ÖZDEMİR KRİSTAL YAPILAR Ayrı ayrı birbirine benzemeyen veya birbirine güçlü afiniteleri olan 2 veya daha fazla elementin birleşmesiyle intermetalik
ATOM YAPISI VE ATOMLAR ARASI BAĞLAR
 ATOM YAPISI VE ATOMLAR ARASI BAĞLAR Atom en küçük partikül, görülmez ve bölünemez parça olarak tanımlanır. Modern anlamda atomlar atomaltı (subatomic ) partiküllerden oluşur. elektronlar, negatif enerji
ATOM YAPISI VE ATOMLAR ARASI BAĞLAR Atom en küçük partikül, görülmez ve bölünemez parça olarak tanımlanır. Modern anlamda atomlar atomaltı (subatomic ) partiküllerden oluşur. elektronlar, negatif enerji
Radyoaktif elementin tek başına bulunması, bileşik içinde bulunması, katı, sıvı, gaz, iyon halinde bulunması radyoaktif özelliğini etkilemez.
 RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
ATOM VE MOLEKÜLLER ARASI BAĞLAR
 ATOM VE MOLEKÜLLER ARASI BAĞLAR 1 Potansiyel enerji (kj/mol) Çekme İtme Atomlararası denge mesafesi Atomlar birbirleri ile sürekli etkileşim içerisindedir. Bu etkileşimlerden biride atomlar arası itme
ATOM VE MOLEKÜLLER ARASI BAĞLAR 1 Potansiyel enerji (kj/mol) Çekme İtme Atomlararası denge mesafesi Atomlar birbirleri ile sürekli etkileşim içerisindedir. Bu etkileşimlerden biride atomlar arası itme
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER
 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
İntermetalik bileşikler
 Ara Bileşikler İntermetalik bileşikler İntermetalik bileşikler farklı elektronegatifliğe sahip, yani en dış yörüngesinde farklı sayıda elektron bulunduran elementler arasında oluşuyor. Bu bileşikler kovalent
Ara Bileşikler İntermetalik bileşikler İntermetalik bileşikler farklı elektronegatifliğe sahip, yani en dış yörüngesinde farklı sayıda elektron bulunduran elementler arasında oluşuyor. Bu bileşikler kovalent
PERİYODİK CETVEL Mendeleev Henry Moseley Glenn Seaborg
 PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
KOVALENT BAĞLARDA POLARLIK. Bileşikler 5. Bölüm
 KOVALENT BAĞLARDA POLARLIK Bileşikler 5. Bölüm Ametallerin Bağ Elektronlarına Sahip Çıkma Ġsteği Aynı periyottaki elementlerin soldan sağa: Çekirdek yükü artar Son katmandaki elektronların çekirdeğe uzaklığı
KOVALENT BAĞLARDA POLARLIK Bileşikler 5. Bölüm Ametallerin Bağ Elektronlarına Sahip Çıkma Ġsteği Aynı periyottaki elementlerin soldan sağa: Çekirdek yükü artar Son katmandaki elektronların çekirdeğe uzaklığı
KRİSTAL KUSURLARI BÖLÜM 3. Bağlar + Kristal yapısı + Kusurlar. Özellikler. Kusurlar malzeme özelliğini önemli ölçüde etkiler.
 KRİSTAL KUSURLARI Bağlar + Kristal yapısı + Kusurlar Özellikler Kusurlar malzeme özelliğini önemli ölçüde etkiler. 2 1 Yarıiletken alttaş üretiminde kullanılan silikon kristalleri neden belli ölçüde fosfor
KRİSTAL KUSURLARI Bağlar + Kristal yapısı + Kusurlar Özellikler Kusurlar malzeme özelliğini önemli ölçüde etkiler. 2 1 Yarıiletken alttaş üretiminde kullanılan silikon kristalleri neden belli ölçüde fosfor
Paslanmaz Çelik Gövde. Yalıtım Sargısı. Katalizör Yüzey Tabakası. Egzoz Emisyonları: Su Karbondioksit Azot
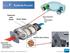 Paslanmaz Çelik Gövde Yalıtım Sargısı Egzoz Emisyonları: Su Karbondioksit Azot Katalizör Yüzey Tabakası Egzoz Gazları: Hidrokarbonlar Karbon Monoksit Azot Oksitleri Bu bölüme kadar, açıkça ifade edilmese
Paslanmaz Çelik Gövde Yalıtım Sargısı Egzoz Emisyonları: Su Karbondioksit Azot Katalizör Yüzey Tabakası Egzoz Gazları: Hidrokarbonlar Karbon Monoksit Azot Oksitleri Bu bölüme kadar, açıkça ifade edilmese
MALZEME BİLGİSİ DERS 5 DR. FATİH AY. www.fatihay.net fatihay@fatihay.net
 MALZEME BİLGİSİ DERS 5 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA BAĞ KUVVETLERİ VE ENERJİLERİ ATOMLARARASI BİRİNCİL BAĞLAR İKİNCİL VEYA VAN DER WAALS BAĞLARI MOLEKÜLLER BÖLÜM III KATILARDA
MALZEME BİLGİSİ DERS 5 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA BAĞ KUVVETLERİ VE ENERJİLERİ ATOMLARARASI BİRİNCİL BAĞLAR İKİNCİL VEYA VAN DER WAALS BAĞLARI MOLEKÜLLER BÖLÜM III KATILARDA
