LENFOMA TEDAVİSİNDE MONOKLONAL ANTİKORLAR: HEMATOLOJİDE BİYOTEKNOLOJİK ÜRÜNLER VE BENZERLERİ (BİYOBENZERLER)
|
|
|
- Yavuz Özmert
- 7 yıl önce
- İzleme sayısı:
Transkript
1 LENFOMA TEDAVİSİNDE MONOKLONAL ANTİKORLAR: HEMATOLOJİDE BİYOTEKNOLOJİK ÜRÜNLER VE BENZERLERİ (BİYOBENZERLER) Dr. Serdal KORKMAZ Sağlık Bilimleri Üniversitesi Kayseri Eğitim ve Araştırma Hastanesi Hematoloji Kliniği 22 Aralık 2016
2 SUNUM PLANI Genel Tanımlar - Biyolojik ürün nedir? - Biyobenzer ilaç nedir? - Biyoeşdeğer ilaç nedir? Biyolojik İlaç Üretim Basamakları? Biyobenzer İlaç Üretim Basamakları? - İmmünojenisite - Ekstrapolasyon - Değiştirilebilirlik ve Otomatik İkame - Farmakovijilans EMA, FDA, WHO rehberlerinin biyobenzerlere bakış açısı Karşılaştırmalı Çalışması Olmayan Biyolojik Ürünler (NCB)! ÖZET
3 ORİJİNAL İLACIN GELİŞTİRİLME / ONAYLANMA AŞAMALARI 1.Drug Discovery and Clinical Research.By SK Gupta, JP Medical Ltd, Jun 1, 2011 ISBN ,
4 BİYOTEKNOLOJİK (BİYOFARMASÖTİK / BİYOLOJİK) ÜRÜN? Canlı organizmalardan (bitki ve hayvan hücreleri, bakteri, virus, mantarlar) re-kombinant DNA (rdna) teknolojisi, kontrollü gen ekspresyonu, antikor metodları gibi biyoteknolojik yöntemler kullanılarak elde edilen protein ya da polipeptid yapıda biyolojik tıbbi ürünlerdir. Biyolojik ilaçların çoğu yüksek düzeyde saflaştırılmış proteinlerdir. Biyolojik ajanlar veya biyolojikler büyük ve komplex bir yapıya sahip olduklarından tam anlamıyla bir kopyasını yapmak mümkün değildir.. Örnek olarak; mabs ve büyüme faktörleri 1.Revers L, et al. CPJ/ RPC 2010;143:
5 Biyolojik Ürünlerin Üretim Süreci Oldukça Karmaşık.. 1.Kuhlmann M, et al. Nephrol Dial Transplant 2006;21:v4-v8
6
7 Basit biyolojik ve Kompleks biyolojik ajanların karşılaştırılması Moleküler karmaşıklık Basit biyolojik (örn: GSF) Basit yapı Kompleks Biyolojik (örn: Rituksimab) Büyük ve Kompleks yapı Etki mekanizması İyi anlaşılmıştır Karmaşık Tedavideki yeri Palyatif tedavi Küratif tedavi Sonlanım noktası Değerlendirmesi kolay (nötrofil sayımı) Değerlendirmesi zor ve uzun (PFS,OS)
8 BİYOBENZER İLAÇ? Önceden ruhsatlandırılmış bir referans/orijinal biyolojik ilaca, klinik ve klinik olmayan parametreler yönünden benzer şekilde geliştirilen ve benzer olduğu onaylanan ilaçtır. Biyobenzer ilaç, biyoeşdeğer ilaç ile karıştırılmamalıdır!! 1. Cortes J, et al. Breast Cancer Res Treat 2014;144:
9 Biyoeşdeğer (Jenerik) ilaç? Jenerik ilaçlar orijinal ilaçlarla aynı özelliklere sahip olan, hasta üzerinde aynı tedaviyi sağlayan ve orijinal ilaçların koruma süreleri bittikten sonra satışa sunulan ürünlerdir. Araştırıcı (innovator) firma tarafından geliştirilerek pazara verilen orijinal ilaçlar referans alınarak jenerik (eşdeğer) ilaçlar üretilir. Orijinal ilaç ile aynı etken maddeyi, aynı dozlarda içeren ancak farklı kuruluşlar (firmalar) tarafından üretilen bir ilacın orijinal ilaç yerine reçete edilebilmesi için biyoeşdeğerliğinin kanıtlanması gereklidir.
10 Biyoeşdeğer (Jenerik) ilaç? Jenerik (eşdeğer) ilaçlar kimyasal sentezle üretilmiş, kimyasal olarak sabit yapıda, küçük moleküllerdir. Biyobenzerler ise biyoteknolojik ürünler olup canlı organizmalar tarafından üretilmektedir. Molekül yapıları çok büyük ve karmaşıktır. Bu yüzden biyobenzerler, jenerik ürün olarak kabul edilemezler ve original ürünler ile karşılaştırma yöntemleri farklıdır.
11 GELENEKSEL KİMYASAL İLAÇLARLA BİYOLOJİK İLAÇLAR ARASINDAKİ FARK Küçük stabil yapı KİMYASAL BİYOLOJİK Orta ila çok büyük yapı, daha az stabil Sentetik moleküllerdir. Genelde doğal olarak bulunmaz Kimyasal reaksiyonlar aracılığıyla üretilir Yaklaşık 50 in-proses kalite testi İnsan vücudunda doğal olarak oluşan, önemli proteinlerle birçok benzerlik İnsan, hayvan ya da bakteriyel kökenli hücre kültürleri gibi değiştirilmiş canlı hücrelerden üretilir Yaklaşık 250 in-proses kalite testi Genelde birkaç gün içinde üretim Uzun üretim döngüleri (haftalar/aylar) Oda sıcaklığında uzun süre saklandığında genelde oldukça stabildir Sıklıkla ağızdan alınır Küçük stabil yapı ve basit imalat prosesi; Tam, birebir kopyası üretilebilir. Genelde soğutucuda saklanmalı; üretim ve saklama sırasında sıcaklık değişiklikleri etkililiği / güvenliliği etkileyebilir Büyük boy ve bileşimleri nedeniyle genelde enjeksiyon yoluyla uygulanır Son derece karmaşık imalat prosesi; tam bir kopyası üretilemez, ancak benzeri üretilebilir. 1. Nacak M et al, J Clin Anal Med 2012;3(2): 251-6
12 BİYOBENZER İLAÇLAR Onay almış ilk biyobenzerler (Bb) destek tedavisi amacıyla kullanılan büyüme faktörleridir.. Avrupa da 2007 yılında epoetin alfa ve filgrastim.. (günümüze kadar 16 Bb ürün EMA tarafından onaylandı) ABD de 2015 yılında filgrastim.. Kanser tedavisinde kullanılan bazı mab için patent süresi Avrupa da doldu ve ABD de de dolmak üzere.. Kısacası, iştah kabartıcı bir şekilde Bb üretimi kapıda 1. Cortes J, et al. Breast Cancer Res Treat 2014;144:
13
14 Bb ilaç üretim basamakları Biyobenzer üretim proğramının hedefi, Bb in orijinal/referans ürüne yüksek oranda benzer olduğunun ortaya konulmasıdır.. Referans biyolojik ürünün kompleks yapısı ve formülüne ulaşım imkanı olmaması nedeniyle reverse (zıt=ters) mühendislik yoluyla orijinal moleküle yüksek oranda benzeyen Bb i üretilir.. (Puzzle çözmek gibi veya bozup yeniden yapmak gibi bir işlem) Bb ilacın kabul süreci de EMA, FDA ve WHO nun önerileri doğrultusunda gerçekleşir.. Her bir basamaktaki verilerin kapsamı ve içeriği titizlikle takip edilmekte ve kanıta dayalı olarak yürütülmektedir.. Herhangi bir basamaktaki uyumsuzluk ajanın Bb olma ihtimalini ortadan kaldırmaktadır.. Örneğin; rituximab Bb çalışmalarından Samsung un SAIT101, Celltrion un CT-P10 Phase I ve Teva nın TL011 (in rheumatology) geçici veya kalıcı olarak durdurulmuştur.
15 Bb ilaç üretim basamakları
16 BİYOBENZER İLAÇ ÜRETİM BASAMAĞINDAKİ METODLAR FARKLI OLABİLİR 1. Nacak M et al. J Clin Anal Med 2012;3(2): 251-6
17 Bb ilaç üretiminde hasta populasyonu Rehberlerin önerisi doğrultusunda Bb klinik çalışmalarında sensitif ve homojen hasta populasyonuna yer verilmektedir. Amaç; etkinlik, güvenlik, immunojenisitede ortaya çıkan bir potansiyel farklılığın hasta populasyonuna değil de Bb e bağlı olduğunu gösterebilmek.. Homojen populasyon denildiğinde; çalışma populasyonundaki hastaların tm evresinin, hastalık ciddiyeti ve tedavi basamağının aynı evre olması Sensitif populasyon denildiğinde; çalışma populasyonunda molekülün klinik ilişkili fonksiyonlarındaki küçük değişiklikleri dahi erken saptamaya elverişli olması.. Bunun için de; 1- Referans ürünün temel çalışmasından bir alt grubun seçilmesi veya 2- Kombinasyondan ziyade tek ajanın etkinliğinin değerlendirilmesi Ancak, bu her iki terim de halen tartışılıyor..
18 Bb ilaç üretimi ve yanıtlar Kanser alanındaki orijinal ilaç çalışmalarında primer endpoint olarak ya OS ya da PFS veya DFS kullanılmakta.. OS; randomizasyondan ölüme kadar geçen süre olarak tanımlanabilir ve direkt klinik etkinliği gösteren altın standart tek parametre.. Ancak, diğer yanıtlara nazaran OS elde etmek daha güç.. Çünkü, daha geniş hasta serilerine, daha uzun zaman ve maliyete neden oluyor.. Bu da potansiyel olarak etkili bir ajanın gecikmeli olarak pazara girişine neden olmakta.. EMA a göre de; OS/PFS gibi yanıtlar, referans ajan ile Bb ürünü kıyaslamak açısından uygun değil.. Çünkü, tm yükü, ECOG, daha önce alınan tedaviler, zemindeki hastalıklar gibi bir takım faktörler nedeniyle bu yanıtlar etkilenebilmekte ve her iki ürün arasında kıyas yapmayı zorlaştırmaktadır.. Unutmayalım ki, karşılaştırma çalışmalarında hedef; Bb in referans ürünle benzer etkinlik ve güvenliğe sahip olup olmadığını ortaya koymaktır. Referans ürün ile yukarıda bahsi geçen yanıtlar zaten önceden elde edilmiştir. Bu nedenle ORR (CR veya PR elde edilen hastaların oranı) gibi yanıtlara, Bb in klinik etkinliğini değerlendirmek için daha çok itibar edilmekte..
19 Bb ilaç üretimi ve yanıtlar ORR ile OS ve PFS in de her zaman ve her hastalık için birbirleriyle örtüştüğünü de söylemek pek mümkün değil Yine de PFS, ORR e göre daha sensitif bir endpointdir, ancak klinik çalışmanın süresini uzatmaktadır. Bb için EMA nın önerisi primer endpoint olarak aktiviteyi daha sensitif ortaya koyabilmek adına ORR kullanılması yönünde.. Son onay için de en az bir veya iki karşılaştırmalı klinik çalışma gereklidir. Bu çalışma veya çalışmalardan en az biri; Bb in güvenilir, saf ve klinik olarak etkili olduğunu ortaya koyacak immunojenisite, farmakokinetik veya farmakodinamik değerlendirme verilerini ortaya koymalıdır..
20 İMMÜNOJENİSİTE? Vücuda giren immünojenin immün yanıtı tetikleyerek antikor oluşturma riskidir.. Antikor oluşumu sonucunda ortaya çıkabilecekler ise; yan etki, etkisizlik İmmünojenisite Kliniğe yansımayacak kadar hafif Küçük Moleküllü Biyolojik İlaçlar Küçük boyutları nedeniyle immün sistem tarafından tanınmaları zordur Potansiyel olarak ölümcül Büyük Moleküllü Biyolojik İlaçlar Büyük yapıları ve kompozisyonları gereği immün yanıtı tetikleme potansiyeli 1. Sharma B et al. Biotechnology Advances 2007;25:
21 İmmunojenisite İmmunojenisite preklinik çalışmalar ile öngörülemez ve spesifik hedef populasyonda klinik olarak değerlendirilmelidir. İmmunojenisite değerlendirilirken mümkün olduğunca daha önceden referans ürünü kullanmış hastaların çalışmaya alımından kaçınılmalıdır.. (ilaca karşı Ab gelişmiş olma ihtimali) mab un dozu da önemlidir; çünkü, yüksek dozlarda mab lar ilaca karşı Ab gelişimini inhibe edebilir. Eğer klinik olarak mümkünse düşük dozda ilaç kullanımı kıyaslama açısından daha net bilgi verir.
22 EKSTRAPOLASYON? Her hangi bir endikasyonda gerekli deneylerle etkililiğini kanıtlamış bir biyobenzerin, ek klinik araştırmalara ihtiyaç duymadan başka bir endikasyonda kullanım izni almasına 'ekstrapolasyon' denir. 1. CHMP,EMA Guideline on similar biological medicinal products containing monoclonal antibodies non-clinical and clinical issues. EMA/CHMP/BMWP/403543/2010, 12/06/WC pdf. Son erişim tarihi:
23 Ekstrapolasyon Orijininal ürün İnfliximab (Remicade); Crohn s hastalığı, ülseratif kolit, ankilozan spondilit, psöriasis, psöriatik artrit gibi bir takım hastalıklarda endikasyonu (+) İnfliximab Bb i olan Remsima R and Inflectra R sadece RA ve AS için onaylı olmasına rağmen EMA tarafından tüm endikasyonlarda kullanılmak üzere onay almıştır..!!! Kısaca, bir ajan belirli bir endikasyon için güvenilir ve etkili iken, bir başka endikasyonda aynı etkinliği gösteremeyebilir. Dolayısıyla, gelecek endişeler nedeniyle ekstrapolasyonun pek de arzulanan ve yaygınlaşması beklenen bir hadise olmadığı aşikardır
24 EKSTRAPOLASYON AÇISINDAN EMA GÖRÜŞÜ * Ekstrapolasyonun yapıldığı durumlarda neden daha ileri çalışmalara ihtiyaç duyulmadan ekstrapolasyon yapıldığı bilimsel olarak açıklanmalıdır. * Bu bilimsel kanıtlar aşağıdaki kıstasları karşılamalıdır: Hastalıkların benzerliği (etiyolojik, patofizyolojik, klinik sunum, vb. açılardan) İlacın yayılım ve etki benzerliği (etki mekanizması, farmakokinetik ve farmakodinamik açıdan) Klinik etkililik ve güvenlilik hedeflerinin ulaşılabilirliği ve benzerliği 1. CHMP,EMA Guideline on similar biological medicinal products containing monoclonal antibodies non-clinical and clinical issues. EMA/CHMP/BMWP/403543/2010, Son erişim tarihi:
25 DEĞİŞTİRİLEBİLİRLİK (INTERCHANGEABİLİTY)? Değiştirilebilirlik; bir ilacın, eşdeğer olduğu kanıtlanmış bir diğer ilacın yerine kullanılabileceğini gösteren bir ifadedir. Değiştirilebilirlik için bilimsel kanıt ve sağlık otoritesi onayı gereklidir. Jenerik ürünlerin, orijinal ürünler ile değiştirilebilir olduğu tüm dünyada kabul edilmektedir. Bb de değiştirilebilirlik için henüz rehber düzeyinde bir bilimsel kanıt olmadığından genelde öneri bazında değerlendirilmektedir. Değiştirilebilirliğin immunojenisite üzerine net etkisinin ne olduğu/olacağı da henüz açık kapılardan birisi FDA değiştirilebilirliğe standart getirmek amacıyla; - Referans üründe olduğu üzere, Bb in kullanıldığı her hastada aynı klinik sonucu ortaya koyacağı beklenmeli - Referans ürünle Bb ürün değiştirildiğinde, güvenlik veya etkinliğin azalması gibi riskler, sadece referans ürünün kullanılması ile ortaya çıkabilecek riskten daha büyük olmamalı
26 OTOMATİK İKAME (AUTOMATİC SUBSTİTUTİON)? Bir ürünün eczanede, doktor onayına ihtiyaç duyulmadan, orijinal ürünün yerine verilmesine 'otomatik ikame' denir. Biyobenzerlerin orijinal ürün ile otomatik olarak ikamesi (veya tam tersi) izlenebilirliğe ve farmakovijilans aktivitelerine zarar riski taşıyabilir. * Otomatik ikameye izin sağlık otoritesinin yetkisine bağlıdır. 1.Mellstedt H et al, Annals of Oncology 2008;19:
27 FARMAKOVİJİLANS? Pharmacon + Vigilancia (ilacın zararlı etkilerine karşı uyanık olmak) * Advers etkilerin ve beşeri tıbbi ürünlere bağlı diğer muhtemel sorunların (suistimal, zehirlenme, etkisizlik) saptanması, değerlendirilmesi, tanımlanması ve önlenmesi ile ilgili bilimsel çalışmalardır. * Hem orijinal ürün hem de Bb için onay alındıktan sonra da devam etmesi gerekli süreklilik arzeden bir basamaktır. * Tüm biyolojik ajan üretici firmaları (Bb üreticileri de dahil) post-marketing güvenlik izlem proğramı ve yan etki bildirimi gibi konuların takibi açısından primer sorumludur. 1.İyi Farmakovijilans Uygulamaları Kılavuzu.EK I TANIMLAR. erişim tarihi:
28 FARMAKOVİJİLANS TAKİBİ Sorumlu belli İkinci ilaca mı bağlı? Sorumlu önceki ilaç mı? Araya giren ilaç mı? İkisinin ardışık kullanılması mı? Sorumlu ilaçların hangisi?
29 Maliyet Bb üreticileri, orijinal ilacın üretimindeki bir takım basamakları otomatik olarak atlamasına rağmen (faz II çalışmaya gerek olmaması, her zaman hayvan çalışmalarının gerekli olmaması gibi) halen üretim maliyeti açısından hedefe ulaşabilmiş değil.. Ancak, teknoloji olarak kendilerini ciddi oranda geliştirmekteler.. Avantaj; pazarlama kısmında 2010 yılından bu yana en çok kullanılan 10 Bb in Avrupa sağlık sistemine 1.4 billion kazandırdığı Önümüzdeki 10 yılda ABD de Bb in sağlık sistemine 9-12 billion $ arasında kazandıracağı tahmin ediliyor..
30 Maliyet ülkeden ülkeye değişiyor, genelde Bb ler %20-80 arasında tasarruf sağlıyor Orijinal Fiyat Biyobenzer - Neupogen (Filgrastim) tek vial [Amgen] $ vs $ vs 13.5 $ - Tevagrastim (Filgrastim) tek vial [Teva] - Zarzio (Filgrastim) tek vial [Sandoz] - Eprex (Epoetin alfa) 30 IU (hem fix hem de kilo bazlı dozda) [Janssen] 7168 vs Binocrit (Epoetin alfa) 30 IU (hem fix hem de kilo bazlı dozda) [Sandoz] - Remicade (infliximab) 100 ml vial [Janssen/MSD] 419 vs Inflectra [Hospira] ve Remsima [Celltrion] (infliximab) 100 ml vial
31 EMA, FDA ve WHO; Biyobenzerlere Yönelik Rehberleri Biyobenzerler için detaylı bir ruhsatlandırma prosedürünü oluşturan ilk bölge Avrupa Birliği WHO Nisan 2010 da biyobenzerler için tavsiye niteliğinde olan kılavuzunu yayınladı, Temmuz 2016 da monoklonal antikorlara özel rehberini yayınladı. FDA ilk kılavuzunu 2012 de yayınladı da ABD de ilk monoklonal antikor romatoloji alanında onaylandı.
32 EMA bakış açısı; Non-klinik çalışmalar Non-klinik çalışmalar, klinik çalışmalardan önce yapılmalıdır Step 1 (in vitro): aşağıdaki özellikler değerlendirilir; - Binding to target antigen(s) - Binding to representative isoforms of the relevant three Fc gamma receptors (FcγRI, FcγRII and FcγRIII), FcRn and complement (C1q) - Fab-associated functions (e.g. neutralization of a soluble ligand, receptor activation or blockade) - Fc-associated functions (e.g. antibody-dependent cellmediated cytotoxicity, ADCC; complement-dependent cytotoxicity, CDC; complement activation) ortaya konulmalıdır.
33 EMA bakış açısı; Non-klinik çalışmalar Step 2: in vivo çalışma yapılmasına ihtiyaç var mı? sorusuna yanıt alınmalıdır. Eğer step 1 de karşılaştırma sonucu yeterli görülürse ve herhangi bir endişe ortada yoksa in vivo çalışma yapılmasına gerek yoktur. Ancak, aşağıdaki durumlarda yapılmalıdır; - Referans üründe tespit edilmemiş bir kalite özelliğinin varlığı (örn; yeni bir post-translasyonel modifikasyon yapısı) - Kalite özelliğinin, referans üründe ölçülenden daha farklı miktarlarda var olması - Formulasyonda farklılık olması
34 EMA bakış açısı; Non-klinik çalışmalar Step 3 (in vivo): eğer step 2 de değerlendirme sonucu in vivo çalışmanın gerekliliğine karar verilirse Bb in farmakokinetik ve/veya farmakodinamik ve güvenlilik özelliklerini ortaya koymak açısından planlanır. Bu basamakta doz toksisite çalışmalarının yapılması önerilmemektedir. Hayvanlarda immunojenisite değerlendirmesi, genelde insanlarda immunojenisiteyi predikte etmemektedir.
35 EMA bakış açısı; klinik çalışmalar Referans ürün ile Bb ürün mutlaka karşılaştırmalı klinik çalışmalar ile kıyas edilmelidir. Step 1 (farmakokinetik ve farmakodinamik): PK çalışmalar ile hedefe yönlenme, lineer ve non-lineer PK, yarılanma zamanı gibi özellikler ortaya konulur. PK çalışmalar PD çalışmalar ile birlikte yapılabilir. PD ile doz-konsantrasyon-cevap veya zaman-cevap ilişkisi ortaya konulmaya çalışılır. PD çalışmalar hele de küçük farklılıkları saptayabilecek hassasiyete sahipse daha değerli sonuçlar elde edilebilir.
36 EMA bakış açısı; klinik çalışmalar Step 2 (klinik etkinlik): randomize, çift-kör, paralel grup karşılaştırmalı klinik çalışmalar ile etkinlik değerlendirilir. Klinik güvenlik: Bb ile özellikle daha önceden referans üründe tesbit edilmiş advers reaksiyonların sıklığı, ciddiyeti ve tipi açısından karşılaştırma yapılmalıdır. Tüm bu basamaklar total olarak kanıta dayalı olacak şekilde değerlendirilerek Bb in onay alıp almayacağı belirlenmektedir.
37 FDA ve WHO gözünden Bb FDA ve WHO da aslında EMA ile aynı görüşte.. Kısaca her iki klavuz da; Bb in yapısal ve fonksiyonel özellikleri ortaya konmalı non-klinik testler yapılmalı insan PK ve PD verileri elde edilmeli klinik immünojenisite verileri olmalı son olarak da karşılaştırmalı klinik çalışmalar yapılmış olmalı ki ben de total olarak değerlendireyim ve onaylayayım diyor..
38 TÜRKİYE KILAVUZU Tam ve bağımsız ürünün dosya bilgileri referans ürünle karşılaştırılması Tam ve bağımsız ürünün dosya bilgileri referans ürünle kapsamlı olarak karşılaştırılması Tam ve bağımsız ürünün dosya bilgileri Kısaltılmış program, molekülün karmaşıklığına bağlı olarak subkronik toksisite çalışması (4 hafta), Lokal tolerans, FK/FD çalışması Klinik öncesi tam çalışma Biyoeşdeğerlilik çalışması Faz I;FK/FD çalışması (farmakokinetik/farmakodinamik) Faz II çalışması gerekmemektedir. Faz III çalışması (Gerektiğinde her bir endikasyonda ) Risk Yönetim Planı Faz I çalışması Faz II çalışması Faz III çalışması (Tüm endikasyonlarda) Risk Yönetim Planı FK: Farmakokinetik FD: Farmakodinamik 1. Biyobenzer Tıbbi Ürünlere İlişkin Kılavuz, Türkiye İlaç ve Tıbbi Cihaz Kurumu
39 Karşılaştırmalı Çalışması Olmayan Biyolojik Ajanlar [Non-Comparable Biologics (NCB)] Bb ajan ile intended copies (non-comparable biologics = NCB) kavramları birbirine karıştırılmamalı Onaylı orijinal biyolojik ürün ile direkt olarak karşılaştırılabilirlik analizleri yapılmayan kopya biyolojik ürünlerdir. Kılavuzlarda belirtilen kalite, güvenlilik ve etkililik gibi temel alanlarda onaylı referans ürüne benzerlik göstermemektedir. NCB ile referans biyolojik ürün arasında kafa kafaya karşılaştırmalı çalışma olmayabileceği gibi, bazı durumlarda NCB ler orijinal ürünün etkililik ve güvenlilik verilerini kullanmaktadır. Bazı ülkelerde bulunan bu kopyaların karşılaştırılmalı çalışmalarının olmadığı, Bb olduğunun kanıtlanmadığı ve EMA-FDA-WHO gibi düzenleyiciler tarafından onayının bulunmadığı unutulmamalıdır Nisan 2007 de, Dr. Reddy s Laboratories (Hyderabad, India) rituximab Bb i olduğunu iddia ettikleri Reditux u Hindistan, Bolivya, Şili ve Peru da piyasaya sürdü, ancak, bu molekül gerçek bir Bb olmadığından EMA ve FDA tarafından onaylanmadı.
40 ÖZET
41 ORİJİNAL VE BİYOBENZER MOLEKÜLLER İÇİN KLİNİK ÇALIŞMA GEREKLİLİKLERİ Biyobenzer Orijinal Hassas ve homojen Hasta Popülasyonu Herhangi bir hasta popülasyonu Orijinal ürünle karşılaştırma Klinik Tasarım Standart tedaviye karşı üstünlük Sonlanım noktaları (ORR) Çalışma sonlanım noktaları Sonlanım noktaları (OS ve PFS) Orijinal ile benzer güvenlilik profili Güvenlik Tedavi standardına karşı kabul edilebilir risk-yarar profili Orijinal ile benzer immunojenisite profili İmmunojenisite Tedavi standardına karşı kabul edilebilir risk-yarar profili Bilimsel gerekçesi varsa mümkün Ekstrapolasyon Mümkün değil /Her bir endikasyon için klinik çalışma gereklidir 1 Cortes J, et al. Breast Cancer res Treat 2014;144:
42 Biyobenzer İlacın Onaylanma Aşamaları Düzenleyici Kurumların Karşılaştırılması EMA AB tarafından geliştirilmiş bir yaklaşım Üye ülke seviyesinde karar verilir. AB INN sistemini kullanmaktadır fakat diğer biyolojik ürünlerden ayırt edilebilmesi için ek olarak ticari ismin kullanılmasını tavsiye etmektedir. Orijinal ürün AB de ruhsatlı olmalıdır fakat AB-dışı ruhsatlı rakibini kullanmak mümkündür. WHO AB ilkelerini takip ediyor, monoklonal antikorlara özel klinik ve klinik-dışı kılavuz yayınlamıştır. WHO kılavuzunda değinilmemiştir. Her birim durum için bilimsel olarak temellendirildiğinde izin verilir. Ruhsat öncesi ve sonrası insanlarda incelenmelidir. WHO kılavuzu uyarınca AB ve ABD de bütün ürünler için farmakovijilans takibi gereklidir. Orijinal ürün tam dosya bazlı ruhsatlı olmalıdır. FDA Ürüne özel kılavuzun olmaması dışında AB ye benzer bir yaklaşım. Değiştirilebilirlik biyobenzerlikten daha yüksek bir standarttır. Pazardaki yan etkilerin farklılaştırılması süreci için yeterli takip gerekmektedir fakat bu durumu detaylandırılmamış.. ABD-dışı veriler ABD deki ruhsatlı ürün ile ilişki olarak kabul edilebilir. WHO ya Özgü FDA e Özgü EMA ya Özgü Genel Kılavuz 1.WHO. Guidelines on biosimilars EMA. Overaching guideline on biosimilars 2014: CHMP/437/04 Rev 1. 3.EMA. Guideline on immunogenicity 2007: EMEA/CHMP/BMWP/14327/ FDA. Guidance on biosimilarity FDA. Guidance on quality 2015:Quality Considerations in Demonstrating Biosimilarity of a Therapeutic Protein Product to a Reference Product 6.FDA. Draft guidance, Q&A on BPCI Act
43 ORİJİNAL BİYOLOJİK VS BİYOBENZER ADAYI VS NCB Orijinal İlaç Benzer Biyolojik İlaç Karşılaştırmalı Çalışması Olmayan Biyolojik İlaç Kalite Tüm kalite testleri Tüm kalite testleri + karşılaştırmalı benzerlik testleri Kalite testlerinin kapsamı bilinmemektedir. Orijinal ilaca benzerliği gösteren testleri içermeyebilir Güvenlilik İmmünojenisiteyi de içeren klinik ve klinik-dışı güvenlilik verileri Biyobenzerlik iddiasını destekleyen, immünojenisite değerlendirmesini içeren klinik ve klinik-dışı güvenlilik verisi. Çalışmalar orijinal ve benzer arasında karşılaştırmalı olarak tasarlanır. Güvenlilik verisinin kapsamı bilinmemektedir. Orijinal biyolojik ilaca benzerlik değerlendirmelerini içermeyebilir. İmmünojenisite verisi oldukça kısıtlı olabilir veya hiç bulunmayabilir. Etkililik Başlıca etkililik çalışmalarından alınan tüm veriler Karşılaştırmalı farmakokinetik, farmakodinamik ve etkililiği içeren karşılaştırmalı klinik program hedeflenir, İstatistiki gücü orijinal ilaç ile noninferiorite veya eşdeğerliği gösterecek şekilde tasarlanır. Klinik data içermeyebilir veya oldukça kısıtlı olabilir. Çalışmalar referans ilaç ile noninferiorite veya eşdeğerliği gösterecek güçte olmayabilir. Çalışmalarda orijinatör referans ürün yer almayabilir. 1 IFPMA Policy Statement: Non-comparable Biotherapeutic Products
44 Onaya giden süreç orijinal ürün için de Bb için de kolay değil, zorlu bir süreçtir.. Monoklonal antikorların geliştirilme süreci preklinik ve klinik çalışmaları ayrıca ruhsat sonrası risk değerlendirme programlarını kapsayacak şekilde olmalıdır. Bb ajanın, orijinal biyolojik ilaçla arasında güvenlik, saflık ve etkililik açısından anlamlı bir farklılık yoktur.. (EMA, FDA, WHO) Birçok ülkenin orijinal ilaca ulaşamadığı bilinen bir gerçek.. Sağlık sistemi açısından önemli bir tasarruf sağladığı da aşikar Bu nedenle; Bb in gelecekte kullanımına kesin gözüyle bakılabilir.. Rekabetin artacağı ve ilaç fiyatlarının yeniden düzenleneceği kesin Biz ne yapabiliriz?
45 SAĞLIK OTORİTESİ KLİNİSYENLER HASTA SEKTÖR MEDYA
46 TEŞEKKÜRLER..
BIYOLOJIK TIBBİ ÜRÜNLERIN ONAYLANMASI VE KULLANIMI
 BIYOLOJIK TIBBİ ÜRÜNLERIN ONAYLANMASI VE KULLANIMI 2017 İçindekiler Giriş... 2 Biyolojik İlaç Tanımı ve Üretim Süreci...4 Biyobenzer Ürün Tanımı...6 Biyobenzer Ürünlerin Benzerliğinin Kanıtlanması ve Ruhsatlandırılması...
BIYOLOJIK TIBBİ ÜRÜNLERIN ONAYLANMASI VE KULLANIMI 2017 İçindekiler Giriş... 2 Biyolojik İlaç Tanımı ve Üretim Süreci...4 Biyobenzer Ürün Tanımı...6 Biyobenzer Ürünlerin Benzerliğinin Kanıtlanması ve Ruhsatlandırılması...
Biyoterapötik İlaçlar
 Uluslararası İlaç Üreticileri ve Dernekleri Federasyonu Biyoterapötik İlaçlar Yeni Nesil Tedavileri Anlamak Biyoterapötik ilaçlar ciddi rahatsızlıklar ve hastalıkların tedavisi ve önlenmesi için modern
Uluslararası İlaç Üreticileri ve Dernekleri Federasyonu Biyoterapötik İlaçlar Yeni Nesil Tedavileri Anlamak Biyoterapötik ilaçlar ciddi rahatsızlıklar ve hastalıkların tedavisi ve önlenmesi için modern
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ HAFTA
 İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 1. HAFTA İLAÇ Hastalıkların teşhisi, tedavisi, profilaksisi (hastalıktan korunma) cerrahi girişimlerin kolaylaştırılması ve
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 1. HAFTA İLAÇ Hastalıkların teşhisi, tedavisi, profilaksisi (hastalıktan korunma) cerrahi girişimlerin kolaylaştırılması ve
Biyobenzerler DOKTOR HAKAN ERDEM MEDICANA INTERNATONAL ANKARA HASTANESİ
 Biyobenzerler DOKTOR HAKAN ERDEM MEDICANA INTERNATONAL ANKARA HASTANESİ BİYOBENZERLER Biyobenzer (biosimilar) ürünler, bir sağlık otoritesi tarafından daha önce ruhsatlandırılmıs bir biyofarmasötik ürün
Biyobenzerler DOKTOR HAKAN ERDEM MEDICANA INTERNATONAL ANKARA HASTANESİ BİYOBENZERLER Biyobenzer (biosimilar) ürünler, bir sağlık otoritesi tarafından daha önce ruhsatlandırılmıs bir biyofarmasötik ürün
Monoklonal Antikorlarda Biyobenzerlik kavramı Farmakovijilans ve Risk Yönetimi
 Monoklonal Antikorlarda Biyobenzerlik kavramı Farmakovijilans ve Risk Yönetimi Doç. Dr. M. Devrim Güner Ufuk Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı 11 Nisan 2015, Antalya Sunum Planı Türkiye
Monoklonal Antikorlarda Biyobenzerlik kavramı Farmakovijilans ve Risk Yönetimi Doç. Dr. M. Devrim Güner Ufuk Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı 11 Nisan 2015, Antalya Sunum Planı Türkiye
BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ
 BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ 19/01/2005 tarihli ve 25705 sayılı Resmi Gazete de yayımlanan Beşeri Tıbbi Ürünler Ruhsatlandırma Yönetmeliği ne dayanılarak, anılan Yönetmeliğin Bölüm II Özel
BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ 19/01/2005 tarihli ve 25705 sayılı Resmi Gazete de yayımlanan Beşeri Tıbbi Ürünler Ruhsatlandırma Yönetmeliği ne dayanılarak, anılan Yönetmeliğin Bölüm II Özel
BİYOYARARLANIM- BİYOEŞDEĞERLİK ÇALIŞMALARI
 BİYOYARARLANIM- BİYOEŞDEĞERLİK ÇALIŞMALARI Doç. Dr. T. Emrah Bozkurt Hace4epe Üniversitesi, Eczacılık Fakültesi, Farmakoloji AbD İlaca Giden Yol 6. Disiplinlerarası Beyin FırFnası ToplanFsı 20 Aralık 2018
BİYOYARARLANIM- BİYOEŞDEĞERLİK ÇALIŞMALARI Doç. Dr. T. Emrah Bozkurt Hace4epe Üniversitesi, Eczacılık Fakültesi, Farmakoloji AbD İlaca Giden Yol 6. Disiplinlerarası Beyin FırFnası ToplanFsı 20 Aralık 2018
Biyobenzer ürünlere genel bakış ve kılavuzlar
 Biyobenzer ürünlere genel bakış ve kılavuzlar Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı e-posta: alperi@hacettepe.edu.tr 27 Şubat 2014, Ankara Biyolojik tıbbi
Biyobenzer ürünlere genel bakış ve kılavuzlar Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı e-posta: alperi@hacettepe.edu.tr 27 Şubat 2014, Ankara Biyolojik tıbbi
Türk Diyabet Cemiyeti BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ
 Türk Diyabet Cemiyeti BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ Ülkemizde diyabet alanında biyobenzer ilaçların markete girmesinden sonra bu alanda bilimsel paydaşlardan bir olan Türk Diyabet Cemiyeti,
Türk Diyabet Cemiyeti BİYOBENZER TIBBİ ÜRÜNLERE İLİŞKİN KILAVUZ Ülkemizde diyabet alanında biyobenzer ilaçların markete girmesinden sonra bu alanda bilimsel paydaşlardan bir olan Türk Diyabet Cemiyeti,
Prof. Dr. İlker Kanzık. Kurucu Ortak ve Genel Müdür IDE Farmasötik Danışmanlık Ltd.Şti.
 BİYOBENZER (BIOSIMILAR) İLAÇLAR Prof. Dr. İlker Kanzık Kurucu Ortak ve Genel Müdür IDE Farmasötik Danışmanlık Ltd.Şti. DNA çift heliks yapısının keşfinden sadece 20 yıl sonra Cohen ve Boyer 1973 yılında
BİYOBENZER (BIOSIMILAR) İLAÇLAR Prof. Dr. İlker Kanzık Kurucu Ortak ve Genel Müdür IDE Farmasötik Danışmanlık Ltd.Şti. DNA çift heliks yapısının keşfinden sadece 20 yıl sonra Cohen ve Boyer 1973 yılında
ÖDEME SÜRECİ. Dr. Akif AKBULAT Fiyat, Mevzuat, Araştırmalar Daire Başkanı Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu
 ÖDEME SÜRECİ Dr. Akif AKBULAT Fiyat, Mevzuat, Araştırmalar Daire Başkanı Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu Neredeyiz? İlaç Düzenlemeleri Türkiye İlaç ve Tıbbi Cihaz Kurumu Fiyatlandırma
ÖDEME SÜRECİ Dr. Akif AKBULAT Fiyat, Mevzuat, Araştırmalar Daire Başkanı Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu Neredeyiz? İlaç Düzenlemeleri Türkiye İlaç ve Tıbbi Cihaz Kurumu Fiyatlandırma
ENDÜSTRİYEL ECZACILIKTA İLAÇ FORMULASYONLARININ TASARIMI VE GELİŞİMİ
 ENDÜSTRİYEL ECZACILIKTA İLAÇ FORMULASYONLARININ TASARIMI VE GELİŞİMİ İlaç (Tıbbi farmasötik ürün); insanlarda ve hayvanlarda hastalıklardan korunma, tanı, tedavi veya bir fonksiyonun düzeltilmesi ya da
ENDÜSTRİYEL ECZACILIKTA İLAÇ FORMULASYONLARININ TASARIMI VE GELİŞİMİ İlaç (Tıbbi farmasötik ürün); insanlarda ve hayvanlarda hastalıklardan korunma, tanı, tedavi veya bir fonksiyonun düzeltilmesi ya da
Farklı Araştırma Türleri Ve Farklı Başvuru Dosyaları
 Farklı Araştırma Türleri Ve Farklı Başvuru Dosyaları Uzm. Meral Demir İ.Ü.İstanbul Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı İ.Ü.İstanbul Tıp Fakültesi Klinik Araştırmalar Etik Kurulu Öğretim Üyesi
Farklı Araştırma Türleri Ve Farklı Başvuru Dosyaları Uzm. Meral Demir İ.Ü.İstanbul Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı İ.Ü.İstanbul Tıp Fakültesi Klinik Araştırmalar Etik Kurulu Öğretim Üyesi
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ HAFTA
 İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 7. HAFTA Yeni Ürün Ruhsat Başvuru Dokümanları Common Technical Document (CTD) Başvuru Formatı Modül 1 İdari Bilgiler CTD başvuru
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 7. HAFTA Yeni Ürün Ruhsat Başvuru Dokümanları Common Technical Document (CTD) Başvuru Formatı Modül 1 İdari Bilgiler CTD başvuru
Biyobenzer ürünlerin klinik değerlendirmesi ve risk yönetimi
 Biyobenzer ürünlerin klinik değerlendirmesi ve risk yönetimi Dr. Seyfullah DAĞISTANLI 07 Mayıs 2012 Biyofarmasötikler ve Biyobenzerler Sempozyumu İZMİR Biofarmasötikler, canlı organizmadan üretilen kompleks
Biyobenzer ürünlerin klinik değerlendirmesi ve risk yönetimi Dr. Seyfullah DAĞISTANLI 07 Mayıs 2012 Biyofarmasötikler ve Biyobenzerler Sempozyumu İZMİR Biofarmasötikler, canlı organizmadan üretilen kompleks
Benzer Biyoterapötik Ürünler
 Uluslararası İlaç Üreticileri ve Dernekleri Federasyonu Benzer Biyoterapötik Ürünler Bilimsel ve Ruhsatlandırma ile İlgili Hususlar İçindekiler Biyoterapötik ilaçlara giriş 1 Biyoterapötik ilaçların üretimi
Uluslararası İlaç Üreticileri ve Dernekleri Federasyonu Benzer Biyoterapötik Ürünler Bilimsel ve Ruhsatlandırma ile İlgili Hususlar İçindekiler Biyoterapötik ilaçlara giriş 1 Biyoterapötik ilaçların üretimi
Biyolojik ajanlar ilaç dünyasının en hızlı gelişen sektörünü
 güncel gastroenteroloji 18/3 Biyobenzerler Erhan ERGİN 1, Nevin ORUÇ 2 Manisa Devlet Hastanesi, 1 Gastroenteroloji Kliniği, Manisa Ege Üniversitesi Tıp Fakültesi, 2 Gastroenteroloji Bilim Dalı, İzmir Biyolojik
güncel gastroenteroloji 18/3 Biyobenzerler Erhan ERGİN 1, Nevin ORUÇ 2 Manisa Devlet Hastanesi, 1 Gastroenteroloji Kliniği, Manisa Ege Üniversitesi Tıp Fakültesi, 2 Gastroenteroloji Bilim Dalı, İzmir Biyolojik
İNSANİ AMAÇLI İLACA ERKEN ERİŞİM PROGRAMI KILAVUZU - Sağlık Bakanlığı Çarşamba, 26 Ekim :49 - Son Güncelleme Çarşamba, 26 Ekim :49
 İNSANİ AMAÇLI İLACA ERKEN ERİŞİM PROGRAMI KILAVUZU (Sağlık Bakanlığı İlaç ve Eczacılık Genel Müdürlüğü Ekim 2005) COMPASSIONATE USE Tanım Bu program ülkemizde, Bakanlıkça ruhsatlandırılmış ve ulaşılabilir
İNSANİ AMAÇLI İLACA ERKEN ERİŞİM PROGRAMI KILAVUZU (Sağlık Bakanlığı İlaç ve Eczacılık Genel Müdürlüğü Ekim 2005) COMPASSIONATE USE Tanım Bu program ülkemizde, Bakanlıkça ruhsatlandırılmış ve ulaşılabilir
İyi Farmakovijilans Uygulamaları (İFU) Kılavuzu. Modül II Ek İzleme
 İyi Farmakovijilans Uygulamaları (İFU) Kılavuzu Modül II Ek İzleme TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU 15.07.2014 İçindekiler BÖLÜM I Giriş 1.1. Giriş... 2 BÖLÜM II Yapılar ve süreçler 2.1. İlaçlara ek
İyi Farmakovijilans Uygulamaları (İFU) Kılavuzu Modül II Ek İzleme TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU 15.07.2014 İçindekiler BÖLÜM I Giriş 1.1. Giriş... 2 BÖLÜM II Yapılar ve süreçler 2.1. İlaçlara ek
BİTKİLERDEN İLACA GİDERKEN TEMEL VE KLİNİK FARMAKOLOJİ
 BİTKİLERDEN İLACA GİDERKEN TEMEL VE KLİNİK FARMAKOLOJİ ITAM Projesi II Toplantısı Tıbbi bitkilerden ilaca giden yol Bezmialem Vakıf Üniversitesi 31 Mayıs 2013 Prof.Dr.Aydin Erenmemişoğlu NEDEN ARAŞTIRMA
BİTKİLERDEN İLACA GİDERKEN TEMEL VE KLİNİK FARMAKOLOJİ ITAM Projesi II Toplantısı Tıbbi bitkilerden ilaca giden yol Bezmialem Vakıf Üniversitesi 31 Mayıs 2013 Prof.Dr.Aydin Erenmemişoğlu NEDEN ARAŞTIRMA
SABĐT KOMBĐNASYONLU BEŞERĐ TIBBĐ ÜRÜNLER
 SABĐT KOMBĐNASYONLU BEŞERĐ TIBBĐ ÜRÜNLER Bu kılavuz- mevcut AB kılavuzlarıyla birlikte değerlendirilmelidir. (örn. Oral Kontraseptiflerin Klinik Araştırması, Kiral Aktif Maddelerin Araştırması, Klinik
SABĐT KOMBĐNASYONLU BEŞERĐ TIBBĐ ÜRÜNLER Bu kılavuz- mevcut AB kılavuzlarıyla birlikte değerlendirilmelidir. (örn. Oral Kontraseptiflerin Klinik Araştırması, Kiral Aktif Maddelerin Araştırması, Klinik
Biyoteknolojik İlaçlar
 Biyoteknolojik İlaçlar Ekim 2016 Telif Hakkı, 2016, İlaç Endüstrisi İşverenler Sendikası Bu yayın İlaç Endüstrisi İşverenler Sendikası na ait olup, yayına ilişkin tüm haklar saklıdır ve Fikir ve Sanat
Biyoteknolojik İlaçlar Ekim 2016 Telif Hakkı, 2016, İlaç Endüstrisi İşverenler Sendikası Bu yayın İlaç Endüstrisi İşverenler Sendikası na ait olup, yayına ilişkin tüm haklar saklıdır ve Fikir ve Sanat
BİYOEŞDEĞERLİK VE FAZ I ÇALIŞMALARI VE ETİK DEĞERLENDİRME AÇISINDAN YAKLAŞIM
 BİYOEŞDEĞERLİK VE FAZ I ÇALIŞMALARI VE ETİK DEĞERLENDİRME AÇISINDAN YAKLAŞIM 30-31 EKİM 2014 İSTANBUL Prof. Dr. Işık TUĞLULAR Ege Üniversitesi İlaç Araştırma-Geliştirme ve Farmakokinetik Uygulama ve Araştırma
BİYOEŞDEĞERLİK VE FAZ I ÇALIŞMALARI VE ETİK DEĞERLENDİRME AÇISINDAN YAKLAŞIM 30-31 EKİM 2014 İSTANBUL Prof. Dr. Işık TUĞLULAR Ege Üniversitesi İlaç Araştırma-Geliştirme ve Farmakokinetik Uygulama ve Araştırma
İLAÇLARIN GÜVENLİ KULLANIMI İLE İLGİLİ TEMEL KAVRAMLAR
 İLAÇLARIN GÜVENLİ KULLANIMI İLE İLGİLİ TEMEL KAVRAMLAR İlaç Beşeri Tıbbi Ürün/Ürün: Hastalığı tedavi etmek ve/veya önlemek, bir teşhis yapmak veya bir fizyolojik fonksiyonu düzeltmek, düzenlemek veya değiştirmek
İLAÇLARIN GÜVENLİ KULLANIMI İLE İLGİLİ TEMEL KAVRAMLAR İlaç Beşeri Tıbbi Ürün/Ürün: Hastalığı tedavi etmek ve/veya önlemek, bir teşhis yapmak veya bir fizyolojik fonksiyonu düzeltmek, düzenlemek veya değiştirmek
İMMUNİZASYON. Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı?
 İMMUNİZASYON Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı? Canlıya antijen verdikten belli bir süre sonra, o canlıda
İMMUNİZASYON Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı? Canlıya antijen verdikten belli bir süre sonra, o canlıda
Jeneriklerin kritik dozları ve klinik etkileri
 Jeneriklerin kritik dozları ve klinik etkileri Dr. Hüseyin Töz Ege Üniversitesi Tıp Fakültesi TİGED 2013, Çeşme, İzmir Dünya nüfusu ve yaşlı nüfus giderek artmakta Sağlık hizmetine gereksinim artmakta
Jeneriklerin kritik dozları ve klinik etkileri Dr. Hüseyin Töz Ege Üniversitesi Tıp Fakültesi TİGED 2013, Çeşme, İzmir Dünya nüfusu ve yaşlı nüfus giderek artmakta Sağlık hizmetine gereksinim artmakta
BİYOTEKNOLOJİK ÜRÜNLER VE BİYOBENZERLER
 BİYOTEKNOLOJİK ÜRÜNLER VE BİYOBENZERLER Prof. Dr. Atila Karaalp Marmara Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı Diyabet Hemşireleri Akademisi 22 Ekim 2016 Girne, Kıbrıs Özet Biyoteknolojik
BİYOTEKNOLOJİK ÜRÜNLER VE BİYOBENZERLER Prof. Dr. Atila Karaalp Marmara Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı Diyabet Hemşireleri Akademisi 22 Ekim 2016 Girne, Kıbrıs Özet Biyoteknolojik
Biyolojik İmmünojenitesi
 Biyolojik İmmünojenitesi Doç.Dr.Savaş Yaylı Karadeniz Teknik Üniversitesi Tıp Fakültesi Deri ve Zührevi Hastalıklar AD, Trabzon III.Dermatoonkoloji Günleri, Bakü, 05.09.2014 İmmünojenite: Sunu planı &
Biyolojik İmmünojenitesi Doç.Dr.Savaş Yaylı Karadeniz Teknik Üniversitesi Tıp Fakültesi Deri ve Zührevi Hastalıklar AD, Trabzon III.Dermatoonkoloji Günleri, Bakü, 05.09.2014 İmmünojenite: Sunu planı &
BİYOTEKNOLOJİK VE BİYOBENZER İLAÇLARIN RUHSATLANDIRILMASI. Uzm.Ecz.Ömer YEMŞEN
 BİYOTEKNOLOJİK VE BİYOBENZER İLAÇLARIN RUHSATLANDIRILMASI Uzm.Ecz.Ömer YEMŞEN İçerik Tanımlar, Ruhsat başvuru formu, Referans ilaç seçimi, Dosya formatı, Ruhsatlandırma süreci, Türkiye de biyobenzer başvurularda
BİYOTEKNOLOJİK VE BİYOBENZER İLAÇLARIN RUHSATLANDIRILMASI Uzm.Ecz.Ömer YEMŞEN İçerik Tanımlar, Ruhsat başvuru formu, Referans ilaç seçimi, Dosya formatı, Ruhsatlandırma süreci, Türkiye de biyobenzer başvurularda
 EKONOMİ StxCm : 129 www.ieis.org.tr www.biopharma.org.tr www.trpharmaexporters.org.tr EKONOMİ StxCm : 49 EKONOMİ StxCm : 36 ANALİZ TÜRKİYE DE BİYOTEKNOLOJİK İLAÇLAR 2017 yılında 3,9 milyar TL düzeyinde
EKONOMİ StxCm : 129 www.ieis.org.tr www.biopharma.org.tr www.trpharmaexporters.org.tr EKONOMİ StxCm : 49 EKONOMİ StxCm : 36 ANALİZ TÜRKİYE DE BİYOTEKNOLOJİK İLAÇLAR 2017 yılında 3,9 milyar TL düzeyinde
AŞI GELİŞTİRİLMESİNE YÖNELİK ÇALIŞMALAR. Dr.O.Mutlu TOPAL İstanbul 19 Aralık 2013
 AŞI GELİŞTİRİLMESİNE YÖNELİK ÇALIŞMALAR Dr.O.Mutlu TOPAL İstanbul 19 Aralık 2013 KEYMEN İLAÇ SANAYİ VE TİCARET A.Ş. HAKKINDA Ülkemizin aşılar ve serumlar için ana tedarikçilerinden biri olan ve aynı zamanda
AŞI GELİŞTİRİLMESİNE YÖNELİK ÇALIŞMALAR Dr.O.Mutlu TOPAL İstanbul 19 Aralık 2013 KEYMEN İLAÇ SANAYİ VE TİCARET A.Ş. HAKKINDA Ülkemizin aşılar ve serumlar için ana tedarikçilerinden biri olan ve aynı zamanda
İLAÇ ARAŞTIRMALARINDA SURROGATE MARKERLAR
 İLAÇ ARAŞTIRMALARINDA SURROGATE MARKERLAR YENİ GELİŞMELER VE GELECEK DR. BURÇAK KARACA 3.TIBBİ ONKOLOJİ KONGRESİ FARMAKOGENOMİK KURSU 24/MART/2010, ANTALYA Giriş Preklinik çalışmalardan elde edilen temel
İLAÇ ARAŞTIRMALARINDA SURROGATE MARKERLAR YENİ GELİŞMELER VE GELECEK DR. BURÇAK KARACA 3.TIBBİ ONKOLOJİ KONGRESİ FARMAKOGENOMİK KURSU 24/MART/2010, ANTALYA Giriş Preklinik çalışmalardan elde edilen temel
AKILCI İLAÇ KULLANIMI
 AKILCI İLAÇ KULLANIMI Yrd.Doç.Dr. Soner METE Ders Hakkında Akılcı ilaç kullanımı (AİK) ile ilgili temel kavram ve tanımların verileceği bu derste, mevzuat ve yasal düzenlemelerin AİK e sağladığı faydalar
AKILCI İLAÇ KULLANIMI Yrd.Doç.Dr. Soner METE Ders Hakkında Akılcı ilaç kullanımı (AİK) ile ilgili temel kavram ve tanımların verileceği bu derste, mevzuat ve yasal düzenlemelerin AİK e sağladığı faydalar
A. Genotoksisite testi
 Bir tıbbi cihazın klinik performansı, hedeflenen kullanım amacının gerekliliklerini yerine getirmesinin yanında; hasta vücuduyla temas ettiği süreç içerisinde, hastada minimum beklenmedik etkiye yol açması
Bir tıbbi cihazın klinik performansı, hedeflenen kullanım amacının gerekliliklerini yerine getirmesinin yanında; hasta vücuduyla temas ettiği süreç içerisinde, hastada minimum beklenmedik etkiye yol açması
İlaç geliştirme süreci
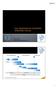 Hamdi Akan Ankara Tıp Fakültesi, Ankara İlaç geliştirme süreci Pre-Klinik araştırmalar Klinik araştırmalar Onay sonrası Keşif Hayvan/in vitro test Sentez ve formülasyon Kısa süreli Uzun süreli Faz I Faz
Hamdi Akan Ankara Tıp Fakültesi, Ankara İlaç geliştirme süreci Pre-Klinik araştırmalar Klinik araştırmalar Onay sonrası Keşif Hayvan/in vitro test Sentez ve formülasyon Kısa süreli Uzun süreli Faz I Faz
ECZACILIK FAKÜLTESİ FARMASÖTİK TEKNOLOJİ
 ECZACILIK FAKÜLTESİ FARMASÖTİK TEKNOLOJİ PROGRAM KOORDİNATÖRÜ Prof.Dr. Tamer BAYKARA Assist. Prof. Dr. Yıldız ÖZALP, yozalp@neu.edu.tr Assist. Prof. Dr. Metin ÇELİK, metin.celik@neu.edu.tr YÜKSEK LİSANS
ECZACILIK FAKÜLTESİ FARMASÖTİK TEKNOLOJİ PROGRAM KOORDİNATÖRÜ Prof.Dr. Tamer BAYKARA Assist. Prof. Dr. Yıldız ÖZALP, yozalp@neu.edu.tr Assist. Prof. Dr. Metin ÇELİK, metin.celik@neu.edu.tr YÜKSEK LİSANS
Eczacılıkta Bilimsel Çalışma İlkeleri II (4 1 5)
 Eczacılıkta Bilimsel Çalışma İlkeleri II (4 1 5) 1 Çalışmanın organizasyonu 2 Çalışmanın organizasyonu 3 Ön çalışmaların yapılması 4 Ön çalışmaların yapılması 5 Ön çalışmaların yapılması 6 Çalışma ile
Eczacılıkta Bilimsel Çalışma İlkeleri II (4 1 5) 1 Çalışmanın organizasyonu 2 Çalışmanın organizasyonu 3 Ön çalışmaların yapılması 4 Ön çalışmaların yapılması 5 Ön çalışmaların yapılması 6 Çalışma ile
BAŞVURU FORMU. Ürünün Ticari İsmi, gücü: 1- BAŞVURUNUN TİPİ
 BAŞVURU FORMU Ürünün Ticari İsmi, gücü: 1- BAŞVURUNUN TİPİ 1.1 - Bu başvuru, Veteriner Tıbbi Ürünlerde Yapılacak Değişikliklerle İlgili Yönetmelik hükümleri doğrultusunda Pazarlama İzni Genişletilmesi
BAŞVURU FORMU Ürünün Ticari İsmi, gücü: 1- BAŞVURUNUN TİPİ 1.1 - Bu başvuru, Veteriner Tıbbi Ürünlerde Yapılacak Değişikliklerle İlgili Yönetmelik hükümleri doğrultusunda Pazarlama İzni Genişletilmesi
Tıbbi Cihaz Klinik Araştırmaları
 Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Geleneksel Bitkisel Tıbbi Ürünler. 15. Hafta
 Geleneksel Bitkisel Tıbbi Ürünler 15. Hafta Bitkisel Tıbbi Ürün Etkin madde olarak bir veya birden fazla bitkisel drog, bitkisel drog preparatı ya da bu bitkisel preparatlardan bir veya bir kaçının yer
Geleneksel Bitkisel Tıbbi Ürünler 15. Hafta Bitkisel Tıbbi Ürün Etkin madde olarak bir veya birden fazla bitkisel drog, bitkisel drog preparatı ya da bu bitkisel preparatlardan bir veya bir kaçının yer
FARMAKOVİJİLANS. Uzm. Dr. Mahluga Jafarova Demirkapu
 FARMAKOVİJİLANS Uzm. Dr. Mahluga Jafarova Demirkapu Konular 1. Farmakovijilans 2. Advers reaksiyonlar 3. İlaçlara bağlı sorunlar 4. Farmakovijilans bilgi akışı 5. Advers ilaç reaksiyonu bildirim formu
FARMAKOVİJİLANS Uzm. Dr. Mahluga Jafarova Demirkapu Konular 1. Farmakovijilans 2. Advers reaksiyonlar 3. İlaçlara bağlı sorunlar 4. Farmakovijilans bilgi akışı 5. Advers ilaç reaksiyonu bildirim formu
KHDAK da Güncel Hedef Tedaviler
 KHDAK da Güncel Hedef Tedaviler Prof.Dr. Adnan Aydıner İstanbul Üniversitesi Onkoloji Enstitüsü İstanbul William, WN et al. Nature Reviews, 2009 a Güncel Hedef Tedaviler EGFR İnhibitörleri EGFR: transmembran
KHDAK da Güncel Hedef Tedaviler Prof.Dr. Adnan Aydıner İstanbul Üniversitesi Onkoloji Enstitüsü İstanbul William, WN et al. Nature Reviews, 2009 a Güncel Hedef Tedaviler EGFR İnhibitörleri EGFR: transmembran
Farklı Araştırma Türleri Ve Etik Değerlendirme Açısından Yaklaşım
 Farklı Araştırma Türleri Ve Etik Değerlendirme Açısından Yaklaşım ETİK KURULLARIN YAPILANMASI İÇİN STANDARDİZASYON GEREKLİLİKLERİ KURSU Dr. Pınar Saip İstanbul Üniversitesi Onkoloji Enstitüsü -Tıbbi Onkoloji
Farklı Araştırma Türleri Ve Etik Değerlendirme Açısından Yaklaşım ETİK KURULLARIN YAPILANMASI İÇİN STANDARDİZASYON GEREKLİLİKLERİ KURSU Dr. Pınar Saip İstanbul Üniversitesi Onkoloji Enstitüsü -Tıbbi Onkoloji
Biyobenzer kavramı ve Türkiye de biyobenzerler
 27.2.2016 Biyolojik ürünler yaşayan hücrelerde üretilir Biyobenzer kavramı ve Türkiye de biyobenzerler Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı e-posta:
27.2.2016 Biyolojik ürünler yaşayan hücrelerde üretilir Biyobenzer kavramı ve Türkiye de biyobenzerler Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı e-posta:
FARMASÖTİK BİYOTEKNOLOJİ
 FARMASÖTİK BİYOTEKNOLOJİ Biyoteknoloji Hücre ve doku biyolojisi kültürü, moleküler biyoloji, mikrobiyoloji, genetik, fizyoloji ve biyokimya gibi doğa bilimleri yanında bilgisayar ve mühendisliklerden yararlanarak,
FARMASÖTİK BİYOTEKNOLOJİ Biyoteknoloji Hücre ve doku biyolojisi kültürü, moleküler biyoloji, mikrobiyoloji, genetik, fizyoloji ve biyokimya gibi doğa bilimleri yanında bilgisayar ve mühendisliklerden yararlanarak,
Prof.Dr.Kemal NAS Dicle Üniversitesi Tıp Fakültesi Fizik Tedavi ve Rehabilitasyon AD, Romatoloji BD
 Prof.Dr.Kemal NAS Dicle Üniversitesi Tıp Fakültesi Fizik Tedavi ve Rehabilitasyon AD, Romatoloji BD Kronik enflamatuar hastalıklar, konak doku ve immun hücreleri arasındaki karmaşık etkileşimlerinden
Prof.Dr.Kemal NAS Dicle Üniversitesi Tıp Fakültesi Fizik Tedavi ve Rehabilitasyon AD, Romatoloji BD Kronik enflamatuar hastalıklar, konak doku ve immun hücreleri arasındaki karmaşık etkileşimlerinden
YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMİ İÇİN YAPILACAK MÜRACAATA DAİR KILAVUZ
 YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMİ İÇİN YAPILACAK MÜRACAATA DAİR KILAVUZ İÇİNDEKİLER 1- GMP Denetimine İlişkin Genel Prensipler 2-Daha Önce Bakanlığımızca Denetlenmiş ve GMP Uygunluğu Almış Başvurular
YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMİ İÇİN YAPILACAK MÜRACAATA DAİR KILAVUZ İÇİNDEKİLER 1- GMP Denetimine İlişkin Genel Prensipler 2-Daha Önce Bakanlığımızca Denetlenmiş ve GMP Uygunluğu Almış Başvurular
FARMAKOLOJİYE GİRİŞ. Yrd.Doç.Dr. Önder AYTEKİN
 FARMAKOLOJİYE GİRİŞ Yrd.Doç.Dr. Önder AYTEKİN Farmakoloji : İlaç Bilimi demektir. Farmakoloji ilaçların ve ilaç olabilme potansiyeli olan maddelerin kaynakları, aktiviteleri, etki mekanizmaları, yararları
FARMAKOLOJİYE GİRİŞ Yrd.Doç.Dr. Önder AYTEKİN Farmakoloji : İlaç Bilimi demektir. Farmakoloji ilaçların ve ilaç olabilme potansiyeli olan maddelerin kaynakları, aktiviteleri, etki mekanizmaları, yararları
Biosimilar Drugs. Biyobenzer İlaçlar. Biyobenzer İlaçlar / Biosimilar Drugs. Muradiye Nacak 1, Zafer Sezer 2, Aydın Erenmemişoğlu 2
 Biosimilar Drugs Biyobenzer İlaçlar Biyobenzer İlaçlar / Biosimilar Drugs Muradiye Nacak 1, Zafer Sezer 2, Aydın Erenmemişoğlu 2 1 Gaziantep Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı, Gaziantep,
Biosimilar Drugs Biyobenzer İlaçlar Biyobenzer İlaçlar / Biosimilar Drugs Muradiye Nacak 1, Zafer Sezer 2, Aydın Erenmemişoğlu 2 1 Gaziantep Üniversitesi Tıp Fakültesi Farmakoloji Anabilim Dalı, Gaziantep,
İlaç Güvenliliğinin Sağlanmasında İlaç Sanayinin Sorumlulukları ve Prosedürler 22.Ulusal Farmakoloji Kongresi 07 Kasım 2013
 İlaç Güvenliliğinin Sağlanmasında İlaç Sanayinin Sorumlulukları ve Prosedürler 22.Ulusal Farmakoloji Kongresi 07 Kasım 2013 Selcen Erdem AIFD Ruhsat Çekirdek Grubu Başkan Yardımcısı Novartis Ruhsatlandırma
İlaç Güvenliliğinin Sağlanmasında İlaç Sanayinin Sorumlulukları ve Prosedürler 22.Ulusal Farmakoloji Kongresi 07 Kasım 2013 Selcen Erdem AIFD Ruhsat Çekirdek Grubu Başkan Yardımcısı Novartis Ruhsatlandırma
BÖLÜM IV KLİNİK ÖNCESİ VE KLİNİK ÇALIŞMALAR
 BÖLÜM IV KLİNİK ÖNCESİ VE KLİNİK ÇALIŞMALAR BÖLÜM IV: KLİNİK ÖNCESİ VE KLİNİK ÇALIŞMALAR KISIM I: KLİNİK ÖNCESİ ÇALIŞMALAR A. Farmakoloji A.1 Farmakodinamik A.2 Direncin gelişimi A.3 Farmakokinetik B Hedef
BÖLÜM IV KLİNİK ÖNCESİ VE KLİNİK ÇALIŞMALAR BÖLÜM IV: KLİNİK ÖNCESİ VE KLİNİK ÇALIŞMALAR KISIM I: KLİNİK ÖNCESİ ÇALIŞMALAR A. Farmakoloji A.1 Farmakodinamik A.2 Direncin gelişimi A.3 Farmakokinetik B Hedef
BİYOBENZER ÜRÜNLERDE KLİNİK UYGULAMADA KARŞILAŞILABİLECEK SORUNLAR VE İMMUNOJENİSİTE
 BİYOBENZER ÜRÜNLERDE KLİNİK UYGULAMADA KARŞILAŞILABİLECEK SORUNLAR VE İMMUNOJENİSİTE Biyofarmasötikler, biyoteknoloji kullanılarak yaşayan organizmalardan kontrollü gen ekspresyonu, rekombinant DNA teknolojisi,
BİYOBENZER ÜRÜNLERDE KLİNİK UYGULAMADA KARŞILAŞILABİLECEK SORUNLAR VE İMMUNOJENİSİTE Biyofarmasötikler, biyoteknoloji kullanılarak yaşayan organizmalardan kontrollü gen ekspresyonu, rekombinant DNA teknolojisi,
TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI)
 TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI) KAMU ARAŞTIRMALARI DESTEK GRUBU (KAMAG) Çağrı Başlığı Monoklonal Antikor
TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI) KAMU ARAŞTIRMALARI DESTEK GRUBU (KAMAG) Çağrı Başlığı Monoklonal Antikor
Prof. Dr. Erdal Cevher Istanbul Üniversitesi, Eczacılık Fakültesi, Farmasötik Teknoloji Anabilim Dalı
 Prof. Dr. Erdal Cevher Istanbul Üniversitesi, Eczacılık Fakültesi, Farmasötik Teknoloji Anabilim Dalı BİYOLOJİK/BİYOFARMASÖTİK ÜRÜN NEDİR? Avrupa İlaç Ajansı (EMA) Biyolojik/Biyofarmasötik ürün, etkin
Prof. Dr. Erdal Cevher Istanbul Üniversitesi, Eczacılık Fakültesi, Farmasötik Teknoloji Anabilim Dalı BİYOLOJİK/BİYOFARMASÖTİK ÜRÜN NEDİR? Avrupa İlaç Ajansı (EMA) Biyolojik/Biyofarmasötik ürün, etkin
Yeni İlaçların Geliştirilmesi
 Yeni İlaçların Geliştirilmesi Prof. Dr. Meral TUNCER B.Ü.Tıp Fakültesi, Farmakoloji AbD AR-GE PROJE HAZIRLAMA, YÖNETME VE UYGULAMA EĞİTİM PROGRAMI Ankara, 24 Aralık 2015 Klinik-Öncesi Değerlendirme Sentezle
Yeni İlaçların Geliştirilmesi Prof. Dr. Meral TUNCER B.Ü.Tıp Fakültesi, Farmakoloji AbD AR-GE PROJE HAZIRLAMA, YÖNETME VE UYGULAMA EĞİTİM PROGRAMI Ankara, 24 Aralık 2015 Klinik-Öncesi Değerlendirme Sentezle
AKILCI İLAÇ KULLANIMI
 AKILCI İLAÇ KULLANIMI AKILCI FARMAKOTERAPİ EĞİTİMİNDE GRONİNGEN MODELİ (AKILCI FARMAKOTERAPİ İLKELERİ) Yrd. Doç. Dr. İlker KELLE DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ Tıbbi Farmakoloji Anabilim Dalı AKILCI
AKILCI İLAÇ KULLANIMI AKILCI FARMAKOTERAPİ EĞİTİMİNDE GRONİNGEN MODELİ (AKILCI FARMAKOTERAPİ İLKELERİ) Yrd. Doç. Dr. İlker KELLE DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ Tıbbi Farmakoloji Anabilim Dalı AKILCI
AKILCI İLAÇ KULLANIMI. Dr. M. Kürşat Tigen
 AKILCI İLAÇ KULLANIMI Dr. M. Kürşat Tigen İLAÇLAR Hastalıklardan korunma, teşhis, tedavi veya vücudun herhangi bir faaliyetini değiştirmek amacıyla kullanılan kimyasal, bitkisel, biyolojik kaynaklı ürünler
AKILCI İLAÇ KULLANIMI Dr. M. Kürşat Tigen İLAÇLAR Hastalıklardan korunma, teşhis, tedavi veya vücudun herhangi bir faaliyetini değiştirmek amacıyla kullanılan kimyasal, bitkisel, biyolojik kaynaklı ürünler
METASTATİK MESANE CA DA TEDAVİ SIRALAMASI
 METASTATİK MESANE CA DA TEDAVİ SIRALAMASI Dr. Mustafa Erman Hacettepe Üniversitesi Kanser Enstitüsü Antalya, Mart 2014 Mesane ca ve kemoterapi Kombinasyon tedavileriyle ~%50-60 yanıt oranı ve %20-30 tam
METASTATİK MESANE CA DA TEDAVİ SIRALAMASI Dr. Mustafa Erman Hacettepe Üniversitesi Kanser Enstitüsü Antalya, Mart 2014 Mesane ca ve kemoterapi Kombinasyon tedavileriyle ~%50-60 yanıt oranı ve %20-30 tam
İlaç Ar-Ge sinde Darboğazlar ve Çözüm Önerileri
 İlaç Ar-Ge sinde Darboğazlar ve Çözüm Önerileri Ahmet Gül İstanbul Üniversitesi İstanbul Tıp Fakültesi İTAM Özgün İlaç Keşfi, İlaç Geliştirilmesi ve İstanbul İlaç Sektörü ne Bilgi ve Teknoloji Aktarma
İlaç Ar-Ge sinde Darboğazlar ve Çözüm Önerileri Ahmet Gül İstanbul Üniversitesi İstanbul Tıp Fakültesi İTAM Özgün İlaç Keşfi, İlaç Geliştirilmesi ve İstanbul İlaç Sektörü ne Bilgi ve Teknoloji Aktarma
KISA ÜRÜN BİLGİSİ. 3. FARMASÖTİK FORM Vajinal Ovül Hafif sarı yağlı süspansiyon içeren sarımtırak oval kapsül şeklindedir.
 1. BEŞERİ TIBBİ ÜRÜNÜN ADI KISA ÜRÜN BİLGİSİ MACMIROR COMPLEX 500 mg + 200.000 IU vajinal ovül 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir vajinal ovül Nifuratel 500 mg; Nistatin 200.000 IU
1. BEŞERİ TIBBİ ÜRÜNÜN ADI KISA ÜRÜN BİLGİSİ MACMIROR COMPLEX 500 mg + 200.000 IU vajinal ovül 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir vajinal ovül Nifuratel 500 mg; Nistatin 200.000 IU
MEDİKAL CİHAZLAR İÇİN KLİNİK VERİ DEĞERLENDİRME
 MEDİKAL CİHAZLAR İÇİN KLİNİK VERİ DEĞERLENDİRME 04.05.2016 AdviQual KLİNİK VERİ DEĞELENDİRMESİNİ NEDEN YAPIYORUZ? Cihazın Temel Gerekliliklere uygunluğunu göstermenin bir metodu Klinik Veri Değerlendirme
MEDİKAL CİHAZLAR İÇİN KLİNİK VERİ DEĞERLENDİRME 04.05.2016 AdviQual KLİNİK VERİ DEĞELENDİRMESİNİ NEDEN YAPIYORUZ? Cihazın Temel Gerekliliklere uygunluğunu göstermenin bir metodu Klinik Veri Değerlendirme
Yöntem ve Test Seçimine Yaklaşım. Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR
 Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
Biyoeşdeğerlik ve Jenerik İlaçlar
 Biyoeşdeğerlik ve Jenerik İlaçlar Prof. Dr. Öner Süzer Cerrahpaşa Tıp Fakültesi Farmakoloji ve Klinik Farmakoloji Anabilim Dalı www.onersuzer.com Güncellenme tarihi: 19 Haziran 2006 Kaynaklar Klinik Farmakolojinin
Biyoeşdeğerlik ve Jenerik İlaçlar Prof. Dr. Öner Süzer Cerrahpaşa Tıp Fakültesi Farmakoloji ve Klinik Farmakoloji Anabilim Dalı www.onersuzer.com Güncellenme tarihi: 19 Haziran 2006 Kaynaklar Klinik Farmakolojinin
İLAÇ BAŞVURU KILAVUZU (KILAVUZ -1)
 İLAÇ BAŞVURU KILAVUZU (KILAVUZ -1) 1. Beşeri tıbbi ürünlerin/beşeri ilaçların SUT eki bedeli ödenecekler listesine dahil edilmesine yönelik başvurunun sunumu hakkında genel talimatlar: 1.1 İlaçların Tebliğ
İLAÇ BAŞVURU KILAVUZU (KILAVUZ -1) 1. Beşeri tıbbi ürünlerin/beşeri ilaçların SUT eki bedeli ödenecekler listesine dahil edilmesine yönelik başvurunun sunumu hakkında genel talimatlar: 1.1 İlaçların Tebliğ
Bitkisel ilaçlarda standardizasyon, emniyet ve etkinlik. 8. Hafta Doç.Dr.Müge Kılıçarslan
 Bitkisel ilaçlarda standardizasyon, emniyet ve etkinlik 8. Hafta Doç.Dr.Müge Kılıçarslan Emniyet Emniyet Rehberinde: 1) Karsinojenite 2) Genotoksisite 3) Toksikokinetikler ve farmakokinetikler 4) Toksisite
Bitkisel ilaçlarda standardizasyon, emniyet ve etkinlik 8. Hafta Doç.Dr.Müge Kılıçarslan Emniyet Emniyet Rehberinde: 1) Karsinojenite 2) Genotoksisite 3) Toksikokinetikler ve farmakokinetikler 4) Toksisite
İLAÇ GÜVENLİLİĞİ İZLEMİ HAKKINDA GENEL BİLGİLER
 İLAÇ GÜVENLİLİĞİ İZLEMİ HAKKINDA GENEL BİLGİLER Doç. Dr. Ahmet AKICI Marmara Ünv. Tıp Fak. Farmakoloji ve Klinik Farmakoloji Anabilim Dalı Ankara, 16 Aralık 2005 İlaç güvenliliği izlemi İlaç üretimi ve
İLAÇ GÜVENLİLİĞİ İZLEMİ HAKKINDA GENEL BİLGİLER Doç. Dr. Ahmet AKICI Marmara Ünv. Tıp Fak. Farmakoloji ve Klinik Farmakoloji Anabilim Dalı Ankara, 16 Aralık 2005 İlaç güvenliliği izlemi İlaç üretimi ve
KISA ÜRÜN BİLGİSİ. Yardımcı maddeler: Polietilen glikol g Polietilen glikol g. Setil alkol g.
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DERİVERİN Merhem 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 25 gram kremde; Aluminyum hidroksid jel (kuru)...2.50 g. Çinko oksid...1.25 g. Borik asid...1.25
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DERİVERİN Merhem 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: 25 gram kremde; Aluminyum hidroksid jel (kuru)...2.50 g. Çinko oksid...1.25 g. Borik asid...1.25
2013 NİSAN TUS FARMAKOLOJİ
 2013 NİSAN TUS FARMAKOLOJİ Doğru Yanıt : E Referans: e-tus İpucu Serisi Farmakoloji Ders Notları Sayfa: 43 Doğru Yanıt :E Doğru Yanıt : B Referans: e-tus İpucu Serisi Farmakoloji Ders Notları Sayfa: 197
2013 NİSAN TUS FARMAKOLOJİ Doğru Yanıt : E Referans: e-tus İpucu Serisi Farmakoloji Ders Notları Sayfa: 43 Doğru Yanıt :E Doğru Yanıt : B Referans: e-tus İpucu Serisi Farmakoloji Ders Notları Sayfa: 197
KISA ÜRÜN BİLGİSİ. 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DROPLEKS kulak damlası. 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin maddeler: Her 1 ml de;
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DROPLEKS kulak damlası 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin maddeler: Her 1 ml de; Fenazon 45.52 mg Lidokain hidroklorür 11.38 mg Yardımcı maddeler: Yardımcı
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI DROPLEKS kulak damlası 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin maddeler: Her 1 ml de; Fenazon 45.52 mg Lidokain hidroklorür 11.38 mg Yardımcı maddeler: Yardımcı
İnsülin Biyobenzerleri
 İnsülin Biyobenzerleri Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı e-posta: alperi@hacettepe.edu.tr 21 Nisan 2017, Girne Biyolojik Tıbbi Ürün Aşılar, toksinler,
İnsülin Biyobenzerleri Prof. Dr. Alper B. İskit Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Farmakoloji Anabilim Dalı e-posta: alperi@hacettepe.edu.tr 21 Nisan 2017, Girne Biyolojik Tıbbi Ürün Aşılar, toksinler,
SAĞLIK SEKTÖRÜ RAPORU
 SAĞLIK SEKTÖRÜ RAPORU İçindekiler DÜNYA ÜRETİMİ... 3 DÜNYA TİCARETİ... 4 TÜRKİYE DE İLAÇ ve ECZACILIK ÜRÜNLERİ SEKTÖRÜ... 5 Türkiye de Sağlık Harcamaları... 5 TÜRKİYE DE DIŞ TİCARET... 6 İhracat... 7 İthalat...
SAĞLIK SEKTÖRÜ RAPORU İçindekiler DÜNYA ÜRETİMİ... 3 DÜNYA TİCARETİ... 4 TÜRKİYE DE İLAÇ ve ECZACILIK ÜRÜNLERİ SEKTÖRÜ... 5 Türkiye de Sağlık Harcamaları... 5 TÜRKİYE DE DIŞ TİCARET... 6 İhracat... 7 İthalat...
KISA ÜRÜN BİLGİSİ. 4. KLİNİK ÖZELLİKLER 4.1 Terapötik endikasyonlar NIZORAL Ovül, akut ve kronik vulvovajinal kandidozun lokal tedavisinde kullanılır.
 KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NIZORAL 400 mg Ovül 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir ovül etkin madde olarak 400 mg ketokonazol içerir. Yardımcı maddeler: Bütil hidroksianizol
KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI NIZORAL 400 mg Ovül 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Her bir ovül etkin madde olarak 400 mg ketokonazol içerir. Yardımcı maddeler: Bütil hidroksianizol
 DENEYSEL ARAŞTIRMALAR MÜDAHALE ARAŞTIRMALARI Dr. Meltem Şengelen HÜTF Halk Sağlığı AD 12 Şubat 2015 Epidemiyoloji Sağlıkla ilgili tüm sorunların ve hastalıkların kişi-yerzaman özelliklerine göre tanımlanması,
DENEYSEL ARAŞTIRMALAR MÜDAHALE ARAŞTIRMALARI Dr. Meltem Şengelen HÜTF Halk Sağlığı AD 12 Şubat 2015 Epidemiyoloji Sağlıkla ilgili tüm sorunların ve hastalıkların kişi-yerzaman özelliklerine göre tanımlanması,
TRANSPLANTASYONDA İNDÜKSİYON TEDAVİSİ. Dr Sevgi Şahin Özel Gaziosmanpaşa Hastanesi
 TRANSPLANTASYONDA İNDÜKSİYON TEDAVİSİ Dr Sevgi Şahin Özel Gaziosmanpaşa Hastanesi TRANSPLANTASYONDA İMMUNSUPRESİF TEDAVİ İndüksiyon İdame Kurtarma Am J Surg 2009 Transplantation 2006 İndüksiyon tedavilerinin
TRANSPLANTASYONDA İNDÜKSİYON TEDAVİSİ Dr Sevgi Şahin Özel Gaziosmanpaşa Hastanesi TRANSPLANTASYONDA İMMUNSUPRESİF TEDAVİ İndüksiyon İdame Kurtarma Am J Surg 2009 Transplantation 2006 İndüksiyon tedavilerinin
Gözlemsel Araştırmalar
 Ocak 2009-1 Klinik Araş+rmalar Derneği Bilgi Kaynağı İlaçla yapılan Gözlemsel Araştırmalar İlaç olmadan yapılan Gözlemsel Araştırmalar Gerekli Dökümanlar Gözlemsel Araştırmalar İçin Nasıl Başvurmalı Türkiye
Ocak 2009-1 Klinik Araş+rmalar Derneği Bilgi Kaynağı İlaçla yapılan Gözlemsel Araştırmalar İlaç olmadan yapılan Gözlemsel Araştırmalar Gerekli Dökümanlar Gözlemsel Araştırmalar İçin Nasıl Başvurmalı Türkiye
1.1. Mevzuat. 1.2. Tanımlamalar
 1 Giriş Herkesin sağlığa ve sağlık hizmetlerine eşit ulaşma hakkının olduğu, sağlık hizmetlerinin kalitesinin yüksek olduğu, dayanışma üzerine kurulu ve tüm toplumun katılımına açık olarak yapılandırılmış
1 Giriş Herkesin sağlığa ve sağlık hizmetlerine eşit ulaşma hakkının olduğu, sağlık hizmetlerinin kalitesinin yüksek olduğu, dayanışma üzerine kurulu ve tüm toplumun katılımına açık olarak yapılandırılmış
İlaçta Ar Ge Kamu Üniversite Sanayi İşbirliğinin Önemi. Prof. Dr. Sedef Kır Hacettepe Üniversitesi Eczacılık Fakültesi
 İlaçta Ar Ge Kamu Üniversite Sanayi İşbirliğinin Önemi Prof. Dr. Sedef Kır Hacettepe Üniversitesi Eczacılık Fakültesi Hacettepe Üniversitesi Eczacılık Fakültesi Misyonumuz Evrensel bilim ve teknolojiyi
İlaçta Ar Ge Kamu Üniversite Sanayi İşbirliğinin Önemi Prof. Dr. Sedef Kır Hacettepe Üniversitesi Eczacılık Fakültesi Hacettepe Üniversitesi Eczacılık Fakültesi Misyonumuz Evrensel bilim ve teknolojiyi
MESANE KORUYUCU YAKLAŞIM. Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D.
 MESANE KORUYUCU YAKLAŞIM Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. Kanser tedavisinde multidisipliner organ koruyucu yaklaşım: Meme kanseri Anal kanal kanseri Larinks kanseri Prostat kanseri
MESANE KORUYUCU YAKLAŞIM Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. Kanser tedavisinde multidisipliner organ koruyucu yaklaşım: Meme kanseri Anal kanal kanseri Larinks kanseri Prostat kanseri
Yıldırım Beyazıt Üniversitesi
 ÜRÜN TANITIM ELEMANLARININ YETERLİLİK BELGESİ EĞİTİM PROGRAMI DERS İÇERİKLERİ (TASLAK) 1. AKILCI İLAÇ KULLANIMI (AİK) Akılcı İlaç Kullanımı (AİK) Nedir? Akılcı Olmayan İlaç Kullanımı Nedir? AİK in ve Genel
ÜRÜN TANITIM ELEMANLARININ YETERLİLİK BELGESİ EĞİTİM PROGRAMI DERS İÇERİKLERİ (TASLAK) 1. AKILCI İLAÇ KULLANIMI (AİK) Akılcı İlaç Kullanımı (AİK) Nedir? Akılcı Olmayan İlaç Kullanımı Nedir? AİK in ve Genel
Biyobenzer Ürünlerde Klinik Uygulamada Karşılaşılabilecek Sorunlar ve İmmunojenisite
 Biyobenzer Ürünlerde Klinik Uygulamada Karşılaşılabilecek Sorunlar ve İmmunojenisite Biyofarmasötikler, biyoteknoloji kullanılarak yaşayan organizmalardan kontrollü gen ekspresyonu, rekombinant DNA teknolojisi,
Biyobenzer Ürünlerde Klinik Uygulamada Karşılaşılabilecek Sorunlar ve İmmunojenisite Biyofarmasötikler, biyoteknoloji kullanılarak yaşayan organizmalardan kontrollü gen ekspresyonu, rekombinant DNA teknolojisi,
TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI)
 TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI) KAMU ARAŞTIRMALARI DESTEK GRUBU (KAMAG) Çağrı Başlığı İnsulin veya
TÜRKİYE BİLİMSEL VE TEKNOLOJİK ARAŞTIRMA KURUMU KAMU KURUMLARI ARAŞTIRMA VE GELİŞTİRME PROJELERİNİ DESTEKLEME PROGRAMI (1007 PROGRAMI) KAMU ARAŞTIRMALARI DESTEK GRUBU (KAMAG) Çağrı Başlığı İnsulin veya
DÖNEM III- SEÇMELİ DERS KURULU II KLİNİK DENEMELER. Klinik Deneme Düzenleri Yrd. Doç. Dr. Anıl DOLGUN
 DÖNEM III- SEÇMELİ DERS KURULU II KLİNİK DENEMELER Klinik Deneme Düzenleri Yrd. Doç. Dr. Anıl DOLGUN SUNUM PLANI Randomize Klinik Deneme Düzenleri Paralel grup (düzen) çalışmaları Çapraz düzen çalışmaları
DÖNEM III- SEÇMELİ DERS KURULU II KLİNİK DENEMELER Klinik Deneme Düzenleri Yrd. Doç. Dr. Anıl DOLGUN SUNUM PLANI Randomize Klinik Deneme Düzenleri Paralel grup (düzen) çalışmaları Çapraz düzen çalışmaları
RİSK DEĞERLENDİRMESİ
 RİSK DEĞERLENDİRMESİ *Kimyasallar ile biyolojik sistemler arasındaki etkileşimleri zararlı, sonuçları yönünden inceleyen bilim dalıdır. *Kimyasalların zararsızlık limitlerini belirleyen bilim dalıdır.
RİSK DEĞERLENDİRMESİ *Kimyasallar ile biyolojik sistemler arasındaki etkileşimleri zararlı, sonuçları yönünden inceleyen bilim dalıdır. *Kimyasalların zararsızlık limitlerini belirleyen bilim dalıdır.
Epidermoid Akciğer Kanseri Sistemik Tedavisinde Gelişmeler
 Epidermoid Akciğer Kanseri Sistemik Tedavisinde Gelişmeler Dr. Özden Altundağ Başkent Üniversitesi Medikal Onkoloji TAKD İÇ ANADOLU BÖLGE TOPLANTISI 10/05/2016, Ankara Akciğer Kanseri Geleneksel Sınıflandırma
Epidermoid Akciğer Kanseri Sistemik Tedavisinde Gelişmeler Dr. Özden Altundağ Başkent Üniversitesi Medikal Onkoloji TAKD İÇ ANADOLU BÖLGE TOPLANTISI 10/05/2016, Ankara Akciğer Kanseri Geleneksel Sınıflandırma
M.Vedat EĞİLMEZ. Eczacı, Farmakolog. Kamu ve Akademik İlişkiler Koordinatörü
 M.Vedat EĞİLMEZ Eczacı, Farmakolog Kamu ve Akademik İlişkiler Koordinatörü Türkiye ilaç endüstrisi 100 yıldan fazla bir geçmişe sahiptir Endüstride, uzun yıllara dayanan uluslararası kalite standartlarında
M.Vedat EĞİLMEZ Eczacı, Farmakolog Kamu ve Akademik İlişkiler Koordinatörü Türkiye ilaç endüstrisi 100 yıldan fazla bir geçmişe sahiptir Endüstride, uzun yıllara dayanan uluslararası kalite standartlarında
T.C. SAĞLIK BAKANLIĞI TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU ÜLKEMİZDE BİTKİSEL ÜRÜNLERİN PİYASAYA ÇIKIŞ SÜREÇLERİ
 T.C. SAĞLIK BAKANLIĞI TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU ÜLKEMİZDE BİTKİSEL ÜRÜNLERİN PİYASAYA ÇIKIŞ SÜREÇLERİ Dr. Ecz. Aslı CAN AĞCA Türkiye İlaç ve Tıbbi Cihaz Kurumu İlaç, Biyolojik ve Tıbbi Ürünler
T.C. SAĞLIK BAKANLIĞI TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU ÜLKEMİZDE BİTKİSEL ÜRÜNLERİN PİYASAYA ÇIKIŞ SÜREÇLERİ Dr. Ecz. Aslı CAN AĞCA Türkiye İlaç ve Tıbbi Cihaz Kurumu İlaç, Biyolojik ve Tıbbi Ürünler
BELGELER. Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD
 BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) Tıbbi laboratuvarlar için uluslar arası kalite standardı 4. bölüm
BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) Tıbbi laboratuvarlar için uluslar arası kalite standardı 4. bölüm
İlaçla-İlgili Sorunlar için Sınıflandırma
 İlaçla-İlgili Sorunlar için Sınıflandırma (14.01.2010 da revize edilmiştir) 2003-2010 Pharmaceutical Care Network Europe Foundation Vakıf, sınıflandırmanın kullanım ve validasyon sonuçları konusunda bilgilendirildiği
İlaçla-İlgili Sorunlar için Sınıflandırma (14.01.2010 da revize edilmiştir) 2003-2010 Pharmaceutical Care Network Europe Foundation Vakıf, sınıflandırmanın kullanım ve validasyon sonuçları konusunda bilgilendirildiği
FARMASÖTİK KİMYAYA GİRİŞ
 FARMASÖTİK KİMYAYA GİRİŞ Farmasötik Kimya Anabilim Dalı 2017 İLAÇLAR İnsan sağlığını korumak Yaşam kalitesini yükseltmek Sağlıklı bir toplumsal yaşam oluşturmak Hastalıkların teşhisi Tedavisi Önlenmesi
FARMASÖTİK KİMYAYA GİRİŞ Farmasötik Kimya Anabilim Dalı 2017 İLAÇLAR İnsan sağlığını korumak Yaşam kalitesini yükseltmek Sağlıklı bir toplumsal yaşam oluşturmak Hastalıkların teşhisi Tedavisi Önlenmesi
Doğal Bileşikler ve Yeni İlaçların Keşfindeki Önemi
 Doğal Bileşikler ve Yeni İlaçların Keşfindeki Önemi Doç. Dr. Ömer KOZ HO Bursa Teknik Üniversitesi, Kimya Bölümü HO BTÜ, 2014-2015 Güz Yarıyılı Seminerleri «Perşembe Seminerleri» 20 Kasım 2014 Bursa Başlıklar:
Doğal Bileşikler ve Yeni İlaçların Keşfindeki Önemi Doç. Dr. Ömer KOZ HO Bursa Teknik Üniversitesi, Kimya Bölümü HO BTÜ, 2014-2015 Güz Yarıyılı Seminerleri «Perşembe Seminerleri» 20 Kasım 2014 Bursa Başlıklar:
Prof. Dr. Hayri T. ÖZBEK Çukurova Ünviversitesi, Algoloji Bilim Dalı
 Prof. Dr. Hayri T. ÖZBEK Çukurova Ünviversitesi, Algoloji Bilim Dalı ĠLAÇ NEDĠR? Dünya Sağlık Örgütü ne (DSÖ) göre; Fizyolojik sistemleri, patolojik durumları alanın yararına değiştirmek, incelemek amacıyla
Prof. Dr. Hayri T. ÖZBEK Çukurova Ünviversitesi, Algoloji Bilim Dalı ĠLAÇ NEDĠR? Dünya Sağlık Örgütü ne (DSÖ) göre; Fizyolojik sistemleri, patolojik durumları alanın yararına değiştirmek, incelemek amacıyla
PROCTOLOG hemoroid krizleri sırasında ağrılı ve kaşıntılı anal semptomların ve fissürlerin semptomatik tedavisinde endikedir.
 KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI PROCTOLOG rektal krem 2. KALİTATİF VE KANTİTATİF BİLEŞİM 100 g. kremde, Etkin madde: Ruskogenin Trimebutin Yardımcı maddeler: Setostearil alkol Propilen glikol
KISA ÜRÜN BİLGİLERİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADI PROCTOLOG rektal krem 2. KALİTATİF VE KANTİTATİF BİLEŞİM 100 g. kremde, Etkin madde: Ruskogenin Trimebutin Yardımcı maddeler: Setostearil alkol Propilen glikol
Yeni Farmakovijilans Yönetmeliği
 Yeni Farmakovijilans Yönetmeliği Prof.Dr.Semra Şardaş Marmara Üniversitesi,Eczacılık Fakültesi TÜRKİYE DE İLAÇ GÜVENLİLİĞİ İLE İLGİLİ MEYDANA GELEN GELİŞMELER 1985 1987 2005 2010 2011 2014 Türk İlaç Advers
Yeni Farmakovijilans Yönetmeliği Prof.Dr.Semra Şardaş Marmara Üniversitesi,Eczacılık Fakültesi TÜRKİYE DE İLAÇ GÜVENLİLİĞİ İLE İLGİLİ MEYDANA GELEN GELİŞMELER 1985 1987 2005 2010 2011 2014 Türk İlaç Advers
İMMÜNSUPRESİF AJANLARIN AKILCI KULLANIMI DR. Y. KAMİL YAKUPOĞLU ONDOKUZ MAYIS ÜNİVERSİTESİ TIP FAKÜLTESİ, ÜROLOJİ A.D. TİGED-2015
 İMMÜNSUPRESİF AJANLARIN AKILCI KULLANIMI DR. Y. KAMİL YAKUPOĞLU ONDOKUZ MAYIS ÜNİVERSİTESİ TIP FAKÜLTESİ, ÜROLOJİ A.D. TİGED-2015 Akılcı İlaç Kullanımı Kişilerin klinik bulgularına ve bireysel özelliklerine
İMMÜNSUPRESİF AJANLARIN AKILCI KULLANIMI DR. Y. KAMİL YAKUPOĞLU ONDOKUZ MAYIS ÜNİVERSİTESİ TIP FAKÜLTESİ, ÜROLOJİ A.D. TİGED-2015 Akılcı İlaç Kullanımı Kişilerin klinik bulgularına ve bireysel özelliklerine
İlaç Sektöründe Ar-Ge ve İnovasyon
 İlaç Sektöründe Ar-Ge ve İnovasyon ITAM Toplantısı İstanbul, 11 Nisan 2013 Turgut Tokgöz Genel Sekreter İlaç endüstrisinde dinamik bir değişim var Yeni ürün portföyü giderek zayıflıyor. Küçük kimyasal
İlaç Sektöründe Ar-Ge ve İnovasyon ITAM Toplantısı İstanbul, 11 Nisan 2013 Turgut Tokgöz Genel Sekreter İlaç endüstrisinde dinamik bir değişim var Yeni ürün portföyü giderek zayıflıyor. Küçük kimyasal
YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMLERİ İÇİN YAPILACAK MÜRACAATLARA DAİR KILAVUZ
 YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMLERİ İÇİN YAPILACAK MÜRACAATLARA DAİR KILAVUZ 1 İÇİNDEKİLER GMP Denetimlerine İlişkin Genel Prensipler A. Yurtdışı Üretim Tesislerinde Yerinde Gerçekleştirilecek
YURT DIŞI ÜRETİM TESİSLERİNİN GMP DENETİMLERİ İÇİN YAPILACAK MÜRACAATLARA DAİR KILAVUZ 1 İÇİNDEKİLER GMP Denetimlerine İlişkin Genel Prensipler A. Yurtdışı Üretim Tesislerinde Yerinde Gerçekleştirilecek
Biyoteknolojik ürünler ve Biyobenzerler Eğitim Kursu
 Biyoteknolojik ürünler ve Biyobenzerler Eğitim Kursu (21 Kasım 2014) 10.30-11.00 Kayıt 11.00 Açılış Konuşmaları Prof.Dr.İsmail Balık/İBGAİD Başkanı Prof.Dr.Nevin Çelebi/G.Ü.Ecz.Fak. 11.10.11.30 Biyofarmasötikler
Biyoteknolojik ürünler ve Biyobenzerler Eğitim Kursu (21 Kasım 2014) 10.30-11.00 Kayıt 11.00 Açılış Konuşmaları Prof.Dr.İsmail Balık/İBGAİD Başkanı Prof.Dr.Nevin Çelebi/G.Ü.Ecz.Fak. 11.10.11.30 Biyofarmasötikler
ECZ 965 Farmasötik Ürünler İçin İyi İmalat Uygulamaları 4. HAFTA. Doç.Dr. Müge Kılıçarslan
 ECZ 965 Farmasötik Ürünler İçin İyi İmalat Uygulamaları 1 4. HAFTA Doç.Dr. Müge Kılıçarslan Rehberde yer alan bazı tanımlar 1: 2 Başlangıç maddesi: Bir farmasötik ürünün üretimde kullanılan ambalaj malzemeleri
ECZ 965 Farmasötik Ürünler İçin İyi İmalat Uygulamaları 1 4. HAFTA Doç.Dr. Müge Kılıçarslan Rehberde yer alan bazı tanımlar 1: 2 Başlangıç maddesi: Bir farmasötik ürünün üretimde kullanılan ambalaj malzemeleri
Yurt Dışından İlaç Temini Ve Kullanımı Kılavuzu
 Yurt Dışından İlaç Temini Ve Kullanımı Kılavuzu YURT DIŞINDAN İLAÇ TEMİNİ VE KULLANIMI KILAVUZU Amaç MADDE 1 - (1) Bu Kılavuz, ülkemizde ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle
Yurt Dışından İlaç Temini Ve Kullanımı Kılavuzu YURT DIŞINDAN İLAÇ TEMİNİ VE KULLANIMI KILAVUZU Amaç MADDE 1 - (1) Bu Kılavuz, ülkemizde ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ
 MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
