ÖZET. Yüksek Lisans Tezi
|
|
|
- Umut Togay
- 6 yıl önce
- İzleme sayısı:
Transkript
1 ÖZET Yüksek Lisans Tezi DEGESİZLEŞTİRCİ BİR GRUP VE AZİDO GRUPLARII BİR ARADA İÇERE Cu(II) KOMPLEKSLERİİ TERMAL AALİZ YÖTEMLERİ İLE İCELEMESİ Melike KUDURACI Ankara Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dalı Danışman : Prof. Dr. Orhan ATAKOL Bu çalışmada yapısında hem azido hem organik bir nitrolanmış ligand içeren Cu(II) kompleksleri hazırlanmış ve nitro grubunun patlamaya olan etkisini araştırmak amacıyla bu kompleksler termal analiz yöntemleri olan termogravimetri (TG) ve diferansiyel taramalı kalorimetri yöntemleriyle incelenmişlerdir. Azido grubu içeren Cu(II) komplekslerinin termal bozunmalarının patlayıcı maddelere benzer olmasından dolayı bu komplekslere - nitro grubu taşıyan ligandlar eklenmiş ve termal tepkimenin değişimi gözlenmiştir. Bu amaçla OO tipinde simetrik Schiff Bazı olan bis-, (salisiliden)-1,3-diaminopropan ve bis- 2,6(pirazol-1- il)piridin in nitrolanmış halleri ligand olarak kullanılmış ve literatürdekilere benzer şekilde kompleksler hazırlanmıştır. Hazırlanan kompleksler sırasıyla bis-, (3-nitrosalisiliden)-1,3- diaminopropan, bis-, (5-nitrosalisiliden)-1,3-diaminopropan, bis-, (3,5- dinitrosalisiliden)-1,3-diaminopropan, bis- 2,6(pirazol-1-il)-3-nitro piridin ve bis- 2,6(5- nitroindazol-1-il)piridin dir. Termal analiz sonuçlarında OO tipindeki Schiff Bazları ile hazırlanan ve dört çekirdekli oldukları tahmin edilen komplekslerde nitro grubunun termal parçalanma tepkimesinin tepkime ısısını azalttığı, pirazolil tipi ligandlarda ise artırdığı belirlenmiştir. Schiff Bazı komplekslerinde gözlenen bu ters sonuç azido grubunun elektron verici buna karşın nitro grubunun elektron çekici olması nedeniyle kompleksin elektron dağılımının homojenleşmesi sonucu kompleksin kararlılığının artması olarak yorumlanmıştır. Ağustos 2010, 106 sayfa Anahtar Kelimeler: Termogravimetri, enerjik madde, Cu(II) azido kompleksleri, azotça zengin kompleks, Cu(II)-pirazolil kompleksleri, patlayıcı madde i
2 ABSTRACT M.SC. Thesis THE IVESTIGATIO OF THE Cu(II) COMPLEXES İCLUDİG BOTH AZİDO AD İTRO GROUPS USİG THERMAL AALİSİS METHODS Melike KUDURACI Ankara University Graduate School of atural and Applied Science Department of Chemistry Supervisor: Prof. Dr. Orhan ATAKOL In this study, Cu(II) complexes having both an azido ligand and a nitrated organic ligand were prepared and these complexes were analyzed with thermogravimetry and differential scanning calorimetry methods to investigate the effects of nitro group to the explosions. Since the thermal degradation of the Cu(II) complexes with azido groups resemble explosive materials, nitro group containing ligands were added to these complexes and the changes in the thermal reactions were examined. For this purpose, the OO type symmetrical Schiff bases, bis-, (salicylidene)-1,3-diaminopropane and bis-2,6(pyrazol-1-yl)pyridine were nitrated to use as ligands and the complexes were prepared according to the literature references. The prepared complexes are bis-, (3-nitrosalicylidene)-1,3-diaminopropane, bis-, (5-nitrosalicylidene)- 1,3-diaminopropane, bis-, (3,5-dinitrosalicylidene)-1,3-diaminopropane, bis-2,6(pyrazol-1- yl)-3-nitropyridine and bis-2,6(5-nitroindazole-1-yl)pyridine, respectively. Thermal analysis results shown that the nitro groups reduce the heat of reaction in the complexes that are prepared from OO type Schiff bases and are estimated to have four nuclei, and they increase the heat of reaction in the complexes with pyrazolyl type ligands. This inverse consequence observed in the Schiff base complexes was interpreted as the change in the stability of the complex as a result of the homogenization of the electron distribution caused by the electron donating behavior of azido group and the electron withdrawing behavior of the nitro group. August 2010, 106 pages Key Words: thermogravimetry, energetic compound, Cu(II) azido complexes, nitrogen rich complex, Cu(II)-pyrazolyl complexes, explosive material ii
3 TEŞEKKÜR Tez çalışmamın her aşamasında beni yönlendiren, bana bilgileri ve hayat görüşleriyle her zaman yol gösteren, benden her zaman gülümsememi isteyen, sabırlı ve sevgi dolu danışman hocam Sayın Prof. Dr. Orhan ATAKOL a teşekkürü bir borç bilirim. Tez çalışmamda bana yardımcı olan Sayın Yrd. Doç. Dr. Ümit ERGU a, Sayın Yrd. Doç. Dr. Sevi ÖZ e, deney çalışmalarım sırasında her zaman yanımda olup beni yalnız bırakmayan sevgili arkadaşım ilüfer KAYA ya, tezimi yazarken teknik konuda benden yardımlarını esirgemeyen arkadaşım Emre AYTÜRE ye ve sayın hocalarıma teşekkürler. Benden ilgisini ve desteğini hiçbir zaman esirgemeyen, her konuda beni cesaretlendiren, yapılamayacak şeyin olmadığını, her umutsuzluğa düştüğümde bana söyleyen canım, her şeyim annem Şerife KUDURACI ya ve sevgili babam M. Hayrettin KUDURACI ya; bir tanecik yol göstericim her şeyim ağabeyim M. Deniz KUDURACI ya ve kardeşim diyebildiğim tek kişi olan yengem Ayşin KUDURACI ya çok teşekkürler. Melike KUDURACI Ankara, Ağustos 2010 iii
4 SİMGELER DİZİİ AFO DSC DTA FGA HMX TG TT, TG H 5-nitroLH 2 3-nitroLH 2 3,5-dinitroLH 2 [Cu-5-nitro-L.Cu( 3 ) 2 ] 2 [Cu-3-nitro-L.Cu( 3 ) 2 ] 2 [Cu-3,5-dinitro-L.Cu( 3 ) 2 ] 2 [Cu-5-nitro-L] Amonium itrate Fuel Oil Diferansiyel Taramalı Kalorimetri Diferansiyel Termal Anlaiz Fretilizer Grade Amonium itrate Siklotetrametilentetranitramin Termogravimetri Trinitrotoluen Trinitrogliserin Entalpi değişimi Bis-, (5-nitrosalisiliden)-1,3-propandiamin Bis-, (5-nitrosalisiliden)-1,3-propandiamin Bis-, (5-nitrosalisiliden)-1,3-propandiamin Cu(II)-Bis-, (5-nitrosalisiliden)-1,3- propandiamin dört çekirdekli azido kompleksi Cu(II)-Bis-, (3-nitrosalisiliden)-1,3- propandiamin dört çekirdekli azido kompleksi Cu(II)-Bis-, (3,5-dinitrosalisiliden)-1,3- propandiamin dört çekirdekli azido kompleksi Cu(II)-Bis-, (5-nitrosalisiliden)-1,3- propandiamin tek çekirdekli kompleksi iv
5 [Cu-3-nitro-L] [Cu-3,5-dinitro-L] 3-nitro-pp 5-nitro-indpp indpp [Cu(3-nitro-pp)( 3 ) 2 ] [Cu(3-nitro-pp)( 3 )(Cl)] [Cu(3-nitro-pp)( 3 )(O 3 )] [i(3-nitro-pp)( 3 ) 2 ] 2 [Cu-5-nitro-indpp( 3 ) 2 ] [Cu-5-nitro-indpp( 3 )(Cl)] [Cu-5-nitro-indpp( 3 )(O 3 )] [i-5-nitro-indpp( 3 ) 2 ] 2 [Cu(indpp)( 3 ) 2 ] Cu(II)-Bis-, (3-nitrosalisiliden)-1,3- propandiamin tek çekirdekli kompleksi Cu(II)-Bis-, (3,5-dinitrosalisiliden)-1,3- propandiamin tek çekirdekli kompleksi Bis-2,6(pirazol-1-il)-3-nitro piridin Bis-2,6(5-nitro indazol-1-il) piridin Bis-2,6(indazol-1-il) piridin Cu(II)-Bis-2,6(pirazol-1-il)-3-nitro piridin diazido tek çekirdekli kompleksi Cu(II)-Bis-2,6(pirazol-1-il)-3-nitro piridin azido kloro tek çekirdekli kompleksi Cu(II)-Bis-2,6(pirazol-1-il)-3-nitro piridin azido nitro tek çekirdekli kompleksi i(ii)-bis-2,6(pirazol-1-il)-3-nitro piridin diazido iki çekirdekli kompleksi Cu(II)- Bis-2,6(5-nitro indazol-1-il) piridin diazido tek çekirdekli kompleksi Cu(II)- Bis-2,6(5-nitro indazol-1-il) piridin azido kloro tek çekirdekli kompleksi Cu(II)- Bis-2,6(5-nitro indazol-1-il) piridin azido nitro tek çekirdekli kompleksi i(ii)- Bis-2,6(5-nitro indazol-1-il) piridin diazido iki çekirdekli kompleksi Cu(II)- Bis-2,6(indazol-1-il) piridin diazido tek çekirdekli kompleksi v
6 [Cu(indpp)( 3 )(Cl)] [Cu(indpp)( 3 )(O 3 )] [i(indpp)( 3 ) 2 ] 2 Cu(II)- Bis-2,6(indazol-1-il) piridin azido kloro tek çekirdekli kompleksi Cu(II)- Bis-2,6(indazol-1-il) piridin azido nitro tek çekirdekli kompleksi i(ii)- Bis-2,6(indazol-1-il) piridin diazido iki çekirdekli kompleksi vi
7 ŞEKİLLER DİZİİ Şekil 2.1 Fransa nın Brest Limanı nda 28 Temmuz 1947 de meydana gelen amonyum nitrat patlamasından bir görüntü... 9 Şekil 2.2 Patlayıcıların sınıflandırılması Şekil 2.3 Termogravimetri; fonksiyonları ve bileşenleri Şekil 2.4 Diferensiyel termal analiz aygıtı Şekil 2.5 Isı akışlı DSC hücresinin şematik gösterimi Şekil 3.1 [Cu 3-nitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 3.2 [Cu 3-nitro-L] Kompleksinin açık yapısı Şekil 3.3 [Cu 5-nitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 3.4 [Cu 5-nitro-L] Kompleksinin açık yapısı Şekil 3.5 [Cu 3,5-dinitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 3.6 [Cu 3,5-dinitro-L] Kompleksinin açık yapısı Şekil 3.7 [Cu(3-nitro-pp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 3.8 [Cu(3-nitro-pp)( 3 )(Cl)] Kompleksinin açık yapısı Şekil 3.9 [Cu(3-nitro-pp)( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 3.10 [i(3-nitro-pp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 3.11 [Cu 5-nitro-indpp( 3 ) 2 ] Kompleksinin açık yapısı Şekil 3.12 [Cu 5-nitro-indpp( 3 )(Cl)] Kompleksinin açık yapısı Şekil 3.13 [Cu 5-nitro-indpp( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 3.14 [i 5-nitro-indpp( 3 ) 2 ] Kompleksinin açık yapısı Şekil 3.15 [Cu(indpp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 3.16 [Cu(indpp)( 3 )(Cl)] Kompleksinin açık yapısı Şekil 3.17 [Cu(indpp)( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 3.18 [i(indpp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 4.1 [Cu(3-nitropp)( 3 ) 2 ], 5 C/dk ısıtma hızındaki termogram Şekil 4.2 [Cu(3-nitropp)( 3 ) 2 ], 10 C/dk ısıtma hızındaki termogram Şekil 4.3 [Cu(3-nitropp)( 3 ) 2 ], 20 C/dk ısıtma hızındaki termogram Şekil 4.4 [Cu(3-nitropp)( 3 ) 2 ], 30 C/dk ısıtma hızındaki termogram Şekil 4.5 [Cu(3-nitropp)( 3 )(Cl)], 5 C/dk ısıtma hızındaki termogram Şekil 4.6 [Cu(3-nitropp)( 3 )(Cl)], 10 C/dk ısıtma hızındaki termogram vii
8 Şekil 4.7 [Cu(3-nitropp)( 3 )(O 3 )], 10 C/dk ısıtma hızındaki termogram Şekil 4.8 [Cu(3-nitropp)( 3 )(O 3 )], 20 C/dk ısıtma hızındaki termogram Şekil 4.9 [i(3-nitropp)( 3 ) 2 ], 5 C/dk ısıtma hızındaki termogram Şekil 4.10 [i(3-nitropp)( 3 ) 2 ], 10 C/dk ısıtma hızındaki termogram Şekil 4.11 [i(3-nitropp)( 3 ) 2 ], 20 C/dk ısıtma hızındaki termogram Şekil 4.12 [Cu(5-ındpp)( 3 ) 2 ], 5 C/dk ısıtma hızındaki termogram Şekil 4.13 [Cu(5-ındpp)( 3 ) 2 ], 10 C/dk ısıtma hızındaki termogram Şekil 4.14 [Cu(5-ındpp)( 3 ) 2 ], 20 C/dk ısıtma hızındaki termogram Şekil 4.15 [Cu(5-ındpp)( 3 ) 2 ], 30 C/dk ısıtma hızındaki termogram Şekil 4.16 [Cu(ındpp)( 3 ) 2 ], 5 C/dk ısıtma hızındaki termogram Şekil 4.17 [Cu(ındpp)( 3 ) 2 ], 10 C/dk ısıtma hızındaki termogram Şekil 4.18 [Cu(ındpp)( 3 ) 2 ], 20 C/dk ısıtma hızındaki termogram Şekil 4.19 [Cu(ındpp)( 3 ) 2 ], 30 C/dk ısıtma hızındaki termogram Şekil 4.20 [Cu(ındpp)( 3 )(Cl)], 5 C/dk ısıtma hızındaki termogram Şekil 4.21 [Cu(ındpp)( 3 )(Cl)], 10 C/dk ısıtma hızındaki termogram Şekil 4.22 [Cu(ındpp)( 3 )(Cl)], 20 C/dk ısıtma hızındaki termogram Şekil 4.23 [Cu(ındpp)( 3 )(Cl)], 30 C/dk ısıtma hızındaki termogram Şekil 4.24 [Cu(ındpp)( 3 )(O 3 )], 5 C/dk ısıtma hızındaki termogram Şekil 4.25 [Cu(ındpp)( 3 )(O 3 )], 10 C/dk ısıtma hızındaki termogram Şekil 4.26 [Cu(ındpp)( 3 )(O 3 )], 20 C/dk ısıtma hızındaki termogram Şekil 4.27 [Cu(ındpp)( 3 )(O 3 )], 30 C/dk ısıtma hızındaki termogram Şekil 4.28 [i(ındpp)( 3 ) 2 ], 5 C/dk ısıtma hızındaki termogram Şekil 4.29 [i(ındpp)( 3 ) 2 ], 10 C/dk ısıtma hızındaki termogram Şekil 4.30 [i(ındpp)( 3 ) 2 ], 20 C/dk ısıtma hızındaki termogram Şekil 4.31 [i(ındpp)( 3 ) 2 ], 30 C/dk ısıtma hızındaki termogram Şekil 4.32 [Cu-3,5-dinitroL], DMF içinde, 5 C/dk ısıtma hızındaki termogram Şekil 4.33 [Cu-3,5-dinitroL], DMF içinde, 10 C/dk ısıtma hızındaki termogram Şekil 4.34 [Cu-3,5-dinitroL], DMF içinde, 20 C/dk ısıtma hızındaki termogram Şekil 4.35 [Cu-3,5-dinitroL], Dioksan içinde, 10 C/dk ısıtma hızındaki termogram Şekil 4.36 [Cu-3-nitroL], DMF içinde, 10 C/dk ısıtma hızındaki termogram viii
9 Şekil 4.37 [Cu-3-nitroL], DMF içinde, 20 C/dk ısıtma hızındaki termogram Şekil 4.38 [Cu-3-nitroL], DMF içinde, 30 C/dk ısıtma hızındaki termogram Şekil 4.39 [Cu-5-nitroL], DMF içinde, 5 C/dk ısıtma hızındaki termogram Şekil 4.40 [Cu-5-nitroL], DMF içinde, 10 C/dk ısıtma hızındaki termogram Şekil 4.41 [Cu-5-nitroL], DMF içinde, 20 C/dk ısıtma hızındaki termogram Şekil 4.42 [Cu-5-nitroL], DMF içinde, 30 C/dk ısıtma hızındaki termogram Şekil 4.43 [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 5 C/dk ısıtma hızındaki termogram Şekil 4.44 [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 10 C/dk ısıtma hızındaki termogram Şekil 4.45 [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 20 C/dk ısıtma hızındaki termogram Şekil 4.46 [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 5 C/dk ısıtma hızındaki termogram Şekil 4.47 [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 10 C/dk ısıtma hızındaki termogram Şekil 4.48 [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 20 C/dk ısıtma hızındaki termogram Şekil 4.49 [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 30 C/dk ısıtma hızındaki termogram Şekil 4.50 [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 5 C/dk ısıtma hızındaki termogram Şekil 4.51 [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 10 C/dk ısıtma hızındaki termogram Şekil 4.52 [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 20 C/dk ısıtma hızındaki termogram Şekil 4.53 [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 30 C/dk ısıtma hızındaki termogram Şekil 5.1 [Cu 3-nitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 5.2 [Cu 3-nitro-L] Kompleksinin açık yapısı Şekil 5.3 [Cu 5-nitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 5.4 [Cu 5-nitro-L] Kompleksinin açık yapısı Şekil 5.5 [Cu 3,5-dinitro-L.Cu( 3 ) 2 ] 2 Kompleksinin açık yapısı Şekil 5.6 [Cu 3,5-dinitro-L] Kompleksinin açık yapısı Şekil 5.7 [Cu(3-nitro-pp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 5.8 [Cu(3-nitro-pp)( 3 )(Cl)] Kompleksinin açık yapısı Şekil 5.9 [Cu(3-nitro-pp)( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 5.10 [i(3-nitro-pp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 5.11 [Cu 5-nitro-indpp( 3 ) 2 ] Kompleksinin açık yapısı Şekil 5.12 [Cu 5-nitro-indpp( 3 )(Cl)] Kompleksinin açık yapısı Şekil 5.13 [Cu 5-nitro-indpp( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 5.14 [i 5-nitro-indpp( 3 ) 2 ] Kompleksinin açık yapısı ix
10 Şekil 5.15 [Cu(indpp)( 3 ) 2 ] Kompleksinin açık yapısı Şekil 5.16 [Cu(indpp)( 3 )(Cl)] Kompleksinin açık yapısı Şekil 5.17 [Cu(indpp)( 3 )(O 3 )] Kompleksinin açık yapısı Şekil 5.18 [i(indpp)( 3 ) 2 ] Kompleksinin açık yapısı x
11 ÇİZELGELER DİZİİ Çizelge 2.1 II. Dünya Savaşında Kullanılan Patlayıcı Karışımları Çizelge 2.2 Termogramlarda gözlenen bazı olaylar 26 Çizelge 5.1 Komplekslerin çeşitli ısıtma hızlarındaki sonuçları.96 Çizelge 5.2 Komplekslerin çeşitli patlama hızlarındaki kj/mol cinsinden patlama ısıları...97 xi
12 İÇİDEKİLER ÖZET... i ASTRACT... ii TEŞEKKÜR... iii SİMGELER DİZİİ... iv ŞEKİLLER DİZİİİ...vii ÇİZELGELER DİZİİ... xi 1. GİRİŞ Tez Çalışmasının Amacı Çalışmanın Önemi Çalışmanın Hipotezi KURAMSAL TEMELLER Patlayıcının Tanımı Patlayıcıların Tarihsel Gelişimi Kara barutun gelişimi itrogliserinin gelişimi Civa fulminat ın gelişimi itroselüloz un gelişimi Dinamit in gelişimi Amonyum nitratın gelişimi Yasal patlayıcıların gelişimi AFO ve sudan etkilenmez tip patlayıcıların gelişimi Pikrik asitin gelişimi Tetril in gelişimi TT nin gelişimi itroguadin in gelişimi PET nin gelişimi RDX ve HMX in gelişimi Patlayıcıların Sınıflandırılması Kimyasal özelliklerine göre patlayıcılar Kullanım amaçlarına göre patlayıcılar xii
13 2.3.3 Üretim şekillerine göre patlayıcılar Güçlerine göre patlayıcılar Patlayıcıların Termokimyası Oksijen Balansı Patlama mekanizmasının yazılması Termokimyasal bir hesaplama örneği Termal Analiz Yöntemleri Hakkında Kuramsal Bilgiler Termal analiz teknikleri Termogravimetri (TG) Diferansiyel termal analiz (DTA) Diferansiyel taramalı kalorimetri (DSC) Kaynak Araştırması MATERYAL VE YÖTEM Patlayıcı Olarak Kullanılan Kompleksler Patlayıcı olarak kullanılan komplekslerin yapıları Kullanılan ligandların hazırlanması Komplekslerin hazırlanması SOUÇLAR VE HESAPLAMALAR TG Sonuçları [Cu-3-nitropp( 3 ) 2 ], 5 ⁰C/dk [Cu-3-nitropp( 3 ) 2 ], 10 ⁰C/dk [Cu-3-nitropp( 3 ) 2 ], 20 ⁰C/dk [Cu-3-nitropp( 3 ) 2 ], 30 ⁰C/dk [Cu-3-nitropp( 3 )(Cl)], 5 ⁰C/dk [Cu-3-nitropp( 3 )(Cl)], 10 ⁰C/dk [Cu-3-nitropp( 3 )(O 3 )], 10 ⁰C/dk [Cu-3-nitropp( 3 )(O 3 )], 20 ⁰C/dk [i-3-nitropp( 3 ) 2 ] 2, 5 ⁰C/dk [Cu-3-nitropp( 3 ) 2 ], 10 ⁰C/dk [Cu-3-nitropp( 3 ) 2 ], 20 ⁰C/dk [Cu-5-nitroindpp( 3 ) 2 ], 5 ⁰C/dk [Cu-5-nitroindpp( 3 ) 2 ], 10 ⁰C/dk xiii
14 [Cu-5-nitroindpp( 3 ) 2 ], 20 ⁰C/dk [Cu-5-nitroindpp( 3 ) 2 ], 30 ⁰C/dk [Cu-indpp( 3 ) 2 ], 5 ⁰C/dk [Cu-indpp( 3 ) 2 ], 10 ⁰C/dk [Cu-indpp( 3 ) 2 ], 20 ⁰C/dk [Cu-indpp( 3 ) 2 ], 30 ⁰C/dk [Cu-indpp( 3 )(Cl)], 5 ⁰C/dk [Cu-indpp( 3 )(Cl)], 10 ⁰C/dk [Cu-indpp( 3 )(Cl)], 20 ⁰C/dk [Cu-indpp( 3 )(Cl)], 30 ⁰C/dk [Cu-indpp( 3 )(O 3 )], 5 ⁰C/dk [Cu-indpp( 3 )(O 3 )], 10⁰C/dk [Cu-indpp( 3 )(O 3 )], 20 ⁰C/dk [Cu-indpp( 3 )(O 3 )], 30 ⁰C/dk [i-indpp( 3 ) 2 ] 2, 5 ⁰C/dk [i -indpp( 3 ) 2 ] 2, 10 ⁰C/dk [i -indpp( 3 ) 2 ] 2, 20 ⁰C/dk [i -indpp( 3 ) 2 ] 2, 30 ⁰C/dk [Cu-3,5-dinitroL], DMF içinde, 5 ⁰C/dk [Cu-3,5-dinitroL], DMF içinde, 10 ⁰C/dk [Cu-3,5-dinitroL], DMF içinde, 20 ⁰C/dk [Cu-3,5-dinitroL], Dioksan içinde, 10 ⁰C/dk [Cu-3-nitroL], DMF içinde, 10 ⁰C/dk [Cu-3-nitroL], DMF içinde, 20 ⁰C/dk [Cu-3-nitroL], DMF içinde, 30 ⁰C/dk [Cu-5-nitroL], DMF içinde, 5 ⁰C/dk [Cu-5-nitroL], DMF içinde, 10 ⁰C/dk [Cu-5-nitroL], DMF içinde, 20 ⁰C/dk [Cu-5-nitroL], DMF içinde, 30 ⁰C/dk [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 5 ⁰C/dk xiv
15 [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 10⁰C/dk [Cu-3,5-dinitroL.Cu( 3 ) 2 ] 2, 20 ⁰C/dk [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 5 ⁰C/dk [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 10 ⁰C/dk [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 20 ⁰C/dk [Cu-3-nitroL.Cu( 3 ) 2 ] 2, 30 ⁰C/dk [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 5 ⁰C/dk [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 10 ⁰C/dk [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 20 ⁰C/dk [Cu-5-nitroL.Cu( 3 ) 2 ] 2, 30 ⁰C/dk YORUMLAR VE TARTIŞMA KAYAKLAR ÖZGEÇMİŞ xv
16 AKARA ÜİVERSİTESİ FE BİLİMLERİ ESTİTÜSÜ YÜKSEK LİSAS TEZİ DEGESİZLEŞTİRCİ BİR GRUP VE AZİDO GRUPLARII BİR ARADA İÇERE Cu(II) KOMPLEKSLERİİ TERMAL AALİZ YÖTEMLERİ İLE İCELEMESİ Melike KUDURACI KİMYA AABİLİM DALI AKARA 2010 Her hakkı saklıdır
17
18 1. GİRİŞ 1.1 Tez Çalışmasının Amacı Kuvvetli elektron çekici gruplar olan nitro ve siyano gibi grupların organik molekülleri dengesizleştirdiği 1846 yılından beri bilinmektedir. Molekülde bu tür grupların sayısı arttıkça moleküldeki elektron dağılım aşırı lokalize (belli bir bölgede yoğunlaşma) olur. Bu yüzden de moleküller dengesiz hale gelir. Başka bir tanımla molekül enerjik molekül haline gelir. Enerjik moleküller kolaylıkla tepkime veren veya bir iç tepkime ile hızlıca küçük moleküllü ürünlere parçalanan bileşiklerdir (Olah 1991). itro ve siyano gruplarının yanı sıra kendisi elektronegatif grup olmadığı halde azit iyonu da kolaylıkla gaz ürünlere dönüşebilen bir iyon olması sebebiyle yeni patlayıcı sentezlerinde kullanılan bir grup olarak karşımıza çıkar. Yaklaşık iki yüz yıl önce 3 - iyonu H 2 - ve 2 O nun tepkimesinden meydana geldiği keşfedilen bir iyondur ve 3 - iyonu üç azot atomundan oluşmaktadır. Azit iyonunun oluşum tepkimesi: O H H H 2 O 3 - iyonu kendi içinde iki rezonans sınır formülüne sahiptir: (1) (2) Koordinasyon kimyası literatürlerinde, 1990 lı yıllara kadar azit içeren moleküllere sıklıkla rastlanmazken, azit iyonu oldukça iyi µ-köprüsü oluşturmasından dolayı 1990 lı yıllardan sonra sıklıkla karşımıza çıkmaya başlamıştır. Azitlerle ilgili ilk çalışmayı 1986 yılında Oliver Kahn ve arkadaşları ortaya koymuş ve bundan sonra sıklıkla kullanılan bir grup olmuştur. 1
19 Üçlü bağlı olan (1) formu, kümüledien bağlı olan (2) formuna göre oldukça kararlıdır. Ancak burada dikkat edilmesi gereken nokta şudur: Bilindiği gibi 2 molekülü yapısında olup çok kararlıdır. Molekül yapısına dikkat edilirse (1) formunda 2 molekülü bir elektronunu a vermiş durumdadır. Bu da 2 nin kararlılığını azaltan bir durumdur. O yüzden oda sıcaklığında kararlı olmasına rağmen 200 o C civarında termal titreşimler çok arttığından, aşağıdaki gibi bir termal tepkime oluşur: + + e - 2 Toplam tepkime: e Çalışmanın Önemi İnsanlığın en önemli mücadele alanlarından birisi uluslararası terörizmdir, terörizmin her yıl ne kadar masum insanın ölümüne neden olduğu herkesçe bilinmektedir. Buna karşın patlayıcı madde tarifleri internette serbestçe dolaşmaktadır. Bu çelişkiyi ortadan kaldırmanın yolu insan yapımı olan patlayıcı maddelerden çekinmek uzak durmak değil aksine bu maddeler ile ilgili mümkün olduğunca fazla bilgi sahibi olmaktır. Patlayıcı maddeler ile ilgili ne kadar çok bilgi sahibi olunursa, mücadele, kontrol ve bertaraf etme o oranda başarılı olur. 2
20 1.3 Çalışmanın Hipotezi Bu çalışmanın hipotezi, birisi azit grubu diğeri nitro grubu olmak üzere elektron dağılımını dengesizleştiren iki fonksiyonlu grubun aynı organik moleküle bağlı olduğu ligandların vermiş oldukları komplekslerin termal bozunmalarında açığa çıkan patlama ısısını ölçerek patlamanın brizans yani tahrip etkisinin daha yükselip yükselmediğine dair bir yorum yapabilmektir. Bu komplekslerin incelenmesinde, termal kararlılık ve patlayıcılık özellikleri açısından şu hedefler sıralanabilir: 1- Kompleks molekülün kütlesi başına, azit iyonu sayısı arttıkça, patlama ısısı artıyor mu? Molekül tamamen ani bir tepkime ile parçalanıyor mu? 2- Azit iyonu ile birlikte nitrat gibi patlayıcı özellikleri arttıran bir iyonun bulunması, patlama ısısını ve sıcaklığını arttırıyor mu? 3
21 2 KURAMSAL TEMELLER 2.1 Patlayıcının Tanımı Patlayıcı madde, ısı veya şok etkisi ile kimyasal değişikliğe uğrayan; yüksek miktarda ısı, fazla hacimde gaz meydana getiren, katı, sıvı veya gaz halindeki kimyasal maddelerdir ( Kuvvetli patlayıcıların pek çoğu kapalı bir sistemde olmadıkları veya bir şok etkisine maruz kalmazlarsa tutuşturuldukları zaman patlamazlar, sadece yanarlar. Patlayıcı maddeler, kararlı ancak aktiflanma enerjileri düşük kimyasal madde veya madde karışımları olup darbe veya kıvılcım gibi bir etkiye maruz kalması sonucu kendi kendine ilerleyen son derece hızlı kimyasal reaksiyonlarla CO, CO 2, H 2 O, 2 gibi aşırı kararlı olan veren moleküllerdir. Yanma süresi çok kısa olduğundan yanma reaksiyonu için gerekli oksijen havadan sağlanamaz. Bu nedenle patlayıcı madde yapısında oksijen içeren madde bulunması gerekir. Günümüzde enerjik moleküller olarak da adlandırılan patlayıcı maddeler, molekül üzerindeki elektron dağılımı heterojen olan kovalent bağlı moleküllerdir. Başka bir tanımlama ile de aktivasyon enerjisi fazla büyük olmayan moleküllerdir. 2.2 Patlayıcıların Tarihsel Gelişimi Kara barutun gelişimi Silah barutu olarak da bilinen kara barut, bilinen ilk patlayıcı maddedir. Çinli simyacıların M.Ö. 220 yıllarında kara barutu tesadüfen keşfettiği yazılı kaynaklarda geçmektedir. Düşük sıcaklıkta gümüşten altını ayırmak için yapılan bir çalışmada tesadüfen bulunmuştur. Reaksiyonun ilk aşamasında odun kömürünü, altın cevherine katmayı unutan simyacılar potasyum nitratı ve sülfürü karışıma ekliyorlar. Simyacılar 4
22 yaptıkları bu hatayı düzeltmeye çalışırken odun kömürünü daha sonraki aşamada eklemişlerdir. Ancak barut oldukça şiddetli bir tepkime ile patlıyor. Barutun Avrupa da tanınması hakkında farklı görüşler vardır. Bu görüşlerden birine göre barut, Markopolo nun gezileri ile Avrupa da tanınmış ve Haçlı seferleriyle de yayılmıştır. Diğer bir görüşe göre ise Avrupa da barutun Çin den bağımsız olarak icat edildiğidir. Kara barut Avrupa da 13.yy a kadar bilinmiyordu. İngiliz bir rahip olan Roger Bacon 1249 da KO 3 ile deney yaparken barutu bulmuştur de ise Berthold Schwartz adında bir rahip de Almanya da Bacon un yazdıkları hakkında çalışmış ve kara barutu sentezleyerek onun özellikleri üzerinde çalışmıştır. Schwartz ın araştırma sonuçları Avrupa nın merkezinde hızla benimsenmiştir. Bunun üzerine 13.yy ın sonlarına doğru kara barut askeri amaçlı kullanılmaya başlanmıştır. Kara barut bir yakıcı madde ve bir de yakıttan oluşur. Kükürt ve odun kömürü karışımı yakıt olarak kullanılır. Bu karışıma potasyum nitrat yakıcı madde olarak eklenir yılında karışım şekillendirildiği bilinmektedir. Buna göre ağır bir tekerlek yardımı ile barut tanecikleri daha küçük parçalar haline getirilerek geliştirilmiş ve zaman içerisinde (15.yy) daha küçük silah ve el bombası yapımında kullanılmıştır. Bunu takiben de 16.yy da daha geliştirilmiş silahların yapımında kullanılmıştır. Askeri amaçlar dışında barut ilk kez yılları arasında kuzey Avrupa daki eiman ehri nde ilk kez inşaat mühendisliği alanında kullanıldığı kayıtlara geçmiştir yılında ise Macaristan da cevher aramada kara barut kullanılmıştır. Yakın zamana kadar da barut Almanya, İsveç ve diğer ülkelerde kazı amaçlı kullanılmaktaydı (Akhavan 1998). 5
23 2.2.2 itrogliserin in gelişimi 19.yy ın ortalarına kadar kara barut kazı amaçlı kullanıldı. Madencilik ve tünel kazmak için daha güçlü patlayıcı maddelere ihtiyaç duyulmaktaydı yılında İtalyan bir profesör olan Ascanio Sabrero sıvı nitrogliserini (C 3 H 5 O 3 (O 2 ) 3 ) sentezledi. Daha sonradan nitrogliserinin patlayıcı yapısını keşfetti fakat sentezlerine devam edemedi. Bundan birkaç yıl sonra İsveçli Immanuel obel, Ascanio Sabrero nun buluşunu geliştirerek oğlu Alfred obel ile birlikte Stockholm da küçük bir imalathane açtı. Onların ilk üretim metodu nitrik asit ve sülfürik asit karışımını gliserin ile karıştırmaktı. Bu karışım soğuk su yardımı ile soğuk tutularak elde çalkalanıp soğuk suya dökülerek sentez tamamlanıyordu. ikinci üretim metodu ise koni biçiminde bir tekne içerisine soğutulmuş asit karışımı ve gliserin karışımı soğuk su ile akıtılarak yapılıyordu. Bu metot nitrogliserinin ılık ve bazik su ile yıkanması, asitliğinin giderilmesi için gerekiyordu. itrogliserin üretimi obel in ailesinin birçok kez zarar görmesine yol açtı. obel in üretim hanesinde birçok patlama olmuştur yılında olan patlamada erkek kardeşi Emil obel hayatını kaybetmiştir yılında Alfred obel Blasting cap(bir infilak maddesini ateşlemede kullanılan ve içinde cıva fulminat gibi hassas bir infilak maddesi bulunan ince bir tüp) diye adlandırılan bir başlatıcı fünye yapmıştır yılının başlıca gelişmelerden birisi de nitrogliserinin taşınması problemine çare bulunmasıdır. Çünkü nitrogliserin etki duyarlığı çok yüksek bir sıvıdır ve herhangi bir etkide çok şiddetli bir patlama ile çevresine zarar vermektedir. Bu amaçla Alfred obel, nitrogliserinin etki duyarlılığını azaltmak için Kleselguhr (diyatomit) denilen bir tül kil ile karıştırılmıştır ve 1867 yılında patentini almıştır (Akhavan 1998). itrogliserin tek bir molekülde oksitleyici (yakıcı) ve yakıtı bulundurması nedeni ile büyük bir gelişmedir. 6
24 2.2.3 Civa fulminat nin gelişimi Cıva Fulminat 17.yy da İsveç ve Alman simyacıları tarafından ilk kez sentezlendi. Alkol ve nitrik asit karışımı cıva ile muamele edilerek güçlü bir patlayıcı amaçlanmıştı. Alman simyacının bulduğu bu patlayıcının kullanım alanı bulunamadığı için unutuldu. Ta ki Edward Howard tarafından İngiltere de tekrar çalışılana kadar. Howard cıva fulminatın özelliklerini inceledi ve kara barutun başlatıcı (ateşleyicisi) olarak kullanılabileceğini söyledi (Akhavan 1998) itroselüloz un gelişimi itrogliserinin bulunduğu zamanlarda farklı çalışma koşulları altında nitroselüloz (pamuk barutu), yılları arasında sentezlenmiştir yılında Bracannot, nişastayı nitroladı; 1838 yılında ise Pelazo, Bracannot un deneylerini kâğıt, pamuk gibi maddelerin nitrolanmasını da ekledi. Fakat bu nitrolama deneyleri sonucunda nitroselüloz elde ettiğinin farkında değildi. itroselülozun üretildiği İngiltere, Fransa ve Avusturya daki birçok fabrika kaza sonucunda yıkıldı. Bu kazaların olduğu yıllarda İngiliz Hükümeti için çalışan Woolwich ve Waltham Abbey 1865 yılında nitroselülozun kararsızlığı konusundaki problemi ortadan kaldıracak bir çözüm buldu. Bu çözüm, nitroselülozu kâğıt hamuruna emdirilmesi esasına dayanıyordu (Akhavan 1998) Dinamit in gelişimi 1875 de Alfred obel, nitrogliserin ve nitroselüloz karışımının jel formunu sentezledi. Daha sonra bu jel dumansız barutun gelişiminde kullanıldı. Bu jel bir nitroselüloz, nitrogliserin ve benzen karışımıdır. İngiliz hükümeti tarafından patenti alınan benzer bileşimde bir rakip patlayıcı da 1889 da cordite diye adlandırıldı. Bu Cordite nin çeşitli formları 1930 lara kadar İngiliz Kuvvetleri tarafından temel properlant olarak kullanıldı de İsveçli kimyager olan Ohlsson ve orrbin dinamitlerin yapısının amonyum nitrat ile geliştirilebileceğini buldular. Daha sonra Alfred obel Ohlsson ve orrbin in çalışmalarını kendi patlayıcı çalışmalarında kullandı (Akhavan 1998). 7
25 2.2.6 Amonyum nitratın gelişimi Amonyum itrat ilk olarak 1654 yılında Glauber tarafından bulundu fakat 19.yy başlarına kadar patlayıcı olarak kullanılmadı. Grindel ve Rubin 19.yy başlarında kara barutun içerisinde kullanılan KO 3 yerine kullanılabilecek başka bir madde ararken amonyum nitratı buldular. Amonyum nitratın patlama özellikleri ise 1849 yılında Reise ve Millon un amonyum nitrat ve odun kömürünü ısıtması sonucu oluşan bir patlama ile anlaşıldı (Akhavan 1998). Dünyada amonyum nitrat ile ilgili patlamalar ve yangınlar olmasına rağmen, amonyum nitrat bir patlayıcı olarak nitelendirilmez. II. Dünya Savaşı sonrasında ABD Hükümeti, Avrupa ya Fretilizer Grade Amonium itrate(fga) ticaretine başladı. Bu madde, %0.35 yağ ve %3,5 kilden oluşuyordu. Bu madde patlayıcı olarak nitelendirilmediği için, sevkiyat sırasında özel önlemler alınmamıştı isan 1947 de Texas daki patlamaya kadar, bir sürü sevkiyat sorunsuz bir biçimde yapılmıştı. 15 isan 1947 de bir Fransız yük gemisi olan Grandcamp, Teksas Limanına demir attı ve ton amonyum nitrat gübre gemiye yüklendi. O gece çıkan yangın tüm gemiyi etkisi altına aldı. Gemiden yükselen yoğun siyah dumanlar yetkilileri telaşlandırdı. Çünkü yaklaşık 1 km ötede bir nükleer santral vardı. İşlerini şansa bırakmak istemeyen yetkililer geminin açık denize çekilmesine karar verdiler. Rumorkörler gemiyi uzaklaştırmaya başlarken kıyıda da meraklı bir kalabalık olan biteni seyrediyordu. Aniden gemiyi bir ateş topu sardı ve çoğu kişinin son gördüğü de bu oldu. Oluşan alev gemiden başlayarak önüne geleni yok etti ve dakikalar sonra nükleer santral de patladı. ükleer santralin patlamasıyla birlikte gemiden sağ kurtulanlarla birlikte yüzlerce çalışan da öldü. Ticaret bölgesinin çoğu yıkıldı ve yangınlar deniz kenarında korumasız olarak duran gaz depolarına kadar ulaştı. Gece yarısından kısa bir süre sonra nitrat taşıyan ikinci bir yük gemisi daha patladı ve tüm olay dizisi tekrar yaşandı. 500 den fazla kişi öldü den fazlası da ağır yaralandı. 8
26 Şekil 2.1 Fransa nın Brest Limanı nda 28 Temmuz 1947 de meydana gelen amonyum nitrat patlamasından bir görüntü. Bunun üzerine amonyum nitrat ile organik ve inorganik karışımlarının patlama özellikleri araştırıldı. Benzer bir patlama Fransa nın Brest Limanı nda 28 Temmuz 1947 de meydana geldi ( Araştırmalar sonucunda amonyum nitratın düşünülenden daha tehlikeli bir madde olduğu, depolanması ve taşınması esnasında daha ciddi düzenlemelerin yapılmasının gerektiği görüldü Yasal patlayıcıların gelişimi 1870 e kadar kömür madenlerinde patlayıcı olarak yalnızca kara barut kullanılıyordu ve birçok patlama meydana geldi. Kara barutu geliştirmek için birçok deneme yapıldı. Kara barutun üretilmesinde üç maddenin toz haline getirilip karıştırılmasından kaynaklanan sakıncalar vardı. Bu olumsuz etkilerden kurtulmak için bu üç kimyasal madde, alkol ile birleştirip tanecikli olarak kurutarak imal edildi. itroselüloz ve nitrogliserin bulunduktan sonra, kömür madenlerinde patlayıcı olarak kullanılması 9
27 denendi. Fakat bunların gaz sıkışması olan madenlerde kullanılmasının uygun olmadığı anlaşıldı. Bazı hükümetler bilim adamlarını bu sakıncalı durumu araştırması için görevlendirdi yılları arasında Fransa da, Büyük Britanya da, Belçika da ve Almanya da komisyonlar oluşturuldu. Fransa daki komisyonda madencilikte kayaların parçalanması için gerekli olan maksimum sıcaklıklar belirlendi. Bu arada Almanya ve İngiltere de patlayıcı maddeyi kararlı tutmanın tek şartının patlama sıcaklığını belli bir sıcaklıkta tutmak olduğu bulundu. Sonrasında, yeni bulunan patlayıcıları test etmek üzere 1880 de Almanya da Gelsenkirchen de bir test laboratuarı kuruldu. Bu test laboratuarı maden koşulları ile benzer olacak şekilde düzenlendi. Bu laboratuarda çeşitli patlayıcılar denendikten sonra amonyum nitrat içeren patlayıcıların madencilikte kullanılması tavsiye edildi. Bu laboratuarda analiz edilip uygun şartları taşıyan patlayıcılar yasal patlayıcılar olarak nitelendirildi. Dinamit ve kara barut bu testi geçemediği için amonyum nitrat içerikli patlayıcılar bunların yerini aldı (Akhavan 1998) AFO ve slurry (sudan etkilenmez) tip patlayıcıların gelişimi 1913 e kadar İngiltere de 287 milyon ton kömürün çıkarılması için yıllık 5000 tondan daha fazla patlayıcı madde kullanılmıştır yılına kadar ise kullanılan patlayıcıların %92 si amonyum nitrat içerikli olduğu bilinmektedir. Kullanılan patlayıcıların maliyetini düşürmek için amonyum nitrat bileşiminde deşiklikler yapılmış ancak bu geliştirilen patlayıcı maddeler suya karşı dayanıksız hale gelmiştir. Madenlerin nemli ortamlar olması nedeniyle bu önemli bir problemdi. Kimyacılar bu problemi ortadan kaldırmak için nem girişlerini engelleyecek bir paketleme sistemi geliştirdiler. Buna rağmen hala kaza patlamaları madenlerde devam ediyordu de üreticiler su geçirmez ve daha zararsız amonyum nitrat içeren patlayıcılar üretmeye başladılar. En bilinen örneği AFO ( Amonyum itrat Fuel Oil) dur (Akhavan 1998) Pikrik asidin gelişimi Pikrik asit daha doğru bir ifadeyle 2,4,6-trinitrofenol (TP) denilen kimyasal bileşiktir. Asidik yapıdaki bu fenol sarı kristal katı halde bulunur. TT benzeri, yüksek oranda 10
28 nitratlanmış diğer bileşikler gibi, pikrik asitte bir patlayıcıdır. Adını "acı" anlamına gelen Yunanca πικρος (pik' ros) kelimesinden alan pikrik asitin tadı, adı gibi acıdır larda Welter tarafından patlayıcı olarak kullanıldı de Turpin tarafından Pikrik asit(trinitrofenol) in karabarutun yerine geçebilecek uygun bir madde olduğu bulundu. İngiliz mühimmatında liddite olarak adlandırılan pikrik asit 1888 de kara barutun yerini aldı de Glauber in simyasında bahsedildiği üzere, pikrik asit muhtemelen ilk bilinen nitro fenoldü. Pikrik asit ipek ve yün için 19. Yüzyılın ikinci yarısında boya olarak kullanılmaktaydı. 1894'de Rusya da Panpushko tarafından pikrik asit hazırlandı ve onun potansiyel patlayıcı özelliği anlaşıldı. Bunun üzerine tüm dünyada askeri patlayıcı olarak kabul gördü (Akhavan 1998) Tetrilin gelişimi Tetril olarak bilinen patlayıcı madde pikrik asit ile aynı zamanlarda geliştirilmiştir. Tetril ilk olarak 1877 de Mertens tarafından hazırlandı ve yapısı Romburrgh tarafından yayınlandı. Tetril 1906 da patlayıcı olarak kullanıldı (Akhavan 1998). Tetrilin patlayıcı gücü TT den yüksek ancak oldukça kararsızdır TT nin gelişimi 1863 de Wilbrand tarafından hazırlanan trinitrotoluen [(TT),(C 7 H 5 3 O 6 )], yaklaşık 1902 lerde Almanlar ve İngilizler tarafından incelendi. 2,4,6-trinitrotoluenin hazırlanması ile ilk detaylı çalışma 1870 de Beilstein ve Kuhlberh tarafından yapıldı. Fakat çalışmaları sırasında 2,4,5- trinitrotolueni buldular de saf 2,4,6- trinitrotoluen Hepp tarafından hazırlandı. Onun yapısı 1883 yılında Claus ve Becker tarafından yayınlandı yılında Almanya da TT üretimine başlandı ve 1899 yılında bir patlayıcı bileşimi yapmak için alüminyum eklendi yılında Alman Askeriyesinde pikrik asidin yerini aldı yılında ise Amerikan askeriyesinde kullanılmaya başlandı e kadar tüm askeriyeler için bir standart oldu (I. Dünya Savaşı) (Akhavan 1998). 11
29 itroguaninin gelişimi Patlayıcı nitroguadin I. Dünya savaşında Almanlar tarafından patlayıcıların ana bileşeni olarak kullanıldı. Bu amonyum nitrat ve parafin ile karıştırılarak bomba topu olarak kullanıldı. itroguadin ayrıca II. Dünya Savaşında ve daha sonra properlantlar içerisinde kullanıldı yılında Jousselin tarafından sentezlenen nitroguadinin özellikleri 1901 yılında Vieille tarafından incelendi. I. Dünya Savaşında nitroguadinin nitro selüloz karışımı falassless properlant olarak kullanıldı. Ancak bu karışım bir arada olduklarında etkileşmektedir. Bu problem 1937 de Dynamit AG Şirketinin Gudol Pulver adındaki nitroguanidin içeren bir properlant karışımını bulması ile çözümlendi. Gudal pulver oldukça az duman çıkartıyordu ve bu nedenle silah ağzındaki birikimlerini azaltarak silahın kullanım ömrünü artırıyordu. I. Dünya savaşından sonra yeni ve daha güçlü patlayıcılar bulmak üzere büyük araştırma programları başladı. Bu programlar sayesinde RDX ve PET geliştirildi (Akhavan 1998) PET nin gelişimi PET ilk olarak 1894 yılında pentaeritrol un nitratlanması ile sentezlendi. PET nin ticari üretimi yapılamadı, çünkü pentaeritrol ün sentezinde kullanılan formaldehit ve asetaldehit II. Dünya savaşından ancak 10 yıl önce bulunmuştu. II. Dünya Savaşı ndan sırasında RDX daha çok kullanıldı. Çünkü PET nin etki duyarlılığı daha fazlaydı ve kimyasal kararlılığı daha azdı. Pentrolit adı ile bilinen %50 PET ve %50 TT karışımı geliştirildi. Bu karışım el bombası, bomba ve fitillerde kullanıldı (Akhavan 1998) RDX ve HMX in gelişimi RDX 1899 yılında bir Alman Kimyager olan Henning tarafından ilaç için kullanıldı yılında Herz tarafından bulunana kadar patlayıcı özelliği bilinmiyordu. Herz hekzaaminin doğrudan nitratlanması ile RDX i hazırlamayı başardı. Ancak, bu ürünün 12
30 verimi düşüktü ve oldukça pahalıydı. Ayrıca yüksek oranda üretim için uygun değildi. Hale 1925 de RDX üretimi için verimi %68 olan bir yöntem geliştirdi dan önce fazla bir gelişme görülmedi. Sonra Meissler RDX üretimi için kesintisiz bir metot geliştirdi; Kanada dan Rossschiessler de hezaamini başlangıç maddesi olarak kullanılmayan bir yöntem geliştirdiler. Aynı zamanda Bachmann da hekzaaminden en fazla verimi sağlayan RDX üretim yöntemi buldu. Bachmann ürünleri B tip RDX olarak biliniyordu ve %8 12 arasında sabit safsızlık içeriyordu. Bu safsızlığın özelliklerinden daha sonra yararlanıldı ve oktajen olarak bilinen HMX geliştirilmiştir. Bachmann ın bu işlemi Kanada hükümeti tarafından II. Dünya savaşı sırasında, daha sonra da Amerika da benimsendi. Bu üretim yöntemi daha ekonomikti ve aynı zamanda yeni patlayıcıların bulunmasına da öncülük etti. Saf RDX Brockmann tarafından geliştirildi ki buda RDX tip A olarak bilinir. Herz in 1920 yılındaki RDX üretimi için patent almasından sonra, İngiltere de bir Askeri Araştırma biriminde RDX için bir üretim yöntemi geliştirildi. Küçük ölçekli bir fabrikada 1933 ile 1939 yılları arasında günde 75 lbs RDX üretildi de ise tam ölçekli bir fabrika Bridgewater da kuruldu. RDX II. Dünya savaşı boyunca ingiliz bombalarını yapmakta kullanılmadı. Fakat patlayıcı karışımlarının gücünü artırmak için TT eklendi. RDX; Almanya, Fransa, İtalya, Japonya, Rusya, Amerika, İspanya ve İsveç te patlayıcı karışımlarında kullanıldı. II. Dünya Savaşı boyunca yeni ve daha güçlü patlayıcı ve patlayıcı karışımlarını araştırma- geliştirmeler devam etti. Torpex(TT/RDX/Aliminyum) ve oktajen olarak bilinen siklotetrametilentetranitramin[(hmx)(c 4 H 8 8 O 8 )] II. Dünya savaşından sonra elde edildi den sonra Octol olarak bilinen patlayıcı karışımı geliştirilmiştir. Bu karışım %75 HMX, %25 TT içeriyordu. Ayrıca II. Dünya Savaşında plastik patlayıcılar üretildi. Bu karışımlar plastikleştirme amacıyla vazelin ya da jelatinleşen nitro grupları içeriyordu (Akhavan 1998). 13
31 Çizelge 2.1 II. Dünya Savaşında Kullanılan Patlayıcı Karışımları (Akhavan 1998). İsim Karışım Baronal Baryum nitrat, TT ve aluminyum Karışım A %83 RDX ve %11 patlayıcı olmayan plastikleştirici Karışım B RDX, TT ve yağ H-6 %45 RDX, %30 TT, %20 Aluminyum ve %5 yağ Minol-2 %40 TT, %40 Amonyum itrat ve %20 Aluminyum Pentolites %50 PET ve %50 TT Picratos %50 Pikrik Asit ve %48 TT Pipe %81 PET ve %19 Gulf Crown E Oil PTX 1 %30 RDX %50 Tetril ve %20 TT PTX 2 %41 44 RDX, %26 28 PET ve %28 33 TT PVA 4 %90 RDX, %8 PVA ve %2 Dibütil fitalat RIPE %85 RDX ve %15 Gulf Crown E Oil Tetrytols %70 Tetril ve %30 TT Torpex %42 RDX, %40 TT ve %18 Aluminyum 14
32 2.3 Patlayıcıların Sınıflandırılması 15
33 2.3.1 Kimyasal özelliklerine göre patlayıcılar 1. Birincil patlayıcılar 2. İkincil patlayıcılar Askeri patlayıcılar Ticari patlayıcılar 3. Propellantlar Silah propellanları Roket propellantları Kullanım amaçlarına göre patlayıcılar Tahrip edici Bu çeşit patlayıcılar, kömür ocaklarında ve tünel inşaatlarında kullanılır. Tahrip edici patlayıcıların en iyilerinden biri, granüller bir madde olan dinamit, temel olarak TG, amonyum nitrat, sodyum nitrat ve talaş tozunun, silindir kutular içine yerleştirilmesinden ibarettir. İstenilen güce göre kullanılan malzemelerin miktarı ve oranı değiştirilebilir. Özellikle jelatin dinamiti, granit tünelleri açmak ve sualtında tahribat yapmak için kullanılır. Ayrıca yeraltı metal madenciliğinde kullanımı önemli ölçüdedir. Bu çeşit dinamit yüksek güçte bir patlayıcı olup, nitroselülozla jelatinlenmiş %25 - %50 nitrogliserin içerir. Amonyum nitratı fazla olan ve içinde biraz sodyum klorür veya sodyum karbonat bulunan dinamit, az alev çıkardığından, metan (grizu) patlamalarına neden olmaz ve bu yüzden kömür ocaklarında güvenli bir şekilde kullanılır. Amonyum nitrat içeren patlayıcılar ucuz ve güvenli olduğundan, inşaatlarda ve yüzey maden ocaklarında kullanılır. Bunlardan başka bir de AFO patlayıcıları vardır. Bunlar 16
34 %95 amonyum nitrat %5 fuel oil karışımından meydana gelir. Kayalarda açılan deliklere akıtılarak kolayca yerleştirilebildiğinden, taş ocaklarında kullanılır Ateşlemeye yarayan Detonatör, ateşleyici anlamına gelir. Detonatör patlayıcılar, hassasiyeti düşük patlayıcılarla yakıt patlayıcılarını ateşlemek amacıyla kullanılır. Hassas patlayıcılar oldukları için ufak bir sıkıştırma ile çabucak ateş alır. Cıva fulminat ve 1930 yılından beri kurşun azotür, detonatör olarak kullanılmaktadır. Kurşun azotür ateşlenince ikinci bir detonatör bölgeyi tetikler. Bu bölgede bulunan bir gram civarındaki PET, RDX veya Tetril ise asıl patlayıcıyı ateşler Askeri Askerî amaçlarla kullanılan patlayıcıların, fiziksel ve kimyasal olarak uzun zaman aşırı sıcakta durmaya dayanıklı olması, çevrelerine bomba düştüğünde bundan etkilenmemesi gerekir. Ayrıca savaş zamanında sıkıntı çekilmemesi için bu patlayıcıların hammaddelerinin de bol olması gerekmektedir. Bu nedenlerle, en iyi askerî patlayıcı TT'dir. Askerî patlayıcılardan olan pentolin (%50 PET, %50 TT) bazukalarda; amotol (%50 amonyum nitrat, %50 TT) uçaktan atılan bombalarda; tritonal (%80 TT, %20 aluminyum) torpidolarda kullanılır Propellantlar Bu patlayıcılar mermi ve roketleri hedefe ulaştırmak için kullanılır. Diğer patlayıcı tiplerinin aksine bu patlayıcılar patlamaz, bol miktarda gaz üretir. Modern tabanca fırlatıcı yakıtı, dumansız bir maddedir. Bu etil eter ve etil alkol karışımı nitro selüloz içerir. Uçak cephaneliklerinde ve uzun menzilli balistik füzelerde katı roket fırlatıcı yakıtı bulunur. 17
35 2.3.3 Üretim şekillerine göre patlayıcılar 1. Fabrikasyon Ticari Askeri 2. El yapımı Güçlerine göre patlayıcılar Alçak patlayıcılar Alçak patlayıcılar, nispeten yavaş olarak patlar veya belirli bir dayanma süresinden sonra katı halden, yaklaşık 400 m/s hızla gaz haline dönüşür. Bunlara dumansız ve kara barutlar örnek olarak verilebilir Yüksek patlayıcılar Bu tür patlayıcı maddelerde, gaz haline dönüşme hızı 3000 m/s ile 9000 m/s arasındadır. Patlama aniden meydana gelir. Bunlara TT, C3 ve C4 örnek gösterilebilir. 18
36 2.4 Patlayıcıların Termokimyası Oksijen balansı Enerjik moleküllerin tepkimeleri genellikle bir iç bozunma tepkimesidir. Ama genelde oksitleyiciler yanında tepkimeden çıkan gaz ürünler, dolayısıyla patlayıcı etkisi artar. Bu iç tepkimelerin mekanizması oksijen balansı adı verilen bir sayısal değere göre yapılır (O Keefe 1995). Oksijen balansı, Ω: X: moleküldeki C ları CO 2 yapmak için gerekli oksijen miktarı, Y: moleküldeki H leri H 2 O yapmak için gerekli oksijen miktarı, Z: moleküldeki metalleri metal oksit yapmak için gerekli oksijen miktarı, : moleküldeki oksijen sayısıdır. Ω, gerekirse % olarak da verilebilir: Ω, genelde alışılagelmiş moleküllerde negatiftir Patlama mekanizmasının yazılması Ω değeri -%40 ın altında ise iç dönüşüm tepkimesi şu esaslara göre gerçekleşir: a. Moleküldeki metal iyonu metal oksit haline dönüşür, b. Moleküldeki Hidrojenler H 2 O haline dönüşür, c. Oksijen artmışsa artan oksijen kadar CO ortaya çıkar. d. Eğer oksijen sayısı çok az ve hidrojenleri bile H 2 O ya çevirmeye yetmiyorsa C 2 H 2 veya C 2 H 4 oluşumu söz konusudur. 19
37 e. Tüm azotlar 2 haline geçer. Ω değeri -%40 ın üzerinde ise iç dönüşüm tepkimesi şu şekilde gerçekleşir: a. Moleküldeki metal iyonu metal oksit haline dönüşür b. Moleküldeki Hidrojenler H 2 O haline dönüşür c. Artan oksijen ile mümkün olduğunca karbon CO 2 haline dönüştürülür, oksijen sayısı yetmiyorsa CO basamağında bırakılır. d. Hala artan oksijen varsa O 2 olarak açığa çıkar. e. Tüm azotlar 2 haline getirilir. Özellikle H 2 O, 2 ve CO 2 çok kararlıdırlar. Bu bağlamda bir patlama tepkimesinden çıkan gaz miktarı ne kadar çok ise tepkime ısısı ve basıncı çok olur. Yeni enerjik madde çalışmaları bu nokta üzerine yoğunlaşmıştır. Özellikle CO 2 in çok oluşabilmesi için Ω değerinin mümkün olduğunca pozitife yaklaşması gerekir. Yani moleküldeki O/C oranı arttığında CO 2 oluşma olasılığı da artar. Burada bir nokta önem kazanmaktadır. Patlayıcı maddenin termal tepkimesi sonucunda CO yerine CO 2 in çıkmasıdır. Çünkü CO 2 in kararlılığı CO in kararlılığından daha fazladır. Başka bir değimle H patlama ısısı daha yüksek değer almaktadır. Tepkime sonucunda gaz çıkışı aynı miktarda olmasına rağmen patlama ısısı yüksek olması nedeni ile CO 2 oluşumu istenmektedir. Bunu yanı sıra enerjik moleküllerin iç tepkimesinde en nötür molekül azottur ve azot diğer atomlardan bağımsız bir şekilde 2 a dönüşür. Bu düşünce ile enerjik moleküllerin geleneksellikten kurtulup yenilenmeye başlandığı 1970 li yıllarda iki nokta önem kazanmıştır: 1. O/C oranını yükseltmek, 2. Molekülde sayısını artırmak. 20
38 O/C oranını artırmak istememizin sebebi oksijen balansını pozitife yaklaştırarak tepkime mekanizmasını değiştirmektir. Moleküldeki sayısını artırmak istememizin sebebiyse kararlı gaz miktarını artırmaktır. Dolayısıyla tepkime ısısını artırmaktır Termokimyasal bir hesaplama örneği Burada TG yani trinitrogliserinin termal bozunma tepkimesinin mekanizmasını açıklayacak olursak: H H C O O 2 H H C C O O O 2 O 2 2,5 H 2 O (g) + 3CO 2 (g) + 0,25 O 2 + 1,5 2 H Burada oksijen balansı değerinin pozitif olduğunu dikkate alarak tepkime mekanizmasını açıklarız. Molekülde metal iyonu olmadığı için metal oksit oluşmaz. Moleküldeki 5 Hidrojeni suya çevirmek için gerekli olan oksijen miktarı 2,5 tanedir. Toplam 9 oksijenden 6,5 oksijen kalır. Bu 6,5 oksijen, 3 karbonu karbon mono oksit yapmak için 3 tane oksijen harcanır. Geriye 3,5 tane oksijen kalır. Buda karbon mono oksiti karbondioksit yapmak için 3 tane oksijen daha kullanılır. Geriye 0,5 oksijen kalır ki buda 0,25 mol oksijen gazı olarak açığa çıkar. İşte çalışmalar bu yönde gelişmiştir yılları arasında organik molekülleri nitrolamak ile yapılan moleküller günümüze yukarıdaki iki kıstas ile tasarlanmaktadır. 2.5 Termal Analiz Yöntemleri Hakkında Kuramsal Bilgiler Termal analiz, uluslararası termal analiz konfederasyonu (ICTA) tarafından, maddedeki fiziksel ve kimyasal değişimleri, sıcaklığın bir fonksiyonu olarak kaydeden bir dizi ölçme tekniğinin tamamıdır şeklinde tanımlanmıştır (Mackenzie vd. 1972). 21
39 Bir maddeye uygulanan termal işlemlerle, ısıtma veya soğutma sırasında meydana gelen tepkimeler nedeni ile olan kütle ve enerji değişimlerinin bulunmasında kullanılan yöntemlere termoanalitik yöntemler denir. Bu tanıma göre bir termal yöntemin, termoanalitik olarak kabul edilebilmesi için aşağıdaki şartları yerine getirmesi gereklidir (Skoog 2001). 1. Fiziksel bir özellik (kütle, sıcaklık, entalpi gibi) ölçülmelidir. 2. Ölçüm doğrudan veya dolaylı olarak sıcaklığın bir fonksiyonu şeklinde ifade edilmelidir. 3. Ölçüm kontrollü bir sıcaklık programı ile gerçekleştirilmelidir Isının madde üzerinde yaptığı fiziksel ve kimyasal değişikliklerden ortaya çıkan sinyallerin büyüklüğüne bağlı olarak gerçekleştirilen analizlere termal analiz denir. Termal yöntemler uzun süredir bilinmelerine rağmen 1970 lerden sonra aletli analiz sınıfına girmiştir Termal analiz teknikleri 1. Termogravimetri (TG) 2. Diferansiyel termal analiz (DTA) 3. Diferansiyel taramalı kalorimetri (DSC) 4. Termo mekanik analiz (TMA) 5. Envolved gaz analiz (EGA) Termogravimetri (TG) Tremogarvimetrik analizde kontrol edilen bir atmosferdeki bir numunenin kütlesi, sıcaklığın veya zamanın fonksiyonu olarak artan sıcaklığa karşı kaydedilir (Skoog 2001). 22
3 )Peroksitlerle deney yapılırken aşağıdakilerden hangisi yapılmamalıdır?
 1)Aşağıdakilerden hangisi kuvvetli patlayıcılar sınıfına girer? Dumansız barut Kibrit Roket yakıtı Havai fişek Dinamit** 2) Yanıcı sıvıları parlayıcı sıvılardan ayıran en önemli fark aşağıdakilerden hangisidir?
1)Aşağıdakilerden hangisi kuvvetli patlayıcılar sınıfına girer? Dumansız barut Kibrit Roket yakıtı Havai fişek Dinamit** 2) Yanıcı sıvıları parlayıcı sıvılardan ayıran en önemli fark aşağıdakilerden hangisidir?
Kaynak: Forum Media Yayıncılık; İş Sağlığı ve güvenliği için Eğitim Seti
 Kaynak: Forum Media Yayıncılık; İş Sağlığı ve güvenliği için Eğitim Seti Kimyasallar; herkesin yaşamının bir parçasıdır. Dünyada 5 7 milyon değişik türde kimyasal madde bulunmaktadır. Kimyasal maddeler
Kaynak: Forum Media Yayıncılık; İş Sağlığı ve güvenliği için Eğitim Seti Kimyasallar; herkesin yaşamının bir parçasıdır. Dünyada 5 7 milyon değişik türde kimyasal madde bulunmaktadır. Kimyasal maddeler
7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri
 ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ 7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri Çalışma Yaprağı Konu Anlatımı-Değerlendirme çalışma Yaprağı- Çözümlü
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ 7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri Çalışma Yaprağı Konu Anlatımı-Değerlendirme çalışma Yaprağı- Çözümlü
Sınırlı miktarları. Etiketler. Özel koşullar
 UN Sınıf Sınıflandır ma Kodu Ambalaj grubu Etiketler Sınırlı miktarları Ambalajlama Portatif UN tankları Ambalaj Karışık Talimatl talimatları ar 2.1.1.3 5. 3.3 3.4.6 4.1.10 4.2.4.2 4.2.4.3 (1) (2) (3a)
UN Sınıf Sınıflandır ma Kodu Ambalaj grubu Etiketler Sınırlı miktarları Ambalajlama Portatif UN tankları Ambalaj Karışık Talimatl talimatları ar 2.1.1.3 5. 3.3 3.4.6 4.1.10 4.2.4.2 4.2.4.3 (1) (2) (3a)
STOKİYOMETRİ. Kimyasal Tepkimelerde Kütle İlişkisi
 STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI
 BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
MOL KAVRAMI I. ÖRNEK 2
 MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar.
 Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI
 ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER YASEMĐN KONMAZ 20338575 Çalışma Yaprağı Ders Anlatımı: REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER: 1.Reaktif Maddelerin
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER YASEMĐN KONMAZ 20338575 Çalışma Yaprağı Ders Anlatımı: REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER: 1.Reaktif Maddelerin
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Örnek : 3- Bileşiklerin Özellikleri :
 Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
TEHLİKELİ MADDE SINIFLANDIRMALARINDA TEHLİKE İŞARET VE LEVHALARININ ÖZELLİKLERİ
 TEHLİKELİ MADDE SINIFLANDIRMALARINDA TEHLİKE İŞARET VE LEVHALARININ ÖZELLİKLERİ Hazırlayan Abdurrahman KAR Tehlikeli Madde Güvenlik Danışmanı (TMGD) Ferhuniye Mah Mümtaz Koru Sok. Çetinkaya İş Merkezi
TEHLİKELİ MADDE SINIFLANDIRMALARINDA TEHLİKE İŞARET VE LEVHALARININ ÖZELLİKLERİ Hazırlayan Abdurrahman KAR Tehlikeli Madde Güvenlik Danışmanı (TMGD) Ferhuniye Mah Mümtaz Koru Sok. Çetinkaya İş Merkezi
ALKOLLER ve ETERLER. Kimya Ders Notu
 ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
maddelere saf maddeler denir
 Madde :Kütlesi olan her şeye madde denir. Saf madde: Aynı cins atom veya moleküllerden oluşan maddeye denir. Fiziksel yollarla kendisinden başka maddelere ayrışmayan maddelere saf maddeler denir Element:
Madde :Kütlesi olan her şeye madde denir. Saf madde: Aynı cins atom veya moleküllerden oluşan maddeye denir. Fiziksel yollarla kendisinden başka maddelere ayrışmayan maddelere saf maddeler denir Element:
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
BİLEŞİKLER VE FORMÜLLERİ
 BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
STOKĐYOMETRĐ. Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK
 STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı. Bölüm 4: Kimyasal Tepkimeler
 Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı Bölüm 4: Kimyasal Tepkimeler İçindekiler 4-1 Kimyasal Tepkimeler ve Kimyasal Eşitlikler 4-2 Kimyasal Eşitlik ve Stokiyometri
Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı Bölüm 4: Kimyasal Tepkimeler İçindekiler 4-1 Kimyasal Tepkimeler ve Kimyasal Eşitlikler 4-2 Kimyasal Eşitlik ve Stokiyometri
AROMATİK BİLEŞİKLER
 AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
Doç. Dr. Cengiz ÇETİN, BEK153 Organik Eserlerde Önleyici Koruma Ders Notu DERS 2 2. POLİMERLER
 DERS 2 2. POLİMERLER 2.1. Yardımcı Terimler Bileşik, birden fazla atomun belirli oranlarda kimyasal reaksiyonu sonucu bir araya gelmesiyle oluşan saf maddedir. Bileşiklerin en küçük yapı taşı moleküllerdir.
DERS 2 2. POLİMERLER 2.1. Yardımcı Terimler Bileşik, birden fazla atomun belirli oranlarda kimyasal reaksiyonu sonucu bir araya gelmesiyle oluşan saf maddedir. Bileşiklerin en küçük yapı taşı moleküllerdir.
Sıcaklık (Temperature):
 Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
KİMYASAL BİLEŞİKLER İÇERİK
 KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA
 İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR
 KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
MADDENİN SINIFLANDIRILMASI
 MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ)
 ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
2+ 2- Mg SO 4. (NH 4 ) 2 SO 4 (amonyum sülfat) bileşiğini katyon ve anyonlara ayıralım.
 KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Yrd.Doç.Dr. Emre YALAMAÇ. Yrd.Doç.Dr. Emre YALAMAÇ İÇERİK
 İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
12-B. 31. I. 4p II. 5d III. 6s
 -B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
-B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
DENEYĐN ADI. Organik bileşiklerde nitel olarak Karbon ve hidrojen elementlerinin aranması
 DENEYĐN ADI Organik bileşiklerde nitel olarak Karbon ve hidrojen elementlerinin aranması Deneyin amacı Organik bir bileşikte karbon ve hidrojen elementlerinin nitel olarak tayin etmek. Nicel ve nitel analiz
DENEYĐN ADI Organik bileşiklerde nitel olarak Karbon ve hidrojen elementlerinin aranması Deneyin amacı Organik bir bileşikte karbon ve hidrojen elementlerinin nitel olarak tayin etmek. Nicel ve nitel analiz
Termal Enerji Depolama Nedir
 RAŞİT AYTAŞ 1 Termal Enerji Depolama Nedir 1.1. Duyulur Isı 1.2. Gizli Isı Depolama 1.3. Termokimyasal Enerji Depolama 2 Termal Enerji Depolama Nedir Termal enerji depolama sistemleriyle ozon tabakasına
RAŞİT AYTAŞ 1 Termal Enerji Depolama Nedir 1.1. Duyulur Isı 1.2. Gizli Isı Depolama 1.3. Termokimyasal Enerji Depolama 2 Termal Enerji Depolama Nedir Termal enerji depolama sistemleriyle ozon tabakasına
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı
 Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
HACETTEPE ÜNĐVERSĐTESĐ EĞĐTĐM FAKÜLTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME
 HACETTEPE ÜNĐVERSĐTESĐ EĞĐTĐM FAKÜLTESĐ KĐMYA ÖĞRETMENLĐĞĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME 8. SINIF FEN VE TEKNOLOJĐ DERSĐ 3. ÜNĐTE: MADDENĐN YAPISI VE ÖZELLĐKLERĐ KONU: BAZLAR ÇALIŞMA YAPRAĞI
HACETTEPE ÜNĐVERSĐTESĐ EĞĐTĐM FAKÜLTESĐ KĐMYA ÖĞRETMENLĐĞĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME 8. SINIF FEN VE TEKNOLOJĐ DERSĐ 3. ÜNĐTE: MADDENĐN YAPISI VE ÖZELLĐKLERĐ KONU: BAZLAR ÇALIŞMA YAPRAĞI
Elektronların Dizilişi ve Kimyasal Özellikleri
 Elektronların Dizilişi ve Kimyasal Özellikleri ELEKTRON ALIŞVERİŞİ VE SONUÇLARI: Helyum (2), neon (10), argon (18)in elektron dağılımları incelendiğinde Eğer bu üç elementin birer elektronu daha olsaydı,
Elektronların Dizilişi ve Kimyasal Özellikleri ELEKTRON ALIŞVERİŞİ VE SONUÇLARI: Helyum (2), neon (10), argon (18)in elektron dağılımları incelendiğinde Eğer bu üç elementin birer elektronu daha olsaydı,
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ AZİT VE NİTRO GRUBU İÇEREN ORGANİK PATLAYICI MADDELERİN TERMAL ANALİZ YÖNTEMLERİ İLE İNCELENMESİ VE YÜKSEK BASINÇLI SIVI KROMATOGRAFİSİ
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ AZİT VE NİTRO GRUBU İÇEREN ORGANİK PATLAYICI MADDELERİN TERMAL ANALİZ YÖNTEMLERİ İLE İNCELENMESİ VE YÜKSEK BASINÇLI SIVI KROMATOGRAFİSİ
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla
 ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
HİDROKARBONLAR ve ALKANLAR. Kimya Ders Notu
 HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
Aşağıda verilen özet bilginin ayrıntısını, ders kitabı. olarak önerilen, Erdik ve Sarıkaya nın Temel. Üniversitesi Kimyası" Kitabı ndan okuyunuz.
 KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
FEN ve TEKNOLOJİ DERSİ / PERİYODİK SİSTEM. Metaller, Ametaller ve Yarı metaller
 Metaller, Ametaller ve Yarı metaller 1 Elementler gösterdikleri benzer özelliklere göre metaller, yarı metaller ve ametaller olarak sınıflandırılabilirler. Periyodik tabloda metal, ametal ve yarı metallerin
Metaller, Ametaller ve Yarı metaller 1 Elementler gösterdikleri benzer özelliklere göre metaller, yarı metaller ve ametaller olarak sınıflandırılabilirler. Periyodik tabloda metal, ametal ve yarı metallerin
GENEL KİMYA 101 ÖDEV 3
 TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ
 ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
MAKİNE VE TEÇHİZAT İŞLERİNDE İSG
 MAKİNE VE TEÇHİZAT İŞLERİNDE İSG 3.HAFTA Hazırlayan: Öğr. Gör. Tuğberk ÖNAL MALATYA 2017 YAKITLAR -YANMA Enerji birçok ülke için günümüzün en önemli sorunlarının başında gelmektedir. Özellikle ülkemiz
MAKİNE VE TEÇHİZAT İŞLERİNDE İSG 3.HAFTA Hazırlayan: Öğr. Gör. Tuğberk ÖNAL MALATYA 2017 YAKITLAR -YANMA Enerji birçok ülke için günümüzün en önemli sorunlarının başında gelmektedir. Özellikle ülkemiz
Radyoaktif elementin tek başına bulunması, bileşik içinde bulunması, katı, sıvı, gaz, iyon halinde bulunması radyoaktif özelliğini etkilemez.
 RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
A- LABORATUAR MALZEMELERİ
 1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
ÖLÇME, DEĞERLENDİRME VE SINAV HİZMETLERİ GENEL MÜDÜRLÜĞÜ
 AY EKİM 06-07 EĞİTİM - ÖĞRETİM YILI. SINIF VE MEZUN GRUP KİMYA HAFTA DERS SAATİ. Kimya nedir?. Kimya ne işe yarar?. Kimyanın sembolik dili Element-sembol Bileşik-formül. Güvenliğimiz ve Kimya KONU ADI
AY EKİM 06-07 EĞİTİM - ÖĞRETİM YILI. SINIF VE MEZUN GRUP KİMYA HAFTA DERS SAATİ. Kimya nedir?. Kimya ne işe yarar?. Kimyanın sembolik dili Element-sembol Bileşik-formül. Güvenliğimiz ve Kimya KONU ADI
5) Çözünürlük(Xg/100gsu)
 1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
Termal analiz esasları;
 Termal analiz esasları; Termal analiz; sıcaklık değişmesine karşı bir katı maddenin fiziksel ve kimyasal reaksiyonlar sonucunda özelliklerindeki değişimlerin ölçülmesi ve yorumlanmasıdır. Sıcaklığa bağlı
Termal analiz esasları; Termal analiz; sıcaklık değişmesine karşı bir katı maddenin fiziksel ve kimyasal reaksiyonlar sonucunda özelliklerindeki değişimlerin ölçülmesi ve yorumlanmasıdır. Sıcaklığa bağlı
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI
 ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 9.Çözünmüş İnorganik ve Organik Katıların Giderimi Yrd. Doç. Dr. Kadir GEDİK İnorganiklerin Giderimi Çözünmüş maddelerin çapları
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 9.Çözünmüş İnorganik ve Organik Katıların Giderimi Yrd. Doç. Dr. Kadir GEDİK İnorganiklerin Giderimi Çözünmüş maddelerin çapları
YANMA. Özgür Deniz KOÇ
 YANMA Özgür Deniz KOÇ 16360057 1 Yanma Tepkimesi Yanma Çeşitleri İÇİNDEKİLER Yavaş Yanma Hızlı Yanma Parlama ve Parlatma Kendi Kendine Yanma 2 Yanma Sınıfları Yanma Kayıpları 3 Yanma Tepkimesi Nedir Bir
YANMA Özgür Deniz KOÇ 16360057 1 Yanma Tepkimesi Yanma Çeşitleri İÇİNDEKİLER Yavaş Yanma Hızlı Yanma Parlama ve Parlatma Kendi Kendine Yanma 2 Yanma Sınıfları Yanma Kayıpları 3 Yanma Tepkimesi Nedir Bir
Zeyfiye TEZEL Mehmet KARACADAĞ
 PROJENİN ADI: POLİMER KATKILI ASFALT ÜRETİMİNİN ARAŞTIRILMASI Zeyfiye TEZEL Mehmet KARACADAĞ ( Kimya Bilim Danışmanlığı Çalıştayı Çalışması 29 Ağustos-9 Eylül 2007) Danışman: Doç.Dr. İsmet KAYA 1 PROJENİN
PROJENİN ADI: POLİMER KATKILI ASFALT ÜRETİMİNİN ARAŞTIRILMASI Zeyfiye TEZEL Mehmet KARACADAĞ ( Kimya Bilim Danışmanlığı Çalıştayı Çalışması 29 Ağustos-9 Eylül 2007) Danışman: Doç.Dr. İsmet KAYA 1 PROJENİN
PERİYODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR
 PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
7. Bölüm: Termokimya
 7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
VIA GRUBU ELEMENTLERİ
 Bölüm 8 VIA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. O, S, Se, Te, Po O ve S: Ametal Se ve Te: Yarı metal Po: Metal *Oksijen genellikle bileşiklerinde
Bölüm 8 VIA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. O, S, Se, Te, Po O ve S: Ametal Se ve Te: Yarı metal Po: Metal *Oksijen genellikle bileşiklerinde
Kimyanın Temel Kanunları
 Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar
 10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
Patlama nedir? Tozların, gazların ve patlayıcıların kimyasal enerjisinin ani büyümesi. www. atexegitim.com
 Patlama nedir? Tozların, gazların ve patlayıcıların kimyasal enerjisinin ani büyümesi Toz patlaması Toz patlaması Toz patlamasının etkileri çok yıkıcı olabilmektedir. Toz Patlaması - Riskler ve Korunma
Patlama nedir? Tozların, gazların ve patlayıcıların kimyasal enerjisinin ani büyümesi Toz patlaması Toz patlaması Toz patlamasının etkileri çok yıkıcı olabilmektedir. Toz Patlaması - Riskler ve Korunma
HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT
 1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
İÇİNDEKİLER TEMEL KAVRAMLAR - 2. 1. Atomlar, Moleküller, İyonlar...36. 1.2. Atomlar...36. 1.2. Moleküller...37. 1.3. İyonlar...37
 vi TEMEL KAVRAMLAR - 2 1. Atomlar, Moleküller, İyonlar...36 1.2. Atomlar...36 1.2. Moleküller...37 1.3. İyonlar...37 2. Kimyasal Türlerin Adlandırılması...38 2.1. İyonların Adlandırılması...38 2.2. İyonik
vi TEMEL KAVRAMLAR - 2 1. Atomlar, Moleküller, İyonlar...36 1.2. Atomlar...36 1.2. Moleküller...37 1.3. İyonlar...37 2. Kimyasal Türlerin Adlandırılması...38 2.1. İyonların Adlandırılması...38 2.2. İyonik
GENEL KİMYA. 6. Konu: Mol Kavramı ve Avagadro Sayısı
 GENEL KİMYA 6. Konu: Mol Kavramı ve Avagadro Sayısı Avagadro Sayısı ve Mol Kavramı Gündelik hayatta bazen maddeleri teker teker ifade etmek yerine toplu halde belirtmeyi tercih ederiz. Örneğin; 30 tane
GENEL KİMYA 6. Konu: Mol Kavramı ve Avagadro Sayısı Avagadro Sayısı ve Mol Kavramı Gündelik hayatta bazen maddeleri teker teker ifade etmek yerine toplu halde belirtmeyi tercih ederiz. Örneğin; 30 tane
ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ
 ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ ALKANLAR Alkanların Fiziksel Özellikleri Alkan bileşikleri apolar yapılı moleküllerden oluşur. Bu yüzden molekülleri arasında zayıf London kuvvetleri bulunmaktadır.
ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ ALKANLAR Alkanların Fiziksel Özellikleri Alkan bileşikleri apolar yapılı moleküllerden oluşur. Bu yüzden molekülleri arasında zayıf London kuvvetleri bulunmaktadır.
Partikül halinde kömürden uzaklaştırılma. Çözelti halinde kömürden uzaklaştırılma
 Partikül halinde kömürden uzaklaştırılma Çözelti halinde kömürden uzaklaştırılma * Kısa analiz (proximate analysis): KÖMÜRE UYGULANAN KİMYASAL ANALİZLER nem, kül, uçucu madde ve sabit karbon oranlanm belirlemede
Partikül halinde kömürden uzaklaştırılma Çözelti halinde kömürden uzaklaştırılma * Kısa analiz (proximate analysis): KÖMÜRE UYGULANAN KİMYASAL ANALİZLER nem, kül, uçucu madde ve sabit karbon oranlanm belirlemede
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI
 TÜBİTAK-BİDEB KİMYA BİLİM DANIŞMANLIĞI ÇALIŞTAYI ORGANİK KİMYA GRUBU BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI Proje Raporu Proje Ekibi Rebi BARIN İbrahim ŞEN Proje Danışmanı
TÜBİTAK-BİDEB KİMYA BİLİM DANIŞMANLIĞI ÇALIŞTAYI ORGANİK KİMYA GRUBU BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI Proje Raporu Proje Ekibi Rebi BARIN İbrahim ŞEN Proje Danışmanı
STOKİYOMETRİ: SABİT ORANLAR YASASI
 STOKİYOMETRİ: SABİT ORANLAR YASASI AMAÇ Bu deneyin amacı sabit oranlar yasasını kanıtlamak ve öğrencilere tartma analizlerinde ve hata hesaplamalarında deneyim kazandırmaktır. TEORİ Stokiyometri, bir bileşiğin
STOKİYOMETRİ: SABİT ORANLAR YASASI AMAÇ Bu deneyin amacı sabit oranlar yasasını kanıtlamak ve öğrencilere tartma analizlerinde ve hata hesaplamalarında deneyim kazandırmaktır. TEORİ Stokiyometri, bir bileşiğin
Burada a, b, c ve d katsayılar olup genelde birer tamsayıdır. Benzer şekilde 25 o C de hidrojen ve oksijen gazlarından suyun oluşumu; H 2 O (s)
 1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
ENDÜSTRİYEL SÜREÇLER MEVCUT VERİLERİN DEĞERLENDİRİLMESİ
 ENDÜSTRİYEL SÜREÇLER MEVCUT VERİLERİN DEĞERLENDİRİLMESİ Erhan ÜNAL 10.03.2010 1 4. ENDÜSTRİYEL PROSESLER 4.1. Genel Çimento Üretimi Kireç Üretimi Kireçtaşı ve Dolomit Kullanımı Soda Külü Üretimi ve Kullanımı
ENDÜSTRİYEL SÜREÇLER MEVCUT VERİLERİN DEĞERLENDİRİLMESİ Erhan ÜNAL 10.03.2010 1 4. ENDÜSTRİYEL PROSESLER 4.1. Genel Çimento Üretimi Kireç Üretimi Kireçtaşı ve Dolomit Kullanımı Soda Külü Üretimi ve Kullanımı
Sınıf 5.1 maddeleri ve bu gibi maddeleri içeren nesneler aşağıdaki şekilde alt gruplara ayrılır:
 2.2.51 Sınıf 5. 1 Yükseltgen maddeler 2.2.51.1 Kriterler 2.2.51.1.1 Sınıf 5.1 başlığı, kendilerinin alevlenir olmaları gerekmediği halde, genellikle oksijen vererek başka malzemelerin yanmasına neden olan
2.2.51 Sınıf 5. 1 Yükseltgen maddeler 2.2.51.1 Kriterler 2.2.51.1.1 Sınıf 5.1 başlığı, kendilerinin alevlenir olmaları gerekmediği halde, genellikle oksijen vererek başka malzemelerin yanmasına neden olan
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ
 ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
ELEMENT Aynı tür atomlardan oluşmuş saf maddelere element denir. ELEMENTLERİN ÖZELLİKLERİ 1. Aynı tür atomlardan oluşurlar. 2. Saf ve homojendirler.
 SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
Çözünürlük kuralları
 Çözünürlük kuralları Bütün amonyum, bileşikleri suda çok çözünürler. Alkali metal (Grup IA) bileşikleri suda çok çözünürler. Klorür (Cl ), bromür (Br ) ve iyodür (I ) bileşikleri suda çok çözünürler, ancak
Çözünürlük kuralları Bütün amonyum, bileşikleri suda çok çözünürler. Alkali metal (Grup IA) bileşikleri suda çok çözünürler. Klorür (Cl ), bromür (Br ) ve iyodür (I ) bileşikleri suda çok çözünürler, ancak
İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I
 İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I D) Elmas E) Oltu taşı 1. I. Civa II. Kil III. Kireç taşı Yukarıdaki maddelerden hangileri simyacılar tarafından kullanılmıştır? D) II ve III E) I, II
İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I D) Elmas E) Oltu taşı 1. I. Civa II. Kil III. Kireç taşı Yukarıdaki maddelerden hangileri simyacılar tarafından kullanılmıştır? D) II ve III E) I, II
Malzeme Bilgisi. Madde ve Özellikleri
 Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
Maddenin Yapısı Hakkında İlk Düşünceler
 Madde ve Özkütle 2 YGS Fizik 1 YGS Kimya Kimya Bilimi başlıklı hazırladığımız bu yazıda; kimya biliminin ne olduğunu, bileşikleri, kimyanın amaçlarını ve sembolik dilini öğrenebilirsiniz. Kimya Bilimi
Madde ve Özkütle 2 YGS Fizik 1 YGS Kimya Kimya Bilimi başlıklı hazırladığımız bu yazıda; kimya biliminin ne olduğunu, bileşikleri, kimyanın amaçlarını ve sembolik dilini öğrenebilirsiniz. Kimya Bilimi
ELEMENTLER VE SEMBOLLERİ
 ELEMENTLER VE SEMBOLLERİ MADDE SAF MADDE ELEMENT BİLEŞİK KARIŞIM HOMOJEN KARIŞIM HETEROJEN KARIŞIM SAF MADDE: Kendisinden başka madde bulundur-mayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran
ELEMENTLER VE SEMBOLLERİ MADDE SAF MADDE ELEMENT BİLEŞİK KARIŞIM HOMOJEN KARIŞIM HETEROJEN KARIŞIM SAF MADDE: Kendisinden başka madde bulundur-mayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran
KİMYA-IV. Aromatik Hidrokarbonlar (Arenler) (5. Konu)
 KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
ALLİL KLORÜR ÜRETİMİ. Gökhan IŞIK O.Okan YEŞİLYURT
 ALLİL KLORÜR ÜRETİMİ Allil klorür üretiminin ana maddesi propilen ve klor dur. Allil klorürün verimli ve ekonomik sentezi 1930 larda yüksek sıcaklıklarda (300-500 C) klorlaşma reaksiyonu ile Shell Geliştirme
ALLİL KLORÜR ÜRETİMİ Allil klorür üretiminin ana maddesi propilen ve klor dur. Allil klorürün verimli ve ekonomik sentezi 1930 larda yüksek sıcaklıklarda (300-500 C) klorlaşma reaksiyonu ile Shell Geliştirme
ÖMRÜNÜ TAMAMLAMIŞ LASTİKLERİN GERİ KAZANIMINDA PİROLİZ YÖNTEMİ
 ÖMRÜNÜ TAMAMLAMIŞ LASTİKLERİN GERİ KAZANIMINDA PİROLİZ YÖNTEMİ Onursal Yakaboylu Aslı İşler Filiz Karaosmanoğlu 1 Onursal Yakaboylu - Atık Sempozyumu / Antalya 19/04/2011 İÇERİK Lastik Atık lastik Atık
ÖMRÜNÜ TAMAMLAMIŞ LASTİKLERİN GERİ KAZANIMINDA PİROLİZ YÖNTEMİ Onursal Yakaboylu Aslı İşler Filiz Karaosmanoğlu 1 Onursal Yakaboylu - Atık Sempozyumu / Antalya 19/04/2011 İÇERİK Lastik Atık lastik Atık
1 mol = 6, tane tanecik. Maddelerde tanecik olarak atom, molekül ve iyonlar olduğunda dolayı mol ü aşağıdaki şekillerde tanımlamak mümkündür.
 1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
HAZIRLAYAN Mutlu ŞAHİN. Hacettepe Fen Bilgisi Öğretmenliği. DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ
 HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ DENEYİN AMACI: Doymuş NaCl çözeltisinin elektroliz sonucu elementlerine ayrışmasının
HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ DENEYİN AMACI: Doymuş NaCl çözeltisinin elektroliz sonucu elementlerine ayrışmasının
HISTOLOJIDE BOYAMA YÖNTEMLERI. Dr. Yasemin Sezgin. yasemin sezgin
 HISTOLOJIDE BOYAMA YÖNTEMLERI Dr. Yasemin Sezgin yasemin sezgin HÜRESEL BOYAMANIN TEMEL PRENSİPLERİ Hem fiziksel hem kimyasal faktörler hücresel boyamayı etkilemektedir BOYAMA MEKANIZMASı Temelde boyanın
HISTOLOJIDE BOYAMA YÖNTEMLERI Dr. Yasemin Sezgin yasemin sezgin HÜRESEL BOYAMANIN TEMEL PRENSİPLERİ Hem fiziksel hem kimyasal faktörler hücresel boyamayı etkilemektedir BOYAMA MEKANIZMASı Temelde boyanın
TY T Temel Yeterlilik Testi
 Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
Element ve Bileşikler
 Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
Doç. Dr. Özlem Esen KARTAL (A Şubesi) Yrd. Doç. Dr. Adil KOÇ (B Şubesi) :16:57 1
 Doç. Dr. Özlem Esen KARTAL (A Şubesi) Yrd. Doç. Dr. Adil KOÇ (B Şubesi) 28.10.2015 12:16:57 1 I. DERS İÇERİĞİ 1.KİMYA MÜHENDİSLİĞİ MESLEĞİNİN TANIMI 2.KİMYA MÜHENDİSLİĞİNİN TARİHSEL GELİŞİMİ 3. MÜHENDİSLİK
Doç. Dr. Özlem Esen KARTAL (A Şubesi) Yrd. Doç. Dr. Adil KOÇ (B Şubesi) 28.10.2015 12:16:57 1 I. DERS İÇERİĞİ 1.KİMYA MÜHENDİSLİĞİ MESLEĞİNİN TANIMI 2.KİMYA MÜHENDİSLİĞİNİN TARİHSEL GELİŞİMİ 3. MÜHENDİSLİK
Karbonmonoksit (CO) Oluşumu
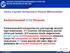 Yanma Kaynaklı Emisyonların Oluşum Mekanizmaları Karbonmonoksit (CO) Oluşumu Karbonmonoksit emisyonlarının ana kaynağı benzinli taşıt motorlarıdır. H/Y oranının CO emisyonu üzerine etkisi çok fazladır.
Yanma Kaynaklı Emisyonların Oluşum Mekanizmaları Karbonmonoksit (CO) Oluşumu Karbonmonoksit emisyonlarının ana kaynağı benzinli taşıt motorlarıdır. H/Y oranının CO emisyonu üzerine etkisi çok fazladır.
PROBLEM 5.1. PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3. Başlama basamağı. Gelişme basamağı. Sonlanma basamağı
 PROBLEM 5.1 PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3 Başlama basamağı Gelişme basamağı Sonlanma basamağı vb. PROBLEM 5.4 Örnek Çözüm PROBLEM 5.5 Örnek Çözüm PROBLEM 5.6 Örnek Çözüm PROBLEM 5.7 PROBLEM 5.8 FENOL
PROBLEM 5.1 PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3 Başlama basamağı Gelişme basamağı Sonlanma basamağı vb. PROBLEM 5.4 Örnek Çözüm PROBLEM 5.5 Örnek Çözüm PROBLEM 5.6 Örnek Çözüm PROBLEM 5.7 PROBLEM 5.8 FENOL
KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ
 Ek 2 ULUSAL ÖĞRENCİ TASARIM YARIŞMASI PROBLEM TANIMI KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ 1. Giriş Türk kömür rezervlerinden metanol üretimi Kömürden metanol üretimi,
Ek 2 ULUSAL ÖĞRENCİ TASARIM YARIŞMASI PROBLEM TANIMI KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ 1. Giriş Türk kömür rezervlerinden metanol üretimi Kömürden metanol üretimi,
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten. Kimyasal Bağlar.
 Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER
 BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI
 KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI Fiziksel ve Kimyasal Olaylar Maddenin şekil, yoğunluk, çözünürlük, genleşme, erime ve kaynama noktaları, sıvı, katı ya da gaz hâlde olması
KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI Fiziksel ve Kimyasal Olaylar Maddenin şekil, yoğunluk, çözünürlük, genleşme, erime ve kaynama noktaları, sıvı, katı ya da gaz hâlde olması
5.111 Ders Özeti #12. Konular: I. Oktet kuralından sapmalar
 5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen
 Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen ix xiii xv xvii xix xxi 1. Çevre Kimyasına Giriş 3 1.1. Çevre Kimyasına Genel Bakış ve Önemi
Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen ix xiii xv xvii xix xxi 1. Çevre Kimyasına Giriş 3 1.1. Çevre Kimyasına Genel Bakış ve Önemi
İstanbul Bilgi Üniversitesi Enerji Sistemleri Mühendisliği. Çevreye Duyarlı Sürdürülebilir ve Yenilenebilir Enerji Üretimi ve Kullanımı
 İstanbul Bilgi Üniversitesi Enerji Sistemleri Mühendisliği Çevreye Duyarlı Sürdürülebilir ve Yenilenebilir Enerji Üretimi ve Kullanımı Günlük Hayatımızda Enerji Tüketimi Fosil Yakıtlar Kömür Petrol Doğalgaz
İstanbul Bilgi Üniversitesi Enerji Sistemleri Mühendisliği Çevreye Duyarlı Sürdürülebilir ve Yenilenebilir Enerji Üretimi ve Kullanımı Günlük Hayatımızda Enerji Tüketimi Fosil Yakıtlar Kömür Petrol Doğalgaz
BİTKİ BESİN MADDELERİ (BBM)
 BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
