Doç. Dr. Meltem ERCAN
|
|
|
- Gizem Açık
- 8 yıl önce
- İzleme sayısı:
Transkript
1 578 ĐÇĐNDEKĐLER 1- Termodinamik kavramlar 2- Termodinamik Yasalar 3- Biyoenerjetik 4- Biyomoleküler Sistemlerde Enerji Aktarımları 5- Canlıların Atp Hidrolizine Bağımlı Olarak Gerçekleştirdikleri Đşler TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ Doç. Dr.
2 580 enerji ve madde alışverişi yapabilirler. Canlılar termodinamik açıdan açık sistem kapsamındadırlar. Dengeli sistemler termodinamiği adı verilen klasik termodinamiğin çalışma alanı izole ve kapalı sistemlerdir. TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ 1- TERMODĐNAMĐK KAVRAMLAR Doç. Dr. Termodinamik enerjinin bilimi olarak tanımlanabilir. Kelime olarak Latince therme (ısı) ve dynamis (güç) sözcüklerinden türemiştir. Termodinamik enerjinin korunumundan faydalanarak mekanik ve termal olayları birbirine bağlayan bir bilimdir. Termodinamikte, fiziksel ve kimyasal olayların gerçekleştirmekte olduğu belirli sınırlar içindeki madde topluluğuna sistem denir. Sistemin durumu üzerinde etki yapabilen ve sistemle temas halinde bulunan ortam ise çevre olarak adlandırılır. Sistem ve çevrenin ikisi birlikte de evreni oluştururlar. Çevre Evren Sistem Sistemler, çevresiyle enerji ve madde alışverişinin olup olmamasına göre 3 ana gruba ayrılırlar. 1- Yalıtılmış Sistem; hacim, kütle ve enerji değişmez. Böyle bir sistemde çevre ile enerji ve madde alışverişinde bulunmaz. 2- Kapalı Sistem; çevre ile yalnızca enerji alışverişi olmaktadır. 3- Açık Sistem; çevreyle Süreç: Termodinamikte bir süreç, sistemde oluşan ve herhangi bir değişmeye neden olan olaydır. Bu değişimler veya süreç 2 ye ayrılır. Dönüşümlü ve Dönüşümsüz Süreç. Termodinamik dönüşümleri; termodinamik değişkenlerine göre gruplamamız mümkündür. Adyabatik Dönüşüm: dq = 0 Bir sistemde bir süreç oluşurken sistemle çevresi arasında ısı alışverişi olmuyorsa. Bu dönüşümün sağlanması sistemin çevresinden izole edilmesi durumunda söz konusudur. Đzotermik Dönüşüm: Bir sistemde bir süreç sabit sıcaklıkta oluşuyorsa dt = 0 Đzotermiktir. Bu tip dönüşümde sistemle çevre arasında ısı alışverişi olur, ancak sistemin sıcaklığı artmaz. Đzohorik Dönüşüm: Süreç sabit hacimde oluşuyorsa dv = 0, Đzobarik Dönüşüm: Bir sistemin basıncı sabit kalarak bir süreç oluşuyorsa. dp=0 Biyolojik reaksiyonlarda basınç, hacim ve sıcaklık gibi fiziksel nicelikler önemli değildir. Çünkü biyolojik reaksiyonlar; Sabit P, Sabit V, Sabit T şartlarında gerçekleşirler. 2- TERMODĐNAMĐK YASALAR Termodinamik çözümlemede, sistemin toplam enerjisini oluşturan değişik enerji biçimlerini makroskobik ve mikroskobik olarak 2 grupta ele almak yararlı olur. Makroskobik Enerji sistemin tümünün bir dış referans noktasına göre sahip olduğu enerjidir, Mikroskobik Enerji; sistemin molekül yapısı ve molekül hareketliliğiyle ilgilidir. Termodinamiğin Sıfırıncı Yasası; Sıfırıncı kanun sıcaklık ve ısı dengesi ile ilgili bir yasadır Termodinamiğin sıfırıncı kanunu; Birbirleriyle ısı temasında bulunan varlıkların oluşturduğu bir sistem yeterli zaman sonunda ısı dengesine ulaşır ve sistem içindeki bütün varlıklar aynı sıcaklığa sahip olurlar şeklinde ifade etmemiz mümkündür. Bu kanun gündelik hayatımızdaki uygulamalarından en önemlisi termometrelerdir. Termodinamiğin Birinci Yasası enerjinin korunumu yasasıdır. Yani evrendeki toplam enerji sabittir, değişmez. Ancak farklılaşabilir. Tüm enerji
3 TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ şekillerinin, ısı enerjisine dönüşmesi mümkündür. Buna karşın, ısı enerjisi diğer enerji şekillerine hiçbir zaman tamamıyla çevrilemez. Çevresi ile enerji alışverişi yapabilen bir sistemin geçirdiği fiziksel veya kimyasal bir olay için 1. YASA matematiksel olarak Q = E + W (1), W = p. V Q = Sistemin çevreden aldığı veya verdiği enerji.( kcal veya kjoule), E = Sistemdeki iç enerji değişikliğidir, W = Sistemin yaptığı veya sistemin üzerine yapılan iş, p = Biyokimyasal reaksiyonlarda sabit, V = Hacimdeki değişme Termodinamiğin Đkinci Yasası; Termodinamiğin 2. yasası, evrenin düzensizlik derecesi daima artar şekilde ifade edilir. Sistemdeki düzensizlik arttıkça, sistemin entropisi artar, yani sistemin faydalı iş verme kabiliyeti azalır. Bu nedenle teorik olarak; evrenin. (Evren = Sistem + Çevre) entropisi sürekli olarak artar Düzenli yapı Düzensiz yapı Q = H Q = E + p. V(1) Entalpi olarak adlandırılır. Entalpi değişikliği, ( H), sabit basınç altında gerçekleşen bir olayda sistemin aldığı veya verdiği ısı enerjisidir. Bu nedenle sistemin enerjisi bir durum fonksiyonudur. Termodinamiğin 1. yasası, bir süreçte enerji dengesiyle ilgili ilişkili bir yasadır. Bu yasaya göre, bir süreç dönüşümlüyse sistemin iç enerjisi SABĐTTĐR. Fiziksel veya kimyasal reaksiyonlar gerçekleşirken bazıları çevreye ısı verirken, bazıları çevreden ısı alırlar. (Enerji Değişimi) 1) Çevreden ısı alarak gerçekleşen olaylar (doğanın yeşermesi gibi) endotermik reaksiyonlar 2) Çevreye ısı vererek gerçekleşen olaylar (buzun erimesi) ise ekzotermik reaksiyonlardır. Reaksiyonların entalpi değişiklikleri ( H) ürünlerin toplam entalpisi ile reaksiyona katılan reaktanların toplam entalpi farkından hesaplanabilir. H = H (ürünler) - H (reaktanlar) Vücudumuzda kullanılan besin maddeleri oksitlendiklerinde enerji açığa çıkarırlar. Besin maddelerinin oksitlenme entalpilari bomba kalorimetresi denen bir aygıtla ölçülebilir. Entalpi değişikliklerinin toplanabilme özelliğine Hess YASASI denir. Hess Yasasından yararlanarak; Herhangi bir reaksiyonun entalpi değişikliği reaksiyonda rol olan reaktant ve ürünlerin oluşum entalpilerinden hesaplanabilir. Katı Sıvı Gaz Sistemin düzensizliğinin artması (düzenliliğin azalması) durumunda S nin değeri pozitifdir (+). Sistemin düzensizliğinin azalması (düzenliliğin artması) durumunda S nin değeri negatifdir (-). Sonuç olarak sistemin entropisi sisteme giren enerji ile artar. S Q / T Bir sistemin iki durumu arasındaki S entropi değişimi yalnız ilk ve son durumuna bağlıdır. Sistem bir durumdan diğer duruma geçerken oluşan süreçlere bağlı değildir. (evren) = (sistem) + (çevre) Đlke olarak, bir sistem bir A durumundan bir B durumuna evrenin entropisi değişmeksizin Se = 0 her zaman geçebilir. Bu tür sürece, dönüşümlü süreç denir. Çünkü sistem aynı ara durumlarından geçerek B den geri A durumuna dönebilir. Se = 0 Geriye dönüşümlü(tersinir) olaylar Se >0 Dönüşümsüz(Tersinmez) olaylar
4 TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ Se < 0 Olanaksız Termodinamiğin birinci ve ikinci yasasının bir arada değerlendirilmesi serbest enerji kavramını oluşturur. Serbest enerji, tepkimenin yönünü ya da gerçekleşebilirliğini belirleyen ve iş için kullanılabilen enerjidir. E T. S = G<0 Bu bağıntı olayların yönünün sistemin iç enerji ve entropi değişiminin ortak işlevi olarak belirlendiğini ortaya koymaktadır. Bu ortak işlev için SERBEST ENERJĐ (Gibbs enerjisi ya da kısaca G) ifadesi kullanılır. Sabit sıcaklık ve basınç altında kimyasal reaksiyonla oluşan ürünlerin toplam serbest enerjisi reaksiyona giren maddelerin toplam serbest enerjisinden küçük ise G negatifdir ( G<0) ve reaksiyon ekzergonik tir. G değeri negatif ( ) ve büyük olan reaksiyonlar (ekzergonik reaksiyonlar), termodinamik olarak elverişli reaksiyonlar olarak tanımlanırlar. Sabit sıcaklık ve basınç altında kimyasal reaksiyonla oluşan ürünlerin toplam serbest enerjisi reaksiyona giren maddelerin toplam serbest enerjisinden büyük ise G pozitifdir ( G>0) ve reaksiyon endergonik tir. G değeri pozitif (+) olan reaksiyonlar (endergonik reaksiyonlar), termodinamik olarak elverişli olmayan reaksiyonlar olarak tanımlanırlar. Sabit sıcaklık ve basınç altında kimyasal reaksiyonla oluşan ürünlerin toplam serbest enerjisi reaksiyona giren maddelerin toplam serbest enerjisine eşit ise G sıfırdır ( G=0) ve sistem dengededir. Sistemde herhangi bir değişiklik olmamaktadır. G < 0 Serbest enerjide azalma yani kendiliğinden gerçekleşebilirliği G > 0 Olayın oluşması için sayısal değer olarak serbest enerjiye ihtiyacı olduğunu gösterir. Termodinamik Yasalara Göre; 1. H<0, S>0, G<0 olduğunda reaksiyon bütün sıcaklıklarda kendiliğinden oluşur. 2. H>0, S<0, G>0 Reaksiyon hiçbir sıcaklıkta kendiliğinden oluşmaz, 3. H<0, S<0, G<0 reaksiyon düşük sıcaklıklarda kendiğinden oluşur, yüksek sıcaklıklarda pozitif ve ters yönde spontan 4. H>0, S>0, G<0 yüksek sıcaklıklarda negatif ve yazıldığı yönde spontan dır. 3- BĐYOENERJETĐK Biyoenerjetik Prensipleri Bütün canlılar varlıklarını sürdürebilmek için 3 tip işi yapmak zorundadırlar ve bunun için enerjiye ihtiyaçları vardır. 1. Kendileri için gerekli olan moleküllerin sentezi (Biyosentez) 2. Moleküllerin ve iyonların aktif taşınması (Ozmotik iş) 3. Hücresel hareket ve kas kasılması (Mekanik işler) Canlı sistemde enerji iletilmelerini, enerji akımlarını ve enerjinin oluşturduğu süreçleri inceleyen bilim dalına biyoenerjetik denir. Termodinamiğin biyolojik süreçlerdeki önemini, kısaca şu şekilde maddeleyebiliriz. 1. Birçok biyolojik enerji dönüşümü, kimyasal reaksiyonları izleyen moleküller arasında yeniden bir enerji dağılımı sonucu oluşur. 2. Biyolojik fonksiyon, organizasyonu oluşturmak için kullanılan enerjiyle ilişkilidir. 3. Termodinamiğe göre, kendi haline bırakılan bir sistem maksimum entropi durumuna doğru yol alır. Halbuki canlının kendisi oldukça karmaşık ve düzenli durumlara doğru gelişir. Doğal termodinamik gidiş yönüne ters yönde etki yapan etken, sisteme eşdeğer enerjinin girmesidir. Bu enerji Güneş enerjisidir. Düzendeki artma (Entropideki azalma) tam olarak sisteme giren ve kullanılan güneş enerjisiyle dengededir. Canlıların enerjiyi kullandıklarını gösteren tipik olaylar; 1. Hücreler kullanacakları maddeleri yüksek konsantrasyonda tutmaya çalışırlar. 2. Hücrelerin hareket etmesi kinetik enerjiyi kullandığını gösterir. 3. Hücreler yaşamlarını ve büyümelerini devam ettirmek için, küçük alt birimlerden makromolekül sentezlemeleri gerekir. Bu işlem içinde enerji gerekir. Hücrelerde biyosentez için kullanılan enerjinin % 90 nı protein sentezinde harcanır.
5 TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ Biyolojik Enerji Akımları 4- BĐYOMOLEKÜLER SĐSTEMLERDE ENERJĐ AKTARIMLARI Yeryüzündeki biyolojik enerjinin ana kaynağı Güneş te meydana çekirdeksel kaynaşma (füsyon) reaksiyonlarıdır. Hidrojen atom çekirdekleri kaynaşarak He atomlarına dönüşürken, yüksek enerjili γ ışınları da çıkmakta, bu ışınların girdiği karmaşık reaksiyonlar sonucu ise ışık fotonları salınmaktadır. Serbest enerjinin en önemli özelliği yararlı iş yapmakta kullanılabilmesidir. Çünkü serbest enerji değişikliği bir olayın spontanlığı ile ilgilidir ve spontan olaylardan da iş yapmakta yararlanılır. Aldığımız besinlerin le veya başka yollarla oksitlenmesi sonucu ortaya çıkan enerjiden iş yapmak için yararlanırız. Bu enerjinin ne kadarının doğrudan işe dönüştürülebileceği söz konusu metabolik yolun verimliliğine bağlıdır. Spontan olaylar Serbest enerji değişikliği iş yapmakta kullanılabilecek enerji miktarının teorik maksimum değerini belirtir. Spontan olmayan olaylar Đş yapmak için sisteme dışarıdan sağlanması gereken minimum enerji miktarıdır. Canlıda Enerji Akışı Canlılar, biyosentez, ozmotik iş ve mekanik iş olmak üzere üç tip iş yapmak için sürekli olarak enerjiye ihtiyaç duyarlar. Biyosentezin amacı, canlının ihtiyacı olan kendine özgü karmaşık moleküllerin yapılmasıdır. Bunun için enerjiye ihtiyaç vardır. Fotosentezin Termodinamik Özellikleri Güneş Enerjisi FOTOSENTEZ; 6CO 2 + 6H 2 O C 6 H 12 O 6 + 6O 2 G = 686 kcal/mol, H = 673 kcal/mol, S = - 43,6 kcal/mol o K SOLUNUM. C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O (Büyük bir enerji düşüşü yaşanır.) G = -686 kcal/mol, H = -673 kcal/mol, S = + 43,6 kcal/mol o K Biyolojik Enerji Akımı Biyolojik enerji akımı başlıca üç aşamada gerçekleşir. 1) Güneş enerjisi, 2) ATP moleküllerinin oluşumunda, 3) ATP içeriğinin çeşitli biyolojik işlerde kullanılmasında Hücrede besin moleküllerinin yükseltgenmesi ile serbestleşen enerji, eşlenik reaksiyonlarla ADP den, ATP ye sentezlenmesi ile korunmakta ve saklanmaktadır. Canlı hücrede ph =7.0 dolaylarında ATP molekülündedir her fosfat grubu (-) yüklüdür ATP molekülünün 4 negatif yükü vardır. Bu nedenle canlı hücrede anyon şeklinde çok az bulunur genel olarak Mg +2 ile kompleks yapar. ATP ye enerji taşıyıcı özelliğini veren trifosfat birimidir. ATP molekülünün bu kısmı 2 kovalent-fosfoanhidrid bağ içerir. ATP hidrolizle ADP ve ortofasfat a (PO 4 ) dönüşürken büyük miktarda ısı açığa çıkarır. Bu yüksek bir NEGATĐF SERBEST ENERJĐ değişikliği demektir. Hidrolizi yüksek bir enerji düşüşü ile gerçekleşen fosfat bileşiklerine yüksek enerjili fosfat bileşikleri, bu bileşiklerdeki fosfoanhidrit bağlarına ise yüksek enerjili bağ adı verilir. Fosfoanhidrit bağı kovalent bir bağdır. ( G =50 100kcal/mol) ve diğer kovalent bağlardan çok farklı bir enerjiye sahip değildir. Bu bağlara yüksek enerjili fosfat bağları denmesinin sebebi bağın kırılmasıyla ortaya çıkan enerji değildir. Bu deyim ile tepkimeye giren fosfat türevinin hidrolizi sonucu kimyasal iş gücündeki değişme anlatılmaktadır. ATP hidrolizinin negatif serbest enerji değişikliği diğer birçok fosforile bileşiğin hidroliz serbest enerji değişikliğinden yüksek olmakla birlikte en yüksek olanı değildir. Fosfat grupları daima yüksek negatif serbest enerjili bileşikten daha düşük negatif serbest enerjili bir bileşiğe transfer edilir. Kısacası; ATP hücrelerde enerji veren reaksiyonlarla, enerji harcayan reaksiyonları bağlayan ortak ara bileşiktir. ATP hidrolizinin termodinamik özellikleri 1. Hücrede suyun nötral ancak polar ortamında ATP molekülünün 3 fosfat grubu protonların ayrışmasıyla 4 negatif yük taşır. ATP nin bu elektronegatif niteliği ve elektronegatif fosfat grupları arasındaki itim, ATP hidrolizinin enerjetiğini belirler. ATP nin hidrolizi sonucu oluşan ürünler ADP -3, iyonları da elektronegatif yükleri nedeniyle yeniden birleşme özelliği göstermezler ve yeni tepkimeler girebilirler. 2. ATP hidrolizinin serbest enerjisinin yüksek negatif değerinin önemli bir nedeni ise tepkime ürünlerinin ADP + fosfatın elektron bulutlarının olanaklı olan en düşük enerji düzeyinde düzenlenmeleridir.
6 TERMODĐNAMĐK PRENSĐPLERĐN BĐYOFĐZĐĞĐ CANLILARIN ATP HĐDROLĐZĐNE BAĞIMLI OLARAK GERÇEKLEŞTĐRDĐKLERĐ ĐŞLER 1. Biyosentez, 2. Etkin (aktif) ileti, 3. Mekanik iş Biyosentezin termodinamik özellikleri a) Küçük ve basit bileşiklerden büyük ve karmaşık makromoleküllerin sentez edildiği biyosentez reaksiyonlarında entropi (düzensizlik) daima azalır. b) Biyosentez reaksiyonlarında yer alan reaktanlar standart konsantrasyonlarında değil sudaki seyreltik çözeltileri halinde bulunurlar. Bu nedenle de yazıldıkları yönde değil ters yönde gerçekleşme eğilimindedirler. Böyle bir reaksiyonu gerçekleştirebilmek için gerekli serbest enerji reaksiyonun standart koşullar için hesaplanan serbest enerji ihtiyacından daha fazladır. Biyosentez reaksiyonlarının diğer termodinamik özellikleri başka biyokimyasal reaksiyonlarla ortaktır. Yani biyosentez reaksiyonları ORTAK ARA BĐLEŞĐKLER kullanımı ilkesine uyarlar. 2) Biyoenerjetik ilkeleri ile iletim; 2 farklı şekilde gerçekleşir. a) Pasif iletim; Pasif taşınmada bir iyon veya molekül yüksek konsantrasyonda bulunduğu ortamdan düşük konsantrasyondaki ortama kendiliğinden geçer. Pasif taşınmada sistemin serbest enerjisi azalır. b) Aktif iletim; Bu tip taşınmada ise bir madde düşük konsantrasyonda olduğu ortamdan yüksek konsantrasyonda olduğu ortama ancak metabolik enerji harcanarak taşınabilir. Aktif taşımada sistemin serbest enerjisi artar. 3) Mekanik Đş; Bütün hücreler kuvvet üreterek mekanik iş yapabilirler. Mekanik işin en belirgin şekli kas kasılmasıdır. Fakat çoğu hücrelerde, hücre içinde de mekanik iş yapılır. Hücre bölünmesi, pinositoz, organel şişmesi ve büzülmesi örnek olarak verilebilir. olarak ürettiği toplam enerjinin izometrik olarak kasılırken ürettiği ısıdan daha fazla olması FENN etkisi olarak adlandırılır. Fenn etkisi, bir kastaki enerji dönüştürme verimi ve ATP kullanımının kasın içinde bulunduğu mekanik koşullara bağlı olduğunu gösterir. KAYNAKLAR Pehlivan F. (1997): Biyofizik. Hacettepe Taş Kitapçılık 2. Baskı, Ankara Yıldırım H. (1985): Biyofizik. Anadolu Üniversitesi, Eskişehir. Çelebi G. (2000): Biyofizik, II. Baskı, Barış Yayınları, Đzmir. Biyofizik Ders Notları, Đ.Ü. Đstanbul, Tıp Fak. 1997, Đstanbul. Pehlivan F. (1997): Biyofizik. Hacettepe Taş Kitapçılık 2.Baskı, Ankara Evcin A. (2006): Termodinamik, Afyonkarahisar Kocatepe Üniversitesi. Moran M.J., Shapiro H.N. (2004): Fundamentals of Engineering Thermodynamics, Wiley; 5th ed. Sonntag R. E., Borgnakke C., Van Wylen G.J. (2002): Fundamentals of Engineering Thermodynamics, Wiley; 6th ed. Uzol S. (2007): Termodinamik II. TOBB Ekonomi ve Teknoloji Üniversitesi. Biyokimyasal Termodinamik.mak.etu.edu.tr/dersler/mak202/docs/MAK202_DersPlani.pdf Joule's Law Joule's Mechanical Equivalent of Heat Apparatus Joule's Equivalent James Prescott Joule ( ) Kas kasılmasının biyoenerjetik özellikleri; Đskelet kasları izotonik ve izometrik olmak üzere iki şekilde kasılabilirler. Đzotonik kasılmada kasın boyu kısalırken gerginliği sabit kalır Bu sırada kimyasal enerji mekanik iş ve ısıya dönüştürülür. Đzometrik kasılmada kasın boyu değişmez fakat içindeki kuvvet artar. Đzometrik kasılmada kas mekanik iş yapmaz. Kimyasal enerji ısıya dönüştürülür. Maksimal uyarma ile izotonik olarak kasılan bir kasın iş ve ısı
Sıcaklık (Temperature):
 Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
ΔH bir sistem ile çevresi arasındaki ısı transferiyle alakalı. Bir reaksiyonun ΔH ını hesaplayabiliyoruz. Hess yasası,
 TERMOKİMYA Termodinamiğin 1. kuralı, iç enerjinin (U) nasıl değiştiğiyle alakalı U U çevre U evren ΔU değişimleri ΔH ile alakalı U PV H ΔH bir ile çevresi arasındaki ısı transferiyle alakalı (@ sabit P)
TERMOKİMYA Termodinamiğin 1. kuralı, iç enerjinin (U) nasıl değiştiğiyle alakalı U U çevre U evren ΔU değişimleri ΔH ile alakalı U PV H ΔH bir ile çevresi arasındaki ısı transferiyle alakalı (@ sabit P)
hesaplama (Ders #16 dan devam) II. İstemli değişim ve serbest enerji III. Entropi IV. Oluşum serbest enerjisi
 5.111 Ders Özeti #17 Bugün için okuma: Bölüm 7.1 İstemli değişme, Bölümler 7.2 ve 7.8 -Entropi, Bölümler 7.12, 7.13, ve 7.15 Serbest Enerji. Ders #18 için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji
5.111 Ders Özeti #17 Bugün için okuma: Bölüm 7.1 İstemli değişme, Bölümler 7.2 ve 7.8 -Entropi, Bölümler 7.12, 7.13, ve 7.15 Serbest Enerji. Ders #18 için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji
3.BÖLÜM: TERMODİNAMİĞİN I. YASASI
 3.BÖLÜM: TERMODİNAMİĞİN I. YASASI S (k) + O SO + ısı Reaksiyon sonucunda sistemden ortama verilen ısı, sistemin iç enerjisinin bir kısmının ısı enerjisine dönüşmesi sonucunda ortaya çıkmıştır. Enerji sistemden
3.BÖLÜM: TERMODİNAMİĞİN I. YASASI S (k) + O SO + ısı Reaksiyon sonucunda sistemden ortama verilen ısı, sistemin iç enerjisinin bir kısmının ısı enerjisine dönüşmesi sonucunda ortaya çıkmıştır. Enerji sistemden
Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar.
 Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Bölüm 3. Maddenin Isıl Özellikleri ve TERMODİNAMİK. Prof. Dr. Bahadır BOYACIOĞLU
 Bölüm 3 Maddenin Isıl Özellikleri ve TERMODİNAMİK Prof. Dr. Bahadır BOYACIOĞLU Termodinamik Yasaları Termodinamiğin 0. Yasası Termodinamiğin I. Yasası Termodinamiğin II. Yasası Termodinamiğin III. Yasası
Bölüm 3 Maddenin Isıl Özellikleri ve TERMODİNAMİK Prof. Dr. Bahadır BOYACIOĞLU Termodinamik Yasaları Termodinamiğin 0. Yasası Termodinamiğin I. Yasası Termodinamiğin II. Yasası Termodinamiğin III. Yasası
Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası
 Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası Sıcaklık, bir gaz molekülünün kütle merkezi hareketinin ortalama kinetic enerjisinin bir ölçüsüdür. Sıcaklık,
Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası Sıcaklık, bir gaz molekülünün kütle merkezi hareketinin ortalama kinetic enerjisinin bir ölçüsüdür. Sıcaklık,
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
BİY 315 BİYOKİMYA GİRİŞ. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
2. Kanun- Enerji dönüşümü sırasında bir miktar kullanılabilir kullanılamayan enerji ısı olarak kaybolur.
 Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA. Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004
 REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
11. SINIF KONU ANLATIMI 2 ATP-2
 11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER
 KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER Biyokimyasal olarak önemli reaksiyon türleri Canlı hücredeki reaksiyonların çoğu, beş genel kategoriden birine uyar: 1) Fonksiyonel grup transferi 2) Oksidasyon
KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER Biyokimyasal olarak önemli reaksiyon türleri Canlı hücredeki reaksiyonların çoğu, beş genel kategoriden birine uyar: 1) Fonksiyonel grup transferi 2) Oksidasyon
ENERJİ DENKLİKLERİ 1
 ENERJİ DENKLİKLERİ 1 Enerji ilk kez Newton tarafından ortaya konmuştur. Newton, kinetik ve potansiyel enerjileri tanımlamıştır. 2 Enerji; Potansiyel, Kinetik, Kimyasal, Mekaniki, Elektrik enerjisi gibi
ENERJİ DENKLİKLERİ 1 Enerji ilk kez Newton tarafından ortaya konmuştur. Newton, kinetik ve potansiyel enerjileri tanımlamıştır. 2 Enerji; Potansiyel, Kinetik, Kimyasal, Mekaniki, Elektrik enerjisi gibi
BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal
 BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal tepkime kavramlarının anlaşılması Termodinamiğin II. yasasının
BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal tepkime kavramlarının anlaşılması Termodinamiğin II. yasasının
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
1. HAFTA Giriş ve Temel Kavramlar
 1. HAFTA Giriş ve Temel Kavramlar TERMODİNAMİK VE ISI TRANSFERİ Isı: Sıcaklık farkının bir sonucu olarak bir sistemden diğerine transfer edilebilen bir enerji türüdür. Termodinamik: Bir sistem bir denge
1. HAFTA Giriş ve Temel Kavramlar TERMODİNAMİK VE ISI TRANSFERİ Isı: Sıcaklık farkının bir sonucu olarak bir sistemden diğerine transfer edilebilen bir enerji türüdür. Termodinamik: Bir sistem bir denge
Redoks Kimyasını Gözden Geçirme
 Redoks Kimyasını Gözden Geçirme I. Yükseltgenme Durumu ya da Sayısı Bir bileşiğin yükseltgenme durumu ya da sayısı, ne derece yükseltgenmiş (elektronca fakir) ya da indirgenmiş (elektronca zengin) bir
Redoks Kimyasını Gözden Geçirme I. Yükseltgenme Durumu ya da Sayısı Bir bileşiğin yükseltgenme durumu ya da sayısı, ne derece yükseltgenmiş (elektronca fakir) ya da indirgenmiş (elektronca zengin) bir
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
TERMODİNAMİĞİN TEMEL EŞİTLİKLERİ
 Serbest İç Enerji (Helmholtz Enerjisi) Ve Serbest Entalpi (Gibbs Enerjisi) Fonksiyonları İç enerji ve entalpi fonksiyonları yalnızca termodinamiğin birinci yasasından tanımlanır. Entropi fonksiyonu yalnızca
Serbest İç Enerji (Helmholtz Enerjisi) Ve Serbest Entalpi (Gibbs Enerjisi) Fonksiyonları İç enerji ve entalpi fonksiyonları yalnızca termodinamiğin birinci yasasından tanımlanır. Entropi fonksiyonu yalnızca
7. Bölüm: Termokimya
 7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
E = U + KE + KP = (kj) U = iç enerji, KE = kinetik enerji, KP = potansiyel enerji, m = kütle, V = hız, g = yerçekimi ivmesi, z = yükseklik
 Enerji (Energy) Enerji, iş yapabilme kabiliyetidir. Bir sistemin enerjisi, o sistemin yapabileceği azami iştir. İş, bir cisme, bir kuvvetin tesiri ile yol aldırma, yerini değiştirme şeklinde tarif edilir.
Enerji (Energy) Enerji, iş yapabilme kabiliyetidir. Bir sistemin enerjisi, o sistemin yapabileceği azami iştir. İş, bir cisme, bir kuvvetin tesiri ile yol aldırma, yerini değiştirme şeklinde tarif edilir.
TERMODİNAMİĞİN BİRİNCİ YASASI
 İç Enerji Fonksiyonu ve C v Isınma Isısı Kimyasal tepkimelerin olmadığı kapalı sistemlerde kütle yanında molar miktar da sabit kalmaktadır. Madde miktarı n mol olan kapalı bir ideal gaz sistemi düşünelim.
İç Enerji Fonksiyonu ve C v Isınma Isısı Kimyasal tepkimelerin olmadığı kapalı sistemlerde kütle yanında molar miktar da sabit kalmaktadır. Madde miktarı n mol olan kapalı bir ideal gaz sistemi düşünelim.
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar.
 Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Enerji ve madde arasındaki iliģkiyi inceler
 TERMODİNAMİK Enerji ve madde arasındaki iliģkiyi inceler Termodinamikte bir organizma, bir hücre veya birbiri ile reaksiyona giren iki madde, sistem olarak tanımlanır. Bir sistem, bir çevre içinde yer
TERMODİNAMİK Enerji ve madde arasındaki iliģkiyi inceler Termodinamikte bir organizma, bir hücre veya birbiri ile reaksiyona giren iki madde, sistem olarak tanımlanır. Bir sistem, bir çevre içinde yer
Fizik 203. Ders 6 Kütle Çekimi-Isı, Sıcaklık ve Termodinamiğe Giriş Ali Övgün
 Fizik 203 Ders 6 Kütle Çekimi-Isı, Sıcaklık ve Termodinamiğe Giriş Ali Övgün Ofis: AS242 Fen ve Edebiyat Fakültesi Tel: 0392-630-1379 ali.ovgun@emu.edu.tr www.aovgun.com Kepler Yasaları Güneş sistemindeki
Fizik 203 Ders 6 Kütle Çekimi-Isı, Sıcaklık ve Termodinamiğe Giriş Ali Övgün Ofis: AS242 Fen ve Edebiyat Fakültesi Tel: 0392-630-1379 ali.ovgun@emu.edu.tr www.aovgun.com Kepler Yasaları Güneş sistemindeki
Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ. Bölüm 8: Ekserji: İş Potansiyelinin bir Ölçüsü
 Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ 1 Amaçlar Termodinamiğin ikinci yasası ışığında, mühendislik düzeneklerinin verimlerini veya etkinliklerini incelemek. Belirli bir çevrede verilen bir halde
Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ 1 Amaçlar Termodinamiğin ikinci yasası ışığında, mühendislik düzeneklerinin verimlerini veya etkinliklerini incelemek. Belirli bir çevrede verilen bir halde
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL
 DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
Kendiliğinden Oluşan Olaylar ISTEMLI DEĞIŞIM: ENTROPI VE SERBEST ENERJI. Entropi. Şelale her zaman aşağı akar, yukarı aktığı görülmemiştir.
 Şelale her zaman aşağı akar, yukarı aktığı görülmemiştir. ISTEMLI DEĞIŞIM: ENTROPI VE SERBEST ENERJI Bir fincan çay içerisine atılan bir küp şeker çözünür ama hiçbir zaman çözünmüş şeker çayın içinde kendiliğinden
Şelale her zaman aşağı akar, yukarı aktığı görülmemiştir. ISTEMLI DEĞIŞIM: ENTROPI VE SERBEST ENERJI Bir fincan çay içerisine atılan bir küp şeker çözünür ama hiçbir zaman çözünmüş şeker çayın içinde kendiliğinden
HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI. Dr. Vedat Evren
 HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI Dr. Vedat Evren Vücuttaki Sıvı Kompartmanları Vücut sıvıları değişik kompartmanlarda dağılmış Vücuttaki Sıvı Kompartmanları Bu kompartmanlarda iyonlar ve diğer çözünmüş
HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI Dr. Vedat Evren Vücuttaki Sıvı Kompartmanları Vücut sıvıları değişik kompartmanlarda dağılmış Vücuttaki Sıvı Kompartmanları Bu kompartmanlarda iyonlar ve diğer çözünmüş
4.BÖLÜM: ENTROPİ 1.İSTEMLİ VE İSTEMSİZ DEĞİŞMELER
 4.BÖLÜM: ENROPİ 1.İSEMLİ VE İSEMSİZ DEĞİŞMELER Doğal bir olayın termodinamikteki anlamı istemli değişmedir. İSEMLİ DEĞİŞMELER, bir dış etki tarafından yönlendirmeye ihtiyaç olmaksızın kendiliğinden meydana
4.BÖLÜM: ENROPİ 1.İSEMLİ VE İSEMSİZ DEĞİŞMELER Doğal bir olayın termodinamikteki anlamı istemli değişmedir. İSEMLİ DEĞİŞMELER, bir dış etki tarafından yönlendirmeye ihtiyaç olmaksızın kendiliğinden meydana
PERİYODİK CETVEL Mendeleev Henry Moseley Glenn Seaborg
 PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
HAZIRLAYAN Mutlu ŞAHİN. Hacettepe Fen Bilgisi Öğretmenliği. DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ
 HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ DENEYİN AMACI: Doymuş NaCl çözeltisinin elektroliz sonucu elementlerine ayrışmasının
HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 6 DENEYİN ADI: DOYMUŞ NaCl ÇÖZELTİSİNİN ELEKTROLİZİ DENEYİN AMACI: Doymuş NaCl çözeltisinin elektroliz sonucu elementlerine ayrışmasının
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır:
 Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Her madde atomlardan oluşur
 2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
Sistem: Belirli bir kütle veya uzayın incelenmek üzere ayrılan bir bölgesi. Sistem bir kristal veya kristalin küçük bir bölümü kadar küçük olabildiği
 Sistem: Belirli bir kütle veya uzayın incelenmek üzere ayrılan bir bölgesi. Sistem bir kristal veya kristalin küçük bir bölümü kadar küçük olabildiği gibi bir kaya veya kayaçlar topluluğu ve hatta tüm
Sistem: Belirli bir kütle veya uzayın incelenmek üzere ayrılan bir bölgesi. Sistem bir kristal veya kristalin küçük bir bölümü kadar küçük olabildiği gibi bir kaya veya kayaçlar topluluğu ve hatta tüm
SU VE HÜCRE İLİŞKİSİ
 SU VE HÜCRE İLİŞKİSİ Oluşturacağı her 1 g organik madde için bitkinin 500 g kadar suyu kökleriyle alması ve tepe (uç) noktasına kadar taşıyarak atmosfere aktarması gerekir. Normal su düzeyinde hayvan hücrelerinin
SU VE HÜCRE İLİŞKİSİ Oluşturacağı her 1 g organik madde için bitkinin 500 g kadar suyu kökleriyle alması ve tepe (uç) noktasına kadar taşıyarak atmosfere aktarması gerekir. Normal su düzeyinde hayvan hücrelerinin
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ
 ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
Radyoaktif elementin tek başına bulunması, bileşik içinde bulunması, katı, sıvı, gaz, iyon halinde bulunması radyoaktif özelliğini etkilemez.
 RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
Serbest radikallerin etkileri ve oluşum mekanizmaları
 Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
3- KİMYASAL ELEMENTLER VE FONKSİYONLARI
 3- KİMYASAL ELEMENTLER VE FONKSİYONLARI Doğada 103 elementin olduğu bilinmektedir. Bunlardan 84 metal elementlerdir. Metal elementler toksik olan ve toksik olmayan elementler olarak ikiye ayrılmaktadır.
3- KİMYASAL ELEMENTLER VE FONKSİYONLARI Doğada 103 elementin olduğu bilinmektedir. Bunlardan 84 metal elementlerdir. Metal elementler toksik olan ve toksik olmayan elementler olarak ikiye ayrılmaktadır.
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
Metabolizma. Metabolizmaya giriş. Metabolizmaya giriş. Metabolizmayı tanımlayacak olursak
 Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Maddeye dışarıdan ısı verilir yada alınırsa maddenin sıcaklığı değişir. Dışarıdan ısı alan maddenin Kinetik Enerjisi dolayısıyla taneciklerinin
 Maddeye dışarıdan ısı verilir yada alınırsa maddenin sıcaklığı değişir. Dışarıdan ısı alan maddenin Kinetik Enerjisi dolayısıyla taneciklerinin titreşim hızı artar. Tanecikleri bir arada tutan kuvvetler
Maddeye dışarıdan ısı verilir yada alınırsa maddenin sıcaklığı değişir. Dışarıdan ısı alan maddenin Kinetik Enerjisi dolayısıyla taneciklerinin titreşim hızı artar. Tanecikleri bir arada tutan kuvvetler
YAZILIYA HAZIRLIK SORULARI. 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ
 YAZILIYA HAZIRLIK SORULARI 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ Fotosentez ile ışık enerjisi kimyasal bağ enerjisine dönüştürülür. Kloroplastsız hücreler fotosentez yapamaz. DOĞRU YANLIŞ SORULARI
YAZILIYA HAZIRLIK SORULARI 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ Fotosentez ile ışık enerjisi kimyasal bağ enerjisine dönüştürülür. Kloroplastsız hücreler fotosentez yapamaz. DOĞRU YANLIŞ SORULARI
5) Çözünürlük(Xg/100gsu)
 1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
Aşağıda verilen özet bilginin ayrıntısını, ders kitabı. olarak önerilen, Erdik ve Sarıkaya nın Temel. Üniversitesi Kimyası" Kitabı ndan okuyunuz.
 KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile
 Su Kimyası Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile canlılık için gerekli ortamı sunar. Canlıların
Su Kimyası Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile canlılık için gerekli ortamı sunar. Canlıların
Kimya ve Enerji. 1. Sistem ve Çevre. 2. Isı, Mekanik İş ve İç Enerji. YKS Fasikülleri. Yakup Demir. a. Sistemlerin
 Bu notlara Youtube dan Kimya Elbistan kanalında ilgili videolarının açıklamalar kısmında ki linkten ücretsiz bir şekilde ulaşabilirsiniz. Fiziksel ve kimyasal değişimlerde meydana gelen ısı değişimini
Bu notlara Youtube dan Kimya Elbistan kanalında ilgili videolarının açıklamalar kısmında ki linkten ücretsiz bir şekilde ulaşabilirsiniz. Fiziksel ve kimyasal değişimlerde meydana gelen ısı değişimini
BMM307-H02. Yrd.Doç.Dr. Ziynet PAMUK
 BMM307-H02 Yrd.Doç.Dr. Ziynet PAMUK ziynetpamuk@gmail.com 1 BİYOELEKTRİK NEDİR? Biyoelektrik, canlıların üretmiş olduğu elektriktir. Ancak bu derste anlatılacak olan insan vücudundan elektrotlar vasıtasıyla
BMM307-H02 Yrd.Doç.Dr. Ziynet PAMUK ziynetpamuk@gmail.com 1 BİYOELEKTRİK NEDİR? Biyoelektrik, canlıların üretmiş olduğu elektriktir. Ancak bu derste anlatılacak olan insan vücudundan elektrotlar vasıtasıyla
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ. Bölüm 4: Kapalı Sistemlerin Enerji Analizi
 Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 1 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan hareketli sınır işi veya PdV işi olmak üzere değişik iş biçimlerinin
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 1 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan hareketli sınır işi veya PdV işi olmak üzere değişik iş biçimlerinin
ELEKTRONLARIN DĠZĠLĠMĠ
 ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
Termodinamik Termodinamik Süreçlerde İŞ ve ISI
 Termodinamik Süreçlerde İŞ ve ISI Termodinamik Hareketli bir pistonla bağlantılı bir silindirik kap içindeki gazı inceleyelim (Şekil e bakınız). Denge halinde iken, hacmi V olan gaz, silindir çeperlerine
Termodinamik Süreçlerde İŞ ve ISI Termodinamik Hareketli bir pistonla bağlantılı bir silindirik kap içindeki gazı inceleyelim (Şekil e bakınız). Denge halinde iken, hacmi V olan gaz, silindir çeperlerine
Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.
 ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER»
 FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
Konular: I. Değerlik bağı teorisi ve melezleģme (Ders #15 den devam) Karmaşık moleküllerde melezleşme tayini
 5.111 Ders Özeti #16 Bugün için okuma: Bölümler 6.13, 6.15, 6.16, 6.17, 6.18, ve 6.20 (3. Baskıda Bölümler 6.14, 6.16, 6.17, 6.18, 6.19 ve 6.21) Kimyasal Değişim Entalpisi. Ders #17 için okuma: Bölüm 7.1
5.111 Ders Özeti #16 Bugün için okuma: Bölümler 6.13, 6.15, 6.16, 6.17, 6.18, ve 6.20 (3. Baskıda Bölümler 6.14, 6.16, 6.17, 6.18, 6.19 ve 6.21) Kimyasal Değişim Entalpisi. Ders #17 için okuma: Bölüm 7.1
MALZEME BİLGİSİ DERS 4 DR. FATİH AY.
 MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
BMM 205 Malzeme Biliminin Temelleri
 BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
PERİYODİK CETVEL. Yanıt : D. www.kimyahocam.com. 3 Li : 1s2 2s 1 2. periyot 1A grubu. 16 S : 1s2 2s 2 2p 6 3s 2 3p 4 3.
 PERİODİK CETVEL Periyodik cetvel, elementlerin atom numaraları temel alınarak düzenlenmiş bir sistemdir. Periyodik cetvelde, nötr atomlarının elektron içeren temel enerji düzeyi sayısı aynı olan elementler
PERİODİK CETVEL Periyodik cetvel, elementlerin atom numaraları temel alınarak düzenlenmiş bir sistemdir. Periyodik cetvelde, nötr atomlarının elektron içeren temel enerji düzeyi sayısı aynı olan elementler
PERİYODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR
 PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
Metabolizma. Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir.
 METABOLİZMAYA GİRİŞ Metabolizma Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir. Metabolizma, hücrede cereyan eden binlerce kimyasal tepkimenin karmaşık bir yol haritasıdır. 2 Metabolizma
METABOLİZMAYA GİRİŞ Metabolizma Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir. Metabolizma, hücrede cereyan eden binlerce kimyasal tepkimenin karmaşık bir yol haritasıdır. 2 Metabolizma
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
BİYOLOJİK MOLEKÜLLERDEKİ
 BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
Su ve çevrenin canlılar için uygunluğu
 Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ
 KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
ISI VE SICAKLIK. 1 cal = 4,18 j
 ISI VE SICAKLIK ISI Isı ve sıcaklık farklı şeylerdir. Bir maddeyi oluşturan bütün taneciklerin sahip olduğu kinetik enerjilerin toplamına ISI denir. Isı bir enerji türüdür. Isı birimleri joule ( j ) ve
ISI VE SICAKLIK ISI Isı ve sıcaklık farklı şeylerdir. Bir maddeyi oluşturan bütün taneciklerin sahip olduğu kinetik enerjilerin toplamına ISI denir. Isı bir enerji türüdür. Isı birimleri joule ( j ) ve
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Doğadaki Enerji Akışı
 Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
ADIM ADIM YGS-LYS 29. ADIM HÜCRE 6- HÜCRE ZARINDAN MADDE GEÇİŞLERİ 3
 ADIM ADIM YGS-LYS 29. ADIM HÜCRE 6- HÜCRE ZARINDAN MADDE GEÇİŞLERİ 3 TURGOR BASINCI: Hücre içindeki suyun hücre çeperine yaptığı basınca TURGOR BASINCI denir. Turgor durumundaki bir hücrenin turgor basıncı
ADIM ADIM YGS-LYS 29. ADIM HÜCRE 6- HÜCRE ZARINDAN MADDE GEÇİŞLERİ 3 TURGOR BASINCI: Hücre içindeki suyun hücre çeperine yaptığı basınca TURGOR BASINCI denir. Turgor durumundaki bir hücrenin turgor basıncı
KİMYA VE ENERJİ SİSTEM VE ÇEVRE
 SİSTEM VE ÇEVRE Kimyasal reaksiyonlar esnasında meydana gelen enerji değişimlerine günlük yaşamımızda sürekli karşılaşırız. Örneğin, doğal gaz ve petrol gibi Yakıtları kapsayan reaksiyonları su ve karbondioksit
SİSTEM VE ÇEVRE Kimyasal reaksiyonlar esnasında meydana gelen enerji değişimlerine günlük yaşamımızda sürekli karşılaşırız. Örneğin, doğal gaz ve petrol gibi Yakıtları kapsayan reaksiyonları su ve karbondioksit
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar
 10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Hidroklorik asit ve sodyum hidroksitin reaksiyonundan yemek tuzu ve su meydana gelir. Bu kimyasal olayın denklemi
 KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
2+ 2- Mg SO 4. (NH 4 ) 2 SO 4 (amonyum sülfat) bileşiğini katyon ve anyonlara ayıralım.
 KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
Hücre Solunumu: Kimyasal Enerji Eldesi
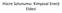 Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
KYM 202 TERMODİNAMİK
 KYM 0 ERMODİNAMİK AKIŞ PROSESLERİNİN ERMODİNAMİĞİ Kimya, petrol ve ilgili endüstrilerin bir çoğunda akışkan hareketi vardır. ermodinamiğin akış proseslerine uygulanması, kütlenin korunumu ile termodinamiğin
KYM 0 ERMODİNAMİK AKIŞ PROSESLERİNİN ERMODİNAMİĞİ Kimya, petrol ve ilgili endüstrilerin bir çoğunda akışkan hareketi vardır. ermodinamiğin akış proseslerine uygulanması, kütlenin korunumu ile termodinamiğin
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6
 PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
Bölüm 7 ENTROPİ. Bölüm 7: Entropi
 Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
5.111 Ders Özeti #18 Bugün için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji Değişimi. Sınav #2 geliyor. (Ders #17 den devam)
 5.111 Ders Özeti #18 Bugün için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji Değişimi. Sınav #2 geliyor. Konular: Termodinamik I. Oluşum serbest enerjisi II. Ġstemlilik üzerine sıcaklığın etkisi
5.111 Ders Özeti #18 Bugün için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji Değişimi. Sınav #2 geliyor. Konular: Termodinamik I. Oluşum serbest enerjisi II. Ġstemlilik üzerine sıcaklığın etkisi
Şekilde görüldüğü gibi Gerilim/akım yoğunluğu karakteristik eğrisi dört nedenden dolayi meydana gelir.
 Bir fuel cell in teorik açık devre gerilimi: Formülüne göre 100 oc altinda yaklaşık 1.2 V dur. Fakat gerçekte bu değere hiçbir zaman ulaşılamaz. Şekil 3.1 de normal hava basıncında ve yaklaşık 70 oc da
Bir fuel cell in teorik açık devre gerilimi: Formülüne göre 100 oc altinda yaklaşık 1.2 V dur. Fakat gerçekte bu değere hiçbir zaman ulaşılamaz. Şekil 3.1 de normal hava basıncında ve yaklaşık 70 oc da
ADIM ADIM YGS-LYS 27. ADIM HÜCRE 4- HÜCRE ZARINDAN MADDE GEÇİŞLERİ
 ADIM ADIM YGS-LYS 27. ADIM HÜCRE 4- HÜCRE ZARINDAN MADDE GEÇİŞLERİ Hücre zarı canlıdır ve seçici-geçirgendir. Bu özelliği nedeniyle bazı maddeler hücre zarından geçebilirken bazı maddeler geçemez. Hücre
ADIM ADIM YGS-LYS 27. ADIM HÜCRE 4- HÜCRE ZARINDAN MADDE GEÇİŞLERİ Hücre zarı canlıdır ve seçici-geçirgendir. Bu özelliği nedeniyle bazı maddeler hücre zarından geçebilirken bazı maddeler geçemez. Hücre
ÖLÇME, DEĞERLENDİRME VE SINAV HİZMETLERİ GENEL MÜDÜRLÜĞÜ
 AY EKİM 06-07 EĞİTİM - ÖĞRETİM YILI. SINIF VE MEZUN GRUP KİMYA HAFTA DERS SAATİ. Kimya nedir?. Kimya ne işe yarar?. Kimyanın sembolik dili Element-sembol Bileşik-formül. Güvenliğimiz ve Kimya KONU ADI
AY EKİM 06-07 EĞİTİM - ÖĞRETİM YILI. SINIF VE MEZUN GRUP KİMYA HAFTA DERS SAATİ. Kimya nedir?. Kimya ne işe yarar?. Kimyanın sembolik dili Element-sembol Bileşik-formül. Güvenliğimiz ve Kimya KONU ADI
Soygazların bileşik oluşturamamasının sebebi bütün orbitallerinin dolu olmasındandır.
 KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
TermoKimya (Thermochemistry)
 TermoKimya (Thermochemistry) Kimyasal tepkimeler sonucu oluşan ısı değişimlerini inceleyen çalışma alanı. ENERJİ Kinetik enerji, Potansiyel enerji Enerji:İş yapabilme kapasitesidir. Kinetik enerji:hareket
TermoKimya (Thermochemistry) Kimyasal tepkimeler sonucu oluşan ısı değişimlerini inceleyen çalışma alanı. ENERJİ Kinetik enerji, Potansiyel enerji Enerji:İş yapabilme kapasitesidir. Kinetik enerji:hareket
YGS ANAHTAR SORULAR #1
 YGS ANAHTAR SORULAR #1 1) Yıkımları sırasında Tüketilen O2 miktarı 2) H2O2 H2O2 H2O2 Grafikte bazı organik bileşiklerin yıkımları sırasında tüketilen oksijen miktarı verilmiştir. Buna göre organik bileşiklerin
YGS ANAHTAR SORULAR #1 1) Yıkımları sırasında Tüketilen O2 miktarı 2) H2O2 H2O2 H2O2 Grafikte bazı organik bileşiklerin yıkımları sırasında tüketilen oksijen miktarı verilmiştir. Buna göre organik bileşiklerin
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten. Kimyasal Bağlar.
 Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
Moleküllerarası Etkileşimler, Sıvılar ve Katılar - 11
 Moleküllerarası Etkileşimler, Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Sıvılar ve Katılar - 11 Maddenin Halleri Maddenin halleri arasındaki
Moleküllerarası Etkileşimler, Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Sıvılar ve Katılar - 11 Maddenin Halleri Maddenin halleri arasındaki
YAZILIYA HAZIRLIK SORULARI. 9. Sınıf
 YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
Buna göre bir işlemde transfer edilen q ısısı, sistemde A dan B ye giderken yapılan adyabatik iş ile nonadyabatik bir iş arasındaki farka eşittir.
 1 1. TANIMLAR (Ref. e_makaleleri) Enerji, Isı, İş: Enerji: Enerji, iş yapabilme kapasitesidir; çeşitli şekillerde bulunabilir ve bir tipten diğer bir şekle dönüşebilir. Örneğin, yakıt kimyasal enerjiye
1 1. TANIMLAR (Ref. e_makaleleri) Enerji, Isı, İş: Enerji: Enerji, iş yapabilme kapasitesidir; çeşitli şekillerde bulunabilir ve bir tipten diğer bir şekle dönüşebilir. Örneğin, yakıt kimyasal enerjiye
5.111 Ders Özeti #12. Konular: I. Oktet kuralından sapmalar
 5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
Bölüm 6 TERMODİNAMİĞİN İKİNCİ YASASI
 Bölüm 6 TERMODİNAMİĞİN İKİNCİ YASASI İKİNCİ YASANIN ESAS KULLANIMI 1. İkinci yasa hal değişimlerinin yönünü açıklayabilir. 2. İkinci yasa aynı zamanda enerjinin niceliği kadar niteliğinin de olduğunu öne
Bölüm 6 TERMODİNAMİĞİN İKİNCİ YASASI İKİNCİ YASANIN ESAS KULLANIMI 1. İkinci yasa hal değişimlerinin yönünü açıklayabilir. 2. İkinci yasa aynı zamanda enerjinin niceliği kadar niteliğinin de olduğunu öne
GENEL KİMYA. 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar
 GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU
 SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU Suyun polaritesinin etkileri Su molekülünün polar olması hidrojen bağlarının oluşmasına neden olur. 2 Su molekülü Oldukça basit yapılıdır. Tekli bağla bağlı olup
SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU Suyun polaritesinin etkileri Su molekülünün polar olması hidrojen bağlarının oluşmasına neden olur. 2 Su molekülü Oldukça basit yapılıdır. Tekli bağla bağlı olup
ELEMENT VE BİLEŞİKLER
 ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
Bir atomdan diğer bir atoma elektron aktarılmasıyla
 kimyasal bağlar Kimyasal bağ, moleküllerde atomları bir arada tutan kuvvettir. Atomlar daha düşük enerjili duruma erişmek için bir araya gelirler. Bir bağın oluşabilmesi için atomlar tek başına bulundukları
kimyasal bağlar Kimyasal bağ, moleküllerde atomları bir arada tutan kuvvettir. Atomlar daha düşük enerjili duruma erişmek için bir araya gelirler. Bir bağın oluşabilmesi için atomlar tek başına bulundukları
