kalsit Elmas Pirit Ametist Beril (zümrüt)
|
|
|
- Umut Paşa
- 6 yıl önce
- İzleme sayısı:
Transkript
1 Mineraller
2
3 kalsit Elmas Beril (zümrüt) Pirit Ametist
4 Elementlerin Periyodik Tablosu En dış elektronu kaybetme eğilimi Atom numarası Element simgesi Atom ağırlığı Metaller Geçiş metalleri Non-metaller Asal gazlar Elektronları paylaşarak en dış yörüngeyi doldurma eğilimi Elektron kazanarak en dış yörüngeyi doldurma eğilimi Asal gazlar Element adı Lantinid Serisi Aktinid serisi Elektron kaybetme eğilimi
5 Elementlerin yerkabuğundaki bolluk oranları Oksijen Silis Alüminyum Demir Kalsiyum Sodyum Potasyum Mağnezyum Diğerleri All others: 1.5%
6 Atom Element Bileşik Mineral Kayaç (en küçük) Bakır-Demir Sülfid Mineralleri (en büyük) Doğal Sülfür Kovellit Atomik % Py Pirit Dg Dijenit Po Pirotit Cc Kalkosit Doğal Bakır Cp Kalkopirit Doğal Demir Bn Bornit
7 Atomun Yapısı Atomu oluşturan parçacıklar Protonlar: pozitif (+) yüklü Nötronlar: nötr (yüksüz) Elektronlar: negatif (-) yüklü Protonlar + nötronlar atomun çekirdeğini oluşturur. Çekirdeğin etrafındaki yörüngede yer alan elektronların oluşturduğu eksenler orbitaller veya enerji-seviyesi kabukları olarak adlandırılır.
8 Atomun Yapısı çekirdek Yüksek hızlı elektronlar (- yüklü) Nötronlar (yüksüz) Protonlar (+ yüklü)
9 Atomun Yapısı Aynı elementin atomları: Protonlarının sayısı aynıdır (yani aynı atom numarasına sahiptirler) Nötron sayıları farklı olabilir (izotoplar olarak adlandırılır) Farklı sayıda elektrona sahip olabilirler. İyon Bir atomun elektron kazanmış veya kaybetmiş halidir.
10 Atomun Yapısı Elektronlar Çekirdek Sodyum Klor Sodyum (Na) atomu 1 elektron kaybeder (pozitif yüklü hale gelir) Klor atomu 1 Elektron kazanır (negatif yüklü hale gelir)
11 Atomun Yapısı İyon Türleri: Katyonlar 1 elektronun kaybı pozitif (+) yüklü hale gelmesine yol açar. Anyonlar 1 elektronun kazanılması negatif (-) yüklü hale gelmesine yol açar. Örnek: Na + (katyon) Cl (anyon) NaCl Kimyasal bileşik (sofra tuzu)
12 Bileşikler Tanım: Bir kimyasal bileşik belli oranda elementin birleşiminden oluşur. Örnek: NaCl H 2 O Bir bileşiğin en küçük miktarı bir molekül olarak adlandırılır. Moleküller kimyasal bağlar ile birarada tutulurlar.
13 Kimyasal Bağlar Kimyasal bağlar: İki veya daha fazla elementi biraraya getirerek bir bileşik oluşturur. Elektronların atomlar arasında dağıtılması ile gelişir. Bağlanmış bir atomda elektron kaybı, elektron kazanımı yada elektronların ortak kullanımı söz konusudur. 4 tip bağ mevcuttur: iyonik kovalent metalik van der Waals
14 Elementlerin Periyodik Tablosu En dış elektronu kaybetme eğilimi Atom numarası Element simgesi Atom ağırlığı Metaller Geçiş metalleri Non-metaller Asal gazlar Elektronları paylaşarak en dış yörüngeyi doldurma eğilimi Elektron kazanarak en dış yörüngeyi doldurma eğilimi Asal gazlar Element adı Lantinid Serisi Aktinid serisi Elektron kaybetme eğilimi
15 Bağlar İyonik bağlar: Elektronlar iyonların birbirini çekmesini sağlayacak şekilde atomlar arasında transfer edilir. (örn. NaCl) elektronlar çekirdek Sodyum (Na + ) Klor (Cl - ) Na + Cl
16 Bağlar İyonik bağlar: Zıt yüklenmiş iyonların birbirini çekmesine göre düzenlenmiştir. Bağlar orta derecede güçlüdür (tuz su içinde çözünür). Klor iyonu Sodyum iyonu
17 Bağlar Kovalen bağlar: Elektron transferi yerine en dış yörüngedeki elektronların paylaşımı ile kurulan bağlardır. Kimyasal bağlar içinde en güçlü olandır ve elektron alıp vermeye meyilli olmayan elementler arasında (C, Si, S, Pb gibi) kurulur. En basit kovalen yapı elmasda görülür.her bir C (karbon) atomu, diğer 4 atom ile çevrelenerek birer çift elektronu paylaşarak duraylı dolu bir dış zarfa sahip olur ve tetrahedron yapısı oluşturur. Paylaşılan elekron çiftleri Chlorine gas molecule, Cl 2 Klor gaz molekülleri Karbon atomları Güçlü bağlar Elmas Elmas
18 Bağlar Metalik Bağlar: Metalik elementlerin yapı biriminde atom çekirdeğinin çekirdek etrafındaki elektron bulutunun yarattığı toplam yük ile bağlanması ile oluşmaktadır.bu şekilde elektronlar yapı içinde ve dışında bağı bozmadan serbestçe hareket ederler, bu nedenle de iyi iletkendirler, daha az gelişir. (örn. bakır, altın, gümüş) Altın, Au
19 Bağlar Van der Waals bağları:bu tür bağlar iyonlar ve atomlar arasında oluşan en zayıf bağ türüdür. Nötr atomlar ve moleküller arasındaki zayıf elektrik çekimi ile kurulur.yaygın olarak katılaşmış gazlarda ve organik bileşiklerde görülmekle birlikte, görüldükleri minerallerde bağların olduğu zonlar zayıflıkları nedeniyle klivaj (dilinim) düzlemleri oluşturur. örnekler: grafit, mikalar Karbon atomları Güçlü bağlar Zayıf bağlar Grafit Grafit
20 Mineraller Bir mineralin tanımı: doğal olarak oluşan inorganik katı karakteristik bir kristal yapısına sahip (yani tekrarlayan 3-Boyutlu geometrik şekle sahip) belirli bir kimyasal bileşime sahip. Bir kayanın tanımı: Minerallerin katı yığışımı (karışımı)
21 Mineraller, belirli bir kimyasal bileşime sahip doğal oluşumlardır. Katı kristalli bir yapıları vardır. Genellikle inorganiktirler. Mineraller, eriyiklerin katılaşması ve kristalleşmesi yoluyla oluşurlar. Örneğin mağmanın soğuması sonucu eriyikler kristalleştiğinde mineralleşme başlar. Bir başka mineral oluşumu ise sıvının içerisinde yer alan elementlerin, sıvının buharlaşması sonucunda kristalleşmesi ile gerçekleşir. Mineralleri meydana getiren Kristalizasyon, atomların uygun dizilimler ile üç boyutlu olarak birbirleriyle bağlanması işlemine denilir. Kristalizasyon, bir ilksel mikroskobik kristalin oluşumu ile başlar. Kristalin dışı doğal olarak oluşmuş düz yüzeylere sahiptir. Bunlara kristal yüzeyleri adı verilir. Bir kristalin dış yüzeyi, içsel atomik dizilişinin bir görüntüsüdür. Kristalizasyon sırasında, oluşan mikroskobik kristal büyür. Kristal büyüklüğünü etkileyen faktörler, yavaş ve düzenli gelişimi ile kristalin gelişebileceği yeterli boşluğun olmasıdır. Bu koşulların yeterli olması kısıtlı olduğundan büyük kristaller nadiren bulunurlar.
22 ATOMDAN KAYAÇLARA OLUŞUM DÜZENİ Atomdan kayaçlara Atomlar Oksijen Silis Kristal (mineral) Kayaç (kumtaşı) Kayadan kristaller görülebilir. Sedimenter kaya Molekül tabakaları Kayaçların çoğu çok farklı minerallerin biraraya gelmesinden oluşur. Ancak bazı kayaçlar tek bir mineralin yığışımından da oluşabilmektedir.
23 Mineral Tanımlamaları Kayaç oluşturan (kayaç yapıcı) mineraller Kayaçların oluşumu sırasında gelişen ve bolluk oranları ve bulunuş sıklıkları açısından en önemli kayaç oluşturan mineral gruplarıdır. Yer kabuğunda bulunan kayaçların çoğu ~30yaygın mineralden oluşur. Esas olarak hemen hemen 8 element kabuğun % 98 gibi bir kısmını oluşturur. Tali (iz) mineraller - Kayaçların bünyesinde yer almalarına karşılık yığışımları (konsantrasyonları) veya bulunuş sıklıkları oldukça düşüktür. İkincil (sekonder) mineraller - Kayacın oluşumu sırasında gelişen birincil (primer) minerallerden farklı olarak oluşumundan sonra alterasyon veya metamorfizma süreçleri ile ardıl olarak oluşmuş minerallerdir.
24
25 Minerallerin Fiziksel Özellikleri Renk: En belirgin özelliktir, fakat genellikle yanıltır. Aynı mineralin farklı renkleri saflık derecesinden kaynaklanır. Örnek: Kuvars
26 Minerallerin Fiziksel Özellikleri Çizgi Rengi: Çizgi Bir mineral tozunun bıraktığı renk (genellikle metalik mineraller için kullanılır) Bir mineralin sırlanmamış porselen üzerinde bıraktığı çizgi rengidir. Örnek: Hematit
27 Minerallerin Fiziksel Özellikleri Parlaklık: Bir mineral yüzeyinin ışığı nasıl yansıttığı ile ölçülür. İki ana türü vardır: Metalik parlaklık Metalik olmayan parlaklık (Non-metalik parlaklık) Metalik örnek: Galen Metalik olmayan örnek: Ortoklas
28 Metalik olmayan mineral Metalik mineral
29 Minerallerin Fiziksel Özellikleri Sertlik: Bir mineralin çizilmeye karşı direncidir. Mohs Sertlik Skalası ile ölçülür. Göreli bir skaladır ve 10 mineralden kuruludur. Talk-1 Jips-2 Kalsit-3 Fluorit-4 Apatit-5 Ortoz-6 Kuvars-7 Topaz-8 Korund-9 Elmas-10.
30 Mohs Sertlik Skalası En sert (10) Elmas En yumuşak (1) Talk Elmas Korund Kesin sertlik değerleri Yaygın objelerin sertliği: -Tırnak (2.5) -Para(3.5) -Cam(5.5) Topaz Kuvars Ortokla s Apatit Fluorit Kalsit Jips Talk Gösterge mineraller Mohs skalası Seramik cam çakı Bakır para Tırnak maddeler
31 Minerallerin Fiziksel Özellikleri Kristal Şekli (veya form): Bir mineralin iç atom yapısının dışa vurumudur. Düzlemsel yüzeyler kristal yüzleri olarak adlandırılır. Her mineralin kristal yüzleri arasındaki açılar sabitdir. Kuvars Pirit
32 Minerallerin Fiziksel Özellikleri Klivaj ve Kırıklar: Bir mineralin kırılma şeklidir. Klivaj: bir mineralin zayıflık düzlemleri boyunca kırılma eğilimidir. Klivaj göstermeyen minerallerde kırılmadan söz edilir. Klivaj düzlemleri kristal yüzeyleri ile karıştırılmamalıdır. Kristal yüzeyleri mineralin yüzeyinden gözlenir ve mineral kırıldığında tekrarlanmaz.
33 Mineral Klivajı ve Kristal şekilleri kübik 3 yönlü klivaj, 6 yüzey ve yüzeyler arasında dik açı oktahedral 4 yönlü klivaj, 8 yüzey dodekahedral 6 yönlü klivaj, 12 yüzey Bazal 1 yönlü klivaj, 2 yüzey
34 Minerallerin Fiziksel Özellikleri Klivaj (1 ve 2 yönde): Klivaj yönü sayısı Görünüm Klivaj yönünün gösterimi Örnek Örnek: mika
35 Minerallerin Fiziksel Özellikleri Klivaj (2 yönde): Klivaj yönü sayısı Görünüm Klivaj yönünün gösterimi Örnek 90 o de 2 ortoklas 90 o de 2 amfibol
36 Minerallerin Fiziksel Özellikleri Klivaj (3 yönde): Klivaj yönü sayısı Görünüm Klivaj yönünün gösterimi Örnek halit 90 o de 3 kalsit 90 o de 3
37 Minerallerin Fiziksel Özellikleri Klivaj (4 yönde): fluorit Klivaj yönü sayısı Görünüm Klivaj yönünün gösterimi Örnek
38 Minerallerin Fiziksel Özellikleri Kırılma: Klivaj göstermeyen minerallerin kırılmasından söz edilir. yumuşak, eğri yüzeyli gibi Kuvars tanımlamalar ile camsı bir mineralin kırılması tanımlanır: konkoidal kırılma
39 Minerallerin Fiziksel Özellikleri Yoğunluk (Spesifik Gravite): Bir mineralin ağırlığının aynı miktardaki suyun ağırlığına bölünmesi ile elde edilir. Metalik mineraller genellikle metalik olmayan (non-metalik) minerallerden daha yüksek yoğunluğa sahiptir. Galen SG=7.5 Kuvars SG=2.67
40 Minerallerin Fiziksel Özellikleri Hidroklorik asit ile reaksiyon (kalsit köpürür) tat (halit tuz tadı verir) Diğer özellikler: dokunma (talk sabunumsu, grafit yağımsı his verir.) manyetizma (magnetit mıknatısı çeker)
41 Mineral Sınıflaması Mineraller kimyasal bileşimleri ve kristal yapıları esas alınarak sınıflandırılırlar.
42 Mineral Grupları-Mineral Sınıflaması Egemen anyon veya katyona göre sınıflanır. İkincil olarak iç mineral yapısına göre sınıflanır. Doğal Element tek elementler; örn. Au Sülfidler S 2- Oksitler (O 2- ) Hidroksitler (OH) Halitler Cl -, F -, Br - Karbonatlar (CO 3 ) 2- Sulfatlar (SO 4 ) 2- Fosfatlar (PO 4 ) Silikatlar 1.Nezosilikatlar, diğer adıyla İzole/Ada Silikatları 2.Sorosilikatlar veya diğer adıyla Çiftli Silikatlar 3.Siklosilikatlar veya diğer adıyla Halka Silikatları 4.İnosilikatlar veya Zincir Silikatları (tek ve çift zincir) 5.Fillosilikatlar veya diğer adıyla Levha Silikatları 6.Tektosilikatlar veya diğer adıyla Çerçeve Silikatları Nitratlar, Boratlar, Tungstatlar, Molibdatlar, Arsenatlar, Vanadatlar...
43 Kristal yapıları Kristal yapıları iyonların yüküne ve boyutlarına bağlı olarak gelişen kristal şekilleridir. En yaygın mineral grubu silikatlardır. Bütün silikat mineralleri silis ve oksijen içerir. 1. Mafik silikat mineralleri demir (Fe) veya mağnezyum (Mg) içerir ve renkleri koyudur. Örnekler: olivin, proksen, amfibol ve biyotit mika 2. Felsik silikatlar demir (Fe) veya mağnezyum (Mg) içermezler ve açık renklidir. Örnekler: feldspat, kuvars, kil mineralleri, muskovit mika Mafik (koyu renkli) ve felsik (açık renkli) terimleri renk indisine göre verilen tanımlamalardır. Kayaları da tanımlamak amacıyla kullanılır.
44 Mafik silikat Felsik silikat
45 Mineral Grupları Silikatlar Silikatlar Tetrahedron Tetrahedron tüm silikat minerallerinin en küçük yapı taşıdır.4 oksijen iyonu daha küçük silis iyonunu çevreler. Si ve O elementleri en dış yörüngelerindeki elektronik duraysızlık nedeniyle, elektron alış verişi yaparak birbirine kenetlenir. Si ve O arasındaki bağlar % 40 İyonik, % 60 kovalent dir Ayrıca, kovalent bağlı SiO2 bileşeni, SiO4-- e yükseltgenerek daha kararlı bir yapıya dönüşür. Silika-oksijen tetrahedronu (SiO 4 ) 4-
46
47 Tekli tetrahedral yapı Katyonlar tetrahedra içinde bağlantı oluşturur.oksijen paylaşımı olmaz. örn. Olivin ve granat Tek zincir silikatları Komşu tetrahedra komşu tetrahedra nın 2 oksijen atomunu paylaşarak bir zincir oluşturur. örn. proksenler Çift zincir silikatları İki zincir oksijenleri paylaşarak bağ oluşturur. örn. amfiboller Levha silikatları Her bir tetrahedron komşu tetrahedrondaki oksijen atomlarının 3 ünü paylaşarak levhaları oluşturur. örn. mikalar, biyotit (mafik) ve muskovit (mafik olmayan) ve kil mineralleri, Çerçeve silikatları Her bir tetrahedron daki her bir oksijen paylaşılır ve 3-boyut oluşturur. örn. feldspat, kuvars
48 Tek li tetrahedron Mineral Grupları Tek zincirler Silikatlar Çift zincirler Üç boyutlu ağlar Levhalar
49 Mineral Grupları Silikatlar Olivin Grubu Koyu silikatlar (Fe-Mg) ferromağnezyen Tekli tetrahedron (Mg,Fe) 2 [SiO 4 ] Klivaj içermez.
50 Mineral Grupları Silikatlar Proksen Grubu Ferromağnezyen / koyu silikatlar (Fe-Mg) Tek zincir 2-yönlü klivaj (90 derece açılı) Ojit
51 Mineral Grupları Silikatlar Amfibol Grubu Ferromağnezyen / koyu silikatlar (Ca, Fe-Mg) Çift zincir 2-yönlü klivaj (90 derece olmayan) Hornblend
52 Mineral Grupları Silikatlar Mika Grubu ve Kil Mineralleri Hafif silikatlar (K, Al) non-ferromağnezyen Levhalar Muskovit 1-yönlü klivaj
53 Mineral Grupları Silikatlar Feldspat Grubu Hafif silikatlar (K-Na-Ca, Al) En yaygın mineral grubu K-feldspat 3-boyutlu ağlar Ortoklas(ortoz) Plajiyoklas 2-yönlü klivaj (90 derece) Ca/Na-feldspat
54 Mineral Grupları Silikatlar Kuvars Hafif silikatlar (saf SiO 2 ) 3-boyutlu ağlar Klivaj yok (konkoidal kırılma) sert, ayrışmaya dayanıklı Kuvars
55 Yaygın bulunan silikat olmayan mineraller ve kullanım alanları Fluorit diş macunu katkısı olarak kullanılır. Kalsit -- kalsiyum karbonat Kireçtaşının ana maddesi Dolomit -- kalsiyum magneziyum karbonat, çimento katkısı ve kireç Jips -- kalsiyum sülfat, dolgu maddesi olarak Galen -- kurşun sülfid, kurşun cevheri eldesinde Pirit -- demir sülfid, sülfirik asit eldesinde Halit -- sodium klorür (sofra tuzu), en yaygın tuz oluşumu
56 Granit (kaya veya kayaç) kuvars (mineral) hornblend (mineral) feldspat (mineral)
57 Apatit Ca 5 (PO 4 ) 3 (OH, Cl,F) -hekzagonal sistem -prizmatik şekil
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
MİNERALLER. Tek mineralden oluşan kayaçlar. Kireçtaşı (Kalsit). Kaya tuzu (Halit). Buzul
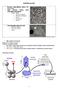 Kayaçlar minerallerden oluşan Yer materyalidir. Çoğu kayaçlar birden fazla mineralden oluşmaktadır. Örnek: Granit Potasyum feldspat. Plajioklas (Feldspat). Kuvars. Hornblende. Biyotit MİNERALLER Tek mineralden
Kayaçlar minerallerden oluşan Yer materyalidir. Çoğu kayaçlar birden fazla mineralden oluşmaktadır. Örnek: Granit Potasyum feldspat. Plajioklas (Feldspat). Kuvars. Hornblende. Biyotit MİNERALLER Tek mineralden
Bazı atomlarda proton sayısı aynı olduğu halde nötron sayısı değişiktir. Bunlara izotop denir. Şekil II.1. Bir atomun parçaları
 8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
oksijen silisyum tetrahedron
 SİLİKATLAR Silikat mineralleri doğada bulunan bütün minerallerin üçte birini, yer kabuğunun bileşiminin ise yüzde doksanını teşkil eder. Silikatlar yalnızca magmatik kayaçların değil aynı zamanda metamorfik
SİLİKATLAR Silikat mineralleri doğada bulunan bütün minerallerin üçte birini, yer kabuğunun bileşiminin ise yüzde doksanını teşkil eder. Silikatlar yalnızca magmatik kayaçların değil aynı zamanda metamorfik
BÖLÜM 2 ATOMİK YAPI İÇERİK. Atom yapısı. Bağ tipleri. Chapter 2-1
 BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
Madde ve Mineraller Bölüm Pearson Education, Inc.
 Madde ve Mineraller Bölüm 2 Mineral in Tanımı Mineraller (4000 ün üzerinde) Kayaçların Ana Yapıtaşı Doğal olarak oluşur Inorganik Katı Düzenli moleküler iç yapı (kristalin) Belirli (fakat fiks olmayan)bir
Madde ve Mineraller Bölüm 2 Mineral in Tanımı Mineraller (4000 ün üzerinde) Kayaçların Ana Yapıtaşı Doğal olarak oluşur Inorganik Katı Düzenli moleküler iç yapı (kristalin) Belirli (fakat fiks olmayan)bir
BİLEŞİKLER VE FORMÜLLERİ
 BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
KONU 11: TAŞIN HAMMADDE OLARAK KULLANIMI: MİNERALLER. Taşın Hammadde Olarak Kullanımı
 KONU 11: TAŞIN HAMMADDE OLARAK KULLANIMI: MİNERALLER Taşın Hammadde Olarak Kullanımı Odun ve kemik gibi, taş da insanın varlığının ilk evrelerinden bu yana elinin altında bulunan ve doğanın ona verdiği
KONU 11: TAŞIN HAMMADDE OLARAK KULLANIMI: MİNERALLER Taşın Hammadde Olarak Kullanımı Odun ve kemik gibi, taş da insanın varlığının ilk evrelerinden bu yana elinin altında bulunan ve doğanın ona verdiği
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ
 ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
ATOMLAR ARASI BAĞLAR Doç. Dr. Ramazan YILMAZ Sakarya Üniversitesi, Teknoloji Fakültesi, Metalurji ve Malzeme Mühendisliği Bölümü Esentepe Kampüsü, 54187, SAKARYA Atomlar Arası Bağlar 1 İyonik Bağ 2 Kovalent
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla
 ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
Örnek : 3- Bileşiklerin Özellikleri :
 Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar.
 Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR. Aytekin Hitit
 ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
FZM 220. Malzeme Bilimine Giriş
 FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Atomsal Yapı ve Atomlararası Bağ1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin
FZM 220 Yapı Karakterizasyon Özellikler İşleme Performans Prof. Dr. İlker DİNÇER Fakültesi, Fizik Mühendisliği Bölümü 1 Atomsal Yapı ve Atomlararası Bağ1 Ders Hakkında FZM 220 Dersinin Amacı Bu dersin
YERKABUĞUNU OLUŞTURAN MİNERALLER İNM 102: İNŞAAT MÜHENDİSLERİ İÇİN JEOLOJİ. Yerkabuğunun Yapısı. Yerkürenin Yapısı. Dr.
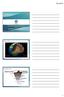 İNM 102: İNŞAAT MÜHENDİSLERİ İÇİN JEOLOJİ 17.03.2015 YERKABUĞUNU OLUŞTURAN MİNERALLER Dr. Dilek OKUYUCU Yerkürenin Yapısı Yerkabuğunun Yapısı 1 Yerkabuğunun Yapısı ~100 km ~10 km Yerkabuğunun Yapısı Yerkabuğunu
İNM 102: İNŞAAT MÜHENDİSLERİ İÇİN JEOLOJİ 17.03.2015 YERKABUĞUNU OLUŞTURAN MİNERALLER Dr. Dilek OKUYUCU Yerkürenin Yapısı Yerkabuğunun Yapısı 1 Yerkabuğunun Yapısı ~100 km ~10 km Yerkabuğunun Yapısı Yerkabuğunu
BÖLÜM 2 ATOMİK YAPI İÇERİK. Atom yapısı. Bağ tipleri. Chapter 2-1
 BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
BÖLÜM 2 ATOMİK YAPI İÇERİK Atom yapısı Bağ tipleri 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (-yüklü) Basit bir atom
TOPRAK OLUŞUMUNDA AŞINMA, AYRIŞMA VE BİRLEŞME OLAYLARI
 TOPRAK OLUŞUMUNDA AŞINMA, AYRIŞMA VE BİRLEŞME OLAYLARI Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Toprak Oluşumunda Kimyasal Ayrıştırma Etmenleri Ana kayanın kimyasal bileşimini değiştirmek
TOPRAK OLUŞUMUNDA AŞINMA, AYRIŞMA VE BİRLEŞME OLAYLARI Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Toprak Oluşumunda Kimyasal Ayrıştırma Etmenleri Ana kayanın kimyasal bileşimini değiştirmek
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
HALOJENLER HALOJENLER
 HALOJENLER HALOJENLER Bu grup bileşimlerinde flor (F), klor (Cl), brom (Br) ve iyot (I) gibi halojen iyonlarının hakim olmaları ile karakterize olurlar. Doğada 85 çeşit halojenli mineral tespit edilmiştir.
HALOJENLER HALOJENLER Bu grup bileşimlerinde flor (F), klor (Cl), brom (Br) ve iyot (I) gibi halojen iyonlarının hakim olmaları ile karakterize olurlar. Doğada 85 çeşit halojenli mineral tespit edilmiştir.
MADDE Kütlesi olan ve alan kaplayan her şey maddedir.
 Bu nedenle su, bitkiler, hayvanlar, atmosfer ile mineraller ve kayaçların tümü maddeden oluşur. Fizikçiler maddeyi üç halde ya da evrede tanımlar: sıvılar, gazlar ve katılar. Atmosferdeki gazlarla birlikte
Bu nedenle su, bitkiler, hayvanlar, atmosfer ile mineraller ve kayaçların tümü maddeden oluşur. Fizikçiler maddeyi üç halde ya da evrede tanımlar: sıvılar, gazlar ve katılar. Atmosferdeki gazlarla birlikte
Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.
 ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
GİRİŞ YERKABUĞUNU OLUŞTURAN MADDELER 1. ATOM 2. ELEMENTLER TANIMLAMALAR
 GİRİŞ YERKABUĞUNU OLUŞTURAN MADDELER Yerkabuğu minerallerden ve bunları oluşturan kayaçlardan meydana gelmiştir. Her türlü inşaatta temel ve üst yapı projeleri hazırlamadan önce, temel zemininde rastlanılacak
GİRİŞ YERKABUĞUNU OLUŞTURAN MADDELER Yerkabuğu minerallerden ve bunları oluşturan kayaçlardan meydana gelmiştir. Her türlü inşaatta temel ve üst yapı projeleri hazırlamadan önce, temel zemininde rastlanılacak
Seramik malzemelerin kristal yapıları
 Seramik malzemelerin kristal yapıları Kararlı ve kararsız anyon-katyon görünümü. Kırmızı daireler anyonları, mavi daireler katyonları temsil eder. Bazı seramik malzemelerin atomlararası bağlarının iyonik
Seramik malzemelerin kristal yapıları Kararlı ve kararsız anyon-katyon görünümü. Kırmızı daireler anyonları, mavi daireler katyonları temsil eder. Bazı seramik malzemelerin atomlararası bağlarının iyonik
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
CANLILARIN KİMYASAL İÇERİĞİ
 CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
BİYOLOJİK MOLEKÜLLERDEKİ
 BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
ATOMLAR ARASI BAĞLAR
 MALZEME 2. HAFTA 1 ATOMSAL BAĞ ATOMLAR ARASI BAĞLAR Atomlar, atomlar arası bağ kuvvetleri ile bir araya gelirler. Malzemenin en küçük yapı taşı olan atomları bağ kuvvetleri bir arada tutar. Atomsal bağların
MALZEME 2. HAFTA 1 ATOMSAL BAĞ ATOMLAR ARASI BAĞLAR Atomlar, atomlar arası bağ kuvvetleri ile bir araya gelirler. Malzemenin en küçük yapı taşı olan atomları bağ kuvvetleri bir arada tutar. Atomsal bağların
Yrd.Doç.Dr. Emre YALAMAÇ. Yrd.Doç.Dr. Emre YALAMAÇ İÇERİK
 İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır:
 Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
MİNERALLER
 MİNERALLER Yer kabuğu mineraller ve minerallerin oluşturduğu kayaçlardan meydana gelmektedir. Bütün inşaat işlerinde proje hazırlanmadan önce mühendislik yapısının (bina, tünel, baraj, yol vs.) yapılacağı
MİNERALLER Yer kabuğu mineraller ve minerallerin oluşturduğu kayaçlardan meydana gelmektedir. Bütün inşaat işlerinde proje hazırlanmadan önce mühendislik yapısının (bina, tünel, baraj, yol vs.) yapılacağı
2. Bölüm: TOPRAK ANA MADDESİ
 2. Bölüm: TOPRAK ANA MADDESİ Topraklar, yerküresinin en üst bölümünde bulunan kayalar, mineraller ve organik maddelerin çeşitli doğal faktörlerin etkileriyle parçalanması, ayrışması ve ayrışan bir kısım
2. Bölüm: TOPRAK ANA MADDESİ Topraklar, yerküresinin en üst bölümünde bulunan kayalar, mineraller ve organik maddelerin çeşitli doğal faktörlerin etkileriyle parçalanması, ayrışması ve ayrışan bir kısım
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ
 ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
ATOMUN YAPISI. Özhan ÇALIŞ. Bilgi İletişim ve Teknolojileri
 ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
Katılar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN. Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 2006
 Katılar Tüm maddeler, yeteri kadar soğutulduğunda katıları oluştururlar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Oluşan katıların doğası atom, iyon veya molekülleri birarada tutan kuvvetlere
Katılar Tüm maddeler, yeteri kadar soğutulduğunda katıları oluştururlar. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Oluşan katıların doğası atom, iyon veya molekülleri birarada tutan kuvvetlere
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6
 PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ
 Bölüm 4 TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. Be, Mg, Ca, Sr, Ba, Ra Magnezyum, kalsiyum, stronsiyum, baryum ve radyumdan
Bölüm 4 TOPRAK ALKALİ METALLER ve BİLEŞİKLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. Be, Mg, Ca, Sr, Ba, Ra Magnezyum, kalsiyum, stronsiyum, baryum ve radyumdan
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı
 Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010
 METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010 WEBSİTE www2.aku.edu.tr/~hitit Dersler İÇERİK Metalik Malzemelerin Genel Karakteristiklerİ Denge diyagramları Ergitme ve döküm Dökme demir ve çelikler
METALİK MALZEMELERİN GENEL KARAKTERİSTİKLERİ BAHAR 2010 WEBSİTE www2.aku.edu.tr/~hitit Dersler İÇERİK Metalik Malzemelerin Genel Karakteristiklerİ Denge diyagramları Ergitme ve döküm Dökme demir ve çelikler
PERİYODİK CETVEL Mendeleev Henry Moseley Glenn Seaborg
 PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
IVA GRUBU ELEMENTLERİ
 Bölüm 6 IVA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. C, Si, Ge, Sn, Pb C: Ametal Si ve Ge: Yarı metal Sn ve Pb: Metal C: +4 ile -4 arası Si
Bölüm 6 IVA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. C, Si, Ge, Sn, Pb C: Ametal Si ve Ge: Yarı metal Sn ve Pb: Metal C: +4 ile -4 arası Si
BMM 205 Malzeme Biliminin Temelleri
 BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
BMM 205 Malzeme Biliminin Temelleri Atom Yapısı ve Atomlar Arası Bağlar Dr. Ersin Emre Ören Biyomedikal Mühendisliği Bölümü Malzeme Bilimi ve Nanoteknoloji Mühendisliği Bölümü TOBB Ekonomi ve Teknoloji
KĠMYASAL ÖZELLĠKLER VE KĠMYASAL BAĞ
 Elektronların Dizilimi ve Kimyasal Özellikler Atomların katmanlarında belirli sayılarda elektron bulunmaktadır. Ancak bir atom, tek katmanlıysa ve bu katmanda iki elektronu varsa kararlıdır. Atomun iki
Elektronların Dizilimi ve Kimyasal Özellikler Atomların katmanlarında belirli sayılarda elektron bulunmaktadır. Ancak bir atom, tek katmanlıysa ve bu katmanda iki elektronu varsa kararlıdır. Atomun iki
INSA 283 MALZEME BİLİMİ. Giriş
 INSA 283 MALZEME BİLİMİ Giriş Malzeme Gereksinimi Bütün mühendislik bilim dallari malzeme ile yakindan iliskilidir. Mühendisler kullanacaklari malzemeyi çok iyi tanıyarak ve genis malzeme tayfi içinde
INSA 283 MALZEME BİLİMİ Giriş Malzeme Gereksinimi Bütün mühendislik bilim dallari malzeme ile yakindan iliskilidir. Mühendisler kullanacaklari malzemeyi çok iyi tanıyarak ve genis malzeme tayfi içinde
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER
 BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
Her madde atomlardan oluşur
 2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır.
 Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır. 1-İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır. 1-İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Piroelektrisite vepiezoelektrisite arasında ne fark vardır? Örnekliyerek açıklayınız.
 15 ARALIK 2014 Piroelektrisite vepiezoelektrisite arasında ne fark vardır? Örnekliyerek açıklayınız. Işığın dalga karakteri göz önüne alındığında madde ile etkileşiminde hangi özellikler gözlenir. İzotropik
15 ARALIK 2014 Piroelektrisite vepiezoelektrisite arasında ne fark vardır? Örnekliyerek açıklayınız. Işığın dalga karakteri göz önüne alındığında madde ile etkileşiminde hangi özellikler gözlenir. İzotropik
TOPRAK ANA MADDESİ Top T rak Bilgisi Ders Bilgisi i Peyzaj Mimarlığı aj Prof. Dr Prof.. Dr Günay Erpul kar.edu.
 TOPRAK ANA MADDESİ Toprak Bilgisi Dersi 2011 2012 Peyzaj Mimarlığı Prof. Dr. Günay Erpul erpul@ankara.edu.tr Toprak Ana Maddesi Topraklar, arz kabuğunu oluşturan kayalar, mineraller ve organik maddelerin
TOPRAK ANA MADDESİ Toprak Bilgisi Dersi 2011 2012 Peyzaj Mimarlığı Prof. Dr. Günay Erpul erpul@ankara.edu.tr Toprak Ana Maddesi Topraklar, arz kabuğunu oluşturan kayalar, mineraller ve organik maddelerin
1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır.
 14 DENEY KATI HAL 1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır. 2. Giriş Atomlar arası (veya moleküller arası) çekim kuvvetleri
14 DENEY KATI HAL 1. Amaç Kristallerin üç boyutlu yapısı incelenecektir. Ön bilgi için İnorganik Kimya, Miessler ve Tarr, Bölüm 7 okunmalıdır. 2. Giriş Atomlar arası (veya moleküller arası) çekim kuvvetleri
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
ELEMENTLERİN SEMBOLLERİ VE ATOM
 ELEMENT VE SEMBOLLERİ SAF MADDE: Kendisinden başka madde bulundurmayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran maddelere denir. Yani elementlerin yapı yaşı atomlardır. BİLEŞİK: En
ELEMENT VE SEMBOLLERİ SAF MADDE: Kendisinden başka madde bulundurmayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran maddelere denir. Yani elementlerin yapı yaşı atomlardır. BİLEŞİK: En
BASİT ANLATIMLA KİMYASAL REAKSİYON Derleyen Selim Yenisey
 BASİT ANLATIMLA KİMYASAL REAKSİYON Derleyen Selim Yenisey Suyu oluşturan hidrojen ve oksijen kolaylıkla alev alan maddeler olduğuna göre su neden yanmaz? veya Neden hidrojen ve oksijen birleşebiliyor?
BASİT ANLATIMLA KİMYASAL REAKSİYON Derleyen Selim Yenisey Suyu oluşturan hidrojen ve oksijen kolaylıkla alev alan maddeler olduğuna göre su neden yanmaz? veya Neden hidrojen ve oksijen birleşebiliyor?
Element atomlarının atom ve kütle numaraları element sembolleri üzerinde gösterilebilir. Element atom numarası sembolün sol alt köşesine yazılır.
 Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur.
 DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler
 Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler Toprakta bulunan katı (mineral ve organik madde), sıvı (toprak çözeltisi ve bileşenleri) ve gaz fazları sürekli olarak etkileşim içerisindedir. Bunlar
Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler Toprakta bulunan katı (mineral ve organik madde), sıvı (toprak çözeltisi ve bileşenleri) ve gaz fazları sürekli olarak etkileşim içerisindedir. Bunlar
MMM291 MALZEME BİLİMİ
 MMM291 MALZEME BİLİMİ Ofis Saatleri: Perşembe 14:00 16:00 ayse.kalemtas@btu.edu.tr, akalemtas@gmail.com Bursa Teknik Üniversitesi, Doğa Bilimleri, Mimarlık ve Mühendislik Fakültesi, Metalurji ve Malzeme
MMM291 MALZEME BİLİMİ Ofis Saatleri: Perşembe 14:00 16:00 ayse.kalemtas@btu.edu.tr, akalemtas@gmail.com Bursa Teknik Üniversitesi, Doğa Bilimleri, Mimarlık ve Mühendislik Fakültesi, Metalurji ve Malzeme
KİMYASAL BAĞLAR Kimyasal bağlar, Moleküllerde atomları birarada tutan
 KİMYASAL BAĞLAR Kimyasal bağlar, Moleküllerde atomları birarada tutan kuvvettir. Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Atomun sembolünün
KİMYASAL BAĞLAR Kimyasal bağlar, Moleküllerde atomları birarada tutan kuvvettir. Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Atomun sembolünün
Soygazların bileşik oluşturamamasının sebebi bütün orbitallerinin dolu olmasındandır.
 KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
Periyodik Tablo(sistem)
 Periyodik Tablo(sistem) Geçmişten Günümüze Periyodik Tablo Bilim adamları elementlerin sayısı arttıkça bunları benzer özelliklerine göre sıralamaya çalışmışlardır.(bunu süpermarketlerdeki ürünlerin dizilişlerine
Periyodik Tablo(sistem) Geçmişten Günümüze Periyodik Tablo Bilim adamları elementlerin sayısı arttıkça bunları benzer özelliklerine göre sıralamaya çalışmışlardır.(bunu süpermarketlerdeki ürünlerin dizilişlerine
ÖĞRENME ALANI : MADDE VE DEĞĐŞĐM ÜNĐTE 3 : MADDENĐN YAPISI VE ÖZELLĐKLERĐ
 ÖĞRENME ALANI : MADDE VE DEĞĐŞĐM ÜNĐTE 3 : MADDENĐN YAPISI VE ÖZELLĐKLERĐ C- BĐLEŞĐKLER VE BĐLEŞĐK FORMÜLLERĐ (4 SAAT) 1- Bileşikler 2- Đyonik Yapılı Bileşik Formüllerinin Yazılması 3- Đyonlar ve Değerlikleri
ÖĞRENME ALANI : MADDE VE DEĞĐŞĐM ÜNĐTE 3 : MADDENĐN YAPISI VE ÖZELLĐKLERĐ C- BĐLEŞĐKLER VE BĐLEŞĐK FORMÜLLERĐ (4 SAAT) 1- Bileşikler 2- Đyonik Yapılı Bileşik Formüllerinin Yazılması 3- Đyonlar ve Değerlikleri
Element ve Bileşikler
 Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
PERİYODİK CETVEL
 BÖLÜM4 W Periyodik cetvel, elementlerin atom numaraları esas alınarak düzenlenmiştir. Bu düzenlemede, kimyasal özellikleri benzer olan (değerlik elektron sayıları aynı) elementler aynı düşey sütunda yer
BÖLÜM4 W Periyodik cetvel, elementlerin atom numaraları esas alınarak düzenlenmiştir. Bu düzenlemede, kimyasal özellikleri benzer olan (değerlik elektron sayıları aynı) elementler aynı düşey sütunda yer
MALZEME BİLGİSİ DERS 4 DR. FATİH AY.
 MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
MALZEME BİLGİSİ DERS 4 DR. FATİH AY www.fatihay.net fatihay@fatihay.net GEÇEN HAFTA TEMEL KAVRAMLAR ATOMLARDA ELEKTRONLAR PERİYODİK TABLO BÖLÜM II ATOM YAPISI VE ATOMLARARASı BAĞLAR BAĞ KUVVETLERİ VE ENERJİLERİ
BİTKİ BESİN MADDELERİ (BBM)
 BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul erpul@ankara.edu.tr Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
ATOM BİLGİSİ Atom Modelleri
 1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten. Kimyasal Bağlar.
 Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
Chemistry, The Central Science, 10th edition Theodore L. Brown; H. Eugene LeMay, Jr.; and Bruce E. Bursten Kimyasal Bağlar Kimyasal Bağlar 3 temel tip bağ vardır: İyonik İyonlar arası elektrostatik etkileşim
MOL KAVRAMI I. ÖRNEK 2
 MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
Bölüm 2: Atomik Yapı & Atomarası Bağlar
 Bölüm 2: Atomik Yapı & Atomarası Bağlar Bağlanmayı ne sağlar? Ne tip bağlar vardır? Bağların sebep olduğu özellikler nelerdir? Chapter 2-1 Atomun yapısı (Birinci sınıf kimyası) atom electronlar 9.11 x
Bölüm 2: Atomik Yapı & Atomarası Bağlar Bağlanmayı ne sağlar? Ne tip bağlar vardır? Bağların sebep olduğu özellikler nelerdir? Chapter 2-1 Atomun yapısı (Birinci sınıf kimyası) atom electronlar 9.11 x
Elektronların Dağılımı ve Kimyasal Özellikleri
 Elektronların Dağılımı ve Kimyasal Özellikleri Helyum (2), neon (10), argon (18)in elektron dağılımları incelendiğinde Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı.
Elektronların Dağılımı ve Kimyasal Özellikleri Helyum (2), neon (10), argon (18)in elektron dağılımları incelendiğinde Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı.
1. ÜNİTE: MODERN ATOM TEORİSİ İyon Yükleri ve Yükseltgenme Basamakları
 1. ÜNİTE: MODERN ATOM TEORİSİ 1.7. İyon Yükleri ve Yükseltgenme Basamakları Yüksüz bir atomun yapısındaki pozitif (+) yüklü protonlarla negatif () yüklü elektronların sayıları birbirine eşittir. Yüksüz
1. ÜNİTE: MODERN ATOM TEORİSİ 1.7. İyon Yükleri ve Yükseltgenme Basamakları Yüksüz bir atomun yapısındaki pozitif (+) yüklü protonlarla negatif () yüklü elektronların sayıları birbirine eşittir. Yüksüz
Müh. Fak. G. Kimya Vize Soru ve Cevapları A Mühendislik Fakültesi Genel Kimya (Kimya Metal. ve Malz.)) Ara Sınav Soruları
 Müh. Fak. G. Kimya Vize Soru ve Cevapları A 08.11.2017 Adı ve Soyadı:.. Fak. No:... Mühendislik Fakültesi Genel Kimya (Kimya Metal. ve Malz.)) Ara Sınav Soruları 1) Bilinen tüm yöntemlerle kendisinden
Müh. Fak. G. Kimya Vize Soru ve Cevapları A 08.11.2017 Adı ve Soyadı:.. Fak. No:... Mühendislik Fakültesi Genel Kimya (Kimya Metal. ve Malz.)) Ara Sınav Soruları 1) Bilinen tüm yöntemlerle kendisinden
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Yapılar nasıl gösterilir ve tanımlanır?
 17 KASIM 2014 Yapı nedir? Yapılar nasıl gösterilir ve tanımlanır? Kordinasyon çokgenlerinin kurgusunda temel ilke nedir? Polimorfizm, izomorfizm ve psödomorfizm arasındaki farkları örnekleyerek açıklayınız.
17 KASIM 2014 Yapı nedir? Yapılar nasıl gösterilir ve tanımlanır? Kordinasyon çokgenlerinin kurgusunda temel ilke nedir? Polimorfizm, izomorfizm ve psödomorfizm arasındaki farkları örnekleyerek açıklayınız.
TABAKALI SİLİKATLAR (Fillosilikatlar)
 TABAKALI SİLİKATLAR (Fillosilikatlar) Kaolinit Al 4 Si 4 O 10 (OH) 8 Serpantin Mg 6 Si 4 O 10 (OH) 8 Pirofillit Al 2 Si 4 O 10 (OH) 8 Talk Mg 3 Si 4 O 10 (OH) 8 Muskovit KAl 2 (AlSi 3 O 10 )(OH) 2 Flogopit
TABAKALI SİLİKATLAR (Fillosilikatlar) Kaolinit Al 4 Si 4 O 10 (OH) 8 Serpantin Mg 6 Si 4 O 10 (OH) 8 Pirofillit Al 2 Si 4 O 10 (OH) 8 Talk Mg 3 Si 4 O 10 (OH) 8 Muskovit KAl 2 (AlSi 3 O 10 )(OH) 2 Flogopit
KIRİSTAL YAPISI, KİMYASI VE MİNERALLERİN BİLEŞİMİ
 KIRİSTL YPISI, KİMYSI VE MİNERLLERİN BİLEŞİMİ Yeryuvarında değişik bileşikler halinde bulunan elementler, çeşitli olaylara bağlı olarak değişiklik gösterebilir: Hidrotermal bozunma, oksidasyon, çözelti
KIRİSTL YPISI, KİMYSI VE MİNERLLERİN BİLEŞİMİ Yeryuvarında değişik bileşikler halinde bulunan elementler, çeşitli olaylara bağlı olarak değişiklik gösterebilir: Hidrotermal bozunma, oksidasyon, çözelti
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ
 KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
KİMYASAL BAĞLAR İYONİK BAĞ KOVALANT BAĞ POLAR KOVALENT BAĞ APOLAR KOVALENT BAĞ Atomlar bağ yaparken, elektron dizilişlerini soy gazlara benzetmeye çalışırlar. Bir atomun yapabileceği bağ sayısı, sahip
CALLİSTER - SERAMİKLER
 CALLİSTER - SERAMİKLER Atomik bağı ağırlıklı olarak iyonik olan seramik malzemeler için, kristal yapılarının atomların yerine elektrikle yüklü iyonlardan oluştuğu düşünülebilir. Metal iyonları veya katyonlar
CALLİSTER - SERAMİKLER Atomik bağı ağırlıklı olarak iyonik olan seramik malzemeler için, kristal yapılarının atomların yerine elektrikle yüklü iyonlardan oluştuğu düşünülebilir. Metal iyonları veya katyonlar
ATOM BİLGİSİ I ÖRNEK 1
 ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
izotop MALZEME BILGISI B2
 1. Giriş 2. Temel Kavramlar 3. Atomlarda Elektronlar 4. Periyodik Tablo 5. Bağ Kuvvetleri ve Enerjileri 6. Atomlararası Birincil Bağlar 7. İkincil bağlar veya Van Der Waals Bağları 8. Moleküller Bu özelliklerinden
1. Giriş 2. Temel Kavramlar 3. Atomlarda Elektronlar 4. Periyodik Tablo 5. Bağ Kuvvetleri ve Enerjileri 6. Atomlararası Birincil Bağlar 7. İkincil bağlar veya Van Der Waals Bağları 8. Moleküller Bu özelliklerinden
2+ 2- Mg SO 4. (NH 4 ) 2 SO 4 (amonyum sülfat) bileşiğini katyon ve anyonlara ayıralım.
 KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA
 İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR
 KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
TOPRAK TOPRAK TEKSTÜRÜ (BÜNYESİ)
 TOPRAK Toprak esas itibarı ile uzun yılların ürünü olan, kayaların ve organik maddelerin türlü çaptaki ayrışma ürünlerinden meydana gelen, içinde geniş bir canlılar âlemini barındırarak bitkilere durak
TOPRAK Toprak esas itibarı ile uzun yılların ürünü olan, kayaların ve organik maddelerin türlü çaptaki ayrışma ürünlerinden meydana gelen, içinde geniş bir canlılar âlemini barındırarak bitkilere durak
ELEKTRONLARIN DĠZĠLĠMĠ
 ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
ELEKTRONLARIN DĠZĠLĠMĠ Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır. 1.Katmanda en çok 2
Atomdan e koparmak için az ya da çok enerji uygulamak gereklidir. Bu enerji ısıtma, sürtme, gerilim uygulama ve benzeri şekilde verilebilir.
 TEMEL ELEKTRONİK Elektronik: Maddelerde bulunan atomların son yörüngelerinde dolaşan eksi yüklü elektronların hareketleriyle çeşitli işlemleri yapma bilimine elektronik adı verilir. KISA ATOM BİLGİSİ Maddenin
TEMEL ELEKTRONİK Elektronik: Maddelerde bulunan atomların son yörüngelerinde dolaşan eksi yüklü elektronların hareketleriyle çeşitli işlemleri yapma bilimine elektronik adı verilir. KISA ATOM BİLGİSİ Maddenin
YAPRAKLANMALI METAMORFİK KAYAÇALAR. YAPRAKLANMASIZ Metamorfik Kayaçlar
 YAPRAKLANMALI METAMORFİK KAYAÇALAR YAPRAKLANMASIZ Metamorfik Kayaçlar Dokanak başkalaşım kayaçlarında gözlenen ince taneli, yönlenmesiz ve yaklaşık eş boyutlu taneli doku gösteren kayaçlara hornfels denir.
YAPRAKLANMALI METAMORFİK KAYAÇALAR YAPRAKLANMASIZ Metamorfik Kayaçlar Dokanak başkalaşım kayaçlarında gözlenen ince taneli, yönlenmesiz ve yaklaşık eş boyutlu taneli doku gösteren kayaçlara hornfels denir.
Ölçme Kontrol ve Otomasyon Sistemleri 1
 Ölçme Kontrol ve Otomasyon Sistemleri 1 Dr. Mehmet Ali DAYIOĞLU Ankara Üniversitesi Ziraat Fakültesi Tarım Makinaları ve Teknolojileri Mühendisliği Bölümü 1. Elektroniğe giriş Akım, voltaj, direnç, elektriksel
Ölçme Kontrol ve Otomasyon Sistemleri 1 Dr. Mehmet Ali DAYIOĞLU Ankara Üniversitesi Ziraat Fakültesi Tarım Makinaları ve Teknolojileri Mühendisliği Bölümü 1. Elektroniğe giriş Akım, voltaj, direnç, elektriksel
BİLEŞİKLER İki ya da daha fazla maddenin belli oranda kimyasal olarak birleşmeleri sonucu oluşturdukları yeni, saf maddeye bileşik denir.
 BİLEŞİKLER İki ya da daha fazla maddenin belli oranda kimyasal olarak birleşmeleri sonucu oluşturdukları yeni, saf maddeye bileşik denir. ÖZELLĠKLERĠ: 1. Yapılarında iki ya da daha fazla madde bulundururlar.
BİLEŞİKLER İki ya da daha fazla maddenin belli oranda kimyasal olarak birleşmeleri sonucu oluşturdukları yeni, saf maddeye bileşik denir. ÖZELLĠKLERĠ: 1. Yapılarında iki ya da daha fazla madde bulundururlar.
Element ve Bileşikler
 Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
Element ve Bileşikler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Bir elementi oluşturan bütün atomların
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER
 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
TOBB Ekonomi ve Teknoloji Üniversitesi. Genel Kimya 101. Yrd.Doç.Dr.Zeynep OBALI e-mail: zobali@etu.edu.tr Ofis: z-83/2
 Genel Kimya 101 Yrd.Doç.Dr.Zeynep OBALI e-mail: zobali@etu.edu.tr Ofis: z-83/2 İyonik Bağ; İyonik bir bileşikteki pozitif ve negatif iyonlar arasındaki etkileşime iyonik bağ denir Na Na + + e - Cl + e
Genel Kimya 101 Yrd.Doç.Dr.Zeynep OBALI e-mail: zobali@etu.edu.tr Ofis: z-83/2 İyonik Bağ; İyonik bir bileşikteki pozitif ve negatif iyonlar arasındaki etkileşime iyonik bağ denir Na Na + + e - Cl + e
JEOLOJĠ TOPOĞRAFYA VE KAYAÇLAR
 JEOLOJĠ TOPOĞRAFYA VE KAYAÇLAR Bir nehir kenarında gezerken çakılların renk ve biçim bakımından birbirlerinden farklı olduğunu görürüz. Bu durum bize, kayaçların farklı ortamlarda oluştuğunu gösterir.
JEOLOJĠ TOPOĞRAFYA VE KAYAÇLAR Bir nehir kenarında gezerken çakılların renk ve biçim bakımından birbirlerinden farklı olduğunu görürüz. Bu durum bize, kayaçların farklı ortamlarda oluştuğunu gösterir.
7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri
 ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ 7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri Çalışma Yaprağı Konu Anlatımı-Değerlendirme çalışma Yaprağı- Çözümlü
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ 7. Sınıf Fen ve Teknoloji Dersi 4. Ünite: Madde ve Yapısı Konu: Elementler ve Sembolleri Çalışma Yaprağı Konu Anlatımı-Değerlendirme çalışma Yaprağı- Çözümlü
