SIĞIR MASTİTİSLERİNDEN VE ÇEVRESEL KAYNAKLARDAN İZOLE EDİLEN ESCHERICHIA COLI SUŞLARININ VİRULENS FAKTÖRLERİNİN BELİRLENMESİ
|
|
|
- Nilüfer Sönmez
- 5 yıl önce
- İzleme sayısı:
Transkript
1 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ SIĞIR MASTİTİSLERİNDEN VE ÇEVRESEL KAYNAKLARDAN İZOLE EDİLEN ESCHERICHIA COLI SUŞLARININ VİRULENS FAKTÖRLERİNİN BELİRLENMESİ Gökçen DİNÇ MİKROBİYOLOJİ ANABİLİM DALI DOKTORA TEZİ DANIŞMAN Prof. Dr. Müjgan İZGÜR ANKARA
2 iii TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ SIĞIR MASTİTİSLERİNDEN VE ÇEVRESEL KAYNAKLARDAN İZOLE EDİLEN ESCHERICHIA COLI SUŞLARININ VİRULENS FAKTÖRLERİNİN BELİRLENMESİ Gökçen DİNÇ MİKROBİYOLOJİ ANABİLİM DALI DOKTORA TEZİ DANIŞMAN Prof. Dr. Müjgan İZGÜR ANKARA
3 ii Ankara Üniversitesi Sağlık Bilimleri Enstitüsü Mikrobiyoloji Doktora Programı çerçevesinde yürütülmüş olan bu çalışma, aşağıdaki jüri tarafından Doktora Tezi olarak kabul edilmiştir. Tez Savunma Tarihi: 08/ 07/ 2009 Prof. Dr. Müjgan İZGÜR Ankara Üniversitesi Jüri Başkanı Prof. Dr. Hakan YARDIMCI Ankara Üniversitesi Prof. Dr. M. Rıfat VURAL Ankara Üniversitesi Prof. Dr. Mehmet AKAN Ankara Üniversitesi Raportör Doç. Dr. Yahya KUYUCUOĞLU Afyon Kocatepe Üniversitesi
4 iii İÇİNDEKİLER Kabul ve Onay ii İçindekiler iii Önsöz v Simgeler ve Kısaltmalar vi Şekiller viii Çizelgeler ix 1. GİRİŞ 1.1. Tarihçe Etiyoloji E. coli nin Virulens Faktörleri Adhezinler Tip 1 Fimbria F17 Fimbria Ailesi P Fimbrialar, S Fimbrialar ve Çeşitli Spesifik Fimbrialar Afimbrial Adhezinler (AFA) Curli Fimbrialar Toksinler Aerobaktin Demir Elde Etme Sistemi Serum Dirençliliği Kolisin Aktivitesi Kapsül Polisakkaritleri Epidemiyoloji Patogenez Semptomlar Teşhis Laboratuvar Muayenesi Bakteriyoskopi Kültür Patojenite Testleri Çeşitli Virulens Özelliklerin Tayini Hayvan Deneyleri Serolojik Testler Moleküler Teknikler Sağaltım Koruma GEREÇ VE YÖNTEM Gereç Örneklerin Toplanması Besiyerleri PCR da Kullanılan Maddeler PCR da Kullanılan Cihaz ve Ekipmanlar Standart Suşlar Hücre Kültürü 33
5 2.2. Yöntem İzolasyon ve İdentifikasyon E. coli Suşlarının Çeşitli Virulens Özelliklerinin Araştırılması Hemoliz Testi Hemaglutinasyon Testi Aerobaktin Demir Elde Etme Sistemlerinin Araştırılması Vero Hücrelerde Toksik Etkinin İncelenmesi Serum Dirençliliği Kolisin Aktivitesi Polimeraz Zincir Reaksiyonu (Polymerase Chain Reaction: PCR) BULGULAR İzolasyon ve İdentifikasyon Bulguları Virulens Faktörlere Ait Bulgular Hemoliz Bulguları Hemaglütinasyon Bulguları Aerobaktin Demir Elde Etme Sistemine Ait Bulgular Vero Hücrelerde Toksik Etkiye Ait Bulgular Serum Dirençliliği Bulguları Kolisin Bulguları PCR Bulguları Fenotipik ve Moleküler Bulguların Karşılaştırılması TARTIŞMA SONUÇ VE ÖNERİLER 64 ÖZET 66 SUMMARY 67 KAYNAKLAR 68 ÖZGEÇMİŞ 76 iv
6 v ÖNSÖZ Birçok ülkede olduğu gibi Türkiye de de, gıda ve tarım sektöründe önemli rol oynayan süt endüstrisinin ve süt sığırı yetiştiriciliğinin karşı karşıya kaldığı sorunların başında Mastitis gelmektedir. Süt veriminin azalması, süt kalitesinin bozulması, sağaltım masrafları ve bazen de hayvanın elden çıkarılması gibi nedenlerden dolayı mastitis, ülke ekonomisi için büyük bir önem taşımaktadır. Ülkemizde mastitislerin neden olduğu yıllık ekonomik kaybın yaklaşık 41.5 milyon TL dolayında olduğu bildirilmektedir. Bu durum göz önüne alındığında, mastitise yol açan etkenler ile hastalık patogenezinde rol oynayan faktörlerin belirlenerek, gerekli önlemlerin alınması ve kaliteli süt üretiminin sağlanması hem ülke ekonomisi, hem insan sağlığı, hem de hayvan sağlığı açısından oldukça önemlidir. Ülkemizde ineklerde mastitisler üzerine birçok araştırma yapılmış olmasına rağmen günümüzde halen süt sığırı yetiştiriciliğinin en önemli problemlerinden biri olarak karşımızda durmaktadır. Mikroorganizma, çevre ve konakçıya bağlı faktörlerin rol aldığı kompleks bir infeksiyon olan mastitise patojenik Escherichia coli suşlarının da yol açtığı bilinmektedir. E. coli nedenli mastitisler hakkında çok sayıda çalışma yapılmış olmasına karşın hastalığın patogenezi ve prognozu ile ilgili birçok soru cevapsız kalmaktadır. Bu nedenle E. coli suşları tarafından oluşturulan olgularda, çevresel kaynaklardan ve mastitislerden izole edilen etkenlerin, virulens özelliklerinin araştırılması oldukça önemlidir. Bu çalışma konusunun belirlenmesinde ve çalışmaların yürütülmesinde, yardım ve desteklerini esirgemeyen değerli danışman hocam Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı öğretim üyesi Sayın Prof. Dr. Müjgan İZGÜR başta olmak üzere, tez izleme komitesindeki hocalarım Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı öğretim üyesi Prof. Dr. Mehmet AKAN ve Ankara Üniversitesi Veteriner Fakültesi Doğum ve Jinekoloji Anabilim Dalı öğretim üyesi Prof. Dr. Rıfat VURAL a, çalışmalarım boyunca katkılarını esirgemeyen Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı Başkanı Sayın Prof. Dr. Nejat AYDIN a, Mikrobiyoloji Anabilim Dalı nın değerli öğretim üyeleri Prof. Dr. K. Serdar DİKER, Prof. Dr. Hakan YARDIMCI, Prof. Dr. Ömer M. ESENDAL ve Doç. Dr. Barış SAREYYÜPOĞLU na, Ankara Üniversitesi Viroloji Anabilim Dalı öğretim üyesi Prof. Dr. Aykut ÖZKUL a, Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı araştırma görevlilerine, doktora ve yüksek lisans yapan arkadaşlarıma, çalışmalarım sırasında sonsuz özveri ile yanımda olan babam Kadir TOSUN, annem Melahat TOSUN, kardeşim Canan TOSUN ve eşim Ferhat DİNÇ e teşekkürlerimi sunarım.
7 vi SİMGELER VE KISALTMALAR APEC bp CaCl 2 CMT CNF cnf1 ColV DAEC DNA EaggEC EHEC EIEC EMB EPEC ETEC fim g HA hlya IL iucd KH 2 PO 4 L LB LPS LT ma mg MgCl 2 Avian Patojenik E. coli base pair Kalsiyum klorür California Mastitis Test Sitotoksik Nekrotizan Faktör Sitotoksik Nekrotizan Faktör 1 i kodlayan gen Kolisin V Diffuz adherent E. coli Deoksiribonükleik asit Enteroagregatif E. coli Enterohemorajik E. coli Enteroinvaziv E. coli Eosine Methylen Blue Enteropatojenik E. coli Enterotoksijenik E. coli Tip 1 fimbriaları kodlayan gen Gram Hemaglütinasyon Alfa-hemolizini kodlayan gen İnterleukin Aerobaktin demir elde etme sistemi ile ilişkili gen Potasyum hidrojen fosfat Litre Luria Bertani Lipopolisakkarit Labil toksin Miliamper Miligram Magnezyum klorür
8 vii MgSO 4 Magnezyum sülfat ml Mililitre mm Milimetre mm Milimolar MnCl 2 Mangan klorür MRHA Mannoz dirençli hemaglütinasyon MSHA Mannoz duyarlı hemaglütinasyon µl Mikrolitre µm Mikromolar Na 2 HPO 4 Di-sodyum hidrojen fosfat NaCl 2 Sodyum klorür NH 4 Cl Amonyum klorür NMEC Neonatal Meningitis E. coli NTEC Nekrotoksijenik E. coli pap P fimbriaları kodlayan gen PBS Pepton Buffer Saline PCR Polimerase Chain Reaction PMN Polimorf Nüklear pmol Pikomol rpm Revolution per minute (dakikadaki devir) ST Stabil Toksin SLT Shiga-Like Toksin TBE Tris Borat EDTA TNF-α Tümör Nekrozis Faktör-alfa trat TraT proteinlerini kodlayan gen TSA Tripticase Soy Agar TSB Tripticase Soy Broth UPEC Üropatojenik E. coli Vero Yeşil Maymun Böbrek Hücresi VP Voges Proskauer VT Verotoksin VTEC Verotoksijenik E. coli
9 viii ŞEKİLLER Şekil 3.1.a. Vero hücrelerin normal görünümü (x20) 43 Şekil 3.1.b. Toksinden etkilenen Vero hücreleri (x20) 43 Şekil 3.2. PCR sonucunda jel elektroforezde hlya pozitif için örnek görüntü 46 Şekil 3.3. PCR sonucunda jel elektroforezde fimh pozitif için örnek görüntü 47 Şekil 3.4. PCR sonucunda jel elektroforezde papef pozitif için örnek görüntü 47 Şekil 3.5. PCR sonucunda jel elektroforezde iucd pozitif için örnek görüntü 48 Şekil 3.6. PCR sonucunda jel elektroforezde trat pozitif için örnek görüntü 48 Şekil 3.7. PCR sonucunda jel elektroforezde cnf 1 pozitif için örnek görüntü 49
10 ix ÇİZELGELER Çizelge 1.1. Patojenik E. coli suşlarının klasifikasyonu 17 Çizelge 2.1. İncelenen süt örnekleri ile ilgili bilgiler 29 Çizelge 2.2. İncelenen rektal svap ve altlık örnekleri ile ilgili bilgiler 30 Çizelge 2.3. Primerlerlerin baz dizileri, bağlandıkları spesifik gen bölgeleri, 38 PCR ürünlerinin uzunlukları ve primerlerin alındığı kaynaklar Çizelge 3.1. İncelenen süt örneklerinde E. coli izolasyon bulguları 40 Çizelge 3.2. İncelenen rektal svap ve altlık örneklerinde E. coli izolasyon bulguları 41 Çizelge 3.3. İncelenen E.coli suşlarında virulens faktörlere ait fenotipik bulgular 41 Çizelge 3.4. E. coli suşlarının izole edildikleri materyal ve kullanılan eritrosit 42 türüne göre MSHA ve MRHA bulguları Çizelge 3.5. İşletme A için fenotipik test sonuçları 44 Çizelge 3.6. İşletme B için fenotipik test sonuçları 45 Çizelge 3.7. PCR sonuçları 46 Çizelge 3.8. İşletme A için moleküler test sonuçları 49 Çizelge 3.9. İşletme B için moleküler test sonuçları 50 Çizelge Fenotipik olarak ve PCR ile incelenen özellikler ve yüzdeleri 52
11 1 1. GİRİŞ 1.1. Tarihçe Escherichia coli nin yazılı bilimsel tarihi 1885 yılında ilk olarak pediyatrist ve bakteriyolog olan Theodor Escherich tarafından tanımlanması ile başlamıştır. Bir çocuğun dışkısından izole edilen etken diyareye neden olduğu için Bacterium coli commune olarak tanımlanmış ve etken 1958 yılında Theodor Escherich e ithafen resmi olarak Escherichia coli adını almıştır (Kuhnert ve ark., 2000; Manning, 2005). Mastitisli sütlerde ise, E. coli nin ilk kez 1896 yılında izole edildiği ve 1903 yılında Kitt adlı bir araştırmacı tarafından meme kanalına E. coli verilmesi ile deneysel olarak infeksiyon oluşturulduğu bildirilmiştir lı yılların sonuna dek İngilteredeki subklinik ve klinik mastitis olgularına Staphylococcus aureus ve Streptococcus agalactiae etkenlerinin yol açtığı ve bu etkenlere karşı beş nokta planı harekete geçirilerek infeksiyonların kontrol altına alındığı, ancak bu planın koliform mastitisleri önlemede işe yaramadığı ve 1960 lı yıllardan itibaren E. coli mastitislerinin insidensinin artmasıyla E. coli nin ölümcül mastitislerin en genel nedeni olduğu açıklanmıştır (Jones, 1999). Barrow ve Hill (1989), İngiltere ve Galler de yaptıkları çalışmalarda mastitis olgularının %90 ından, E. coli izole etmişlerdir. Yine 1995 yılında Hollanda da yapılan bir çalışmada E. coli nedenli mastitis olguları %27,71 oranında saptanmıştır (Lipman ve ark., 1995). Ülkemizde ise, Arda ve İstanbulluoğlu (1978) tarafından yapılan çalışmada sığırlarda E. coli mastitisleri %10,4 oranında saptanırken, yapılan bir başka çalışmada Ateş ve ark. (1991) mastitis olgularından %1,2 oranında E. coli izole ettiklerini açıklamışlardır. Kaya ve ark. (1993) tarafından yapılan çalışmada E. coli nedenli mastitis oranı %23,58 olarak saptanmış ve 2000 yılında yapılan bir çalışmada ise, sığır mastitislerinin %16,4 ünden koliform bakteri izole edildiği bu bakterilerin ise %91,9 unun E. coli olduğu bildirilmiştir (Bülbül, 2000).
12 2 1.2 Etiyoloji E. coli Bacteria aleminin, Proteobacteria bölümü, Gamma proteobacteria sınıfı, Enterobacteriales takımı, Enterobacteriaceae ailesi, Escherichia cinsi içerisinde yer alan ve prokaryotlar içerisinde çok iyi tanımlanarak sayısız biyokimyasal, biyolojik ve biyoteknolojik çalışmada model olarak kullanılabilen bir bakteri türüdür. (Scheutz ve Strockbine, 2005; Han ve Lee, 2006). E. coli düzgün, silindirik, µm x µm boyutlarında Gram negatif çomak şekilli, sporsuz, aerob veya fakültatif anaerob ve genellikle peritrik flagellaya sahip hareketli bir bakteridir. E. coli suşlarında kapsül veya mikrokapsül sıklıkla mevcuttur ve E. coli ph değerlerinde ürer. Sıvı besiyerinde hızlı üreyerek kısa sürede bulanıklık oluşturan E. coli nutrient agar, kanlı agar ile bazı selektif ve diferensiyel besiyerlerinde 37 C de 24 saatte gözle görülebilir S tipli koloniler oluşturur (Sussman, 1997; İzgür, 1999; Scheutz ve Strockbine, 2005). En önemli özelliği laktozu fermente edebilme yeteneği olan E. coli, laktozu fermente ederek MacConkey (MC) besiyerinde pembe koloniler oluştur. Ayrıca E. coli, identifikasyonunda kullanılan Eosin-methylene blue (EMB) agarda koyu yeşil-siyah metalik parıldama meydana getirir. Bazı E. coli suşları için Kanlı agarda hemoliz karakteristik bir özelliktir (Quinn ve ark., 2002). E. coli nin diğer Enterobakterilerden ayrımında çeşitli moleküler ve biyokimyasal özelliklerinden de yararlanılır. E. coli de % G+C oranı dir. E. coli İndol üretimi, Metil Red testi, Katalaz testi, Lizin dekarboksilaz üretim testi ve ß-galaktosidaz testinde pozitiftir. Üreaz aktivitesi, Triple Sugar Iron (TSI) Agarda H 2 S üretimi, Oksidaz testi, Voges Proskauer testi ve sitrattan yararlanım özelliği negatiftir. E. coli nitratı nitrite indirger. Glikoz, laktoz, D-mannitol, D-mannoz, D- sorbitol, L-arabinoz, D-ksiloz, maltoz, trehaloz, ramnoz gibi karbonhidratları asit ve gaz oluşturarak ayrıştırır (Koneman ve ark., 1992; Sussman, 1997; Quinn ve ark., 2002).
13 3 E. coli nin antijenik yapısı oldukça komplike olup, özellikle patojen suşlarda bu yapılar önem kazanmaktadır. E. coli yüzey antijenlerine göre sınıflandırılan çok sayıda serotipe ayrılır. Fakat hücre duvarının iç tabakası tüm E. coli serotiplerinde ortaktır ve Enterobacteriaceae familyasında genel bir özelliktir (İzgür, 1999; Burvenich ve ark., 2003). Kauffman tarafından 1944 yılında E. coli serolojik klasifikasyon şeması hazırlanmıştır ve günümüzde modifiye şekli kullanılmaktadır. Modifiye Kauffman şemasına göre E. coli O (somatik), H (flagellar) ve K (kapsüler) yüzey antijen profillerine göre serotiplendirilmiştir. Toplam 170 farklı O antijeni tanımlanmıştır. K antijenlerinin varlığı bakteriyel aglütinasyon testleri ile saptanmıştır. O antiserumu ile aglütine edilemeyen E. coli suşlarının kültürün ısıtılması ile aglütine edilebilir hal aldığında K antijeninin varlığı anlaşılmıştır. Moleküler yapıların ortaya konulmasıyla K yüzey antijeninin yalnızca asidik polisakkaritleri içerdiği belirlenmiş ve böylece protein yapıdaki fimbrial antijenler bu gruptan çıkarılarak F antijenler olarak tanımlanmışlardır E. coli suşlarının O, H, K antijenlerine göre 700 ün üzerinde antijenik tipi veya serotipi saptanmıştır (Orskov ve Orskov, 1985; Nataro ve Kaper, 1998, Kaper ve ark., 2004; Baylis ve ark., 2006). E. coli nin somatik O antijenleri lipopolisakkarit kompleksleri olup termostabil özellikte yüzey antijenleridir. E. coli lerin serotiplendirilmesinde önem taşırlar. Makro veya mikro aglütinasyon testleri ile ortaya konulabilirler. Ancak, kapsüler ve fimbrial antijenlere sahip E. coli lerde, somatik antijenlerin ortaya konulması güçlük yarattığından, bu suşların 120 C de 2 saat ısıtıldıktan sonra aglutinasyona tabi tutulmasında yarar vardır (Gaastra ve Graaf, 1982; İzgür, 1999). Flagellar H antijenleri protein yapısındadırlar. Isıya dayanıksızdırlar ve 100 C de inaktive olurlar. H antijenleri aglutinasyonla ortaya konulabilen antijenler olup hareketli E. coli suşlarında bulunurlar (Gaastra ve Graaf, 1982; İzgür, 1999). Kapsüler K antijenleri çoğunlukla asidik polisakkarit özellikte olup, kapsül taşıyan E. coli suşlarında somatik O antijenlerinin üzerinde bulunurlar. Bu nedenle K antijeni bulunduran suşlar, O antiserumları ile aglutine olmazlar. K
14 4 antijenleri, 120 C de 2 saat içerisinde tahrip olan K(A) antijenleri ve 100 C de tahrip olan K (B) antijenleri olmak üzere iki önemli komponentten oluşur (Gaastra ve Graaf, 1982; İzgür, 1999). Fimbrial antijenler (pilus antijenleri), fimbrialarda bulunan protein yapısında antijenlerdir. Bu antijenler de K antijenleri gibi bir suşun O antijenine göre identifiye edilmesini önlerler. Fimbrialar E. coli lerde virulens faktör olarak kabul edilirler ve hemaglütinasyon özelliklerine göre E. coli lerin Mannoz sensitif-ms veya Mannoz rezistan-mr olarak ayrılmasını sağlarlar (İzgür, 1999). E. coli insanlarda ve hayvanlarda normal bağırsak florasının bir üyesi olarak kabul edilen bir bakteridir. (Burvenich ve ark., 2003; Kaper ve ark., 2004). Ancak bazı suşlar patojenik özelliklere sahiptirler. Patojenik ve nonpatojenik E. coli suşları arasındaki temel fark ise patojenik suşların çeşitli virulens faktörlere sahip olmasıdır (China ve Goffaux, 1999) E. coli nin Virulens Faktörleri E. coli patojenitesi, patotipe göre değişen ve çok sayıda virulens faktörü içeren kompleks, multi-faktöriyel bir mekanizmadır. Patojenik E. coli suşları neden oldukları hastalık tipine ve infekte ettikleri hayvan türüne spesifiktirler ve spesifik hastalıkların patogenezinde sahip oldukları virulens faktörlerinin önemli rolü vardır. Çünkü patojenik E. coli suşları ile konak organizma arasındaki ilişki bakteri tarafından sentezlenen virulens faktörlerin varlığına bağlıdır (China ve Goffaux, 1999; İzgür, 1999; Kuhnert ve ark., 2000). Virulens faktörleri kodlayan genler, bakteri genomunda veya plazmidlerde bulunurlar. Virulens faktörler konağı infekte etmede, konağın savunma sistemi ile savaşmada ve kolonizasyonda rol oynarlar. Özellikle ekstraintestinal infeksiyonların şekillenmesinde mukozal yüzeylere kolonizasyon, epitel hücre tabakasını geçiş, komplementin bakterisidal etkisine direnç, fagositozdan kurtulma ve canlı kalarak çoğalma yeteneği önemlidir (Harel ve ark., 1993; Le Bouguenec ve Bertin, 1999).
15 5 Ancak bakteriler sürekli olarak virulens faktörleri sentezlemezler, yalnızca çevreden veya konakçıdan ilgili sinyalleri aldıkları zaman sentezlerler. Yapılan çalışmalarla, in vitro olarak virulens gen ekspresyonunu uyaran faktörler saptanmıştır. Bu faktörlere örnek olarak sıcaklık, ozmolarite, ph, nitrojen, demir, şeker ve aminoasit konsantrasyonları verilebilir (Lehtolainen, 2004). E. coli suşlarına ait virulens faktörlerin ana grubunda adhezinler, toksinler, konak hücrelerine salınan proteinler, polisakkarit kapsül, komplement tarafından öldürülmeye direnç ve aerobaktin sideroforları gibi çeşitli faktörler vardır (Harel ve ark., 1993; China ve Goffaux, 1999) Adhezinler Patojenik mikroorganizmalar kendilerini korumak ve konakçı bariyerlerini aşmak için çeşitli ortak yollara sahiptirler. Bu yolların ilk aşaması mikroorganizmanın konak hücreye sıkı bir şekilde yapışması yani adhezyondur. Adhezyon, bakteri hücrelerinin kolonizasyonu ve infeksiyonun oluşumunda büyük önem taşımaktadır Bakterilerin ökaryotik hücrelere adhezyon yeteneği, konakçı dokularına kolonizasyon için oldukça gerekli bir özelliktir. Birçok patojenik organizma için adherens, epitelyal hücre yüzeylerine başarılı bir kolonizasyon açısından kommensal mikroorganizmalar ile rekabette büyük bir öneme sahiptir (Gaastra ve Graaf, 1982; Clegg ve Gerlach, 1987). Mikroorganizmalar konakçı sekresyonlarındaki immun ve immun olmayan engelleri aştıktan sonra mukoza yüzeyini yıkayan sekresyonlar ile uzaklaştırılmaktan kurtulmak için hücre epitellerine bağlanmalarının yanısıra burada üreyerek epitel hücrelerinin dökülmesiyle uzaklaştırılan bakterilerin yerlerine yeni bakterilerin yapışmasını sağladıklarından adhezyon patojenite yönünden önem taşımaktadır. Patojenik mikroorganizmalar konak dokularına bağlanarak idrar, kan, bağırsak içeriği vb. sekresyonların etkisinden kurtulurlar ki bağlanma işlemi mukozal yüzeylere kolonizasyon için gerekli ilk basamaktır (Johnson, 1991; Bülbül, 2000).
16 6 Bakteri konak hücreye adhezyon ve kolonizasyon için adhezinlere ihtiyaç duyar. Konak hücrelere kolonizasyon bakteri yüzeyindeki adhezinlerle sağlanır ki bu adhezinler konak hücre yüzeyindeki spesifik reseptörleri tanıma ve bağlanma özelliğindedirler. Fimbria bakteri ile konakçı hücre arasında teması sağlar, fimbrianın distalinde yer alan ve adhezin olarak tanımlanan protein yapı ise konak hücre üzerindeki reseptörlere bağlanarak adhezyonu gerçekleştirir. Adhezinler fimbria üzerinde yer alabildiği gibi direkt mikroorganizma üzerinde yer alan afimbrial adhezinler de mevcuttur. Sığırlarda infeksiyona neden olan E. coli suşlarında çok sayıda farklı adhezin saptanmıştır (Le Bougenic ve Bertin, 1999; Soto ve Hutgren, 1999; Wizeman ve ark., 1999). E. coli suşlarına ait fimbrialar hemaglütinasyon özelliklerine göre Tip I ve Tip II olmak üzere iki gruba ayrılırlar. Hemaglütinasyon aktivitesi D-mannoz varlığında inhibe edilen fimbrialar mannoz sensitif (Tip I / F1 ) fimbrialar olarak tanımlanırken hemaglütinasyon aktivitesinin D-mannoz ile önlenemediği fimbrialar mannoz rezistant (Tip II; P fimbria, S fimbria vb.) fimbrialar olarak adlandırılırlar (Johnson, 1991; İzgür, 1999) Tip 1 Fimbria: Patojenik ve patojenik olmayan E. coli suşlarının büyük bir çoğunluğu Tip 1 fimbriaya sahiptir (Gaastra ve Graaf, 1982). E. coli suşlarında tip 1 fimbrialar moleküler ağırlıkları olan polipeptid altünitelerden oluşan polimer özellikte ve bakteri yüzeyinden köken alan yaklaşık 1 µm uzunlukta flamentöz protein yapılardır. Tip 1 fimbrianın E. coli suşlarının memelilerin mukozal hücrelerine kolonizasyondaki rolü mannoz reseptör-ilişkili adherens şeklindedir. Tip 1 fimbria E. coli suşlarına çok sayıda farklı ökaryotik hücreye yani lökositlere, epitelyal hücrelere, bazı hayvan türlerine ait eritrositlere adhezyon özelliği sağlar. Tip I fimbria bulunan E. coli suşları α-d-mannoz bulunmayan ortamda kanatlı ve kobay eritrositlerini aglutine etme özelliği ile karakterizedirler (Clegg ve Gerlach, 1987; Bloch ve ark., 1992; Otto ve ark., 1999). Tip I fimbriaların özellikle bağırsak ve sidik kesesi epitel hücrelerine yapışma özelliği vardır ve bu durum E. coli suşlarının hastalık yapmasına yardımcı olur (Arda, 2000). Tip 1 fimbria FimA,
17 7 FimG, FimF ve FimH alt ünitelerinden oluşur ve tip I fimbrianın adhezyon özelliğinde rol oynayan fima geninin yanısıra 3 genin daha varlığı saptanmıştır. Bu genler fimf, fimg ve fimh genleri olarak tanımlanmıştır. Ayrıca ilgili gen ürünlerinin, üropatojenik E. coli suşlarında varlığı saptanan ve adhezyonda rol alan pape, papf ve papg gen ürünleri ile benzer oldukları da bildirilmiştir (Sokurenko ve ark., 1994; Schilling ve ark., 2001). Mastitisli sütlerden izole edilen E. coli suşlarında Tip 1 fimbrianın rolü hemaglütinasyon testleri ile araştırılmış ve bu konuda yapılan bir çalışmada mastitislerden izole edilen E. coli suşlarının %14 ünün sığır eritrositlerini hemaglütine ettiği saptanmıştır (Hogan ve ark., 1990) F17 Fimbria Ailesi: Son yıllarda evcil hayvanlarda ve insanlarda patojenik E. coli suşlarında F17 fimbria ailesinin varlığı saptanmıştır. F17 fimbria ailesi; sığırların enterotoksijenik E. coli suşu tarafından sentezlenen F17a, septisemik ve diyareli buzağı ve kuzulardan izole edilen E. coli suşlarının sentezlediği F17b, septisemik E. coli suşlarından izole edilen F17c ve sığır enterotoksijenik E. coli suşları ile diyareli buzağılardan izole edilen E. coli suşlarından sentezlenen F17d yi (F111 olarak da tanımlanır) içermektedir. Ayrıca insanlarda üriner sistem enfeksiyonuna yol açan E. coli suşlarında saptanan G fimbrianın da F17 fimbria ailesine ait olduğu saptanmıştır. Patojenik E. coli suşlarında F17 fimbrial adhezinler, genellikle diğer virulens faktörlerle (aerobaktin, serum dirençliliği, CNF2, K99, CS31A veya AFA adhezinler) ilişkilidirler. Ayrıca, F17 fimbrial adhezinleri kodlayan genlerin kromozomda lokalize olduğu bildirilmiştir (Bertin ve ark., 1996; Le Bouguenec ve Bertin, 1999). Çoğunlukla diyare ve septisemi olgularından izole edilen E. coli suşlarında saptanan F17 fimbria ailesinin, mastitisli ineklere ait sütlerden izole edilen E.coli suşları tarafından da eksprese edildiği bildirilmiştir. Ancak F17 fimbrianın mastitis patogenezindeki rolü tam olarak bilinmemektedir (Le Bouguenec ve Bertin, 1999).
18 P Fimbrialar, S Fimbrialar ve Çeşitli Spesifik Fimbrialar: Ekstraintestinal infeksiyonlara neden olan E. coli suşları tarafından eksprese edilen en önemli mannoz dirençli adhezinler P fimbrialardır (Soto ve Hultgren, 1999). Bu fimbrialar, üropatojenik suşlarla ilgili olan fimbria tipleridir ve pyelonefritisle ilişkili pilus (Pap) veya P fimbria olarak tanımlanırlar. P fimbrialar insanlarda ve köpeklerde UPEC suşları tarafından sentezlenirken, buzağı ve domuzlarda diyare ve septisemilere neden olan F165-1 olarak adlandırılan suşlar tarafından sentezlenirler. P fimbria, böbrek ve sidik kesesindeki tüm önemli epitelyal ve endotelyal yüzeylere adherensi sağlar. P fimbrialar pyelonefritis, ürosepsis ve sistitis şekillenmesinde rol oynarlar. S, P fimbrialar ve X adhezinler, genellikle insanlarda üriner sistem infeksiyonlarına yol açan E. coli suşlarında saptanmıştır. Üriner sistem infeksiyonlarında etkenin üroepitelyal hücrelere adhezyonu infeksiyon patogenezinde en önemli olgudur. Bu fimbriaların bakterinin üriner kanal epiteline adherensi için gerekli olduğu ve infeksiyonun tekrarlanmasında rol oynadıkları düşünülmektedir (Korhonen ve ark., 1988; Blanco ve ark., 1992; Mainil ve ark., 1997). P fimbrianın F7-1, F7-2 ve F8 den F16 ya kadar tanımlanan 11 farklı serolojik tipinin olduğu bildirilmiştir. P fimbrianın özellikle E. coli O1, O4, O6, O18 serotiplerinde bulunduğu anlaşılmıştır (Johnson ve ark., 2000). Ayrıca Blanco ve ark. (1992), yaptıkları bir çalışma ile P fimbriaya sahip E. coli suşlarının α-hemolizin ve CNF üretimine göre Hly + CNF +, Hly + CNF - ve Hly - CNF - olmak üzere üç gruba ayrıldığını saptamışlardır. S fimbria ise mannoz dirençli adhezinlerden olup üriner sistem infeksiyonları ve daha ziyade neonatal sepsis, meningitis ve bakteriyemilerde rol oynar (Korhonen ve ark., 1988; Siitonen, 1992). S ve P fimbriaları kodlayan genlerin (sırasıyla sfa operonu ve pap/prs operonları) kromozom üzerinde lokalize olduğu saptanmıştır (Daigle ve ark., 1994; Mainil ve ark., 1997). Ayrıca E. coli suşlarının K88, K99, 987P, F41, CFA1, CS1, CS2, CS4, CS14, CS17, CS19 fimbrialar gibi bazı spesifik fimbria türlerine ve dolayısıyla fimbrial adhezinlere de sahip olabildikleri bildirilmiştir (Soto ve Hultgren, 1999; Le Bougenic ve Bertin, 1999).
19 Afimbrial Adhezinler (AFA); Adhezinler, fimbria ya da pilus olarak bilinen yapılar üzerinde yer alabildiği gibi hücre yüzeyi ile ilişkili olan afimbrial adhezin özelliğinde de olabilirler. Bu yapılar hücre yüzeyinde ince bir ağ görünümünde, bobin benzeri sarmal yapıda veya bir flamentöz kapsüler kaplama şeklinde gözlenebilirler. Afimbrial adhezinler (AFA), hücre kültürlerine diffuz adherensi sağlayan, farklı afa genleri tarafından kodlanan polipeptid özellikteki yapılardır. Sığırlardan izole edilen E. coli suşlarında afa-7 ve afa-8 genleri belirlenmiş ve afa-8 geninin afa-7 geninden daha fazla bulunduğu saptanmıştır (Johnson, 1991; Mainil ve ark., 1997; Lalioui ve ark., 1999). F17c ve sitotoksik nekrotizan faktör 2 (CNF2) yi kodlayan genleri taşıyan plazmidlerin üzerinde afa-8 genlerinin de bulunduğu belirlenmiştir (Bertin ve ark., 1996; Le Bougenic ve Bertin, 1999). Kaipainen ve ark. (2002), klinik mastitis olgularından izole ettikleri E. coli suşlarında Afa8 i saptamışlar ve bu suşların aynı zamanda F17 fimbriaya ve CNF2 ye de sahip olduklarını bildirmişlerdir. Bir diğer afimbrial adhezin ise sığır patojenik E. coli suşlarında bulunmuştur ve kapsül benzeri olan yapı CS31A adhezin olarak adlandırılmıştır. CS31A adhezin, septisemili veya diyareli buzağılarda tanımlanmıştır. (Bertin ve ark., 1996; Le Bougenic ve Bertin, 1999). CS31A adhezinin özellikle F17c fimbria ile ilişkili olduğu ve CS31A adhezini kodlayan genlerin aerobaktin üretimi, antimikrobiyal dirençlilik gibi diğer virulens faktörleri de kodlayan genleri taşıyan büyük plazmidlerin üzerinde yer aldığı belirlenmiştir (Bertin ve ark., 1998) Curli Fimbrialar; Birçok klinik E. coli suşu ince, uzun, düzensiz ve hücre yüzeyinde yüksek oranda kümelenmiş ve curli olarak tanımlanan yapılara sahiptirler. Curli fimbrialar konak hücrelerdeki fibronektin, plazminojen gibi çeşitli proteinlere bağlanmada rol oynarlar. Curli fimbrialar son derece stabil yapılardır ki depolarizasyonları için kimyasal uygulama gerekir. E. coli suşlarına ait olan curli fimbriaların ana komponenti 15.3 kda lık protein olan CsgA dır. CsgB ise minor komponent olarak curli fimbriaların yapısında yer alır (Soto ve Hultgren, 1999; Pawar ve ark., 2005). Curli fimbriaların ilk olarak 1989 yılında yapılan bir çalışma ile sığır mastitislerinden izole edilen E. coli suşlarında saptandığı bildirilmiştir (Ryu
20 10 ve ark., 2004). Curli fimbriaların bakterinin adhezyon ve kolonizasyon yeteneğini, çeşitli immunolojik yolları aktive edebileceği, inflamasyonu ve klinik bulguların şiddetini arttırabileceği düşünülmüştür (Dyer ve ark., 2007). Karczmarczyk ve ark. (2008), yaptıkları bir çalışma ile mastitisli sütlerden izole edilen E. coli suşlarının hem aerobik hem de anaerobik şartlarda oda sıcaklığı ve daha yüksek sıcaklıkta curli fimbria sentezleyebildiğini saptamışlar ve bu fimbriaların sığır mastitislerinin patogenezinde rol oynayabileceklerini düşünmüşlerdir Toksinler Patojenik E. coli suşları, farklı aktivitelere sahip toksinler üretebilmektedirler ve E. coli suşları ekzotoksinler ve endotoksinler olarak sınıflandırılan toksinleriyle patolojik etkilere neden olurlar. Mikroorganizmalar tarafından bağırsakta üretilen toksinler enterotoksinler olarak tanımlanırlar (Bülbül, 2000). Enterotoksinler genellikle buzağı, kuzu, domuz yavrusu gibi genç hayvanlarda bağırsak infeksiyonlarına neden olan E. coli suşları tarafından sentezlenirler (İzgür, 1999). İnsan ve hayvanlarda hastalıklara yol açan toksijenik E. coli suşları Enterotoksijenik E. coli suşları (ETEC), Verotoksijenik E. coli suşları (VTEC) ve Nekrotoksijenik E. coli suşları (NTEC) olarak üç grupta incelenirler (Blanco ve ark., 1997). Enterotoksijenik suşlar, patogenezde önemli rol oynayan ısıya dayanıklı stabil toksin (ST) ve ısıya duyarlı labil toksin (LT) olmak üzere temel iki grup enterotoksin üreterek çocuklarda, buzağılarda, domuz yavrularında, kuzularda diyareye yol açarlar ve bu toksinler diyarenin ana nedenidirler. Isıya duyarlı toksinleri LTI ile LTII ve ısıya dayanıklı toksinleri STIa, STIb ve STII genetik, antijenik ve fonksiyonel olarak iyi bir şekilde nitelendirilmişlerdir (Blanco ve ark., 1997; Nataro ve Kaper, 1998). Verotoksijenik suşlar, Verotoksin (VT) üretirler ki bu toksine Shiga benzeri toksin (SLT) de denilir. Verotoksin, O157:H7 serotipindeki enterohemorajik E. coli suşları ve bazı enteropatojenik E. coli suşları tarafından üretilir. Verotoksijenik E. coli suşları insanlarda diyare, hemorajik kolitis, hemolitik üremik sendrom ve trombositopenik purpuraya neden olurken, hayvanlarda diyare ve ödem hastalığına
21 11 yol açarlar. Verotoksinler VT1, VT2 ve VT2 varyantları (VT2v, vtx2ha, vtx2hb) şeklinde antijenik, genetik ve fonksiyonel olarak üç grupta incelenmişlerdir (Blanco ve ark., 1990; Nataro ve Kaper, 1998). Nemeth ve ark. (1994), sığır mastitislerinden izole ettikleri E. coli suşlarının yalnızca %8 inin vero hücrelerde toksik etki gösterdiğini saptamışlardır. Nekrotoksijenik E. coli suşları (NTEC) ise hücre nekrozuna neden olan sitotoksik nekrotizan faktörleri (CNF) sentezlerler (Blanco ve ark., 1992) li yıllarda yapılan bir çalışma ile E. coli S5 suşunda plazmid tarafından kodlanan ve Vir toksin olarak tanımlanan bir toksinin saptandığı bildirilmiştir (Pohl ve ark., 1993). Caprioli ve ark. (1983), enteritli bebeklerden izole ettikleri E. coli suşlarının tavşan dokularında nekrotik lezyonlara yol açan bir toksine sahip olduğunu saptamışlar ve bunu sitotoksik nekrotizan faktör (CNF) olarak tanımlamışlardır. Ancak daha sonraları Vir toksin ve CNF ün aynı etkiyi gösterdiği ve serolojik olarak ilişkili olduğu anlaşılarak CNF ü CNF1, Vir toksini ise CNF2 olarak tanımlamışlardır (Caprioli ve ark., 1983; Pohl ve ark., 1993). CNF1 pozitif suşlar özellikle ekstraintestinal infeksiyonlardan izole edilmişlerdir ve bu suşlar genellikle hemolitik olup P ve S fimbria aileleri veya Afa ailesi adhezinleri yönünden de pozitiftirler (Mainil ve ark., 1997; Kaipainen ve ark., 2002). CNF1 üreten E. coli suşlarının insanlarda enteritis, nefritis, septisemi; ineklerde ve domuzlarda diyare; boğalarda septisemi; kedi ve köpeklerde üriner sistem infeksiyonlarında saptandığı bildirilmiştir. Ayrıca sığır E. coli suşlarında CNF1 in CNF2 den daha az yaygın olarak bulunduğu saptanmıştır. CNF2 üreten E. coli suşlarının ise özellikle sığırlarda yaygın olduğu, sığır ve kuzularda enterit ve septisemilere neden olduğu anlaşılmıştır (Pohl ve ark., 1993, Kaipainen ve ark., 2002). CNF2 üreten E. coli suşlarının birçoğunun ayrıca F17b fimbria ve aerobaktin de sentezlediği ve serumun öldürücü etkisine karşı dirençli olduğu saptanmıştır. CNF1 üretimi kromozom tarafından kodlanırken, CNF2 yi kodlayan genler Vir plazmidi üzerinde lokalize olmuştur (Falbo ve ark., 1993; Mainil ve ark., 1997; Mainil ve ark., 1999). CNF pozitif suşların pneumoni, metritis, abortus ve mastitis olgularından da izole edildiği bildirilmiştir (Pohl ve ark., 1993). Lipman ve ark. (1995), sığır mastitislerinden izole ettikleri E. coli suşlarında LT ve ST1 toksinlerini kodlayan genlerin varlığını ve
22 12 CNF1 ile CNF2 üretimini araştırmışlar, ancak yalnızca bir E. coli suşunun CNF1 ürettiğini belirlemişlerdir. E. coli suşlarında patojenitede önemli rol oynayan faktörlerden birisi de endotoksin veya lipopolisakkarittir (LPS). LPS, toksik özelliği sağlayan Lipid A ve "O" antijen olarak tanımlanan polisakkarid üniteden oluşur (Burvenich ve ark., 2003). Gram negatif bakterilerde, konakçıda hasara yol açan temel virulens faktör endotoksindir. Endotoksin, hem toksik bir bileşiktir hem de konağın savunma mekanizmasını indükler. Endotoksin bakteri öldüğünde açığa çıkarak inflamatuvar yanıtı başlatır. Ruminantlarda patofizyolojik etkileri doza bağlı olup, metabolik ve klinik belirtilerin çeşitliliğine yol açar. Klinik mastitislerde anoreksi, ateş, dehidrasyon, diyare ve süt üretiminde azalma gibi belirtilerin direkt ya da dolaylı olarak endotoksinin sistemik veya lokal etkisi sonucu olduğu bildirilmiştir. Koliform mastitisler, kan-süt bariyeri hasar gördüğünde bakteriyemi ve septisemiye neden olabilir. Septisemi ile sonuçlanan koliform mastitislere nadiren rastlanır fakat septisemi şekillenmiş ise çoğunlukla ölümle sonuçlanır (Diker, 1984; Hogan ve Smith., 2003). Ayrıca endotoksinin meme içerisine infüzyonunun E. coli infeksiyonu ile karşılaştırıldığında benzer semptomlar meydana getirdiği ve dahası LPS nedenli mastitislerin, hızlandırılmış biyolojik yanıta neden olması ile karakterize olduğu da bildirilmiştir (Diez-Fraile ve ark., 2002) Aerobaktin Demir Elde Etme Sistemi Birçok enterik bakteride özelikle, invaziv hastalıklarla ilişkili olanlarda, ikinci bir siderofor olarak aerobaktin bulunmaktadır (Payne, 1988; Harel ve ark., 1993). Bu hidroksimat, ilk olarak Aerobacter aerogenes suşlarında bildirilmiştir. Daha sonra ise, Shigella flexneri, E. coli, Salmonella spp., Klebsiella spp, Enterobacter spp., Citrobacter spp., Proteus spp., Serratia spp. ve Morganella spp. de identifiye edilmiştir. Aerobaktin iki lizin ve bir sitrat molekülünden oluşan, moleküler ağırlığı küçük olan bir moleküldür (Johnson, 1991). Aerobaktin basit bir genetik sistem tarafından kodlanmaktadır ve biyosentezi için dört gen (iuca, iucb, iucc, iucd) gereklidir Biyosentez iucd ürünü tarafından lizinin oksidasyonu ile başlar.
23 13 Hidroksilizinin asetilasyonu ise iucb nin fonksiyonudur. iuca ve iucc, iki asetilhidroksilizin yan zincirinin sitrata bağlanmasını katalize eden sentetazın alt ünite genleridir. Aerobaktin ile ilişkili olan beşinci gen (iuta) ise dış membran reseptörünü kodlar ve bu reseptör E. coli de Da büyüklüğündedir. Aerobaktin ile ilgili olan bu beş gen tek bir operon üzerindedir ve E. coli de aerobaktin sentezi fur lokusu tarafından kontrol edilir. Bazı Salmonella spp., Shigella spp. ve enteroinvaziv E. coli izolatlarında ilgili genlerin kromozomal yerleşimli olduğu bildirilmiştir. Ayrıca, aerobaktin genleri plazmid tarafından da kodlanabilmektedir. ColV ve F1me plazmidleri üzerinde bu genler saptanmıştır (Payne, 1988). Virulenste demir transport sistemlerinin rolü ColV plazmidi taşıyan E. coli suşlarında anlaşılmıştır. En erken 1949 yılında E. coli suşlarında kolisin V üretimi ile virulens arasında bir korelasyonun olduğu biliniyordu. Araştırıcılar yaptıkları çalışmalarla ColV plazmidi kaybının suşları ColV + suşlara göre daha az patojen bir hale getirdiğini saptamışlardır (Payne, 1988). Aerobaktin varlığı, özellikle çiftlik hayvanlarında ekstraintestinal infeksiyonlara, kanatlılarda koliseptisemilere, insanlarda ürosepsis, pyelonefritis ve sistitislere neden olan etkenlerde saptanmıştır (Payne, 1988; Harel ve ark., 1993). Ayrıca, hayvanlarda aerobaktin sentezleyen üropatojenik E. coli suşlarının, üretmeyen suşlara göre daha letal etkili olduğu bildirilmiştir (Zhang ve Normark, 1996). Aerobaktin varlığının sığır mastitislerindeki rolü üzerine çeşitli çalışmalar yapılmıştır. Örneğin, Nemeth ve ark. (1994), mastitis olgularından izole ettikleri E. coli suşlarının %20 sinde aerobaktin varlığını saptamışlardır. Kaipainen ve ark. (2002), mastitise neden olan Finlandiya orjinli E. coli suşlarının %11.3 ünde, İsrail orijinli E. coli suşlarının ise %4.4 ünde aerobaktin kodlayan geni saptamışlardır. Lehtolainen (2004), mastitisli ineklerden izole ettiği E. coli suşlarının %8.4 ünü aerobaktin pozitif olarak bulmuştur.
24 Serum Dirençliliği Serumun bakterisidal etkisinden kurtulma yeteneği önemli bir virulens faktördür ve patojenitede rol oynar. Plazmidlerin varlığı, polisakkarit kapsül, lipopolisakkarit O yan zincirin tipi ve yüzey proteinlerinin serum dirençliliği ile bağlantılı olduğu bildirilmiştir (Sanchez-Carlo ve ark., 1984; Montenegro ve ark., 1985). Serum dirençliliği, Gram negatif bakterilerde en çok çalışılan virulens faktörlerden birisidir. Serumun öldürücü etkisine karşı direnç, özellikle bakteri yüzeyindeki yapılarla ilişkilidir. Kapsül veya dış membran proteinlerinin (OmpA ve TraT gibi), komplement komponentlerine ve membran atak kompleksine karşı savunmada rol alarak öldürücü etkiyi önledikleri saptanmıştır (Lehtolainen, 2004). Kısacası, serum dirençliliği TraT ve iss proteinleri gibi plazmidler tarafından kodlanan dış membran proteinleri ile lipopolisakkarit, K1 kapsül antijeni gibi bir çok faktör ile bağlantılıdır (Barrow ve Hill., 1989; Nemeth ve ark., 1991). TraT, 25 kda molekül ağırlığına sahip bir yüzey lipoproteinidir ve TraT yi kodlayan trat geni büyük konjugatif plazmidler (IncF plazmidler) üzerinde bulunur. TraT nin, komplementin membran atak kompleksinin inhibisyonunda ve bakterinin fagositoza karşı direnç göstermesinde rol aldığı düşünülmüştür (Aguero ve ark., 1984; Montenegro ve ark., 1985). TraT ile birlikte çalıştığı düşünülen K1 kapsüler antijeni, E. coli suşlarını serumun öldürücü etkisinden korur. Yapılan bir çalışmada, K1 kapsüler antijen, özellikle ekstraintestinal infeksiyonlara yol açan E. coli suşlarının patogenezinde önemli bir virulens faktör olarak gösterilirken bu etkiyi bakteri hücreleri üzerine komplement hareketini bloke ederek sağladığı düşünülmüştür ve TraT proteininin insanlardan izole edilen E. coli suşlarında K1 kapsüler antijenin varlığı ile ilişkili olduğu bildirilmiştir (Montenegro ve ark., 1985). Ancak daha sonraları yapılan çalışmalarda ise, K1 in serum direnci yada trat geni ile bir ilişkisinin saptanamadığı açıklanmıştır (Nemeth ve ark., 1991; Lehtolainen, 2004).
25 15 Bazı araştırıcılar tarafından mastitise neden olan E. coli suşlarının virulensinde serum dirençliliğinin rolü araştırılmıştır. Sanchez-Carlo ve ark. (1984), akut mastitisli ineklerden izole ettikleri E. coli suşlarının virulensinde serum dirençliliğinin önemli olduğunu saptamışlardır. Barrow ve Hill (1989), mastitis olgularından izole ettikleri E. coli suşlarının %99 unun serum dirençli olduğunu ve dolayısıyla serum dirençliliğinin virulenste önemli rol oynadığını bildirmişlerdir. Nemeth ve ark. (1991), sığır mastitislerinden izole edilen E. coli suşlarının %64 ünün serum dirençli olduğunu bildirmişler ve yine Nemeth ve ark. (1994), yaptıkları bir diğer çalışmada sığır mastitislerinden izole edilen E. coli suşlarının %76 sının serum dirençli olduğunu saptamışlardır. Bülbül (2000), çalışmasında izole ettiği E. coli suşlarının %98.1 inin serum dirençli olduğunu saptayarak serum dirençliliğinin mastitis olgularında önemli bir virulens faktör olduğunu bildirmiştir Kolisin Aktivitesi E. coli suşlarının bazıları kolisin denilen bakteriyosinler sentezlerler. A dan V ye kadar isimlendirilmiş 20 ye yakın kolisin tespit edilmiştir. Fajlarla aynı ortak reseptörlere tutunarak da etkili olabilen bu kolisinler vasıtasıyla da E. coli suşları gruplandırılabilmektedirler (İzgür, 1999). Genellikle kolisin sentezleyen türler bu maddeyi sentezlemeyenlere antimikrobiyal etki gösterirler (İzgür, 1983). Genel olarak A ve B şeklinde iki gruba ayrılan, lipopolisakkarit protein komplekslerinden oluşan kolisinlerinlerin sentezi kolisinojenik faktörler olarak da adlandırılan plazmidler tarafından kontrol edilir. Kolisinler, bakteri yüzeyindeki özel reseptörlere bağlanarak etki ederler. Kolisinlerin bağlanması için özel reseptörleri olmayan bakteriler kolisin dirençli olarak adlandırılır. Duyarlı hücre ile kolisin arasındaki etkileşim, kolisin moleküllerinin hücre yüzeyine bağlanması, bu moleküllerin hücre duvarını geçmesi ve kolisin ile hücre içi yapılar arasındaki biyokimyasal tepkimeler olmak üzere üç aşamada gerçekleşir. Kolisinler DNA ve RNA yı tahrip ederek, glikojen sentezini durdurarak ve hücre duvarının lipid tabakasına etki ederek aktif transportu engellemek suretiyle etkilerini göstermektedirler (İzgür, 1983).
26 16 Çeşitli araştırmacılar tarafından mastitise neden olan E. coli suşlarında virulens özellik olarak kolisin üretiminin etkisi araştırılmıştır. Barrow ve Hill (1989), sığır mastitislerinden izole ettikleri 422 E. coli suşunun %18 inin kolisin ürettiğini ve bunlardan da %5 inin kolisin V ürettiğini saptamışlardır. Nemeth ve ark. (1994), yaptıkları çalışmada sığır mastitislerinden izole ettikleri E. coli suşlarının %14 ünün kolisin ürettiğini ve bunlardan da %6 sının kolisin V ürettiğini saptayarak kolisin üretiminin mastitis olgularında önemli bir virulens özellik olmadığını bildirmişlerdir. Bülbül (2000), çalışmasında izole ettiği E. coli suşlarının çok azının kolisin aktivitesi gösterdiğini saptayarak kolisin üretiminin mastitise neden olan E. coli suşları için virülens faktörü olarak önem taşımadığını açıklamıştır Kapsül polisakkaritleri E. coli suşlarında kapsül fiziksel, kimyasal, genetik ve mikrobiyolojik açıdan Grup1, 2, 3 ve 4 olmak üzere dört gruba ayrılmıştır. E. coli suşları kimyasal yönden farklı özellikte olan 80 in üzerinde kapsüler polisakkarit üretebilirler. Çoğunlukla UPEC ve NMEC suşlarında çok sayıda bulunurlar ve bu ekstraintestinal suşların virulensine önemli ölçüde katkı sağlarlar. UPEC ve NMEC suşlarında en çok bulunan kapsül tipi ise K1 ve K5 dir. Kapsül polisakkaritleri antifagositik aktiviteye sahiptirler ve bakteriyi serumun komplement aracılı öldürücü etkisinden korurlar (Kuhnert ve ark. 2000; Russo, 2002; Taylor ve Roberts, 2005). Nemeth ve ark. (1991), yaptıkları bir çalışmada mastitislerden izole ettikleri E. coli suşlarının %3 ünde K1 kapsül antijeninin varlığını saptamışlardır. Kaipainen ve ark. (2002) ise, klinik mastitislerden izole ettikleri suşlarda K1 ve K5 kapsül antijenlerinin varlığını araştırmışlar, fakat hiçbir suşta bu antijenlere rastlayamamışlardır. Patojenik E. coli suşları fenotipik özellikleri, neden oldukları hastalığın klinik belirtileri, patogenezleri, epidemiyolojileri, spesifik virulens faktörleri ve O:H serotipleri esas alınarak sınıflandırılmışlardır. Çeşitli özelliklerine göre tanımlanan
27 17 patojenik E. coli suşlarının klasifikasyonu Çizelge 1.1 de gösterilmiştir (Kuhnert ve ark., 2000; Quinn ve ark., 2002; Scheutz ve Strockbine, 2005). Çizelge 1.1. Patojenik E. coli suşlarının klasifikasyonu (Kuhnert ve ark., 2000; Quinn ve ark., 2002; Scheutz ve Strockbine, 2005). İntestinal patojenik E. coli suşları (IPEC) Patojenik E. coli suşları Ekstraintestinal patojenik E. coli suşları (ExPEC) Enteropatojenik E. coli (EPEC) Enterotoksijenik E. coli (ETEC) Enteroinvaziv E. coli (EIEC) Enteroagregatif E. coli (EaggEC) Diffuz adherent E. coli (DAEC) Verotoksijenik E. coli (VTEC/STEC) - Enterohemorajik E. coli (EHEC) Üropatojenik E. coli (UPEC) Neonatal meningitis E. coli (NMEC) Çeşitli ekstraintestinal infeksiyonlara yol açan E. coli suşları IPEC suşlarından olan EPEC ve ETEC suşları yeni doğmuş buzağı, kuzu, domuz ve insanlarda diyareye, EIEC suşları insan ve hayvanlarda diyare ve dizanteriye, VTEC/STEC suşları insan ve buzağılarda diyare, buzağılarda hemorajik kolit, domuz yavrularında ödem hastalığına, EHEC suşları özellikle insanlarda hemorojik kolitis-hemolitik üremik sendroma, DAEC ve EaggEC suşları ise özellikle insanlarda diyareye yol açarlar (Kuhnert ve ark., 2000; Quinn ve ark., 2002; Scheutz ve Strockbine, 2005). ExPEC suşlarından olan UPEC suşları insanlarda, köpek ve kedilerde üriner sistem infeksiyonlarına, NMEC suşları ise bebeklerde neonatal meningitis ve sepsise neden olurlar. Bununla birlikte, bazı ExPEC suşları yeni doğan hayvanlarda (kuzu, buzağı, tay, civciv, domuz yavrusu gibi) septisemilere (kolibasillozis), domuzlarda ödem hastalığına ve mastitis-metritis-agalactiae sendromuna yol açarlar. Taylarda genital sistem infeksiyonlarına, yara infeksiyonlarına, pneumonilere ve tüm evcil dişi hayvanlarda özellikle ineklerde mastitise neden olurlar (Kuhnert ve ark., 2000; Quinn ve ark., 2002; Scheutz ve Strockbine, 2005).
28 18 Ayrıca, kanatlı hayvanlarda embriyonal ölümlere, koligranulomaya, enteritise, salpingitise, sinovitise, epikarditise, hava kesesi yangısına, sarı kesesi yangısına ve omfalitise neden olan ve sekonder etken olarak da çoğunlukla İnfeksiyöz Bronşitis, Newcastle ve CRD infeksiyonlarından izole edilen Avian Patojenik E. coli (APEC) suşları vardır (Provence ve Curtis., 1994; İzgür, 2002) Epidemiyoloji E. coli, özellikle yüksek verimli süt ineklerinde genellikle doğum dönemine yakın veya laktasyonun erken döneminde lokal ve bazen de şiddetli sistemik semptomlarla seyreden mastitise yol açar. Çevresel mastitis olarak da adlandırılan bu durum yüksek verimli süt ineklerinde verim düzeyini ve kalitesini etkileyebildiği gibi infeksiyonun şiddetli olduğu vakalarda ölüm de şekillenebilir (Burvenich ve ark., 2003). Koliform mastitisler sporadik ve bazen de enzootik olarak seyredebilirler. Enzootik olgular genellikle verimin yüksek olduğu ve diğer mastitis olgularının azaltıldığı sürülerde ortaya çıkar (Diker, 1984). Mikroorganizmanın opurtunistik olması mastitisin şekillenmesinde rol oynayan faktörler arasında olup bu durum konağın fizyolojik ve immunolojik durumu ve mikrobiyal faktörler ile de ilişkilidir (Sanchez-Carlo ve ark., 1984). Yüksek süt verimli ineklerin özellikle doğum öncesi dönemde ciddi derecede immunosupresyondan etkilendiği bilinir. Yüksek süt üretimi nedeniyle oluşan negatif enerji ve protein dengesi ketozis, nutrisyonel dengesizlikler gibi çeşitli metabolik bozukluklara yol açarak bağışıklık sistemi üzerinde olumsuz etkilere neden olur (Goff ve Horst, 1997; Mallard ve ark., 1998; Burvenich ve ark., 2003). Ayrıca kandaki keton cisimciklerinin artan plazma konsantrasyonunun, laktasyonun başlangıcındaki hayvanlarda yüksek oranda enerji gereksinimine yol açtığı, bu durumun da PMN lökosit fonksiyonu üzerinde negatif etki yarattığı ve mastitise duyarlılığı arttırdığı da bildirilmiştir (Burvenich ve ark., 2003).
29 19 Koliform bakteriler çok yaygın oldukları ve meme başı derisinden sık sık izole edildikleri halde koliform orijinli mastitisler azdır. Bu durum, birçok koliform etkenin sütteki humoral ve sellüler faktörlere karşı duyarlılığına bağlıdır. Sütteki koliform etkenlere karşı şekillenen doğal antikorlar ve memedeki lökositoz bu organizmaların birçoğu ile meme infeksiyonlarının şekillenmesini önler. Bu nedenle, meme bezi diğer patojenlerle infekte olduğunda ve lökositoz şekillendiğinde koliform infeksiyon gelişmez. Dolayısıyla, koliform mastitis meme bezinin diğer patojenlerle infekte olmadığı zaman şekillenir (Berkin ve Milli., 1984). Koliform infeksiyonlar laktasyonun herhangi bir devresinde veya kuru dönemde oluşabilir. Ancak, inekler doğumdan kısa bir süre veya 2-3 ay sonra daha duyarlıdırlar. E. coli infeksiyonları buzağılama ve laktasyonun erken döneminde kuru dönemin son iki haftasına oranla daha sıklıkla orijin alırlar. Birçok koliform mastitisin doğumdan hemen sonra görülmesi, başlangıçta infeksiyonun hayvana kuru dönemde yerleştiğini düşündürmüştür. Fakat, daha sonra yapılan araştırmalarda kurudaki memenin E. coli infeksiyonlarına dirençli olduğu ve doğumdan birkaç gün önce bu direncin ortadan kalktığı da belirlenmiştir. Buna rağmen yeni yapılan araştırmalarda laktasyonun ilk iki ayında ortaya çıkan klinik koliform mastitislerin % 65 inin kuru dönemde orijin aldıkları bildirilmiştir (Diker, 1984; Hogan ve Smith., 2003). Laktasyon sırasındaki koliform mastitisler buzağılama döneminde en yüksek oranda gözlenirler. Laktasyon sırasında şekillenen E. coli mastitislerinin süresi 10 günden fazla değildir. Doksan günden fazla süren E. coli nedenli kronik mastitis olgularının görülme oranı ise oldukça nadirdir. Laktasyonda ve kuru dönemde şekillenen koliform mastitis olgularının görülme sıklığı üzerinde mevsimlerin de etkisi vardır. Klinik koliform mastitislerin görülme oranı, kapalı sistemde yetiştirilen ineklerde yaz aylarında en yüksek orandadır. Ayrıca yaz aylarında buzağılayan yaşlı hayvanlar genellikle klinik koliform mastitisin şekilleneceği en yüksek riske sahip hayvan populasyonudur (Hogan ve Smith., 2003). İneklerin E. coli nedenli mastitislere duyarlılığı ve infeksiyonun şiddeti patojen etkene ve hayvanın immun yanıtına bağlı olduğu için E. coli nedenli mastitislerin sonucu ve şiddeti aynı sürüdeki inekler arasında ve aynı hayvanın farklı laktasyon
30 20 dönemlerinde değişiklik gösterir. E. coli nin neden olduğu mastitislerin oranı ülkelere göre farklılıklar göstermektedir. Örneğin İngiltere de %14.4, Finlandiya da bu oran %20 den az, İsrail de %60 dan fazla olarak bildirilmiştir (Bradley, 2002; Shpigel ve ark., 1998). E. coli nedenli mastitislerde dışkı ile kontaminasyon infeksiyonun ana kaynağıdır. E. coli ineklerin normal bağırsak florasında ve yaşadıkları çevrede bol miktarda bulunduğundan meme başlarına bulaşma riski her zaman söz konusudur. Ayrıca, çeşitli yetiştirme faktörleri laktasyondaki meme bezlerinin çevrede yüksek oranda bulunan koliform etkenlere maruz kalımı üzerinde etkilidir. Koliform bakterilerin asıl kaynağı altlık, temizlenmemiş kaplar, enfekte sulardır. Bulaşma kaynakları içerisinde özellikle kontamine altlıklar, koliform mastitisin şekillenmesinde en önemli nedenlerdendir. Altlıklardaki bakteri sayısının azalması koliform etkenlerin neden olduğu klinik mastitislerin görülme oranını azaltır. Bunun dışında toprak, su ve bakıcılar da bulaşmada rol oynarlar. Ayrıca barınma koşulları, barınakdaki nem oranı da infeksiyon için gerekli ön koşulları hazırlar. Dolayısı ile kötü ahır şartları ve yetiştirme hataları, koliform mastitislerin şekillenmesi için predispoze faktörlerdir (Diker, 1984; Nemeth ve ark., 1994; Burvenich ve ark., 2003). İnfeksiyon çoğunlukla çevrenin E. coli ile fekal kontaminasyonunu takiben etkenin meme kanalı yolu ile meme bezine ulaşması sonucu şekillenmektedir. Ayrıca vasküler veya lenfatik sistem yoluyla da etkenin meme bezine ulaşarak mastitise yol açması mümkündür (Kaipainen ve ark.,2002; Hogan ve ark.,2003) Patogenez Koliform mastitisler, genellikle patojen etkenin meme başı kanalından meme başı sisternasına girmesi ile başlar (Berkin ve Milli, 1984). Özellikle enteritis ve septisemiden sonra kan yoluyla memeye taşınan infeksiyonlardan söz edilmişse de, bu durum çok seyrek oluşur. Memeye giriş yolları aynı olmasına rağmen, kokal etkenlerden farklı olarak koliform bakteriler meme başı kanalına kolonize olmazlar (Diker, 1984). Streptokok ve Stafilokok mastitislerinde infekte memeden infekte
31 21 olmayan memeye bulaşma sağım esnasında sağıcıların elleri, meme havluları ve süt malzemesi ile olurken koliform bakteriler, memeye sağım esnasında değil de sağım dışında bir zamanda girerler. (Berkin ve Milli.,1984). Ayrıca, bir çok olguda etkenler muhtemelen meme bezi epiteline veya paranşimine adhere yada invaze olmazlar. Ancak kronik veya tekrarlayan mastitislere neden olan bazı E. coli suşları epitel dokuya adhezyon ve invazyon yeteneğine sahip olabilirler (Dopfer ve ark., 2000). Meme bezine ulaşan bakteriler burada hızla çoğalırlar ve birkaç saat içerisinde sütteki konsantrasyonları yaklaşık olarak 10 8 cfu/ml ye ulaşır. Bu erken dönemi takiben memeye lökosit göçü başlar. Dolayısıyla etkenin çoğalması meme bezindeki lökosit sayısına ve lökositlerin bölgeye hareket hızına bağlıdır. Özellikle vasküler nötrofillerin toplanması ve aktivasyonu hastalığın ortaya çıkışı ve şiddeti üzerinde etkilidir ve koliform mastitisin patogenezinde anahtar rol oynar. Artan sayıdaki polimorf lökositler koliformları fagosite ederler. Fagositoz olayı nedeniyle bakteri sayısı hızla azalırken, lize olan bakterilerden açığa çıkan endotoksin miktarı artar Açığa çıkan endotoksin yangısal reaksiyon zincirinin başlamasına yol açar. IL-1 ve TNF gibi yangı mediatörleri, aktive olan fagositlerden serbest bırakılır ve absorbe edilen endotoksinlerin de etkisiyle semptomlar şekillenir (Diker, 1984; Burvenich ve ark., 2003; Hogan ve Smith, 2003). Hızlı bakteriyel proliferasyon, hastalığın başlaması için ön koşul olup klinik bulguların şiddeti ve iyileşme oranı ile ilişkilidir. Deneysel olarak infekte edilen ineklerin sütlerinde etken sayısının infeksiyondan saat sonra pik yaptığı belirlenmiştir. Bakteriyel üreme oranlarının doğum sonrası dönemde ve yaşlı hayvanlarda daha yüksek olduğu ve bu artışın da hastalığın şiddeti ile ilişkili olduğu bildirilmiştir. Bu olguların gidişatı meme bezi hücrelerinin organizmayı tanımasıyla sitokinler gibi yangı mediatörlerinin salınımı ile ilişkilidir. Tümor nekrozis faktör-α (TNF-α), interferon-γ, interleukin-1 (IL-1) ve interleukin-8 (IL-8) gibi sitokinler meme bezindeki lökositler ile vasküler lökositlerin endotelyal hücrelere göçü ve adhezyonunu aktive ederler (Shpigel, 2001).
32 22 Ayrıca, meme içi endotoksin infüzyonunun, doğal yolla oluşan akut klinik koliform mastitiste şekillenen klinik belirtileri ortaya çıkardığı bildirilmiştir ki; bu durum koliform mastitislerde görülen belirtilerden endotoksinin sorumlu olduğuna işaret etmektedir (Diker, 1984). Endotoksin TNF-α, IL-1, IL-6, IL-8 ve faktör XII (Hageman faktör) gibi yangısal mediatörlerin salınımına aracılık eder. Yangı mediatörleri hem lokal olarak meme bezinde gelişen yangıdan hem de eğer sepsis gelişmişse meydana gelen sistemik bulgulardan sorumludurlar. Lokal ve sistemik inflamasyon hem infekte olan hem de infekte olmayan meme lobunun süt üretimini negatif olarak etkiler. Ancak endotoksinin çeşitli dozlarda meme içi infüzyonu ile başlatılan infeksiyonun, saha infeksiyonundan ve deneysel olarak oluşturulan koliform mastitislerden farklı olduğu da bildirilmiştir. Endotoksinin deneysel olarak meme içi infüzyonu ile bakteriyel infeksiyonun karşılaştırılması amacıyla yapılan elektron mikroskobik çalışmalarda polimorfnüklear lökosit invazyonu ile meme bezindeki lezyonların farklı biçimde olduğu gözlenmiştir (Shipigel, 2001) Semptomlar E. coli nedenli mastitisler genellikle sporadiktir ve klinik belirtiler çok şiddetli hatta öldürücü olabileceği gibi yalnızca meme bezlerinde lokal belirtiler gösteren formda da olabilir. Hastalığın şiddeti konak yanıtına bağlı iken etkenin virulens faktörlerinin de önemli rol oynadığı bildirilmiştir (Shipigel ve ark., 1998; Kaipainen ve ark., 2002). Ayrıca, meme loblarında ve sütte gözlenen değişikliklerin mastitisin saptanmasında ilk bulgular olmasına rağmen, bunların infeksiyonun şiddetini tahmin etmede yeterli olmadığı belirlenmiştir. Çünkü E. coli nedenli mastitislerde infeksiyonun şiddetinin direkt olarak sütteki bakteri sayısı ve özellikle de infekte olmamış meme lobunun süt üretimindeki azalma ile ilgili olduğu bildirilmiştir (Burvenich ve ark., 2003). E. coli mastitisleri tipik olarak ani başlar ve çoğunlukla erken postpartum dönemde akut formda şekillenir. Ancak akut infeksiyonların yanısıra perakut,
33 23 periyodik akut parlamaların şekillendiği kronik ve subklinik infeksiyonlar da meydana gelebilir (Jain, 1979; Diker, 1984). Tipik olarak perakut olgular kısa sürede şiddetli semptomlarla ortaya çıkarlar ve çoğunlukla doğumdan hemen sonra şekillenirler. İnfekte meme şiş, sıcak ve dokunulduğunda ağrılıdır. Süt ise sulanmış, yeşilimsi, pıhtı ve flakonlar içerir. Hayvanda ateş, tremor, iştahsızlık, depresyon ve rumen stazisi gözlenir. Bazı durumlarda ise beden ısısı aşırı düşmüş olabilmektedir (Diker, 1984; Baştan, 2002). Perakut mastitisli ineklerde hastalığa ait herhangi bir semptom şekillenmeden endotoksemi sonucu bir kaç gün içerisinde ölüm de gözlenebilir. Fakat, inek güçlü bir immun sisteme sahip ise E. coli ile infeksiyondan 12 saat sonra tüm bakterileri elimine de edebilir. Bu ineklerde mastitise ait herhangi bir semptom gözlenmez (Berkin ve Milli., 1984). Ancak, bakteriyemi ve endotoksemi nadiren olur ve yalnızca çok şiddetli olgularda şekillenir. Deneysel olarak indüklenen koliform mastitislerde etkenin meme bezinden orijin alarak, sistemik invazyonu ve bakteriyeminin şekillenmediği bildirilmiştir (Pyörälä ve ark., 1994; Shipigel ve ark., 1998). Akut koliform mastitisler ise yaz aylarında ısı stresi altındaki ineklerde daha sık şekillenir ve bazen tedavisi yapılsa bile ölümler görülebilir (Baştan, 2002). Akut olgularda infeksiyon meme parankiminde şiddetli bir bozukluk şekillendirmez, bu nedenle de iyileşmeyi takiben süt veriminde bir düşüş görülmez ancak çok şiddetli olgularda hayvan ölmese bile süt üretimi kalıcı olarak kaybedilebilir (Jain, 1979; Berkin ve Milli., 1984). İnfekte meme bölümü şişkin, sert ve duyarlıdır. Süt sulu ve seröz olabilir. Özellikle ilk sağılan sütte pıhtılar bulunabilir ve bu durum birkaç gün devam eder (Diker, 1984). Kronik koliform mastitisler uzun bir sürede tekrarlayan klinik belirtiler ile ortaya çıkarlar. İnfeksiyon sırasında anormal süt salgısı, yangı tablosu ve sistemik belirtiler şekillenebilir ve sütteki bakteri sayısı artar. Ara dönemde ise süt normal görülür ve infeksiyon ancak sütteki somatik hücre sayısı ve biyokimyasal değişiklikler ile belirlenebilir (Diker, 1984).
34 24 Subklinik olgular ise koliform mastitisin enzootik hale geçtiği bir sürüde yaygın olarak şekillenir ve özellikle buzağılama sırasında çoğalır ancak, pek çoğu belirlenemez (Diker, 1984) Teşhis Mastitislerin teşhisi, meme lobları ve sütün klinik muayenesi ile sütün kimyasal, fiziksel, hücresel ve bakteriyolojik muayenelerine dayanır. Klinik mastitislerde meme loblarının inspeksiyonu ve palpasyonu, sütün genel görünümü (rengi, kokusu, kan veya serum varlığı) teşhis için önemlidir. Subklinik mastitislerde ise sütün görünümünde bir değişiklik olmadığından somatik hücre sayımı, çeşitli biyokimyasal testler, süt ph sının belirlenmesi, sütün elektrik iletkenliğinin ölçülmesi, California Mastitis Test (CMT), sütün bakteriyolojik muayenesi ile teşhise gidilir. Ancak, koliform mastitisin kesin teşhisi bakteriyolojik incelemeler ile mümkündür (Baştan, 2002; Hamann ve ark., 2005) Laboratuvar Muayenesi Laboratuvar muayenesi için sütün laboratuvara uygun koşullarda gelmesi gerekir. Bunun için hayvan memeleri önce temiz su ile yıkanır ve %70 lik alkol veya bir dezenfektan ile dezenfekte edilir. Steril tülbent ile kurulanır. İlk süt sağılarak atıldıktan sonra steril tüplere her memeden ayrı ayrı alınır, süt örnekleri bekletilmeden laboratuvara gönderilir. Eğer örnekler hemen gönderilmeyecekse soğukta saklanır (Leloğlu, 1999) Bakteriyoskopi Süt örneğinden bir öze yardımı ile alınarak lam üzerine yayma froti hazırlanır ve Gram boyama yapıldıktan sonra mikroskopta incelenir. Bu muayene direkt süt
35 25 örneğinden yapılabildiği gibi santrifüje edilip tortudan da froti hazırlanarak inceleme yapılabilir (Aydın ve Akay., 1984) Kültür Süt örneklerinden Kanlı agara, Mac Conkey agara direkt olarak ekim yapılabileceği gibi santrifüj edildikten sonra tortudan da ekim yapılabilir. 37 C de saatlik inkubasyondan sonra üreyen koloniler E. coli yönünden makroskopik ve mikroskopik morfolojileri ve biyokimyasal özelliklerine göre (karbonhidrat fermentasyon testleri, H 2 S, İndol, MR, VP, Nitrat, vs.) identifiye edilirler (İzgür, 1999; Quinn ve ark., 2002) Patojenite Testleri Çeşitli Virulens Özelliklerin Tayini İzole edilen E. coli suşunda etkenin patojenitesinde rol oynadığı düşünülen serum dirençliliği, toksin üretimi, kolisin aktivitesi, hemolizin üretimi, aerobaktin sideroforlarının, kapsül polisakkaritlerinin, plazmidlerin ve adhezinlerin varlığı gibi çeşitli virulens faktörlerin konvansiyonel yöntemlerle tayininin yapılması, etkenin patojenitesinin belirlenmesi açısından önemlidir. Bu amaçla hemoliz testi, hemaglütinasyon testi, serum dirençliliği testi, hücre kültüründe sitotoksik aktivite testi, kolisin testi, aerobaktin demir elde etme sistemi varlığı, plazmid varlığı ve kapsül varlığının saptanması için testler yapılır (Sanchez-Carlo ve ark., 1984; Barrow ve Hill, 1989; Nemeth ve ark.,1994).
36 Hayvan Deneyleri Besiyerinde izole edilen etkenlerin patojen olup olmadıkları deney hayvanlarından tavşan, fare ve kobaylara enjekte edilmek suretiyle tayin edilir (Aydın ve Akay., 1984) Serolojik testler Mastitislerden izole edilen koliform etkenlerin serolojik tiplendirilmesi etkenin fenotipinin ve patojenitesinin belirlenmesine yardımcı olur (Hogan ve Smith., 2003). E. coli serotiplerine karşı hazırlanmış antiserumlar kullanılarak, üreyen kolonilerin lam üzerinde yapılan aglütinasyon testleriyle hangi serolojik gruba ait oldukları, dolayısıyla antijenik özellikleri saptanabilir (İzgür, 1999) Moleküler teknikler Fenotipik tiplendirme yöntemleri gibi moleküler yöntemler de suşların tanımlanmasında oldukça önemlidir. Moleküler tabanlı tanı yöntemlerinin gelişmesi ile virulens özellikler gen düzeyinde saptanmaya başlanmıştır. N-terminal aminoasit sekans analizi, DNA sequencing, Southern blot ve hibridizasyon teknikleri ile Polimeraz zincir reaksiyonu (PCR) kullanılan moleküler teknikler arasındadır. PCR, virulens genlerinin hızlı ve direkt olarak saptanmasını sağlar. PCR tekniği kullanılarak mastitislerden izole edilen E. coli suşlarında f17a, f17b, f17c, f17d, afa7, afa8d, afa8e, sfa, pap, cnf1, cnf2, iucd, trat, eaea, eagg, einv, stx1, stx2 vb. genlerin varlığı araştırılmıştır (Lipman ve ark., 1995; Kuhnert ve ark. 2000; Hogan ve Smith, 2003, Bean ve ark., 2004; Lehtolainen, 2004). Kaipainen ve ark. (2002) ise multipleks PCR ile mastitislerden izole ettikleri E. coli suşlarında trat, cnf1, cnf2, aer, f17, sfa, pap, afa8d, afa8e genlerinin varlığını araştırarak mastitisdeki rollerini incelemişlerdir. Ayrıca çeşitli araştırmacılar tarafından ERIC ve REP primerleri
37 27 kullanarak sığır mastitislerinden izole edilen E. coli suşlarında genotiplendirme yapılmıştır (Al-Talhi ve Al Bashan, 2005; Wenz ve ark., 2006) Sağaltım Perakut ve akut koliform mastitislerin sağaltımında sağım, antibiyotiklerin kullanımı, antienflamatuar ajanların kullanımı ve destekleyici sağaltım uygulanır. Sütte bulunan bakteri, endotoksin ve yangısal ürünler, sık sağım (günde 6-8 kez) ile memeden uzaklaştırılmalıdır. Bu amaçla damar içi oksitosin de kullanılabilir. Koliform grubu bakterilerin neden olduğu mastitislerde parenteral antibiyotik uygulaması ile sık sağım uygulaması birlikte yapılabilir. Antibiyotik olarak oksitetrasiklin, ampisinsodyum veya sülfanamidler uygulanabilir. Parenteral tedaviye ek olarak ampisilin ve sefalosporinler meme içi verilmelidir (Diker, 1984; Baştan, 2002). Akut koliform mastitislerde primer problem endotoksinin indüklediği şok durumudur. İnfeksiyondan ciddi derecede etkilenen ineklere ilk 24 saat içerisinde intravenöz yolla lt. kadar sıvı verilmesi gereklidir (Erskine, 1995) Antienflamatuar ajanlar özellikle siklo-oksijenaz inhibitörleri (Non-steroidal antiinflamatuarlar) ve kortikosteroidler koliform mastitislerde lokal inflamasyonu ve sistemik bulguların şiddetinin azaltılması amacıyla kullanılırlar. Bu amaçla fluniksin meglumin uygulanabilir, ayrıca alternatif olarak deksamethazon sodyum sülfat, flurbiprofen veya karprofen de uygulanabilir (Shpigel, 2001; Baştan, 2002) Koruma Bu etkenler genellikle ineğin barındığı ortamda bulunduklarından hayvanları korumada genel kural barınma yerlerinin temiz ve kuru olmasının sağlanmasıdır ki; koliform bakteriler açısından kontaminasyonun asıl kaynağı altlıktır. Altlıkdaki bakteri sayısının azaltılması klinik mastitis olgularının da azalmasını sağlar. Nem oranı düşük, sönmüş kireçle karıştırılmış toprak en uygun altlıktır. Sağım öncesi teat dipping (meme başının antiseptikli solüsyonlara batırılması) uygulaması da bulaşmayı önlemek açısından etkilidir. Sağım öncesi germisidal dezenfektanların
38 28 kullanımı laktasyon sürecinde yeni koliform mastitislerin şekillenme oranını azaltır (Smith, 1983; Baştan, Hogan ve Smith, 2003). Koliform mastitislerde korunmada spesifik immuniteyi sağlamak 1980 li yılların sonlarına dek mümkün değildi. Ancak daha sonraları E. coli O111:B4 veya J5 suşu olarak tanımlanan Rc mutantı aşılamalarda kullanılmaya başlandı (Hogan ve Smith, 1998). Ancak bu aşılamanın meme içi infeksiyonları engellemede çok etkin olmadığı fakat klinik mastitislerin şekillenme oranını düşürdüğü ve lokal inflamasyon ile sistemik klinik bulguları hafifleterek hastalık şiddetini azalttığı anlaşılmıştır (Hogan ve ark., 1992; Hogan ve ark., 1995; Alluwaimi, 2001). Ayrıca, Wilson ve ark. (2007) yaptıkları bir çalışma ile J5 bakterin ile aşılamanın, fagositoz ve bakterilerin meme bezinden uzaklaştırılmasında rol oynayan J5-spesifik IgG1 ve IgG2 üretimini önemli ölçüde artırdığını, somatik hücre sayısını azalttığını, süt üretimindeki kaybı azalttığını saptamışlardır. Bu tez çalışmasında mastitisli ineklerden süt ve rektal svap ile barınaklardan altlık örnekleri alınarak, izole edilen E. coli suşlarının virulens faktörlerinden hemoliz, mannoz duyarlı ve mannoz dirençli hemaglutinasyon, aerobaktin demir elde etme sistemi, vero hücrelerde toksik etki, sitotoksik nekrotizan faktör 1, serum dirençliliği, kolisin aktivitesi özelliklerinin fenotipik ve/veya moleküler olarak incelenmesi amaçlanmıştır.
39 29 2. GEREÇ VE YÖNTEM 2.1.Gereç Örneklerin Toplanması E. coli izolasyonu için gerekli olan mastitis şüpheli süt, altlık ve rektal svap örnekleri yılları arasında Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı na çeşitli işletmelerden gönderilen materyallerden ve ayrıca Ankara (işletme B ve işletme E), Balıkesir (işletme A ve işletme D) ve Çorum (işletme C) daki ticari süt sığırcılığı işletmelerinden sağlandı (Çizelge 2.1., Çizelge 2.2.). Çizelge 2.1. İncelenen süt örnekleri ile ilgili bilgiler Yetiştirici Tipi Mastitis Şüpheli Süt Örneği Sayısı A 194 Ticari Süt Sığırcılığı İşletmesi B 284 C 100 D 416 E 16 Aile İşletmesi 17 Toplam 1027
40 30 Çizelge 2.2. İncelenen rektal svap ve altlık örnekleri ile ilgili bilgiler Örnek Alınan İşletme Alınan Örnek Türü Alınan Örnek Sayısı Rektal Svap 30 İşletme A Altlık 25 Rektal Svap 25 İşletme B Altlık Besiyerleri Etken izolasyonu amacıyla %5 koyun kanı içeren Kanlı Agar ile birlikte özellikle identifikasyon amacıyla MacConkey Agar ve Eosin Metilen Blue Agar (Difco, A.B.D.) ve izole edilen suşların pasajı için Nutrient Agar ve Nutrient Buyyon (Oxoid, İngiltere) kullanıldı. Suşların hemoliz özelliklerinin belirlenmesi için %5 koyun kanlı agardan ve izole edilen suşların hemaglütinasyon aktiviteleri ile kolisin aktivitelerinin incelenmesi öncesinde etkenin üretilmesi amacıyla Nutrient Buyyon dan yararlanıldı. Suşların serum dirençlilik durumunun ve kolisin aktivitesinin incelenmesi amacıyla Tripticase Soy Agar (TSA, Oxoid, İngiltere) ve suşlarda demir sideroforlarının varlığının belirlenmesi amacıyla da demir kısıtlayıcı besiyeri olarak M9 buyyon kullanıldı. Bu besiyerinin bileşimi aşağıda verilmiştir. Di-Sodyum Hidrojen Fosfat (Na 2 HPO 4 ) (Merck, Almanya) 6 g Potasyum Hidrojen Fosfat (KH 2 PO 4 ) (Merck, Almanya) 3 g Amonyum Klorür (NH 4 Cl) (Merck, Almanya) 1 g Sodyum Klorür (NaCl 2 ) (Merck, Almanya) 0,5 g Distile su 1 L
41 31 Besiyeri hazırlanıp 121 C de 15 dk. otoklavlanarak su banyosunda 50 C ye soğutulduktan sonra aşağıdaki maddeler eklenerek sıvı besiyeri hazırlandı. Kalsiyum Klorür (CaCl 2 : 0.01 M) (Merck, Almanya) 10 ml Magnezyum Sülfat (MgSO 4 : 1 M ) (Merck, Almanya) 1 ml Casamino Acide (Merck, Almanya) 5 g Glikoz (Merck, Almanya) 2 g L-Triptofan (Merck, Almanya) 20 mg/ml Tiamin (Merck, Almanya) 5 mg/ml 2,2 -dipyridil (Merck, Almanya) 200 µm Ayrıca bu besiyerine %2 Agar agar (Merck, Almanya) ilave edilmesiyle M9 agar hazırlanarak kullanıldı. İzole edilen suşların Hemaglütinasyon aktivitesinin belirlenmesi amacıyla %3 D-mannozlu eritrosit süspansiyonu hazırlanmasında D-Mannoz (Merck, Almanya) ve suşların verotoksin aktivitesinin saptanması amacıyla Dulbecco s Modified Eagle s Medium [DMEM] (Gibco, İngiltere) kullanıldı. DNA ekstraksiyonu yapmak amacıyla suşlar Luria Bertoni buyyon (LB, Difco, A.B.D) kullanılarak üretildi. İzolasyon ve identifikasyonu yapılan suşların -20 C de saklanması amacıyla %20 Gliserin (Merck, Almanya) içeren Tripticase Soy Broth (TSB, Oxoid, İngiltere) dan yararlanıldı PCR da Kullanılan Maddeler PCR da Etanol (%95 lik) (Merck, Almanya), Tris Borat EDTA (TBE) (AppliChem, Almanya), Ticari Ekstraksiyon kiti (Fermentas, Litvanya), Dietilpirokarbonatlı su (DEPC-treated water) (Fermentas, Litvanya), 10xPCR Buffer (Fermentas, Litvanya),
42 32 25 mm MgCl 2 (Fermentas, Litvanya), 10 mm dntp karışımı (Fermentas, Litvanya), Taq DNA polimeraz (Fermentas, Litvanya), Primerler (Operon, Almanya), DNA marker (100 bp) (Fermentas, Litvanya), Agarose (Prona, EU), Ethidium Bromide (Fermantas, Litvanya), 6xLoading Dye (Fermentas, Litvanya) kullanıldı PCR da Kullanılan Cihaz ve Ekipmanlar Bu çalışmada hassas terazi (Scaltec sbc41, Almanya), santrifüj (Hettich, Almanya), steril kabin (laminar flow) (Bioair Instruments, Aura 2000, Mac, İtalya), vorteks (Fine Vortex, Kore), ph metre 420A (Orion, ABD), DNA Thermal Cycler (Biometra, Almanya), Jel elektroforez cihazı ve güç kaynağı (Wealtec elite 3000 plus, A.B.D.), UV transillüminatörlü bilgisayarlı görüntüleme sistemi (Gene Genius, Syngene, Bio Imaging System, UK), Termal printer (Sony, Japan) kullanıldı Standart Suşlar Çalışmada izole edilen suşların virulens özelliklerinin fenotipik ve/veya genotipik olarak saptanması amacıyla E. coli 140 KH 89 (alfa hemolizin, hlya), (MRHA, papef), 239 KH 89 (CNF, cnf1), pabn1(aerobaktin, iucd) suşları Prof. Dr. Jacques Mainil (Chaire de Bacteriologie et de Pathologie des Maladies Bacteriennes, Faculte de Medecine Veterinarie, Universite de Liege, B Brussels, Belgium)' den, E. coli M37189 (MSHA, fimh) ve M36923 (serum direnci, trat) suşları Dr. Geoff Werrett (Bristol University, Departmant of Clinical Veterinary Sciences, UK) den ve E. coli K12 RSKK suşu (kolisin duyarlı suş) ise T.C. Sağlık Bakanlığı Refik Saydam Hıfzıssıhha Merkezi Başkanlığı Kültür Koleksiyonundan sağlanarak pozitif kontrol suşları olarak kullanıldı. Negatif kontrol olarak ise yukarıda bildirilen özellikleri göstermeyen ve Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı, Kürsü Koleksiyonundan sağlanan E. coli ATCC suşu kullanıldı.
43 Hücre Kültürü İzole edilen E. coli suşlarının Vero hücrelerinde toksik etkilerinin incelenmesi için Ankara Üniversitesi Veteriner Fakültesi Viroloji Anabilim Dalında hazırlanan Vero (Yeşil Maymun Böbrek Hücresi) hücre kültürü kullanıldı Yöntem İzolasyon ve İdentifikasyon E. coli suşlarının izolasyonu için toplanan örneklerden direkt olarak Kanlı Agar, MacConkey Agar ve Eosin Metilen Blue Agar a ekim yapılarak 37 C de saat inkubasyona bırakıldı. İnkubasyon sonrası şekillenen kolonilerin makroskobik ve mikroskobik morfolojileri incelenerek etken için spesifik olan (İndol, H 2 S, Metil Red, Voges Proskauer vb.) biyokimyasal testler ile identifikasyona gidildi (Scheutz ve Strockbine, 2005). E. coli olarak tanımlanan suşlar daha sonra virulens özelliklerinin araştırılması amacıyla %20 gliserinli TSB de süspanse edilerek -20 C de saklandı E. coli Suşlarının Çeşitli Virulens Özelliklerinin Araştırılması Hemoliz Testi E. coli izolatlarının hemolizin üretme özellikleri %5 koyun kanı içeren Kanlı Agarda 37 C de saat sonra koloniler etrafında oluşan hemolize göre belirlendi (Siitonen, 1992).
44 Hemaglutinasyon Testi İzole edilen bakterilerin hemaglutinasyon özelliklerini belirlemek amacıyla sığır, koyun ve tavuklardan, antikoagulanlı tüplere alınan kanlar santrifüj edilerek yıkanmış eritrositler elde edildi ve bu eritrositlerden PBS kullanılarak %2 lik iki ayrı eritrosit süspansiyonu hazırlandı. Süspansiyonlardan birine D-mannoz ilave edilmezken diğer süspansiyona %3 D-mannoz ilave edildi. İzole edilen E. coli suşları nutrient buyyona inokule edilerek 18 saat 37 C de inkube edildi. İnkubasyon sonrası hazırlanan her bir buyyon kültüründen 50 şer µl 2 ayrı mikropleyt gözüne konuldu ve gözlerden birisine %3 D-mannoz içeren eritrosit süspansiyonundan 50 µl ilave edilirken, diğer göze mannozsuz eritrosit süspansiyonundan 50 µl eklendi ve pipete edilerek 18 saat 37 C de inkubasyona bırakıldılar. Süre sonunda hemaglütinasyon göstermeyen suşlar negatif, mannozsuz ve mannozlu eritrositlerle hemaglutinasyon oluşturanlar MRHA pozitif ve mannozsuz eritrositlerle hemaglütinasyon oluşturup mannozlu eritrositlerle oluşturmayanlar ise MSHA pozitif olarak değerlendirildi (Sanchez-Carlo ve ark., 1984) Aerobaktin Demir Elde Etme Sistemlerinin Araştırılması İzole edilen bakterilerde aerobaktin demir elde etme sistemlerinin varlığını belirlemek amacıyla 200 μm 2,2 -dipyridil içeren minimal tuz karışımı bulunan M9 buyyona TSA da aktive edilen suşlar geçilerek 37 C de 24 saat inkubasyona bırakıldı. İnkubasyon sonrası buyyon kültüründen 1 ml alınıp aynı besiyerinde tekrar pasajlanarak 37 C de 24 saat inkubasyona bırakıldı. Daha sonra buyyon kültüründen bir öze dolusu alınıp M9 agara ekim yapılarak 37 C de 24 saat inkube edildi. İnkubasyon sonrasında M9 agarda üreme gösterenler aerobaktin demir elde etme sistemine sahip suşlar olarak değerlendirildi (Stuart ve ark,1980).
45 Vero Hücrelerde Toksik Etkinin İncelenmesi E. coli suşlarında Vero hücrelerde toksik etkinin belirlenmesi amacıyla Vero hücre kültürü kullanıldı. Bu amaçla, antibiyotik (Penisilin 100 IU/ml ve Streptomisin 100 mg/ml) içeren ve %10 fötal dana serumu ile zenginleştirilmiş Dulbecco s Modified Eagle s Medium (DMEM) vasatında üretilen Vero hücreleri tripsin enzimi (1:250, Gibco, İngiltere) ile hücre kültürü şişesinden kaldırıldı. Aynı vasat bileşimi ile 4 x 10 4 hücre/ml olacak şekilde sulandırılan Vero hücreleri 24 gözlü hücre kültürü pleytinin gözlerine 1 ml hacminde konularak pleyt %5 CO 2 li 37 C lik etüvde 24 saat inkube edilerek Vero hücrelerde toksik etkinin saptanması için hazırlandı. Toksik aktivitenin belirlenmesinde Miyao ve ark. (1998) tarafından bildirilen yöntem modifiye edilerek kullanıldı. TSA agarda aktive edilen suşlar 5 ml TSB ye geçilerek 37 C de 20 saat çalkalayıcıda inkubasyona bırakıldı. İnkubasyon sonrası her örnekten 1,5 ml alınarak ayrı ayrı steril ependorflara geçirildi ve rpm de 10 dk santrifüj edildi. Elde edilen süpernatant 0,2 µm lik por çaplı tek kullanımlık filtreden süzülerek kültür filtratı elde edildi. 24 gözlü mikropleytlerde hazırlanan hücre kültürüne elde edilen kültür filtratlarından 100 er µl konularak 37 C de CO 2 li etüvde inkubasyona bırakıldı. 24, 48 ve 72 saat sonra faz kontrast mikroskop kullanılarak hücrelerdeki morfolojik değişikliklere ve ayrılmalara göre değerlendirme yapıldı Serum dirençliliği E. coli izolatlarının serum dirençliliklerinin belirlenmesi amacıyla Trypticase Soy Agar (TSA) kullanılarak üretilen bakteriler PBS içerisinde McFarland No. 3 e göre süspanse edildi ve bu süspansiyondan 0,25 ml alınarak 50 C ye gelmiş TSA nın 5 ml si ile karıştırılarak katı besiyeri hazırlandı. Hazırlanan bu agar içine açılan küçük çukurcuklara sığır ve koyun serumları konularak 4 C de 4 saat bekletilmesini takiben 37 C de bir gece inkübe edildikten sonra serum yerleştirilen çukurcukların etrafında üreme olup olmamasına göre değerlendirildi (Sanchez-Carlo ve ark., 1984).
46 Kolisin aktivitesi İzole edilen E. coli suşlarının 18 saatlik buyyon kültüründen TSA besiyeri üzerine iğne uçlu öze ile hat şeklinde inokule edilerek 35 C de bir gece inkübe edildi. Daha sonra 1 saat kloroform buharına tutularak inaktive edilen kültürler kazınarak alındı, 30 dk. daha kloroform buharı ile inaktive edildi ve kloroformun uçması için petri kapağı 15 dk. açık bırakıldı. Kolisin duyarlı E. coli K12 RSKK suşu ilk ekim hattına dik olarak inokule edilerek 24 saat inkübe edildi. İki hattın birleştiği yerdeki inhibisyona göre incelenen suş kolisin aktif olarak değerlendirildi. Bu test kolisin aktif suşlar ile izole edilen diğer suşlar çaprazlanarak tekrarlandı ve iki hattın birleştiği yerde inhibisyon alanı varsa test edilen suş kolisin duyarlı olarak belirlendi (İzgür, 1981) Polimeraz Zincir Reaksiyonu (Polymerase Chain Reaction: PCR) PCR için sırasıyla ekstraksiyon, amplifikasyon, elektroforez ve görüntüleme işlemleri gerçekleştirildi. E. coli suşları TSA da aktive edildikten sonra LB broth a ekilerek 37 C de 18 saat inkube edildi. İnkubasyon sonrası her kültürden 1 er ml alınarak ependorflara aktarıldı. Daha sonra tüpler rpm de 2 dk. santrifüj edildi ve süpernatant atılarak pelet kısmı 1 ml steril distile su ile süspanse edilerek DNA ekstraksiyonu için kullanıldı (Sambrook ve Russell, 2002). Ekstraksiyon DNA ekstraksiyonu için ticari bir kit olan Fermantas Genomik DNA Purifikasyon kiti kullanıldı. Ekstraksiyon işlemi kit prosedürüne göre aşağıda bildirilen şekilde yapıldı. 200 µl örnek 400 µl lizis solüsyonu ile karıştırılarak 65 C de 5 dk. inkube edildi.
47 µl kloroform eklenerek karıştırıldı ve rpm de 2 dk. santrifüj edildi. 720 µl steril distile su, 80 µl 10x konsantre solüsyonu ile karıştırılarak presipitasyon solüsyonu hazırlandı. Santrifüj sonrası tüpün üst kısmındaki DNA içeren sıvı faz yeni bir tüpe alındı ve üzerine 800 µl presipitasyon solüsyonu eklendi. Oda sıcaklığında 1-2 dk. karıştırıldı rpm de 2 dk. santifüj edildi. Süpernatant tamamiyle alındı. DNA peletine 100 µl 1,2 M NaCl solüsyonu eklenip vortekslenerek DNA peletinin iyice çözünmesi sağlandı. 300 µl soğuk etanol eklenerek DNA nın presipite olması için -20 C de 10 dk. bekletildi rpm de 3 dk. santrifüj edildi. Üst kısımdaki etanol dökülerek pelet %70 lik soğuk etanol ile yıkandı. DNA 100 µl distile suda iyice karıştırılarak çözdürüldü. Ekstraksiyonu yapılan DNA örnekleri amplifikasyon işlemleri yapılana kadar -20 C de template DNA olarak kullanılmak üzere saklandı. Amplifikasyon Primerler Çalışmada hemoliz için hlya, Tip 1 fimbria için fimh, P fimbria için papef, aerobaktin demir sideroforlarının varlığı için iucd, sitotoksik nekrotizan faktör 1 için cnf1, serum dirençliliği için trat genlerinin varlığını araştırmak amacıyla ilgili genlere spesifik olarak sentezletilen ticari primer çiftleri kullanıldı. Kullanılan primerlerin baz dizileri, ilgili gen bölgeleri, ürün uzunlukları ve primerlerin alındığı kaynaklar Çizelge 2.3. de sunulmuştur.
48 38 Çizelge Primerlerlerin baz dizileri, bağlandıkları spesifik gen bölgeleri, PCR ürünlerinin uzunlukları ve primerlerin alındığı kaynaklar. Primer Sekans Hedef Gen Ürün Uzunluğu Kaynaklar TraT1 TraT2 5 - GATGGCTGAACCGTGGTTATG CACACGGGTCTGGTATTTATGC -3 TraT 307 bp Kaipainen ve ark., 2002 Pap3 Pap4 5 - GCAACAGCAACGCTGGTTGCATCAT AGAGAGAGCCACTCTTATACGGACA -3 papef 336 bp Yamamoto ve ark., 1995 Cnf1 Cnf2 5 - AAGATGGAGTTTCCTATGCAGGAG CATTCAGAGTCCTGCCCTCATTATT -3 cnf1 498 bp Yamamoto ve ark., 1995 FimH1 FimH2 5 - TGCAGAACGGATAAGCCGTGG GCAGTCACCTGCCCTCCGTGG -3 fimh 508 bp Johnson ve Stell, Aer1 Aer2 5 - TACCGGATTGTCATATGCAGACCGT AATATCTTCCTCCAGTCCGGAGAAG -3 iucd 602 bp Yamamoto ve ark., 1995 Hly1 Hly2 5 - AACAAGGATAAGCACTGTTCTGGCT ACCATATAAGCGGTCATTCCCGTCA -3 hlya 1177 bp Yamamoto ve ark., 1995 PCR Karışımı PCR karışımı her bir örnek için 25 µl lik final hacimde olacak şekilde aşağıdaki gibi hazırlandı ; 2,5 µl 10 x PCR tamponu (Fermentas, Litvanya), 2 µl MgCl 2 (Fermentas, Litvanya), 0,5 µl 10 mm dntp (Fermentas, Litvanya), 0,2 µl Primer I, 0,2 µl Primer II (Operon, Almanya), 0,2 µl Taq DNA Polimeraz (Fermentas, Litvanya) ve DEPC water (Fermentas, Litvanya) ile 23 µl lik hacme tamamlandı. Bu karışımdan her bir tüpe 23 µl konuldu ve üzerine 2 µl örneğe ait template DNA eklenerek toplam 25 µl lik final hacim hazırlandı.
49 39 Amplifikasyon İşlemi Amplifikasyon işlemi hlya, papef, iucd, cnf1 gen bölgelerinin saptanması için Yamamoto ve ark. (1995) nın belirttiği protokol modifiye edilerek ve fimh için ise Johnson ve Stell (2000) in belirttiği protokole göre yapıldı. Buna göre amplifikasyon işlemi sırasıyla; 94 C de 3 dk. bekletilerek ön denatürasyon, 94 C de 60 sn. denaturasyon, 63 C de 60 sn. primer bağlanması, 72 C de 120 sn. ekstensiyon aşamasını içeren 30 siklustan oluştu. En son aşamada 72 C de 7 dk. bekletilerek reaksiyon sonlandırıldı. trat gen bölgesinin saptanması amacıyla ise Kaipainen ve ark. (2002) nın belirttiği protokol modifiye edilerek uygulandı. Buna göre amplifikasyon işlemi sırasıyla 94 C de 3 dk. bekletilerek ön denatürasyon, 94 C de 60 sn. denatürasyon, 60 C de 60 sn. primer bağlanması, 72 C de 120 sn. ekstensiyon aşamasını içeren 30 siklustan oluştu. En son aşamada 72 C de 7 dk. bekletilerek reaksiyon tamamlandı. Elektroforez Amplifiye edilen her örnekten 10 µl alınıp 2 µl 6xLoading Dye solüsyonu ile karıştırılarak, 20 cm lik %1,5 luk agoroz (Prona, EU) jele yüklendi. Jeldeki birinci göze 4 µl DNA Marker (Gene Ruler 100 bp DNA Ladder Plus, Fermantas, Litvanya) konularak 160 Volt ta 70 dk. elektroforez işlemi gerçekleştirildi (Sambrook ve Russell, 2002). Örneklerin Görüntülenmesi Biyo-görüntüleme sistemi (Gene Genius, Syngene, İngiltere) kullanılarak jeldeki örnekler görüntülendi.
50 40 3. BULGULAR 3.1. İzolasyon ve İdentifikasyon Bulguları Bu çalışmada yılları arasında Ankara Üniversitesi Veteriner Fakültesi Mikrobiyoloji Anabilim Dalı na çeşitli işletmelerden gönderilen mastitis şüpheli sütler ile Ankara (işletme B ve işletme E), Balıkesir (işletme A ve işletme D) ve Çorum (işletme C) daki ticari süt sığırcılığı yapan işletmelerden sağlanan mastitis şüpheli sütlerle birlikte toplam 1027 adet süt örneği ile 55 adet rektal svap ve 45 adet altlık materyali kullanıldı. Mastitis şüpheli süt örneklerinden 92 adet, rektal svaplardan 46 ve altlık örneklerinden 38 adet olmak üzere toplam 176 adet E. coli suşu izole ve identifiye edilerek virulens özellikleri incelendi (Çizelge 3.1. ve Çizelge 3.2.). Çizelge 3.1. İncelenen süt örneklerinde E. coli izolasyon bulguları Yetiştirici Tipi Mastitis Şüpheli Süt Örneği Sayısı İzole Edilen E. coli sayısı A Ticari Süt Sığırcılığı İşletmesi B C D E 16 0 Aile İşletmesi 17 5 Toplam
51 41 Çizelge 3.2. İncelenen rektal svap ve altlık örneklerinde E. coli izolasyon bulguları Örnek Alınan İşletme İşletme A Alınan Örnek Türü Alınan Örnek Sayısı İzole Edilen E. coli sayısı Rektal Svap Altlık İşletme B Rektal Svap Altlık Virulens Faktörlere Ait Bulgular Hemoliz Bulguları İzole edilen E. coli suşlarının kanlı agarda incelenmesi sonucunda mastitisli sütlerden izole edilen suşlardan 5 (%5,4) inde, rektal suşlardan 3 (%6,5) ünde ve altlık suşlarından 3 (%7,8) ünde olmak üzere tüm suşların 11 (%6,2) inde hemolitik aktivite saptandı. Sonuçlar Çizelge 3.3. de gösterildi. Çizelge 3.3. İncelenen E. coli suşlarında virulens faktörlere ait fenotipik bulgular Materyal Türü Suş Sayısı Hemoliz Hemaglütinasyon Aerobaktin Kolisin Serum Dirençliliği Süt 92 5 (%5,4) 35 (%38,0) 12 (%13,0) 1 (%1,0) 92 (%100) Rektal svap 46 3 (%6,5) 7 (%15,2) 3 (%6,5) 1 (%2,1) 46 (%100) Altlık 38 3 (%7,8) 3 (%7,8) 3 (%7,8) 0 (%0) 38 (%100) Toplam (%) (%6,2) 45 (%25,5) 18 (%10,2) 2 (%1,1) 176 (%100)
52 Hemaglütinasyon Bulguları Süt, rektal svap ve altlık örneklerinden izole edilen E. coli suşlarının hemaglütinasyon aktiviteleri koyun, sığır ve kanatlı eritrositleri kullanılarak incelendi. Toplam 176 adet E. coli suşundan 45 i (%25,5) farklı hayvan eritrositlerini farklı oranlarda hemaglütine etti (Çizelge 3.3.). Sığır eritrositleri ile suşların 8 (%4,5) i MSHA ve 7 (%3,9) si MRHA, koyun eritrositleri ile suşların 4 (%2,2) ü MSHA ve 4 (%2,2) ü MRHA, kanatlı eritrositleri ile suşların 8 (%4,5) i MSHA ve 14 (%7,9) ü MRHA olarak saptandı. İncelenen suşların izole edildikleri materyal ve kullanılan eritrosit türüne göre MSHA ve MRHA özellikleri ve oranları Çizelge 3.4. de sunuldu. Çizelge 3.4. E. coli suşlarının izole edildikleri materyal ve kullanılan eritrosit türüne göre MSHA ve MRHA bulguları Materyal Türü Suş Sayısı Kullanılan Eritrosit Türü Sığır Eritrositi Koyun Eritrositi Kanatlı Eritrositi MSHA MRHA MSHA MRHA MSHA MRHA Süt 92 8 (%8,6) 6 (%6,5) 3 (%3,2) 4 (%4,3) 3 (%3,2) 11(%11,9) Rektal svap 46 0 (%0) 1 (%2,1) 1 (%2,1) 0 (%0) 3 (%6,5) 2 (%4,3) Altlık 38 0 (%0) 0 (%0) 0 (%0) 0(%0) 2 (%5,2) 1 (%2,6) Toplam (%4,5) 7 (%3,9) 4 (%2,2) 4 (%2,2) 8 (%4,5) 14(%7,9) Aerobaktin Demir Elde Etme Sistemine Ait Bulgular İzole ve identifiye edilen E. coli suşlarından 18 (%10,2) i, 2,2 - dipyridil ilave edilerek hazırlanan M9 besiyerinde üreme göstererek aerobaktin demir elde etme sistemine sahip olarak değerlendirildi (Çizelge 3.3.).
53 Vero Hücrelerde Toksik Etkiye Ait Bulgular Vero hücrelerde toksik etkinin incelenmesi amacıyla farklı işletmelere ait, farklı fenotipik ve moleküler özellikleri gösteren suşlardan örnekleme ile seçilen 22 si süt, 10 u rektal svap ve 8 i altlık orijinli toplam 40 adet E. coli suşundan 3 ü süt örneği orijinli ve 1 i rektal svap orijinli toplam 4 (%10) adet E. coli suşunun Vero hücre kültüründe toksik etkiye yol açarak hücrelerde morfolojik değişikliklere ve ayrılmalara neden olduğu saptandı. Normal Vero hücrelerinin ve toksinin etkilediği hücrelerin mikroskobik görünümü Şekil 3.1.a. ve 3.1.b. de sunuldu. Şekil 3.1.a. Vero hücrelerin normal görünümü (x20) Şekil 3.1.b. Toksinden etkilenen Vero hücreleri (x20) Serum Dirençliliği Bulguları Sığır ve koyun serumlarının kullanıldığı testte süt, rektal svap ve altlık örneklerinden izole ve identifiye edilen E. coli suşlarının tümü kullanılan serum çeşitlerinin tamamına karşı serum dirençli olarak bulundu (Çizelge 3.3.).
54 Kolisin Bulguları Kolisin duyarlı E. coli K12 suşu kullanılarak kolisin sentezleme durumu incelenen E. coli suşlarından 1 (%1,0) i süt örneği ve 1 (%2,1 i de rektal svapdan izole ve identifiye edilen 2 (%1,1) adet E. coli suşunun kolisin ürettiği saptandı. Kolisin üreten bu 2 suş kullanılarak yapılan çaprazlamalarda ise 1 i süt, 3 ü rektal svapdan izole ve identifiye edilen 4 adet (%2,2) E. coli suşunun duyarlı olduğu belirlendi (Çizelge 3.3.). Yapılan çalışmalar sonucu fenotipik olarak elde edilen verilerin materyal türü de dikkate alınarak işletmelere göre dağılımı Çizelge 3.5. ve 3.6 da sunuldu. Çizelge 3.5. İşletme A için fenotipik test sonuçları Materyal Türü Suş Sayısı Hemoliz Hemaglütinasyon Aerobaktin Kolisin Serum Dirençliliği Süt 75 4 (%5,3) 28 (%37,3) 11 (%14,6) 1 (%1,3) 75 (%100) Rektal svap 26 2 (%7,6) 5 (%19,2) 2 (%7,6) 1 (%3,8) 26 (%100) Altlık 21 2 (%9,5) 2 (%9,5) 2 (%9,5) 0 (%0) 21 (%100) Toplam (%) (%6,5) 35 (%28,6) 15 (%12,2) 2 (%1,6) 122 (%100) Materyallerin sağlandığı A işletmesinde mastitis şüpheli sütlerden izole edilen 75 adet suşdan 4 (%5,3) ünde, 26 adet rektal suşdan 2 (%7,6) sinde ve 21 adet altlık suşundan 2 (%9,5) sinde olmak üzere bu işletmeden izole edilen 122 adet suşun 8 (%6,5) inde hemolitik aktivite belirlendi. Sütlerden izole edilen suşların 28 (%37,3) i, rektal suşların 5 (%19,2) i, altlık suşlarının 2 (%9,5) si ve tüm suşların 35 (%28,6) i hemaglütinasyon özelliği gösterdi. İşletmeden izole edilen süt orijinli suşlardan 11 (%14,6) i, rektal suşlardan 2 (%7,6) si, altlık suşlarından 2 (%9,5) si ve tüm suşların 15 (%12,2) i demir kısıtlayıcı madde içeren besiyerinde üredi. Suşlardan 1 (%1,3) i süt örneği orijinli ve 1 (%3,8) i de rektal orijinli olmak üzere tüm suşlardan 2 (%1,6) sinde kolisin üretimi saptandı. Kolisin üreten bu iki suşla
55 45 yapılan çaprazlamalarda ise yine aynı işletmeye ait olan 1 (%1,3) i süt örneğinden ve 3 (%11,5) i rektal svaptan izole edilen 4 (%3,2) adet E. coli suşunun kolisin duyarlı olduğu belirlendi. İşletmeye ait süt, rektal svap ve altlık örneklerinden izole edilen 122 adet suşun tamamı (%100) kullanılan tüm serum çeşitlerine karşı serum dirençli olarak bulundu (Çizelge 3.5.). Ayrıca Vero hücrelerde toksik etki gösteren 4 E. coli suşu (3 ü süt, 1 i rektal svap orijinli) bu işletmeden izole edildi. Çizelge 3.6. İşletme B için fenotipik test sonuçları Materyal Türü Suş Sayısı Hemoliz Hemaglütinasyon Aerobaktin Kolisin Serum Dirençliliği Süt 10 1 (%10,0) 4 (%40,0) 1 (%10,0) 0 (%0) 10 (%100) Rektal svap 20 1 (%5,0) 2 (%10,0) 1 (%5,0) 0 (%0) 20 (%100) Altlık 17 1 (%5,8) 1 (%5,8) 1 (%5,8) 0 (%0) 17 (%100) Toplam (%) 47 3 (%6,3) 7 (%14,8) 3 (%6,3) 0 (%0) 47 (%100) Materyal alınan B işletmesinden ise 47 adet E. coli suşu izole edildi (Çizelge 3.6.). Süt örneğinden izole edilen 10 adet E. coli suşundan 1 (%10,0) i, 20 adet rektal suşdan 1 (%5,0) i ve 17 adet altlık suşundan 1 (%5,8) i olmak üzere toplam 3 (%6,3) suşda hemolitik aktivite gözlendi. İzole edilen suşlardan 4 (%40) ü süt örneği, 2 (%10,0) si rektal ve 1 (%5,8) i altlık orijinli 7 (%14,8) suş hemaglütinasyon özelliği gösterdi. İncelenen suşlarda kolisin (%0) aktivitesine rastlanılmazken, süt örneklerinden izole edilen suşlarından 1 (%10,0) i, rektal suşlardan 1 (%5,0) i, altlık suşlarından 1 (%5,8) i ve dolayısıyla tüm suşlardan 3 (%6,3) ü demir kısıtlı besiyerinde üredi. İşletmeden izole edilen suşların tamamı (%100) serum dirençli olarak bulundu. Ayrıca, bu işletmeden Vero hücrelerde toksik etkisi incelenmek üzere seçilen E. coli suşlarının hiçbirinde toksik aktivite gözlenmedi
56 PCR Bulguları Süt, rektal svap ve altlık örneklerinden izole ve identifiye edilen E. coli suşları hemoliz, Tip 1 fimbria, P fimbria, aerobaktin demir elde etme sisteminin varlığı, serum dirençliliği ve sitotoksik nekrotizan faktör 1 yönünden PCR ile incelendi. Sırası ile bu virulens faktörlerin kodlanmasında rol oynayan hlya, fimh, papef, iucd, trat ve cnf1 genlerinin varlığı araştırıldı (Çizelge 3.7). Çizelge 3.7. PCR sonuçları Materyal Türü Suş Sayısı hlya fimh papef iucd cnf1 trat Süt 92 5 (%5,4) 1 (%1,0) 1 (%1,0) 8 (%8,6) 0 (%0) 44 (%47,8) Rektal svap 46 3 (%6,5) 0 (%0) 0 (%0) 3 (%6,5) 0 (%0) 21 (%45,6) Altlık 38 3 (%7,8) 0 (%0) 0 (%0) 3 (%7,8) 0 (%0) 16 (%42,1) Toplam (%) (%6,2) 1 (%0,5) 1 (%0,5) 14 (%7,9) 0 (%0) 81 (%46,0) Çalışmada hemoliz özelliği ile ilişkili olan hlya geni 5 (%5,4) i süt, 3 (%6,5) ü rektal svap, 3 (%7,8) ü altlık orijinli toplam 11 adet E. coli (%6,2) suşunda saptandı (Şekil 3.2.). M bp hlya 1177 bp Şekil 3.2. PCR sonucunda jel elektroforezde hlya pozitif için örnek görüntü. M: Marker (100 bp), 1.Negatif kontrol, 2. Pozitif kontrol, 3. Pozitiflik saptanan örnek.
57 47 Mannoz duyarlı hemaglütinasyonda rol oynayan Tip 1 fimbria ile ilişkili fimh geni yalnızca süt orijinli 1 (%1,0) E. coli suşunda saptandı. Buna göre MSHA şekillendiren 20 adet suşda %5, mastitisli süt örneklerinden izole edilen MSHA pozitif 14 adet suşda ise % 7,1 oranında fimh geni bulundu (Şekil 3.3.). M bp fimh 508 bp Şekil 3.3. PCR sonucunda jel elektroforezde fimh pozitif için örnek görüntü. M: Marker (100 bp), 1.Negatif kontrol, 2. Pozitif kontrol, 4. Pozitiflik saptanan örnek. P fimbria ile ilişkili papef geni süt orijinli 1 (%1,0) E. coli suşunda belirlendi. MRHA şekillendiren 25 adet suşda %4,0 ve süt örneklerinden izole edilen 21 adet MRHA pozitif suşda ise %4,7 oranında papef geni saptandı (Şekil 3.4.). M bp papef 336 bp Şekil 3.4. PCR sonucunda jel elektroforezde papef pozitif için örnek görüntü. M: Marker (100 bp), 1.Negatif kontrol, 2. Pozitif kontrol, 6. Pozitiflik saptanan örnek.
58 48 Aerobaktin demir elde etme sistemi ile ilişkili iucd geni mastitis şüpheli süt orijinli E. coli suşlarından 8 (%8,6) inde, rektal suşlardan 3 (%6,5) ünde ve altlık suşlarından 3 (%7,8) ünde olmak üzere tüm suşların 14 (%7,9) ünde saptandı (Şekil 3.5.). M bp iucd 602 bp Şekil 3.5. PCR sonucunda jel elektroforezde iucd pozitif için örnek görüntü. M: Marker (100 bp), 1.Negatif kontrol, 2. Pozitif kontrol, 5. Pozitiflik saptanan örnek. Serum dirençliliği ile ilişkili olan trat geni mastitis şüpheli sütlerden izole edilen E. coli suşlarından 44 (%47,8) ünde, rektal suşların 21 (%45,6) inde ve altlıktan izole edilen suşların 16 (%42,1) sında olmak üzere toplam 81 (%46,0) inde bulundu (Şekil 3.6). M bp trat 307 bp Şekil 3.6. PCR sonucunda jel elektroforezde trat pozitif için örnek görüntü. M:Marker (100 bp). 1. Negatif kontrol, 2. Pozitif kontrol. 3, 7, 9, 12 Pozitiflik saptanan örnekler.
59 49 Çalışmada izole ve identifiye edilen E. coli suşlarının hiçbirinde sitotoksik nekrotizan faktör 1 ile ilişkili olan cnf1 geninin varlığına rastlanılmadı (Şekil 3.7.). M bp cnf bp Şekil 3.7. PCR sonucunda jel elektroforezde cnf 1 pozitif için örnek görüntü. M: Marker (100 bp), 1. Negatif kontrol, 2. Pozitif kontrol. Yapılan çalışmalar sonucu moleküler olarak elde edilen verilerin materyal türü de dikkate alınarak işletmelere göre dağılımı Çizelge 3.8 ve 3.9 da sunuldu. Çizelge 3.8. İşletme A için moleküler test sonuçları Materyal Türü Suş Sayısı hlya fimh papef iucd cnf1 trat Süt 75 4 (%5,3) 1 (%1,3) 1 (%1,3) 7 (%9,3) 0 (%0) 33 (%44,0) Rektal svap 26 2 (%7,6) 0 (%0) 0 (%0) 2 (%7,6) 0 (%0) 12 (%46,1) Altlık 21 2 (%9,5) 0 (%0) 0 (%0) 2 (%9,5) 0 (%0) 9 (%42,8) Toplam (%) (%6,5) 1 (%0,8) 1 (%0,8) 11 (%9,0) 0 (%0) 54 (%44,2) Materyal alınan A işletmesinde süt örneğinden izole edilen 75adet suşdan 4 (%5,3) ü, 26 adet rektal suşdan 2 (%7,6) si, 21 adet altlık suşundan 2 (%9,5) si olmak üzere 122 adet suşun 8 (%6,5) i hlya pozitif bulundu. Fimbria ile ilişkili olan fimh ve papef genleri yalnızca 1 er adet süt orijinli suşda (%0,8) saptandı. Süt
Enterobakteriler. Dr. Kaya Süer. YDÜ Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD
 Enterobakteriler Dr. Kaya Süer YDÜ Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Enterobakteriler Nerelerde bulunur? Toprak, Su, Sebze-meyve İnsan ve Hayvan bağırsak florası Enterobaktriler
Enterobakteriler Dr. Kaya Süer YDÜ Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Enterobakteriler Nerelerde bulunur? Toprak, Su, Sebze-meyve İnsan ve Hayvan bağırsak florası Enterobaktriler
ENTEROBAKTERİ İNFEKSİYONLARI
 ENTEROBAKTERİ İNFEKSİYONLARI 1 Escherichia Salmonella Klebsiella Enterobacter Morganella Proteus Providencia Serratia Shigella Yersinia ENTEROBACTERIACEAE AİLESİ 2 Escherichia coli nin neden olduğu infeksiyonlar
ENTEROBAKTERİ İNFEKSİYONLARI 1 Escherichia Salmonella Klebsiella Enterobacter Morganella Proteus Providencia Serratia Shigella Yersinia ENTEROBACTERIACEAE AİLESİ 2 Escherichia coli nin neden olduğu infeksiyonlar
ENTEROBAKTERİ İNFEKSİYONLARI
 ENTEROBAKTERİ İNFEKSİYONLARI Escherichia Salmonella Klebsiella Enterobacter Morganella Proteus Providencia Serratia Shigella Yersinia ENTEROBACTERIACEAE AİLESİ Escherichia coli Escherichia cinsi Birçok
ENTEROBAKTERİ İNFEKSİYONLARI Escherichia Salmonella Klebsiella Enterobacter Morganella Proteus Providencia Serratia Shigella Yersinia ENTEROBACTERIACEAE AİLESİ Escherichia coli Escherichia cinsi Birçok
Enterohemorajik Escherichia coli nin Gıda Güvenliği Yönünden Önemi
 Enterohemorajik Escherichia coli nin Gıda Güvenliği Yönünden Önemi Escherichia coli Enterobacteriaceae familyasında Gram negatif Mezofil E. coli Min.-Maks. Opt. Sıcaklık( o C) 7-45 37 ph değeri 4.4-9.0
Enterohemorajik Escherichia coli nin Gıda Güvenliği Yönünden Önemi Escherichia coli Enterobacteriaceae familyasında Gram negatif Mezofil E. coli Min.-Maks. Opt. Sıcaklık( o C) 7-45 37 ph değeri 4.4-9.0
İMMUNİZASYON. Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı?
 İMMUNİZASYON Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı? Canlıya antijen verdikten belli bir süre sonra, o canlıda
İMMUNİZASYON Bir bireye bağışıklık kazandırma! Bireyin yaşı? İmmunolojik olarak erişkin mi? Maternal antikor? Konak antijene duyarlı mı? Sağlıklı mı? Canlıya antijen verdikten belli bir süre sonra, o canlıda
ENTERİK BAKTERİLER. Enterik bakteriler barsak florasında bulunan bakterilerdir
 12.Hafta:Enterik Bakteriler ENTERİK BAKTERİLER Enterik bakteriler barsak florasında bulunan bakterilerdir Barsakta yaşayan enterik bakterilerin en klasiği E- coli dir ve non-patojendir.yine barsakta yaşayan
12.Hafta:Enterik Bakteriler ENTERİK BAKTERİLER Enterik bakteriler barsak florasında bulunan bakterilerdir Barsakta yaşayan enterik bakterilerin en klasiği E- coli dir ve non-patojendir.yine barsakta yaşayan
Hücre çeperi (Hücre duvarı)
 Hücre çeperi (Hücre duvarı) Mycoplasmalar dışındaki tüm prokaryotlarda vardır. Görevleri: Bakteriyi kendi iç basıncına karşı korur(hücre içi ozmotik basıncı % 10-20 sakkaroz çözeltisi yoğunluğuna eşittir).
Hücre çeperi (Hücre duvarı) Mycoplasmalar dışındaki tüm prokaryotlarda vardır. Görevleri: Bakteriyi kendi iç basıncına karşı korur(hücre içi ozmotik basıncı % 10-20 sakkaroz çözeltisi yoğunluğuna eşittir).
Salmonella. XLT Agar'da Salmonella (hidrojen sülfür oluşumuna bağlı olarak siyah) ve Citrobacter (sarı) kolonileri
 Enterobacteriaceae İnsan sağlığı açısından en önemli bakteri ailesidir. Doğal ortamları insan ve hayvan bağırsaklarıdır. Tipik klinik semptomlarla seyreden hastalığın (tifo, basilli dizanteri, veba) etkeni
Enterobacteriaceae İnsan sağlığı açısından en önemli bakteri ailesidir. Doğal ortamları insan ve hayvan bağırsaklarıdır. Tipik klinik semptomlarla seyreden hastalığın (tifo, basilli dizanteri, veba) etkeni
Takım: Bacillales Familya: Staphylococcaceae Genus: Staphylococcus
 Staphylococcus Takım: Bacillales Familya: Staphylococcaceae Genus: Staphylococcus Gram pozi:f kok Düzensiz yığınlar oluşturmaya eğilimli Kokların çapı yaklaşık 1 µm Fakülta:f anaerob (fermenta:f) Katalaz
Staphylococcus Takım: Bacillales Familya: Staphylococcaceae Genus: Staphylococcus Gram pozi:f kok Düzensiz yığınlar oluşturmaya eğilimli Kokların çapı yaklaşık 1 µm Fakülta:f anaerob (fermenta:f) Katalaz
İlk «sarı renkli koliform» olarak 1929 da rapor edildi
 Tarihçe İlk «sarı renkli koliform» olarak 1929 da rapor edildi Bebekte septisimiyaya neden olmuştur 1958 ve 1961 de İngiltere de yine iki ölümcül menenjit vakasına neden olmuştur Enterobacter sakazakii
Tarihçe İlk «sarı renkli koliform» olarak 1929 da rapor edildi Bebekte septisimiyaya neden olmuştur 1958 ve 1961 de İngiltere de yine iki ölümcül menenjit vakasına neden olmuştur Enterobacter sakazakii
MASTĠTĠSLĠ SÜTLERDEN ĠZOLE EDĠLEN ESCHERİCHİA COLİ SUġLARINDA VĠRÜLENS GENLERĠN ARAġTIRILMASI
 T.C. ADNAN MENDERES ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ MĠKROBĠYOLOJĠ YÜKSEK LĠSANS PROGRAMI MASTĠTĠSLĠ SÜTLERDEN ĠZOLE EDĠLEN ESCHERİCHİA COLİ SUġLARINDA VĠRÜLENS GENLERĠN ARAġTIRILMASI NERGĠZ VURUCU
T.C. ADNAN MENDERES ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ MĠKROBĠYOLOJĠ YÜKSEK LĠSANS PROGRAMI MASTĠTĠSLĠ SÜTLERDEN ĠZOLE EDĠLEN ESCHERİCHİA COLİ SUġLARINDA VĠRÜLENS GENLERĠN ARAġTIRILMASI NERGĠZ VURUCU
ENTEROBACTERIACEAE FAMİLYASI
 ENTEROBACTERIACEAE FAMİLYASI GENEL ÖZELLİKLER Gram nega;f Çomak Sporsuz Aerobik veya Fakülta;f anaerob Genellikle Haraketli( S. Pullorum ve S. Gallinarum hariç) Katalaz pozi;f; Oksidaz Nega;f FAMİLYA:
ENTEROBACTERIACEAE FAMİLYASI GENEL ÖZELLİKLER Gram nega;f Çomak Sporsuz Aerobik veya Fakülta;f anaerob Genellikle Haraketli( S. Pullorum ve S. Gallinarum hariç) Katalaz pozi;f; Oksidaz Nega;f FAMİLYA:
DOMUZ PLEUROPNEUMONİSİ. Dr. Kemal METİNER
 DOMUZ PLEUROPNEUMONİSİ Dr. Kemal METİNER Ekonomik kayıp Solunum güçlüğü Büyüme geriliği Akut formda ölüm ETİYOLOJİ Actinobacillus pleuropneumoniae Gram negatif, kokobasil ETİYOLOJİ Biyotipleri: Biyotip
DOMUZ PLEUROPNEUMONİSİ Dr. Kemal METİNER Ekonomik kayıp Solunum güçlüğü Büyüme geriliği Akut formda ölüm ETİYOLOJİ Actinobacillus pleuropneumoniae Gram negatif, kokobasil ETİYOLOJİ Biyotipleri: Biyotip
MEME LOBU YANGISI. süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri. süt endüstrisinde önemli ekonomik kayıp
 MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp 2 HAYVAN Sağlığı fonksiyonel meme lobunun kaybı
MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp 2 HAYVAN Sağlığı fonksiyonel meme lobunun kaybı
MEME LOBU YANGISI. süt endüstrisinde önemli ekonomik kayıp. süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek.
 MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp fonksiyonel meme lobunun kaybı hayvanın ölümü
MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp fonksiyonel meme lobunun kaybı hayvanın ölümü
İzolasyon ve İdentifikasyon
 İzolasyon ve İdentifikasyon (9. Hafta) 1 İzolasyon : Ayırmak İzolasyon Mikrobiyolojide izolasyon? Hangi amaçlarla izolasyon yapılır? Endüstriyel mikroorganizmalar Bozulma ve/veya hastalık etmeni mikroorganizmalar
İzolasyon ve İdentifikasyon (9. Hafta) 1 İzolasyon : Ayırmak İzolasyon Mikrobiyolojide izolasyon? Hangi amaçlarla izolasyon yapılır? Endüstriyel mikroorganizmalar Bozulma ve/veya hastalık etmeni mikroorganizmalar
E.COLI İNFEKSİYONLARI
 E.COLI İNFEKSİYONLARI Etiyoloji E. coli Enterobacteriaceae familyasının Escherichia genusu Gram negatif sporsuz Genellikle hareketli Bazı suşlar da kapsüllü Kanatlılarda hastalık yapan E. coli lere Avian
E.COLI İNFEKSİYONLARI Etiyoloji E. coli Enterobacteriaceae familyasının Escherichia genusu Gram negatif sporsuz Genellikle hareketli Bazı suşlar da kapsüllü Kanatlılarda hastalık yapan E. coli lere Avian
Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması
 Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması Aycan Gundogdu, Ph.D. Erciyes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim
Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması Aycan Gundogdu, Ph.D. Erciyes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim
Gram (+)Bakterilerde Duvar Yapısı Gram (-) Bakterilerde Duvar Yapısı Lipopolisakkaritin Önemi
 Gram (+)Bakterilerde Duvar Yapısı Çoğunluğu peptidoglikan yapıdır. Bunun yanında teikoik asitte içerirler. Bu yapı gliserol veya Ribitolün PO4 gruplarına bağlanmasıyla oluşur. Teikoik asitler peptidoglikan
Gram (+)Bakterilerde Duvar Yapısı Çoğunluğu peptidoglikan yapıdır. Bunun yanında teikoik asitte içerirler. Bu yapı gliserol veya Ribitolün PO4 gruplarına bağlanmasıyla oluşur. Teikoik asitler peptidoglikan
Staphylococcus türleri ile ilgili genel bilgiler ve analiz yöntemleri klinik mikrobiyoloji ve gıda mikrobiyolojisi bölümlerinde de bulunmaktadır.
 Staphylococcus 01. Genel Bilgiler 02. Etiyoloji 03. Epidemiyoloji 04. Hastalık belirtileri 05. Laboratuvar Tanısı 05.01. Bakteriyoskopi 05.02. Kültür 05.03. Hayvan Deneyi 05.04. Serolojik Testler 05.05.
Staphylococcus 01. Genel Bilgiler 02. Etiyoloji 03. Epidemiyoloji 04. Hastalık belirtileri 05. Laboratuvar Tanısı 05.01. Bakteriyoskopi 05.02. Kültür 05.03. Hayvan Deneyi 05.04. Serolojik Testler 05.05.
ANTRAKS (ŞARBON) septisemik, bulaşıcı, zoonoz
 ANTRAKS (ŞARBON) septisemik, bulaşıcı, zoonoz ÖLÜMden hemen önce ya da sonra doğal boşluklardan KAN PIHTILAŞMAMA KOYU RENK alma DALAKta büyüme ÖDEM ETİYOLOJİ Bacillus anthracis Gram pozitif kapsüllü *
ANTRAKS (ŞARBON) septisemik, bulaşıcı, zoonoz ÖLÜMden hemen önce ya da sonra doğal boşluklardan KAN PIHTILAŞMAMA KOYU RENK alma DALAKta büyüme ÖDEM ETİYOLOJİ Bacillus anthracis Gram pozitif kapsüllü *
SALMONELLA ARANMASI. a. GENEL ÖZELLİKLERİ
 SALMONELLA ARANMASI a. GENEL ÖZELLİKLERİ Enterobacteriaceae familyasına ait, Gram negatif, spor oluşturmayan, fakültatif anaerob, çubuk formunda olup, çoğu (S.pullorum, S.gallinarum ve S.arizonea türleri
SALMONELLA ARANMASI a. GENEL ÖZELLİKLERİ Enterobacteriaceae familyasına ait, Gram negatif, spor oluşturmayan, fakültatif anaerob, çubuk formunda olup, çoğu (S.pullorum, S.gallinarum ve S.arizonea türleri
DİYARELİ OLGULARDAN ELDE EDİLEN DIŞKI ÖRNEKLERİNDE E. COLİ O157: H7 ARAŞTIRILMASI
 DİYARELİ OLGULARDAN ELDE EDİLEN DIŞKI ÖRNEKLERİNDE E. COLİ O157: H7 ARAŞTIRILMASI Fatma Nesime GELEN Mikrobiyoloji Anabilim Dalı Tez Danışmanı Prof. Dr. Halil YAZGI Yüksek Lisans Tezi- 2014 T.C. ATATÜRK
DİYARELİ OLGULARDAN ELDE EDİLEN DIŞKI ÖRNEKLERİNDE E. COLİ O157: H7 ARAŞTIRILMASI Fatma Nesime GELEN Mikrobiyoloji Anabilim Dalı Tez Danışmanı Prof. Dr. Halil YAZGI Yüksek Lisans Tezi- 2014 T.C. ATATÜRK
GIDALARDA ÖNEMLİ MİKRO ORGANİZMALAR: Gıdalarda önem taşıyan mikroorganizmalar; bakteriler, funguslar (maya-küf) ve virüslerdir.
 GIDALARDA ÖNEMLİ MİKRO ORGANİZMALAR: Gıdalarda önem taşıyan mikroorganizmalar; bakteriler, funguslar (maya-küf) ve virüslerdir. Bu mikroorganizmalardan; bakteriler ve funguslar gıdalarda çoğalarak gıdaların
GIDALARDA ÖNEMLİ MİKRO ORGANİZMALAR: Gıdalarda önem taşıyan mikroorganizmalar; bakteriler, funguslar (maya-küf) ve virüslerdir. Bu mikroorganizmalardan; bakteriler ve funguslar gıdalarda çoğalarak gıdaların
KEDİ VE KÖPEKLERİN ÜROGENİTAL SİSTEM İNFEKSİYONLARINDAN İZOLE EDİLEN ESCHERICHIA COLI LERİN VİRULENS FAKTÖRLERİNİN BELİRLENMESİ
 TÜRKĠYE CUMHURĠYETĠ ANKARA ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ KEDİ VE KÖPEKLERİN ÜROGENİTAL SİSTEM İNFEKSİYONLARINDAN İZOLE EDİLEN ESCHERICHIA COLI LERİN VİRULENS FAKTÖRLERİNİN BELİRLENMESİ Orkun
TÜRKĠYE CUMHURĠYETĠ ANKARA ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ KEDİ VE KÖPEKLERİN ÜROGENİTAL SİSTEM İNFEKSİYONLARINDAN İZOLE EDİLEN ESCHERICHIA COLI LERİN VİRULENS FAKTÖRLERİNİN BELİRLENMESİ Orkun
Diyabette Bakteri Endotel İlişkisi ve Bakteriyel Adherans. Doç. Dr. Hüseyin BASKIN Dokuz Eylül Üniversitesi Tıp Fakültesi Mikrobiyoloji Anabilim Dalı
 Diyabette Bakteri Endotel İlişkisi ve Bakteriyel Adherans Doç. Dr. Hüseyin BASKIN Dokuz Eylül Üniversitesi Tıp Fakültesi Mikrobiyoloji Anabilim Dalı Diyabette Bakteri Endotel İlişkisi ve Bakteriyel Adherans
Diyabette Bakteri Endotel İlişkisi ve Bakteriyel Adherans Doç. Dr. Hüseyin BASKIN Dokuz Eylül Üniversitesi Tıp Fakültesi Mikrobiyoloji Anabilim Dalı Diyabette Bakteri Endotel İlişkisi ve Bakteriyel Adherans
MİKROBİYOLOJİ SORU KAMPI 2015
 Canlıların prokaryot ve ökoaryot olma özelliğini hücre komponentlerinden hangisi belirler? MİKROBİYOLOJİ SORU KAMPI 2015 B. Stoplazmik membran C. Golgi membranı D. Nükleer membran E. Endoplazmik retikulum
Canlıların prokaryot ve ökoaryot olma özelliğini hücre komponentlerinden hangisi belirler? MİKROBİYOLOJİ SORU KAMPI 2015 B. Stoplazmik membran C. Golgi membranı D. Nükleer membran E. Endoplazmik retikulum
BAKTERİLERDE EKSTRAKROMOZAL GENETİK ELEMENTLER
 BAKTERİLERDE EKSTRAKROMOZAL GENETİK ELEMENTLER Plazmid ve Epizomlar Bakterilerin kendi kromozomlarının yanı sıra, kromozom dışı bazı genetik parçacıklar bulunmaktadır Bakteri kromozomundan daha küçük yapıda
BAKTERİLERDE EKSTRAKROMOZAL GENETİK ELEMENTLER Plazmid ve Epizomlar Bakterilerin kendi kromozomlarının yanı sıra, kromozom dışı bazı genetik parçacıklar bulunmaktadır Bakteri kromozomundan daha küçük yapıda
Enzimlerinin Saptanmasında
 Gram Negatif Bakterilerde Karbapenemaz Enzimlerinin Saptanmasında OXA-48 K-Se T, Blue-Carba Test ve PCR Testlerinin Etkinliğinin Karşılaştırılması Ayham Abulaila, Fatma Erdem, Zerrin Aktaş, Oral Öncül
Gram Negatif Bakterilerde Karbapenemaz Enzimlerinin Saptanmasında OXA-48 K-Se T, Blue-Carba Test ve PCR Testlerinin Etkinliğinin Karşılaştırılması Ayham Abulaila, Fatma Erdem, Zerrin Aktaş, Oral Öncül
Staphylococcus Gram pozitif koklardır.
 Staphylococcus Gram pozitif koklardır. 0.8-1µm çapında küçük, yuvarlak veya oval bakterilerdir. Hareketsizdirler. Spor oluşturmazlar ve katalaz enzimi üretirler. Gram boyama Koagülaz, alfatoksin, lökosidin,
Staphylococcus Gram pozitif koklardır. 0.8-1µm çapında küçük, yuvarlak veya oval bakterilerdir. Hareketsizdirler. Spor oluşturmazlar ve katalaz enzimi üretirler. Gram boyama Koagülaz, alfatoksin, lökosidin,
Pastırmada Enterokoklar
 Pastırmada Enterokoklar Özlem ERTEKİN 1 Güzin KABAN 2 Mükerrem KAYA 2 1 Munzur Üniversitesi Gıda Mühendisliği Bölümü, TUNCELİ 2 Atatürk Üniversitesi Gıda Mühendisliği Bölümü, ERZURUM Laktik asit bakterileri
Pastırmada Enterokoklar Özlem ERTEKİN 1 Güzin KABAN 2 Mükerrem KAYA 2 1 Munzur Üniversitesi Gıda Mühendisliği Bölümü, TUNCELİ 2 Atatürk Üniversitesi Gıda Mühendisliği Bölümü, ERZURUM Laktik asit bakterileri
İnsan ve tüm sıcak kanlı hayvanların kalın bağırsağının normal flora üyesi
 İnsan ve tüm sıcak kanlı hayvanların kalın bağırsağının normal flora üyesi Gram negatif, Fakültatif anaerop, Hareketli bir çomaktır. Genetik olarak heterojen bir grup Özgün virulans faktörlerine sahip
İnsan ve tüm sıcak kanlı hayvanların kalın bağırsağının normal flora üyesi Gram negatif, Fakültatif anaerop, Hareketli bir çomaktır. Genetik olarak heterojen bir grup Özgün virulans faktörlerine sahip
DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER
 DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER 1. Vankomisin Vankomisin, Nocardia Orientalis in (eskiden Streptomyces orientalis olarak bilinen) belli suşlarından elde edilen amfoterik
DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER 1. Vankomisin Vankomisin, Nocardia Orientalis in (eskiden Streptomyces orientalis olarak bilinen) belli suşlarından elde edilen amfoterik
DOMUZ PLEUROPNEUMONİSİ. Dr. Kemal METİNER
 DOMUZ PLEUROPNEUMONİSİ Dr. Kemal METİNER Ekonomik kayıp Solunum güçlüğü Büyüme geriliği Ölüm (perakut ve akut form) ETİYOLOJİ Actinobacillus pleuropneumoniae Gram negatif, kokobasil ETİYOLOJİ Biyotipleri:
DOMUZ PLEUROPNEUMONİSİ Dr. Kemal METİNER Ekonomik kayıp Solunum güçlüğü Büyüme geriliği Ölüm (perakut ve akut form) ETİYOLOJİ Actinobacillus pleuropneumoniae Gram negatif, kokobasil ETİYOLOJİ Biyotipleri:
GIDA KAYNAKLI HASTALIKLAR. Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır.
 GIDA KAYNAKLI HASTALIKLAR Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır. Gıda Enfeksiyonu: Patojen bir m.o ile kontamine olmuş bir gıdanın yenmesi sonucu oluşan
GIDA KAYNAKLI HASTALIKLAR Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır. Gıda Enfeksiyonu: Patojen bir m.o ile kontamine olmuş bir gıdanın yenmesi sonucu oluşan
Mikrobiyolojide Moleküler Tanı Yöntemleri. Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D
 Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
VİROLOJİ -I Antiviral İmmunite
 VİROLOJİ -I Antiviral İmmunite Prof.Dr. Yılmaz Akça Prof.Dr. Feray Alkan Prof.Dr. Aykut Özkul Prof. Dr. Seval Bilge-Dağalp Prof.Dr. M. Taner Karaoğlu Prof.Dr. Tuba Çiğdem Oğuzoğlu DOĞAL SAVUNMA HATLARI-DOĞAL
VİROLOJİ -I Antiviral İmmunite Prof.Dr. Yılmaz Akça Prof.Dr. Feray Alkan Prof.Dr. Aykut Özkul Prof. Dr. Seval Bilge-Dağalp Prof.Dr. M. Taner Karaoğlu Prof.Dr. Tuba Çiğdem Oğuzoğlu DOĞAL SAVUNMA HATLARI-DOĞAL
T.C. Sağlık Bakanlığı Türkiye Halk Sağlığı Kurumu
 1 DIġKI ÖRNEKLERĠNDE SHIGA TOKSĠN OLUġTURAN E. COLI LERĠN SEROTĠP, VĠRÜLANS GENLERĠ VE ANTĠBĠYOTĠKLERE DĠRENÇLERĠNĠN DEĞERLENDĠRĠLMESĠ Dr. Revasiye GÜLEŞEN Mikrobiyoloji Referans Laboratuvarları Daire
1 DIġKI ÖRNEKLERĠNDE SHIGA TOKSĠN OLUġTURAN E. COLI LERĠN SEROTĠP, VĠRÜLANS GENLERĠ VE ANTĠBĠYOTĠKLERE DĠRENÇLERĠNĠN DEĞERLENDĠRĠLMESĠ Dr. Revasiye GÜLEŞEN Mikrobiyoloji Referans Laboratuvarları Daire
VİBRİONACEAE FAMİLYASI. Dr.Tuncer ÖZEKİNCİ D.Ü TIP FAKÜLTESİ TIBBİ MİKROBİYOLOJİ A.D
 VİBRİONACEAE FAMİLYASI Dr.Tuncer ÖZEKİNCİ D.Ü TIP FAKÜLTESİ TIBBİ MİKROBİYOLOJİ A.D Genel Özellikleri Gram negatif basiller Polar flajellası ile hareketli Sporsuz, kapsülsüz Fakültatif anaerop Fermentatif
VİBRİONACEAE FAMİLYASI Dr.Tuncer ÖZEKİNCİ D.Ü TIP FAKÜLTESİ TIBBİ MİKROBİYOLOJİ A.D Genel Özellikleri Gram negatif basiller Polar flajellası ile hareketli Sporsuz, kapsülsüz Fakültatif anaerop Fermentatif
BAL ÜRETİM SÜRECİNDE KRİTİK KONTROL NOKTALARININ BELİRLENMESİ, SEKONDER KONTAMİNASYON KAYNAKLARININ
 BAL ÜRETİM SÜRECİNDE KRİTİK KONTROL NOKTALARININ BELİRLENMESİ, SEKONDER KONTAMİNASYON KAYNAKLARININ ve TEHLİKELERİN TANIMLANMASI, RİSK FAKTÖRLERİNİN VE KORELASYON İLİŞKİLERİNİN ORTAYA KONMASI Hayrettin
BAL ÜRETİM SÜRECİNDE KRİTİK KONTROL NOKTALARININ BELİRLENMESİ, SEKONDER KONTAMİNASYON KAYNAKLARININ ve TEHLİKELERİN TANIMLANMASI, RİSK FAKTÖRLERİNİN VE KORELASYON İLİŞKİLERİNİN ORTAYA KONMASI Hayrettin
BAKTERİLERİN GENETİK KARAKTERLERİ
 BAKTERİLERİN GENETİK KARAKTERLERİ GENETİK MATERYALLER VE YAPILARI HER HÜCREDE Genetik bilgilerin kodlandığı bir DNA genomu bulunur Bu genetik bilgiler mrna ve ribozomlar aracılığı ile proteinlere dönüştürülür
BAKTERİLERİN GENETİK KARAKTERLERİ GENETİK MATERYALLER VE YAPILARI HER HÜCREDE Genetik bilgilerin kodlandığı bir DNA genomu bulunur Bu genetik bilgiler mrna ve ribozomlar aracılığı ile proteinlere dönüştürülür
MEME LOBU YANGISI. süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri. süt endüstrisinde önemli ekonomik kayıp
 MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp HAYVAN Sağlığı fonksiyonel meme lobunun kaybı
MASTİT 1 MEME LOBU YANGISI süt veriminde azalma sütün imhası laboratuvar giderleri ilaç giderleri vet.hek. giderleri süt endüstrisinde önemli ekonomik kayıp HAYVAN Sağlığı fonksiyonel meme lobunun kaybı
Bacillus anthracis. Hayvanlarda şarbon etkenidir. Bacillus anthracis. Gram boyama. Bacillus anthracis. Bacillus anthracis
 Bacillus anthracis Gram pozitif, obligat aerop sporlu, çomak şeklinde bakterilerdir. 1µm eninde, 2-4 µm uzunluğunda, konkav sonlanan, kirpiksiz bakterilerdir. Bacillus anthracis in doğal yaşam ortamı topraktır.
Bacillus anthracis Gram pozitif, obligat aerop sporlu, çomak şeklinde bakterilerdir. 1µm eninde, 2-4 µm uzunluğunda, konkav sonlanan, kirpiksiz bakterilerdir. Bacillus anthracis in doğal yaşam ortamı topraktır.
Normal Mikrop Florası. Prof.Dr.Cumhur Özkuyumcu
 Normal Mikrop Florası Prof.Dr.Cumhur Özkuyumcu Vücudun Normal Florası İnsan vücudunun çeşitli bölgelerinde bulunan, insana zarar vermeksizin hatta bazı yararlar sağlayan mikroorganizma topluluklarına vücudun
Normal Mikrop Florası Prof.Dr.Cumhur Özkuyumcu Vücudun Normal Florası İnsan vücudunun çeşitli bölgelerinde bulunan, insana zarar vermeksizin hatta bazı yararlar sağlayan mikroorganizma topluluklarına vücudun
AMİNOGLİKOZİD ANTİBİYOTİKLER Aminoglikozid antibiyotikler Streptomyces veya Micromonospora türü mikroorganizmalardan elde edilirler.
 AMİNOGLİKOZİD ANTİBİYOTİKLER Aminoglikozid antibiyotikler Streptomyces veya Micromonospora türü mikroorganizmalardan elde edilirler. Bu grupta; streptomisin, dihidrostreptomisin, neomisin, framisetin,
AMİNOGLİKOZİD ANTİBİYOTİKLER Aminoglikozid antibiyotikler Streptomyces veya Micromonospora türü mikroorganizmalardan elde edilirler. Bu grupta; streptomisin, dihidrostreptomisin, neomisin, framisetin,
Probiyotik suşları. Prof Dr Tarkan Karakan Gazi Üniversitesi Gastroenteroloji Bilim Dalı
 Probiyotik suşları Prof Dr Tarkan Karakan Gazi Üniversitesi Gastroenteroloji Bilim Dalı İnsan ve bakteri ilişkisi İnsan vücudundaki bakterilerin yüzey alanı = 400 m 2 (Tenis kortu kadar) İnsandaki gen
Probiyotik suşları Prof Dr Tarkan Karakan Gazi Üniversitesi Gastroenteroloji Bilim Dalı İnsan ve bakteri ilişkisi İnsan vücudundaki bakterilerin yüzey alanı = 400 m 2 (Tenis kortu kadar) İnsandaki gen
Streptococcus. 01. Genel Bilgiler. 02. Etiyoloji
 Streptococcus 01. Genel Bilgiler 02. Etiyoloji 03. Epidemiyoloji 04. Hastalık belirtileri 05. Laboratuvar Tanısı 05.01. Bakteriyoskopi 05.02. Kültür 05.03. Hayvan Deneyi 05.04. Serolojik Testler 05.05.
Streptococcus 01. Genel Bilgiler 02. Etiyoloji 03. Epidemiyoloji 04. Hastalık belirtileri 05. Laboratuvar Tanısı 05.01. Bakteriyoskopi 05.02. Kültür 05.03. Hayvan Deneyi 05.04. Serolojik Testler 05.05.
Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan
 Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan ekstraselluler matriks içinde, birbirlerine yapışarak meydana getirdikleri
Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan ekstraselluler matriks içinde, birbirlerine yapışarak meydana getirdikleri
Gram Negatif Bakteriler
 Gram Negatif Bakteriler Escherichia cinsi Salmonella cinsi Bordetella cinsi Burkholderia cinsi Morexella cinsi Pasteurella cinsi Actinobacillus cinsi Taylorella cinsi Brucella cinsi Escherichia Salmonella
Gram Negatif Bakteriler Escherichia cinsi Salmonella cinsi Bordetella cinsi Burkholderia cinsi Morexella cinsi Pasteurella cinsi Actinobacillus cinsi Taylorella cinsi Brucella cinsi Escherichia Salmonella
CORYNEBACTERİUM İNFEKSİYONLARI
 CORYNEBACTERİUM İNFEKSİYONLARI FAMİLYA: Corynebacteriaceae Genus: Corynebacterium Evcil hayvanlarda değişik suppurajf durumlara neden olan piyojenik mikroorganizmalardır. İnfeksiyon öncesinde genellikle
CORYNEBACTERİUM İNFEKSİYONLARI FAMİLYA: Corynebacteriaceae Genus: Corynebacterium Evcil hayvanlarda değişik suppurajf durumlara neden olan piyojenik mikroorganizmalardır. İnfeksiyon öncesinde genellikle
BAKTERİLERDE GENETİK MADDE AKTARILMASI
 BAKTERİLERDE GENETİK MADDE AKTARILMASI Bakterilerde genetik maddenin bir kısmı bakteriden bakteriye aktarılabilmekte ve bunun sonucunda önemli genetik değişmeler olmaktadır Verici hücre ile alıcı hücre
BAKTERİLERDE GENETİK MADDE AKTARILMASI Bakterilerde genetik maddenin bir kısmı bakteriden bakteriye aktarılabilmekte ve bunun sonucunda önemli genetik değişmeler olmaktadır Verici hücre ile alıcı hücre
SALMONELLA İNFEKSİYONLARI
 SALMONELLA İNFEKSİYONLARI Salmonella etkenleri Fam.:Enterobacteriaceae Cins: Salmonella Tür: 1. S. enterica (S. cholera suis) 2. S. bongori S. enterica 7 alt grup S. enterica 1. S. enterica subsp. enterica
SALMONELLA İNFEKSİYONLARI Salmonella etkenleri Fam.:Enterobacteriaceae Cins: Salmonella Tür: 1. S. enterica (S. cholera suis) 2. S. bongori S. enterica 7 alt grup S. enterica 1. S. enterica subsp. enterica
VETERİNER MİKROBİYOLOJİ ANABİLİM DALI
 VETERİNER MİKROBİYOLOJİ ANABİLİM DALI VETERİNER MİKROBİYOLOJİ DOKTORA PROGRAMI (Program Kodu: 5361) Sıra No Dersin Kodu GÜZ YARIYILI Dersin Adı Z/S T U K AKTS 1. 5361101 Genel Mikrobiyoloji I 2. 5361102
VETERİNER MİKROBİYOLOJİ ANABİLİM DALI VETERİNER MİKROBİYOLOJİ DOKTORA PROGRAMI (Program Kodu: 5361) Sıra No Dersin Kodu GÜZ YARIYILI Dersin Adı Z/S T U K AKTS 1. 5361101 Genel Mikrobiyoloji I 2. 5361102
Clostridium. Clostridium spp. Clostridium endospor formu. Bacillus ve Clostridium
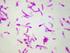 Clostridium Gram pozitif, sporlu çomaklar olup anaeropturlar. Doğal yaşam ortamları toprak, ayrıca insan ve hayvanların bağırsaklarıdır. Hastalık etkeni türlerde patojenite ekzotoksin veya ekzoenzim üretimi
Clostridium Gram pozitif, sporlu çomaklar olup anaeropturlar. Doğal yaşam ortamları toprak, ayrıca insan ve hayvanların bağırsaklarıdır. Hastalık etkeni türlerde patojenite ekzotoksin veya ekzoenzim üretimi
KANATLI ORİJİNLİ ESCHERİCHİA COLİ SUŞLARININ VİRÜLENS ÖZELLİKLERİNİN FENOTİPİK VE MOLEKÜLER METOTLARLA BELİRLENMESİ
 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ KANATLI ORİJİNLİ ESCHERİCHİA COLİ SUŞLARININ VİRÜLENS ÖZELLİKLERİNİN FENOTİPİK VE MOLEKÜLER METOTLARLA BELİRLENMESİ Zafer CANTEKİN MİKROBİYOLOJİ
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ KANATLI ORİJİNLİ ESCHERİCHİA COLİ SUŞLARININ VİRÜLENS ÖZELLİKLERİNİN FENOTİPİK VE MOLEKÜLER METOTLARLA BELİRLENMESİ Zafer CANTEKİN MİKROBİYOLOJİ
İnsan Mikrobiyom Projesi. Prof. Dr. Tanıl Kocagöz
 İnsan Mikrobiyom Projesi Prof. Dr. Tanıl Kocagöz Human Microbiome Project İnsan Mikrobiyom Projesi (İMP) 2007 yılında NIH tarafından başlatıldı 300 gönüllünün 5 vücut bölgesinden değişik zamanlarda, toplam
İnsan Mikrobiyom Projesi Prof. Dr. Tanıl Kocagöz Human Microbiome Project İnsan Mikrobiyom Projesi (İMP) 2007 yılında NIH tarafından başlatıldı 300 gönüllünün 5 vücut bölgesinden değişik zamanlarda, toplam
BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI
 BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0 2 5 Enstitünün Belirlediği
BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0 2 5 Enstitünün Belirlediği
ADIM ADIM YGS LYS Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI
 ADIM ADIM YGS LYS 177. Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI Hastalık yapıcı organizmalara karşı vücudun gösterdiği dirence bağışıklık
ADIM ADIM YGS LYS 177. Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI Hastalık yapıcı organizmalara karşı vücudun gösterdiği dirence bağışıklık
Hayvansal Kaynaklardan İzole Edilen Escherichia coli suşlarının Konvansiyonel ve Moleküler Tiplendirilmesi Müjgan İzgür, Mehmet Akan, Orkun Babacan, O
 ANKARA ÜNİVERSİTESİ BİLİMSEL ARAŞTIRMA PROJESİ KESİN RAPORU Hayvansal Kaynaklardan İzole Edilen Escherichia coli suşlarının Konvansiyonel ve Moleküler Tiplendirilmesi Müjgan İzgür Mehmet Akan Orkun Babacan
ANKARA ÜNİVERSİTESİ BİLİMSEL ARAŞTIRMA PROJESİ KESİN RAPORU Hayvansal Kaynaklardan İzole Edilen Escherichia coli suşlarının Konvansiyonel ve Moleküler Tiplendirilmesi Müjgan İzgür Mehmet Akan Orkun Babacan
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ
 15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması
 Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması Melisa Akgöz 1, İrem Akman 1, Asuman Begüm Ateş 1, Cem Çelik 1, Betül Keskin 1, Büşra Betül Özmen
Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması Melisa Akgöz 1, İrem Akman 1, Asuman Begüm Ateş 1, Cem Çelik 1, Betül Keskin 1, Büşra Betül Özmen
ÇOKLU TÜP FERMANTASYON YÖNTEMİ İLE TOPLAM KOLİFORM TAYİNİ. Koliform Bakteri Grubunun Tanımı
 ÇOKLU TÜP FERMANTASYON YÖNTEMİ İLE TOPLAM KOLİFORM TAYİNİ Koliform Bakteri Grubunun Tanımı Koliform grubunu oluşturan bakteriler; tamamı aerobik veya fakültatif anaerobik olan, gram negatif, spor oluşturmayan,
ÇOKLU TÜP FERMANTASYON YÖNTEMİ İLE TOPLAM KOLİFORM TAYİNİ Koliform Bakteri Grubunun Tanımı Koliform grubunu oluşturan bakteriler; tamamı aerobik veya fakültatif anaerobik olan, gram negatif, spor oluşturmayan,
Mustafa EMREM
 Mustafa EMREM 162161022 Bakterilerdeki transformasyonun ilk kanıtları İngiliz bilim adamı Frederick Griffith tarafından elde edilmiştir. Genetik materyal aktarımı Dikey Gen Transferi ebeveyn ile yavru
Mustafa EMREM 162161022 Bakterilerdeki transformasyonun ilk kanıtları İngiliz bilim adamı Frederick Griffith tarafından elde edilmiştir. Genetik materyal aktarımı Dikey Gen Transferi ebeveyn ile yavru
Y. pestis, Y. pseudotuberculosis, Y. enterocolitica
 Yersinia Enterobacteriaceae ailesindedir Y. pestis, Y. pseudotuberculosis, Y. enterocolitica Y.frederiksenii, Y.kristensenii,Y.intermedia Yersinia pestis Veba hastalığının etkeni (Kara ölüm) İlk pandemi
Yersinia Enterobacteriaceae ailesindedir Y. pestis, Y. pseudotuberculosis, Y. enterocolitica Y.frederiksenii, Y.kristensenii,Y.intermedia Yersinia pestis Veba hastalığının etkeni (Kara ölüm) İlk pandemi
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ
 VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
Gıda Kaynaklı İnfeksiyon Hastalıkları
 Gıda Kaynaklı İnfeksiyon Hastalıkları Dr. Serap Şimşek-Yavuz İstanbul Üniversitesi, İstanbul Tıp Fakültesi, İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Gıda Kaynaklı İnfeksiyon Hastalıkları
Gıda Kaynaklı İnfeksiyon Hastalıkları Dr. Serap Şimşek-Yavuz İstanbul Üniversitesi, İstanbul Tıp Fakültesi, İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Gıda Kaynaklı İnfeksiyon Hastalıkları
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ
 7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
Özel Formülasyon DAHA İYİ DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
 Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
CİLT MİKROBİYOTASI PROF.DR. NİLGÜN SOLAK BÜLENT ECEVİT Ü. TIP FAK. DERMATOLOJİ AD
 CİLT MİKROBİYOTASI PROF.DR. NİLGÜN SOLAK BÜLENT ECEVİT Ü. TIP FAK. DERMATOLOJİ AD CİLT MİKROBİYOTASI CİLT MİKROFLORASI DERİ MİKROBİYOTASI DERİ MİKROFLORASI DERİ Deri en büyük organımız 2 m² alan Vücudu
CİLT MİKROBİYOTASI PROF.DR. NİLGÜN SOLAK BÜLENT ECEVİT Ü. TIP FAK. DERMATOLOJİ AD CİLT MİKROBİYOTASI CİLT MİKROFLORASI DERİ MİKROBİYOTASI DERİ MİKROFLORASI DERİ Deri en büyük organımız 2 m² alan Vücudu
Ne yediğimizi düşünüyoruz? Gerçekte ne yiyoruz?
 Gıda kaynaklı hastalıklar : Gıda Kaynaklı Hastalıklar GIDA KAYNAKLI HASTALIKLAR Çok kişiyi etkileyen salgınlara Büyük işgücü kayıplarına Ekonomik kayıplara neden olmaktadır. 3 Ne yediğimizi düşünüyoruz?
Gıda kaynaklı hastalıklar : Gıda Kaynaklı Hastalıklar GIDA KAYNAKLI HASTALIKLAR Çok kişiyi etkileyen salgınlara Büyük işgücü kayıplarına Ekonomik kayıplara neden olmaktadır. 3 Ne yediğimizi düşünüyoruz?
Mikroorganizmalar gözle görülmezler, bu yüzden mikroskopla incelenirler.
 10. Sınıf Enfeksiyondan Korunma 2.Hafta ( 22-26 / 09 / 2014 ) ENFEKSİYON ETKENLERİNİN SINIFLANDIRILMASI 1.) BAKTERİLER 2.) VİRÜSLER Slayt No : 2 Mikroorganizmaların Sınıflandırılması ; a.) Sayısal Yöntem,
10. Sınıf Enfeksiyondan Korunma 2.Hafta ( 22-26 / 09 / 2014 ) ENFEKSİYON ETKENLERİNİN SINIFLANDIRILMASI 1.) BAKTERİLER 2.) VİRÜSLER Slayt No : 2 Mikroorganizmaların Sınıflandırılması ; a.) Sayısal Yöntem,
laboratuar muayeneleri esastır.
 Brucella ların neden olduğu Brucellosis; sığır, koyun, keçi, domuz, koç vs. gibi hayvanlarda, özellikle, testis, meme, uterus gibi genital organlara yerleşerek yavru atmalara ve infertiliteye yol açan
Brucella ların neden olduğu Brucellosis; sığır, koyun, keçi, domuz, koç vs. gibi hayvanlarda, özellikle, testis, meme, uterus gibi genital organlara yerleşerek yavru atmalara ve infertiliteye yol açan
KIRIM KONGO KANAMALI ATEŞİ HASTALIĞI (KKKA) VE KARADENİZ BÖLGESİ NDEKİ DURUMU
 KIRIM KONGO KANAMALI ATEŞİ HASTALIĞI (KKKA) VE KARADENİZ BÖLGESİ NDEKİ DURUMU Hamza KADI Veteriner Hekim Samsun Veteriner Kontrol Enstitüsü Viroloji Laboratuvarı Tarihçe 12. yy da bugünkü Tacikistan bölgesinde
KIRIM KONGO KANAMALI ATEŞİ HASTALIĞI (KKKA) VE KARADENİZ BÖLGESİ NDEKİ DURUMU Hamza KADI Veteriner Hekim Samsun Veteriner Kontrol Enstitüsü Viroloji Laboratuvarı Tarihçe 12. yy da bugünkü Tacikistan bölgesinde
İnfeksiyon tanısında yeni yaklaşımlar Biyosensörler. Barış OTLU İnönü Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Malatya.
 İnfeksiyon tanısında yeni yaklaşımlar Biyosensörler Barış OTLU İnönü Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Malatya. Bakterilerin tanımlanması Bakterilerin tanımlanması Bakterilerin
İnfeksiyon tanısında yeni yaklaşımlar Biyosensörler Barış OTLU İnönü Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Malatya. Bakterilerin tanımlanması Bakterilerin tanımlanması Bakterilerin
Replikasyon, Transkripsiyon ve Translasyon. Yrd. Doç. Dr. Osman İBİŞ
 Replikasyon, Transkripsiyon ve Translasyon Yrd. Doç. Dr. Osman İBİŞ DNA replikasyonu DNA nın replikasyonu, DNA molekülünün, sakladığı genetik bilgilerin sonraki nesillere aktarılması için kendi kopyasını
Replikasyon, Transkripsiyon ve Translasyon Yrd. Doç. Dr. Osman İBİŞ DNA replikasyonu DNA nın replikasyonu, DNA molekülünün, sakladığı genetik bilgilerin sonraki nesillere aktarılması için kendi kopyasını
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ
 7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
Kanatlı Hayvan Hastalıkları
 Kanatlı Hayvan Hastalıkları Kanatlı sektörü ile ilgili genel bilgiler 1930 Merkez Tavukçuluk Enstitüsü 1952 Saf ırkların ilk kez ithal edilmesi 1963 Damızlık (Parent stock) ithali 1970 Yatırımlarda artma
Kanatlı Hayvan Hastalıkları Kanatlı sektörü ile ilgili genel bilgiler 1930 Merkez Tavukçuluk Enstitüsü 1952 Saf ırkların ilk kez ithal edilmesi 1963 Damızlık (Parent stock) ithali 1970 Yatırımlarda artma
GURM (Strangles) (su sakağısı)
 GURM (Strangles) (su sakağısı) TEK TIRNAKLI ÜST solunum yollarında yangı RETROFARİNJİYAL ve SUBMANDİBULAR lenf yumrularında ABSE oluşumu AKUT, BULAŞICI ETİYOLOJİ Streptococcus equi subspecies equi Gram
GURM (Strangles) (su sakağısı) TEK TIRNAKLI ÜST solunum yollarında yangı RETROFARİNJİYAL ve SUBMANDİBULAR lenf yumrularında ABSE oluşumu AKUT, BULAŞICI ETİYOLOJİ Streptococcus equi subspecies equi Gram
TEMEL VETERİNER MİKROBİYOLOJİ VE İMMÜNOLOJİ (LBV106U) KISA ÖZET. kolayaof
 DİKKATİNİZE: BURADA SADECE ÖZETİN İLK ÜNİTESİ SİZE ÖRNEK OLARAK GÖSTERİLMİŞTİR. ÖZETİN TAMAMININ KAÇ SAYFA OLDUĞUNU ÜNİTELERİ İÇİNDEKİLER BÖLÜMÜNDEN GÖREBİLİRSİNİZ. TEMEL VETERİNER MİKROBİYOLOJİ VE İMMÜNOLOJİ
DİKKATİNİZE: BURADA SADECE ÖZETİN İLK ÜNİTESİ SİZE ÖRNEK OLARAK GÖSTERİLMİŞTİR. ÖZETİN TAMAMININ KAÇ SAYFA OLDUĞUNU ÜNİTELERİ İÇİNDEKİLER BÖLÜMÜNDEN GÖREBİLİRSİNİZ. TEMEL VETERİNER MİKROBİYOLOJİ VE İMMÜNOLOJİ
ORGANİZMALARDA BAĞIŞIKLIK MEKANİZMALARI
 ORGANİZMALARDA BAĞIŞIKLIK MEKANİZMALARI Organizmalarda daha öncede belirtildiği gibi hücresel ve humoral bağışıklık bağışıklık reaksiyonları vardır. Bunlara ilave olarak immünoljik tolerans adı verilen
ORGANİZMALARDA BAĞIŞIKLIK MEKANİZMALARI Organizmalarda daha öncede belirtildiği gibi hücresel ve humoral bağışıklık bağışıklık reaksiyonları vardır. Bunlara ilave olarak immünoljik tolerans adı verilen
Mikotoksin nedir? En sık karşılaşılan mikotoksinler; Aspergillus Penicillium Fusarium Alternaria
 Mikotoksin nedir? Aspergillus Penicillium Fusarium Alternaria belirli nem ve ısı koşullarında oluşturdukları fungal metabolitler En sık karşılaşılan mikotoksinler; o aflatoksinler, o okratoksin, o trikotesen,
Mikotoksin nedir? Aspergillus Penicillium Fusarium Alternaria belirli nem ve ısı koşullarında oluşturdukları fungal metabolitler En sık karşılaşılan mikotoksinler; o aflatoksinler, o okratoksin, o trikotesen,
Hedefe Spesifik Beslenme Katkıları
 Hedefe Spesifik Beslenme Katkıları Hayvan Beslemede Vitamin ve Minerallerin Önemi Vitaminler, çiftlik hayvanlarının, büyümesi, gelişmesi, üremesi, kısaca yaşaması ve verim vermesi için gerekli metabolik
Hedefe Spesifik Beslenme Katkıları Hayvan Beslemede Vitamin ve Minerallerin Önemi Vitaminler, çiftlik hayvanlarının, büyümesi, gelişmesi, üremesi, kısaca yaşaması ve verim vermesi için gerekli metabolik
BALIKLARDA PSEUDOMONAS İNFEKSİYONLARI. Yüksel DURMAZ Uzman Veteriner Hekim
 BALIKLARDA PSEUDOMONAS İNFEKSİYONLARI Yüksel DURMAZ Uzman Veteriner Hekim Pseudomonas ailesi içinde sınıflandırılma yapılmış ve 25 tür kapsadığı görülmüştür. Patojen olan ve olmayan Pseudomonas türleri
BALIKLARDA PSEUDOMONAS İNFEKSİYONLARI Yüksel DURMAZ Uzman Veteriner Hekim Pseudomonas ailesi içinde sınıflandırılma yapılmış ve 25 tür kapsadığı görülmüştür. Patojen olan ve olmayan Pseudomonas türleri
HAYVANSAL GIDALARDA LISTERIA TÜRLERİNİN VARLIĞININ KONVANSİYONEL VE İMMUNOLOJİK YÖNTEMLERLE ARAŞTIRILMASI
 TÜRKİYE 12. GIDA KONGRESİ 05-07 EKİM 2016; EDİRNE HAYVANSAL GIDALARDA LISTERIA TÜRLERİNİN VARLIĞININ KONVANSİYONEL VE İMMUNOLOJİK YÖNTEMLERLE ARAŞTIRILMASI Ayla EYİ GENCAN *, İlker Turan AKOĞLU, İbrahim
TÜRKİYE 12. GIDA KONGRESİ 05-07 EKİM 2016; EDİRNE HAYVANSAL GIDALARDA LISTERIA TÜRLERİNİN VARLIĞININ KONVANSİYONEL VE İMMUNOLOJİK YÖNTEMLERLE ARAŞTIRILMASI Ayla EYİ GENCAN *, İlker Turan AKOĞLU, İbrahim
Mikrobiyal Gelişim. Jenerasyon süresi. Bakterilerde üreme eğrisi. Örneğin; (optimum koşullar altında) 10/5/2015
 Mikrobiyal Gelişim Tek hücreli organizmalarda sayı artışı Bakterilerde en çok görülen üreme şekli ikiye bölünmedir (mikroorganizma sayısı) Çok hücreli organizmalarda kütle artışı Genelde funguslarda görülen
Mikrobiyal Gelişim Tek hücreli organizmalarda sayı artışı Bakterilerde en çok görülen üreme şekli ikiye bölünmedir (mikroorganizma sayısı) Çok hücreli organizmalarda kütle artışı Genelde funguslarda görülen
HİPERVİRÜLAN ESCHERİCHİA COLİ ST131 KLONU ÜLKEMİZDE YENİ Mİ?
 HİPERVİRÜLAN ESCHERİCHİA COLİ ST131 KLONU ÜLKEMİZDE YENİ Mİ? Elif Aktaş, Nezahat Gürler, Nafia Canan Gürsoy, Barış Otlu, Bahar Akgün Karapınar, Zuhal Kalaycı Çekin, Gülsüm İnanç, Emin Bulut, Çiğdem Kayacan
HİPERVİRÜLAN ESCHERİCHİA COLİ ST131 KLONU ÜLKEMİZDE YENİ Mİ? Elif Aktaş, Nezahat Gürler, Nafia Canan Gürsoy, Barış Otlu, Bahar Akgün Karapınar, Zuhal Kalaycı Çekin, Gülsüm İnanç, Emin Bulut, Çiğdem Kayacan
İntestinal Mikrobiyota Nedir? Ne yapar? Dr. Taylan Kav Hacettepe Üniversitesi Tıp Fakültesi Gastroenteroloji BD
 İntestinal Mikrobiyota Nedir? Ne yapar? Dr. Taylan Kav Hacettepe Üniversitesi Tıp Fakültesi Gastroenteroloji BD En iyi mikrop ölü mikrop (mu)? Vücudumuzdaki Mikroplar Bakteriler Mantarlar Virüsler Bakterilerle
İntestinal Mikrobiyota Nedir? Ne yapar? Dr. Taylan Kav Hacettepe Üniversitesi Tıp Fakültesi Gastroenteroloji BD En iyi mikrop ölü mikrop (mu)? Vücudumuzdaki Mikroplar Bakteriler Mantarlar Virüsler Bakterilerle
Riketsia, Bedsonia, Klamidya ve virüsler canlı ortamlarda ürerler. Canlı ortamlar üç kısma ayrılır.
 MİKRO ORGANİZMALARIN ÜRETİLMESİ İÇİN BESİYERLERİ Mikroorganizmaları izole etmek ve saf kültür olarak üretebilmek için birçok ortamlar geliştirilmiştir (Besiyerleri, vasatlar). Besi yerleri başlıca iki
MİKRO ORGANİZMALARIN ÜRETİLMESİ İÇİN BESİYERLERİ Mikroorganizmaları izole etmek ve saf kültür olarak üretebilmek için birçok ortamlar geliştirilmiştir (Besiyerleri, vasatlar). Besi yerleri başlıca iki
CANDİDA İLE UYARILMIŞ VAJİNAL VE BUKKAL EPİTEL HÜCRELERİNİN SİTOKİN ÜRETİMİ
 CANDİDA İLE UYARILMIŞ VAJİNAL VE BUKKAL EPİTEL HÜCRELERİNİN SİTOKİN ÜRETİMİ Emine Yeşilyurt, Sevgi Özyeğen Aslan, Ayşe Kalkancı, Işıl Fidan, Semra Kuştimur Gazi Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji
CANDİDA İLE UYARILMIŞ VAJİNAL VE BUKKAL EPİTEL HÜCRELERİNİN SİTOKİN ÜRETİMİ Emine Yeşilyurt, Sevgi Özyeğen Aslan, Ayşe Kalkancı, Işıl Fidan, Semra Kuştimur Gazi Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji
*Barsak yaraları üzerine çalışmalarda probiyotikler, yaraların iyileşmesi ve kapanması amaçlı test edilmiştir.
 * *Aşılama öncesinde ve beraberinde probiyotik kullanma veya aşının içine serokonversiyon oranını arttıracağına inanılan suşların eklenmesi ilgili çalışmalar son birkaç yılda hızla artmıştır. *Şimdiye
* *Aşılama öncesinde ve beraberinde probiyotik kullanma veya aşının içine serokonversiyon oranını arttıracağına inanılan suşların eklenmesi ilgili çalışmalar son birkaç yılda hızla artmıştır. *Şimdiye
Viral gastroenteritlerin laboratuvar tanısı
 Viral gastroenteritlerin laboratuvar tanısı Dr.Gülay Korukluoğlu Dr.Dilek Yağcı Çağlayık Türkiye Halk Sağlığı Kurumu Akut gastroenteritler özellikle gelişmekte olan ülkelerde önemli bir mortalite ve morbidite
Viral gastroenteritlerin laboratuvar tanısı Dr.Gülay Korukluoğlu Dr.Dilek Yağcı Çağlayık Türkiye Halk Sağlığı Kurumu Akut gastroenteritler özellikle gelişmekte olan ülkelerde önemli bir mortalite ve morbidite
Plazmitler konak kromozomundan bağımsız olarak replike olabilen genetik elemanlardır.virüslerden farklı olarak,plazmitlerin hücre dışı formları
 Plazmitler konak kromozomundan bağımsız olarak replike olabilen genetik elemanlardır.virüslerden farklı olarak,plazmitlerin hücre dışı formları yoktur ve hücre içerisinde genellikle halkasal serbest DNA
Plazmitler konak kromozomundan bağımsız olarak replike olabilen genetik elemanlardır.virüslerden farklı olarak,plazmitlerin hücre dışı formları yoktur ve hücre içerisinde genellikle halkasal serbest DNA
ORTOPEDİK PROTEZ ENFEKSİYONLARINDA SONİKASYON DENEYİMİ
 ORTOPEDİK PROTEZ ENFEKSİYONLARINDA SONİKASYON DENEYİMİ Dr. Şua Sümer Selçuk Üniversitesi Tıp Fakültesi Enf. Hast. ve Klin. Mikr. AD 17 Mayıs 2016 Prostetik eklem ameliyatları yaşlı popülasyonun artışına
ORTOPEDİK PROTEZ ENFEKSİYONLARINDA SONİKASYON DENEYİMİ Dr. Şua Sümer Selçuk Üniversitesi Tıp Fakültesi Enf. Hast. ve Klin. Mikr. AD 17 Mayıs 2016 Prostetik eklem ameliyatları yaşlı popülasyonun artışına
KANATLI HAYVANLARDA AVIAN INFLUENZA (=TAVUK VEBASI)
 KANATLI HAYVANLARDA AVIAN INFLUENZA (=TAVUK VEBASI) Avian Influenza (AI), uluslararası bir problemdir Etken Orthomyxoviridae, Influenza A virusu Influenza virusları A, B, C olmak üzere üç gruba ayrılmıştır.
KANATLI HAYVANLARDA AVIAN INFLUENZA (=TAVUK VEBASI) Avian Influenza (AI), uluslararası bir problemdir Etken Orthomyxoviridae, Influenza A virusu Influenza virusları A, B, C olmak üzere üç gruba ayrılmıştır.
HAYVANLARDA BRUCELLOSİS VE. Uzm.Vet.Hek.Nedret AYDIN
 HAYVANLARDA BRUCELLOSİS VE EPİDEM DEMİYOLOJİSİ Uzm.Vet.Hek.Nedret AYDIN Brucella larınneden olduğu Brucellosis; sığır, koyun, keçi, domuz, koç vs. gibi hayvanlarda, özellikle, testis, meme, uterus gibi
HAYVANLARDA BRUCELLOSİS VE EPİDEM DEMİYOLOJİSİ Uzm.Vet.Hek.Nedret AYDIN Brucella larınneden olduğu Brucellosis; sığır, koyun, keçi, domuz, koç vs. gibi hayvanlarda, özellikle, testis, meme, uterus gibi
Flagella-H, protein yapısında, ısıya, asit ve alkollere hassas; formaldehit e dirençlidir.
 Familia Enterobacteriaceae Genel Özellikleri Prof. Dr. Figen Erkoç ve Fatma Türkmenoğlu (040559029) Gazi Eğitim Fakültesi, Gazi Üniversitesi Aralık 2007 Genel Özellikler: 1. Gram (-) 2. Basil 3. Sporsuz
Familia Enterobacteriaceae Genel Özellikleri Prof. Dr. Figen Erkoç ve Fatma Türkmenoğlu (040559029) Gazi Eğitim Fakültesi, Gazi Üniversitesi Aralık 2007 Genel Özellikler: 1. Gram (-) 2. Basil 3. Sporsuz
Karaciğer koruyucu DAHA İYİ DAHA SAĞLIKLI, DAHA İYİ VERİMLİ SÜRÜLER İÇİN HEPALYX
 Karaciğer koruyucu DAHA İYİ Karaciğer fonksiyonu Antioksidan aktivite Protein sentezi Anti-fibrotik aktivite Süt Verimi Süt Proteini Metabolik Sağlık Performans Bağışıklık Karlılık DAHA SAĞLIKLI, DAHA
Karaciğer koruyucu DAHA İYİ Karaciğer fonksiyonu Antioksidan aktivite Protein sentezi Anti-fibrotik aktivite Süt Verimi Süt Proteini Metabolik Sağlık Performans Bağışıklık Karlılık DAHA SAĞLIKLI, DAHA
Eklem Protez Enfeksiyonlarında Antimikrobiyal Tedavi
 Eklem Protez Enfeksiyonlarında Antimikrobiyal Tedavi Dr. Çağrı Büke Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı 26.12.15 KLİMİK - İZMİR 1 Eklem protezleri
Eklem Protez Enfeksiyonlarında Antimikrobiyal Tedavi Dr. Çağrı Büke Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı 26.12.15 KLİMİK - İZMİR 1 Eklem protezleri
İnfeksiyöz laringotraehitis
 İnfeksiyöz laringotraehitis Etiyoloji Herpes virus Epidemiyoloji Hastalık yaygın Doğal konakçı tavuk Erkekler daha duyarlı Sıcak mevsimlerde daha fazla Her yaştaki hayvanlar duyarlı fakat 6 haftadan büyükler
İnfeksiyöz laringotraehitis Etiyoloji Herpes virus Epidemiyoloji Hastalık yaygın Doğal konakçı tavuk Erkekler daha duyarlı Sıcak mevsimlerde daha fazla Her yaştaki hayvanlar duyarlı fakat 6 haftadan büyükler
Salmonella Enfeksiyonları
 Salmonella Enfeksiyonları Dr. Recep ÖZTÜRK İstanbul Universitesi, Cerrahpaşa Tıp Fakültesi, Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Ana Bilim Dalı Salmonella Enfeksiyonları Salmonella cinsi bakteriler,
Salmonella Enfeksiyonları Dr. Recep ÖZTÜRK İstanbul Universitesi, Cerrahpaşa Tıp Fakültesi, Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Ana Bilim Dalı Salmonella Enfeksiyonları Salmonella cinsi bakteriler,
