Simetrik (Homolitik) veya Radikalik Parçalanma: Bağ parçalanırken, bağı oluşturan iki elektrondan her biri farklı atomlar üzerinde kalır.
|
|
|
- Umut Aysel Çolak
- 5 yıl önce
- İzleme sayısı:
Transkript
1 ORGANİK REAKSİYONLAR 01. Giriş 02. Katılma Reaksiyonları Nükleofilik Katılma Reaksiyonları Elektrofilik Katılma Reaksiyonları 03. Eliminasyon (Çıkarma) Reaksiyonları 04. Yerdeğiştirme (Sübstitüsyon) Reaksiyonları SN1 Reaksiyonları SN2 Reaksiyonları Nükleofilik Sübstitüsyon Reaksiyonlarının Eliminasyon Reaksiyonlarıyla Karşılaştırılması Sübstitüsyon ve Eliminasyon Reaksiyonlarının Reaktifliklerinin RX Yapısına Bağlı Olarak Karşılaştırılması Elektrofilik Sübstitüsyon Reaksiyonları Aromatik Sübstitüsyon Reaksiyonları Önemli Elektrofilik Aromatik Sübstitüsyon Reaksiyonları 05. Çevrilme Reaksiyonları Elektronca Fakir Sistemlerin Çevrilme Reaksiyonları Elektronca Zengin Sistemlerin Çevrilme Reaksiyonları Allilik Çevrilmeler ( İkili ve Üçlü Bağların Göçmesi) Termal Çevrilme Reaksiyonları 06. Yükseltgenme İndirgenme Reaksiyonları Yükseltgenme Reaksiyonlarına Örnekler İndirgenme Reaksiyonlarına Örnekler Yükseltgenme İndirgenme Reaksiyonlarına Örnekler 01. Giriş Kimyasal reaksiyonlar gerçekleşirken atomlar arasındaki bağlar çözülür ve başka bir düzende yeniden sıralanır. Organik reaksiyonların çoğunda atomlar arasındaki bağlar parçalanırken kısa ömürlü bileşikler oluşur. Simetrik (Homolitik) veya Radikalik Parçalanma: Bağ parçalanırken, bağı oluşturan iki elektrondan her biri farklı atomlar üzerinde kalır. İyonik (Heterolitik) Parçalanma: Bağ parçalanırken, bağı oluşturan her iki elektronda aynı atom üzerinde kalır. Oluşan (-) yüklü karbon atomu karbanyon, (+) yüklü karbon atomu karbonyum (karbokatyon) adını alır. Bazen, heterolitik parçalanma sonucu kısa ömürlü nötr bileşikler (karbenler) oluşur. Bunlarda hem oktet boşluğu, hem de ortaklanmamış elektron çifti vardır.
2 Reaksiyona giren bileşenlere substrat ve reaktif denir. Molekülde reaksiyon merkezi olan organik maddeye substrat denir. Substrat reaksiyonda etkiyen maddedir. Reaktif ise reaksiyonda etkiyen maddedir. Organik ve inorganik yapıda olabilir. Organik reaksiyonlar, reaksiyona giren reaktifin özelliğine göre çeşitli gruplara ayrılır. -Katılma reaksiyonları -Eliminasyon (çıkarma) reaksiyonları -Yerdeğiştirme reaksiyonları -Çevrilme reaksiyonları -Yükseltgenme indirgenme reaksiyonları Reaktifler ise, nükleofilik, elektrofilik ve radikalik olmak üzere üçe ayrılır. Nükleofil: Üzerindeki elektron çiftiyle reaksiyona giren ve ayrıştığında negatif yüklü iyonlar veren reaktiflerdir. Örneğin, Lewis bazları, OH-, RO-, R-C=C-, R-MgX (R-), R-Li (R-), LiAlH 4 (H - ), CN -, H 2 O, NH 3 Elektrofil: Üzerinde pozitif yük taşıyan, ayrıştığında pozitif yüklü iyonlar veren veya üzerinde bir oktet boşluğu olan reaktiflerdir. Örneğin, Lewis asitleri, H +, AlCl 3, BF 3, H 2 SO 4 (SO 3 + ), HNO 3 (NO 2 + ), X 2 (X + ) Radikal: Yüksek ısı, ışık veya peroksit etkisiyle radikal oluşturabilen bileşiklerdir. Örneğin, Br 2, HBr 02. Katılma Reaksiyonları bağlarının kırılması ile moleküle atom veya grupların eklenmesidir. Bu tip reaksiyonlarda molekülün doymamışlık derecesi azalır Nükleofilik Katılma Reaksiyonları
3 Elektrofilik Katılma Reaksiyonları Markovnikov kuralı:1869 yılında Vladimis Markovnikov; hidrojen halojenürlerün alkenlere katılırken (H + ) nin hidrojen sayısı fazla olan karbona bağlandığını buldu.
4 Anti-Markovnikov kuralı: Ortamda O 2 yada peroksit varlığında birincil alkilbromürler oluşur. Bu durumda HBr katılması iyonik yerine serbest radikal mekanizması ile olur. Serbest radikallerin kararlılık sırası :3 2 1şeklindedir. Br radikalinin oluşumu: ROOR 2RO. RO. +HBr ROH +Br. Br radikalinin alkene katılması Alkinlerde de benzer şekilde reaksiyonlar gerçekleşir. 03. Eliminasyon (Çıkarma) Reaksiyonları Reaksiyona giren moleküle bağlı atom veya atom gruplarının sayısı azalır ve molekülün doymamışlık derecesi artar. Eliminasyon reaksiyonları genellikle çift ve üçlü bağların oluştuğu reaksiyonlardır. Reaksiyon sonunda birden fazla alken oluşma ihtimali varsa en fazla dallanmış alken (daha kararlı olan alken) daha çok oluşur (Saytzeff kuralı).
5 Farklı alkil grupları içeren kuaterner amonyum bazlarından büyük bir çoğunlukla oluşan alken çift bağ etrafında en az dallanmış olan alkendir. (Hofmann kuralı) Tersiyer amin oksitler hafif ısıtılmakla bir iç eliminasyon ile alkenleri verirler. (Cope Eliminasyonu) t-amin oksitler t-aminlerin hidrojen peroksitle ısıtılmasıyla elde edilirler. 04. Yerdeğiştirme (Sübstitüsyon) Reaksiyonları Reaksiyona giren moleküldeki atom veya atom gruplarının molekülden ayrılıp yerine başka atom veya atom grupları girmesidir. Molekülün doymamışlık derecesi değişmez. Nükleofillerle yapılan yer değiştirme reaksiyonlarına nükleofilik sübstitüsyon denir. Reaksiyonun hızı reaksiyona giren maddelerin sadece birinin konsantrasyonu ile orantılı ise SN1, birinin konsantrasyonunun karesi veya ikisinin konsantrasyonu ile orantılı ise SN2 reaksiyonu denir. Nükleofil Substrat Ürün HO - + RL ROH alkol
6 H 2 O + RL ROH alkol RO - + RL ROR eter ROH + RL ROR eter HS - + RL RSH tiyol NH 3 + RL RNH 2 p-amin RNH 2 + RL R 2 NH s-amin R 2 NH + RL R 3 N t-amin R 3 N + RL R 3 N + L - Kuaterner amonyum bil N RL RN 3 alkil azit I - + RL RI alkil iyodür RCOO - + RL RCOOR ester CN - + RL RCN nitril L= -X, -OSO3R, -OTs Bir reaksiyonda karbonyum iyonu oluşuyorsa reaksiyon mekanizması S N 1 dir. S N 1 reaksiyonlarında reaktiflik sırası, karbokatyonların kararlılıklarıyla da paralel olan 3 o > 2 o >> 1 o > CH 3 -X şeklindedir S N 1 Reaksiyonları S N 1 reaksiyonları iki basamaktan meydana gelir - Hız belirleyen, yavaş basamak Alkil halojenürün karbokatyon oluşturmak için iyonlaşması - Hızlı basamak Nükleofilin karbokatyona katılması Örneğin, t-bütil bromürün sodyum hidroksit içeren su içinde çözünmesi Yavaş basamak
7 Hızlı basamak Reaksiyon, Enerji diyagramında gösterilecek olursa, karbokatyon oluşumu yüksek enerjili (yavaş) basamaktır. Karbokatyona nükleofil katılması ise oldukça hızlıdır.
8 S N 2 Reaksiyonları S N 2 reaksiyonları ise bimolekülerdir. Yani, reaksiyonun yavaş olan basamağında ortamda iki tür vardır. Örneğin bütil bromürlerin aseton içinde iyodürle reaksiyonları S N 2 mekanizmasıyla gerçekleşmektedir. Hız, hem alkil halojenürün konsantrasyonuna hem de iyodür iyonunun (nükleofil) konsantrasyonuna bağlıdır. S N 2 reaksiyonlarında reaktiflik sırası, CH 3 -X > 1 o > 2 o >> 3 o şeklindedir. S N 2 reaksiyonları tek basamakta gerçekleştiği için, ( nükleofilin alkil halojenüre saldırısı) reaksiyonda bir ara ürün olmaz. Geçiş hali, nükleofil ve karbon atomu arasında bir bağ oluşurken, aynı zamanda karbon atomu ve ayrılan grup arasındaki bağın kopması sırasında oluşur.
9 S N 2 reaksiyonu için enerji diyagramı tek basamakta gösterilir.
10 Çok az gözlenen diğer bir nükleofilik yerdeğiştirme reaksiyonu da molekül içi yer değiştirme reaksiyonudur ( S N i ) Nükleofilik Sübstitüsyon Reaksiyonlarının Eliminasyon Reaksiyonlarıyla Karşılaştırılması Genel olarak bir nükleofil, ("Nü:-") bir alkil halojenürle karşılaştığı zaman iki olay meydana gelebilir 1. nükleofil, halojen atomunun yerini alabilir veya, 2. nükleofil baz gibi davranır ve dehidrohalojenleme (halojenür çıkışı) ile alken oluşur. Örnekten de görüldüğü gibi, ilk reaksiyon nükleofilik bimoleküler sübstitüsyon reaksiyonu (SN2), ikinci reaksiyon ise bimoleküler eliminasyon reaksiyonudur (E2).
11 Daha önce de gösterildiği şekilde, SN1 reaksiyonunun yavaş olan basamağında karbokatyon oluşuyordu. Eğer bir nükleofil karbokatyona saldırırsa, sübstitüsyon (yerdeğiştirme) reaksiyonu meydana gelir. Alternatif olarak, bir baz karbokatyona komşu olan bir karbon atomundan bir hidrojen atomu koparabilir. Bu işlem de eliminasyon reaksiyonu olarak adlandırılır ve bu mekanizma hız belirleyen basamakta sadece tek bir tür içerdiğinden E1 reaksiyonu olarak adlandırılır. Nükleofillerin bağıl kuvvetleri hakkında bazı genellemeler yapılabilir : - Negatif yüklü nükleofiller konjuge asitlerinden daha kuvvetlidir. ( OH - iyonu H 2 0 dan daha kuvvetlidir.) - Nükleofilik güç, çözücüye bağlı olarak periyodik cetvelde aynı grup içinde atom numarası arttıkça artar. Bazlık gücü ise azalır. ( I - > Br - > Cl - >F - ) - Aynı atomun nükleofil olduğu grup içinde nükleofilik güç ile bazik güç paralellik gösterir. ( C 2 H 5 O - > HO - > C 6 H 5 O - > CH 3 CO 2 - > CH 3 OH > H 2 O ) t- bütil bromürün suda çözünmesine bakacak olursak, ortak bir ara ürün içerildiği için E1 ve SN1 reaksiyonları birbirleriyle yarışırlar. Reaksiyonun tamamı şu basamakları içerir : - Alkil halojenürün karbokatyon oluşturmak için iyonlaşması. - Karbokatyona bir nükleofilin saldırısı (S N 1) Veya,
12 -Bir bazın, karbokatyona komşu olan bir karbon atomunda bulunan bir hidrojene saldırması (E1). - Bütün bu dört reaksiyonun reaktifliklerini karşılaştıracak olursak, - Primer alkil halojenürler SN2 mekanizması üzerinden reaksiyona girerler. - Sekonder alkil halojenürler nükleofillerle SN2 mekanizması üzerinden reaksiyona girerken, kuvvetli bazlarla E2 mekanizmasını tercih ederler. - Tersiyer alkil halojenürler kuvvetli bazlarla E2 mekanizması üzerinden reaksiyona girerken, bazik olmayan ortamda SN1 ve E1 mekanizmaları birbiriyle yarışır Sübstitüsyon ve Eliminasyon Reaksiyonlarının Reaktifliklerinin RX Yapısına Bağlı Olarak Karşılaştırılması Genel olarak RCH 2 X (Primer) Çoğunlukla SN2 sübstitüsyon reaksiyonu üzerinden yürür. R 2 CHX (Sekonder) Bazik olmayan nükleofillerle SN2 sübstitüsyon reaksiyonu, kuvvetli bazlarla E2 eliminasyon reaksiyonu üzerinden yürür. R 3 CH (Tersiyer) Çoğunlukla E2 eliminasyon reaksiyonu üzerinden yürür. (Bazik olmayan çözücüler içinde SN1 sübstitüsyonu ile E1 eliminasyonu birbiriyle yarışır.) Elektrofilik Sübstitüsyon Reaksiyonları -Karboksilli asitler fosfor trihalojenürün katalitik etkisiyle halojenlerle reaksiyona girerek -haloasitlere dönüşürler. Karboksil grubuna -konumunda hidrojen taşımayan asitler bu reaksiyonu vermezler. -Karbon atomunda üç hidrojen taşıyan karboksilli asitler trihaloasitlere, iki hidrojen içerenler dihaloasitlere, bir hidrojen içerenler ise monohaloasitlere dönüşürler.
13 (Hell-Volhard Zelinsky reaksiyonu) Aromatik Sübstitüsyon Reaksiyonları Aromatik halkaya bağlı bir atom ya da grubun başka bir atom veya grupla yer değiştirmesine aromatik sübstitüsyon denir. Aromatik sübstitüsyon reaksiyonlarında hangi ürünlerin oluşabileceği ve bu ürünlerin oluşumunun kolaylık derecesini önceden kestirebilmek için halkaya bağlı sübstitüentler iki ayrı grup altında toplanmıştır. Birinci sınıf sübstitüentlerde halkaya direkt olarak bağlanan atomlardan çoğu ortaklanmamış bir elektron içerir, bazıları ise eksi yüklü olmaya yatkındır. Bu nedenle bu tür sübstitüentler aromatik halkaya elektrofilik reaksiyonları kolaylaştıran ve aromatik halkaya bağlanacak reaktifleri esas olarak o-, p- konumlarına yönlendiren sübstitüentlerdir. İkinci sınıf sübstitüentlerde ise, aromatik halkaya direkt olarak bağlanan atomlardan bazısı artı yüklü; bazısı ise artı yüklü olmaya yatkındır. Bu nedenle ikinci sınıftan sübstitüentler halkadan elektron çekerek nükleofilik reaksiyonları kolaylaştırır; elektrofilik reaksiyonları güçleştirir ve aromatik halkaya bağlanacak reaktifleri esas olarak m- konumuna yönlendirirler.
14 Birinci sınıftan yönelticiler o-, p- yönelticiler İkinci sınıftan yönelticiler m- yönelticiler -N(CH 3 ) 2 -N + (CH 3 ) 3 Kuvvetli -NH 2 + -NO 2 -OH -SO 3 H -OCH 3 -CN Orta -NHCOCH3 -COOH -OCOCH3 -COOR -CH 3 -CHO Zayıf -I -COR -Br -CONH 2 -Cl + -NH 3 Çok zayıf -C 6 H 5 - -CH 2 COOH Önemli Elektrofilik Aromatik Sübstitüsyon Reaksiyonları Aromatik Nitrolama İkinci bir nitro grubu halkaya meta konumundan bağlanır. Reaksiyon ilk gruba göre daha zor yürür (Örnek: m-dinitrobenzen sentezi). Aromatik Sülfolama
15 Aromatik Halojenleme Friedel Crafts Reaksiyonları: Aromatik bileşikler, bir Lewis asitinin yardımıyla asit halojenürler ve asit anhidritlerle reaksiyona girerler. Aromatik ketonların elde edildiği bu reaksiyon Friedel Crafts açilleme reaksiyonu olarak bilinir. Asit halojenürlerle yapılan Friedel Crafts reaksiyonunda reaktifin ne olduğu asit holojenür ve kullanılan lewis asidinin yapısına bağlıdır. Eğer asit halojenürün yapısı açilyum oluşturuyorsa veya reaksiyonda kuvvetli bir lewis asidi kullanılıyorsa reaktif açilyum iyonudur. 05. Çevrilme Reaksiyonları
16 Kimyasal bir reaksiyonda reaksiyona giren molekülün karbon iskeleti, molekülde bulunan bir atom veya grubun molekül içinde bulunan bir başka atoma göçmesiyle değişirse, böyle bir reaksiyona çevrilme reaksiyonu denir Elektronca Fakir Sistemlerin Çevrilme Reaksiyonları Pinakol-Pinakolon Çevrilmesi : Komşu alkollerin çok zincirli ketonlar vermek için su çıkışıyla dehidrate olmaları sonucunda meydana gelir. İlk olarak asidik ortamda OH grubu yapıdan su şeklinde ayrılır. Daha sonra elektronca fakir olan karbon atomuna bir grup göç eder Elektronca Zengin Sistemlerin Çevrilme Reaksiyonları Benzil-Benzilik Asit çevrilmesi 1,2-Diketonlar, sulu baz etkisiyle benzilik asit çevrilmesine uğrarlar. Böylece oluşan tuzun asitlendirilmesiyle serbest benzilik asit elde edilir Allilik Çevrilmeler ( İkili ve Üçlü Bağların Göçmesi)
17 Alilik pozisyonlardaki sübstitüsyon (yerdeğiştirme) reaksiyonları, genellikle ikili bağın karbon iskeletinde kendi orijinal pozisyonundan komşu pozisyona göçmesini içerir. Bu göçmenin olabilmesi için muhtemel dört yol vardır : Nu: Nükleofil L: Ayrılan grup E: Elektrofil S N 1 mekanizmasıyla çevrilme : S N 2 mekanizmasıyla çevrilme :
18 S E 1 mekanizmasıyla çevrilme : S E 2 mekanizmasiyla çevrilme : Termal Çevrilme Reaksiyonları Cope çevrilmesi : Yüksek sıcaklıkta gerçekleşen çoğu reaksiyon radikal ve iyon oluşturur fakat çevrilme reaksiyonları gaz fazında gerçekleştiği için başlangıç maddesinin radikal ve iyon gibi parçalara ayrılması olası değildir. Bağlar, aynı geçiş halinde oluşur ve kırılırlar. Cope çevrilmesi buna en güzel örnektir.
19 06. Yükseltgenme İndirgenme Reaksiyonları Yükseltgenme ve indirgenme reaksiyonları katılma, eliminasyon ve sübstitüsyon reaksiyonları ile birlikte yürüyen değişimleri içerir. İnorganik kimyada yükseltgenme elektron kaybetme; indirgenme ise elektron kazanma olarak tanımlanır. Organik bileşikler de yükseltgenme reaksiyonlarına girerler; ancak bunlar için tam bir elektron transferinden söz etmek mümkün değildir. Elementel atomun yükseltgenme sayısı 0 kabul edilir. Karbonun kendinden daha elektronegatif bir grupla bağ yapması yükseltgenme; daha az elektronegatif bir grupla bağ yapması ise indirgenme olarak isimlendirilir. Organik bir bileşiğe hidrojen bağlanması her zaman bir indirgenmedir. C atomunun yükseltgenme sayısı, kendinden daha az elektronegatif bir atomla yaptığı her bir bağ için -1; kendinden daha fazla elektronegatif bir atomla yaptığı her bağ için +1 değeri alır. İkili ve üçlü bağlar sırasıyla 2 ve 3 değerini alır. Karbon-karbon bağları oksidasyon sayısını değiştirmez. Örnek: CH 4 (n= -4) CO 2 (n= +4) CCl 4 (n= +4) CH 2 -Cl 2 ( n = -2+2= 0) Hidrojenasyon (çifte bağa H 2 katımı) bir indirgenmedir. (2e- almış) Karbonun yanması, organik bileşiklerde önemli bir yükseltgenme reaksiyonudur. (8e- vermiş) Yükseltgenme Reaksiyonlarına Örnekler
20 06.02.İndirgenme Reaksiyonlarına Örnekler (Clemensen indirgnmesi) Bazı indirgen ajanlar ve bu ajanların hangi bileşiği hangi bileşiğe indirgediğine dair tablo aşağıda verilmiştir.
21 H 2 (Pd, Pt, LiAlH 4 NaBH 4 Na Diğer PtO 2 ) R-X R-H R-NO2 R-NH Zn/HCl R-CHO R-CH2OH Sn, Zn R-COX RCH2OH R-COR RCHOHR Yavaş R-COOH RCH2OH R-COOR RCH2OH R-CONH2 RCH2NH R-C=N RCH2NH R-SO-R R-S-R +
22 06.03.Yükseltgenme İndirgenme Reaksiyonlarına Örnekler Cannizaro reaksiyonu (Benzoik asit-benzil alkol deneyi) Benzokain Reaksiyon Mekanizması
23 Benzoin (Açiloin) Kondenzasyonu Reaksiyon Mekanizması
24 Diazoaminobenzen Reaksiyon Mekanizması
25 Diazonyum Tuzlarının diğer bazı reaksiyonları İyodoform (Haloform) Reaksiyonu Reaksiyon Mekanizması
26
ATOMLAR ARASI BAĞLARIN POLARİZASYONU. Bağ Polarizasyonu: Bağ elektronlarının bir atom tarafından daha fazla çekilmesi.
 ATOMLAR ARASI BAĞLARIN POLARİZASYONU Tüm kimyasal reaksiyonlardaki ortak nokta: elektron (e - ) alışverişi e - transferi sonucu bazı bağlar kırılır, bazı bağlar yer değiştirir ya da yeni bağlar oluşabilir.
ATOMLAR ARASI BAĞLARIN POLARİZASYONU Tüm kimyasal reaksiyonlardaki ortak nokta: elektron (e - ) alışverişi e - transferi sonucu bazı bağlar kırılır, bazı bağlar yer değiştirir ya da yeni bağlar oluşabilir.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
Oksidasyon ve Redüksiyon Reaksiyonları Oksidasyon Reaksiyonları
 1.1.1. Oksidasyon ve Redüksiyon Reaksiyonları 1.1.1.1. Oksidasyon Reaksiyonları Bir organik molekülün oksidasyonu, oksijen miktarının artışı veya hidrojen miktarının azalması olarak tanımlanabilir. Başka
1.1.1. Oksidasyon ve Redüksiyon Reaksiyonları 1.1.1.1. Oksidasyon Reaksiyonları Bir organik molekülün oksidasyonu, oksijen miktarının artışı veya hidrojen miktarının azalması olarak tanımlanabilir. Başka
1. ORGANİK REAKSİYONLARA GİRİŞ
 1. ORGANİK REAKSİYONLARA GİRİŞ Genel olarak ele alındığında farmasötik kimya bilim alanında, hastalık etkenlerine karşı veya fizyo-patalojik bozuklukları düzenleyecek kimyasal maddeler tasarlanır. Bu yapılara
1. ORGANİK REAKSİYONLARA GİRİŞ Genel olarak ele alındığında farmasötik kimya bilim alanında, hastalık etkenlerine karşı veya fizyo-patalojik bozuklukları düzenleyecek kimyasal maddeler tasarlanır. Bu yapılara
Bu bilgiler ışığında yukarıdaki C atomlarının yükseltgenme basamaklarını söyleyelim:
 Organik Bileşiklerde C atomunun Yükseltgenme Basamağının Bulunması Yükseltgenme basamağı, C'a bağlı atomların elektronegatifliğine göre değişmektedir. C'un başlangıçta yükseltgenme basamağını 0 gibi düşünelim.
Organik Bileşiklerde C atomunun Yükseltgenme Basamağının Bulunması Yükseltgenme basamağı, C'a bağlı atomların elektronegatifliğine göre değişmektedir. C'un başlangıçta yükseltgenme basamağını 0 gibi düşünelim.
T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER
 T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER ALKOL, ETER VE EPOKSİTLER: YAPILARI VE FİZİKSEL ÖZELLİKLERİ Alkoller, doymuş bir karbon atomuna bağlı bir hidroksil (-OH)
T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER ALKOL, ETER VE EPOKSİTLER: YAPILARI VE FİZİKSEL ÖZELLİKLERİ Alkoller, doymuş bir karbon atomuna bağlı bir hidroksil (-OH)
Serbest radikallerin etkileri ve oluşum mekanizmaları
 Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
Organik Reaksiyonlara Giriş
 rganik eaksiyonlara Giriş Dr. Kayhan BLELLİ Temel haldeki bazı elementlerin elektron dizilişleri Değerlik Elektronları (idrojen): 1s 1 1 (Karbon): 1s 2 2s 2 2p 2 4 N (Azot): 1s 2 2s 2 2p 3 5 (ksijen):
rganik eaksiyonlara Giriş Dr. Kayhan BLELLİ Temel haldeki bazı elementlerin elektron dizilişleri Değerlik Elektronları (idrojen): 1s 1 1 (Karbon): 1s 2 2s 2 2p 2 4 N (Azot): 1s 2 2s 2 2p 3 5 (ksijen):
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
Organik Reaksiyonlara Giriş
 Formal Yük rganik eaksiyonlara Giriş Araş. Gör. Kayhan BLELLİ Formal Yük = 4 0 4 = 0 Değerlik Elektronları sayısı 6 4 2 = 0 Bağ Sayısı rtaklanmamış Elektronların sayısı : : Atomun Yaptığı 6 6 1 = 1 3 eaksiyon
Formal Yük rganik eaksiyonlara Giriş Araş. Gör. Kayhan BLELLİ Formal Yük = 4 0 4 = 0 Değerlik Elektronları sayısı 6 4 2 = 0 Bağ Sayısı rtaklanmamış Elektronların sayısı : : Atomun Yaptığı 6 6 1 = 1 3 eaksiyon
ALKOLLER ve ETERLER. Kimya Ders Notu
 ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI
 / / Adı Soyadı : Numara : ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI Soru Puan BAŞARILAR 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 TOPLAM 100 1. Açık formülü olan bileşiğin genel
/ / Adı Soyadı : Numara : ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI Soru Puan BAŞARILAR 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 TOPLAM 100 1. Açık formülü olan bileşiğin genel
KİMYA-IV. Alkenler (3. Konu)
 KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA. Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004
 REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
SEMRA SOLAK BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ ÖĞRENCİSİ
 200620105037 SEMRA SOLAK BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ ÖĞRENCİSİ James Mason CRAFT Charles FRİEDEL 1877 yılında Fransız kimyager Charles FRİEDEL ve Amerikalı çalışma arkadaşı
200620105037 SEMRA SOLAK BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ ÖĞRENCİSİ James Mason CRAFT Charles FRİEDEL 1877 yılında Fransız kimyager Charles FRİEDEL ve Amerikalı çalışma arkadaşı
Alkinler (Asetilenler)
 Organik-İnorganik Kimya Alkinler (Asetilenler) ALKİNLER (ASETİLENLER) Genel formülleri C n H 2n-2 şeklinde olan ve yapılarında en az bir üçlü bağ içeren bileşiklerdir. Bu bileşiklere, moleküllerindeki
Organik-İnorganik Kimya Alkinler (Asetilenler) ALKİNLER (ASETİLENLER) Genel formülleri C n H 2n-2 şeklinde olan ve yapılarında en az bir üçlü bağ içeren bileşiklerdir. Bu bileşiklere, moleküllerindeki
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö
 BALIKESİR ÜNİVERSİTESİ 2008-2009 2009 EĞİE ĞİTİM ÖĞRETİM M YILI BAHAR DÖNEMİ ORGANİK K SENTEZ DERSİ ÖDEVİ HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö 200610105034 FRİEDEL EDEL-CRAFTS REAKSİYONLARI Friedel-Crafts
BALIKESİR ÜNİVERSİTESİ 2008-2009 2009 EĞİE ĞİTİM ÖĞRETİM M YILI BAHAR DÖNEMİ ORGANİK K SENTEZ DERSİ ÖDEVİ HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö 200610105034 FRİEDEL EDEL-CRAFTS REAKSİYONLARI Friedel-Crafts
AROMATİK BİLEŞİKLERİN NİTROLANMASI
 Elektrofilik Aromatik Sübstitüsyon Elektrofil parçacığa atak sonucunda arenyum iyonu oluşumu: AMATİK BİLEŞİKLEİN NİTLANMASI Uzm. Ecz. Dilan KNYA Proton kaybı ile sübstitüsyon ürününün elde edilmesi: Nitrolama
Elektrofilik Aromatik Sübstitüsyon Elektrofil parçacığa atak sonucunda arenyum iyonu oluşumu: AMATİK BİLEŞİKLEİN NİTLANMASI Uzm. Ecz. Dilan KNYA Proton kaybı ile sübstitüsyon ürününün elde edilmesi: Nitrolama
KİMYA-IV. Alkenler (3. Konu)
 KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
Kimya.12 3.Ünite Konu Özeti
 Kimya.12 3.Ünite Konu Özeti 1. ORGANĠK REDOKS TEPKĠMELERĠ 2. YER DEĞĠġTĠRME (SÜBSTĠTÜSYON) TEPKĠMELERĠ 3. KATILMA TEPKĠMELERĠ 4. AYRILMA (ELĠMĠNASYON) TEPKĠMELERĠ 5. KONDENZASYON TEPKĠMELERĠ Hazırlayan
Kimya.12 3.Ünite Konu Özeti 1. ORGANĠK REDOKS TEPKĠMELERĠ 2. YER DEĞĠġTĠRME (SÜBSTĠTÜSYON) TEPKĠMELERĠ 3. KATILMA TEPKĠMELERĠ 4. AYRILMA (ELĠMĠNASYON) TEPKĠMELERĠ 5. KONDENZASYON TEPKĠMELERĠ Hazırlayan
KİMYA-IV. Aromatik Hidrokarbonlar (Arenler) (5. Konu)
 KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV. Aromatik Hidrokarbonlar (Arenler) (5. Konu)
 KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KARBOKSİLLİ ASİTLER#2
 KARBOKSİLLİ ASİTLER#2 ELDE EDİLME TEPKİMELERİ KİMYASAL ÖZELLİKLERİ KULLANIM ALANLARI ELDE EDİLME TEPKİMELERİ 1. Birincil (primer) alkollerin ya da aldehitlerin yükseltgenmesiyle elde edilir. Örnek: İzobütil
KARBOKSİLLİ ASİTLER#2 ELDE EDİLME TEPKİMELERİ KİMYASAL ÖZELLİKLERİ KULLANIM ALANLARI ELDE EDİLME TEPKİMELERİ 1. Birincil (primer) alkollerin ya da aldehitlerin yükseltgenmesiyle elde edilir. Örnek: İzobütil
PROBLEM 1.1 a ) Örnek Çözüm b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s
 PROBLEM 1.1 b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s 2 3p 4 ) ç ) 14 Si; 1s 2 2s 2 2p 6 3s 2 3p 2 (Değerlik elektronları:
PROBLEM 1.1 b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s 2 3p 4 ) ç ) 14 Si; 1s 2 2s 2 2p 6 3s 2 3p 2 (Değerlik elektronları:
ORGANİK KİMYA. Prof.Dr. Özlen Güzel Akdemir. Farmasötik Kimya Anabilim Dalı
 ORGANİK KİMYA Prof.Dr. Özlen Güzel Akdemir Farmasötik Kimya Anabilim Dalı Ders sunumlarına erişim için : http://aves.istanbul.edu.tr/oguzel/dokumanlar 2018-2019 EĞİTİM-ÖĞRETİM YILI ORGANİK KİMYA DERS PLANI
ORGANİK KİMYA Prof.Dr. Özlen Güzel Akdemir Farmasötik Kimya Anabilim Dalı Ders sunumlarına erişim için : http://aves.istanbul.edu.tr/oguzel/dokumanlar 2018-2019 EĞİTİM-ÖĞRETİM YILI ORGANİK KİMYA DERS PLANI
FONKSİYONLU ORGANİK BİLEŞİKLER I
 FNKSİYNLU GANİK BİLEŞİKLE rganik bileşiklerde, bileşiğin temel kimyasal ve fiziksel özelliklerini belirleyen ve formülleri yazıldığında tanınmalarını sağlayan atom gruplarına fonksiyonel gruplar denir.
FNKSİYNLU GANİK BİLEŞİKLE rganik bileşiklerde, bileşiğin temel kimyasal ve fiziksel özelliklerini belirleyen ve formülleri yazıldığında tanınmalarını sağlayan atom gruplarına fonksiyonel gruplar denir.
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI
 BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
HİDROKARBONLAR HİDROKARBONLAR 2. AROMATİK 1. ALİFATİK HİDROKARBONLAR HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) DOYMAMIŞ
 HİDROKARBONLAR HİDROKARBONLAR HİDROKARBONLAR 1. ALİFATİK HİDROKARBONLAR 2. AROMATİK HİDROKARBONLAR DOYMUŞ HİDROKARBONLAR DOYMAMIŞ HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) BİTİŞİK İKİ HALKALI (NAFTALİN)
HİDROKARBONLAR HİDROKARBONLAR HİDROKARBONLAR 1. ALİFATİK HİDROKARBONLAR 2. AROMATİK HİDROKARBONLAR DOYMUŞ HİDROKARBONLAR DOYMAMIŞ HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) BİTİŞİK İKİ HALKALI (NAFTALİN)
HİDROKARBONLAR ve ALKENLER. Ders Notu
 HİDROKARBONLAR ve ALKENLER Ders Notu HİDROKARBONLAR ve ALKENLER Karbon atomları arası en az bir çift bağ içerdiklerinden doymamış hidrokarbonlardır,. Çift bağdan biri sigma, diğeri pi bağıdır. Çift bağlı
HİDROKARBONLAR ve ALKENLER Ders Notu HİDROKARBONLAR ve ALKENLER Karbon atomları arası en az bir çift bağ içerdiklerinden doymamış hidrokarbonlardır,. Çift bağdan biri sigma, diğeri pi bağıdır. Çift bağlı
ASİTLER- BAZLAR. Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur.
 ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ
 ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ)
 ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
HİDROKARBONLAR ve ALKİNLER. Kimya Ders Notu
 HİDROKARBONLAR ve ALKİNLER Kimya Ders Notu HİDROKARBONLAR ve ALKiNLER Karbon atomları arasında en az bir üçlü bağ içerdiklerinden doymamış hidrokarbonlardır. Üçlü bağdan biri sigma, diğerleri pi bağıdır.
HİDROKARBONLAR ve ALKİNLER Kimya Ders Notu HİDROKARBONLAR ve ALKiNLER Karbon atomları arasında en az bir üçlü bağ içerdiklerinden doymamış hidrokarbonlardır. Üçlü bağdan biri sigma, diğerleri pi bağıdır.
AROMATİK BİLEŞİKLER
 AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
PROBLEM 9.1. Örnek çözüm PROBLEM 9.2
 PROBLEM 9.1 Örnek çözüm PROBLEM 9.2 1-Bromo-3-metilsikloheksan sentezi için 4-metilsikloheksen ya da 3-metilsikloheksen kullanılabilir. 2-Bromo-2,3-dimetilbütan sentezi için 2,3-dimetil-2-büten ya da 2,3-dimetil-1-büten
PROBLEM 9.1 Örnek çözüm PROBLEM 9.2 1-Bromo-3-metilsikloheksan sentezi için 4-metilsikloheksen ya da 3-metilsikloheksen kullanılabilir. 2-Bromo-2,3-dimetilbütan sentezi için 2,3-dimetil-2-büten ya da 2,3-dimetil-1-büten
PROBLEM 7.1 Örnek çözüm PROBLEM 7.2 Örnek çözüm PROBLEM 7.3 Örnek çözüm PROBLEM 7.4
 PROBLEM 7.1 Örnek çözüm PROBLEM 7.2 Örnek çözüm PROBLEM 7.3 Örnek çözüm PROBLEM 7.4 a) 3 o RX ler S N 2 yer değiştirme tepkimeleri veremeyeceklerinden bu tepkime gerçekleşmez. (Burada oluşması beklenilen
PROBLEM 7.1 Örnek çözüm PROBLEM 7.2 Örnek çözüm PROBLEM 7.3 Örnek çözüm PROBLEM 7.4 a) 3 o RX ler S N 2 yer değiştirme tepkimeleri veremeyeceklerinden bu tepkime gerçekleşmez. (Burada oluşması beklenilen
HİDROKARBONLAR ve ALKANLAR. Kimya Ders Notu
 HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö)
 EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö) 200620105028 KONU BAŞLIKLARI 1)AMİNLERİN ADLANDIRILMASI 2)GABRİEL SENTEZİ AMİNLERİN ADLANDIRILMASI Aminler amonyaktaki bir, iki
EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö) 200620105028 KONU BAŞLIKLARI 1)AMİNLERİN ADLANDIRILMASI 2)GABRİEL SENTEZİ AMİNLERİN ADLANDIRILMASI Aminler amonyaktaki bir, iki
12-B. 31. I. 4p II. 5d III. 6s
 -B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
-B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
Bileşikteki atomların cinsini ve oranını belirten formüldür. Kaba formül ile bileşiğin molekül ağırlığı hesaplanamaz.
 BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
POLİMER KİMYASI -2. Prof. Dr. Saadet K. Pabuccuoğlu
 POLİMER KİMYASI -2 Prof. Dr. Saadet K. Pabuccuoğlu Polimerize Olabilirlik Nedir? Bir monomerin polimerize olabilirliği termodinamik ve kinetik düşüncelere bağlıdır. Termodinamikçe uygun olan her monomer,
POLİMER KİMYASI -2 Prof. Dr. Saadet K. Pabuccuoğlu Polimerize Olabilirlik Nedir? Bir monomerin polimerize olabilirliği termodinamik ve kinetik düşüncelere bağlıdır. Termodinamikçe uygun olan her monomer,
KİMYA-IV. Alkinler (4. Konu)
 KİMYA-IV Alkinler (4. Konu) Alkinler (Asetilenler) En az bir tane karbon-karbon üçlü bağı içeren hidrokarbonlara alkinler veya asetilenler denir. C C 2 Alkinler Yalnızca bir tane karbon-karbon üçlü bağı
KİMYA-IV Alkinler (4. Konu) Alkinler (Asetilenler) En az bir tane karbon-karbon üçlü bağı içeren hidrokarbonlara alkinler veya asetilenler denir. C C 2 Alkinler Yalnızca bir tane karbon-karbon üçlü bağı
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
Aşağıda verilen özet bilginin ayrıntısını, ders kitabı. olarak önerilen, Erdik ve Sarıkaya nın Temel. Üniversitesi Kimyası" Kitabı ndan okuyunuz.
 KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
8. Bölüm Alkenlerin Tepkimeleri
 = Bağının Reaktivitesi 8. Bölüm Alkenlerin Tepkimeleri pi bağındaki elektronlar daha serbesttirler. Bu pi elektronları Elektrofillere saldırırlar. Karbokatyon araürünü oluşur. Nükleofil karbokatyona eklenir.
= Bağının Reaktivitesi 8. Bölüm Alkenlerin Tepkimeleri pi bağındaki elektronlar daha serbesttirler. Bu pi elektronları Elektrofillere saldırırlar. Karbokatyon araürünü oluşur. Nükleofil karbokatyona eklenir.
veya Monoalkoller OH grubunun bağlı olduğu C atomunun komşu C atomlarına bağlı olarak primer, sekonder ve tersiyer olmak üzere sınıflandırılabilirler:
 ALKLLE Genel formülleri: n 2n+2 ( n 2n+1 = ) Fonksiyonel grupları: Alkollerin sistematik adlandırmasında en uzun zincirdeki atomuna göre alkan adının sonuna ol eki getirilir. Yapısında 1 tane grubu bulunduran
ALKLLE Genel formülleri: n 2n+2 ( n 2n+1 = ) Fonksiyonel grupları: Alkollerin sistematik adlandırmasında en uzun zincirdeki atomuna göre alkan adının sonuna ol eki getirilir. Yapısında 1 tane grubu bulunduran
KİMYA-IV. Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu)
 KİMYA-IV Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu) Alkoller Bir alkil grubuna (R-) bir hidroksil (-OH) grubunun bağlanmasıyla oluşan yapılardır. Genel formülleri R-OH şeklindedir. Alkollerin
KİMYA-IV Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu) Alkoller Bir alkil grubuna (R-) bir hidroksil (-OH) grubunun bağlanmasıyla oluşan yapılardır. Genel formülleri R-OH şeklindedir. Alkollerin
PROBLEM 5.1. PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3. Başlama basamağı. Gelişme basamağı. Sonlanma basamağı
 PROBLEM 5.1 PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3 Başlama basamağı Gelişme basamağı Sonlanma basamağı vb. PROBLEM 5.4 Örnek Çözüm PROBLEM 5.5 Örnek Çözüm PROBLEM 5.6 Örnek Çözüm PROBLEM 5.7 PROBLEM 5.8 FENOL
PROBLEM 5.1 PROBLEM 5.2 Örnek Çözüm PROBLEM 5.3 Başlama basamağı Gelişme basamağı Sonlanma basamağı vb. PROBLEM 5.4 Örnek Çözüm PROBLEM 5.5 Örnek Çözüm PROBLEM 5.6 Örnek Çözüm PROBLEM 5.7 PROBLEM 5.8 FENOL
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
1. İskelet yapısını çiziniz. H ve F daima uç atomlardır. En düşük iyonlaşma enerjisine sahip element merkez atomudur (bazı istisnalar mevcuttur).
 5.111 Ders Özeti #11 Bugün için okuma: Bölüm 2.7 (3. Baskıda 2.8) Rezonans ve Bölüm 2.8 (3. Baskıda 2.9) Formal Yük. Ders #12 için okuma: Bölüm 2.9 (3. Baskıda 2.10) Radikaller ve Biradikaller, Bölüm 2.10
5.111 Ders Özeti #11 Bugün için okuma: Bölüm 2.7 (3. Baskıda 2.8) Rezonans ve Bölüm 2.8 (3. Baskıda 2.9) Formal Yük. Ders #12 için okuma: Bölüm 2.9 (3. Baskıda 2.10) Radikaller ve Biradikaller, Bölüm 2.10
Tepkimeler ve Mekanizmaları
 3. BölümB ORGANĐK K TEPKĐMELERE GĐRĐŞG ĐŞ Tepkimeler ve Mekanizmaları Genel olarak tepkimeler dört sınıfa ayrılabilir: Yer değiştirmeler Katılmalar Ayrılmalar Çevrilmeler MEKANĐZMA: Reaktanların ürünlere
3. BölümB ORGANĐK K TEPKĐMELERE GĐRĐŞG ĐŞ Tepkimeler ve Mekanizmaları Genel olarak tepkimeler dört sınıfa ayrılabilir: Yer değiştirmeler Katılmalar Ayrılmalar Çevrilmeler MEKANĐZMA: Reaktanların ürünlere
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 3. YAZILI
 / / Adı Soyadı : Numara : ÖĞRETİM YL. DÖNEM 1. SNF / KİMYA DERSİ / 3. YAZL Soru Puan 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 TOPLAM 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 100 1. X: 3 NH Y:3 N 3
/ / Adı Soyadı : Numara : ÖĞRETİM YL. DÖNEM 1. SNF / KİMYA DERSİ / 3. YAZL Soru Puan 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 TOPLAM 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 100 1. X: 3 NH Y:3 N 3
AMİNLER SEKONDER AMİN
 AMİNLER (ALKİLLENMİŞ AMONYAK) AMİNLER (RNH 2 )PRİMER AMİN TERSİYER AMİN(R 3 N) SEKONDER AMİN R 2 NH Aminler Alkillenmiş Amonyak olarak tanımlanır. Azot Atomuna bağlı 2 tane H atomu varsa(bir tane alkil
AMİNLER (ALKİLLENMİŞ AMONYAK) AMİNLER (RNH 2 )PRİMER AMİN TERSİYER AMİN(R 3 N) SEKONDER AMİN R 2 NH Aminler Alkillenmiş Amonyak olarak tanımlanır. Azot Atomuna bağlı 2 tane H atomu varsa(bir tane alkil
ONDOKUZ MAYIS ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ KİMYA MÜHENDİSLİĞİ BÖLÜMÜ ORGANİK KİMYA LABORATUVARI
 ONDOKUZ MAYIS ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ KİMYA MÜHENDİSLİĞİ BÖLÜMÜ ORGANİK KİMYA LABORATUVARI NÜKLEOFİLİK YERDEĞİŞTİRME REAKSİYONU -1 DENEY 4 : S N 1 REAKSİYONU : T- BÜTİL KLORÜRÜN SENTEZİ TEORİ
ONDOKUZ MAYIS ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ KİMYA MÜHENDİSLİĞİ BÖLÜMÜ ORGANİK KİMYA LABORATUVARI NÜKLEOFİLİK YERDEĞİŞTİRME REAKSİYONU -1 DENEY 4 : S N 1 REAKSİYONU : T- BÜTİL KLORÜRÜN SENTEZİ TEORİ
Halojenür Çeşitleri. Bölüm 6 Alkil Halojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri. IUPAC Adlandırması (Sistematik Adlandırma)
 Bölüm 6 Alkil alojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri 2006, Prentice all 1 alojenür Çeşitleri Alkil: alojen, X, direkt olarak sp 3 melezleşmiş karbona bağlıdır. Vinil: X, alkenin
Bölüm 6 Alkil alojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri 2006, Prentice all 1 alojenür Çeşitleri Alkil: alojen, X, direkt olarak sp 3 melezleşmiş karbona bağlıdır. Vinil: X, alkenin
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BUADA ÖZET BİLGİ VEİLMİŞTİ. DAHA AYINTILI BİLGİ İÇİN VEİLEN KAYNAK KİTAPLAA BAKINIZ. KAYNAKLA 1) P. Volhardt, N. Schore; rganic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E. Craine,
BUADA ÖZET BİLGİ VEİLMİŞTİ. DAHA AYINTILI BİLGİ İÇİN VEİLEN KAYNAK KİTAPLAA BAKINIZ. KAYNAKLA 1) P. Volhardt, N. Schore; rganic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E. Craine,
ALKENLER. Genel formülleri: C n H 2n
 ALKENLER Genel formülleri: C n H 2n İsimlendirme kuralı: İkili bağ taşıyan en uzun karbon zinciri saptanır, aynı sayıda karbon taşıyan alkanın isminin sonundaki -an eki yerine -en son eki getirilir. H
ALKENLER Genel formülleri: C n H 2n İsimlendirme kuralı: İkili bağ taşıyan en uzun karbon zinciri saptanır, aynı sayıda karbon taşıyan alkanın isminin sonundaki -an eki yerine -en son eki getirilir. H
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
Halojenür Çeşitleri. Bölüm 6 Alkil Halojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri
 Bölüm 6 Alkil alojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri 2006, Prentice all 1 alojenür Çeşitleri Alkil: alojen, X, direkt olarak sp 3 melezleşmiş karbona bağlıdır. Vinil: X, alkenin
Bölüm 6 Alkil alojenürler: Nükleofilik Yer Değiştirme ve Ayrılma Tepkimeleri 2006, Prentice all 1 alojenür Çeşitleri Alkil: alojen, X, direkt olarak sp 3 melezleşmiş karbona bağlıdır. Vinil: X, alkenin
BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031
 BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031 Organik kimyada bilinen ilk tepkimelerden (metod) biridir. Bu reaksiyonun mucidi bilim adamı, Viktor Grignard, bu tepkime sayesinde 1912 Kimya Nobel ödülünün
BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031 Organik kimyada bilinen ilk tepkimelerden (metod) biridir. Bu reaksiyonun mucidi bilim adamı, Viktor Grignard, bu tepkime sayesinde 1912 Kimya Nobel ödülünün
Bölüm 7 Alkenlerin Yapısı ve Sentezi
 Bölüm 7 Alkenlerin Yapısı ve Sentezi Burak Esat Fatih Üniversitesi 2006, Prentice all Giriş Karbon-karbon ikili bağı içeren hidrokarbonlardır Bazen olefinler olarak da adlandırılırlar, olefin= oil-forming
Bölüm 7 Alkenlerin Yapısı ve Sentezi Burak Esat Fatih Üniversitesi 2006, Prentice all Giriş Karbon-karbon ikili bağı içeren hidrokarbonlardır Bazen olefinler olarak da adlandırılırlar, olefin= oil-forming
Bölüm 11 Alkoller ve Eterler. Alkollerin Yapısı. Sınıflandırma. Hidroksil (-OH) fonksiyonel grubu Oksijen sp 3 melezleşmiştir. =>
 Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
Hidroklorik asit ve sodyum hidroksitin reaksiyonundan yemek tuzu ve su meydana gelir. Bu kimyasal olayın denklemi
 KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
Alkenlerin Kimyasal Özellikleri KATILMA TEPKİMELERİ
 Alkenlerin Kimyasal Özellikleri KATILMA TEPKİMELERİ ALKENLERİN KİMYASAL ÖZELLİKLERİ Alkenler sahip oldukları pi bağları sayesinde pek çok farklı kimyasal tepkimeyi gerçekleştirebilirler. Buna göre alkenlerin
Alkenlerin Kimyasal Özellikleri KATILMA TEPKİMELERİ ALKENLERİN KİMYASAL ÖZELLİKLERİ Alkenler sahip oldukları pi bağları sayesinde pek çok farklı kimyasal tepkimeyi gerçekleştirebilirler. Buna göre alkenlerin
ÇÖZELTILERDE DENGE. Asitler ve Bazlar
 ÇÖZELTILERDE DENGE Asitler ve Bazlar Zayıf Asit ve Bazlar Değişik asitler için verilen ph değerlerinin farklılık gösterdiğini görürüz. Bir önceki konuda ph değerinin [H₃O + ] ile ilgili olduğunu gördük.
ÇÖZELTILERDE DENGE Asitler ve Bazlar Zayıf Asit ve Bazlar Değişik asitler için verilen ph değerlerinin farklılık gösterdiğini görürüz. Bir önceki konuda ph değerinin [H₃O + ] ile ilgili olduğunu gördük.
4-ALKENLER (Olefinler)
 4-ALKENLER (Olefinler) Alkenler yapılarında C=C karbon-karbon çift bağları içeren bileşiklerdir ve bunlara olefinler de denir, yaygın olarak kullanılan isim alkenlerdir. Alkenler tabiatta birçok yerde
4-ALKENLER (Olefinler) Alkenler yapılarında C=C karbon-karbon çift bağları içeren bileşiklerdir ve bunlara olefinler de denir, yaygın olarak kullanılan isim alkenlerdir. Alkenler tabiatta birçok yerde
Bolum 11&12 Eterler, Epoksitler, Sülfitler
 Bolum 11&12 Eterler, Epoksitler, Sülfitler Giriş Eter Formülü R--R (R ve R alkil veya aril). Simetrik ve asimetrik olabilir Örnekler: C 3 C 3 C 3 2 Yapı ve Polarite Eğik moleküler geometri ksijen sp 3
Bolum 11&12 Eterler, Epoksitler, Sülfitler Giriş Eter Formülü R--R (R ve R alkil veya aril). Simetrik ve asimetrik olabilir Örnekler: C 3 C 3 C 3 2 Yapı ve Polarite Eğik moleküler geometri ksijen sp 3
BALIKESİR ÜNİVERSİTESİ EĞİTİM ÖĞRETİM YILI ORGANİK SENTEZ ÖDEVİ HAZIRLAYAN: *Lokman LİV *FEF / KİMYA 1.ÖĞRETİM *
 BALIKESİR ÜNİVERSİTESİ 2008-2009EĞİTİM ÖĞRETİM YILI ORGANİK SENTEZ ÖDEVİ HAZIRLAYAN: *Lokman LİV *FEF / KİMYA 1.ÖĞRETİM *200610105035 ALDOL KONDENSASYONU Enolat Anyonlarının Aldehit ve Ketonlara Katılması
BALIKESİR ÜNİVERSİTESİ 2008-2009EĞİTİM ÖĞRETİM YILI ORGANİK SENTEZ ÖDEVİ HAZIRLAYAN: *Lokman LİV *FEF / KİMYA 1.ÖĞRETİM *200610105035 ALDOL KONDENSASYONU Enolat Anyonlarının Aldehit ve Ketonlara Katılması
5-AROMATİK BİLEŞİKLER.
 5-AROMATİK BİLEŞİKLER. Organik kimyada çok geç tanınan, yapısı ve reaktifliği çok geç anlaşılan bileşiklerdir. İlk önce kimyacıların karşısına çıkan C6H5- temel yapısını içeren moleküller anlaşılmakta
5-AROMATİK BİLEŞİKLER. Organik kimyada çok geç tanınan, yapısı ve reaktifliği çok geç anlaşılan bileşiklerdir. İlk önce kimyacıların karşısına çıkan C6H5- temel yapısını içeren moleküller anlaşılmakta
POLİMER KİMYASI -12. Prof. Dr. Saadet K. Pabuccuoğlu
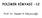 POLİMER KİMYASI -12 Prof. Dr. Saadet K. Pabuccuoğlu İYONİK POLİMERİZASYON Başlama Tipi Monomer Radikal Katyonik Anyonik Etilen + - + 1-alkil alkenler (α-olefinler) - - + 1,1-dialkil alkenler - + - 1,3-dienler
POLİMER KİMYASI -12 Prof. Dr. Saadet K. Pabuccuoğlu İYONİK POLİMERİZASYON Başlama Tipi Monomer Radikal Katyonik Anyonik Etilen + - + 1-alkil alkenler (α-olefinler) - - + 1,1-dialkil alkenler - + - 1,3-dienler
ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ
 ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ ALKANLAR Alkanların Fiziksel Özellikleri Alkan bileşikleri apolar yapılı moleküllerden oluşur. Bu yüzden molekülleri arasında zayıf London kuvvetleri bulunmaktadır.
ALKANLAR FİZİKSEL VE KİMYASAL ÖZELLİKLERİ ALKANLAR Alkanların Fiziksel Özellikleri Alkan bileşikleri apolar yapılı moleküllerden oluşur. Bu yüzden molekülleri arasında zayıf London kuvvetleri bulunmaktadır.
2,5-Heksandion, C1 ve C3 karbonlarındaki hidrojenlerin baz tarafından alınmasıyla iki farklı enolat oluşturabilir:
 PROBLEM 14.1 PROBLEM 14.2 Tepkimenin yükseltgen koşullarında diol bileşiğinin önce bir hidroksil grubu yükseltgenerek (A) ve (B) bileşiklerinin karışımını oluşturur. Tepkime sırasında bu iki bileşik tekrar
PROBLEM 14.1 PROBLEM 14.2 Tepkimenin yükseltgen koşullarında diol bileşiğinin önce bir hidroksil grubu yükseltgenerek (A) ve (B) bileşiklerinin karışımını oluşturur. Tepkime sırasında bu iki bileşik tekrar
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI
 ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI Prof. Dr. Mustafa DEMİR M.DEMİR 0ASİT VE BAZ KAVRAMLARI Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır.
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI Prof. Dr. Mustafa DEMİR M.DEMİR 0ASİT VE BAZ KAVRAMLARI Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır.
ERKAN ALTUN
 2008-200 2009 EĞİTİM M VE ÖĞRETİM M YILI 200610105003 ERKAN ALTUN RGANİK K SENTEZLER SCHMİDTH REAKSİYNLARI Hidrojen azidin elektrofillerle (karbonil bileşikleri,tersiyer ikleri,tersiyer alkoller,alkenler
2008-200 2009 EĞİTİM M VE ÖĞRETİM M YILI 200610105003 ERKAN ALTUN RGANİK K SENTEZLER SCHMİDTH REAKSİYNLARI Hidrojen azidin elektrofillerle (karbonil bileşikleri,tersiyer ikleri,tersiyer alkoller,alkenler
Aromatik nitro bileşiklerinin sentezlerinde aşağıdaki yollardan faydalanılabilir.
 1.1.1. Nitrolama ve Aromatik Nitro Bileşikleri Farmasötik önemi olan kimyasal maddeler arasında aromatik nitro bileşikleri (Ar-NO 2) önemli bir yer tutmaktadır. Nitro (-NO 2) grubu ilaç etken maddelerinin
1.1.1. Nitrolama ve Aromatik Nitro Bileşikleri Farmasötik önemi olan kimyasal maddeler arasında aromatik nitro bileşikleri (Ar-NO 2) önemli bir yer tutmaktadır. Nitro (-NO 2) grubu ilaç etken maddelerinin
Birbiri ile ikili bağla bağlanmış karbon ve. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
 ALDEHİT ve KETNLAR Birbiri ile ikili bağla bağlanmış karbon ve oksijene (C=) karbonil grubu denir. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
ALDEHİT ve KETNLAR Birbiri ile ikili bağla bağlanmış karbon ve oksijene (C=) karbonil grubu denir. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
ADI VE SOYADI GÜZ YARIYILI MBG ORGANİK KİMYA FİNAL SINAVI
 1 ADI VE SYADI : 2013-2014 GÜZ YAIYILI MBG GAİK KİMYA İAL SIAVI 20.01.2014 SIAV AKKKIDA BİLGİ: 40 TAE TEST SUSU (50 PUA), 5 TAE KLASİK SU (50 PUA) VADI. SULA ve ÇÖZÜMLE 1.Aşağıdaki yapılardan hangisinde
1 ADI VE SYADI : 2013-2014 GÜZ YAIYILI MBG GAİK KİMYA İAL SIAVI 20.01.2014 SIAV AKKKIDA BİLGİ: 40 TAE TEST SUSU (50 PUA), 5 TAE KLASİK SU (50 PUA) VADI. SULA ve ÇÖZÜMLE 1.Aşağıdaki yapılardan hangisinde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1
 ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1 Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır. Hangi tanımın
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1 Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır. Hangi tanımın
BİLEŞİKLER VE FORMÜLLERİ
 BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
Hidrojen ve halojenin yer aldığı veya almadığı koşullarda karbon ve oksijen içeren bileşikler
 Uluslararası Patent Sınıflandırması C Sınıfı2 Hidrojen ve halojenin yer aldığı veya almadığı koşullarda karbon ve oksijen içeren bileşikler (kolesterol veya türevlerinin irradyasyon ürünleri 401/00; irradyasyonsuz
Uluslararası Patent Sınıflandırması C Sınıfı2 Hidrojen ve halojenin yer aldığı veya almadığı koşullarda karbon ve oksijen içeren bileşikler (kolesterol veya türevlerinin irradyasyon ürünleri 401/00; irradyasyonsuz
Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır.
 7. ASİTLER VE BAZLAR Arrhenius AsitBaz Tanımı (1884) (Svante Arrhenius) Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır. HCl H + + Cl NaOH
7. ASİTLER VE BAZLAR Arrhenius AsitBaz Tanımı (1884) (Svante Arrhenius) Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır. HCl H + + Cl NaOH
KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü
 KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 13 Asitler ve
KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 13 Asitler ve
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
Ödevleri teslim ederken bu soru sayfası da verilmek zorundadır.
 12. BÖLÜM: ARENLERİN REAKSİYONLARI: ELEKTROFİLİK AROMATİK YER DEĞİŞTİRME TEPKİMELERİ (ÖDEV TESLİM TARİHİ 13/03/2017) 1) Aşağıda verilen tepkimelerin ana organik ürününü yazınız. 2) aşağıda verilen bileşiği
12. BÖLÜM: ARENLERİN REAKSİYONLARI: ELEKTROFİLİK AROMATİK YER DEĞİŞTİRME TEPKİMELERİ (ÖDEV TESLİM TARİHİ 13/03/2017) 1) Aşağıda verilen tepkimelerin ana organik ürününü yazınız. 2) aşağıda verilen bileşiği
5.111 Ders Özeti #12. Konular: I. Oktet kuralından sapmalar
 5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
NÜKLEOFİLİK YERDEĞİŞTİRME REAKSİYONLARI
 NÜKLEOFİLİK YERDEĞİŞTİRME REAKSİYONLARI NEGATİF BİR İYON VEYA PAYLAŞILMAMIŞ ELEKTRON ÇİFTİ BULUNAN NÖTRAL BİR MOLEKÜL OLARAK BİLİNEN NÜKLEOFİL, ORGANİK BİR SUBSTRATTAN AYRILAN GRUBUN YERİNİ ALIR. NÜKLEOFİLİK
NÜKLEOFİLİK YERDEĞİŞTİRME REAKSİYONLARI NEGATİF BİR İYON VEYA PAYLAŞILMAMIŞ ELEKTRON ÇİFTİ BULUNAN NÖTRAL BİR MOLEKÜL OLARAK BİLİNEN NÜKLEOFİL, ORGANİK BİR SUBSTRATTAN AYRILAN GRUBUN YERİNİ ALIR. NÜKLEOFİLİK
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL
 DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar.
 Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
www.kimyahocam.com HİDROKARBONLAR I ÖRNEK 1
 İDROKARBONLAR Yalnızca karbon (C) ve hidrojen () elementlerinden oluşan bileşiklere hidrokarbon denir. Karbon elementinin atom numarası 6 dır. Elektron dizilişi, 1s 2 2s 2 2p 2 olup değerlik elektron say
İDROKARBONLAR Yalnızca karbon (C) ve hidrojen () elementlerinden oluşan bileşiklere hidrokarbon denir. Karbon elementinin atom numarası 6 dır. Elektron dizilişi, 1s 2 2s 2 2p 2 olup değerlik elektron say
6. Deney Hidrokarbonların Belirlenmesi
 6. Deney Hidrokarbonların Belirlenmesi Genel Prensipler Yapıları ve kimyasal davranışları esas alındığında, hidrokarbonlar üç kategoriye ayrılabilir. Doymuş Alifatik Hidrokarbonlar: Tüm karbon atomlarının
6. Deney Hidrokarbonların Belirlenmesi Genel Prensipler Yapıları ve kimyasal davranışları esas alındığında, hidrokarbonlar üç kategoriye ayrılabilir. Doymuş Alifatik Hidrokarbonlar: Tüm karbon atomlarının
4. Asetilen katımı: Aldehit ve ketonlara
 4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
amonyak primer amin sekonder amin tersiyer amin
 DENEY 9-Bölüm 1 AMĐNLE VE DĐAZONYUM BĐLEŞĐKLEĐ Genel Prensipler Aminler amonyak üzerindeki hidrojenlerin organik gruplar ile değiştirilmesi sonucu türetilen organik bazlardır. Değiştirilen hidrojenlerin
DENEY 9-Bölüm 1 AMĐNLE VE DĐAZONYUM BĐLEŞĐKLEĐ Genel Prensipler Aminler amonyak üzerindeki hidrojenlerin organik gruplar ile değiştirilmesi sonucu türetilen organik bazlardır. Değiştirilen hidrojenlerin
Lewis Nokta Yapıları ve VSEPR
 6 DENEY Lewis Nokta Yapıları ve VSEPR 1. Giriş Bu deneyde moleküllerin Lewis Nokta yapıları belirlenecek ve VSEPR kuralları ile molekülün geometrisi ve polaritesi tayin edilecektir. 2. Lewis Nokta Yapıları
6 DENEY Lewis Nokta Yapıları ve VSEPR 1. Giriş Bu deneyde moleküllerin Lewis Nokta yapıları belirlenecek ve VSEPR kuralları ile molekülün geometrisi ve polaritesi tayin edilecektir. 2. Lewis Nokta Yapıları
