KİMYA II DERS NOTLARI
|
|
|
- Bulut Akyıldız
- 9 yıl önce
- İzleme sayısı:
Transkript
1 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 KİMYA II DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Birden fazla maddenin kimyasal özellikleri değişmeyecek şekilde rasgele oranlarda bir araya getirilmesi ile oluşturulan yeni maddelere karışım adı verilir. Maddenin üç hali (katı, sıvı ve gaz) doğada ve hemen her türlü kullanımda tek başına bulunmaz. Katı, sıvı ve gaz fazındaki iki veya daha fazla madde birbirleriyle çeşitli şekillerde karışarak fiziksel karışım sistemlerini oluştururlar. Bu konuda fiziksel karışımların türleri, genel özellikleri incelenecek, karışımların özelliklerinin nitel ve nicel açıklamasında kullanılan yasa ve teorilere yer verilecektir. Karışımların Özellikleri Saf değildirler Karışımı oluşturan maddelerin kimyasal özellikleri korunur Fiziksel yollarla ayrıştırılabilirler Erime ve kaynama noktaları sabit değildir Sabit bir özkütleleri yoktur Karışımı oluşturan maddeler arasında sabit bir oran yoktur 1 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
2 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Karışımlar ikiye ayrılırlar ; Homojen Karışımlar: Her yerinde aynı özellikleri gösteren karışımlara homojen karışım denir. Çözelti olarak ta adlandırılan homojen karışımlar tek bir madde gibi davranırlar. Heterojen Karışımlar:değişik yerlerinde farklı özellikler gösteren karışımlara heterojen karışımlar denir. Heterojen karışımlar emülsiyon ve süspansiyon olmak üzere ikiye ayrılırlar. Emülsiyon: Bir sıvının başka bir sıvı içinde oluşturduğu heterojen karışımlara emülsiyon karışım adı verilir. Heterojen Karışımlar Elde edilen karışımın fiziksel özellikleri çoğunlukla karışımı meydana getiren maddelerin fiziksel özelliklerinin ortalamasıdır. Heterojen bir karışımda fazlardan biri diğeri içinde ince dağılmış halde bulunur. İki fazlı bu karışımlara genelde dispers sistemler adı verilir. Herhangi bir faz içinde dağılmış olan faza dispers faz veya iç faz, dispers fazın dağıldığı ve ortamı teşkil eden faza ise dispersiyon aracı veya dış faz denir. Süspansiyon: Bir sıvı içerisinde bir katının tam olarak çözülmeyip küçük zerrecikler halinde dağılmasıyla oluşan heterojen karışımlara emülsiyon karışım adı verilir. Maddenin hallerine bağlı olarak çeşitli dispers sistemler söz konusu olabilir. En çok bilinen dispers sistemlerin bazıları tabloda verilmiştir. Disperse Faz Katı Sıvı Gaz Dispersiyon Ortamı Gaz Gaz Sıvı Sistem Duman Sis Köpük Karbon-Hava Su-Hava Sabun-Su Katı Sıvı Süspansiyon Kireç sütü Sıvı Sıvı Emülsiyon Benzen-Su 2 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
3 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Dispers sistemler akışkan olmaları ve çoğunlukla homejen görüntü vermeleri nedeni ile çözeltilere benzetilerek kolloidal çözelti kavramı ile tanımlanırlar. Ancak kaba süspansiyonları bu tanımın dışında tutmak gerekir. Genellikle ince dağılan maddenin veya moleküllerinin boyutu 1-1 Å (,1-1 mm) arasında ise meydana gelen karışıma kolloidal çözelti denir. Tanecikler bundan daha büyükse kaba süspansiyon, daha küçük ise gerçek çözelti sınırı başlar. Kolloidal Çözeltiler Gerçek bir çözelti, molekül veya iyon birimine çözünerek parçalanma sonucunda meydana gelir. Bir çözücü içinde çözünen bir madde molekül veya iyonlarına ayrılır ve bu küçük iyonlar veya moleküller çözücü içinde öyle dağılır ki çözelti göze saydam görünür. Gerçek çözelti homojendir. Kolloidal bir çözelti ise gerçek çözeltiden farklı olarak heterojendir, saydamlığı az veya bazen hiç yoktur. Çözünen maddenin molekülleri (makro moleküller) veya maddenin tanecikleri büyük ise böyle bir madde çözücü içinde dağılarak kolloidal çözelti oluşturur. Kolloidal çözeltiler; Sol, Emülsiyon, Köpük gibi bazı gruplara ayrılır. Soller Soller, katı, sıvı veya gaz içinde bir katı maddenin dispersiyona uğramasıyla oluşur. Bunlardan ikincisi (sıvı içinde katı) olanlar genel olarak Kolloid adını alır. Su içinde altın, su içinde arsenik sülfür, su içinde kükürt kolloidlere örnek olarak verilebilir. Dispersiyon ortamı su ise böyle bir sol hidrosol adını alır. Ortam alkol ise alkosol denir. Eğer kolloid parçacıkları suyu kendilerine çekerlerse hidrofilik sol (hidratize oksitler, nişasta ve protein solleri), suyu çekmezlerse hidrofobik sol (gümüş klorür baryum sülfat suda dispersiyona uğramışsa hidrofobik sol meydana gelir) adları kullanılır. 3 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
4 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Ayrıca daha genel olarak, Liyofil terimi sıvı çeken veya sıvı seven kolloidler için ve liyofob terimi de sıvı çekmeyenler için kullanılır. Kolloid parçacıkların en önemli özelliklerinden biri de elektrikçe yüklü olmalarıdır. Dispersiyon ortamı gaz olduğunda meydana gelen bu sol katı aerosol adını alır duman, volkan tozları, amonyum klorür buharı gibi. Benzer şekilde dispers faz bir sıvı dispersiyon ortamı bir gaz ise buna sıvı aerosol (sis) denir. Emülsiyonlar ve Köpükler Emülsiyon, benzen içinde su ve süt örneklerinde olduğu gibi, birbiri içinde çözünmeyen iki sıvıdan birinin diğeri içindeki dispersiyonu ile elde edilir. Elektrik yükleri ve çok küçük olan boyutları sayesinde dispers sistem oluşturabilirler. Ayrıca dispersiyona uğrayan maddenin konsantrasyonu küçüktür. Tanecikler birinciye göre çok büyük olduğundan, yüzeylerindeki elektrik yükü onları kolloidal halde tutmaya yetmez. O halde böyle bir emülsiyonu yapabilmek ve koruyabilmek için özel bazı maddeler katılması gereklidir. Bu maddelere emülgatör denir. Bu maddeler dispers faz ile dispersiyon ortamı arasında bir ara yüzey meydana getirerek kolloidal sistemin bozulmasını önler. Emülsiyon yapıcı böyle maddeler arasında; jelatin ve sabun tipinde maddeler sayılabilir. Sabunun temizleyici etkisi de kirdeki yağları emülsiyona çevrilmesi ile mümkün olmaktadır. Suda emülsiyon haline gelen yağ ve diğer kir maddeleri su ile yıkanınca kolayca uzaklaştırılmış olurlar. Sıvı içinde gaz dispersiyona uğramışsa bu köpük verir. Katı içinde katı dispersiyona uğramışsa katı sol (Al 2 O 3 ve krom içeren kıymetli taşlar) elde edilir. Katı içinde sıvı halinde katı emülsiyon (kuvartz, opal) söz konusudur. Katı içinde gaz dispersiyona uğramışsa katı köpükten (süngerimsi volkanik taşlar) söz edilir. Kolloidlerin Genel ve Optik Özellikleri Kaba bir dispersiyon karışımı basit bir süzgeçten geçirilirse taneciklerle sıvıyı birbirinden ayırmak mümkün olur. Kolloidal çözelti ise süzme ile ayrılamaz. Ancak özel filtreler kullanılırsa bu ayırma mümkün olur. Seramik maddelerden yapılan bu tür filtrelere ultra filtre denir. Kolloid süspansiyonlarda taneciklerin çok büyük olmasından dolayı difüzyon yok gibidir. Gerçek çözeltide ise bilindiği gibi iyonlar sürekli hareket halinde olup çözelti içinde bir yerden başka bir yere doğru belli bir hızla difüzlenirler. Kolloidal taneciklerin gözlenmesi ultramikroskop ya da elektron mikroskobu ile yapılır. 4 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
5 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Kolloid çözeltiler bazen gerçek bir çözelti gibi saydam görünebilir, bazen de saydam olmayan bulanık (opak) şekildedirler. Saydam olan kolloid bir çözelti, bir ışık demeti ile aydınlatılıp buna dik yönden gözlenirse bulanık görünür. Buna Tyndall olayı denir. Tyndall olayı sayesinde kolloid parçacıklarının görülebilmesi mümkündür. Homojen Karışımlar Fiziksel ve kimyasal bazı özelikleri bakımından benzer olan iki veya daha fazla madde birbirleriyle atomik boyutta (ölçülerde) karışarak homojen karışımları meydana getirirler. Meydana gelen bu karışımların fiziksel özellikleri bileşenlerin fiziksel özelliklerinin ortalamasıdır. Homojen karışımlar genelde çözelti olarak adlandırılır ve maddenin 3 hali göz önüne alınırsa, 9 türlü çözeltinin mümkün olabildiği görülür. Çözeltiler tek fazlı sistemlerdir ve karışım içersinde miktarca çok olan bileşene çözücü, az olana çözünen madde denir. Örneğin alkol ve suyun meydana getirdiği çözeltide su oranı fazla olduğunda, alkol suda çözünmüştür. Alkol oranı fazla ise, çözücü alkol çözünen madde sudur. Çözeltilerle İlgili Kavramlar Çözünürlük : Belli bir sıcaklıkta doymuş bir çözeltinin birim hacimde çözünmüş bulunan madde miktarıdır. Birimi g/ 1 ml veya mol/l olabilir. Doymuş Çözelti : Çözeltide belli bir sıcaklıkta çözünen maddenin limit miktarının çözülmesiyle elde edilen çözeltidir. Çökme : Bir kimyasal reaksiyon sonucunda çözünürlüğü az olan bileşiğin meydana gelmesi ile gerçekleşir. Pb(NO 3 ) 2 çözeltisine KI ilavesi Suya ilave edilen KI 5 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
6 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Çözeltilerle İlgili Kavramlar Kristalizasyon : Bir çözeltinin sıcaklığı artırılır ve bir miktar daha çözünen ilave edilirse, doymuş çözelti elde edilir. Soğutmayla, sonradan ilave edilen miktar, homojen çözelti ortamından ayrılarak katı faz oluşturur. Çözünürlük çarpımı : Belli bir sıcaklıkta doymuş bir çözeltide bulunan çözünmüş madde iyonlarının molar derişimlerinin çarpımıdır. Disosyasyon : İyonik yapılı bileşiklerin çözücü içerisinde iyonlarına ayrılması suretiyle çözünmesidir. Örneğin : AlCI 3 Al CI - Çözeltilerle İlgili Kavramlar Asosyasyon : Çözünen madde iyonlarının birleşerek tekrar molekülü oluşturmalarıdır. CH 3 COOH CH 3 COO - + H + dengesinde sağ tarafa olan reaksiyon disosyasyon, sol tarafa olan ise asosyasyon olarak adlandırılır. Solvasyon : Çözünen madde iyonlarının çözücü molekülleri ile sarılmasıdır. Çözücü su olduğunda hidrasyon adını alır. Cu H 2 O Cu[(H 2 O) 4 ] +2 Raoult Kanunu Çözeltinin buhar basıncı, çözücünün mol kesri ile çözücünün saf buhar basıncı çarpımına eşittir. P = P. x P çözelti = çözeltinin buhar basıncı P çözücü = saf çözücünün buhar basıncı X çözücü = çözücünün mol kesri Raoult Kanunu P P. x P = P çözelti = Pçözünen + Pçözücü = P.(1 x P P = x P = P P = x çözelti çözünen P ) çözünen. çözücü P çözünen. çözücü x çözünen + x çözücü =1 6 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
7 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi C de 15 mol su içerisinde 1 mol glukoz çözünüyor. Bu sıcaklıkta saf suyun buhar basıncı mmhg olduğuna göre bileşenlerin mol kesirlerini ve çözeltinin buhar basıncını bulunuz. P = P. x P X g X Su = = = = = = C de 5 g suda 18.3 g NaCI ün çözülmesiyle hazırlanan çözeltinin buhar basıncı kaç mmhg dır? Saf çözücüye göre buhar basıncındaki düşme ne kadardır? Bu sıcaklıkta saf suyun buhar basıncı mmhg dır X 58.5 NaCI = = P = P. x 5 X 18 Su = = P = = mmhg P = Pçözücü Pçözelti = = 2. 57mmHg 25 C de Saf suyun buhar basıncındaki düşme 1.5 mmhg olması için 32 g suya kaç g sakkaroz eklenmelidir? Bu sıcaklıkta saf suyun buhar basıncı 23.8 mmhg dır. Sakkaroz un molekül ağırlığı ise 342 g/mol. P = P P = x çözelti P çözünen. çözücü m 1.5 = m m = 41 g 7 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
8 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Kaynama Noktası Yükselmesi Ebülyoskopi Diğer taraftan bir çözücüye, uçucu olmayan bir madde eklenmesi ile çözücü moleküllerinin kaçma eğiliminin daha küçük olmasına bağlı olarak, çözeltinin buhar basıncının düşmesi, çözeltilerin kaynama ve donma noktalarını etkiler. Uçucu olmayan bir çözünen etkisi ile buhar basıncı düşürülen çözelti, saf çözücünün normal kaynama noktasında kaynamaz ve çözeltinin buhar basıncını atmosferik basınca eşit yapabilmek için sıcaklığının çözücünün normal kaynama sıcaklığının üstüne çıkarılması gerekir. Burada T b, kaynama noktası yükselmesi, m çözelti molalitesi Kb, çözücünün molal kaynama noktası yükselmesi sabitidir. Kb'nin değeri çözücünün cinsine bağlı olup, çözünen maddeye bağlı değildir. Örneğin H 2 O için K b değeri,512 C/m iken benzen için 2,53 C/m, etil alkol için 1,22 C/m, karbon tetraklorür için 5,2 C/m, kloroform için 3,63 C/m'dir. T b = K b m Donma Noktasında Düşme Kriyoskopi Çözeltilerin donma noktaları saf çözücülerden daha düşüktür. Elektrolit olmayan seyreltik bir çözeltinin donma noktası alçalması çözünen maddenin konsantrasyonu ile doğru, çözünen maddenin mol tartısı ile ters orantılıdır Ebülyoskopi ve Kriyoskopi sabitleri T f, donma noktası alçalması, m çözelti molalitesi K f, çözücünün molal donma noktası alçalması sabitidir. 8 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
9 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Sulu çözeltilerin molal donma noktası düşmesi sabiti -1,86 C/m olduğuna göre, 1 gram suda 9 gram glikoz (C 6 H 12 O 6 ) çözülerek hazırlanan çözeltinin kaynama ve donma noktaları nedir? (Glikozun mol kütlesi, 18 g/mol'dür). Çözeltinin molalitesi 1 g suda çözünmüş glikozun mol sayısına eşittir. suyun normal donma noktası, C olduğundan çözeltinin donma noktası, C -,93 C = -,93 C bulunur. Suyun normal kaynama noktası 1 C'dır. Buna göre çözeltinin kaynama noktası; 1 +,256 = 1,256 C'dır. 5,12 gram elektrolit olmayan naftalin (C 1 H 8 ), 1 gram CCl 4 'de çözündüğünde çözeltinin kaynama noktası 2 C yükselmektedir. Buna göre CCl 4 'ün kaynama noktası sabiti kaçtır? (C: 12, H: 1) T b = K b m =. b k K b = 5 Mol kütlesi bilinmeyen bir maddenin 4 gramı 2 gram suda çözülüyor. Çözelti C da donuyor. Buna göre çözünen maddenin mol kütlesi nedir? = ( 1.86). M A.2 M A = 14.9 g/mol 9 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
10 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Soru? Otomobillerde kullanılan antifiriz etilen glikolün sudaki çözeltisidir. 25 C ye dayanabilen bir antifiriz yapmak istesek 1 kg suya ne kadar etilen glikol (C 2 H 6 O 2 ) katmamız gerekir. C : 12 H : 1 O : 16 Osmotik Basınç ve Osmoz Olayı Yarı geçirgen bir zarla ayrılmış çözücü ve çözeltiden ibaret bir sistemde saf çözücü moleküllerinin çözeltiye geçmesine osmoz denir. Örneğin sulu şeker çözeltisi/su sisteminde su molekülleri yarı geçirgen zardan geçer ancak şeker molekülleri geçemez. Bu şekilde çözücü moleküllerinin saf çözücüden çözeltiye doğru yarı geçirgen zardan geçişini durdurmak için çözelti tarafından uygulanan basınca osmotik basınç denir. Kırmızı kan hücresinde çözünmüş bulunan taneciklerin derişimi yaklaşık olarak.3 M dır. Hücreler yarıgeçirgen bir zarla (membran) çevrilidir. 298 K de hücreler kan plazmasından uzaklaşıyorsa hücre içindeki osmotik basınç ne kadardır? Burada π Osmotik basınç c molar konsantrasyon R gaz sabiti T mutlak sıcaklıktır 1 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
11 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27 Osmoz Olayının Kullanımı 11 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 27
KARIŞIMLAR. İki ya da daha fazla saf maddenin özelliklerini kaybetmeden bir araya gelmesiyle oluşan maddelere karışım denir.
 KARIŞIMLAR KARIŞIMLARIN SINIFLANDIRILMASI: İki ya da daha fazla saf maddenin özelliklerini kaybetmeden bir araya gelmesiyle oluşan maddelere karışım denir. Karışımların özellikleri: Saf olmayan maddelerdir.
KARIŞIMLAR KARIŞIMLARIN SINIFLANDIRILMASI: İki ya da daha fazla saf maddenin özelliklerini kaybetmeden bir araya gelmesiyle oluşan maddelere karışım denir. Karışımların özellikleri: Saf olmayan maddelerdir.
ÇÖZELTĐLERDEKĐ TANECĐK SAYISINA BAĞLI ÖZELLĐKLER
 ÇÖZELTĐLERDEKĐ TANECĐK SAYISINA BAĞLI ÖZELLĐKLER Çözeltilerin kısmi buhar basıncı Đdeal çözelti (Molalite) Kaynama noktası yükselmesi Donma noktası alçalması Osmoz olayı Hedef: Çözeltideki tanecik sayısına
ÇÖZELTĐLERDEKĐ TANECĐK SAYISINA BAĞLI ÖZELLĐKLER Çözeltilerin kısmi buhar basıncı Đdeal çözelti (Molalite) Kaynama noktası yükselmesi Donma noktası alçalması Osmoz olayı Hedef: Çözeltideki tanecik sayısına
BİTKİ FİZYOLOJİSİ. 2. Hafta
 BİTKİ FİZYOLOJİSİ 2. Hafta 1 Su Bitki Bünyesinin Bileşimi Bitkilerin hayatsal faaliyetleri için çok gerekli olan maddedir. - Hücre protoplazmasının %80-95 ini oluşturur. - Tüm metabolik olaylarda kullanılan
BİTKİ FİZYOLOJİSİ 2. Hafta 1 Su Bitki Bünyesinin Bileşimi Bitkilerin hayatsal faaliyetleri için çok gerekli olan maddedir. - Hücre protoplazmasının %80-95 ini oluşturur. - Tüm metabolik olaylarda kullanılan
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ
 ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
Çözeltiler ve Fiziksel Özellikleri
 Çözelti Türleri: Bazı Terimler Çözeltiler ve Fiziksel Özellikleri Çözeltiler, homojen karışımlardır. Homojendir. Çünkü, bileşimi ve özellikleri tekdüzedir. Karışımdır. Çünkü, oranları değişen iki veya
Çözelti Türleri: Bazı Terimler Çözeltiler ve Fiziksel Özellikleri Çözeltiler, homojen karışımlardır. Homojendir. Çünkü, bileşimi ve özellikleri tekdüzedir. Karışımdır. Çünkü, oranları değişen iki veya
Maddenin Ayırtedici Özellikleri
 Maddenin Ayırtedici Özellikleri Bir maddeyi diğer maddelerden ayırmaya yarayan özellikleri Ayırtedici Özellikler denir. Bunlar; Özkütle (Yoğunluk) Erime Noktası Kaynama Noktası Çözünürlük Esneklik İletkenlik
Maddenin Ayırtedici Özellikleri Bir maddeyi diğer maddelerden ayırmaya yarayan özellikleri Ayırtedici Özellikler denir. Bunlar; Özkütle (Yoğunluk) Erime Noktası Kaynama Noktası Çözünürlük Esneklik İletkenlik
PROJE TABANLI DENEY UYGULAMALARI KARIŞIMLARIN BĐLEŞENLERĐNE AYRILMASI
 PROJE TABANLI DENEY UYGULAMALARI KARIŞIMLARIN BĐLEŞENLERĐNE AYRILMASI ORTAÖĞRETĐM KĐMYA DENEYLERĐ PROF. DR. ĐNCĐ MORGĐL GÜLDEN KAYA HACETTEPE ÜNĐVERSĐTESĐ ANKARA 2007 PROJE HEDEF SORUSU: KARIŞIMLARIN BĐLEŞENLERĐNE
PROJE TABANLI DENEY UYGULAMALARI KARIŞIMLARIN BĐLEŞENLERĐNE AYRILMASI ORTAÖĞRETĐM KĐMYA DENEYLERĐ PROF. DR. ĐNCĐ MORGĐL GÜLDEN KAYA HACETTEPE ÜNĐVERSĐTESĐ ANKARA 2007 PROJE HEDEF SORUSU: KARIŞIMLARIN BĐLEŞENLERĐNE
Kimyafull Gülçin Hoca
 KOLLİGATİF ÖZELLİKLER Kimyafull Gülçin Hoca Buhar basıncının düşmesi Kaynama sıcaklığının yükselmesi Donma sıcaklığının düşmesi Ozmotik basınç A) BUHAR BASINCI DÜŞMESİ RAOULT yasası: Bir çözeltiyi oluşturan
KOLLİGATİF ÖZELLİKLER Kimyafull Gülçin Hoca Buhar basıncının düşmesi Kaynama sıcaklığının yükselmesi Donma sıcaklığının düşmesi Ozmotik basınç A) BUHAR BASINCI DÜŞMESİ RAOULT yasası: Bir çözeltiyi oluşturan
ELEMENT Aynı tür atomlardan oluşmuş saf maddelere element denir. ELEMENTLERİN ÖZELLİKLERİ 1. Aynı tür atomlardan oluşurlar. 2. Saf ve homojendirler.
 SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
SAF MADDE: Aynı cins atom ya da moleküllerden oluşmuş maddelere, saf medde ÖR. Elementler saf maddelerdir. Çünkü; hepsi aynı cins atomlardan oluşmuşlardır. Bileşikler saf maddelerdir. Çünkü; hepsi aynı
Hücrede Madde Alışverişi
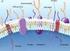 Hücrede Madde Alışverişi Basit difüzyon Hücre Zarından Madde Geçişleri Küçük moleküllerin geçişi Glikoz, Karbondioksit, Oksijen, Vitamin, Su, Amonyak, Aminoasit, Yağ asidi, Mineral, Gliserol Pasif taşıma
Hücrede Madde Alışverişi Basit difüzyon Hücre Zarından Madde Geçişleri Küçük moleküllerin geçişi Glikoz, Karbondioksit, Oksijen, Vitamin, Su, Amonyak, Aminoasit, Yağ asidi, Mineral, Gliserol Pasif taşıma
6.PPB (milyarda bir kısım) Kaynakça Tablo A-1: Çözelti Örnekleri... 5 Tablo B-1:Kolloidal Tanecikler... 8
 İçindekiler A. ÇÖZELTİLER... 2 1.Çözünme... 2 2.Homojenlik... 4 3.Çözelti... 5 4.Çözünürlük... 5 Çözünürlüğe Sıcaklık Ve Basınç Etkisi... 6 B. KARIŞIMLAR... 7 1.Çözeltiler... 7 2.Kolloidal Karışımlar...
İçindekiler A. ÇÖZELTİLER... 2 1.Çözünme... 2 2.Homojenlik... 4 3.Çözelti... 5 4.Çözünürlük... 5 Çözünürlüğe Sıcaklık Ve Basınç Etkisi... 6 B. KARIŞIMLAR... 7 1.Çözeltiler... 7 2.Kolloidal Karışımlar...
Aeresol. Süspansiyon. Heterojen Emülsiyon. Karışım. Kolloidal. Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m m
 Aeresol Süspansiyon Karışım Heterojen Emülsiyon Kolloidal Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m - 10-6 m Homojen Çözelti Dağılan Faz Dağılma Fazı Kolloid Tipi katı katı,sıvı,gaz sol katı
Aeresol Süspansiyon Karışım Heterojen Emülsiyon Kolloidal Çözelti < 10-9 m Süspansiyon > 10-6 m Kolloid 10-9 m - 10-6 m Homojen Çözelti Dağılan Faz Dağılma Fazı Kolloid Tipi katı katı,sıvı,gaz sol katı
Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir maddeye çözeltinin bileşenleri denir.
 GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
GENEL KİMYA 101 ÖDEV 3
 TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
Çözeltiler. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN. Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Kocatepe Üniversitesi 2006
 Çözeltiler Çözelti, iki veya daha fazla maddenin homojen bir karışımı olup, en az iki bileşenden oluşur. Bileşenlerden biri çözücü, diğeri ise çözünendir. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr.
Çözeltiler Çözelti, iki veya daha fazla maddenin homojen bir karışımı olup, en az iki bileşenden oluşur. Bileşenlerden biri çözücü, diğeri ise çözünendir. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr.
KOLLOİD KİMYASI. kimyaca.com. Hazırlayan : Yücel GİDER
 KOLLOİD KİMYASI Kolloid; bir maddenin diğer bir madde içerisinde çıplak gözle görülemeyecek boyutta dağılmasıyla oluşan heterojen karışıma verilen isimdir. Örneğin: Kan, sis, duman... Hazırlayan : Yücel
KOLLOİD KİMYASI Kolloid; bir maddenin diğer bir madde içerisinde çıplak gözle görülemeyecek boyutta dağılmasıyla oluşan heterojen karışıma verilen isimdir. Örneğin: Kan, sis, duman... Hazırlayan : Yücel
ELEMENTLER VE BİLEŞİKLER
 ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
7. Sınıf Maddenin Tanecikli Yapısı ve Çözünme Kazanım Kontrol Sınavı
 7. Sınıf Maddenin Tanecikli Yapısı ve Çözünme Kazanım Kontrol Sınavı 1- Bir katyona ait atom parçacıkları ve sayısını gösteren sütun grafiği aşağıdakilerden hangisi gibi olabilir? Öğretmen: Çocuklar bu
7. Sınıf Maddenin Tanecikli Yapısı ve Çözünme Kazanım Kontrol Sınavı 1- Bir katyona ait atom parçacıkları ve sayısını gösteren sütun grafiği aşağıdakilerden hangisi gibi olabilir? Öğretmen: Çocuklar bu
Malzeme Bilgisi. Madde ve Özellikleri
 Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
Bölüm 14 Çalışma Soruları 8
 Çözünürlük (100 g suda g tuz) Bölüm 14 Çalışma Soruları 8 8.1) Çözünürlüğün gerçekleşmesi için, çözücü ve çözünen parçacıkları arasındaki moleküller arası çekim kuvvetlerinin, çözünen-çözünen etkileşimlerine
Çözünürlük (100 g suda g tuz) Bölüm 14 Çalışma Soruları 8 8.1) Çözünürlüğün gerçekleşmesi için, çözücü ve çözünen parçacıkları arasındaki moleküller arası çekim kuvvetlerinin, çözünen-çözünen etkileşimlerine
HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI. Hazırlayan: Hale Sümerkan. Dersin Sorumlusu: Prof. Dr.
 HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI Hazırlayan: Hale Sümerkan Dersin Sorumlusu: Prof. Dr.Đnci Morgil ANKARA 2008 ÇÖZELTĐLER Çözeltiler, iki ya da daha fazla
HACETTEPE ÜNĐVERSĐTESĐ ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞTĐRME KONU ANLATIMI Hazırlayan: Hale Sümerkan Dersin Sorumlusu: Prof. Dr.Đnci Morgil ANKARA 2008 ÇÖZELTĐLER Çözeltiler, iki ya da daha fazla
ELEMENT VE BİLEŞİKLER
 ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
KARIŞIMLAR. Çözünme: En az iki maddenin birbiri içinde homojen bir şekilde dağılmasına çözünme denir.
 ÇÖZÜCÜLER VE ÇÖZELTİLER KARIŞIMLAR Çözünme: En az iki maddenin birbiri içinde homojen bir şekilde dağılmasına çözünme denir. Çözelti: Boyutu 10 nanometreden küçük olacak şekilde dağılmış maddelerin oluşturduğu
ÇÖZÜCÜLER VE ÇÖZELTİLER KARIŞIMLAR Çözünme: En az iki maddenin birbiri içinde homojen bir şekilde dağılmasına çözünme denir. Çözelti: Boyutu 10 nanometreden küçük olacak şekilde dağılmış maddelerin oluşturduğu
5) Çözünürlük(Xg/100gsu)
 1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
DENEY I ÇÖZELTİ KONSANTRASYONLARI. Genel Bilgi
 DENEY I ÇÖZELTİ KONSANTRASYONLARI Genel Bilgi 1. Çözelti İki ya da daha fazla maddenin herhangi bir oranda bir araya gelerek oluşturdukları homojen karışıma çözelti denir. Diğer bir deyişle, bir maddenin
DENEY I ÇÖZELTİ KONSANTRASYONLARI Genel Bilgi 1. Çözelti İki ya da daha fazla maddenin herhangi bir oranda bir araya gelerek oluşturdukları homojen karışıma çözelti denir. Diğer bir deyişle, bir maddenin
MALZEME BİLGİSİ. Atomların Yapısı
 MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Atomların Yapısı 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (- yüklü) Basit
MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Atomların Yapısı 1 Atomların Yapıları Atomlar başlıca üç temel atom altı parçacıktan oluşur; Protonlar (+ yüklü) Nötronlar (yüksüz) Elektronlar (- yüklü) Basit
FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU
 FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU Fizyolojiye Giriş Temel Kavramlar Fizyolojiye Giriş Canlıda meydana gelen fiziksel ve kimyasal değişikliklerin tümüne birden yaşam denir. İşte canlı organizmadaki
FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU Fizyolojiye Giriş Temel Kavramlar Fizyolojiye Giriş Canlıda meydana gelen fiziksel ve kimyasal değişikliklerin tümüne birden yaşam denir. İşte canlı organizmadaki
 1. 250 ml 0,20 M CuSO 4 (aq) çözeltisi hazırlamak için gerekli olan CuSO 4.5H 2 O kütlesini bulunuz. Bu çözeltiden 100 ml 0,10 M CuSO 4 (aq) çözeltisini nasıl hazırlarsınız?( Cu: 63,5; S:32; O:16; H:1)
1. 250 ml 0,20 M CuSO 4 (aq) çözeltisi hazırlamak için gerekli olan CuSO 4.5H 2 O kütlesini bulunuz. Bu çözeltiden 100 ml 0,10 M CuSO 4 (aq) çözeltisini nasıl hazırlarsınız?( Cu: 63,5; S:32; O:16; H:1)
Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir.
 Anahtar Kavramlar Çözelti çözücü çözünen homojen hetorojen derişik seyreltik Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Solduğumuz hava;
Anahtar Kavramlar Çözelti çözücü çözünen homojen hetorojen derişik seyreltik Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Solduğumuz hava;
8. Sınıf Fen ve Teknoloji. KONU: Sıvılarda ve Gazlarda Basınç
 Sıvılar bulundukları kabın her yerine aynı basıncı uygulamazlar. Katılar zemine basınç uygularken sıvılar kabın her yerine basınç uygularlar. Sıvı basıncı, kapta bulunan sıvının hacmine, kabın şekline
Sıvılar bulundukları kabın her yerine aynı basıncı uygulamazlar. Katılar zemine basınç uygularken sıvılar kabın her yerine basınç uygularlar. Sıvı basıncı, kapta bulunan sıvının hacmine, kabın şekline
Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen
 ÇÖZÜCÜ VE ÇÖZÜNEN ETKİLEŞİMLERİ: Çözünme olayı ve Çözelti Oluşumu: Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen Çözünme İyonik Çözünme Moleküler
ÇÖZÜCÜ VE ÇÖZÜNEN ETKİLEŞİMLERİ: Çözünme olayı ve Çözelti Oluşumu: Bir maddenin başka bir madde içerisinde homojen olarak dağılmasına ÇÖZÜNME denir. Çözelti=Çözücü+Çözünen Çözünme İyonik Çözünme Moleküler
Cuma materyallerinden. Le Châtelier İlkesi: Denge halindeki bir sisteme dış etki uygulandığı zaman, denge dış etkiyi şekilde davranır.
 35.1 5.111 Ders 35 Kinetik Konu: Kataliz Bölüm 13 (kısım 13.14-13.15) Cuma materyallerinden Le Châtelier İlkesi: Denge halindeki bir sisteme dış etki uygulandığı zaman, denge dış etkiyi şekilde davranır.
35.1 5.111 Ders 35 Kinetik Konu: Kataliz Bölüm 13 (kısım 13.14-13.15) Cuma materyallerinden Le Châtelier İlkesi: Denge halindeki bir sisteme dış etki uygulandığı zaman, denge dış etkiyi şekilde davranır.
Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen. olarak dağılmasından oluşan sistemlere denir.
 3. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI Çözelti: Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından oluşan sistemlere denir. Çözelti derişimi
3. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI Çözelti: Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından oluşan sistemlere denir. Çözelti derişimi
Örneğin; İki hidrojen (H) uyla, bir oksijen (O) u birleşerek hidrojen ve oksijenden tamamen farklı olan su (H 2
 On5yirmi5.com Madde ve özellikleri Kütlesi, hacmi ve eylemsizliği olan herşey maddedir. Yayın Tarihi : 21 Ocak 2014 Salı (oluşturma : 2/9/2016) Kütle hacim ve eylemsizlik maddenin ortak özelliklerindendir.çevremizde
On5yirmi5.com Madde ve özellikleri Kütlesi, hacmi ve eylemsizliği olan herşey maddedir. Yayın Tarihi : 21 Ocak 2014 Salı (oluşturma : 2/9/2016) Kütle hacim ve eylemsizlik maddenin ortak özelliklerindendir.çevremizde
HAZIRLAYAN Mutlu ŞAHİN. Hacettepe Fen Bilgisi Öğretmenliği
 HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 1 DENEYİN ADI: ÇÖZELTİLER DENEYİN AMACI: FARKLI DERİŞİMLERDE ÇÖZELTİ HAZIRLAYABİLME TEORİK BİLGİ: Katı, sıvı ve gazların birbirleri içerisinde
HAZIRLAYAN Mutlu ŞAHİN Hacettepe Fen Bilgisi Öğretmenliği DENEY NO: 1 DENEYİN ADI: ÇÖZELTİLER DENEYİN AMACI: FARKLI DERİŞİMLERDE ÇÖZELTİ HAZIRLAYABİLME TEORİK BİLGİ: Katı, sıvı ve gazların birbirleri içerisinde
EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR
 EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR KĐMYA ĐLE ĐLĐŞKĐSĐ ve GÜNLÜK HAYATLA ĐLĐŞKĐSĐ ŞEKERĐN ÇAYDA YA DA BAŞKA BĐR SIVIDA KARIŞTIRILDIĞINDA KAYBOLMASI, KĐMYADA ÇÖZÜNME OLGUSUYLA AÇIKLANABĐLĐR.
EYVAH ŞEKERĐM KAYBOLDU!!!!! 9. SINIF 4. ÜNĐTE KARIŞIMLAR KĐMYA ĐLE ĐLĐŞKĐSĐ ve GÜNLÜK HAYATLA ĐLĐŞKĐSĐ ŞEKERĐN ÇAYDA YA DA BAŞKA BĐR SIVIDA KARIŞTIRILDIĞINDA KAYBOLMASI, KĐMYADA ÇÖZÜNME OLGUSUYLA AÇIKLANABĐLĐR.
Maddelerin Sınıflandırılması. Yrd. Doç. Dr. H. Hasan YOLCU
 Maddelerin Sınıflandırılması Yrd. Doç. Dr. H. Hasan YOLCU Maddelerin Sınıflandırılması Madde Evet Saf Madde Sabit bir bileşimi varmı. Kimyasal formülle belirtilemiliyor mu? Hayır Karışım Element Bileşik
Maddelerin Sınıflandırılması Yrd. Doç. Dr. H. Hasan YOLCU Maddelerin Sınıflandırılması Madde Evet Saf Madde Sabit bir bileşimi varmı. Kimyasal formülle belirtilemiliyor mu? Hayır Karışım Element Bileşik
4. Açısal momentum kuantum sayısı (,) 2 olan bir orbital türü ile ilgili, 5. Orbitaller Maksimum elektron sayısı
 Kuantum Sayıları Ve rbitaller 1. Başkuantum sayısı (n) belirtilen temel enerji düzeylerinden hangisinde bulunabilecek maksimum orbital sayısı yanlış verilmiştir? Başkuantum sayısı (n) Maksimum orbital
Kuantum Sayıları Ve rbitaller 1. Başkuantum sayısı (n) belirtilen temel enerji düzeylerinden hangisinde bulunabilecek maksimum orbital sayısı yanlış verilmiştir? Başkuantum sayısı (n) Maksimum orbital
KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR?
 KARIŞIMLAR KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR? Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Karışımlar görünümlerine
KARIŞIMLAR KARIŞIM NEDİR? YANDAKİ RESİMDE GÖRÜLEN SALATA KARIŞIM MIDIR? Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen maddelere karışım denir. Karışımlar görünümlerine
GIDA İŞLEME VE ANALİZ TEKNİKLERİ I
 GIDA İŞLEME VE ANALİZ TEKNİKLERİ I RAPOR NO: 1 GRUP NO: 3 KONU: Bazı gıdalarda dondurma prosesi ve donma noktası alçalmasının tespiti ÖĞRETMENİN ADI SOYADI: Doç. Dr. Nesimi AKTAŞ ÖĞRENCİNİN ADI SOYADI:
GIDA İŞLEME VE ANALİZ TEKNİKLERİ I RAPOR NO: 1 GRUP NO: 3 KONU: Bazı gıdalarda dondurma prosesi ve donma noktası alçalmasının tespiti ÖĞRETMENİN ADI SOYADI: Doç. Dr. Nesimi AKTAŞ ÖĞRENCİNİN ADI SOYADI:
1- ELEMENTLER: 2. BÖLÜM SAF MADDELER. saf madde denir.
 2. BÖLÜM SAF MADDELER Saf madde: Aynı cins taneciklerden oluşan ( yani aynı cins atomlardan ya da aynı cins moleküllerden oluşan ) maddelere saf madde denir. SAF MADDELER - Elementler - Bileşikler olmak
2. BÖLÜM SAF MADDELER Saf madde: Aynı cins taneciklerden oluşan ( yani aynı cins atomlardan ya da aynı cins moleküllerden oluşan ) maddelere saf madde denir. SAF MADDELER - Elementler - Bileşikler olmak
GIDALARIN BAZI FİZİKSEL NİTELİKLERİ
 GIDALARIN BAZI FİZİKSEL NİTELİKLERİ 1 Gıdaların bazı fiziksel özellikleri: Yoğunluk Özgül ısı Viskozite Gıdaların kimyasal bileşimi ve fiziksel yapılarına bağlı olarak BELLİ SINIRLARDA DEĞİŞİR!!! Kimyasal
GIDALARIN BAZI FİZİKSEL NİTELİKLERİ 1 Gıdaların bazı fiziksel özellikleri: Yoğunluk Özgül ısı Viskozite Gıdaların kimyasal bileşimi ve fiziksel yapılarına bağlı olarak BELLİ SINIRLARDA DEĞİŞİR!!! Kimyasal
ELEMETLER VE BİLEŞİKLER ELEMENTLER VE SEMBOLLERİ
 ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
Maddeyi Oluşturan Tanecikler-Madde Hallerinin Tanecikli Yapısı. Maddeyi Oluşturan Tanecikler- Madde Hallerinin Tanecikli Yapısı
 Maddeyi Oluşturan Tanecikler- Madde Hallerinin Tanecikli Yapısı a) Saf Madde Kendine özgü fiziksel ve kimyasal özellikleri olan, ayırt edici özellikleri bulunan ve bu ayırt edici özellikleri sabit olan
Maddeyi Oluşturan Tanecikler- Madde Hallerinin Tanecikli Yapısı a) Saf Madde Kendine özgü fiziksel ve kimyasal özellikleri olan, ayırt edici özellikleri bulunan ve bu ayırt edici özellikleri sabit olan
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
HEDEF:Çözünürlük konusunun ve çözünürlüğe etki eden faktörlerin anlatılması
 PROJE HEDEF SORUSU:Tentürdiyot nasıl yapılır? HEDEF VE DAVRANIŞLAR: HEDEF:Çözünürlük konusunun ve çözünürlüğe etki eden faktörlerin anlatılması DAVRANIŞLAR: 1)Çözünürlük konusuna giriş yapılır ve günlük
PROJE HEDEF SORUSU:Tentürdiyot nasıl yapılır? HEDEF VE DAVRANIŞLAR: HEDEF:Çözünürlük konusunun ve çözünürlüğe etki eden faktörlerin anlatılması DAVRANIŞLAR: 1)Çözünürlük konusuna giriş yapılır ve günlük
GAZLAR GAZ KARIŞIMLARI
 DALTON KISMİ BASINÇLAR YASASI Aynı Kaplarda Gazların Karıştırılması Birbiri ile tepkimeye girmeyen gaz karışımlarının davranışı genellikle ilgi çekicidir. Böyle bir karışımdaki bir bileşenin basıncı, aynı
DALTON KISMİ BASINÇLAR YASASI Aynı Kaplarda Gazların Karıştırılması Birbiri ile tepkimeye girmeyen gaz karışımlarının davranışı genellikle ilgi çekicidir. Böyle bir karışımdaki bir bileşenin basıncı, aynı
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA
 İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR
 KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI 3.1. Çözeltiler için kullanılan temel kavramlar
 1.10.2015. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI.1. Çözeltiler için kullanılan temel kavramlar Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından
1.10.2015. ÇÖZELTİLER VE ÇÖZELTİ KONSANTRASYONLARI.1. Çözeltiler için kullanılan temel kavramlar Homojen karışımlardır. Çözelti iki veya daha fazla maddenin birbiri içerisinde homojen olarak dağılmasından
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ HAZIRLAYAN FEHMİ GÜR
 ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ HAZIRLAYAN FEHMİ GÜR KOLİGATİF ÖZELLİKLER Uçucu olmayan maddelerin çözeltilerinin bazı fiziksel özellikleri; saf çözücününkinden farklıdır. Bu çözeltiler hazırlanırken,
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ HAZIRLAYAN FEHMİ GÜR KOLİGATİF ÖZELLİKLER Uçucu olmayan maddelerin çözeltilerinin bazı fiziksel özellikleri; saf çözücününkinden farklıdır. Bu çözeltiler hazırlanırken,
Dispers Sistemlerin Sınıflandırılması
 DİSPERS SİSTEMLER Dispers Sistemlerin Sınıflandırılması 1-Dispers sistemde bulunan iki fazın gaz, sıvı veya katı oluşuna göre sınıflandırılabilirler. 2-Dispers sistemde dispers fazın partikül büyüklüğüne
DİSPERS SİSTEMLER Dispers Sistemlerin Sınıflandırılması 1-Dispers sistemde bulunan iki fazın gaz, sıvı veya katı oluşuna göre sınıflandırılabilirler. 2-Dispers sistemde dispers fazın partikül büyüklüğüne
MADDENİN HALLERİ VE TANECİKLİ YAPI
 MADDENİN HALLERİ VE TANECİKLİ YAPI MADDE BİLGİSİ Kütlesi hacmi ve eylemsizliği olan her şeye madde denir. Maddenin şekil almış haline cisim denir. Cam bir madde iken cam bardak bir cisimdir. Maddeler doğada
MADDENİN HALLERİ VE TANECİKLİ YAPI MADDE BİLGİSİ Kütlesi hacmi ve eylemsizliği olan her şeye madde denir. Maddenin şekil almış haline cisim denir. Cam bir madde iken cam bardak bir cisimdir. Maddeler doğada
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER»
 FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
YouTube:Kimyafull Gülçin Hoca Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ
 Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ ppm Toplam madde miktarının milyonda 1 birimlik maddesine denir. NOT: 1 kg su = 1 Litre ppm =. 10 6 1 kg çözeltide çözünen maddenin mg olarak kütlesine
Serüveni DERİŞİM BİRİMLERİ Ppm-ppb SORU ÇÖZÜMLERİ ppm Toplam madde miktarının milyonda 1 birimlik maddesine denir. NOT: 1 kg su = 1 Litre ppm =. 10 6 1 kg çözeltide çözünen maddenin mg olarak kütlesine
TURUNCU RENGĐN DANSI NASIL OLUR?
 KĐMYA EĞĐE ĞĐTĐM M SEMĐNER NERĐ PROF. DR. ĐNCĐ MORGĐL TURUNCU RENGĐN DANSI NASIL OLUR? HAZIRLAYAN: GÜLÇĐN YALLI KONU: ÇÖZELTĐLER KONU BAŞLIĞI: TURUNCU RENGĐN DANSI NASIL OLUR? ÇÖZELTĐLER Fiziksel özellikleri
KĐMYA EĞĐE ĞĐTĐM M SEMĐNER NERĐ PROF. DR. ĐNCĐ MORGĐL TURUNCU RENGĐN DANSI NASIL OLUR? HAZIRLAYAN: GÜLÇĐN YALLI KONU: ÇÖZELTĐLER KONU BAŞLIĞI: TURUNCU RENGĐN DANSI NASIL OLUR? ÇÖZELTĐLER Fiziksel özellikleri
Erciyes Üniversitesi Gıda Mühendisliği Bölümü Gıda Analizleri ve Teknolojisi Laboratuvar Föyü Sayfa 1
 LABORATUVAR KURALLARI VE ÇÖZELTİ HAZIRLAMA LABORATUVAR KURALLARI 1. Laboratuvar çalışmaları sırasında elbiselerin özellikle yakıcı ve tehlikeli maddelerden korunması için laboratuara önlükle gelinmelidir.
LABORATUVAR KURALLARI VE ÇÖZELTİ HAZIRLAMA LABORATUVAR KURALLARI 1. Laboratuvar çalışmaları sırasında elbiselerin özellikle yakıcı ve tehlikeli maddelerden korunması için laboratuara önlükle gelinmelidir.
1 mol = 6, tane tanecik. Maddelerde tanecik olarak atom, molekül ve iyonlar olduğunda dolayı mol ü aşağıdaki şekillerde tanımlamak mümkündür.
 1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
KONU-II KARIŞIMLARI AYIRMA YÖNTEMLERİ. Yoğunluk farkından yararlanarak yapılan ayırma işlemleri.
 KONU-II KARIŞIMLARI AYIRMA YÖNTEMLERİ I. Tanecik Büyüklüğünden Yararlanarak Yapılan Ayırma İşlemler: Büyüklükleri farklı maddelerin ayrılmasında kullanılan basit yöntemlerdir. 1. AYIKLAMA: Fındık patozdan
KONU-II KARIŞIMLARI AYIRMA YÖNTEMLERİ I. Tanecik Büyüklüğünden Yararlanarak Yapılan Ayırma İşlemler: Büyüklükleri farklı maddelerin ayrılmasında kullanılan basit yöntemlerdir. 1. AYIKLAMA: Fındık patozdan
Elektronların Dizilimi ve Kimyasal Bağlar
 Elektronların Dizilimi ve Kimyasal Bağlar Elektronların Dizilimi Elektronlar çekirdek çevresindeki yörüngelerde dönerek hareket ederler. Çekirdeğe en yakın yörünge 1 olmak üzere dışa doğru 2, 3,4... olarak
Elektronların Dizilimi ve Kimyasal Bağlar Elektronların Dizilimi Elektronlar çekirdek çevresindeki yörüngelerde dönerek hareket ederler. Çekirdeğe en yakın yörünge 1 olmak üzere dışa doğru 2, 3,4... olarak
Genel Kimya. Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK. Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü
 Genel Kimya Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü ÇÖZELTİ VE TÜRLERİ Eğer bir madde diğer bir madde içinde molekül, atom veya iyonları
Genel Kimya Bölüm 7: ÇÖZELTİLER VE ÇÖZÜNÜRLÜK Yrd. Doç. Dr. Mustafa SERTÇELİK Kafkas Üniversitesi Kimya Mühendisliği Bölümü ÇÖZELTİ VE TÜRLERİ Eğer bir madde diğer bir madde içinde molekül, atom veya iyonları
TEKSTİL ENDÜSTRİSİNDE YÜZEY AKTİF MADDELERİN KULLANIMI
 TEKSTİL ENDÜSTRİSİNDE YÜZEY AKTİF MADDELERİN KULLANIMI M. Fikri ÇİFTÇİ Aralık 2015, İzmir [0] TMMOB Kimya Mühendisleri Odası TEKSTİL ENDÜSTRİSİNDE YÜZEY AKTİF MADDELERİN KULLANIMI 1 M. Fikri ÇİFTÇİ Kimya
TEKSTİL ENDÜSTRİSİNDE YÜZEY AKTİF MADDELERİN KULLANIMI M. Fikri ÇİFTÇİ Aralık 2015, İzmir [0] TMMOB Kimya Mühendisleri Odası TEKSTİL ENDÜSTRİSİNDE YÜZEY AKTİF MADDELERİN KULLANIMI 1 M. Fikri ÇİFTÇİ Kimya
SU Dr. Fatih Büyükserin
 SU Dr. Fatih Büyükserin SU Organizma ağırlığının yüzde % 70 ini oluşturur Su molekülleri arasındaki çekim kuvvetleri ve suyun az da olsa iyonlaşma eğilimi Biyomoleküllerin yapı ve görevlerinin oluşmasında
SU Dr. Fatih Büyükserin SU Organizma ağırlığının yüzde % 70 ini oluşturur Su molekülleri arasındaki çekim kuvvetleri ve suyun az da olsa iyonlaşma eğilimi Biyomoleküllerin yapı ve görevlerinin oluşmasında
A- LABORATUAR MALZEMELERİ
 1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
KARIŞIMLAR. Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir.
 KARIŞIMLAR Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir. 1-HETEROJEN KARIŞIMLAR (ADİ KARIŞIMLAR) Karışımı oluşturan maddeler karışımın her
KARIŞIMLAR Birden çok maddenin kimyasal bağ oluşturmadan bir arada bulunmasıyla meydana gelen mad-delere karışım denir. 1-HETEROJEN KARIŞIMLAR (ADİ KARIŞIMLAR) Karışımı oluşturan maddeler karışımın her
TABANLI DENEY UYGULAMASI
 KĐMYA EĞĐE ĞĐTĐMĐNDE PROJE TABANLI DENEY UYGULAMASI DERS SORUMLUSU: PROF.DR. ĐNCĐ MORGĐL HAZIRLAYAN ORAY COSKUN PROJE HEDEF SORUSU SOLUDUĞUMUZ HAVADAKĐ SO2 VARLIĞININ TESBĐTĐ VE SO2 NĐN KÜRESEL ISINMAYA
KĐMYA EĞĐE ĞĐTĐMĐNDE PROJE TABANLI DENEY UYGULAMASI DERS SORUMLUSU: PROF.DR. ĐNCĐ MORGĐL HAZIRLAYAN ORAY COSKUN PROJE HEDEF SORUSU SOLUDUĞUMUZ HAVADAKĐ SO2 VARLIĞININ TESBĐTĐ VE SO2 NĐN KÜRESEL ISINMAYA
T.C TRAKYA ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ GLOBULAR PROTEİN ÇÖZELTİLERİNDE ETKİN ETKİLEŞME POTANSİYELLERİ. Yıldız GİRGİN YÜKSEK LİSANS TEZİ
 T.C TRAKYA ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ GLOBULAR PROTEİN ÇÖZELTİLERİNDE ETKİN ETKİLEŞME POTANSİYELLERİ Yıldız GİRGİN YÜKSEK LİSANS TEZİ FİZİK ANABİLİM DALI Danışman:Prof. Dr. Serap DALGIÇ 2010
T.C TRAKYA ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ GLOBULAR PROTEİN ÇÖZELTİLERİNDE ETKİN ETKİLEŞME POTANSİYELLERİ Yıldız GİRGİN YÜKSEK LİSANS TEZİ FİZİK ANABİLİM DALI Danışman:Prof. Dr. Serap DALGIÇ 2010
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME
 ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME KONU: MADDE VE ÖZELLĐKLERĐ (Konu Anlatımı) Hazırlayan: Pınar ÖZCAN Ders Sorumlusu: Prof. Dr. Đnci MORGĐL ANKARA,2008 MADDE VE ÖZELLĐKLERĐ MADDE Kütlesi, hacmi
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME KONU: MADDE VE ÖZELLĐKLERĐ (Konu Anlatımı) Hazırlayan: Pınar ÖZCAN Ders Sorumlusu: Prof. Dr. Đnci MORGĐL ANKARA,2008 MADDE VE ÖZELLĐKLERĐ MADDE Kütlesi, hacmi
Karbonhidrat Nedir? Bitkiler klorofil, güneş enerjisi, su ve karbondioksiti kullanarak karbonhidratları sentezlerler.
 Karbonhidratlar Karbonhidrat Nedir? Karbonhidratlar vücudumuza enerji sağlayan besin maddelerinde en fazla bulunan besin öğesidir. Daha çok bitkisel kaynaklı besin maddelerinde yaygın olarak bulunur. Bitkiler
Karbonhidratlar Karbonhidrat Nedir? Karbonhidratlar vücudumuza enerji sağlayan besin maddelerinde en fazla bulunan besin öğesidir. Daha çok bitkisel kaynaklı besin maddelerinde yaygın olarak bulunur. Bitkiler
6. Aşağıdaki tablodan yararlanarak X maddesinin ne olduğunu (A, B,C? ) ön görünüz.
 1. Lavosier yasası nedir, açıklayınız. 2. C 2 H 4 + 3O 2 2CO 2 + 2 H 2 O tepkimesine göre 2,0 g etilenin yeterli miktarda oksijenle yanması sonucu oluşan ürünlerin toplam kütlesi nedir, hesaplayınız. 3.
1. Lavosier yasası nedir, açıklayınız. 2. C 2 H 4 + 3O 2 2CO 2 + 2 H 2 O tepkimesine göre 2,0 g etilenin yeterli miktarda oksijenle yanması sonucu oluşan ürünlerin toplam kütlesi nedir, hesaplayınız. 3.
KARIŞIMLARIN SINIFLANDIRILMASI
 IN SINIFLANDIRILMASI Doğadaki maddelerin çoğu saf halde bulunmaz. Çevremizde gördüğümüz maddeler genellikle karışım halindedir. Soluduğumuz hava, yediğimiz çikolata, kek, içtiğimiz meyve suyu, süt hatta
IN SINIFLANDIRILMASI Doğadaki maddelerin çoğu saf halde bulunmaz. Çevremizde gördüğümüz maddeler genellikle karışım halindedir. Soluduğumuz hava, yediğimiz çikolata, kek, içtiğimiz meyve suyu, süt hatta
MALZEME BİLGİSİ. Atomlar Arası Bağlar
 MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Atomlar Arası Bağlar 1 Giriş Atomları bir arada tutarak iç yapıyı oluştururlar Malzemelerin mukavemeti, elektriksel ve ısıl özellikleri büyük ölçüde iç yapıya
MALZEME BİLGİSİ Dr.- Ing. Rahmi ÜNAL Konu: Atomlar Arası Bağlar 1 Giriş Atomları bir arada tutarak iç yapıyı oluştururlar Malzemelerin mukavemeti, elektriksel ve ısıl özellikleri büyük ölçüde iç yapıya
ÖĞRETİM TEKNOLOJİLERİ VE MATERYAL GELİŞTİRME DERSİ
 ÖĞRETİM TEKNOLOJİLERİ VE MATERYAL GELİŞTİRME DERSİ FEN VE TEKNOLOJİ DERSİ 7.SINIF MADDENİN TANECİKLİ YAPISI ÜNİTESİ KARIŞIMLAR KONUSU İLE İLGİLİ ÇALIŞMA YAPRAĞI DERS SORUMLUSU: PROF. DR.İNCİ MORGİL HAZIRLAYAN:
ÖĞRETİM TEKNOLOJİLERİ VE MATERYAL GELİŞTİRME DERSİ FEN VE TEKNOLOJİ DERSİ 7.SINIF MADDENİN TANECİKLİ YAPISI ÜNİTESİ KARIŞIMLAR KONUSU İLE İLGİLİ ÇALIŞMA YAPRAĞI DERS SORUMLUSU: PROF. DR.İNCİ MORGİL HAZIRLAYAN:
Serüveni. 1.ÜNİTE: KİMYA BİLİMİ Kimyanın Sembolik Dili #3
 Serüveni 1.ÜNİTE: KİMYA BİLİMİ Kimyanın Sembolik Dili #3 MADDE SAF MADDE SAF OLMAYAN MADDE(KARIŞIM) ELEMENT BİLEŞİK HOMOJEN KARIŞIM HETEROJEN KARIŞIM METAL İYONİK BİLEŞİKLER SÜSPANSİYON AMETAL KOVALENT
Serüveni 1.ÜNİTE: KİMYA BİLİMİ Kimyanın Sembolik Dili #3 MADDE SAF MADDE SAF OLMAYAN MADDE(KARIŞIM) ELEMENT BİLEŞİK HOMOJEN KARIŞIM HETEROJEN KARIŞIM METAL İYONİK BİLEŞİKLER SÜSPANSİYON AMETAL KOVALENT
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar
 10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
7. Sınıf Fen ve Teknoloji
 KONU: Karışımlar Birden fazla maddenin özelliklerini kaybetmeden oluşturdukları topluluğa karışım denir. İçme suyu, gazoz, limonata, meyve suyu, yemekler, salata, süt, ayran, hava, sis, çamur vb. birer
KONU: Karışımlar Birden fazla maddenin özelliklerini kaybetmeden oluşturdukları topluluğa karışım denir. İçme suyu, gazoz, limonata, meyve suyu, yemekler, salata, süt, ayran, hava, sis, çamur vb. birer
GENEL ÖZELLİKLERİ: Tüm canlılarda sudan sonra en fazla bulunan moleküllerdir. Canlının kuru ağırlığının %50 si proteindir. Oldukça büyük ve kompleks
 PROTEİNLER GENEL ÖZELLİKLERİ: Tüm canlılarda sudan sonra en fazla bulunan moleküllerdir. Canlının kuru ağırlığının %50 si proteindir. Oldukça büyük ve kompleks maddelerdir. Hücrede ribozom organelinde
PROTEİNLER GENEL ÖZELLİKLERİ: Tüm canlılarda sudan sonra en fazla bulunan moleküllerdir. Canlının kuru ağırlığının %50 si proteindir. Oldukça büyük ve kompleks maddelerdir. Hücrede ribozom organelinde
ALKiNLER; ÇALIŞMA SORULARI
 ALKiNLER; ÇALIŞMA SORULARI SORU 1.) Aşağıda formülü verilen bileşiklerin sistematik adını, sistematik adı verilen bileşiklerin ise formülünü yazınız. SORU 2.) 3, 4 gram alkinin tam olarak yanabilmesi için
ALKiNLER; ÇALIŞMA SORULARI SORU 1.) Aşağıda formülü verilen bileşiklerin sistematik adını, sistematik adı verilen bileşiklerin ise formülünü yazınız. SORU 2.) 3, 4 gram alkinin tam olarak yanabilmesi için
... ... ... ... 2... ... ... 13... ... ... Ders: Konu: TEOG. Yaprak No: Copyright: MİKRO ANLATIM. Kazanım: Üslü sayılar ile ilgili kuralları hatırlar.
 Ders: Konu: TEOG Yaprak No: Copyright: MİKRO ANLATIM Matematik Üslü Sayılar- ÇALIŞMA DEFTERİ Bilal KICIROĞLU Kazanım: Üslü sayılar ile ilgili kuralları hatırlar. ÜSLÜ SAYILAR- Bu içerikte öncelikle üslü
Ders: Konu: TEOG Yaprak No: Copyright: MİKRO ANLATIM Matematik Üslü Sayılar- ÇALIŞMA DEFTERİ Bilal KICIROĞLU Kazanım: Üslü sayılar ile ilgili kuralları hatırlar. ÜSLÜ SAYILAR- Bu içerikte öncelikle üslü
SIVILAR VE ÖZELLİKLERİ
 SIVILAR VE ÖZELLİKLERİ Sıcaklık düşürüldükçe kinetik enerjileri azalan gaz molekülleri sıvı hale geçer. Sıvı haldeki tanecikler birbirine temas edecek kadar yakın olduğundan aralarındaki çekim kuvvetleri
SIVILAR VE ÖZELLİKLERİ Sıcaklık düşürüldükçe kinetik enerjileri azalan gaz molekülleri sıvı hale geçer. Sıvı haldeki tanecikler birbirine temas edecek kadar yakın olduğundan aralarındaki çekim kuvvetleri
KİMYA ÖĞRETMENLİK ALAN BİLGİSİ - DENEME SINAVI DENEME. Diğer sayfaya geçiniz. 4. ph ı 13 olan 25 ml NaOH çözeltisine ph ı 2 olan H 2
 KİMYA 1. DENEME ÖĞRETMENLİK ALAN BİLGİSİ - DENEME SINAVI 1. Gerçekte kütlesi 8,23 gram olan bir kimyasal madde bir öğrenci tarafından üç kez tartılıyor. Tartım sonuçlarını 8,41g; 8,42g; 8,41g olarak buluyor.
KİMYA 1. DENEME ÖĞRETMENLİK ALAN BİLGİSİ - DENEME SINAVI 1. Gerçekte kütlesi 8,23 gram olan bir kimyasal madde bir öğrenci tarafından üç kez tartılıyor. Tartım sonuçlarını 8,41g; 8,42g; 8,41g olarak buluyor.
KARIŞIMLAR. Karışımların Ayrılması
 KARIŞIMLAR Karışımların Ayrılması Günlük yaşamda kullandığımız eşyaların, giydiğimiz kıyafetlerin, yediğimiz yiyeceklerin, içtiğimiz suyun hepsi birer karışımdır. Nehir, göl, baraj sularını doğal haliyle
KARIŞIMLAR Karışımların Ayrılması Günlük yaşamda kullandığımız eşyaların, giydiğimiz kıyafetlerin, yediğimiz yiyeceklerin, içtiğimiz suyun hepsi birer karışımdır. Nehir, göl, baraj sularını doğal haliyle
KİMYA. davranış. umunu, reaksiyonlar sırass. imleri (enerji. vs..) gözlem ve deneylerle inceleyen, açıklayan a
 KİMYA Maddenin yapısını, özelliklerini, farklı koşullardaki davranış ışlarını,, bir maddeden diğer bir madde oluşumunu, umunu, reaksiyonlar sırass rasındaki değişimleri imleri (enerji vs..) gözlem ve deneylerle
KİMYA Maddenin yapısını, özelliklerini, farklı koşullardaki davranış ışlarını,, bir maddeden diğer bir madde oluşumunu, umunu, reaksiyonlar sırass rasındaki değişimleri imleri (enerji vs..) gözlem ve deneylerle
Kütlesi,hacmi,eylemsizliği olan,tanecikli yapıdaki her şeye madde denir. Yer yüzünde gözümüzle görebildiğimiz her şey maddedir.
 Madde Tanımı Kütlesi,hacmi,eylemsizliği olan,tanecikli yapıdaki her şeye madde denir. Yer yüzünde gözümüzle görebildiğimiz her şey maddedir. MADDENİN MADDENİN HALLERİ HALLERİ maddenin haller i MADDENİN
Madde Tanımı Kütlesi,hacmi,eylemsizliği olan,tanecikli yapıdaki her şeye madde denir. Yer yüzünde gözümüzle görebildiğimiz her şey maddedir. MADDENİN MADDENİN HALLERİ HALLERİ maddenin haller i MADDENİN
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER
 ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER Ders Sorumlusu: Prof. Dr. Đnci MORGĐL HAZIRLAYAN: NAZLI KIRCI ANKARA,2008 KONU ANLATIMI ÇÖZELTĐLER Đki ya da daha fazla kimyasal maddenin herhangi
ÖĞRETĐM TEKNOLOJĐSĐ VE MATERYAL GELĐŞTĐRME ÇÖZELTĐLER Ders Sorumlusu: Prof. Dr. Đnci MORGĐL HAZIRLAYAN: NAZLI KIRCI ANKARA,2008 KONU ANLATIMI ÇÖZELTĐLER Đki ya da daha fazla kimyasal maddenin herhangi
STOKİYOMETRİ. Kimyasal Tepkimelerde Kütle İlişkisi
 STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
Maddeyi Oluşturan Tanecikler
 Maddeyi Oluşturan Tanecikler a) Saf Madde : Kendine özgü fiziksel ve kimyasal özellikleri olan, ayırt edici özellikleri bulunan ve bu ayırt edici özellikleri sabit olan maddelere saf madde denir. Elementler
Maddeyi Oluşturan Tanecikler a) Saf Madde : Kendine özgü fiziksel ve kimyasal özellikleri olan, ayırt edici özellikleri bulunan ve bu ayırt edici özellikleri sabit olan maddelere saf madde denir. Elementler
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı
 Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Sıvılardan ekstraksiyon:
 Sıvılardan ekstraksiyon: Sıvı haldeki bir karışımdan bir maddenin, bu maddenin içinde bulunduğu çözücü ile karışmayan ve bu maddeyi çözen bir başka çözücü ile çalkalanarak ilgili maddenin ikinci çözücüye
Sıvılardan ekstraksiyon: Sıvı haldeki bir karışımdan bir maddenin, bu maddenin içinde bulunduğu çözücü ile karışmayan ve bu maddeyi çözen bir başka çözücü ile çalkalanarak ilgili maddenin ikinci çözücüye
İDEAL GAZ KARIŞIMLARI
 İdeal Gaz Karışımları İdeal gaz karışımları saf ideal gazlar gibi davranırlar. Saf gazlardan n 1, n 2,, n i, mol alınarak hazırlanan bir karışımın toplam basıncı p, toplam hacmi v ve sıcaklığı T olsun.
İdeal Gaz Karışımları İdeal gaz karışımları saf ideal gazlar gibi davranırlar. Saf gazlardan n 1, n 2,, n i, mol alınarak hazırlanan bir karışımın toplam basıncı p, toplam hacmi v ve sıcaklığı T olsun.
Soru3) 2KMnO 4 5H 2 C 2 O 4 3H 2 SO 4 K 2 SO 4 2MnSO 4 10CO 2 8H 2 O
 Soru 1) Mn(OH) 2 (k) H 3 AsO 4 (suda) Mn 3 (AsO 4 ) 2 (k) H 2 O(s) Yukarıdaki kimyasal tepkime en küçük tamsayılarla denkleştirilirse su molekülünün katsayısı kaç olur? a) 6 b) 2 c)12 c) 3 < Soru3) 2KMnO
Soru 1) Mn(OH) 2 (k) H 3 AsO 4 (suda) Mn 3 (AsO 4 ) 2 (k) H 2 O(s) Yukarıdaki kimyasal tepkime en küçük tamsayılarla denkleştirilirse su molekülünün katsayısı kaç olur? a) 6 b) 2 c)12 c) 3 < Soru3) 2KMnO
KİMYASAL BİLEŞİKLER İÇERİK
 KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
ÇÖZELTİLERDE YÜZDELİK İFADELER. Ağırlıkça yüzde (% w/w)
 ÇÖZELTİ HAZIRLAMA İki veya daha çok maddenin çıplak gözle veya optik araçlarla yan yana fark edilememesi ve mekanik yollarla ayrılamaması sonucu oluşturdukları karışıma çözelti adı verilir. Anorganik kimyada,
ÇÖZELTİ HAZIRLAMA İki veya daha çok maddenin çıplak gözle veya optik araçlarla yan yana fark edilememesi ve mekanik yollarla ayrılamaması sonucu oluşturdukları karışıma çözelti adı verilir. Anorganik kimyada,
KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ
 KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ KOLLİGATİF ÖZELLİKLER Çözeltinin derişimine bağlı özelliklerine KOLİGATİF ÖZELLİK denir. Kaynama noktası Buhar basıncı Donma noktası Osmotik Basınç Çözünen Madde çözündüğünde:
KOLLİGATİF ÖZELLİKLER SORU ÇÖZÜMÜ KOLLİGATİF ÖZELLİKLER Çözeltinin derişimine bağlı özelliklerine KOLİGATİF ÖZELLİK denir. Kaynama noktası Buhar basıncı Donma noktası Osmotik Basınç Çözünen Madde çözündüğünde:
Kimyasal Bağ. Atomları birarada tutan kuvvetlere kimyasal bağ denir
 Kimyasal Bağlar Kimyasal Bağ Atomları birarada tutan kuvvetlere kimyasal bağ denir İyonik bağ Kovalent bağ Polar Kovalent bağ Apolar Kovalent bağ Metalik bağ Lewis bağ teorisi Kimyasal bağlanma için atomun
Kimyasal Bağlar Kimyasal Bağ Atomları birarada tutan kuvvetlere kimyasal bağ denir İyonik bağ Kovalent bağ Polar Kovalent bağ Apolar Kovalent bağ Metalik bağ Lewis bağ teorisi Kimyasal bağlanma için atomun
