Besinler (karbonhidrat, yağ, protein), Su, Canlılığın devamı için organizmanın gereksinim duyduğu vazgeçilmez faktörlerdir.
|
|
|
- Tunç Hikmet
- 8 yıl önce
- İzleme sayısı:
Transkript
1 Basınç Isı, Oksijen, Besinler (karbonhidrat, yağ, protein), Su, Canlılığın devamı için organizmanın gereksinim duyduğu vazgeçilmez faktörlerdir. 1 2 Su, yaşayan sistemlerde büyük ölçüde bulunan bir bileşiktir. Bir çok organizmanın %70 den fazlası sudan oluşur. Şüphesiz, ilk canlı organizmalar sıvı ortamlardan çıkmıştır ve evrimsel süreç yaşamın başladığı sıvı medyum ile şekillenmiştir. Su yaşam için gereklidir. Bütün hücreleri dolduran su, besin maddelerinin taşındığı, metabolizmanın enzimatik tepkimelerinin ve kimyasal enerjinin gerçekleştiği ortamı oluşturur. Su molekülü ile suyun iyonizasyon ürünleri olan H ve OH iyonları, enzimler ve diğer proteinler, nukleik asitler ve lipidler gibi hücrelerin tüm bileşenlerinin yapılarını, birbiriyle ilişkilerini ve çeşitli özelliklerini etkilemektedir. Vücut neredeyse tüm yağ dokusunu ve proteinlerinin yarıdan fazlasını bile kaybetse yaşamaya devam eder %10-15 oranında su kaybı ölümle sonuçlanır 3 4 SUYUN GÖREVĐ besin maddelerinin taşınması enzimatik tepkimelerinin gerçekleşmesi kimyasal enerjinin oluşumu Bir çok biyolojik molekül için çözgen Metabolik ısıyı absorblar Vücut ısısının düzenlenmesinde yardımcı Suyun özellikleri: Yüksek yüzey gerilimi: Yüksek kaynama noktası: Moleküler ağırlığına göre kaynama noktası en yüksek sıvı sudur. Örneğin, amonyak molekül ağırlığı yaklaşık 17 olmasına karşın -30 C de kaynarken suyun molekül ağırlığı 18 dir ve 100 C de kaynar. Yoğunluk sıcaklığa bağlıdır: Katı su (buz) sıvı sudan daha az yoğundur. Bu özellik göllerin üstten itibaren donmasına neden olur, böylece balıkların yaşamasına olanak sağlar
2 Buz su üzerinde bir örtü oluşturarak sucul yaşamın devamlılığını sağlar 7 8 SUYUN YÜKSEK YÜZEY GERĐLĐMĐ Su, bir dipoldür. Oksijenin 6 dış elektronundan ikisi hidrojen ile kovalent bağ oluşturur. Diğer dört elektron bağ oluşturmaz ve iki çift oluşturur. Bu çiftler kısmi negatif yükün bir odağıdırlar ve hidrojen atomları kısmen pozitif yüklü hale gelir. Pozitif ve negatif yükler birbiriyle bağlanır ve hidrojen ve oksijen atomları arasında hidrojen bağları oluşur. Yapısındaki H bağları ile : (a) Yüzey gerilimi örümcek ağlarında suyu damla haline getirir (b) Bazı böcekler su üzerinde yürüyebilir 9 10 BĐR SU MOLEKÜLÜNÜN OLUŞUMU SUYUN VE HĐDROJEN BAĞININ ÖZELLĐKLERĐ Oluşan küme, suya yapışkansızlık özelliğini verir. Bu sıvı fazda moleküllerin yerleşimi düzensiz H-bağları nedeniyle düzensizdir. Su donduğunda H-bağları kafes şeklinde su molekülleri oluşturur
3 Su molekülleri arasında oluşan hidrojen bağları, oda sıcaklığında suyun sıvı halde bulunmasını ve kristal su (buz) için karakteristik olan aşırı düzenli moleküllerin oluşmasını sağlar. Buz içinde her bir su molekülü maksimum 4 hidrojen bağı oluşturur. Böylece düzenli bir kristal kafes şekli oluşur. Oysa oda sıcaklığı ya da atmosferik basınç altındaki sıvı fazda her bir su molekülü ortalama 3,4 H bağı oluşturur. Buzdaki kristal kafes yapısı, sıvı sudaki aynı sayıda su moleküllerinden daha fazla yer kapladığı için buz, sıvı haldeki 17 sudan daha az yoğundur ve bu 18 nedenle suyun üzerinde kalmaktadır 3
4 Sıvıların çoğu donduklarında, yapılarında bulunan moleküller birbirine daha çok yakınlaşır. Su donduğunda ise moleküller birbirinden uzaklaşır ve sıvı haldekine göre daha fazla yer kaplar. Bu nedenle buzun yoğunluğu, yani ağırlığı sıvı haldeki suya göre azalır ve buz suda yüzer. Katı su (buz) Sıvı su Gaz su Buzda su molekülleri hidrojen bağları aracılığı ile rijit durumdadır Su molekülleri hareket ederken hidrojen bağları sürekli olarak yıkılır Gaz durumunda su hidrojen bağı oluşturmaz SIVI SĐSTEMLERDEKĐ ZAYIF ETKĐLEŞĐMLER Polar biyomoleküller suda kolaylıkla çözülür, çünkü bu moleküller su-su etkileşimlerini su-solut etkileşimleri haline getirir. Non-polar biyomoleküller su-su etkileşimlerine engel olurlar, ancak su-solut etkileşimi oluşturamazlar. Bunun sonucu olarak da nonpolar moleküller suda çözülmezler. Sıvı solüsyonlarda nonpolar moleküller birlikte kümeler oluştururlar. 23 Suda kolaylıkla çözülen bileşenlere hidrofilik denir. Bunun tersine, kloroform ve benzen gibi nonpolar çözücülerde çözülen bileşenlere hidrofobik adı verilir. Amfipatik bileşenler polar (ya da yüklü) ve nonpolar bölgeler içerirler. Amfipatik bileşenler su ile karıştırıldığında iki zıt durumla karşılaşır: polar ya da yüklü hidrofilik bölge solventle etkileşir ve çözülmeye gider, ancak nonpolar hidrofobik bölge tam tersi bir davranışla su ile etkileşmekten Doç.Dr.Erdal kaçınır. BALCAN 24 4
5 Su, solusyonları oluşturur Solvent Bir solüsyon iki ya da daha fazla bileşenin homojen olarak karışımından meydana gelir. Çözücü ajan (çözgen) Su Solvent + Solute Solusyon Metan Şekerli su, tuzlu su, Pepsi Solüt Çözülen bileşen Hydrofilik Moleküller (su-seven) Tuzlu sudaki tuz Şekerli sudaki şeker Suda çözülen bileşenler tuz, şeker Hidrofobik Moleküller (sudan korkan) Suda çözünmezler yağlar, mumlar SUYUN ĐYONĐZASYONU, ZAYIF ASĐTLER ve ZAYIF BAZLAR Su moleküllerinde çok küçük oranlarda hidrojen (H+) ya da hidroksil (OH-) iyonlarına ayrışma olmaktadır. Çözeltilerine H iyonu verebilen maddeler asit Çözeltilerinden H iyonu alabilen maddeler baz
6 ASĐT-BAZ ve TAMPON SĐSTEM KAVRAMI Vücutta asit-baz dengesinin düzenlenmesi aslında hidrojen iyon konsantrasyonunun düzenlenmesi anlamına gelir. H iyon konsantrasyonundaki çok küçük sapmalar bile hücrelerdeki kimyasal reaksiyonlarda belirgin değişimler yaratarak bazı tepkimeleri baskılar bazılarını da hızlandırır. Bu nedenle H iyon konsantrasyonunun düzenlenmesi homeostasis için büyük önem taşır. Kimyada Tampon çözeltiler Organizmalarda Tampon sistemler 31 ASĐT-BAZ ve TAMPON SĐSTEM KAVRAMI Asit: proton verici molekül ya da iyonlar. H + düzeyini arttırarak ph yı düşürürler. Baz: proton alıcısı molekül ya da iyonlar. H + düzeyini düşürerek ph yı arttırırlar 32 Tampon çözelti: bir asit ya da baz ilavesiyle ph ı önemli ölçüde değiştirmeden H + iyonu ekleyen ya da çıkartan çözeltilerdir. Bir zayıf asit ile onun konjuge bazından ya da zayıf bir baz ile onun kojuge asidinden oluşur. Yani tampon madde bir eriyiğe kuvvetli bir asit ya da baz eklendiğinde olabilecek değişikliği en aza indirir. Konjuge asit-baz çiftinin bulunduğu ve ph değişimlerine karşı direnç gösteren çözeltilerdir. 33 Asit HA B - + H + HCO 3 + H H + + Baz H + + A - (A; HA nın konjuge bazıdır, HA; A nın konjuge asididir) (A ve HA asit-baz çiftidir) BH (B; BH nin konjuge bazıdır, BH; B nin konjuge asididir) (B ve BH asit-baz çiftidir) H 2 CO 3 (karbonik asit-bikarbonat T.S.) Vücutta asit-baz dengesinin düzenlenmesi aslında hidrojen iyon konsantrasyonunun düzenlenmesi anlamına gelir. H iyon konsantrasyonundaki çok küçük sapmalar bile hücrelerdeki kimyasal reaksiyonlarda belirgin değişimler yaratarak bazı tepkimeleri baskılar bazılarını da hızlandırır. Bu nedenle H iyon konsantrasyonunun 34 düzenlenmesi homeostasis için büyük önem taşır. ph [H + ] Alkalemi Asidemi 36 6
7 37 38 VÜCUT SUYU Bir insanın ortalama %60-80 i sudan oluşur. VÜCUT SIVISININ KAYNAĞI VÜCUT SIVISINI ETKĐLEYEN FAKTÖRLER 1. Besinler, içkiler 1. Genotip 2. Metabolik olaylar 2. Yaş 3. Ortam sıcaklığı 4. Beslenme kalitesi 5. Fizyolojik koşullar VÜCUT SIVISININ KAYBI 1.Đdrar 2. Feçes 3. Ter 4. Fizyolojik (laktasyon, gebelik)
8 ĐNTRASELLÜLER SIVI (ISS) Toplam vücut sıvısının 2/3 sini oluşturur. Major katyonu K + dur. TOPLAM VÜCUT SIVISI EKSTRASELLÜLER SIVI (ESS) Toplam vücut sıvısının 1/3 ünü oluşturur. Major katyonu Na +2 dur Đntrasellüler sıvı Đnterstisyel sıvı Plazma Ekstrasellüler sıvı Đnterstisyel sıvı ESS nin ¾ ünü oluşturur Plazma ESS nin ¼ ünü oluşturur Ortalama ağırlıkta (70 kg) bir kişide toplam su miktarı yaklaşık 40 litre (vücut ağırlığının %57 si) kadardır. Vücut 43 sıvıları su ve su içinde çözünmüş maddeleri içerir. Đntrasellüler: hücre içindeki sıvı Ekstrasellüler: hücre dışındaki sıvı Đnterstisyel: doku hücrelerini çevreleyen sıvı Plazma: kanın sıvı kısmı 44 VÜCUT SIVILARININ DAĞILIMI Diğer Plazma Đnterstisyel Đntrasellüler Toplam vücut sıvısı yüzdesi VÜCUT SIVILARI Đntrasellüler Sitoplazma Yaşamın sürdürülebilmesi için gerekli reaksiyonlar Ekstrasellüler Plazma Lenfatik sıvı Serebrospinal sıvı Đdrar Sindirim sıvıları Destek ürünlerinin, atıkların ve bilginin taşınması Besinlerin yıkımı
9 VÜCUT SIVILARINDAKĐ ĐYONLAR Hücre içerisinde potasyum ve fosfat Đnterstisyel sıvıda sodyum ve klorür Plazmada sodyum ve klorür Đnterstisyel sıvı ile plazma arasındaki değişimler hidrostatik ve onkotik (osmotik) basınca bağlıdır. Hidrostatik basınç ve osmotik basınç ters yönde etkilidir. Hidrostatik basınç etkin olduğunda sıvıyı zarın öteki tarafına iter, osmotik basınç ise zarın öteki tarafından sıvıyı kendi tarafına çeker. Normalde kanın hidrostatik ve onkotik basıncı interstisyel sıvınınkinden çok daha yüksek 49 olduğu için madde ve gaz alışverişinde önem kazanırlar Herhangi bir su kitlesinde, suyun yüzeyindeki basınç atmosfer basıncına eşittir, fakat yüzeyden aşağıya doğru her 13.6 mm mesafede basınç 1 mm Hg yükselir. Suyun ağırlığından kaynaklanan bu basınca hidrostatik basınç denir. Kapiller yatağının artere yakın bölümünde hidrostatik basınç yüksektir (35 mmhg), sıvı damardan dokuya geçer. Venüle yakın kapiller bölümünde osmotik basınç ön plana geçer ve doku sıvısını damara çeker. Bu arada doku 52 sıvısının elektrolitleri ve küçük moleküllü proteinleri de damara girer. Ekstrasellüler ve intrasellüler sıvıların normal hacim ve bileşimlerinin devamlılığı yaşamın sürdürülebilirliği açısından büyük önem taşır. Bu sürdürülebilirlikte rol alan üç tip homeostasis bulunur: Hacim=Sıvı dengesi (ödem, dehidratasyon, hiperemi) Elektrolit dengesi (hipo-hipernatremi, hipohiperkalemi, hipo-hiperkalsemi.) Hücre içi O.B. >hücre dışı O.B. Hücre içi O.B. = hücre dışı O.B. Hücre içi O.B. < hücre dışı O.B. Asit-baz dengesi Doç.Dr.Erdal (asidoz, BALCANalkaloz)
10 HACĐM = SIVI DENGESĐ Hücrelerin normal yapı ve fonksiyonlarını sürdürebilmeleri için onları besleyen vücut sıvılarının, Belirli bir hacimde Belirli bir kimyasal yapıda olmaları Belirli bir hızda hareket etmeleri gerekir. Hücre dışındaki Osmotik Doç.Dr.Erdal basınç BALCAN daha fazla Vücut sıvılarının bu özelliklerindeki bozukluklar sonucunda çeşitli patolojik tablolar ortaya çıkar ÖDEM: Hücre içi sıvının artışı ve seröz boşluklarda sıvı birikimi DEHĐDRATASYON: Vücuttaki su miktarının normalin altına düşmesi HĐPEREMĐ: Dokunun damarları içindeki kan miktarının artması (Aktif Hiperemi: arteriollerin genişlemesi ile dokuya gelen kan miktarının artması, Pasif Hiperemi: venalardaki kan akımının ödem ödem yavaşlaması) 57 hiperemi 58 ASĐT-BAZ DENGESĐ Vücut sıvılarının kimyasal yapıları ya da ph değeri, enzimlerin katalitik aktiviteleri ve biyolojik makromoleküller üzerine etkilidir. Bu nedenle kan ve idrarda ph ölçümü hastalıkların tanınmasında yararlı olur. Normal koşullarda ekstrasellüler sıvıların ph ı (ortalama 7.4) arasındadır. 59 Vücudun intrasellüler kısmında metabolik faaliyetler sonucu oluşan ürünler (fosforik asit, sülfirik asit, HCl, laktik asitler gibi organik asitler) vücudun reaksiyonunu asit tarafa kaydırır. Organizmanın bunu önlemesi (yani ph ın 7.4 de sabit tutulması) 3 temel mekanizma ile olur: A.Kan ve hücreler içindeki tampon sistemler B.Solunum (CO 2 atılımı) C.Böbrekler (inorganik asit atılımı) 60 10
11 Vücut metabolizması sırasında üç çeşit asit üretilir: Karbondioksit (karbonik asit) atılırlar akciğerlerden Organik asitler (laktik asit ve keton cisimleri) vücut tarafından kullanılırlar Đnorganik asitler (kükürtlü amino asitlerden ve organik fosfor içeren bileşiklerden kaynaklanırlar) böbreklerden atılırlar 61 Asit Kaynak Normal Akıbet Günlük Üretim (mmol) CO 2 (karbonik asit) Organik Asitler Laktik asit Keton cisimleri Mineral Asitler Sülfirik asit Fosforik asit Đnsanlarda üretilen asitler Hücresel solunum Anaerobik glikoliz Yağ asidi oksidasyonu Kükürtlü amino asitler Organik fosfor içeren bileşikler Akciğerlerle atılır Glukoneogenez Doku oksidasyonu Böbreklerle atılır Organizmanın ph ı 7.4 de sabit tutmasındaki 3 temel mekanizma: A.Kan ve hücreler içindeki tampon sistemler B.Solunum (CO 2 atılımı) C.Böbrekler (inorganik asit atılımı) 63 A. KAN VE EKSTRASELLÜLER SIVIDAKĐ TAMPONLAR: Ekstrasellüler ve intrasellüler sıvıda dört ana tampon grup vardır: 1. Karbonik asit-bikarbonat tampon sistemi 2. Protein tampon sistemi 3. Hemoglobin tampon sistemi 4.Fosfat tampon sistemi Tampon (Baz) H + + HCO 3 H + + HPO 4 H + + Hb - H + + Prot - H tampon (asit) H 2 CO 3 CO 2 +H 2 O H 2 PO 4 H.Hb (deoksihemoglobin) H.Prot 64 Biyolojik Tampon Sistemleri TAMPON SĐSTEMLER ISS ESS Karbonik asit-bikarbonat tampon sistemi: ESS nin en önemli tampon sistemidir Fosfat tampon sistemi: idrar ve ISS nın ph nın tamponlanmasında görevlidir. FOSFAT T.S. PROTEĐN TAMPON SĐSTEMLER KARBONĐK ASĐT- BĐKARBONAT T.S. Protein tampon sistem: ESS ve ISS deki ph ın düzenlenmesine yardımcı olur. Bu tampon sistemi diğer tampon sistemleriyle etkileşir. 65 Hemoglobin TS (sadece eritrositler) HÜCRE Amino asit TS (tüm proteinler) Plazma protein TS 66 11
12 KARBONĐK ASĐT ASĐT--BĐKARBONAT TAMPON SĐSTEMĐ -Kan plazması ile akciğerler arasında görev yapar. -Primer görevi, ESS deki organik ve fikse asitler gibi etkenlerin neden olduğu ph değişikliğini önlemektir. -Proton vericisi olarak H2CO3, proton alıcısı olarak HCO3 bulunur. -Denge eşitliği: H+ + HCO3- = H2CO3 -Bu denklemde H+ eklenmesi dengeyi sağa kaydırır. Karbonik asit göreceli olarak kuvvetli bir asittir. Bu yüzden oluşabilecek problemler karbonik asidin erimiş CO2 ile dengeye girmesi ile çözümlenebilir: H2CO3 = CO2 + H2O -Bu sistem yaklaşık ph 7.4 de tamponlama yapar OH- + H eritrosit HHb eritrosit HHb H2O HbO2 O2 O2 CO2 HbO2 H+ HCO3 - H+ CO2 + H2O H2CO3 HCO3- H2CO3 Kapiller akciğerler : Karbonik anhidraz HHb: deoksihemoglobin HbO2: oksihemoglobin (oksijenlenmiş hemoglobin) Doç.Dr.Erdal BALCAN HCO3 : H+ iyonlarını tamponlar. (karbonik asit-bikarbonat T.S.) Dokular Klorid iyonları elektrolit dengesini sürdürmek için içeriye girer : Karbonik anhidraz 71 HHb: deoksihemoglobin (H+ iyonlarını tamponlar-hemoglobin T.S.) O2 salınımı 72 HbO2: oksihemoglobin (oksijenlenmiş hemoglobin 12
13 HEMOGLOBĐN ve CO 2 TRANSPORTU Hemoglobin, CO 2 nin akciğerlere transportunda sınırlı bir rol oynar. Mevcut CO 2 nin yaklaşık %25 i bir hemoglobin kompleks olan karbaminohemoglobin olarak transfer edilir: HB + CO 2 HbCO 2 %5 plazmada çözünmüş olarak taşınır %70 i ise bikarbonat iyonu (HCO 3- ) şeklinde akciğerler tarafından alınır. 2. FOSFAT TAMPON SĐSTEMĐ -Bütün hücrelerin sitoplazmalarında görev alır. -Önemli bir idrar tamponudur. -Proton vericisi olarak H 2 PO 4- (dihidrojen fosfat) proton alıcısı olarak HPO 4-2 (monohidrojen fosfat) bulunur. - ph arasında tamponlama yapar. Asidik bir solüsyonda monohidrojen fosfat ortamdan bir proton alarak tamponlama yapar 1. Bazik bir ortamda dihidrojen fosfat proton salarak tamponlama yapar 2. Bu nedenle fosfat tampon sistemi içinde bulunduğu solüsyona bağlı olarak hidrojen iyonu alır ya da verir PROTEĐN TAMPON SĐSTEMĐ ESS ve ISS de ph düzenlenmesini yapan bir tampon sistemdir. Proteinler tampon olarak görev yaparlar. Bikarbonat iyonu oluşumu sırasında ortaya çıkan H + iyonları kan proteinleri tarafından absorbe edilir. Nötral solüsyonlarda (ph= 7.0) amino asitler çift iyonize formda olur. Böyle dipolar iyonlara zwitterionik (Almanca hibrit) denir. Düşük ph lı solüsyonlarda karboksilat iyonları (-COO - ) bol hidrojen iyonları ile rekombine olur (katyon). H H NH + 3 C R NH 3 + C R COO - COOH Yüksek ph lı solüsyonlarda H iyonlarının azlığı, amino grubunun ya da karboksilat iyonunun hidrojen iyonu bağlama şansını azaltır (anyon) COO H NH 2 C R Plazma proteinleri kanın tamponlama kapasitesini arttırırlar. Đnterstisyel sıvı ph nın düzenlenmesine yardımcı ekstrasellüler protein fibrilleri ve amino asitler içerir. Aktive bir hücrenin ISS da yapısal proteinler ve diğer proteinler hücresel metabolizma ile oluşturulan piruvik asit, laktik asit gibi organik asitlerin neden olduğu yıkıcı ph değişikliklerini önlerler. ESS ile ISS arasında bir değişim olduğu için protein tampon sistemi ESS nın ph ının stabilitesine de yardımcı olur. Örneğin: ESS nın ph ı azaldığı zaman hücreler H iyonlarını ESS nın dışına pompalarlar ya da ISS ya alarak hücre içi proteinlerle tamponlanmasına neden olurlar. ESS nın ph ı arttığında hücre içinden hücre dışına H iyonları pompalanır. 4. HEMOGLOBĐN TAMPON SĐSTEMĐ ISS nın yaklaşık %5 ini oluşturan eritrositler normalde plazma içerisinde bulunur. Bu hücreler yoğun olarak hemoglobin ve karbonik anhidraz enzimi içerir. Bu hücrelerin (eritrositlerin) ESS da ph ya önemli bir etkisi vardır, çünkü bu hücreler CO 2 i absorblar ve onu karbonik aside dönüştürür. CO 2 eritosit membranını kolaylıkla geçer. Karbonik asit disosiye olurken HCO 3 iyonları klorür kayması yoluyla plazmaya geçer. H iyonları ise hemoglobin molekülleri tarafından tamponlanır. Bu, hemoglobin tampon sistem olarak adlandırılır. Bu tampon sistemi, ESS nın ph sı üzerine ani etkili tek ISS tampon sistemidir. Hb tampon sistemi, plazma PCO 2 düzeyi düştüğünde ya da yükseldiğinde ortaya çıkan şiddetli ph değişikliklerinin engellenmesinde yardımcı olur
14 HHb O 2 HbO 2 - : Karbonik anhidraz eritrosit H + HCO 3 - Kapiller CO 2 + H 2 O H 2 CO 3 HHb: deoksihemoglobin (H + iyonlarını tamponlar) O 2 salınımı HbO 2 : oksihemoglobin (oksijenlenmiş Doç.Dr.Erdal hemoglobin) BALCAN Dokular Klorid iyonları elektrolit dengesini sürdürmek için içeriye girer 79 HHb O 2 H 2 O CO 2 HbO 2 H + H 2 CO 3 HCO 3 : Karbonik anhidraz HHb: deoksihemoglobin (H+ iyonlarını tamponlar) O2 salınımı HbO 2 : oksihemoglobin (oksijenlenmiş hemoglobin) 80 HEMOGLOBĐN TAMPON SĐSTEM H + düzeyinin düzenlenmesinde önemli bir rol oynar. Tamponlama yeteneği, yapısındaki amino asitlerin polar gruplarına bağlıdır. Oksijenin yaklaşık %98 i hemoglobin tarafından taşınır. Oksihemoglobin Deoksihemoglobin oksijenli form oksijensiz form Ortalama bir kişi her 100 ml kanda yaklaşık 15 gram hemoglobin taşır ESS nın ph ı üzerine ani etkili tek ISS tampon sistemidir. Hb tampon sistemi plazma PCO 2 düzeyi düştüğünde ya da yükseldiğinde ortaya çıkan şiddetli ph değişikliklerinin engellenmesinde yardımcı olur Karbonik asit/bikarbonat tampon sistemi Protein tampon sistemi Ekstrasellüler sıvı Organizmanın ph ı 7.4 de sabit tutmasındaki 3 temel mekanizma: A.Kan ve hücreler içindeki tampon sistemler Protein tampon sistemi Fosfat tampon sistemi Hemoglobin tampon sistemi Đntrasellüler sıvı 83 B.Solunum (CO 2 atılımı) C.Böbrekler (inorganik asit atılımı) 84 14
15 B. SOLUNUM Solunum sisteminin asıl görevi kan gazları diye tanımlanan oksijen(o 2 ) ve karbondioksit (CO 2 ) in değiştirilmesidir. Akciğerler, karbondioksidi uzaklaştırarak ya da muhafaza ederek asit-baz dengesinin düzenlenmesinde yardımcı olur. ph solunum hızının ve derinliğinin değişimi ile düzenlenebilir. Hiperventilasyon: solunumun hızının ve derinliğinin artması. Kanda CO 2 azalır, ph Hipoventilasyon: solunum hızının ve derinliğinin azalması. Kanda CO 2 artar, ph Akciğerde hava değişiminin (ventilasyon ventilasyon) sağlanması, alveollerde kan gazlarının değişimi, Kanda gazların taşınması, Dokuda gazların değişimi ve Hücrede solunum. 1. PERĐFERĐK DOKULAR AKCĐĞERLER PERĐFERĐK DOKULAR Eritrositler periferik dokulara oksijen sağlarlar ve CO 2 metabolizmasında anahtar bir rol oynarlar. Hücre içinde oluşan CO 2 ekstrasellüler sıvıya difüze olarak PCO 2 nı arttırır. Eritrositlere geçen CO 2 burada karbonik anhidraz enzimi ile hidrolize edilerek H + ve HCO 3- a ayrılır. Arteryel kana göre kısmi basıncı (PO 2 ) dokularda daha düşük olduğu için oksijen hemoglobinden ayrılarak dokulara geçer (PO 2 O 2 ile bağlanan Hb yüzdesi ) 87 HHb O 2 HbO 2 - : Karbonik anhidraz eritrosit H + HCO 3 - Kapiller CO 2 + H 2 O H 2 CO 3 HHb: deoksihemoglobin (H + iyonlarını tamponlar) O 2 salınımı HbO 2 : oksijenlenmiş hemoglobin 1. PERĐFERĐK DOKULAR (PO 2 ) (PCO 2 ) Dokular Klorid iyonları elektrolit dengesini sürdürmek için içeriye girer 88 AKCĐĞERLER 2. AKCĐĞERLER Gazların taşınma işlemi akciğerlerde tersine döner. PCO 2 akciğerlerde düşük olduğu için karbondioksit ekstrasellüler sıvıdan alveollere difüze olur. Bikarbonat gradient farkından dolayı eritrositlere difüze olur ve klorür iyonu ekstrasellüler ortama döner. Alveollerde PO 2 venöz kana göre daha yüksek olduğu için oksijen eritrositlere difüze olarak Hb e bağlanır. Karbondioksit sudan başka Hb ile de reaksiyona girerek karbominohemoglobin (HbCO 2 ) bileşiğini oluşturarak da salınır. 89 HHb O 2 H 2 O CO 2 HbO 2 H + H 2 CO 3 HCO 3 (PO 2 ) : Karbonik anhidraz HHb: deoksihemoglobin (H+ iyonlarını tamponlar) O 2 salınımı HbO 2 : oksihemoglobin (oksijenlenmiş hemoglobin) (PCO 2 ) 90 15
16 Karbondioksidin alveollerden atılması ve hemoglobinin oksijenlenmesi solunum merkezi tarafından kontrol edilen solunum hızına bağlıdır. Hipotalamusta yer alan merkezdeki reseptörler karbondioksit ve H+ miktarlarındaki artışlara yanıt verir Böylece PCO 2 yükseldiğinde veya ph düştüğünde solunum hızı artar. Ayrıca aorta ve karotis damarlarında oksjen basıncındaki değişikliklere duyarlı kemoreseptörler vardır. HEMOGLOBĐN ve OKSĐJEN TAŞINIMI Akciğerlerde O 2 hemoglobin tarafından tutulur. Kan hücrelere ulaştığı zaman O 2 hemoglobinden ayrılır: HEMOGLOBĐN ve CO 2 TRANSPORTU Hemoglobin, CO 2 nin akciğerlere transportunda sınırlı bir rol oynar. Mevcut CO 2 nin yaklaşık %25 i bir hemoglobin kompleks olan karbaminohemoglobin olarak transfer edilir: HB + CO 2 HbCO 2 %5 plazmada çözünmüş olarak taşınır %70 i ise bikarbonat iyonu (HCO 3- ) şeklinde akciğerler tarafından alınır. KAN GAZLARI VE ÖNEMĐ: Oksijen ve karbon dioksidin arter, ven veya kapiller kandaki kısmi basınçlarına kan gazları adı verilir. 1.Tanı amaçlı akciğerlerin oksijenlenme kapasitesinin değerlendirilmesi. 2.Tanı amaçlı kandaki oksijen basıncının değerlendirilmesi. 3.Solunum yeterliliğinin değerlendirilmesi 4.Asit-baz dengesinin değerlendirilmesinde önemlidir Referans değerler: PO 2 (arteriyel): mmhg PCO 2 (arteriyel): mmhg Arttığı Haller: PO 2 : oksijen tedavisi PCO 2 : Solunumsal asidoz, kompanse metabolik alkoloz. Azaldığı Haller: PO 2 : Hipoksemi, kardiyak outputun azalması, karbon monoksit zehirlenmesi, anestezi, solunumsal distres sendromu, alveolar hipoventilasyon. PCO 2 : Solunumsal alkaloz, kompanse metabolik asidoz 95 Organizmanın ph ı 7.4 de sabit tutmasındaki 3 temel mekanizma: A.Kan ve hücreler içindeki tampon sistemler B.Solunum (CO 2 atılımı) C.Böbrekler (inorganik asit atılımı) 96 16
17 C. BÖBREKLER Böbrekler, bikarbonat geri emilimi ve H + iyonları ile asidik anyonların atılması başta olmak üzere asit-baz dengesinde bir çok önemli role sahiptir. Asidik durumlarda H + iyonlarının fazlalığı atılır, daha fazla bikarbonat iyonları yapılır ve kan ph ı artar. Bazik durumlarda bikarbonat iyonları elimine edilerek kan ph ı azaltılır. ph dengesinin düzenlenmesi uzun sürer. Böbrekler, bikarbonat ve hidrojen iyonlarının salınımına ya da tutulmasına neden olarak dengeyi sağlar. KAYNAKLAR 1. Lehninger Principles of Biochemistry. Nelson DL, Cox MM, 4th ed. W. H. Freeman ed Basic Concepts in Biochemistry. HF second ed. McGraw Hill Biochemistry. Berg JM, Tymoczko JL, Stryer L. 5th ed. Freeman and Com Molecular Biology of the Cell Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P. 5th ed
ASİT- BAZ DENGESİ VE DENGESİZLİKLERİ. Prof. Dr. Tülin BEDÜK 2016
 ASİT- BAZ DENGESİ VE DENGESİZLİKLERİ Prof. Dr. Tülin BEDÜK 2016 Herhangi bir çözeltinin asitliği veya bazlığı içindeki hidrojen iyonunun (H + ) konsantrasyonuna bağlıdır. Beden sıvılarının asit-baz dengesi
ASİT- BAZ DENGESİ VE DENGESİZLİKLERİ Prof. Dr. Tülin BEDÜK 2016 Herhangi bir çözeltinin asitliği veya bazlığı içindeki hidrojen iyonunun (H + ) konsantrasyonuna bağlıdır. Beden sıvılarının asit-baz dengesi
Yrd.Doç.Dr. Erdal Balcan 1
 VÜCUTTA ASİT-BAZ DENGESİ BOZUKLUKLARI ASİDOZ Kan ph ının ALKALOZ Kan ph ının ASİDOZLAR: Vücut ekstrasellüler sıvılarında H + artmasından ya da bazların azalmasından ileri gelir. Vücut normal ph ının (7.35-7.45)
VÜCUTTA ASİT-BAZ DENGESİ BOZUKLUKLARI ASİDOZ Kan ph ının ALKALOZ Kan ph ının ASİDOZLAR: Vücut ekstrasellüler sıvılarında H + artmasından ya da bazların azalmasından ileri gelir. Vücut normal ph ının (7.35-7.45)
TAMPONLAR-pH ve pk HESAPLAMALARI
 Genel tanımlamalar TAMPONLAR-pH ve pk HESAPLAMALARI YRD. DOÇ.DR SEDAT MOTOR Tamponlarla ilgili açıklamalara geçmeden önce asit, baz, ph ve pk kavramlarını hatırlayalım. Suda çözündügü zaman (H + ) iyonu
Genel tanımlamalar TAMPONLAR-pH ve pk HESAPLAMALARI YRD. DOÇ.DR SEDAT MOTOR Tamponlarla ilgili açıklamalara geçmeden önce asit, baz, ph ve pk kavramlarını hatırlayalım. Suda çözündügü zaman (H + ) iyonu
Başlıca organizma sıvılarının ve salgılarının ortalama ph değerleri.
 Asid-baz dengesi ph Başlıca organizma sıvılarının ve salgılarının ortalama ph değerleri. Organizma sıvıları, salgıları Ortalama ph Kan 7.4 Süt 6.7 Safra 7.8 İdrar 6.0 Pankreas özsuyu 8.0 Bağırsak özsuyu
Asid-baz dengesi ph Başlıca organizma sıvılarının ve salgılarının ortalama ph değerleri. Organizma sıvıları, salgıları Ortalama ph Kan 7.4 Süt 6.7 Safra 7.8 İdrar 6.0 Pankreas özsuyu 8.0 Bağırsak özsuyu
Fizyoloji. Vücut Sıvı Bölmeleri ve Özellikleri. Dr. Deniz Balcı.
 Fizyoloji Vücut Sıvı Bölmeleri ve Özellikleri Dr. Deniz Balcı deniz.balci@neu.edu.tr Ders İçeriği 1 Vücut Sıvı Bölmeleri ve Hacimleri 2 Vücut Sıvı Bileşenleri 3 Sıvıların Bölmeler Arasındaki HarekeF Okuma
Fizyoloji Vücut Sıvı Bölmeleri ve Özellikleri Dr. Deniz Balcı deniz.balci@neu.edu.tr Ders İçeriği 1 Vücut Sıvı Bölmeleri ve Hacimleri 2 Vücut Sıvı Bileşenleri 3 Sıvıların Bölmeler Arasındaki HarekeF Okuma
ph = 6,1 + log [CO 2 ]
![ph = 6,1 + log [CO 2 ] ph = 6,1 + log [CO 2 ]](/thumbs/19/198833.jpg) ASİT-BAZ DENGESİ Asit-baz dengesi tanımı Biyolojik reaksiyonların hepsi optimum bir ph ortamında normal olarak cereyan ederler; ortamın ph değerinin değişmesi, önemli bozukluklara neden olur. Organizmada
ASİT-BAZ DENGESİ Asit-baz dengesi tanımı Biyolojik reaksiyonların hepsi optimum bir ph ortamında normal olarak cereyan ederler; ortamın ph değerinin değişmesi, önemli bozukluklara neden olur. Organizmada
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
SOLUNUM SİSTEMİ VE EGZERSİZ
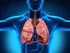 SOLUNUM SİSTEMİ VE EGZERSİZ Solunum Sisteminin Temel Anatomisi Burun veya ağız Farinks Larinks Trakea Bronşlar Bronşioller Alveoller İletim bölgesi: gaz değişimine katılmayan ağız, burun, larinks, trakea,
SOLUNUM SİSTEMİ VE EGZERSİZ Solunum Sisteminin Temel Anatomisi Burun veya ağız Farinks Larinks Trakea Bronşlar Bronşioller Alveoller İletim bölgesi: gaz değişimine katılmayan ağız, burun, larinks, trakea,
Kanın fonksiyonel olarak üstlendiği görevler
 EGZERSİZ VE KAN Kanın fonksiyonel olarak üstlendiği görevler Akciğerden dokulara O2 taşınımı, Dokudan akciğere CO2 taşınımı, Sindirim organlarından hücrelere besin maddeleri taşınımı, Hücreden atık maddelerin
EGZERSİZ VE KAN Kanın fonksiyonel olarak üstlendiği görevler Akciğerden dokulara O2 taşınımı, Dokudan akciğere CO2 taşınımı, Sindirim organlarından hücrelere besin maddeleri taşınımı, Hücreden atık maddelerin
VÜCUT SIVILARI. Yrd.Doç.Dr. Önder AYTEKİN. Copyright 2004 Pearson Education, Inc., publishing as Benjamin Cummings
 VÜCUT SIVILARI Yrd.Doç.Dr. Önder AYTEKİN Su Dengesi Vücudumuzun önemli bir bölümü sudan oluşur ve su dengesi vücudun en önemli sorunlarından birisidir. Günlük olarak alınan ve vücuttan atılan su miktarı
VÜCUT SIVILARI Yrd.Doç.Dr. Önder AYTEKİN Su Dengesi Vücudumuzun önemli bir bölümü sudan oluşur ve su dengesi vücudun en önemli sorunlarından birisidir. Günlük olarak alınan ve vücuttan atılan su miktarı
Her madde atomlardan oluşur
 2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
2 Yaşamın kimyası Figure 2.1 Helyum Atomu Çekirdek Her madde atomlardan oluşur 2.1 Atom yapısı - madde özelliği Elektron göz ardı edilebilir kütle; eksi yük Çekirdek: Protonlar kütlesi var; artı yük Nötronlar
Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile
 Su Kimyası Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile canlılık için gerekli ortamı sunar. Canlıların
Su Kimyası Tüm yaşayan organizmalar suya ihtiyaç duyarlar Çoğu hücre suyla çevrilidir ve hücrelerin yaklaşık %70 95 kadarı sudan oluşur. Yerküre içerdiği su ile canlılık için gerekli ortamı sunar. Canlıların
9. SINIF KONU ANLATIMI 5 CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU
 9. SINIF KONU ANLATIMI 5 CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU Canlıların yapısına katılan maddeler çeşitli özellikler nedeni ile temel olarak iki grupta incelenir. Canlının Temel Bileşenleri
9. SINIF KONU ANLATIMI 5 CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU Canlıların yapısına katılan maddeler çeşitli özellikler nedeni ile temel olarak iki grupta incelenir. Canlının Temel Bileşenleri
ADIM ADIM YGS-LYS 5. ADIM CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU
 ADIM ADIM YGS-LYS 5. ADIM CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU Canlıların yapısına katılan maddeler çeşitli özellikler nedeni ile temel olarak iki grupta incelenir. Canlının Temel Bileşenleri
ADIM ADIM YGS-LYS 5. ADIM CANLININ TEMEL BİLEŞENLERİ -İNORGANİK MADDELER 1- SU Canlıların yapısına katılan maddeler çeşitli özellikler nedeni ile temel olarak iki grupta incelenir. Canlının Temel Bileşenleri
SOLUNUM SİSTEMİ VE EGZERSİZ
 SOLUNUM SİSTEMİ VE EGZERSİZ Egzersiz sırasında çalışan kaslar, ihtiyaç duydukları enerji için oksijen (O 2 ) kullanır ve karbondioksit (CO 2 ) üretir. Akciğerler, hava ile kanın karşılaştığı ı organlardır.
SOLUNUM SİSTEMİ VE EGZERSİZ Egzersiz sırasında çalışan kaslar, ihtiyaç duydukları enerji için oksijen (O 2 ) kullanır ve karbondioksit (CO 2 ) üretir. Akciğerler, hava ile kanın karşılaştığı ı organlardır.
CANLILARDA TAMPONLAMA
 CANLILARDA TAMPONLAMA ph= -log [H + ] / Sorensen, H potansiyeli örnekler Hücreler ve organizmalar özgül ve sabit bir sitozol ve hücre dışı sıvı ph sını korurlar Böylece biyomoleküllerin en uygun iyonik
CANLILARDA TAMPONLAMA ph= -log [H + ] / Sorensen, H potansiyeli örnekler Hücreler ve organizmalar özgül ve sabit bir sitozol ve hücre dışı sıvı ph sını korurlar Böylece biyomoleküllerin en uygun iyonik
ayxmaz/biyoloji Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H
 Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Akciğer ve Dokularda Gazların Değişimi ve Taşınması
 Akciğer ve Dokularda Gazların Değişimi ve Taşınması Prof.Dr.Fadıl ÖZYENER Fizyoloji Anabilim Dalı Tartışma konuları: Eksternal ve internal solunum Oksijenin kanda taşınması Karbondioksidin kanda taşınması
Akciğer ve Dokularda Gazların Değişimi ve Taşınması Prof.Dr.Fadıl ÖZYENER Fizyoloji Anabilim Dalı Tartışma konuları: Eksternal ve internal solunum Oksijenin kanda taşınması Karbondioksidin kanda taşınması
SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU
 SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU Suyun polaritesinin etkileri Su molekülünün polar olması hidrojen bağlarının oluşmasına neden olur. 2 Su molekülü Oldukça basit yapılıdır. Tekli bağla bağlı olup
SU ve ÇEVRENİN CANLILAR İÇİN UYGUNLUĞU Suyun polaritesinin etkileri Su molekülünün polar olması hidrojen bağlarının oluşmasına neden olur. 2 Su molekülü Oldukça basit yapılıdır. Tekli bağla bağlı olup
SU VE HÜCRE İLİŞKİSİ
 SU VE HÜCRE İLİŞKİSİ Oluşturacağı her 1 g organik madde için bitkinin 500 g kadar suyu kökleriyle alması ve tepe (uç) noktasına kadar taşıyarak atmosfere aktarması gerekir. Normal su düzeyinde hayvan hücrelerinin
SU VE HÜCRE İLİŞKİSİ Oluşturacağı her 1 g organik madde için bitkinin 500 g kadar suyu kökleriyle alması ve tepe (uç) noktasına kadar taşıyarak atmosfere aktarması gerekir. Normal su düzeyinde hayvan hücrelerinin
Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O.
 Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O. Kan Gazı Nedir? Kanın a s i t ve b a z d u r u m u n u b e l i r l e m e a m a c ı y l a kan gazı değerlerinin belirlenmesi gerekir. Ortaya çıkan
Öğr. Gör. Ahmet Emre AZAKLI İKBÜ Sağlık Hizmetleri M.Y.O. Kan Gazı Nedir? Kanın a s i t ve b a z d u r u m u n u b e l i r l e m e a m a c ı y l a kan gazı değerlerinin belirlenmesi gerekir. Ortaya çıkan
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
ARTER KAN GAZI ANALİZİNİN ORGANİZMAYA AİT YANSITTIKLARI; Klinikte AKG ne işe yarar?
 ARTER KAN GAZI ANALİZİNİN ORGANİZMAYA AİT YANSITTIKLARI; Klinikte AKG ne işe yarar? AKCİĞERLERİN PRİMER GÖREVİ GAZ ALIŞVERİŞİNİ SAĞLAMAKTIR. AKG analizi ile Asit Baz dengesi Oksijenizasyon Gaz alışverişi
ARTER KAN GAZI ANALİZİNİN ORGANİZMAYA AİT YANSITTIKLARI; Klinikte AKG ne işe yarar? AKCİĞERLERİN PRİMER GÖREVİ GAZ ALIŞVERİŞİNİ SAĞLAMAKTIR. AKG analizi ile Asit Baz dengesi Oksijenizasyon Gaz alışverişi
Suyun Fizikokimyasal Özellikleri
 Suyun Fizikokimyasal Özellikleri Su bitkinin yaşamında yaşamsal bir rol oynar. Bitki tarafından yapılan her gram başına organik madde için kökler tarafından 500 gr su alınır. Bu su, bitkinin bir ucundan
Suyun Fizikokimyasal Özellikleri Su bitkinin yaşamında yaşamsal bir rol oynar. Bitki tarafından yapılan her gram başına organik madde için kökler tarafından 500 gr su alınır. Bu su, bitkinin bir ucundan
Su ve çevrenin canlılar için uygunluğu
 Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır.
 7. ASİTLER VE BAZLAR Arrhenius AsitBaz Tanımı (1884) (Svante Arrhenius) Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır. HCl H + + Cl NaOH
7. ASİTLER VE BAZLAR Arrhenius AsitBaz Tanımı (1884) (Svante Arrhenius) Suda çözündüğünde hidrojen iyonu verebilen maddeler asit, hidroksil iyonu verebilenler baz olarak tanımlanmıştır. HCl H + + Cl NaOH
DÖNEM 2- I. DERS KURULU AMAÇ VE HEDEFLERİ
 DÖNEM 2- I. DERS KURULU AMAÇ VE HEDEFLERİ Kan, kalp, dolaşım ve solunum sistemine ait normal yapı ve fonksiyonların öğrenilmesi 1. Kanın bileşenlerini, fiziksel ve fonksiyonel özelliklerini sayar, plazmanın
DÖNEM 2- I. DERS KURULU AMAÇ VE HEDEFLERİ Kan, kalp, dolaşım ve solunum sistemine ait normal yapı ve fonksiyonların öğrenilmesi 1. Kanın bileşenlerini, fiziksel ve fonksiyonel özelliklerini sayar, plazmanın
Solunum Sistemi Fizyolojisi
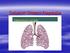 Solunum Sistemi Fizyolojisi 1 2 3 4 5 6 7 Solunum Sistemini Oluşturan Yapılar Solunum sistemi burun, agız, farinks (yutak), larinks (gırtlak), trakea (soluk borusu), bronslar, bronsioller, ve alveollerden
Solunum Sistemi Fizyolojisi 1 2 3 4 5 6 7 Solunum Sistemini Oluşturan Yapılar Solunum sistemi burun, agız, farinks (yutak), larinks (gırtlak), trakea (soluk borusu), bronslar, bronsioller, ve alveollerden
HÜCRE ZARINDA TAŞINIM
 HÜCRE ZARINDA TAŞINIM Yrd. Doç. Dr. Aslı AYKAÇ YDÜ TIP FAKÜLTESİ BİYOFİZİK AD Küçük moleküllerin zardan geçişi Lipid çift tabaka Polar moleküller için geçirgen olmayan bir bariyerdir Hücre içindeki suda
HÜCRE ZARINDA TAŞINIM Yrd. Doç. Dr. Aslı AYKAÇ YDÜ TIP FAKÜLTESİ BİYOFİZİK AD Küçük moleküllerin zardan geçişi Lipid çift tabaka Polar moleküller için geçirgen olmayan bir bariyerdir Hücre içindeki suda
ADIM ADIM YGS LYS Adım BOŞALTIM SİSTEMİ 3
 ADIM ADIM YGS LYS 184. Adım BOŞALTIM SİSTEMİ 3 2) Geri Emilim (Reabsorpsiyon) Bowman kapsülüne gelen süzüntü geri emilim olmadan dışarı atılsaydı zararlı maddelerle birlikte yararlı maddelerde kaybedilirdi.
ADIM ADIM YGS LYS 184. Adım BOŞALTIM SİSTEMİ 3 2) Geri Emilim (Reabsorpsiyon) Bowman kapsülüne gelen süzüntü geri emilim olmadan dışarı atılsaydı zararlı maddelerle birlikte yararlı maddelerde kaybedilirdi.
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Asit-Baz Dengesi. Yrd.Doç.Dr.Filiz Bakar
 Asit-Baz Dengesi Yrd.Doç.Dr.Filiz Bakar ph Kavramı Asit-Baz Ê İlk modern tanım, İsveç'li bilim adamı Svonte ARHENİUS (1884) tarafından yapıldı Ê Sudaki çözeltilerine H+ iyonu veren maddeler "asit" Ê Sudaki
Asit-Baz Dengesi Yrd.Doç.Dr.Filiz Bakar ph Kavramı Asit-Baz Ê İlk modern tanım, İsveç'li bilim adamı Svonte ARHENİUS (1884) tarafından yapıldı Ê Sudaki çözeltilerine H+ iyonu veren maddeler "asit" Ê Sudaki
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
Yrd. Doç. Dr. Murat Sarıtemur Atatürk Üniversitesi Tıp Fakültesi Acil Tıp AD 2014
 Yrd. Doç. Dr. Murat Sarıtemur Atatürk Üniversitesi Tıp Fakültesi Acil Tıp AD 2014 Neden kan gazı analizi? Oksijenizasyon ve ventilasyonun değerlendirilmesi Asit-baz dengesini değerlendirmek ph / P a CO
Yrd. Doç. Dr. Murat Sarıtemur Atatürk Üniversitesi Tıp Fakültesi Acil Tıp AD 2014 Neden kan gazı analizi? Oksijenizasyon ve ventilasyonun değerlendirilmesi Asit-baz dengesini değerlendirmek ph / P a CO
CANLILARIN TEMEL BİLEŞENLERİ
 1 CANLILARIN TEMEL BİLEŞENLERİ Canlıların temel bileşenleri; inorganik ve organik bileşikler olmak üzere ikiye ayrılır. **İnorganik bileşikler: Canlılar tarafından sentezlenemezler. Dışarıdan hazır olarak
1 CANLILARIN TEMEL BİLEŞENLERİ Canlıların temel bileşenleri; inorganik ve organik bileşikler olmak üzere ikiye ayrılır. **İnorganik bileşikler: Canlılar tarafından sentezlenemezler. Dışarıdan hazır olarak
FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU
 FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU Fizyolojiye Giriş Temel Kavramlar Fizyolojiye Giriş Canlıda meydana gelen fiziksel ve kimyasal değişikliklerin tümüne birden yaşam denir. İşte canlı organizmadaki
FİZYOLOJİ LABORATUVAR BİLGİSİ VEYSEL TAHİROĞLU Fizyolojiye Giriş Temel Kavramlar Fizyolojiye Giriş Canlıda meydana gelen fiziksel ve kimyasal değişikliklerin tümüne birden yaşam denir. İşte canlı organizmadaki
İLERİ KARDİYAK YAŞAM DESTEĞİ KURSU ASİT-BAZ DENGESİ VE KAN GAZI ANALİZİ
 İLERİ KARDİYAK YAŞAM DESTEĞİ KURSU ASİT-BAZ DENGESİ VE KAN GAZI ANALİZİ AMAÇ: Katılımcıların bu sunumun sonunda kan gazı ve asit baz dengesi ile ilgili bilgilerini artırmaları amaçlanmıştır. HEDEFLER:
İLERİ KARDİYAK YAŞAM DESTEĞİ KURSU ASİT-BAZ DENGESİ VE KAN GAZI ANALİZİ AMAÇ: Katılımcıların bu sunumun sonunda kan gazı ve asit baz dengesi ile ilgili bilgilerini artırmaları amaçlanmıştır. HEDEFLER:
HAYVANSAL ÜRETİM FİZYOLOJİSİ
 HAYVANSAL ÜRETİM FİZYOLOJİSİ 9. Hafta Prof. Dr. Gürsel DELLAL 1 Su, Elektrolitler ve Asit-Baz Dengesi Hücreler yaşamlarını su olmadan sürdüremezler. Su tüm vücuda dağılmış durumdadır ve ergin hayvanın
HAYVANSAL ÜRETİM FİZYOLOJİSİ 9. Hafta Prof. Dr. Gürsel DELLAL 1 Su, Elektrolitler ve Asit-Baz Dengesi Hücreler yaşamlarını su olmadan sürdüremezler. Su tüm vücuda dağılmış durumdadır ve ergin hayvanın
5.111 Ders Özeti #22 22.1. (suda) + OH. (suda)
 5.111 Ders Özeti #22 22.1 Asit/Baz Dengeleri Devamı (Bölümler 10 ve 11) Konular: Zayıf baz içeren dengeler, tuz çözeltilerinin ph sı ve tamponlar Çarşamba nın ders notlarından 2. Suda Baz NH 3 H 2 OH Bazın
5.111 Ders Özeti #22 22.1 Asit/Baz Dengeleri Devamı (Bölümler 10 ve 11) Konular: Zayıf baz içeren dengeler, tuz çözeltilerinin ph sı ve tamponlar Çarşamba nın ders notlarından 2. Suda Baz NH 3 H 2 OH Bazın
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur.
 Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
OKSİJENLİ SOLUNUM
 1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
5.111 Ders Özeti #21 21.1
 5.111 Ders Özeti #21 21.1 AsitBaz Dengesi Bölüm 10 Okunsun Konular: Asit ve Bazların Sınıflandırılması, Suyun Öziyonlaşması, ph Fonksiyonları, Asit ve Baz Kuvvetleri, Zayıf Asit İçeren Dengeler. Asit ve
5.111 Ders Özeti #21 21.1 AsitBaz Dengesi Bölüm 10 Okunsun Konular: Asit ve Bazların Sınıflandırılması, Suyun Öziyonlaşması, ph Fonksiyonları, Asit ve Baz Kuvvetleri, Zayıf Asit İçeren Dengeler. Asit ve
00220 Gıda Biyokimyası
 00220 Gıda Biyokimyası Hazırlayan: Doç.Gökhan DURMAZ 00220 Gıda Biyokimyası-Şubat 2013 1 Bu notların hazırlanmasında aşağıdaki eserlerden yararlanılmıştır; Biyokimya, Engin Gözükara, Nobel Tip Kitabevi,
00220 Gıda Biyokimyası Hazırlayan: Doç.Gökhan DURMAZ 00220 Gıda Biyokimyası-Şubat 2013 1 Bu notların hazırlanmasında aşağıdaki eserlerden yararlanılmıştır; Biyokimya, Engin Gözükara, Nobel Tip Kitabevi,
Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir maddeye çözeltinin bileşenleri denir.
 GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
GENEL KİMYA 1 LABORATUARI ÇALIŞMA NOTLARI DENEY: 8 ÇÖZELTİLER Dr. Bahadır KESKİN, 2011 @ YTÜ Fiziksel özellikleri her yerde aynı olan (homojen) karışımlara çözelti denir. Bir çözeltiyi oluşturan her bir
Suda çözünebilen nişasta molekülleri pityalin (amilaz) enzimiyle küçük moleküllere parçalanır.
 CANLILARDA ENERJİ Besinlerin Enerjiye Dönüşümü Besin öğeleri: Karbonhidratlar, yağlar, proteinler, vitaminler, mineraller Besin maddelerindeki bu öğelerin vücut tarafından kullanılabilmesi için sindirilmesi
CANLILARDA ENERJİ Besinlerin Enerjiye Dönüşümü Besin öğeleri: Karbonhidratlar, yağlar, proteinler, vitaminler, mineraller Besin maddelerindeki bu öğelerin vücut tarafından kullanılabilmesi için sindirilmesi
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER»
 FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
FARMASÖTİK TEKNOLOJİ I «ÇÖZELTİLER» Uygun bir çözücü içerisinde bir ya da birden fazla maddenin çözündüğü veya moleküler düzeyde disperse olduğu tektür (homojen: her tarafta aynı oranda çözünmüş veya dağılmış
Paylaşılan elektron ya da elektronlar, her iki çekirdek etrafında dolanacaklar, iki çekirdek arasındaki bölgede daha uzun süre bulundukları için bu
 4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
4.Kimyasal Bağlar Kimyasal Bağlar Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir. Pek çok madde farklı element atomlarının birleşmesiyle meydana gelmiştir. İyonik bağ
Biyokimya. Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler)
 Biyokimya Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler) Bölüm 1: Biyokimya ve önemi: 1. Biyokimya tanımı, önemi ve boyutsal
Biyokimya Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler) Bölüm 1: Biyokimya ve önemi: 1. Biyokimya tanımı, önemi ve boyutsal
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1
 ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1 Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır. Hangi tanımın
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI M.DEMİR ASİT VE BAZ KAVRAMLARI 1 Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır. Hangi tanımın
Solunum. Solunum ve odunsu bitkilerin büyümesi arasında yüksek bir korelasyon bulunmaktadır (Kozlowski ve Pallardy, 1997).
 SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
BİY 315 BİYOKİMYA GİRİŞ. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.-
 1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.- Biyokimya sözcüğü biyolojik kimya (=yaşam kimyası) teriminin kısaltılmış şeklidir. Daha eskilerde, fizyolojik kimya terimi kullanılmıştır. Gerçekten de Biyokimya
1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.- Biyokimya sözcüğü biyolojik kimya (=yaşam kimyası) teriminin kısaltılmış şeklidir. Daha eskilerde, fizyolojik kimya terimi kullanılmıştır. Gerçekten de Biyokimya
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI
 ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI Prof. Dr. Mustafa DEMİR M.DEMİR 0ASİT VE BAZ KAVRAMLARI Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır.
ASİTLER VE BAZLAR ASİT VE BAZ KAVRAMLARI Prof. Dr. Mustafa DEMİR M.DEMİR 0ASİT VE BAZ KAVRAMLARI Asit ve baz, değişik zamanlarda değişik şekillerde tanımlanmıştır. Bugün bu tanımların hepsi de kullanılmaktadır.
[embeddoc url= /10/VÜCUT-SIVILARI.docx download= all viewer= microsoft ]
![[embeddoc url= /10/VÜCUT-SIVILARI.docx download= all viewer= microsoft ] [embeddoc url= /10/VÜCUT-SIVILARI.docx download= all viewer= microsoft ]](/thumbs/64/51472037.jpg) VÜCUT SIVILARI [embeddoc url= http://enfeksiyonhastaliklari.com/wp-content/uploads/2015 /10/VÜCUT-SIVILARI.docx download= all viewer= microsoft ] SODYUM ( Na+) Na+; Sodyum klor ile birlikte serumun en
VÜCUT SIVILARI [embeddoc url= http://enfeksiyonhastaliklari.com/wp-content/uploads/2015 /10/VÜCUT-SIVILARI.docx download= all viewer= microsoft ] SODYUM ( Na+) Na+; Sodyum klor ile birlikte serumun en
Solunum: Solunum sistemi" Eritrositler" Dolaşım sistemi"
 Solunum Fizyolojisi Solunum: O 2 'nin taşınarak hücrelere ulaştırılması, üretilen CO 2 'in uzaklaştırılması." Bu işlevin gerçekleştirilebilmesi için üç sistem koordinasyon içinde çalışır:" " Solunum sistemi"
Solunum Fizyolojisi Solunum: O 2 'nin taşınarak hücrelere ulaştırılması, üretilen CO 2 'in uzaklaştırılması." Bu işlevin gerçekleştirilebilmesi için üç sistem koordinasyon içinde çalışır:" " Solunum sistemi"
HISTOLOJIDE BOYAMA YÖNTEMLERI. Dr. Yasemin Sezgin. yasemin sezgin
 HISTOLOJIDE BOYAMA YÖNTEMLERI Dr. Yasemin Sezgin yasemin sezgin HÜRESEL BOYAMANIN TEMEL PRENSİPLERİ Hem fiziksel hem kimyasal faktörler hücresel boyamayı etkilemektedir BOYAMA MEKANIZMASı Temelde boyanın
HISTOLOJIDE BOYAMA YÖNTEMLERI Dr. Yasemin Sezgin yasemin sezgin HÜRESEL BOYAMANIN TEMEL PRENSİPLERİ Hem fiziksel hem kimyasal faktörler hücresel boyamayı etkilemektedir BOYAMA MEKANIZMASı Temelde boyanın
solunum >solunum gazlarının vücut sıvısı ile hücreler arasındaki değişimidir.
 GAZ ALIŞVERİŞİ O2'li solunum yapan canlıların bazılarında O2'in alınıp CO2'in atılmasını sağlayan yapılar bulunur.bu yapı ve organlar solunum sistemini oluşturur. solunum ------>solunum organlarıyla dış
GAZ ALIŞVERİŞİ O2'li solunum yapan canlıların bazılarında O2'in alınıp CO2'in atılmasını sağlayan yapılar bulunur.bu yapı ve organlar solunum sistemini oluşturur. solunum ------>solunum organlarıyla dış
ÇÖZELTİLERDE DENGE (Asit-Baz)
 ÇÖZELTİLERDE DENGE (AsitBaz) SUYUN OTOİYONİZASYONU Saf suyun elektrik akımını iletmediği bilinir, ancak çok hassas ölçü aletleriyle yapılan deneyler sonucunda suyun çok zayıf da olsa iletken olduğu tespit
ÇÖZELTİLERDE DENGE (AsitBaz) SUYUN OTOİYONİZASYONU Saf suyun elektrik akımını iletmediği bilinir, ancak çok hassas ölçü aletleriyle yapılan deneyler sonucunda suyun çok zayıf da olsa iletken olduğu tespit
Aşağıda verilen özet bilginin ayrıntısını, ders kitabı. olarak önerilen, Erdik ve Sarıkaya nın Temel. Üniversitesi Kimyası" Kitabı ndan okuyunuz.
 KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
KİMYASAL BAĞLAR Aşağıda verilen özet bilginin ayrıntısını, ders kitabı olarak önerilen, Erdik ve Sarıkaya nın Temel Üniversitesi Kimyası" Kitabı ndan okuyunuz. KİMYASAL BAĞLAR İki atom veya atom grubu
BİYOLOJİK MOLEKÜLLERDEKİ
 BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ
 KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
SU VE KİMYASAL BAĞLAR. Yrd. Doç. Dr. Osman İBİŞ
 SU VE KİMYASAL BAĞLAR Yrd. Doç. Dr. Osman İBİŞ Kimyasal Bağlar ve Çeşitleri Nelerdir? Kimyasal bağ, çekirdekteki atomları bir arada tutan kuvvettir. İki ya da daha fazla atom arasında elektron alışverişi
SU VE KİMYASAL BAĞLAR Yrd. Doç. Dr. Osman İBİŞ Kimyasal Bağlar ve Çeşitleri Nelerdir? Kimyasal bağ, çekirdekteki atomları bir arada tutan kuvvettir. İki ya da daha fazla atom arasında elektron alışverişi
BİTKİ BESLEME DERS NOTLARI
 BİTKİ BESLEME DERS NOTLARI Dr. Metin AYDIN KONYA 2011 BİTKİ BESİN ELEMENTLERİNİN GÖREVLERİ, ALINIŞ FORMLARI ve KAYNAKLARI Besin Elementi Bitkideki Görevi Alınış Formu Kaynakları Karbon (C) Karbonhidratların
BİTKİ BESLEME DERS NOTLARI Dr. Metin AYDIN KONYA 2011 BİTKİ BESİN ELEMENTLERİNİN GÖREVLERİ, ALINIŞ FORMLARI ve KAYNAKLARI Besin Elementi Bitkideki Görevi Alınış Formu Kaynakları Karbon (C) Karbonhidratların
Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem. Prof.Dr.Mitat KOZ
 Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem Prof.Dr.Mitat KOZ Mikrodolaşım? Besin maddelerinin dokulara taşınması ve hücresel atıkların uzaklaştırılması. Küçük arteriyoller her bir doku
Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem Prof.Dr.Mitat KOZ Mikrodolaşım? Besin maddelerinin dokulara taşınması ve hücresel atıkların uzaklaştırılması. Küçük arteriyoller her bir doku
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı
 Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
ELEMENT VE BİLEŞİKLER
 ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
BİLEŞİKLER VE FORMÜLLERİ
 BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER
 BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
BİYOKİMYAYA GİRİŞ: ATOM, MOLEKÜL, ORGANİK BİLEŞİKLER Biyokimyanın tanımı yaşamın temel kimyası ile ilgilenen bilim dalı (Bios, Yunancada yaşam demektir.) canlı sistemin yapısını ve fonksiyonlarını kimyasal
ASİD BAZ DENGESİ. Prof Dr Salim Çalışkan
 ASİD BAZ DENGESİ Prof Dr Salim Çalışkan H + ve ph Normal kan [H + ] 40 nmol/l Tampon mekanizmalar ile dar limitlerde tutulur (±5) ph = - log [H + ] = - log [40±5] = 7.40 ± 0.05 ph için kritik limitler
ASİD BAZ DENGESİ Prof Dr Salim Çalışkan H + ve ph Normal kan [H + ] 40 nmol/l Tampon mekanizmalar ile dar limitlerde tutulur (±5) ph = - log [H + ] = - log [40±5] = 7.40 ± 0.05 ph için kritik limitler
Örnek : 3- Bileşiklerin Özellikleri :
 Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI. Dr. Vedat Evren
 HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI Dr. Vedat Evren Vücuttaki Sıvı Kompartmanları Vücut sıvıları değişik kompartmanlarda dağılmış Vücuttaki Sıvı Kompartmanları Bu kompartmanlarda iyonlar ve diğer çözünmüş
HÜCRE MEMBRANINDAN MADDELERİN TAŞINMASI Dr. Vedat Evren Vücuttaki Sıvı Kompartmanları Vücut sıvıları değişik kompartmanlarda dağılmış Vücuttaki Sıvı Kompartmanları Bu kompartmanlarda iyonlar ve diğer çözünmüş
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM. o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ
 Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Serüveni 3. ÜNİTE KİMYASAL TÜRLER ARASI ETKİLEŞİM GÜÇLÜ ETKİLEŞİM o İYONİK BAĞ o KOVALENT BAĞ o METALİK BAĞ KİMYASAL TÜR 1. İYONİK BAĞ - - Ametal.- Kök Kök Kök (+) ve (-) yüklü iyonların çekim kuvvetidir..halde
Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler
 Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler Toprakta bulunan katı (mineral ve organik madde), sıvı (toprak çözeltisi ve bileşenleri) ve gaz fazları sürekli olarak etkileşim içerisindedir. Bunlar
Toprağın Katı ve Sıvı Fazı Arasındaki Etkileşimler Toprakta bulunan katı (mineral ve organik madde), sıvı (toprak çözeltisi ve bileşenleri) ve gaz fazları sürekli olarak etkileşim içerisindedir. Bunlar
Metabolizma ATP ATP 19/11/2015. BESLENME, METABOLİZMA ve TERMOREGULASYON. Enerji için Protein Kullanımı. Müge BULAKBAŞI Yüksek Hemşire
 Metabolizma BESLENME, METABOLİZMA ve TERMOREGULASYON Müge BULAKBAŞI Yüksek Hemşire Metabolizma : Hücrelerin yaşamını sürdürebilmeleri için gerekli kimyasal süreçlerin tümüne metabolizma denir. Metabolik
Metabolizma BESLENME, METABOLİZMA ve TERMOREGULASYON Müge BULAKBAŞI Yüksek Hemşire Metabolizma : Hücrelerin yaşamını sürdürebilmeleri için gerekli kimyasal süreçlerin tümüne metabolizma denir. Metabolik
ÇÖZÜNÜRLÜK DENGESİ (Kçç)
 ÇÖZÜNÜRLÜK DENGESİ (Kçç) ÇÖZELTİLERDE ÇÖZÜNME VE ÇÖKELME OLAYLARI Çözeltiler doymuşluklarına göre üçe ayrılırlar: 1- Doymamış çözeltiler: Belirli bir sıcaklıkta ve basınçta çözebileceğinden daha az miktarda
ÇÖZÜNÜRLÜK DENGESİ (Kçç) ÇÖZELTİLERDE ÇÖZÜNME VE ÇÖKELME OLAYLARI Çözeltiler doymuşluklarına göre üçe ayrılırlar: 1- Doymamış çözeltiler: Belirli bir sıcaklıkta ve basınçta çözebileceğinden daha az miktarda
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır:
 Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
Atomlar birleştiği zaman elektron dağılımındaki değişmelerin bir sonucu olarak kimyasal bağlar meydana gelir. Üç çeşit temel bağ vardır: İyonik bağlar, elektronlar bir atomdan diğerine aktarıldığı zaman
YAZILIYA HAZIRLIK TEST SORULARI. 11. Sınıf
 YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
Kan Gazı. Dr.Kenan Ahmet TÜRKDOĞAN Isparta Devlet Hastanesi. II. Isparta Acil Günleri Solunum Acilleri, 19 Ocak 2013 Isparta
 Kan Gazı Dr.Kenan Ahmet TÜRKDOĞAN Isparta Devlet Hastanesi II. Isparta Acil Günleri Solunum Acilleri, 19 Ocak 2013 Isparta Normal Değerler ph 7.35-7.45 (ort. 7.40) ph 7.35 ise Asidoz 7.45 ise Alkaloz ph
Kan Gazı Dr.Kenan Ahmet TÜRKDOĞAN Isparta Devlet Hastanesi II. Isparta Acil Günleri Solunum Acilleri, 19 Ocak 2013 Isparta Normal Değerler ph 7.35-7.45 (ort. 7.40) ph 7.35 ise Asidoz 7.45 ise Alkaloz ph
5.111 Ders Özeti #23 23.1
 5.111 Ders Özeti #23 23.1 Asit/Baz Dengeleri (Devam) Konu: Titrasyon Cuma günü ders notlarından Asidik tampon etkisi: Zayıf asit, HA, protonlarını ortamdaki kuvvetli bazın OH iyonlarına aktarır. Zayıf
5.111 Ders Özeti #23 23.1 Asit/Baz Dengeleri (Devam) Konu: Titrasyon Cuma günü ders notlarından Asidik tampon etkisi: Zayıf asit, HA, protonlarını ortamdaki kuvvetli bazın OH iyonlarına aktarır. Zayıf
ASİTLER- BAZLAR. Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur.
 ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir.
 Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
ASİTLER, BAZLAR ve TUZLAR
 ASİTLER, BAZLAR ve TUZLAR 1. ASİTLER Sulu çözeltilerine Hidrojen İyonu veren maddelere asit denir. Ör 1 HCl : Hidroklorik asit HCl H + + Cl - Ör 2 H 2 SO 4 : Sülfürik asit H 2 SO 4 2H + + SO 4-2 Ör 3 Nitrik
ASİTLER, BAZLAR ve TUZLAR 1. ASİTLER Sulu çözeltilerine Hidrojen İyonu veren maddelere asit denir. Ör 1 HCl : Hidroklorik asit HCl H + + Cl - Ör 2 H 2 SO 4 : Sülfürik asit H 2 SO 4 2H + + SO 4-2 Ör 3 Nitrik
Asit Baz Dengesi Hedefler
 KAN GAZI Hedefler asit-baz dengesini tanımlamakta kullanılan bazı temel terimler hangi bozukluğun mevcut olduğunu hızlıca belirleme uygun kompanzasyon var mı ayırıcı tanıyı yapmak Asit Baz Dengesi Tanımlar
KAN GAZI Hedefler asit-baz dengesini tanımlamakta kullanılan bazı temel terimler hangi bozukluğun mevcut olduğunu hızlıca belirleme uygun kompanzasyon var mı ayırıcı tanıyı yapmak Asit Baz Dengesi Tanımlar
ELEMENTLER VE BİLEŞİKLER
 ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA MOLEKÜLLER ARASI KUVVETLER Moleküller Arası Kuvvetler Yüksek basınç ve düşük sıcaklıklarda moleküller arası kuvvetler gazları ideallikten saptırır. Moleküller arası kuvvetler molekülde kalıcı
GENEL KİMYA MOLEKÜLLER ARASI KUVVETLER Moleküller Arası Kuvvetler Yüksek basınç ve düşük sıcaklıklarda moleküller arası kuvvetler gazları ideallikten saptırır. Moleküller arası kuvvetler molekülde kalıcı
Solunum, genel anlamda canlı organizmada gaz değişimini ifade etmek için kullanılır.
 SOLUNUM SİSTEMLERİ Solunum, genel anlamda canlı organizmada gaz değişimini ifade etmek için kullanılır. 1. Dış Solunum Solunum organlarıyla dış ortamdan hava alınması ve verilmesi, yani soluk alıp vermeye
SOLUNUM SİSTEMLERİ Solunum, genel anlamda canlı organizmada gaz değişimini ifade etmek için kullanılır. 1. Dış Solunum Solunum organlarıyla dış ortamdan hava alınması ve verilmesi, yani soluk alıp vermeye
TAMPON ÇÖZELTİLER-2. Prof.Dr.Mustafa DEMİR M.DEMİR(ADU) 12-TAMPON ÇÖZELTİLER-2 1
 TAMPON ÇÖZELTİLER-2 Prof.Dr.Mustafa DEMİR M.DEMİR(ADU) 12-TAMPON ÇÖZELTİLER-2 1 Tampon çözelti Tampon çözelti: Konjuge asit-baz çiftinin bulunduğu ve ph değişmelerine karşı direnç gösteren çözeltilere
TAMPON ÇÖZELTİLER-2 Prof.Dr.Mustafa DEMİR M.DEMİR(ADU) 12-TAMPON ÇÖZELTİLER-2 1 Tampon çözelti Tampon çözelti: Konjuge asit-baz çiftinin bulunduğu ve ph değişmelerine karşı direnç gösteren çözeltilere
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU
 13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
YAZILI SINAV CEVAP ANAHTARI BİYOLOJİ
 YAZILI SINAV CEVAP ANAHTARI BİYOLOJİ CEVAP 1: (TOPLAM 9 PUAN) 1.1: Eğer terleme ve su emilimi arasındaki ilişkide ortam sıcaklığının etkisini öğrenmek istiyorsa; deneyi aynı sayıda yaprağa sahip aynı tür
YAZILI SINAV CEVAP ANAHTARI BİYOLOJİ CEVAP 1: (TOPLAM 9 PUAN) 1.1: Eğer terleme ve su emilimi arasındaki ilişkide ortam sıcaklığının etkisini öğrenmek istiyorsa; deneyi aynı sayıda yaprağa sahip aynı tür
Kimyasal Toprak Sorunları ve Toprak Bozunumu-I
 Kimyasal Toprak Sorunları ve Toprak Bozunumu-I asitleşme-alkalileşme (tuzluluk-alkalilik) ve düşük toprak verimliliği Doç. Dr. Oğuz Can TURGAY ZTO321 Toprak İyileştirme Yöntemleri Toprak Kimyasal Özellikleri
Kimyasal Toprak Sorunları ve Toprak Bozunumu-I asitleşme-alkalileşme (tuzluluk-alkalilik) ve düşük toprak verimliliği Doç. Dr. Oğuz Can TURGAY ZTO321 Toprak İyileştirme Yöntemleri Toprak Kimyasal Özellikleri
Aktif ve pasif iyon alımı
 Aktif ve pasif iyon alımı Moleküllerin membranı geçerek taşınmaları için aktif proses her zaman gerekli değildir. Moleküllerin bir kısmı dış ortamdan membran içine konsantrasyon farkına bağlı olarak çok
Aktif ve pasif iyon alımı Moleküllerin membranı geçerek taşınmaları için aktif proses her zaman gerekli değildir. Moleküllerin bir kısmı dış ortamdan membran içine konsantrasyon farkına bağlı olarak çok
Sıvılardan ekstraksiyon:
 Sıvılardan ekstraksiyon: Sıvı haldeki bir karışımdan bir maddenin, bu maddenin içinde bulunduğu çözücü ile karışmayan ve bu maddeyi çözen bir başka çözücü ile çalkalanarak ilgili maddenin ikinci çözücüye
Sıvılardan ekstraksiyon: Sıvı haldeki bir karışımdan bir maddenin, bu maddenin içinde bulunduğu çözücü ile karışmayan ve bu maddeyi çözen bir başka çözücü ile çalkalanarak ilgili maddenin ikinci çözücüye
ENDÜSTRIDE VE CANLILARDA ENERJI. Canlılarda Enerji
 ENDÜSTRIDE VE CANLILARDA ENERJI Canlılarda Enerji Besinlerin Enerjiye Dönüşümü İnsanların gün boyunca hareketlerinin devamını, hastalanınca iyileşmelerini, fizyolojik ve psikolojik tepkilerinin devamlılığını
ENDÜSTRIDE VE CANLILARDA ENERJI Canlılarda Enerji Besinlerin Enerjiye Dönüşümü İnsanların gün boyunca hareketlerinin devamını, hastalanınca iyileşmelerini, fizyolojik ve psikolojik tepkilerinin devamlılığını
ÇÖZÜNME ve ÇÖZÜNÜRLÜK
 ÇÖZÜNME ve ÇÖZÜNÜRLÜK Prof. Dr. Mustafa DEMİR M.DEMİR 05-ÇÖZÜNME VE ÇÖZÜNÜRLÜK 1 Çözünme Olayı Analitik kimyada çözücü olarak genellikle su kullanılır. Su molekülleri, bir oksijen atomuna bağlı iki hidrojen
ÇÖZÜNME ve ÇÖZÜNÜRLÜK Prof. Dr. Mustafa DEMİR M.DEMİR 05-ÇÖZÜNME VE ÇÖZÜNÜRLÜK 1 Çözünme Olayı Analitik kimyada çözücü olarak genellikle su kullanılır. Su molekülleri, bir oksijen atomuna bağlı iki hidrojen
HÜCRE ZARINDA TAŞIMA PROF. DR. SERKAN YILMAZ
 HÜCRE ZARINDA TAŞIMA PROF. DR. SERKAN YILMAZ Hücre içi ve hücre dışı sıvılar bileşimleri yönünden oldukça farklıdır. Hücre içi sıvı intraselüler sıvı, hücre dışı sıvı ise ekstraselüler sıvı adını alır.
HÜCRE ZARINDA TAŞIMA PROF. DR. SERKAN YILMAZ Hücre içi ve hücre dışı sıvılar bileşimleri yönünden oldukça farklıdır. Hücre içi sıvı intraselüler sıvı, hücre dışı sıvı ise ekstraselüler sıvı adını alır.
MİNERALLER. Dr. Diyetisyen Hülya YARDIMCI
 MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
GENEL KİMYA. 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar
 GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
GENEL KİMYA 4. Konu: Kimyasal türler, Kimyasal türler arasındaki etkileşimler, Kimyasal Bağlar Kimyasal Türler Doğada bulunan bütün maddeler tanecikli yapıdadır. Maddenin özelliğini gösteren küçük yapı
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ
 ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
ÇÖZELTİLERİN KOLİGATİF ÖZELLİKLERİ Çözeltilerin sadece derişimine bağlı olarak değişen özelliklerine koligatif özellikler denir. Buhar basıncı düşmesi, Kaynama noktası yükselmesi, Donma noktası azalması
