DURAYLI İZOTOPLAR. Prof. Dr Miraç AKÇAY ınjeokimya (KTÜ) kitabından Yararlanılmıştır.
|
|
|
- Irmak Şen
- 7 yıl önce
- İzleme sayısı:
Transkript
1 DURAYLI İZOTOPLAR Prof. Dr Miraç AKÇAY ınjeokimya (KTÜ) kitabından Yararlanılmıştır.
2 Her hangi bir atom, çekirdeğinde bulunan proton ve nötron sayıları yardımıyla kolaylıkla tanımlanabilir. Proton sayısı (Z) elementlerin atom numarasını, nötron sayısı (N) ise nötron numarasını verir. Bir atom çekirdeğindeki proton ve nötronların toplam sayısı ise atomun kütle numarasını (A) ifade eder. Buna göre bir atom çekirdeğinin bileşimi A=Z+N Formülüyle ifade edilir. Elementlerin atom çekirdeklerinin tanımlanabilmesi açısından kolaylık sağlaması düşüncesiyle, periyodik tablolarda her elementin kütle numarası (A) ve atom numarası (yani) proton sayısı (Z) belirtilir. Kütle numarası üst indis olarak, atom numarası ise alt indis olarak yazılır. Böylece, O16/8 oksijen atomunun çekirdeğinde 8 proton bulunduğunu ve dolayısıyla nötr halde atom çekirdeği etrafında toplam 8 adet elektron olduğunu, çekirdekte toplam 16 tane proton ve nötron bulunduğunu gösterir
3 Doğada varlığı bilinen elementler, atom numarası (Z) Y ekseninde, nötron numarası (N) X ekseninde olacak tarzda bir X Y grafiğine yerleştirildiğinde, herhangi bir atom numarasına sahip olan bir elementin farklı nötron sayılarına sahip birkaç atomdan oluştuğu görülür
4 Bu şekilde, aynı atom numarasına sahip olan, fakat nötron sayıları farklı olan atomlar birbirlerinin izotopları olarak isimlendirilirler. Diğer bir deyişle, izotoplar, bir elementin proton sayısı aynı, fakat nötron sayısı farklı atomlarıdır. Bu nedenle izotoplar birbirlerine son derece benzer kimyasal özelliklere sahiptir. Sadece kütlelerinde farklılık söz konusudur.
5 Z N grafiğinde düşey olarak sıralanan ve nötron sayıları aynı, fakat proton sayıları farklı atomlar izoton (isotone) olarak adlandırılırlar. Yani izotonlar, farklı elementlerin atomlarına karşılık gelmektedir. Aynı diyagramda çapraz konumda bulunan ve kütle numaraları (A) aynı olan atomlar da izobar olarak adlandırılırlar. Bu tür atomların proton (Z) ve nötron (N) sayıları farklıdır.
6 Bu tanımlar arasında jeokimyasal olarak en önemli olan izotoplardır. Şu ana kadar evrende toplam 112 farklı elementin bulunduğu tespit edilmiş olmasına karşın, bu elementlere ait 1700 civarında farklı atom çekirdeğinin bulunduğu bilinmektedir. Bunlardan bir kısmı zamana bağlı olarak başka atom çekirdeklerine dönüşebilirler. Diğer bir deyişle bazı izotoplar yarılanma ömrü denen belirli bir zaman dilimi içinde radyoaktif olarak parçalanarak başka bir elementin bir izotopu haline dönüşebilirler. Örnek olarak 87 Rb'un 86 Sr'a dönüşmesi gibi. Bu tür izotoplar duraysız(radyojenikveya radyoaktif) izotoplar olarak adlandırılırlar ve kayaçların yaş tayinlerinde kullanılırlar. Buna karşın bazı izotoplar da zaman içinde başka İzotoplara dönüşmezler ki bu tür izotoplara da duraylı izotoplar denir.
7 Duraylı izotoplar, zamana bağlı olarak değişime uğramadıklarından, herhangi bir jeolojik olayıngelişiminde yol gösterici olarak kullanılabilirler. Örneğin, bir maden yatağının oluşması esnasında rol oynayan çözeltilerin ne tür bir kaynaktan geldiği, yani suyun magmatik mi, meteorik mi yoksa deniz suyu mu olduğu, bu tür duraylı izotoplar yardımıyla belirlenebilir. Bilinen bütün elementler arasında sadece 21 tanesi saftır, yani tek bir izotopu vardır.
8 Duraylı olan izotoplar bütün izotoplar arasında daha az bir oran tutar (260 duraylı izotop / 1700 duraysızizotop; Şekil 9.1). Buna göre izotopların duraylı olması bir istisnadır. Zira nötron sayısı proton sayısı diyagramında (Şekil 9.1) duraylı izotoplar diyagramın orta kesiminde yer almakta ve her iki taraflarından duraysız izotoplar tarafından çevrelenmektedirler. Yani, duraylı izotoplarda nötron ve proton sayıları yaklaşık eşittir (N/Z~1). Bu oran, proton sayısı 20 den az olan izotoplar için l iken, artan kütle numarası ile birlikte yaklaşık l,5'e kadar çıkabilir. Sadece ve e izotoplarında nötron sayısı proton sayısından azdır.
9 2. DURAYLI İZOTOPLARIN JEOKİMYADA KULLANIMI Doğada bilinen 271 adet duraylı izotoptan sadece birkaçı, jeolojik amaçlı olarak kullanılabilir. Bunlar atom numarası düşük olan, birden fazla duraylı izotopu olan ve kayaçlar içerisindeki bolluk dereceleri çok daha fazla olan elementlere ait izotoplardır: hidrojen, oksijen, karbon ve kükürt.
10 Bu elementlere (hidrojen, oksijen, karbon ve kükürt) ait izotopların bileşikleri içerisindeki bolluk dereceleri, değişik jeolojik, jeokimyasal ve coğrafik olaylara bağlı olarak sürekli değişim gösterir, yani farklılaşmaya uğrar. Bu nedenle, bu duraylı izotoplar maden yataklarının oluşumlarının yorumlanmasına dair yapılan çalışmaların ayrılmaz bir parçasıdır. Li, B ve Si de izotop farklılaşmasına uğrayan izotoplara sahiptir. Fakat bu elementler sadece belirli tür bileşikler içerisinde bulunduklarından (çok yaygın olmadıklarından) duraylı izotop çalışmalarında kullanılmazlar. Be, F, Na, Al ve P gibi bazı elementler de sadece tek duraylı izotopları olduğu için, yani herhangi bir izotop farklılaşması söz konusu olamayacağı için duraylı izotop çalışmalarında kullanılamazlar.
11 Ancak hiçbir jeolojik (maden jeolojik) çalışmada, bir şekilde (sistematik veya gelişigüzel olarak) araziden derlenmiş olan örneklerin tüm kayaç veya içerdikleri minerallerden bazıları üzerinde yapılacak izotop analizleri sonucunda elde edilecek olan sonuçların doğrudan yorumlanabilmesi mümkün değildir. Her izotop analiz sonucu ancak jeolojik verilerle birlikte ele alınırsa anlamlı olur. Duraylı izotop analizleri ile paralel gerçekleştirilmesi zaruri olan çalışmalar şunlardır: Örnek derleme aşamasında yapılması gereken jeolojik ve yapısal gözlemler (ölçümler), Maden yataklarında mineral birlikteliği ve dizinimi, Cevher ve gang mineralleri arasında birlikte (dengede) oluşmuş olan mineral çiftlerinin belirlenmesi, Cevher ve gang minerallerinin mikroprob analizleri ile mineral kimyalarının belirlenmesi, Cevher ve gang mineralleri üzerinde sıvı kapanım çalışmaları (homojenleşme sıcaklığı, tuzluluk, sıvı/gaz hacim ölçümü, gaz konsantrasyonu, kaynama belirtileri...), Cevher ve yan kayaç üzerinde ana ve iz element çalışmaları
12 Bu çalışmaların yapılmış olması durumunda, duraylı izotop analizleri sonucunda elde edilen sonuçlar şu noktalarda çalışmalara direkt katkı sağlayabilir (Ohmoto, 1986): Sıcaklık, basınç ve oluşum derinliği gibi cevherin oluşumuna ait fiziksel oluşum şartları (jeotermometre olarak), Cevher oluşturucu çözeliticinin kaynağı ve kütlesi, besleme sisteminin geometrisi ve hidrotermal faaliyetin toplam süresi gibi maden yataklarının ve sıcak su kaynaklarının hidrolojik özellikleri, Özellikle kükürt, karbon ve metaller gibi cevher oluşturan bileşenlerin kaynaklan ve cevher oluşturan çözeltinin kimyasal bileşimi, Çalışılan minerallere ait redoks durumu (oksijen potansiyeli), sülfat/sülfit oranı, metal/sülfit oranları, ph, CO 2 /CH 4 oranları, Metal ve kükürtün hidrotermal çözelti içinde taşınması ve cevher çökelimine ilişkin mekanizmalar, Cevher oluşturucu magmaların kökeni ve oluşum işlemleri Bu katkıların elde edilebilmesi için tek bir duraylı izotopun kullanılması yeterli değildir. Her ne kadar bütün duraylı izotoplar (H, O, C, S) bu katkılardan bir kısmını karşılayabilecek olsa da, her izotopun cevap verecek olduğu sorular ayrıdır ve bu nedenle cevap aranan soruya göre hangi tür izotop çalışmasının yapılacağına karar verilmelidir.
13 İzotop Farklılaşması Herhangi bir elemente ait izotopların (örneğin 16 O, 1S O; 32 S, 34 S), o elementi barındıran bileşikler içerisindeki (örneğin H 2 O; FeS 2 ) bolluk derecelerinin, değişik jeolojik, jeokimyasal, coğrafik, fiziksel ve kimyasal olaylar sonucunda değişim göstermesine izotop farklılaşması denir. H, C, O, S ve N gibi elementlerin izotoplarının, bileşikleri içerisindeki bolluk dereceleri kolaylıkla değişim gösterir (Çizelge 9.1). Buna karşın Li, B ve Si gibi elementlerin izotopları ise kolaylıkla farklılaşmazlar. İzotop farklılaşması, herhangi bir duraylı izotopun jeolojik ve jeokimyasal problemlerin çözümünde kullanılıp kullanılamayacağını denetleyen asıl etkendir. İzotop değişim reaksiyonları, duraylı izotop içeren moleküllerin reaksiyon hızlarındaki farklılıklardan kaynaklanan kinetik işlemler ve fızikokimyasal etkenler izotop farklılaşmasına neden olan başlıca faktörlerdir.
14 3. HİDROJEN İZOTOPLARI Litolojik birimler içerisinde bünyesinde H elementi barındıran mineraller (Özellikle sulu silikatlar) son derece boldur. Bunlara ilave olarak, hidrotermal çözeltilerin etkileri sonucunda oluşan alterasyon mineralleri arasında da bu tür mineraller bulunmaktadır. Örnek olarak, klorit ve serizit cevher kütleleri içerisinde ve yan kayaçlar içerisinde son derece yoğundur. Klorit, serizit, muskovit, serpantin ve talk, hidrojen izotop analizi için kullanılabilecek olan minerallerdir. Ayrıca, değişik mineraller içerisindeki sıvı kapanımlar da hidrojen İzotop analizleri için kullanılabilirler. Ancak hidrojen izotopu sadece bu minerallerin H izotop değerini ve sıvı kapanım içindeki suyun H izotop bileşimini belirlemek için kullanılır; jeotermometre olarak kullanılamaz. Zira, sulu silikatların (örneğin kaolen serizit) izotopik farklılaşma faktörleri sıcaklıktan bağımsızdır, minerallerin kimyasal bileşimlerine son derece duyarlıdır (örneğin biyotit) ve bir çok sulu silikat için iyi kalibre edilmemiştir. Sıvı ile mineraller arasında H değişiminin düşük sıcaklıklarda bile çok kolaylıkla gerçekleşebilmesi; dolayısıyla, maden yatakları bünyesinde oluşmuş olan sulu silikatların hidrojenizotopbileşiminin, sistem içerisinde daha sonra etkili olan çözeltiler tarafından kolaylıkla değiştirilebilmesi hidrojen izotopunun jeotermometre olarak kullanılmasını sınırlayan diğer bir etkendir (Çöle ve Ohmoto, 1984).
15 Hidrojen izotop bileşimi belirlenmek istenen OH iyonu içeren mineral veya mineralleri içinde bulundukları kayaçtan ayırmak gerekir. Bunun için, kayaç gereken tane boyutuna göre öğütüldükten sonra, gerek ağır sıvılar kullanarak (mineralleri yoğunluk farklarına göre birbirlerinden ayırarak), gerekse manyetik ayırıcılar kullanarak mineral ayırımı gerçekleştirilir. Ayrılan mineralin bünyesindeki OH iyonu, değişik kimyasal yöntemlerle su olarak mineralden alınır. Bazı durumlarda OH iyonu H 2 gazı olarak elde edilir (Savın ve Epstein, 1970) ki, bu durumda H 2 gazının bakır oksit ile reaksiyona sokularak H2o'ya çevrilmesi gerekir. Elde edilen su yaklaşık 750 C'de uranyum üzerinden geçirilerek, H 2 gazına çevrilir ve bu gaz, H ve D izotoplarının göreceli bolluklarını belirlemek için kütle spektrometresi yardımıyla analiz edilir.
16 Buna göre, sıvı ile bu mineraller arasındaki denge reaksiyonlarında, sıvı OH içeren silikatlı minerale nazaran D bakımından daha zenginleşir. Ayrıca, Mg ve Al bakımından zengin mineraller, Fe bakımından zengin minerallere göre, D bakımından daha zengindir. Bu nedenledir ki, muskovit kendisiyle dengede oluşan biyotite göre D bakımından daha zengin iken, dengede oluşmuş biyotit ve hornblend benzer D/H oranları ve benzer Mg/Fe oranları içerirler. Şekil 9.5'te de görüleceği gibi, H izotop farklılaşması yüksek sıcaklıklarda son derece büyük değerlere erişmektedir (örneğin 400 C'de muskovit dengede bulunduğu sıvıya nazaran D bakımından yaklaşık %o27 daha zenginleşmiştir). H izotop farklılaşma faktörleri düşük sıcaklıklara Savİnve Epstein (1970), Lawrence ve Taylor (1971) tarafından uyarlanmış olup, bu sıcaklıklarda farklılaşma çok daha az olmaktadır. Bu nedenle,
17 4. OKSİJEN İZOTOPLARI Oksijen doğada en bol bulunan elementtir. Gaz. sıvı ve katı bileşikler içerisinde bulunur. Bu tür oksijenli bileşikler çok geniş sıcaklık aralıklarında duraylı olduklarından oksijen, izotop jeokimyasında en kullanışlı elementlerden biridir. Oksijen elementinin 16 O, 17 O ve 18 O olmak üzere üç duraylı izotopu vardır. Doğadaki tüm oksijenin % 99,762'sini 16 O, % 0,038'ini 17 O ve % 0,2'sini ise 18 O oluşturur (Çizelge 9.1). İzotop analizlerinde, bu üç izotoptan, en bol bulunan 16 O ve 18 O izotopları kullanılır ve 18 O/ 16 O oranı ölçülür. Oksijen izotop analizleri, silikatlar, oksitler, karbonatlar ve sülfatlar ve ayrıca sıvı kapanımlar içerisindeki sıvının üzerinde yapılır
18
19
20
21 İzotopların tüm kimyasal özellikleri aynıdır ve aynı elemente aittirler (proton sayıları eşit). Bir elementin izotoplarının özellikleri de aynıdır. Sadece atom ağırlıkları farklıdır. Örneğin, Cl atomunun 17 protonu, 17 de elektronu bulunmaktadır. Ancak nötron sayısı ve buna bağlı olarak atom ağırlığı atomdan atoma değişmektedir. Normalde 1 Cl atomunun ağırlığı, A=17p +17n=34 olması gerekirken, nötron sayısının değişmesi sonucu, A 1 =17p+18n=35 veya A 2 =17p+20n=37 olabilmektedir. Bu nedenle elementlerin çoğu tam sayılı bir atom ağırlığı vermemekte ve izotop oranına göre ondalık kısım değişmektedir.
22 Doğada 300 e yakın duraylı (stabile) izotop bulunmaktadır. Bunlar jeolojik dönem içinde değişmezler. En çok duraylı izotopu olan element, Sezyumdur (Cs, 30 izotop). Teknetiyum (Tc, Z=43) ve Premesiyum (Pm, Z=61) gibi tek sayılı atom numarası olan bazı elementlerin hiç izotopu bulunmamaktadır. Bir atom büyüklüğü oranında duraysızdır. Tüm ağır elementlerin (Z>82) atomları duraylı hale gelmek, yani fazla yükünü atmak için, ışın yayarlar. Bunlara radyoaktif veya duraysız (instabile) izotop denir. Yayılan ışınların en önemlileri alfa, beta ve gama ışınlarıdır. Bu ışınların yayılmasiyla bir element zamanla, yani jeolojik süreçte, başka izotopa dönüşür. Bunun sonucu olarak miktarı da azalır. Bir radyoaktif izotopun miktarının yarısının değişimi için gereken süreye Yarılanma Süresi (t 1/2 )denir.
23 Örneğin, yarılanma süresi t 1/2 =14,3 gün olan 100 g P izotopu, 14,3 gün sonra 50 g'a, 28,6 gün sonra 25 g'a ve 42,9 gün sonra 12,5 g'a düşer. Radyoaktif etkinliklerle yayılan gama ışınları, röntgen ışını, olarak kullanılırlar. Alfa ve beta ışınlarıysa, Tracer element (iz sürücü element), yapay element ve nükleer enerji üretiminde ( 235 U 3,9.109 kj/g atom, en iyi kömür kj/t enerji verir) ve mutlak yaş tayininde kullanılırlar. Bunların yanında ortam (karasal/denizel, ısı derecesi) ve köken incelemelerinde duraylı izotoplardan yararlanılır.
24 Th-232 izotopunun yarılanması
Radyoaktif elementin tek başına bulunması, bileşik içinde bulunması, katı, sıvı, gaz, iyon halinde bulunması radyoaktif özelliğini etkilemez.
 RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
RADYOAKTİFLİK Kendiliğinden ışıma yapabilen maddelere radyoaktif maddeler denir. Radyoaktiflik çekirdek yapısıyla ilişkilidir. Radyoaktif bir atom hangi bileşiğin yapısına girerse o bileşiği radyoaktif
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER
 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOM ALTI TANECİKLER ATOM ALTI TANECİKLER: Atom numarası=proton sayısı=çekirdek yükü Kütle numarası (Nükleon sayısı)=proton sayısı+ nötron sayısı Kütle No iyon yükü Atom
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Serüveni 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOMUN BÖLÜNEBİLİRLİĞİ ATOM ALTI TANECİKLER
 Serüveni 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOMUN BÖLÜNEBİLİRLİĞİ ATOM ALTI TANECİKLER ATOMUN BÖLÜNEBİLİRLİĞİ: ATOM ALTI TANECİKLER SÜRTÜNME İLE ELEKTRİKLENME ELEKTROLİZ DENEYİ FARADAY SÜRTÜNME İLE ELEKTRİKLENME:
Serüveni 2.ÜNİTE:ATOM VE PERİYODİK SİSTEM ATOMUN BÖLÜNEBİLİRLİĞİ ATOM ALTI TANECİKLER ATOMUN BÖLÜNEBİLİRLİĞİ: ATOM ALTI TANECİKLER SÜRTÜNME İLE ELEKTRİKLENME ELEKTROLİZ DENEYİ FARADAY SÜRTÜNME İLE ELEKTRİKLENME:
Yrd. Doç. Dr. H. Hasan YOLCU. hasanyolcu.wordpress.com
 Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
Yrd. Doç. Dr. H. Hasan YOLCU hasanyolcu.wordpress.com En az iki atomun belli bir düzenlemeyle kimyasal bağ oluşturmak suretiyle bir araya gelmesidir. Aynı atomda olabilir farklı atomlarda olabilir. H 2,
proton sayısı Proton sayısı nötron sayısı izotop
 JEOKİMYA DERS 2 ATOM ÇEKİRDEĞİ Atomun merkezinde atomun büyüklüğüne oranla çok küçük pozitif yüklü bir çekirdek ve onun etrafında da elektronlar bulunmaktadır. Atom çekirdeğinde atom numarası kadar artı
JEOKİMYA DERS 2 ATOM ÇEKİRDEĞİ Atomun merkezinde atomun büyüklüğüne oranla çok küçük pozitif yüklü bir çekirdek ve onun etrafında da elektronlar bulunmaktadır. Atom çekirdeğinde atom numarası kadar artı
İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I
 İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I D) Elmas E) Oltu taşı 1. I. Civa II. Kil III. Kireç taşı Yukarıdaki maddelerden hangileri simyacılar tarafından kullanılmıştır? D) II ve III E) I, II
İSRAFİL ARSLAN KİM ÖĞR. YGS ÇALIŞMA KİMYA SORULARI I D) Elmas E) Oltu taşı 1. I. Civa II. Kil III. Kireç taşı Yukarıdaki maddelerden hangileri simyacılar tarafından kullanılmıştır? D) II ve III E) I, II
STOKİYOMETRİ. Kimyasal Tepkimelerde Kütle İlişkisi
 STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
Element atomlarının atom ve kütle numaraları element sembolleri üzerinde gösterilebilir. Element atom numarası sembolün sol alt köşesine yazılır.
 Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
Atom üç temel tanecikten oluşur. Bunlar proton, nötron ve elektrondur. Proton atomun çekirdeğinde bulunan pozitif yüklü taneciktir. Nötron atomun çekirdeğin bulunan yüksüz taneciktir. ise çekirdek etrafında
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN. Temel kavramlar Atomsal yapı
 Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Temel kavramlar Atomsal yapı İçerik Temel kavramlar Atom modeli Elektron düzeni Periyodik sistem 2 Temel kavramlar Bütün maddeler kimyasal elementlerden oluşur.
Malzeme Bilgisi Prof. Dr. Akgün ALSARAN Temel kavramlar Atomsal yapı İçerik Temel kavramlar Atom modeli Elektron düzeni Periyodik sistem 2 Temel kavramlar Bütün maddeler kimyasal elementlerden oluşur.
PERİYODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR
 PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
PERİODİK CETVEL-ÖSS DE ÇIKMIŞ SORULAR 1. Bir elementin periyodik cetveldeki yeri aşağıdakilerden hangisi ile belirlenir? A) Atom ağırlığı B) Değerliği C) Atom numarası D) Kimyasal özellikleri E) Fiziksel
MOL KAVRAMI I. ÖRNEK 2
 MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
5) Çözünürlük(Xg/100gsu)
 1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
1) I. Havanın sıvılaştırılması II. abrika bacasından çıkan SO 3 gazının H 2 O ile birleşmesi III. Na metalinin suda çözünmesi Yukardaki olaylardan hangilerinde kimyasal değişme gerçekleşir? 4) Kütle 1
ATOMUN YAPISI. Özhan ÇALIŞ. Bilgi İletişim ve Teknolojileri
 ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
ATOMUN YAPISI ATOMLAR Atom, elementlerin en küçük kimyasal yapıtaşıdır. Atom çekirdeği: genel olarak nükleon olarak adlandırılan proton ve nötronlardan meydana gelmiştir. Elektronlar: çekirdeğin etrafında
GENEL KİMYA. 6. Konu: Mol Kavramı ve Avagadro Sayısı
 GENEL KİMYA 6. Konu: Mol Kavramı ve Avagadro Sayısı Avagadro Sayısı ve Mol Kavramı Gündelik hayatta bazen maddeleri teker teker ifade etmek yerine toplu halde belirtmeyi tercih ederiz. Örneğin; 30 tane
GENEL KİMYA 6. Konu: Mol Kavramı ve Avagadro Sayısı Avagadro Sayısı ve Mol Kavramı Gündelik hayatta bazen maddeleri teker teker ifade etmek yerine toplu halde belirtmeyi tercih ederiz. Örneğin; 30 tane
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü
 KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 5 ATOM ÇEKİRDEĞİNİN
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 5 ATOM ÇEKİRDEĞİNİN
PERİYODİK CETVEL Mendeleev Henry Moseley Glenn Seaborg
 PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
PERİYODİK CETVEL Periyodik cetvel elementleri sınıflandırmak için hazırlanmıştır. İlkperiyodik cetvel Mendeleev tarafından yapılmıştır. Mendeleev elementleri artan kütle numaralarına göre sıralamış ve
Yrd.Doç.Dr. Emre YALAMAÇ. Yrd.Doç.Dr. Emre YALAMAÇ İÇERİK
 İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
İÇERİK Elementlere, Bileşiklere ve Karışımlara atomik boyutta bakış Dalton Atom Modeli Atom Fiziğinde Buluşlar - Elektronların Keşfi - Atom Çekirdeği Keşfi Günümüz Atom Modeli Kimyasal Elementler Periyodik
ATOM BİLGİSİ I ÖRNEK 1
 ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
ATOM BİLGİSİ I Elementlerin özelliklerini ta ıyan en küçük yapıta ı atomdur. Son çözümlemede, bütün maddelerin atomlar toplulu u oldu unu söyleyebiliriz. Elementler, aynı tür atomlardan, bile ik ve karı
STOKĐYOMETRĐ. Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK
 STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
VIA GRUBU ELEMENTLERİ
 Bölüm 8 VIA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. O, S, Se, Te, Po O ve S: Ametal Se ve Te: Yarı metal Po: Metal *Oksijen genellikle bileşiklerinde
Bölüm 8 VIA GRUBU ELEMENTLERİ Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler derste verilecektir. O, S, Se, Te, Po O ve S: Ametal Se ve Te: Yarı metal Po: Metal *Oksijen genellikle bileşiklerinde
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
Hayat Kurtaran Radyasyon
 Hayat Kurtaran Radyasyon GÜNLÜK HAYAT KONUSU: Kanser tedavisinde kullanılan radyoterapi KĐMYA ĐLE ĐLĐŞKĐSĐ: Radyoterapi bazı maddelerin radyoaktif özellikleri dolayısıyla ışımalar yapması esasına dayanan
Hayat Kurtaran Radyasyon GÜNLÜK HAYAT KONUSU: Kanser tedavisinde kullanılan radyoterapi KĐMYA ĐLE ĐLĐŞKĐSĐ: Radyoterapi bazı maddelerin radyoaktif özellikleri dolayısıyla ışımalar yapması esasına dayanan
ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur.
 DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
DERS: KİMYA KONU : ATOM YAPISI ATOM NEDİR? -Atom elementin özelliğini taşıyan en küçük parçasına denir. Her canlı-cansız madde atomdan oluşmuştur. Atom Modelleri Dalton Bütün maddeler atomlardan yapılmıştır.
Kimyanın Temel Kanunları
 Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Periyodik Tablo. Elementleri artan atom numaralarına ve tekrar eden fiziksel kimyasal özelliklerine göre sınıflandırır.
 Periyodik Tablo Elementleri artan atom numaralarına ve tekrar eden fiziksel kimyasal özelliklerine göre sınıflandırır. 1828 Berzelius elementleri sembolize etmek için harfleri kullandı. 1829 Döbereiner
Periyodik Tablo Elementleri artan atom numaralarına ve tekrar eden fiziksel kimyasal özelliklerine göre sınıflandırır. 1828 Berzelius elementleri sembolize etmek için harfleri kullandı. 1829 Döbereiner
1. Hafta. İzotop : Proton sayısı aynı nötron sayısı farklı olan çekirdeklere izotop denir. ÖRNEK = oksijenin izotoplarıdır.
 1. Hafta 1) GİRİŞ veya A : Çekirdeğin Kütle Numarası (Nükleer kütle ile temel kütle birimi arasıdaki orana en yakın bir tamsayı) A > Z Z: Atom Numarası (Protonların sayısı ) N : Nötronların Sayısı A =
1. Hafta 1) GİRİŞ veya A : Çekirdeğin Kütle Numarası (Nükleer kütle ile temel kütle birimi arasıdaki orana en yakın bir tamsayı) A > Z Z: Atom Numarası (Protonların sayısı ) N : Nötronların Sayısı A =
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla
 ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
ATOM ve YAPISI Maddelerin gözle görülmeyen (bölünmeyen) en parçasına atom denir. Atom kendinden başka hiçbir fiziksel ya da kimyasal metotlarla kendinden farklı atomlara dönüşemezler. Atomda (+) yüklü
ATOM BİLGİSİ Atom Modelleri
 1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
1. Atom Modelleri BÖLÜM2 Maddenin atom adı verilen bir takım taneciklerden oluştuğu fikri çok eskiye dayanmaktadır. Ancak, bilimsel bir (deneye dayalı) atom modeli ilk defa Dalton tarafından ileri sürülmüştür.
BİLEŞİKLER VE FORMÜLLERİ
 BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
BİLEŞİKLER VE FORMÜLLERİ Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur). Bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere
KİMYASAL BİLEŞİKLER İÇERİK
 KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
TY T Temel Yeterlilik Testi
 Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.
 ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
ATOM ve YAPISI Elementin özelliğini taşıyan en küçük parçasına denir. Atom Numarası Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı
 Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani madde yani bileşik
Örnek : 3- Bileşiklerin Özellikleri :
 Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
MADDENİN SINIFLANDIRILMASI
 MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR. Aytekin Hitit
 ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
ATOMİK YAPI VE ATOMLAR ARASI BAĞLAR Aytekin Hitit Malzemeler neden farklı özellikler gösterirler? Özellikler Fiziksel Kimyasal Bahsi geçen yapısal etkenlerden elektron düzeni değiştirilemez. Ancak diğer
K MYA ATOM VE PER YOD K CETVEL. Kavram Dersaneleri 10 ÖRNEK 1 :
 K MYA ATOM VE PER YOD K CETVEL ÖRNEK 1 : Bir elementin 60 X +2 iyonunda 25 elektron vard r. Ayn elementin, 58 X izotopunun atomundaki proton (p), nötron (n) ve elektron (e) say lar kaçt r? ÖRNEK 2: Bir
K MYA ATOM VE PER YOD K CETVEL ÖRNEK 1 : Bir elementin 60 X +2 iyonunda 25 elektron vard r. Ayn elementin, 58 X izotopunun atomundaki proton (p), nötron (n) ve elektron (e) say lar kaçt r? ÖRNEK 2: Bir
Bazı atomlarda proton sayısı aynı olduğu halde nötron sayısı değişiktir. Bunlara izotop denir. Şekil II.1. Bir atomun parçaları
 8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
8 II. MİNERALLER II.1. Element ve Atom Elementlerin en ufak parçasına atom denir. Atomlar, proton, nötron ve elektron gibi taneciklerden oluşur (Şekil II.1). Elektron negatif, proton pozitif elektrik yüküne
RADYONÜKLİTLERİN KİMYASI VE ANALİZİ
 RADYONÜKLİTLERİN KİMYASI VE ANALİZİ 6. ALKALİ TOPRAK METALLERİN RADYOKİMYASI Doç. Dr. Gaye Çakal ALKALİ TOPRAK METALLERİN RADYOKİMYASI 1. ALKALİ TOPRAK METALLERİN EN ÖNEMLİ RADYONÜKLİTLERİ 2. ALKALİ TOPRAK
RADYONÜKLİTLERİN KİMYASI VE ANALİZİ 6. ALKALİ TOPRAK METALLERİN RADYOKİMYASI Doç. Dr. Gaye Çakal ALKALİ TOPRAK METALLERİN RADYOKİMYASI 1. ALKALİ TOPRAK METALLERİN EN ÖNEMLİ RADYONÜKLİTLERİ 2. ALKALİ TOPRAK
3- KİMYASAL ELEMENTLER VE FONKSİYONLARI
 3- KİMYASAL ELEMENTLER VE FONKSİYONLARI Doğada 103 elementin olduğu bilinmektedir. Bunlardan 84 metal elementlerdir. Metal elementler toksik olan ve toksik olmayan elementler olarak ikiye ayrılmaktadır.
3- KİMYASAL ELEMENTLER VE FONKSİYONLARI Doğada 103 elementin olduğu bilinmektedir. Bunlardan 84 metal elementlerdir. Metal elementler toksik olan ve toksik olmayan elementler olarak ikiye ayrılmaktadır.
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
ATOMİK YAPI Atom, birkaç türü birleştiğinde çeşitli molekülleri, bir tek türü ise bir kimyasal öğeyi oluşturan parçacıktır. Atom, elementlerin özelliklerini taşıyan en küçük yapı birimi olup çekirdekteki
Giriş. Radyoaktivite bir atomun, ve ışınları yayarak başka bir elementin atomuna dönüşmesi olayıdır.
 Giriş Radyoaktivite bir atomun, ve ışınları yayarak başka bir elementin atomuna dönüşmesi olayıdır. Bu özellikteki elementlere radyoaktif element denir. Doğada bulunan kayaçlar farklı oranlarda radyoaktif
Giriş Radyoaktivite bir atomun, ve ışınları yayarak başka bir elementin atomuna dönüşmesi olayıdır. Bu özellikteki elementlere radyoaktif element denir. Doğada bulunan kayaçlar farklı oranlarda radyoaktif
Fen ve Teknoloji 8. 1 e - Ca +2 F -1 CaF 2. 1e - Mg +2 Cl -1. MgCl 2. Bileşik formülü bulunurken; Verilen elementlerin e- dizilimleri
 KİMYASAL TEPKİMELER Anahtar Kavramlar Kimyasal Tepkime Kimyasal Denklem Yanma Tepkimesi KAZANIM 3.1 Yükü bilinen iyonların oluşturduğu bileşiklerin formüllerini yazar. *Mg ve Cl atomlarının oluşturacağı
KİMYASAL TEPKİMELER Anahtar Kavramlar Kimyasal Tepkime Kimyasal Denklem Yanma Tepkimesi KAZANIM 3.1 Yükü bilinen iyonların oluşturduğu bileşiklerin formüllerini yazar. *Mg ve Cl atomlarının oluşturacağı
1 mol = 6, tane tanecik. Maddelerde tanecik olarak atom, molekül ve iyonlar olduğunda dolayı mol ü aşağıdaki şekillerde tanımlamak mümkündür.
 1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
GENEL KİMYA. 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar
 GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü
 KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 2 KİMYASAL HESAPLAMALAR
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 2 KİMYASAL HESAPLAMALAR
ATOMİK YAPI. Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0
 ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
ATOMİK YAPI Elektron Yükü=-1,60x10-19 C Proton Yükü=+1,60x10-19 C Nötron Yükü=0 Elektron Kütlesi 9,11x10-31 kg Proton Kütlesi Nötron Kütlesi 1,67x10-27 kg Bir kimyasal elementin atom numarası (Z) çekirdeğindeki
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü
 KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. HAFTALARA GÖRE KONU
KİM-117 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. HAFTALARA GÖRE KONU
maddelere saf maddeler denir
 Madde :Kütlesi olan her şeye madde denir. Saf madde: Aynı cins atom veya moleküllerden oluşan maddeye denir. Fiziksel yollarla kendisinden başka maddelere ayrışmayan maddelere saf maddeler denir Element:
Madde :Kütlesi olan her şeye madde denir. Saf madde: Aynı cins atom veya moleküllerden oluşan maddeye denir. Fiziksel yollarla kendisinden başka maddelere ayrışmayan maddelere saf maddeler denir Element:
ATOMUN YAPISI ATOMUN ÖZELLİKLERİ
 ATOM Elementlerin özelliğini taşıyan, en küçük yapı taşına, atom diyoruz. veya, fiziksel ve kimyasal yöntemlerle daha basit birimlerine ayrıştırılamayan, maddenin en küçük birimine atom denir. Helyum un
ATOM Elementlerin özelliğini taşıyan, en küçük yapı taşına, atom diyoruz. veya, fiziksel ve kimyasal yöntemlerle daha basit birimlerine ayrıştırılamayan, maddenin en küçük birimine atom denir. Helyum un
HİDROJEOLOJİ. Su Kimyasının Önemi
 HİDROJEOLOJİ 9.Hafta Su Kimyası Prof.Dr.N.Nur ÖZYURT nozyurt@hacettepe.edu.tr Su Kimyasının Önemi Yüzey ve yeraltısuları farklı oranlarda çözünmüş ve askıda maddeler içerirler. Suyun kimyasal bileşimi
HİDROJEOLOJİ 9.Hafta Su Kimyası Prof.Dr.N.Nur ÖZYURT nozyurt@hacettepe.edu.tr Su Kimyasının Önemi Yüzey ve yeraltısuları farklı oranlarda çözünmüş ve askıda maddeler içerirler. Suyun kimyasal bileşimi
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA
 İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek bir madde
İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR
 KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
KARIŞIMLAR İKİ YADA DAHA FAZLA MADDENİN ÖZELLİKLERİNİ KAYBETMEDEN ÇEŞİTLİ ORANLARDA KARIŞMASI İLE OLUŞAN TOPLULUĞA KARIŞIM DENİR KARIŞIMLAR İKİ SINIFTA İNCELENİR Her tarafında aynı özelliği gösteren, tek
HİDROJEOLOJİ. Su Kimyası. 9.Hafta. Prof.Dr.N.Nur ÖZYURT
 HİDROJEOLOJİ 9.Hafta Su Kimyası Prof.Dr.N.Nur ÖZYURT nozyurt@hacettepe.edu.tr Su Kimyasının Önemi Yüzey ve yeraltısuları farklı oranlarda çözünmüş ve askıda maddeler içerirler. Suyun kimyasal bileşimi
HİDROJEOLOJİ 9.Hafta Su Kimyası Prof.Dr.N.Nur ÖZYURT nozyurt@hacettepe.edu.tr Su Kimyasının Önemi Yüzey ve yeraltısuları farklı oranlarda çözünmüş ve askıda maddeler içerirler. Suyun kimyasal bileşimi
BİYOLOJİK MOLEKÜLLERDEKİ
 BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
BİYOLOJİK MOLEKÜLLERDEKİ KİMYASALBAĞLAR BAĞLAR KİMYASAL VE HÜCRESEL REAKSİYONLAR Yrd. Doç.Dr. Funda BULMUŞ Atomun Yapısı Maddenin en küçük yapı taşı olan atom elektron, proton ve nötrondan oluşmuştur.
Burada a, b, c ve d katsayılar olup genelde birer tamsayıdır. Benzer şekilde 25 o C de hidrojen ve oksijen gazlarından suyun oluşumu; H 2 O (s)
 1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
Sıcaklık (Temperature):
 Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar.
 Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
şeklinde, katı ( ) fazın ağırlık oranı ise; şeklinde hesaplanır.
 FAZ DİYAGRAMLARI Malzeme özellikleri görmüş oldukları termomekanik işlemlerin sonucunda oluşan içyapılarına bağlıdır. Faz diyagramları mühendislerin içyapı değişikliği için uygulayacakları ısıl işlemin
FAZ DİYAGRAMLARI Malzeme özellikleri görmüş oldukları termomekanik işlemlerin sonucunda oluşan içyapılarına bağlıdır. Faz diyagramları mühendislerin içyapı değişikliği için uygulayacakları ısıl işlemin
ELEMETLER VE BİLEŞİKLER ELEMENTLER VE SEMBOLLERİ
 ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
CANLILARIN KİMYASAL İÇERİĞİ
 CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
CANLILARIN KİMYASAL İÇERİĞİ Prof. Dr. Bektaş TEPE Canlıların Savunma Amaçlı Kimyasal Üretimi 2 Bu ünite ile; Canlılık öğretisinde kullanılan kimyasal kavramlar Hiyerarşi düzeyi Hiyerarşiden sorumlu atom
Bölüm 4, Ders 2: Periyodik Tablo
 Büyük Fikirler Basit Fikirlerdir Bölüm 4, Ders 2: Periyodik Tablo Temel Kavramlar Periyodik tablo tüm maddeleri oluşturan atomlar hakkında bilgi içeren bir tablodur. Element tek cins atomlardan oluşan
Büyük Fikirler Basit Fikirlerdir Bölüm 4, Ders 2: Periyodik Tablo Temel Kavramlar Periyodik tablo tüm maddeleri oluşturan atomlar hakkında bilgi içeren bir tablodur. Element tek cins atomlardan oluşan
2. HAMLE web:
 2. HAMLE Nötron sayısı İZOTOP ATOM 1-Proton sayıları... nötron ve kütle numaraları.. atomlardır. 2-İzotop atomların fiziksel özellikleri. 3-Nötr izotop atomlar kimyasal özellikleri. 4-İzotop atomlar aynı
2. HAMLE Nötron sayısı İZOTOP ATOM 1-Proton sayıları... nötron ve kütle numaraları.. atomlardır. 2-İzotop atomların fiziksel özellikleri. 3-Nötr izotop atomlar kimyasal özellikleri. 4-İzotop atomlar aynı
ELEMENT VE BİLEŞİKLER
 ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
KONU ANLATIMLI ÇALIŞMA YAPRAĞI
 KONU ANLATIMLI ÇALIŞMA YAPRAĞI PERĐYODĐK CETVEL 1) Periyodik cetvel elementlerin artan atom numaralarına göre dizilimini gösteren bir tablodur.bu tabloda belli kimyasal özellikleri birbirine yakın olan
KONU ANLATIMLI ÇALIŞMA YAPRAĞI PERĐYODĐK CETVEL 1) Periyodik cetvel elementlerin artan atom numaralarına göre dizilimini gösteren bir tablodur.bu tabloda belli kimyasal özellikleri birbirine yakın olan
www.ilketkinlik.com www.ilketkinlik.com/blog www.muzikkitabisarkilari.com www.ingilizcedefteri.com Online Test www.ilketkinlik.com/sinavilketkinlikte
 www.ilketkinlik.com www.ilketkinlik.com/blog www.muzikkitabisarkilari.com www.ingilizcedefteri.com Online Test www.ilketkinlik.com/sinavilketkinlikte atomu ile ilgili şu bilgiler veriliyor; Kütle numarası
www.ilketkinlik.com www.ilketkinlik.com/blog www.muzikkitabisarkilari.com www.ingilizcedefteri.com Online Test www.ilketkinlik.com/sinavilketkinlikte atomu ile ilgili şu bilgiler veriliyor; Kütle numarası
ELEMENTLERİN SEMBOLLERİ VE ATOM
 ELEMENT VE SEMBOLLERİ SAF MADDE: Kendisinden başka madde bulundurmayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran maddelere denir. Yani elementlerin yapı yaşı atomlardır. BİLEŞİK: En
ELEMENT VE SEMBOLLERİ SAF MADDE: Kendisinden başka madde bulundurmayan maddelere denir. ELEMENT: İçerisinde tek cins atom bulunduran maddelere denir. Yani elementlerin yapı yaşı atomlardır. BİLEŞİK: En
PERİYODİK CETVEL
 BÖLÜM4 W Periyodik cetvel, elementlerin atom numaraları esas alınarak düzenlenmiştir. Bu düzenlemede, kimyasal özellikleri benzer olan (değerlik elektron sayıları aynı) elementler aynı düşey sütunda yer
BÖLÜM4 W Periyodik cetvel, elementlerin atom numaraları esas alınarak düzenlenmiştir. Bu düzenlemede, kimyasal özellikleri benzer olan (değerlik elektron sayıları aynı) elementler aynı düşey sütunda yer
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar.
 Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
Elementlerin büyük bir kısmı tabiatta saf hâlde bulunmaz. Çoğunlukla başka elementlerle bileşikler oluşturmuş şekilde bulunurlar. Elementlerin bileşik oluşturma istekleri onların kararlı yapıya ulaşma
TEMEL KĐMYA YASALARI A. KÜTLENĐN KORUNUMU YASASI (LAVOISIER YASASI)
 TEMEL KĐMYA YASALARI A. KÜTLENĐN KORUNUMU YASASI (LAVOISIER YASASI) Kimyasal olaylara giren maddelerin kütleleri toplamı oluşan ürünlerin toplamına eşittir. Buna göre: X + Y Z + T tepkimesinde X ve Y girenler
TEMEL KĐMYA YASALARI A. KÜTLENĐN KORUNUMU YASASI (LAVOISIER YASASI) Kimyasal olaylara giren maddelerin kütleleri toplamı oluşan ürünlerin toplamına eşittir. Buna göre: X + Y Z + T tepkimesinde X ve Y girenler
Faz ( denge) diyagramları
 Faz ( denge) diyagramları İki elementin birbirleriyle karıştırılması sonucunda, toplam iç enerji mimimum olacak şekilde yeni atom düzenleri meydana gelir. Fazlar, İç enerjinin minimum olmasını sağlayacak
Faz ( denge) diyagramları İki elementin birbirleriyle karıştırılması sonucunda, toplam iç enerji mimimum olacak şekilde yeni atom düzenleri meydana gelir. Fazlar, İç enerjinin minimum olmasını sağlayacak
İçerdikleri 87Rb ve 87Sr, 86Sr miktarına göre kayaçların ve minerallerin i yaşlarının tespiti Rubidyum Stronsiyum izotop sisteminin kullanımının
 Rubidyum Stronsiyum yaş tayini Radyometrik yaş tayini tekniği İçerdikleri 87Rb ve 87Sr, 86Sr miktarına göre kayaçların ve minerallerin i yaşlarının tespiti Rubidyum Stronsiyum izotop sisteminin kullanımının
Rubidyum Stronsiyum yaş tayini Radyometrik yaş tayini tekniği İçerdikleri 87Rb ve 87Sr, 86Sr miktarına göre kayaçların ve minerallerin i yaşlarının tespiti Rubidyum Stronsiyum izotop sisteminin kullanımının
ELEMENTLER VE BİLEŞİKLER
 ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENTLER VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri a) ELEMENTLER Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
MADDE VE ÖZELLİKLERİ. Kimya Konu Tarama Testi-2
 MADDE VE ÖZELLİKLERİ Kimya Konu Tarama Testi-2 SORU 1: I. Renk, koku, tat ve uçuculuk tüm maddelerin ortak özelliğidir. II. Özkütle, esneklik katsayısı ve kaynama noktası tüm maddelerin ayırt edici özelliğidir.
MADDE VE ÖZELLİKLERİ Kimya Konu Tarama Testi-2 SORU 1: I. Renk, koku, tat ve uçuculuk tüm maddelerin ortak özelliğidir. II. Özkütle, esneklik katsayısı ve kaynama noktası tüm maddelerin ayırt edici özelliğidir.
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir.
 MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
MADDE NEDİR? Çevremize baktığımızda gördüğümüz her şey örneğin, dağlar, denizler, ağaçlar, bitkiler, hayvanlar ve hava birer maddedir. Her maddenin bir kütlesi vardır ve bu tartılarak bulunur. Ayrıca her
Elektrot Potansiyeli. (k) (k) (k) Tepkime vermez
 Elektrot Potansiyeli Uzun metal parçası, M, elektrokimyasal çalışmalarda kullanıldığında elektrot adını alır. M n+ metal iyonları içeren bir çözeltiye daldırılan bir elektrot bir yarı-hücre oluşturur.
Elektrot Potansiyeli Uzun metal parçası, M, elektrokimyasal çalışmalarda kullanıldığında elektrot adını alır. M n+ metal iyonları içeren bir çözeltiye daldırılan bir elektrot bir yarı-hücre oluşturur.
NELER KAZANACAĞIZ?
 NELER KAZANACAĞIZ? Mendeleyev in periyodik sistem üzerine yaptığı çalışmaları ve Moseley in katkılarını, Atomların katman-elektron dağılımlarıyla periyodik sistemdeki yerleri arasındaki ilişkiyi (İlk 20
NELER KAZANACAĞIZ? Mendeleyev in periyodik sistem üzerine yaptığı çalışmaları ve Moseley in katkılarını, Atomların katman-elektron dağılımlarıyla periyodik sistemdeki yerleri arasındaki ilişkiyi (İlk 20
A- LABORATUAR MALZEMELERİ
 1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
1- Cam Aktarma ve Ölçüm Kapları: DENEY 1 A- LABORATUAR MALZEMELERİ 2- Porselen Malzemeler 3- Metal Malzemeler B- KARIŞIMLAR - BİLEŞİKLER Nitel Gözlemler, Faz Ayırımları, Isısal Bozunma AMAÇ: Karışım ve
GENEL KĐMYA I. Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK
 GENEL KĐMYA I Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK GENEL KĐMYA 1 Đlkeler ve Modern Uygulamalar Petrucci Harwood - Herring Çeviri Editörleri Tahsin Uyar - Serpil Aksoy MODERN ÜNĐVERSĐTE KĐMYASI C.E.MORTIMER
GENEL KĐMYA I Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK GENEL KĐMYA 1 Đlkeler ve Modern Uygulamalar Petrucci Harwood - Herring Çeviri Editörleri Tahsin Uyar - Serpil Aksoy MODERN ÜNĐVERSĐTE KĐMYASI C.E.MORTIMER
Nötronlar kinetik enerjilerine göre aşağıdaki gibi sınıflandırılırlar
 Nötronlar kinetik enerjilerine göre aşağıdaki gibi sınıflandırılırlar Termal nötronlar (0.025 ev) Orta enerjili nötronlar (0.5-10 kev) Hızlı nötronlar (10 kev-10 MeV) Çok hızlı nötronlar (10 MeV in üzerinde)
Nötronlar kinetik enerjilerine göre aşağıdaki gibi sınıflandırılırlar Termal nötronlar (0.025 ev) Orta enerjili nötronlar (0.5-10 kev) Hızlı nötronlar (10 kev-10 MeV) Çok hızlı nötronlar (10 MeV in üzerinde)
Hidroklorik asit ve sodyum hidroksitin reaksiyonundan yemek tuzu ve su meydana gelir. Bu kimyasal olayın denklemi
 KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
KİMYASAL DENKLEMLER İki ya da daha fazla maddenin birbirleri ile etkileşerek kendi özelliklerini kaybedip yeni özelliklerde bir takım ürünler meydana getirmesine kimyasal olay, bunların formüllerle gösterilmesine
12-B. 31. I. 4p II. 5d III. 6s
 -B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
-B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
ATOM ATOMUN YAPISI 7. S I N I F S U N U M U. Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir.
 ATO YAP Atomu oluşturan parçacıklar farklı yüklere sahiptir Atomda bulunan yükler; negatif yükler ve pozitif yüklerdir Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir Atomu oluşturan
ATO YAP Atomu oluşturan parçacıklar farklı yüklere sahiptir Atomda bulunan yükler; negatif yükler ve pozitif yüklerdir Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir Atomu oluşturan
ÖN SÖZ. Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik
 ÖN SÖZ Sevgili Öğrenciler, Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik Testi Kimya Soru Bankası kitabımızı sizlere sunmaktan onur duyuyoruz. Başarınıza
ÖN SÖZ Sevgili Öğrenciler, Üniversiteye hazırlık yolunda, yeni sınav sistemine uygun olarak hazırladığımız YKS Alan Yeterlilik Testi Kimya Soru Bankası kitabımızı sizlere sunmaktan onur duyuyoruz. Başarınıza
PERİYODİK CETVEL. Yanıt : D. www.kimyahocam.com. 3 Li : 1s2 2s 1 2. periyot 1A grubu. 16 S : 1s2 2s 2 2p 6 3s 2 3p 4 3.
 PERİODİK CETVEL Periyodik cetvel, elementlerin atom numaraları temel alınarak düzenlenmiş bir sistemdir. Periyodik cetvelde, nötr atomlarının elektron içeren temel enerji düzeyi sayısı aynı olan elementler
PERİODİK CETVEL Periyodik cetvel, elementlerin atom numaraları temel alınarak düzenlenmiş bir sistemdir. Periyodik cetvelde, nötr atomlarının elektron içeren temel enerji düzeyi sayısı aynı olan elementler
İmal Usulleri. Döküm Tekniği
 İmal Usulleri Döküm Tekniği Örnek Heterojen Çekirdeklenme Alışılmamış laboratuar deneyleri dışında, sıvı metal için homojen çekirdeklenme asla olmaz. Uygulamadaki sıvı metallerin içinde hemen her zaman
İmal Usulleri Döküm Tekniği Örnek Heterojen Çekirdeklenme Alışılmamış laboratuar deneyleri dışında, sıvı metal için homojen çekirdeklenme asla olmaz. Uygulamadaki sıvı metallerin içinde hemen her zaman
Bileşikteki atomların cinsini ve oranını belirten formüldür. Kaba formül ile bileşiğin molekül ağırlığı hesaplanamaz.
 BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
1. ATOMLA İLGİLİ DÜŞÜNCELER
 1. ATOMLA İLGİLİ DÜŞÜNCELER Democritus Maddenin tanecikli yapıda olduğunu ileri sürmüş ve maddenin bölünemeyen en küçük parçasına da atom (Yunanca a-tomos, bölünemez ) adını vermiştir Lavoisier Gerçekleştirdiği
1. ATOMLA İLGİLİ DÜŞÜNCELER Democritus Maddenin tanecikli yapıda olduğunu ileri sürmüş ve maddenin bölünemeyen en küçük parçasına da atom (Yunanca a-tomos, bölünemez ) adını vermiştir Lavoisier Gerçekleştirdiği
en.wikipedia.org Prof.Dr. Atike NAZİK, Çukurova Üniversitesi
 METAMORFİZMA VE METAMORFİK KAYAÇLAR I en.wikipedia.org Prof.Dr. Atike NAZİK, Çukurova Üniversitesi KAYAÇ DÖNGÜSÜ VE METAMORFİK KAYAÇLAR METAMORFİZMA Metamorfizma; Yunanca değişme anlamına gelen meta ve
METAMORFİZMA VE METAMORFİK KAYAÇLAR I en.wikipedia.org Prof.Dr. Atike NAZİK, Çukurova Üniversitesi KAYAÇ DÖNGÜSÜ VE METAMORFİK KAYAÇLAR METAMORFİZMA Metamorfizma; Yunanca değişme anlamına gelen meta ve
2- Bileşim 3- Güneş İç Yapısı a) Çekirdek
 GÜNEŞ 1- Büyüklük Güneş, güneş sisteminin en uzak ve en büyük yıldızıdır. Dünya ya uzaklığı yaklaşık 150 milyon kilometre, çapı ise 1.392.000 kilometredir. Bu çap, Yeryüzünün 109 katı, Jüpiter in de 10
GÜNEŞ 1- Büyüklük Güneş, güneş sisteminin en uzak ve en büyük yıldızıdır. Dünya ya uzaklığı yaklaşık 150 milyon kilometre, çapı ise 1.392.000 kilometredir. Bu çap, Yeryüzünün 109 katı, Jüpiter in de 10
1. ÜNİTE: MODERN ATOM TEORİSİ
 . ÜNİTE: MODERN ATOM TEORİSİ.4. Elektron Dizilimi ve Periyodik Sisteme Yerleşim Atomun Kuantum Modeli oluşturulduktan sonra Bohr, yaptığı çalışmalarda periyodik cetvel ile kuantum teorisi arasında bir
. ÜNİTE: MODERN ATOM TEORİSİ.4. Elektron Dizilimi ve Periyodik Sisteme Yerleşim Atomun Kuantum Modeli oluşturulduktan sonra Bohr, yaptığı çalışmalarda periyodik cetvel ile kuantum teorisi arasında bir
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6
 PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
PERİYODİK SİSTEM VE ELEKTRON DİZİLİMLERİ#6 Periyodik sistemde yatay sıralara Düşey sütunlara.. adı verilir. 1.periyotta element, 2 ve 3. periyotlarda..element, 4 ve 5.periyotlarda.element 6 ve 7. periyotlarda
FEN BİLİMLERİ FEN ve TEKNOLOJİ
 KPSS 2017 önce biz sorduk 50 Soruda 32 soru ÖABT FEN BİLİMLERİ FEN ve TEKNOLOJİ TAMAMI ÇÖZÜMLÜ SORU BANKASI KİMYA Eğitimde 30. yıl KOMİSYON ÖABT Fen Bilimleri/ Fen ve Teknoloji Öğretmenliği Soru Bankası
KPSS 2017 önce biz sorduk 50 Soruda 32 soru ÖABT FEN BİLİMLERİ FEN ve TEKNOLOJİ TAMAMI ÇÖZÜMLÜ SORU BANKASI KİMYA Eğitimde 30. yıl KOMİSYON ÖABT Fen Bilimleri/ Fen ve Teknoloji Öğretmenliği Soru Bankası
1. Giriş 2. Yayınma Mekanizmaları 3. Kararlı Karasız Yayınma 4. Yayınmayı etkileyen faktörler 5. Yarı iletkenlerde yayınma 6. Diğer yayınma yolları
 1. Giriş 2. Yayınma Mekanizmaları 3. Kararlı Karasız Yayınma 4. Yayınmayı etkileyen faktörler 5. Yarı iletkenlerde yayınma 6. Diğer yayınma yolları Sol üstte yüzey seftleştirme işlemi uygulanmış bir çelik
1. Giriş 2. Yayınma Mekanizmaları 3. Kararlı Karasız Yayınma 4. Yayınmayı etkileyen faktörler 5. Yarı iletkenlerde yayınma 6. Diğer yayınma yolları Sol üstte yüzey seftleştirme işlemi uygulanmış bir çelik
MİNERALLER. Tek mineralden oluşan kayaçlar. Kireçtaşı (Kalsit). Kaya tuzu (Halit). Buzul
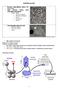 Kayaçlar minerallerden oluşan Yer materyalidir. Çoğu kayaçlar birden fazla mineralden oluşmaktadır. Örnek: Granit Potasyum feldspat. Plajioklas (Feldspat). Kuvars. Hornblende. Biyotit MİNERALLER Tek mineralden
Kayaçlar minerallerden oluşan Yer materyalidir. Çoğu kayaçlar birden fazla mineralden oluşmaktadır. Örnek: Granit Potasyum feldspat. Plajioklas (Feldspat). Kuvars. Hornblende. Biyotit MİNERALLER Tek mineralden
MADDENİN YAPISI ve ÖZELLİKLERİ
 MADDENİN YAPISI ve ÖZELLİKLERİ ÜNİTE : MADDENİN YAPISI ve Üniteye Giriş ÖZELLİKLERİ Her madde kendinden küçük atomlardan oluşmuştur. Ancak her madde aynı atomlardan oluşmamıştır. Maddeyi oluşturan atomlar
MADDENİN YAPISI ve ÖZELLİKLERİ ÜNİTE : MADDENİN YAPISI ve Üniteye Giriş ÖZELLİKLERİ Her madde kendinden küçük atomlardan oluşmuştur. Ancak her madde aynı atomlardan oluşmamıştır. Maddeyi oluşturan atomlar
