Biyolojik hidrojen üretim prosesleri
|
|
|
- Aysun Kurtuluş
- 10 yıl önce
- İzleme sayısı:
Transkript
1 BAÜ FBE Dergisi Cilt:11, Sayı:2, Aralık 2009 Biyolojik hidrojen üretim prosesleri N. GENÇ * Kocaeli Üniv., Mühendislik Fak., Çevre Müh. Böl., ĐZMĐT Özet Hidrojen alternatif yakıt olarak büyük bir potansiyele sahip temiz bir enerji taşıyıcısıdır. Hidrojen üretimi için çeşitli teknolojiler vardır. Biyolojik hidrojen üretim prosesleri termokimyasal ve elektrokimyasal proseslere kıyaslandığında daha çevre dostu ve çok az enerji yoğunluklu olduğu bulunmuştur. Hidrojen biyolojik olarak biofotoliz, foto-fermentasyon ve karanlık-fermentasyon veya bu proseslerin kombinasyonu ile üretilebilir. Literatüre göre, maksimum hidrojen verimi 7,1 mol H 2 /mol glukoz olarak bulunmuştur. Düşük hidrojen verimi ve düşük hidrojen üretim hızı bu proseslerin ticarileşmesinde en önemli engeldir. Genetik olarak modifiye edilmiş mikroorganizmaların gelişimi, prosesin işletme şartlarının iyileştirilmesi, kombine proseslerin gelişimi gibi ilerlemeler biohidrojen teknolojisinin hızlı bir şekilde ticarileşmesini sağlayacaktır. Anahtar kelimeler: Biohidrojen, biofotoliz, foto- ve karanlık- fermentasyon, kombine proses Abstract Biological hydrogen production processes Hydrogen is a clean energy carrier which has a great potential to be an alternative fuel. There are a variety of technologies for hydrogen production. Biological hydrogen production processes are found to be more environment friendly and less energy intensive as compared to thermochemical and electrochemical processes. Hydrogen can be produced biologically by biophotolysis, photo-fermentation and dark-fermentation by combination of these processes. According to literature, maximum hydrogen yield is found to be 7.1 mol H 2 /mol glucose. However, major bottlenecks for the commercialization of these processes are lower H 2 yield and rate of H 2 production. The advancements such as the development of genetically modified microorganism, improvement of operational conditions of process, development of combined process to improve energy conversion efficiency should allow for rapid commercialization of biohydrogen technology. Keywords: Biohydrogen, biophotolysis, process photo- and dark-fermentation, combined * Nevim GENÇ, [email protected], Tel:
2 N. GENÇ 1-Giriş Hidrojen yüksek enerji değerine sahip bir yakıttır (3042 cal/m 3 ). Yandığı zaman oluşan ana ürün su olduğu için kirlilik yaratmayan bir yakıt olduğu düşünülür. Diğer gaz halindeki yakıtlara kıyaslandığında çevreye ve insanlara zararsızdır. Hidrojen başlıca fosil yakıtlardan, biyokütleden ve sudan çeşitli metotlar kullanılarak üretilir. Bu proseslerden buhar reformasyon, kömür gazlaştırma ve suyun elektrolizi metotlarında enerji kaynağı olarak fosil yakıtlar bazen de hidroelektrik kullanılır. Termokimyasal ve elektrokimyasal metotlar yoğun enerji kullanırlar ve her zaman için çevreye dost değillerdir. Örneğin termal metotlar ısı enerjisi, elektrolitik metotlar elektrik enerjisi fotolitik metotlar ışık enerjisi kullanır. Yenilenebilir olmayan enerji kaynaklarının kullanılması ve sürdürülebilir olmaması bir dezavantaj oluşturmaktadır. Biyolojik hidrojen üretim prosesleri ise çevre sıcaklığı ve basıncında işletildiği için daha az enerji tüketimi söz konusudur. Bu prosesler düşük enerji tüketimine sahip oldukları ve yenilenebilir kaynakların kullanımı açısından yeni bir alan yarattıkları için çevre dostudur [1]. Günümüzde hidrojenin %40 ı doğal gazdan, %30 u ağır yağlar ve naftadan, %18 i kömürden, %4 ü elektrolizden ve yaklaşık %1 i biyokütleden üretilmektedir. Enerji alanındaki darboğazın aşılması üzerine çalışmaların yoğunlaştığı günümüzde, sürdürülebilir bir gelişme ve atık miktarının azaltılması dikkate alındığı zaman, yenilenebilir kaynaklardan biyohidrojen üretimi önemli ölçüde dikkat çekmiştir. Atık maddelerin kullanımı ve temiz enerji kaynağı üretimi, biyohidrojen üretim proseslerini tercih edilebilir bir yaklaşım yapmaktadır. Burada, bu gerçekler ışığında biyohidrojen üretim prosesleri değerlendirilmiştir. 2-Biyolojik hidrojen üretim prosesleri Sürdürülebilir gelişme ve atık oranının azaltılmasına olan ilginin artmasından dolayı son yıllarda biyohidrojen üretimi üzerine olan çalışmalarda da büyük artış gözlenmiştir. Biyolojik hidrojen üretim prosesleri aşağıdaki bölümlerde detaylı olarak açıklanmıştır Yeşil alg ve mavi-yeşil alg (cyanobacter) kullanılarak suyun biyofotolizi Yeşil alg ve mavi-yeşil algler, su moleküllerini hidrojen iyonuna ve oksijene direkt ve indirekt biyofotoliz ile parçalarlar Direkt biyofotoliz Bu proseste güneş enerjisi direkt olarak fotosentetik reaksiyonlar ile suyu hidrojen iyonu ve oksijene ayırır. Üretilen hidrojen iyonları, hidrojenaz enzimi ile hidrojen gazına dönüşür [2, 3]. Biyofotoliz prosesinde kullanılan Fe-hidrojenaz aktivitesi oksijene karşı hassas olduğu için özel şartlar gereklidir. Yeşil alg ile suyun hidrojene dönüşümü reaksiyon (1) ile ifade edilir. 2H + H + O (1) 2O ışıkenerjisi Yeşil bitkilerde sadece CO 2 indirgenmesi meydana gelir, çünkü hidrojen oluşumunu sağlayan enzimler yani hidrojenaz yoktur. Mikroalgler, hem ökaryotik (yeşil algler gibi) hem de prokaryotik (cyanobacteria veya mavi-yeşil algler), hidrojenaz enzimine sahiptirler ve uygun şartlar altında hidrojen üretebilirler. Direkt biyofotoliz reaksiyonunda elektronlar sudan iki fotosistem (PSII ve PSI) aracılığı ile hidrojene akar. 18
3 Biyolojik hidrojen üretim prosesleri Direkt biyofotoliz suyun parçalanması PSII ve ferredoxin-indirgenmesi fotosistem PSI den meydana gelir [4]. Đyi bilinen H 2 üreten yeşil alg, Chlamydomonas reinhardtii, anaerobik şartlar altında ya H 2 üretebilir ya da elektron vericisi olarak H 2 kullanabilir. Üretilen hidrojen iyonları, hücrelerde hidrojenaz enzimi varlığı ile elektronlu (indirgenmiş ferredoksin tarafından verilmiş) ortamda hidrojen gazına dönüşür. Fotosistem II (PSII) elektronlar üretir, bu elektronlar fotosistem I (PSI) tarafından absorbe olan ışık enerjisini kullanan ferredoksine (Fd) transfer olur. Hidrojenazın varlığında H 2 üretimi için indirgenmiş ferredoksinden direkt olarak elektronları hidrojenaz kabul eder [5]. H O PSII 2 O2 PSI Fd Hidrojenaz H 2 (2) Alg ile hidrojen üretimi, yenilenebilir kaynak olarak ucuz ve hemen hemen her yerde bulunabilen suyun kullanımı ve hava kirleticilerinden biri olan CO 2 tüketimi açısından ekonomik ve sürdürülebilir metot olarak düşünülebilir. Mikroorganizmalar hidrojene ilaveten oksijen de üretir. Üretilen oksijenin hidrojenaz enzimi üzerine kuvvetli bir engelleyici etkisi bu prosesin en önemli sınırlayıcı etmenidir. Oksijenin etkisini önlemek için oksijene daha az hassas organizmaların tanımlanması, hidrojen ve oksijen döngülerinin ayrılması, ve\veya fotosentezin (oksijen üretimi) solunuma (oksijen tüketimi) oranının değiştirilmesi çalışmaları başlamıştır. Çözeltiye sülfat ilavesinin oksijen üretimi ve hassasiyetini, bununla birlikte hidrojen üretim mekanizmasını da baskıladığı belirlenmiştir [6]. Düşük hidrojen üretim potansiyeli ve hiçbir atığın kullanılmıyor olması diğer dezavantajlarıdır [3]. Direkt biyofotoliz prosesi 1 atm oksijen basıncına yakın kısmı basınçta işletilmelidir. Direkt biyofotolizde literatürde açıklanan hidrojen üretim hızı 0,07 mmol/saat L dır [2]. Bu proses oldukça zayıf ve hassas bir yapıya sahiptir. Hız oldukça düşüktür (diğer fotosentetik reaksiyonların onda birinden daha az), kısa ömürlüdür (yaklaşık 15 dakika devam eder). Bütün bunların sebebi O 2 birikimine bağlanmıştır [4] Đndirekt biyofotoliz Direkt biyofotolizde gözlenen O 2 nin engelleyici etkisinden kaçınmak için, indirekt biyofotoliz önerilmiştir. Đndirekt biyofotoliz şu adımlardan meydana gelir: 1. Fotosistemde biyokütlenin oluşumu 2. Alg hücrelerindeki glukozun 1 molu başına 2 mol asetat ve 4 mol hidrojenin aerobik karanlık fermentasyonda üretimi 3. 2 mol asetatın hidrojene dönüşümü 6CO + + O (mikroalg) (3) 2 6H 2O + ışıkenerjisi C6H12O H12O6 2H 2O 4H 2 + 2CH 3COOH 2CO2 3COOH 4H 2O + ışıkenerjisi 8H H 2O ışıkenerjisi 12H C + + (cyanobacteria) (4) 2CH + + CO (5) Toplam reaksiyon 12 + O2 (6) Đlk olarak N 2 yokluğunda nitrojenaz ile H 2 üretebilen azotu bağlayabilen cyanobacteria incelenmiş [4]. Cyanobacteria enerji kaynağı olarak güneş enerjisi ve karbon kaynağı olarak CO 2 kullanımına sahiptir. Hücreler, hücresel maddeleri üretmek için ilk olarak CO 2 alırlar ve ardından hidrojen üretimi için kullanılırlar [2]. 19
4 N. GENÇ Cyanobacteria iyi bilinen bir mavi-yeşil alg olup büyük ve farklı bir fotoototrofik mikroorganizma grubunu teşkil eder. Fotosentetik pigmentler içerir ve oksijenli ortamda fotosentez yapabilir. Hidrojen, hem hidrojenaz hem de nitrojenaz enzimleri ile üretilir. Azotu bağlayabilen veya bağlayamayan cyanobacteria türleri mevcuttur. Cyanobacteria nin gereksinimleri, hava (N 2 ve O 2 ), su, mineral tuzlar ve ışıktır [5]. Cyanobacteria veya mavi-yeşil alg gram pozitif bakteridir [1]. Anabaena cylindrica en iyi bilinen hidrojen üreten cyanobacterium dur. Fakat bir başka hidrojen üreten cyanobacterium olan Anabaena variabilis yüksek hidrojen veriminden dolayı son yıllarda çok daha fazla dikkat çekmiştir [5]. Anabaena variabilis in mutant türünün indirekt biyofotolizinde hidrojen üretim hızı 0,355 mmol/saat L olarak açıklanmıştır [2]. Nitrojenazın aktivitesi oksijen ile engellenir. Bu yüzden hidrojen üretimi anaerobik şartlar altında meydana gelir. H 2 nin foto üretimi üzerine CO 2 nin engelleyici etkisi açıklanmış olmakla birlikte, hidrojen gelişim safhasında CO 2 bazı kültürler için gereklidir. Düşük CO 2 derişimlerinin (%4-18 w/v) büyüme evresinde hücre yoğunluğunu artırarak sonraki evrede daha yüksek hidrojen üretimine yol açtığı belirtilmiştir [5] 2.2- Fotosentetik bakteri ile organik bileşiklerden hidrojen üretimi Moleküler hidrojen üreten fotosentetik mikroorganizma güneş enerjisi varlığında indirgenmiş bileşikleri (organik asitleri), azotun yetersiz olduğu şartlar altında nitrojenaz ile katalizler. Bu mikroorganizmalar suyu parçalamada yeterince etkili değillerdir. Bununla birlikte anaerobik şartlar altında, bu mikroorganizmalar elektron vericisi olarak asetik asit gibi basit organik asitleri kullanmaya yeteneklidirler. Bu elektronlar, ATP formunda enerji kullanan ferredoksin ile nitrojenaza taşınır. Azot mevcut olmadığı zaman, nitrojenaz enzimi protonu hidrojen gazına indirgeyebilir. Hidrojen üretim reaksiyonu aşağıda verilmiştir [2] C CO (7) 6H12O6 H 2O + ışıkenerjisi 12H 2 6 Fotofermentasyon prosesindeki biyokimyasal yolizi ise aşağıdaki şekilde ifade edilmiştir [5]. 2 ( CH 2O) Ferredok sin Nitrojenaz H 2 2 ATP ATP (8) CO, fotosentetik bakteri ile mikrobiyal değişim reaksiyonunun kullanıldığı hidrojen üretimi için de kullanılabilir. CO + H 2O CO2 + H 2 (9) Literatürde mmol/ saat L derecesinde hidrojen üretim hızı rapor edilmiştir [2]. Bu prosesin en önemli faydaları [1]: 1- Yüksek teorik dönüşüm verimine sahip oluşu 2- Farklı biyolojik sistemlerde aktivitenin yitirilmesi problemine sebep olan O 2 - gelişim olmayışı 3- Geniş spektrumdaki ışığın kullanılabilirliği 20
5 Biyolojik hidrojen üretim prosesleri 4- Atıklardan türeyebilen organik substratları ve onları tüketebilmesi, atıksu arıtımı ile birlikte kullanım potansiyeline sahip oluşu Fotosentetik mikroorganizma, anaerobik ortamda ışığa bağımlı elektron taşınım işlemi ile organik bileşiklerden hidrojen üretir. Fotosentetik bakterinin en uygun büyüme sıcaklığı o C aralığı ve ph ı 7,0 dır [3]. Fotosentetik bakterinin kullanımındaki avantaj, bu organizmaların çok yönlü metabolik yeteneğine sahip oluşu ve PSII nın olmayışıdır, böylece H 2 üretiminin O 2 ile engellenmesi önlenmiş olur. Bu bakterilerin fotosentezi yürütebilmesi için organik veya inorganik elektron kaynağına ihtiyacı vardır. Geniş aralıktaki ucuz bileşikleri kullanabilir. Pek çok organik atığın kullanımı bu konuda uygun bulunmuştur [5]. Endüstriyel atıklardan hidrojen gazı üretiminde en önemli problemlerden biri ışığın nüfuziyetini azaltan atıksuyun rengidir. Yüksek amonyak derişimlerinin nitrojenaz enzimini engellemesi ile hidrojen verimliliğini azaltması da diğer bir problemdir. Endüstriyel atıklardaki yüksek organik madde içeriği (KOĐ) ve bazı zehirli bileşikler (ağır metaller, fenoller ve PAH), hidrojen üretiminden önce ön arıtım ile giderilmelidir [3]. Fotosentetik mikroorganizmalar arasında, mor fotosentetik bakterilerin çok iyi hidrojen ürettiği bilinmektedir [7]. Fotofermentatif hidrojen üretiminde mor kükürtsüz bakteri (PNS), güneş ışığı veya suni ışıktan elde edilen ışık enerjisi ile elektron vericisi olarak küçük zincirli organik asitleri kullanabilir. Fotosentetik bakterilerin bu özelliği, karanlık fermentasyon çıktılarının daha ileri seviyede parçalanması ve H 2 üretiminin tamamlanmasında kullanım imkanını da artırır. PNS bakteri ile biokimyasal proses nitrojenaz tarafından katalizlenir. Bu yüzden, yeterli ATP kaynağı, etkili fotofermentatif hidrojen üretimi için ana parametrelerden biridir. Işıktan elde edilen enerji, PNS bakteriye organik asitlerin hidrojene dönüşümünde termodinamik bariyeri yenmesine imkan verir. PNS bakteri geniş dalga boyu aralıktaki ışığı ( nm) absorbe etme yeteneğine sahip olup, hidrojen üretim mekanizması membran üzerinden elektron transfer işleminden ibarettir. Tungsten ve lüminesans tipte suni ışık kullanılması durumunda, anoksik ortamda hidrojen üretimi için 11,7±2,9 W/m 2, hücre büyümesi için ise 7,3±1,5 W/m 2 üniform ışık yoğunluğu kullanılabilir. Uygun değerden daha yüksek bir ışık yoğunluğu, hem biyokütlenin büyümesi, hem de PNS bakterileri tarafından hidrojenin foto üretimi için herhangi bir engelleyici etkiye yol açmadı. Fotobiyoreaktörün tasarımı, uygun ışık kullanımı ve ışığın nüfuziyeti, yüksek hidrojen üretim verimi için esastır. Basak ve Das (2009) tarafından yapılan çalışmada üniform ışık dağılımının sağlandığı silindirik halka şeklindeki reaktörde hidrojen verimi 1 mol DL malik asit başına 4,5±0,05 mol H 2 olarak elde edilmiştir. Teorik olarak ise 1 mol DL malik asit başına 6 mol H 2 elde edilebilmektedir [8]. Rhodobacter sphaeroides anaerobik şartlar altında nitrojenaz-hidrojenaz enzim sistemi ile organik asitten hidrojen üretebilen en iyi bilinen PNS bakterisidir. Kapdan ve diğ., (2009) tarafında asitle hidrolize edilmiş buğday nişastası ile fotofermentatif hidrojen üretiminde üç farklı Rhodobacter sphaeroides türünün etkinliği incelenmiştir [9]. Sonuçlar göstermiştir ki, hidrojen üretim verimleri R-RV türü için 1,23 mol H 2 /mol glukoz R-DSMZ için 0,97 mol H 2 /mol glukoz R-NRLL için 0,82 mol H 2 /mol glukoz olmuştur. Hidrojen veriminde bakteri türü olduğu kadar tüketilen organik asitler de etkilidir. Uyar ve diğ., (2009) tarafından Rhodobacter sphaeroides O.U.001 ile farklı uçucu yağ asitleri içeren ortamdaki fotofermentatif hidrojen üretimi incelenmiştir [10] o C de W/m 2 ışık yoğunluğunda 6,7 ph da işletilen fotoreaktörde mikrobiyal hidrojen üretiminin belirlenmesinde substrat dönüşüm verimliliği 21
6 N. GENÇ değerlendirilmiştir. Substrat dönüşüm verimliliği büyüme veya alternatif biyosentezden daha ziyade hidrojen üretimi için kullanılan substratın ne oranda olduğunun ölçüsüdür. Bazı substratlar için reaksiyonlar şu şekildedir: Malate için C 4H 6O5 + 3H 2O 6H 2 + 4CO2 (10) Laktat için C 3H 6O3 + 3H 2O 6H 2 + 3CO2 (11) Asetat için C 2H 4O2 + 2H 2O 4H 2 + 2CO2 (12) Propiyonat için C 3H 6O2 + 4H 2O 7H 2 + 3CO2 (13) Butirat için C 4H 8O2 + 6H 2O 10H 2 + 4CO2 (14) Çalışmada en yüksek substrat dönüşüm verimliliği ve hidrojen üretim hızı, en kısa lag süresi (aşılamanın başlaması ile gaz üretiminin başlaması arasında geçen süre) ve en yüksek hidrojen miktarı malate içeren ortamda elde edilmiştir, butirat ise en düşük miktarda kalmıştır. Bunun sebebi ise butiratın poli-β- hidroksibütirat (PHB) maddesine kolay dönüşüm olasılığı ile açıklanmıştır. PHB üretimi, fotohidrojen üretimi ile rekabet eder; bu rekabetin sebebi ise PHB üretimi ve hidrojen üretiminde organik asitlerin metabolizmasından oluşan aynı indirgeyici gücün kullanılmalarıdır. Yapılan çalışmada substrat karışımının fotofermentasyonu sırasında ise substrat dönüşümü ve hidrojen üretiminin daha yüksek olduğu bulunmuştur. Fotofermentasyon performansı mikrobiyal kültürün tipine ve karbon kaynağına olduğu kadar ışık yoğunluğuna da bağlı olarak değişir. Işık yoğunluğunun artması, hidrojen verimi ve üretim hızı üzerinde pozitif etki etki yaratır, fakat ışık dönüşüm verimi üzerine ters etkiye sahiptir [11]. Karanlık şartlar altındaki hidrojen üretimi genel olarak ışınlanmış şartlarda elde edilenden düşüktür. Bununla birlikte ışık/ karanlık döngüler, hidrojen üretim hızını ve hücre derişimlerini sürekli ışınlanmaya kıyasla biraz daha artırdığı belirlenmiştir [3]. Obeid ve diğ., (2009) tarafından yapılan çalışmada Rhodobacter capsulatus ile fotofermentasyon ile hidrojen üretiminde ışık yoğunluğunun etkisi incelenmiştir [12]. Karbon ve hidrojen kaynağı olarak laktatın kullanıldığı çalışmada ışık yoğunluğunun artışı ile hidrojen üretim hızının arttığı görülmüştür lux de hidrojen üretim hızı, 6000 lux de elde edilenden 6 kat yüksek olmuştur. Ayrıca ışık yoğunluğunun artışı biyokütle üretimini de artırmıştır. Işık yoğunluğunun 6000 lux den lux e çıkması biyokütle üretimini ifade eden protein derişimini 3,1g/L den 4 g/l ye artırmıştır. Daha önce de ifade edildiği üzere nitrojenaz, fotosentetik bakteri ile hidrojen gaz üretimini hızlandıran ana enzimdir. Enzimin aktivitesi oksijen, amonyak veya yüksek N/C oranında engellenmiş olur. Bu yüzden sınırlandırılmış amonyum ve oksijensiz şartlar gereklidir. Hidrojen gazı üretimini azot kaynağı olarak albumin, glutamat ve maya ekstraktı gibi proteinler artırırken, amonyak tuzları varlığında düştüğü belirlenmiştir. Yüksek azot derişimlerinde metabolizmanın değişmesi sonucu organik maddenin hidrojen üretiminden daha ziyade hücre sentezine kanalize olması, aşırı biyokütle büyümesine ve ışık yayınımının azalmasına sebep olur. Amonyak tükendikten sonra ise hidrojen üretim aktivitesi gerçek seviyesine dönebilir. Karbonhidratın varlığında amonyak gideriminin artacağı ve hidrojen üretiminin teşvik edileceği rapor edilmiştir. Yüksek seviyede amonyak içeren atıksudan hidrojen üretimi için amonyak giderimi ve hidrojen üretim prosesini içeren iki safhalı sistemler önerilmiştir [3]. 22
7 Biyolojik hidrojen üretim prosesleri Foto-fermentatif bakteride hidrojenaz hidrojen gazı kullanan bir enzimdir, ve bu yüzden nitrojenaz aktivitesine antagonistiktir (düşmandır). Hidrojenaz aktivitesi, hidrojen gazı üretimini sınırlayacaktır. Hidrojenazı eksik foto-fermentatif bakteri mutant kültürleri 2-3 kat daha fazla hidrojen üretebilmektedir [3]. 2.3-Organik bileşiklerden fermentatif hidrojen üretimi (Karanlık fermentasyon) Hidrojen, karbonhidratça zengin substrat üzerinde karanlıkta büyüyen anaerobik bakteri ile de üretilebilir. Fermentasyon yolizine ve en son ürüne bağlı olarak glukozdan farklı miktarda hidrojen üretilebilir. Laboratuvar denemelerinde hidrojen üretim hızı 77 mmol/saat L olarak elde edilmiştir [2]. Organik atıkların anaerobik asetojenizinde üç tip fermentasyon meydana gelir; bunlar propiyonik asit, bütirik asit ve etanol tipli fermentasyondur. Aynı işletme koşullarında yapılan çalışma göstermiştir ki organik atıktan hidrojen üretiminde etanol tipli fermentasyon (2,96 mol/kg MLVSS gün), propiyonik asit ( 0,022 mol/kg MLVSS gün) ve bütirik asit ( 0,57 mol/kg MLVSS gün) tipli fermentasyondan daha uygun olduğu bulunmuştur [13]. Endüstriyel üretim için fermentasyon ile hidrojen üretimi bazı avantajlara sahiptir. Bunlar [1]: 1-Fermentatif bakteri yüksek hidrojen gelişim hızına sahiptir 2-Fermentatif bakteriler organik maddeden gün ve gece boyunca sabit olarak hidrojen üretebilirler 3-Fermentatif bakteriler, üretim sisteminde iyi bir büyüme hızına sahiptirler Bundan dolayı hidrojen üretiminde fermentatif üretim prosesleri fotokimyasal proseslerden çok daha avantajlıdır. Hidrojen üretim hızı, eşirilebilir ve zengin elektron kaynağı ve aktif hidrojenaz faktörlerinin bileşimi ile en yüksek seviyesine ulaşabilir [1]. Fermentatif elektron üretimi: Heterotrofik organizmalarda, anaerobik büyüme şekli, enerji üreten reaksiyonlarda meydana gelen elektronların tabiatı gereği özel problemler ortaya koyar. Bu durum özellikle biyosentetik aktivite için, enerji kaynağı olarak hizmet eden büyük miktarda organik bileşikler parçalandığı zaman gözlenir. Bundan dolayı zorunlu ve fakültatif anaerobların metabolizmasında elektron akışını düzenlemek için çeşitli kontroller gereklidir. Bunlardan biri bazı organizmaların hidrojenaz aktivitesi ile moleküler hidrojen (H 2 ) formunda aşırı elektronları uzaklaştırmasıdır. Piruvatın parçalanma yolizi, reaksiyon (15) de görüldüğü gibi, asetil-coa ve format oluşturur. CH 3 COCOOH + HCoA CH 3COCoA + HCOOH (15) Format parçalanması ise reaksiyon (16) gereği H 2 meydana getirir. HCOOH H 2 + CO 2 (16) Asetil CoA hem asetatı (reaksiyon 17) hem de etanolü (reaksiyon 18) meydana getirir. CH 3 COCoA + H 2O CH 3COOH + HCoA (17) 23
8 N. GENÇ + 2NADH + 2H CH 3CH 2 CH 3 COCoA + OH + H. CoA + 2NAD (18) Hidrojen gelişimi için diğer yolizi, NADH yolizi olarak tanımlanır. Bu yolizinde, hidrojen reaksiyon (19) gereği NADH ın yeniden oksidasyonu ile üretilir NADH + H H 2 + NAD (19) Bu NADH, glukozun piruvata fermentatif dönüşümü sırasında oluşur. reaksiyon (20) de gösterilmiştir. Bu yolizi + 2NAD 2CH 3 C6 H12O6 + COCOOH + 2NADH + 2H (20) Aktif Hidrojenaz: Hidrojenaz enzimi fermentatif hidrojen üretiminde önemli rol oynar Fermentatif hidrojen üretimini etkileyen faktörler Substrat: Kimyasal içerik dikkate alındığında termofilik fermentasyon için üç farklı biokütleden söz edilebilir [14]. Şeker içeren biyokütle (şeker pancarı, şeker kamışı) Nişastalı biyokütle (patates, hububat) Lignoselülozik biyokütle (çimen, ağaç, saman) Bu biyokütleler çeşitli tarımsal atıklar olabileceği gibi biyokütle işleyen endüstrilerden kaynaklanabilen atıklar da (pancar küspesi, melas, patates kabuğu, elma küspesi, buğday kepeği) olabilmektedir. Şeker [15, 16], nişasta [17, 18] ve selülozdan [19] fermentatif hidrojen üretimi üzerine çok sayıda araştırmalar yapılmıştır. Magnusson ve diğ., (2008) tarafından işlem görmemiş farklı selülozik atıkların Clostridium thermocellum ile parçalanabilirliği değerlendirilmiştir [20]. Elde edilen sonuçlar laboratuvar saflığındaki α -selüloz ile kıyaslandığı zaman, atıkların hidrojen üretiminde iyi bir potansiyel ve değerli son ürünler elde edildiğini göstermiştir. 5 g/l atık kullanılması ile elde edilen hidrojen üretimi 1,18-1,27 mmol H 2 /g glukoz arasıda iken 1,1 g/l α -selüloz kullanılması ile elde edilen hidrojen üretimi ise 0,76 mmol H 2 /g glukoz olmuştur. Urbaniec ve Grabarczyk, (2009) tarafından çeşitli biyokütlelerin (şeker pancarı, patates, buğday kepeği, sıkıştırılmış pancar küspesi ve buğday sapı) fermentatif hidrojen üretim verimlilikleri değerlendirilmiştir [14]. Đncelenen atıklardan en yüksek hidrojen verimi, düşük su içeriğinden dolayı (yaklaşık %10) buğday kepeği ve buğday sapında elde edilmiştir. Bazı substratlar, karmaşık yapılarından dolayı fermentatif hidrojen üretimi için ideal değillerdir. Bu atıklara bazı ön işlemler uygulandıktan sonra kullanılabilirler. Örneğin atıksu arıtım ünitelerinden oluşan atık aktif çamura ultrasonikasyon, asidifikasyon, dondurma ve çözündürme, sterilizasyon, metan bakterilerinin engellenmesi ve mikrodalga gibi uygun ön işlemleri uygulandıktan sonra kullanılabilir [21]. Biyokütleye uygulanan ön işlem metodu ham maddenin tipine bağlı olarak değişir. Sukroz içeren biyokütlede ön işlem adımı, meyve suyunun ekstre edilmesini içerir. Nişasta ve lignoselülozik biyokütlenin ön işlemi, polisakkaritlerin basit şekerlere dönüşümünde hidroliz adımı gerektiğinden dolayı çok karmaşıktır. Fermentasyon biriminden önce ligninin giderimi önemli bir problemdir. Çünkü selüloz ve + 24
9 Biyolojik hidrojen üretim prosesleri hemiselülozun aksine lignin basit şekerlere dönüşmez ve hidrojen üreten mikroorganizmaların büyümesini engelleyebilir. Biyohidrojen Üreten Bakteri: Anaerobik şartlarda hidrojen üretebilen çok sayıda mikroorganizma tipi vardır. Zorunlu anaerobik bakteriler en genel sınıfdır. Bununla birlikte hidrojenaz enzimi bulunan birkaç fakültatif bakteri de, hidrojen üreticisi olarak tanımlanmıştır. Bunlar zorunlu anaerobik bakteriden daha düşük hidrojen üretim hızına sahiptirler. Anaerobik bakteriler tarafından hidrojen üretiminde iki yolizi vardır, bunlar bütirat yolizi veya asetat yolizi. Teorik olarak asetat yolizi ile 1 mol glukozdan 4 mol hidrojen üretilebilir, bütirat yolizinde ise 2 mol hidrojen üretilir. Fakültatif anaerob, oksijenin mevcut olduğu durumda aerobik solunum ile ATP üretir ve anaerobik fermentasyona dönme eğilimindedir. Zorunlu anaerobik bakterilerin büyümesi, iz miktardaki oksijenin engelleyici etkisinden dolayı oldukça güçtür. L- cysteine gibi indirgeyici ajanların kullanılması, anaerobik ortamın korunmasında alternatif bir yoldur, ancak işetim maliyetini artıracaktır [22, 23]. L-cysteine fermentasyon sistemlerinde yükseltgenme-indirgenme potansiyeli (ORP) değerini baskılar. L-cysteine ilavesinden sonra ORP değeri -171mV dan -226~-272mV seviyelerine düşmüştür. Ayrıca L-cysteine bakteri tarafından substrat kullanım hızını artırabilir. 0,6 mm L-cysteine ilavesi hidrojen verimini %15,2 artırmıştır [24]. Maliyet artışına karşın co-kültürün kullanılması önerilmektedir. Böyle bir durumda indirgeyici ajan kullanmaksızın bir mikroorganizma türü sıvıdaki çözünmüş oksijeni tüketerek ortam diğer mikroorganizma türünün hidrojen üretimini yapabileceği anaerobik şartlar sağlanmış olacaktır [22]. Reaktör Tipi: Geleneksel tam karışımlı sürekli reaktörlerde, çok kısa hidrolik alıkonma sürelerinde (HRT) biyokütlenin dışarıya yıkanması söz konusudur. Bu suretle karışık sıvıdaki biyokütle derişimi ve hidrojen üretimi sınırlanır. Tutuklanmış-hücreli reaktörler bu tip reaktörlere bir alternatifdir. HRT nin artışı, hidrojen üreten bakterinin hidrojen üretimini artıracak, ancak çok yüksek seviyedeki HRT azaltacaktır [21]. Sürekli reaktörlerde hidrolik alıkonma süresi ve organik yükleme hızı gibi parametrelerin uygun seçilmesi ile hidrojen üretim verimi artırılabilir. Hacimsel hidrojen üretim hızı artıkça reaktör boyutu küçülür ve sürdürülebilirlik ve temiz enerji üretimi için reaktörün maliyeti azalmış olur [25]. Bunun yanı sıra sabit gaz üretiminin sağlanması için işletme parametrelerine dikkat edilmelidir [26]. Babu ve diğ., (2009) tarafından fermentatif H 2 üretimi ve substrat parçalanması üzerine bağlı ve süspanse büyümeye sahip reaktörlerin etkisi incelenmiştir [27]. Elde edilen sonuçlar gösterdi ki, hidrojen verimi ve substrat giderimi bağlı büyümeye sahip biyofilm reaktöründe (28,98 mmolh 2 /gün, 1,25 kgkođ/m 3 gün), süspanse büyümeli reaktörden (20,93 mmolh 2 /gün, 1,08 kgkođ/m 3 gün) daha yüksek olmuştur. Azot ve Fosfor: Protein, nükleik asit ve enzimlerin yapısında azot bulunduğu için hidrojen üreten bakterinin büyümesinde azot çok önemlidir [21]. Uygun derişimde amonyak azotu fermentatif hidrojen üretimi için faydalıdır, yüksek derişimlerde ise hidrojen üretimini inhibe edebilir, çünkü bakterinin hücre içi ph ını değiştirebilir, enerji gereksinimini artırabilir veya belirli enzimleri inhibe edebilir. Fermentatif hidrojen üretimi sırasında 0,1 g N/L amonyak derişiminde en yüksek hidrojen verimliliği (298,8 ml/g glukoz) elde edilmiştir [28]. Fosfata ise hem nütrient değeri hem de tamponlama kapasitesi özelliğinden dolayı gereksinim duyulur [21]. 25
10 N. GENÇ Metal Đyonu: Katyonlar ATP sentezinde, NAD yükseltgenme/indirgenmesinde ve enzim aktivitesinde önemli rol oynarlar. Uygun derişimlerde olduğu takdirde mikrobiyal metabolizmayı artırır. Fakat aşırı derişimlerde, yüksek osmotik basınç ve yanlış enzim bağlantısı yaratması sebebi ile hücrenin aktivite kaybına ve plasmolizine sebep olabilir. Sodyum pek çok atıksuda bulunması ve tamponlayıcı madde olarak kullanılan kimyasallarda yer alması bakımından en önemli katyon olmuştur. Kim ve diğ., (2009) tarafından sodyumum zehirleyci etkisi incelenmiştir [29]. Sonuçlar göstermiştir ki 6 g Na + /L den yüksek sodyum derişimlerine ani maruz bırakılması durumunda substrat giderim verimliliği ve mikrobiyal katabolizmanın engellendiği, metabolik yolizinin değişimi ile hidrojen üretiminin düştüğü saptanmıştır. Yapılan diğer bir çalışmada 1,87 g/l üstündeki sodyum derişimlerinin metan üretimini engellediği 2,75 g/l de ise zehirleyici etki gösterdiği saptanmıştır [30]. Fe 2+ yokluğunda hidrojen üreten fermentatif bakteri büyümesi, metabolizması ve hidrojen üretim yeteneği etkilenecektir. Demir hidrojenaz için gereklidir. Mg 2+, önemli bir etkileyici faktördür. Magnezyum önemli bir kofaktördür. Glikoliz prosesinde stoplazmadaki yaklaşık 10 enzimin Mg 2+ ile aktive olması beklenir [22, 23]. Sıcaklık: Uygun aralıkta sıcaklık artışı, hidrojen üreten bakterinin yeteneğini artırır. Fakat çok yüksek seviyelerdeki sıcaklık azaltır. Mezofilik aralık için en uygun sıcaklık 37 o C, termofilik aralık için ise 55 o C dır. Asidin engelleyici etkisi ve ph değişimi: Hidrojen asidojeniz prosesinde tek ürün değildir, asetat, bütirat ve etanol aynı zamanda meydana gelir. Kültür ortamı yüksek şeker ile beslendiği zaman üretilen yüksek derişimdeki asitler hidrojen üretimini engeller. Yüksek derişimde çözünmeyen asitlerin olması halinde, çözeltinin iyonik gücü artar ve prosesin yönü hidrojen üretiminden organik çözücü üretimine doğru döner. Polar olmayan ayrışmayan asitler, düşük ph da hücre duvarından nüfüze olduğu zaman yüksek iç ph ında hücre içindeki protonlar salınır ve inhibisyon etkisi meydana gelir. Bu enerji ihtiyacı artışına sebep olur. Hücre içi asit derişimini koruyacak ana parametre hücre dış ortamının ph ıdır. Hidrojen üretimi için optimum ph 5-7 aralığındadır, optimum 5,5 dır [22]. Hidrojen kısmı basıncı: Standart fermentatif yolizi teorik olarak maksimum 4 mol H 2 /mol glukoz üretir. Uygulamada yaygın olarak 2,4-3,2 mol H 2 /mol glukoz olarak gözlenir. Üretilen gaz H 2, CO 2, CH 4, CO ve bazı hidrojen sülfitler içerir. Bu yüzden saflaştırılması gerekir. Karanlık fermentasyon proseslerinde hidrojen kısmı basıncı önemli bir faktördür, çünkü hidrojen basıncı artıkça hidrojen üretimi azalır [6]. Hidrojen üretimindeki ana enzim hidrojenaz tersinir olarak okside olur ve ferrodoksini indirger. Đndirgenmiş ferrodoksinin oksidasyonu sıvı fazdaki hidrojen derişimi arttığı zaman oluşamaz ve oksitlenmiş ferrodoksin indirgenmesi meydana gelecektir. Kısacası sıvı fazdaki hidrojen, protona okside olacak, böylece hidrojen verimi azalır [22]. Bu sınırlamaya kesin çözüm, hidrojen üretilirken uzaklaştırılmasıdır. Kısmı basıncın azaltılması için vakum uygulanması, azot ve hidrojen geçirebilen membranların kullanımı, güçlü karıştırma ve inert gazın püskürtülmesi gibi yöntemler uygulanbilmekte [31, 32] Fotosentetik ve fermentatif bakterinin kullanıldığı hibrit sistemler 1 mol glukozun tam olarak parçalanmasında 12 mol hidrojen üretilir. Ancak glukozun hidrojen ve karbondioksite tam parçalanması mümkün değildir, çünkü bu reaksiyonun 26
11 Biyolojik hidrojen üretim prosesleri gerçekleşmesi termodinamik olarak mümkün değildir. Dış enerji kaynağı ile (fotofermentasyonda foton-enerjisi) teorik olarak 1 mol glukoz başına 12 mol hidrojen üretebilir. Ancak bu proses ışığın yokluğunda işletilemez. Diğer taraftan dış enerjinin yokluğunda (karanlık fermentasyon durumunda) fermentatif bakteri ile 1 mol glukozun oksidasyonunda maksimum 4 mol hidrojen ve bazı yan ürünler meydana gelir. Yan ürün olarak sadece asetat meydana geldiği zaman reaksiyon (4) gibidir. Karanlık fermentasyon safhasında üretilen asetat, fotosentetik bakteri ile hidrojen üretmek için oksitlenebilir (reaksiyon 5) [2]. Bundan dolayı en yüksek verimde sürekli hidrojen üretimi, karanlık- ve fotofermentasyon metotlarının kombine edilmesi ile sağlanabilir [2]. Ekonomik biyohidrojen üretimi için 8 mol H 2 /mol glukoz yeterli olacağı ifade edilmiştir. Şimdiye kadar yapılan çalışmalarda karanlık fermentasyonla 2,5 mol H 2 /mol glukoz üretilebildiği, kombine veya ard arda gelen fermentasyonlar ile bu değerin 7 mol H 2 /mol glukoz a çıkabildiği ifade edilmiştir [9]. Karanlık ve fotofermentasyon kombine sistemlerinde, ilk adım karmaşık organik kaynağın asit veya enzimatik hidroliz adımı ile şekere dönüşümüdür. Đkinci adım, karanlık fermentasyonda asetojenik anaerobik organizmalar ile uçucu yağ asitlerine (VFA), hidrojene ve CO 2 ye dönüşümü, en son adım ise foto heterotrofik bakteri ile bu yağ asitlerinin CO 2 ve H 2 ye daha ileri fermentasyonudur [33]. Şekil 1 de kombine sistemlerin genel akış şeması verilmiştir. Kombine sistemler hidrojen veriminin artırılmasında uygun bir strateji olarak önerilir. Su ve diğ., (2009) tarafından kombine sistemde nişastadan hidrojen üretimi değerlendirilmiştir [34]. Sukroz ve glukoz, biyohidrojen üretiminin ticarileştirilmesi için pahalı substrat olduğu düşünülür. Nişasta ise dünyada çok fazla bulunan bir organik bileşiktir, etkili düşük maliyetli substrat olarak hizmet eder. Çalışmada karanlık fermentasyon safhasında, ısı ile ön işlemden geçirilerek metanojenik aktivitesi engellenmiş anaerobik çamur, fotofermentasyon safhasında Rhodopseudomonas palustris kullanılmıştır. Nişasta jelatin haline getirildikten sonra ve enzimatik hidrolizden sonra kullanıldığı zaman, maksimum hidrojen verimi sırası ile 240,4 den 258,5 ve 276,1 ml H 2 /g nişasta ya artmıştır. Karanlık fermentasyondaki metabolitler (başlıca asetat ve butirat) fotofermentasyonda substrat olarak kullanılmıştır. En yüksek hidrojen verimi 131,9 ml H 2 /g nişasta olmuştur. Kombine sistemde, en yüksek hidrojen verimi, sadece karanlık fermentasyonda 240,4 mlh 2 /g nişasta dan 402,3 ml H 2 /g nişasta ya artmıştır. Kombinasyon sistemlerinin ticari uygulamalar için iyi bir potansiyele sahip olduğu ifade edilmiştir. Fotofermentasyonda en önemli problemler besin ihtiyacının karşılanması, çevresel şartların (T=30-35 o C, ph=6,8-7,5, ışık yoğunluğu=4-6 klux) kontrolü ve yüksek VFA derişimi (>2500 mg/l) ve NH 4 -N (>50 mg/l) nin sebep olduğu engelleyici etkilerdir. [33]. 27
12 N. GENÇ CO 2 Gazın iyileştirilmesi H 2 Biyokütle H 2 + CO 2 H 2 + CO 2 Işık Biyokütleye ön işlem Termofilik fermentasyon Fotofermentasyon Fermente olamayan kısım Fermente olamayan kısım Şekil 1: Đki safhalı hibrit sistemler [14] Foto- ve karanlık fermentasyon teknolojileri bazı dezavantajlara sahiptır. Fotofermentasyonla H 2 üretiminde en önemli konulardan biri organik asit kaynağıdır. Saf organik asitlerin kullanımı ekonomik değildir. Diğer taraftan bu proseslerde kullanılan organik atıklar saf kimyasallar olmadığı için organik asitlere ilaveten fotobakteriler ile metabolize edilemeyen nişasta ve selüloz gibi maddeler de içerir. Bu olumsuzlukları gidermek için asidojenikler ile H 2 üretiminin geliştirildiği, metan üretiminin engellendiği ve organik asitlerin meydana geldiği anaerobik prosesler önerilmektedir. Fakat bu proseslerde teorik olarak bile 1 mol glukoz başına 4 mol den daha fazla hidrojen üretilememektedir. Bu proseslerin olumsuzluklarını önleyecek metotlardan biri her iki prosesi tek prosese entegre etmektir, yani karanlık asidojenik fermentasyon H 2 ve organik asitler üretecek ve mor fotofermentatif bakteriler H 2 üretimi için organik asitleri kullanacak. Entegre proseslerin optimize edilmesi halinde atık arıtımı ile aynı anda yüksek H 2 çıktısı elde etmek mümkün olacaktır [35]. Srikanth ve diğ.,(2009) tarafından karanlık fermentasyon ile üretilen uçucu yağ asitlerinin (asetik asit ve bütirik asit) fotofermentasyon ile hidrojen üretiminde birincil substrat olarak uygunluğu değerlendirilmiştir [36]. Deney sonuçları göstermiştir ki asetik asitin en yüksek H 2 üretimi ve substrat parçalanması (3,51 mol /kg KOĐ gün ve 1,22 kgkođ/m 3 gün), bütirik asitten (3,33 mol/kg KOĐ gün ve 1,19 kgkođ/m 3 gün) yüksek olmuştur. Bunun sebebi asetik asitin basit yapısı ve kolay parçalanabilirliğidir. Karanlık ve fotofermentasyonun birlikte kullanımı substrat olarak atıksu kullanıldığı zaman ekonomik bakımdan gelecek vaad eden ideal bir yol olarak görülür. Kombine sistemlerde ilk basamak olan karanlık fermentasyon çıktısının tanımlanması, ardından gelen fotofermentatif H 2 üretim sisteminin başarısını etkilemektedir. Bu yüzden kombine sistemlerde her iki adım birlikte düşünülerek optimize edilmelidir. Belokopytov ve diğ., (2009) tarafından nişastanın fermentatif hidrojen üretiminde fotofermentatif hidrojen üretimini engelleyebilecek faktörlerin etkisi incelenmiştir [35]. Amonyum giderilmesinin ve demir iyonu ilavesinin fermentatif hidrojen üretimini artırdığı ve ardından gelen fotofermentatif hidrojen üretimi için faydalı olabileceği açıklanmıştır. 0,5 mm derişimdeki amonyum, mor bakteri ile hidrojenin fotoüretimi için uygun olabileceği ifade edilmektedir. 10 mg/l derişiminde çinko ilavesi metanojenleri engellediği, fakat fotofermentatif üretimi engellemediği gözlenmiştir. 28
13 Biyolojik hidrojen üretim prosesleri Ardışık sistemlerden oluşan kombine hidrojen üretim sistemlerine diğer bir alternatif karanlık ve ışık fermentasyonların aynı reaktör içinde yapılan sistemlerdir (burada karanlık ve ışık fermentasyonlar aynı fermentasyon ortamında meydana gelir). Bu sistemde aynı anda VFA nın oluşumu (karanlık fermentasyon) ve fermentasyonu (ışık fermentasyon) ile toplam fermentasyon süresinin azaltılması ve ortamda VFA birikiminin önlenmesi avantajlarına sahiptir. Böylece karanlık fermentasyon ile üretilen yüksek VFA derişimleri ile oluşan engelleyici etki giderilmiş olur. Argu ve diğ., (2009) tarafından yapılan çalışmada aynı fermantörde öğütülmüş buğday nişastasının kombine karanlık-foto fermenrasyonunda hidrojen üretimi incelenmiştir [33]. Karanlık fermentasyon için ısı ile ön işlem görmüş asidojenik çamur, fotofermentasyon için Rhodobacter sp. karışımı kullanılmıştır. En yüksek kümülatif hidrojen oluşumu (76 ml), hidrojen verimi (176 ml H 2 /g nişasta) ve oluşum hızı (12,2 ml H 2 /g biyokütle saat) 1/7= karanlık/foto biokütle oranında elde edilmiştir. Foto ve karanlık fermentasyonun tek başına uygulanması durumunda elde edilen hidrojen verimleri kombine fermentasyondan biraz daha yüksek bulunmuştur. Ancak 1/7= karanlık/foto biyokütle oranında elde edilen kombine fermentasyonda elde edilen hidrojen üretim hızı foto ve karanlık fermentasyonun tek başına uygulanması durumunda elde edile hızdan (5 ml H 2 /g biokütle saat) önemli ölçüde yüksek bulunmuştur. Bu kombine sistemin kullanımı hidrojen verimliliğini geliştirmesinin yanısıra fermentasyon süresini de azalttığı belirlenmiştir. Karanlık ve fotofermentasyon birimlerinin ard arda kullanıldığı hibrit sistemler, karanlık veya foto-fermentasyon prosesinin tek olarak kullanıldığı sistemlere karşı belli avantajlara sahip. Hidrojen üretiminde karanlık fermentasyon çıktısı, foto fermentasyon için yeterli miktarda organik asit sağlar. Böylece organik asit mevcudiyeti ile oluşabilecek sınırlamalar engellenmiş olacaktır. Fotofermentatif bakteri ile organik asitlerin daha ileri kullanımı daha iyi çıkış kalitesi sağlayacaktır. Prosesin iki mikrobiyal bileşeni için ortam içeriği ve çevresel şartların uyumu sağlanarak sistem kontrol edilebilecektir. Anaerobik fermentasyon çıktısında amonyak derişimi ve C/N oranı, fotosentetik bakteri için engelleyici düzeyde olmamalıdır. Fotofermentasyondan önce, fotosentetik bakterinin uygun performans gösterebileceği ph=7 ve organik asit derişiminin düzenlenebilmesi için karanlık fermentasyon çıktılarının seyreltilmesi ve nötralizasyonu gereklidir[3] Biyokatalizlenmiş elektroliz Hidrojen üretmek için asetatı (veya karanlık fermentasyon çıktısının) oksitlemenin diğer bir yolu, güneş enerjisi yerine elektrik enerjisi formunda dış enerjinin sağlanmasıdır. Bu yaklaşımda asetat elektroliz hücresinin anodik bölmesinde yer alır, ve bakteri ile üretilen protonlar ve elektronlar katotda toplanır (katot, hidrojen üretim reaksiyonunu katalizleyen platin elektrodudur). Anodik ve katodik reaksiyonlar reaksiyon (21) ve (22) de verilmiştir [2]. Anod = CH 3 COOH + 2H 2O 2CO2 + 8H 8e (21) Katot = 8H + 8e 4H 2 (22) 29
14 N. GENÇ Katotta hidrojen üretmek için yaklaşık 100mV gereklidir. 250 mv da 1 mol asetat başına 2,9 mol H 2 üretimi (ortalama olarak %73 verim) elde edilmiştir. Benzer şekilde 500 mv da asetat ile %53±3,5 verim elde edilmiştir [2]. Alg ve fotosentetik bakteri sudan ototrofik olarak hidrojen gazı üretmek için gün ışığı kullanabilir, fakat verimlilikleri düşüktür. Birçok uzman bu prosesler için yüksek yüzey alanı gerektiğinden dolayı asla uygulanabilir olamayacağı görüşündedir. Glukoz gibi karbonhidratlar ve nişasta ve selüloz gibi polisakkaritler, ortalama 2,5±4,3 m 3 /m 3 gün hızında hidrojen gazına fermente olabilirler. Fermentasyonda çözünen organik yan ürünlerin hidrojene dönüşümü endotermik reaksiyon ile olur, dış enerji girdisi olmaksızın bu moleküller hidrojene dönüşemez. Bakteri tarafından kullanılan metot ise gün ışığına bağlıdır. Yapılan çalışmalarda, mikrobiyal yakıt hücrelerini (MFC) temel alan elektroliz tipteki prosesler hidrojen gazı üretmek için kullanılabileceği ortaya çıkmıştır [37]. MFC de, bakteri organik maddeyi okside eder, CO 2 ve protonları solusyonun içine salar ve elektronları elektroda (anoda) salar. Elektronlar anoddan katoda doğru akar, katotda elektronlar oksijenin indirgenmesinde tükenir. Katotda oksijen mevcut olduğu zaman, akım üretilebilir, fakat oksijen olmadığında, akım üretimi kendilinden oluşmaz. Bununla birlikte akım üretimi anod ve katot arasında küçük voltaj uygulanması ile (pratikte >0,2V) yaratılırsa, hidrojen gazı protonların indirgenmesi ile katotda üretilir. Bu proses elektrohidrojenesis veya mikrobiyal elektroliz olarak, reaktör ise mikrobiyal elektroliz hücresi (MEC) olarak adlandırılmıştır. Đki bölmeli MEC nin şematik gösterimi Şekil 2 de verilmiştir. MEC, önceden biyokatalizlenmiş elektroliz hücresi (BEC) veya biyoelektrokimyasal olarak desteklenmiş mikrobiyal reaktör (BEAMR) olarak da ifade edilmiştir. MEC hidrojen üreten bir elektroliz reaktörüdür oysa MFC elektrik üreten bir yakıt hücresidir [37, 6, 5]. Güç kaynağı CO 2 e e H 2 H 2 Anod Katot Membran Şekil 2: Đki bölmeli MEC [37] Wagner ve diğ., (2009) tarafından yapılan çalışmada domuz gübresi atıksuyunun MEC prosesinde metan ve hidrojen üretimi incelenmiştir [38]. Atıksuyun MEC sisteminde hidrojen üretilirken başarılı bir şekilde arıtıldığı ve 0,9-1,0 m 3 /m 3 gün seviyesinde hidrojen üretildiği saptanmıştır. 30
15 Biyolojik hidrojen üretim prosesleri 2.6- Çok safhalı entegre prosesler Ham maddeden hidrojen üretiminin artırılması için çok safhalı hidrojen üretim prosesleri düşünülmüştür. Đlk olarak karanlık fermentasyonu müteakiben foto fermentasyonun olduğu iki safhalı prosesler ele alınmıştır. Üç hatta dört safhalı farklı şekillerde de olabileceği ifade edilmiştir. Bu proseste biyokütle ilk olarak karanlık fermentasyon reaktörüne beslenir, reaktörün çıkışı yüksek organik asit içeriğinde olduğu için fotofermentasyon prosesine gönderilir. Bu proses asıl olarak kızıl ötesi ışığı kullandığı için güneş ışığı önce direkt fotoliz reaktöründen (burada görünür ışık kullanılır, fakat kızıl ötesi ışığı kullanılmaz) filtrelenir. Daha ileri safha olarak ise mikrobiyal elektroliz hücresinin kullanımı önerilmiştir [6]. Çeşitli hidrojen üretim metotları içinde karanlık fermentasyon düşük enerji gereksinimi, yüksek hidrojen verimi, organik atık maddenin kullanılabilirliği gibi sebeplerden dolayı en çok tercih edilendir. Ancak elde edilen çıktı metan üretimi için uygun bir substrat olan yüksek VFA lar içeriyor olması bir dezavantaj oluşturur. Bunu önlemek için önerilen iki safhalı anaerobik sistem, fermentatif hidrojen üretimi ve metan fermentasyonundan oluşur [30, 39, 40]. Hidrojen ve metan üretimi ayrı reaktörlerde gerçekleşir. Böyle sistemlerde ilk safhada yavaş büyüyen asidojenler ve hidrojen üreten organizmalar bulunur. Burada VFA lar ve hidrojen üretilir. Đkinci safhada yavaş büyüyen asetojenler ve metanojenler bulunur, bu safhada VFA lar metan ve CO 2 ye dönüşür. Wang ve Zhao, (2009) tarafından besin atıklarının iki safhalı anaerobik arıtımı incelenmiştir [41]. En uygun şartlar altında en yüksek H 2 ve CH 4 verimleri sırası ile 0,065 ve 0,546 m 3 /kg uçucu katı gün olmuştur. Teorik en yüksek verimleri ise 0,118±0,001 ve 0,611±0,015 m 3 /kg uçucu katı olmuştur. Biyoparçalanabilirlik analizleri ise giren KOĐ nin %5,78 inin ilk safhada hidrojene dönüştüğü, ikinci safhada ise giren KOĐ inin %82,18 inin metana dönüştüğü bulunmuştur. Sonuç Biyohidrojen üretimi konusunda yapılan çalışmalar farklı işletme şartlarında (reaktör tipi, çevresel şartlar, kullanılan substarat vb.) yapıldığı için elde edilen sonuçların karşılaştırılması güçtür. Tablo 1 de farklı biyohidrojen yöntemlerinin hidrojen üretim, hızları avantaj ve dezavantajları ile birlikte sunulmuştur. Pratikte etkili ve ekonomik olarak uygun bir hidrojen üretim prosesinin işetilmesi son derece önemli bir konudur. Bu yönde çeşitli stratejiler açıklanmıştır. Organik substratların karanlık fermentatif dönüşümü ile veya foto-biyolojik prosesle H 2 üretimi iki işlevinden (substrat giderimi ve H 2 üretimi) dolayı çok önemlidir. Fermentasyonla H 2 üretimi metabolik ürün olarak organik asit oluşumu ile birlikte görülür, ancak bu mikroorganizmalar asitleri parçalayamaz. Bu eriyen asit metabolitlerinin oluşumu ve birikimi sistemde ph ın aşırı düşmesine sebep olur ve H 2 üretim prosesini engeller. Asidofilik şartlar metanojenik prosesi baskılar ve organik kaynaklardan H 2 formunda enerji dönüşümü sadece %15 seviyelerinde kalır. Atıksuda kullanılmayan karbon kaynağının ilave hidrojen üretimi için kullanımı, prosesin pratik uygulanabilirliğini destekleyecektir [36]. Biyolojik yöntemler içinde karanlık fermentasyon, yenilenebilir hidrojen üretiminde etkili bir yoldur. Bunun birkaç sebebi vardır. Đlki substrat olarak kolaylıkla bulunabilen 31
16 N. GENÇ atığı kullanıyor olmasıdır. Gerekli reaktörün tasarımı basittir ve çok iyi bilinen anaerobik arıtımı temel alan bir teknolojiyi kullanır. Bu prosesin en uygun şartlarda işletimi için biyoproses parametrelerinin analizi yapılmalı, rekabet edici reaksiyonlar önlenmeli, H 2 kısmı basıncı azaltılmalı ve termofilik türlerin kullanımı teşvik edilmelidir. Fermentatif parçalanmada substrat dönüşümünü tamamlamak için ikinci safha olarak uygulanabilecek prosesler önerilmiştir, bunlar metan fermentasyonu, fotofermentasyon ve MEC dır[42]. Tablo 1: Biyohidrojen üretim proseslerinin karşılaştırılması [5, 6] Proses Avantajları Dezavantajları Direkt biyofotoliz Đndirekt biyofotoliz Fotofermentasyon Karanlık fermentasyon Su ve güneş ışığından direkt olarak H 2 üretilebilir, güneş enerjisi dönüşümü oldukça yüksektir. Cyanobacteria sudan H 2 üretebilir, nitrojenaz enzimi H 2 üreten ana enzimdir Farklı atık madde ve geniş spektrumdaki ışık kullanılabilir Işık olmaksızın tüm gün boyunca H 2 üretilebilir. Farklı karbon kaynakları substrat olarak kullanılabilir, yan ürün olarak değerli metabolitler üretir, anaerobik prosesdir, bu yüzden oksijenin sınırlanması problemi yoktur. Yüksek ışık yoğunluğu gerekli, O 2 sistem için zararlı, düşük fotokimyasal verimlilik elde edilir. H 2 parçalanmasını durdurmak için hidrojeni uzaklaştıran hidrojenaz enzimi giderilmelidir. O 2 nitrojenaz üzerinde inhibitor etki yaratır. Işık dönüşüm verimliliği çok düşüktür, sadece %1-5 Fermentör çıkışının daha ileri arıtımına ihtiyaç vardır. O 2, hidrojenaz için kuvvetli bir engelleyicidir. Üretilen gaz karışımı CO 2 içerir, özel ayırma teknikleri ile ayrılması gerekir H 2 üretim hızı (mmol/l saat) 0,07 0,355 0,16 8,2-121 Biyolojik hidrojen üretim prosesleri düşük verim ve üretim hızlarına sahip oluşu, bu proseslerin pratik uygulamalarında büyük bir engel oluşturmaktadır. Substrattaki karbon ve protonun üçte ikisi diğer ürünlere dönüşür. Hidrojen üretim hızı ve verimini artırmak için birkaç yaklaşım önerilmiştir. Bu yaklaşımlardan ilki geleneksel üretim tekniklerinde biohidrojen üretiminin artırılması olarak ele alınmıştır. Bu kapsamda reaktörün tipi ve mikrobiyal kültür seçimi, mevcut metabolik yolizinde değişikliklerin sağlanması ele alınmıştır. Đkinci yaklaşımda ise substrat dönüşümünün tamamlanması düşünülmektedir. Pratik biohidrojen fermentasyon prosesi ya stokiyometrik dönüşümü sağlayacak ilave yolizlerinin girişimi ile yada iki safhalı sistemlerin geliştirilmesi ile sağlanabilecektir [43]. Hidrojen üreten bakterinin üretilmesi üzerine yeni tekniklerin gelişiyor olması, olağan dışı mikroorganizma ve enzim türleri üzerine çalışmaların yoğunlaşmış olması ve modern biyoteknoloji ile hidrojen üretim verimliliğinin artırılması hidrojen enerjisinin geleceği açısından ümit verici yeniliklerdir [23]. Biyolojik hidrojen üretim proseslerinin geniş aralıkta yenilenebilir substart kaynakları kullanılarak yüksek hidrojen verimliliğinde işletilmesi ile büyük ölçekte uygulanabilirliği artacaktır [44]. Hidrojen yenilenebilir biyokütleden üretilmesi durumunda yenilenebilir temiz enerji taşıyıcısı olarak kabul edilir. Bu kapsamda özellikle tarımsal atıkalar, evsel ve evsel nitelikli endüstriyel atıklar öncelikle düşünülmelidir. Gıda işleme proseslerinden 32
17 Biyolojik hidrojen üretim prosesleri kaynaklanan atıklar, yüksek karbonhidrat, protein ve lipit içeriğinde dolayı alternatif enerji üretimi için büyük potansiyele sahiptir. Bununla birlikte gida işleme atıklarının etkili kullanımı için atığın ana bileşenlerinin dikkatli analizi ve olası dönüşüm proseslerinin (termal, kimyasal ve biyolojik enerji prosesleri) ekonomik analizi yapılmalıdır. Örneğin süt işleme atıksuları hem laktik asit ve propiyonik asit gibi değerli kimyasalların üretiminde kullanılabilir, hem de etanol, metan veya hidrojen üretiminde de kullanılabir. Atıklar için dönüşüm prosesi tasarlanacağı zaman tüm olası problemler ve oluşabilecek ilave maliyetler göz önünde bulundurulmalıdır. Ekonomik ve çevresel faydalar sağlayan prosesi seçmek için, proses tasarımında ekonomik analizler yapılmalıdır. Enerji dönüşüm metodu belirleneceği zaman, atığın potansiyelini optimize etmek için farklı enerji formları arasında en iyi seçenek analiz edilmelidir. Yüksek protein ve\veya yağ asiti içeren atıklar ile hidrojen fermentasyonu ve gazlaştırma metotları, etanol ve metan üretiminden daha uygun olacaktır. Enerji üretim verimliliğini en yükseğe çıkarmak ve potansiyel problemleri en aza indirmek için farklı proseslerin bileşimi düşünülebilir [45]. Kaynaklar [1] Das, D. ve Veziroğlu, T.N., Hydrogen production by biological processes: a survey of literature, International Journal of Hydrogen Energy, 26, 13-28, (2001). [2] Manish, S. ve Banerjee, R., Comparison of biohydrogen production processes, International Journal of Hydrogen Energy, 33, , (2008). [3] Kapdan, Đ.K. ve Kargi, F., Bio-hydrogen production from waste materials, Enzyme and Microbial Technology, 38, , (2006). [4] Benemann, J.R., Hydrogen production by microalgae, Journal of Applied Phycology, 12, , (2000). [5] Das, D. ve Veziroğlu, T.N., Advances in biological hydrogen production processes, International Journal of Hydrogen Energy, 33, , (2008). [6] Holladay, J. D., Hu, J., King, D. L. ve Wang, Y., An overview of hydrogen production Technologies, Catalysis Today, 139, , (2009). [7] Melnicki, M. R., Bianchi, L., Philippis, R. D. ve Melis, A., Hydrogen production during stationary phase in purple photosynthetic bacteria, International Journal of Hydrogen Energy, 2008, 33, , (2008). [8] Basak, N. ve Das, D., Photofermentative hydrogen production using purple nonsulfur bacteria Rhodobacter sphaeroides O.U.001 in an annular photobioreactor: A case study, Biomass and Bioenergy, 33, (2009). [9] Kapdan, Đ. K., Kargı, F., Öztekin, R. ve Argun, H., Bio-hydrogen production from acid hydrolyzed wheat starch by photo-fermentation using different Rhodobacter sp, International Journal of Hydrogen Energy, 34, , (2009). 33
18 N. GENÇ [10] Uyar, B., Eroğlu, Đ. ve Yücel, M., Gündüz, U., Photofermentative hydrogen production from volatile fatty acids present in dark fermentation effluents, International Journal of Hydrogen Energy, 34, , (2009). [11] Nath, K. ve Das, D., Effect of light intensity and initial ph during hydrogen production by an integrated dark and photofermentation process, International Journal of Hydrogen Energy, 2009, doi: /j.ijhydene [12] Obeid, J., Magnin, J. P., Flaus, J. M., Adrot, O., Willison, J. C. ve Zlatev, R., Modelling of hydrogen production in batch cultures of the photosynthetic bacterium Rhodobacter capsulatus, International Journal of Hydrogen Energy, 34, , (2009). [13] Li, J., Zheng, G., He, J., Chang, S. ve Qin, Z., Hydrogen-producing capability of anaerobic activated sludge in three types of fermentations in a continuous stirred-tank reactor, Biotechnology Advances, 27, , (2009). [14] Urbaniec, K. ve Grabarczyk, R., Raw materials for fermentative hydrogen production, Journal of Cleaner Production,17, , (2009). [15] Davila-Vazquez, G., Alatriste-Mondragon, F., de Leon-Rodriguez, A. ve Razo- Flores, E, Fermentative hydrogen production in batch experiments using lactose, cheese whey and glucose: Influence of initial substrate concentration and ph, International Journal of Hydrogen Energy, 33, , (2008). [16] Chen, W.H., Sung, S. ve Chen, S.Y., Biological hydrogen production in an anaerobic sequencing batch reactor: ph and cyclic duration effect, International Journal of Hydrogen Energy, 34, , (2009). [17] Argun, H., Kargi, F. ve Kapdan, Đ.K., Öztekin, R, Batch dark fermentation of powdered wheat starch to hydrogen gas: Effects of the initial substrate and biomass concentrations, International Journal of Hydrogen Energy,33, , (2008). [18] Lin, C.Y., Chang, C.C. ve Hung, C.H., Fermentative hydrogen production from starch using natural mixed culture, International Journal of Hydrogen Energy, 33, , (2008). [19] Lin, C.Y. ve Hung, W.C., Enhancement of fermentative hydrogen/ethanol production from cellulose using mixed anaerobic cultures, International Journal of Hydrogen Energy, 33, , (2008). [20] Magnusson, L., Islam, R., Sparling, R., Levin, D. ve Çiçek, N., Direct hydrogen production from cellulosic waste materials with a single-step dark fermentation process, International Journal of Hydrogen Energy, 33, , (2008). [21] Wang, J. ve Wan, W., Factors influencing fermentative hydrogen production: A review, International Journal of Hydrogen Energy,34, , (2009). 34
19 Biyolojik hidrojen üretim prosesleri [22] Chong, M.L., Sabaratnam, V., Shirai, Y. ve Hassan, M.A., Biohydrogen production from biomass and industrial wastes by dark fermentation, International Journal of Hydrogen Energy,34, , (2009). [23] Liu, X., Ren, N., Song, F., Yang, C. ve Wang, A., Recent advances in fermentative biohydrogen production, Progress in Natural Science,18, , (2008). [24] Yuan, Z., Yang, H., Zhi, X. ve Shen J., Enhancement effect of L-cysteine on dark fermentative hydrogen production, International Journal of Hydrogen Energy, 33, , (2008). [25] Davila-Vazquez, G., Cota-Navarro, C. B., Rosales-Colunga, L. M., Leon- Rodriquez, A. ve Roza-Flores, E., Continuous biohyrdogen production using cheese whey: Improving the hydrogen production rate, International Journal of Hydrogen Energy, 34, , (2009). [26] Krupp, M. ve Widmann, R., Biohydrogen production by dark fermentation: Experiences of continuous operation in large lab scale, International Journal of Hydrogen Energy, 34, , (2009). [27] Babu, V. L., Mohan, S. V. ve Sarma, P. N., Influence of reactor configuration on fermentative hydrogen production during wastewater treatment, International Journal of Hydrogen Energy, 34, , (2009). [28] Wang, B., Wan, W. ve Wang J, Effect of ammonia concentration on fermentative hydrogen production by mixed cultures, Bioresource Technology, 100, , (2009). [29] Kim, D. H., Kim, S. H. ve Shin, H. S., Sodium inhibition of fermentative hydrogen production, International Journal of Hydrogen Energy, 34, , (2009). [30] Kyazze, G., Dinsdale, R., Guwy, A.J., Hawkes, F.R., Premier, G.C. ve Hawkes, D.L., Performance characteristics of a two-stage dark fermentative system producing hydrogen and methane continuously, Biotechnology and Bioengineering, 97, , (2007). [31] Li, C. ve Fang, H.H.P., Fermentative hydrojen production from wastewater and solid wastes by mixed cultures, Critical Reviews in Environmental Science and Technology, 37, 1-39, (2007). [32] Kraemer, J.T. ve Bagley, D.M., Improving the yield from fermentative hydrogen production, Biotechnology Letters, 29, , (2007). [33] Argun, H., Kargı, F. ve Kapdan Đ.K., Hydrogen production by combined dark and light fermentation of ground wheat solution, International Journal of Hydrogen Energy, 34, , (2009). 35
20 N. GENÇ [34] Su, H., Cheng, J., Zhou, J., Song, W. ve Cen, K., Improving hydrogen production from cassava starch by combination of dark and photo fermentation, International Journal of Hydrogen Energy, 34, , (2009). [35] Belokopytov, B.F., Laurinavichius, K.S., Laurinavichene, T.V., Ghirardi, M.L., Seibert, M. ve Tsygankov, A.A., Towards the integration of dark- and photofermentative waste treatment. 2. Optimization of starch-dependent fermentative hydrogen production, International Journal of Hydrogen Energy, 34, , (2009). [36] Srikanth, S., Mohan, S.V., Devi, M.P., Peri, D. ve Sarma, P.N., Acetate and butyrate as substrates for hydrogen production through photo-fermentation: Process optimization and combined performance evaluation, International Journal of Hydrogen Energy, 2009, doi: /j.ijhydene [37] Logan, B.E., Call, D., Cheng, S., Hamelers, H.V.M., Sleutels, T.H.J.A., Jeremiasse, A.W. ve Rozendal, R.A., Microbial electrolysis cells for high yield hydrogen gas production from organic matter, Environmental Science and Technology, 42, , (2008). [38] Wagner, R.C., Regan, J.M., Oh, S.E., Zuo, Y. ve Logan, B.E., Hydrogen and methane production from swine wastewater using microbial electrolysis cells, Water Research, 43, , (2009). [39] Chu, C.F., Li, Y.Y., Xu, K.Q., Ebie, Y. ve Inamori, Y., A ph- and temperaturephase two-stage process for hydrogen and methane production from food waste, International Journal of Hydrogen Energy, 33, , (2008). [40] Xie, B., Cheng, J., Zhou, J., Song, W. ve Cen, K., Cogeneration of hydrogen and methane from glucose to improve energy conversion efficiency, International Journal of Hydrogen Energy, 33, , (2008). [41] Wang, X. ve Zhao, Y., A bench scale study of fermentative hydrogen and methane production from food waste in integrated two-stage process, International Journal of Hydrogen Energy, 34, , (2009). [42] Hallenbeck, P.C., Fermentative hydrogen production: Principles, progress and prognosis, International Journal of Hydrogen Energy, 2009, doi: /j.ijhydene [43] Hallenbeck, P.C. ve Ghosh, D., Advances in fermentative biohydrogen production: the way forward?, Trends in Biotechnology, 27, 5, , (2009). [44] Mathews, J. ve Wang, G., Metabolic pathway engineering for enhanced biohydrogen production, International Journal of Hydrogen Energy, 2009, doi: /j.ijhydene [45] Digman, B. ve Kim, D.S., Review: Alternative energy from food processing wastes, Environmental Progress, 27, , (2008). 36
33343 Yenişehir-Mersin/Türkiye
 Hidrojen Enerjisi, Üretim Mekanizmaları ve Çevresel Önemi 1 Habibe Elif GÜLŞEN, 1 Halil KUMBUR, 1 Gamze KOYUNCU 1 Mersin Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, 33343 Yenişehir-Mersin/Türkiye
Hidrojen Enerjisi, Üretim Mekanizmaları ve Çevresel Önemi 1 Habibe Elif GÜLŞEN, 1 Halil KUMBUR, 1 Gamze KOYUNCU 1 Mersin Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, 33343 Yenişehir-Mersin/Türkiye
6. BÖLÜM MİKROBİYAL METABOLİZMA
 6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
Bilinen en eski yöntemdir. Bu alanda verim yükseltme çalışmaları sürdürülmektedir.
 1) Biyokütle Dönüşüm Teknolojileri Doğrudan yakma (Direct combustion) Piroliz (Pyrolysis) Gazlaştırma (Gasification) Karbonizasyon (Carbonization) Havasız çürütme, Metanasyon (Anaerobic digestion) Fermantasyon
1) Biyokütle Dönüşüm Teknolojileri Doğrudan yakma (Direct combustion) Piroliz (Pyrolysis) Gazlaştırma (Gasification) Karbonizasyon (Carbonization) Havasız çürütme, Metanasyon (Anaerobic digestion) Fermantasyon
Solunum. Solunum ve odunsu bitkilerin büyümesi arasında yüksek bir korelasyon bulunmaktadır (Kozlowski ve Pallardy, 1997).
 SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
1. Kıyı Bölgelerinde Çevre Kirliliği ve Kontrolü KÇKK
 1. Kıyı Bölgelerinde Çevre Kirliliği ve Kontrolü KÇKK Kentsel Atıksu Arıtım Tesislerinde Geliştirilmiş Biyolojik Fosfor Giderim Verimini Etkileyen Faktörler Tolga Tunçal, Ayşegül Pala, Orhan Uslu Namık
1. Kıyı Bölgelerinde Çevre Kirliliği ve Kontrolü KÇKK Kentsel Atıksu Arıtım Tesislerinde Geliştirilmiş Biyolojik Fosfor Giderim Verimini Etkileyen Faktörler Tolga Tunçal, Ayşegül Pala, Orhan Uslu Namık
OKSİJENLİ SOLUNUM
 1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
Çizelge 2.6. Farklı ph ve su sıcaklığı değerlerinde amonyak düzeyi (toplam amonyağın yüzdesi olarak) (Boyd 2008a)
 - Azotlu bileşikler Su ürünleri yetiştiricilik sistemlerinde oksijen gereksinimi karşılandığı takdirde üretimi sınırlayan ikinci faktör azotlu bileşiklerin birikimidir. Ana azotlu bileşikler; azot gazı
- Azotlu bileşikler Su ürünleri yetiştiricilik sistemlerinde oksijen gereksinimi karşılandığı takdirde üretimi sınırlayan ikinci faktör azotlu bileşiklerin birikimidir. Ana azotlu bileşikler; azot gazı
ÇEVRE KİMYASI LABORATUVARI II DERSİ İÇİN KAYNAK NOT: BU NOTTAKİ HER BİLGİDEN SORUMLUSUNUZ.
 ÇEVRE KİMYASI LABORATUVARI II DERSİ İÇİN KAYNAK NOT: BU NOTTAKİ HER BİLGİDEN SORUMLUSUNUZ. KAYNAK : https://www.slideshare.net/tamilsilambarasan/ecology-45668344 KAYNAK : https://www.slideshare.net/tamilsilambarasan/sulphur-cycle
ÇEVRE KİMYASI LABORATUVARI II DERSİ İÇİN KAYNAK NOT: BU NOTTAKİ HER BİLGİDEN SORUMLUSUNUZ. KAYNAK : https://www.slideshare.net/tamilsilambarasan/ecology-45668344 KAYNAK : https://www.slideshare.net/tamilsilambarasan/sulphur-cycle
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
Fermentatif biyohidrojen üretim proseslerinde hidrojen veriminin geliştirilmesindeki yaklaşımlar
 5 Erciyes Üniversitesi Fen Bilimleri Enstitüsü Dergisi 6(3): 5-39 (010) Fermentatif biyohidrojen üretim proseslerinde hidrojen veriminin geliştirilmesindeki yaklaşımlar Nevim GENÇ Kocaeli Üniv., Müh. Fa.,
5 Erciyes Üniversitesi Fen Bilimleri Enstitüsü Dergisi 6(3): 5-39 (010) Fermentatif biyohidrojen üretim proseslerinde hidrojen veriminin geliştirilmesindeki yaklaşımlar Nevim GENÇ Kocaeli Üniv., Müh. Fa.,
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI
 ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 9.Çözünmüş İnorganik ve Organik Katıların Giderimi Yrd. Doç. Dr. Kadir GEDİK İnorganiklerin Giderimi Çözünmüş maddelerin çapları
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 9.Çözünmüş İnorganik ve Organik Katıların Giderimi Yrd. Doç. Dr. Kadir GEDİK İnorganiklerin Giderimi Çözünmüş maddelerin çapları
Metabolizma. Metabolizmaya giriş. Metabolizmaya giriş. Metabolizmayı tanımlayacak olursak
 Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Hücre Solunumu: Kimyasal Enerji Eldesi
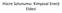 Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Biyogaz Temel Eğitimi
 Biyogaz Temel Eğitimi Sunanlar: Dursun AYDÖNER Proje Müdürü Rasim ÜNER Is Gelistime ve Pazarlama Müdürü Biyogaz Temel Eğitimi 1.Biyogaz Nedir? 2.Biyogaz Nasıl Oluşur? 3.Biyogaz Tesisi - Biyogaz Tesis Çeşitleri
Biyogaz Temel Eğitimi Sunanlar: Dursun AYDÖNER Proje Müdürü Rasim ÜNER Is Gelistime ve Pazarlama Müdürü Biyogaz Temel Eğitimi 1.Biyogaz Nedir? 2.Biyogaz Nasıl Oluşur? 3.Biyogaz Tesisi - Biyogaz Tesis Çeşitleri
Doğadaki Enerji Akışı
 Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT
 1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
Öğr. Gör. Dr. İlker BÜYÜK (Botanik, 10. Hafta): Fotosentez FOTOSENTEZ
 FOTOSENTEZ Elektron Koparılması ve Floresans Enerjisi Elektronlar negatif (e - ) ve protonlar pozitif (p + ) yüklüdür. Bu nedenle protonlar elektronları çekerler. Elektronlar ise, belli bir enerjiye sahiptir
FOTOSENTEZ Elektron Koparılması ve Floresans Enerjisi Elektronlar negatif (e - ) ve protonlar pozitif (p + ) yüklüdür. Bu nedenle protonlar elektronları çekerler. Elektronlar ise, belli bir enerjiye sahiptir
12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU
 12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU HÜCRESEL SOLUNUM HÜCRESEL SOLUNUM Besinlerin hücre içerisinde parçalanması ile ATP üretimini sağlayan mekanizmaya HÜCRESEL SOLUNUM denir. Canlılar
12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU HÜCRESEL SOLUNUM HÜCRESEL SOLUNUM Besinlerin hücre içerisinde parçalanması ile ATP üretimini sağlayan mekanizmaya HÜCRESEL SOLUNUM denir. Canlılar
Ötrifikasyon. Ötrifikasyonun Nedenleri
 Ötrifikasyon Ötrifikasyon, göllerin olgunlaşma aşamalarında meydana gelen dogal bir olay. Genç göller düşük oranlarda besin içermekte dolayısıyla biyolojik aktivite az..oligotrofik göller Yaşlı göller,
Ötrifikasyon Ötrifikasyon, göllerin olgunlaşma aşamalarında meydana gelen dogal bir olay. Genç göller düşük oranlarda besin içermekte dolayısıyla biyolojik aktivite az..oligotrofik göller Yaşlı göller,
YAKIT PİLLERİ. Cihat DEMİREL
 YAKIT PİLLERİ Cihat DEMİREL 16360030 İçindekiler Yakıt pilleri nasıl çalışır? Yakıt Pili Çalışma Prensibi Yakıt pilleri avantaj ve dezavantajları nelerdir? 2 Yakıt Pilleri Nasıl Çalışır? Tükenmez ve hiç
YAKIT PİLLERİ Cihat DEMİREL 16360030 İçindekiler Yakıt pilleri nasıl çalışır? Yakıt Pili Çalışma Prensibi Yakıt pilleri avantaj ve dezavantajları nelerdir? 2 Yakıt Pilleri Nasıl Çalışır? Tükenmez ve hiç
Akvaryum veya küçük havuzlarda amonyağın daha az zehirli olan nitrit ve nitrata dönüştürülmesi için gerekli olan bakteri populasyonunu (nitrifikasyon
 Azotlu bileşikler Ticari balık havuzlarında iyonize olmuş veya iyonize olmamış amonyağın konsantrasyonlarını azaltmak için pratik bir yöntem yoktur. Balık havuzlarında stoklama ve yemleme oranlarının azaltılması
Azotlu bileşikler Ticari balık havuzlarında iyonize olmuş veya iyonize olmamış amonyağın konsantrasyonlarını azaltmak için pratik bir yöntem yoktur. Balık havuzlarında stoklama ve yemleme oranlarının azaltılması
Organik Atıkların Değerlendirilmesi- BİYOGAZ: Üretimi ve Kullanımı ECS KĐMYA ĐNŞ. SAN. VE TĐC. LTD. ŞTĐ.
 Organik Atıkların Değerlendirilmesi- BİYOGAZ: Üretimi ve Kullanımı ECS KĐMYA ĐNŞ. SAN. VE TĐC. LTD. ŞTĐ. BİYOGAZ NEDİR? Anaerobik şartlarda, organik atıkların çeşitli mikroorganizmalarca çürütülmesi sonucu
Organik Atıkların Değerlendirilmesi- BİYOGAZ: Üretimi ve Kullanımı ECS KĐMYA ĐNŞ. SAN. VE TĐC. LTD. ŞTĐ. BİYOGAZ NEDİR? Anaerobik şartlarda, organik atıkların çeşitli mikroorganizmalarca çürütülmesi sonucu
Anaerobik fermantasyonla biyohidrojen üretim verimine etki eden faktörler
 SAÜ Fen Bil Der 19. Cilt, 2. Sayı, s. 171-186, 2015 Anaerobik fermantasyonla biyohidrojen üretim verimine etki İlknur Şentürk 1*, Hanife Büyükgüngör 2 ÖZ 01.07.2014 Geliş/Received, 24.09.2014 Kabul/Accepted
SAÜ Fen Bil Der 19. Cilt, 2. Sayı, s. 171-186, 2015 Anaerobik fermantasyonla biyohidrojen üretim verimine etki İlknur Şentürk 1*, Hanife Büyükgüngör 2 ÖZ 01.07.2014 Geliş/Received, 24.09.2014 Kabul/Accepted
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Bitkide Fosfor. Aktif alım açısından bitki tür ve çeşitleri arasında farklılıklar vardır
 Fosfor alımı ve taşınımı Kök hücreleri ve > Bitkide Fosfor ksilem özsuyunun P kapsamı > toprak çözeltisinin P kapsamı (100-1000 kat) P alımı aktif alım şeklinde gerçekleşir Aktif alım açısından bitki tür
Fosfor alımı ve taşınımı Kök hücreleri ve > Bitkide Fosfor ksilem özsuyunun P kapsamı > toprak çözeltisinin P kapsamı (100-1000 kat) P alımı aktif alım şeklinde gerçekleşir Aktif alım açısından bitki tür
Katı Atık Yönetiminde Arıtma Çamuru. Enes KELEŞ Kasım / 2014
 Katı Atık Yönetiminde Arıtma Çamuru Enes KELEŞ Kasım / 2014 İÇİNDEKİLER Arıtma Çamuru Nedir? Arıtma Çamuru Nerede Oluşur? Arıtma Çamuru Çeşitleri Arıtma Çamuru Nerelerde Değerlendirilebilir? 1. Açık Alanda
Katı Atık Yönetiminde Arıtma Çamuru Enes KELEŞ Kasım / 2014 İÇİNDEKİLER Arıtma Çamuru Nedir? Arıtma Çamuru Nerede Oluşur? Arıtma Çamuru Çeşitleri Arıtma Çamuru Nerelerde Değerlendirilebilir? 1. Açık Alanda
YAZILIYA HAZIRLIK SORULARI. 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ
 YAZILIYA HAZIRLIK SORULARI 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ Fotosentez ile ışık enerjisi kimyasal bağ enerjisine dönüştürülür. Kloroplastsız hücreler fotosentez yapamaz. DOĞRU YANLIŞ SORULARI
YAZILIYA HAZIRLIK SORULARI 11. Sınıf 1 CANLILARDA ENERJİ DÖNÜŞÜMLERİ Fotosentez ile ışık enerjisi kimyasal bağ enerjisine dönüştürülür. Kloroplastsız hücreler fotosentez yapamaz. DOĞRU YANLIŞ SORULARI
2. Kanun- Enerji dönüşümü sırasında bir miktar kullanılabilir kullanılamayan enerji ısı olarak kaybolur.
 Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
FERMENTASYON. Bir maddenin bakteriler, mantarlarve diğer mikroorganizmalar aracılığıyla, genellikle ısı vererek ve köpürerek
 FERMENTASYON Bir maddenin bakteriler, mantarlarve diğer mikroorganizmalar aracılığıyla, genellikle ısı vererek ve köpürerek kimyasal olarak çürümesi olayıdır Fermantasyon anaerobik şartlarda, glikoliz
FERMENTASYON Bir maddenin bakteriler, mantarlarve diğer mikroorganizmalar aracılığıyla, genellikle ısı vererek ve köpürerek kimyasal olarak çürümesi olayıdır Fermantasyon anaerobik şartlarda, glikoliz
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ
 HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
BİYOKÜTLE ÇEVRİM YÖNTEMLERİ
 BİYOKÜTLE ÇEVRİM YÖNTEMLERİ BİYOKÜTLE ÇEVRİM YÖNTEMLERİ YAKITLAR UYGULAMA ALANLARI ORMAN ATIKLARI HAVASIZ ÇÜRÜTME BİYOGAZ ELEKTRİK ÜRETİMİ TARIM ATIKLARI PİROLİZ ETANOL ISINMA ENERJİ BİTKİLERİ DOĞRUDAN
BİYOKÜTLE ÇEVRİM YÖNTEMLERİ BİYOKÜTLE ÇEVRİM YÖNTEMLERİ YAKITLAR UYGULAMA ALANLARI ORMAN ATIKLARI HAVASIZ ÇÜRÜTME BİYOGAZ ELEKTRİK ÜRETİMİ TARIM ATIKLARI PİROLİZ ETANOL ISINMA ENERJİ BİTKİLERİ DOĞRUDAN
Solunumda organik bileşikler karbondioksite yükseltgenir ve absorbe edilen oksijen ise suya indirgenir.
 Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Kojenerasyon Teknolojileri Yavuz Aydın, Yağmur Bozkurt İTÜ
 Kojenerasyon Teknolojileri Yavuz Aydın, Yağmur Bozkurt 13.04.2017 - İTÜ 11.04.2017 2 Kombine Çevrim Santraller Temel amaç elektrik üretimidir En son teknolojilerle ulaşılan çevrim verimi %62 civarındadır.
Kojenerasyon Teknolojileri Yavuz Aydın, Yağmur Bozkurt 13.04.2017 - İTÜ 11.04.2017 2 Kombine Çevrim Santraller Temel amaç elektrik üretimidir En son teknolojilerle ulaşılan çevrim verimi %62 civarındadır.
WASTEWATER TREATMENT PLANT DESIGN
 WASTEWATER TREATMENT PLANT DESIGN Prof.Dr. Özer ÇINAR İstanbul, Turkey 1 2 Aktif Çamur Prosesi Kirleticilerin, mikroorganizmalar tarafından besin ve enerji kaynağı olarak kullanılmak suretiyle atıksudan
WASTEWATER TREATMENT PLANT DESIGN Prof.Dr. Özer ÇINAR İstanbul, Turkey 1 2 Aktif Çamur Prosesi Kirleticilerin, mikroorganizmalar tarafından besin ve enerji kaynağı olarak kullanılmak suretiyle atıksudan
Sigma 28, 369-395, 2010 Review Paper / Derleme Makalesi AN EXAMINATION OF USED DIFFERENT WASTE MATERIALS AND BIOHYDROGEN PRODUCTION METHODS
 Journal of Engineering and Natural Sciences Mühendislik ve Fen Bilimleri Dergisi Sigma 28, 369-395, 2010 Review Paper / Derleme Makalesi AN EXAMINATION OF USED DIFFERENT WASTE MATERIALS AND BIOHYDROGEN
Journal of Engineering and Natural Sciences Mühendislik ve Fen Bilimleri Dergisi Sigma 28, 369-395, 2010 Review Paper / Derleme Makalesi AN EXAMINATION OF USED DIFFERENT WASTE MATERIALS AND BIOHYDROGEN
KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ
 Ek 2 ULUSAL ÖĞRENCİ TASARIM YARIŞMASI PROBLEM TANIMI KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ 1. Giriş Türk kömür rezervlerinden metanol üretimi Kömürden metanol üretimi,
Ek 2 ULUSAL ÖĞRENCİ TASARIM YARIŞMASI PROBLEM TANIMI KÖMÜRÜN GAZLAŞTIRILMASI YOLUYLA ELDE EDİLEN SENTEZ GAZINDAN METANOL ÜRETİMİ 1. Giriş Türk kömür rezervlerinden metanol üretimi Kömürden metanol üretimi,
11. SINIF KONU ANLATIMI 2 ATP-2
 11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU
 13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
Ayxmaz/biyoloji. Azot döngüsü. Azot kaynakları 1. Atmosfer 2. Su 3. Kara 4. Canlılar. Azot döngüsü
 Azot döngüsü Azot kaynakları 1. Atmosfer 2. Su 3. Kara 4. Canlılar Azot döngüsü 1. Azot bitkiler tarafından organik moleküllerin (A.asit,organik baz vb.)yapısına katılır. 2. Bitkiler azotu sadece NO3-
Azot döngüsü Azot kaynakları 1. Atmosfer 2. Su 3. Kara 4. Canlılar Azot döngüsü 1. Azot bitkiler tarafından organik moleküllerin (A.asit,organik baz vb.)yapısına katılır. 2. Bitkiler azotu sadece NO3-
FOTOSENTEZ. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal bağ enerjisine çeviren olaydır.
 1 FOTOSENTEZ *Fotosentez: Klorofilli canlıların, ışık enerjisini kullanarak; inorganik maddelerden organik besin sentezlemesine fotosentez denir. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal
1 FOTOSENTEZ *Fotosentez: Klorofilli canlıların, ışık enerjisini kullanarak; inorganik maddelerden organik besin sentezlemesine fotosentez denir. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal
Özel Formülasyon DAHA İYİ DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
 Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
BİYOKÜTLE ENERJİ SANTRALİ BİOKAREN ENERJİ
 BİYOKÜTLE ENERJİ SANTRALİ BİOKAREN ENERJİ BİYOKÜTLE SEKTÖRÜ Türkiye birincil enerji tüketimi 2012 yılında 121 milyon TEP e ulaşmış ve bu rakamın yüzde 82 si ithalat yoluyla karşılanmıştır. Bununla birlikte,
BİYOKÜTLE ENERJİ SANTRALİ BİOKAREN ENERJİ BİYOKÜTLE SEKTÖRÜ Türkiye birincil enerji tüketimi 2012 yılında 121 milyon TEP e ulaşmış ve bu rakamın yüzde 82 si ithalat yoluyla karşılanmıştır. Bununla birlikte,
Biyolojik Besi Maddesi Gideren Atıksu Arıtma Tesisi Geri Devir Çamurunda Farklı Dezentegrasyon Uygulamalarının İncelenmesi
 Biyolojik Besi Maddesi Gideren Atıksu Arıtma Tesisi Geri Devir Çamurunda Farklı Dezentegrasyon Uygulamalarının İncelenmesi Nevin Yağcı, Işıl Akpınar İstanbul Teknik Üniversitesi, İnşaat Fakültesi, Çevre
Biyolojik Besi Maddesi Gideren Atıksu Arıtma Tesisi Geri Devir Çamurunda Farklı Dezentegrasyon Uygulamalarının İncelenmesi Nevin Yağcı, Işıl Akpınar İstanbul Teknik Üniversitesi, İnşaat Fakültesi, Çevre
BARTIN ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ METALURJİ VE MALZEME MÜHENDİSLİĞİ MALZEME LABORATUARI II DERSİ AKIMLI VE AKIMSIZ KAPLAMALAR DENEY FÖYÜ
 BARTIN ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ METALURJİ VE MALZEME MÜHENDİSLİĞİ MALZEME LABORATUARI II DERSİ AKIMLI VE AKIMSIZ KAPLAMALAR DENEY FÖYÜ Gelişen teknoloji ile beraber birçok endüstri alanında kullanılabilecek
BARTIN ÜNİVERSİTESİ MÜHENDİSLİK FAKÜLTESİ METALURJİ VE MALZEME MÜHENDİSLİĞİ MALZEME LABORATUARI II DERSİ AKIMLI VE AKIMSIZ KAPLAMALAR DENEY FÖYÜ Gelişen teknoloji ile beraber birçok endüstri alanında kullanılabilecek
HÜCRESEL SOLUNUM OKSİJENSİZ SOLUNUM
 1 HÜCRESEL SOLUNUM *Hücresel solunum: Besinlerin parçalanarak ATP sentezlenmesine, hücresel solunum denir. ----------------------- OKSİJENSİZ SOLUNUM ----------------------- (ANAEROBİK SOLUNUM = FERMANTASYON)
1 HÜCRESEL SOLUNUM *Hücresel solunum: Besinlerin parçalanarak ATP sentezlenmesine, hücresel solunum denir. ----------------------- OKSİJENSİZ SOLUNUM ----------------------- (ANAEROBİK SOLUNUM = FERMANTASYON)
Elçin GÜNEŞ, Ezgi AYDOĞAR
 Elçin GÜNEŞ, Ezgi AYDOĞAR AMAÇ Çorlu katı atık depolama sahası sızıntı sularının ön arıtma alternatifi olarak koagülasyon-flokülasyon yöntemi ile arıtılabilirliğinin değerlendirilmesi Arıtma alternatifleri
Elçin GÜNEŞ, Ezgi AYDOĞAR AMAÇ Çorlu katı atık depolama sahası sızıntı sularının ön arıtma alternatifi olarak koagülasyon-flokülasyon yöntemi ile arıtılabilirliğinin değerlendirilmesi Arıtma alternatifleri
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
İLERİ ARITIM YÖNTEMLERİNDEN FENTON REAKTİFİ PROSESİ İLE ENDÜSTRİYEL BİR ATIK SUYUN ISLAK HAVA OKSİDASYONU
 İLERİ ARITIM YÖNTEMLERİNDEN FENTON REAKTİFİ PROSESİ İLE ENDÜSTRİYEL BİR ATIK SUYUN ISLAK HAVA OKSİDASYONU Gülin AYTİMUR, Süheyda ATALAY Ege Üniversitesi Müh. Fak. Kimya Müh. Bölümü 351-Bornova İzmir ÖZET
İLERİ ARITIM YÖNTEMLERİNDEN FENTON REAKTİFİ PROSESİ İLE ENDÜSTRİYEL BİR ATIK SUYUN ISLAK HAVA OKSİDASYONU Gülin AYTİMUR, Süheyda ATALAY Ege Üniversitesi Müh. Fak. Kimya Müh. Bölümü 351-Bornova İzmir ÖZET
Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol)
 hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
ayxmaz/biyoloji Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H
 Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Stres Koşulları ve Bitkilerin Tepkisi
 Stres Koşulları ve Bitkilerin Tepkisi Stres nedir? Olumsuz koşullara karşı canlıların vermiş oldukları tepkiye stres denir. Olumsuz çevre koşulları bitkilerde strese neden olur. «Biyolojik Stres»: Yetişme
Stres Koşulları ve Bitkilerin Tepkisi Stres nedir? Olumsuz koşullara karşı canlıların vermiş oldukları tepkiye stres denir. Olumsuz çevre koşulları bitkilerde strese neden olur. «Biyolojik Stres»: Yetişme
BİYODİZEL BİYOETANOL BİYOGAZ
 BİYODİZEL BİYOETANOL BİYOGAZ Prof. Dr. Bülent B KESKİNLER BİYODİZEL Biyodizel Üretim Prosesleri Kesikli (500-10000 ton/yıl) Yarı kesikli Sürekli (>30000 ton/yıl) 1. Homojen Kataliz a) Asit katalizör: H
BİYODİZEL BİYOETANOL BİYOGAZ Prof. Dr. Bülent B KESKİNLER BİYODİZEL Biyodizel Üretim Prosesleri Kesikli (500-10000 ton/yıl) Yarı kesikli Sürekli (>30000 ton/yıl) 1. Homojen Kataliz a) Asit katalizör: H
ayxmaz/lisebiyoloji.com
 Adı/Soyadı: Sınıf/No: / Fotosentez İnceleme Çalışma 1. Verilen terimleri kullanarak aşağıdaki ifadeleri tamamlayın. A.Terimler: Klorofil, Kloroplast, Mavi ve kırmızı ışık dalgalarının,yeşil ışık dalgalarının,
Adı/Soyadı: Sınıf/No: / Fotosentez İnceleme Çalışma 1. Verilen terimleri kullanarak aşağıdaki ifadeleri tamamlayın. A.Terimler: Klorofil, Kloroplast, Mavi ve kırmızı ışık dalgalarının,yeşil ışık dalgalarının,
ÜNİTE 7 : HÜCRESEL SOLUNUM
 ÜNİTE 7 : HÜCRESEL SOLUNUM Yaşam için gerekli enerjinin tümü güneşten gelir.güneşte hidrojen füzyonla helyuma dönüşür ve ışık üretilir.yeşil bitkiler güneş ışığının enerjisini fotosentezle glukozdaki kimyasal
ÜNİTE 7 : HÜCRESEL SOLUNUM Yaşam için gerekli enerjinin tümü güneşten gelir.güneşte hidrojen füzyonla helyuma dönüşür ve ışık üretilir.yeşil bitkiler güneş ışığının enerjisini fotosentezle glukozdaki kimyasal
YAZILIYA HAZIRLIK SORULARI. 9. Sınıf
 YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
Ekosistem ve Özellikleri
 Ekosistem ve Özellikleri Öğr. Gör. Özgür ZEYDAN http://cevre.beun.edu.tr/zeydan/ Ekosistem Belirli bir bölgede yaşayan ve birbirleriyle sürekli etkileşim halindeki canlılar (biyotik faktörler) ve cansız
Ekosistem ve Özellikleri Öğr. Gör. Özgür ZEYDAN http://cevre.beun.edu.tr/zeydan/ Ekosistem Belirli bir bölgede yaşayan ve birbirleriyle sürekli etkileşim halindeki canlılar (biyotik faktörler) ve cansız
GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER
 GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER Mikroorganizmaların gıdalarla gelişmesi; Gıdanın karekteristik özelliğine, Gıdada bulunan m.o lara ve bunlar arası etkileşime, Çevre koşullarına bağlı
GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER Mikroorganizmaların gıdalarla gelişmesi; Gıdanın karekteristik özelliğine, Gıdada bulunan m.o lara ve bunlar arası etkileşime, Çevre koşullarına bağlı
KATI ATIKLARIN ARITILMASINDA MİKROORGANİZMALARIN KULLANIMI
 ÇEVREYE ZARAR VEREN MADDELERİN ORTADAN KALDIRILMASINDA MİKROORGANİZMALARIN KULLANIMI ÖZET Mikroorganizmalar, çıplak gözle görülemeyecek kadar küçük ve tek hücreli canlılardır. Bakteriler, mayalar, küfler,
ÇEVREYE ZARAR VEREN MADDELERİN ORTADAN KALDIRILMASINDA MİKROORGANİZMALARIN KULLANIMI ÖZET Mikroorganizmalar, çıplak gözle görülemeyecek kadar küçük ve tek hücreli canlılardır. Bakteriler, mayalar, küfler,
GIDA BİYOTEKNOLOJİSİ UYGULAMA DERSİ NO:5 Enzim Analizleri
 1. Enzimler GIDA BİYOTEKNOLOJİSİ UYGULAMA DERSİ NO:5 Enzim Analizleri Enzimler, hücreler ve organizmalardaki reaksiyonları katalizleyen ve kontrol eden protein yapısındaki bileşiklerdir. Reaksiyon hızını
1. Enzimler GIDA BİYOTEKNOLOJİSİ UYGULAMA DERSİ NO:5 Enzim Analizleri Enzimler, hücreler ve organizmalardaki reaksiyonları katalizleyen ve kontrol eden protein yapısındaki bileşiklerdir. Reaksiyon hızını
BİYOKÜTLEDEN FOTOSENTETİK BAKTERİLERLE HİDROJEN ÜRETİMİ
 BİYOKÜTLEDEN FOTOSENTETİK BAKTERİLERLE HİDROJEN ÜRETİMİ Inci Eroglu, Kimya Mühendisliği Bölümü ve Biyoteknoloji EABD, ODTÜ Meral Yücel, Biyoloji Bölümü ve Biyoteknoloji EABD, ODTÜ Ufuk Gündüz, Biyoloji
BİYOKÜTLEDEN FOTOSENTETİK BAKTERİLERLE HİDROJEN ÜRETİMİ Inci Eroglu, Kimya Mühendisliği Bölümü ve Biyoteknoloji EABD, ODTÜ Meral Yücel, Biyoloji Bölümü ve Biyoteknoloji EABD, ODTÜ Ufuk Gündüz, Biyoloji
YAZILIYA HAZIRLIK TEST SORULARI. 11. Sınıf
 YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
BİTKİ BESİN MADDELERİ (BBM)
 BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul [email protected] Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
BİTKİ BESİN MADDELERİ (BBM) Toprak Bilgisi Dersi Prof. Dr. Günay Erpul [email protected] Işık Enerjisinin Kimyasal Enerjiye Dönüştürülmesi Fotosentez, karbon (C), oksijen (O) ve hidrojen (H) atomlarını
HAKKIMIZDA. Firmamız 2006 yılının Ocak ayında arıtma sistemleri kurmak ve çevre teknolojilerini geliştirmek amacıyla kurulmuştur.
 01 HAKKIMIZDA Firmamız 2006 yılının Ocak ayında arıtma sistemleri kurmak ve çevre teknolojilerini geliştirmek amacıyla kurulmuştur. Multiclair, temel prensip olarak Elektroflokülasyon yöntemini kullanan
01 HAKKIMIZDA Firmamız 2006 yılının Ocak ayında arıtma sistemleri kurmak ve çevre teknolojilerini geliştirmek amacıyla kurulmuştur. Multiclair, temel prensip olarak Elektroflokülasyon yöntemini kullanan
Biyokütle Nedir? fosil olmayan
 Biyokütle Enerjisi Biyokütle Nedir? Yeşil bitkilerin güneş enerjisini fotosentez yolu ile kimyasal enerjiye dönüştürerek depolaması sonucu oluşan biyolojik kütle, biyolojik kökenli fosil olmayan organik
Biyokütle Enerjisi Biyokütle Nedir? Yeşil bitkilerin güneş enerjisini fotosentez yolu ile kimyasal enerjiye dönüştürerek depolaması sonucu oluşan biyolojik kütle, biyolojik kökenli fosil olmayan organik
Serbest radikallerin etkileri ve oluşum mekanizmaları
 Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
İÇİNDEKİLER 2
 Özgür Deniz KOÇ 1 İÇİNDEKİLER 2 3 4 5 6 Elektrotlar Katalizörler Elektrolit Çalışma Sıcaklığı Karbon Nikel, Ag, Metal oksit, Soy Metaller KOH(potasyum hidroksit) Çözeltisi 60-90 C (pot. 20-250 C) Verimlilik
Özgür Deniz KOÇ 1 İÇİNDEKİLER 2 3 4 5 6 Elektrotlar Katalizörler Elektrolit Çalışma Sıcaklığı Karbon Nikel, Ag, Metal oksit, Soy Metaller KOH(potasyum hidroksit) Çözeltisi 60-90 C (pot. 20-250 C) Verimlilik
FOTOSENTEZ C 6 H 12 O 6 + 6 O 2. Fotosentez yapan canlılar: - Bitkiler - Mavi yeşil algler - Bazı bakteriler - Bazı protistalar. Glikoz IŞIK KLOROFİL
 Fotosentez FOTOSENTEZ Işık enerjisinin kullanılarak organik bileşiklerin üretilmesidir. Yeşil yapraklı bitkilerin inorganik maddelerden (H 2 O, CO 2 ), ışık enerjisi ve klorofil yardımı ile organik besin
Fotosentez FOTOSENTEZ Işık enerjisinin kullanılarak organik bileşiklerin üretilmesidir. Yeşil yapraklı bitkilerin inorganik maddelerden (H 2 O, CO 2 ), ışık enerjisi ve klorofil yardımı ile organik besin
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
BİTKİLERDE SOLUNUM REAKSİYONLARI. Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi
 BİTKİLERDE SOLUNUM REAKSİYONLARI Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi Havanın serbest O2 kullanarak bitki hücrelerinde şekerlerin, yağların ya da diğer organik moleküllerin oksitlenmesi
BİTKİLERDE SOLUNUM REAKSİYONLARI Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi Havanın serbest O2 kullanarak bitki hücrelerinde şekerlerin, yağların ya da diğer organik moleküllerin oksitlenmesi
Prof. Dr. Filiz Özçelik. Ankara Üniversitesi Mühendislik Fakültesi Gıda Mühendisliği Bölümü
 Prof. Dr. Filiz Özçelik Ankara Üniversitesi Mühendislik Fakültesi Gıda Mühendisliği Bölümü Fermantasyon Nedir? Mikroorganizmaların enerji temin etme yolları Solunum: Son elektron (H) alıcısı (akseptörü)oksijen
Prof. Dr. Filiz Özçelik Ankara Üniversitesi Mühendislik Fakültesi Gıda Mühendisliği Bölümü Fermantasyon Nedir? Mikroorganizmaların enerji temin etme yolları Solunum: Son elektron (H) alıcısı (akseptörü)oksijen
Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen
 Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen ix xiii xv xvii xix xxi 1. Çevre Kimyasına Giriş 3 1.1. Çevre Kimyasına Genel Bakış ve Önemi
Öğretim Üyeleri İçin Ön Söz Öğrenciler İçin Ön Söz Teşekkürler Yazar Hakkında Çevirenler Çeviri Editöründen ix xiii xv xvii xix xxi 1. Çevre Kimyasına Giriş 3 1.1. Çevre Kimyasına Genel Bakış ve Önemi
Çukurova Bölgesinde Oluşan Tarımsal ve Hayvansal Atıklardan Biyogaz Yoluyla Enerji Üretimi
 Çukurova Bölgesinde Oluşan Tarımsal ve Hayvansal Atıklardan Biyogaz Yoluyla Enerji Üretimi Yrd.Doç.Dr. N.Altınay Perendeci Dr. Aslı Çığgın Akdeniz Üniversitesi, Mühendislik Fakültesi Hüseyin Karışlı Erka
Çukurova Bölgesinde Oluşan Tarımsal ve Hayvansal Atıklardan Biyogaz Yoluyla Enerji Üretimi Yrd.Doç.Dr. N.Altınay Perendeci Dr. Aslı Çığgın Akdeniz Üniversitesi, Mühendislik Fakültesi Hüseyin Karışlı Erka
Aktif ve pasif iyon alımı
 Aktif ve pasif iyon alımı Moleküllerin membranı geçerek taşınmaları için aktif proses her zaman gerekli değildir. Moleküllerin bir kısmı dış ortamdan membran içine konsantrasyon farkına bağlı olarak çok
Aktif ve pasif iyon alımı Moleküllerin membranı geçerek taşınmaları için aktif proses her zaman gerekli değildir. Moleküllerin bir kısmı dış ortamdan membran içine konsantrasyon farkına bağlı olarak çok
ÖĞRENME ALANI : CANLILAR VE HAYAT ÜNİTE 6 : CANLILAR VE ENERJİ İLİŞKİLERİ
 ÖĞRENME ALANI : CANLILAR VE HAYAT ÜNİTE 6 : CANLILAR VE ENERJİ İLİŞKİLERİ B FOTOSENTEZ : 1 Güneş Enerjisinin Dönüştürülüp Depolanması 2 Fotosentez Olayı (Karbondioksit Özümlemesi) 3 Fotosentez Hızını Etkileyen
ÖĞRENME ALANI : CANLILAR VE HAYAT ÜNİTE 6 : CANLILAR VE ENERJİ İLİŞKİLERİ B FOTOSENTEZ : 1 Güneş Enerjisinin Dönüştürülüp Depolanması 2 Fotosentez Olayı (Karbondioksit Özümlemesi) 3 Fotosentez Hızını Etkileyen
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI
 ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 6.Endüstriyel Kirlenme Kontrolü - Nötralizasyon Yrd. Doç. Dr. Kadir GEDİK Birçok endüstrinin atıksuyu asidik veya bazik olduğundan alıcı ortama veya kimyasal ve/veya
ÇEV416 ENDÜSTRİYEL ATIKSULARIN ARITILMASI 6.Endüstriyel Kirlenme Kontrolü - Nötralizasyon Yrd. Doç. Dr. Kadir GEDİK Birçok endüstrinin atıksuyu asidik veya bazik olduğundan alıcı ortama veya kimyasal ve/veya
3) Oksijenin pek çok bileşiğindeki yükseltgenme sayısı -2 dir. Ancak, H 2. gibi peroksit bileşiklerinde oksijenin yükseltgenme sayısı -1 dir.
 5.111 Ders Özeti #25 Yükseltgenme/İndirgenme Ders 2 Konular: Elektrokimyasal Piller, Faraday Yasaları, Gibbs Serbest Enerjisi ile Pil-Potansiyelleri Arasındaki İlişkiler Bölüm 12 YÜKSELTGENME/İNDİRGENME
5.111 Ders Özeti #25 Yükseltgenme/İndirgenme Ders 2 Konular: Elektrokimyasal Piller, Faraday Yasaları, Gibbs Serbest Enerjisi ile Pil-Potansiyelleri Arasındaki İlişkiler Bölüm 12 YÜKSELTGENME/İNDİRGENME
1) Biyokütleye Uygulanan Fiziksel Prosesler
 1) Biyokütleye Uygulanan Fiziksel Prosesler 1. Su giderme 2. Kurutma 3. Boyut küçültme 4. Yoğunlaştırma 5. Ayırma Su giderme işleminde nem, sıvı fazda gideriliyor. Kurutma işleminde nem, buhar fazda gideriliyor.
1) Biyokütleye Uygulanan Fiziksel Prosesler 1. Su giderme 2. Kurutma 3. Boyut küçültme 4. Yoğunlaştırma 5. Ayırma Su giderme işleminde nem, sıvı fazda gideriliyor. Kurutma işleminde nem, buhar fazda gideriliyor.
Onuncu Ulusal Kimya Mühendisliği Kongresi, 3-6 Eylül 2012, Koç Üniversitesi, İstanbul
 REACTİVE BLUE 160 BOYARMADDESİ İÇEREN TEKSTİL ENDÜSTRİSİ BOYAMA PROSESİ ATIKSUYUNUN ELEKTROKOAGÜLASYON YÖNTEMİ İLE ARITIMINDA İŞLETİM KOŞULLARININ ENERJİ TÜKETİMİNE ETKİSİ Bahadır K. KÖRBAHTİ, Gül Seren
REACTİVE BLUE 160 BOYARMADDESİ İÇEREN TEKSTİL ENDÜSTRİSİ BOYAMA PROSESİ ATIKSUYUNUN ELEKTROKOAGÜLASYON YÖNTEMİ İLE ARITIMINDA İŞLETİM KOŞULLARININ ENERJİ TÜKETİMİNE ETKİSİ Bahadır K. KÖRBAHTİ, Gül Seren
DAHA İYİ ÖZEL FORMÜLASYON. Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık
 ÖZEL FORMÜLASYON DAHA İYİ Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALİYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA İÇİN AGRALYX
ÖZEL FORMÜLASYON DAHA İYİ Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALİYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA İÇİN AGRALYX
Biyogaz Yakıtlı Kojenerasyon Uygulamaları
 Biyogaz Yakıtlı Kojenerasyon Uygulamaları Sedat Akar Turkoted Yönetim Kurulu Üyesi Biyogaz Nedir? Biyogaz, mikrobiyolojik floranın etkisi altındaki organik maddelerin oksijensiz bir ortamda çürütülmesi
Biyogaz Yakıtlı Kojenerasyon Uygulamaları Sedat Akar Turkoted Yönetim Kurulu Üyesi Biyogaz Nedir? Biyogaz, mikrobiyolojik floranın etkisi altındaki organik maddelerin oksijensiz bir ortamda çürütülmesi
ÇEVRE MÜHENDĠSLĠĞĠ BÖLÜMÜ 0010020036 KODLU TEMEL ĠġLEMLER-1 LABORATUVAR DERSĠ DENEY FÖYÜ
 DENEY NO: 5 HAVAANDIRMA ÇEVRE MÜHENDĠSĠĞĠ BÖÜMÜ Çevre Mühendisi atmosfer şartlarında suda çözünmüş oksijen ile yakından ilgilidir. Çözünmüş oksijen (Ç.O) su içinde çözünmüş halde bulunan oksijen konsantrasyonu
DENEY NO: 5 HAVAANDIRMA ÇEVRE MÜHENDĠSĠĞĠ BÖÜMÜ Çevre Mühendisi atmosfer şartlarında suda çözünmüş oksijen ile yakından ilgilidir. Çözünmüş oksijen (Ç.O) su içinde çözünmüş halde bulunan oksijen konsantrasyonu
BİTKİSEL VE HAYVANSAL ATIKLARDAN BİYOGAZ VE ENERJİ ÜRETİM TESİSİ
 BİTKİSEL VE HAYVANSAL ATIKLARDAN BİYOGAZ VE ENERJİ ÜRETİM TESİSİ Tesisin Amacı Organik yapıdaki hammaddelerin oksijensiz ortamda bakteriler yoluyla çürütülerek enerji potansiyeli olan biyogaza ve biyogazın
BİTKİSEL VE HAYVANSAL ATIKLARDAN BİYOGAZ VE ENERJİ ÜRETİM TESİSİ Tesisin Amacı Organik yapıdaki hammaddelerin oksijensiz ortamda bakteriler yoluyla çürütülerek enerji potansiyeli olan biyogaza ve biyogazın
İal-biyoloji METABOLİZMA/SOLUNUM. 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir?
 METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
BİTKİ BESLEME DERS NOTLARI
 BİTKİ BESLEME DERS NOTLARI Dr. Metin AYDIN KONYA 2011 BİTKİ BESİN ELEMENTLERİNİN GÖREVLERİ, ALINIŞ FORMLARI ve KAYNAKLARI Besin Elementi Bitkideki Görevi Alınış Formu Kaynakları Karbon (C) Karbonhidratların
BİTKİ BESLEME DERS NOTLARI Dr. Metin AYDIN KONYA 2011 BİTKİ BESİN ELEMENTLERİNİN GÖREVLERİ, ALINIŞ FORMLARI ve KAYNAKLARI Besin Elementi Bitkideki Görevi Alınış Formu Kaynakları Karbon (C) Karbonhidratların
Anaerobik Arıtma ve Biyogaz Üretim Tesisi. Çağatay Arıkan-Ak Gıda Kalite Güvence Müdürü
 Anaerobik Arıtma ve Biyogaz Üretim Tesisi Çağatay Arıkan-Ak Gıda Kalite Güvence Müdürü Ak Gıda yı Tanıyalım Ak Gıda bir Yıldız Holding kuruluşu 1996 da Sakarya Akyazı ilçesinde küçük bir tesisin alınması
Anaerobik Arıtma ve Biyogaz Üretim Tesisi Çağatay Arıkan-Ak Gıda Kalite Güvence Müdürü Ak Gıda yı Tanıyalım Ak Gıda bir Yıldız Holding kuruluşu 1996 da Sakarya Akyazı ilçesinde küçük bir tesisin alınması
BİYOGAZ YAKITLI MİKRO KOJENERASYON UYGULAMALARI
 BİYOGAZ YAKITLI MİKRO KOJENERASYON UYGULAMALARI Dünya nüfusunun hızlı bir şekilde artmaya devam etmesi, sanayileşmenin yeni boyutlar kazanması ve insanoğlunun geleneksel yaşam şartlarından kurtularak yaşama
BİYOGAZ YAKITLI MİKRO KOJENERASYON UYGULAMALARI Dünya nüfusunun hızlı bir şekilde artmaya devam etmesi, sanayileşmenin yeni boyutlar kazanması ve insanoğlunun geleneksel yaşam şartlarından kurtularak yaşama
2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları
 B) RADYASYON UYGULAMALARI Radyasyon = enerji yayılması 1)Elektromanyetik radyasyon. UV, X ve γ ışınları 2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları İyonizan ışınların canlı hücreler üzerine
B) RADYASYON UYGULAMALARI Radyasyon = enerji yayılması 1)Elektromanyetik radyasyon. UV, X ve γ ışınları 2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları İyonizan ışınların canlı hücreler üzerine
1.018/7.30J Ekoloji I: Dünya Sistemi Güz 2009
 1.018/7.30J Ekoloji I: Dünya Sistemi Güz 2009 OKUMALAR: Ders Kitabı, syf. 43, 84-88; 673-674 Luria. 1975. Overview of photosynthesis. Kaiser, J. 1995. Can deep bacteria live on nothing but rocks and water?
1.018/7.30J Ekoloji I: Dünya Sistemi Güz 2009 OKUMALAR: Ders Kitabı, syf. 43, 84-88; 673-674 Luria. 1975. Overview of photosynthesis. Kaiser, J. 1995. Can deep bacteria live on nothing but rocks and water?
ÇEVRE TEKNOLOJİLERİ POLİTİKA, STRATEJİ VE HEDEFLER
 Teknoloji Alanı: Su Kaynaklarında Kirliliğinin Önlenmesi ve Kontrolü Hedef 2: Bu bakterilerin ve ortamından alınma tekniklerinin geliştirilmesi Hedef 3: Kontamine bakterinin etkisiz hale getirilme yöntemlerinin
Teknoloji Alanı: Su Kaynaklarında Kirliliğinin Önlenmesi ve Kontrolü Hedef 2: Bu bakterilerin ve ortamından alınma tekniklerinin geliştirilmesi Hedef 3: Kontamine bakterinin etkisiz hale getirilme yöntemlerinin
Ekolojik Yerleşimlerde Atık Yönetiminin Temel İlkeleri
 i Ekolojik Yerleşimlerde Atık Yönetiminin Temel İlkeleri Ekoljik yerleşimler kaynakların kullanımında tutumludur. Atık Yönetimi ve geri dönüşüm bu yerleşimlerde kaynak yönetiminin ayrılmaz bir bileşenidir.
i Ekolojik Yerleşimlerde Atık Yönetiminin Temel İlkeleri Ekoljik yerleşimler kaynakların kullanımında tutumludur. Atık Yönetimi ve geri dönüşüm bu yerleşimlerde kaynak yönetiminin ayrılmaz bir bileşenidir.
ELEKTROLİTİK TOZ ÜRETİM TEKNİKLERİ. Prof.Dr.Muzaffer ZEREN
 Prof.Dr.Muzaffer ZEREN Bir çok metal (yaklaşık 60) elektroliz ile toz haline getirilebilir. Elektroliz kapalı devre çalışan ve çevre kirliliğine duyarlı bir yöntemdir. Kurulum maliyeti ve uygulama maliyeti
Prof.Dr.Muzaffer ZEREN Bir çok metal (yaklaşık 60) elektroliz ile toz haline getirilebilir. Elektroliz kapalı devre çalışan ve çevre kirliliğine duyarlı bir yöntemdir. Kurulum maliyeti ve uygulama maliyeti
MEMM4043 metallerin yeniden kazanımı
 metallerin yeniden kazanımı 2016-2017 güz yy. Prof. Dr. Gökhan Orhan MF212 katot - + Cu + H 2+ SO 2-4 OH- Anot Reaksiyonu Cu - 2e - Cu 2+ E 0 = + 0,334 Anot Reaksiyonu 2H 2 O O 2 + 4H + + 4e - E 0 = 1,229-0,0591pH
metallerin yeniden kazanımı 2016-2017 güz yy. Prof. Dr. Gökhan Orhan MF212 katot - + Cu + H 2+ SO 2-4 OH- Anot Reaksiyonu Cu - 2e - Cu 2+ E 0 = + 0,334 Anot Reaksiyonu 2H 2 O O 2 + 4H + + 4e - E 0 = 1,229-0,0591pH
Yanma Kaynaklı Kirleticiler
 Dokuz Eylül Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, Buca/İZMİR Yanma Kaynaklı Kirleticiler Prof.Dr. Abdurrahman BAYRAM Telefon: 0232 3017113-3017080 Faks: 0232 4530922 E-Mail: [email protected]
Dokuz Eylül Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, Buca/İZMİR Yanma Kaynaklı Kirleticiler Prof.Dr. Abdurrahman BAYRAM Telefon: 0232 3017113-3017080 Faks: 0232 4530922 E-Mail: [email protected]
Sigma 28, 235-248, 2010
 Journal of Engineering and Natural Sciences Mühendislik ve Fen Bilimleri Dergisi Review Paper / Derleme Makalesi BIOHYDROGEN PRODUCTION FROM WASTE SLUDGE Sigma 28, 235-248, 2010 Nevim GENÇ* Kocaeli Üniversitesi,
Journal of Engineering and Natural Sciences Mühendislik ve Fen Bilimleri Dergisi Review Paper / Derleme Makalesi BIOHYDROGEN PRODUCTION FROM WASTE SLUDGE Sigma 28, 235-248, 2010 Nevim GENÇ* Kocaeli Üniversitesi,
Biyokimyasal Oksijen İhtiyacı (BOİ) Doç.Dr.Ergün YILDIZ
 Biyokimyasal Oksijen İhtiyacı (BOİ) Doç.Dr.Ergün YILDIZ Giriş BOİ nedir? BOİ neyi ölçer? BOİ testi ne için kullanılır? BOİ nasıl tespit edilir? BOİ hesaplamaları BOİ uygulamaları Bazı maddelerin BOİ si
Biyokimyasal Oksijen İhtiyacı (BOİ) Doç.Dr.Ergün YILDIZ Giriş BOİ nedir? BOİ neyi ölçer? BOİ testi ne için kullanılır? BOİ nasıl tespit edilir? BOİ hesaplamaları BOİ uygulamaları Bazı maddelerin BOİ si
ODORIENT. Biyolojik Koku Arıtma Sistemi. www.bioorient.com.tr
 Biyolojik Koku Arıtma Sistemi www.bioorient.com.tr www.bioorient.com.tr organik atıkların düşük oksijenli ortamlarda bile en verimli şekilde giderimini sağlayan özel bir bakteri kültürüdür. İçeriğindeki
Biyolojik Koku Arıtma Sistemi www.bioorient.com.tr www.bioorient.com.tr organik atıkların düşük oksijenli ortamlarda bile en verimli şekilde giderimini sağlayan özel bir bakteri kültürüdür. İçeriğindeki
YGS YE HAZIRLIK DENEMESi #22
 YGS YE HAZIRLIK DENEMESi #22 1) Zigottan başlayıp yeni bir bireyin meydana gelmesiyle sonlanan olayların hepsine birden gelişme denir. Embriyonun gelişimi sırasında, I. Morula II. Gastrula III. Blastula
YGS YE HAZIRLIK DENEMESi #22 1) Zigottan başlayıp yeni bir bireyin meydana gelmesiyle sonlanan olayların hepsine birden gelişme denir. Embriyonun gelişimi sırasında, I. Morula II. Gastrula III. Blastula
