TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
|
|
|
- Serkan Türker
- 7 yıl önce
- İzleme sayısı:
Transkript
1 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ FARKLI BÜYÜKLÜKTEKİ SIĞIR OOSİTLERİNİN MATURASYON VE FERTİLİZASYONU ÜZERİNE İNSÜLİN BENZERİ BÜYÜME FAKTÖRÜ-1 (IGF-1) VE EPİDERMAL BÜYÜME FAKTÖRÜNÜN (EGF) ETKİLERİNİN ARAŞTIRILMASI Duygu Burcu TOPUZOĞLU DOĞUM ve JİNEKOLOJİ ANABİLİM DALI DOKTORA TEZİ DANIŞMAN Prof. Dr. İ. Hakkı İZGÜR ANKARA
2 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ FARKLI BÜYÜKLÜKTEKİ SIĞIR OOSİTLERİNİN MATURASYON VE FERTİLİZASYONU ÜZERİNE İNSÜLİN BENZERİ BÜYÜME FAKTÖRÜ 1 (IGF-1) VE EPİDERMAL BÜYÜME FAKTÖRÜNÜN (EGF) ETKİLERİNİN ARAŞTIRILMASI Duygu Burcu TOPUZOĞLU DOĞUM VE JİNEKOLOJİ ANABİLİM DALI DOKTORA TEZİ DANIŞMAN Prof. Dr. İ. Hakkı İZGÜR Bu tez, Türkiye Bilimsel ve Teknolojik Araştırmalar Kurumu tarafından 109O022 proje numarası ile desteklenmiştir 2011-ANKARA
3 ii İÇİNDEKİLER Kabul ve Onay İçindekiler ii Önsöz v Simgeler ve Kısaltmalar vi Şekiller ix Çizelgeler x 1 GİRİŞ İn Vitro Embriyo Üretimi Mezbaha Materyalinden Oosit Toplama Teknikleri Canlı Hayvanlardan Oosit Toplama Tekniği (OPU) Sığır Oositlerinin Sınıflandırılması ve Seçimi İn Vitro Oosit Maturasyonu Sitoplazmik Maturasyon Nükleer Maturasyon İn Vitro Maturasyona Etki Eden Faktörler Oosit Vericisinin Fizyolojik Durumu Vericinin Yaşı Östrus Siklusu ve Folliküler Dalga İlişkisi Follikül ve Oosit Büyüklüğü Kumulus Oosit Kompleksi Maturasyon Süresi Sıcaklık, Nem ve Çevresel Gaz Bileşimleri Maturasyon Ortamlarının Ozmotik Değerleri Ovaryumların Taşınma Koşulları İn Vitro Maturasyon Vasatları ve Kullanılan Katkı Maddeleri Hormonlar Büyüme Faktörleri Protein (Serum ve Albumin) Katkıları Antioksidan Katkıları Hücresel Katkılar Maturasyon İn Vitro Fertilizasyon Spermin Kapasitasyonu ve Akrozom Reaksiyonu Sperm Hazırlama Yöntemleri İn Vitro Fertilizasyonun Değerlendirilmesi İn Vitro Embriyo Kültürü GEREÇ VE YÖNTEM Ovaryumların Toplanması Oosit Aspirasyonu ve Oositlerin Seçimi Oositlerin Gruplandırılması Ekilibrasyon ve Kültür Şartları Maturasyon Kriterlerinin Değerlendirilmesi Spermanın İn Vitro Fertilizasyon İçin Hazırlanması Hemasitometre ile Spermatozoon Konsantrasyonunun Belirlenmesi 35
4 iii 2.8. Kumulus Oosit Komplekslerinin İn Vitro Fertilizasyon İçin 35 Hazırlanması 2.9. İn Vitro Kapasitasyon İn Vitro Fertilizasyon Stok Solüsyonlar ve Vasatların Hazırlanması Embriyo Kültürü Embriyonik Gelişim Aşamalarının ve Embriyo Kalitesinin 40 Değerlendirilmesi İstatistiksel Analiz Çalışmada Kullanılan Kimyasal Maddeler ve Sarf Malzemeleri BULGULAR Folliküler Aspirasyon ve Elde Edilen Oosit Bulguları Büyüme Faktörlerinin Oositlerin Maturasyon Oranlarına Etkisi IGF-1 in Farklı Oosit Çaplarına Göre Maturasyona Etkisi EGF nin Farklı Oosit Çaplarına Göre Maturasyona Etkisi IGF-1 ve EGFKombinasyonunun Farklı Oosit Çaplarına Göre 46 Maturasyona Etkisi Kontrol Grubu Maturasyon Oranları Farklı Oosit Çaplarına Göre Büyüme Faktörlerinin Maturasyona Etkisi Büyüme Faktörlerinin Fertilizasyon Sonrası 2-4 Hücreli Embriyo 51 Gelişimi Üzerine Etkisi IGF-1 in 2-4 Hücreli Embriyo Gelişimi Üzerine Etkisi EGF nin 2-4 Hücreli Embriyo Gelişimi Üzerine Etkisi IGF-1 ve EGF Kombinasyonunun 2-4 Hücreli Embriyo Gelişimi 54 Üzerine Etkisi Kontrol Grubu 2-4 Hücreli Embriyo Gelişim Oranları Farklı Oosit Çaplarına Göre Büyüme Faktörlerinin 2-4 Hücreli Embriyo 56 Gelişimi Üzerine Etkisi 3.5. Büyüme Faktörlerinin Fertilizasyon Sonrası 4-8 Hücreli Embriyo 59 Gelişimi Üzerine Etkisi IGF-1 in 4-8 Hücreli Embriyo Gelişimi Üzerine Etkisi EGF nin 4-8 Hücreli Embriyo Gelişimi Üzerine Etkisi IGF-1 ve EGFKombinasyonunun 4-8 Hücreli Embriyo Gelişimi Üzerine 62 Etkisi Kontrol Grubu 4-8 Hücreli Gelişim Oranları Farklı Oosit Çaplarına Göre Büyüme Faktörlerinin 4-8 Hücreli Embriyo 64 Gelişim Aşamasına Etkisi 3.6. Büyüme Faktörlerinin Blastosist Gelişimi Üzerine Etkisi IGF-1 in Blastosist Gelişimi Üzerine Etkisi EGF nin Blastosist Gelişimi Üzerine Etkisi IGF-1 ve EGF Kombinasyonunun Blastosist Gelişimi Üzerine Etkisi Kontrol Grubunun Blastosist Gelişimi Üzerine Etkisi Farklı Oosit Çaplarına Göre Büyüme Faktörlerinin Blastosist 74 Gelişimine Etkisi 4. TARTIŞMA SONUÇ VE ÖNERİLER 84 ÖZET 86 SUMMARY 87
5 KAYNAKLAR 88 ÖZGEÇMİŞ 96 iv
6 v ÖNSÖZ Biyoteknoloji, hücre ve dokular ile teknolojik çalışmaların birleştirilmesi veya benzer materyallerin, endüstrinin faydasına sunulması olarak tanımlanmaktadır. Son yıllarda ucuz ve bol hayvansal gıdanın üretilmesi ve insanlarda üreme sorunlarının çözümüne model oluşturması yönünden, evcil hayvanlarda reprodüktif biyoteknoloji üzerine çalışmalarda kayda değer bir artış vardır. Başta ineklerde ve diğer evcil memelilerde reproduktif amaçla yapılan biyoteknolojik çalışmalar; in vitro yöntemle embriyo elde etme (IVP), embriyo kültürü, oosit ve embriyo dondurma, embriyo transferi, embriyo cerrahisi, klonlama, pronukleus transplantasyonu, spermanın in vitro kapasitasyonu ve mikro enjeksiyonu ile fertilizasyon çalışması, transgenik hayvanların üretimi, biyoreaktörlerden ürün eldesi ve kök hücre çalışmaları gibi alanlarda yoğunlaşmaktadır. İn vitro ortamda embriyo eldesi için gerekli temel şart, sağlıklı ineklerden elde edilen oositlerin laboratuar ortamında yüksek oranda maturasyonu ve fertilizasyon sonrası kaliteli blastosist eldesi için gerekli olan metodolojiler gün geçtikçe çeşitlilik kazanmaktadır. Yapılan güncel çalışmaların büyük bir çoğunluğu farklı kimyasalların ve doku üretim vasatlarının oositlerin maturasyon ve bölünme oranlarını arttırmaya yönelik çalışmalardır. Hayvancılık alanında embriyo transferi ile verim performansı üstün dişilerin immatur oositlerinden üstün özellikli yavrular elde edilebilmektedir. Sunulan projede, güncelliği korumakta olan ve halen daha tam olarak gün ışığına çıkmamış bir sıra karmaşık aşamadan oluşan sığır oositlerinin in vitro ortamda maturasyonu ve fertilizasyonu üzerine insülin benzeri büyüme faktörü-1 ve epidermal büyüme faktörlerinin etkisinin araştırılarak daha kaliteli ve daha çok sayıda embriyo üretilebilirliği amaçlanmıştır. Sunulan araştırma projesinin (Proje No:109O022) gerçekleştirilmesini destekleyen Türkiye Bilimsel ve Teknolojik Araştırma kurumuna, projenin kabulünden bu güne geçen sürede önerileri ve fikirlerinden yararlandığımız değerli hakem/danışman öğretim üyelerine sonsuz teşekkür ve şükranlarımızı sunarız.
7 vi SİMGELER ve KISALTMALAR < Küçüktür > Büyüktür % Yüzde Derece C Santigrad derece µg Mikrogram µl Mikrolitre µm Mikrometre Ark. bff BSA CaCl 2 camp CO 2 COC Arkadaşları Sığır follikül sıvısı Sığır serum albumini Kalsiyum klorür Siklik adenozin monofosfat Karbondioksit Kumulus oosit kompleksi CR1 Charles Rosekrans 1 ECS EFAF EGF FCS Frac V FSH G g GVBD H 2 O Östrustaki inek serumu Essential fatty acid free Epidermal büyüme faktörü Fötal buzağı serumu Fraksiyon V Follikül stimüle edici hormon Gauge Gram Germinal vezikül yıkımlanması Su
8 vii IGF-1 IL IVC IVF IVM KCl KSOM LH M II MgCl 2 ml mm mm mrna Na NaCl NaH 2 PO 4 NaHCO 3 ng PHE PL-1 PL-2 PL-3 PO 4 RNA SOF TALP İnsülin benzeri büyüme faktörü-1 İnterlökin İn vitro kültür İn vitro fertilizasyon İn vitro maturasyon Potasyum klorür Potasyum simpleks optimizasyon medyumu Lüteinleştirici hormon Metafaz II Magnezyum klorür Mililitre Milimetre Milimolar Messenger RNA Sodyum Sodyum klorür Sodyum fosfat Bikarbonat Nanogram Penisilamin hipotaurin epinefrin Park-Lin 1 solüsyonu Park-Lin 2 solüsyonu Park-Lin 3 solüsyonu Fosfat Ribonükleik asit Sentetik ovidukt sıvısı Tyrode nin albumin laktat piruvat vasatı TCM -199 Doku kültürü medyumu 199 TGF-α Transforming growth factor α
9 viii TGF-β TL X 2 Transforming growth factor β Tyrode nin laktat solüsyonu Ki-kare değeri
10 ix ŞEKİLLER Şekil Oosit çapı ölçümleri 32 Şekil Maturasyon öncesi ve maturasyon sonrası oositlerin görünümü 34 Şekil Büyüme faktörlerinin oositlerin maturasyon oranlarına etkisi 44 Şekil IGF-1 in farklı oosit çaplarına göre maturasyona etkisi 45 Şekil EGF nin farklı oosit çaplarına göre maturasyona etkisi 46 Şekil IGF-1 ve EGF kombinasyonunun farklı oosit çaplarına göre maturasyona etkisi 47 Şekil Kontrol grubu maturasyon oranları 48 Şekil Farklı büyüme faktörü katkılarının çapı 110 µm olan oositlerin maturasyon 49 oranları Şekil Farklı büyüme faktörü katkılarının çapı µm olan oositlerin maturasyon oranları 50 Şekil Farklı büyüme faktörü katkılarının çapı 150 µm olan oositlerin maturasyon oranları 51 Şekil Büyüme faktörlerinin fertilizasyon sonrası 2-4 hücreli embriyo gelişimi üzerine etkisi 52 Şekil IGF-1 in 2-4 hücreli embriyo gelişimi üzerine etkisi 53 Şekil EGF nin 2-4 hücreli embriyo gelişimi üzerine etkisi 54 Şekil IGF-1 ve EGF kombinasyonunun farklı oosit çaplarına göre 2-4 hücreli embriyo gelişimi üzerine etkisi 55 Şekil Kontrol grubu 2-4 hücreli embriyo bölünme oranları 56 Şekil Çapı µm arasında olan oositlerde erken dönem bölünme oranları 57 Şekil Çapı µm arasında olan oositlerde erken dönem bölünme oranları 58 Şekil Çapı 150 µm den büyük oositlerde erken dönem bölünme oranları 59 Şekil Büyüme faktörlerinin fertilizasyon sonrası 4-8 hücreli embriyo gelişimi üzerine 60 etkisi Şekil IGF-1 in 4-8 hücreli embriyo gelişimi üzerine etkisi 61 Şekil EGF nin 4-8 hücreli embriyo gelişimi üzerine etkisi 62 Şekil IGF-1 ve EGF Kombinasyonunun 4-8 Hücreli Embriyo Gelişimi Üzerine Etkisi 63 Şekil Kontrol grubu 4-8 hücreli embriyo bölünme oranları 64 Şekil Çalışma ve kontrol gruplarında çapı 110 µm den küçük olan oositlerin hücreye bölünme oranları Şekil Çalışma ve kontrol gruplarında çapı µm arasında olan oositlerin 4-8 hücreye bölünme oranları Şekil Çalışma ve kontrol gruplarında çapı 150 µm den büyük oositlerin 4-8 hücreye bölünme oranları Şekil Mature olan oositlerin çap gözetmeksizin gruplar arası ortalama blastosist gelişim oranları Şekil hücreli embriyoların çap gözetmeksizin gruplar arası ortalama blastosist gelişim oranları Şekil Oosit çapı gözetmeksizin büyüme faktörlerinin gruplar arası ortalama blastosist oluşumu Şekil Embriyo kaliteleri 70 Şekil IGF-1 in farklı oosit çaplarına göre blastosist gelişim oranları 71 Şekil EGF nin farklı oosit çaplarına göre blastosist gelişim oranları 72 Şekil Grup 3 ün farklı oosit çaplarına göre blastosist gelişim oranları 73 Şekil Grup 4 ün farklı oosit çaplarına göre blastosist gelişim oranları 74 Şekil Çapı 110 µm den küçük oositlerin blastosist gelişim oranları 75 Şekil Çapı µm oositlerin blastosist gelişim oranları 75 Şekil Çapı 150 µm den büyük oositlerin blastosist gelişim oranları
11 x ÇİZELGELER Çizelge Grup I in oluşturulması ve uygulama prosedürü 33 Çizelge Grup II nin oluşturulması ve uygulama prosedürü 33 Çizelge Grup III ün oluşturulması ve uygulama prosedürü 33 Çizelge Grup IV ün oluşturulması ve uygulama prosedürü 33 Çizelge Stok solüsyonlarının hazırlanması ve saklanması (Hansen, 2000). 37 Çizelge TL solüsyonlarının hazırlanması (Hansen, 2000) 38 Çizelge TALP Vasatının Hazırlanması (Hansen, 2000) 38 Çizelge CR1 stok vasatının hazırlanması (Hansen, 2000) 39 Çizelge CR1aa kültür vasatının hazırlanması (Hansen, 2000) 39 Çizelge Büyüme faktörlerinin oositlerin maturasyon oranlarına etkisi 43 Çizelge IGF-1 in farklı oosit çaplarına göre maturasyona etkisi 44 Çizelge EGF nin farklı oosit çaplarına göre maturasyona etkisi 45 Çizelge IGF-1 ve EGF kombinasyonunun farklı oosit çaplarına göre maturasyona 46 etkisi Çizelge Kontrol grubu maturasyon oranları 47 Çizelge Farklı büyüme faktörü katkılarının çapı 110 µm olan oositlerin maturasyon oranları Çizelge Farklı büyüme faktörü katkılarının çapı µm olan oositlerin maturasyon oranları Çizelge Farklı büyüme faktörü katkılarının çapı 150 µm olan oositlerin maturasyon oranları 50 Çizelge Büyüme faktörlerinin fertilizasyon sonrası 2-4 hücreli embriyo gelişimi üzerine etkisi 51 Çizelge IGF-1 in 2-4 hücreli embriyo gelişimi üzerine etkisi 52 Çizelge EGF nin 2-4 hücreli embriyo gelişimi üzerine etkisi 53 Çizelge IGF-1 ve EGF kombinasyonunun farklı oosit çaplarına göre 2-4 hücreli embriyo gelişimi üzerine etkisi 54 Çizelge Kontrol grubu 2-4 hücreli embriyo bölünme oranları 55 Çizelge Çapı 110 µm den küçük oositlerde erken dönem bölünme oranları 57 Çizelge Çapı µm arasında olan oositlerde erken dönem bölünme oranları 58 Çizelge Çapı 150 µm den büyük oositlerde erken dönem bölünme oranları 58 Çizelge Büyüme faktörlerinin fertilizasyon sonrası 4-8 hücreli embriyo gelişimi 59 üzerine etkisi Çizelge IGF-1 in 4-8 hücreli embriyo gelişimi üzerine etkisi 60 Çizelge EGF nin 4-8 hücreli embriyo gelişimi üzerine etkisi 61 Çizelge IGF-1 ve EGF Kombinasyonunun 4-8 Hücreli Embriyo Gelişimi Üzerine 62 Etkisi Çizelge Kontrol grubu 4-8 hücreli embriyo bölünme oranları 63 Çizelge Çalışma ve kontrol gruplarında çapı 110 µm den küçük olan oositlerin 4-8 hücreye bölünme oranları 65 Çizelge Çalışma ve kontrol gruplarında çapı µm arasında olan oositlerin 4-8 hücreye bölünme oranları 66 Çizelge Çalışma ve kontrol gruplarında çapı 150 µm den büyük oositlerin 4-8 hücreye bölünme oranları 66 Çizelge Mature olan oositlerin çap gözetmeksizin gruplar arası ortalama blastosist gelişim oranları. 68 Çizelge hücreli embriyoların çap gözetmeksizin gruplar arası ortalama blastosist gelişim oranları
12 xi Çizelge Oosit çapı gözetmeksizin büyüme faktörlerinin gruplar arası ortalama blastosist oluşumu ve embriyo kaliteleri (4-8 hücreli embriyoların blastosiste bölünme oranları) Çizelge IGF-1 in farklı oosit çaplarına göre blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları) Çizelge EGF nin farklı oosit çaplarına göre blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları Çizelge Grup 3 ün farklı oosit çaplarına göre blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları Çizelge Grup 4 ün farklı oosit çaplarına göre blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları) Çizelge Çapı 110 µm den küçük oositlerin blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları) Çizelge Çapı µm oositlerin blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları Çizelge Çapı 150 µm den büyük oositlerin blastosist gelişim oranları (4-8 hücreli embriyoların blastosiste bölünme oranları)
13 1 1.GİRİŞ Son yıllarda çiftlik hayvanlarında oositlerin in vitro maturasyonu ve fertilizasyonu üzerine yoğun araştırmalar yapılmaktadır. Bu çalışmalar sonucunda çok önemli aşamalar sağlanmış ve oositler in vivo veya in vitro ortamda kültüre edildikten sonra elde edilen embriyoların taşıyıcı hayvanlara nakledilmesiyle gebelik oranlarındaki artışların görülmesiyle yöntemlerin başarısı ispatlanmıştır (Otoi ve ark., 1997, Sağırkaya ve ark., 2007). In vitro teknikler oositlerin in vitro maturasyonu, fertilizasyonu ve erken embriyonik gelişme, ve preimplantasyon periyodu için gerekli ucuz ve sağlıklı sığır embriyolarının sağlamasında önemli bir yer tutmaktadır. Başarılı ve güvenilir bir oosit maturasyonu (hem sitoplazmik hem de nükleer maturasyon) embriyonik ve fötal gelişim üzerine olumlu etki yapmaktadır (Sağırkaya ve ark., 2007). Bununla beraber, in vitro üretim sistemlerinde kaliteli blastosist aşamasına ulaşabilen oosit sayısı hala değişiklik göstermekte (Fukui ve ark., 1991; Otoi ve ark., 1997) ve bu oran yapılan bir çalışmada %6-20 düzeyinde olduğu bildirilmektedir (Fukui ve ark., 1991). Mezbahalardan elde edilen materyaller, in vitro embriyo üretimi için kalite ve gelişim kapasitesi bakımından farklılıklar göstermektedir. Hayvanlarda reproduktif biyoteknoloji alanında üretim açısından avantaj yaratmasına rağmen in vitro ortamda sığırlarda embriyo üretim başarı oranı %25-50 yi geçememektedir. Bu oranın düşük olmasındaki başlıca nedeni, henüz in vitro maturasyon ve in vitro kültür koşullarının sağlanmasında yaşanan sıkıntılardır. Tatmin edici bir başarı düzeyi olmasa da gelişmiş ülkelerin pek çoğunda in vitro fertilizasyon hayvan ıslahını sağlamak amacıyla kullanımda yerini almıştır. Ülkemizde hayvansal gıdalarından yararlanma oranının gelişmiş ülkelere oranla oldukça düşük olması nedeniyle hayvansal protein kullanımını arttırmak için bu gibi tekniklerin hayvancılığa
14 2 verebileceği katkıların üzerinde önemle durulmalı ve bu konuda çalışmalar sürdürülmelidir (Akyol, 2006) İn Vitro Embriyo Üretimi İn vitro embriyo üretimi, ovaryumların toplanması, toplanan ovaryumlardan oositlerin aspirasyonu, aspire edilen oositlerin in vitro maturasyonu (IVM), mature oositlerin in vitro fertilizasyonu (IVF) ve embriyo kültürü (EC) aşamalarından oluşan bir işlemdir (Leibfried-Rutledge ve ark., 1999; Küplülü ve Ün, 2001). İn vitro embriyo üretimi basamaklarının her biri sırasıyla bir sonrakinin başarısını etkilemektedir (Korkmaz, 2008) Mezbaha Materyalinden Oosit Toplama Teknikleri Sığır oositlerinin toplanmasında, folliküllerin izolasyonu, diseksiyon, aspirasyon veya folliküllerin dilimlenmesi veya oviduktun flushing işlemine tabi tutulması şeklinde olur. Oosit elde etme tekniği, pre veya postovulatör oositler ihtiyacına göre ve mezbahadan ya da doku veya canlı hayvanlardan elde edilmesine göre değişiklik gösterir. Canlı hayvanlarda, ovariektomi yöntemiyle alınan ovaryumlardan veya ultrasonografik veya laparoskopik yöntemle ovaryumlardan oosit elde edilebilir. Mezbahadan elde edilecek ovaryumlardan embriyo üretimi için çeşitli yöntemler geliştirilmiştir (Gordon, 2003). Mezbahadan elde edilen ovaryumların veziküler foliküllerinden, uygun enjektör, iğne, pipet, vakumlu aspirasyon iğnesi gibi araçların yardımıyla oositlerin toplanması yaygın bir tekniktir. Aspirasyon tekniğinin dezavantajı bu yolla folliküllerin % ından oositlerin toplanabilmesidir. Bu nedenle ovaryum dilimlenmesi tekniği ile birlikte daha etkin şekilde oosit toplanabilir.
15 3 Aspirasyon tekniğinin bir avantajı ise, bu tekniğin hızlı bir şekilde uygulanabilmesi ile embriyo üretimi için gerekli olan çabukluğun sağlanmasıdır. Ovaryumlardan folliküler aspirasyon yöntemiyle oosit toplamak için çoğunlukla 18 veya 21 G luk iğneler kullanılır ile mmhg oranında basınçla toplanan oosit kalitesini yükseltmek mümkündür. Yüzeysel ve veziküler karakterdeki follikillerin 2-8 mm çapında olanlarından aspirasyon yapılabilir (Kanagawa ve ark., 1995). Bir diğer teknik follikül diseksiyon tekniğidir ve bu teknik öncelikle koyunlarda kullanılmış, veziküler folliküllerin (2-8 mm) diseksiyonunu takiben, parçalayarak oosit toplanmasını esas almaktadır. Follikül diseksiyonunda amaç, öncelikle oositi çevreleyen kumulus hücrelerine zarar vermeden oosit elde edilmesidir. En büyük avantajı atretik ve atretik olmayan folliküllerin belirlenebilmesidir. Follikülün homojen olarak saydam veya açık renkte olması, iyi bir damarlaşma görülmesi, stratum granulozum tabakasının düzenli oluşu, follikülün atretik olmadığını göstermektedir. Bunun tam tersi olarak, atretik follikülleri donuk gri renklidir ve damarlaşmaları zayıftır. Diseksiyon tekniğinde aspirasyon tekniğinde olduğu gibi, oositi çevreleyen kumulus hücrelerine zarar verilmediği için ve aspirasyonla her zaman alınması mümkün olmayan kaliteli oositlere ait kumulus oophorus kompleksi, follikül duvarına sıkıca bağlandığı için, fazla sayıda kaliteli oosit elde etmek mümkün olmaktadır (Gordon, 2003). Ovaryum dilimleme tekniği direkt veya aspirasyon sonrası olarak uygulanabilen bir tekniktir. Bu yöntemle ovaryum başına arasında oosit elde etmek mümkün olmaktadır. Özellikle koyun, keçi gibi küçük ovaryumlu hayvanlarda, ovaryum yüzeyinin dilimlenmesinin iyi sonuçlar verdiği, bu teknikle, çok sayıda oosit elde edilmekle birlikte, mayotik olarak yetersiz oositler de toplanabileceği, çok sayıda ovaryumla çalışılabileceği gibi uygun olmamakla birlikte, az sayıdaki ovaryum için önerilmektedir (Duran, 2000).
16 4 Transilluminasyon (ışık geçirgen) aspirasyon tekniği, Arav (2001) tarafından geliştirilmiştir ve oosit aspirasyonu için kortikal folliküllerin görüntülenmesinin sağlanması için, ovaryumun medulla ve korteksinde ışık geçirgenliğinin kullanılmasından dolayı bu tekniğe ışık geçirgen (transilliminasyon) aspirasyon tekniği (TAO) denilmektedir. Bu teknik ile ovaryum başına elde edilen oosit oranının %50 artırılabileceği bildirilmektedir (Arav, 2001; Gordon, 2003). Klasik ışıklandırmalara oranla, ovaryumun merkezinin aydınlatılabilmesi ile çok daha fazla sayıda follikül gözlenebilmektedir ve geleneksel olarak 18G luk iğneyle aspirasyon işlemi yapılan bu teknikle ovaryum başına 7,3 oosit elde edildiği bildirilmektedir (Arav, 2001) Canlı Hayvanlardan Oosit Toplama Tekniği (OPU) Hormonla uyarılmış ya da uyarılmamış ineklerde, 7.5 MHz lik özel OPU probu ve aspirasyon sistemine sahip ultrasonografi cihazları ile haftada bir kez ovaryumlardan oosit aspire edilebilir. İneklerde süperovulasyonla embriyo elde etmek amacıyla iki süperovulasyon arasında 2-3 aylık bir zaman bırakmak gerektiği, halbuki bu yöntem sayesinde çok kısa aralıklarla, üstün genetik karakterli inek ve düvelerden çok sayıda olgun olmayan ya da olgun oosit toplanarak laboratuvarda embriyo elde edilebileceği ve ayrıca, prepubertal düvelerden, gebe ve genital kanallarında fizyolojik bozukluklara sahip hayvanlardan da yararlanabilindiği bildirilmiştir (Yang ve ark., 1998). Transvaginal yolla ultrasonografi rehberliğinde oositlerin toplanması, folliküler yapının belirlenebilmesi nedeniyle avantaj oluşturmakta, ayrıca bu yöntemle, siklus döneminin tayininin mümkün olması nedeniyle regresyona ve atreziye doğru giden folliküller de saptanabilmekte ve bu nedenle oositlerin maturasyonu ve daha sonraki gelişim oranları artış gösterebilmektedir (Greve ve Madison, 1991). Bu gibi yararları yanında
17 5 anılan tekniğin aspirasyon vakumu, hayvanlara hormon tedavisinin yapılıp yapılmaması, punksiyon sıklığı, siklusun dönemi ve operatörün deneyimi gibi birçok faktörden etkilenmesi önemli bir dezavantaj olarak değerlendirilmekte, ayrıca bu teknikte çıplak oosit sayısının artış gösterdiği belirtilmektedir (Ward ve ark., 2003) Sığır Oositlerinin Sınıflandırılması ve Seçimi İn vitro embriyo üretiminde iyi kaliteli oositlerin seçimi ve sınıflandırılması yüksek başarı sağlamada önemli bir adımdır. Morfolojik sınıflandırmada oositin sitoplazma görüntüsü ve çevreleyen hücrelerle olan bağı dikkate alınmaktadır. Günümüzde kumulus oosit kompleksi (KOK) morfolojisi yönünden en çok kullanılan üç sınıflandırma yöntemi ile değerlendirilmektedir (Gordon, 2003). De Loos ve ark. na (1991) göre 1. Kalite; Kompakt çok katlı kumulus hücre katmanı, homojen ooplazma ve şeffaf görünümlü kumulus oosit kompleksi, 2. Kalite; Kompakt çok katlı kumulus hücre katmanı, homojen ooplazma ancak oosit periferinde karaltılı görünüm, daha az şeffaf görünüm 3. Kalite; Daha az kompakt çok katlı kumulus hücre katmanı, düzensiz ooplazmada koyu lekeler, 1 ve 2 den daha karanlık görünümlü, 4. Kalite; Şişmiş kumulus katmanı, koyu jel kıvamında kumulus hücreleri, ooplazma düzensiz ve koyu lekeli ve tüm kumulus oosit kompleksleri karanlık ve düzensiz görünümlü oositler olarak bildirilmektedir. Younis ve arkadaşlarına (1989) göre: Seçkin oositler; homojen görünümlü ooplazmalı ve zona pellusidaya sıkıca tutunmuş kompakt kumulus hücre katmanlı, Seçkin olmayan oositler; Tam olmayan diğer tip kumulus
18 6 hücre katmanları ve heterojen görünümlü ooplazma içeren oositler olarak belirtilmektedir. Brackett ve Zuelke (1993) nin tarif ettiği sınıflandırmada ise: 1. Kalite; 4 kattan fazla sayıda kompakt kumulus hücre katmanı ve ooplazma kumlu görünüme sahip, 2. Kalite; 2-3 katlı kompakt kumulus hücre katmanı ve ooplazma kumlu veya hafif kumlu görünümlü, 3. Kalite; 1-2 katlı hafif/düzensiz kompakt kumulus hücre katmanı ve ooplazma hafif kumlu ya da homojen görünüme sahip, 4. Kalite; Çıplak oosit ve homojen/jel görünümlü ooplazması bulunan oositler olarak nitelendirilmektedir. Yalnızca kumulus hücrelerinin morfolojik durumuna bakılarak A, B, C ve D şeklinde de sınıflandırma yapılmaktadır. Homojen görünümlü bir sitoplazma, oositi çevreleyen, bozulmamış ve kompakt yapıda kumulus hücreleri, matur olmayan oositlerin maturasyon ve embriyonik gelişimlerin en önemli işaretlerindendir (Kanagawa, 1995; Akyol, 2006). Oosit değerlendirmede pratik olarak sadece kumuluslara bakıldığında; A kalite: etrafında 5-6 sıradan daha fazla kumulus hücreleri bulunan ve homojen yapı gösteren oositler, B kalite: etrafında 2-4 sıra kumulus hücre bulunan veya az bir kısmında kumulus bulunmayan oositler, C kalite: etrafında kumulus hücresi bulunmayan oositler, D kalite: etrafındaki kumulus hücre yığını dejenere durumda olan oositler olarak ayrılmaktadır (Akyol, 2006) İn Vitro Oosit Maturasyonu Oosit maturasyonu, germinal vezikül aşamasından metafaz II aşamasına ve birinci polar cisimciğin atılımıyla sonuçlanan birçok nükleer ve sitoplazmik değişiklikleri içeren uzun ve karışık bir süreç olarak tanımlanmaktadır. Oosit maturasyonu sırasında birbirinden farklı birçok madde sentezlenir ve
19 7 depolanır ve bu maddelerin embriyogenezisi meydana getirebilecek yetenekteki embriyonik genomu embriyonik gelişim sırasında desteklediği bildirilmiştir. Oosit maturasyonu sırasında, kumulus hücreleri de maddelerin üretimine yardımcı olmakta, nükleer ve sitoplazmik maturasyonu kontrol eden gonadotropinlere cevap olacak maddeler sentezledikleri bildirilmiştir (Loutradis ve ark., 2006) Sitoplazmik Maturasyon Oosit maturasyonu sırasında oluşan karmaşık olaylar sadece, nükleer maturasyonda kromozom ayrılmasının ayarlanması dinamiğine bağlı olmayıp, aynı zamanda sürecin meydana gelebilmesi için gerekli, sitoplazmik organellerin yeniden dağılması, messenger RNA (mrna) nın, proteinlerin ve kopyalama faktörlerinin depolanmasına bağlıdır. Sitoplazma içinde depolanan proteinler, oosit maturasyonu ve bunu takip eden embriyonik genomun aktive edilmesi ve yeni proteinlerin oluşumuna ihtiyaç duyulacağı erken embriyonik gelişimin meydana gelebilmesi için ciddi öneme sahiptir. Bu evre embriyonik genom aktivasyonu olarak adlandırılmıştır ve bu süreç, belirli genlerin ortaya çıkması, embriyogenezisin ve pre-implantasyon aşamasının başarısını belirlemektedir (Meirelles ve ark., 2004; Ferreira ve ark., 2009). Sitoplazmik maturasyon, oositi fertilizasyona ve bunu takip edecek olan erken embriyonik gelişime hazırlayacak olan ve nükleer maturasyona paralel olarak hücre sitoplamazmasında meydana gelen bir kaç fenomenden meydana gelen bir süreçtir. Oositin kalitesi sitoplazmik maturasyona bağlıdır ve yetersiz veya hatalı bir sitoplazmik maturasyon geçiren oosit, fertilizasyon yeteneğinden ve bunun devamında meydana gelecek olaylardan yoksun kalır. Sitoplazmik maturasyon sırasında meydana gelen olaylar arasında RNA sentezi ve protein üretimi oluşmaktadır. Oositin içindeki RNA nın büyük
20 8 bir bölümü follikülogenezis sırasında sentezlemektedir (Loutradis ve ark., 2006) Nükleer Maturasyon Nükleer maturasyon, mayozu yeniden başlatması ve metafaz II yi ilerletmesi için oositin hazırlanmasıdır. Germinal vezikül yıkımlanması (GVBD) siklusun ortasında LH dalgasıyla başladığı, bununla birlikte in vitro ortamda kültüre edilen kumulus-oosit kompleksinin kendiliğinden mayozu devam ettirme yeteneğine sahip olduğu bildirilmiştir (Cha ve Chain, 1998; Chian, 2004). Germinal vezikül yıkımlanmasına, siklik adenozine monofosfat (camp), purinler, steroidler, inositol 1,4,5-trifosfat (IP3), Ca +2 ve bir çok mekanizmanın sebep olduğu düşünülmektedir. Ayarlayıcı faktörler, gap junctionlar sayesinde kumulus hücreleri ve oosit arasında kolayca geçiş sağlamaktadır. Kültür vasatlarına eklenen yüksek konsantrasyonlardaki camp ve purin hipoksantin germinal vesikül yıkımlanmasına engel olur. Buna ek olarak, folliküler hücrelerden köken alan camp nin gap junction aracılığı ile oosite geçişinin oosit maturasyonunu inhibe ettiği ileri sürülmektedir (Loutradis ve ark., 1994). Bunun aksine, kültür vasatlarına LH eklenmesinin germinal vezikül yıkımlanmasını artırdığı da bildirilmiştir. Germinal vezikül yıkımlanması ve oositin metafaz II aşamasına yönelebilmesi için protein sentezi vazgeçilmezdir. Protein sentezi eksikliğinde, mayozun yeniden başlamasından sorumlu sitoplazmik bir protein olan maturasyon-destekleyici faktörün (MPF) aktive edilemediği belirtilmiştir (Ferreira ve ark., 2009). Maturasyon-destekleyici faktör, siklin (siklin B) ve siklin-bağımsız kinaz (p34 cac2 serin/treonin kinaz) olmak üzere iki proteinden oluşmaktadır. Siklinler, siklin-bağımsız kinazları bağlayarak ve aktif bir kompleks oluştururlar, ve böylece hücre siklusunu kontrol ederler. Maturasyondestekleyici faktör, G2 aşamasından M-hücre siklusu fazına geçiş için gerekli olan belli hücre içi proteinleri fosforilasyona uğratarak hücre siklusunun
21 9 ilerlemesini uyarır ve bölünmeyen hücrelerde bile mitozun başlamasına neden olur. Oositler interfaz aşamasındayken, inaktif siklin-kinaz seviyeleri yüksek seyretmektedir. Siklin-kinaz kompleksi aktive olduğunda, germinal vezikül yıkımlanmasını uyarır. Bununla beraber, oositler fertilizasyondan hemen önce metafaz II aşamasında bekledikleri sırada, p34 cac2 serin/treonin kinaz konsantrasyonları yüksektir. Oositlerin metafaz II aşamasında beklemesinden aynı zamanda oositin nükleer maturasyonunu da düzenleyen sitostatik faktörün (CSF) sorumlu olduğu düşünülmektedir. Germinal vezikül yıkımlanması, metafaz II beklemesi ve bunu takiben metafaz II den anafaz II ye geçiş p34 cac2 serin/treonin kinaz gibi hücre siklusunu kontrol eden proteinelerin aktivasyonuna veya inaktivasyonuna bağlı olduğu belirtilmiştir (Ferreira ve ark., 2009) İn Vitro Maturasyona Etki Eden Faktörler Oosit Vericisinin Fizyolojik Durumu Pubertasa girmiş dişi hayvanlar oosit elde edilmesi için kullanılabilmektedir. Bu dişilerin oosit kaynağı olarak kullanılabilmeleri için ovaryumlarında antral folliküllerin bulunması yeterli olmakta buna karşın patolojik hipoplastik ovaryumlara sahip hayvanların, postpartum dönemdeki hayvanların veya doğumuna az bir zaman kalmış olan hayvanların verici olarak kullanılması uygun görülmemektedir. Vericilerden toplanan oositlerin sayılarında ve kalitelerinde farklılıklar görülmekte ve bakım besleme koşulları, genetik, çevresel koşullar, sağlık koşullarının iyileştirilmesiyle vericilerden elde edilen oositlerin sayısı ve kalitesinde artış görüldüğü bildirilmiştir (Galli ve Lazzari, 1996; Akyol, 2006).
22 10 Pubertasa ulaşmamış dişi hayvanlardan çeşitli yöntemlerle oosit toplanabilse de, bu hayvanlardan elde edilen oositlerin maturasyon ve bunun devamında yaşayabilir embriyo oluşabilme yeteneği için gerekli hormon reseptörlerinin bulunmayışı, maturasyon ve embriyo geliştirme yeteneklerinin sınırlı kalmasına neden olduğu bildirilmiştir (Nagai, 2001; Akyol, 2006) Vericinin Yaşı Bir oosit için kapasite, döllenme yeteneğine sahip olma ve belli bir aşamadan sonra embriyo meydana getirebilme anlamına gelir. Tam bir kapasite ise bir embriyonun gebelik meydana getirme ve normal bir yavru doğumu ile sonuçlanması demektir. Fertil oositler sadece pubertas döneminde periyodik olarak ovulasyonla ilişkili gonadotropin salınımına sahip dişilerden elde edilmektedir. Bu durumda, vericinin embriyogenezisi meydana getirebilecek oositlerin bu yeteneği nasıl kazandırdığı sorusunu akla getirmektedir. Bu amaçla yapılan bir çalışmada 5-11 aylık yaş aralığından rastgele seçilen dişilere herhangi bir gonadotropin uygulaması yapılmadan transvaginal yolla ultrasonografi eşliğinde 2-10 mm çapındaki folliküllerden toplanan oositlere rutin ivm/ivf prosedürleri uygulanmış ve sonunda embriyo gelişim oranlarının yaş büyüdükçe arttığı görülmüştür (Yang ve ark., 1998). Yeni doğan buzağılarda antral folliküller büyümesini tamamlamış oositleri içermesine rağmen, bu oositlerin daha sonra embriyo teknolojilerinde kullanılması pratik olmadığı bildirilmiştir (Armstrong, 2001; Palma ve ark., 2001) Östrus Siklusu ve Folliküler Dalga İlişkisi Seksüel siklusun evresi, ovaryumlardan elde edilen oositlerin sayısı, oositlerin gelişim yetenekleri ve fertilizasyon başarıları ile yakından ilişkilidir.
23 11 Ovaryum üzerinde korpus luteumun varlığında bu ovaryumlardan toplanan oosit sayısı, korpus luteum ile birlikte dominant follikülün bulunması durumunda toplanan oosit sayısına göre daha fazla bulunmuştur. Bununla birlikte, ovaryum üzerinde yalnızca dominant follikülün bulunduğu durumlarda, elde edilen oosit sayısı diğerleriyle karşılaştırıldığında en düşük olarak bulunmuştur (Varisanga ve ark., 1998; Akyol, 2006). Folliküler atrezi aşamasında da bu folliküllerin in vitro maturasyon oranları düşük olarak saptanmıştır. Bu nedenle, atrezi döneminden önceki folliküler aşamada toplanan oositlerin maturasyon oranlarının daha yüksek olduğu söylenebilir (Hagemann, 1999; Kojiman, 1999; Mori, 2001; Akyol, 2006). Oositlerin östrus siklusu dönemine göre sitoplazmasında ve kromatinlerinde değişiklikler olmasına rağmen maturasyon ve fertilizasyon oranlarında farklılık saptanmıştır (Leibfield ve ark, 1985; Arlotto ve ark., 1996; Soom ve Kruif, 1996). Ayrıca yine gebe hayvanlarda oosit kalitesi açısından herhangi bir farklılığa rastlanmamıştır (Soom ve Kruif, 1996), bunların aksine Wit ve ark. (2000), in vitro embriyo üretiminde kullanılan oositlerin toplandığı folliküllerin, folliküler döneminin ve östrus siklusu döneminin sonuçları etkileyebileceğini bildirmişlerdir. Bu durumun sebebi ise oositlerin maruz kaldıkları östradiol, progesteron, FSH ve LH nın farklı seviyelerde olabilecekleri şeklinde açıklamışlardır Follikül ve Oosit Büyüklüğü Yapılan bir çalışmada sığır oositlerinin gelişim kapasitesi üzerine follikül büyüklüğü ve kalitesinin etkili olduğu ortaya konulmuştur (Lucas ve ark., 2002). Bu çalışmalarda belli folliküler faktörlerin sitoplazmik maturasyon üzerine ve bunu takip neden embriyo gelişimi üzerine etkisi olduğu görülmüştür. Barnes ve ark., (1991) küçük folliküllerden elde edilen oositlerin
24 12 nükleer olarak mature olmalarına rağmen sitoplazmik olarak immatür olduklarını belirtmişlerdir. Arlotto ve ark., (1996) ise büyük follikülerden elde edilen büyük oositler ile küçük follikülerden elde edilen küçük oositlerin maturasyon kapasitelerinin aynı olmasına rağmen büyük follikülerden elde edilen oositlerde gelişim kapasitesinin daha yüksek oranda olduğunu belirtmişlerdir. Bu yüzden IVF çalışmalarda 7 mm ve daha büyük çaptaki folliküllerden elde edilen oositler tercih edilmektedir. Bu nedenle, iyi kalitede embriyo üretimi için follikül çapı, oosit toplamada kullanılabilecek en önemli kriter olarak kabul edilmektedir (Otoi ve ark., 1997). Çiftlik hayvanlarında oositlerin in vitro ortamda gelişimlerinin iyi olabilmesi için iyi kaliteli oositlerin seçiminde follikül büyüklüğü, atrezi aşaması, folliküler sıvıdaki progesteron seviyesi gibi bir çok kriter bulunmaktadır. Bununla beraber yapılan çalışmalar kumulus oosit kompleksinin morfolojisinin, corona radiata hücrelerinin morfolojisinin ve follikül büyüklüğünün de oosit gelişimi ile ilgili olduğunu göstermiştir. Oosit büyümesi sırasında RNA sentezinin bu aşamada yoğun olmasından dolayı, oositin büyüklüğü, oosit büyümesi için bir indikatördür (Crozet ve ark., 1981; Lazzari ve ark.,1994; Lucas ve ark., 2002). Oosit çapı ve in vitro maturasyon sırasında oositin mayoz bölünmeye gitmesi ve bunu sonlandırması arasındaki ilişki insan, sığır, manda, domuz ve köpek gibi birçok canlı türünde ortaya konmuştur. Sığırlarda periferal folliküllerden elde edilen oositler, çapı ne olursa olsun benzer mayotik yetenek gösterirken, kortikal folliküllerden elde edilen oositler büyüklükleriyle ilişkili bir yetenek göstermişlerdir. Buna göre, daha küçük oositler, mayotik maturasyon için anormal bir yol izleme eğilimi ve buna bağlı olarak maturasyon sürecinde bozukluk göstermişlerdir. Sığırlarda, in vitro maturasyon ve in vitro fertilizasyon sırasında follikül büyüklüğünün oosit performansı ve oosit ve follikül büyüklüğü arasındaki ilişki daha önce de ortaya konmuştur. Domuzlarda, hem follikül hem de oosit çapının oositlerdeki nükleer maturasyon derecesi ile ilişkilidir (Shirazi ve Sadeghi, 2007).
25 Kumulus Oosit Kompleksi Mayotik dinlenme evresinde oositin gerekli ihtiyaçlarının karşılanmasından ve gelişim yeteneği kazanmasında granuloza ve teka hücrelerinin rolü olduğu, oositin, granuloza hücreleriyle birlikte oluşturduğu yapının kumulus oosit kompleksi olarak adlandırıldığı belirtilmiştir (Takashi, 1998; Akyol, 2006). Parakrin ve otokrin sistemler, hormonlar ve büyüme faktörleri sayesinde granuloza hücreleri ve oosit yakın bir ilişkide olduğu ve hücreler arası iyonların geçişini sağlayan gap junction adı verilen özel bölgeler sayesinde oosit ve kumulus hücreleri arasında direkt bir bağlantı bulunduğu bildirilmiştir (Hagemann, 1999; Akyol, 2006) Maturasyon Süresi İn vitro maturasyona alınan immatur sığır oositleri 0-6,6. saatlerde germinal vezikül (GV) oluşumu, saatlerde germinal vezikül yıkımı (GVBD), saatlerde kromozom dekondenzasyonu, saatlerde birinci metafaz, saatlerde birinci anafaz ile telofaz ve saatler arasında da ikinci metafaz aşamalarını geçirdikleri, GVBD ve birinci polar cisimciğin atılması, kumulus hücrelerinin ekspansiyonu ile yakından ilişkili olduğu ve inek oositlerinin in vitro maturasyonunda, maturasyon zamanı olarak 18 saatten 27 saate kadar değişik süreler bildirilmekle birlikte çoğunlukla saat kullanıldığı belirtilmiştir (Akyol, 2006) Sıcaklık, Nem ve Çevresel Gaz Bileşimleri Maturasyon ortamının sıcaklığı, oositin maturasyon ve fertilizasyon yeteneğini etkileyen önemli faktörlerdendir. Germinal vezikül yıkımlanması ve
26 14 birinci metafazın son aşamaları oosit maturasyon sürecinde en hassas dönem olup, düşük sıcaklık düzeylerinde mayoz iğ iplikçiklerinin oluşumu durduğu ve in vitro maturasyon süreci içerisinde, 39 C o ye yakın sıcaklık değerlerinde normal iğ iplikçikleri morfolojisinin korunduğu ve maturasyon oranının optimum düzeye ulaştığı bildirilmiştir (Ocana ve ark., 1999,). İnkubatör ortamında, maturasyon ortamının evaporasyonla derişiminin ve ph sının değişmemesi için çevresel nemin % 95 in üzerinde olması gerekir (Nagai,1999). Oosit maturasyonu için yüksek konsantrasyondaki oksijenin, oositler üzerindeki olumsuz etkisini azaltmak amacıyla gaz ortamına alternatif olarak % 5 CO 2, % 5 O 2 ve % 90 N 2 bileşimi kullanılmakta, yüksek oksijen konsantrasyonunun oosit maturasyonunu bloke ettiği ve in vitro kültür koşullarında % 20 oksijen oranının yüksek kabul edildiği ve % 5-10 oksijen düzeylerinin en uygun maturasyon oranı sağladığı kaydedilmiştir (Tervit ve ark., 1972; Takahashi ve ark., 1996) Maturasyon Ortamlarının Ozmotik Değerleri İn vitro oosit kültürü için optimum olması gereken bir diğer değer ise maturasyon ortamının ozmotik basınç değeridir ve in vitro ortamın ozmotik basıncı (308 mosm) olarak hazırlanması gerektiği, maturasyon vasatının ozmotik basıncının normal değerin üzerinde olduğu durumlarda, kültüre edilen oositlerde yüksek oranda dejenerasyon görüldüğü (Bae ve Foote, 1980) ve yüksek ozmotik basınca sahip vasatlarda oositin gelişim yeteneğinin önemli oranda düştüğü bildirilmiştir (Mazur ve Schneider, 1986; Gardner, 1998).
27 Ovaryumların Taşınma Koşulları Mezbahada kesilen hayvanların ovaryumlarının taşındığı ortam IVM, IVF ve sonraki aşamalar için büyük önem taşımaktadır. Abdoon (2003), toplanan ovaryumların 30 Cº de 1-2 saat içerisinde laboratuvara getirilmesinin önemli olduğu belirtirken, Pollard ve ark. (1996), taşıma vasatının 35 Cº nin altında olmasının embriyo üretim aşamalarını önemli derecede etkilediğini bildirmişlerdir İn Vitro Maturasyon Vasatları ve Kullanılan Katkı Maddeleri Oositin in vitro maturasyonu için kullanılan vasatların önemli bir yere sahip olduğu yapılan çalışmalarda gösterilmiştir. Bu vasatlar, oositlerin metafaz II aşamasına ulaşmasını sağlamanın yanında, fertilizasyon yeteneği kazandırması ve bunun devamında gelişim yeteneğine sahip embriyo oluşumuna da katkı sağlarlar (Bae ve Loote, 1980; Akyol, 2006). Maturasyon vasatlarının temel amacı oositin optimum ihtiyaçlarının sağlanmasıdır ve maturasyon vasatları basit ve kompleks olarak ikiye ayrılırlar (Abdoon, 2003; Akyol, 2006). Bikarbonat tampon sistemlerinin kullanıldığı temel fizyolojik tuzlardan oluşan vasatlar basit vasatlar olarak kabul edilirken, basit vasatlara ek olarak vitaminler, amino asitler gibi maddeleri içeren Ham s F-10, Ham s F-12, Brister BMCO-3, Waymouth s MB 752/1, Dulbecco s B2, KRB (Krebs Medium), MEM (Minimum Essential Medium), TALP (Tyrode s Albumine Lactate Pyruvate Medium), Menezo-B2, TCM-199 (Tissue Culture Medium- 199) kompleks vasatlara örnek olup, bunlardan TCM-199 in vitro çalışmalarda en sıklıkla kullanılmaktadır (Brackett ve ark., 1989; Greve ve Madison, 1991; Liu ve ark., 1991; Polat ve Salmanoğlu, 2005; Akyol, 2006).
28 16 Maturasyonda kullanılacak vasatlar hazırlanırken su en önemli basamağı oluşturur ve her türlü kontaminasyondan ve yabancı maddelerden arındırılmış olmasına dikkat edilmelidir. Bu amaçla en yüksek kalitedeki saf su kullanılmalıdır (Gordon, 2003; Akyol, 2006). Mezbahadan toplanan ovaryumlardaki folliküllerden elde edilen oositlerin in vitro ortamda maturasyon yetenekleri yüksek olsa da, daha sonraki aşamalarda gelişim yetenekleri, vasatlarda gerekli olan optimum koşulların tam olarak sağlanamaması nedeniyle, in vivo ortamda mature olan oositlere oranla oldukça düşüktür. İn vitro ortamın tam olarak in vivo ortama benzetilememesinin yanında, vasatlarda kullanılabilecek serumlar, büyüme faktörleri, hormonlar ve diğer katkı maddeleri, oositin in vitro ortamda gelişim yeteneğini olumlu yönde etkileyebilmektedir (Romero ve Seidel, 1996; Choi ve ark., 2001; Polat ve Salmanoğlu, 2005) Hormonlar İneklerde ovaryum fonksiyonlarının düzenlenmesinden sorumlu olan anahtar hormonlar FSH ve LH; ve bir diğer hipofiz hormonu olan prolaktinin ovaryum üzerindeki etkileri daha önce yapılan çalışmalarda belirlenmiştir. Literatürde bulunan in vitro maturasyon ile ilgili yapılan çalışmalarda daha bir çok farklı gonadotropinlerin (FSH ve LH) ve steroidlerin (Östradiol) maturasyon vasatlarına eklenmesi uygulamaları yapılmıştır. İrlandada, Liu ve arkadaşları (1991), maturasyon vasatlarına bu hormonlar eklenmese de maturasyonun gerçekleştiğini bunun da nedeninin maturasyona katılan hem serum hem de granuloza hücrelerinin bu hormonları ihtiva etmesinden kaynaklandığını belirtmişlerdir. Aynı zamanda granuloza hücrelerinin kültür ortamında bulundukları süre içinde steroidogenezis yeteneğine bağlı olarak östradiol ürettikleri bilinmektedir (Gordon, 2003).
29 17 Gonadotropik hormonların oosit maturasyonu, fertilizasyonu ve erken embriyo gelişimi üzerine olan etkileri farklı olduğu belirtilmiştir. Kumulus ve granuloza hücrelerinde reseptörleri bulunan FSH, granuloza hücrelerindeki aromataz aktiviteyi canlandırarak folliküler mikroçevrenin androjen karakterden östrojene dönüşmesini sağlar (Polat ve Salmanoğlu, 2005; Akyol, 2006). İn vivo koşullarda FSH, ovaryumdan östrojen ve inhibin salınımını uyarırken, in vitro ortamda etkinliği kumulus hücrelerinin varlığına bağlıdır. İn vitro şartlarda FSH nın kumulus hücre ekspansiyonu ve sperm kapasitasyonu ile fertilizasyon aşamasında etkili olduğu bildirilmektedir (Eyestone ve Boer, 1993; Izadyar ve ark., 1998; Polat ve Salmanoğlu, 2005; Akyol, 2006). İn vitro maturasyonda kullanılan FSH nın 0,15 ng/ml, 1,5 ng/ml veya 15 ng/ml dozlarında kullanımı, siklik AMP artışını uyararak kumulus hücrelerinde genişleme meydana getirdiği bildirilmektedir (Choi ve ark., 2001; Polat ve Salmanoğlu, 2005). Lüteinleştirici Hormon (LH) nın rolü oosit maturasyonundan daha çok in vitro fertilizasyon sonrası erken embriyonik gelişimde ortaya çıktığı bildirilmektedir (Fukui ve Ono, 1989; Zuelke ve Brackett, 1993; Akyol, 2006). Kültür vasatlarına ilave edilen LH oositin kumulus hücrelerinin yardımıyla glikoz kullanımı artırarak maturasyon ortamında pirüvik asit yapımını hızlandırmaktadır. Böylece hücrede glikolizis uyarılmaktadır. LH nın etkisini gösterebilmesi için, teka hücrelerindeki LH reseptörlerine yani dolayısıyla kumulus-oosit komplekslerine ihtiyaç vardır (Zuelke ve Brackett, 1993; Akyol, 2006). Zuelke ve Brackett ın (1990) yaptıkları bir çalışmada, in vitro fertilizasyonda kültür vasatına LH eklenmesinin fertilizasyon oranını yükselttiği görülmüştür. Birçok araştırıcı oosit maturasyonu amacıyla FSH ve LH kombine halde vasata katılması halinde iyi derecede maturasyon ve fertilizasyon sonucu aldıklarını bildirmektedir (Fukushima ve Fukui, 1985; Birler ve ark., 1997; Marquant ve Humblot, 1998; Akyol, 2006).
30 18 Prolaktin, maturasyon vasatının içeriğine bağlı olarak, oositin in vitro ortamda mayozunu destekler. Erken gelişim dönemindeki oositte, Ca +2 seviyesini kontrol altında tutarak bazı kromozom dejenarasyonlarını önlediği (Akyol, 2006), epitel hücrelerinin yüzeyinin bozulmasını ve follikül duvarında bulunan bağlayıcı dokuların ayrışmasını engellediği bildirilmektedir (Yoshimura ve ark., 1991; Polat ve Salmanoğlu, 2005). Östrojen ve progesteron, in vitro koşullarda oosit maturasyonunu uyarmak amacıyla ve çoğunlukla gonadotropinlerle birlikte kültür vasatlarına katılmaktadırlar (Mori, 2001). İn vitro koşullarda Östradiol 17-β (E2), etkisini hedef organlardaki reseptörler yardımıyla göstererek, epitel mitogenezisi, sekretorik protein yapımı, apoptozis gibi durumlarda epitel hücrelerinin başkalaşımı ve bu hücrelerdeki progesteron reseptörleri üzerinde düzenleyici rol oynarlar. Epitel hücrelerinin proliferasyonunda, östrojen ve büyüme faktörleri (GF) birlikte gelişimi düzenlerler ve epidermal büyüme faktörlerinin ve onların reseptör sayısının artmasını sağlarlar (Cooke ve ark., 1992; Akyol, 2006). Östradiolün follikül gelişiminde ve ovulasyonda önemli rol oynadığı bildirilmiştir. Östradiolün etkisiyle granuloza hücrelerinin gonadotropinlere karşı cevabıyla steroid sentezi artmakta, bu da follikül hücrelerinin proliferasyonunu ve farklılaşmasını sağlamaktadır. Ovulatör LH yükselişiyle birlikte, oositin follikül içinde nükleer maturasyonu başlar. Ovulasyondan sonra zamanla östradiol düzey düşmeye ve progesteron düzeyi artmaya başlar. Oosit maturasyonu için östradiol/progesteron dengesinin büyük önemi vardır (Gordon, 2003). Sığır oositlerinin in vitro maturasyon vasatına ilave edilen östradiol miktarının yüksek oranda (>1µg/ml) olması nükleer maturasyon ve polar cisimciğin atılması üzerine olumsuz etki yaptığı ve ayrıca çekirdek bozukluğu yüzdesini artırdığı bildirilmiştir (Beker ve ark., 2002).
31 Büyüme Faktörleri Büyüme faktörlerinin sığır oositlerinin in vitro maturasyonu üzerine uyarıcı etkileri olduğu bilinmektedir ve her geçen gün bu düşünce daha da fazla önem kazanmaktadır. Epidermal büyüme faktörü (EGF) ve insülin benzeri büyüme faktörü-1 (IGF-1) üzerinde en fazla çalışılan ovaryum fonksiyon düzenleyicilerdir (Grupen ve ark., 1997) ve maturasyon süresince metabolizmayı uyarıcı etki yapmaktadırlar (Gandolfi ve ark.,1996). Her ikisi de güçlü birer granuloza hücre mitojenidir ve FSH ve LH nın reseptörleri üzerine bağlanma kapasitelerini arttırırlar (Grupen ve ark., 1997). İnsülin benzeri büyüme faktörü-1 (IGF-1), birçok türde oosit maturasyonunu stimüle eden ve daha sonraki embriyo gelişimini sağlayan bir faktördür. İnsülin benzeri büyüme faktörü-1 in kültür vasatlarına eklenmesinin, insan, fare ve tavşan embriyolarında hücre proliferasyonunu arttırması ve apoptozisi düşürerek preimplantasyon şansını arttırması gibi yararları olduğu belirtilmiştir (Makarevich ve Markkula, 2002). Apoptozis in vitro ortamda kültüre edilen blastosistlerde doğal ortama göre suboptimal şartlar meydana geldiğinde oluşan bir olaydır. İnsülin benzeri büyüme faktörü-1 embriyo gelişimi sırasında ve daha sonra organogenezis sırasında apoptozisi engelleyen bir faktör olarak önemli bir rol oynamaktadır (Lin ve ark, 2003). Son yıllarda memelilerde follikülogenezis üzerine IGF-1 in rolü geniş bir şekilde araştırılmaktadır (Monget ve Brody, 2000; Nuttinck ve ark., 2004) ve yapılan araştırmalar IGF-1 in sığırlarda oosit maturasyonu, erken embriyonik gelişim ve gebelik oranları üzerine etkisi olduğunu göstermektedir (Moreira ve ark., 2002 ). İnsülin benzeri büyüme faktörü-1 in, in vitro ortamda hem teka hem de granuloza hücrelerinin proliferasyonunu ve değişimlerini uyardığı göstermektedir. Buna ek olarak, IGF-1, FSH tarafından uyarılmış camp üretimini, aromataz aktiviteyi ve granuloza hücreleri tarafından LH
32 20 reseptör oluşumunu arttırarak etki etmektedir (Monget ve Brody, 2000). İnsulin benzeri büyüme faktörünün folliküler hücre proliferasyonu ve steroidogenezis üzerine etkileri konusunda birçok çalışma yapılmıştır. Sığırlar üzerine yapılan birkaç çalışma, terminal büyüme sırasında lokal ovaryum kökenli IGF sistemi ile folliküler hücre proliferasyonu ve değişiminden sorumlu gonadotropinler arasında etkileşim olduğundan bahsetmektedir. Yine birkaç çalışmada oositin gonadotropin ve IGF uyarımlı steroidogenezisi ayarlayan kumulus hücreleriyle birlikte çalışan parakrin büyüme faktörleri salgıladığını ortaya koymuştur. Maturasyon vasatlarında IGF-1 in varlığının, sığır oositlerinin mayoz ilerlemesini tetiklediği görülmüştür (Nuttinck ve ark., 2004). Bu bulgular aynı zamanda IGF-1 in FSH regülasyonunu sağlayarak granuloza hücrelerinin indüklenmesinde sinerjistik olarak etkidiğini desteklemektedir. Follikül stimüle edici hormon un granuloza hücre kültürlerinde IGF-1 reseptörlerini arttırdığı ve FSH nın, IGF-1 aracılığı ile etki ettiği bildirilmiştir. İnsan, sığır, rat ve fare araştırmalarında, preantral folliküllerin in vitro kültürlerine IGF-1 eklendiğinde FSH ile sinerjistik etki göstererek, folliküler gelişimi stimüle ettiği görülmüştür. Ayrıca diğer türlerde, IGF-1 in, kompakt kumulus hücreleriyle sarılı oositlerde nükleer maturasyonu indükleyici rol oynadığı belirtilmiştir (Demeestre ve ark., 2004). Yapılan çalışmalarda epidermal büyüme faktörünün de (EGF) oosit maturasyonu üzerine etkileri araştırılmış, EGF nin oosit maturasyonu sırasında sentezlenmeyen proteinlerin oluşumunu stimüle ettiği görülmüştür. EGF nin folliküler gelişim üzerinde etkisi ise parakrin/otokrin biçimde regülatör bir rol oynamak veya oositlerde mayozun yeniden başlamasını tetikleyen faktörlerden biri olarak açıklanmıştır (Purohit ve ark., 2005). Park ve Lin in (1993) yaptığı çalışmada, EGF nin sığır oosilerinin maturasyonu ve erken embriyonik gelişim üzerine olan etkilerini araştırmışlardır. Sığır oositleri in vitro ortamda mature edilmişler ve daha sonra dondurulup çözülen HBS solusyonunda kapasite ediliş boğa
33 21 spermasıyla tekrar kültüre edilmişlerdir. Oosit-sperm kompleksi 4 günlük bir inkübasyon periyodundan sonra bölünme oranları yönünden değerlendirilmiştir. Sonuçlar şu sıraya göre değerlendirilmiştir. Buna göre; 1) sığır oositleri, %10 luk FCS veya EGF+ BSA içeren Park-Lin 1 medyumunda (PL-1) mature edildikten sonra fertilizasyondan sonra elde edilen embriyo bölünme oranları (%18), tek başına FCS uygulanan (%10) gruptan daha başarılı bulunmuştur. 2) Sığır oositleri EGF içermeyen Park-Lin 2 (PL-2) medyumunda olgunlaştırılıp edilip daha sonra bu oositlerin EGF içeren PL-2 medyumunda gelişim için bırakılması sonucunda, embriyonik bölünme oranı %22. 6 olarak bulunmuştur. 3) Sığır oositleri EGF içeren PL-2 medyumunda mature edilip daha sonra tekrar EGF içeren PL-2 medyumunda gelişime bırakıldıklarında, embriyonik bölünme oranla %35.8 olarak bulunmuştur. 4) Sığır oositleri EGF içermeyen PL-3 medyumunda mature edildikten sonra PL3 medyumunda gelişim için bırakıldığında embriyonik bölünme oranı %50 olarak bulunmuştur. 5) Sığır oositleri EGF içeren PL-3 medyumunda mature edildikten sonra embriyonik bölünme oranları %53 olarak bulunmuştur. Sonuçlar, EGF nin direkt olarak oosit maturasyonu ve daha sonraki embriyonik gelişim üzerine etkisi olduğu tespit edilmiştir. Purohit ve ark. (2005), yaptıkları çalışmada EGF ve IGF-1 kombinasyonunun sığır oositlerinin in vitro maturasyon ve fertilizasyonu üzerine olan etkisini araştırmışlardır. Daha önceki çalışmalarda kullanılan standart dozlamalar (EGF 10 ng/ml, IGF-1 50 ng/ml) kullanılmıştır. Çalışmanın sonuçlarında; kontrol grubuyla EGF+IGF-1 kombinasyonu uygulanan gruplar arasında karşılaştırma yapıldığında metafaz- II aşamasına ulaşabilen oositlerin oranında artış görülmüş ve yine bu sonuçlar EGF+IGF-1 kombinasyonu kullanılan grupla, tek başına EGF veya IGF-1 kullanılan gruplarla karşılaştırıldığında arada önemli bir fark bulunmamıştır. Sakaguchi ve ark. nın (2000) benzer konuda yaptığı çalışmada, büyüme faktörlerinin sığır oositlerinin maturasyonu, fertilizasyonu, polar
34 22 cisimcik oluşumu ve gelişim yeteneği üzerine arttırıcı etkileri olduğunu bildirmişlerdir Protein (Serum ve Albumin) Katkıları Sığır follikül sıvısı (bff), follikül duvarındaki hücrelerden sentezlenen steroidler ve glikoproteinler gibi bileşenlerden ve folliküler metabolik aktivitelerin sonucunda oluşan bir modifiye serum transudatıdır. Lonergan (1992), in vitro maturasyon vasatına %10-20 oranında sığır follikül sıvısı ilavesinin embriyonik gelişime destek verdiğini bildirmiştir. Aynı zamanda Iritani ve ark. (1992) da %20-30 bff ilavesinin embriyonik gelişime destek verdiğini belirtmişlerdir. Bu durum çeşitli çalışmalarda bff de bulunan çeşitli faktörlerin oositin kalitesini olumlu yönde etkilediği fikrini ortaya koymaktadır. Ancak Ayoub ve Hunter (1993), sığırlarda, küçük folliküllerden elde edilen bff nin mayozu inhibe ettiğini bildirmişlerdir. Östrus başlangıcından, diöstrusun ortasına kadar geçen sürede orta ve küçük boyutlu folliküllerden elde edilen bff nin, erken proöstrus dönemine göre GVBD inhibisyonunun daha fazla olduğu bildirilmiştir (Romero ve Seidel, 1996). Choi ve ark. (2001) maturasyon vasatına yüksek oranda (%10-20) ilave edilen bff nin mayozun yeniden başlamasını, fertilizasyon oranlarını ve embriyo gelişimini inhibe ettiğini belirtmişlerdir. Embriyo kültüründe, gelişim yeteneğinin düşmemesi ve metabolik aktivitelerin aksamaması için ortamda protein olması önemlidir. Oositlerin in vitro maturasyonuna yardımcı olmak için ve embriyo için gerekli olan bazı hormon, büyüme ve beslenme faktörlerini içerdikleri düşünüldüğü için, kültür ortamlarına fötal buzağı serumu (FCS), östrustaki sığır serumu, kastre edilmiş boğa serumu veya proöstrustaki sığır serumu gibi çeşitli serumlar ve sığır serum albumini (BSA) ilaveleri yapılmaktadır (Ocana ve ark., 1999; Gomez ve Diez, 2000; Polat ve Salmanoğlu, 2005).
35 23 İn vitro fertilizasyonda protein kaynağı olarak sıklıkla sığır serum albumini ve sığır serumu kullanılmaktadır. Sığır serum albumininin (BSA), saf olarak elde edilemediğinden kültür süresince değişik sonuçlar verebilir (Ali ve Sirard, 2002; Polat ve Salmanoğlu, 2005). İn vitro maturasyonda fötal buzağı serumunun (FCS), BSA ya göre daha etkili olduğu bildirilmektedir (Polat ve Salmanoğlu, 2005). Fötal buzağı serumu, in vitro maturasyonda kumulus hücrelerinin yaşama yeteneklerinin düzenlenmesi ve birinci mayoz bölünmenin tamamlanması açısından önemliyken, in vitro fertilizasyondan sonra morula ve blastosist aşamasına ulaşan embriyo sayısını da artırdığı belirtilmektedir (Polat ve Salmanoğlu, 2005). LH ve östrustaki inek serumu (ECS) ile birlikte kullanıldığında fertilizasyon ve ilk bölünme oranının da önemli ölçüde arttığı bildirilmektedir (Schellander ve ark., 1990). Östrustaki sığır serumunda östrodiol seviyesi en yüksek seviyede olduğu dönemde LH seviyesinde de artış gözlemlendiği için vasatlara ilave edildiğinde blastosist aşamasına ulaşan oosit sayılarında artış gözlemlendiği bildirilmiştir (Glieldt ve ark., 1996; Polat ve Salmanoğlu, 2005). Yapılan bir çalışmada proöstrustaki sığır serumu yüksek düzeyde LH ve prolaktin içerdiği için in vitro maturasyon vasatlarına %20 oranında eklendiği zaman, fertilizasyondan sonra ECS ye göre daha yüksek oranda embriyo elde edildiği belirtilmiştir (Younis ve ark., 1989; Polat ve Salmanoğlu, 2005) Antioksidan Katkıları İn vitro kültür ortamında oositlerin, yüksek oksijen varlığına bağlı olarak oluşan oksidatif ürünlerin olumuz etkilerinden korunması amacıyla ortama antioksidan maddelerin ilave edilmesi önem taşımaktadır. Bu amaçla, β- merkaptoetanol, bazı tokoferoller (DL-α-tocopherol), etoksikuin gibi bazı antioksidanlar kullanılmaktadır (Fujitani ve ark.,1997; Akyol, 2006).
36 Hücresel Katkılar Vasatlara hücresel katkının amacı, ortamdaki serbest oksijen yoğunluğunun azaltılmasının yanında 8-16 hücre aşamasındaki embriyonun gelişiminin durmasını önlemektir. Bu amaçla farklı türlerdeki dokulardan elde edilen farklı hücre tipleri kullanılmaktadır. Yaygın olarak; kumulus/granuloza, teka hücreleri, sığır oviduktu epitel hücreleri, sitokinler kullanılmaktadır (Wiemer ve ark., 1991). Kumulus hücrelerinin glikolizisle beslenmeye katkısı olduğu ve maturasyon vasatlarında 3-5 milyon kumulus/granuloza hücresi bulunmasının yüksek oranda oositlerin in vitro fertilizasyon sonrası blastosist aşamasına ulaştığı görülmüştür (Polat ve Salmanoğlu, 2005). Teka hücreleri granuloza hücreleri tarafından östrojen biyosentezi için, transforme edici bütüme faktörü- β (TGF-β) ve transforme edici bütüme faktörü-α (TGF-α) gibi diğer büyüme faktörlerinin salınımında rol oynamaktadırlar (Polat ve Salmanoğlu, 2005). Sitokinler, annenin immunolojik olarak gebeliğe hazırlanmasında, fertlizasyonda ve erken gebelikte endokrinolojik olayların meydana gelmesinde rol oynarlar. Makrofajlar, T ve B lenfositler, monositler ve interlökinler (IL) sitokinleri oluşturmaktadır. İnterlökinlerle ilgili bilgiler sınırlı olsa da, insan rekombinant IL-1 in follikülün maturasyonu ve farklılaşmasında rol oynadığı belirtilmiştir (Polat ve Salmanoğlu, 2005) Maturasyon Maturasyon, kumulus hücrelerinin genişlemesi, oositin birinci metafaz safhasına girerek, germinal vezikülün yıkımlanmasını takiben, ilk polar
37 25 cisimciğin çıkısı ve oositin metafaz 2 safhasına geçmesi olarak tanımlanır. Oositte maturasyonun degerlendirilmesi, kumulus hücre ekspansiyonuna ve ilk polar cisimciğin varlığına bakılarak yapılmaktadır (Akyol, 2006) İn Vitro Fertilizasyon Spermin Kapasitasyonu ve Akrozom Reaksiyonu Normal şartlar altında in vivo ortamda başarılı bir fertlizasyon için, memeli spermatozoasında zona pellusidaya penetre olup oositin plazma membranı ile birleşmesi için gerekli bir dizi hücre dışı olaylar zinciri olan kapasitasyon ve bunu izleyen akrozom reaksiyonu oluşur. Bu karmaşık olaylar in vivo ortamda sadece belli sayıda spermatozoanın fertilizasyon şansı bulmasının yanında, doğru zamanda doğru yerde başarılı bir fertilizasyon gerçekleştirmesine olanak sağlar. Fertilizasyon yeteneğinin düzenlenmesinde elde edilen başarının arttırılabilmesi için pek çok yöntem geliştirilmiştir. Fertilizasyon süresi boyunca spermatozoanın iki önemli rolü vardır: (i) normal gelişim için gerekli olan babaya ait gen modellerinin kendi cinsi/türü için tanınmasında haploid sayılı kromozomlara katkı sağlamak, (ii) oosit aktivasyonunu ve embriyonik gelişimi desteklemek için gerekli metabolik olayların kendiliğinden başlamasını tetiklemek. İn vivo ortamda, memeli spermatozoasının fertilizasyon yeteneğinden elde edilen sonuç, uzun süreli bir olay, dişinin alt genital sisteminden, oviduktun üst ampullar bölgesine göç edebilecek yeteneğe sahip hücrelere gereksinim duyulan bir durumdur den beri yapılan çalışmalarda, spermatozoanın erkek genital sisteminin terk ettikten sonra, hala yüksek oranda motil olmasına rağmen, fertil olmadıkları bildirilmiştir. Fertilizasyon yeteneklerini kazabilmeleri için
38 26 kapasitasyon denilen fertilizasyon yeteneği olmayan hücreleri potansiyel fertil hücrelere dönüştüren, türe özgü, bir dizi karmaşık değişiklik geçirmek zorundadırlar (Fraser, 1998). Kapasitasyon aşamasından sonra spermatozoa, oosit ve oositin diğer bağımlı bölümlerinden (kumulus hücreleri, zona pellusida) gelecek olan moleküler uyarımlara karşı cevap verebilecek hale gelir ve daha sonra akrozom reaksiyonu gerçekleşir (Fraser, 1998). In vitro ortamda, kapasitasyonun belirlenebilmesi için Bryan boyası, trypan blue-giemsa, nigrosin-eosin-giemsa, fast green-eosin B, trypan blue- Bismarck, brown-rose Bengal gibi boyamalar yaygın olarak kullanılmaktadır (Serin ve Tekin, 2003). Akrozom, sperm nukleusunun anterior kısmını içine alacak şekilde zarla kapatan bir yapıdır ve birçok hidrolize edici enzim içermektedir. Normal bir fertilizasyon için gereken ilk koşul olarak, akrozom reaksiyonu sırasında akrozom içeriği zona pellucidanın tetiklemesiyle serbest bırakılır (Birck ve ark., 2010). Membran reaksiyonu, baştan sona plazma membranı ile dış akrozomal membranın birleşmesini ve vezikülasyonu başlatır. Daha sonra, bir çeşit akrozomal içeriğin serbest bırakılması ve iç akrozomal membranın dışa doğru bırakılması olayı meydana gelir (Jankovicova ve ark., 2006). Bu nedenle, boğalarda akrozom reaksiyonuna uğrayacak olan sperm populasyonu, aynı zamanda fertilizasyon yeteneğine sahip olan sperm populasyonunu işaret eder. İn vitro ortamda akrozom reaksiyonunu indüklenmesinde klasik bir yöntem olarak kalsiyum iyonofor A23187 kullanılmaktadır. Kalsiyum iyonofor, sperm plazma membanındaki Ca +2 kanalları seviyesinde etki etmektedir ve Ca +2 akışını dolayısıyla, uygun yolları tetikleyerek plazma membranı ve dış akrozomal membran arasındaki kaynaşmayı sağlamaktadır (Birck ve ark., 2010). Birbirini takip eden spermatozoon kapasitasyonu ve akrozom reaksiyonu, ineklerde 6 saat içinde tamamlanmaktadır. Bu aşamalar sırasında oviduktun silier hücreleri östrodiol tarafından uyarılmıştır ve
39 27 oluşturdukları ritmik hareketlerle oosit oviduktta ilerletilir. Bu sırada kumulus hücreleri yavaş yavaş yok olmaya başlar (Liebfried-Rutledge, 1999) Sperm Hazırlama Yöntemleri Spermin, rutin olarak in vitro fertlizasyonda kullanılabilmesi için çeşitli yöntemlerle fertilizasyona hazırlanması gerekmektedir. Bu yöntemler, kullanılacak kaliteli sperm sayısını arttırmak ve seminal plazma/krioprotektan, ve diğer başka maddelerin uzaklaştırılmasında kullanılmaktadır. Sperm hazırlama için, swim-up, Percoll gradient ve glasswool filtrasyon yöntemi gibi yöntemler kullanılmaktadır. Bu yöntemler arasında fertilizasyon veya blastosist oluşum oranları arasında fark bulunmasa da, sığır IVF laboratuvarlarında en sıklıkla kullanılan yöntem Percoll gradient tekniğidir (Machado ve ark., 2009). Percoll gradient tekniğinin temeli motil spermatozoonlar ile motil olmayan spermatozoonların birbirinden ayrılmasına dayanmaktadır. Daha önce yapılan çalışmalarda da Percoll gradient kullanımının sadece kullanılacak motil sperm sayısını arttırmasının yanında aynı zamanda normal morfolojiye sahip hücre sayısını arttırdığı, tam bir akrozom ve membran reaksiyonu sağladığı bildirilmiştir. Farklı yoğunluklardaki (%45-%90) Percoll gradient in santrifüj kuvvetiyle birleşmesiyle sperm-oosit etkileşimini, fertilizasyonu ve embriyo oluşumunu pozitif yönde etkilediği de bildirilmektedir (Machado ve ark., 2009). Sperm hazırlama yöntemlerinden bir diğeri de swim-up yöntemidir. Swim-up yöntemi, dondurulmuş spermin çözdürülüp, motilitesi yüksek olan spermlerin uygun TALP solusyonunda inkübasyondan sonra, solüsyonun yüzeyinde yüzdürülmesi esasına dayanmaktadır. Bu yöntem kolay ve ucuz
40 28 olması yönünden en çok tercih edilen yöntemlerden biri olarak bildirilmiştir (Wolf ve ark., 2008) İn Vitro Fertilizasyonun Değerlendirilmesi İn vitro embriyo üretiminde, fertilizasyonun belirlenmesi için önemli ölçütler Shioya (1993) tarafından şu şekilde bildirilmiştir; 1. Spermatozoon kuyruğunun ooplazma içinde saptanması, 2. Spermatozoon başının ooplazma içerisinde görülmesi, 3. Ooplazma içinde dişi ve erkek pronükleusların varlığı, 4. Birinci ve ikinci kutup hücrelerinin saptanması, 5. Zona pellusida veya perivitellin boşlukta spermatozoon varlığı, 6. İkinci mayoz bölünmenin telofaz aşamasının ya da oosit aktivasyonunun tespiti. Brackett ve ark. (1981) tarafından yapılan bir çalışmada ise perivitellin boşlukta çift kutup hücresinin görülmesi, bölünmelerin başlangıcı ve kortikal granüllerin kaybolması fertilizasyon ölçütü olarak kullanılmaktadır İn Vitro Embriyo Kültürü İn vitro üretimler 3 ana aşamadan meydana gelmektedir, in vitro oosit maturasyonu, in vitro fertilizasyon ve in vitro embriyo kültürü. Son 20 yıldır yapılan çok yönlü araştırmalar ve çeşitlilik gösteren tekniklere rağmen, yapılan çalışmaların sonuçlarından yetersiz sonuçlar alınmaktadır; immatur oositlerin %90 ı profaz I aşamasından metafaz II aşamasına geçip mature
41 29 olabilmekte, bunlardan en fazla %80 i başarılı bir fertilizasyon aşamasını tamamlayıp, tohumlamayı takiben saat içinde 2 hücreli aşamaya geçebilmektedir. Bununla birlikte immatur oositlerin sadece %30-40 ı tohumlamadan 7-8 gün sonra blastosist aşamasına erişebilmektedir (Rizos ve ark., 2008). Preimplantasyon aşamasındaki embriyolar birçok çalışmaya ilham kaynağı olmuştur. İn vitro üretilen sığır embriyoları, fertilizasyondan sonraki 1 hafta içinde şekillenen fizyolojik olaylar üzerinde çalışmalar yapmak için birçok yönden elde edilebilir veriler sağlamaktadır. İn vitro ortamda fertilizasyondan sonraki aşamalarda memeli embriyoları, birkaç oosit bölünme aşamasından sonra blastosist oluşumunu gerçekleştirebilmek için uygun çevre ortamına gereksinim duyarlar (Rizos ve ark, 2008). Preimlantasyon döneminde embriyolar, içeriği basit tuzlu çözeltilerden ve karbonhidratlardan (örneğin: Charles Rosenkrans 1 (CR1), sentetik ovidukt sıvısı (SOF) ve potasyum simpleks optimizasyon medyumu (KSOM)) oluşan vasatlarda gelişimlerini sürdürebildikleri gibi daha karmaşık yapıya sahip bileşenlerden, doku kültür medyumu-199 (TCM-199) gibi, ortamlarda da gelişimlerini sürdürebilirler (Rizos ve ark, 2008). Daha öncede bahsedildiği gibi embriyo üretimindeki en büyük düşüş in vitro aşamaların embriyo üretim aşamalarının son kısmında, fertilizasyon sonrası kültürde, 2 hücreli aşamadan blastosist oluşuna kadar geçen sürede meydana gelmektedir. Elde edilen blastosist sayısına bakıldığında tohumlama sonrası embriyo kültürünün en kritik dönem olduğu görülmektedir. Bununla birlikte, oosit kalitesinin, blastosist oluşturabilecek immatur oositlerin oranını etkilediği bilinmektedir (Rizos ve ark, 2008).
42 30 Fertilizasyon sonrası 6 günlük periyotta, zigottan blastosist oluşumuna kadar geçen sürede, blastosistin kalitesini etkileyecek çeşitli gelişimsel olaylar meydana gelmektedir. Bunlar; ilk bölünme, 8 hücreliden 16 hücreli aşamaya kadarki zamanda embriyonik genomun aktivasyonu, 5.günde, embriyonun hücreler arası iletişimini sağlayan morulanın kompaksiyonu ve 6.-7.günlerde blastosist oluşumu olarak bildirilmiştir (Rizos ve ark, 2008). Bu bilgilerin dışında in vitro üretilen blastosistlerin, in vivo ortamda üretilen blastosistlere oranla daha az kaliteli olduğu, daha koyu renkli bir sitoplazmaya sahip oldukları, daha hassas bir zona pellusida ya sahip oldukları, hücreler arası iletişim bağlarının zayıf olduğu, metabolizmalarında farklılıklar olduğu ve kromozomal anomalilere daha yatkın oldukları daha önce yapılan çalışmalarda belgelenmiştir (Rizos ve ark, 2008). Bu tez çalışmasının amacı, farklı büyüklükteki sığır oositlerinin maturasyon vasatlarına ilave edilen insülin benzeri büyüme faktörü-1 (IGF-1) ve epidermal büyüme faktörünün (EGF) oosit maturasyonu, fertilizasyonu ve embriyo kalitesi üzerine ne gibi etkilerinin olduğunun araştırılmasıdır.
43 31 2. GEREÇ VE YÖNTEM 2.1. Ovaryumların Toplanması Çalışmada kullanılan oositlerin toplandığı ovaryumlar Ankara ili, Çubuk belediye mezbahasında kesilen inek ve düvelerden elde edildi. Karkaslardan alınan ovaryumlar çevre dokularından uzaklaştırıldı. Taşıma vasatı olarak 35ºC ye ayarlanmış termos ile antibiyotik-antimikotik solüsyon katkılı %0,9 luk NaCl kullanıldı. Ovaryumların karkastan alınıp, oositlerin maturasyon vasatına konulmasına kadar olan sürenin 4 saati geçmemesine özen gösterildi. İn vitro fertilizasyon laboratuvarına getirilen ovaryumlar, kandan ve taşıma vasatından uzaklaştırılmak amacıyla 30 C deki %0,9 luk NaCl ile yıkanıp, içinde %0,9 luk NaCl bulunan behere alındı Oosit Aspirasyonu ve Oositlerin Seçimi Aspirasyon işlemi 18 G luk kanüller takılmış 5 ml lik contasız plastik tek kullanımlık enjektörlerle gerçekleştirildi. Aspirasyon için 2-8 mm çapındaki folliküller tercih edildi. Elde edilen follikül sıvıları 15 ml lik santrifüj tüplerinde biriktirildi. Oositlerin çökmesi için tüpler 38,5 C ayarlanmış etüvde 10 dakika süre ile bekletildi. Bu süre sonunda üstteki süpernatant atılarak üzerine bir miktar daha önceden hazırlanan oosit arama vasatı (%1 fötal buzağı serumu (FCS) içeren laktatlı ringer solüsyonu) eklenerek oositlerin çökmesi için 10 dakika daha beklendi.
44 32 Etüvden çıkarılan tüp, üzerindeki süpernatant tekrar uzaklaştırılarak, tüpün kalan kısmına arama vasatı eklenip karıştırılarak, içerik daha önceden hazırlanmış olan 90 mm lik petriye aktarıldı. Zuelke ve Brackett (1993) nin tarif ettiği şekilde seçilen oositler, içinde arama vasatı bulunan 60 mm lik petriye aktartıldı. Daha sonra içinde maturasyon vasatı (TCM-199+%5 FCS) bulunan 35 mm lik 3 ayrı petride yıkanan oositler Lucas ve ark. (2002) nın tarif ettiği şekilde, Leica Application Suite programı kullanılarak zona kalınlığını da dahil edilerek, çaplarına göre ayrıldı (<110 m, m, >150 m), her 100 µl sinde 20 oosit olacak şekilde hazırlanan, gruplarına göre büyüme faktörleri eklenmiş (IGF-I 50 ng/ml, EGF10 ng/ml ve IGF-I 50 ng/ml +EGF 10 ng/ml) ve üzeri mineral yağ ile kaplanmış 100 µl lik maturasyon vasatı droplarına aktarılarak %5 CO 2 li 38,5 C deki etüvde 24 saat maturasyon için bekletildi. Şekil : Oosit çapı ölçümleri
45 Oositlerin Gruplandırılması Çizelge : Grup I in oluşturulması ve uygulama prosedürü Grup I n Oosit çapı (µm) Uygulama Grup 1A TCM 199+IGF-I (50ng/ml) Grup1B TCM 199+IGF-I (50ng/ml) Grup1C TCM 199+IGF-I (50ng/ml) Çizelge : Grup II nin oluşturulması ve uygulama prosedürü Grup II n Oosit çapı(µm) Uygulama Grup 2A TCM 199+EGF (10ng/ml) Grup 2B TCM 199+EGF (10ng/ml) Grup 2C TCM 199+EGF (10ng/ml) Çizelge : Grup III ün oluşturulması ve uygulama prosedürü Grup III n Oosit çapı(µm) Uygulama Grup 3A TCM 199+EGF+IGF-I Grup 3B TCM 199+EGF+IGF-I Grup 3C TCM 199+EGF+IGF-I Çizelge : Grup IV ün oluşturulması ve uygulama prosedürü Grup IV n Oosit çapı(µm) Uygulama Grup 4A TCM 199 Grup 4B TCM 199 Grup 4C TCM 199
46 Ekilibrasyon ve Kültür Şartları Tüm gruplarda kullanılan vasatlar, oositler maturasyona başlamadan 1 gün önce veya en az 12 saat önce %5 CO 2 li 38,5 C de ve maksimum nem ortamında ekilibrasyona bırakıldı Maturasyon Kriterlerinin Değerlendirilmesi Şekil : Maturasyon öncesi ve maturasyon sonrası oositlerin görünümü Maturasyon süresinin tamamlanmasının ardından oositlerin kumulus ekspansiyonları kaydedilmiştir. Maturasyon oranının belirlenmesi için kumulus ekspansiyonu görülen oositler pipetasyon işlemi ile kumulus hücrelerinden tamamen ayrılmış ve stereo mikroskop altında 1.kutup hücresinin atılımı açısından incelenmiştir. 1.kutup hücresi atan oositler matur olarak değerlendirilip bu oositlerin tümüne in vitro fertilizasyon uygulanmıştır.
BİYOTEKNOLOJİ NEDİR? Canlılar aracılığı ile ürün ve hizmet üretmektir
 BİYOTEKNOLOJİ NEDİR? Canlılar aracılığı ile ürün ve hizmet üretmektir Reprodüktif Biyoteknolojinin Amacı Canlılarda in vivo ve in vitro koşullarda gen kaynaklarının uzun süreli korunması ve daha fazla
BİYOTEKNOLOJİ NEDİR? Canlılar aracılığı ile ürün ve hizmet üretmektir Reprodüktif Biyoteknolojinin Amacı Canlılarda in vivo ve in vitro koşullarda gen kaynaklarının uzun süreli korunması ve daha fazla
İN VİTRO EMBRİYO ÜRETİMİ
 İN VİTRO EMBRİYO ÜRETİMİ İn vitro döllemenin tarihçesi Karl von Baer (1825): Modern embriyolojinin babası olarak da kabul edilir. Köpek ovaryumu ve ovositleri üzerine ilk ciddi çalışmaları yapmıştır. Walter
İN VİTRO EMBRİYO ÜRETİMİ İn vitro döllemenin tarihçesi Karl von Baer (1825): Modern embriyolojinin babası olarak da kabul edilir. Köpek ovaryumu ve ovositleri üzerine ilk ciddi çalışmaları yapmıştır. Walter
FERTİLİZASYON-Döllenme
 FERTİLİZASYON-Döllenme Tanım Spermatozoon ile Oosit II nin birleşerek yeni bir canlı olan ZİGOT u şekillendirmesi Ovulasyonla yumurta yoluna atılan Oosit korona radiata hücreleri ile sarılıdır. - Oosit
FERTİLİZASYON-Döllenme Tanım Spermatozoon ile Oosit II nin birleşerek yeni bir canlı olan ZİGOT u şekillendirmesi Ovulasyonla yumurta yoluna atılan Oosit korona radiata hücreleri ile sarılıdır. - Oosit
Sığrlarda Embryo Transferi. Prof.Dr.Serhat Pabuccuoğlu
 Sığrlarda Embryo Transferi Prof.Dr.Serhat Pabuccuoğlu BİYOTEKNOLOJİ NEDİR? Canlılar aracılığı ile ürün ve hizmet üretmektir Reprodüktif Biyoteknolojinin Amacı Canlılarda in vivo ve in vitro koşullarda
Sığrlarda Embryo Transferi Prof.Dr.Serhat Pabuccuoğlu BİYOTEKNOLOJİ NEDİR? Canlılar aracılığı ile ürün ve hizmet üretmektir Reprodüktif Biyoteknolojinin Amacı Canlılarda in vivo ve in vitro koşullarda
DİŞİ EŞEY HÜCRELERİNİN GELİŞMESİ OLGUNLAŞMASI. Doç. Dr. A. Gürol BAYRAKTAROĞLU
 DİŞİ EŞEY HÜCRELERİNİN GELİŞMESİ OLGUNLAŞMASI Doç. Dr. A. Gürol BAYRAKTAROĞLU OVOGENEZİS Dişi eşey hücresinin gelişip olgunlaşmasına ovogenezis denir. Spermatogenezisteki gibi çoğalma, büyüme ve olgunlaşma
DİŞİ EŞEY HÜCRELERİNİN GELİŞMESİ OLGUNLAŞMASI Doç. Dr. A. Gürol BAYRAKTAROĞLU OVOGENEZİS Dişi eşey hücresinin gelişip olgunlaşmasına ovogenezis denir. Spermatogenezisteki gibi çoğalma, büyüme ve olgunlaşma
Çiftlik Hayvanlarında Embriyo Aktarımı. Prof Dr Fatin Cedden
 Çiftlik Hayvanlarında Embriyo Aktarımı Prof Dr Fatin Cedden İlk embriyo transferi 1890 da Walter Heape tarafından Büyük Britanya da tavşan üzerinde gerçekleştirildi Sığırda yapılan ilk embriyo transferi
Çiftlik Hayvanlarında Embriyo Aktarımı Prof Dr Fatin Cedden İlk embriyo transferi 1890 da Walter Heape tarafından Büyük Britanya da tavşan üzerinde gerçekleştirildi Sığırda yapılan ilk embriyo transferi
In vitro Embryo Production and Transfer in Cattle. Numan AKYOL* Sedat Hamdi KIZIL* Tahir KARAŞAHİN*
 Lalahan İN VİTRO Hay. SIĞIR Araşt. EMBRİYOSU Enst. Derg. ÜRETİM 2007, 47 VE (1) TRANSFERİ 1-8 İN VİTRO SIĞIR EMBRİYOSU ÜRETİM VE TRANSFERİ In vitro Embryo Production and Transfer in Cattle Numan AKYOL*
Lalahan İN VİTRO Hay. SIĞIR Araşt. EMBRİYOSU Enst. Derg. ÜRETİM 2007, 47 VE (1) TRANSFERİ 1-8 İN VİTRO SIĞIR EMBRİYOSU ÜRETİM VE TRANSFERİ In vitro Embryo Production and Transfer in Cattle Numan AKYOL*
YUMURTA TİPLERİ BÖLÜNME ŞEKİLLERİ İNVİTRO FERTİLİZASYON VE EMBRİYO NAKLİ. Doç. Dr. Alev Gürol BAYRAKTAROĞLU
 YUMURTA TİPLERİ BÖLÜNME ŞEKİLLERİ İNVİTRO FERTİLİZASYON VE EMBRİYO NAKLİ Doç. Dr. Alev Gürol BAYRAKTAROĞLU Yumurta tipleri : Çeşitli hayvan yumurtaları, taşıdıkları lecithus (vitellus) maddesinin azlığına
YUMURTA TİPLERİ BÖLÜNME ŞEKİLLERİ İNVİTRO FERTİLİZASYON VE EMBRİYO NAKLİ Doç. Dr. Alev Gürol BAYRAKTAROĞLU Yumurta tipleri : Çeşitli hayvan yumurtaları, taşıdıkları lecithus (vitellus) maddesinin azlığına
Fertilizasyon ve Erken Embriyogenez
 Fertilizasyon ve Erken Embriyogenez Prof.Dr. Alp Can Histoloji-Embriyoloji ABD Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim] Tanımsal (deskriptif embriyoloji) Gelişim mekanizmaları İnsanın
Fertilizasyon ve Erken Embriyogenez Prof.Dr. Alp Can Histoloji-Embriyoloji ABD Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim] Tanımsal (deskriptif embriyoloji) Gelişim mekanizmaları İnsanın
ÇOK HÜCRELİ ORGANİZMALARIN GELİŞİMİ
 ÇOK HÜCRELİ ORGANİZMALARIN GELİŞİMİ Seçici gen ifadesi embriyonun gelişmesini sağlayan 4 temel işlevi denetler: 1. Hücre çoğalması 2. Hücre farklılaşması 3. Hücre etkileşimleri 4. Hücre hareketi HÜCRE
ÇOK HÜCRELİ ORGANİZMALARIN GELİŞİMİ Seçici gen ifadesi embriyonun gelişmesini sağlayan 4 temel işlevi denetler: 1. Hücre çoğalması 2. Hücre farklılaşması 3. Hücre etkileşimleri 4. Hücre hareketi HÜCRE
Genital siklus Pubertaya ulaşan bir dişide, hipotalamus ve hipofiz bezinin kontrolü altında ovaryum ve uterusta bazı değişiklikler meydana gelir.
 Genital siklus Pubertaya ulaşan bir dişide, hipotalamus ve hipofiz bezinin kontrolü altında ovaryum ve uterusta bazı değişiklikler meydana gelir. Ovaryumda meydana gelen değişiklikler ovogenezis ve ovulasyon
Genital siklus Pubertaya ulaşan bir dişide, hipotalamus ve hipofiz bezinin kontrolü altında ovaryum ve uterusta bazı değişiklikler meydana gelir. Ovaryumda meydana gelen değişiklikler ovogenezis ve ovulasyon
Sığır oositlerinin in vitro maturasyonuna follikül uyarıcı hormon ve insan menopozal gonadotropininin etkisi*
 Ankara Üniv Vet Fak Derg, 53, 25-29, 2006 Sığır oositlerinin in vitro maturasyonuna follikül uyarıcı hormon ve insan menopozal gonadotropininin etkisi* Hasan Ceyhun MACUN 1, Mustafa KAYMAZ 2 1 Kırıkkale
Ankara Üniv Vet Fak Derg, 53, 25-29, 2006 Sığır oositlerinin in vitro maturasyonuna follikül uyarıcı hormon ve insan menopozal gonadotropininin etkisi* Hasan Ceyhun MACUN 1, Mustafa KAYMAZ 2 1 Kırıkkale
Prof Dr Bülent GÜLEKLİ Dokuz Eylül Üniversitesi Tıp Fakültesi Kadın Hastalıkları ve Doğum ABD Reprodüktif Endokrinoloji Bilim Dalı Öğretim Üyesi
 Üreme Tıbbı Derneği ve TJOD Ankara Şubesi Ortak Eğitim Toplantısı HER YÖNÜYLE PCOS 24 Şubat 2013 Prof Dr Bülent GÜLEKLİ Dokuz Eylül Üniversitesi Tıp Fakültesi Kadın Hastalıkları ve Doğum ABD Reprodüktif
Üreme Tıbbı Derneği ve TJOD Ankara Şubesi Ortak Eğitim Toplantısı HER YÖNÜYLE PCOS 24 Şubat 2013 Prof Dr Bülent GÜLEKLİ Dokuz Eylül Üniversitesi Tıp Fakültesi Kadın Hastalıkları ve Doğum ABD Reprodüktif
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İNTRASTOPLAZMİK SPERM ENJEKSİYONU (İCSİ) YAPILAN SIĞIR OOSİTLERİNDE KALSİYUM İYONOF
 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İNTRASTOPLAZMİK SPERM ENJEKSİYONU (İCSİ) YAPILAN SIĞIR OOSİTLERİNDE KALSİYUM İYONOFOR, 6-DİMETİLAMİNOPURİN ve ETANOLÜN EMBRYO GELİŞİMİNE
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İNTRASTOPLAZMİK SPERM ENJEKSİYONU (İCSİ) YAPILAN SIĞIR OOSİTLERİNDE KALSİYUM İYONOFOR, 6-DİMETİLAMİNOPURİN ve ETANOLÜN EMBRYO GELİŞİMİNE
DOKUZ EYLÜL ÜNİVERSİTESİ
 3/0/016 00:00:00 Döner Sermaye İşletmesi Teklif No 016130 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 6/0/016 TARİHİ, SAAT
3/0/016 00:00:00 Döner Sermaye İşletmesi Teklif No 016130 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 6/0/016 TARİHİ, SAAT
ÜREME SİSTEMİ FİZYOLOJİSİ DOÇ.DR.MİTAT KOZ
 ÜREME SİSTEMİ FİZYOLOJİSİ DOÇ.DR.MİTAT KOZ Kadın ve erkek üreme sistemi dölün üretilmesi amacı ile özelleşmiş özel organlardan oluşmaktadır. Bazı üreme organları cinsiyet hücrelerini üretir, diğerleri
ÜREME SİSTEMİ FİZYOLOJİSİ DOÇ.DR.MİTAT KOZ Kadın ve erkek üreme sistemi dölün üretilmesi amacı ile özelleşmiş özel organlardan oluşmaktadır. Bazı üreme organları cinsiyet hücrelerini üretir, diğerleri
Transgenik Hayvan Üretimi. Hayvancılıkta biyoteknoloji dersi
 Transgenik Hayvan Üretimi Hayvancılıkta biyoteknoloji dersi TRANSGENİK HAYVAN TEKNOLOJİSİ Transgenik hayvanlar gen transferi yoluyla hücrelerinde yabancı genleri taşıyan hayvanlardır. Çiftlik hayvanlarına
Transgenik Hayvan Üretimi Hayvancılıkta biyoteknoloji dersi TRANSGENİK HAYVAN TEKNOLOJİSİ Transgenik hayvanlar gen transferi yoluyla hücrelerinde yabancı genleri taşıyan hayvanlardır. Çiftlik hayvanlarına
GENEL SORU ÇÖZÜMÜ ENDOKRİN SİSTEM
 GENEL SORU ÇÖZÜMÜ ENDOKRİN SİSTEM 1) Aşağıdaki hormonlardan hangisi uterusun büyümesinde doğrudan etkilidir? A) LH B) Androjen C) Östrojen Progesteron D) FUH Büyüme hormonu E) Prolaktin - Testosteron 2)
GENEL SORU ÇÖZÜMÜ ENDOKRİN SİSTEM 1) Aşağıdaki hormonlardan hangisi uterusun büyümesinde doğrudan etkilidir? A) LH B) Androjen C) Östrojen Progesteron D) FUH Büyüme hormonu E) Prolaktin - Testosteron 2)
GENİTAL SİKLUS Östrus Siklusu
 GENİTAL SİKLUS Östrus Siklusu Tanım Purbertiye ulaşan bir dişide hormonların kontrolü (hipotalamus, hipofiz ve ovaryum dan salınan) altında ovaryum ve uterusta meydana gelen değişiklikler Genital siklus
GENİTAL SİKLUS Östrus Siklusu Tanım Purbertiye ulaşan bir dişide hormonların kontrolü (hipotalamus, hipofiz ve ovaryum dan salınan) altında ovaryum ve uterusta meydana gelen değişiklikler Genital siklus
Seksüel Siklus ve Suni Tohumlama
 Seksüel Siklus ve Suni Tohumlama Siklus: Belli aralıklarla aynı biçimde yinelenen olayları kapsayan dönem; hormonların etkisiyle üreme organlarının belirli dönemlerde gösterdigi degişim, döngü. Siklik
Seksüel Siklus ve Suni Tohumlama Siklus: Belli aralıklarla aynı biçimde yinelenen olayları kapsayan dönem; hormonların etkisiyle üreme organlarının belirli dönemlerde gösterdigi degişim, döngü. Siklik
10. SINIF KONU ANLATIMI. 16 ÜREME BÜYÜME GELİŞME Döllenme ve Aile Planlaması Soru Çözümü
 10. SINIF KONU ANLATIMI 16 ÜREME BÜYÜME GELİŞME Döllenme ve Aile Planlaması Soru Çözümü DÖLLENME Dişi üreme sistemine giren sperm hücreleri yumurta hücresinin salgıladığı FERTİLİZİN sayesinde yumurta hücresini
10. SINIF KONU ANLATIMI 16 ÜREME BÜYÜME GELİŞME Döllenme ve Aile Planlaması Soru Çözümü DÖLLENME Dişi üreme sistemine giren sperm hücreleri yumurta hücresinin salgıladığı FERTİLİZİN sayesinde yumurta hücresini
DEHİDRE KÖPEKLERDE BİKARBONATLI SODYUM KLORÜR SOLÜSYONUNUN HEMATOLOJİK VE BİYOKİMYASAL PARAMETRELERE ETKİSİ
 T.C. ADNAN MENDERES ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İÇ HASTALIKLARI ANABİLİM DALI VİH-YL 2007 0002 DEHİDRE KÖPEKLERDE BİKARBONATLI SODYUM KLORÜR SOLÜSYONUNUN HEMATOLOJİK VE BİYOKİMYASAL PARAMETRELERE
T.C. ADNAN MENDERES ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İÇ HASTALIKLARI ANABİLİM DALI VİH-YL 2007 0002 DEHİDRE KÖPEKLERDE BİKARBONATLI SODYUM KLORÜR SOLÜSYONUNUN HEMATOLOJİK VE BİYOKİMYASAL PARAMETRELERE
Giriş Fertilizasyon Pre-Embriyogenez
 Giriş Fertilizasyon Pre-Embriyogenez Prof.Dr. Alp Can Histoloji-Embriyoloji Anabilim Dalı Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim] İnsanın gelişimindeki yapı-işlev ilişkisi Tanımsal (deskriptif
Giriş Fertilizasyon Pre-Embriyogenez Prof.Dr. Alp Can Histoloji-Embriyoloji Anabilim Dalı Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim] İnsanın gelişimindeki yapı-işlev ilişkisi Tanımsal (deskriptif
ENDOKRİN BEZ EKZOKRİN BEZ. Tiroid bezi. Deri. Hormon salgısı. Endokrin hücreler Kanal. Kan akımı. Ter bezi. Ekzokrin hücreler
 ENDOKRİN SİSTEM Endokrin sistem, sinir sistemiyle işbirliği içinde çalışarak vücut fonksiyonlarını kontrol eder ve vücudumuzun farklı bölümleri arasında iletişim sağlar. 1 ENDOKRİN BEZ Tiroid bezi EKZOKRİN
ENDOKRİN SİSTEM Endokrin sistem, sinir sistemiyle işbirliği içinde çalışarak vücut fonksiyonlarını kontrol eder ve vücudumuzun farklı bölümleri arasında iletişim sağlar. 1 ENDOKRİN BEZ Tiroid bezi EKZOKRİN
S r Oositlerinin n Vitro Maturasyonunda Kullan lan Vasat Katk lar
 Bülent POLAT 1 M. R fat SALMANO LU 2 S r Oositlerinin n Vitro Maturasyonunda Kullan lan Vasat Katk lar Özet Bu makalede s r oositlerinin in vitro maturasyonunda kullan lan vasat katk lar hakk nda bilgi
Bülent POLAT 1 M. R fat SALMANO LU 2 S r Oositlerinin n Vitro Maturasyonunda Kullan lan Vasat Katk lar Özet Bu makalede s r oositlerinin in vitro maturasyonunda kullan lan vasat katk lar hakk nda bilgi
Prof Dr Bulent GULEKLI Dokuz Eylul Universitesi Tıp Fakültesi Kadın Hast ve Doğum Anabilim Dalı ve Üreme Endokrinolojis Bilim dalı Izmir
 Prof Dr Bulent GULEKLI Dokuz Eylul Universitesi Tıp Fakültesi Kadın Hast ve Doğum Anabilim Dalı ve Üreme Endokrinolojis Bilim dalı Izmir ART için ovarian stimulasyonu ve ovulasyon indüksiyonundaki problemler
Prof Dr Bulent GULEKLI Dokuz Eylul Universitesi Tıp Fakültesi Kadın Hast ve Doğum Anabilim Dalı ve Üreme Endokrinolojis Bilim dalı Izmir ART için ovarian stimulasyonu ve ovulasyon indüksiyonundaki problemler
HÜCRE SĠNYAL OLAYLARI PROF. DR. FATMA SAVRAN OĞUZ
 HÜCRE SĠNYAL OLAYLARI PROF. DR. FATMA SAVRAN OĞUZ Çok hücreli organizmaların kompleks omurgalılara evrimi, hücreler birbirleriyle iletişim kuramasalardı mümkün olmazdı. Hücre-hücre Hücre-matriks etkileşimini
HÜCRE SĠNYAL OLAYLARI PROF. DR. FATMA SAVRAN OĞUZ Çok hücreli organizmaların kompleks omurgalılara evrimi, hücreler birbirleriyle iletişim kuramasalardı mümkün olmazdı. Hücre-hücre Hücre-matriks etkileşimini
YGS YE HAZIRLIK DENEMESi #5
 YGS YE HAZIRLIK DENEMESi #5 Miktar 1) I.Hemoglobinin yapısındaki karbon atomu sayısını tespit etmek II. Solunumda kullanılacak gazların hangi molekülle taşınacağını tespit etmek III. Kanın ph ını tespit
YGS YE HAZIRLIK DENEMESi #5 Miktar 1) I.Hemoglobinin yapısındaki karbon atomu sayısını tespit etmek II. Solunumda kullanılacak gazların hangi molekülle taşınacağını tespit etmek III. Kanın ph ını tespit
DİŞİ ÜREME ORGANLARI
 DİŞİ ÜREME ORGANLARI Dişi üreme organları dişi gamet hücresi ovumu (yumurtayı) üreten ovaryumlar ile ovumun döllendiği, döllenme sonrasında gebeliğin şekillendiği ve gelişen yavrunun dışarı çıkarıldığı
DİŞİ ÜREME ORGANLARI Dişi üreme organları dişi gamet hücresi ovumu (yumurtayı) üreten ovaryumlar ile ovumun döllendiği, döllenme sonrasında gebeliğin şekillendiği ve gelişen yavrunun dışarı çıkarıldığı
ÜNİTE 7 FERTİLİZASYON VE ZİGOTUN OLUŞUMU
 ÜNİTE 7 FERTİLİZASYON VE ZİGOTUN OLUŞUMU Prof. Dr. Süleyman KAPLAN 7.1. Fertilizasyondan Hemen Önce Gametlerin Durumu Erkek cinsiyet hücresi olan sperm fertilizasyondan önce sitoplâzmasının çoğunu kaybederek
ÜNİTE 7 FERTİLİZASYON VE ZİGOTUN OLUŞUMU Prof. Dr. Süleyman KAPLAN 7.1. Fertilizasyondan Hemen Önce Gametlerin Durumu Erkek cinsiyet hücresi olan sperm fertilizasyondan önce sitoplâzmasının çoğunu kaybederek
DOKUZ EYLÜL ÜNİVERSİTESİ
 07/02/2019 00:00:00 Döner Sermaye İşletmesi Teklif No: 2019832 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 11/02/2019 TARİHİ,
07/02/2019 00:00:00 Döner Sermaye İşletmesi Teklif No: 2019832 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 11/02/2019 TARİHİ,
ENDOMETRİAL KO-KÜLTÜRÜN BAŞARILI OLARAK ETKİLEDİĞİ HASTA TOPLULUĞU KİMLERDİR?
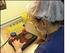 ENDOMETRİAL KO-KÜLTÜRÜN BAŞARILI OLARAK ETKİLEDİĞİ HASTA TOPLULUĞU KİMLERDİR? Bio. Semra Sertyel ALMAN HASTANESİ IVF LABORATUARLARI YÜT de başarıyı etkileyen faktörler Kadın yaşı Erkek Faktörü Uygun olmayan
ENDOMETRİAL KO-KÜLTÜRÜN BAŞARILI OLARAK ETKİLEDİĞİ HASTA TOPLULUĞU KİMLERDİR? Bio. Semra Sertyel ALMAN HASTANESİ IVF LABORATUARLARI YÜT de başarıyı etkileyen faktörler Kadın yaşı Erkek Faktörü Uygun olmayan
DOKUZ EYLÜL ÜNİVERSİTESİ
 03/0/016 00:00:00 Döner Sermaye İşletmesi Teklif No 016835 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 08/0/016 TARİHİ, SAAT
03/0/016 00:00:00 Döner Sermaye İşletmesi Teklif No 016835 İLAN HASTANEMİZİN İHTİYACI OLAN AŞAĞIDA YAZILI MALZEME(LER) TEKLİF ALMA SURETİYLE SATIN ALINACAKTIR. İLGİLENEN FİRMALARIN 08/0/016 TARİHİ, SAAT
YGS YE HAZIRLIK DENEMESi #13
 YGS YE HAZIRLIK DENEMESi #13 1) Canlılarda özelliklerin genlerle kontrol edildiği ve her genin en az bir özellikten sorumlu olduğu bilindiğine göre, I. Diploid canlılarda her özellik için iki gen bulunması
YGS YE HAZIRLIK DENEMESi #13 1) Canlılarda özelliklerin genlerle kontrol edildiği ve her genin en az bir özellikten sorumlu olduğu bilindiğine göre, I. Diploid canlılarda her özellik için iki gen bulunması
Farklı büyüklüklerdeki sığır oositlerinin maturasyonu üzerine insülin benzeri büyüme faktörü- 1 in (IGF-1) etkisi*
 Farklı büyüklüklerdeki sığır oositlerinin maturasyonu üzerine insülin benzeri büyüme faktörü- 1 in (IGF-1) etkisi* Duygu Burcu TOPUZOĞLU** Öz: Bu çalışmanın amacı farklı büyüklüklerdeki oositlerin maturasyonu
Farklı büyüklüklerdeki sığır oositlerinin maturasyonu üzerine insülin benzeri büyüme faktörü- 1 in (IGF-1) etkisi* Duygu Burcu TOPUZOĞLU** Öz: Bu çalışmanın amacı farklı büyüklüklerdeki oositlerin maturasyonu
MİTOZ ÇALIŞMA KÂĞIDI A. Aşağıdaki resimli bulmacayı çözünüz.
 MİTOZ ÇALIŞMA KÂĞIDI A. Aşağıdaki resimli bulmacayı çözünüz. B. Numaralandırılmış evrelerle ilgili aşağıdaki cümlelerde ifadeyi doğru tamamlayan koyu renkli ifadeyi yuvarlak içine alınız. 2. / 5. resimde
MİTOZ ÇALIŞMA KÂĞIDI A. Aşağıdaki resimli bulmacayı çözünüz. B. Numaralandırılmış evrelerle ilgili aşağıdaki cümlelerde ifadeyi doğru tamamlayan koyu renkli ifadeyi yuvarlak içine alınız. 2. / 5. resimde
P U B E R TA S, SUNİ T O H U M L A M A, G E B E L İ K V E T E R İ N E R HEKİ M : A H M E T K E S K İ N
 S I Ğ I R L A R D A P U B E R TA S, SUNİ T O H U M L A M A, G E B E L İ K V E D O Ğ U M V E T E R İ N E R HEKİ M : A H M E T K E S K İ N PUBERTAS Üreme yeteneğinin elde edilme olgusudur. Pubertas İlk kızgınlık
S I Ğ I R L A R D A P U B E R TA S, SUNİ T O H U M L A M A, G E B E L İ K V E D O Ğ U M V E T E R İ N E R HEKİ M : A H M E T K E S K İ N PUBERTAS Üreme yeteneğinin elde edilme olgusudur. Pubertas İlk kızgınlık
LYS ANAHTAR SORULAR #6. Mitoz ve Mayoz Bölünme Eşeyli ve Eşeysiz Üreme İnsanda Üreme
 LYS ANAHTAR SORULAR #6 Mitoz ve Mayoz Bölünme Eşeyli ve Eşeysiz Üreme İnsanda Üreme 1) 2n = 40 kromozomlu memeli türünde, Dişinin ovaryumlarında yumurta hücresi oluşurken anafaz I evresinde gonozomların
LYS ANAHTAR SORULAR #6 Mitoz ve Mayoz Bölünme Eşeyli ve Eşeysiz Üreme İnsanda Üreme 1) 2n = 40 kromozomlu memeli türünde, Dişinin ovaryumlarında yumurta hücresi oluşurken anafaz I evresinde gonozomların
T.C. ADNAN MENDERES ÜNĐVERSĐTESĐ SAĞLIK BĐLĐMLERĐ ENSTĐTÜSÜ MÜDÜRLÜĞÜNE AYDIN
 T.C. ADNAN MENDERES ÜNĐVERSĐTESĐ SAĞLIK BĐLĐMLERĐ ENSTĐTÜSÜ MÜDÜRLÜĞÜNE AYDIN Veteriner Doğum ve Jinekoloji Anabilim Dalı Yüksek Lisans Programı öğrencisi Vet. Hek. Ziver ÜSTÜN tarafından hazırlanan Sıcak
T.C. ADNAN MENDERES ÜNĐVERSĐTESĐ SAĞLIK BĐLĐMLERĐ ENSTĐTÜSÜ MÜDÜRLÜĞÜNE AYDIN Veteriner Doğum ve Jinekoloji Anabilim Dalı Yüksek Lisans Programı öğrencisi Vet. Hek. Ziver ÜSTÜN tarafından hazırlanan Sıcak
HÜCRE BÖLÜNMESİ VE ÜREME. Mitoz Bölünme ve Eşeysiz Üreme 1
 HÜCRE BÖLÜNMESİ VE ÜREME Mitoz Bölünme ve Eşeysiz Üreme 1 Hücrenin bölünmeye başlamasından itibaren onu takip eden diğer hücre bölünmesine kadar geçen zaman aralığına hücre döngüsü denir. Hücreler belli
HÜCRE BÖLÜNMESİ VE ÜREME Mitoz Bölünme ve Eşeysiz Üreme 1 Hücrenin bölünmeye başlamasından itibaren onu takip eden diğer hücre bölünmesine kadar geçen zaman aralığına hücre döngüsü denir. Hücreler belli
Gonadlar: Dişide ovaryumlar (yumurtalıklar), erkekte de testislerdir. Gametler: Yeni bir canlının gelişmesini başlatmak için bir araya gelen dişi ve
 Gonadlar: Dişide ovaryumlar (yumurtalıklar), erkekte de testislerdir. Gametler: Yeni bir canlının gelişmesini başlatmak için bir araya gelen dişi ve erkek cinsiyet hücreleridir. Gametogenezis: Dişi ve
Gonadlar: Dişide ovaryumlar (yumurtalıklar), erkekte de testislerdir. Gametler: Yeni bir canlının gelişmesini başlatmak için bir araya gelen dişi ve erkek cinsiyet hücreleridir. Gametogenezis: Dişi ve
Çiftlik Hayvanlarında Cinsiyetin Denetimi
 Çiftlik Hayvanlarında Cinsiyetin Denetimi Cinsiyetin belirlenmesi Demokritus (MÖ: 470-402) Sağ testisten erkek, sol testisten dişi yavruların dünyaya geldiğini ileri sürmüştür. Fötal yaşamda cinsiyetin
Çiftlik Hayvanlarında Cinsiyetin Denetimi Cinsiyetin belirlenmesi Demokritus (MÖ: 470-402) Sağ testisten erkek, sol testisten dişi yavruların dünyaya geldiğini ileri sürmüştür. Fötal yaşamda cinsiyetin
İnfertil Dişiler. Çiftleşme zorlukları. Deneyimsiz erkek. Normal çiftleşmeden sonra başarısız gebelik. Seyrek östrus. Deneyimsiz dişi.
 İnfertil Dişiler Çiftleşme zorlukları Deneyimsiz erkek Deneyimsiz dişi Erkekte fizyolojik problemler Dişide Dişinin hazır olmaması Vulval stenosis Vestibuler konstrüksiyon Vaginal Vaginal hiperplazi ya
İnfertil Dişiler Çiftleşme zorlukları Deneyimsiz erkek Deneyimsiz dişi Erkekte fizyolojik problemler Dişide Dişinin hazır olmaması Vulval stenosis Vestibuler konstrüksiyon Vaginal Vaginal hiperplazi ya
İN-VİTRO FERTİLİZASYON (IVF) VE EMBRİYO TRANSFERİ (ET)
 İN-VİTRO FERTİLİZASYON (IVF) VE EMBRİYO TRANSFERİ (ET) Yardımcı üreme tekniklerinin (YÜT) (Assisted Reproduction Techniques, ART) temel amacı, infertil çiftin sağlıklı bir bebek sahibi olmasıdır. IVF-ET
İN-VİTRO FERTİLİZASYON (IVF) VE EMBRİYO TRANSFERİ (ET) Yardımcı üreme tekniklerinin (YÜT) (Assisted Reproduction Techniques, ART) temel amacı, infertil çiftin sağlıklı bir bebek sahibi olmasıdır. IVF-ET
Spermatozoanın Dişi Genital Kanalındaki Hareketi. Üreme Biyolojisi ve Yapay Tohumlama Prof. Dr. Fatin CEDDEN
 Spermatozoanın Dişi Genital Kanalındaki Hareketi Üreme Biyolojisi ve Yapay Tohumlama Prof. Dr. Fatin CEDDEN Döllenme Sperm hücresinin ovuma girip kaynaşması olayına (fekondasyon) Döllenme denir. Bu olgu
Spermatozoanın Dişi Genital Kanalındaki Hareketi Üreme Biyolojisi ve Yapay Tohumlama Prof. Dr. Fatin CEDDEN Döllenme Sperm hücresinin ovuma girip kaynaşması olayına (fekondasyon) Döllenme denir. Bu olgu
Şekil 1. Mitoz bölünmenin profaz evresi.
 KONU 9. HÜCRE BÖLÜNMESİ MİTOZ BÖLÜNME Mitoz bölünme tek hücreli canlılardan, çok hücreli canlılara ve insana kadar birçok canlı grubu tarafından gerçekleştirilebilir. Mitoz bölünme sonunda bölünen hücrelerden
KONU 9. HÜCRE BÖLÜNMESİ MİTOZ BÖLÜNME Mitoz bölünme tek hücreli canlılardan, çok hücreli canlılara ve insana kadar birçok canlı grubu tarafından gerçekleştirilebilir. Mitoz bölünme sonunda bölünen hücrelerden
Hücre. 1 µm = 0,001 mm (1000 µm = 1 mm)!
 HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
Oosit Olgunlaşma Süreci ve Düzenleyici Faktörler
 ARŞİV 2009; 18: 227 Oosit Olgunlaşma Süreci ve Düzenleyici Faktörler Arş.Gör.Dr. Yurdun KUYUCU Prof.Dr. Özgül TAP OOGENEZİS Gametogenezis, özelleşmiş üreme hücreleri olan gametlerin oluşum ve gelişme sürecidir.
ARŞİV 2009; 18: 227 Oosit Olgunlaşma Süreci ve Düzenleyici Faktörler Arş.Gör.Dr. Yurdun KUYUCU Prof.Dr. Özgül TAP OOGENEZİS Gametogenezis, özelleşmiş üreme hücreleri olan gametlerin oluşum ve gelişme sürecidir.
Reprodüktif Endokrinoloji. Prof. Dr. Mithat EVECEN
 Reprodüktif Endokrinoloji Prof. Dr. Mithat EVECEN HORMON Kelime: Yun. Uyarma, Canlandırma, Harekete geçirme. Tanım: Bir hücre ya da dokuda sentezlenen ve buralardan kan, lenf ve ya sinir yoluyla vücudun
Reprodüktif Endokrinoloji Prof. Dr. Mithat EVECEN HORMON Kelime: Yun. Uyarma, Canlandırma, Harekete geçirme. Tanım: Bir hücre ya da dokuda sentezlenen ve buralardan kan, lenf ve ya sinir yoluyla vücudun
HÜCRENİN YAŞAM DÖNGÜSÜ
 HÜCRENİN YAŞAM DÖNGÜSÜ *Hücrenin yaşam döngüsü: Hücrenin; bir bölünme sonundan, ikinci bir bölünme sonuna kadar olan zaman sürecinde; geçirdiği yaşamsal olaylara hücrenin yaşam döngüsü denir. Hücreler,
HÜCRENİN YAŞAM DÖNGÜSÜ *Hücrenin yaşam döngüsü: Hücrenin; bir bölünme sonundan, ikinci bir bölünme sonuna kadar olan zaman sürecinde; geçirdiği yaşamsal olaylara hücrenin yaşam döngüsü denir. Hücreler,
Adolesanlarda Polikistik Over Sendromu tanısında Anti Müllerien Hormon (AMH) ve İnsülin Like Peptit -3 (INSL3) ün tanısal değeri
 Adolesanlarda Polikistik Over Sendromu tanısında Anti Müllerien Hormon (AMH) ve İnsülin Like Peptit -3 (INSL3) ün tanısal değeri Ayça Kömürlüoğlu 1, E. Nazlı Gönç 2, Z. Alev Özön 2, Nurgün Kandemir 2,
Adolesanlarda Polikistik Over Sendromu tanısında Anti Müllerien Hormon (AMH) ve İnsülin Like Peptit -3 (INSL3) ün tanısal değeri Ayça Kömürlüoğlu 1, E. Nazlı Gönç 2, Z. Alev Özön 2, Nurgün Kandemir 2,
KLONLAMA. Prof. Dr. Fatma Savran Oğuz
 KLONLAMA Prof. Dr. Fatma Savran Oğuz Tek yumurta ikizleri doğal klonlardır. Araştırıcılar ilk önceleri bu doğal olayı taklit ederek klonlama çalışmalarına başlamışlardır. Tek yumurta ikizlerinde embriyo
KLONLAMA Prof. Dr. Fatma Savran Oğuz Tek yumurta ikizleri doğal klonlardır. Araştırıcılar ilk önceleri bu doğal olayı taklit ederek klonlama çalışmalarına başlamışlardır. Tek yumurta ikizlerinde embriyo
BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2
 İÇİNDEKİLER Sayfa BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2 CANLILARIN OLUŞUMU... 5 CANLILARIN ORTAK ÖZELLİKLERİ... 9 CANLILARIN SINIFLANDIRILMASI... 11 SİSTEMATİK... 13 BİTKİ VE HAYVANLARIN
İÇİNDEKİLER Sayfa BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2 CANLILARIN OLUŞUMU... 5 CANLILARIN ORTAK ÖZELLİKLERİ... 9 CANLILARIN SINIFLANDIRILMASI... 11 SİSTEMATİK... 13 BİTKİ VE HAYVANLARIN
İneklerde Üremenin Kontrolü Embriyo Transferi
 İneklerde Üremenin Kontrolü Embriyo Transferi PROF.DR.SERHAT PABUCCUOĞLU 28.10.2013 İNEKLERDE ÜREMENİN KONTROLÜ EMBRİYO TRANSFERİ 1 Konu Başlıkları İneklerde Üremenin kontrolü Başarıyı etkileyen faktörler
İneklerde Üremenin Kontrolü Embriyo Transferi PROF.DR.SERHAT PABUCCUOĞLU 28.10.2013 İNEKLERDE ÜREMENİN KONTROLÜ EMBRİYO TRANSFERİ 1 Konu Başlıkları İneklerde Üremenin kontrolü Başarıyı etkileyen faktörler
Türk Tarım - Gıda Bilim ve Teknoloji Dergisi
 Türk Tarım Gıda Bilim ve Teknoloji Dergisi, 3(7): 510-514, 2015 Türk Tarım - Gıda Bilim ve Teknoloji Dergisi www.agrifoodscience.com Türk Bilim ve Teknolojisi Folikül Büyüklüğü ve Folikül Uyarıcı Hormon
Türk Tarım Gıda Bilim ve Teknoloji Dergisi, 3(7): 510-514, 2015 Türk Tarım - Gıda Bilim ve Teknoloji Dergisi www.agrifoodscience.com Türk Bilim ve Teknolojisi Folikül Büyüklüğü ve Folikül Uyarıcı Hormon
BESİN MADDELERİNİN KSİLEM VE FLOEMDE UZUN MESAFE
 BESİN MADDELERİNİN KSİLEM VE FLOEMDE UZUN MESAFE TAŞINIMI Su, mineral elementler ve küçük molekül ağırlıklı organik bileşiklerin bitkilerde uzun mesafe taşınımları ksilem ve floemde gerçekleşir. Ksilemde
BESİN MADDELERİNİN KSİLEM VE FLOEMDE UZUN MESAFE TAŞINIMI Su, mineral elementler ve küçük molekül ağırlıklı organik bileşiklerin bitkilerde uzun mesafe taşınımları ksilem ve floemde gerçekleşir. Ksilemde
İLK TRİMESTERDE PROGESTERON. Dr. Tuncay Nas Gazi Üniversitesi Kadın Hastalıkları ve Doğum Anabilim
 İLK TRİMESTERDE PROGESTERON Dr. Tuncay Nas Gazi Üniversitesi Kadın Hastalıkları ve Doğum Anabilim Progesteron Gebeliğin oluşumu ve devamında çok önemli bir hormondur Progestinler Progesteron (Progestan
İLK TRİMESTERDE PROGESTERON Dr. Tuncay Nas Gazi Üniversitesi Kadın Hastalıkları ve Doğum Anabilim Progesteron Gebeliğin oluşumu ve devamında çok önemli bir hormondur Progestinler Progesteron (Progestan
YGS YE HAZIRLIK DENEMESi #12
 YGS YE HAZIRLIK DENEMESi #12 1) İnsanda döllenme sırasında, I. Spermdeki çekirdek, sentrozomun yumurtaya geçmesi II. Spermdeki akrozomun patlayarak zona pellusidayı eritmesi III. Yumurtadaki salgı maddelerinin
YGS YE HAZIRLIK DENEMESi #12 1) İnsanda döllenme sırasında, I. Spermdeki çekirdek, sentrozomun yumurtaya geçmesi II. Spermdeki akrozomun patlayarak zona pellusidayı eritmesi III. Yumurtadaki salgı maddelerinin
Reprodüktif Endokrinoloji. Prof. Dr. Mithat EVECEN
 Reprodüktif Endokrinoloji Prof. Dr. Mithat EVECEN TANIMLAR: Hormon: Yunanca = uyarma, canlandırma, harekete geçirme. Tanım: Bir hücre ya da dokuda sentezlenen ve buralardan kan, lenf ve sinir yoluyla vücudun
Reprodüktif Endokrinoloji Prof. Dr. Mithat EVECEN TANIMLAR: Hormon: Yunanca = uyarma, canlandırma, harekete geçirme. Tanım: Bir hücre ya da dokuda sentezlenen ve buralardan kan, lenf ve sinir yoluyla vücudun
Sayfa BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2
 İÇİNDEKİLER Sayfa BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2 CANLILARIN OLUŞUMU... 6 CANLILARIN ORTAK ÖZELLİKLERİ... 11 CANLILARIN SINIFLANDIRILMASI... 13 SİSTEMATİK... 34 BİTKİ VE
İÇİNDEKİLER Sayfa BİYOLOJİ VE BİLİMSEL YÖNTEM... 1 Bilim ve Bilimsel Yöntem... 2 CANLILARIN OLUŞUMU... 6 CANLILARIN ORTAK ÖZELLİKLERİ... 11 CANLILARIN SINIFLANDIRILMASI... 13 SİSTEMATİK... 34 BİTKİ VE
ÖZET CEVAP: Oosit retrivalin hemen ardından intrauterin hcg uygulaması implantasyon oranlarını, kimyasal ve klinik gebelik oranlarını artırmaktadır.
 Intrauterine administration of hcg immediately after oocyte retrieval and the outcome of ICSI: a randomized controlled trial Oosit Retrivalden hemen sonra intrauterin hcg uygulamasının ICSI sonuçları üzerine
Intrauterine administration of hcg immediately after oocyte retrieval and the outcome of ICSI: a randomized controlled trial Oosit Retrivalden hemen sonra intrauterin hcg uygulamasının ICSI sonuçları üzerine
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN
 İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN Fertilizasyonda 46 kromozom Her bir kromozom çift kromadit-(92) Hücre bölündükten sonra her hücre de 46 kromozom bulunur Mitoz bölünme G1
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN Fertilizasyonda 46 kromozom Her bir kromozom çift kromadit-(92) Hücre bölündükten sonra her hücre de 46 kromozom bulunur Mitoz bölünme G1
Sunum planı. Hipofiz Epifiz Tiroid Paratiroid ve Pankreas hormonları
 Dr. Suat Erdoğan Sunum planı Hipofiz Epifiz Tiroid Paratiroid ve Pankreas hormonları Hipofiz bezi (hypophysis) Hipofizial çukurlukta bulunur (sella turcica) 9 adet hormon üretir İki bölümü vardır: Anterior
Dr. Suat Erdoğan Sunum planı Hipofiz Epifiz Tiroid Paratiroid ve Pankreas hormonları Hipofiz bezi (hypophysis) Hipofizial çukurlukta bulunur (sella turcica) 9 adet hormon üretir İki bölümü vardır: Anterior
Prenatal devre insan ve memeli hayvanlarda uterus içerisinde geçer. Kanatlı hayvanlarda ise yumurta içinde kuluçkada geçen devredir.
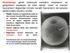 Embriyoloji, genel anlamıyla canlıların oluşmasını ve gelişmesini inceleyen bir bilim dalıdır. İnsan ve memeli hayvanların doğumdan önceki, kanatlı hayvanların ise kuluçka dönemindeki hayatını inceler.
Embriyoloji, genel anlamıyla canlıların oluşmasını ve gelişmesini inceleyen bir bilim dalıdır. İnsan ve memeli hayvanların doğumdan önceki, kanatlı hayvanların ise kuluçka dönemindeki hayatını inceler.
NUTRI -PASS. Amonyak ve çözünebilir protein bağlayıcı DAHA İYİ
 Amonyak ve çözünebilir protein bağlayıcı NUTRI -PASS DAHA İYİ Protein Kullanımı Enerji Kullanımı Süt Kalitesi Karaciğer Fonksiyonları Döl Verimi BY-PASS PROTEİN ÜRETİMİNİ VE ENERJİ ÇEVRİMİNİ ARTTIRMAK,
Amonyak ve çözünebilir protein bağlayıcı NUTRI -PASS DAHA İYİ Protein Kullanımı Enerji Kullanımı Süt Kalitesi Karaciğer Fonksiyonları Döl Verimi BY-PASS PROTEİN ÜRETİMİNİ VE ENERJİ ÇEVRİMİNİ ARTTIRMAK,
Dişi genital organları; Ovaryum,ovidukt, uterus, serviks, vagina, vulva Ovaryum; sağda ve solda karın boşluğuna asılı olarak bulunan 1 çift organdır.
 OVOGENEZİS Dişi eşey hücresinin gelişip olgunlaşmasına ovogenezis denir. Spermatogenezisteki gibi çoğalma, büyüme ve olgunlaşma evreleri vardır. Dişi üreme sistemi; ovumun üretilmesi, erkek ve dişi eşey
OVOGENEZİS Dişi eşey hücresinin gelişip olgunlaşmasına ovogenezis denir. Spermatogenezisteki gibi çoğalma, büyüme ve olgunlaşma evreleri vardır. Dişi üreme sistemi; ovumun üretilmesi, erkek ve dişi eşey
ıo. Urünün raf ömrü üretim tarihinden itibaren i yıl olmalıdır.
 12)VİTRİFİKASYON KİT TEKNİK ŞART AMESİ I. Oosit, Embryo ve Blastosistlerin Vitrifikasyon yöntemi ile dondurulması amacı ile kullaru lmalıd ır. 2. Ürün Equilihrnıion Solution - ES (white cap) i x 1 ml.
12)VİTRİFİKASYON KİT TEKNİK ŞART AMESİ I. Oosit, Embryo ve Blastosistlerin Vitrifikasyon yöntemi ile dondurulması amacı ile kullaru lmalıd ır. 2. Ürün Equilihrnıion Solution - ES (white cap) i x 1 ml.
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ
 15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
12. SINIF KONU ANLATIMI 7 GENETİK MÜHENDİSLİĞİ VE BİYOTEKNOLOJİ ÇALIŞMA ALANLARI
 12. SINIF KONU ANLATIMI 7 GENETİK MÜHENDİSLİĞİ VE BİYOTEKNOLOJİ ÇALIŞMA ALANLARI GENETİK MÜHENDİSLİĞİ Belirli bir amaca yönelik olarak genetik madde üzerinde yapılan çalışmaları içerir. Canlıların genlerine
12. SINIF KONU ANLATIMI 7 GENETİK MÜHENDİSLİĞİ VE BİYOTEKNOLOJİ ÇALIŞMA ALANLARI GENETİK MÜHENDİSLİĞİ Belirli bir amaca yönelik olarak genetik madde üzerinde yapılan çalışmaları içerir. Canlıların genlerine
CANLILARIN ORTAK ÖZELLİKLERİ
 1 CANLILARIN ORTAK ÖZELLİKLERİ 1.Hücresel yapıdan oluşur 2.Beslenir 3.Solunum yapar 4.Boşaltım yapar 5.Canlılar hareket eder 6.Çevresel uyarılara tepki gösterir 7.Büyür ve gelişir (Organizasyon) 8.Üreme
1 CANLILARIN ORTAK ÖZELLİKLERİ 1.Hücresel yapıdan oluşur 2.Beslenir 3.Solunum yapar 4.Boşaltım yapar 5.Canlılar hareket eder 6.Çevresel uyarılara tepki gösterir 7.Büyür ve gelişir (Organizasyon) 8.Üreme
Canlılarda mitoz, amitoz ve mayoz olmak üzere üç çeşit bölünme görülür.
 HÜCRE BÖLÜNMELERİ Canlılarda mitoz, amitoz ve mayoz olmak üzere üç çeşit bölünme görülür. I. MİTOZ BÖLÜNME Mitoz bölünme tek hücreli canlılardan, çok hücreli canlılara ve insana kadar bir çok canlı grubu
HÜCRE BÖLÜNMELERİ Canlılarda mitoz, amitoz ve mayoz olmak üzere üç çeşit bölünme görülür. I. MİTOZ BÖLÜNME Mitoz bölünme tek hücreli canlılardan, çok hücreli canlılara ve insana kadar bir çok canlı grubu
Giriş ve Genel Tanımlamalar Fer/lizasyon
 Dönem 1-Sunum 1/ 2016 Giriş ve Genel Tanımlamalar Fer/lizasyon Prof.Dr. Alp Can Ankara Üniversitesi Tıp Fakültesi Histoloji-Embriyoloji ABD www.alpcan.com Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim]
Dönem 1-Sunum 1/ 2016 Giriş ve Genel Tanımlamalar Fer/lizasyon Prof.Dr. Alp Can Ankara Üniversitesi Tıp Fakültesi Histoloji-Embriyoloji ABD www.alpcan.com Embriyoloji (Gelişim Bilimi) [embriyo=cenin, logos=bilim]
Mayoz Bölünmenin Oluşumu
 MAYOZ BÖLÜNME NEDİR? 03 Ocak 2012, 23:39 Osman BEDEL MAYOZ BÖLÜNME NEDİR? Kromozom sayılarının nesiller boyu sabit tutulması mayoz bölünme ile sağlanır. Mayoz özel bir hücre bölünmesidir. Bu bölünme ile
MAYOZ BÖLÜNME NEDİR? 03 Ocak 2012, 23:39 Osman BEDEL MAYOZ BÖLÜNME NEDİR? Kromozom sayılarının nesiller boyu sabit tutulması mayoz bölünme ile sağlanır. Mayoz özel bir hücre bölünmesidir. Bu bölünme ile
İNFERTİL HASTANIN HORMON DEĞERLENDİRMESİ NASIL YAPILMALIDIR? DOÇ. DR. ERCAN BAŞTU
 İNFERTİL HASTANIN HORMON DEĞERLENDİRMESİ NASIL YAPILMALIDIR? DOÇ. DR. ERCAN BAŞTU İstanbul Üniversitesi İstanbul Tıp Fakültesi Kadın Hastalıkları ve Doğum Anabilim Dalı Reprodük>f Endokrinoloji ve İnfer>lite
İNFERTİL HASTANIN HORMON DEĞERLENDİRMESİ NASIL YAPILMALIDIR? DOÇ. DR. ERCAN BAŞTU İstanbul Üniversitesi İstanbul Tıp Fakültesi Kadın Hastalıkları ve Doğum Anabilim Dalı Reprodük>f Endokrinoloji ve İnfer>lite
YAZILIYA HAZIRLIK TEST SORULARI. 10. Sınıf
 YAZILIYA HAZIRLIK TEST SORULARI 10. Sınıf 1) Hücre döngüsünün interfaz evresini yeni tamamlamış bir hücre ile bu hücrenin döngü sonunda oluşturduğu yeni hücrelerde; I. DNA miktarı II. Gen Sayısı III. Gen
YAZILIYA HAZIRLIK TEST SORULARI 10. Sınıf 1) Hücre döngüsünün interfaz evresini yeni tamamlamış bir hücre ile bu hücrenin döngü sonunda oluşturduğu yeni hücrelerde; I. DNA miktarı II. Gen Sayısı III. Gen
FARKLI KO TROLLÜ OVERYA HİPERSTİMULASYO PROTOKOLLERİ İ FOLLİKÜLOGE EZDE ROL OY AYA FOLLİKÜLER SIVI MARKIRLARI ÜZERİ E ETKİSİ. Dr. Ayşenur KAYA KAHVECİ
 TÜRKİYE CUMHURİYETİ A KARA Ü İVERSİTESİ TIP FAKÜLTESİ FARKLI KO TROLLÜ OVERYA HİPERSTİMULASYO PROTOKOLLERİ İ FOLLİKÜLOGE EZDE ROL OY AYA FOLLİKÜLER SIVI MARKIRLARI ÜZERİ E ETKİSİ Dr. Ayşenur KAYA KAHVECİ
TÜRKİYE CUMHURİYETİ A KARA Ü İVERSİTESİ TIP FAKÜLTESİ FARKLI KO TROLLÜ OVERYA HİPERSTİMULASYO PROTOKOLLERİ İ FOLLİKÜLOGE EZDE ROL OY AYA FOLLİKÜLER SIVI MARKIRLARI ÜZERİ E ETKİSİ Dr. Ayşenur KAYA KAHVECİ
2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları
 B) RADYASYON UYGULAMALARI Radyasyon = enerji yayılması 1)Elektromanyetik radyasyon. UV, X ve γ ışınları 2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları İyonizan ışınların canlı hücreler üzerine
B) RADYASYON UYGULAMALARI Radyasyon = enerji yayılması 1)Elektromanyetik radyasyon. UV, X ve γ ışınları 2)Subatomik parçacıklardan oluşan radyasyon. α, β ışınları İyonizan ışınların canlı hücreler üzerine
Sperm sıvısı ve sperm sıvısının bileşimi
 Sperm sıvısı ve sperm sıvısının bileşimi Çiftlik Hayvanlarında Üreme Biyolojisi ve Yapay Tohumlama Prof Dr Fatin CEDDEN Giriş Sperm sıvısı (semen) spermatozoa ve seminal plazmadan meydana gelir Seminal
Sperm sıvısı ve sperm sıvısının bileşimi Çiftlik Hayvanlarında Üreme Biyolojisi ve Yapay Tohumlama Prof Dr Fatin CEDDEN Giriş Sperm sıvısı (semen) spermatozoa ve seminal plazmadan meydana gelir Seminal
İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın
 İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın Hücre iletişimi Tüm canlılar bulundukları çevreden sinyal alırlar ve yanıt verirler Bakteriler glukoz ve amino asit gibi besinlerin
İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın Hücre iletişimi Tüm canlılar bulundukları çevreden sinyal alırlar ve yanıt verirler Bakteriler glukoz ve amino asit gibi besinlerin
ıı. Üretici, ithalatçı veya bavi olarak TITUBB da kayıtlı olunmalı ve kayıtlı olunduğuna
 145 MiKRON(!-lm) DENUDP.SYON pipeti TEKNiK Ş.~RTNAMESi 1. ICSI'den önce oositten kümülüs kümesini soymak, fertilizasyon kontrolü, oositin manipulasyonu. ernbr ivolar, blastokistler ve blastomerler için
145 MiKRON(!-lm) DENUDP.SYON pipeti TEKNiK Ş.~RTNAMESi 1. ICSI'den önce oositten kümülüs kümesini soymak, fertilizasyon kontrolü, oositin manipulasyonu. ernbr ivolar, blastokistler ve blastomerler için
TOPRAK TOPRAK TEKSTÜRÜ (BÜNYESİ)
 TOPRAK Toprak esas itibarı ile uzun yılların ürünü olan, kayaların ve organik maddelerin türlü çaptaki ayrışma ürünlerinden meydana gelen, içinde geniş bir canlılar âlemini barındırarak bitkilere durak
TOPRAK Toprak esas itibarı ile uzun yılların ürünü olan, kayaların ve organik maddelerin türlü çaptaki ayrışma ürünlerinden meydana gelen, içinde geniş bir canlılar âlemini barındırarak bitkilere durak
CANLILARDA ÜREME. Üreme canlıların ortak özelliğidir. Her canlının kendine benzer canlı meydana getirebilmesi üreme ile gerçekleşir
 CANLILARDA ÜREME EYLÜL 3.HAFTA MİTOZ VE EŞEYSİZ ÜREME Her canlının kendine benzer canlı meydana getirebilmesi üreme ile gerçekleşir Üreme canlıların ortak özelliğidir 3 4 Canlılar hücrelerden meydana gelir
CANLILARDA ÜREME EYLÜL 3.HAFTA MİTOZ VE EŞEYSİZ ÜREME Her canlının kendine benzer canlı meydana getirebilmesi üreme ile gerçekleşir Üreme canlıların ortak özelliğidir 3 4 Canlılar hücrelerden meydana gelir
YGS YE HAZIRLIK DENEMESi #8
 YGS YE HAZIRLIK DENEMESi #8 1) Arkebakteriler sıra dışı koşullarda bile yapısı bozulmadan kalabilen enzimlere sahiptir. Arkelere ait bu enzimler, I. Kalitesi düşük metal cevherlerinin işlenmesi, II. Zehirli
YGS YE HAZIRLIK DENEMESi #8 1) Arkebakteriler sıra dışı koşullarda bile yapısı bozulmadan kalabilen enzimlere sahiptir. Arkelere ait bu enzimler, I. Kalitesi düşük metal cevherlerinin işlenmesi, II. Zehirli
BÖLÜM I HÜCRE FİZYOLOJİSİ...
 BÖLÜM I HÜCRE FİZYOLOJİSİ... 1 Bilinmesi Gereken Kavramlar... 1 Giriş... 2 Hücrelerin Fonksiyonel Özellikleri... 2 Hücrenin Kimyasal Yapısı... 2 Hücrenin Fiziksel Yapısı... 4 Hücrenin Bileşenleri... 4
BÖLÜM I HÜCRE FİZYOLOJİSİ... 1 Bilinmesi Gereken Kavramlar... 1 Giriş... 2 Hücrelerin Fonksiyonel Özellikleri... 2 Hücrenin Kimyasal Yapısı... 2 Hücrenin Fiziksel Yapısı... 4 Hücrenin Bileşenleri... 4
Çiftlik Hayvanlarında Türlere Göre Üreme Özellikleri. Prof. Dr. Fatin CEDDEN
 Çiftlik Hayvanlarında Türlere Göre Üreme Özellikleri Prof. Dr. Fatin CEDDEN Koyunlarda Seksüel Döngü Ilıman iklim kuşağından köken alan koyunlar mevsime bağlı kızgınlık gösterirler. Günlerin kısalmaya
Çiftlik Hayvanlarında Türlere Göre Üreme Özellikleri Prof. Dr. Fatin CEDDEN Koyunlarda Seksüel Döngü Ilıman iklim kuşağından köken alan koyunlar mevsime bağlı kızgınlık gösterirler. Günlerin kısalmaya
10. SINIF KONU ANLATIMI 6 MAYOZ BÖLÜNME-3
 10. SINIF KONU ANLATIMI 6 MAYOZ BÖLÜNME-3 Mayoz Bölünmenin Genel Özellikleri Üreme ana hücrelerinde görülür. Üreme hücrelerinin oluşmasını sağlar. Sadece 2n kromozomlu hücrelerde görülür. 4 yeni hücre
10. SINIF KONU ANLATIMI 6 MAYOZ BÖLÜNME-3 Mayoz Bölünmenin Genel Özellikleri Üreme ana hücrelerinde görülür. Üreme hücrelerinin oluşmasını sağlar. Sadece 2n kromozomlu hücrelerde görülür. 4 yeni hücre
YGS YE HAZIRLIK DENEMESi #4
 YGS YE HAZIRLIK DENEMESi #4 1) Bir hücrenin X maddesini difüzyonla almakta olduğu görülmüştür. Bu hücre ve içerisinde bulunduğu ortamla ilgili, I. Ortamdaki X yoğunluğu hücreden daha fazladır. II. X in
YGS YE HAZIRLIK DENEMESi #4 1) Bir hücrenin X maddesini difüzyonla almakta olduğu görülmüştür. Bu hücre ve içerisinde bulunduğu ortamla ilgili, I. Ortamdaki X yoğunluğu hücreden daha fazladır. II. X in
Mitoz bölünme, hücredeki kalıtım maddesinin yavru hücrelere eşit miktarda bölünmesini sağlayan karmaşık bir olaydır.
 Mitoz bölünme, hücredeki kalıtım maddesinin yavru hücrelere eşit miktarda bölünmesini sağlayan karmaşık bir olaydır. Hücre mitozla bölünmeden önce DNA eşlemesi olur. Hücre mitozla bölünmeye başlamadan
Mitoz bölünme, hücredeki kalıtım maddesinin yavru hücrelere eşit miktarda bölünmesini sağlayan karmaşık bir olaydır. Hücre mitozla bölünmeden önce DNA eşlemesi olur. Hücre mitozla bölünmeye başlamadan
İndüklenmiş Pluripotent Kök Hücre
 İndüklenmiş Pluripotent Kök Hücre Kök Hücre Blastosist adı verilen hücre kümesinden alınan hücrelerin her birine embriyonik kök hücre denir. İç Hücre Kitlesi Bu hücreler pluripotensi özelliklerini koruyarak
İndüklenmiş Pluripotent Kök Hücre Kök Hücre Blastosist adı verilen hücre kümesinden alınan hücrelerin her birine embriyonik kök hücre denir. İç Hücre Kitlesi Bu hücreler pluripotensi özelliklerini koruyarak
Embriyolojiye Giriş ve Tarihçe. Prof.Dr.Murat AKKUŞ
 Embriyolojiye Giriş ve Tarihçe Prof.Dr.Murat AKKUŞ Embriyolojinin Tanımı Embriyoloji, tüm canlıların türe özgü şekillerini alıncaya kadar geçirdikleri gelişme evrelerini inceleyen bilim dalıdır Embriyoloji
Embriyolojiye Giriş ve Tarihçe Prof.Dr.Murat AKKUŞ Embriyolojinin Tanımı Embriyoloji, tüm canlıların türe özgü şekillerini alıncaya kadar geçirdikleri gelişme evrelerini inceleyen bilim dalıdır Embriyoloji
Fizyoloji. Vücut Sıvı Bölmeleri ve Özellikleri. Dr. Deniz Balcı.
 Fizyoloji Vücut Sıvı Bölmeleri ve Özellikleri Dr. Deniz Balcı deniz.balci@neu.edu.tr Ders İçeriği 1 Vücut Sıvı Bölmeleri ve Hacimleri 2 Vücut Sıvı Bileşenleri 3 Sıvıların Bölmeler Arasındaki HarekeF Okuma
Fizyoloji Vücut Sıvı Bölmeleri ve Özellikleri Dr. Deniz Balcı deniz.balci@neu.edu.tr Ders İçeriği 1 Vücut Sıvı Bölmeleri ve Hacimleri 2 Vücut Sıvı Bileşenleri 3 Sıvıların Bölmeler Arasındaki HarekeF Okuma
HÜCRELERARASI İLETİŞİM
 HÜCRELERARASI İLETİŞİM Bazı sorular!!! Bitki hücreleri ne hakkında konuşur? Bir hücre diğerine ne söyler ve diğer hücre buna nasıl cevap verir? Bu sorulara, önce mikroorganizmalar arasındaki iletişime
HÜCRELERARASI İLETİŞİM Bazı sorular!!! Bitki hücreleri ne hakkında konuşur? Bir hücre diğerine ne söyler ve diğer hücre buna nasıl cevap verir? Bu sorulara, önce mikroorganizmalar arasındaki iletişime
Embriyo Kriyoprezervasyonu
 ÜREME TIBBI VE CERRAHİSİ DERNEĞİ İnfertilite Tedavisinde Güncel Yaklaşımlar Toplantısı Ankara, 21.12.2014 Embriyo Kriyoprezervasyonu Dr. Sinan Özkavukcu Ankara Üniversitesi Tıp Fakültesi ÜYTE Merkezi Laboratuvar
ÜREME TIBBI VE CERRAHİSİ DERNEĞİ İnfertilite Tedavisinde Güncel Yaklaşımlar Toplantısı Ankara, 21.12.2014 Embriyo Kriyoprezervasyonu Dr. Sinan Özkavukcu Ankara Üniversitesi Tıp Fakültesi ÜYTE Merkezi Laboratuvar
İMMATÜR SIĞIR OOSİTLERİNİN VİTRİFİKASYON TEKNİĞİ ile ETİLEN GLİKOL ve DMSO KULLANARAK PAYETLERDE DONDURULMASI
 ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İMMATÜR SIĞIR OOSİTLERİNİN VİTRİFİKASYON TEKNİĞİ ile ETİLEN GLİKOL ve DMSO KULLANARAK PAYETLERDE DONDURULMASI Yunus ÇETİN DOĞUM VE JİNEKOLOJİ ANABİLİM DALI
ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ İMMATÜR SIĞIR OOSİTLERİNİN VİTRİFİKASYON TEKNİĞİ ile ETİLEN GLİKOL ve DMSO KULLANARAK PAYETLERDE DONDURULMASI Yunus ÇETİN DOĞUM VE JİNEKOLOJİ ANABİLİM DALI
BMM307-H02. Yrd.Doç.Dr. Ziynet PAMUK
 BMM307-H02 Yrd.Doç.Dr. Ziynet PAMUK ziynetpamuk@gmail.com 1 BİYOELEKTRİK NEDİR? Biyoelektrik, canlıların üretmiş olduğu elektriktir. Ancak bu derste anlatılacak olan insan vücudundan elektrotlar vasıtasıyla
BMM307-H02 Yrd.Doç.Dr. Ziynet PAMUK ziynetpamuk@gmail.com 1 BİYOELEKTRİK NEDİR? Biyoelektrik, canlıların üretmiş olduğu elektriktir. Ancak bu derste anlatılacak olan insan vücudundan elektrotlar vasıtasıyla
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN
 İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN G1 kromozomu S sonu G2 kromozomu Genler Sentromer Kardeş kromatid Dublike olmamış Dublike olmuş Mitoza girerken kromozomlar iki kromatid halindedir.
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof.Dr. Filiz AYDIN G1 kromozomu S sonu G2 kromozomu Genler Sentromer Kardeş kromatid Dublike olmamış Dublike olmuş Mitoza girerken kromozomlar iki kromatid halindedir.
HAYVANSAL HÜCRELER VE İŞLEVLERİ. YRD. DOÇ. DR. ASLI SADE MEMİŞOĞLU RESİM İŞ ZEMİN KAT ODA: 111
 HAYVANSAL HÜCRELER VE İŞLEVLERİ YRD. DOÇ. DR. ASLI SADE MEMİŞOĞLU RESİM İŞ ZEMİN KAT ODA: 111 asli.memisoglu@deu.edu.tr KONULAR HAYVAN HÜCRESİ HAYVAN, BİTKİ, MANTAR, BAKTERİ HÜCRE FARKLARI HÜCRE ORGANELLERİ
HAYVANSAL HÜCRELER VE İŞLEVLERİ YRD. DOÇ. DR. ASLI SADE MEMİŞOĞLU RESİM İŞ ZEMİN KAT ODA: 111 asli.memisoglu@deu.edu.tr KONULAR HAYVAN HÜCRESİ HAYVAN, BİTKİ, MANTAR, BAKTERİ HÜCRE FARKLARI HÜCRE ORGANELLERİ
Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem. Prof.Dr.Mitat KOZ
 Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem Prof.Dr.Mitat KOZ Mikrodolaşım? Besin maddelerinin dokulara taşınması ve hücresel atıkların uzaklaştırılması. Küçük arteriyoller her bir doku
Doku kan akışının düzenlenmesi Mikrodolaşım ve lenfatik sistem Prof.Dr.Mitat KOZ Mikrodolaşım? Besin maddelerinin dokulara taşınması ve hücresel atıkların uzaklaştırılması. Küçük arteriyoller her bir doku
Akıllı Defter. 9.Sınıf Biyoloji. vitaminler,hormonlar,nükleik asitler. sembole tıklayınca etkinlik açılır. sembole tıklayınca ppt sunumu açılır
 9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
HORMONLAR VE ETKİ MEKANİZMALARI
 HORMONLAR VE ETKİ MEKANİZMALARI Receptörler İntrasellüler hidrofobik(llipofilik)ligandlara baglananlar Nükleer hormon reseptörleri Guanylate siklaz(nitrikoksid receptor) Hücre yüzey hidrofilik ligandlara
HORMONLAR VE ETKİ MEKANİZMALARI Receptörler İntrasellüler hidrofobik(llipofilik)ligandlara baglananlar Nükleer hormon reseptörleri Guanylate siklaz(nitrikoksid receptor) Hücre yüzey hidrofilik ligandlara
