PARASETAMOL KULLANIMININ RAT KARACİĞER SERBEST RADİKAL METABOLİZMASI İLE İLİŞKİSİ: N- ASETİLSİSTEİN İN ETKİSİ
|
|
|
- İbrahi̇m Demirören
- 7 yıl önce
- İzleme sayısı:
Transkript
1 T.C. GAZİ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ TIBBİ BİYOKİMYA ANABİLİM DALI PARASETAMOL KULLANIMININ RAT KARACİĞER SERBEST RADİKAL METABOLİZMASI İLE İLİŞKİSİ: N- ASETİLSİSTEİN İN ETKİSİ Yüksek Lisans Tezi PERİHAN HAVARE Tez Danışmanı Prof. Dr. ORHAN CANBOLAT ANKARA Temmuz 2011
2 I
3 İÇİNDEKİLER Kabul ve Onay İçindekiler Tablo ve Grafik Listesi Şekil Listesi Kısaltmalar I II IV V VI 1- GİRİŞ VE AMAÇ 1 2- GENEL BİLGİLER Serbest Radikaller Reaktif Oksijen Türleri Süperoksit Hidrojen Peroksit Hidroksil Singlet Oksijen Reaktif Nitrojen Türleri Nitrik Oksit Serbest Radikal Kaynakları Endojen Serbest Radikal Kaynakları Ekzojen Serbest Radikal Kaynakları Serbest Radikallerin Biyomoleküller Üzerine Etkisi DNA ya Etkisi Lipidlere Etkisi Proteinlere Etkisi Antioksidan Sistemler Endojen Antioksidanlar Ekzojen Antioksidanlar Enzim Olan Antioksidanlar Katalaz Süperoksit Dismutaz 20 II
4 Glutatyon-S-Transferaz Glutatyon Redüktaz Glutatyon Peroksidaz Enzim Olmayan Antioksidanlar Glutatyon Parasetamol Parasetamolün Tarihçesi Parasetamolün Yapısı ve Özellikleri Parasetamolün Metabolizması Parasetamolün Hepatotoksik Etkisi Parasetamol Toksisitesinde Klinik ve Medikal Tedavi N-Asetilsistein MATERYAL VE METOD Çalışmada Kullanılan İlaçlar Çalışma Grupları Kullanılan Materyaller Yöntemler İstatistik BULGULAR TARTIŞMA SONUÇ ÖZET SUMMARY KAYNAKLAR TEŞEKKÜR ÖZGEÇMİŞ EKLER 91 III
5 TABLO VE GRAFİK LİSTESİ Tablo 1: Reaktif oksijen ve nitrojen türleri 7 Tablo 2: Endojen antioksidanlar 18 Tablo 3: Ekzojen antioksidanlar 19 Tablo 4: Parasetamol içeren bazı ürünler ve içerdikleri parasetamol miktarı 26 Tablo 5: Parasetamol zehirlenmesinde belirti ve bulgular 37 Tablo 6: Parasetamol zehirlenmesinde NAS ın uygulama protokolleri 45 Tablo 7: Grupların AST ve ALT değerleri 57 Tablo 8: Grupların SOD, GSHPx, GST, CAT aktiviteleri ve MDA düzeyleri 58 Tablo 9: Ölçülen parametrelere ait gruplar arası istatistiksel değerlendirme 59 sonuçları Tablo 10: Histopatolojik değişiklikler 65 Grafik 1: MDA standart grafiği 50 Grafik 2: Protein standart grafiği 55 Grafik 3: Karaciğer dokusu SOD aktiviteleri sonuçları 60 Grafik 4: Karaciğer dokusu GSHPx aktiviteleri sonuçları 60 Grafik 5: Karaciğer dokusu Glutatyon-S-Transferaz aktiviteleri sonuçları 61 Grafik 6: Karaciğer dokusu Katalaz aktiviteleri sonuçları 61 Grafik 7: Grupların ALT değerleri 62 Grafik 8: Grupların AST değerleri 62 Grafik 9: Grupların MDA düzeyleri 63 IV
6 ŞEKİL LİSTESİ Şekil 1: Serbest Oksijen radikallerinin oluşum basamakları 6 Şekil 2: Serbest radikal hasarına bağlı olarak oluşan ürünler 17 Şekil 3: Glutatyonun yapısı 23 Şekil 4: Parasetamolün kimyasal yapısı 25 Şekil 5: Parasetamolün 3 boyutlu yapısı 25 Şekil 6: Parasetamol metabolizması 28 Şekil 7: Parasetamolün organlar arasındaki dağılımı 30 Şekil 8: Parasetamolün hepatik nekroz yapıcı mekanizması 33 Şekil 9: N-Asetilsisteinin kimyasal yapısı 39 Şekil 10: TBA-MDA kompleksi oluşumu 49 V
7 KISALTMALAR ALT: Alanin amino transferaz APAP: Parasetamol AST: Aspartat amino transferaz ATP: Adenozin tri-fosfat Ca +2 : Kalsiyum CAT: Katalaz COX: Siklooksijenaz DNA: Deoksiribonükleik asit FDA: Amerikan Federal İlaç ve Gıda Kurumu GSH: Redükte Glutatyon GSHPx: Glutatyon peroksidaz GSSG: Okside Glutatyon GST: Glutatyon-S-Transferaz GÜDAM: Gazi Üniversitesi Laboratuar Hayvanları Yetiştirme ve Deneysel Araştırma Merkezi H 2 O 2 : Hidrojen peroksit HOCl: Hipoklorik asit Ip: İntraperitonel IU: İnternasyonel ünite Iv: İntravenöz LPO: Lipid peroksidasyonu M: Molar MDA: Malondialdehit mg: miligram VI
8 mm: Milimolar MPT: Mitekondriyal membran permeabilite transisiyon NADPH: Nikotinamid- adenin- dinükleotit-fosfat NAPQI: N-asetil- p-benzokinonimin NAPSQI: N-asetil-p-benzosemikinonimin NAS: N-asetilsistein NO: Nitrik oksit NOS: Nitrik oksit sentaz - O 2 : Süperoksit radikali OH : Hidroksil radikali OONO- : Peroksinitrit PAR-CG: Parasetamol-sisteinilglisin konjugatı PAR-CYS: Parasetamol-sistein konjugatı PAR-GLUC: Parasetamol-glukoronid konjugatı PAR-SG: Parasetamol-glutatyon konjugatı PAR-SULP: Parasetamol-sülfat konjugatı PGES: Prostoglandin endoperoksit sentetaz Sf: Serum fizyolojik SOD: Süperoksit dismutaz VII
9 1. GİRİŞ VE AMAÇ Parasetamol (Asetaminofen, N-asetil-p-aminofenol, N-(4- hidroksifenil) asetamid, APAP) çok sık kullanılan güçlü bir analjezik ve antipiretiktir. Tıpta ilk olarak 1893 yılında kullanılmış fakat 1949 yılından sonra kullanımı artmıştır. Reçeteli ve reçetesiz satılabilen parasetamolün kolay ulaşılabilir ve ucuz olması tercih edilmesinin en önemli nedenleridir. Parasetamolün klinik dozlarda kullanımı güvenlidir. Fakat yüksek dozda alımı ölümcül olabilmektedir. 1 Parasetamol aspirine göre yaklaşık olarak eşit derecede analjezik ve antipiretik etki yapar. Ancak aspirinden farklı olarak antiinflamatuar etkinliği oldukça düşüktür. Parasetamolün terapötik dozlarda güvenli olmasına rağmen aşırı doz alımının hepatik ve renal hasara neden olduğunu gösteren çok sayıda çalışma vardır. 2,3,4,5 İlaca bağlı zehirlenmelerde en yüksek oran parasetamole aittir. Son on yılda Parasetamolün neden olduğu karaciğer toksisitesi Avrupa ve Amerika da artmıştır. Yalnızca 2006 yılında Amerika da parasetamole bağlı 140 bin zehirlenme olayı görülmüş, bu hastaların 100 den fazlası hayatını kaybetmiştir. 6 Terapötik dozlarda alınan parasetamol glukoronik asit ve sülfatla birleşerek atılır. Çok az miktarda ise N-asetil p-benzokinoimine (NAPQI) dönüşür. Karaciğer sitokrom p450 enzim sistemiyle oluşan bu metabolit, glutatyonla (GSH) birleşerek merkapturik asit olarak atılabilir. Yüksek dozda alınan parasetamol, NAPQI nın birikmesine neden olur. 7 NAPQI ara ürünü hücreler için toksik etkiye sahiptir. NAPQI hepatik hücre makromoleküllerine bağlanarak yapısal moleküllerin ve enzim sisteminin 1
10 bozulmasına neden olur. 8,9 Hücre içi glutatyonun tüketimine bağlı olarak hücre içi antioksidan savunma mekanizmalarında baskılanma olur ve bu olay hücreyi nekroza götüren bir dizi reaksiyonu başlatır. Glutatyon; sistein, glutamil ve glisinden meydana gelen bir tripeptittir. Yapısındaki sisteinin tiyol grubundan ve yüksek konsantrasyonundan dolayı önemli bir antioksidandır. Hücre içinde indirgenmiş halde bulunan glutatyon; proteinlerin, sistein ve koenzim A gibi moleküllerin tiyol gruplarının ve antioksidan moleküllerin yapısının korunmasını sağlar. N-asetilsistein (NAS), L-sistein ve redükte glutatyonun asetillenmiş öncülüdür. Hücre içinde sülfhidril birikimine neden olarak indirgenmiş glutatyonun öncü maddesi olarak rol oynar. 10,11 Glutatyon stoklarını yeniler, süperoksit dismutaz (SOD) aktivitesini artırır, hidroksil (OH ) radikallerini azaltır ve lipit peroksidasyonunu engeller. Glutatyon özellikle radikal metabolizması için merkezi role sahip olan glutatyon peroksidaz (GSHPx) enzimi çin önemli bir subsrattır. Hücre içi redükte/okside glutatyon (GSH / GSSG) oranları serbest radikallerin detoksifiye edilmesi bakımından büyük önem sahiptir. Dolayısıyla hücre içi GSH / GSSG oranlarının regülasyonu radikal metabolizması bakımından önem taşımaktadır. NAS bir glutatyon prekürsörü olduğundan APAP toksisitesine bağlı olan zehirlenmelerde hastalara NAS tedavisi uygulanmaktadır. 12,13 NAS, NAPQI ı temizleyici etki göstermektedir. 14,15 Erken dönemde verilen NAS (ilk 8 saatte) bu şekilde etki gösterirken uzun süre ve yüksek doz verilen verilen NAS ın karaciğer toksisitesine yol açabileceğine işaret eden çalışmalar mevcuttur. Çalışmamızda yüksek dozda parasetamol kullanımına bağlı olarak meydana gelebilecek hepatotoksisitenin ve yüksek ve tekrarlayan doz NAS ın bu toksisiteden korunmadaki rolü serbest radikalleri 2
11 metabolize eden enzimler açısından araştırılmıştır. Parasetamol toksisitesinin karaciğer hücrelerine olan etkisi ve NAS kullanımının toksisiteden korunmadaki rolünü araştırmak amacıyla karaciğer hücrelerindeki hücresel seviyedeki değişim mikroskobik olarak değerlendirilecektir. Çalışmamızda serbest radikal metabolizmasında rol alan enzimler olan ; Süperoksit dismutaz (SOD), Katalaz (CAT), Glutatyon peroksidaz (GSHPx) ve Glutatyon-S-Transferaz (GST) enzim aktiviteleri ile lipit peroksidasyonunun göstergesi olan malondialdehit ( MDA ) seviyeleri rat karaciğer hücrelerinde ölçülerek Parasetamol ve NAS moleküllerinin radikal metabolizmasıyla olan ilişkisi değerlendirilecektir. Bu ilişki değerlendirilirken özellikle yüksek doz parasetamol kullanımına karşı tek doz, tekrarlanan dozlar ve parasetamol kullanımı öncesi koruyucu olarak verilecek N-asetilsisteinin metabolizma üzerine etkisinin araştırılması planlanmaktadır. 3
12 2. GENEL BİLGİLER 2.1. SERBEST RADİKALLER Serbest radikaller yapılarında eşleşmemiş elektron bulunduran atom veya moleküllerdir. 16 Radikallerin çoğu başka moleküllerden bir elektron alarak ya da moleküllere bir elektron vererek etki yaparlar. 16 Kimyasal tepkimeler dış orbitallerdeki elektronlarla gerçekleştiği için dış orbitalde ortaklanmamış elektron bulunması reaktiviteyi artırır. Bu nedenle serbest radikaller oldukça reaktiftir. Serbest radikallerin en önemli tepkimeleri oksijen türevleri ile geçiş elementleri ile gerçekleştirdiği tepkimelerdir. Serbest radikaller ve oksidatif stres teorisinin kökeni 19.yüzyılın sonlarına dayanmasına rağmen 1970 lerin başına kadar bu radikallerin biyolojik sistemlerdeki önemi bilim çevrelerinde kabul görmemiştir. Bunun nedeni radikallerin çok dayanıksız yapıda olması ve belirlenebilmeleri için gerekli tekniklerin olmamasıdır. Günümüzde ise ileri teknikler sayesinde radikaller iyi bir şekilde çalışılmakta olup mekanizmaları aydınlatılabilmiştir. 16 Serbest radikaller başlıca 3 şekilde oluşabilmektedir. 1- Kovalent bağın homolitik kırılması: Bir molekülü oluşturan kovalent bağın yüksek enerjili elektromanyetik dalgalar ve yüksek sıcaklık gibi nedenlerle oluşan kırılmada bağ yapısındaki iki elektronun her birinin ayrı parçada kalmasıyla serbest radikaller meydana gelmektedir. 17 4
13 X : Y X + Y 2- Normal bir molekülün elektron kaybetmesi: Radikal olmayan bir molekülden elektron kaybı sırasında dış orbitalinde ortaklanmamış elektron kalıyorsa, radikal formu oluşur. 17 X : Y X: + Y + 3- Normal bir moleküle tek bir elektronun eklenmesi: Radikal özelliği taşımayan bir moleküle bir elektron transferi ile son orbitalde ortaklanmamış elektron oluşuyorsa bu indirgenme radikal oluşumuna neden olur. X + e - X - Oksijen (O 2 ) bütün canlılar için vazgeçilmez olmasıyla birlikte aynı zamanda toksik etki de gösterebilen bir elementtir. Oksijen; karbon, hidrojen, kükürt ve nitrojen ile birlikte organik moleküllerin temel yapısal atomlarını oluşturur. Yapısal görevinin yanında aerobik canlıların enerji metabolizmasındaki rolüyle de hayati rol üstlenmiştir. Çok sayıda hidroksilaz ve oksidaz enzimi oksijeni substrat olarak kullanıp organik moleküllerin yapılarına katılımını katalizler. 17 Toksik etkisine bakıldığında ise moleküler oksijen aerobik canlılarda bazı enzimleri inhibe eder. Karbondioksit fiksasyonunu katalizleyen ribuloz bifosfat karboksilaz ve nitrojen fiksasyonunu katalizleyen nitrojenaz enzimleri örnek verilebilir. 17 Ayrıca oksijen tek elektron aldığında hücre lipitleri, proteinleri ve DNA sını tahrip eden ileri derecede reaktif oksijen radikallerine dönüşür. 18 5
14 Reaktif Oksijen Türleri Oksijen, biyolojik sistemlerdeki en önemli serbest radikal kaynağıdır. Toplam sekiz elektronu bulunan oksijen dış orbitalinde paylaşılmamış iki elektron içerir. Bu yüzden oksijen bir diradikaldir. Oksijen dört elektron alma gücündedir ve bu elektronları alarak suya indirgenir. Oksijenin bir elektron alması ile süperoksit radikali (O - 2 ) oluşur. Süperoksit bir eşleşmemiş elektron taşıdığı için bir radikaldir. Süperoksit bir elektron alarak hidrojen peroksite (H 2 O 2 ) indirgenir. Hidroksil radikali (OH. ) indirgenme dizisindeki bir elektron indirgenmesiyle oluşurken son elektronun alınmasıyla da su oluşur. 18 Şekil 1: Serbest oksijen radikallerinin oluşum basamakları Serbest radikal denilince akla oksijen radikalleri gelmektedir. Fakat oksijen radikallerinin yanı sıra nitrojenden meydana gelen radikaller de bulunmaktadır. 6
15 Tablo 1: Reaktif oksijen ve nitrojen türleri 18 Radikaller Radikal olmayanlar Süperoksit (O 2 - ) Hidrojen peroksit (H 2 O 2 ) Hidroksil (OH. ) Lipit hidroperoksit (LOOH) Peroksil (ROO. ) Hipohalöz asit (HOX) Organik radikaller (R ) Azot dioksit (NO 2 ) Semikinon radikali (HQ ) Singlet oksijen ( 1 O 2 ) Organik peroksit radikali (RCOO. ) Nitrik oksit (NO. ) Hipoklorik asit (HOCl) Peroksinitrit (ONOO-) Organizmada serbest radikallerin oluşması ve bu radikallerin antioksidan sistem tarafından ortamdan kaldırılması arasında bir denge vardır. Bu dengenin serbest radikaller lehine bozulması sonucu oksidatif stres meydana gelir. Serbest oksijen radikallerinin ateroskleroz, diabettus mellitus, amfizem, hiperoksi, romatoid artrit, kanser, pankreatitis gibi bir çok hastalığın patogenezinde rol oynadığı düşünülmektedir Süperoksit (0 2 - ) Süperoksit radikali, oksijenin bir elektron almasıyla meydana gelir. O 2 + e - O 2.- 7
16 Süperoksit, dehidrojenazlar ve oksidazlar başta olmak üzere bir çok enzimin katalitik etkisi sırasında oluşur. Süperoksit üreten mekanizmaların başında mitokondriumun iç membranında oksijenin suya dönüşümünü sağlayan elektron transport zinciri gelir. Mitokondrinin enerji metabolizması sırasında tüketilen oksijenin yaklaşık %1-5 i süperoksit radikali yapımı ile sonuçlanır. Flavin nükleotitleri, glikoz, katekolaminler, ferrodoksin, adrenalin, tiyol bileşimleri gibi moleküller de oksijen varlığında - okside olarak 0 2 oluştururlar. Damar endotelinde nitrik oksiti (NO) nötralize etmek için devamlı süperoksit oluşumu görülmektedir. Aktive olan fagositik lökositler de süperoksit üretir. Süperoksitin önemi hidrojen peroksit kaynağı olması ve geçiş metalleri iyonlarının indirgeyicisi olmasından kaynaklanmaktadır. Süperoksit, süperoksit dismutaz ile ya da kendiliğinden hidrojen peroksite çevirilir Hidrojen peroksit (H 2 O 2 ) Moleküler oksijenin iki elektron alması ya da süperoksit radikalinin bir elektron almasıyla peroksit oluşur. Bu molekülün iki hidrojen atomuyla birleşmesi sonucu hidrojen peroksit meydana gelir. O 2 + 2e - + 2H + H 2 O 2 O e - + 2H + H 2 O 2 Hidrojen peroksit, radikal olmamasına rağmen hidroksil radikali üretebilmesi nedeniyle radikal olarak sınıflandırılan zayıf bir okside edici ajandır. Fe ve Cu gibi geçiş metalleri varlığında Fenton tepkimesi ile, süperoksit varlığında Haber-Weiss tepkimesi sonucu en zararlı ve en reaktif radikal olan hidroksil radikalinin oluşmasını katalize 8
17 eder. Hidrojen peroksit lipitte çözünebildiğinden zarlardan sızabilir ve mitokondri gibi lokalize Fe veya Cu içeren noktalarda OH üretir. H 2 O 2 fagositoz yapan hücreler tarafından içsel ve enzimatik olarak üretilen güçlü bir okside edici ajan olan hipoklorik asitin (HOCl) de öncülüdür. Hidrojen peroksit ultraviyole ışıkta hidroksil radikaline dönüşebilmektedir. H 2 O 2 uv 2 OH Hidrojen peroksit özellikle proteinlerdeki hem grubu demiri ile tepkimeye girerek ferril ve perferril radikali oluşumuna neden olur. Bu formdaki reaktif demir çok güçlü oksitleyici özelliğe sahip olup hücre zarında lipit peroksidasyonu gibi radikal tepkimeleri başlatabilir. Hidrojen peroksitin ortadan kaldırılması katalaz ve glutatyon peroksidaz enzimleri tarafından sağlanır Hidroksil (OH ) En reaktif ve toksik etkili radikal hidroksil radikalidir. Fenton ve Haber-Weiss tepkimeleri sonucunda oluşur. Serbest oksijen radikalleri OH radikallerine dönüşerek toksik etkilerini gösterirler. OH serbest radikalle uyarılan doku hasarında son mediatördür. Son derece reaktif olan OH canlı hücrelerde lipit, aminoasit ve nükleotitler gibi moleküllerle reaksiyona girerek hasar oluşturur. H 2 O 2 + O 2 - OH + OH - + O 2 Haber-Weiss Reaksiyonu 9
18 Fe +3 + O 2 - O 2 + Fe +2 Fenton Reaksiyonu Fe +2 + H 2 O 2 Fe +3 + OH - + OH Vücutta en önemli OH kaynağı hidrojen peroksitin eksik indirgenmesidir. H 2 O 2 nin iki elektronla indirgenmesiyle su oluşurken Cu ve Fe gibi metallerin katalizörlüğünde tek elektronla indirgenmesi OH yapımına neden olur. Ayrıca OH canlılarda sulu ortamda iyonlaştırıcı radyasyonun etkisiyle su moleküllerinin iyonlaşmasıyla da oluşabilir. Hidroksil radikali tepkimeleri; elektron transferi tepkimeleri, hidrojen çıkarma tepkimeleri ve katılma tepkimeleri olarak gerçekleşir. Bu tepkimeler OH radikalinin paylaşılmamış elektron içeren dış orbitaline elektron alma ilgisinin bir sonucudur. OH nin katılma tepkimeleri pürin ve pirimidin bazları, aromatik aminoasitler gibi elektron bakımından zengin moleküllerle gerçekleşir. Hidrojen çıkarma tepkimeleri ise organik moleküllerden hidrojen atomu alarak suya indirgendiği tepkimelerdir. Hidrojen çıkarma tepkimeleri zincir olarak gerçekleşebilir. Bu tepkimelere lipit peroksidasyonu örnek verilebilir. OH ; nükleik asitler, proteinler ve lipitleri hedef olarak seçer. DNA da baz modifikasyonları, baz delesyonları ve zincir kırılmaları meydana getirebilir. Sonuçta hücre ölümüne sebep olur. OH, zar lipitlerinin peroksidasyonuyla zarın yapısını bozarak geçirgenliği artırır ve hücre ölümüne neden olur. 10
19 Singlet Oksijen ( 1 O 2 ) Yapısında eşleşmemiş elektron bulundurmadığından gerçek bir radikal değildir. Oksijenin enerji alarak uyarılması sonucu elektronlarından birinin kendi spinin tersi bir orbitale yer değiştirmesiyle oluşur. Çok yüksek reaktiviteye sahiptir. Singlet oksijen; pigmentlerin ışığı absorbe etmesi ile, hidroperoksitlerin metal varlığında yıkımı ile, bazı sitokrom p450 tepkimelerinde oluşabilir Reaktif Nitrojen Türleri Nitrik Oksit (NO) Nitrik oksit, oksijen gibi yaşam için hem gerekli hem de toksik bir maddedir. Vasküler tonusun ve hücresel adezyonun düzenlenmesinde, immün cevap ve nöronal aşırım gibi birçok fizyolojik olayda görev alır. 20 Düşük konsantrasyonlarda fizyolojik olarak bir nörotransmitter ve vazodilatasyona neden olan bir hormon olarak görev yapar. Ancak yüksek konstransyonlarda hücre moleküllerine bağlanarak onları etkisiz hale getirir. Nitrik oksit, nitrojen merkezli bir radikaldir. Paylaşılmamış elektron nitrojen atomuna ait ise de bu elektron hem nitrojen hem de oksijen atomu üzerinde delokalizedir. Bu yüzden NO tam bir radikal özellik taşımaz. NO uzun ömürlüdür. Oksijen radikallerinin tersine NO yu ortadan kaldıracak bir enzim yoktur. Oksijen radikalleri çok fazla yolla üretilebilmelerine rağmen NO yu oluşturan kaynaklar sınırlıdır. Nitro bileşiklerinin metabolizması sırasında oluşan NO dışında, endojen NO oluşturan tek mekanizma nitrik oksit sentaz (NOS) enzimleridir. 11
20 NO, L-Arjinin den NOS aracılığıyla sentezlenir. Sentezi için nikotinamid adenin dinükleotit fosfat (NADPH), kalmodulin, oksijen ve dört kofaktöre (hem, flavin mononükleotid, flavin adenin dinükleotid ve tetrahidrobiyopterin) gereksinim vardır. 20 NOS un 3 farklı izoformu bulunur. Endoteliyal NOS (enos), nöronal NOS (nnos) ve indüklenebilir NOS ( inos). enos ve nnos yapısal NOS lar olarak adlandırılır. Yapısal NOS lar nöronal yapılar, endotel hücreleri, endokard, miyokard ve trombositlerde bulunur. Yapısal NOS lar kofaktör olarak Ca +2 ve kalmodulin bağımlıdır. enos için L-Arjinin tek substrattır. inos aktivitesi kalsiyumdan bağımsızdır ve ortamda arjinin bulunduğu sürece aktiftir. inos, makrofajlarda, epitel hücrelerinde ve damar düz kas hücrelerinde bulunur. 20 NOS L-Arjinin + O 2 + NADPH L-Sütrilin + NO + NADP + NO diğer serbest radikallerle kolaylıkla reaksiyona girebilir (peroksil ve alkil radikalleri). NO lipit radikalleri ile tepkimeye girmesi nedeniyle antioksidan özellik gösterir. Yüksek miktardaki NO üretimine paralel yüksek miktarda süperoksit varlığında oldukça sitotoksik olan peroksinitrit (OONO-) oluşur. OONO-, tirozin kalıntılarının nitritlenmesine ve proteinlerin sülfidril gruplarının oksitlenmesine neden olur Serbest Radikal Kaynakları Serbest radikaller normal hücresel metabolizma sürecinde oluşabildiği gibi dış etkenlerle de oluşabilmektedir. 12
21 Endojen Serbest Radikal Kaynakları Mitokondriyal elektron transport zinciri Mitokondriyal serbest radikallerin en önemli kaynağı elektron transport zincirindeki sızıntıdır. Mitokondri, sitokrom oksidaz sistemi ile oksijeni suya indirgeyerek ATP üretir. Normal oksijen kullanımının %1-2 sinin reaktif oksijen üretimine neden olduğu düşünülmektedir. 22 Ksantin oksidazın katalitik döngüsü Ksantin oksidaz hasarlanmamış dokularda bir dehidrojenaz olarak vardır. Pürinlerin yıkılım yolunda hipoksantinden ksantin ve ksantinden ürik asit oluşum basamaklarında elektron alıcısı olarak moleküler oksijenden daha çok NAD + kullanır. Oksijensizliğe bağlı olarak ADP nin ATP ye fosforilasyonunun azaldığı durumlarda (iskemi durumlarında) ADP yıkılır ve pürin bazı, ksantin oksidazın bir oksidaz olarak etkili olmasıyla hipoksantine dönüştürülür. Ksantin oksidazın, oksidaz olarak aktivite göstermesi durumunda hipoksantin ksantine ve ksantin ürik aside dönüşürken moleküler oksijen kullanılır. Sonuçta hidrojen peroksit ve süperoksit radikali oluşur. Ksantin oksidazın iskemireperfüzyon hasarında önemli faktör olduğu düşünülmektedir. İskemi sonrası reperfüzyon ve hipoksiden sonra reoksijenasyon doku hasarına yol açabilir. Bu özel durumlar mikrosirkülasyon kaybı, şok, organ transplantasyonu, cerrahi müdahale bölgesindeki kansızlık veya damarların klemplenmesi gibi bazı hastalıklarda ortaya çıkabilir
22 Endoplazmik retikulum ve nükleer membranda membrana bağlı sitokromların oksidasyonu Endoplazmik retikulum membranında bulunan sitokrom p450 enzim sistemi birçok ksenobiyotiğin detoksifikasyonunu katalizler. Bazı durumlarda sitokrom p450 enzim sistemi ile yüksek miktarda süperoksit oluşumu görülebilir. Araşidonik asit metabolizması Fagositik hücrelerin uyarılması fosfolipaz ve protein kinazın aktivasyonuna ve plazma membranından araşidonik asit salınımına neden olur. Araşidonik asidin enzimatik oksidasyonu ve eikazonoitlerin biyosentezi sırasında oksijen radikalleri meydana gelir. Aktive olmuş makrofajlar, nötrofiller ve eozonofillerde solunumsal patlama NADPH oksidaz nötrofillerin plazma zarında bulunur. Solunumsal patlama, süperoksit oluşturmak üzere bir elektronun NADPH tan O 2 ye aktarılmasını katalize eden NADPH oksidazın etkinliği sonucu oluşan bir olaydır. Oluşan süperoksit, hidrojen peroksiti meydana getirir. Miyeloperoksidaz varlığında H 2 O 2; klor, brom ve iyotla birleşerek hipohalöz asitleri oluşturur. Diğer taraftan H 2 O 2 demir varlığında hidroksil radikalini oluşturur. Fagosite edilmiş bakterinin ölümü reaktif oksijen türleri ile yapılırken bazen de bu oksidan türler antioksidan sistemi aşarak normal hücrelere zarar verirler
23 Ekzojen Serbest Radikal Kaynakları Radyasyon, sigara, aşırı egzersiz, ilaçlar, pestisitler, virüsler, alkol, çevre kirleticileri ekzojen serbest radikalleri kaynaklarından bazılarıdır SERBEST RADİKALLERİN BİYOMOLEKÜLLER ÜZERİNE ETKİSİ Serbest radikaller hücrenin antioksidan kapasitesini aştıkları zaman hücre makromoleküllerine saldırırlar. DNA ya bağlanarak baz modifikasyonlarına, membran lipitlerine saldırarak membran bütünlüğünün bozulmasına, proteinleri oksitleyerek fonksiyonlarının değişmesine neden olurlar DNA ya Etkisi DNA, hücre membranı ve histon proteinleri tarafından iyice korunmasına rağmen serbest radikaller DNA yı hedef alarak hücrede mutasyona neden olurlar. DNA ya en büyük zararı hidroksil radikali verir. OH, bazlarla ve şekerle reaksiyona girerek baz mofikasyonları, şeker lezyonları, DNA-protein çapraz bağları, tek ve çift dal kırıkları oluşturabilir. Oksijen radikalleri bazlara etki ederek timin-glikol, timidin glikol, 5-15
24 hidroksimetilurasil, 8-hidroksiadenin, 8-okso-2deguanozin (8OHdG) gibi modifikasyonlara neden olurlar Lipidlere Etkisi Lipidler serbest radikallere karşı oldukça hassas moleküllerdir. Serbest radikaller özellikle çoklu doymamış yağ asitlerinin yapısındaki ikili bağları hedef alırlar. Lipid peroksidasyonu sonucu ortaya çıkan ürünler radikal hasarın incelenmesinde önemli rol oynamaktadır. Yağ asitlerinin peroksidasyonu zincir reaksiyonu şeklinde meydana gelir. Doymamış yağ asidi ile başlatıcı bir radikalin reaksiyonu sonucu bir hidrojen atomu transferiyle yağ asidi radikali oluşur. Yağ asidi radikaline oksijen eklenmesiyle peroksi radikali meydana gelir. Peroksi radikalleri diğer bir yağ asidi molekülünden ayrılan bir hidrojenle birleşip hidroperoksitler ve yeni lipid radikallerine dönüşür. Böylece lipid peroksidasyonu bir zincir reaksiyonu şeklinde devam eder. Sonuçta malondialdehit, etan ve pentan gibi ürünler oluşur Proteinlere Etkisi Serbest radikaller proteinleri oksitleyerek inaktive edebilir, fonksiyonlarını değiştirebilirler. Serbest radikallerin hedefi proteinlerin yapısındaki sülfür içeren amino asitlerdir. Bu nedenle yapısında metiyonin, triptofan, sistein, tirozin, fenil alanin, histidin gibi aminoasitleri bulunduran proteinler reaktif oksijen türlerine karşı daha duyarlıdır. 16
25 Şekil 2 : Serbest radikal hasarına bağlı olarak oluşan ürünler. Serbest radikaller DNA, hücre membranları, proteinler gibi farklı makromoleküllerle reaksiyona girerek farklı ürünler oluşturabilirler
26 2.3. ANTİOKSİDAN SİSTEMLER Hücreler serbest radikallerin hasarlarına karşı pek çok savunma mekanizması geliştirmişlerdir. Bunların başında antioksidan enzimler gelir. Hücre içinde enzim olmayan antioksidanlar da hücreleri oksidatif hasara karşı savunmada görev yapar Endojen Antioksidanlar Tablo 2: Endojen antioksidanlar Enzim olan endojen antioksidanlar Enzim olmayan endojen antioksidanlar Süperoksit dismutaz Katalaz Glutatyon peroksidaz Glutatyon-S-Transferaz Mitokondriyal sitokrom oksidaz Hidroperoksidaz Melatonin Ürat Seruloplazmin Transferrin Miyoglobin Hemoglobin Ferritin Albumin Laktoferrin Glutatyon Sistein Metiyonin 18
27 Ekzojen Antioksidanlar Tablo 3: Ekzojen antioksidanlar 26 Vitamin olan ekzojen antioksidanlar α- Tokoferol, β- Karoten, Askorbik asit, Folik asit. İlaç olarak kullanılan ekzojen antioksidanlar Rekombinant süperoksit dismutaz NADPH oksidaz inhibitörleri (lokal anestezikler, kalsiyum kanal blokerleri, nonsteroid antiinflamatuar ilaçlar) Ksantin oksidaz inhibitörleri (allopürinol, oksipürinol, pterin aldehit, tugsten) Trolox-C Sitokinler (TNF-IL-1) Ebselen ve asetilsistein Nonenzimatik serbest radikal toplayıcılar (mannitol, albumin) Enzim Olan Antioksidanlar Katalaz (CAT, EC ) Katalaz (CAT), molekül ağırlığı 248 kda olan ve yapısında kovalent olmayan bağ ile bağlı dört protoporfirin içeren bir enzimdir. Katalaz esas olarak peroksizomlarda bulunur. Hemen hemen bütün 19
28 dokularda bulunmasına rağmen en yüksek aktivite peroksizomların yüksek oranda bulunduğu karaciğer, böbrek ve eritrositlerde görülür. Katalaz, hidrojen peroksitin suya dönüşümünü katalizler. Hidrojen peroksit bir radikal olmamasına rağmen Fenton ve Haber - Weiss reaksiyonlarına girerek oldukça toksik olan OH radikalini oluşturur. Bu nedenle hidrojen peroksitin ortadan kaldırılması gerekmektedir. CAT H 2 O 2 + H 2 O 2 2 H 2 O + O Süperoksit Dismutaz (SOD, EC ) Süperoksit radikali bütün aerobik hücrelerde oluşur ve bütün aerobik hücreler süperoksite karşı savunmada SOD içerirler. SOD; bakır, çinko ve mangan içerdiğinden metalloenzim olarak adlandırılır. Süperoksit dismutazın canlılarda 3 türü bulunmaktadır. Bakır ve çinko içeren süperoksit dismutaz (Cu-ZnSOD), mangan içeren SOD (MnSOD) ve demir içeren (FeSOD). Cu-ZnSOD stoplazmada bulunur ve dimerik yapıdadır. Enzim her bir dimerik protein için birer molekül bakır ve çinko içerir. MnSOD tetramerik yapıda olup mitokondri matriksinde bulunur. FeSOD ise tetramerik yapıda bir enzimdir. Bakteriler MnSOD ve FeSOD un her ikisini de bulundururlar. Fakat FeSOD hayvan hücrelerinde bulunmamaktadır. 27 İnsanlarda SOD genindeki bir bozukluk sonucu Lou Gehrig hastalığı görülür. Bu durum Cu-ZnSOD genindeki nokta mutasyonlarla ve azalan sitozolik SOD aktivitesi ile ilişkilidir. Cu-ZnSOD un inhibisyonu spinal nöronların apoptozuna neden olur
29 Süperoksit radikalleri, SOD tarafından katalizlenen reaksiyonda hidrojen peroksite ve moleküler oksijene dönüşür. Bu reaksiyon hücresel H 2 O 2 nin ana kaynağıdır. O O 2 - SOD O 2 + H 2 O Glutatyon-S-Transferaz (GST, EC, ) Glutatyon-S-Transferazların (GST) en önemli fonksiyonları ksenobiyotik metabolizmasında açığa çıkan reaktif ara ürünlerin detoksifikasyonudur. GST ler hücrede sitozolde veya mikrozomal kısımlarda bulunabilirler. GST ler glutatyon ile geniş bir grup elektrofilik kimyasal bileşiğin konjugasyonunu katalizleyerek detoksifiye olmalarını sağlar. Detoksifikasyon dışında GST ler hücre içi taşıyıcı protein olarak da görev alırlar. Ayrıca lipid peroksitlere karşı antioksidan özellik gösterirler Glutatyon Redüktaz (GR, EC ) Glutatyon vücudu oksidatif hasara karşı koruyan temel moleküllerden biridir. Glutatyon; glutamat, sistein ve glisinden oluşmuş bir tripeptittir. Glutatyon redüktaz, stoplazmada yer alan 48 kda molekül ağırlığında bir enzimdir. Glutatyon redüktaz H 2 O 2 ve lipid peroksitlerinin indirgenmesi sırasında oluşan GSSH yi GSH haline getirmekle görevlidir. 21
30 Glutatyon Peroksidaz (GSHPx, EC ) Glutatyon peroksidaz sitozolde yer alır. Dört selenyum atomu içerdiğinden seleno-sistein bileşiği sınıfına girer ve katalitik aktivitesini bu özelliği sağlar. Ko-substrat olarak glutatyona ihtiyaç duyar. 29 Karaciğerde yüksek oranda bulunur. Glutatyonun, glutatyon disülfite oksidasyonunu katalizler. Ayrıca GSHPx hidrojen peroksitin suya dönüşümünü sağlar Enzim Olmayan Antioksidanlar Glutatyon Glutatyon; glutamik asit, sistein ve glisinden oluşan bir tripeptittir. Düşük molekül ağırlıklı bir molekül olup bütün aerobik hücrelerde milimolar konsantrasyonlarda bulunur. 30 Hücrelerdeki en önemli antioksidandır. Proteinlerdeki sülfidril gruplarını (-SH) redükte halde tutar ve bu grupları oksidasyona karşı korur. Glutatyon hücrede redükte (GSH) ve okside (GSSG) halde bulunur. Glutatyonun en önemli görevi hücreleri oksidatif ve nitrozatif strese karşı korumaktır. Serbest radikallerle reaksiyonlara girerek radikalleri ortadan kaldırır. Glutatyon; ksenobiyotiklerin detoksifikasyonunda, sistein transportu ve depolanmasında, prostoglandin metabolizmasının düzenlenmesinde, sinyal iletiminde, gen ekspresyonunda ve apoptoz olayında görev alır. 30,31 Glutatyon, hemoglobinin oksitlenerek methemoglobine dönüşmesinin engellenmesinde de rol oynar. 22
31 Glutatyonun sentezi γ-glutamilsisteinil sentetaz ve glutatyon sentetaz enzimlerinin katalizlediği iki adımda gerçekleşir. 31,32 Şekil 3: Glutatyonun kimyasal yapısı 23
32 2.4. PARASETAMOL Parasetamolün Tarihçesi Parasetamol içeren ilaçların ana bileşiği asetanilid, tıbba 1886 yılında Cahn ve Hepp tarafından tesadüfen keşfiyle girdi. Son derece toksik olduğunun anlaşılması üzerine türevleri denendi. 33 Bunların içinde fenasetin uygun bulunarak 1877 de tedavide kullanılmaya başlandı. Fenasetin nefropatiyle ilişkilendirilene kadar yaygın olarak kullanıldı. Parasetamol ilk kez 1877 de Harmon Northop Morse tarafından p- nitrofenolün asetik asitle redüksiyonu sonucu sentezlendi. Fakat parasetamolü klinikte ilk olarak 1893 te Von Mering kullandı te Brodie ve Axelrod parasetamolün fenasetin ve asetanalidin aktif metaboliti olduğunu ve daha az toksik olduğunu bildirdiler. 34 Parasetamol 1955 yılında Amerika da para-acetylaminophenol ün kısaltması olan Tylenol adıyla, 1956 yılında ise parasetamol 500 mg tablet halinde Panadol adı altında İngiltere de piyasaya sürüldü. Reçeteli ve reçetesiz satılan, güvenli bir analjezik ve antipiretik olarak önem kazanan parasetamol çok çeşitli kombinasyonlarla marketlerdeki yerini alırken yıllarında reçetesiz alınan ağrı kesicilerin toksik olduğu yönündeki fikir yaygınlaştı. Fakat 1980 li yıllarda aspirinin Reye sendromuyla ilişkilendirilmesi tekrar parasetamolün tercih edilmesini sağladı Parasetamolün Yapısı ve Özellikleri Parasetamol güçlü bir analjezik ve antipiretiktir. Sentetik nonopioid bir p-aminofenol derivesi olan parasetamol fenasetinin aktif 24
33 metabolitidir. Kimyasal adı N-(4-hidroksifenil) asetamid dir. Moleküler formülü C 8 H 9 NO 2 dir (Şekil 1). Molekül ağırlığı , erime noktası 169 ºC dir. Parasetamolün oral alımında emilim %60-98, rektal formunun emilimi %40 civarındadır. Plazma proteinlerine %10-30 arasında bağlanır. Plasenta ve kan-beyin bariyerini geçer. 36 Parasetamol antiinflamatuar özelliklere sahip değildir, inflamasyona bağlı hastalıklarda tek başına kullanılmaz. Gastrik lezyonlara neden olmaz. Trombosit agregasyonunu önleyici etkisi zayıftır ve kanama zamanını uzatmaz. Parasetamol günümüzde özellikle pediatride aspirinin alternatifi olarak kullanılmaktadır. Parasetamol nonsteroid antiinflamatuar ilaçlarla kombine edildiğinde onların analjezik etkilerini artırır. Parasetamol kafein, fenasetin, efedrin, kodein, antihistaminikler gibi ilaçlarla da kombine edilerek grip tedavisinde kullanılır. 37 Parasetamol çok hafif geçen deri döküntüleri ve alerjik reaksiyonlar gibi yan etkilere sahiptir. Döküntüler genellikle eritematöz veya ürtiker şeklindedir. Bazen ciddi durumlar ortaya çıkabilir, ilaç ateşi veya mukozal lezyonlar eşlik edebilir. Yüksek dozlarda bulantı, kusma, iştahsızlık, karın ağrıları görülebilir ve hipoglisemik koma oluşabilir. Parasetamolün analjezik ve antipiretik etkileri aspirininkine benzer ancak antiinflamatuar etkisi oldukça zayıftır. Periferik dokularda parasetamol, zayıf bir siklooksijenaz (COX) inhibitörüdür. 38 Şekil 4: Parasetamolün kimyasal yapısı Şekil 5: Parasetamolün 3 boyutlu yapısı 25
34 Parasetamole bağlı zehirlenmelerin nedeni doz aşımıdır. Günlük maksimum doz yetişkinlerde 4 gramdır. Yetişkinlerde 7.5 gramın üzerine çıkılması durumunda hepatotoksisite riski çok yüksektir. 39 Doz aşımı yapılmasının en büyük nedeni kişilerin bilmeden aynı anda birden fazla asetaminofen etkin maddeli ilaç kullanmalarıdır. Amerikan Federal İlaç ve Gıda Kurumu (FDA) verilerine göre 1998 ile 2001 yılları arasında istemeden yapılan parasetamol doz aşımı 307 vakanın %25 i birden fazla asetaminofen içeren ilaç almıştır. FDA ya göre parasetamolün yararlarının fazla olması risklerinin göz ardı edilmesinin en önemli nedenidir. 39 Tablo 4: Parasetamol içeren bazı ürünler ve içerdikleri parasetamol miktarı 39 İlaç dozaj (mg) Asetaminofen miktarı Reçetesiz satılan ürünler Tylenol Arthritis 650 Midol 500 Pamprin 500 Tylenol Extra-Strength 500 Tylenol Allergy,Flu,PM 325 Excedrin 250 Reçeteli satılan ürünler Vicodin ES 750 Darvocet-N Lorcet 10/ Lortab 500 Vicodin 500 Tylox 500 Percocet Fioricet 325 Norco 325 Ultracet
35 Parasetamolün Metabolizması Parasetamol oral yolla alındığında çabuk absorbe edilir ve etkisini erken gösterir. 2 saatte plazma konsantrasyon düzeyi maksimuma ulaşır. Fakat opioidlerle, antikolinerjik ilaçlarla hatta yiyeceklerle bile alındığında bu süre uzar. Parasetamol alındıktan sonra 3-4 saat kadar analjezik etki gösterir. Terapötik dozu yetişkinler için günlük maksimum 4 gramdır. Parasetamol karaciğerde metabolize edilir. Normal dozlarda alınan parasetamolün büyük bir kısmı glukoronik asit ve sülfat ile (%85-90) konjuge olarak böbreklerden atılır. %5 lik kısmı ise değişmeden idrarla atılır. Az miktarda parasetamol (%5-10) ise P450 enzim sistemi ile (başta CYP2E1, CYP1A2, CYP2A6 ve CYP3A4) toksik bir metabolit olan NAPQI ya dönüşür. 40 Bu metabolit glutatyon tarafından inaktif metabolitlere çevirilerek böbreklerden atılır. Overdoz alımlarda fazla miktarda oluşan NAPQI glutatyonu tüketir. NAPQI nın bu etkisi özellikle glutatyon metabolizması açısından önemlidir. Glutatyonun tükenmesine bağlı olarak NAPQI proteinlerin yapısında bulunan sisteine bağlanır. Bu tip kovalent bağlanma proteinlerin inaktivasyonuna neden olarak hepatik hücre ölümüne yol açar. 27
36 PARASETAMOL %85-90 oranında glukuronik asit ve sülfürik asit ile birleşerek atılır %5-10 oranında p450 enzim sistemi ile NAPQI oluşur %5 oranında değişmeden idrarla atılır NAPQI Glutatyonla birleşerek merkaptürik asit ve sistein konjugatları şeklinde atılır Hücre proteinlerine bağlanarak karaciğer nekrozu meydana getirir Şekil 6: Parasetamol metabolizması 40 Parasetamolün biyotransformasyonu majör ve minör olmak üzere 2 yolla gerçekleşir. Majör yolda parasetamol, glukoronik asit ve sülfata dönüşür. Minör yolda ise hepatotoksisiteden sorumlu olan NAPQI oluşur. NAPQI sitokrom p450 enzim sistemiyle meydana gelir. Güçlü elektrofilik bir metabolit olan NAPQI terapötik dozlarda glutatyon ile birleşerek detoksifiye edilir. NAPQI merkapturik asit ve sistein konjugatlarına dönüştürülerek atılırken toksik dozlarda alındığında NAPQI glutatyonu tüketerek hücrede proteinlere bağlanır ve sonuçta hepatosit nekrozuna neden olur. Karaciğerde parasetamol üridin difosfoglukronil transferaz enzimi aracılığında parasetamolün glukronid konjugatına (PAR- GLUC), sülfotransferaz aracılığıyla da parasetamolün sülfat konjugatına 28
37 (PAR-SULP) dönüşür. Oluşan bu ürünlerin bir kısmı safraya geçerken bir kısmı da kana geçer. Parasetamolün az bir kısmı sitokrom p450 enzim sistemiyle NAPQI oluşturur. NAPQI nın bir bölümü protein arilasyonu oluştururken bir bölümü de glutatyon ile birleşir ve parasetamol glutatyon konjugatını (PAR-SG) meydana getirir. Oluşan PAR-SG konjugatı safraya gönderilir. Burada PAR-SG, parasetamol sisteinilglisin konjugatına (PAR- CG) sonrasında ise parasetamol sistein konjugatına (PAR-CYS) dönüşerek bağırsağa geçer. PAR-CYS, bağırsaktan kan dolaşımına katılır. Böbreklerde ise parasetamol, prostoglandin endoperoksit sentetaz (PGES) enzimiyle N-Asetil-p-benzosemikinonimin (NAPSQI) dönüşür. N- Asetil-p-benzosemikinonimin böbrekte NAPQI ya dönüşür
38 Şekil 7: Parasetamolün organlar arasındaki dağılımı 30
39 Parasetamolün toksik dozda alımından sonra karaciğer gibi böbrekler de etkilenmektedir. Parasetamol overdozunda hepatotoksisite çok sık görülürken nefrotoksisite ise daha az ortaya çıkmaktadır. Böbrek yetmezliği yaklaşık olarak yüzde bir oranında görülmektedir. Böbrek yetmezliği genel olarak hepatik nekroz ile birlikte meydana gelmektedir (%10-40). 43 İntihar amacıyla 500 mg asetaminofen ve 10 mg kodein fosfat içeren ilaçtan 60 adet alan, toplamda 30 g alan bir kişide karaciğer yetmezliği gelişmeden böbrek yetmezliği geliştiği gözlemlenmiştir. 43 Bu sebeple toksik dozda parasetamol alan kişilerin hepatotoksisite olmasa bile nefrotoksisite ihtimaline karşı gözetim altında tutulması gerektiği vurgulanmıştır Parasetamolün Hepatotoksik Etkisi Terapötik dozlarda alındığında güvenli olan parasetamol yüksek dozda alındığında hepatik nekroza neden olur. Nekroz yapıcı etkisine aktif metaboliti olan NAPQI neden olmaktadır. 44 NAPQI az miktarlarda oluşur ve glutatyon tarafından ortadan kaldırılır. Ancak yüksek dozda alınan parasetamol glutatyonun tükenmesine neden olur. Glutatyonun %70 inin tükenmesi durumunda NAPQI detoksifikasyon kapasitesini aşarak hepatik nekroza neden olur. 45 Nekroz NAPQI nın proteinlerin sistein kalıntılarına bağlanmasıyla başlar. Ancak bundan sonraki olaylar serisi tam olarak bilinmemektedir. Son zamanlarda bu konuda çok sayıda çalışma yapılmış olup bazı mekanizmalar üzerinde durulmaktadır. En önemli olaylar arasında lipid peroksidasyonu, Ca +2 homeostazisinin bozulması ve mitokondriyal membranın çökmesi gelmektedir. 46,47 31
40 NAPQI ilk olarak glutatyon depolarını boşaltır. Glutatyonun tükenmesinden sonra NAPQI mitokondri membran ve plazma proteinlerine kovalent bağlanır. Bu olaylar hücresel Ca +2 homeostazisini bozarak sitozolik Ca +2 düzeyinin artmasına neden olur. Kalsiyumun hücre içinde birikmesiyle hücre ölümüne neden olan intrasellüler proteazlar aktive olur. Mitokondriyal proteinlerin modifikasyona uğramaları ve hücre içi Ca +2 artışıyla mitokondriyal solunumda ATP sentezinin azalmasına yol açar. ATP sentezinin azalmasıyla mitokondri yüksek miktarda süperoksit üretmeye başlar. Süperoksit, hidrojen peroksite dönüşerek lipit peroksidasyonu başlatabilir. Diğer yandan süperoksit nitrik oksit ile birleşerek peroksinitrit oluşturabilir. Glutatyon yokluğunda peroksinitrit, protein oksidasyonu ve nitrasyonuna neden olur. Böylece mitokondriyal disfonksiyon meydana gelir. Bu durum membran transition potansiyelinin çökmesine neden olarak nekroz oluşturur. Söz konusu mekanizmalar son yıllarda üzerinde en çok durulan konular olup ancak henüz tam olarak açıklanamamıştır. Parasetamolün muhtemel hepatotoksik etkisi özet olarak aşağıdaki mekanizmalarla açıklanmaktadır Sitokrom p450 enzimleriyle reaktif metabolit NAPQI oluşur. NAPQI glutatyonu tüketerek proteinlere kovalent bağlanır. 2- Glutatyonun kaybı ve hepatositlerde nitrojen ve oksijen radikallerinin artmasıyla hücreler nekrotik değişikliğe giderler. Bu etki özellikle glutatyon kullanan enzimler açısından önem taşımaktadır. 3- Artan oksidatif stres kalsiyum dengesinin bozulmasına ve mitokondri membran permeabilite transisiyona (MPT) neden olur. 4- Mitokondriyal MPT; oksidatif stres, mitokondriyal membran potansiyelinin kaybı ve ATP sentez gücünün azalmasıyla oluşur. 5- ATP nin kaybı ise hücreyi nekroza götürür. 32
41 Şekil 8: Parasetamolün hepatik nekroz yapıcı mekanizması 48 Parasetamole bağlı hepatotoksisitede serbest radikallerin büyük rolü vardır. Bu karşın az miktarda verilen parasetamolün serbest radikallerin indüklediği beyin toksisitesine karşı serbest radikalleri inhibe 33
42 ederek koruyucu etki gösterdiği belirtilmiştir. 49 NAPQI nın düşük dozlarda glutatyonla reaksiyonunu glutatyon-s-transferaz katalizler. 50 Yüksek miktardaki NAPQI ise glutatyonu tüketir. NAPQI nın glutatyonu tüketmesi oksidatif hasarın da başlangıcı sayılır. NAPQI proteinlere bağlanmasıyla mitokondriyal disfonksiyon görülür, solunum inhibe olur, hepatik ATP düzeyleri düşer, mitokondriyal oksidatif stres meydana gelir ve peroksinitrit formasyonları oluşur. 51 Süperoksit dismutaz ve glutatyon peroksidaz antioksidan sistemin başlıca iki enzimidir. SOD, süperoksit radikallerini GSHPx in substratı olan hidrojen peroksite dönüştürür. GSHPx ise hidrojen peroksitin suya dönüşümünü katalizler. Ancak parasetamole bağlı ilaç toksisitesinde söz konusu enzimlerin durumu tartışmalıdır. Son yıllarda antioksidan enzimlerin parasetamol toksisitesindeki koruyucu etkileri üzerinde çalışmalar yoğunlaşmıştır. Yapılan çalışmalar SOD ve GSHPx in olmadığı (knockout) durumlarda hepatik hasara karşı daha dirençli olunduğu şeklindedir. SOD - / - (SOD knockout) farelerle doğal ırk farelerin APAP toksisitesine karşı etkilerinin incelendiği çalışmada SOD - / - farelerin APAP toksisitesine karşı daha dirençli oldukları görülmüştür. SOD süperoksit iyonlarının temizlenmesine görev alır. SOD enzimi olmadığında hücrede süperoksit birikimi olur. Bu iyonlar NAPQI nın oluşumunu katalizleyen CYP2E1 enzimini down regüle eder. Böylece reaktif metabolitin oluşumu önlenmiş olur. Ayrıca CYP2E1 in inhibisyonu protein nitrasyonunu da önler. 52 Parasetamolün toksik olmayan dozlarda bile tekrarlanması sitokrom p450 enzim sistemini indükleyebilir ve aynı enzim sistemini kullanan ilaçlarla beklenmeyen ilaç-ilaç etkileşimlerine neden olabilir. 53 Peroksinitrit parasetamol hepatotoksisitesinde kritik bir mediatördür. Parasetamolden hemen sonra glutatyon verilmesi peroksinitrit oluşumunu, mitokondriyal oksidatif stresi ve hücre hasarını önler. SOD ve GSHPx, ilaçların neden olduğu oksidatif streste aynı etkiyi 34
43 göstermemektedirler. Asetaminofenin indüklediği hepatik hasarın karşılaştırıldığı bir çalışmada SOD - / - ve GSHPx - / - gruplarından SOD - / -, hepatik hücre ölümünü engellerken GSHPx - / - daha az koruma sağlamıştır. 54 Başka bir çalışmada GSHPx - / - ve hem GSHPx - / - hem de SOD - / - gruplarının fare primer hepatositlerinde asetaminofen toksisitesi üzerine etkisine bakılmıştır. Gruplara APAP ve NAPQI verilmiştir. Doğal ırka kıyasla GSHPx - / - ve GSHPx - / - SOD - / - grubunun APAP ın indüklediği hücre ölümüne karşı daha dirençli oldukları fakat NAPQI nın indüklediği hücre hasarına karşı daha az dirençli oldukları görülmüştür. Gruplar arasında glutatyon-s-transferaz aktiviteleri açısından fark bulunmamıştır. Sonuçta fare primer hepatositlerinde GSHPx - / - SOD - / - grubunun parasetamol toksisitesine karşı dayanıklılığının arttığı belirtilmiştir. 55 Mirochnitchenko ve ark. transgenik farelerde insan SOD, glutatyon peroksidazın intraselüler (GPI) ve ekstraselüler (GPP) formlarını kullanarak yaptıkları çalışmada SOD ve GPP transgenik farelerde öldürücü doz parasetamole karşı direnç gösterdiklerini belirtmişlerdir. Buna karşın GPI grubunda kontrol grubuna kıyasla parasetamole daha hassas olduklarını gözlemlemişlerdir. Yine bu grupta glutatyonun yenilenmesi gecikirken GPP grubunda çok az glutatyon deplesyonu olduğu ve glutatyonun yerine çok hızlı konulduğunu belirtmişlerdir. Bu sonuçlara göre glutatyon peroksidazın iki formunun zıt etki gösterdiği sonucuna varmışlardır. 56 Knight ve ark. parasetamol toksisitesinde peroksinitritin rolünü araştırmak amacıyla yaptıkları çalışmada parasetamol vermelerinden 0-3 saat sonrasına kadar değişen zamanlarda glutatyon vermişlerdir. 0. saatte verilen glutatyonun mitokondriyal oksidatif stresi tamamen engellediğini belirtmişlerdir. 1,5-2,25 saat sonra verilen glutatyonun hepatik ve mitokondriyal glutatyonu restore ettiği fakat okside glutatyon oluşumunu önleyemediğini göstermişlerdir. 3 saat sonra verilen glutatyonun ise etkisiz olduğunu belirtmişlerdir. Burada yeni sentezlenen glutatyonun peroksinitriti temizleyici rol oynadığını fakat oksidatif stresi engellemediği sonucuna varmışlardır. 57 Çiğremiş ve ark. parasetamol 35
44 toksisitesinde antioksidan sistemin regülasyonunu araştırmak amacıyla tavşanlar üzerinde 250 mg/kg APAP vererek yaptıkları çalışmada hepatosellüler nekroz, glutatyon deplesyonu ve nitrotirozin oluşumu gibi toksik değişiklikler olmasına rağmen antioksidan enzim sisteminde önemli değişiklik saptamamışlardır. 58 Yapılan çalışmalar parasetamol toksisitesinde serbest radikallerin ve antioksidan enzimlerin üzerinde yoğunlaşmıştır. Özellikle peroksinitrit oluşumu büyük anlam ifade etmektedir. Çalışmalar peroksinitritin APAP toksisitesindeki önemini vurgulamaktadır Antioksidan enzimlerin olmaması da toksisiteyi önlemektedir. Ancak antioksidan enzimlerin olmaması APAP toksisitesine karşı koruma sağlarken hücre oksidanların saldırısına maruz kalmaktadır Parasetamol Toksisitesinde Klinik ve Medikal Tedavi Parasetamole bağlı toksisite dört aşamada değerlendirilir. İlk aşama parasetamolün alındığı ilk 24 saat olup bulantı, kusma, karın ağrısı gibi belirtiler görülebilmekle beraber hiçbir belirti görülmeyebilir. İkinci aşamada (25-72 saat) protrombin zamanı uzar, transaminazlar yükselir. Üçüncü aşama ise (73-96 saat) karaciğer fonksiyon bozukluğunun en fazla olduğu safhadır. Transaminazlar çok yüksek düzeylere çıkabilir. Ölüm çoklu organ yetmezliğine bağlı olarak veya karaciğer yetmezliğinin ciddi komplikasyonları sonucu meydana gelir. Son aşamada ise iyileşen hastalarda karaciğer fonksiyonları normale döner. İyileşme parasetamol alımından sonra iki hafta kadar sürer. Klinik semptomlar kaybolur
45 Tablo 5: Parasetamol zehirlenmesinde belirti ve bulgular 64 Zehirlenme Evreleri Belirti ve Bulgular 1.EVRE (İlk 24 saat) Hastada belirti olmayabilir İştahsızlık, bulantı, kusma, halsizlik Transaminazlarda yükselme 2.EVRE (25-72saat) İştahsızlık, bulantı, kusma Karnın sağ üst kadranında ağrı Transaminazlarda yükselme Bilurubin düzeyinde artma Protrombin zamanında uzama Böbrek işlevlerinde bozulma 3.EVRE (73-96 saat) Fulminan karaciğer yetmezliği (sarılık, pıhtılaşma bozukluğu, hepatik ensefalopati) Çoklu organ yetmezliğine bağlı ölüm 4.EVRE Karaciğer fonksiyonları normale döner Parasetamol zehirlenmesinde belirgin semptomlar görülmediği için eğer yapılabiliyorsa hastanın öyküsü dinlendikten sonra serum parasetamol düzeyi ölçülerek tanı konabilir. Parasetamol alımından sonra gelişen toksisite riskinin en doğru belirlenebileceği yöntem 4 saat sonra kanın parasetamol düzeyinin belirlenmesidir. Plazma parasetamol konsantrasyonu Rumack-Matthew nomogramına göre değerlendirilir. Bu sonuca göre uygulanacak tedavi belirlenebilir hatta bazı durumlarda karaciğer transplantasyonu için hazırlıklar yapılabilir. Parasetamol toksisitesinden en çok etkilenen organlar karaciğer ve böbreklerdir. Bu 37
46 sebeple karaciğer ve böbrek fonksiyonları dikkatle takip edilmelidir. Parasetamol nedenli hepatotoksisite karaciğer enzimlerinin ciddi miktarlarda yükselmesi ve protrombin zamanının uzaması ile karakterizedir. Parasetamol toksisitesinde öncelikle hastanın solunum ve dolaşım fonksiyonlarına bakılır. Gerekiyorsa temel ve ileri yaşam desteği verilir. Protrombin zamanının uzamasına bağlı kanama varsa kas ya da ven içine K1 vitamini verilir. 64 Parasetamol zehirlenmesinde gastrointestinal dekontaminasyon, aktif kömür ve oral asetilsistein ve antidot tedavisi gibi yöntemler uygulanmaktadır. Parasetamol ağız yoluyla toksik dozda alındıktan ilk 1 saat içinde mide yıkanabilir ve aktif kömür verilebilir. Fakat aktif kömür kullanımı NAS emilimini azaltabilmektedir. 64 Bu sebeple eğer NAS verilecekse aralarında en az 1-2 saat fark olmalıdır. 30 adet rat deneye alınarak yapılan bir çalışmada 500 mg/kg/doz parasetamol oral olarak verilmiştir. 2 saat sonra ratlara mide lavajı ve aktif kömür uygulaması yapılmıştır. Yapılan mide yıkama ve aktif kömür kullanımının tedavide etkin olmadığı ve bu iki yaklaşımın birbirlerine üstünlüklerinin bulunmadığı kanısına varılmıştır. 65 Parasetamol toksisitesinde en yaygın kullanılan yöntem ise antidot tedavisidir. Parasetamol zehirlenmesinde en önemli nokta glutatyonun tükenmesidir. Glutatyon hepatositlerden geçemediği için glutatyonu yerine koymak yerine sentezinin hızlandırılması gerekmektedir. Bu yüzden kullanılacak antidotların glutatyon sentezine katkı yapacak özellikte olmaları gerekir. Parasetamol zehirlenmesinde kullanılan bazı antidotlar NAS, sisteamin ve metiyonin dir. 38
47 2.5. N-ASETİLSİSTEİN NAS, L-sisteinin N-asetillenmiş öncülüdür. NAS mukolitik bir ajan olarak tanımlanmıştır fakat daha sonra antioksidan etkisi keşfedilerek parasetamol toksisitesinde antidot olarak kullanılmaya başlanmıştır. 66 Molekül formülü C 5 H 9 N0 3 S ve molekül ağırlığı g/mol dür. %20 lik solüsyonunun ph si ve solüsyon hiperosmolardır. Yarılanma ömrü 2-6 saattir. Oral ve intravenöz formları vardır. Oral NAS alındıktan sonra hızlıca emilir, karaciğerde ilk geçiş metabolizmasına uğrar. Biyoyararlanımı düşüktür ve %20-30 u değişmeden idrarla atılır. İntravenöz kullanım için hazırlanan NAS kontrollü oda sıcaklığında bozulmadan 24 saat stabil kalabilir. NAS, içerdiği sülfhidril grubundan dolayı bozuk yumurta gibi kokar. 66 Şekil 9: N-Asetilsisteinin kimyasal yapısı NAS, bir sistein ve glutatyon prekürsörüdür. Güçlü bir antioksidan olan NAS proteinlerdeki disülfid bağlarını indirger, serbest 39
48 radikalleri temizler ve metalleri bağlar. En önemli farmakolojik etkisini parasetamol toksisitesinde sistein ve glutatyonu yenileyerek gösterir. 66 NAS kimyasal yapı olarak sisteine benzer. Fakat asetil grubunun olması sisteine oranla tiyol reaktivitesini azaltmaktadır. NAS ın daha az toksik olması, oksidasyona karşı daha hassas olması ve suda iyi çözülebilmesi, sistein verilmesinden daha iyi bir sistein kaynağı olmasını sağlamaktadır. 67 NAS ve glutatyon serbest radikalleri direkt temizleyici etki gösterirler. Hipokloröz asidi ve hidroksil radikalini ortadan kaldırırken hidrojen peroksit ile daha yavaş reaksiyona girmektedir. 68 NAS güçlü bir radikal temizleyicidir ancak bu etkisi SOD, CAT, GSH-Px gibi antioksidan enzimlerin etkisinden daha düşüktür. 69 Parasetamol toksisitesinin meydana gelmesinde hepatositlerde radikallerin birikmesi de sorumludur. Normal şartlarda glutatyon tarafından ortadan kaldırılan radikaller glutatyonun tükenmesiyle hepatositlerde birikir ve lipid peroksidasyonuna neden olur. Ancak parasetamol toksisitesinde lipid peroksidasyonu ve serbest radikaller hasarın tek sorumluları değildir. Parasetamole bağlı ilk hepatotoksisitenin ortaya çıkmasından kısa bir süre sonra Mitchell ve ark. sisteinin koruyucu etkisinin bulunduğunu keşfetmişlerdir. Fakat NAS ın parasetamol hepatotoksisitesinde antidot olarak kullanılmasını ilk kez Prescott ve Matthew 1974 yılında önermişlerdir yılında da Prescott parasetamol zehirlenmesinde NAS ı hastalara vermiş ve başarılı sonuçlar almasıyla NAS parasetamol toksisitesinde kullanılmaya başlanmıştır. 71 Parasetamol toksisitesinde NAS ın oral ve intravenöz formu kullanılmaktadır. İntravenöz (iv) NAS çoğu ülkede yaygın olarak kullanılırken Amerika da FDA nın onayı ile 2004 yılında kullanılmaya başlanmıştır. Toksik dozlarda alınan parasetamolün oluşturduğu NAPQI 40
49 glutatyonun detoksifikasyon kapasitesinin aşılmasına neden olur. Glutatyonun %70 nin tükenmesi durumunda toksik etki gözlenir. NAS, parasetamol toksisitesi tedavisinde glutatyon prekürsörü olarak görev yapar. Glutatyonun yeniden sentezlenerek reaktif NAPQI nın detoksifikasyonunu sağlar. Ayrıca NAS, içerdiği tiyol grubuyla hücrede oluşan serbest radikallerin ortadan kaldırılmasında antioksidan olarak görev alır. Çalışmalar ilk 8 saatte verilen NAS ın hepatotoksisiteyi önlediğini göstermektedir. NAS ın koruyucu etkisi birçok çalışmada gösterilmiştir. 72,73 İlk 8 saatte verilen NAS ın parasetamol toksisitesini ortadan kaldırdığını gösteren çalışmalara rağmen erken NAS verilmesi durumunda dahi toksisite gelişebilmekte hatta ölümlere neden olabilmektedir. 74 Doyon ve Klein Schwartz ın parasetamol zehirlenmesi şikayetiyle ilk 8 saatte gelen 77 hasta üzerinde yaptıkları çalışmada hastalara uyguladıkları en az 21 saatlik ıv NAS tedavisinde hastaların 4 tanesinde hepatotoksisite ortaya çıkmıştır. Bu 4 hastadan biri hayatını kaybederken bir hasta da karaciğer transplantasyonuna gereksinim duymuştur. Ölen hastada ıv NAS tedavisine 4. saatten sonra başlandığı ve plazma APAP konsantrasyonunun nomogramda belirtilen tedavi çizgisinin üzerinde olduğu belirtilmiştir. Bu hastaya ara verilmeden ıv NAS verilmesine rağmen hastaneye yattıktan 7 gün sonra hayatını kaybetmiştir. Otopsi sonucuna göre karaciğerde sentrilobüler nekroz, böbreklerde fokal tubüler nekroz ve akut bronkopnömoni görüldüğü saptanmıştır. 74 Yang ve arkadaşlarının uzun süre NAS kullanımının etkisini araştırmak için yaptıkları çalışmada 72 saat NAS (12 saatte bir 100 mg/kg NAS, toplam 72 saat) uyguladıkları ratlarla kontrol grubunu kıyasladıklarında serum transaminazlarının anlamlı derecede yüksek 41
50 bulunmuştur. Histopatolojik incelemede ise periportal alanda hepatosit vakuolizasyonu görülmüş ve uzun süreli NAS kullanımının karaciğer rejenerasyonunu geciktirdiği sonucuna varılmıştır. 75 Saito ve ark. parasetamolden sonra glutatyon ve NAS vererek yaptıkları çalışmada ikisinin de peroksinitrit oluşumu ve DNA fragmantasyonuyla ortaya çıkan karaciğer hasarını büyük oranda engellediğini göstermişlerdir. ATP düzeylerini de ölçtükleri çalışmada NAS ve GSH nin parasetamol toksisitesinde, peroksinitrit ve serbest oksijen radikallerini temizleyerek ve mitokondriyal enerji metabolizmasını destekleyerek etki gösterdiğini belirtmişlerdir. 76 Görüldüğü üzere genel olarak NAS ın güvenli bir antidot olmasının yanında farklı sonuçlar da ortaya çıkmaktadır. Bu da NAS üzerinde neden bu kadar fazla araştırma yapıldığını açıklamaktadır. Yapılan çalışmalar oral ve iv NAS tedavilerinin arasında bir fark olmadığını göstermektedir. Oral NAS nadiren anjiyoödemle ilişkilendirilirken daha çok, kötü tadı nedeniyle bulantı ve kusma şikayetlerine neden olur. Buna karşın iv NAS tedavisinde şikayetler daha ciddidir. Yetişkin iv NAS dozu verilen çocuklarda hiponatremi görülebilir. İv NAS anafilaktoid reaksiyonlara neden olur. 77 Iv NAS alan hastaların %3-6 sında anafilaktoid reaksiyonlar görülürken oral NAS alan hastalarda bu oran çok daha düşüktür. Anafilaktoid reaksiyonların muhtemelen ilk dk meydana geldiği düşünülmektedir. 78 Anafilaktoid reaksiyonlara bağlı birkaç ölüm meydana geldiği belirtilmiştir. 79,80 Araştırmacılar ölümlerin meydana gelmesinin iv NAS tedavisi sırasında yapılan kişisel hatalardan da kaynaklanabileceğini bildirmiştir. 42
51 NAS sadece parasetamol toksisitesinde kullanılmamaktadır. 81 Solunum sistemi hastalıklarında ortaya çıkan inflamasyonun iyileştirilmesinde kullanılmaktadır. Balgamın viskozitesini ve öksürüğün şiddetini azaltır. 82 Ayrıca cerrahi işlem sonrasında oluşabilecek komplikasyonları önler. NAS, nitrik oksitin üretilmesi sırasında vazodilatör olarak görev alır. 82 NAS, birçok ksenobiyotik maddenin oluşturduğu radikallere karşı koruyucu etki gösterir. 83 Kemoterapi gören hastalarda ifosfamidin neden olduğu nefrotoksisite ciddi bir yan etkidir. NAS ratlarda ifosfamidin neden olduğu nefrotoksisiteyi engellemektedir. 84 NAS ın koruyucu etkisinin bilinmesi sebebiyle yeni antidotların bulunması için bu maddelerin etkileri NAS ile kıyaslanarak çalışmalar yapılmakta ve alınan sonuçlara göre NAS a alternatif olup olmayacağı tartışılmaktadır. Bunlardan bazıları taurin, hipotaurin, 4- metilpirazol ve S-adenozil-L-metiyonin dir. Yapılan bir çalışmada NAS, taurin ve hipotaurinin eşit miktarlarda verildiklerinde APAP toksisitesi sebebiyle oluşan oksidatif stres ve hepatosellüler hasarı eşit derecede azalttığı saptanmıştır. Taurin ve hipotaurin GSH biyosentezinde görev almamalarına rağmen, NAS gibi hücredeki GSH depolarını koruyarak ve GSH/GSSG dengesinin korunmasını sağlayarak etki göstermişlerdir. 85 İnsanlarda metanol ve etilen glikol toksitesinde kullanılan 4- metilpirazol P450 sistemindeki izoenzimlerden P450 2E1 in inhibisyonuna neden olur. Bu amaçla parasetamol toksisitesi üzerine etkisi araştırılan çalışmada NAS ile 4-metilpirazol kıyaslandığında etkinlik açısından aralarında anlamlı bir fark görülmemiştir. Bununla birlikte 4-metilpirazolün 43
52 kullanımının daha kolay olduğu ve parasetamol toksisitesi için bir antidot olarak kullanılabileceği belirtilmiştir. 86 S-Adenozil-L-Metiyonin (SAMe) transmetilasyon ve transsülfürasyon reaksiyonlarında görev alır. SAMe nin alkol ve karbon tetraklorür gibi hepatoksinlerin etkilerini azalttığı bilinmektedir. Terneus ve ark. SAMe ile NAS ın eşit dozlarını kullanarak (1,25 mmol/kg) yaptıkları çalışmada parasetamol toksisitesini birbirlerine yakın derecede azalttıklarını göstermişlerdir. NAS ile benzer etkiyi göstermesi SAMe nin APAP toksisitesinde bir antidot olabileceği belirtilmiştir. 87 NAS ın dozu ve verilme şekli konusunda farklı fikirler vardır. Prescott ve ark. yaptığı 20 saatlik 300 mg/kg iv NAS uygulamasının parasetamol zehirlenmesi şikayetiyle ilk 8 saatte başvuran hastaların tamamında karaciğer toksisitesini önlediğini göstermişlerdir. 88 Smilkstein ve ark. ise hastalara toplam 72 saat oral NAS vererek yaptıkları çalışmada uyguladıkları tedavinin Prescott un 20 saatlik tedavisi kadar etkili olduğunu ve 10 saatten fazla bir sürede başvuran hastalarda oral NAS ın iv NAS tan daha etkili olduğunu belirtmişlerdir. Bunun nedeni olarak da uyguladıkları protokolde NAS dozunun daha fazla olması ve tedavinin daha uzun sürmesi olarak belirtmişlerdir
53 Tablo 6: Parasetamol zehirlenmesinde NAS ın uygulama protokolleri* Ağız yoluyla uygulama** Doz Yükleme 140 mg/kg Sürdürme 70 mg/kg 4 saat arayla 17 kez (72 saatte toplam 1330 mg/kg) Ven içine 20 saatlik uygulama Doz Yükleme: 150 mg/kg/15 dakikada Sürdürme 50 mg/kg/4 saatte 100 mg/kg/16 saatte (20saatte toplam 300 mg/kg) Ven içine 48 saatlik uygulama Doz ( 1:5 seyreltilir) Yükleme: 140 mg/kg/1 saatte Sürdürme 70 mg/kg/1 saat 4 saat arayla 12 kez (48 saatte toplam 980 mg/kg) Veriliş şekli Veriliş şekli*** Veriliş şekli*** % 10-% 20 lik NAC % 0,9 serum fizyolojik veya % % 5 dekstroz içinde solusyonları, meyve suyu 5 lik dekstroz içinde içinde % 5 lik hale getirilerek * Alerjik reaksiyon görülebilir. ** Aktif kömürle birlikte kullanılmamalıdır. *** Çocuklarda NAS 40 mg/ml solüsyon haline getirilerek uygulanmalıdır. Metiyonin, NAS gibi hücre koruyucu mekanizmada etkilidir, hücre içi glutatyonun yenilenmesinde görev alır. Alınan metiyonin sisteine dönüşerek glutatyon sentezine katılır. Iv NAS, metiyoninden daha güçlü etkilidir. Metiyonin daha çok, NAS ın etkili olmadığı ya da NAS ı tolere edemeyen hastalarda kullanılır. 90 Metiyonin yetişkinlerde oral (4x2.5 g 12 saat) olarak verilir. 6 yaş üzeri çocuklarda yetişkinlerle aynı şekilde verilirken 6 yaş altı çocuklarda (1 g, her 4 saatte) maksimum 4 g olarak verilir. Metiyonin in şizofren hastalarda ve karaciğer hastalarında dikkatli kullanımı tavsiye edilmektedir. 90 Parasetamol toksisitesi tedavisinde kullanılan bir başka antidot sisteamindir. NAS, sisteamin ve metiyoninin koruyucu etkilerinin karşılaştırıldığı çalışmada NAS ın daha etkili olduğu, en az etkili olanın 45
54 metiyonin olduğu görülmüştür. Yine bu çalışmada sisteaminin şiddetli yan etkileri olduğu, metiyoninin ise toksik olabileceği için NAS kullanımının daha doğru olduğu vurgulanmıştır. Toksisitenin ilk görüldüğü yıllardan bu yana en uygun antidotun bulunabilmesi için yapılan çalışmaların sonucunda en az yan etkili olması ve güçlü etkisi sebebiyle NAS tercih edilmiştir. 91,92 Bununla birlikte NAS a alternatif olabilecek ve NAS tan daha az yan etki gösteren ya da hiç yan etkilere sahip olmayan bir antidot bulunması için çalışmalar yapılmaktadır. 46
55 3. MATERYAL VE METOD Bu çalışma Gazi Üniversitesi Tıp Fakültesi Hayvan Deneyleri Yerel Etik Kurulu nun onayı ile (Onay no: ) Gazi Üniversitesi Laboratuvar Hayvanları Yetiştirme ve Deneysel Araştırmalar Merkezi nde (GÜDAM) gerçekleştirildi. Çalışmada kullanılan ratlar GÜDAM dan temin edildi. Ağırlıkları g arasında değişen toplam 36 adet erkek Wistar-Albino rat üzerinde planlanan çalışmada, denekler 6 gruba ayrıldı. Çalışmada parasetamol ezilip toz haline getirildikten sonra serum fizyolojik (sf) ile sulandırılarak oral gavaj yoluyla verildi. N- Asetilsistein ise intraperitonel (i.p) verildi Çalışmada Kullanılan İlaçlar Parasetamol (APAP) (Vermidon 500 mg - Sandoz ) N-Asetilsistein (NAS) ( Asist 300 mg 3ml ampul- Bilim İlaç Şirketi ) 3.2. Çalışma Grupları Grup 1 (n=6): Kontrol grubu kabul edilerek i.p serum fizyolojik verildi. Grup 2 (n=6): 1000 mg/kg APAP verildi. Grup 3 (n=6): 400 mg/kg i.p NAS verildi. Grup 4 (n=6): 1000 mg/kg APAP uygulamasını takiben 30 dakika sonra 400 mg/kg i.p NAS verildi. Grup 5 (n=6): 1000 mg/kg APAP uygulamasını takiben 30 dakika ve 12 saat sonra 400 mg/kg i.p NAS verildi. Grup 6 (n=6): 1000 mg/kg APAP uygulanmadan 30 dakika önce 400 mg/kg i.p NAS verildi. 47
56 Son uygulamadan 24 saat sonra ratlara anestezi verilerek kanları alındı rpm de kanlar 5 dakika santrifüj edildi. Serumlar alınarak -80 derecede çalışma zamanına kadar saklandı. Organlar serum fizyolojik içinde yıkanıp alüminyum folyoya sarılarak sıvı azot içerisinde çalışmanın sonuna kadar bırakıldı. Bütün ratların çalışılacak organları alındıktan sonra organlar sıvı azottan çıkarılarak -80 derecede çalışma gününe kadar saklandı. Organların bir kısmı da histopatolojik inceleme için, formaldehit içerisine konularak Ankara Eğitim ve Araştırma Hastanesi Patoloji Bölümü ne gönderildi. Analiz günü çalışılacak parametreler için karaciğer dokuları ayrı ayrı porsiyonlara ayrıldı. Heidolph DIAX900 marka homojenizatörle 1/5 oranında serum fizyolojik içinde dakika homojenize edildi. Homojenatlar santrifüj edilerek süpernatantları ayrıldı. Bu işlem bütün parametreler için ayrı ayrı uygulandı. Dokuların Süperoksit dismutaz, Katalaz, Glutatyon peroksidaz ve Glutatyon-S-transferaz aktiviteleri ve MDA düzeyleri spektrofotometrik (Schimadzu, UV 1601) olarak ölçüldü. AST ve ALT enzimleri ise otoanalizörde (Roche Moduler P 800) çalışıldı Kullanılan Materyaller Homojenizatör (Heidolph DIAX 900) Santrifüj (Hermle Z 380 K) Hassas terazi (Schimadzu, Libror, AEG 220) Spektrofotometre (Schimadzu, UV 1601) Vorteks (Heidolf Reox 2000) ph metre (Jenway) Su banyosu Otomatik pipetler ve pipet uçları Cam deney tüpleri ve diğer malzemeler 48
57 3.4. Yöntemler 1-Karaciğer Dokusunda Malondialdehit (MDA)Tayini Malondialdehit tayini Van Ye TM ve arkadaşlarının tarif ettiği metoda göre çalışıldı. 93 Metodun prensibi: İki mol TBA (tiyobarbitürik asit) asidik ortamda ve ºC sıcaklıkta bir mol MDA ile birleşerek mor renkli TBA-MDA kompleksini oluşturur. Bu kompleksin verdiği absorbans 532 nm de spektrofotometrik olarak ölçülür. Şekil 11. TBA-MDA kompleksi oluşumu. Şekil 10: TBA-MDA kompleksi oluşumu Kullanılan Reaktifler Fosfat Tamponu : 100 mm, ph:6 Na 2 HPO 4 /KH 2 PO 4 % 20 lik TCA çözeltisi % 1 lik TBA çözeltisi MDA standardı: 1,1,3,3-Tetraetoksi propan standart çözelti olarak kullanıldı. 1,1,3,3-Tetraetoksi propandan önce 10 mm lık stok çözelti hazırlandı, stok çözeltiden uygun seyreltmelerle 10, 25, 50, 75 ve 100 µm lık standart çözeltiler hazırlanarak standart grafik çizildi. 49
58 Absorbans Absorbans=f (Konsantrasyon) grafiğinin eğiminden de numunelerdeki MDA miktarları hesaplandı. Sonuçlar nmol/mg.protein olarak ifade edildi. Deneyin Yapılışı: Doku örneklerinde MDA miktarları ölçümü için, dokular 1/4 oranında serum fizyolojik içerisinde dakika 4000 devirde homojenize edildi. Ham homojenat 5000 rpm de 10 dakika santrifüj edilerek süpernatantlar alındı. Her bir numune için kör çalışıldı. Numune tüplerine tampon çözelti, etanol, TBA, TCA ve numune/standart eklenirken, kör tüplerine TBA hariç diğerleri eklenerek hazırlandı. 60 dakika kaynar su banyosunda ( ºC) bekletildikten sonra çeşme suyu altında soğutuldu, 5000xg de 20 dakika santrifüj edildi. Süpernatantları ayrıldı. Daha sonra kör tüplerine TBA eklendi iyice karıştırıldı ve 532 nm de her bir tüpün absorbansı distile suya karşı okundu. MDA Standart Grafiği y = 0,06 X 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0, [MDA] μm Grafik 1: MDA Standart Grafiği 50
59 2-Karaciğer Dokusunda Süperoksid Dismutaz (SOD) Aktivitesi Tayini Karaciğer doku örneklerinde SOD aktivitesi Durak İ ve arkadaşlarının tarif ettiği metoda göre çalışıldı. 94 Metodun prensibi: Nitroblue tetrazolium un (NBT) süperoksit üreticisi olan ksantin-ksantin oksidaz sistemi tarafından indirgenmesi esasına dayanmaktadır. Kullanılan reaktifler Ksantin (0.30mM) NBT (150μM) Na 2 CO 3 (400mM) BSA (1g/l) XO (167U/l) CuCl 2 (8mM) Deneyin yapılışı: Numune tüplerine ölçüm reaktifi, numune ve ksantin oksidaz enzimi; kör tüplerine ise ölçüm reaktifi ve ksantin oksidaz enzimi konuldu. Tüpler 25 C da 20 dakika inkübe edildi. İnkübasyondan sonra numune tüplerine CuCl 2, kör tüplerine ise CuCl 2 ve numune eklendi. İyice karıştırıldıktan sonra her bir tüpün absorbansı 560 nm de distile suya karşı okundu. Sonuçlar IU/mg. protein olarak verildi. İnternasyonel ünite (1 enzim ünitesi,iu) optimal şartlarda 1mikromol substratı 1 dakikada ürüne dönüştüren enzim aktivitesidir. 51
60 3-Karaciğer Dokusunda Glutatyon Peroksidaz (GSH-Px) Aktivitesi Tayini: GSH-Px aktivitesi Paglia DE ve arkadaşlarının metoduna göre çalışıldı. 95 Metodun prensibi: 340 nm de NADPH ın absorbans değişimine dayanmaktadır. Enzim aktivitesi ise NADPH ın ε değerinden (6.22 μmol/ml) yararlanılarak hesaplandı. Kullanılan Reaktifler: GSH: (150 mm) ; NADPH: (3mM); H 2 O 2 : (100mM); NaN 3 : (2M); Fosfat tamponu (ph: 7,0; 50 mm): GSH-red: Sıvı enzimden (NH 4 ) 2 SO 4 ile seyreltilerek kullanılır. Deneyin yapılışı: Numune tüplerine Fosfat tamponu+5mm EDTA, NaN 3, GSH, NADPH, GSH-red ve numune konuldu. Kör tüpüne ise H 2 O 2 hariç diğer reaktifler konuldu. 340 nm de suya karşı sıfırlandıktan sonra körün absorbansı ve H 2 O 2 ilave edilir edilmez numunedeki absorbans azalması 0.,1.,2.,3. dakikalarda okundu. Sonuçlar IU/mg. protein olarak verildi. 52
61 4- Karaciğer Dokusunda Katalaz Aktivitesinin Ölçümü: Doku örneklerinde Katalaz aktivitesinin ölçümü Aebi H nın metoduna göre yapıldı. 96 Metodun prensibi: 240 nm de katalaz tarafından yıkılan hidrojen peroksitin absorbans değişiminin izlenmesi esasına dayanmaktadır. Kullanılan reaktifler Fosfat tamponu(50mm,ph=7) Tamponlanmış H 2 O 2 çözeltisi Deneyin yapılışı: Tampon çözelti ile sıfır ayarı yapılmış spektrofotometreye içerisinde tamponlanmış H 2 O 2 çözeltisi bulunan küvet konuldu. Absorbans değişimi bir süre takip edildi. Daha sonra numune ilave edildi, küvet karıştırılarak numunenin absorbansı 240 nm de 3-5 dakika takip edildi. Lineer olan bölge hesaplamada kullanıldı. Sonuçlar IU/mg.protein olarak verildi. 5- Karaciğer Dokusunda Glutatyon-S- Transferaz Tayini: Glutatyon-S-Transferaz aktivitesi tayini Habig WH ve arkadaşlarının tarif ettiği metoda göre çalışıldı. 97 GST 1-Cloro-2,4-dinitrobenzen (CDNB) + GSH S-2,4-dinitrofenilglutatyon (DNPG) + H + + Cl - 53
62 Yukarıdaki reaksiyon sonucu oluşan DNPG bileşiğinin 340 nm de absorbans artışı takip edilmektedir. Reaktifler 100 mm. ph:6 fosfat tamponu CDNB (1-Kloro 2,4-Dinitrobenzen): 25 mm, saf etanolde çözüldü. GSH:50 mm (tamponda çözüldü) Deneyin Yapılışı: Numune ve kör tüplerine fosfat tamponu, CDNB, numune eklenip iyice karıştırıldı. 340 nm de köre karşı sıfır ayarı yapıldıktan sonra numunedeki absorbans değişimi 1-3 dakika takip edildi. Daha sonra küvete redükte glutatyon (GSH) eklendi ve absorbans değişimi 3 dakika boyunca takip edildi. GST aktivitesi DNPG un ε katsayısından yararlanılarak hesaplandı (ε: 10 mm -1.cm -1 ). Sonuçlar spesifik aktivite (IU/mg.protein) olarak verildi. 6- Karaciğer Dokusunda Protein Tayini: Homojenat ve süpernatantlardaki protein miktarı Lowry metoduna göre yapıldı. 98 Protein standartı olarak BSA (Sigma) kullanıldı mg/ml konsantrasyon aralığında standartlar kullanılarak standart grafik çizildi ve eğimden numunelerdeki protein miktarı hesaplandı. Sonuçlar mg/ml olarak verildi. 54
63 Absorbans 0,6 0,5 0,4 0,3 0,2 0,1 0 Protein Standart Grafiği y = 2,58X 0 0,05 0,1 0,15 0,2 0,25 Protein (mg/ml) Grafik 2: Protein Standart Grafiği Metodun Prensibi: Alkali ortamda proteinler Cu 2+ ile Cu 2+ - protein kompleksi oluşturarak, Folin-Ciocalteau-Phenol reaktifini redükleyerek mavi-mor renkli ürün oluşturması esasına dayanmaktadır. Rengin koyuluğu ortamdaki protein konsantrasyonuyla doğru orantılıdır. Deneyin Yapılışı: Kör ve numune tüplerine 2.5 ml C reaktifi ve numune tüpüne 10μl süpernatant eklendikten sonra iyice karıştırılarak laboratuvar sıcaklığında 10 dakika bekletildi. Kör ve numune tüplerine 250 μl D reaktifi eklendikten sonra laboratuar sıcaklığında 30 dakika inkübe edildi ve 700 nm de numunelerin absorbansları köre karşı okundu. Sonuçlar standart eğim grafiğinden yararlanılarak hesaplandı. 55
64 3.5. İstatistik: Bütün istatistiksel analizler SPSS 15.0 istatistik programı ile yapıldı. Gruplar arasındaki anlamlılık farkı Mann- Whitney U testi ve Kruskal Wallis analizi ile belirlendi. p<0,05 istatistiksel olarak anlamlı kabul edildi. 56
65 4. BULGULAR Tüm gruplara ait Malondialdehit düzeyleri (nmol/mg.protein), Alanin aminotransferaz (U/L), Aspartat aminotransferaz (U/L), Süperoksit dismutaz (IU/mg.protein), Katalaz (IU/mg.protein), Glutatyon peroksidaz ( IU/mg.protein), Glutatyon-s-transferaz (IU/mg.protein) olarak verilmiştir ve sonuçlar Tablo 7 ve 8 de görülmektedir. Tablo 7: Grupların AST(U/L) ve ALT(U/L) enzim aktiviteleri AST ALT Grup 1 137,7±48,3 75,0±9,7 Grup 2 116,7±25,0 86,0±23,7 Grup 3 100,7±24,3 72,5±13,8 Grup 4 124,5±21,4 78,0±10,3 Grup 5 136,3±95,3 60,0±13,7 Grup 6 124,8±46,6 59,5±8,2 57
66 Tablo 8: Rat Karaciğer dokularına ait ortalama±standart sapma olarak SOD (U/mg protein), GSH-Px (IU/mg protein), GST (miu/mg protein), CAT (IU/ mg protein) enzim aktiviteleri ve MDA (nmol/mg protein) seviyeleri. SOD CAT GSH-Px GST MDA Grup 1 0,87±0,14 57,0±23,7 0,53±0,14 0,02±0,01 0,04±0,02 Grup 2 0,77±0,19 34,9±15,0 0,41±0,08 0,01±0,00 0,03±0,02 Grup 3 1,17±0,24 46,8±6,3 0,54±0,08 0,01±0,00 0,04±0,01 Grup 4 0,88±0,43 40,1±10,6 0,56±0,06 0,01±0,00 0,03±0,01 Grup 5 1,32±0,33 67,3±26,6 0,61±0,07 0,03±0,03 0,04±0,02 Grup 6 1,12±0,12 70,4±8,6 0,50±0,10 0,01±0,00 0,02±0,02 58
67 Tablo 9: Ölçülen parametrelere ait gruplar arası İstatistiksel değerlendirme sonuçları SOD GSHPx CAT GST AST ALT MDA Grup (1-2) Grup (1-3) Grup (1-4) Grup (1-5) Grup (1-6) Grup (2-3) Grup (2-4) Grup (2-5) Grup (2-6) Grup (3-4) Grup (3-5) Grup (3-6) Grup (4-5) Grup (4-6) Grup (5-6) p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,01 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,01 p>0,05 p>0,05 p>0,05 p>0,05 p<0,05 p>0,05 p<0,05 P<0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 P<0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,01 P<0,01 p<0,01 p>0,05 p>0,05 p>0,05 p>0,05 p<0,01 p>0,05 p<0,01 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,01 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 p>0,05 p<0,01 p>0,05 p>0,05 p<0,05 p>0,05 p>0,05 P<0,01 p>0,05 p>0,05 p>0,05 p>0,05 p>0,05 59
68 GSH-Px (IU/mgprotein) SOD (IU/mgprotein) Karaciğer Dokusu SOD Aktiviteleri Sonuçları 1,4 1,32 1,2 1,17 1,12 1 0,8 0,87 0,77 0,88 0,6 Seri 1 0,4 0,2 0 grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 3: Tüm gruplara ait SOD aktiviteleri (IU/mgprotein) ortalama±standart hata olarak verilmiştir. Karaciğer Dokusu GSHPx Aktiviteleri Sonuçları 0,7 0,6 0,5 0,53 0,54 0,56 0,61 0,5 0,4 0,41 0,3 Seri 1 0,2 0,1 0 grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 4: Tüm gruplara ait GSHPx aktiviteleri (IU/mgprotein) ortalama±standart hata olarak verilmiştir. 60
69 CAT (IU/ mgprotein) GST (IU/mgprotein) Karaciğer Dokusu Glutatyon-S-Transferaz Aktiviteleri Sonuçları 0,03 0,03 0,025 0,02 0,02 0,015 0,01 0,01 0,01 0,01 0,01 Seri 1 0,005 0 grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 5: Tüm grupların GST aktiviteleri (IU/mgprotein) ortalama±standart hata olarak verilmiştir. Karaciğer Dokusu Katalaz Aktiviteleri Sonuçları ,3 70, ,9 46,8 40,1 Seri grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 6: Tüm gruplara ait CAT (IU/mgprotein) aktiviteleri ortalama±standart hata olarak verilmiştir. 61
70 AST (U/L) ALT (U/L) Grupların ALT Değerleri , , Seri grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik verilmiştir. 7: Grupların ALT değerleri (U/L) ortalama±standart hata olarak Grupların AST Değerleri ,7 116,7 100,7 124,5 136,3 124, Seri grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 8: Grupların AST değerleri (U/L) ortalama±standart hata olarak verilmiştir. 62
71 MDA (nmol/mgprotein) Karaciğer Dokusu MDA Düzeyleri 0,04 0,04 0,04 0,04 0,035 0,03 0,03 0,03 0,025 0,02 0,02 0,015 Seri 1 0,01 0,005 0 grup 1 grup 2 grup 3 grup 4 grup 5 grup 6 Grafik 9: Tüm gruplara ait karaciğer MDA (nmol/mgprotein) düzeyleri ortalama±standart hata olarak verilmiştir. Grupların SOD aktiviteleri kıyaslandığında kontrol grubu ile 3.grup (yalnızca NAS verilen grup) arasında istatistiksel olarak anlamlı bir artış görülmüştür (p<0,05). Kontrol grubu ile 5.grup (parasetamol verildikten yarım saat ve 12 saat sonra NAS verilen grup) arasında anlamlı bir artış olmuştur (p<0,01). Kontrol grubu ile 6.grup (parasetamolden yarım saat önce NAS verilen grup) karşılaştırıldığında da SOD aktivitesinde anlamlı bir artış gözlenmiştir (p<0,01). 2.grup (yalnızca parasetamol verilen grup) ile 3.grup karşılaştırıldığında anlamlı bir artış olduğu görülürken (p<0,05), 2.grup ve 5.grup arasında da anlamlı bir artış olmuştur (p<0,01). 2.grup ve 6.grup karşılaştırıldığında ise yine anlamlı bir fark görülmüştür (p<0,01). 2.grup ile 3.grubun glutatyon peroksidaz aktiviteleri kıyaslandığında anlamlı bir artış olduğu görülmüştür (p<0,05). 2. ve 4. 63
72 gruplar arasında da anlamlı artış olmuştur (p<0,05). 2.grup ve 5.gruba bakıldığında GSHPx aktivitelerinde anlamlı bir artış olmuştur (p<0,01). 5 ve 6.grupların GSHPx aktivitelerinde ise 6.grupta 5.gruba göre anlamlı bir azalma meydana gelmiştir (p<0,01). Katalaz aktiviteleri değerlendirildiğinde 2.grup ve 5.grup arasında istatistiksel olarak anlamlı artış görülmüştür (p<0,01). 2.grup ve 6.grup arasında anlamlı bir artış olmuştur (p<0,01). 3.grup ve 5.grup arasında anlamlı bir artış görülürken (p<0,05), 3.grup ve 6.grup karşılaştırıldığında anlamlı bir artış görülmüştür (p<0,01). 4.grup ve 5.grup karşılaştırıldığında anlamlı bir artış olmuştur (p<0,05). 4.grup ve 6.grup arasında da anlamlı bir artış olduğu gözlenmiştir (p<0,01). Grupların ALT değerlerine bakıldığında kontrol grubu ve 6.grup arasında istatistiksel olarak anlamlı bir azalma görülmüştür (p<0,05). 2.grup ve 6.grup arasında da anlamlı azalma olmuştur (p<0,05). 4.grup ve 5.grup karşılaştırıldığında anlamlı bir azalma olduğu görülürken (p<0,05). 4.grup ve 6.grup arasında da anlamlı bir azalma olmuştur. (p<0,05). ALT değerleri gruplar arasında en yüksek olarak 2. grupta yani yalnızca parasetamol verilen grupta görülmüştür. En düşük ALT değerleri konjesyon görülen 5 ve 6.grupta belirlenmiştir. AST değerleri karşılaştırıldığında en yüksek değer kontrol grubuna aittir (137,7±48,3). Diğer en yüksek AST değerinin parasetamol verildikten yarım saat ve 12 saat sonra NAS verilen grup olan 5.grupta olduğu görülmüştür (136,3±95,3). En düşük AST değeri yalnızca NAS verilen 3.grupta belirlenmiştir (100,7±24,3). 64
73 Histopatolojik değerlendirme Ratların karaciğerleri alındıktan sonra karaciğerler serum fizyolojik içinde yıkanarak formaldehit içerisine konuldu. Grupların histopatolojik değerlendirmesi Ankara Eğitim ve Araştırma Hastanesi Patoloji Bölümü nde yapıldı. Hematoksilen eozin ile boyanan dokular mikroskopta incelendi. Sonuçlar aşağıdaki tabloda verilmiştir. Tablo 10: Histopatolojik değişiklikler Histolojik Parametreler Hepatosit nekrozu Hepatosit vakuolizasyonu Grup 1 Kontrol grubu Grup mg/kg Grup mg/kg Grup mg/kg APAP+30dk (i.p. APAP NAS sonra 400 salin) mg/kg NAS Sentral ven çevresinde Periportal alanda + Grup 5 Grup mg/kg 400 APAP + 30 mg/kg dk ve 12 NAS+30 saat sonra dk 400 mg/kg sonra NAS 1000 mg/kg APAP İnflamatuar hücre infiltrasyonu Konjesyon
74 Resim 1 (Grup 1: Kontrol grubu) (HE, X20) Resim 2 (Grup 2: Yalnızca Parasetamol verilen grup) (HE, X20) 66
75 Resim 3 (Grup 3: Yalnızca NAS verilen grup) (HE, X20) Resim 4 (Grup 4: Parasetamol verildikten 30 dk sonra NAS verilen grup) (HE, X20) 67
76 Resim 5 (Grup 5: Parasetamol verildikten 30 dk ve 12 saat sonra NAS verilen grup) (HE, X20) Resim 6 (Grup 6: NAS verildikten 30 dk sonra parasetamol verilen grup) (HE, X20) 68
ASETOMİNOFEN ZEHİRLENMELERİ UZ. DR. MEHMET YİĞİT SAĞLIK BİLİMLERİ ÜNİVERSİTESİ HASEKİ EĞİTİM VE ARAŞTIRMA HASTANESİ «
 ASETOMİNOFEN ZEHİRLENMELERİ UZ. DR. MEHMET YİĞİT SAĞLIK BİLİMLERİ ÜNİVERSİTESİ HASEKİ EĞİTİM VE ARAŞTIRMA HASTANESİ « Sunum planı Epidemiyoloji Farmakokinetik Klinik özellikler Tanı Tedavi Sonuç Epidemiyoloji
ASETOMİNOFEN ZEHİRLENMELERİ UZ. DR. MEHMET YİĞİT SAĞLIK BİLİMLERİ ÜNİVERSİTESİ HASEKİ EĞİTİM VE ARAŞTIRMA HASTANESİ « Sunum planı Epidemiyoloji Farmakokinetik Klinik özellikler Tanı Tedavi Sonuç Epidemiyoloji
OKSİDAN- ANTİOKSİDAN SİSTEM PROF.DR.GÜLER BUĞDAYCI
 1 OKSİDAN- ANTİOKSİDAN SİSTEM PROF.DR.GÜLER BUĞDAYCI Amaç 2 SR oluşturdukları hasar ve ilişkili hastalıklar Vücuttaki oksijen kaynakları Radikal hasara karşı koruyular; antioksidan sistem GİRİŞ Aerobik
1 OKSİDAN- ANTİOKSİDAN SİSTEM PROF.DR.GÜLER BUĞDAYCI Amaç 2 SR oluşturdukları hasar ve ilişkili hastalıklar Vücuttaki oksijen kaynakları Radikal hasara karşı koruyular; antioksidan sistem GİRİŞ Aerobik
Serbest radikal. yörüngelerinde) eşleşmemiş tek. gösteren, nötr ya da iyonize tüm atom veya moleküllere denir.
 Superoxide Dismutase Hazırlayanlar: Funda İLHAN (050559017) Ebru KORKMAZ (050559021) Mehtap BİRKAN (050559008) Nihan BAŞARAN (050559007) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ İ ÜNİVERSİTESİİ
Superoxide Dismutase Hazırlayanlar: Funda İLHAN (050559017) Ebru KORKMAZ (050559021) Mehtap BİRKAN (050559008) Nihan BAŞARAN (050559007) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ İ ÜNİVERSİTESİİ
BİYOİNORGANİK KİMYA 5. HAFTA
 BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR
 SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR Yard.Doç.Dr Doç.Dr.. Mustafa ALTINIŞIK ADÜ Tıp Fakültesi Biyokimya AD AYDIN-2000 1 Sunum Planı Oksijen, reaktif oksijen türleri (ROS) ve serbest radikaller
SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR Yard.Doç.Dr Doç.Dr.. Mustafa ALTINIŞIK ADÜ Tıp Fakültesi Biyokimya AD AYDIN-2000 1 Sunum Planı Oksijen, reaktif oksijen türleri (ROS) ve serbest radikaller
SERBEST RADİKALLER, OKSİDATİF STRES VE ANTİOKSİDAN SİSTEMLER
 SERBEST RADİKALLER, OKSİDATİF STRES VE ANTİOKSİDAN SİSTEMLER SERBEST RADİKALLER Serbest radikaller dış yörüngelerinde eşlenmemiş elektron bulundurmaları nedeniyle diğer bileşiklerden farklı kimyasal bileşiklerdir.
SERBEST RADİKALLER, OKSİDATİF STRES VE ANTİOKSİDAN SİSTEMLER SERBEST RADİKALLER Serbest radikaller dış yörüngelerinde eşlenmemiş elektron bulundurmaları nedeniyle diğer bileşiklerden farklı kimyasal bileşiklerdir.
FAZ II Enzimlerine bağlı genetik polimorfizmler - 1
 FAZ II Enzimlerine bağlı genetik polimorfizmler - 1 1 İlaçların,öncelikle yararlı etkileri için kullanılmaktadır. Ancak bazen ilaç kullanımı yan etkiler gösterebilmektedir. Bazı hastalarda aynı ilaç için
FAZ II Enzimlerine bağlı genetik polimorfizmler - 1 1 İlaçların,öncelikle yararlı etkileri için kullanılmaktadır. Ancak bazen ilaç kullanımı yan etkiler gösterebilmektedir. Bazı hastalarda aynı ilaç için
Suyun Radyasyon Kimyası
 Suyun Radyasyon Kimyası Radyobiyolojide ve reaktör teknolojisinde kimyasal işlemlerde su ve sulu çözeltilerin önemi nedeniyle suyun radyasyon kimyası deneysel ve teorik çalışmalarda esas konu olmuştur.
Suyun Radyasyon Kimyası Radyobiyolojide ve reaktör teknolojisinde kimyasal işlemlerde su ve sulu çözeltilerin önemi nedeniyle suyun radyasyon kimyası deneysel ve teorik çalışmalarda esas konu olmuştur.
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ
 15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
OKSİDATİF STRES VE ANTİOKSİDANLAR
 OKSİDATİF STRES VE ANTİOKSİDANLAR Oksidatif Stres Analiz Parametreleri ve Oksantest Oksante Ar-Ge Laboratuvarı 2012 OKSİDATİF STRES VE ANTİOKSİDANLAR Serbest radikaller, besinlerin oksijen kullanılarak
OKSİDATİF STRES VE ANTİOKSİDANLAR Oksidatif Stres Analiz Parametreleri ve Oksantest Oksante Ar-Ge Laboratuvarı 2012 OKSİDATİF STRES VE ANTİOKSİDANLAR Serbest radikaller, besinlerin oksijen kullanılarak
Serbest radikallerin etkileri ve oluşum mekanizmaları
 Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
Serbest radikallerin etkileri ve oluşum mekanizmaları Serbest radikallerin yapısında, çoğunlukla oksijen yer almaktadır. (reaktif oksijen türleri=ros) ROS oksijen içeren, küçük ve oldukça reaktif moleküllerdir.
OKSİJENLİ SOLUNUM
 1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
Farmasötik Toksikoloji
 Farmasötik Toksikoloji 2014 2015 4.Not Doç.Dr. Gül ÖZHAN BİYOTRANSFORMASYON Endojen maddelerin ve ksenobiyotiklerin metabolizma reaksiyonları ile suda çözünen bileşiklere dönüştürülmesi. Biyotransformasyon
Farmasötik Toksikoloji 2014 2015 4.Not Doç.Dr. Gül ÖZHAN BİYOTRANSFORMASYON Endojen maddelerin ve ksenobiyotiklerin metabolizma reaksiyonları ile suda çözünen bileşiklere dönüştürülmesi. Biyotransformasyon
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
Olgu sunumu. Sunu planı; - olgu. - epidemiyolji. - farmakoloji. - klinik
 Sunu planı; - olgu Olgu sunumu Dr.murat BERBEROĞLU Akdeniz Üniversitesi Tıp fakültesi ACİL TIP ANABİLİM DALI 03.11.09 - epidemiyolji - farmakoloji - klinik - tanı - tedavi - algoritim 21 yaşında, bayan
Sunu planı; - olgu Olgu sunumu Dr.murat BERBEROĞLU Akdeniz Üniversitesi Tıp fakültesi ACİL TIP ANABİLİM DALI 03.11.09 - epidemiyolji - farmakoloji - klinik - tanı - tedavi - algoritim 21 yaşında, bayan
6. BÖLÜM MİKROBİYAL METABOLİZMA
 6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın
 İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın Mitokondri, ökaryotik organizmanın farklı bir organeli Şekilleri küremsi veya uzun silindirik Çapları 0.5-1 μm uzunlukları 2-6 μm Sayıları
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın Mitokondri, ökaryotik organizmanın farklı bir organeli Şekilleri küremsi veya uzun silindirik Çapları 0.5-1 μm uzunlukları 2-6 μm Sayıları
21.11.2008. I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI.
 Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu)
 Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
ĐÇERĐK. Vitamin B6 Formları. LOGO www.themegallery.com. Tarihsel Bakış. Yapısal Formüller. 4 Piridoksin Piridoksal Piridoksamin Piridoksal-fosfat
 LOGO ĐÇERĐK Tarihsel Bakış B6 Vitamininin Genel Özellikleri Kimyasal Ve Biyolojik Fonksiyonları Biyokimyasal Fonksiyonları YRD. DOÇ. DR. BEKİR ÇÖL SUNAN: DUYGU BAHÇE Emilim, Transport ve Metabolizma İmmün
LOGO ĐÇERĐK Tarihsel Bakış B6 Vitamininin Genel Özellikleri Kimyasal Ve Biyolojik Fonksiyonları Biyokimyasal Fonksiyonları YRD. DOÇ. DR. BEKİR ÇÖL SUNAN: DUYGU BAHÇE Emilim, Transport ve Metabolizma İmmün
Toksisiteye Etki Eden Faktörler
 Toksisiteye Etki Eden Faktörler Toksik etki (toksisite) Tüm ksenobiyotiklerin biyolojik sistemlerde oluşturdukları zararlı etki. 2 Kimyasal Madde ile İlgili Faktörler Bir kimyasal maddenin metabolizmasında
Toksisiteye Etki Eden Faktörler Toksik etki (toksisite) Tüm ksenobiyotiklerin biyolojik sistemlerde oluşturdukları zararlı etki. 2 Kimyasal Madde ile İlgili Faktörler Bir kimyasal maddenin metabolizmasında
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
Hücre Solunumu: Kimyasal Enerji Eldesi
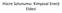 Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Dr. Hülya ÇAKMAK Gıda Mühendisliği Bölümü ANTİOKSİDANLAR
 Dr. Hülya ÇAKMAK Gıda Mühendisliği Bölümü ANTİOKSİDANLAR ANTİOKSİDANLAR Aktif oksijen türevleri (ROS) normal metabolizma sırasında vücudumuzun ürettiği yan ürünlerdir. Ancak bazı dış kaynaklardan da serbest
Dr. Hülya ÇAKMAK Gıda Mühendisliği Bölümü ANTİOKSİDANLAR ANTİOKSİDANLAR Aktif oksijen türevleri (ROS) normal metabolizma sırasında vücudumuzun ürettiği yan ürünlerdir. Ancak bazı dış kaynaklardan da serbest
III-Hayatın Oluşturan Kimyasal Birimler
 III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI TRİGLİSERİTLERİN SENTEZİ
 9. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI Palmitoleik ve oleik asitlerin sentezi için palmitik ve stearik asitler hayvansal organizmalardaki çıkş maddeleridir.
9. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI Palmitoleik ve oleik asitlerin sentezi için palmitik ve stearik asitler hayvansal organizmalardaki çıkş maddeleridir.
Bakır (Cu) Bakır anemi de kritik bir rol oynar.
 Bakır (Cu) Bakır anemi de kritik bir rol oynar. Vücutta küçük miktarda bakır varlığı olmaz ise demirin intestinal yolaktan emilimi ve kc de depolanması mümkün değildir. Bakır hemoglobin yapımı için de
Bakır (Cu) Bakır anemi de kritik bir rol oynar. Vücutta küçük miktarda bakır varlığı olmaz ise demirin intestinal yolaktan emilimi ve kc de depolanması mümkün değildir. Bakır hemoglobin yapımı için de
Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol)
 hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
Organik Bileşikler. Karbonhidratlar. Organik Bileşikler YGS Biyoloji 1
 Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
Yeni Tanı Hipertansiyon Hastalarında Tiyol Disülfid Dengesi
 Yeni Tanı Hipertansiyon Hastalarında Tiyol Disülfid Dengesi İhsan Ateş 1, Nihal Özkayar 2,Bayram İnan 1, F. Meriç Yılmaz 3, Canan Topçuoğlu 3, Özcan Erel 4, Fatih Dede 2, Nisbet Yılmaz 1 1 Ankara Numune
Yeni Tanı Hipertansiyon Hastalarında Tiyol Disülfid Dengesi İhsan Ateş 1, Nihal Özkayar 2,Bayram İnan 1, F. Meriç Yılmaz 3, Canan Topçuoğlu 3, Özcan Erel 4, Fatih Dede 2, Nisbet Yılmaz 1 1 Ankara Numune
KALP HASTALIKLARINDA OKSĐDATĐF STRESĐN ÖNEMĐ. Dr. Sabri DEMĐRCAN
 KALP HASTALIKLARINDA OKSĐDATĐF STRESĐN ÖNEMĐ Dr. Sabri DEMĐRCAN Oksijen Toksisitesi - 1 Bilinen bütün canlı türleri, organik moleküllerin içindeki oksijene gereksinim duyarlar. Anaerobik canlılardaki oksijenin
KALP HASTALIKLARINDA OKSĐDATĐF STRESĐN ÖNEMĐ Dr. Sabri DEMĐRCAN Oksijen Toksisitesi - 1 Bilinen bütün canlı türleri, organik moleküllerin içindeki oksijene gereksinim duyarlar. Anaerobik canlılardaki oksijenin
2. Kanun- Enerji dönüşümü sırasında bir miktar kullanılabilir kullanılamayan enerji ısı olarak kaybolur.
 Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU
 13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
BİYOİNORGANİK KİMYA. Prof. Dr. Ahmet KARADAĞ
 BİYOİNORGANİK KİMYA Prof. Dr. Ahmet KARADAĞ 2018 Biyoinorganik Kimya 10.HAFTA İÇİNDEKİLER 1. Asit Katalizi İşleten Enzimler 2. Demir-Kükürt Proteinler ve Hem dışı Demir 1.Asit Katalizi İşleten Enzimler
BİYOİNORGANİK KİMYA Prof. Dr. Ahmet KARADAĞ 2018 Biyoinorganik Kimya 10.HAFTA İÇİNDEKİLER 1. Asit Katalizi İşleten Enzimler 2. Demir-Kükürt Proteinler ve Hem dışı Demir 1.Asit Katalizi İşleten Enzimler
GLİKOJEN METABOLİZMASI
 METABOLİZMASI DİLDAR KONUKOĞLU TIBBİ BİYOKİMYA 8.4.2015 DİLDAR KONUKOĞLU 1 YAPISI Alfa-[1,6] glikozid Alfa- [1-4] glikozid bağı yapısal olarak D-glukozdan oluşmuş dallanmış yapı gösteren homopolisakkarittir.
METABOLİZMASI DİLDAR KONUKOĞLU TIBBİ BİYOKİMYA 8.4.2015 DİLDAR KONUKOĞLU 1 YAPISI Alfa-[1,6] glikozid Alfa- [1-4] glikozid bağı yapısal olarak D-glukozdan oluşmuş dallanmış yapı gösteren homopolisakkarittir.
Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı
 YAĞ ASİTLERİNİN OKSİDASYONU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPOSİTLERDEN MOBİLİZASYONU ATGL; adiposit triaçilgliserol lipaz, HSL; hormona duyarlı
YAĞ ASİTLERİNİN OKSİDASYONU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPOSİTLERDEN MOBİLİZASYONU ATGL; adiposit triaçilgliserol lipaz, HSL; hormona duyarlı
Solunum. Solunum ve odunsu bitkilerin büyümesi arasında yüksek bir korelasyon bulunmaktadır (Kozlowski ve Pallardy, 1997).
 SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
Özel Formülasyon DAHA İYİ DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
 Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
Özel Formülasyon DAHA İYİ Yumurta Verimi Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALIYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA IÇIN AGRALYX!
ALFA LİPOİK ASİT (ALA)
 ALFA LİPOİK ASİT (ALA) Bitki ve hayvan dokularında doğal olarak bulunan ditiyol türevi bir bileşiktir. Endojen olarak mitokondride oktanoik asitten sentezlenir. ALA mitokondrideki enerji üretiminden sorumlu
ALFA LİPOİK ASİT (ALA) Bitki ve hayvan dokularında doğal olarak bulunan ditiyol türevi bir bileşiktir. Endojen olarak mitokondride oktanoik asitten sentezlenir. ALA mitokondrideki enerji üretiminden sorumlu
5.111 Ders Özeti #12. Konular: I. Oktet kuralından sapmalar
 5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
5.111 Ders Özeti #12 Bugün için okuma: Bölüm 2.9 (3. Baskıda 2.10), Bölüm 2.10 (3. Baskıda 2.11), Bölüm 2.11 (3. Baskıda 2.12), Bölüm 2.3 (3. Baskıda 2.1), Bölüm 2.12 (3. Baskıda 2.13). Ders #13 için okuma:
Akıllı Defter. 9.Sınıf Biyoloji. vitaminler,hormonlar,nükleik asitler. sembole tıklayınca etkinlik açılır. sembole tıklayınca ppt sunumu açılır
 9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
BİY 315 Lipid Metabolizması-II. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 Lipid Metabolizması-II Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Yağ Asidi Oksidasyonu Besinlerin sindirimi sonucu elde edilen yağlar, bağırsaktan geçerek lenf sistemine ulaşır ve bu
BİY 315 Lipid Metabolizması-II Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Yağ Asidi Oksidasyonu Besinlerin sindirimi sonucu elde edilen yağlar, bağırsaktan geçerek lenf sistemine ulaşır ve bu
T.C. GAZİ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA (TIP) ANABİLİM DALI
 T.C. GAZİ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA (TIP) ANABİLİM DALI OKSİDATİF STRES BELİRTEÇLERİNİN VE HYALURONİK ASİTİN KORONER ARTER HASTALIĞININ ANJİOGRAFİK YAYGINLIK VE CİDDİYETİ İLE İLİŞKİSİ
T.C. GAZİ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA (TIP) ANABİLİM DALI OKSİDATİF STRES BELİRTEÇLERİNİN VE HYALURONİK ASİTİN KORONER ARTER HASTALIĞININ ANJİOGRAFİK YAYGINLIK VE CİDDİYETİ İLE İLİŞKİSİ
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon
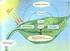 Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
Metabolizma. Metabolizmaya giriş. Metabolizmaya giriş. Metabolizmayı tanımlayacak olursak
 Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
DAHA İYİ ÖZEL FORMÜLASYON. Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık
 ÖZEL FORMÜLASYON DAHA İYİ Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALİYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA İÇİN AGRALYX
ÖZEL FORMÜLASYON DAHA İYİ Yumurta Verim Kabuk Kalitesi Yemden Yararlanma Karaciğer Sağlığı Bağırsak Sağlığı Bağışıklık Karlılık DAHA DÜŞÜK MALİYETLE DAHA SAĞLIKLI SÜRÜLER VE DAHA FAZLA YUMURTA İÇİN AGRALYX
11. SINIF KONU ANLATIMI 2 ATP-2
 11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
Prof. Dr. Şule PEKYARDIMCI
 13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA. Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004
 REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
Yağ Asitlerinin Biyosentezi. Prof. Dr. Fidancı
 Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
DEMİR İÇEREN İLAÇLARLA ZEHİRLENME UZM.DR. SEVGİ YUMRUTEPE MALATYA EĞİTİM VE ARAŞTIRMA HASTANESİ 22.O4.2018
 DEMİR İÇEREN İLAÇLARLA ZEHİRLENME UZM.DR. SEVGİ YUMRUTEPE MALATYA EĞİTİM VE ARAŞTIRMA HASTANESİ 22.O4.2018 GİRİŞ Demir ilaçları anemi tedavisinde (özellikle gebelerde ve çocuklarda) En sık 6 yaş altı çocuklarda
DEMİR İÇEREN İLAÇLARLA ZEHİRLENME UZM.DR. SEVGİ YUMRUTEPE MALATYA EĞİTİM VE ARAŞTIRMA HASTANESİ 22.O4.2018 GİRİŞ Demir ilaçları anemi tedavisinde (özellikle gebelerde ve çocuklarda) En sık 6 yaş altı çocuklarda
Hedefe Spesifik Beslenme Katkıları
 Hedefe Spesifik Beslenme Katkıları Hayvan Beslemede Vitamin ve Minerallerin Önemi Vitaminler, çiftlik hayvanlarının, büyümesi, gelişmesi, üremesi, kısaca yaşaması ve verim vermesi için gerekli metabolik
Hedefe Spesifik Beslenme Katkıları Hayvan Beslemede Vitamin ve Minerallerin Önemi Vitaminler, çiftlik hayvanlarının, büyümesi, gelişmesi, üremesi, kısaca yaşaması ve verim vermesi için gerekli metabolik
TAURİNİN İSKEMİ REPERFÜZYON HASARINDA MMP-2, MMP-9 VE İLİŞKİLİ SİNYAL İLETİ YOLAĞI ÜZERİNE ETKİLERİ
 TAURİNİN İSKEMİ REPERFÜZYON HASARINDA MMP-2, MMP-9 VE İLİŞKİLİ SİNYAL İLETİ YOLAĞI ÜZERİNE ETKİLERİ CEMRE URAL 1, ZAHİDE ÇAVDAR 1, ASLI ÇELİK 2, ŞEVKİ ARSLAN 3, GÜLSÜM TERZİOĞLU 3, SEDA ÖZBAL 5, BEKİR
TAURİNİN İSKEMİ REPERFÜZYON HASARINDA MMP-2, MMP-9 VE İLİŞKİLİ SİNYAL İLETİ YOLAĞI ÜZERİNE ETKİLERİ CEMRE URAL 1, ZAHİDE ÇAVDAR 1, ASLI ÇELİK 2, ŞEVKİ ARSLAN 3, GÜLSÜM TERZİOĞLU 3, SEDA ÖZBAL 5, BEKİR
Sitrik Asit Döngüsü. (Trikarboksilik Asit Döngüsü, Krebs Döngüsü)
 Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
İal-biyoloji METABOLİZMA/SOLUNUM. 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir?
 METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
Kolesterol Metabolizması. Prof. Dr. Fidancı
 Kolesterol Metabolizması Prof. Dr. Fidancı Kolesterol oldukça önemli bir biyolojik moleküldür. Membran yapısında önemli rol oynar. Steroid hormonların ve safra asitlerinin sentezinde öncül maddedir. Diyet
Kolesterol Metabolizması Prof. Dr. Fidancı Kolesterol oldukça önemli bir biyolojik moleküldür. Membran yapısında önemli rol oynar. Steroid hormonların ve safra asitlerinin sentezinde öncül maddedir. Diyet
o Serin o Triyonin o Sistein o Metiyonin o Arjinin o Histidin
 III.PROTEİNLER Karbon,hidrojen,oksijen ve azot elementlerinden oluşmuş organik bileşiklerdir.yapısında bazen sülfür,fosfor veya demir de bulunabilir. Proteinler canlılarda en fazla bulunan organik madde
III.PROTEİNLER Karbon,hidrojen,oksijen ve azot elementlerinden oluşmuş organik bileşiklerdir.yapısında bazen sülfür,fosfor veya demir de bulunabilir. Proteinler canlılarda en fazla bulunan organik madde
9- RADYASYONUN ETKİ MEKANİZMALARI 9.1- RADYASYONUN İNDİREKT (DOLAYLI) ETKİSİ
 9- RADYASYONUN ETKİ MEKANİZMALARI 9.1- RADYASYONUN İNDİREKT (DOLAYLI) ETKİSİ Radyasyonun indirekt etkisi iyonlaştırdığı su moleküllerinin oluşturdukları serbest radikaller aracılığıyla olmaktadır. Çünkü
9- RADYASYONUN ETKİ MEKANİZMALARI 9.1- RADYASYONUN İNDİREKT (DOLAYLI) ETKİSİ Radyasyonun indirekt etkisi iyonlaştırdığı su moleküllerinin oluşturdukları serbest radikaller aracılığıyla olmaktadır. Çünkü
Doğadaki Enerji Akışı
 Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
Doymamış Yağ Asitlerinin Transformasyonu. Prof. Dr. Fidancı
 Doymamış Yağ Asitlerinin Transformasyonu Prof. Dr. Fidancı Bir hücre bir uyarıya yanıt verdiğinde biyoaktif mediatörler sıklıkla zarlardaki lipidlerden oluşur. Biyoaktif mediatörlerin bir grubu, 20 karbonlu
Doymamış Yağ Asitlerinin Transformasyonu Prof. Dr. Fidancı Bir hücre bir uyarıya yanıt verdiğinde biyoaktif mediatörler sıklıkla zarlardaki lipidlerden oluşur. Biyoaktif mediatörlerin bir grubu, 20 karbonlu
SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR
 SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR Yaşam için oksijen (O 2 ) Havasız yerde yaşayamayız. Yaşamımızı sürdürmek için havanın moleküler oksijenini (O 2 ) tükettiğimizi biliyoruz. Total oksijen tüketimimizin
SERBEST OKSİJEN RADİKALLERİ VE ANTİOKSİDANLAR Yaşam için oksijen (O 2 ) Havasız yerde yaşayamayız. Yaşamımızı sürdürmek için havanın moleküler oksijenini (O 2 ) tükettiğimizi biliyoruz. Total oksijen tüketimimizin
TIBBİ BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI
 TIBBİ BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Yöntemleri Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0
TIBBİ BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Yöntemleri Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0
BİYOLOJİK OKSİDASYON. Doç.Dr.Remisa GELİŞGEN
 BİYOLOJİK OKSİDASYON Doç.Dr.Remisa GELİŞGEN OKSİDASYON-REDÜKSİYON REAKSİYONLARI Elektronların bir atom veya molekülden bir diğerine geçişleri redoks reaksiyonu olarak adlandırılmaktadır. Redoks : e-transferi
BİYOLOJİK OKSİDASYON Doç.Dr.Remisa GELİŞGEN OKSİDASYON-REDÜKSİYON REAKSİYONLARI Elektronların bir atom veya molekülden bir diğerine geçişleri redoks reaksiyonu olarak adlandırılmaktadır. Redoks : e-transferi
Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir.
 Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir. Yaşamın temelini oluşturan kimyasal tepkimelerin tümü Metabolizma olarak adlandırılmaktadır. Bitki hücrelerinde
Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir. Yaşamın temelini oluşturan kimyasal tepkimelerin tümü Metabolizma olarak adlandırılmaktadır. Bitki hücrelerinde
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ
 KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
BİY 315 BİYOKİMYA GİRİŞ. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
BÖLÜM I HÜCRE FİZYOLOJİSİ...
 BÖLÜM I HÜCRE FİZYOLOJİSİ... 1 Bilinmesi Gereken Kavramlar... 1 Giriş... 2 Hücrelerin Fonksiyonel Özellikleri... 2 Hücrenin Kimyasal Yapısı... 2 Hücrenin Fiziksel Yapısı... 4 Hücrenin Bileşenleri... 4
BÖLÜM I HÜCRE FİZYOLOJİSİ... 1 Bilinmesi Gereken Kavramlar... 1 Giriş... 2 Hücrelerin Fonksiyonel Özellikleri... 2 Hücrenin Kimyasal Yapısı... 2 Hücrenin Fiziksel Yapısı... 4 Hücrenin Bileşenleri... 4
BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI
 BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0 2 5 Enstitünün Belirlediği
BİYOKİMYA ANABİLİM DALI LİSANSÜSTÜ DERS PROGRAMI SAĞLIK BİLİMLERİ ENSİTÜSÜ İ Yüksek Lisans Programı SZR 101 Bilimsel Araştırma Ders (T+ U) 2+2 3 6 AD SZR 103 Akılcı İlaç Kullanımı 2+0 2 5 Enstitünün Belirlediği
Referans:e-TUS İpucu Serisi Biyokimya Ders Notları Sayfa:368
 21. Aşağıdakilerden hangisinin fizyolojik ph'de tamponlama etkisi vardır? A) CH3COC- / CH3COOH (pka = 4.76) B) HPO24- / H2PO-4 (pka = 6.86) C) NH3/NH+4(pKa =9.25) D) H2PO-4 / H3PO4 (pka =2.14) E) PO34-/
21. Aşağıdakilerden hangisinin fizyolojik ph'de tamponlama etkisi vardır? A) CH3COC- / CH3COOH (pka = 4.76) B) HPO24- / H2PO-4 (pka = 6.86) C) NH3/NH+4(pKa =9.25) D) H2PO-4 / H3PO4 (pka =2.14) E) PO34-/
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur.
 Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.-
 1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.- Biyokimya sözcüğü biyolojik kimya (=yaşam kimyası) teriminin kısaltılmış şeklidir. Daha eskilerde, fizyolojik kimya terimi kullanılmıştır. Gerçekten de Biyokimya
1-GİRİ 1.1- BİYOKİMYANIN TANIMI VE KONUSU.- Biyokimya sözcüğü biyolojik kimya (=yaşam kimyası) teriminin kısaltılmış şeklidir. Daha eskilerde, fizyolojik kimya terimi kullanılmıştır. Gerçekten de Biyokimya
Notlarımıza iyi çalışan kursiyerlerimiz soruların çoğunu rahatlıkla yapılabileceklerdir.
 Biyokimya sınavı orta zorlukta bir sınavdı. 1-2 tane zor soru ve 5-6 tane eski soru soruldu. Soruların; 16 tanesi temel bilgi, 4 tanesi ise detay bilgi ölçmekteydi. 33. soru mikrobiyolojiye daha yakındır.
Biyokimya sınavı orta zorlukta bir sınavdı. 1-2 tane zor soru ve 5-6 tane eski soru soruldu. Soruların; 16 tanesi temel bilgi, 4 tanesi ise detay bilgi ölçmekteydi. 33. soru mikrobiyolojiye daha yakındır.
MİNERALLER. Dr. Diyetisyen Hülya YARDIMCI
 MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
YGS YE HAZIRLIK DENEMESi #18
 YGS YE HAZIRLIK DENEMESi #18 1) Bakterilerin gerçekleştirdiği, I. Kimyasal enerji sayesinde besin sentezleme II. Işık enerjisini kimyasal bağ enerjisine dönüştürme III. Kimyasal bağ enerjisini ATP enerjisine
YGS YE HAZIRLIK DENEMESi #18 1) Bakterilerin gerçekleştirdiği, I. Kimyasal enerji sayesinde besin sentezleme II. Işık enerjisini kimyasal bağ enerjisine dönüştürme III. Kimyasal bağ enerjisini ATP enerjisine
Hücre. 1 µm = 0,001 mm (1000 µm = 1 mm)!
 HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
ADIM ADIM YGS LYS Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI
 ADIM ADIM YGS LYS 177. Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI Hastalık yapıcı organizmalara karşı vücudun gösterdiği dirence bağışıklık
ADIM ADIM YGS LYS 177. Adım DOLAŞIM SİSTEMİ 5 İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI İNSANDA BAĞIŞIKLIK VE VÜCUDUN SAVUNULMASI Hastalık yapıcı organizmalara karşı vücudun gösterdiği dirence bağışıklık
Propiverin HCL Etki Mekanizması. Bedreddin Seçkin
 Propiverin HCL Etki Mekanizması Bedreddin Seçkin 24.10.2015 Propiverin Çift Yönlü Etki Mekanizmasına Sahiptir Propiverin nervus pelvicus un eferent nörotransmisyonunu baskılayarak antikolinerjik etki gösterir.
Propiverin HCL Etki Mekanizması Bedreddin Seçkin 24.10.2015 Propiverin Çift Yönlü Etki Mekanizmasına Sahiptir Propiverin nervus pelvicus un eferent nörotransmisyonunu baskılayarak antikolinerjik etki gösterir.
ÇİSEM İLGİN ( ) LÜTFİYE ALAÇAM ( ) Prof. Dr. Figen ERKOÇ GAZİ ÜNİVERSİTESİ
 HAZIRLAYLANLAR ÇİSEM İLGİN (040559015) LÜTFİYE ALAÇAM (040559003) ZEYNEP HALICI (040559014) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ ÜNİVERSİTESİ 1 TRANSAMİNAZLAR Transaminazlar veya Aminotransferazlar
HAZIRLAYLANLAR ÇİSEM İLGİN (040559015) LÜTFİYE ALAÇAM (040559003) ZEYNEP HALICI (040559014) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ ÜNİVERSİTESİ 1 TRANSAMİNAZLAR Transaminazlar veya Aminotransferazlar
ANTİSEPTİKLERİN KULLANIM YERLERİ
 ANTİSEPTİKLER 1 Kavramlar: Antiseptik: Canlılar üzerinde (cilde ve dışarı açılan boşlukların mukozasına) dıştan uygulanmak suretiyle kullanılan antimikrobik ilaçlardır. Dezenfektan: Cansız cisimler (cerrahi
ANTİSEPTİKLER 1 Kavramlar: Antiseptik: Canlılar üzerinde (cilde ve dışarı açılan boşlukların mukozasına) dıştan uygulanmak suretiyle kullanılan antimikrobik ilaçlardır. Dezenfektan: Cansız cisimler (cerrahi
Maskeli Hipertansiyonda Anormal Tiyol Disülfid Dengesi
 Maskeli Hipertansiyonda Anormal Tiyol Disülfid Dengesi İhsan Ateş 1, Mustafa Altay 1, Nihal Özkayar 2, F. Meriç Yılmaz 3, Canan Topçuoğlu 3, Murat Alışık 4, Özcan Erel 4, Fatih Dede 2 1 Ankara Numune Eğitim
Maskeli Hipertansiyonda Anormal Tiyol Disülfid Dengesi İhsan Ateş 1, Mustafa Altay 1, Nihal Özkayar 2, F. Meriç Yılmaz 3, Canan Topçuoğlu 3, Murat Alışık 4, Özcan Erel 4, Fatih Dede 2 1 Ankara Numune Eğitim
FARMAKOKİNETİK KİŞİSEL VARYASYONLAR NEDENLERİ VE KLİNİK SONUÇLARI
 FARMAKOKİNETİK KİŞİSEL VARYASYONLAR NEDENLERİ VE KLİNİK SONUÇLARI Ercüment KARASULU Ege Üniversitesi İlaç Araştırma-Geliştirme ve Farmakokinetik Araştırma - Uygulama Merkezi ( ARGEFAR ) 24 MART 2010 İlaçların
FARMAKOKİNETİK KİŞİSEL VARYASYONLAR NEDENLERİ VE KLİNİK SONUÇLARI Ercüment KARASULU Ege Üniversitesi İlaç Araştırma-Geliştirme ve Farmakokinetik Araştırma - Uygulama Merkezi ( ARGEFAR ) 24 MART 2010 İlaçların
BİLİRUBİN METABOLİZMASI. Yrd. Doç. Dr. İlyas Yolbaş Çocuk Sağlığı ve Hastalıkları ABD
 BİLİRUBİN METABOLİZMASI Yrd. Doç. Dr. İlyas Yolbaş Çocuk Sağlığı ve Hastalıkları ABD Dersin amaçı Bilirubin oluşumunu ve atılımını öğrenmek İndirek ve direk bilirubinin özelliklerini öğrenmek Arttığı ve
BİLİRUBİN METABOLİZMASI Yrd. Doç. Dr. İlyas Yolbaş Çocuk Sağlığı ve Hastalıkları ABD Dersin amaçı Bilirubin oluşumunu ve atılımını öğrenmek İndirek ve direk bilirubinin özelliklerini öğrenmek Arttığı ve
T. C. İSTANBUL BİLİM ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA ANABİLİM DALI YÜKSEK LİSANS PROGRAMI EĞİTİM-ÖĞRETİM YILI MÜFREDATI
 I. YARIYILI T. C. İSTANBUL BİLİM ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA ANABİLİM DALI YÜKSEK LİSANS PROGRAMI 2016-2017 EĞİTİM-ÖĞRETİM YILI MÜFREDATI B 601 Temel Biyokimya I Zorunlu 3 0 3 4 B
I. YARIYILI T. C. İSTANBUL BİLİM ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ BİYOKİMYA ANABİLİM DALI YÜKSEK LİSANS PROGRAMI 2016-2017 EĞİTİM-ÖĞRETİM YILI MÜFREDATI B 601 Temel Biyokimya I Zorunlu 3 0 3 4 B
MİTOKONDRİ Doç. Dr. Mehmet GÜVEN
 MİTOKONDRİ Doç.. Dr. Mehmet GÜVENG Hemen hemen bütün b ökaryotik hücrelerde ve ökaryotik mikroorganizmalarda bulunur. Eritrositlerde, bakterilerde ve yeşil alglerde mitokondri yoktur. Şekilleri (küremsi
MİTOKONDRİ Doç.. Dr. Mehmet GÜVENG Hemen hemen bütün b ökaryotik hücrelerde ve ökaryotik mikroorganizmalarda bulunur. Eritrositlerde, bakterilerde ve yeşil alglerde mitokondri yoktur. Şekilleri (küremsi
M. (arpa şekeri) +su S (çay şekeri) + su L.. (süt şekeri)+ su
 KARBONHİDRATLAR Karbonhidratlar yapılarında.. (C),.. (H) ve. (O) atomu bulunduran organik bileşiklerdir. Karbonhidratların formülü ( ) ile gösterilir. Nükleik asitlerin, ATP nin, hücre, bitkilerde yapısına
KARBONHİDRATLAR Karbonhidratlar yapılarında.. (C),.. (H) ve. (O) atomu bulunduran organik bileşiklerdir. Karbonhidratların formülü ( ) ile gösterilir. Nükleik asitlerin, ATP nin, hücre, bitkilerde yapısına
LABORATUVAR TESTLERİNİN KLİNİK YORUMU
 LABORATUVAR TESTLERİNİN KLİNİK YORUMU Alanin Transaminaz ( ALT = SGPT) : Artmış alanin transaminaz karaciğer hastalıkları ( hepatosit hasarı), hepatit, safra yolu hastalıklarında ve ilaçlara bağlı olarak
LABORATUVAR TESTLERİNİN KLİNİK YORUMU Alanin Transaminaz ( ALT = SGPT) : Artmış alanin transaminaz karaciğer hastalıkları ( hepatosit hasarı), hepatit, safra yolu hastalıklarında ve ilaçlara bağlı olarak
Nihal ALEM YÜKSEK LİSANS TEZİ BİYOLOJİ
 ASKORBİK ASİDİN HÜCRE YAŞLANMASI ÜZERİNE ETKİSİ Nihal ALEM YÜKSEK LİSANS TEZİ BİYOLOJİ GAZİ ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ HAZİRAN 2007 ANKARA iv ASKORBİK ASİDİN HÜCRE YAŞLANMASI ÜZERİNE ETKİSİ
ASKORBİK ASİDİN HÜCRE YAŞLANMASI ÜZERİNE ETKİSİ Nihal ALEM YÜKSEK LİSANS TEZİ BİYOLOJİ GAZİ ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ HAZİRAN 2007 ANKARA iv ASKORBİK ASİDİN HÜCRE YAŞLANMASI ÜZERİNE ETKİSİ
Yağ Asitlerinin β Oksidayonu. Prof. Dr. Fidancı
 Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
T.C. KAHRAMANMARAŞ SÜTÇÜ İMAM ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ KİMYA ANABİLİM DALI
 T.C. KAHRAMANMARAŞ SÜTÇÜ İMAM ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ KİMYA ANABİLİM DALI STREPTOZOTOSİN İLE DİABET OLUŞTURULMUŞ FARELERDE ASPİRİN VE E VİTAMİNİN DOKULARDA LİPİD PEROKSİDASYONU VE ANTİOKSİDAN
T.C. KAHRAMANMARAŞ SÜTÇÜ İMAM ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ KİMYA ANABİLİM DALI STREPTOZOTOSİN İLE DİABET OLUŞTURULMUŞ FARELERDE ASPİRİN VE E VİTAMİNİN DOKULARDA LİPİD PEROKSİDASYONU VE ANTİOKSİDAN
TÜM VÜCUT RADYOTERAPİSİNİN FARKLI YAŞ GRUPLARINDAKİ RATLARDA BEYİN DOKUSU LİPİD PEROKSİDASYONU VE ANTİOKSİDAN SİSTEM PARAMETRELERİ ÜZERİNE ETKİLERİ.
 T.C. İNÖNÜ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ TÜM VÜCUT RADYOTERAPİSİNİN FARKLI YAŞ GRUPLARINDAKİ RATLARDA BEYİN DOKUSU LİPİD PEROKSİDASYONU VE ANTİOKSİDAN SİSTEM PARAMETRELERİ ÜZERİNE ETKİLERİ. YÜKSEK
T.C. İNÖNÜ ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ TÜM VÜCUT RADYOTERAPİSİNİN FARKLI YAŞ GRUPLARINDAKİ RATLARDA BEYİN DOKUSU LİPİD PEROKSİDASYONU VE ANTİOKSİDAN SİSTEM PARAMETRELERİ ÜZERİNE ETKİLERİ. YÜKSEK
Özgeçmiş: Özellik yok Alışkanlıklar: Alkol, sigara, madde kullanımı yok
 Dr. Neşe ÇOLAK ORAY 21 yaşında 55 kg bayan hasta 3 saat önce 80 adet Parasetamol 500mg tablet Bulantı dışında ek yakınması yok Suicidal düşünce Özgeçmiş: Özellik yok Alışkanlıklar: Alkol, sigara, madde
Dr. Neşe ÇOLAK ORAY 21 yaşında 55 kg bayan hasta 3 saat önce 80 adet Parasetamol 500mg tablet Bulantı dışında ek yakınması yok Suicidal düşünce Özgeçmiş: Özellik yok Alışkanlıklar: Alkol, sigara, madde
Kanın fonksiyonel olarak üstlendiği görevler
 EGZERSİZ VE KAN Kanın fonksiyonel olarak üstlendiği görevler Akciğerden dokulara O2 taşınımı, Dokudan akciğere CO2 taşınımı, Sindirim organlarından hücrelere besin maddeleri taşınımı, Hücreden atık maddelerin
EGZERSİZ VE KAN Kanın fonksiyonel olarak üstlendiği görevler Akciğerden dokulara O2 taşınımı, Dokudan akciğere CO2 taşınımı, Sindirim organlarından hücrelere besin maddeleri taşınımı, Hücreden atık maddelerin
ALKOLE BAĞLI OLMAYAN HEPATİK FİBROZ MODELİNDE BETAİN TEDAVİSİNİN İYİLEŞTİRİCİ ETKİSİ
 ALKOLE BAĞLI OLMAYAN HEPATİK FİBROZ MODELİNDE BETAİN TEDAVİSİNİN İYİLEŞTİRİCİ ETKİSİ İlknur Bingül*, A. Fatih Aydın*, Canan Başaran-Küçükgergin*, Işın Doğan-Ekici**, Jale Çoban***, Semra Doğru-Abbasoğlu*,
ALKOLE BAĞLI OLMAYAN HEPATİK FİBROZ MODELİNDE BETAİN TEDAVİSİNİN İYİLEŞTİRİCİ ETKİSİ İlknur Bingül*, A. Fatih Aydın*, Canan Başaran-Küçükgergin*, Işın Doğan-Ekici**, Jale Çoban***, Semra Doğru-Abbasoğlu*,
İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın
 İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın Hücre iletişimi Tüm canlılar bulundukları çevreden sinyal alırlar ve yanıt verirler Bakteriler glukoz ve amino asit gibi besinlerin
İ. Ü İstanbul Tıp Fakültesi Tıbbi Biyoloji Anabilim Dalı Prof. Dr. Filiz Aydın Hücre iletişimi Tüm canlılar bulundukları çevreden sinyal alırlar ve yanıt verirler Bakteriler glukoz ve amino asit gibi besinlerin
Canlının yapısında bulunan organik molekül grupları; o Karbonhidratlar o Yağlar o Proteinler o Enzimler o Vitaminler o Nükleik asitler ve o ATP
 Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
