|
|
|
- Ahmet Ertuğ
- 8 yıl önce
- İzleme sayısı:
Transkript
1 SSK Reçetelerinin serbest eczanelerden karþýlanmasý ile birlikte mesleðimizde yeni bir dönem baþlamýþtýr. Çaðdaþ ülkelerdeki gibi artýk tüm Ayakta Tedavi Reçeteleri eczanelerimizden karþýlanmaktadýr. Tüm yaþadýðýmýz sýkýntýlara raðmen sistem zaman içinde düzelecektir. Adana Eczacý Odasý sýkýntýlarýmýzýn en aza indirilmesi ile ilgili kurumlar nezdinde tüm gayretlerini gösteriyor. Her yeni uygulamada doðaldýr ki bir takým aksaklýklar yaþanacaktýr. Yeni yapýlanan Sosyal Güvenlik Kurumu ve Genel Saðlýk Sigortasý yasalaþtýðýnda yeni uygulamalar gündemimize gelecek; 2006 da da bu deðiþiklikler devam edecektir. Bizler eczanelerimizi, personelimizi ve kendimizi yeni düzenlemelere karþý hazýrlamalýyýz. Mesleðimize ve Eczanelerimize bugünden daha çok sahip çýkmalýyýz. Pazar payýnýn yeniden þekillenmesiyle birlikte SSK Ýlaç Listesi ve Uygulama Talimatý el kitapçýðýmýz olacak gibi... Ýyi çalýþmalar.. Saygýlarýmla Ecz. Burhanettin BULUT T.E.B. 4. Bölge Adana Eczacý Odasý Baþkaný
2 ÝÇÝNDEKÝLER Birinci Bölüm 5 Yasal Dayanak Ýkinci Bölüm 7 Reçete Yazým ve Ýlaç Kullaným Ýlkeleri Üçüncü Bölüm 8 Bazý Özel Hastalýklara ve Ýlaç Kullanýmýna Ýliþkin Düzenlemeler Dördüncü Bölüm 27 Ýlaç Kullanýmýna Ýliþkin Özel Düzenlemeler Beþinci Bölüm 30 Diðer Düzenlemeler Altýncý Bölüm 32 Yeni Ruhsat Alan Ýlaçlara Ýliþkin Ýlkeler Jenerik ve Genel Ýsimleri Ýle Listeye Giren Ýlaçlar (Ek 1) 33 Antebiotikler (Ek 2) 53 B- Ticari Ýsmi Ýle Listeye Giren Ýlaçlar (Ek 3) 63 Enteral Beslenme Üniteleri (Ek 4) Ýlaç Katký Payý Alýnmayacak Hastalara Ýlaçlar (Ek 5) 81 SSk Provizyon Sisteminde Kullanýlan Rapor Teþhis Kodlarý 103
3 2005 Yýlý Sosyal Sigortalar Kurumu Baþkanlýðý Ýlaç Listesi ve Uygulama Talimatý (Seri No:2005/1) BÝRÝNCÝ BÖLÜM Yasal Dayanak Madde 1 - Bu Talimat, Sosyal Sigortalar Kurumu Baþkanlýk Makamýnýn tarihli Olurlarýna dayanýlarak Ýlaç Komisyonu tarafýndan hazýrlanmýþ ve Kurum Yönetim Kurulu'nun günlü, XVII/257 sayýlý Kararý ile onaylanmýþtýr. Tanýmlar Madde 2 - Bu Talimatta yer alan; a) Kurum : Sosyal Sigortalar Kurumu Baþkanlýðý'ný, b) Genel Müdürlük: Sosyal Sigortalar Kurumu Baþkanlýðý Saðlýk Ýþleri Genel Müdürlüðü'nü, c) Sigortalý: 506 sayýlý Sosyal Sigortalar Kanunu'na ve 2925 Sayýlý Tarým Ýþçileri Sosyal Sigortalar Kanunu'na göre hastalýk sigortasý yönünden saðlýk yardýmlarýndan yararlandýrýlanlar ile iþsizlik sigortasý kapsamýnda olup, saðlýk hizmetinden yararlanan kimseleri, d) Saðlýk Bakanlýðýna baðlý Saðlýk Kurum ve Kuruluþlarý: Saðlýk Bakanlýðýna baðlý olup, sigortalýlara saðlýk hizmeti veren hastane, sanatoryum, prevantoryum, dispanser, saðlýk ocaðý, ana çocuk saðlýðý merkezi v.b. saðlýk kuruluþlarýný, e) Üniversite Hastanesi:- Üniversitelere baðlý týp fakülteleri hastanelerini, - Anýlan kuruluþlarca oluþturulan vakýflara ait hastaneleri, - Yüksek Öðretim Kurumu tarafýndan üniversite olarak tescil edilen vakýf hastanelerini, f) Eðitim ve Araþtýrma Hastanesi: Eðitim hizmeti veren Saðlýk Bakanlýðýna baðlý hastaneler, g) Sözleþmeli Kiþi: Kurum ile kendi uzman tabiplik veya uðraþý dallarýnda saðlýk hizmeti sunumu için sözleþme veya protokol imzalamýþ bulunan; - Hastane - Taný ve Tedavi Merkezi - Laboratuvar - Klinik-Poliklinik - Serbest Tabip ve Diþ Tabibi - Eczane, v.b. özel hukuk özel kiþilerini, h) Sözleþmeli Kuruluþ: Kurum ile kendi uzman tabiplik veya uðraþý dallarýnda saðlýk hizmeti sunumu için sözleþme veya protokol imzalamýþ bulunan; - Hastane - Taný ve Tedavi Merkezi 5
4 - Laboratuvar - Klinik-Poliklinik - Eczane v.b.özel hukuk tüzel kiþilerini, ý) Resmi Saðlýk Kurum ve Kuruluþlarý: Saðlýk Bakanlýðý, Üniversitelere ait saðlýk kurum ve kuruluþlarý ile 5283 sayýlý Kanunun 2. maddesinde belirtilen, Kurumun saðlýk hizmeti satýn aldýðý kuruluþlarý, j) Ýþyeri Hekimi: 4857 Sayýlý Ýþ Kanunu'na göre iþverenlerce çalýþtýrýlan ve Kurum tarafýndan yetkilendirilen tabip ve uzman tabipleri, k) Birim Amiri: Saðlýk Bakanlýðý'na, Üniversitelere, Resmi Kurum ve Kuruluþlara baðlý yataklý ve yataksýz saðlýk kuruluþlarýnýn baþtabipleri veya bu yetkiye sahip diðer görevlileri, l) Eþdeðer Ýlaç: Ayný etkin maddeyi ayný doz ve ayný farmasötik formda içeren, diðer bir deyiþle farmasötik açýdan eþdeðer olan ilacý, m) En Ucuz Ýlaç: Eþdeðer ilaçlardan en ucuz olanýný, ifade eder. Kapsam Madde 3 - Bu Talimat hükümleri Kurum saðlýk yardýmýndan yararlanma hakký bulunan sigortalýlar ile iþsizlik sigortasý kapsamýnda olup, saðlýk hizmetinden yararlanan kimselere uygulanýr. Yükümlülük ve Sorumluluk Madde 4 - Bu Talimat hükümleri; a) Sözleþmeli kiþi ve kuruluþlar ile bunlarýn birim amiri ve ilgili çalýþanlarýný, b) Saðlýk Bakanlýðý'na baðlý saðlýk kurum ve kuruluþlarýný, üniversite hastanelerini ve bunlarýn birim amiri ve ilgili diðer çalýþanlarýný, c) Diðer resmi saðlýk kurum ve kuruluþlarý ile bunlarýn birim amirlerini ve ilgili diðer çalýþanlarýný, d) Ýþyeri tabiplerini, baðlar. e) Bir ilacýn Saðlýk Bakanlýðýnca izin verilen endikasyon ve kullaným dozu dýþýnda kullanýlmasý, ancak Saðlýk Bakanlýðý tarafýndan kiþilere veya ilaca verilen özel kullaným izinleri, Resmi saðlýk tesisleri saðlýk kurulu raporlarý ile onaylanmak ve Genel Müdürlükce uygun görülmek kaydýyla bu hükmün dýþýndadýr. Bu Talimat hükümlerine uyulmamasý durumunda Kurum' un uðrayacaðý zarar, ilgililerin alacaðýndan mahsup veya mümkün olmamasý durumunda yasal yollar kullanýlarak doðrudan tahsil ve tazmin edilir. 6
5 ÝKÝNCÝ BÖLÜM Reçete Yazým ve Ýlaç Kullaným Ýlkeleri Ýlaç kullanýmýnda aþaðýda belirtilen konular temel alýnacaktýr. Tüm reçetelere mutlaka taný yazýlacaktýr. Tanýsý yazýlmayan reçeteler eczaneler tarafýndan kabul edilmeyecektir. Reçetelerde reçeteyi yazan hekimin imza ve kaþesi, kaþede Kurumun adý, tabibin uzmanlýk dalý ve diploma numarasý mutlaka bulunacaktýr. Madde 5 - Ayaktan yapýlan tedavilerde; bu Talimatýn 7. maddesinde belirtilen durumlar dýþýnda; reçetelere en fazla dört kalemi ve beþ günlük tedavi dozunu aþmayacak þekilde ilaç yazýlacaktýr. Ýlacýn beþ günlük tedavi dozunu belirlemek üzere, reçetede mutlak surette günlük kullaným dozu da belirtilecektir. Ancak, tedaviyi yapan tabip tarafýndan tedavinin 5 günü aþan sürede devam edeceðine karar verilen hastalýklarda kullanýlacak ilaçlar, taný ve tedavi süresi tabibin el yazýsý ile reçetede belirtilmek koþuluyla en fazla 1 aylýk doza kadar yazýlabilecektir. Ýlacýn piyasada bulunan en küçük ambalajý, 5 günlük tedavi dozundan fazla ise, bu ilaç bir kutu olarak verilecektir. Madde 6 - Saðlýk tesislerinde yatarak tedavi edilen sigortalýlar için gerekli olan ve bu hastane eczanesinde bulunmayan ilaçlar en fazla beþ günlük tedavi dozunu geçmeyecek þekilde reçeteye yazýlabilecektir. Bu reçetelerde mutlak surette günlük tedavi dozu da yazýlacak, 5 günlük tedavi dozunu aþan ilaç eczaneler tarafýndan kesinlikle verilmeyecektir. Bu Talimatta özel kullaným koþullarý (kültür antibiyogram, rapor gibi) belirtilen ilaçlarda bu koþullara da aynen uyulacaktýr. Ancak, saðlýk tesislerinde uzun süre yatarak tedavi gören tüberküloz hastalarýna, kullaným dozu belgelenmek kaydýyla l aylýk miktarda ilaç verilebilecektir (Ýlaç verilmesi ile ilgili Saðlýk Bakanlýðý'nca yapýlan düzenlemelere uyulacaktýr). Bu talimattaki özel düzenlemeler saklýdýr. Madde 7 - Bu Talimata ekli "Katký Payý Alýnmayacak Ýlaçlar Listesi"nde yer alan hastalýklarda kullanýlacak ilaçlar saðlýk kurulu raporuna (bu talimattaki özel düzenlemeler saklý kalmak kaydýyla) istinaden reçeteye en fazla 3 aylýk miktarda, diðer tabipler tarafýndan da yazýlabilecektir. Katký Payý Alýnmayacak Hastalýklar Listesinde bulunan hastalýklarda rapora istinaden bir reçetede 4 kalem sýnýrlamasý bulunmamaktadýr. Menopozda ve disfonksiyonel uterin kanamalarýnda kullanýlan ilaçlar ise rapor koþulu aranmaksýzýn en fazla 3 aylýk süreli ihtiyaç miktarýnda yazýlabilecektir. Bu konuda Talimatta belirtilen özel düzenlemeler saklýdýr. 7
6 Madde 8 - Ayaktan yapýlacak radyolojik tetkikler için kullanýlacak tüm iyonik ve noniyonik radyoopak maddelerden katký payý alýnmayacaktýr. Radyoopak maddelerden katký payý alýnmamasý için ayrýca rapor düzenlenmeyecek, reçeteye hastalýðýn tanýsý, ilgili tabipçe yazýlýp imzalanacaktýr. Ayaktan yapýlan intravenöz pyelografi (I.V.P.) ve histerosalfingografi (HSG) tetkiklerinde kullanýlacak noniyonik radyoopak maddelerden 50 ml.lik bir kutu kullanýlmasý halinde yalnýzca ilgili tabipçe reçete düzenlenecek, reçeteye radyoopak madde ve yapýlacak tetkikin ne olduðu açýkça yazýlacaktýr. 50 ml.yi aþan dozda noniyonik radyoopak madde kullanýlmasý halinde ise ayrýca kullanýlma nedeni ilgili uzman tabip tarafýndan reçeteye yazýlacaktýr. Madde 9 - Bu Talimattaki ilkelere uyulmaksýzýn düzenlenmiþ reçeteler sözleþmeli eczanelere geldiðinde ilaçlar verilmeyecek, gerekli düzeltmeler yapýlmak üzere reçete ilgili tabibe geri gönderilecektir. Madde 10 - Þahsi tedavi için yurtdýþýndan getirtilecek ilaçlar, reçeteye 3 aylýk doza kadar yazýlabilecektir. Bu konuda Genel Yazý ve Genelgelerle duyurulan gerekliliklere de aynen uyulacaktýr. ÜÇÜNCÜ BÖLÜM Bazý Özel Hastalýklara ve Ýlaç kullanýmýna Ýliþkin Düzenlemeler Madde 11 - Altýn Preparatlarý, Biyolojik Ajanlar, Leflunomid Kullaným Ýlkeleri: a) Altýn preparatlarý kullanýmýndan önce diðer antiromatizmal ilaçlar ile tedavi yapýlacaktýr. Bu tedaviye cevap alýnamamasý durumu, c maddesinde, adý geçen uzman tabiplik dallarýndan birinin bulunduðu Resmi saðlýk kurulu raporunda; taný, daha önce uygulanan tedavi, klinik bulgular, ilacýn adý, dozu ve kullaným süresi, ayrýntýlý tedavi þemasý detaylý olarak belirtilmek koþuluyla, bu ilaçlar reçeteye yazýlabilecektir. Tedavinin devamý gerektiðinde; bugüne kadar yapýlan tedaviden alýnan sonuçlar, tedavinin ne kadar süredir devam ettiði, ilacýn adý, dozu ve kullaným süresi ile ayrýntýlý tedavi þemasýný belirten bir rapor daha düzenlenecektir. b) Romatolojide biyolojik ajanlardan Anti TNF Ýlaçlarýn (Ýnfliksimab, Etanarsept, Adalimumab gibi) kullaným ilkeleri; - En az 2 farklý hastalýk modifiye edici antiromatizmal ilacý, en az 3er ay olmak üzere kullanmýþ olmasýna raðmen hastalýk aktivitesinin kontrol altýna alýnamadýðý (Hastalýk Aktivite Skoru DAS 28 > 5.1) veya yan etki nedeniyle bu ilaçlarýn kullanýlamadýðý resmi saðlýk kurulu raporunda belirtilen romatoid artritli hastalarda, - Biri maximum doz indometazin olmak üzere en az 2 nonsteroid antiinflamatuar ilacý maximum dozunda kullanmasýna raðmen yeterli cevap alýnamayan veya yan etkileri nedeniyle bu ilaçlarýn kullanýlamadýðý aksiyel tutulumlu ankilozan spondilitli hastalarda, 8
7 sulfasalazin veya metotreksat kullanýlmasýna raðmen cevap alýnamayan veya yan etkileri nedeniyle bu ilaçlarýn kullanýlamadýðý periferik eklem tutulumlu ankilozan spondilitli hastalarda (Bath Ankilozan Spondilit Hastalýk Aktivite Ýndeksi BASDAÝ > 4, Visual Analog Skoru VAS 0-10cm), - Hastalýk modifiye edici ajanlardan en az ikisi (tek tek veya kombinasyon þeklinde) standart dozda en az altý ay kullanýlmýþsa ve yanýt alýnmamýþsa (bir ay arayla yapýlmýþ iki ayrý muayenede en az üç hassas eklem ve en az üç þiþ eklem olmasý) veya toksisiteden dolayý altý aydan daha kýsa sürede yukarýdaki ilaçlar kesilmek zorunda kalmýþsa psöriatik artrit tedavisinde, Anti TNF ilaçlar kullanýlabilecektir. c) Yukarýda a ve b maddesinde belirtilen ilaçlar; Fizik Tedavi ve Rehabilitasyon, Eriþkin ve Pediyatrik Romatoloji, Ýmmunoloji Uzman tabiplerinin en az birinin bulunduðu Üniversite hastaneleri ile Eðitim ve araþtýrma hastanelerinde ve Immunoloji ve/veya Romatoloji uzman tabibinin bulunduðu Resmi saðlýk kurumlarýnda düzenlenecek resmi saðlýk kurulu raporuna dayanýlarak, bu uzman tabiplerden biri tarafýndan reçete edilebilecektir. Intravenöz formlarý, mutlaka ilacýn baþlandýðý Üniversite hastaneleri ile Eðitim ve araþtýrma hastanelerinde veya Ýmmunoloji ve/veya Romatoloji uzman tabibinin bulunduðu resmi saðlýk tesisinde uygulanacaktýr. Subkütan formlarýnýn ilk dozlarý ilacýn baþlandýðý Üniversite hastaneleri ile Eðitim ve araþtýrma hastanelerinde veya Ýmmunoloji ve/veya Romatoloji uzman tabibinin bulunduðu resmi saðlýk tesisinde tabip gözetiminde yapýlacak, uygun enjeksiyon tekniði konusunda hastaya veya hasta yakýnýna eðitim verildikten sonra ilgili uzman tabip uygun gördüðü taktirde hastane dýþýnda uygulanmak üzere iki aylýk dozlar halinde reçete edilebilecektir. Hastalar iki ayda bir Üniversite hastaneleri ile Eðitim ve araþtýrma hastanelerinde veya Immunoloji ve/veya Romatoloji uzman tabibinin bulunduðu resmi saðlýk tesisinde muayene edilecek, ilk ilaç etkinliði üç ay sonunda deðerlendirilecek, yeterli cevap alýnamamýþsa (Romatoid Artrit için, DAS 28'de 0.6 puandan, Ankilozan Spondilit için, BASDAÝ'de 2 birimden daha az düzelme olmasý, psöriatik artrit için, psöriatik artrit yanýt kriterlerine "PSARC" göre yanýt alýnamamasý durumunda) ilaca devam edilmeyecektir. d) Psoriyazis Vulgariste Üniversite hastaneleri ve Eðitim ve Araþtýrma hastanelerinde Cilt Hastalýklarý Uzman Tabibinin yer aldýðý diðer hastalýk modifiye edici ilaçlara dirençli olduðunu, kullanýlacak ilacýn miktar ve süresini belirten resmi saðlýk kurulu raporuna dayanýlarak Cilt Hastalýklarý Uzman Tabiplerince yazýlabilecektir. e) Yalnýzca Saðlýk Bakanlýðý'nca onay verilmiþ endikasyonlarda kullanýlacaktýr. f) Crohn hastalýðýnda; diðer tedavilere yanýt vermeyen fistülize vakalarda hastalýðýn taný, kullanýlan ilacýn ismi, günlük kullaným dozu ve kullaným süresini belirten Gastroenteroloji uzman tabibinin bulunduðu resmi saðlýk kurulu raporuna dayanýlarak Resmi saðlýk 9
8 tesislerinde klinik koþullarda uygulanacaktýr. g) Leflunomid Kullaným Ýlkeleri; Metotreksat kullanýmýný tolere edemediði ve diðer hastalýk modifiye edici ilaçlarla kontrol altýna alýnamadýðý belgelenmiþ romatoid artritli hastalarda Fizik Tedavi ve rehabilitasyon, Romatoloji veya Immunoloji Uzman tabiplerinden birinin yer aldýðý resmi saðlýk kurulu raporu ile verilebilir. Tedavinin devamýnda reçete bu uzman tabipler tarafýndan düzenlenecektir. Reçetelere en fazla üç aylýk tedaviye yetecek miktarda ilaç yazýlabilecektir. h) Tedavinin devamý yukarýdaki hastanelerde yapýlan tedaviden alýnan sonuçlar, tedavinin ne kadar süredir devam ettiði, ilacýn adý, dozu ve kullaným süresi ile ayrýntýlý tedavi þemasý düzenlenen bir yýllýk raporda belirtilecek yukarýdaki saðlýk tesislerinde reçetelenecektir. Madde 12 - Amfoterisin-B ve Kaspofungin Verilme Ýlkeleri: Hastanýn böbrek ve karaciðer fonksiyonlarý normal ise ilk tercih klasik Amfoterisin-B veya Fluconazol'dür. Klasik Amfoterisin-B'ye allerjik reaksiyon gösterdiðinin resmi saðlýk kurulu raporuyla belgelenmesi ya da hastanýn karaciðer veya böbrek fonksiyon testlerinin laboratuvar verileri ile bozuk olduðunun klinik olarak belgelenmesi hallerinde raporda belirtilen Lipozomal veya Lipid kompleks Amfoterisin-B kullanýlabilecektir. Kaspofungin Saðlýk Bakanlýðýnca onaylý endikasyonuna göre kullanýlabilir. Kaspofungin, Lipozomal ve Lipid Kompleks Amfoterisin-B EHU onayý ile mutlak surette yatarak tedavide kullanýlabilecektir. Madde 13 - Antidepresan ve Antipsikotik Ýlaçlarýn Kullaným Ýlkeleri: 13-1 Antidepresanlar, Psikiyatri (Eriþkin ve Çocuk) veya Nöroloji Uzman Tabipleri tarafýndan yazýlacaktýr. Resmi kurumlarýn saðlýk tesislerinde, en az bir Psikiyatri uzman tabibinin yer aldýðý resmi saðlýk kurulu raporuna dayanýlarak, diðer tabipler tarafýndan da yazýlabilecektir. Trisiklik ve tetrasiklik Antidepresan ilaçlar diðer tabiplerce de, yukarýdaki kýsýtlamalar olmaksýzýn, yazýlabilecektir Yeni nesil (Atipik) Antipsikotiklerle (Klozapin, Olanzapin, Risperidon, Amisülpirid, Ketiapin, Ziprasidon) tedaviye mutlaka psikiyatri uzman tabibince baþlanacaktýr. Resmi saðlýk tesislerinde, en az bir Psikiyatri Uzman tabibinin bulunduðu resmi saðlýk kurulu raporuna dayanýlarak diðer tabipler tarafýndan da yazýlabilecektir. Yeni nesil (atipik) antipsikotikler dýþýndaki antipsikotik ilaçlar diðer tabiplerce de yukarýdaki kýsýtlamalar olmaksýzýn yazýlabilecektir Psikiyatri kliniði dýþýnda yatan hastalara, klinikte tedavi eden tabiplerce baþlanmýþ olan antidepresan ilaçlar, tedavinin idamesi için, psikiyatri dýþýndaki diðer uzman tabipler tarafýndan da hasta taburcu olduðu tarihten itibaren en fazla iki aylýk dozda reçete 10
9 edilebilecektir. Tedavinin iki aydan daha uzun devamý gerektiðinde mutlaka psikiyatri veya nöroloji uzman tabipleri tarafýndan yazýlacaktýr Demansta, atipik antipsikotik ilaçlar, psikiyatri veya nöroloji uzman tabibi tarafýndan veya bu tabiplerden birinin bulunduðu resmi saðlýk kurulu raporuna dayanýlarak diðer tabiplerce yazýlacaktýr Antidepresanlar ve Antipsikotikler için düzenlenecek raporda, hastanýn tedavisinde kullanýlacak ilaç veya ilaçlarýn; jenerik ismi, günlük kullaným dozu, ilacýn kullanýlacaðý süre belirtilecektir. En fazla 12 ay süreli olarak düzenlenecek olan bu raporun yalnýzca resimli ilk nüshasý sigortalýya verilecek ve yeniden reçete edilmesi durumunda raporun arkasýnda bu amaçla hazýrlanmýþ sütunlara tabip tarafýndan yazýlacak, imzalanarak kaþe basýlacaktýr. Eczane tarafýndan da ilacýn verildiðine dair raporun arkasýna kaþe basýlarak imzalanacaktýr. Bir defada verilecek ilaç miktarý 2 aylýk dozu aþamayacaktýr. Madde 14 - Anti Rh Kullaným Ýlkeleri: a) Doðum Sonu Kullaným; Doðum belgesi, anne-bebek kan grubu belgesi, Direkt Coombs testi negatifliðini gösteren belge ve Anti Rh reçetesine dayanýlarak verilecektir. b) Düþük veya küretaj sonrasý kullanýmý; Resmi ve anlaþmalý saðlýk tesisinde annenin ve babanýn kan grubu belgesi, düþük veya küretaj olduðuna dair bir saðlýk kuruluþunun belgeleri ekinde Anti Rh reçetesine dayanýlarak verilecektir. c) Antenatal Kullaným; Anne-baba kan grubu belgeleri ve Ýndirekt Coombs testi negatifliðini gösteren belge ile saðlýk kurulu raporunda doz ve kullaným süresi belirtilerek verilecektir. d) Idiopatik (Ýmmun) Trombositopeni'de Kullanýmý: Ýntravenöz formu Rh pozitif ve splenektomisiz hastalarda resmi saðlýk kurulu raporunda doz ve kullaným süresi belirtilerek verilebilir. Reçeteler Hematoloji uzman tabibince düzenlenecektir. Madde 15 - Antitrombin III Kullaným Ýlkeleri: Hastalýðýn tanýsý, günlük kullaným dozu ve süresini belirten resmi saðlýk kurulu raporuna dayanýlarak en fazla 3 günlük dozda verilebilecektir. Yeniden kullanýmý gerektiðinde bir önce verilen ilacýn kullanýldýðýnýn yeni düzenlenecek raporda belirtilmesi ve bu raporda da hastalýðýn tanýsý, günlük kullaným dozu ve süresinin kayýtlý olmasý gereklidir. Madde 16 - Aþý Uygulamasý: Koruyucu nitelikteki aþýlar (Grip, kabakulak, kýzamýkçýk v.b) liste dýþý olup Kurumca karþýlanmayacaktýr. Ancak, tedavi edici içerikli olan ve hastalýðýn ölümcül sonuç doðurmasý nedeniyle kullanýmýnda mutlak zorunluluk bulunan aþýlarýn kullaným esaslarý aþaðýda belirtilmiþtir. 11
10 a) Allerji Aþýlarý Kurumca yalnýzca enjektabl yolla kullanýlan alerji aþýlarý verilecektir. Allerjik hastalýklarda aþý uygulanmasýna baþlanýlmasý için aþaðýda belirtilen esaslara uyulacaktýr. 1) Aþýlanmasý düþünülen hastalar en az bir yýl hastanýn bulunduðu yerdeki resmi saðlýk tesisinde çocuk, kulak-burun-boðaz, göðüs hastalýklarý veya bulunmamasý durumunda iç hastalýklarý uzman tabiplerince izlenecek, bu süre içersinde allerjenden kaçýnma konusunda bilgilendirilecek ve medikal tedavi uygulanacaktýr. Hastanýn durumunun izlenmesi için, medikal tedavi uygulayan uzman tabipçe bir dosya açýlacak ve tedavi ile ilgili tüm bilgiler bu dosyada toplanacaktýr. Dosyalar saðlýk tesisinde izleyen uzman tabip tarafýndan korunacak ve izin, hastalýk, nakil, istifa v.b. durumlarda birim amiri tarafýndan görevlendirilecek bir diðer uzman tabibe devredilecektir. Bu süre sonunda aþýya baþlanmasý düþünülüyorsa, hasta, Çocuk veya Eriþkin Alerji Uzmaný tabiplerince deðerlendirilecek ve bu uzmanýn yer aldýðý resmi saðlýk kurulu raporu ile aþý tedavisi baþlanabilecektir. Ýlk tedaviden sonraki reçeteler bu saðlýk kurulu raporuna dayanýlarak Çocuk hastalýklarý, Kulak Burun Boðaz, Göðüs Hastalýklarý, veya Göðüs Hastalýklarý Uzman Tabibinin bulunmadýðý yerlerde Dahiliye uzman tabiplerince yazýlabilecektir. 2) Aþý Uygulanmasýna Baþlama Kýstaslarý 2.1) Çocuk Hastalar Ýçin 2.1.1) Sadece doðal inhalan allerjenlere karþý duyarlýlýðý olan bronþiyal astým,allerjik rinit ve arý venom allerjisi tanýlarýnda aþý tedavisi uygulanabilecektir. Ýnhalan allerji tedavisine baþlanabilmesi için deri testi veya spesifik IgE tayini yapýlmasý gereklidir ) Hasta üç yaþýn üzerinde olmalýdýr ) Bronþiyal astým tanýsý olan hastalarda yedi yaþ ve üzerindekilerin solunum fonksiyon testi yapýlarak FEV1 deðerinin o yaþ için beklenen deðerin % 70' inden düþük olmamasý, reversibilitenin pozitif olmasý gereklidir ) Hastanýn kronik ve sistemik baþka bir hastalýðý olmamalýdýr. 2.2) Eriþkin Hastalar Ýçin 2.2.1) Sadece doðal inhalan allerjenlere karþý duyarlýlýðý olan bronþiyal astým, allerjik rinit ve arý venom allerjisi tanýlarýnda aþý tedavisi uygulanabilecektir. Ýnhalan allerji tedavisine baþlanabilmesi için deri testi ve spesifik IgE tayini yapýlmasý gereklidir ) Hastanýn kronik ve sistemik baþka bir hastalýðý olmamalýdýr. 2.3) Uygulama Kýstaslarý Uygulama, yukarýdaki baþlama kýstaslarýnýn açýkça belirtildiði resmi saðlýk kurulu raporuna dayanýlarak yapýlacaktýr. 12
11 2.3.1) Aþý uygulamasý tam teþekküllü resmi saðlýk tesisinde ve öncelikle hastayý allerji yönünden izleyen uzman tabibin kontrol ve sorumluluðunda, bu tabibin bulunmamasý durumunda yukarýda belirtilen branþ uzmanlarýndan biri tarafýndan yapýlacaktýr ) Allerji aþýlarýndan arý venom alerjisi dýþýndakilerden katký payý alýnacaktýr. 2.4) Sonlandýrma Kýstaslarý 2.4.1) Aþý uygulamasýndan 18 ayda tedaviye cevap alýnamazsa tedavi sonlandýrýlacaktýr ) Aþý uygulamasý arý venom allerjisi dýþýnda en fazla 5 yýl sürebilecektir. Uygulamalar birim amirliklerince denetlenecektir. b) Hepatit B, Kuduz, Tetanoz Aþýlarý Hepatit-B, kuduz, tetanoz aþýsý Saðlýk Bakanlýðý tarafýndan temin edildiðinden Kurum tarafýndan verilmeyecek, bu konuda yayýmlanmýþ Genel Yazý esaslarýna göre Ýl Saðlýk Müdürlüklerinden temin edilecektir. c) Hepatit A Aþýsý Kronik karaciðer hastalýðý olduðu laboratuvar verileriyle saptanan kiþilere Anti HAV IgG negatif ise Hepatit-A aþýsý uygulanabilecektir. d) Pnömokok, Meningokok ve H.Ýnfluenza Bakteri Aþýlarý Splenektomiden önce, sonra, organ transplantasyonu yapýlanlara, immun yetmezliði olan hastalara, tekrarlayan pnömokoksik menenjitlerde, astým, KOAH (Kronik Obstrüktiv Akciðer Hastalýðý), kronik kor pulmonale hastalýklarýnda gerekli durumlarda verilecektir. e) Suçiçeði Aþýsý ve Hiperimmun Globulini - Onkoloji - Organ transplantasyonu - Ýmmunosupresif tedavi alan hastalar - Kronik böbrek yetmezliði hastalarý - Kollagen doku hastalýðý - Ýmmun yetmezlikli hastalar - Bronþiyal astým hastalarý, - AIDS hastalarý - Kronik solunum, endokrin, kardiyovasküler hastalýðý olanlara ilgili uzman tabibin imzasý ile verilebilir. - Doðuma bir haftadan daha kýsa süre kaldýðýnda suçiçeði geçiren annenin bebeðine VZIG Ýmmunglobin ÝM uygulanacaktýr. Madde 17 - Botulismus Antitoksini: Botulismus zehirlenmelerinde Botulismus antitoksini aþaðýda belirtilen kurallara göre kullanýlacaktýr. a) Botulismus hastalýðýnýn tedavisine baþlamadaki gecikmenin hayati tehlike doðurabileceði gözönüne alýnarak elde mevcut belgelerle ilacýn temini iþlemlerine baþlanacak, bedeli firmaya ödenmeden önce aþaðýda (b) alt bendinde belirtilen rapor 13
12 ve belgelerin eksiksiz olmasýna dikkat edilecektir. b) Botulismus antitoksini Anestezi, Nöroloji ve Enfeksiyon Hastalýklarý Uzman Tabiplerince bunlarýn bulunmadýðý yerlerde Ýç Hastalýklarý ve Çocuk Hastalýklarý Uzman Tabiplerince kullanýlacaktýr. Botulismus hastalýðýnýn tedavisinde Botulismus antitoksini için belirlenen maksimum tedavi dozu (literatürde belirtilen doz) 250 ml lik serumlardan 2 adettir. Bu nedenle; - Tedavi için 2 kutu veya daha az serum kullanýlacak ise hasta adýna düzenlenecek saðlýk kurulu raporunda kullanýlacak ilacýn dozu ve tedavi süresi mutlaka belirtilecektir. - Tedavi için 2 kutuyu aþan miktarda serum gerektiði takdirde bu kez mutlaka hasta adýna hangi nedenle 2 kutuyu aþan serumun gerekli olduðunu açýklayan resmi saðlýk kurulu raporu düzenlenecek ve raporda kullanýlacak ilacýn tedavi süresi ve dozu belirtilmiþ olacaktýr. - Kullanýlan serumun miktarýna bakýlmaksýzýn, hasta tabelasý ile günlük hasta izleme formlarýnýn baþtabiplikçe onaylý birer örneði hasta faturasýna eklenecektir. Madde 18 - Botulismus Toksini Tip A a) Uygulama Üniversite hastaneleri ile Eðitim ve Araþtýrma Hastanelerinde aþaðýda b maddesinde belirtilen uzman tabipler tarafýndan klinik koþullarda yapýlacaktýr. b) Botulismus toksini, ancak organik nedenleri ekarte edilmiþ ve týbbi tedaviye cevap vermeyen vakalarda, bu durumu belirten ve kullanýlacak ilacýn dozuyla, kullaným süresini belirten resmi saðlýk kurulu raporuna dayanýlarak; Fizik Tedavi ve Rehabilitasyon, Nöroloji veya Göz Hastalýklarý uzman tabipleri tarafýndan reçeteye yazýlabilecektir. - Göz adelesi felçleri - Blefarospazm - Hemifasiyal spazm - Servikal distoni (spazmodik tortikollis) - EMG esnasýnda uygulanacak fokal distoni ve eriþkinlerde inme sonrasý fokal spastisite vakalarýnda kullanýlabilecektir. c) Pediyatrik Serebral Palside Botulismus Toksini Kullanýmý - Yalnýzca Üniversite hastaneleri ile Eðitim ve Araþtýrma Hastanelerinde pediyatrik nörolog tarafýndan tanýsý konulmuþ hastalarda, - 10 yaþa kadar sistemik hastalýðý, kemiksel deformite, kanama diyatezi, fikst kontroktür olmayan hastalarda, en fazla iki adeleye uygulanmak üzere, - Ortopedi, Fizik Tedavi ve Rehabilitasyon, Çocuk Nöroloji uzman tabiplerinin katýlýmýyla oluþturulacak resmi saðlýk kurulu raporuna dayanýlarak uygulanarak, - Tedaviden yarar görüp tekrarý düþünülen hastalarda altý ay sonra yeni bir resmi saðlýk kurulu raporu düzenlenerek en fazla iki uygulama, 14
13 -Tek seansta Botox için toplam 300 üniteyi, Dysport için 1000 üniteyi aþmamak üzere, yapýlacaktýr. Madde 19- Büyüme Hormonu Kullaným Esaslarý A) Çocuklarda; Boy sapmasý patolojik olan hastanýn (-2.5 SD'den daha negatif) en az altý ay veya olayýn özelliðine göre bir yýl büyüme hýzý izlendikten sonra, taný kriterlerine dayanýlarak resmi saðlýk tesislerinde Pediyatrik Endokrinoloji uzman tabibi tarafýndan büyüme hormonu eksikliði tanýsý konularak tedaviye baþlanacak ve yine aþaðýda belirtilen kriterlere göre tedavi sonlandýrýlacaktýr. a) Taný Kriterleri (Büyüme Geriliði Olan Çocuklarda Büyüme Hormonu Uygulanmasýna Baþlama) 1) Büyüme Hormonu, büyümeyi etkileyen sistemik bir hastalýðý olmayan bu bölümde yer alan uygulama kýstaslarýna uygun ve malnutrisyon saptanmayan hastalara verilebilecektir. 2) Yýllýk büyüme hýzý; yaþ 6 cm.nin altýnda, - 4 yaþ-puberte 4, 5 cm.nin altýnda, - Pubertede; izleme süresi ve büyüme hýzý hastanýn diðer bulgularýna göre Pediyatrik Endokrinoloji uzman tabibi tarafýndan deðerlendirilecektir, 3) Kemik yaþý; - Puberte öncesi için kronolojik yaþa göre en az 2 yýl geri olacaktýr. - Pubertal dönem için sadece epifizler açýk olacaktýr. 4) Ötiroid hastalarda uygulanan büyüme hormonu uyarý testlerinden en az ikisine (laboratuvarýn kriterlerine göre) yetersiz yanýt alýnarak büyüme hormonu eksikliði tanýsý konmalýdýr. 5) Hastanýn yaþ grubu ve pubertal bulgularý gerektiriyorsa büyüme hormonu testleri yapýlmadan mutlaka priming yapýlmalýdýr. 6) Boy sapmasý patolojik olan (yani -2, 5 SD'den daha kötü), yýllýk uzama hýzý yetersiz olan, kemik yaþý takvim yaþýna göre 2 yýldan daha fazla geri olan, ancak yapýlan iki farmakolojik uyarý testine yeterli yanýt alýnan hastalara uyku esnasýnda büyüme hormonu profili çýkartýlmalý ve hastada büyüme hormonu eksikliði olmamasýna raðmen eðer büyüme hormonu salýnýmýnda bir bozukluk sözkonusu ise, yani nörosekretuar disfonksiyon söz konusu ise hasta büyüme hormonu tedavisi alabilecektir. b) Puberte Kriterleri Erkeklerde Gonadarj (testis hacimlerinin) 4 ml. ve üzerine çýkmasý, kýzlarda T2 düzeyinde telarþýn olmasý, kýzlarda kemik yaþýnýn 8'in, erkeklerde 10'un üzerine çýkmasý, pubertenin baþlangýcý olarak kabul edilecektir. 15
14 c) Uygulama Kriterleri 1) Hastanelerde kemik yaþý ve büyüme hýzý tetkikleri yapýlarak "Büyüme Hormonu Eksikliði" öntanýsý konan hastalar, kesin taný ve tedavisinin saðlanmasý için, Pediyatrik endokrinoloji uzman tabibi bulunan resmi saðlýk tesisine gerekli belgelerle birlikte gönderilecektir. 2) Büyüme hormonu tedavisine karar verilen hastalarda içinde Pediyatrik Endokrinoloji uzman tabibinin bulunduðu resmi saðlýk kurulu raporuna dayanýlarak baþlanabilecektir. Rapora hastanýn taný ve tedavi þemasý ile ilgili ayrýntýlý bilgi yazýlacaktýr. Bu rapor en fazla bir yýl süreyle geçerli olacaktýr. Hastanýn tedavisi bu rapora dayanýlarak ve tedavi þemasýna göre resmi saðlýk tesislerinde görevli Pediyatrik endokrinoloji uzman tabibince yapýlacaktýr. 3) Hasta zorunlu haller dýþýnda; 3 aylýk aralýklarla tedavinin baþlandýðý merkeze kontrole gelecek, tedavi altýnda büyüme hýzý altý ay aralýklarla deðerlendirilecek, tedavinin devamý ya da sonlandýrýlmasý belirtilen kriterlere göre Pediyatrik Endokrinoloji uzman tabibince deðerlendirilecektir. 4) Bu hastalara en fazla 3 aylýk ilaç verilebilecektir. 5) Uygulama kriterleri hastanýn aktif ilaç kullandýðý süre esas alýnarak deðerlendirilecektir. d) Sonlandýrma Kriterleri 1) Epifiz hattý kapandýðýnda, 2) Yýllýk büyüme hýzý 5 cm. ve altýnda olduðunda, 3) Boy uzunluðu kýzlarda 1, 55 m.ye erkeklerde 1, 65 m.ye ulaþtýðýnda, tedavi sonlandýrýlacaktýr. 4) Tedavi esnasýnda boy 25. percentile ulaþtýðýnda tedavi sonlandýrýlacaktýr. e) Reçeteler Pediyatrik Endokrinoloji uzman tabibince yazýlacaktýr. B) Eriþkinlerde; 1) Epifiz hatlarý açýk olan eriþkin yaþtaki hastalarýn büyüme hormonu kullaným esaslarý, çocuk yaþ grubu ile aynýdýr. 2) Epifiz hatlarý kapalý olan hastalarda: a) Çocukluk yaþ grubunda büyüme hormonu eksikliði tanýsý konulup, büyüme hormonu tedavisi verilen ve epifizleri kapandýðý için tedavisi kesilen hastalarda tekrarlanan iki adet büyüme hormonu uyarý testine yetersiz yanýt alýnmýþsa(kontrendikasyon yoksa testlerden biri Ýnsülin Tolerans Testi olarak tercih edilmelidir.) eriþkin dozda büyüme hormonu tedavisi baþlanabilir. b) Eriþkin yaþ grubunda hipotalamohipofizer hastalýklara baðlý büyüme hormonu eksikliði düþünülen hastalarda, 2 adet büyüme hormonu uyarý testine yetersiz yanýt alýnmýþsa(kontrendikasyon yoksa testlerden biri Ýnsülin Tolerans Testi olarak tercih edilmelidir.) eriþkin dozda büyüme hormonu tedavisi baþlanabilir. 16
15 3) Hipofiz hormonlarýndan(prolaktin ve büyüme hormonu dýþýnda) bir veya daha fazla ek ön hipofiz hormonu eksikliði varsa, bir adet büyüme hormonu uyarý testi (kontrendikasyon yoksa Ýnsülin Tolerans Testi tercih edilmelidir.) taný için yeterlidir. 4) Ýnsülin tolerans testine göre büyüme hormonu eksikliði tanýsý için pik büyüme hormonu cevabýnýn 3mcg/L'den küçük olmasý gereklidir. 5) Büyüme hormonu, büyüme hormonu tedavisine karar verilen hastalara, Üniversite Hastanesi ve Eðitim ve Araþtýrma Hastanelerinin Endokrinoloji Bölümleri ile Endokrinoloji kliniði olan ihtisas hastanelerince hazýrlanan resmi saðlýk kurulu raporuna dayanýlarak baþlanabilecektir. Rapora hastanýn taný ve tedavi þemasý ile ilgili ayrýntýlý bilgi yazýlacaktýr. Bu rapor en fazla bir yýl süreyle geçerli olacaktýr. 6) Reçeteler Eriþkin Endokrinoloji uzman tabibince yazýlacaktýr. Madde 20 - Demans Hastalýðýnda Ýlaçlarýn Kullaným Ýlkeleri: Demans Ýlaçlarý, kýsa kognitif muayene ile demans saptanan hastalarda bir yýl süreli saðlýk kurulu raporuna dayanýlarak verilebilecektir. Madde 21 - Düþük Molekül Aðýrlýklý Heparinlerin Kullaným Ýlkeleri: Hastalýðýn tanýsý günlük dozu ve kullanýlacak ilaç miktarýný ve süresini gösteren resmi saðlýk kurumlarýnca düzenlenen resmi saðlýk kurulu raporuna dayanýlarak ilgili uzman tabiplerce yazýlacaktýr. Bu tür ilaçlarýn yeniden reçete edilmesi de yalnýzca uzman tabiplerce yapýlabilecektir. Hastanede yatan hastalarda ve acil müdahale gerektiren durumlarda acil servislerde rapor aranmaksýzýn bu ilaçlar diðer tabiplerce de kullanýlabilecektir. Madde 22 - Enteral ve Paranteral Beslenme Ürünleri Verilme Ýlkeleri: Enteral beslenme ürünleri, normal çocuk beslenmesinde kullanýlanlar hariç olmak üzere ayaktan tedavide malnütrisyonu olan veya oral beslenemeyen ancak enteral beslenmesi gereken tüm hastalara resmi saðlýk kurulu raporuyla kullanýlabilir. Parenteral beslenme ürünleri yatan hastalar dýþýnda Resmi saðlýk tesislerinde düzenlenmiþ resmi saðlýk kurulu raporu ile malign hastalara, kýsa barsak sendromuna, oral veya tüple beslenemeyen hastalara verilebilir. Raporda, hastalýðýn tanýsý, kullanýlacak beslenme ürününün Talimatta belirtildiði þekilde grubu veya ticari ismi, beden kitle indeksi, günlük kalori ihtiyacý ve buna göre belirlenen günlük kullaným miktarý açýkça yazýlacaktýr. Bu raporlarda kullaným süresi belirtilecek, ancak rapor en fazla 6 ay süreli olabilecektir Kronik nörolojik hastalýklarda ürün kullanýmý için verilen rapor süresi 1 yýl olabilecektir. Ýlaçlar en fazla iki aylýk miktarda verilecektir. Metabolik ve Enzim bozukluðu olan hastalara verilen mamalar bu hüküm dýþýnda olup, bu bölümün 31. maddesine göre verilecektir. Madde 23 - Eritropoietin ve Türevi Preparatlarýn Kullaným Ýlkeleri: a) Eritropoietin ve Türevi içeren ilaçlarýn kronik böbrek yetmezliði tedavisi gören 17
16 hastalara kullanýmý ve reçeteye yazýmý aþaðýda belirtilen esaslara göre yapýlacaktýr. 1) Eritropoietin tedavisinin baþlangýcýnda ve idamesinde; hastanýn resmi saðlýk tesislerinde Serum Demir ve Demir Baðlama Kapasitesi, Hemoglobin, Hemotokrit tetkikleri yapýldýktan sonra, varsa Eriþkin veya Çocuk Nefroloji Uzman tabibinin, bulunmadýðý taktirde Ýç Hastalýklarý veya Çocuk Hastalýklarý Uzman Tabiplerinden birinin yer aldýðý resmi saðlýk kurulu raporu düzenlenecektir. Hastanýn reçetesi bu rapora göre düzenlenecek ve raporun bir örneði reçeteye eklenecektir. Reçeteler uzman tabiplerce yazýlacaktýr. Eritropoietin reçetelerine hastalarýn kilolarý (kuru aðýrlýk) yazýlacak kg baþýna uygulanacak Eritropoietin miktarý ve hastanýn Hemoglobin ve Hemotokrit deðerleri reçetede belirtilecektir. Hemotokrit deðeri % 27 (yirmi yedi)'nin üstünde olan hastalara Eritropoietin tedavisine baþlanmayacaktýr. Bu deðer Hemoglobin için 9 (dokuz) gr/dl 'nin üstünde olacaktýr. Baþlangýç tedavisi olarak iskemik kalp hastalýðý bulunan hastalarda Htc deðeri 30'un altýna düþtüðünde Eriþkin veya Çocuk Nefroloji uzman tabibinin kararý ile Eritropoietin tedavisi baþlanabilir. Tedaviye baþlangýç dozu: Eritropoietin için, IU/kg/hafta, Darbopoietin için, mcg/kg/haftadýr. 2) Hemotokrit deðeri % 30 (otuz)'a ve Hemoglobin deðeri de 10 (on) gr/dl 'ye ulaþan hastalarda deðerlerin bu seviyede tutulmasýna yönelik hemoglobin deðeri 11 (onbir) gr/dl'yi ve hemotokrit deðeri % 33 (otuzüç)'ü aþmamak üzere idame tedavisine devam edilecektir. Ýdame dozu: Eritropoietin için, IU/kg/hafta, Darbopoietin için, mcg/kg/haftadýr. 3) Hastanýn tedavi öncesi yapýlan muayenesinde aþaðýdaki belirtilerin saptanmasý durumunda hastaya Eritropoietin uygulanmayacaktýr. - Demir eksikliði (TSAT <%20 ve/veya ferritin <100 µg/l) - Kan kaybý - Hemoliz - Kronik enfeksiyon - Alüminyum toksisitesi - Sekonder hiperparatiroidi - Ciddi týkayýcý periferik arter hastalýðý - Regüle edilemeyen hipertansiyon - Arterio-venöz fistül trombozu - Konvülsiyon - Kemik iliðini infiltre eden durumlar 18
17 4) Ýlaç uygulamasý sigortalýnýn tedavi ve izlem gördüðü merkezde yapýlacak ve gerekli kayýtlar, ilgili merkezce tutulan dosyalara iþlenecektir. 5) Eritropoietin direnci (3 ay boyunca tedavide kullanýlan Eritropoietin dozu 150 U/kg olduðu halde kan deðerlerinde deðiþme olmamasý Eritropoietin direnci olduðunu gösterir) durumunda tedaviye devam edilmeyecektir. 6) Eritropoietin kullanan hastalara, ilacýn takibinin yapýlabilmesi için resimli bir karne verilecektir. Bu karnede hastanýn; tanýsý, hematokrit, hemoglobin, serum demir ve demir baðlama bulgularý, kullanýlacak ilacýn adý, birim dozu, kullanma süresi ve kullaným dozu ile her defasýnda verilen Eritropoietin preparatýnýn adý ve miktarý ilgili tabip tarafýndan yazýlarak imzalanacaktýr. 7) Ýlaç yalnýzca subkutan uygulanacaktýr. b) Eritropoietin ve Türevlerini Ýçeren Ýlaçlarýn Kronik Böbrek Yetmezliðinin Dýþýnda Kullanýmý; 1) Eritropoietin ve Türevleri Ýçeren Ýlaçlarýn Kronik Böbrek Yetmezliði dýþýnda Saðlýk Bakanlýðýnca belirlenen endikasyonlarýnda ve Saðlýk Bakanlýðýnca belirlenen kurallarla resmi saðlýk tesislerinde düzenlenen Eriþkin veya Çocuk Hematoloji veya Onkoloji uzman tabiplerinden birinin yer aldýðý resmi saðlýk kurulu raporuna dayanýlarak kullanýlacaktýr. 2) Yeni doðanda eritropoietin kullanýmý: resmi saðlýk tesislerinde düzenlenen resmi saðlýk kurulu raporuna dayanýlarak, doðum aðýrlýðý 1500 gr.'ýn altýnda ve 32 gebelik haftasýndan önce doðan bebeklere 200 ÝU/kg hafta 3 kez 6 hafta süre ile uygulanabilir. c) Eritropoietin ve türevlerinden katký payý alýnmamasý için düzenlenen raporlarýn süresi en fazla 6 aylýk olabilecektir. Bir defada en fazla 1 aylýk ilaç verilebilecektir. d) Eritropoietin ve türevleri endikasyon muadili olarak birbirlerinin yerine kullanýlabilirler. Madde 24 - Gaucher Hastalýðý Tedavi Esaslarý: a)taný Kriterleri; Hastanýn enzim düzeyi (Glucocerebrosidaze) belirlenerek, enzimatik taný konulacak veya Mutasyon analizi yurt içinde resmi bir saðlýk kurumunda yapýlacaktýr. b)enzim tedavisine baþlama kriterleri; 1 - Tedavi endikasyonu olan hastalýk tipleri - Tip I (Non Nöronopatik Form) - Tip III (Kronik Nöronopatik Form) dür. - Tip II (Akut Nöronopatik Form) için enzim tedavisi yapýlmayacaktýr. 2 - Hastalýðýn tanýsý, Üniversite hastaneleri ile Eðitim ve Araþtýrma Hastanesinde, Çocuk veya Eriþkin Gastroenteroloji veya Metabolizma uzman tabiplerinin de yer aldýðý bir Saðlýk Kurulu tarafýndan konulacak ve hastaya taný ve tedavi ile ilgili tüm bilgileri içeren resmi saðlýk kurulu raporu düzenlenecektir. 19
18 c)tedavi Kriterleri; 1-Hastanýn tedavisi Çocuk veya Eriþkin Gastroenteroloji veya Metabolizma uzman tabiplerinin yer aldýðý resmi saðlýk kurulu tarafýndan düzenlenecek rapor esaslarý doðrultusunda, hastayý sevk eden birim tarafýndan yapýlacaktýr. Tip I ve Tip III için aþaðýdaki kriterlerden herhangi biri mevcut olan hastalar: 1.1 Tanýsý 5 yaþ altýnda konulan hastalar (Tip II hariç) 1.2 Hepatosplenomegali ile birlikte hipersplenizm bulgularý olan hastalar (Hb<9 gm, BK<3000, Plt<50000) veya Karaciðer Fonksiyon Testi bozukluðu 1.3 Semptomatik anemi (diðer nedenler ekarte edilip) 1.4 Kemik tutulumu (X-Ray, MRI veya CT ile gösterilmiþ lezyon veya akut aðrý krizi) 1.5 Akciðer tutulumu 1.6 Aðýr büyüme geriliði 1.7 Moleküler taný yapýlabilirse: Aðýr genotipi (N370S/N370S dýþýnda) olan hastalarda yukarýdaki bulgular daha hafif olsa da verilebilir (asemptomatik olmayacak) 2. Tip II (Akut Nöronopatik Form) ve Nörolojik bulgusu olanlarda Alfa Galactosidase tedavisi uygun deðildir. 3. Enzim preparatý reçeteye Çocuk ve Eriþkin Metabolizma veya Gastroenteroloji Uzman Tabiplerince 3 ayý aþmayacak miktarda ve hastanýn tedavisini yürüten merkez tarafýndan yazýlacak ve ilaçlar hastaya 1'er aylýk miktarda verilecektir. 4. Kullaným dozu iki haftada bir U/kg olup, bu tedavi klinik koþullarda uygulanacaktýr. c) Tedavinin Kesilmesi; 1 - Hasta 3 ayda bir taný ve tedavi aldýðý merkezde kontrol edilecektir. Ýzlemde karaciðerdalak boyutlarýnýn deðerlendirilmesi ve tam kan sayýmý ile karaciðer enzimlerinin tayini, eðer gerek görülür ise 1 yýllýk periyotlar ile karaciðer-dalak boyutlarýnýn volumetrik, kemik lezyonlarýnýn takibi uygundur. 2 - Hastanýn tedavisinin yapýldýðý resmi saðlýk tesisinde hastalar adýna dosyalar açýlacak ve tüm bilgiler bu dosyada muhafaza edilecektir. 3 - Tanýyý koyan resmi saðlýk tesisi tarafýndan hastanýn tedaviye baþlama öncesi kriter/kriterlerindeki düzelme durumu dökümante edilecektir. 4 - Halen tedavi almakta olan hastalarýn tedaviye devam edip etmeyecekleri Talimatta yer alan tedavi kriterlerine göre deðerlendirilecektir. 5 - Tedaviye cevap alýnamadýðý belirlenen durumlarda tedavi kesilecektir ( Ýzleme parametrelerinde tedavi baþlandýktan en az 6 ay sonra hiçbir düzelme meydana gelmez ise). Madde 25 - Glokom Ýlaçlarý: Glokom ilaçlarý ile tedaviye Göz Hastalýklarý Uzman tabibi tarafýndan baþlanacaktýr. Göz Hastalýklarý uzman tabibinin bulunduðu, kullanýlacak ilacýn etken maddesi, kullaným dozu ve süresini belirten resmi saðlýk kurulu raporu mevcut ise diðer tabiplerce de reçeteye yazýlabilecektir. 20
19 Madde 26 - Hiperimmun Gamaglobulinler ve RSV immunglobulini: a) Resmi ve sözleþmeli saðlýk tesislerinde yatan hastalara hastalýðýn tanýsý ve kullanýlan Hiperimmunglobulinin dozu ve ne kadar süre kullanýlacaðýný belirten resmi saðlýk kurulu raporu ile verilebilecektir. Hepatit B, Tetanoz, Kuduz immun serumlarý, hayati önemi haiz olduðundan enfeksiyon hastalýklarý uzman tabibi veya bunun bulunmadýðý durumlarda tedaviyi yapan tabip tarafýndan birim amiri onayýyla verilebilecektir. b) Palivizumab etken maddesini içeren ilaçlar, 35 haftanýn altýnda doðan ve bronkopulmoner displazi tanýsý almýþ 12 aylýktan küçük bebeklere Yeni doðan uzman tabibi bulunan resmi saðlýk kurumlarýnda bu tabibin yer aldýðý ve ilacýn dozu, süresi ve kullaným aralýðýný belirten rapora dayanýlarak, Ekim-Mart aylarý arasýnda, ayda bir kez ve en fazla 2 yaþýna kadar kullanýlabilir. Reçeteler Yeni Doðan veya Çocuk Hastalýklarý Uzman tabiplerince düzenlenir. Madde 27 - Human Albumin Verilme Ýlkeleri: Resmi saðlýk tesislerinde yatarak tedavi gören sigortalýlara Human Albumin preparatlarý albümin düzeyi 2.5 g/dl ve altýnda ise uzman tabip imzasýyla verilebilir. Hastane eczanesinde bulunmadýðý durumlarda, günlük doz ve tedavi protokolünü ve kan albümin düzeyinin 2.5g/dl ve altýnda olduðunu gösterir saðlýk kurulu raporuna dayanýlarak en fazla 3 (üç) günlük dozda verilecektir. Dializ tedavisi gören hastalarda Human Albumin preparatlarý doz, tedavi ve kan albümin seviyesinin 2.5g/dl ve altýnda olduðunu gösterir saðlýk kurulu raporuna dayanýlarak klinik koþullarda uygulanacaktýr. Madde 28 - Ýnterferon Kullaným Ýlkeleri: a) Kronik Viral Hepatitlerde Alfa Ýnterferon Kullaným Ýlkeleri; 1) Kronik viral hepatitlerde Çocuk veya Eriþkin Gastroenteroloji ve Enfeksiyon Hastalýklarý Uzman tabibi bulunan resmi saðlýk tesislerinde bu uzman tabiplerden birinin yer aldýðý resmi saðlýk kurulu raporuna dayanýlarak aþaðýda belirtilen kriterlere göre uygulanacaktýr. 2) Kronik Hepatit B'de 3-6 aydan fazla süredir ALT düzeyleri normalin en az 1,5 katýndan fazla, HBV DNA pozitif olan histolojik olarak kronik hepatit saptanan kompanse kronik Hepatit-B'li hastalara uygulanýr. Tedavi süresi 6 ayý, tedavi dozu haftada 35 milyon üniteyi geçemez. 3) Kronik Hepatit C'de ALT düzeyleri normalin en az 1,5 katýndan fazla, Anti HCV ve HCV RNA'sý pozitif histolojik olarak kronik hepatit saptanan, kompanse karaciðer hastalýðý bulgularý olan hastalara Ribavirinle kombine uygulanýr. Ancak Ribavirin kontrendikasyonu var ise interferon monoterapisi uygulanacaktýr. Gerek monoterapide gerekse Ribavirin + Ýnterferon kombine tedavisinin ayýnda tedaviye cevap alýnamamasý halinde tedavi sonlandýrýlacaktýr. Tedavi süresi 12 ayý, tedavi dozu haftada 18 milyon üniteyi geçemez. 21
20 4) Hepatit-D'de 6 aydan fazla süredir ALT düzeyi normalin en az 1,5 katýndan fazla, Anti deltasý pozitif olan histolojik olarak kronik Hepatit saptanan, kompanse karaciðer hastalýðý bulgularý olan hastalara uygulanýr. Tedavi süresi 24 ayý, tedavi dozu haftada 35 milyon üniteyi geçemez. 5) Pegile Ýnterferonlarýn kullaným ilkeleri; 3.maddede belirtilen Kronik Hepatit C tedavisine baþlama kriterlerine uygun olarak yalnýz 18 yaþýn üzerindeki hastalarda, naive kronik Hepatit-C vakalarýnda ve interferon tedavisinde nüks hastalarda kullanýlacaktýr. Tedavi süresi 12 ayý geçemeyecektir ayda tedaviye yanýt alýnamamasý durumunda tedavi kesilecektir. Madde 29 - Kanser Ýlaçlarý Verilme Ýlkeleri: a) Resmi saðlýk tesislerinde kemoterapi yapýlacak kanserli hastalara Saðlýk Bakanlýðýnýn ilgili mevzuatý doðrultusunda, kür tedavisi uygulanýyor ise kür protokolünü gösterir saðlýk kurulu raporuna dayanýlarak bir kürlük, kür tedavisi uygulanmayanlarda ise en fazla 1 aylýk dozda ilaç verilebilir. Ancak; Hormonlar ve Hormon Antagonistleri ile Maligniteye baðlý metastatik olgularda kullanýlan yardýmcý ilaçlar, saðlýk kurulu raporu ile 3 aylýk dozlarda verilebilir. b) Kanser ilaçlarý diðer ilaçlarda olduðu gibi Saðlýk Bakanlýðýnýn izin verdiði endikasyonlarda kullanýlacaktýr. Bu nedenle resmi saðlýk kurulu raporunda ilk tedavi veya rekürrent hastalýkta kullaným muhakkak belirtilecektir. Bir kanser ilacýnýn endikasyonu dýþýnda talep edilmesi halinde Talimatýn 4-e Maddesi doðrultusunda iþlem yapýlacaktýr. c) Bu ilaçlar hastalýðýn tanýsý, günlük dozu, kullanýlacak ilaç miktarý ve süresini gösteren resmi saðlýk kurumlarýnca düzenlenen resmi saðlýk kurulu raporuna dayanýlarak ilgili uzman tabiplerce yazýlacaktýr. Bu tür ilaçlarýn yeniden reçete edilmesi yalnýzca uzman tabiplerce yapýlabilecektir. Madde 30 - Klopidogrel kullaným ilkeleri: Klopidogrel içeren ilaçlar yalnýzca aþaðýda belirlenen durumlarda kullanýlabilir. a) Koroner veya periferik stent uygulanan hastalarda toplam 6 ayý geçmemek üzere, kullaným süresinin belirtildiði, resmi saðlýk kurulu raporu ile, Kardiyoloji, Ýç hastalýklarý ve Kalp Damar Cerrahisi Uzman tabipleri tarafýndan kullanýlabilir. b) Akut koroner sendrom tanýsýyla hastaneye yatýrýlýp EKG deðiþikliði veya troponin pozitifliði tespit ve dokümante edilmiþ olan miyokard infarktüsü veya anstabil angina hastalarýnda resmi saðlýk tesislerinde düzenlenen ve ilacýn kullaným gerekçesi, dozu ve en fazla toplam 9 ayý geçmemek üzere kullaným süresinin belirtildiði, resmi saðlýk kurulu raporu ile, Kardiyoloji, Ýç hastalýklarý ve Kalp Damar Cerrahisi Uzman tabipleri tarafýndan kullanýlabilir. Nüks vakalarda ilaç kullaným süresi yeniden baþlatýlabilir. 22
21 c)asetilsalisilik asit alerjisi veya major gastrointestinal intolerans nedeniyle asetilsalisilik asit kullanýlmasýna kontrendikasyon bulunduðunun gastroenteroloji uzman tabibince belirlenmesi ve Resmi Saðlýk Tesislerinde düzenlenecek resmi saðlýk kurulu raporunda diðer antiagregan ilaçlarýn kullanýlamama gerekçesi ile birlikte belirtilmesi halinde ve en fazla 1 yýlý geçmemek üzere kullaným süresi belirtilerek; kalp kapak biyoprotezi bulunanlarda, koroner arter hastalýðý veya týkayýcý periferik arter hastalýðý veya serebral iskemik olayý (iskemik inme) tespit ve dokümante edilen yüksek riskli hastalarda ve Kardiyoloji, Ýç hastalýklarý, Nöroloji ve Kalp Damar Cerrahisi ve Hematoloji Uzman tabipleri tarafýndan kullanýlabilir. d) Yatan hastalarda rapor þartý aranmadan ilgili uzman tabip tarafýndan yazýlabilecektir. Madde 31 - Doðuþtan Metabolik Hastalýklar ve Malabsorbsiyona Neden Olan Diðer Hastalýklar: a) Çocuk mamalarý, gýda olmasý nedeniyle listeye dahil edilmemiþtir. Ancak; Doðuþtan metabolik hastalýðý olan hastalarýn kullandýklarý özel mamalar ile bu hastalýk nedeniyle besleme desteði alýnmasý gereken modüler ürünler, Enzim bozukluðu olan kistik fibrozisli hastalar için tedavi edici içerikli olanlar ile malabsorbsiyona neden olan bir hastalýðý olan hastalarýn kullandýklarý özel mamalar, Ýki yaþýna kadar inek sütü alerjisi olan bebeklerin kullandýklarý özel (baþlangýç ve devam) mamalarý, Resmi saðlýk tesislerince düzenlenen, taný ve tedaviye iliþkin ayrýntýlý bilgileri içeren resmi saðlýk kurulu raporu alýnmasý koþuluyla verilebilir. Metabolik enzim bozukluðu olan hastalýklarda taný metabolizma uzman tabibinin bulunduðu resmi saðlýk tesisinde konulacak ve hastalýðýn tanýsý, kullanýlacak ilaçlarýn cins, kullaným dozu ve süresi metabolizma uzman tabibinin yer aldýðý resmi saðlýk kurulu raporu ile tespit edilecektir. Tedavinin devamý bu rapora dayanýlarak mahallinde Çocuk ve Ýç Hastalýklarý Uzman Tabiplerince yapýlabilecektir. Tanýya ait Metabolizma Uzman Tabibinin yer aldýðý rapor hasta tarafýndan muhafaza edilecek, rapor süresinin bitiminde yeni rapor bu rapora dayanýlarak Çocuk ve Ýç Hastalýklarý Uzman Tabiplerince de düzenlenebilecektir.hasta istenildiði zaman tanýyý belgeleyen bu raporu ibraz etmek zorundadýr. Bu tür mamalarý kullanan hastalara resimli bir mama karnesi verilecek ve bu karneye de tanýya ait raporun tarih, sayýsý ve verildiði saðlýk tesisinin adý yazýlacaktýr. Her mama alýþý karneye iþlenecektir. Bu grup hastalarýn tedavisi için gereken unlar da mamalarda olduðu gibi ayný þekilde verilecek ve karneye iþlenecektir. Ancak, mamül ürünler (makarna, bisküvi v.b) bu kapsamýn dýþýndadýr. 23
22 b) Çölyak Hastalýðýnda; özel formüllü unlar ve mamul ürünler, Çocuk veya Eriþkin Gastroenteroloji uzman tabibinin yer aldýðý resmi saðlýk kurulu raporuna dayanýlarak verilecektir. Tedavinin devamý için özel formüllü unlar ve mamul ürünler, bu uzmanlar veya Çocuk ve Ýç hastalýklarý Uzman tabiplerince de ayda en fazla 5 kg (5 kg'ýn en fazla 2 kg'ý mamul ürün olabilecektir) hesabýyla reçeteye yazýlabilecek ve katký payý alýnarak verilecektir. Madde 32 - Multiple Skleroz Hastalýðýnda Beta interferon ve Copolimer-I Kullaným Ýlkeleri: Hastalarýnýn seçiminde uygulanacak kriterler: a) Hastaya klinik ve laboratuvar olarak kesin Multipl Skleroz tanýsý konulmuþ olmasý, b) Disabilite skorunun (E.D.S.S.) 0-5,5 arasýnda olmasý, hastanýn yardýmsýz olarak en az 100 m. yürüyebilmesi, c) Olgularýn Remitting-Relapsing veya sekonder progresif türü olmasý, d) Manyetik Rezonans Görüntüleme tetkikinde altý ay içerisinde plaklarýn volümü veya sayýsýnda artýþýn belirlenmesi, e) Ýki yýl içerisinde en az iki atak geçirmesi, yeni vak'alarda ise bir yýl içerisinde iki atak geçirmiþ olmasý, gerekmektedir. Ýlaç Üniversite hastaneleri ile Eðitim ve Araþtýrma hastanelerinde Nöroloji uzman tabibinin bulunduðu resmi saðlýk kurulu raporuna dayanýlarak verilecektir. Reçeteler Nöroloji uzman tabibi tarafýndan yazýlacaktýr. Tedavi için gerekli ilaçlarýn Üniversite hastaneleri ile Eðitim ve Araþtýrma Hastanelerinde uygulanmasý esas olmakla birlikte gerekli durumlarda hastaya uygulama ile ilgili eðitim verildikten sonra ilaçlar bir aylýk dozu aþmayacak þekilde verilebilir. Madde 33 - Osteoporoz ilaçlarýnýn kullaným ilkeleri: Aþaðýdaki hasta gruplarýnda Osteoporoz tedavisinde kullanýlan bifosfonatlarýn veya diðer osteoporoz ilaçlarýnýn kullanýmýnda (calsitonin, raloksifen v.b.) resmi kuruluþlarca saðlýk kurulu raporu düzenlenecek, düzenlenen raporda tedavi süresi belirtilecek, DEXA yöntemiyle belirlenmiþ kemik mineral yoðunluk deðerini gösteren belge rapora eklenecektir. a) Osteoporotik patolojik kýrýk bulunan ve lomber bölgeden posteroanterior veya lateral yapýlan kemik mineral yoðunluk (KMY) ölçümünde total L2-4 (veya total L1-4) veya femoral bölgeden yapýlan KMY ölçümünde total femur veya femur boynundan elde edilen "T"deðerlerinden herhangi birinin -1 veya daha düþük olduðu hastalarda, b) Lomber bölgeden posteroanterior veya lateral yapýlan KMY ölçümünde total L2-4 (veya total L1-4) veya femoral bölgeden yapýlan KMY ölçümünde total femur veya femur boynundan elde edilen "T" deðerlerinden herhangi birinin -2,5 veya daha düþük olduðu hastalarda, 24
Tebliğ. 2005 Yılı Sosyal Sigortalar Kurumu Başkanlığı İlaç Listesi ve Uygulama Talimatı (Seri No:2005/1) R.G.Tarih: 11.04.2005 R.G.
 Tebliğ 2005 Yılı Sosyal Sigortalar Kurumu Başkanlığı İlaç Listesi ve Uygulama Talimatı (Seri No:2005/1) R.G.Tarih: 11.04.2005 R.G.Sayı: 25783 Yasal Dayanak Madde 1 - Bu Talimat, Sosyal Sigortalar Kurumu
Tebliğ 2005 Yılı Sosyal Sigortalar Kurumu Başkanlığı İlaç Listesi ve Uygulama Talimatı (Seri No:2005/1) R.G.Tarih: 11.04.2005 R.G.Sayı: 25783 Yasal Dayanak Madde 1 - Bu Talimat, Sosyal Sigortalar Kurumu
2005 YILI BAĞ-KUR UYGULAMALARINA AÇIKLIK GETİREN TALİMAT
 2005 YILI BAĞ-KUR UYGULAMALARINA AÇIKLIK GETİREN TALİMAT (Yürürlülük Tarihi: 20 Nisan 2005) Bilindiği üzere, Kurumumuz sigortalı ve hak sahiplerinin reçete muhteviyatı ilaçlarını eczanelerden temin edebilmeleri
2005 YILI BAĞ-KUR UYGULAMALARINA AÇIKLIK GETİREN TALİMAT (Yürürlülük Tarihi: 20 Nisan 2005) Bilindiği üzere, Kurumumuz sigortalı ve hak sahiplerinin reçete muhteviyatı ilaçlarını eczanelerden temin edebilmeleri
2005 Mali Yılı Bütçe Uygulama Talimatı ( Sıra No: 18 ) (Tedavi Yardımı)
 2005 Mali Yılı Bütçe Uygulama Talimatı ( Sıra No: 18 ) (Tedavi Yardımı) R.G. Tarihi:15.12.2005 R.G. Sayısı:26024 Bilindiği üzere, tedavi yardımına ilişkin (4) sıra numaralı 2005 Mali Yılı Bütçe Uygulama
2005 Mali Yılı Bütçe Uygulama Talimatı ( Sıra No: 18 ) (Tedavi Yardımı) R.G. Tarihi:15.12.2005 R.G. Sayısı:26024 Bilindiği üzere, tedavi yardımına ilişkin (4) sıra numaralı 2005 Mali Yılı Bütçe Uygulama
 www.adanaeo.org.tr Adana Eczacý Odasý Yýl:1 Sayý:4 Aralýk 2005 TEB Kongresi 15-18 Aralýk 2005 te yapýldý. Adana Eczacý Odasý geçmiþten bugüne TEB Kongrelerinde etkili olarak temsil edildi. Bu dönemde TEB
www.adanaeo.org.tr Adana Eczacý Odasý Yýl:1 Sayý:4 Aralýk 2005 TEB Kongresi 15-18 Aralýk 2005 te yapýldý. Adana Eczacý Odasý geçmiþten bugüne TEB Kongrelerinde etkili olarak temsil edildi. Bu dönemde TEB
TÜSAD İnfeksiyon Çalışma Grubu
 TÜSAD İnfeksiyon Çalışma Grubu Neden Grip Aşısı Yaptırmalıyız? Grip her yýl görülür ve günlük yaþamý etkiler Her yýl trafik kazalarýndan daha fazla insan grip nedeniyle ölmektedir. Özellikle çocuklar,
TÜSAD İnfeksiyon Çalışma Grubu Neden Grip Aşısı Yaptırmalıyız? Grip her yýl görülür ve günlük yaþamý etkiler Her yýl trafik kazalarýndan daha fazla insan grip nedeniyle ölmektedir. Özellikle çocuklar,
 YÜRÜRLÜKTE BULUNAN TEDAVÝ YARDIMINA ÝLÝÞKÝN UYGULAMA TEBLÝÐÝ ÝLE 15.06.2007 TARÝHÝNDE YÜRÜRLÜÐE GÝRECEK OLAN 8 SIRA NOLU TEBLÝÐ ARASINDAKÝ FARKLILIKLAR Hak sahiplerinin saðlýk kurum ve kuruluþlarýnda yapýlan
YÜRÜRLÜKTE BULUNAN TEDAVÝ YARDIMINA ÝLÝÞKÝN UYGULAMA TEBLÝÐÝ ÝLE 15.06.2007 TARÝHÝNDE YÜRÜRLÜÐE GÝRECEK OLAN 8 SIRA NOLU TEBLÝÐ ARASINDAKÝ FARKLILIKLAR Hak sahiplerinin saðlýk kurum ve kuruluþlarýnda yapýlan
 EK-2/C AYAKTA TEDAVÝDE SAÐLIK RAPORU (UZMAN HEKÝM RAPORU/SAÐLIK KURULU RAPORU) ÝLE VERÝLEBÝLECEK ÝLAÇLAR LÝSTESÝ 1. Ýmmünsupresifler (topikal formlarý dahil) 2. Betanekol 3. Bifosfonatlar (Madde 12.7.17
EK-2/C AYAKTA TEDAVÝDE SAÐLIK RAPORU (UZMAN HEKÝM RAPORU/SAÐLIK KURULU RAPORU) ÝLE VERÝLEBÝLECEK ÝLAÇLAR LÝSTESÝ 1. Ýmmünsupresifler (topikal formlarý dahil) 2. Betanekol 3. Bifosfonatlar (Madde 12.7.17
34
 EK - 2A SÝSTEMÝK ANTÝMÝKROBÝK VE DÝÐER ÝLAÇLARIN REÇETELEME KURALLARI Tedavi için gerekli görülen antibiyotikler, aþaðýda belirtilen esaslara göre reçete edilecektir. Aþaðýdaki Listedeki kýsaltma ve ibareler
EK - 2A SÝSTEMÝK ANTÝMÝKROBÝK VE DÝÐER ÝLAÇLARIN REÇETELEME KURALLARI Tedavi için gerekli görülen antibiyotikler, aþaðýda belirtilen esaslara göre reçete edilecektir. Aþaðýdaki Listedeki kýsaltma ve ibareler
2. Talimatın 11 inci maddesi aşağıdaki şekilde değiştirilmiştir. 11. Reçetelerin Düzenlenmesi
 Tebliğ Maliye Bakanlığından: 2005 Mali Yılı Bütçe Uygulama Talimatı ( Sıra No: 18 ) (Tedavi Yardımı) Bilindiği üzere, tedavi yardımına ilişkin (4) sıra numaralı 2005 Mali Yılı Bütçe Uygulama Talimatı (Bundan
Tebliğ Maliye Bakanlığından: 2005 Mali Yılı Bütçe Uygulama Talimatı ( Sıra No: 18 ) (Tedavi Yardımı) Bilindiği üzere, tedavi yardımına ilişkin (4) sıra numaralı 2005 Mali Yılı Bütçe Uygulama Talimatı (Bundan
SUT HEPATİTLERİ NASIL TEDAVİ EDİYOR? Doç. Dr. Cemal Bulut Ankara Eğitim ve Araştırma Hastanesi
 SUT HEPATİTLERİ NASIL TEDAVİ EDİYOR? Doç. Dr. Cemal Bulut Ankara Eğitim ve Araştırma Hastanesi 1990 yılı 1 Şubat 2003 Sayı : 25011 11 Şubat 2004, Sayı: 25370 2004 Mali Yılı Bütçe Uygulama Talimatı (
SUT HEPATİTLERİ NASIL TEDAVİ EDİYOR? Doç. Dr. Cemal Bulut Ankara Eğitim ve Araştırma Hastanesi 1990 yılı 1 Şubat 2003 Sayı : 25011 11 Şubat 2004, Sayı: 25370 2004 Mali Yılı Bütçe Uygulama Talimatı (
2007/82 Nolu SGK GENELGESÝ(Fatura Bedellerinin Ödenmesinde Karþýlaþýlan Sorunlar) Cuma, 26 Ekim 2007
 2007/82 Nolu SGK GENELGESÝ(Fatura Bedellerinin Ödenmesinde Karþýlaþýlan Sorunlar) Cuma, 26 Ekim 2007 GENELGE 2007/ 82 2007/46 sayýlý Fatura Bedellerinin Ödenmesi konulu Genelge gereði Kurum web sayfasýnda
2007/82 Nolu SGK GENELGESÝ(Fatura Bedellerinin Ödenmesinde Karþýlaþýlan Sorunlar) Cuma, 26 Ekim 2007 GENELGE 2007/ 82 2007/46 sayýlý Fatura Bedellerinin Ödenmesi konulu Genelge gereði Kurum web sayfasýnda
Dövize Endeksli Kredilerde KKDF
 2009-10 Dövize Endeksli Kredilerde KKDF Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/10 Dövize Endeksli Kredilerde KKDF 1. Genel Açýklamalar: 88/12944 sayýlý Kararnameye iliþkin olarak
2009-10 Dövize Endeksli Kredilerde KKDF Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/10 Dövize Endeksli Kredilerde KKDF 1. Genel Açýklamalar: 88/12944 sayýlý Kararnameye iliþkin olarak
YAZI ÝÞLERÝ KARARLAR VE TUTANAKLAR DAÝRE BAÞKANLIÐI
 YAZI ÝÞLERÝ KARARLAR VE TUTANAKLAR DAÝRE BAÞKANLIÐI ENCÜMEN VE KARARLAR ÞUBE MÜDÜRLÜÐÜ 5393 Sayýlý Belediye Kanununun 35. maddesi gereði Baþkanlýk Makamýnca Encümen Gündemine girmek üzere havale edilen
YAZI ÝÞLERÝ KARARLAR VE TUTANAKLAR DAÝRE BAÞKANLIÐI ENCÜMEN VE KARARLAR ÞUBE MÜDÜRLÜÐÜ 5393 Sayýlý Belediye Kanununun 35. maddesi gereði Baþkanlýk Makamýnca Encümen Gündemine girmek üzere havale edilen
T.C MALİYE BAKANLIĞI. Bütçe ve Mali Kontrol Genel Müdürlüğü. Sayı: B.07.0.BMK Konu: Tedavi Yardımı *
 T.C MALİYE BAKANLIĞI Bütçe ve Mali Kontrol Genel Müdürlüğü Sayı: B.07.0.BMK.0.18.100. Konu: Tedavi Yardımı 01.03.2007 * 3704... BAKANLIĞINA... BAŞKANLIĞINA... GENEL MÜDÜRLÜĞÜNE... VALİLİĞİNE... REKTÖRLÜĞÜNE
T.C MALİYE BAKANLIĞI Bütçe ve Mali Kontrol Genel Müdürlüğü Sayı: B.07.0.BMK.0.18.100. Konu: Tedavi Yardımı 01.03.2007 * 3704... BAKANLIĞINA... BAŞKANLIĞINA... GENEL MÜDÜRLÜĞÜNE... VALİLİĞİNE... REKTÖRLÜĞÜNE
2006 MALÝ YILI BÜTÇE UYGULAMA TALÝMATI NDA DÝKKAT EDÝLECEK HUSUSLAR Deðerli Meslektaþým, 2006 Mali Yýlý Bütçe Uygulama Talimatý (BUT) tarih
 2006 SSK SÖZLEÞMESÝNDE DÝKKAT EDÝLECEK HUSUSLAR Deðerli meslektaþým, Odamýz yönetim kurulu ve mevzuat komisyonumuz tarafýndan SSK protokolü incelenmiþ olup farklýlýklar ve deðiþiklikler aþaðýdadýr. 1)
2006 SSK SÖZLEÞMESÝNDE DÝKKAT EDÝLECEK HUSUSLAR Deðerli meslektaþým, Odamýz yönetim kurulu ve mevzuat komisyonumuz tarafýndan SSK protokolü incelenmiþ olup farklýlýklar ve deðiþiklikler aþaðýdadýr. 1)
Larson'un 1960'larda veciz olarak belirttiði gibi,
 5 Prof. Dr. Semih KESKÝL Larson'un 1960'larda veciz olarak belirttiði gibi, yaþlýlarýn acil hastalýklarý diye bir durum yoktur. Bizimde burada söz konusu edeceðimiz yaþlýlar arasýndaki acil týbbi durumlardýr.
5 Prof. Dr. Semih KESKÝL Larson'un 1960'larda veciz olarak belirttiði gibi, yaþlýlarýn acil hastalýklarý diye bir durum yoktur. Bizimde burada söz konusu edeceðimiz yaþlýlar arasýndaki acil týbbi durumlardýr.
Vergi Usul Kanunu Ceza Hadleri
 2008-107 Vergi Usul Kanunu Ceza Hadleri Ýstanbul, 24 Aralýk 2008 Sirküler Sirküler Numarasý : Elit - 2008/107 Vergi Usul Kanunu'nda Yer Alan Ve 01.01.2009 Tarihinden Ýtibaren Uygulanacak Had Ve Tutarlar
2008-107 Vergi Usul Kanunu Ceza Hadleri Ýstanbul, 24 Aralýk 2008 Sirküler Sirküler Numarasý : Elit - 2008/107 Vergi Usul Kanunu'nda Yer Alan Ve 01.01.2009 Tarihinden Ýtibaren Uygulanacak Had Ve Tutarlar
 PROTOKOL SSK Baþkanlýðý Saðlýk Ýþleri Genel Müdürlüðü ile Türk Eczacýlarý Birliði Merkez Heyeti arasýnda eczanelerden temin edilecek ilaçlarla ilgili olarak Kurumumuz ile eczaneler arasýnda yapýlacak sözleþme
PROTOKOL SSK Baþkanlýðý Saðlýk Ýþleri Genel Müdürlüðü ile Türk Eczacýlarý Birliði Merkez Heyeti arasýnda eczanelerden temin edilecek ilaçlarla ilgili olarak Kurumumuz ile eczaneler arasýnda yapýlacak sözleþme
Yat, Kotra Ve Her Türlü Motorlu Özel Tekneler Ýçin Geçerli Olan KDV Ve ÖTV Ora
 2009-40 Yat, Kotra Ve Her Türlü Motorlu Özel Tekneler Ýçin Geçerli Olan KDV Ve ÖTV Ora Ýstanbul, 25 Aðustos 2009 Sirküler Numarasý : Elit - 2009/40 Sirküler Yat, Kotra Ve Her Türlü Motorlu Özel Tekneler
2009-40 Yat, Kotra Ve Her Türlü Motorlu Özel Tekneler Ýçin Geçerli Olan KDV Ve ÖTV Ora Ýstanbul, 25 Aðustos 2009 Sirküler Numarasý : Elit - 2009/40 Sirküler Yat, Kotra Ve Her Türlü Motorlu Özel Tekneler
STAJ BÝLGÝLERÝ. Önemli Açýklamalar
 Öðrencinin Adý ve Soyadý Doðum Yeri ve Yýlý Fakülte Numarasý Bölümü Yaptýðý Staj Dalý Fotoðraf STAJ BÝLGÝLERÝ Ýþyeri Adý Adresi Telefon Numarasý Staj Baþlama Tarihi Staj Bitiþ Tarihi Staj Süresi (gün)
Öðrencinin Adý ve Soyadý Doðum Yeri ve Yýlý Fakülte Numarasý Bölümü Yaptýðý Staj Dalý Fotoðraf STAJ BÝLGÝLERÝ Ýþyeri Adý Adresi Telefon Numarasý Staj Baþlama Tarihi Staj Bitiþ Tarihi Staj Süresi (gün)
Ücretlerin Bankalardan Ödenmesi Zorunlu Hale Getirilmiþtir
 2008-96 Ücretlerin Bankalardan Ödenmesi Zorunlu Hale Getirilmiþtir Ýstanbul, 19 Kasým 2008 Sirküler Sirküler Numarasý : Elit - 2008/96 Ücretlerin Bankalardan Ödenmesi Zorunlu Hale Getirilmiþtir 4857 sayýlý
2008-96 Ücretlerin Bankalardan Ödenmesi Zorunlu Hale Getirilmiþtir Ýstanbul, 19 Kasým 2008 Sirküler Sirküler Numarasý : Elit - 2008/96 Ücretlerin Bankalardan Ödenmesi Zorunlu Hale Getirilmiþtir 4857 sayýlý
Kýsa Çalýþma ve Kýsa Çalýþma Ödeneði
 2009-17 Kýsa Çalýþma ve Kýsa Çalýþma Ödeneði Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/17 Kýsa Çalýþma ve Kýsa Çalýþma Ödeneði Türkiye Ýstatistik Kurumu (TÜÝK) tarafýndan 9 Þubat
2009-17 Kýsa Çalýþma ve Kýsa Çalýþma Ödeneði Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/17 Kýsa Çalýþma ve Kýsa Çalýþma Ödeneði Türkiye Ýstatistik Kurumu (TÜÝK) tarafýndan 9 Þubat
Tablo 2 Üniversitelerdeki Týpta Uzmanlýk Eðitim Dallarý ve Kontenjanlarý
 Bu tabloda yer alan dallara yalnýz týp fakültesi mezunlarý baþvurabilirler. Bu adaylar, Tablo-2 ve Tablo-3'ün birinden 8'i geçmemek üzere en çok 14 dalý tercihleri arasýnda gösterebilirler. Eðitim görmek
Bu tabloda yer alan dallara yalnýz týp fakültesi mezunlarý baþvurabilirler. Bu adaylar, Tablo-2 ve Tablo-3'ün birinden 8'i geçmemek üzere en çok 14 dalý tercihleri arasýnda gösterebilirler. Eðitim görmek
TEBLİĞ. MADDE 2 Aynı Tebliğin 4.2.1.C-1 numaralı maddesinin onbirinci fıkrası aşağıdaki şekilde değiştirilmiştir.
 26 Eylül 2013 PERŞEMBE Resmî Gazete Sayı : 28777 Sosyal Güvenlik Kurumundan: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597
26 Eylül 2013 PERŞEMBE Resmî Gazete Sayı : 28777 Sosyal Güvenlik Kurumundan: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597
Çevre Temizlik Vergisi Oranlarý
 2007-17 Çevre Temizlik Vergisi Oranlarý Ýstanbul, 28 Aralýk 2007 Sirküler Sirküler Numarasý : Elit - 2007/17 Çevre Temizlik Vergisi Oranlarý Belediye Gelirleri Kanunu'nun Mükerrer 44 üncü maddesi uyarýnca,
2007-17 Çevre Temizlik Vergisi Oranlarý Ýstanbul, 28 Aralýk 2007 Sirküler Sirküler Numarasý : Elit - 2007/17 Çevre Temizlik Vergisi Oranlarý Belediye Gelirleri Kanunu'nun Mükerrer 44 üncü maddesi uyarýnca,
1-5018 sayılı Kamu Mali Yönetimi ve Kontrol Kanuna ekli; (I) sayılı cetvelde sayılmış olan genel bütçe kapsamındaki kamu idarelerinde,
 37.A.00. 01209 Ankara, 29.03.2010 BÖLGE ECZACI ODASI YÖNETİM KURULU BAŞKANLIĞINA Sosyal Güvenlik Kurumu Başkanlığı tarafından, 25.03.2010 tarih 27532 sayılı Mükerrer Resmi Gazete de Sağlık Uygulama Tebliği
37.A.00. 01209 Ankara, 29.03.2010 BÖLGE ECZACI ODASI YÖNETİM KURULU BAŞKANLIĞINA Sosyal Güvenlik Kurumu Başkanlığı tarafından, 25.03.2010 tarih 27532 sayılı Mükerrer Resmi Gazete de Sağlık Uygulama Tebliği
ÇANKAYA BELEDİYESİNİN ÖZEL HASTANELERLE YAPMIŞ OLDUĞU PROTOKOLLERLE ALINAN İNDİRİM ORANLARI
 ÇANKAYA BELEDİYESİNİN ÖZEL HASTANELERLE YAPMIŞ OLDUĞU PROTOKOLLERLE ALINAN İNDİRİM ORANLARI ÖZEL ÇANKAYA YAŞAM HASTANESİ Ayaktan Tedavi: %15 Yatarak Tedavi: %15 Diyet: %10 Lazer epilasyon: %10 Check-up:
ÇANKAYA BELEDİYESİNİN ÖZEL HASTANELERLE YAPMIŞ OLDUĞU PROTOKOLLERLE ALINAN İNDİRİM ORANLARI ÖZEL ÇANKAYA YAŞAM HASTANESİ Ayaktan Tedavi: %15 Yatarak Tedavi: %15 Diyet: %10 Lazer epilasyon: %10 Check-up:
7. ÝTHÝB KUMAÞ TASARIM YARIÞMASI 2012
 7. ÝTHÝB KUMAÞ TASARIM YARIÞMASI 2012 KÝMLER KATILABÝLÝR? Yarýþma, Türkiye Cumhuriyeti sýnýrlarý dahilinde veya yurtdýþýnda okuyan T.C. vatandaþlarý veya K.K.T.C vatandaþý, 35 yaþýný aþmamýþ, en az lise
7. ÝTHÝB KUMAÞ TASARIM YARIÞMASI 2012 KÝMLER KATILABÝLÝR? Yarýþma, Türkiye Cumhuriyeti sýnýrlarý dahilinde veya yurtdýþýnda okuyan T.C. vatandaþlarý veya K.K.T.C vatandaþý, 35 yaþýný aþmamýþ, en az lise
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 0 Nisan 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 0 Nisan 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP A TEORİK DERS PROGRAMI
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP A TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 7 Kasım 0 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP A TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 7 Kasım 0 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 09 Şubat 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 09 Şubat 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 08 Eylül 0 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 0-05 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 08 Eylül 0 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SSK Affý. Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit /75. Sirküler
 2008-75 SSK Affý Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit - 2008/75 Sirküler Sosyal Güvenlik Kurumu'na Olan Prim Borçlarýnýn Ödeme Kolaylýðýndan Yararlanmamýþ Olanlara, Tekrar Baþvuru Ýmkâný Ge
2008-75 SSK Affý Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit - 2008/75 Sirküler Sosyal Güvenlik Kurumu'na Olan Prim Borçlarýnýn Ödeme Kolaylýðýndan Yararlanmamýþ Olanlara, Tekrar Baþvuru Ýmkâný Ge
İlaç 4.1 - Reçete ve sağlık raporu yazım ilkeleri 4.1.1 - Ayakta tedavilerde reçetelerin düzenlenmesi
 İlaç 4.1 - Reçete ve sağlık raporu yazım ilkeleri (1) İlaç bedellerinin Kurum tarafından ödenebilmesi için, reçete yazımında ve rapor düzenlenmesinde aşağıda belirtilen hususlar uygulanacaktır. 4.1.1 -
İlaç 4.1 - Reçete ve sağlık raporu yazım ilkeleri (1) İlaç bedellerinin Kurum tarafından ödenebilmesi için, reçete yazımında ve rapor düzenlenmesinde aşağıda belirtilen hususlar uygulanacaktır. 4.1.1 -
ADANA ANKARA. Ankara Dýþkapý Yýldýrým Beyazýt Eðitim ve Araþtýrma Hastanesi. Adana Numune Eðitim ve Araþtýrma Hastanesi
 Tablo 3 Saðlýk Bakanlýðý Eðitim Araþtýrma Hastanelerinde, Saðlýk Bakanlýðý Adýna Týp Fakültelerinde Diðer Kurumlarda Uzmanlýk Eðitimi Yapýlacak Dallar Kontenjanlarý Adý Türü Adý Türü ADANA Adana Numune
Tablo 3 Saðlýk Bakanlýðý Eðitim Araþtýrma Hastanelerinde, Saðlýk Bakanlýðý Adýna Týp Fakültelerinde Diðer Kurumlarda Uzmanlýk Eðitimi Yapýlacak Dallar Kontenjanlarý Adý Türü Adý Türü ADANA Adana Numune
.:: TÇÝD - Tüm Çeviri Ýþletmeleri Derneði ::.
 Membership TÜM ÇEVÝRÝ ÝÞLETMELERÝ DERNEÐÝ YÖNETÝM KURULU BAÞKANLIÐINA ANTALYA Derneðinizin Tüzüðünü okudum; Derneðin kuruluþ felsefesi ve amacýna sadýk kalacaðýmý, Tüzükte belirtilen ilke ve kurallara
Membership TÜM ÇEVÝRÝ ÝÞLETMELERÝ DERNEÐÝ YÖNETÝM KURULU BAÞKANLIÐINA ANTALYA Derneðinizin Tüzüðünü okudum; Derneðin kuruluþ felsefesi ve amacýna sadýk kalacaðýmý, Tüzükte belirtilen ilke ve kurallara
Motorlu Taþýtlar Vergisi Oranlarý
 2007-18 Motorlu Taþýtlar Vergisi Oranlarý Ýstanbul, 28 Aralýk 2007 Sirküler Sirküler Numarasý : Elit - 2007/18 Motorlu Taþýtlar Vergisi Oranlarý Motorlu Taþýtlar Vergisi Kanunu'nun 10 uncu maddesi uyarýnca,
2007-18 Motorlu Taþýtlar Vergisi Oranlarý Ýstanbul, 28 Aralýk 2007 Sirküler Sirküler Numarasý : Elit - 2007/18 Motorlu Taþýtlar Vergisi Oranlarý Motorlu Taþýtlar Vergisi Kanunu'nun 10 uncu maddesi uyarýnca,
Laboratuvar Akreditasyon Baþkanlýðý Týbbi Laboratuvarlar
 Laboratuvar Akreditasyon Baþkanlýðý Týbbi Laboratuvarlar Týbbi Laboratuvar Akreditasyonu Akreditasyon, Akreditasyon; Laboratuvarların, Muayene, Belgelendirme kuruluşlarının ve Yeterlilik Deneyi Sağlayıcı
Laboratuvar Akreditasyon Baþkanlýðý Týbbi Laboratuvarlar Týbbi Laboratuvar Akreditasyonu Akreditasyon, Akreditasyon; Laboratuvarların, Muayene, Belgelendirme kuruluşlarının ve Yeterlilik Deneyi Sağlayıcı
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 05-06 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 07 Eylül 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 05-06 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI Hft Tarih Saat Konu Süre Öğretim Üyesi 07 Eylül 05 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
düþürücü kullanmamak c-duruma uygun ilaç kullanmamak Ateþ Durumunda Mutlaka Hekime Götürülmesi Gereken Haller:
 Ayna-Gazetesi-renksiz-11-06.qxp 26.10.2006 23:39 Seite 2 Çocuklarda Ateþ Deðerli Ayna okuyucularý, bundan böyle bu sayfada sizleri saðlýk konusunda bilgilendireceðim. Atalarýmýz ne demiþti: olmaya devlet
Ayna-Gazetesi-renksiz-11-06.qxp 26.10.2006 23:39 Seite 2 Çocuklarda Ateþ Deðerli Ayna okuyucularý, bundan böyle bu sayfada sizleri saðlýk konusunda bilgilendireceðim. Atalarýmýz ne demiþti: olmaya devlet
SAĞLIK UYGULAMA TEBLİĞİ 6. İLAÇ TEMİNİ VE ÖDEME ESASLARI (Değişik: 22/06/2012-28331/15 md. Yürürlük: 01/07/2012) 6.1. Reçete ile Sağlık Raporu ve
 SAĞLIK UYGULAMA TEBLİĞİ 6. İLAÇ TEMİNİ VE ÖDEME ESASLARI (Değişik: 22/06/2012-28331/15 md. Yürürlük: 01/07/2012) 6.1. Reçete ile Sağlık Raporu ve İlaç Yazım İlkeleri (1) İlaç bedellerinin Kurum tarafından
SAĞLIK UYGULAMA TEBLİĞİ 6. İLAÇ TEMİNİ VE ÖDEME ESASLARI (Değişik: 22/06/2012-28331/15 md. Yürürlük: 01/07/2012) 6.1. Reçete ile Sağlık Raporu ve İlaç Yazım İlkeleri (1) İlaç bedellerinin Kurum tarafından
Kamu Ýhalelerine Katýlacak Olan Mükelleflere Verilecek Vergi Borcu Olmadýðýna Dair Belge Ýle Ýlgili Cuma, 31 Aðustos 2007
 Kamu Ýhalelerine Katýlacak Olan Mükelleflere Verilecek Vergi Borcu Olmadýðýna Dair Belge Ýle Ýlgili Cuma, 31 Aðustos 2007 Taþpýnar Muhasebe Kamu Ýhalelerine Katýlacak Olan Mükelleflere Verilecek Vergi
Kamu Ýhalelerine Katýlacak Olan Mükelleflere Verilecek Vergi Borcu Olmadýðýna Dair Belge Ýle Ýlgili Cuma, 31 Aðustos 2007 Taþpýnar Muhasebe Kamu Ýhalelerine Katýlacak Olan Mükelleflere Verilecek Vergi
Akut Hepatit C: Bir Olgu Sunumu. Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa
 Akut Hepatit C: Bir Olgu Sunumu Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa Olgu 24 yaşında erkek hasta 6. sınıf tıp öğrencisi Ortopedi polikliniğine başvurmuş Rutin
Akut Hepatit C: Bir Olgu Sunumu Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa Olgu 24 yaşında erkek hasta 6. sınıf tıp öğrencisi Ortopedi polikliniğine başvurmuş Rutin
Sosyal Güvenlik Kurumu Başkanlığından: SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ
 Sosyal Güvenlik Kurumu Başkanlığından: SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597 sayılı Resmî Gazete de yayımlanan Sosyal Güvenlik
Sosyal Güvenlik Kurumu Başkanlığından: SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597 sayılı Resmî Gazete de yayımlanan Sosyal Güvenlik
Sosyal Güvenlik Kurumu Başkanlığı ile Türk Eczacıları Birliği
 Yurtdışı Sigortalılarının İlaç Temini Hakkında Sosyal Güvenlik Kurumu Başkanlığı ile Türk Eczacıları Birliği arasında 02.07.2007 tarihinde imzalanan 2007 Yılı SGK Protokolü kapsamında sözleşmeli eczanelerce
Yurtdışı Sigortalılarının İlaç Temini Hakkında Sosyal Güvenlik Kurumu Başkanlığı ile Türk Eczacıları Birliği arasında 02.07.2007 tarihinde imzalanan 2007 Yılı SGK Protokolü kapsamında sözleşmeli eczanelerce
Seri Numaralý Kdv Genel Tebliði
 2007-50 108 Seri Numaralý Kdv Genel Tebliði Sirküler Sirküler Numarasý : Elit - 2007/50 108 Seri Numaralý Kdv Genel Tebliði 108 seri numaralý KDV Genel Tebliði ile, katma deðer vergisi uygulamalarý konusunda
2007-50 108 Seri Numaralý Kdv Genel Tebliði Sirküler Sirküler Numarasý : Elit - 2007/50 108 Seri Numaralý Kdv Genel Tebliði 108 seri numaralý KDV Genel Tebliði ile, katma deðer vergisi uygulamalarý konusunda
Motorlu Taþýtlar Vergisi Tutarlarý
 2011-20 Motorlu Taþýtlar Vergisi Tutarlarý Sirküler2011/20 Ýstanbul, 05.01.2011 Motorlu Taþýtlar Vergisi Tutarlarý(2011 Yýlý) Motorlu Taþýtlar Vergisi Kanunu (MTVK)'nun 10 uncu maddesi uyarýnca, her takvim
2011-20 Motorlu Taþýtlar Vergisi Tutarlarý Sirküler2011/20 Ýstanbul, 05.01.2011 Motorlu Taþýtlar Vergisi Tutarlarý(2011 Yýlý) Motorlu Taþýtlar Vergisi Kanunu (MTVK)'nun 10 uncu maddesi uyarýnca, her takvim
SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR
 1 Ağustos 2013 PERŞEMBE Resmî Gazete Sayı : 28725 Sosyal Güvenlik Kurumundan: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597
1 Ağustos 2013 PERŞEMBE Resmî Gazete Sayı : 28725 Sosyal Güvenlik Kurumundan: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 24/3/2013 tarihli ve 28597
TÜRK ECZACILARI BİRLİĞİ MERKEZ HEYETİ
 Evrak Tarih ve Sayısı: 11/12/2018-9117 *BD6513574212* TÜRK ECZACILARI BİRLİĞİ MERKEZ HEYETİ Sayı : 41.A.00/ Konu : 21.03.2018 Tarihli SUT Değişikliğine Açtığımız Dava Akabinde Yürütümü Durdurulan Üç Madde
Evrak Tarih ve Sayısı: 11/12/2018-9117 *BD6513574212* TÜRK ECZACILARI BİRLİĞİ MERKEZ HEYETİ Sayı : 41.A.00/ Konu : 21.03.2018 Tarihli SUT Değişikliğine Açtığımız Dava Akabinde Yürütümü Durdurulan Üç Madde
düzenlemeler saklı kalmak kaydıyla) 28 günlük dozda, (SUT ta yer alan özel düzenlemeler saklı kalmak kaydıyla) reçete edilebilir. reçete edilebilir.
 MADDELER ÖNCEKİ HALİ SONRAKİ HALİ YÜRÜRLÜLÜK MADDE 1 6.1.4. Reçetelere yazılabilecek ilaç miktarı 6.1.4. Reçetelere yazılabilecek ilaç miktarı (5) Sağlık raporu aranmaksızın; (5) Sağlık raporu aranmaksızın;
MADDELER ÖNCEKİ HALİ SONRAKİ HALİ YÜRÜRLÜLÜK MADDE 1 6.1.4. Reçetelere yazılabilecek ilaç miktarı 6.1.4. Reçetelere yazılabilecek ilaç miktarı (5) Sağlık raporu aranmaksızın; (5) Sağlık raporu aranmaksızın;
1. Böleni 13 olan bir bölme iþleminde kalanlarýn
 4. SINIF COÞMAYA SORULARI 1. BÖLÜM 3. DÝKKAT! Bu bölümde 1 den 10 a kadar puan deðeri 1,25 olan sorular vardýr. 1. Böleni 13 olan bir bölme iþleminde kalanlarýn toplamý kaçtýr? A) 83 B) 78 C) 91 D) 87
4. SINIF COÞMAYA SORULARI 1. BÖLÜM 3. DÝKKAT! Bu bölümde 1 den 10 a kadar puan deðeri 1,25 olan sorular vardýr. 1. Böleni 13 olan bir bölme iþleminde kalanlarýn toplamý kaçtýr? A) 83 B) 78 C) 91 D) 87
Tehlikeli Atýk Çözümünde EKOVAR...
 ARA DEPOLAMA www. ekovar.com info@ ekovar.com Hilal Mah. 50. Sokak, 4. Cad. No: 8/8 Yýldýz - Çankaya / ANKARA Tel : +(90) 312 442 13 05 +(90) 312 442 11 43 Faks : +(90) 312 442 13 06 Tehlikeli Atýk Çözümünde
ARA DEPOLAMA www. ekovar.com info@ ekovar.com Hilal Mah. 50. Sokak, 4. Cad. No: 8/8 Yýldýz - Çankaya / ANKARA Tel : +(90) 312 442 13 05 +(90) 312 442 11 43 Faks : +(90) 312 442 13 06 Tehlikeli Atýk Çözümünde
MALÝ TATÝL 1 TEMMUZ-20 TEMMUZ 2015 Cumartesi, 04 Temmuz 2015
 MALÝ TATÝL 1 TEMMUZ-20 TEMMUZ 2015 Cumartesi, 04 Temmuz 2015 Taþpýnar Muhasebe MALÝ TATÝL 1 TEMMUZ-20 TEMMUZ 2015 MALÝ TATÝL NEDENÝ ÝLE BEYAN VE ÖDEME TARÝHLERÝ UZAYAN BEYANNAME VE BÝLDÝRÝMLER BEYANNAME/BÝLDÝRÝM
MALÝ TATÝL 1 TEMMUZ-20 TEMMUZ 2015 Cumartesi, 04 Temmuz 2015 Taþpýnar Muhasebe MALÝ TATÝL 1 TEMMUZ-20 TEMMUZ 2015 MALÝ TATÝL NEDENÝ ÝLE BEYAN VE ÖDEME TARÝHLERÝ UZAYAN BEYANNAME VE BÝLDÝRÝMLER BEYANNAME/BÝLDÝRÝM
ÝNSAN KAYNAKLARI VE EÐÝTÝM DAÝRE BAÞKANLIÐI
 ÝNSAN KAYNAKLARI VE EÐÝTÝM DAÝRE BAÞKANLIÐI MEMUR PERSONEL ÞUBE MÜDÜRLÜÐÜ GÖREV TANIMI Memur Personel Þube Müdürlüðü, belediyemiz bünyesinde görev yapan memur personelin özlük iþlemlerinin saðlýklý bir
ÝNSAN KAYNAKLARI VE EÐÝTÝM DAÝRE BAÞKANLIÐI MEMUR PERSONEL ÞUBE MÜDÜRLÜÐÜ GÖREV TANIMI Memur Personel Þube Müdürlüðü, belediyemiz bünyesinde görev yapan memur personelin özlük iþlemlerinin saðlýklý bir
Aile Hekimliðinde Genogram
 Aile Hekimliðinde Genogram Prof. Dr. Ýsmail Hamdi KARA, Düzce Üniversitesi Týp Fakültesi Aile Hekimliði AD, Düzce Aile Hekimliði Dersleri - 02.06.2010 15:30 1 I. Tanýmlar Hastalarý yalnýz bir birey olarak
Aile Hekimliðinde Genogram Prof. Dr. Ýsmail Hamdi KARA, Düzce Üniversitesi Týp Fakültesi Aile Hekimliði AD, Düzce Aile Hekimliði Dersleri - 02.06.2010 15:30 1 I. Tanýmlar Hastalarý yalnýz bir birey olarak
İlave ücret alınması İlave ücret alınması
 YÜRÜRLÜKTE BULUNAN SUT 1.8.4 - Yardımcı üreme yöntemi katılım payları (1) Yardımcı üreme yöntemi tedavilerinde birinci denemede %30, ikinci denemede %25 üçüncü denemede %20 oranında olmak üzere bu tedaviler
YÜRÜRLÜKTE BULUNAN SUT 1.8.4 - Yardımcı üreme yöntemi katılım payları (1) Yardımcı üreme yöntemi tedavilerinde birinci denemede %30, ikinci denemede %25 üçüncü denemede %20 oranında olmak üzere bu tedaviler
DÖNEM 4 PEDİATRİ STAJI DERS PROGRAMI B GRUBU (12/11/ /01/2019) 14/11/2018 Çarşamba
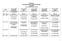 DÖNEM 4 PEDİATRİ STAJI DERS PROGRAMI B GRUBU (12/11/2018-18/01/2019) Saat 12/11/2018 08: 30 10: 20 Pediatri Stajının İşleyişi 13/11/2018 14/11/2018 15/11/2018 16/11/2018 Poliklinik ve servis Poliklinik
DÖNEM 4 PEDİATRİ STAJI DERS PROGRAMI B GRUBU (12/11/2018-18/01/2019) Saat 12/11/2018 08: 30 10: 20 Pediatri Stajının İşleyişi 13/11/2018 14/11/2018 15/11/2018 16/11/2018 Poliklinik ve servis Poliklinik
17a EK 17-A ÖYKÜ KONTROL LÝSTESÝ. ² Rahim Ýçi Araçlar - Ek 17-A²
 EK 17-A RÝA ÝÇÝN DEÐERLENDÝRME KONTROL LÝSTESÝ ÖYKÜ KONTROL LÝSTESÝ Hizmet verenin sorularý: Hizmet alana aþaðýdaki sorularý sorun: Hizmet veren için kurallar: Eðer yanýtlar evet sütununda ise aþaðýdaki
EK 17-A RÝA ÝÇÝN DEÐERLENDÝRME KONTROL LÝSTESÝ ÖYKÜ KONTROL LÝSTESÝ Hizmet verenin sorularý: Hizmet alana aþaðýdaki sorularý sorun: Hizmet veren için kurallar: Eðer yanýtlar evet sütununda ise aþaðýdaki
TEBLİĞİN 4.1.5 NUMARALI MADDESİNİN DOKUZUNCU FIKRASI YÜRÜRLÜKTEN KALDIRILMIŞTIR.
 4.1.5 - Elektronik reçete uygulaması (9) Yeniden e-reçete düzenlenmeksizin yapılacak ilaç temini; a) İlk defa reçete edilecek ilaçlar hariç olmak üzere sürekli kullanılan ilaçlarda uygulanır. b) EK-4/D
4.1.5 - Elektronik reçete uygulaması (9) Yeniden e-reçete düzenlenmeksizin yapılacak ilaç temini; a) İlk defa reçete edilecek ilaçlar hariç olmak üzere sürekli kullanılan ilaçlarda uygulanır. b) EK-4/D
Bakým sigortasý - Sizin için bilgiler. Türkischsprachige Informationen zur Pflegeversicherung. Freie Hansestadt Bremen.
 Gesundheitsamt Freie Hansestadt Bremen Sozialmedizinischer Dienst für Erwachsene Bakým sigortasý - Sizin için bilgiler Türkischsprachige Informationen zur Pflegeversicherung Yardýma ve bakýma muhtaç duruma
Gesundheitsamt Freie Hansestadt Bremen Sozialmedizinischer Dienst für Erwachsene Bakým sigortasý - Sizin için bilgiler Türkischsprachige Informationen zur Pflegeversicherung Yardýma ve bakýma muhtaç duruma
Saðlýk karnesi Pazartesi, 13 Temmuz 2009
 Saðlýk karnesi Pazartesi, 13 Temmuz 2009 Taþpýnar Muhasebe Sýk sorulan sorular (1) SAÐLIK KARNESÝ (*) (*) Konuyla ilgili 2007/96 sayýlý SOSYAL GÜVENLÝK KISA VADELÝ SÝGORTALAR DAÝRE BAÞKANLIÐININ (Konu
Saðlýk karnesi Pazartesi, 13 Temmuz 2009 Taþpýnar Muhasebe Sýk sorulan sorular (1) SAÐLIK KARNESÝ (*) (*) Konuyla ilgili 2007/96 sayýlý SOSYAL GÜVENLÝK KISA VADELÝ SÝGORTALAR DAÝRE BAÞKANLIÐININ (Konu
MEVZUAT ASGARÝ GEÇÝM ÝNDÝRÝMÝ GELÝR VERGÝSÝ GENEL TEBLÝÐÝ (SERÝ NO: 265) (R.Gazete: 14 Aralýk 2007-26720)
 MEVZUAT 1. Giriþ ASGARÝ GEÇÝM ÝNDÝRÝMÝ GELÝR VERGÝSÝ GENEL TEBLÝÐÝ (SERÝ NO: 265) (R.Gazete: 14 Aralýk 2007-26720) 5615 sayýlý Kanunla 193 sayýlý Gelir Vergisi Kanununda yapýlan deðiþiklikler sonucu vergi
MEVZUAT 1. Giriþ ASGARÝ GEÇÝM ÝNDÝRÝMÝ GELÝR VERGÝSÝ GENEL TEBLÝÐÝ (SERÝ NO: 265) (R.Gazete: 14 Aralýk 2007-26720) 5615 sayýlý Kanunla 193 sayýlý Gelir Vergisi Kanununda yapýlan deðiþiklikler sonucu vergi
STAJ BÝLGÝLERÝ. Önemli Açýklamalar
 2017 Öðrencinin Adý ve Soyadý Doðum Yeri ve Yýlý Fakülte Numarasý Bölümü Yaptýðý Staj Dalý Fotoðraf STAJ BÝLGÝLERÝ Ýþyeri Adý Adresi Telefon Numarasý Staj Baþlama Tarihi Staj Bitiþ Tarihi Staj Süresi (gün)
2017 Öðrencinin Adý ve Soyadý Doðum Yeri ve Yýlý Fakülte Numarasý Bölümü Yaptýðý Staj Dalý Fotoðraf STAJ BÝLGÝLERÝ Ýþyeri Adý Adresi Telefon Numarasý Staj Baþlama Tarihi Staj Bitiþ Tarihi Staj Süresi (gün)
Gelir Vergisi Kesintisi
 2009-16 Gelir Vergisi Kesintisi Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/16 Gelir Vergisi Kesintisi 1. Gelir Vergisi Kanunu Uyarýnca Kesinti Yapmak Zorunda Olanlar: Gelir Vergisi
2009-16 Gelir Vergisi Kesintisi Ýstanbul, 12 Mart 2009 Sirküler Sirküler Numarasý : Elit - 2009/16 Gelir Vergisi Kesintisi 1. Gelir Vergisi Kanunu Uyarýnca Kesinti Yapmak Zorunda Olanlar: Gelir Vergisi
YÜRÜRLÜKTE BULUNAN SUT TARİHLİ DEĞİŞİKLİK YÜRÜRLÜK TARİHLERİ
 YÜRÜRLÜKTE BULUNAN SUT 26.11.2016 TARİHLİ DEĞİŞİKLİK YÜRÜRLÜK TARİHLERİ 1.8.4 - Yardımcı üreme yöntemi katılım payları (1) Yardımcı üreme yöntemi tedavilerinde birinci denemede %30, ikinci denemede %25
YÜRÜRLÜKTE BULUNAN SUT 26.11.2016 TARİHLİ DEĞİŞİKLİK YÜRÜRLÜK TARİHLERİ 1.8.4 - Yardımcı üreme yöntemi katılım payları (1) Yardımcı üreme yöntemi tedavilerinde birinci denemede %30, ikinci denemede %25
 HER YILIN MODASI... ÝMALATÇI / ÝTHALATÇI FÝRMANIN UNVANI/TITLE MERKEZ ADRESÝ / ADDRESS TELEFON / PHONE MÜÞTERÝ HÝZMETLERÝ TELEFAKS / FAX FÝRMA YETKÝLÝSÝNÝN ÝMZA - KAÞESÝ / SIGNATURE & SEAL KARACA
HER YILIN MODASI... ÝMALATÇI / ÝTHALATÇI FÝRMANIN UNVANI/TITLE MERKEZ ADRESÝ / ADDRESS TELEFON / PHONE MÜÞTERÝ HÝZMETLERÝ TELEFAKS / FAX FÝRMA YETKÝLÝSÝNÝN ÝMZA - KAÞESÝ / SIGNATURE & SEAL KARACA
Kronik Hepatit B Tedavisi Zor Olgular
 Kronik Hepatit B Tedavisi Zor Olgular Dr. Faruk KARAKEÇİLİ Erzincan Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı 22.01.2016 HATAY Tedavisi Zor Olgular! Zor hasta
Kronik Hepatit B Tedavisi Zor Olgular Dr. Faruk KARAKEÇİLİ Erzincan Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı 22.01.2016 HATAY Tedavisi Zor Olgular! Zor hasta
KAMU PERSONELİNİN GENEL SAĞLIK SİGORTASI KAPSAMINA ALINMASI İLE İLGİLİ DUYURU
 KAMU PERSONELİNİN GENEL SAĞLIK SİGORTASI KAPSAMINA ALINMASI İLE İLGİLİ DUYURU Bilindiği üzere Kurumumuzca 18/12/2009 tarih ve 27436 sayılı Resmi Gazetede yayımlanan Kamu Personelinin Genel Sağlık Sigortası
KAMU PERSONELİNİN GENEL SAĞLIK SİGORTASI KAPSAMINA ALINMASI İLE İLGİLİ DUYURU Bilindiği üzere Kurumumuzca 18/12/2009 tarih ve 27436 sayılı Resmi Gazetede yayımlanan Kamu Personelinin Genel Sağlık Sigortası
Ad ve Soyadý:... Baba Adý:... Doðum Tarihi:.../.../...
 Sayýn Aday, 2004 Týpta Uzmanlýk Eðitimi (TUS) Nisan Dönemi sonunda boþ kalan kontenjanlar olduðu takdirde Ek Yerleþtirme yapýlacaktýr. Kayýt yaptýrýlmayan ve yerleþtirmeden boþ kalan kontenjanlarýn listesi
Sayýn Aday, 2004 Týpta Uzmanlýk Eðitimi (TUS) Nisan Dönemi sonunda boþ kalan kontenjanlar olduðu takdirde Ek Yerleþtirme yapýlacaktýr. Kayýt yaptýrýlmayan ve yerleþtirmeden boþ kalan kontenjanlarýn listesi
2012/2013 Yılı İstatistiki Verileri
 T.C SAĞLIK BAKANLIĞI TÜRKİYE KAMU HASTANELERİ KURUMU Ankara 1.Bölge Kamu Hastaneleri Birliği Genel Sekreterliği Ankara Dışkapı Yıldırım Beyazıt Eğitim Araştırma Hastanesi / Yılı İstatistiki Verileri /
T.C SAĞLIK BAKANLIĞI TÜRKİYE KAMU HASTANELERİ KURUMU Ankara 1.Bölge Kamu Hastaneleri Birliği Genel Sekreterliği Ankara Dışkapı Yıldırım Beyazıt Eğitim Araştırma Hastanesi / Yılı İstatistiki Verileri /
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI.
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 03 Eylül 08 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP B TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 03 Eylül 08 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
1. ÝTHÝB TEKNÝK TEKSTÝL PROJE YARIÞMASI
 Yarýþmanýn Amacý 1. ÝTHÝB 1.ÝTHÝB Teknik Tekstiller Proje Yarýþmasý, Ýstanbul Tekstil ve Hammaddeleri Ýhracatçýlarý Birliði'nin Türkiye Ýhracatçýlar Meclisi'nin katkýlarýyla Türkiye'de teknik tekstil sektörünün
Yarýþmanýn Amacý 1. ÝTHÝB 1.ÝTHÝB Teknik Tekstiller Proje Yarýþmasý, Ýstanbul Tekstil ve Hammaddeleri Ýhracatçýlarý Birliði'nin Türkiye Ýhracatçýlar Meclisi'nin katkýlarýyla Türkiye'de teknik tekstil sektörünün
 Adana CZACI ODASI www.adanaeo.org.tr Yýl:1 Sayý:1 Kasým 2005 Deðerli Meslektaþlarým; GÜNCEL 2005 Seçimli Olaðan Genel Kurul Yapýldý. Ýlgi ve katýlýmýn yüksek olduðu seviyeli bir Genel Kurul yaptýk. En
Adana CZACI ODASI www.adanaeo.org.tr Yýl:1 Sayý:1 Kasým 2005 Deðerli Meslektaþlarým; GÜNCEL 2005 Seçimli Olaðan Genel Kurul Yapýldý. Ýlgi ve katýlýmýn yüksek olduðu seviyeli bir Genel Kurul yaptýk. En
Tebliğ. 2005 Mali Yılı Bütçe Uygulama Talimatı (Sıra No : 6) (Tedavi Yardımı)
 Tebliğ 2005 Mali Yılı Bütçe Uygulama Talimatı (Sıra No : 6) (Tedavi Yardımı) Bilindiği üzere, tedavi yardımına ilişkin (4) sıra nolu 2005 Mali Yılı Bütçe Uygulama Talimatı (Bundan sonra Talimat olarak
Tebliğ 2005 Mali Yılı Bütçe Uygulama Talimatı (Sıra No : 6) (Tedavi Yardımı) Bilindiği üzere, tedavi yardımına ilişkin (4) sıra nolu 2005 Mali Yılı Bütçe Uygulama Talimatı (Bundan sonra Talimat olarak
Faaliyet Raporu. Banvit Bandýrma Vitaminli Yem San. A.Þ. 01 Ocak - 30 Eylül 2010 Dönemi
 10 Faaliyet Raporu Banvit Bandýrma Vitaminli Yem San. A.Þ. 01 Ocak - 30 Eylül 2010 Dönemi Ýçindekiler Yönetim ve Denetim Kurulu Temettü Politikasý Risk Yönetim Politikalarý Genel Kurul Tarihine Kadar Meydana
10 Faaliyet Raporu Banvit Bandýrma Vitaminli Yem San. A.Þ. 01 Ocak - 30 Eylül 2010 Dönemi Ýçindekiler Yönetim ve Denetim Kurulu Temettü Politikasý Risk Yönetim Politikalarý Genel Kurul Tarihine Kadar Meydana
Kronik HCV İnfeksiyonlarında Güncel Tedavi Yaklaşımları Dr. Kaya Süer
 Kronik HCV İnfeksiyonlarında Güncel Tedavi Yaklaşımları Dr. Kaya Süer Near East University Faculty of Medicine Infectious Diseases and Clinical Microbiology HCV tarihçesi 1989 Hepatitis C (HCV) genomu
Kronik HCV İnfeksiyonlarında Güncel Tedavi Yaklaşımları Dr. Kaya Süer Near East University Faculty of Medicine Infectious Diseases and Clinical Microbiology HCV tarihçesi 1989 Hepatitis C (HCV) genomu
ENTERAL BESLENME SOLÜSYONLARI RAPORLARINDA ARANMASI GEREKEN GENEL BİLGİLER 13.08.2015
 ENTERAL BESLENME SOLÜSYONLARI RAPORLARINDA ARANMASI GEREKEN GENEL BİLGİLER 13.08.2015 RAPOR SÜRESİ 6 AY DIR 1- MALNÜTRİSYONTANIMI OLAN TÜM HASTALIKLARDA ÖDENİR. MALNÜTRİSYON TANIMI OLARAK; ERİŞKİN HASTALARDA
ENTERAL BESLENME SOLÜSYONLARI RAPORLARINDA ARANMASI GEREKEN GENEL BİLGİLER 13.08.2015 RAPOR SÜRESİ 6 AY DIR 1- MALNÜTRİSYONTANIMI OLAN TÜM HASTALIKLARDA ÖDENİR. MALNÜTRİSYON TANIMI OLARAK; ERİŞKİN HASTALARDA
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI.
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 0 Şubat 09 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP D TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 0 Şubat 09 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
(3) Tedavinin etkinliğine (tedaviye cevapsızlık/yetersiz cevap) yönelik değerlendirme kriterleri aşağıdaki gibidir:
 4.2.33- Göz hastalıklarında ilaç kullanım ilkeleri (1) Bevacizumab, ranibizumab, aflibersept, deksametazon intravitreal implant ve verteporfin etkin maddelerini içeren ilaçların; üçüncü basamak sağlık
4.2.33- Göz hastalıklarında ilaç kullanım ilkeleri (1) Bevacizumab, ranibizumab, aflibersept, deksametazon intravitreal implant ve verteporfin etkin maddelerini içeren ilaçların; üçüncü basamak sağlık
HEPATİTLER (SARILIK HASTALIĞI) VE 0212 5294400 2182 KRONİK BÖBREK HASTALIKLARI VE 0212 5294400 2182
 İSTANBUL SAĞLIK MÜDÜRLÜĞÜ 2013 YILI HASTA OKULU PLANI HASTANE ADI TARİH SAAT KONU EĞİTİM YERİ HASTA OKULU PROGRAMI İÇİN HASTA VE YAKINLARININ İLETİŞİM KURABİLECEKLERİ TELEFON NUMARASI HASEKİ 28/01/2013
İSTANBUL SAĞLIK MÜDÜRLÜĞÜ 2013 YILI HASTA OKULU PLANI HASTANE ADI TARİH SAAT KONU EĞİTİM YERİ HASTA OKULU PROGRAMI İÇİN HASTA VE YAKINLARININ İLETİŞİM KURABİLECEKLERİ TELEFON NUMARASI HASEKİ 28/01/2013
 Adana Eczacý Odasý www.adanaeo.org.tr Ecz. Burhanettin BULUT Baþkan Saðlýk ve ilaç alaný, tarihinde görülmemiþ müdahalelere konu oluyor. Saðlýkta devrim denilen uygulamalarýn makyajý dökülünce saðlýk ihtilal
Adana Eczacý Odasý www.adanaeo.org.tr Ecz. Burhanettin BULUT Baþkan Saðlýk ve ilaç alaný, tarihinde görülmemiþ müdahalelere konu oluyor. Saðlýkta devrim denilen uygulamalarýn makyajý dökülünce saðlýk ihtilal
düzenlemeler saklı kalmak kaydıyla) 28 günlük dozda, (SUT ta yer alan özel düzenlemeler saklı kalmak kaydıyla) reçete edilebilir. reçete edilebilir.
 MADDELER ÖNCEKİ HALİ SONRAKİ HALİ YÜRÜRLÜLÜK MADDE 1 6.1.4. Reçetelere yazılabilecek ilaç miktarı 6.1.4. Reçetelere yazılabilecek ilaç miktarı (5) Sağlık raporu aranmaksızın; (5) Sağlık raporu aranmaksızın;
MADDELER ÖNCEKİ HALİ SONRAKİ HALİ YÜRÜRLÜLÜK MADDE 1 6.1.4. Reçetelere yazılabilecek ilaç miktarı 6.1.4. Reçetelere yazılabilecek ilaç miktarı (5) Sağlık raporu aranmaksızın; (5) Sağlık raporu aranmaksızın;
01/08/2013 TARİHLİ SUT REVİZYONU ESKİ HALİ YENİ HALİ NE GETİRECEK SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİ
 DEĞİŞİKLİK MADDESİ MADDE 1: 1.9.1 1.9.1 - (İlave ücret alınması) birinci fıkrası ESKİ HALİ HALİ NE GETİRECEK SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİ (1) Kurumla sözleşmeli; vakıf üniversiteleri
DEĞİŞİKLİK MADDESİ MADDE 1: 1.9.1 1.9.1 - (İlave ücret alınması) birinci fıkrası ESKİ HALİ HALİ NE GETİRECEK SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİ (1) Kurumla sözleşmeli; vakıf üniversiteleri
Ovacýk Altýn Madeni'ne dava öncesi yargýsýz infaz!
 Asýlsýz iddia neden ortaya atýldý? Ovacýk Altýn Madeni'ne dava öncesi yargýsýz infaz! 19 Haziran 2004 tarihinde, Ovacýk Altýn Madeni ile hiçbir ilgisi olmayan Arsenik iddialarý ortaya atýlarak madenimiz
Asýlsýz iddia neden ortaya atýldý? Ovacýk Altýn Madeni'ne dava öncesi yargýsýz infaz! 19 Haziran 2004 tarihinde, Ovacýk Altýn Madeni ile hiçbir ilgisi olmayan Arsenik iddialarý ortaya atýlarak madenimiz
OKUL ÖNCESÝ EÐÝTÝM KURUMLARI YÖNETMELÝÐÝNDE DEÐÝÞÝKLÝK YAPILMASINA D YÖNETMELÝK Çarþamba, 10 Eylül 2008
 OKUL ÖNCESÝ EÐÝTÝM KURUMLARI YÖNETMELÝÐÝNDE DEÐÝÞÝKLÝK YAPILMASINA D YÖNETMELÝK Çarþamba, 10 Eylül 2008 6 Eylül 2008 CUMARTESÝ Resmî Gazete Sayý : 26989 YÖNETMELÝK Millî Eðitim Bakanlýðýndan: OKUL ÖNCESÝ
OKUL ÖNCESÝ EÐÝTÝM KURUMLARI YÖNETMELÝÐÝNDE DEÐÝÞÝKLÝK YAPILMASINA D YÖNETMELÝK Çarþamba, 10 Eylül 2008 6 Eylül 2008 CUMARTESÝ Resmî Gazete Sayý : 26989 YÖNETMELÝK Millî Eðitim Bakanlýðýndan: OKUL ÖNCESÝ
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI.
 SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 5 Nisan 09 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
SDÜ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI 08-09 EĞİTİM YILI DÖNEM IV GRUP C TEORİK DERS PROGRAMI. Hft Tarih Saat Konu Süre Öğretim Üyesi 5 Nisan 09 09.00 İç Hastalıkları ve Anamnez () Toraks muayenesi
a) Başlangıç tedavisine göre görme keskinliğinde artış olmaması veya görme keskinliğinin azalması veya
 4.2.33- Göz hastalıklarında ilaç kullanım ilkeleri (1) Bevacizumab, ranibizumab, aflibersept, deksametazon intravitreal implant ve verteporfin etkin maddelerini içeren ilaçların; üçüncü basamak sağlık
4.2.33- Göz hastalıklarında ilaç kullanım ilkeleri (1) Bevacizumab, ranibizumab, aflibersept, deksametazon intravitreal implant ve verteporfin etkin maddelerini içeren ilaçların; üçüncü basamak sağlık
(NOT: Ekleri 132 sayfa olduğundan burada yer verilmemiştir.)
 Subject :2004 MALĐ YILI TEDAVĐ YARDIMI BÜTÇE UYGULAMA TALĐMATI HAKKINDA 2004/24 Date :Thu, 19 Feb 2004 17:36:30 +0200 From :IMI DUYURU To :hmpersonel@hazine.gov.tr 11.02.2004
Subject :2004 MALĐ YILI TEDAVĐ YARDIMI BÜTÇE UYGULAMA TALĐMATI HAKKINDA 2004/24 Date :Thu, 19 Feb 2004 17:36:30 +0200 From :IMI DUYURU To :hmpersonel@hazine.gov.tr 11.02.2004
EÞÝTSÝZLÝKLER. I. ve II. Dereceden Bir Bilinmeyenli Eþitsizlik. Polinomlarýn Çarpýmý ve Bölümü Bulunan Eþitsizlik
 l l l EÞÝTSÝZLÝKLER I. ve II. Dereceden Bir Bilinmeyenli Eþitsizlik Polinomlarýn Çarpýmý ve Bölümü Bulunan Eþitsizlik Çift ve Tek Katlý Kök, Üslü ve Mutlak Deðerlik Eþitsizlik l Alýþtýrma 1 l Eþitsizlik
l l l EÞÝTSÝZLÝKLER I. ve II. Dereceden Bir Bilinmeyenli Eþitsizlik Polinomlarýn Çarpýmý ve Bölümü Bulunan Eþitsizlik Çift ve Tek Katlý Kök, Üslü ve Mutlak Deðerlik Eþitsizlik l Alýþtýrma 1 l Eþitsizlik
Tablo 3 SAÐLIK BAKANLIÐI EÐÝTÝM VE ARAÞTIRMA HASTANELERÝNE ALINACAK ASÝSTAN SAYILARI ADANA ANKARA
 Bu tabloda yer alan dallarý, týp fakültesi mezunlarý ile Tababet Uzmanlýk Tüzüðünün 6. maddesinin B bendi uyarýnca diðer fakülte, yüksekokul veya bölümlerden mezun olan adaylar tercih edebilirler. mezunlarý,
Bu tabloda yer alan dallarý, týp fakültesi mezunlarý ile Tababet Uzmanlýk Tüzüðünün 6. maddesinin B bendi uyarýnca diðer fakülte, yüksekokul veya bölümlerden mezun olan adaylar tercih edebilirler. mezunlarý,
Tablo 2 Üniversitelerdeki Týpta Uzmanlýk Eðitim Dallarý ve Kontenjanlarý
 Tablo 2 Ünirsitelerdeki Týpta Uzmanlýk Eðitim Dallarý Kontenjanlarý * larý ile ilgili Açýklamalarýný mutlaka okuyunuz. 1 Adý Adý Abant Ýzzet Baysal Ünirsitesi 1011163 Çocuk Saðlýðý Hastalýklarý 5 K 1 -
Tablo 2 Ünirsitelerdeki Týpta Uzmanlýk Eðitim Dallarý Kontenjanlarý * larý ile ilgili Açýklamalarýný mutlaka okuyunuz. 1 Adý Adý Abant Ýzzet Baysal Ünirsitesi 1011163 Çocuk Saðlýðý Hastalýklarý 5 K 1 -
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı. Rehberler Es lig inde Hasta Yo netimi
 Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
TEBLİĞ. MADDE 2 Aynı Tebliğin 6.1.5 numaralı maddesine aşağıdaki dokuzuncu fıkra eklenmiştir.
 10 Ocak 2013 PERŞEMBE Resmî Gazete Sayı : 28524 Sosyal Güvenlik Kurumu Başkanlığından: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 25/3/2010 tarihli
10 Ocak 2013 PERŞEMBE Resmî Gazete Sayı : 28524 Sosyal Güvenlik Kurumu Başkanlığından: TEBLİĞ SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ MADDE 1 25/3/2010 tarihli
Kronik Hepatit C Tedavisinde Güncel Yaklaşımlar
 Kronik Hepatit C Tedavisinde Güncel Yaklaşımlar Asıl Dr. Alpay alt başlık ARIstilini düzenlemek için tıklatın İzmir Bozyaka Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji
Kronik Hepatit C Tedavisinde Güncel Yaklaşımlar Asıl Dr. Alpay alt başlık ARIstilini düzenlemek için tıklatın İzmir Bozyaka Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji
T.C YARGITAY 9. HUKUK DAÝRESÝ Esas No : 2005 / 37239 Karar No : 2006 / 3456 Tarihi : 13.02.2006 KARAR ÖZETÝ : ALT ÝÞVEREN - ÇALIÞTIRACAK ÝÞÇÝ SAYISI
 Yargýtay Kararlarý T.C Esas No : 2005 / 37239 Karar No : 2006 / 3456 Tarihi : 13.02.2006 KARAR ÖZETÝ : ALT ÝÞVEREN - ÇALIÞTIRACAK ÝÞÇÝ SAYISI Davalý þirketin ayný il veya diðer illerde baþka iþyerinin
Yargýtay Kararlarý T.C Esas No : 2005 / 37239 Karar No : 2006 / 3456 Tarihi : 13.02.2006 KARAR ÖZETÝ : ALT ÝÞVEREN - ÇALIÞTIRACAK ÝÞÇÝ SAYISI Davalý þirketin ayný il veya diðer illerde baþka iþyerinin
 Adana Eczacý Odasý www.adanaeo.org.tr Ecz. Burhanettin BULUT Baþkan BÝRAZ DA UZAÐA BAKABÝLMELÝ... GÜNCEL 14 Mayýs "Eczacýlýk Günü" etkinliklerimizi son yýllarýn en yüksek katýlýmlarýyla gerçekleþtirdik.
Adana Eczacý Odasý www.adanaeo.org.tr Ecz. Burhanettin BULUT Baþkan BÝRAZ DA UZAÐA BAKABÝLMELÝ... GÜNCEL 14 Mayýs "Eczacýlýk Günü" etkinliklerimizi son yýllarýn en yüksek katýlýmlarýyla gerçekleþtirdik.
ÖTV. Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit /58. Sirküler. Baz Yaðlar Ýle Tütün Ve Tütün Mamullerinden Alýnan
 2008-58 ÖTV Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit - 2008/58 Sirküler Baz Yaðlar Ýle Tütün Ve Tütün Mamullerinden Alýnan Özel Tüketim Vergisi Bakanlar Kurulu'nun, Özel Tüketim Vergisi Kanunu'nun
2008-58 ÖTV Ýstanbul, 21 Temmuz 2008 Sirküler Numarasý : Elit - 2008/58 Sirküler Baz Yaðlar Ýle Tütün Ve Tütün Mamullerinden Alýnan Özel Tüketim Vergisi Bakanlar Kurulu'nun, Özel Tüketim Vergisi Kanunu'nun
(6) İşyeri hekimleri veya birden fazla işyerine hizmet veren ortak sağlık birimleri ile özel poliklinikler tarafından verilen sağlık hizmetleri için
 YÜRÜRLÜKTEKĠ S.U.T. NE GÖRE 2.2 - Finansmanı sağlanan sağlık hizmetlerinin sağlanma yöntemleri ve ödeme kuralları (6) İşyeri hekimleri veya birden fazla işyerine hizmet veren ortak sağlık birimleri ile
YÜRÜRLÜKTEKĠ S.U.T. NE GÖRE 2.2 - Finansmanı sağlanan sağlık hizmetlerinin sağlanma yöntemleri ve ödeme kuralları (6) İşyeri hekimleri veya birden fazla işyerine hizmet veren ortak sağlık birimleri ile
2008 YILI SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ YAYIMLANDI
 06.04.2009/75 2008 YILI SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ YAYIMLANDI ÖZET : 2008 Yılı Sosyal Güvenlik Kurumu Sağlık Uygulama Tebliğinde değişiklikler
06.04.2009/75 2008 YILI SOSYAL GÜVENLİK KURUMU SAĞLIK UYGULAMA TEBLİĞİNDE DEĞİŞİKLİK YAPILMASINA DAİR TEBLİĞ YAYIMLANDI ÖZET : 2008 Yılı Sosyal Güvenlik Kurumu Sağlık Uygulama Tebliğinde değişiklikler
Türkiye'de yaşayan 345 Suriyeli Göçmenin Hemodiyaliz Deneyimi: Türk Hemodiyaliz Hastaları ile Karşılaştırılmalı Veri Tabanı Çalışması
 Türkiye'de yaşayan 345 Suriyeli Göçmenin Hemodiyaliz Deneyimi: Türk Hemodiyaliz Hastaları ile Karşılaştırılmalı Veri Tabanı Çalışması Meltem Gürsu 1, Mustafa Arıcı 2, Kenan Ateş 3, Rümeyza Kazancıoğlu
Türkiye'de yaşayan 345 Suriyeli Göçmenin Hemodiyaliz Deneyimi: Türk Hemodiyaliz Hastaları ile Karşılaştırılmalı Veri Tabanı Çalışması Meltem Gürsu 1, Mustafa Arıcı 2, Kenan Ateş 3, Rümeyza Kazancıoğlu
