Bölüm 2 KİMYASAL TEPKİMELER VE DOĞALGAZIN YANMASI
|
|
|
- Gül Kaldırım
- 4 yıl önce
- İzleme sayısı:
Transkript
1 ME418 Doğalgaz Sistemleri Bahar, 2018 Bölüm 2 KİMYASAL TEPKİMELER VE DOĞALGAZIN YANMASI Ceyhun Yılmaz Afyon Kocatepe Üniversitesi Teknoloji Fakültesi Makine Mühendisliği Bölümü
2 AMAÇLAR Yakıt ve yanma kavramını öğretmek Denkleştirilmiş kimyasal tepkime eşitliklerini belirlemek için tepkimeli sistemlere kütlenin korunumu yasasını uygulamak. Yakıt hava oranı, kuramsal hava yüzdesi ve çiğlenme sıcaklığı gibi yanma analizinde kullanılan parametreleri tanımlamak. Hem kararlı akış ile hacmi kontrol edilen hem de kütlesi sabit olan sistemler için enerji denkliklerini tepkimeli sistemlere uygulamak. Tepkime entalpisini, yanma entalpisini ve yakıtların ısı değerlerini hesaplamak. Tepkimeleri karışımların adyabatik alevlenme sıcaklıklarını belirlemek. 2
3 YAKITLAR VE YANMA YAKIT: Isı enerjisi verecek şekilde yanabilen herhangi bir maddeye yakıt denir. En iyi bilinen yakıtlar esas olarak hidrojen ve karbondan meydana gelir. Bunlara hidrokarbon yakıtlar denir ve C n H m genel formülü ile gösterilirler. Her fazda hidrokarbon yakıt bulunur. Örnek olarak kömür, gaz yağı ve doğal gaz verilebilir. Kömürün ana bileşeni karbondur. Kömür değişen miktarlarda oksijen,hidrojen, azot, kükürt, nem ve kül de içerir. Most liquid hydrocarbon fuels are obtained from crude oil by distillation. 3
4 Mol veya hacimsel kuru hava %20.9 oksijen, %78.1 azot,% 0.9 argon ve az miktarda karbon dioksit, helyum, neon ve hidrojenden meydana gelir. Yanma işlemi incelenirken, havadaki argon azot olarak işlem görür ve az miktarda bulunan diğer gazlar göz ardı edilir. O zaman, kuru hava, yaklaşık molce %2 oksijen ve %79 azotdan ibarettir. Bu nedenle, yanma odasına giren her mol oksijen 0.79/0.21= 3.76 mol azot bulunur. Combustion is a chemical reaction during which a fuel is oxidized and a large quantity of energy is released. Each kmol of O 2 in air is accompanied by 3.76 kmol of N 2. 4
5 Yakıtın oksijen ile temas etmesinin yanma işleminin başlaması için yeterli olmadığından da söz edilmelidir. Yanmanın başlaması için yakıt tutuşma sıcaklığının üstüne getirilmelidir. Bazı maddelerin atmosferde bulunan havadaki minimum tutuşma sıcaklıkları yaklaşık olarak benzin 260 C, karbon 400 C, hidrojen 580 C, karbon monoksit 610 C ve metanın 630 C şeklindedir. Bundan başka, yanmanın başlaması için, yakıt ve hava oranları yanma için uygun aralıkta olmalıdır. Örneğin, doğal gaz %5 den küçük yaklaşık %15 den büyük derişimlerde yanmayacaktır. The mass (and number of atoms) of each element is conserved during a chemical reaction. In a steady-flow combustion process, the components that enter the reaction chamber are called reactants and the components that exit are called products. Her bir elementin (ve atom sayısının) kütlesi kimyasal tepkimesırasında sabit kalır. 5
6 Air-fuel ratio (AF): Yanma işlemlerinin analizinde, yakıt ve hava miktarlarını sayısal olarak ifade etmek için sık sık kullanılan büyüklük hava-yakıt oranı (HY) dır. Genellikle kütleye göre ifade edilir ve yanma işlemlerinde havanın kütlesinin yakıtın kütlesine oranı olarak tanımlanır (Yani, hava yakıt oranı havanın mol sayısının yakıtın mol sayısına oranı şeklinde mol sayısına göre de ifade edilebilir. Burada önceki tanım kullanılacaktır. Hava-yakıt oranının tersi yakıt-hava oranıdır. m kütle N mol sayısı M mol kütlesi Hava yakıt oranı (HY) yanma işleminde birim kütle yakıt başına kullanılan hava miktarını anlatır. 6
7 KURAMSAL VE GERÇEK YANMA İŞLEMLERİ Complete combustion: If all the carbon in the fuel burns to CO 2, all the hydrogen burns to H 2 O, and all the sulfur (if any) burns to SO 2. Incomplete combustion: If the combustion products contain any unburned fuel or components such as C, H 2, CO, or OH. Reasons for incomplete combustion: 1 Insufficient oxygen, 2 insufficient mixing in the combustion chamber during the limited time that the fuel and the oxygen are in contact, and 3 dissociation (at high temperatures). Yanma işlemi yakıtın yanabilen tüm bileşenleri tamamen yandığında tamamlanır. 7
8 Stokiyometrik veya kuramsal hava: Bir yakıtın tam yanması için gereken minimum hava miktarına stokiyometrik veya kuramsal hava denir. Stokiyometrik veya kuramsal yanma: Bir yakıtın kuramsal hava ile tamamen yanması sırasında meydana gelen ideal yanma işlemine yakıtın stokiyometrik veya kuramsal yanması denir. Fazla hava: Gerçek yanma işlemlerinde, tam yanmayı sağlamak ve yanma odasının sıcaklığını kontrol etmek için stokiyometrik miktardan daha fazla hava kullanmak genel bir uygulamadır. Stokiyometrik miktardan fazla hava miktarına fazla hava denir Eksik hava: Stokiyometrik miktardan daha az havaya eksik hava denir Eşdeğerlik oranı: Yanma işlemlerinde kullanılan hava miktarı gerçek yakıt-hava oranının kuramsal yakıt hava oranına oranı demek olan eşdeğerlik oranı ile ifade edilir. 50% fazla hava = 150% teorik hava 200% fazla hava = 300% teorik hava 90% teorik hava = 10% eksik hava The complete combustion process with no free oxygen in the products is called theoretical combustion. 8
9 Yanma işleminin tam olduğu varsayıldığında ve kullanılan yakıt ve havanın miktarlarının tam olarak bilindiğinde ürün bileşiminin önceden bilinmesi nispeten kolaydır. Bu durumda yapılması gereken tek şey, hiçbir ölçüme gerek kalmadan, yanma eşitliğinde yer alan her bir elemente kütle denkliğini uygulamaktır. Bununla beraber, gerçek yanma işlemlerinde yapılacak iş o kadar basit değildir. Çünkü, gerçek yanma işlemleri fazla hava olsa bile çok zor tamamlanır. Bu yüzden, yalnız kütle denkliğine dayanarak ürün bileşimini belirlemek imkansızdır. O zaman, sahip olunan tek seçenek, üründe bulunan her bir bileşenin miktarını doğrudan ölçmektir. Yanma gazlarının bileşimini analiz etmek için genel olarak kullanılan cihaz Orsat gaz analizörüdür. Determining the mole fraction of the CO 2 in combustion gases by using the Orsat gas analyzer. 9
10 Bu cihazda, yanma gazlarının bir örneği toplanır oda sıcaklığına ve basıncına soğutulur ve o basınç ve sıcaklıktaki hacmi ölçülür. Sonra, örnek CO2 i absorplayan bir kimyasal ile temas ettirilir. Kalan gazlar oda sıcaklık ve basıncına geri döner ve onların kapladıkları yeni hacim ölçülür. Hacimdeki azalmanın ilk hacme oranı CO2 in hacim kesridir ve eğer gazların ideal davrandığı varsayılırsa bu CO2 in mol kesrine eşittir. Diğer gazların mol kesirleri aynı işlem tekrarlanarak belirlenir. Orsat analizinde, gaz örneği su üzerinde toplanır ve her zaman doygun halde tutulur. Bu yüzden, suyun buhar basıncı tüm deney boyunca sabit kalır. Bu nedenle, deney odasında su buharının varlığı yok sayılır ve veriler kuru hayaya göre verilir. Bununla beraber, yanma sırasında oluşan H2O miktarı yanma eşitliği denkleştirilerek kolayca belirlenir. 10
11 OLUŞUM ENTALPİSİ VE YANMA ENTALPİSİ Bir kimyasal tepkime sırasında,molekül içinde atomları bağlayan bazı kimyasal bağlar kırılır ve yenileri oluşur. Bu bağlar ile ilgili kimyasal enerji genellikle ürünler ve girdiler için bir maddenin mikroskobik enerji biçimleri duyulur, gizli, kimyasal, ve nükleer enerjiden oluşur ve farklıdır. Bu yüzden, kimyasal tepkime meydana gelen bir işlemde enerji, denkliklerinde mutlaka hesaba katılması gereken kimyasal enerji değişiklikleri olacaktır. Her bir girdi atomunun bozulmadan kaldığı (nükleer enerji değişimi yok) varsayıldığında ve kinetik ve potansiyel enerjilerdeki her hangi bir değişimin göz ardı edildiğinde kimyasal tepkime sırasında bir sistemin enerjisindeki değişme hal değişiminden ve kimyasal bileşimdeki bir değişmeden ileri gelir. 11
12 Tepkime entalpisi,h R : Tepkime entalpisi, tüm tepkime için, belli bir haldeki ürünlerin entalpileri ile aynı haldeki girdilerin entalpileri arasındaki fark olarak tanımlanır. Yanma entalpisi h C : Yanma işleminde, tepkime entalpisi genellikle yanma entalpisi,hy, olarak adlandırılır. Bu 1 kmol (veya 1 kg) yakıt belli bir basınç ve sıcaklıkta tamamen yandığı zaman ortaya çıkan ısı miktarını temsil eder. Oluşum entalpisi h f : Bu özellik belli bir haldeki bir maddenin kendi kimyasal bileşiminden ileri gelen entalpi olarak görülen oluşum entalpisi, h o dir. Başlangıç noktası oluşturmak üzere, tüm kararlı elementlerin (O 2, N 2, H 2, ve C gibi) 25 C ve 1 atm deki standart referans haldeki oluşum entalpileri sıfır kabul edilir. Yani, tüm kararlı elementler için h ol = 0 dır. (Bu 0.01 C deki doygun sıvı suyun iç enerjisinin sıfır olarak alınmasından farklı değildir). 12
13 Yanma entalpisi, bir yakıtın belli bir haldeki kararlı akım işlemi sırasında yanarken ortaya çıkan enerji miktarını gösterir. 13
14 Enthalpy of formation: The enthalpy of a substance at a specified state due to its chemical composition. 14
15 Isıl değer: Bir yakıt kararlı akım işleminde tamamen yandığında ve ürünler girdilerin haline döndüğünde ortaya çıkan ısı miktarı olarak tanımlanır. (HHV) üst ısıl değer: Isı değeri ürünlerde bulunan suyun fazına bağlıdır. Ürünlerdeki su sıvı halde olduğunda ısı değerine üst ısı değeri denir. (LHV) alt ısıl değer:ürünlerdeki su buhar fazında ise alt ısı değeri denir. Burada m, birim kütledeki yakıt başına ürünlerdeki suyun kütlesi, ve h fg belli bir sıcaklıkta suyun buharlaşma entalpisidir. For the fuels with variable composition (i.e., coal, natural gas, fuel oil), the heating value may be determined by burning them directly in a bomb calorimeter. 15
16 TEPKİMELİ SİSTEMLERİN BİRİNCİ YASA ANALİZİ Kimyasal olarak tepkimeye giren sistemlerde onların kimyasal enerjilerinin değişmesi gerekir ve bu nedenle, kimyasal enerjideki değişimleri açıkça ifade edebilmek için, enerji denklik bağıntılarının yeniden yazılması daha uygundur. Bu ilk önce kararlı akım sistemleri için sonra da kapalı sistemler için yapılır. Sürekli Akış Sistemleri The enthalpy of a chemical component at a specified state Burada parantez içindeki terim belli bir haldeki duyulan entalpi,h, ile 25 C ve 1 atm deki standart referans haldeki duyulan entalpi,ho, arasındaki fark olan standart referans hale göre duyulan entalpiyi göstermektedir. Bu tanım, oluşumlarında kullanılan referans hale bakılmaksızın tablolardan alınan entalpi değerlerini kullanma imkanı tanır. 16
17 17
18 Sisteme verilen ısı ve sistem tarafından yapılan iş pozitif büyüklükler alarak, yukarıdaki enerji denklik bağıntısı aşağıda olduğu gibi daha kısaolarak ifade edilebilir. Eğer belli bir tepkimenin yanma entalpisi h Y elde edilebilirse, 1 mol yakıtiçin kararlı akım eşitliği Yanma odasında normal olarak ısı çıkışı olur ama hiç ısı girişi olmaz. O zaman, tipik kararlı akım yanma işleminin enerji denkliği 18
19 Kapalı Sistemler Kimyasal olarak tepkimeye giren durağan kapalı sistemler için genel bir enerji denklik bağıntısı Egiriş Eçıkış Esistem aşağıdaki gibi yazılabilir. Bir kimyasal bileşenin iç enerjisinin entalpiye bağlı olarak ifadesi. oluşum iç enerjisi u ol entalpi tanımı oluşum entalpisi h f yakıtın faz durumuna bağlı olduğu için yakıtın katı, sıvı veya gaz olduğunun bilinmesi gerekir. Ayrıca, kendi entalpisini belirlemek için, yanma odasına girdiğinde yakıtın halinin de bilinmesi gerekir. 19
20 ADYABATİK ALEV SICAKLIĞI Hiç bir iş etkileşim ve kinetik ve potansiyel enerjide herhangi bir değişim olmağında, yanma işleminde ortaya çıkan kimyasal enerji ya çevreye ısı olarak verilir ya da yanma ürünlerinin sıcaklıklarının yükseltme için içeride kullanılır. Isı kaybı azaldıkça sıcaklıktaki yükselme artar. Çevreye hiç ısı kaybının olmadığı sınır halinde, (Q= 0), ürünlerin sıcaklıkları tepkimenin adyabatik alev veya adyabatik yanma sıcaklığı denilen maksimum değerine ulaşacaktır. Olduğu için Kararlı akım yanma işleminde adyabatik alev sıcaklığı Eşitlik Q=0 ve W =0 konularak bulunabilir. Bir yanma odasının sıcaklığı tam yanma olduğunda ve çevreye hiç ısı kaybı olmadığında maksimumdur. (Q=0). 20
21 Bir yakıtın adiyabatik alev sıcaklığı şunlara bağlıdır: (1) Tepkimeye giren maddelerin durumu (2) Reaksiyonun tamamlanma derecesi (3)Kullanılan hava miktarı Oluşum entalpisi h f yakıtın faz durumuna bağlı olduğu için yakıtın katı, sıvı veya gaz olduğunun bilinmesi gerekir. Ayrıca, kendi entalpisini belirlemek için, yanma odasına girdiğinde yakıtın halinin de bilinmesi gerekir. Entalpi hesaplamalarında, yakıt ve havanın yanma odasına karışım halinde mi yoksa ayrı ayrımı girdiğinin bilinmesi özellikle önemlidir. Yanma ürünleri düşük sıcaklıklara soğutulduğunda, gaz ürünler içindeki suyun bir kısmının yoğuşma olasılığının göz önüne alınması gerekir. Yanma odasında meydana gelen maksimum sıcaklık kuramsal adiyabatik sıcaklıktan daha düşüktür. 21
22 ENTROPY CHANGE OF REACTING SYSTEMS entropy balance for any system (including reacting systems) undergoing any process for a closed or steady-flow reacting system for an adiabatic process (Q = 0) The entropy change associated with a chemical relation. 22
23 Entropy of a component P 0 = 1 atm P i partial pressure y i mole fraction P m total pressure of mixture. When evaluating the entropy of a component of an ideal-gas mixture, we should use the temperature and the partial pressure of the component. The absolute entropy values are listed in Tables A 18 through A 25 for various ideal gases at the specified temperature and at a pressure of 1 atm. The absolute entropy values for various fuels are listed in Table A 26 at the standard reference state of 25 C and 1 atm. At a specified temperature, the absolute entropy of an ideal gas at pressures other than P 0 = 1 atm can be determined by subtracting R u ln (P/P 0 ) from the tabulated value at 1 atm. 23
24 SECOND-LAW ANALYSIS OF REACTING SYSTEMS Exergy destruction The reversible work for a steady-flow combustion process that involves heat transfer with only the surroundings at T 0 When both the reactants and the products are at T 0 Gibbs function The difference between the exergy of the reactants and of the products during a chemical reaction is the reversible work associated with that reaction. 24
25 For the very special case of T react = T prod = T 0 = 25 C We can conclude from the above equation that the value (the negative of the Gibbs function of formation at 25 C and 1 atm) of a compound represents the reversible work associated with the formation of that compound from its stable elements at 25 C and 1 atm in an environment at 25 C and 1 atm. 25
26 Özet Yanma Hava-yakıt oranı Stokiyometrik veya kuramsal yanma Yanma entalpisi Oluşum entalpisi Bir yakıtın ısıl değeri yakıt kararlı akım işleminde tamamen yandığı ve ürünler girdilerin haline geri döndüğünde ortaya çıkan ısı miktarı olarak tanımlanır. Bir yakıtın ısıl değeri o yakıtın yanma entalpisinin mutlak değerine eşittir. Adyabatik alev sıcaklığı 26
%20 Fazla hava dikkate alınarak yanma denklemi aşağıdaki şekilde yazılır:
 Zonguldak Karaelmas Üniversitesi 2010-2011 Güz Dönemi Mühendislik Fakültesi Makine Mühendisliği Bölümü 10 Kasım 2010 Çarşamba, 17:00 MAK 411 Yanma Teorisi Arasınav Sorular ve Çözümleri Soru 1 %90 Metan
Zonguldak Karaelmas Üniversitesi 2010-2011 Güz Dönemi Mühendislik Fakültesi Makine Mühendisliği Bölümü 10 Kasım 2010 Çarşamba, 17:00 MAK 411 Yanma Teorisi Arasınav Sorular ve Çözümleri Soru 1 %90 Metan
STOKİYOMETRİ. Kimyasal Tepkimelerde Kütle İlişkisi
 STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
STOKİYOMETRİ Kimyasal Tepkimelerde Kütle İlişkisi Sülfür oksijen içerisinde yanarak kükürt dioksit oluşturur. Modeller elementel sülfürü (S8), oksijeni ve kükürt dioksit moleküllerini göstermektedir. Her
İDEAL GAZ KARIŞIMLARI
 İdeal Gaz Karışımları İdeal gaz karışımları saf ideal gazlar gibi davranırlar. Saf gazlardan n 1, n 2,, n i, mol alınarak hazırlanan bir karışımın toplam basıncı p, toplam hacmi v ve sıcaklığı T olsun.
İdeal Gaz Karışımları İdeal gaz karışımları saf ideal gazlar gibi davranırlar. Saf gazlardan n 1, n 2,, n i, mol alınarak hazırlanan bir karışımın toplam basıncı p, toplam hacmi v ve sıcaklığı T olsun.
Sıcaklık (Temperature):
 Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
Sıcaklık (Temperature): Sıcaklık tanım olarak bir maddenin yapısındaki molekül veya atomların ortalama kinetik enerjilerinin ölçüm değeridir. Sıcaklık t veya T ile gösterilir. Termometre kullanılarak ölçülür.
E = U + KE + KP = (kj) U = iç enerji, KE = kinetik enerji, KP = potansiyel enerji, m = kütle, V = hız, g = yerçekimi ivmesi, z = yükseklik
 Enerji (Energy) Enerji, iş yapabilme kabiliyetidir. Bir sistemin enerjisi, o sistemin yapabileceği azami iştir. İş, bir cisme, bir kuvvetin tesiri ile yol aldırma, yerini değiştirme şeklinde tarif edilir.
Enerji (Energy) Enerji, iş yapabilme kabiliyetidir. Bir sistemin enerjisi, o sistemin yapabileceği azami iştir. İş, bir cisme, bir kuvvetin tesiri ile yol aldırma, yerini değiştirme şeklinde tarif edilir.
KİMYASAL BİLEŞİKLER İÇERİK
 KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
KİMYASAL BİLEŞİKLER İÇERİK Mol, Molar Kütle Kimyasal Formülden Yüzde Bileşiminin Hesaplanması Bir Bileşiğin Yüzde Bileşiminden Kimyasal Formülünün Hesaplanması Organik Bileşiklerin Kimyasal Bileşiminin
Bölüm 3 SAF MADDENİN ÖZELLİKLERİ
 Bölüm 3 SAF MADDENİN ÖZELLİKLERİ 1 Amaçlar Amaçlar Saf madde kavramının tanıtılması Faz değişimi işleminin fizik ilkelerinin incelenmesi Saf maddenin P-v-T yüzeylerinin ve P-v, T-v ve P-T özelik diyagramlarının
Bölüm 3 SAF MADDENİN ÖZELLİKLERİ 1 Amaçlar Amaçlar Saf madde kavramının tanıtılması Faz değişimi işleminin fizik ilkelerinin incelenmesi Saf maddenin P-v-T yüzeylerinin ve P-v, T-v ve P-T özelik diyagramlarının
Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı. Bölüm 4: Kimyasal Tepkimeler
 Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı Bölüm 4: Kimyasal Tepkimeler İçindekiler 4-1 Kimyasal Tepkimeler ve Kimyasal Eşitlikler 4-2 Kimyasal Eşitlik ve Stokiyometri
Genel Kimya Prensipleri ve Modern Uygulamaları Petrucci Harwood Herring 8. Baskı Bölüm 4: Kimyasal Tepkimeler İçindekiler 4-1 Kimyasal Tepkimeler ve Kimyasal Eşitlikler 4-2 Kimyasal Eşitlik ve Stokiyometri
Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar.
 Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
NOT: Toplam 5 soru çözünüz, sınav süresi 90 dakikadır. SORULAR VE ÇÖZÜMLER
 Adı- Soyadı: Fakülte No : Gıda Mühendisliği Bölümü, 2015/2016 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Dönem Sonu Sınavı Soru ve Çözümleri 07.01.2016 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
Adı- Soyadı: Fakülte No : Gıda Mühendisliği Bölümü, 2015/2016 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Dönem Sonu Sınavı Soru ve Çözümleri 07.01.2016 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
Katlı oranlar kanunu. 2H 2 + O 2 H 2 O Sabit Oran ( 4 g 32 g 36 g. 2 g 16 g 18 g. 1 g 8 g 9 g. 8 g 64 g 72 g. N 2 + 3H 2 2NH 3 Sabit Oran (
 Sabit oranlar kanunu Bir bileşiği oluşturan elementlerin kütleleri arasında sabit bir oran vardır. Bu sabit oranın varlığı ilk defa 799 tarihinde Praust tarafından bulunmuş ve sabit oranlar kanunu şeklinde
Sabit oranlar kanunu Bir bileşiği oluşturan elementlerin kütleleri arasında sabit bir oran vardır. Bu sabit oranın varlığı ilk defa 799 tarihinde Praust tarafından bulunmuş ve sabit oranlar kanunu şeklinde
TERMODİNAMİK ÇALIŞMA SORULARI
 TRMODİNAMİK ÇALIŞMA SORULARI SÜRKLİ AKIŞLI AÇIK SİSTMLR LÜLLR YAYICILAR 5-8 Sürekli akışlı adyabatik bir lülede, ava lüleye 00 kpa basınç, 00 o C sıcaklık ve 45 m/s ızla girmekte, 00 kpa basınç ve 0 m/s
TRMODİNAMİK ÇALIŞMA SORULARI SÜRKLİ AKIŞLI AÇIK SİSTMLR LÜLLR YAYICILAR 5-8 Sürekli akışlı adyabatik bir lülede, ava lüleye 00 kpa basınç, 00 o C sıcaklık ve 45 m/s ızla girmekte, 00 kpa basınç ve 0 m/s
Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar Temel: 100 mol kuru su gazı. caklık k ve 5 bar basınc
 Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar 007 ÖRNEK 5-165 00 0 C sıcakls caklık k ve 5 bar basınc ncında nda olan bir kızgk zgın n buhar, 100 0 C sıcakls caklıkta kta olan kızgk zgın n kok kömürük üzerinden
Yrd. Doç. Dr. Atilla EVCİN Afyonkarahisar 007 ÖRNEK 5-165 00 0 C sıcakls caklık k ve 5 bar basınc ncında nda olan bir kızgk zgın n buhar, 100 0 C sıcakls caklıkta kta olan kızgk zgın n kok kömürük üzerinden
GAZLAR GAZ KARIŞIMLARI
 DALTON KISMİ BASINÇLAR YASASI Aynı Kaplarda Gazların Karıştırılması Birbiri ile tepkimeye girmeyen gaz karışımlarının davranışı genellikle ilgi çekicidir. Böyle bir karışımdaki bir bileşenin basıncı, aynı
DALTON KISMİ BASINÇLAR YASASI Aynı Kaplarda Gazların Karıştırılması Birbiri ile tepkimeye girmeyen gaz karışımlarının davranışı genellikle ilgi çekicidir. Böyle bir karışımdaki bir bileşenin basıncı, aynı
1. HAFTA Giriş ve Temel Kavramlar
 1. HAFTA Giriş ve Temel Kavramlar TERMODİNAMİK VE ISI TRANSFERİ Isı: Sıcaklık farkının bir sonucu olarak bir sistemden diğerine transfer edilebilen bir enerji türüdür. Termodinamik: Bir sistem bir denge
1. HAFTA Giriş ve Temel Kavramlar TERMODİNAMİK VE ISI TRANSFERİ Isı: Sıcaklık farkının bir sonucu olarak bir sistemden diğerine transfer edilebilen bir enerji türüdür. Termodinamik: Bir sistem bir denge
Kimyanın Temel Kanunları
 Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
Kimyanın Temel Kanunları A. Kütlenin Korunumu Kanunu Lavoiser miktarı belli olan kalay (Sn) parçasını içinde bir miktar hava bulunan bir fanusa koyarak tartmış.daha sonra fanusu içindekilerle birlikte
3.BÖLÜM: TERMODİNAMİĞİN I. YASASI
 3.BÖLÜM: TERMODİNAMİĞİN I. YASASI S (k) + O SO + ısı Reaksiyon sonucunda sistemden ortama verilen ısı, sistemin iç enerjisinin bir kısmının ısı enerjisine dönüşmesi sonucunda ortaya çıkmıştır. Enerji sistemden
3.BÖLÜM: TERMODİNAMİĞİN I. YASASI S (k) + O SO + ısı Reaksiyon sonucunda sistemden ortama verilen ısı, sistemin iç enerjisinin bir kısmının ısı enerjisine dönüşmesi sonucunda ortaya çıkmıştır. Enerji sistemden
!" #$%&'! ( ')! *+*,(* *' *, -*.*. /0 1, -*.*
 2. BÖLÜM SAF MADDELERİN ERMODİNAMİK ÖZELLİKLERİ Saf madde Saf madde, her noktasında aynı e değişmeyen bir kimyasal bileşime sahip olan maddeye denir. Saf maddenin sadece bir tek kimyasal element eya bileşimden
2. BÖLÜM SAF MADDELERİN ERMODİNAMİK ÖZELLİKLERİ Saf madde Saf madde, her noktasında aynı e değişmeyen bir kimyasal bileşime sahip olan maddeye denir. Saf maddenin sadece bir tek kimyasal element eya bileşimden
Bölüm 7 ENTROPİ. Bölüm 7: Entropi
 Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
Kurutma Tekniği. Nemli Havanın Tanımı
 Kurutma Tekniği Nemli Havanın Tanımı Kurutucu Akışkanın (Nemli havanın) Termodinamik Tanımı Kuru hava: İçerisinde su buharı bulunmayan hava. Atmosferik hava: Kuru hava ve su buharının olduğu hava Kurutucu
Kurutma Tekniği Nemli Havanın Tanımı Kurutucu Akışkanın (Nemli havanın) Termodinamik Tanımı Kuru hava: İçerisinde su buharı bulunmayan hava. Atmosferik hava: Kuru hava ve su buharının olduğu hava Kurutucu
ENERJİ DENKLİKLERİ 1
 ENERJİ DENKLİKLERİ 1 Enerji ilk kez Newton tarafından ortaya konmuştur. Newton, kinetik ve potansiyel enerjileri tanımlamıştır. 2 Enerji; Potansiyel, Kinetik, Kimyasal, Mekaniki, Elektrik enerjisi gibi
ENERJİ DENKLİKLERİ 1 Enerji ilk kez Newton tarafından ortaya konmuştur. Newton, kinetik ve potansiyel enerjileri tanımlamıştır. 2 Enerji; Potansiyel, Kinetik, Kimyasal, Mekaniki, Elektrik enerjisi gibi
Chapter 3 SAF MADDENİN ÖZELLİKLERİ
 Chapter 3 SAF MADDENİN ÖZELLİKLERİ Ceyhun Yılmaz Afyon Kocatepe Üniversitesi Objectives Saf madde kavramının tanıtılması. Faz değişimi işleminin fizik ilkelerinin incelenmesi. Saf maddenin P-v-T yüzeylerinin
Chapter 3 SAF MADDENİN ÖZELLİKLERİ Ceyhun Yılmaz Afyon Kocatepe Üniversitesi Objectives Saf madde kavramının tanıtılması. Faz değişimi işleminin fizik ilkelerinin incelenmesi. Saf maddenin P-v-T yüzeylerinin
DOĞAL GAZ YAKITLI BİR YANMA ODASINDA HAVA VE YAKIT SICAKLIKLARININ SICAKLIK, ENTALPİ VE ENTROPİ ÜZERİNDEKİ ETKİLERİNİN İNCELENMESİ
 Ordu Üniv. Bil. Tek. Derg., Cilt:4, Sayı:2, 2014,24-31/Ordu Univ. J. Sci. Tech., Vol:4, No:2,2014,24-31 DOĞAL GAZ YAKITLI BİR YANMA ODASINDA HAVA VE YAKIT SICAKLIKLARININ SICAKLIK, ENTALPİ VE ENTROPİ ÜZERİNDEKİ
Ordu Üniv. Bil. Tek. Derg., Cilt:4, Sayı:2, 2014,24-31/Ordu Univ. J. Sci. Tech., Vol:4, No:2,2014,24-31 DOĞAL GAZ YAKITLI BİR YANMA ODASINDA HAVA VE YAKIT SICAKLIKLARININ SICAKLIK, ENTALPİ VE ENTROPİ ÜZERİNDEKİ
Soru No Program Çıktısı 3, ,10 8,10
 Öğrenci Numarası Adı ve Soyadı İmzası: CEVAP ANAHTARI Açıklama: Sınavda ders notları ve dersle ilgili tablolar serbesttir. Sorular eşit puanlıdır. SORU 1. Bir teknik sisteme 120 MJ enerji verilerek 80000
Öğrenci Numarası Adı ve Soyadı İmzası: CEVAP ANAHTARI Açıklama: Sınavda ders notları ve dersle ilgili tablolar serbesttir. Sorular eşit puanlıdır. SORU 1. Bir teknik sisteme 120 MJ enerji verilerek 80000
BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal
 BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal tepkime kavramlarının anlaşılması Termodinamiğin II. yasasının
BÖLÜM 19 KİMYASAL TERMODİNAMİK ENTROPİ VE SERBEST ENERJİ Öğrenme Hedefleri ve Anahtar Kavramlar: Kendiliğinden, tersinir, tersinmez ve izotermal tepkime kavramlarının anlaşılması Termodinamiğin II. yasasının
MOL KAVRAMI I. ÖRNEK 2
 MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
MOL KAVRAMI I Maddelerin taneciklerden oluştuğunu biliyoruz. Bu taneciklere atom, molekül ya da iyon denir. Atom : Kimyasal yöntemlerle daha basit taneciklere ayrılmayan ve elementlerin yapıtaşı olan taneciklere
STOKĐYOMETRĐ. Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK
 STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
STOKĐYOMETRĐ Yrd.Doç.Dr. İbrahim İsmet ÖZTÜRK 3. Stokiyometri 3.1. Atom Kütlesi 3.1.1.Ortalama Atom Kütlesi 3.2. Avagadro Sayısı ve Elementlerin Mol Kütleleri 3.3. Molekül Kütlesi 3.4. Kütle Spektrometresi
Özgül ısı : Q C p = m (Δ T)
 Özgül ısı : Bir maddenin faz değişimine uğramaksızın belli bir sıcaklığa ulaşması için, bu maddenin birim kütlesi tarafından kazanılan veya kaybedilen ısı miktarıdır. Q C p = m (Δ T) 1 Gıdaların Özgül
Özgül ısı : Bir maddenin faz değişimine uğramaksızın belli bir sıcaklığa ulaşması için, bu maddenin birim kütlesi tarafından kazanılan veya kaybedilen ısı miktarıdır. Q C p = m (Δ T) 1 Gıdaların Özgül
1 mol = 6, tane tanecik. Maddelerde tanecik olarak atom, molekül ve iyonlar olduğunda dolayı mol ü aşağıdaki şekillerde tanımlamak mümkündür.
 1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
1 GENEL KİMYA Mol Kavramı 1 Mol Kavramı Günlük hayatta kolaylık olsun diye, çok küçük taneli olan maddeler tane yerine birimlerle ifade edilir. Örneğin pirinç alınırken iki milyon tane pirinç yerine ~
Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli)
 Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli) Kişilik, enerjiyi yönetebilme ve verimli kullanabilme kabiliyetinin bir göstergesidir (A. Midilli) SUMMER COURSE ON EXERGY AND
Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli) Kişilik, enerjiyi yönetebilme ve verimli kullanabilme kabiliyetinin bir göstergesidir (A. Midilli) SUMMER COURSE ON EXERGY AND
KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ
 KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ 1. Aşağıda verilen birim çevirme işlemlerini yapınız. a) 554 m 4 day. kg cm 4 min. g (38472.2 cm4 min. g ) b) 5.37x10 3 kj min hp (120 hp) c) 760 miles h
KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ 1. Aşağıda verilen birim çevirme işlemlerini yapınız. a) 554 m 4 day. kg cm 4 min. g (38472.2 cm4 min. g ) b) 5.37x10 3 kj min hp (120 hp) c) 760 miles h
TermoKimya (Thermochemistry)
 TermoKimya (Thermochemistry) Kimyasal tepkimeler sonucu oluşan ısı değişimlerini inceleyen çalışma alanı. ENERJİ Kinetik enerji, Potansiyel enerji Enerji:İş yapabilme kapasitesidir. Kinetik enerji:hareket
TermoKimya (Thermochemistry) Kimyasal tepkimeler sonucu oluşan ısı değişimlerini inceleyen çalışma alanı. ENERJİ Kinetik enerji, Potansiyel enerji Enerji:İş yapabilme kapasitesidir. Kinetik enerji:hareket
Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli)
 Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli) Kişilik, enerjiyi yönetebilme ve verimli kullanabilme kabiliyetinin bir göstergesidir (A. Midilli) SUMMER COURSE ON EXERGY AND
Entropi tünelinden çıkmanın tek yolu ekserji iksirini içmektir! (A. Midilli) Kişilik, enerjiyi yönetebilme ve verimli kullanabilme kabiliyetinin bir göstergesidir (A. Midilli) SUMMER COURSE ON EXERGY AND
KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ
 KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ 1. Aşağıda verilen birim çevirme işlemlerini yapınız. ) 554 ) 5.37x10.. h ) 760 h ) 921 ) 800, ) 25 ) 23.. ) 0.981.. ) 8.314... ) 0.052..h 2. Bir atık su
KYM 101 KİMYA MÜHENDİSLĞİNE GİRİŞ PROBLEM SETİ 1. Aşağıda verilen birim çevirme işlemlerini yapınız. ) 554 ) 5.37x10.. h ) 760 h ) 921 ) 800, ) 25 ) 23.. ) 0.981.. ) 8.314... ) 0.052..h 2. Bir atık su
3. Kimyasal Bileşikler
 TOBB Ekonomi ve Teknoloji Üniversitesi 3. Kimyasal Bileşikler Mol kavramı ve kimyasal bileşikler Kimyasal Bileşik Formülleri (Kaba vs Molekül Formülü) Yüzde bileşimin hesaplanması Yakma analizi TOBB Ekonomi
TOBB Ekonomi ve Teknoloji Üniversitesi 3. Kimyasal Bileşikler Mol kavramı ve kimyasal bileşikler Kimyasal Bileşik Formülleri (Kaba vs Molekül Formülü) Yüzde bileşimin hesaplanması Yakma analizi TOBB Ekonomi
Dokuz Eylül Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, Buca/İZMİR. Yanma. Prof.Dr. Abdurrahman BAYRAM
 Dokuz Eylül Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, Buca/İZMİR Yanma Prof.Dr. Abdurrahman BAYRAM Telefon: 0232 3017494 Faks: 0232 3017498 E-Mail: abayram@deu.edu.tr ÇEV 3016 Hava
Dokuz Eylül Üniversitesi, Mühendislik Fakültesi, Çevre Mühendisliği Bölümü, Buca/İZMİR Yanma Prof.Dr. Abdurrahman BAYRAM Telefon: 0232 3017494 Faks: 0232 3017498 E-Mail: abayram@deu.edu.tr ÇEV 3016 Hava
FOSİL YAKITLARIN YANMASI
 Kömür, sıvı yakıtlar ve doğal gazın yakılması sırasında açığa çıkan bazı gazların zehirleyici etkileri ve çevre için zararları vardır. Kükürtdioksit (SO 2 ) ve (NO x ) ler bu zararlı gazların miktar ve
Kömür, sıvı yakıtlar ve doğal gazın yakılması sırasında açığa çıkan bazı gazların zehirleyici etkileri ve çevre için zararları vardır. Kükürtdioksit (SO 2 ) ve (NO x ) ler bu zararlı gazların miktar ve
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI
 ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER YASEMĐN KONMAZ 20338575 Çalışma Yaprağı Ders Anlatımı: REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER: 1.Reaktif Maddelerin
ÖĞRETĐM TEKNOLOJĐLERĐ VE MATERYAL GELĐŞĐMĐ ÇALIŞMA YAPRAĞI REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER YASEMĐN KONMAZ 20338575 Çalışma Yaprağı Ders Anlatımı: REAKSĐYON HIZINA ETKĐ EDEN FAKTÖRLER: 1.Reaktif Maddelerin
ISI VE SICAKLIK. 1 cal = 4,18 j
 ISI VE SICAKLIK ISI Isı ve sıcaklık farklı şeylerdir. Bir maddeyi oluşturan bütün taneciklerin sahip olduğu kinetik enerjilerin toplamına ISI denir. Isı bir enerji türüdür. Isı birimleri joule ( j ) ve
ISI VE SICAKLIK ISI Isı ve sıcaklık farklı şeylerdir. Bir maddeyi oluşturan bütün taneciklerin sahip olduğu kinetik enerjilerin toplamına ISI denir. Isı bir enerji türüdür. Isı birimleri joule ( j ) ve
NOT: Toplam 5 soru çözünüz, sınav süresi 90 dakikadır. SORULAR VE ÇÖZÜMLER
 Adı- Soyadı : Fakülte No : Gıda Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Bütünleme Sınavı Soru ve Çözümleri 23.01.2015 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
Adı- Soyadı : Fakülte No : Gıda Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Bütünleme Sınavı Soru ve Çözümleri 23.01.2015 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
TEKNİK FİZİK ÖRNEK PROBLEMLER-EK2 1
 TEKNİK FİZİK ÖRNEK PROBLEMLER-EK2 ÖRNEK PROBLEM (KİNETİK ENERJİ) RÜZER şirketi 40 kw güce sahip bir rüzgar çiftliği kurmayı planlamıştır. Tasarlanan rüzgar türbinine gelecek rüzgarın debisi 000 kg/s dir.
TEKNİK FİZİK ÖRNEK PROBLEMLER-EK2 ÖRNEK PROBLEM (KİNETİK ENERJİ) RÜZER şirketi 40 kw güce sahip bir rüzgar çiftliği kurmayı planlamıştır. Tasarlanan rüzgar türbinine gelecek rüzgarın debisi 000 kg/s dir.
KİNETİK GAZ KURAMI. Doç. Dr. Faruk GÖKMEŞE Kimya Bölümü Hitit Üniversitesi Fen Edebiyat Fakültesi 1
 Kinetik Gaz Kuramından Gazların Isınma Isılarının Bulunması Sabit hacimdeki ısınma ısısı (C v ): Sabit hacimde bulunan bir mol gazın sıcaklığını 1K değiştirmek için gerekli ısı alışverişi. Sabit basınçtaki
Kinetik Gaz Kuramından Gazların Isınma Isılarının Bulunması Sabit hacimdeki ısınma ısısı (C v ): Sabit hacimde bulunan bir mol gazın sıcaklığını 1K değiştirmek için gerekli ısı alışverişi. Sabit basınçtaki
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ
 Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ http://public.cumhuriyet.edu.tr/alipinarbasi/ 1 Prof. Dr. Ali PINARBAŞI Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ http://public.cumhuriyet.edu.tr/alipinarbasi/ 1 Prof. Dr. Ali PINARBAŞI Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak
TY T Temel Yeterlilik Testi
 Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
Ortaöğretim lanı MF - 01 TY T Temel Yeterlilik Testi Kimya Ders Föyü Mol Mol: Maddeyi oluşturan tanecikleri saymayı kolaylaştıran bir paketleme sistemidir. 1. 3 S atomu için verilen; I. 1 mol S atomu 3
7. Bölüm: Termokimya
 7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
7. Bölüm: Termokimya Termokimya: Fiziksel ve kimyasal değişimler sürecindeki enerji (ısı ve iş) değişimlerini inceler. sistem + çevre evren Enerji: İş yapabilme kapasitesi. İş(w): Bir kuvvetin bir cismi
BAŞKENT ÜNİVERSİTESİ MAKİNE MÜHENDİSLİĞİ BÖLÜMÜ MAK 402 MAKİNE MÜHENDİSLİĞİ LABORATUVARI DENEY - 5 PSİKROMETRİK İŞLEMLERDE ENERJİ VE KÜTLE DENGESİ
 BAŞKENT ÜNİVERSİTESİ MAKİNE MÜHENDİSLİĞİ BÖLÜMÜ MAK 402 MAKİNE MÜHENDİSLİĞİ LABORATUVARI DENEY - 5 PSİKROMETRİK İŞLEMLERDE ENERJİ VE KÜTLE DENGESİ BAŞKENT ÜNİVERSİTESİ MAKİNA MÜHENDİSLİĞİ BÖLÜMÜ MAK 402
BAŞKENT ÜNİVERSİTESİ MAKİNE MÜHENDİSLİĞİ BÖLÜMÜ MAK 402 MAKİNE MÜHENDİSLİĞİ LABORATUVARI DENEY - 5 PSİKROMETRİK İŞLEMLERDE ENERJİ VE KÜTLE DENGESİ BAŞKENT ÜNİVERSİTESİ MAKİNA MÜHENDİSLİĞİ BÖLÜMÜ MAK 402
Termodinamik. Öğretim Görevlisi Prof. Dr. Lütfullah Kuddusi. Bölüm 4: Kapalı Sistemlerin Enerji Analizi
 Termodinamik Öğretim Görevlisi Prof. Dr. Lütfullah Kuddusi 1 Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 2 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan
Termodinamik Öğretim Görevlisi Prof. Dr. Lütfullah Kuddusi 1 Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 2 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan
MAKİNE VE TEÇHİZAT İŞLERİNDE İSG
 MAKİNE VE TEÇHİZAT İŞLERİNDE İSG 3.HAFTA Hazırlayan: Öğr. Gör. Tuğberk ÖNAL MALATYA 2017 YAKITLAR -YANMA Enerji birçok ülke için günümüzün en önemli sorunlarının başında gelmektedir. Özellikle ülkemiz
MAKİNE VE TEÇHİZAT İŞLERİNDE İSG 3.HAFTA Hazırlayan: Öğr. Gör. Tuğberk ÖNAL MALATYA 2017 YAKITLAR -YANMA Enerji birçok ülke için günümüzün en önemli sorunlarının başında gelmektedir. Özellikle ülkemiz
T.C. Ölçme, Seçme ve Yerleştirme Merkezi
 T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 17 HAZİRAN 2017 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 17 HAZİRAN 2017 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
SORULAR VE ÇÖZÜMLER. Adı- Soyadı : Fakülte No :
 Adı- Soyadı : Fakülte No : Gıda Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Dönem Sonu Sınavı Soru ve Çözümleri 06.01.2015 Soru (puan) 1 (15) 2 (15) 3 (15) 4 (20)
Adı- Soyadı : Fakülte No : Gıda Mühendisliği Bölümü, 2014/2015 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Dönem Sonu Sınavı Soru ve Çözümleri 06.01.2015 Soru (puan) 1 (15) 2 (15) 3 (15) 4 (20)
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL
 DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
DERSĐN SORUMLUSU : PROF.DR ĐNCĐ MORGĐL HAZIRLAYAN : HALE ÜNAL KĐMYASAL REAKSĐYONLARA GĐRĐŞ -Değişmeler ve Tepkime Türleri- Yeryüzünde bulunan tüm maddeler değişim ve etkileşim içerisinde bulunur. Maddelerdeki
SAKARYA ÜNİVERSİTESİ SAKARYA MESLEK YÜKSEKOKULU
 TERMODİNAMİK Öğr. Gör. SAKARYA ÜNİVERSİTESİ SAKARYA MESLEK YÜKSEKOKULU TERMODİNAMİĞİN BİLİM OLARAK YERİ VE TEMEL KAVRAMLARI, TARİF EDİLEN SİSTEMLERİ VE BUNLARA AİT TEMEL ÖZELLİKLER. TERMODİNAMİĞİN TANIMI
TERMODİNAMİK Öğr. Gör. SAKARYA ÜNİVERSİTESİ SAKARYA MESLEK YÜKSEKOKULU TERMODİNAMİĞİN BİLİM OLARAK YERİ VE TEMEL KAVRAMLARI, TARİF EDİLEN SİSTEMLERİ VE BUNLARA AİT TEMEL ÖZELLİKLER. TERMODİNAMİĞİN TANIMI
ENERJİ YÖNETİMİ VE POLİTİKALARI
 ENERJİ YÖNETİMİ VE POLİTİKALARI KAZANLARDA ENERJİ VERİMLİLİĞİ ÖĞRENCİNİN ADI:KUBİLAY SOY ADI:KOÇ NUMARASI:15360038 KAZANLAR Yakıtın kimyasal enerjisini yanma yoluyla ısı enerjisine dönüştüren ve bu ısı
ENERJİ YÖNETİMİ VE POLİTİKALARI KAZANLARDA ENERJİ VERİMLİLİĞİ ÖĞRENCİNİN ADI:KUBİLAY SOY ADI:KOÇ NUMARASI:15360038 KAZANLAR Yakıtın kimyasal enerjisini yanma yoluyla ısı enerjisine dönüştüren ve bu ısı
YANMA. Derlenmiş Notlar. Mustafa Eyriboyun ZKÜ - 2009
 YANMA Derlenmiş Notlar Mustafa Eyriboyun ZKÜ - 2009 FAZ DENGESĐ Denge çözümlerinde, yanma sonrası ürün konsantrasyonlarının hesaplanmasında üç farklı yöntem kullanılabilir (Pratt and Wormeck, 1976): Bunlar,
YANMA Derlenmiş Notlar Mustafa Eyriboyun ZKÜ - 2009 FAZ DENGESĐ Denge çözümlerinde, yanma sonrası ürün konsantrasyonlarının hesaplanmasında üç farklı yöntem kullanılabilir (Pratt and Wormeck, 1976): Bunlar,
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ. Bölüm 4: Kapalı Sistemlerin Enerji Analizi
 Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 1 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan hareketli sınır işi veya PdV işi olmak üzere değişik iş biçimlerinin
Bölüm 4 KAPALI SİSTEMLERİN ENERJİ ANALİZİ 1 Amaçlar Özellikle otomobil motoru ve kompresör gibi pistonlu makinelerde yaygın olarak karşılaşılan hareketli sınır işi veya PdV işi olmak üzere değişik iş biçimlerinin
Bölüm 5 KONTROL HACİMLERİ İÇİN KÜTLE VE ENERJİ ÇÖZÜMLEMESİ
 Bölüm 5 KONTROL HACİMLERİ İÇİN KÜTLE VE ENERJİ ÇÖZÜMLEMESİ Kütlenin korunumu: Kütle de enerji gibi korunum yasalarına uyar; başka bir deyişle, var veya yok edilemez. Kapalı sistemlerde: Sistemin kütlesi
Bölüm 5 KONTROL HACİMLERİ İÇİN KÜTLE VE ENERJİ ÇÖZÜMLEMESİ Kütlenin korunumu: Kütle de enerji gibi korunum yasalarına uyar; başka bir deyişle, var veya yok edilemez. Kapalı sistemlerde: Sistemin kütlesi
Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası
 Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası Sıcaklık, bir gaz molekülünün kütle merkezi hareketinin ortalama kinetic enerjisinin bir ölçüsüdür. Sıcaklık,
Termal Genleşme İdeal Gazlar Isı Termodinamiğin 1. Yasası Entropi ve Termodinamiğin 2. Yasası Sıcaklık, bir gaz molekülünün kütle merkezi hareketinin ortalama kinetic enerjisinin bir ölçüsüdür. Sıcaklık,
BÖLÜM 1: TEMEL KAVRAMLAR
 Sistem ve Hal Değişkenleri Üzerinde araştırma yapmak üzere sınırladığımız bir evren parçasına sistem, bu sistemi çevreleyen yere is ortam adı verilir. İzole sistem; Madde ve her türden enerji akışına karşı
Sistem ve Hal Değişkenleri Üzerinde araştırma yapmak üzere sınırladığımız bir evren parçasına sistem, bu sistemi çevreleyen yere is ortam adı verilir. İzole sistem; Madde ve her türden enerji akışına karşı
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
GENEL KİMYA ÇÖZELTİLER Homojen karışımlara çözelti denir. Çözelti bileşiminin ve özelliklerinin çözeltinin her yerinde aynı olması sebebiyle çözelti, «homojen» olarak nitelendirilir. Çözeltinin değişen
Bölüm 15 Kimyasal Denge. Denge Kavramı
 Öğrenme hedefleri ve temel beceriler: Bölüm 15 Kimyasal Denge Kimyasal denge ile ne kastedildiğini anlamak ve reaksiyon oranları ile nasıl ilgili olduğunu inceler Herhangi bir reaksiyon için denge sabiti
Öğrenme hedefleri ve temel beceriler: Bölüm 15 Kimyasal Denge Kimyasal denge ile ne kastedildiğini anlamak ve reaksiyon oranları ile nasıl ilgili olduğunu inceler Herhangi bir reaksiyon için denge sabiti
GENEL KİMYA. 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar
 GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
GENEL KİMYA 7. Konu: Kimyasal reaksiyonlar, Kimyasal eşitlikler, Kimyasal tepkime türleri, Kimyasal Hesaplamalar Kimyasal Reaksiyonlar Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki kimyasal değişme
Bölüm 3 SAF MADDENİN ÖZELLİKLERİ
 Bölüm 3 SAF MADDENİN ÖZELLİKLERİ 1 Amaçlar Saf madde kavramının tanıtılması Faz değişimi işleminin fizik ilkelerinin incelenmesi Saf maddenin P-v-T yüzeylerinin ve P-v, T-v ve P-T özelik diyagramlarının
Bölüm 3 SAF MADDENİN ÖZELLİKLERİ 1 Amaçlar Saf madde kavramının tanıtılması Faz değişimi işleminin fizik ilkelerinin incelenmesi Saf maddenin P-v-T yüzeylerinin ve P-v, T-v ve P-T özelik diyagramlarının
Termodinamik Termodinamik Süreçlerde İŞ ve ISI
 Termodinamik Süreçlerde İŞ ve ISI Termodinamik Hareketli bir pistonla bağlantılı bir silindirik kap içindeki gazı inceleyelim (Şekil e bakınız). Denge halinde iken, hacmi V olan gaz, silindir çeperlerine
Termodinamik Süreçlerde İŞ ve ISI Termodinamik Hareketli bir pistonla bağlantılı bir silindirik kap içindeki gazı inceleyelim (Şekil e bakınız). Denge halinde iken, hacmi V olan gaz, silindir çeperlerine
TEKNİK FİZİK/TERMODİNAMİK-ÖRNEK PROBLEMLER 1
 TEKNİK FİZİK/TERMODİNAMİK-ÖRNEK PROBLEMLER 1 1. TERMODİNAMİK ENERJİ Örnek Problem 1.1: Isıl kapasite/özgül ısı Yalıtımlı kapalı bir kapta bulunan 2.00 kg hava 10 0 C sıcaklıktan 22 0 C sıcaklığa kadar
TEKNİK FİZİK/TERMODİNAMİK-ÖRNEK PROBLEMLER 1 1. TERMODİNAMİK ENERJİ Örnek Problem 1.1: Isıl kapasite/özgül ısı Yalıtımlı kapalı bir kapta bulunan 2.00 kg hava 10 0 C sıcaklıktan 22 0 C sıcaklığa kadar
ΔH bir sistem ile çevresi arasındaki ısı transferiyle alakalı. Bir reaksiyonun ΔH ını hesaplayabiliyoruz. Hess yasası,
 TERMOKİMYA Termodinamiğin 1. kuralı, iç enerjinin (U) nasıl değiştiğiyle alakalı U U çevre U evren ΔU değişimleri ΔH ile alakalı U PV H ΔH bir ile çevresi arasındaki ısı transferiyle alakalı (@ sabit P)
TERMOKİMYA Termodinamiğin 1. kuralı, iç enerjinin (U) nasıl değiştiğiyle alakalı U U çevre U evren ΔU değişimleri ΔH ile alakalı U PV H ΔH bir ile çevresi arasındaki ısı transferiyle alakalı (@ sabit P)
TAMGA ENDÜSTRİYEL KONTROL SİSTEMLERİ LTD.ŞTİ., ENERJİ YÖNETİMİNDE SINIRSIZ ÇÖZÜMLER SUNAR. HOŞGELDİNİZ
 TAMGA ENDÜSTRİYEL KONTROL SİSTEMLERİ LTD.ŞTİ., ENERJİ YÖNETİMİNDE SINIRSIZ ÇÖZÜMLER SUNAR. HOŞGELDİNİZ TAMGA TRİO YANMA VERİMİ Yakma ekipmanları tarafından yakıtın içerdiği enerjinin, ısı enerjisine dönüştürülme
TAMGA ENDÜSTRİYEL KONTROL SİSTEMLERİ LTD.ŞTİ., ENERJİ YÖNETİMİNDE SINIRSIZ ÇÖZÜMLER SUNAR. HOŞGELDİNİZ TAMGA TRİO YANMA VERİMİ Yakma ekipmanları tarafından yakıtın içerdiği enerjinin, ısı enerjisine dönüştürülme
GENEL KİMYA. 10. Hafta.
 GENEL KİMYA 10. Hafta. Gazlar 2 Gaz halindeki elementler 25 0 C ve 1 atmosfer de gaz halinde bulunan elementler 3 Gaz halindeki bileşikler 4 Gazların Genel Özellikleri Gazlar, bulundukları kabın şeklini
GENEL KİMYA 10. Hafta. Gazlar 2 Gaz halindeki elementler 25 0 C ve 1 atmosfer de gaz halinde bulunan elementler 3 Gaz halindeki bileşikler 4 Gazların Genel Özellikleri Gazlar, bulundukları kabın şeklini
Konular: I. Değerlik bağı teorisi ve melezleģme (Ders #15 den devam) Karmaşık moleküllerde melezleşme tayini
 5.111 Ders Özeti #16 Bugün için okuma: Bölümler 6.13, 6.15, 6.16, 6.17, 6.18, ve 6.20 (3. Baskıda Bölümler 6.14, 6.16, 6.17, 6.18, 6.19 ve 6.21) Kimyasal Değişim Entalpisi. Ders #17 için okuma: Bölüm 7.1
5.111 Ders Özeti #16 Bugün için okuma: Bölümler 6.13, 6.15, 6.16, 6.17, 6.18, ve 6.20 (3. Baskıda Bölümler 6.14, 6.16, 6.17, 6.18, 6.19 ve 6.21) Kimyasal Değişim Entalpisi. Ders #17 için okuma: Bölüm 7.1
FİZİKOKİMYA I ARASINAV SORU VE CEVAPLARI 2013-14 GÜZ YARIYILI
 Soru 1: Aşağıdaki ifadeleri tanımlayınız. a) Sistem b)adyabatik sistem c) Kapalı sistem c) Bileşen analizi Cevap 1: a) Sistem: Üzerinde araştırma yapmak üzere sınırladığımız bir evren parçasına verilen
Soru 1: Aşağıdaki ifadeleri tanımlayınız. a) Sistem b)adyabatik sistem c) Kapalı sistem c) Bileşen analizi Cevap 1: a) Sistem: Üzerinde araştırma yapmak üzere sınırladığımız bir evren parçasına verilen
GENEL KİMYA 101 ÖDEV 3
 TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
TOBB EKONOMİ VE TEKNOLOJİ ÜNİVERSİTESİ-27 Kasım 2013 Bütün Şubeler GENEL KİMYA 101 ÖDEV 3 ÖNEMLİ! Ödev Teslim Tarihi: 6 Aralık 2013 Soru 1-5 arasında 2 soru Soru 6-10 arasında 2 soru Soru 11-15 arasında
Havacılık Meteorolojisi Ders Notları. 1. Atmosfer ve İçeriği
 Havacılık Meteorolojisi Ders Notları 1. Atmosfer ve İçeriği Yard.Doç.Dr. İbrahim Sönmez Ondokuz Mayıs Üniversitesi Ballıca Kampüsü Havacılık ve Uzay Bilimleri Fakültesi Meteoroloji Mühendisliği Bölümü
Havacılık Meteorolojisi Ders Notları 1. Atmosfer ve İçeriği Yard.Doç.Dr. İbrahim Sönmez Ondokuz Mayıs Üniversitesi Ballıca Kampüsü Havacılık ve Uzay Bilimleri Fakültesi Meteoroloji Mühendisliği Bölümü
SINAV SÜRESİ 90 DAKİKADIR. BAŞARILAR
 FİZİKSEL KİMYA I FİAL SIAVI 0.0.0 : AD SYAD : İMZA SRU 5 Toplam PUA 0. Zn(k) + C(g) ----> Zn(g) + C (g) reaksiyonu için standart reaksiyon entalpisinin sıcaklığa bağımlılığı olduğuna göre reaksiyon için;
FİZİKSEL KİMYA I FİAL SIAVI 0.0.0 : AD SYAD : İMZA SRU 5 Toplam PUA 0. Zn(k) + C(g) ----> Zn(g) + C (g) reaksiyonu için standart reaksiyon entalpisinin sıcaklığa bağımlılığı olduğuna göre reaksiyon için;
YANMA. Özgür Deniz KOÇ
 YANMA Özgür Deniz KOÇ 16360057 1 Yanma Tepkimesi Yanma Çeşitleri İÇİNDEKİLER Yavaş Yanma Hızlı Yanma Parlama ve Parlatma Kendi Kendine Yanma 2 Yanma Sınıfları Yanma Kayıpları 3 Yanma Tepkimesi Nedir Bir
YANMA Özgür Deniz KOÇ 16360057 1 Yanma Tepkimesi Yanma Çeşitleri İÇİNDEKİLER Yavaş Yanma Hızlı Yanma Parlama ve Parlatma Kendi Kendine Yanma 2 Yanma Sınıfları Yanma Kayıpları 3 Yanma Tepkimesi Nedir Bir
MADDENİN SINIFLANDIRILMASI
 MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
MADDENİN SINIFLANDIRILMASI MADDE Saf madde Karışımlar Element Bileşik Homojen Karışımlar Heterojen Karışımlar ELEMENT Tek cins atomlardan oluşmuş saf maddeye element denir. ELEMENTLERİN ÖZELLİKLERİ Elementler
TAM KLİMA TESİSATI DENEY FÖYÜ
 T.C BURSA TEKNİK ÜNİVERSİTESİ DOĞA BİLİMLERİ, MİMARLIK ve MÜHENDİSLİK FAKÜLTESİ MAKİNE MÜHENDİSLİĞİ BÖLÜMÜ TAM KLİMA TESİSATI DENEY FÖYÜ 2015-2016 Bahar Yarıyılı Prof.Dr. Yusuf Ali KARA Arş.Gör.Semih AKIN
T.C BURSA TEKNİK ÜNİVERSİTESİ DOĞA BİLİMLERİ, MİMARLIK ve MÜHENDİSLİK FAKÜLTESİ MAKİNE MÜHENDİSLİĞİ BÖLÜMÜ TAM KLİMA TESİSATI DENEY FÖYÜ 2015-2016 Bahar Yarıyılı Prof.Dr. Yusuf Ali KARA Arş.Gör.Semih AKIN
NOT: Toplam 5 soru çözünüz, sınav süresi 90 dakikadır. SORULAR VE ÇÖZÜMLER
 Adı- Soyadı: Fakülte No : Gıda Mühendisliği Bölümü, 2015/2016 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Bütünleme Sınavı Soru ve Çözümleri 20.01.2016 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
Adı- Soyadı: Fakülte No : Gıda Mühendisliği Bölümü, 2015/2016 Öğretim Yılı, Güz Yarıyılı 00391-Termodinamik Dersi, Bütünleme Sınavı Soru ve Çözümleri 20.01.2016 Soru (puan) 1 (20) 2 (20) 3 (20) 4 (20)
Binaların Isı Merkezlerinde Bulunan Kalorifer Kazanlarının Yanma Havası ve Hava Fazlalık Katsayılarına Göre Yanma Gazlarının Özelliklerindeki Değişim
 Binaların Isı Merkezlerinde Bulunan Kalorifer Kazanlarının Yanma Havası ve Hava Fazlalık Katsayılarına Göre Yanma Gazlarının Özelliklerindeki Değişim Okan KON 1*, Bedri YÜKSEL 1 1 Balıkesir Üniversitesi
Binaların Isı Merkezlerinde Bulunan Kalorifer Kazanlarının Yanma Havası ve Hava Fazlalık Katsayılarına Göre Yanma Gazlarının Özelliklerindeki Değişim Okan KON 1*, Bedri YÜKSEL 1 1 Balıkesir Üniversitesi
KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI
 KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI Fiziksel ve Kimyasal Olaylar Maddenin şekil, yoğunluk, çözünürlük, genleşme, erime ve kaynama noktaları, sıvı, katı ya da gaz hâlde olması
KONU: KÜTLENĐN KORUNUMU (8.sınıf) ÇALIŞMA YAPRAĞI KONU ANLATIMI Fiziksel ve Kimyasal Olaylar Maddenin şekil, yoğunluk, çözünürlük, genleşme, erime ve kaynama noktaları, sıvı, katı ya da gaz hâlde olması
HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT
 1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
1 HİDROJEN ÜRETİMİ BUĞRA DOĞUKAN CANPOLAT 16360018 2 HİDROJEN ÜRETİMİ HİDROJEN KAYNAĞI HİDROKARBONLARIN BUHARLA İYİLEŞTİRİMESİ KISMİ OKSİDASYON DOĞAL GAZ İÇİN TERMAL KRAKİNG KÖMÜR GAZLAŞTIRMA BİYOKÜTLE
2+ 2- Mg SO 4. (NH 4 ) 2 SO 4 (amonyum sülfat) bileşiğini katyon ve anyonlara ayıralım.
 KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
Burada a, b, c ve d katsayılar olup genelde birer tamsayıdır. Benzer şekilde 25 o C de hidrojen ve oksijen gazlarından suyun oluşumu; H 2 O (s)
 1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
1 Kimyasal Tepkimeler Kimyasal olaylar elementlerin birbirleriyle etkileşip elektron alışverişi yapmaları sonucu oluşan olaylardır. Bu olaylar neticesinde bir bileşikteki atomların sayısı, dizilişi, bağ
Çözüm: m 1 = m 2 = 1g, G = 6.66 x 10-8 cm 3 /s.g, r = 1 cm. m m 1 2 F = G r 2 1 x 1. F = 6.66 x 10-8 1 F = 6.66 x 10-8 din (= g.
 1 ÖRNEKLER (Ref. e_makaleleri) 1. Kütleleri 1g olan ve birbirlerinden 1 cm uzaklıkta bulunan iki kütle arasındaki çekim kuvveti, din cinsinden, ne kadar olur? 10-13 cm uzaklıktaki iki nötron arasındaki
1 ÖRNEKLER (Ref. e_makaleleri) 1. Kütleleri 1g olan ve birbirlerinden 1 cm uzaklıkta bulunan iki kütle arasındaki çekim kuvveti, din cinsinden, ne kadar olur? 10-13 cm uzaklıktaki iki nötron arasındaki
Malzeme Bilgisi. Madde ve Özellikleri
 Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
Malzeme Bilgisi Madde: Boşlukta yer kaplayan, kütlesi ve hacmi olan katı, sıvı veya gaz şeklinde bulunan her şeye madde denir. Ayırt edici özellikler: Bir maddenin diğer maddelerden farklılık gösterenyanları,
İÇERİK. Amaç Yanma Dizel motorlardan kaynaklanan emisyonlar Dizel motor kaynaklı emisyonların insan ve çevre sağlığına etkileri Sonuç
 SAKARYA 2011 İÇERİK Amaç Yanma Dizel motorlardan kaynaklanan emisyonlar Dizel motor kaynaklı emisyonların insan ve çevre sağlığına etkileri Sonuç Yanma prosesinin incelenmesi ve temel yanma ürünleri Sıkıştırmalı
SAKARYA 2011 İÇERİK Amaç Yanma Dizel motorlardan kaynaklanan emisyonlar Dizel motor kaynaklı emisyonların insan ve çevre sağlığına etkileri Sonuç Yanma prosesinin incelenmesi ve temel yanma ürünleri Sıkıştırmalı
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar
 10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
10. Sınıf Kimya Konuları KİMYANIN TEMEL KANUNLARI VE TEPKİME TÜRLERİ Kimyanın Temel Kanunları Kütlenin korunumu, sabit oranlar ve katlı oranlar kanunları Demir (II) sülfür bileşiğinin elde edilmesi Kimyasal
O )molekül ağırlığı 18 g/mol ve 1g suyun kapladığı hacimde
 1) Suyun ( H 2 O )molekül ağırlığı 18 g/mol ve 1g suyun kapladığı hacimde 10 6 m 3 olduğuna göre, birbirine komşu su moleküllerinin arasındaki uzaklığı Avagadro sayısını kullanarak hesap ediniz. Moleküllerin
1) Suyun ( H 2 O )molekül ağırlığı 18 g/mol ve 1g suyun kapladığı hacimde 10 6 m 3 olduğuna göre, birbirine komşu su moleküllerinin arasındaki uzaklığı Avagadro sayısını kullanarak hesap ediniz. Moleküllerin
Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ. Bölüm 8: Ekserji: İş Potansiyelinin bir Ölçüsü
 Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ 1 Amaçlar Termodinamiğin ikinci yasası ışığında, mühendislik düzeneklerinin verimlerini veya etkinliklerini incelemek. Belirli bir çevrede verilen bir halde
Bölüm 8 EKSERJİ: İŞ POTANSİYELİNİN BİR ÖLÇÜSÜ 1 Amaçlar Termodinamiğin ikinci yasası ışığında, mühendislik düzeneklerinin verimlerini veya etkinliklerini incelemek. Belirli bir çevrede verilen bir halde
ELEMETLER VE BİLEŞİKLER ELEMENTLER VE SEMBOLLERİ
 ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
ELEMENTLER VE SEMBOLLERİ Elementler Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere element denir. Elementler çok sayıda
Karbonmonoksit (CO) Oluşumu
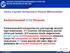 Yanma Kaynaklı Emisyonların Oluşum Mekanizmaları Karbonmonoksit (CO) Oluşumu Karbonmonoksit emisyonlarının ana kaynağı benzinli taşıt motorlarıdır. H/Y oranının CO emisyonu üzerine etkisi çok fazladır.
Yanma Kaynaklı Emisyonların Oluşum Mekanizmaları Karbonmonoksit (CO) Oluşumu Karbonmonoksit emisyonlarının ana kaynağı benzinli taşıt motorlarıdır. H/Y oranının CO emisyonu üzerine etkisi çok fazladır.
Bölüm 7 ENTROPİ. Bölüm 7: Entropi
 Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
Bölüm 7 ENTROPİ 1 Amaçlar Termodinamiğin ikinci kanununu hal değişimlerine uygulamak. İkinci yasa verimini ölçmek için entropi olarak adlandırılan özelliği tanımlamak. Entropinin artış ilkesinin ne olduğunu
hesaplama (Ders #16 dan devam) II. İstemli değişim ve serbest enerji III. Entropi IV. Oluşum serbest enerjisi
 5.111 Ders Özeti #17 Bugün için okuma: Bölüm 7.1 İstemli değişme, Bölümler 7.2 ve 7.8 -Entropi, Bölümler 7.12, 7.13, ve 7.15 Serbest Enerji. Ders #18 için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji
5.111 Ders Özeti #17 Bugün için okuma: Bölüm 7.1 İstemli değişme, Bölümler 7.2 ve 7.8 -Entropi, Bölümler 7.12, 7.13, ve 7.15 Serbest Enerji. Ders #18 için okuma: Bölüm 7.16 Biyolojik Sistemlerde Serbest-Enerji
Maddenin Fiziksel Özellikleri
 ÜNİTE 5 Maddenin Fiziksel Özellikleri Amaçlar Bu üniteyi çalıştıktan sonra, maddeyi yakından tanıyacak, maddenin hallerini bilecek, maddenin fiziksel özelliklerini öğrenecek, fiziksel değişmeleri kavrayacaksınız.
ÜNİTE 5 Maddenin Fiziksel Özellikleri Amaçlar Bu üniteyi çalıştıktan sonra, maddeyi yakından tanıyacak, maddenin hallerini bilecek, maddenin fiziksel özelliklerini öğrenecek, fiziksel değişmeleri kavrayacaksınız.
GENEL KİMYA. Yrd.Doç.Dr. Tuba YETİM
 GENEL KİMYA KİMYASAL REAKSİYONLAR Kimyasal Tepkime Kimyasal tepkime, Bir ya da birkaç maddenin (tepkenler) yeni bir bileşik grubuna (ürünler) dönüştürülmesi işlemidir. Tepkenler Ürünler NO + 1/2 O 2 NO
GENEL KİMYA KİMYASAL REAKSİYONLAR Kimyasal Tepkime Kimyasal tepkime, Bir ya da birkaç maddenin (tepkenler) yeni bir bileşik grubuna (ürünler) dönüştürülmesi işlemidir. Tepkenler Ürünler NO + 1/2 O 2 NO
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
OREN1066 TEKNİK FİZİK / TERMODİNAMİK ÖRNEK PROBLEMLER
 1 1. TERMODİNAMİK Örnek Problem 1.1: Isıl kapasite Yalıtımlı kapalı bir kapta bulunan 2.00 kg hava 10 0 C sıcaklıktan 22 0 C sıcaklığa kadar ısıtılmaktadır. Isıtmada harcanan enerji 5.76 kcal kadardır.
1 1. TERMODİNAMİK Örnek Problem 1.1: Isıl kapasite Yalıtımlı kapalı bir kapta bulunan 2.00 kg hava 10 0 C sıcaklıktan 22 0 C sıcaklığa kadar ısıtılmaktadır. Isıtmada harcanan enerji 5.76 kcal kadardır.
İKİ KADEMELİ GAZ BRÜLÖRLERİ TWO STAGE GAS BURNERS
 Lİ GAZ BRÜLÖRLERİ TWO STAGE GAS BURNERS Doğru seçimle başlamak Starting the right selection ÜRET GAZ BRÜLÖRLERİ 30 7500 kw TS EN 676 + A2 çerçevesinde CE 1312 sertifikasyonu ile üretilen üflemeli tip Üret
Lİ GAZ BRÜLÖRLERİ TWO STAGE GAS BURNERS Doğru seçimle başlamak Starting the right selection ÜRET GAZ BRÜLÖRLERİ 30 7500 kw TS EN 676 + A2 çerçevesinde CE 1312 sertifikasyonu ile üretilen üflemeli tip Üret
ÖZGEÇMİŞ. Derece Alan Üniversite Yıl. Teknik Eğitim Fakültesi, Makina Eğitimi. Fen Bilimleri Enstitüsü, Makina Eğitimi A.B.
 ÖZGEÇMİŞ ADI SOYADI ÜNAVI : VOLKAN : KIRMACI : YRD. DOÇ. DR. UZMANLIK ALANI : Isı transferi, Isıtma, Soğutma, Doğalgaz, Havalandırma ve İklimlendirme sistemleri. ÖĞRENİM DURUMU Derece Alan Üniversite Yıl
ÖZGEÇMİŞ ADI SOYADI ÜNAVI : VOLKAN : KIRMACI : YRD. DOÇ. DR. UZMANLIK ALANI : Isı transferi, Isıtma, Soğutma, Doğalgaz, Havalandırma ve İklimlendirme sistemleri. ÖĞRENİM DURUMU Derece Alan Üniversite Yıl
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM
 MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
MADDENİN YAPISI VE ÖZELLİKLERİ ATOM ATOMUN YAPISI Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atomu oluşturan parçacıklar farklı yüklere sa-hiptir. Atomda bulunan yükler; negatif
ELEMENT VE BİLEŞİKLER
 ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
ELEMENT VE BİLEŞİKLER 1- Elementler ve Elementlerin Özellikleri: a) Elementler: Aynı cins atomlardan oluşan, fiziksel ya da kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere
Gazların Özellikler Barometre Basıncı Basit Gaz Yasaları
 İÇERİK Gazların Özellikler Barometre Basıncı Basit Gaz Yasaları Boyle Yasası Charles Yasası Avogadro Yasası Gaz Davranışları ve Standart Koşullar İdeal ve Genel Gaz Denklemleri Gaz Karışımları Gaz Yasalarına
İÇERİK Gazların Özellikler Barometre Basıncı Basit Gaz Yasaları Boyle Yasası Charles Yasası Avogadro Yasası Gaz Davranışları ve Standart Koşullar İdeal ve Genel Gaz Denklemleri Gaz Karışımları Gaz Yasalarına
