ENERJİ VE CANLILAR Potansiyel enerji Kinetik enerji
|
|
|
- Selim Mencik
- 8 yıl önce
- İzleme sayısı:
Transkript
1 ENERJİ VE CANLILAR Yaşamak iş yapmaktır. Enerji de iş yapma kapasitesi olarak tanımlanır. Hücreler küçük organik moleküllerden DNA ve proteinler gibi polimerler sentezler, çevreleriyle madde alış verişi yapar, hareket eder ya da biçim değiştirir, büyür ve ürer, kısaca hücreler karmaşık içyapılarını sürdürebilmek için, iş yapmak zorundadır. Hücrelerin iş yapması, enerjiyi bir şekilden (formdan) diğerine dönüştürebilme (değiştirebilme) yeteneklerine dayanır. Hücreler enerjiyi dış kaynaklardan elde etmek zorundadır. Enerji birçok ekosisteme güneş enerjisi halinde girer. Güneş ışığı bitkiler ve diğer fotosentetik organizmalar için enerji kaynağıdır. Hayvanlar ya bitkileri ya da bitkilerle beslenen diğer hayvanları yiyerek enerji sağlar. Hücrelerin organik moleküllerde depolanmış kimyasal enerjiyi nasıl elde ettiklerini ve bu enerjiyi hücresel işlerin çoğunu yürüten ATP molekülünü üretmek için nasıl kullandıklarını, diğer bir deyişle canlı organizmalarda enerjinin dönüşümünü (enerji akışını) inceleyen çalışmalar biyoenerjetik olarak isimlendirilir. Enerji iki şekilde ortaya çıkar: Potansiyel enerji depolanmış enerjidir. Bu enerji cismin durumundan, konumundan ya da yapısı nedeniyle sahip olduğu enerjidir. Örneğin bir barajın arkasında toplanan su, yükseklik nedeniyle enerji depolar. Top yukarı atılınca en üst noktada hızı sıfır olduğu ana kadar potansiyel enerjisi çoğalır, çünkü yer ile olan yüksekliği artmıştır. Bir potansiyel enerji çeşidi olan kimyasal enerji moleküllerdeki atomların düzenlenişlerinden kaynaklanır ve moleküllerde depolanır. Kinetik enerji hareket enerjisidir. Bu enerji cisim hareket ettiği sürece vardır; cisim hızlanınca artar, yavaşlayınca azalır. Hızı sıfır olan bir cismin kinetik enerjisi de sıfırdır. Bir tepenin üzerindeki kaya parçası potansiyel enerjiye sahiptir, tepeden aşağı doğru yuvarlanmaya başladığı zaman potansiyel enerjinin bir kısmı kinetik enerjiye çevrilir. Canlı organizmaların başardıkları işin bir kısmı potansiyel enerjinin kinetik enerjiye dönüşmesini kapsamaktadır. Işık da iş yapmada kullanılabilen kinetik enerji çeşididir. Yeşil bitkilerdeki fotosentez ışık enerjisi ile başarılır. Isı yani termal enerji, moleküllerin rastgele hareketinden kaynaklanan kinetik enerjidir. Enerji mekaniksel enerji, ısı enerjisi (termal enerji), ses enerjisi, elektrik enerjisi, ışık enerjisi, nükleer enerji veya radyoaktif ışıma gibi şekillere (formlara) dönüşebilir. Böyle değişik şekillerde ortaya çıkabilmesi sebebiyle enerji değişik şekillerde ölçülebilir. Enerjinin her şekli ısıya çevrilebildiğinden ısı enerjisi en uygun enerji ölçüm şeklidir. Biyolojide kullanılan ısı birimi kilokaloridir (kcal). (Bir kcal 1000 kaloriye(cal) eşittir ve 1 kalori bir gram suyun sıcaklığını 1 C (celcius) yükseltmek için gereksinim duyulan ısıdır.) Fizikte kullanılan başka bir enerji birimi jul (joule) dür ve kaloriye eşittir. Kimyasal tepkimeler moleküllerdeki atomları moleküllerde depolanmış olan potansiyel enerjiyi kinetik enerjiye dönüştürecek şekilde yeniden düzenlediğinde, kimyasal enerji kullanışlı hale gelir. Bu tip bir dönüşüm örneğin, bir otomobil motorunda benzin içindeki hidrokarbonlar pistonları iten enerjiyi açığa çıkaracak şekilde oksijen ile tepkimeye girdiğinde gerçekleşir. Organizmalar da kimyasal enerjiyi buna benzer biçimde kullanır. Hücre solunumu ve diğer katabolik yollar, şeker ve diğer karmaşık moleküllerde depolanmış olan enerjiyi açığa çıkararak, bu enerjinin hücresel işlerde kullanılmasını sağlar. Merdivene tırmanan bir çocuk, besinlerdeki organik moleküllerde depolanmış olan enerjinin bir kısmını, tırmanma sırasındaki hareketlerin kinetik enerjisine dönüştürür. Bu yakıt moleküllerinde depolanmış olan enerji ise bitkiler tarafından başarılan fotosentez sırasında güneş enerjisinden sağlanır. (Dünyadaki yaşam güneşten gelen enerji akışına bağlıdır. Güneşin dünyamıza sağladığı enerji yılda 13x10 23 kaloriden daha fazladır. Bu enerjinin %30 kadarı uzaya yansır, %20 kadarı atmosferde absorblanır. Dünyanın yüzeyine ulaşan %50 enerjinin bir kısmı yeryüzünde absorblanır ve ısıya dönüştürülür. Çok küçük bir kısım güneş enerjisi de (yaklaşık %1 kadarı) bitkiler, algler ve fotosentetik bakteriler tarafından fotosentez olayı esnasında yakalanır. Fotosentezde güneş ışığının yakalanmasından elde edilen enerji küçük molekülleri (su ve karbondioksit) daha büyük karmaşık moleküllere (şekerler) dönüştürmek için kullanılır. Enerji şeker moleküllerindeki atomlar arasında
2 kovalent bağlarda potansiyel enerji olarak depolanır. Kovalent bağın kuvveti onu parçalamak için gereksinim duyulan enerji miktarı olarak hesap edilir. Örneğin karbon-hidrojen bağlarının bir molünü parçalamak için 98.8 kcal gerekir.) Organizmalar enerji dönüştüren varlıklardır. Evrendeki ve dolayısıyla biyolojik sistemlerdeki enerji dönüşümü termodinamiğin iki kanununa göre işler: (Termodinamik, fiziğin enerji ve enerjinin şekil değiştirmesi ile uğraşan dalıdır. Günümüzde enerji ve entropi bilimi olarak da tanımlanmaktadır.) Termodinamiğin Birinci Yasası (Entalpi) Termodinamiğin birinci yasasına göre, Evrenin enerjisi sabittir. Enerji aktarılabilir ve dönüştürülebilir, ancak yeniden yaratılamaz ya da yok edilemez. Bu yasa enerjinin sakınımı prensibi olarak da bilinir. Elektrik şirketi enerji üretmez, enerjiyi kullanışlı bir forma dönüştürür. Işığı kimyasal enerjiye dönüştüren bir yeşil bitki enerji üreticisi değil, enerji dönüştürücüsüdür. Enerji değişik formlarda depolanabilir ve daha sonra diğer formlara dönüşebilir. Örneğin bir otomobilin motorunda benzinin kimyasal bağlarında depolanmış enerji otomobilin hareket etmesini sağlayan kinetik enerjiye dönüşür. Benzer şekilde canlılar karbonhidratları parçaladıkları zaman kimyasal bağlarda depolanmış olan enerjiyi mekanik enerjiye, elektriksel impulslara, ısıya ve ışık enerjisine çevirir. Bu enerji dönüşümlerinde enerji ne yaratılmaktadır ne de yok edilmektedir. Termodinamiğin İkinci Yasası (Entropi) Enerji bir başka biçime dönüşürken yüzde yüz bir dönüşüm gerçekleşmez; ortada hiçbir zaman kullanılamayacak bir enerji biçimi, düzensizlik, entropi ortaya çıkar. Evrenin entropisi sürekli artar. Enerji dönüşümlerinin çoğunda enerjinin bir kısmı ısıya dönüşür. Bir arabanın yakıt deposunda depolanmış kimyasal enerjinin sadece %25 i arabanın hareketine dönüştürüldüğü halde, geriye kalan %75 lik kısmı motordan ısı olarak kaybolur. Bu ısı hızla çevreye yayılır. Benzer şekilde canlılar da besinlerde depolanmış enerjinin sadece belirli bir kısmını kinetik enerjiye dönüştürür, diğer kısmı ısıya dönüşür. (Kalabalık bir odanın sıcak hale gelmesinin nedeni budur.) Bir sistemin ısıyı iş yapmada kullanabilmesi, yalnızca sıcaklık farklılığı olduğu zaman mümkündür. Sıcaklık farklılığı ısının sıcak yerden soğuk yere doğru akmasıyla sonuçlanır. Canlı hücrenin içinde olduğu gibi tekdüze bir sıcaklık varsa, ısı enerjisi sadece madde kütlesini, örneğin bir organizmayı ısıtmak için kullanılabilir. Termodinamiğin birinci ve ikinci yasalarını birleştirerek şu sonuca varabiliriz: Evrendeki enerji miktarı sabittir ancak, enerjinin niteliği sabit değildir. Canlı sistemler çevrelerinin, dolayısıyla evrenin entropisini artırır (Sistem, kütle ve enerji dönüşümlerinin incelendiği bölge olarak tanımlanır. İncelenen sistemin dışında kalan ve sistemin üzerinde etkisi olan her şeye de çevre denir. Evren, sistem ve çevreden oluşur.) Hücreler daha az organize yapıdaki (daha az düzenli) başlangıç maddelerini (atom ve moleküller) kullanarak, düzenli yapılar oluşturur. Örneğin, amino asitler özgün diziler şeklinde düzenlenerek polipeptit zincirleri yapılır. Ancak bir organizma çevreden düzenli haldeki madde ve enerjiyi de alır ve bunları daha az düzenli formlara çevirir. Örneğin bir hayvan yediği besinle nişasta, protein ve diğer karmaşık molekülleri alır. Katabolik yollar bu molekülleri yıktığında, bu hayvan çevreye karbon dioksit ve su verir. Bu küçük ve basit moleküller besinin içerdiğinden daha az kimyasal enerji depolar. Kimyasal enerjinin tükenişi, metabolizma sırasında üretilen ısının sorumlusudur. Geniş ölçekte, enerji bir ekosisteme ışık formunda girer ve ekosistemden ısı şeklinde çıkar. Bu nedenle, biyolojik düzenin evrimi termodinamik yasalarıyla tam bir uyum içindedir. Serbest Enerji Organizmalar serbest enerji harcayarak yaşar. Serbest enerji anlaşılması zor bir kavramdır. Serbest enerji sıcaklığın tekdüze olduğu bir sistemde iş yapmak için var olan enerjidir. Sistemin serbest enerji miktarı G harfi ile sembolize edilir. G nin iki tane bileşeni vardır: sistemin toplam enerjisi (H ile
3 sembolize edilir) ve sistemin entropisi (S ile sembolize edilir). Serbest enerji bu etmenlerle aşağıdaki eşitlik çerçevesinde ilişkilidir: G = H TS Bu eşitlikteki T, Kelvin (K) birimi cinsinden mutlak sıcaklığı gösterir (0 C = 273 K). (Bu eşitlikte sıcaklığın entropiyi artırdığına dikkat ediniz.) Bir sistem başlangıç durumundan farklı bir duruma doğru ilerlerken, serbest enerjideki değişiklik ΔG ile gösterilir: Bunu başka bir şekilde ifade edersek: ΔG = G son durum G başlangıç durumu ΔG = ΔH TΔS Serbest enerji değişikliklerine göre kimyasal tepkimeler, ekzergonik (enerji veren) ya da endergonik (enerji alan) olarak sınıflandırılabilir. Ekzergonik tepkime için ΔG negatiftir (ΔG < O). (Kendiliğinden cereyan eden bir olay için ΔG nin eksi (ΔG < O) bir değere sahip olması gerekir, o nedenle ekzergonik tepkimeler kendiliğinden cereyan eder.) Hücre solunumunu ekzergonik tepkimeye bir örnek olarak verebiliriz: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O [ΔG = -686 kcal/mol (ya da kj/mol)] Standart koşullar altında solunumla yıkılan bir mol (l80 g) glukoz için 686 kcal (ya da 2870 kj) iş enerjisi sağlanır. Enerjinin korunması gerektiğinden, solunum ürünlerinin depoladıkları enerji, reaktantların enerjisinden 686 kcal daha azdır. Endergonik tepkime çevresinden enerji soğuran tepkimedir. Bu tip bir tepkime moleküllerde serbest enerji depoladığı için ΔG pozitiftir. Bu tip tepkimeler kendiliğinden cereyan etmez. Eğer bir kimyasal süreç bir yöne doğru ilerlerken ekzergonik ise bunun zıt yönünde ilerleyen süreç endergonik olmak zorundadır. Solunum için ΔG = -686 kcal/mol olduğuna göre, karbon dioksit ve sudan şeker üreten fotosentez için ΔG = +686 kcal/mol'dür. Bitkilerin yaprak hücrelerinde gerçekleşen şeker üretimi, ışık enerjisinin soğurulmasından güç alan endergonik bir süreçtir. (Diğer bir ifadeyle, güneş ışığı serbest enerji kaynağıdır.) Biyoenerjetiğin temel kuralı enerji eşleşmesidir: Enerji eşleşmesi ekzergonik sürecin endergonik sürecin sürdürülebilmesi için kullanılmasıdır. Hücrelerdeki enerji eşleşmesinin çoğuna aracılık eden molekül ATP dir. ATP Hücreler üç temel iş yapar: 1. Mekanik iş. Kas hücrelerinin kasılması, sil hareketi ve hücre bölünmesi sırasında kromozomların hareketi. 2. Taşıma işi. Bileşiklerin zarlardan kendiliğinden geçiş yönünün tersine yönde pompalanması. 3. Kimyasal iş. Kendiliğinden cereyan etmeyecek olan endergonik tepkimeleri (örneğin monomerlerden polimerlerin sentezi) gerçekleştirmek. Birçok durumda hücresel işlere güç sağlayan enerji kaynağı ATP dir. ATP (adenozin trifosfat) RNA da bulunan nükleotit tiplerinden birisidir. ATP, azotlu baz olan adenine bağlı bir riboz ve bu riboza bağlı üç tane fosfat grubu içerir. ATP deki fosfat grupları arasında yer alan bağlar hidroliz ile kırılabilir. En uçtaki fosfat bağı kırıldığında, bir molekül inorganik fosfat (P i ) ATP den ayrılır ve ATP adenozin difosfat (ADP) haline gelir. Bu tepkime ekzergonik olup, laboratuvar koşullarında bir mol ATP nin hidrolizi 7.3 kcal'lik enerji salar: ATP + H 2 O ADP + P i [ΔG = -7.3 kcal/mol (ya da -31 kj/mol)]
4 Bu değer standart koşullar altında ölçülen serbest enerji değişikliğidir. Ancak hücre içindeki kimyasal ve fiziksel koşullar standart koşullara uymaz. Test tüpünde değil de hücre içinde cereyan eden tepkimenin gerçek ΔG si yaklaşık olarak -13 kcal/mol olup, bu değer standart koşullardaki ATP hidrolizinin saldığı enerjiden %78 daha fazladır. Fosfat bağları çok kırılgandır. Bunun nedeni, üç fosfat grubunun da eksi yüklü olmasıdır: Aynı tipteki bu yüklerin birbirlerine yakın konumda bulundukları için birbirlerini itmesi ATP molekülünün o bölgesinde kararsızlık yaratır ve bağ hidroliz ile kolayca yıkılır. Hücreler özgül enzimlerin yardımıyla ATP hidroliz enerjisini doğrudan doğruya endergonik olaylarla eşleştirme yeteneğindedir. Özgül enzimler bir fosfat grubunu ATP den diğer moleküllere aktararak, enerji eşleşmesini sağlar. Fosfat grubunu alan molekül fosforile olur. Hemen hemen bütün hücresel işler ATP den diğer moleküllere fosfat grubu aktarımı ve bu moleküllerin enerji içeriğinin artmasına bağlıdır. Örneğin ATP kas hareketi için güç sağladığı zaman, kasılma proteinlerine fosfat grupları aktarır. ATP yenilenebilen bir kaynaktır ve ADP ye fosfat eklenmesiyle yeniden oluşturulabilir. ATP nin ADP den yeniden oluşturulması endergoniktir: ADP + P i ATP + H 2 O [ΔG = +7.3 kcal/mol (standart koşullar)] ADP nin fosforilasyonu için gereken serbest enerji hücredeki yıkım tepkimelerinden (katabolizma), özellikle de hücre solunumundan sağlanır. Bitkiler güneş enerjisini de ATP üretmek için kullanır. İnorganik fosfat ve enerjinin bu şekilde gidip gelişi ATP döngüsü olarak adlandırılır ve bu döngü hücredeki enerji gerektiren olayları, enerji üreten olaylara bağlar. ATP döngüsü büyük bir hızla çalışır. Örneğin çalışmakta olan bir kas hücresi, tüm ATP havuzunu bir dakikada yeniler. Bu dönüşüm, her hücrede, her saniye 10 milyon ATP molekülünün kullanılması ve yeniden oluşturulması anlamına gelir. Eğer ATP, ADP nin fosforilasyonu ile yenilenemiyor olsaydı, insanlar her gün hemen hemen vücut ağırlıkları kadar ATP tüketiyor olacaklardı. Oksidasyon - Redüksiyon Kimyasal tepkimelerde, kimyasal bağlarda depolanmış enerji yeni bağlara aktarılır. Bu tepkimelerin bir kısmında, elektronlar bir atom veya molekülden başkasına geçer. Bir atom veya molekül elektron kaybederse, onun oksitlendiği (yükseltgendiği) söylenir ve bu süreç oksitlenme (oksidasyon, yükseltgenme) olarak isimlendirilir. Biyolojik sistemlerde oksijen en yaygın elektron alıcısıdır. Bir atom veya molekül elektron kazandığı zaman redüklendiği (indirgendiği) söylenir ve olay redüksiyon (indirgenme) olarak adlandırılır. Oksitlenme sırasında bir atomun kaybettiği her bir elektronun redüklenme esnasından başka bir atom tarafından kazanılması sebebiyle oksitlenme ve redüklenme daima birlikte ortaya çıkar. Bu yüzden bu çeşit kimyasal tepkimeler oksitlenme-redüklenme (redoks) tepkimeleri olarak isimlendirilir. Enerji bir molekülden başka bir moleküle redoks tepkimeleri vasıtasıyla aktarılır. Bir molekülün redüklenmiş formu oksitlenmiş formundan daha yüksek enerji seviyesine sahiptir. Bir atomdan başka birine geçen elektronlar enerjilerini de taşımaları sebebiyle oksitlenme-redüklenme reaksiyonları biyolojik sistemlere enerji akışında anahtar rol oynar. Işık elektrona enerji katabilir ve o elektronu daha yüksek enerji seviyesine iter. Bu elektron bir atomdan ayrılıp başka bir atoma hareket ettiği zaman elektronun kazanmış olduğu enerji de aktarılmış olur. Kazanılmış enerji potansiyel kimyasal enerji olarak depolanır, elektron orijinal enerji seviyesine geri döndüğü zaman serbest bırakılır. Aktivasyon Enerjisi Bir kimyasal tepkimenin başlayabilmesi için başlangıçta enerji girişine ihtiyaç duyulur. Bu durum kendiliğinden meydana gelebilen ekzergonik tepkimeler için de geçerlidir. Yeni bağların kurulabilmesi için mevcut bağların kırılması gereklidir ve enerjiye gereksinim vardır. Mevcut kimyasal bağların bozulması ve kimyasal tepkimenin başlaması için gereksinim duyulan ilave enerji aktivasyon enerjisi olarak isimlendirilir.
5 Ekzergonik tepkimelerin hızı tepkimeyi başlatmak için gereksinim duyulan aktivasyon enerjisine bağlıdır. Büyük aktivasyon enerjisine sahip tepkimeler çok yavaş yürüme eğilimindedir. Çünkü az sayıda molekül başlangıç enerji eşiğini aşmayı başarabilir. Bu tepkimeyi başlatmak için gereksinim duyulan aktivasyon enerjisini kimyasal bağları etkileyerek düşüren süreç kataliz olarak adlanır, bunu yapan maddeler katalizörlerdir. Katalizörler bir reaksiyon sonunda değişmeden kalır. ENZİMLER Enzimlerin yapısını, fonksiyonlarını, kataliz mekanizmalarını ve enzimlerin katalizlediği her türlü metabolik ve biyokimyasal reaksiyonların neden ve nasıl gerçekleştiğini inceleyen bilime enzimoloji denir. İnsanlarda görülen hastalıkların tanı veya ayırıcı tanısının yapılması ve tedavisinde enzimatik ölçümlerin uygulanması ile ilgilenen bilim dalı klinik enzimoloji olarak adlandırılır. Canlıda yaşamın sürdürülmesi sırasında gerçekleşen tüm kimyasal tepkimelere metabolizma denir. Metabolizmanın moleküllerin yıkımının olduğu ekzergonik tepkimeleri katabolizma, yeni bileşiklerin yapıldığı, endergonik olan sentez tepkimeleri anabolizma olarak adlandırılır. Enzimler canlıların metabolik tepkimelerinin oluşmasında iş gören, protein yapısındaki biyolojik (doğal) katalizörlerdir. Ribozimler (RNA enzimleri) ise RNA dan yapılmış bir başka biyolojik katalizör sınıfıdır. Katalizör, kendisi harcanmaksızın tepkime hızını değiştiren bir kimyasal ajandır. Enzimlerin kimyasal katalizörlerden en önemli farkı özgül (spesifik) olmaları, yani belirli maddeler arasındaki belirli tepkimeleri katalize etmeleridir. Enzimlerin etki ettiği molekül ya da moleküllere substrat adı verilir. Enzimler substratlarına özgüldür. Enzim substratına (ya da substratlarına) bağlanır. Enzim ile substrat bağlandığında, enzimin katalitik etkisi substratı tepkimenin ürününe (ya da ürünlerine) dönüştürür. Bu olay aşağıdaki şekilde özetlenebilir. Enzim Substrat(lar) Ürün(ler) Enzimin özel adı tepkime okunun üstüne yazılır. Örneğin, sükraz enzimi (birçok enzimin adı -az soneki ile biter) disakkarit olan sükrozu, glukoz ve fruktoz monomerlerine yıkar. Sükraz Sükroz + H 2 O Glukoz + Fruktoz Bir enzim izomerler gibi birbirlerine çok benzeyen bileşikleri bile ayırt edebilir. Böylece her enzim belirli bir tepkimeyi katalizler. Örneğin, sükraz sadece sükroz üzerine etki edebilir ve maltoz gibi diğer disakkaritleri etkilemez. Bir enzimin özgüllüğü onun biçiminden (üç boyutlu konformasyonundan) kaynaklanır. Bir hücrede olağanüstü sayıda enzim vardır. Örneğin bir bakteri hücresinde 2000 civarında, bir memeli hücresinde den fazla enzim vardır. Enzimlerin Yapısı ve Fonksiyonu Enzimlerin bazıları basit proteinlerdir. Pepsin, tripsin, üreaz böyle enzimlere örnek olarak gösterilebilir. Bunların katalitik etki gösteren kısmı doğrudan doğruya proteinin polipeptit zinciridir. Birçok enzim katalitik etki gösterebilmek için protein yapısında olmayan yardımcılara gereksinim duyar. Kofaktör olarak adlandırılan bu yardımcılar ya organik ya da inorganik moleküllerdir. Çinko, demir, bakır, molibden, mangan, magnezyum, kalsiyum, klor, nikel gibi elementler inorganik yapıdaki kofaktörlerdir. Örneğin, tükürükteki amilaz nişastayı yalnız Cl iyonlarının bulunduğu ortamda parçalayabilir. Katalaz Fe, Sitokrom oksidaz Cu, DNA polimeraz Zn, Üreaz Ni e kofaktör olarak ihtiyaç duyar. Eğer kofaktör bir organik molekül olup zayıf bağlanmışsa koenzim, sıkı bağlanmışsa
6 prostetik grup olarak adlandırılır. Vitaminlerin çoğu koenzimdir ya da koenzimlerin öncü maddeleridir (ön maddeleridir, prokürsörleridir). (Bazı kaynaklarda kofaktör terimi sadece inorganik moleküller için kullanılır, ayrıca kofaktör ve koenzim prostetik grup olarak ifade edilir.) Enzimin protein kısmına apoenzim, kofaktörle birleşmiş olan apoenzim kompleksine ise holoenzim denir. Enzimin protein kısmı genelde globülerdir ve enzim çeşidine göre amino asitten oluşur. Enzim molekülleri genellikle iki yada daha fazla polipeptit zincirinden oluştukları için kuaterner (dördüncül) yapıdadır. Ribonükleaz 1, hekzokinaz 2, adenilat kinaz 3, laktat dehidrogenaz 4, glutamin sentetaz 12 ve piruvat dehidrogenaz kompleksinde 72 alt ünite (polipeptit) bulunur. Enzim molekülünün sadece belirli bir kısmı substrata bağlanır. Enzimin substrata bağlandığı yere aktif bölge adı verilir. Aktif bölge genellikle enzimin birkaç (3-4) amino asidi tarafından oluşturulur. Protein molekülündeki diğer amino asitler, aktif bölgenin konfigürasyonunu korumaya yönelik iskeleti oluşturur. Enzimin özgüllüğü aktif bölgenin biçimi ile substratın biçimi arasındaki uygunluktan ileri gelir. Tepkime için gerekli bu uygunluk anahtar-kilit durumuna benzetilir. Aktif bölge enzimin katalitik merkezidir. Aktif bölge esnektir; substrat aktif bölgeye girdiğinde, enzimin biçimi biraz değişir ve aktif bölge substratı daha rahat sarabilecek hale gelir. İndüklenmiş uyum denilen bu şekil değişikliği aktif bölgedeki kimyasal grupları, kimyasal tepkimeyi katalizleme yeteneklerini artıracak konumlara getirir. Kofaktör de aktif bölgeye bağlanır. Bir enzimatik tepkimede substrat, enzim-substrat kompleksini oluşturmak üzere, aktif bölgeye bağlanır. Birçok durumda substrat hidrojen bağları ve iyonik bağlar gibi zayıf etkileşimlerle aktif bölgede tutulur. Aktif bölgeyi oluşturan az sayıdaki amino asidin yan zincirleri (R grupları) substratın ürüne dönüşümünü katalizler ve ürün aktif bölgeden ayrılır. Enzim bir başka substrat molekülünü aktif bölgeye kabul etmek üzere serbest kalır. Bu döngü o kadar hızlı cereyan eder ki, tek bir enzim molekülü bir saniyede binlerce substrat molekülünü etkileyebilir. Örneğin, sığır karaciğerinden elde edilen ve bir molekül demir içeren katalaz enzimi, bir dakikada, 0 C de hidrojen peroksit (H 2 O 2 ) molekülünü H 2 O ve 1/2O 2 ye parçalayabilir. (Enzimin saniyede etki ettiği substrat molekülü sayısına Enzimin Etkinlik Değeri = Turnover Sayısı denir. Bu, 0 C de katalaz enzimi için dir.) (Bir molekül katalaz enziminin parçaladığı H 2 O 2 i demir atomu yalnız başına ancak 300 senede parçalayabilir, ya da mol başına kalori aktivasyon enerjisi vermek gerekir. Kolloidal platin bu aktivasyon enerjisini kal/mol a, katalaz enzimi de 5500 kal/mol a düşürür.) Bazı enzimler daha da hızlıdır. Örneğin karbonik anhidraz C enzimi dakikada 36 milyon molekülü değişikliğe uğratır. Diğer katalizörler gibi enzimler de, tepkimeden değişmeden çıkar. Dolayısıyla çok az miktardaki enzim katalitik döngülerde tekrar tekrar işlev görerek, büyük bir metabolik etki yaratır. Metabolik tepkimelerin çoğu geri dönüşümlü olduğu için, bir enzim ileri ve geri tepkimelerin her ikisini de katalizleyebilir. Hangi tepkimenin baskın olacağı reaktant ve ürünlerin bağıl derişimlerine bağlıdır. Canlı hücrelerde tepkimeler kural olarak 0-50 C; çoğunlukla da C arasında meydana gelir. Bu sıcaklık aralığında tepkimelerin oluşması enzimlerin aktivasyon enerjisini düşürmeleri ile olur. Enzimler aktivasyon enerjisini düşürmek ve tepkimeyi hızlandırmak için çeşitli mekanizmalar kullanır. İki ya da daha fazla sayıdaki reaktantı içeren tepkimelerde aktif bölge, substratlar arasında tepkime cereyan edebilmesi için, onların doğru konumlarda bir araya gelmelerini sağlayan bir kalıp görevi yapar. Aktif bölge substratları indüklenmiş uyum içinde tutarken, enzim de substrat moleküllerine baskı yaparak, tepkime sırasında kırılması gereken kritik kimyasal bağları esnetip, büker. Aktivasyon enerjisi bağların kırılma güçlüğü ile orantılı olduğundan, substratın şeklinin değişmesi, dönüşüm durumuna ulaşmak için soğurulması gereken termal enerji miktarını azaltır. Aktif bölge aynı zamanda belirli bir tepkime tipine aracı olan bir mikroçevre oluşturur. Örneğin aktif bölge asidik yan zincirlere (R grupları) sahip amino asitler içeriyorsa, bu cep düşük ph'ya sahip
7 olacaktır. Böyle durumlarda asidik bir amino asit, tepkimenin katalizindeki önemli basamaklardan birisi olan substrata H + aktarımını kolaylaştırabilir. Bir başka kataliz mekanizması, aktif bölgenin kimyasal tepkimeye doğrudan doğruya katılmasıdır. Bazı durumlarda bu süreç substrat ile enzim üzerindeki bir amino asit yan zinciri arasında kovalent bağ kurulmasını içerebilir. Tepkimenin daha sonraki basamakları yan zincirlerin başlangıçtaki durumlarına geri dönmelerini sağlar. Böylece aktif bölge reaksiyondan önceki durumunu yeniden kazanır. Protein yapıları farklı, fakat katalizledikleri kimyasal tepkime aynı olan enzimlere izoenzim veya izozim adı verilmektedir. Örneğin pirüvik asidin laktik aside dönüşümünü katalizleyen laktat dehidrogenaz (dehidrojenaz) (LDH) enziminin 5 tane izoenzimi vardır. Kreatinin kinaz, hekzokinaz, aldolaz, alkali fosfataz vb enzimlerin izoenzimleri de saptanmıştır. Koenzimler Koenzim veya koenzimlerin öncü maddesi olan birçok vitamin insanlar ve diğer hayvanlarda sentez edilemediğinden yiyeceklerle alınması gerekir. Koenzimler genellikle aktif yere veya aktif yerin oldukça yakınında enzime ya geçici olarak veya sürekli olarak bağlanır. Koenzimler, fonksiyonlarına göre genellikle üç grupta incelenebilirler: 1- Hidrojen ve elektron transfer eden koenzimler 2- Fonksiyonel grup transfer eden koenzimler 3- Liyaz, izomeraz ve ligazların koenzimleri Hidrojen ve elektron transfer eden koenzimler Enzimler tarafından katalizlenen birçok oksitlenme-redüklenme reaksiyonunda elektronlar enzimin aktif yerinden elektron alıcısı (akseptörü) olarak iş gören koenzime çiftler halinde geçer; genellikle elektron çiftleriyle hidrojen iyonları birlikte aktarılır. Daha sonra koenzim kabul ettiği elektronları başka bir reaksiyonda serbest bırakır (farklı bir enzime/koenzime elektronları transfer eder). Bu şekilde koenzimler hücrede enerji transferinde kritik rol oynar. Bu rolleri sebebiyle koenzimler genelde elektron taşıyıcıları olarak tanımlanır. Bu grubun en önemli koenzimleri NAD, NADP, FAD, FMN, Koenzim Q, Demir porfirinler, Demirkükürt proteinleri ve -Lipoik asittir. NAD: Bir hidrojen akseptörü olan NAD (Nikotinamit Adenin Dinükleotit) molekülü bir birine bağlı iki nükleotitten oluşur: Nikotinamit monofosfat (NMP) ve adenin monofosfat (AMP) dan oluşan iki nükleotit fosfat gruplarıyla birleşmiştir. NAD molekülündeki iki nükleotit farklı işlevleri yerine getirir: AMP birçok enzim tarafından tanınan şekli sağlayan çekirdek olarak görev yapar. NMP elektronları kabul ederek redüklenme işini başarır. NAD bütün canlı hücrelerde triptofan (bitkilerde ve bazı bakterilerde aspartik asit), niasin (nikotinik asit, vitamin B3) ve ATP kullanılarak sil baştan sentezlenebilmektedir (de novo sentez). Normal ph seviyelerinde hücrede NAD oksitlenmiş olarak bulunur ve pozitif yük taşır, bu nedenle NAD + şeklinde gösterilir. Redüklenmiş şekli ise NADH diye gösterilir. NAD + reaksiyona giren moleküllerden 2 hidrojen atomu, dolayısıyla da iki elektron almış olur. Bu atomlardan birini tümden, elektronuyla birlikte bünyesine bağlar. Diğer hidrojen atomunu ise elektron (hidrit iyon: H ) ve proton (H + ) şeklinde ayırır ki o elektronu da kendi bünyesine bağlar; proton ise ortama serbest bırakılır. Sağlıklı bir memeli hücresinde NAD + /NADH oranı 700 civarındadır. NAD + sitoplazmada ve mitokondride benzer yoğunluklarda bulunur; mitokondri zarında bulunan taşıyıcı proteinler bu molekülü içeri alır, ancak içeride koenzim olarak iş gören formları dışarı çıkarılmaz.
8 NADP: Hücrelerde NAD ye ATP den alınan bir fosfat grubu eklenerek NADP (nikotinamit adenin dinükleotit fosfat) elde edilir. (Bazı bakteriler aynı işlem için doğrudan inorganik fosfattan da yararlanabilir.) Oksitlenmiş şekli NADP +, redüklenmiş hali ise NADPH olarak gösterilir. NADP, NAD ile benzer şekilde çalışır, ancak görev aldığı olaylar sınırlıdır: Yağ asitlerinin, kolesterolün ve nükleik asitlerin sentezinde, fotosentezde indirgeyici molekül rolünü üstlenir. Reaktif oksijen radikallerinin indirgenmesinde (dolayısıyla da zararsız hale getirilmesinde), aromatik bileşiklerin, steroitlerin, alkollerin, bazı ilaçların sitokrom oksidaz aracılığıyla indirgenmelerinde rol alır. FAD: Yapısal olarak NAD ye çok benzer; ancak, NAD deki nikotinamit yerine, FAD (flavin adenin dinükleotit) de flavin grubu bulunur. Hücreler riboflavin (B 2 ) ve ATP yi kullanarak, aynen NAD ye benzer şekilde FAD sentezi yapar. Oksitlenmiş hali FAD +, redüklenmiş hali ise FADH 2 olarak gösterilir. İşlev bakımından NAD ye benzer; ancak, görev alanı daha kısıtlıdır. NAD gibi enerji metabolizmasında büyük önemi vardır. NAD, NADP ve FAD mobil elektron taşıyıcılarıdır. Sabit elektron taşıyıcıları mitokondri ve kloroplastlarda zarlarda stratejik lokalizasyonlarda bulunur. Mitokondrilerin iç zarlarında ve kloroplastların tilakoit zarlarında lokalize olmuşlardır. Fonksiyonel grup transfer eden koenzimler Bu grupta, Piridoksal-5-fosfat (PLP) Tiamin pirofosfat (TPP) Koenzim A (CoA) Biotin (vitamin H) Tetrahidrofolat (H 4 folat) Koenzim B 12 (5 ' -deoksiadenozil kobalamin) bulunur. Koenzim A (CoA): Nükleotit yapısında, ısıya dayanıklı bir moleküldür. Hücrede, pantotenik asit (vitamin B5), sistein, adenin, riboz, fosfat ve ATP kullanılarak sentezlenir. Hücrede açil (CoA-O=R) ve asetil (CoA-COCH3) grupların taşıyıcısı olarak çalışır. Asetil grubu (asetik asit) bağlamış forma asetil CoA adı verilir. Asetil CoA hayvanlarda karbonhidrat ve yağ metabolizmasında, yağ asitlerinin hem sentezinde hem de onlardan enerji elde etmede, sinir hücrelerindeki iletimde görevli nörotransmitter olan asetilkolinin sentezinde, vücuda alınan sülfonamidlerin (bir antibiyotik çeşidi) asetillenerek zararsız hale getirilmesinde görev alır. Birçok enzimin yapımında substrat olarak kullanılır. İki asetil CoA birleştirilerek asetoasetil CoA ya dönüştürülür, o da kolesterol ve keton cisimlerinin sentezinde görev yapmaktadır. Histon proteinlerinin çalışmasında büyük önem taşıyan asetilasyonda (asetillenme) görev alır. Liyaz, izomeraz ve ligazların koenzimleri Hidrojen ve elektron transfer eden koenzimler ile fonksiyonel grup transfer eden koenzimlerin bazıları liyaz, izomeraz ve ligazların koenzimleri olarak da görev görür. Bazı hallerde ara ürün, koenzim olarak işlev yapar. Multi Enzim Kompleksleri Hücrede genelde tepkimelerin farklı kademelerini katalizleyen enzimler birbirlerine bağlı (kovalent bağlı değil) birlikler oluşturur; böyle birbirine bağlı ve sıralı şekilde birbiri ardı sıra faaliyet gösteren enzim toplulukları multi enzim kompleksleri olarak isimlendirilir. Multi enzim kompleksleri önemli avantajlar sağlar: 1) Tepkimenin hızı enzimin substratla karşılaşma olasılığı ile sınırlanmaz. Bir tepkimenin ürünü serbest bırakılmaksızın bir sonraki enzime teslim edilir. Böylece multi enzim kompleksi difüzyon süresini ortadan kaldırarak tepkimelerin serbest enzimlere göre 10 kat daha hızlı gerçekleşmesini sağlar.
9 2) Tepkime serilerinden geçişler esnasında substrat multi enzim kompleksinden hiç ayrılmadığından istenmeyen tepkime olasılığı ortadan kalkar. 3) Multi enzim kompleksinde meydana gelen tepkimelerin hepsi bir birim olarak kontrol edilebilir. Piruvat ve koenzim A (CoA) nın asetil koenzim A ya dönüşünü katalizleyerek Krebs çemberine girişi kontrol eden piruvat dehidrogenaz bir multi enzim kompleksidir. Bu kompleks üç ayrı enzimin birçok kopyasından oluşur (20-30 kopya piruvat dehidrogenaz, 60 kopya dihidrolipoil transasetilaz ve 6 kopya dihidrolipoil dehidrogenaz) ve 5 farklı koenzimi (CoA, NAD +, FAD +, lipoik asit ve tiamin pirofosfat) vardır. En iyi araştırılmış enzim sistemlerinden birisi de iki karbonlu öncül maddelerden yağ asitlerinin sentezini katalizleyen yağ asidi sentaz kompleksidir. Bu multi enzim kompleksinde yedi farklı enzim bulunur. Elektron taşıma zinciri de 4 multi enzim kompleksi içerir. Mitokondri iç zarına yerleşmiş olan bu multi enzim kompleksleri zarda lateral olarak serbestçe hareket eder. Enzim Aktivitesini Etkileyen Etkenler Sıcaklık, ph, tuz derişimi ve özgül (spesifik) düzenleyici (regülatör) moleküllerin bağlanması gibi enzimlerin üç boyutlu şeklini değiştiren herhangi fiziksel veya kimyasal etken enzimin bir tepkimeyi katalizleme yeteneğini etkileyebilir. 1) Sıcaklık Katalizlenmeyen bir tepkimede sıcaklığın yükselmesi rastgele molekül hareketini arttıracağından tepkimenin hızı yükselir. Enzimler tarafından katalizlenen bir tepkimenin hızı optimum sıcaklık olarak tanımlanan bir sıcaklığa kadar artar. Optimum sıcaklığın altındaki sıcaklıklarda, enzimlerin şeklini etkileyen hidrojen bağları ve hidrofobik etkileşimler enzimin esnekliğini azaltır, bu nedenle substratın bağlanması güçleşir. Optimum sıcaklıktan daha yüksek sıcaklıklarda enzimin şeklini sürdürmesini sağlayan kuvvetler aşırı şekilde zayıflar ve enzim aktivitesini azaltır. Çok yüksek sıcaklıklarda enzimler denatüre olarak aktivitelerini kaybeder. İnsan enzimlerinin çoğu 35 C ve 40 C arasında optimum sıcaklıklara sahiptir. Çok sıcak su kaynaklarında yaşayan bakteriler çok kararlı (stabil) enzimlere sahiptir. Böyle enzimlerin optimum sıcaklıkları 70 C veya daha yüksek olabilir. Örneğin, termofilik bir bakteri olan ve kaplıca veya jeotermal bölgelerde yaşayan Thermus aquaticus tan elde edilen DNA polimeraz enzimi yüksek sıcaklıklarda (94 C) çalışabilir. 2) ph Glutamik asit ve lisin gibi karşıt yüklere sahip aminoasit bakiyeleri arasındaki iyonik etkileşimler enzimleri bir arada tutar. Böyle etkileşimler enzimin çözündüğü sıvının hidrojen iyonu konsantrasyonuna (ph) duyarlıdır. Bu yüzden birçok enzim genellikle 6-8 arasında değişen optimum ph lere sahiptir. Çok asit ortamlarda fonksiyonunu sürdüren enzimler üç boyutlu şeklini sürdürebilen proteinlerdir. Pepsin enzimi ph si 2 olan midede proteinleri sindirebilir. Optimum ph değerinden saptıkça, protein yapı denatüre olacağından enzimin katalizlediği tepkime yavaşlar ve zamanla da durur. 3) Aktivatörler ve İnhibitörler Enzim aktivitesi enzime bağlanan ve onun şeklinin değişmesine sebep olan maddelerin varlığına duyarlıdır. Bu maddeler vasıtasıyla bir hücre belirli zamanlarda enzimi aktifleştirerek ve inaktif hale getirerek enzim aktivitesini düzenleyebilir. Bir enzime bağlanarak aktivitesini azaltan bir madde inhibitör olarak isimlendirilir. Genellikle, biyokimyasal sürecin (yolak) son ürünü sürecin daha önce gelen bir reaksiyonunun inhibitörü olarak etki eder; bu durum feedback inhibisyon diye isimlendirilir. Enzim inhibisyonu kompetitif (yarışmalı, rekabet eden) inhibisyon ve kompetitif olmayan (yarışmasız, rekabet etmeyen) inhibisyon olmak üzere iki önemli yolla ortaya çıkar. Kompetitif inhibisyonda, inhibitör madde enzimin substratına çok benzerdir ve enzimin aktif yerine bağlanarak enzimi bloke
10 eder; enzime bağlı kaldığı sürece reaksiyonunun hızını azaltır. Kompetitif olmayan inhibisyonda ise inhibitör enzimin aktif yerinden başka bir yerine bağlanır. Böyle bir bağlanma enzimin şeklini değiştirir ve substratını bağlayamaz duruma gelir. Pek çok kompetitif olmayan inhibitör allosterik yer diye isimlendirilen enzimin özel bir kısmına bağlanır. Bu yerler kimyasal açma-kapama düğmeleri gibi iş görür. Allosterik yere bir maddenin bağlanması enzimin aktif ve inaktif konfigürasyonları arasında enzimi değiştirebilir. Allosterik yere bağlanan bir madde enzim aktivitesini azaltıyorsa allosterik inhibitör olarak isimlendirilir. Bunun alternatifi olarak, allosterik yere bağlanan bir madde enzimi aktif konfigürasyonunda muhafaza ediyorsa, bu yüzden enzimin aktivitesi artıyorsa böyle maddelere de allosterik aktivatör adı verilir. Mg, Cl, Na, Fe aktivatör, Pb, Cu, Sn, CO, CN ve zehirler inhibitör olarak görev yapar. 4) Tuz Konsantrasyonu Proteinin denatürasyonuna neden olabilecek tuz konsantrasyonları enzimlerin çalışmasını engeller. 5) Yüzey Alanı Substratın yüzey alanı ne kadar büyük olursa veya substratla buluşma alanı ne kadar fazla ise enzimatik tepkimeler de o kadar hızlı olur. 6) Su Enzimler ortamdaki su oranı %15'in altına düştüğünde çalışmaz. İşte, kuru yiyeceklerin bozulmadan kalması da, bu besinlerde üreyebilen mikrorganizmaların enzim etkinliklerinin durmasından kaynaklanmaktadır. 7) Enzim Konsantrasyonu Enzimatik tepkimenin hızı enzim konsantrasyonuna bağlı olarak doğrusal olarak artar. Ortamda ne kadar çok enzim molekülü varsa ve çalışıyorsa, yeterli substrat olduğu sürece tepkime de hızla sürer. Ancak, in vivo koşullarda enzimin lokalize olduğu yerde her zaman yeterince substrat bulunmadığından dolayı enzim miktarının yüksek konsantrasyonlarda bulunmasına rağmen tepkime hızı yukarıda anlatıldığı şekilde olmaz. 8) Substrat Konsantrasyonu Substrat konsantrasyonu artıkça tepkime de hızla artar, ancak bir süre sonra enzim substrat doygunluğuna ulaşınca tepkimenin hızı aynı kalır. Substrat konsantrasyonu açısından önemli bir durum da, aşırı miktarda ortamda var olan substratın enzimi inhibe etmesidir. Ortamda çok fazla miktarlarda substrat bulunması, substrat moleküllerinin enzime bağlanmasını zorlaştırır. Buna aşırı substrat inhibisyonu denir. Enzimlerin Adlandırılması Enzimlerin adlandırılması genel olarak katalize ettikleri reaksiyonun niteliğine göre yapılır. Örneğin fosfor ekleyen enzime fosforilaz, dekarboksilasyon reaksiyonu (substrattan CO2 ayırma) katalize eden enzime dekarboksilaz denir. DNA polimeraz, laktat dehidrojenaz ve adenilat siklaz, tepkimeyi tanımlayan adlandırmalardır. Çoğu zamansa enzimler etki ettikleri maddenin sonuna "az" eki getirilerek isimlendirilir; örneğin, kitine etki eden kitinaz, pektine etki eden pektinaz, laktoza etki eden laktaz, lipitlere etki eden lipaz, üreye etki eden üreaz, nişastaya etki eden amilaz gibi. Enzimler etkili olduğu substratın veya katalize ettikleri reaksiyonun sonuna "litik" eki getirilmek yoluyla da isimlendirilirler. Örneğin proteinleri parçalayan enzimlere "proteazlar" denildiği gibi "proteolitik enzimler" de denilir. Lipitleri veya lipoitleri parçalayan enzimler "lipolitik enzimler" diye adlandırılırlar. Hidroliz tepkimesiyle polimerleri monomerlerine parçalayan enzimlere "hidrolitik enzimler" denir. Bu çeşit adlandırma daha çok geniş enzim sınıfları için kullanılır.
11 Enzimlerin Sınıflandırılması Uluslararası enzim komisyonu enzimleri, katalizledikleri tepkime tiplerine ve tepkimelerin mekanizmalarına göre 6 ana grup halinde sınıflandırmıştır: 1- Oksidoredüktazlar: Redoks tepkimelerini katalizler. Genelde koenzim kullanır. a) Dehidrogenazlar: Elektron kazandırıcı tepkimeleri etkiler. b) Oksidazlar: Elektron kaybeden tepkimeleri etkiler. c) Redüktazlar: Substratı bir redüktör aracılığıyla indirgeyen enzimlere denir. Örneğin asetaldehit redüktaz, asetaldehiti alkole redükler. d) Transhidrogenazlar: Bir molekülden diğerine hidrojen taşıyarak onu redükler. e) Hidroksilazlar: Substratlarına bir hidroksil ya da su molekülü katan enzimlere denir. Örneğin fenilalanin hidroksilaz bir hidroksil grubunu fenilalanine ekleyerek onu tirozine dönüştürür. 2- Transferazlar: Hidrojenin dışında bir atomun veya atom grubunun (metil, karboksil, glikozil, amino, fosfat grupları) bir molekülden diğerine aktarılmasını sağlar. Örneğin, dekarboksilazlar karboksilik asitlerden CO2 çıkmasını sağlar. Aspartat transaminaz, alanin transaminaz, heksokinaz, kreatin kinaz transfera grubu enzimleridir. Transferazlar da oksidoredüktazlar gibi koenzime gereksinim duyar. 3- Hidrolazlar: Bir molekül su sokmak suretiyle ya da su molekülü aracılığıyla moleküllerin yıkılmasını sağlayan enzimlerdir. Ester, peptit, asit anhidrit ve glikozit bağlarına etki eder. a) Esterazlar: Ester bağını yıkan enzimlerdir (lipaz, ribonükleaz, fosfataz, pirofosfataz, glikozidaz, kolesterol esteraz). b) Proteazlar (Proteinazlar): Peptit bağını yıkan ezimlerdir. Örnek: Tripsin. 4- Liyazlar (Sentazlar): Çeşitli gruplar arasındaki bağları su molekülü çıkarmadan yıkar ve bu atomlar arasına çift bağ koyar. Pirüvat dekarboksilaz, sitrat sentaz, adenilat siklaz gibi. 5- İzomerazlar: Bir molekül içindeki geometrik ve yapısal değişiklikleri katalizler. Örnek: Triozfosfat izomeraz, Glukoz-6-fosfat izomeraz. 6- Ligazlar (Sentetazlar): Enerji kullanarak çeşitli gruplar arasında bağ oluşmasını sağlayan enzimlerdir. Örnek: DNA ligaz. Enzim Hastalık İlişkisi Enzim etkinliği organizma için zorunlu olduğundan, kritik bir enzimdeki herhangi bir bozukluk (yanlış üretim, aşırı üretim, az üretim veya yokluk) hastalığa yol açabilir. Bu durum genellikle genetik bir kusur ile ilişkilidir. Genellikle genetik bir kusurdan dolayı laktaz enziminin yeterince salınamaması nedeniyle süt şekerinin (laktoz) yeterli sindirilememesi ile ilişkili olan laktoz intoleransı (Laktoz intoleransı olan kişilerde süt alımından yarım saat ile 2 saat arası bir süre sonra mide bulantısı, kramplar, dolgunluk, şişkinlik, gaz, ishal görülebilir.), fenilketonüri (Fenilalanin'in tirozine dönüşümünü gerçekleştiren fenilalanin hidroksilaz enziminin genetik bir kusur sonucunda doğru bir şekilde üretilememesi ve dolayısıyla da kanda fenilalanin ve bazı metabolitlerin birikimi sonucu küçük çocuklarda zeka geriliği ve gelişme noksanlığı görülmesi) ve albinizm (Tirozin metabolizmasıyla ilgili bazı enzimlerdeki kalıtsal kusurlar sonucu deri ve kıllara rengini veren melanin pigmentinin üretilememesi) enzim kusurlarıyla ilişkili hastalıklardan sadece birkaçıdır. Kalp ve akciğer hastalıkları, karaciğer hastalıkları, kas hastalıkları, kemik hastalıkları, pankreas hastalıkları, kanser, genetik hastalıklar, hematolojik hastalıklar ve zehirlenmelerde hücre zarı hasarı, hücre ölümü, enzim üretiminde artış gibi nedenlerle hücresel enzimler hücre dışına çıkar. Bu enzimlerin ölçümü hastalığın tanısına yardımcı olur.
12 Enzimlerin Endüstride Kullanımı Endüstride kullanılan kimi enzimler doğadaki canlılardan (Genetiği değiştirilmiş bakteri ve mantarlar) elde edilirken kimileri sentetik olarak da üretilir. - Antibiyotiklerin sentezinde enzimlerden yararlanılır. - Deterjanlarda bulunan enzimler lekelerdeki protein ve yağları parçalar. (Deterjan enzimleri, 624 milyon-1.6 milyar dolar olarak tahmin edilen toplam biyokatalizör pazarının neredeyse yarısını oluşturuyor.) - Ekmek endüstrisinde, nişastayı şekere parçalayan, fungal alfa amilaz kullanılır. Bu enzimler normalde 50 o C de etkisizleşir ve pişirme sırasında imha olur. - Bebek gıdalarının önceden sindirimini sağlamak amacıyla tripsin kullanılır. - Bira üretiminde arpanın ezilmesiyle ortaya çıkan enzimler nişasta ve proteinleri parçalar ve ortaya basit şekerler, amino asitler ve peptitler çıkar; bunlar da fermantasyonda kullanılır. - Genç geviş getiren hayvanların bezli midesinden (şirden) elde edilen rennin (kimozin), peynir üretiminde, proteinin hidrolizini sağlar. - Lipazlar, mavi küflü rokfor peynirinin üretiminde, peynirin olgunlaşması için kullanılır. - Laktazlar, laktozun glikoz ve galaktoza parçalanmasını sağlarlar. Laktoz intoleranslı kişilerin süt ürünlerinden yararlanmasını sağlar. - DNA'nın manipülasyonu amacıyla gen mühendisliğinde, farmakolojide, tarımda ve tıpta restriksiyon enzimleri, DNA ligaz ve polimerazlar kullanılır. - Nişastanın glikoz ya da fruktoz gibi basit şekerlere dönüştürülmesi için de biyoteknoloji ürünü enzimler kullanılır. Mısır gibi tahıllar bu yöntemle kolayca tatlandırıcıya dönüştürülür. - Tekstil sektöründe özellikle iplik ve kumaş işleme süreçlerinde enzimler kullanılır. Dokuma sırasında kumaş kaplamada kullanılan koruyucu nişasta, amilaz ile sökülür. - Deriyi tüylerden arındırmak için tripsin kullanılır. - Atık kağıt, mantardan ayrıştırılan enzimlerce parçalanıp geri dönüşüme kazandırılır. Kâğıt liflerinin dayanıklılığın artırılması için de enzimler kullanılır. - Tavuklarda sindirim kanalının kısa olması nedeniyle yemlerine katılan proteaz ve amilaz yemden yararlanmayı artırır.
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
Hücre Solunumu: Kimyasal Enerji Eldesi
 Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir.
 Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir. Yaşamın temelini oluşturan kimyasal tepkimelerin tümü Metabolizma olarak adlandırılmaktadır. Bitki hücrelerinde
Hücreler, kimyasal yasaların geçerli olduğu kimyasal fabrikalar olarak da kabul edilmektedir. Yaşamın temelini oluşturan kimyasal tepkimelerin tümü Metabolizma olarak adlandırılmaktadır. Bitki hücrelerinde
Enzimler. Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO
 Enzimler Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO Enzimler Biyokimyasal olayların vücutta yaşam ile uyumlu bir şekilde gerçekleşmesini sağlayan katalizörlerdir. Katalitik RNA moleküllerinin
Enzimler Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO Enzimler Biyokimyasal olayların vücutta yaşam ile uyumlu bir şekilde gerçekleşmesini sağlayan katalizörlerdir. Katalitik RNA moleküllerinin
Prof.Dr.Gül ÖZYILMAZ
 Prof.Dr.Gül ÖZYILMAZ ENZİMLER; Tüm canlıların yapısında bulunan, Esas olarak proteinden oluşmakla beraber, organik-inorganik maddeleri de bünyesinde barındıran, Biyokimyasal tepkimeleri gerçekleştiren
Prof.Dr.Gül ÖZYILMAZ ENZİMLER; Tüm canlıların yapısında bulunan, Esas olarak proteinden oluşmakla beraber, organik-inorganik maddeleri de bünyesinde barındıran, Biyokimyasal tepkimeleri gerçekleştiren
Enzimler ENZİMLER ENZİMLER ENZİMLER İSİMLENDİRME ENZİMLER
 Enzimler Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Vücuttaki tüm reaksiyonlar, tüm işlem sonunda kendileri değişmeden reaksiyonların hızını artıran protein katalizörler olan enzimler
Enzimler Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Vücuttaki tüm reaksiyonlar, tüm işlem sonunda kendileri değişmeden reaksiyonların hızını artıran protein katalizörler olan enzimler
6. BÖLÜM MİKROBİYAL METABOLİZMA
 6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
2. Kanun- Enerji dönüşümü sırasında bir miktar kullanılabilir kullanılamayan enerji ısı olarak kaybolur.
 Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
Enerji Dönüşümleri Enerji Enerji; bir maddeyi taşıma veya değiştirme kapasitesi anlamına gelir. Enerji : Enerji bir formdan diğerine dönüştürülebilir. Kimyasal enerji ;moleküllerinin kimyasal bağlarının
Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol)
 hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
ayxmaz/biyoloji Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H
 Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Metabolizma. Metabolizmaya giriş. Metabolizmaya giriş. Metabolizmayı tanımlayacak olursak
 Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Organik Bileşikler. Karbonhidratlar. Organik Bileşikler YGS Biyoloji 1
 Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
OKSİJENLİ SOLUNUM
 1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
Metabolizma. Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir.
 METABOLİZMAYA GİRİŞ Metabolizma Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir. Metabolizma, hücrede cereyan eden binlerce kimyasal tepkimenin karmaşık bir yol haritasıdır. 2 Metabolizma
METABOLİZMAYA GİRİŞ Metabolizma Organizmadaki kimyasal tepkimelerin tümüne metabolizma adı verilir. Metabolizma, hücrede cereyan eden binlerce kimyasal tepkimenin karmaşık bir yol haritasıdır. 2 Metabolizma
Enzimlerin Yapısı. Enzimler biyokatalizörlerdir,
 Enzimler biyokatalizörlerdir,, Prof. Dr. Muhsin KONUK H 2 O 2 H 2 O + ½ O 2 A.E = 18.16 kkal/mol Kollaidal platin A.E= 11.71 kkal/mol Katalaz A.E = 1.91 kkal/mol Enzimlerin Yapısı Basit enzimler: Pepsin,
Enzimler biyokatalizörlerdir,, Prof. Dr. Muhsin KONUK H 2 O 2 H 2 O + ½ O 2 A.E = 18.16 kkal/mol Kollaidal platin A.E= 11.71 kkal/mol Katalaz A.E = 1.91 kkal/mol Enzimlerin Yapısı Basit enzimler: Pepsin,
Aktivasyon enerjisi. Enzim kullanılmayan. enerjisi. Girenlerin toplam. enerjisi. Enzim kullanılan. Serbest kalan enerji. tepkimenin aktivasyon
 ENZİMLER Enzimler Canlı sistemlerde meydana gelen tüm yapım ve yıkım reaksiyonlarına metabolizma denir Metabolizma faaliyetleri birer biyokimyasal tepkimedir. Ve bu tepkimelerin başlayabilmesi belirli
ENZİMLER Enzimler Canlı sistemlerde meydana gelen tüm yapım ve yıkım reaksiyonlarına metabolizma denir Metabolizma faaliyetleri birer biyokimyasal tepkimedir. Ve bu tepkimelerin başlayabilmesi belirli
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ
 HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
YAZILIYA HAZIRLIK SORULARI. 9. Sınıf
 YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
YAZILIYA HAZIRLIK SORULARI 9. Sınıf DOĞRU YANLIŞ SORULARI Nitel gözlemlerin güvenilirliği nicel gözlemlerden fazladır. Ökaryot hücrelerde kalıtım materyali çekirdek içinde bulunur. Ototrof beslenen canlılar
III-Hayatın Oluşturan Kimyasal Birimler
 III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
Canlının yapısında bulunan organik molekül grupları; o Karbonhidratlar o Yağlar o Proteinler o Enzimler o Vitaminler o Nükleik asitler ve o ATP
 Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı
 Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı Canlılarda Enerji Dönüşümleri Canlılarda Solunum: Enerjinin Açığa Çıkışı Canlı hücrede gerçekleşen tüm metabolik olaylar enerji gerektirir. Hayvanlar
Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı Canlılarda Enerji Dönüşümleri Canlılarda Solunum: Enerjinin Açığa Çıkışı Canlı hücrede gerçekleşen tüm metabolik olaylar enerji gerektirir. Hayvanlar
Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler
 Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler proteindir. Katalitik aktiviteleri doğal protein konformasyonunun
Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler proteindir. Katalitik aktiviteleri doğal protein konformasyonunun
Solunumda organik bileşikler karbondioksite yükseltgenir ve absorbe edilen oksijen ise suya indirgenir.
 Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Doğadaki Enerji Akışı
 Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
Doğadaki Enerji Akışı Güneş enerjisi Kimyasal enerjisi ATP Fotosentez olayı ile enerjisi Hareket enerjisi Isı enerjisi ATP Enerjinin Temel Molekülü ATP + H 2 O ADP + H 2 O ADP + Pi + 7300 kalori AMP +
BİY 315 BİYOKİMYA GİRİŞ. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
BİY 315 BİYOKİMYA GİRİŞ Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi 1 Anlatım Planı 1. Makromoleküller ve Su 2. Amino asitler ve Peptidler 3. Proteinler 4. Enzimler 5. Karbohidratlar 6. Nükleik
ENZİMLERİN GENEL ÖZELLİKLERİ - II. Doç Dr. Nurzen SEZGİN
 ENZİMLERİN GENEL ÖZELLİKLERİ - II Doç Dr. Nurzen SEZGİN bstrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate
ENZİMLERİN GENEL ÖZELLİKLERİ - II Doç Dr. Nurzen SEZGİN bstrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate
İal-biyoloji METABOLİZMA/SOLUNUM. 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir?
 METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
YAZILIYA HAZIRLIK SORULARI. 9. Sınıf 2 KARBONHİDRAT LİPİT (YAĞ)
 YAZILIYA HAZIRLIK SORULARI 9. Sınıf 2 KARBONHİDRAT LİPİT (YAĞ) DOĞRU YANLIŞ SORULARI Depo yağlar iç organları basınç ve darbelerden korur. Steroitler hücre zarının yapısına katılır ve geçirgenliğini artırır.
YAZILIYA HAZIRLIK SORULARI 9. Sınıf 2 KARBONHİDRAT LİPİT (YAĞ) DOĞRU YANLIŞ SORULARI Depo yağlar iç organları basınç ve darbelerden korur. Steroitler hücre zarının yapısına katılır ve geçirgenliğini artırır.
Prof. Dr. Şule PEKYARDIMCI
 13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
Enerji, Enzimler ve Metabolizma
 8 Enerji, Enzimler ve Metabolizma 8 Başlıklar 8.1 Biyolojik enerji dönüşümlerinde fizik yasaları 8.2 Biyokimyasal enerjide ATP 8.3 Enzimler 8.4 Enzimler nasıl çalışır? 8.5 Enzim aktivitelerinin kontrolü
8 Enerji, Enzimler ve Metabolizma 8 Başlıklar 8.1 Biyolojik enerji dönüşümlerinde fizik yasaları 8.2 Biyokimyasal enerjide ATP 8.3 Enzimler 8.4 Enzimler nasıl çalışır? 8.5 Enzim aktivitelerinin kontrolü
BİYOİNORGANİK KİMYA 5. HAFTA
 BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
YAZILIYA HAZIRLIK TEST SORULARI. 11. Sınıf
 YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
YAZILIYA HAZIRLIK TEST SORULARI 11. Sınıf 1) Oksijenli solunumda, oksijen molekülleri, I. Oksidatif fosforilasyon II. Glikoliz II. Krebs Evrelerinden hangilerinde kullanılır? A) Yalnız I B) Yalnız II C)
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon
 Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
11. SINIF KONU ANLATIMI 2 ATP-2
 11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
11. SINIF KONU ANLATIMI 2 ATP-2 Fotosentez ve kemosentez reaksiyonları hem endergonik hem ekzergonik reaksiyonlardır. ATP molekülü ile hücrenin endergonik ve ekzergonik reaksiyonları arasında enerji transferini
Solunum. Solunum ve odunsu bitkilerin büyümesi arasında yüksek bir korelasyon bulunmaktadır (Kozlowski ve Pallardy, 1997).
 SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
SOLUNUM Solunum Solunum, canlı hücrelerdeki organik maddelerin oksidasyonuyla, enerjinin açığa çıkarılması olayı olarak tanımlanır. Açığa çıkan enerji, kimyasal enerji (ATP) olarak depolanır. Solunum ürünleri,
21.11.2008. I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI.
 Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
-- Giriş -- Enzimler ve katalizörler -- Enzimlerin isimlendirilmesi -- Enzimlerin etki mekanizması -- Enzimlerin yapısı -- Enzimler ve prostetik
 -- Giriş -- Enzimler ve katalizörler -- Enzimlerin isimlendirilmesi -- Enzimlerin etki mekanizması -- Enzimlerin yapısı -- Enzimler ve prostetik gruplar -- Enzimlerin sınıflandırılması -- Önemli koenzim
-- Giriş -- Enzimler ve katalizörler -- Enzimlerin isimlendirilmesi -- Enzimlerin etki mekanizması -- Enzimlerin yapısı -- Enzimler ve prostetik gruplar -- Enzimlerin sınıflandırılması -- Önemli koenzim
12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU
 12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU HÜCRESEL SOLUNUM HÜCRESEL SOLUNUM Besinlerin hücre içerisinde parçalanması ile ATP üretimini sağlayan mekanizmaya HÜCRESEL SOLUNUM denir. Canlılar
12 HÜCRESEL SOLUNUM GLİKOLİZ VE ETİL ALKOL FERMANTASYONU HÜCRESEL SOLUNUM HÜCRESEL SOLUNUM Besinlerin hücre içerisinde parçalanması ile ATP üretimini sağlayan mekanizmaya HÜCRESEL SOLUNUM denir. Canlılar
Bitki Fizyolojisi. 6. Hafta
 Bitki Fizyolojisi 6. Hafta 1 Fotosentezin karanlık tepkimelerinde karbondioksit özümlemesi; 1. C 3 bitkilerinde (Calvin-Benson mekanizması ile), 2. C 4 bitkilerinde (Hatch-Slack mekanizması ile), 3. KAM
Bitki Fizyolojisi 6. Hafta 1 Fotosentezin karanlık tepkimelerinde karbondioksit özümlemesi; 1. C 3 bitkilerinde (Calvin-Benson mekanizması ile), 2. C 4 bitkilerinde (Hatch-Slack mekanizması ile), 3. KAM
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA. Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004
 REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
REAKSİYON KİNETİĞİ, REAKSİYONLARLA İLGİLİ TEMEL KAVRAMLAR VE METABOLİZMA Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Reaksiyon (tepkime) türleri 1 Gerçekte tüm organik tepkimeler dört sınıftan
www.demiraylisesi.com
 YÖNETİCİ MOLEKÜLLER C, H, O, N, P atomlarından meydana gelir. Hücrenin en büyük yapılı molekülüdür. Yönetici moleküller hücreye ait genetik bilgiyi taşır, hayatsal faaliyetleri yönetir, genetik bilginin
YÖNETİCİ MOLEKÜLLER C, H, O, N, P atomlarından meydana gelir. Hücrenin en büyük yapılı molekülüdür. Yönetici moleküller hücreye ait genetik bilgiyi taşır, hayatsal faaliyetleri yönetir, genetik bilginin
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
9. Hafta: Enzimler ve Enzim Kinetiği Prof. Dr. Şule PEKYARDIMCI ENZİMLERİN SINIFLANDIRILMASI
 9. Hafta: Enzimler ve Enzim Kinetiği Prof. Dr. Şule PEKYARDIMCI Enzimler, proteinlerin en büyük ve en çok özelleşmiş grubunu oluştururlar. Enzimler, canlı organizmalardaki kimyasal reaksiyonları hızlandıran
9. Hafta: Enzimler ve Enzim Kinetiği Prof. Dr. Şule PEKYARDIMCI Enzimler, proteinlerin en büyük ve en çok özelleşmiş grubunu oluştururlar. Enzimler, canlı organizmalardaki kimyasal reaksiyonları hızlandıran
METABOLİZMA REAKSİYONLARI. Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV
 METABOLİZMA REAKSİYONLARI Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV METABOLİZMA Canlı sistemde maddelerin uğradığı kimyasal değişikliklerin hepsine birden metabolizma, bu değişiklikleri meydana
METABOLİZMA REAKSİYONLARI Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV METABOLİZMA Canlı sistemde maddelerin uğradığı kimyasal değişikliklerin hepsine birden metabolizma, bu değişiklikleri meydana
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
METABOLİZMA. Dr. Serkan SAYINER
 METABOLİZMA Dr. Serkan SAYINER serkan.sayiner@neu.edu.tr Genel Bakış Canlı organizmalar, kendilerini yenilemek, gelişmek ve üremek için kimyasal maddelere gereksinim duyarlar. Çünkü organizmanın tamamı
METABOLİZMA Dr. Serkan SAYINER serkan.sayiner@neu.edu.tr Genel Bakış Canlı organizmalar, kendilerini yenilemek, gelişmek ve üremek için kimyasal maddelere gereksinim duyarlar. Çünkü organizmanın tamamı
YGS YE HAZIRLIK DENEMESi #21
 YGS YE HAZIRLIK DENEMESi #21 1) Aşağıda bazı dönüşüm tepkimeleri gösterilmiştir. a 2) Enzimlerin çalışma hızına etki eden faktörlerle ilgili; RH RH ADP + Pi ATP I II b Buna göre a ve b yönlerindeki değişimlerle
YGS YE HAZIRLIK DENEMESi #21 1) Aşağıda bazı dönüşüm tepkimeleri gösterilmiştir. a 2) Enzimlerin çalışma hızına etki eden faktörlerle ilgili; RH RH ADP + Pi ATP I II b Buna göre a ve b yönlerindeki değişimlerle
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir.
 Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
Sitrik Asit Döngüsü. (Trikarboksilik Asit Döngüsü, Krebs Döngüsü)
 Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu)
 Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
BITKI FIZYOLOJISININ TANıMı
 BITKI FIZYOLOJISININ TANıMı Bitki fizyolojisi, bitkilerin, yaşamları boyunca cereyan eden çeşitli yaşamsal olayların belirti ve nedenlerini inceleyen bir bilimdir. Canlılarda meydana gelen fiziksel ve
BITKI FIZYOLOJISININ TANıMı Bitki fizyolojisi, bitkilerin, yaşamları boyunca cereyan eden çeşitli yaşamsal olayların belirti ve nedenlerini inceleyen bir bilimdir. Canlılarda meydana gelen fiziksel ve
Akıllı Defter. 9.Sınıf Biyoloji. vitaminler,hormonlar,nükleik asitler. sembole tıklayınca etkinlik açılır. sembole tıklayınca ppt sunumu açılır
 9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
9.Sınıf Biyoloji 1 Akıllı Defter vitaminler,hormonlar,nükleik asitler sembole tıklayınca etkinlik açılır sembole tıklayınca ppt sunumu açılır sembole tıklayınca video açılır 1 VİTAMİNLER ***Vitaminler:
Organik bileşikler; karbonhidratlar, lipidler, proteinler, vitaminler ve nükleik asitler olmak üzere beş gruba ayrılır.
 ORGANİK BİLEŞİKLER **Organik bileşikler: Canlılar tarafından sentezlenirler. Yapılarında C, H, atomlarını bulundururlar. Organik bileşikler; karbonhidratlar, lipidler, proteinler, vitaminler ve nükleik
ORGANİK BİLEŞİKLER **Organik bileşikler: Canlılar tarafından sentezlenirler. Yapılarında C, H, atomlarını bulundururlar. Organik bileşikler; karbonhidratlar, lipidler, proteinler, vitaminler ve nükleik
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
FOTOSENTEZ. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal bağ enerjisine çeviren olaydır.
 1 FOTOSENTEZ *Fotosentez: Klorofilli canlıların, ışık enerjisini kullanarak; inorganik maddelerden organik besin sentezlemesine fotosentez denir. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal
1 FOTOSENTEZ *Fotosentez: Klorofilli canlıların, ışık enerjisini kullanarak; inorganik maddelerden organik besin sentezlemesine fotosentez denir. 1. Fotosentez, güneş enerjisini, besin içindeki saklı kimyasal
Yağ Asitlerinin β Oksidayonu. Prof. Dr. Fidancı
 Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER
 PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER Öncelikle, protein sentezinin yapılabilmesi için aşağıdakilerin mutlaka mevcut olması gerekmektedir: DNA Aktifleyici enzimler Üç çeşit RNA (mrna, trna, rrna) Ribozomlar
PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER Öncelikle, protein sentezinin yapılabilmesi için aşağıdakilerin mutlaka mevcut olması gerekmektedir: DNA Aktifleyici enzimler Üç çeşit RNA (mrna, trna, rrna) Ribozomlar
HÜCRESEL SOLUNUM OKSİJENSİZ SOLUNUM
 1 HÜCRESEL SOLUNUM *Hücresel solunum: Besinlerin parçalanarak ATP sentezlenmesine, hücresel solunum denir. ----------------------- OKSİJENSİZ SOLUNUM ----------------------- (ANAEROBİK SOLUNUM = FERMANTASYON)
1 HÜCRESEL SOLUNUM *Hücresel solunum: Besinlerin parçalanarak ATP sentezlenmesine, hücresel solunum denir. ----------------------- OKSİJENSİZ SOLUNUM ----------------------- (ANAEROBİK SOLUNUM = FERMANTASYON)
YGS ANAHTAR SORULAR #2
 YGS ANAHTAR SORULAR #2 1) Bir hayvan hücresinde laktoz yapımı ile ilgili olarak, sitoplazmadaki madde miktarının değişimlerini gösteren grafik aşağıdakilerden hangisi olamaz? A) Glikoz B) Su miktarı 2)
YGS ANAHTAR SORULAR #2 1) Bir hayvan hücresinde laktoz yapımı ile ilgili olarak, sitoplazmadaki madde miktarının değişimlerini gösteren grafik aşağıdakilerden hangisi olamaz? A) Glikoz B) Su miktarı 2)
YGS YE HAZIRLIK DENEMESi #2
 YGS YE HAZIRLIK DENEMESi #2 1) Aşağıdaki grafikte, ph derecesi ile X, Y ve Z enzimlerin tepkime hızı arasındaki ilişki gösterilmiştir. 2) Aşağıdaki şemada kloroplast ile mitokondri arasındaki madde alış
YGS YE HAZIRLIK DENEMESi #2 1) Aşağıdaki grafikte, ph derecesi ile X, Y ve Z enzimlerin tepkime hızı arasındaki ilişki gösterilmiştir. 2) Aşağıdaki şemada kloroplast ile mitokondri arasındaki madde alış
BİYOLOJİ DERS NOTLARI YGS-LGS YÖNETİCİ MOLEKÜLLER
 www.benimdershanem.esy.es Bilgi paylaştıkça çoğalır. BİYOLOJİ DERS NOTLARI YGS-LGS YÖNETİCİ MOLEKÜLLER NÜKLEİK ASİTLER Nükleik asitler, bütün canlı hücrelerde ve virüslerde bulunan, nükleotid birimlerden
www.benimdershanem.esy.es Bilgi paylaştıkça çoğalır. BİYOLOJİ DERS NOTLARI YGS-LGS YÖNETİCİ MOLEKÜLLER NÜKLEİK ASİTLER Nükleik asitler, bütün canlı hücrelerde ve virüslerde bulunan, nükleotid birimlerden
ÜNİTE 7:HÜCRESEL SOLUNUM
 ÜNİTE 7:HÜCRESEL SOLUNUM Hücreler iş yapabilmek için enerjiye gereksinim duyarlar. Enerji ekosisteme güneş enerjisi yoluyla gelir ve ototrof canlılar sayesinde güneş enerjisi besinlerdeki kimyasal bağ
ÜNİTE 7:HÜCRESEL SOLUNUM Hücreler iş yapabilmek için enerjiye gereksinim duyarlar. Enerji ekosisteme güneş enerjisi yoluyla gelir ve ototrof canlılar sayesinde güneş enerjisi besinlerdeki kimyasal bağ
2008-2009 Güz Yarı Dönemi
 BİY315 ENZİMLER Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi ENZİMLER Canlılarda meydana gelen biyokimyasal reaksiyonları gerçekleştiren katalizörlere enzim denir.enzimler yapı olarak iki kısımda
BİY315 ENZİMLER Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi ENZİMLER Canlılarda meydana gelen biyokimyasal reaksiyonları gerçekleştiren katalizörlere enzim denir.enzimler yapı olarak iki kısımda
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ
 15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
15- RADYASYONUN NÜKLEİK ASİTLER VE PROTEİNLERE ETKİLERİ İyonlaştırıcı radyasyonların biyomoleküllere örneğin nükleik asitler ve proteinlere olan etkisi hakkında yeterli bilgi yoktur. Ancak, nükleik asitlerden
ENDÜSTRIDE VE CANLILARDA ENERJI. Canlılarda Enerji
 ENDÜSTRIDE VE CANLILARDA ENERJI Canlılarda Enerji Besinlerin Enerjiye Dönüşümü İnsanların gün boyunca hareketlerinin devamını, hastalanınca iyileşmelerini, fizyolojik ve psikolojik tepkilerinin devamlılığını
ENDÜSTRIDE VE CANLILARDA ENERJI Canlılarda Enerji Besinlerin Enerjiye Dönüşümü İnsanların gün boyunca hareketlerinin devamını, hastalanınca iyileşmelerini, fizyolojik ve psikolojik tepkilerinin devamlılığını
YGS ANAHTAR SORULAR #1
 YGS ANAHTAR SORULAR #1 1) Yıkımları sırasında Tüketilen O2 miktarı 2) H2O2 H2O2 H2O2 Grafikte bazı organik bileşiklerin yıkımları sırasında tüketilen oksijen miktarı verilmiştir. Buna göre organik bileşiklerin
YGS ANAHTAR SORULAR #1 1) Yıkımları sırasında Tüketilen O2 miktarı 2) H2O2 H2O2 H2O2 Grafikte bazı organik bileşiklerin yıkımları sırasında tüketilen oksijen miktarı verilmiştir. Buna göre organik bileşiklerin
BİTKİLERDE SOLUNUM REAKSİYONLARI. Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi
 BİTKİLERDE SOLUNUM REAKSİYONLARI Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi Havanın serbest O2 kullanarak bitki hücrelerinde şekerlerin, yağların ya da diğer organik moleküllerin oksitlenmesi
BİTKİLERDE SOLUNUM REAKSİYONLARI Prof. Dr. Necmi İŞLER Tarla Bitkileri Bölümü Öğretim Üyesi Havanın serbest O2 kullanarak bitki hücrelerinde şekerlerin, yağların ya da diğer organik moleküllerin oksitlenmesi
M. (arpa şekeri) +su S (çay şekeri) + su L.. (süt şekeri)+ su
 KARBONHİDRATLAR Karbonhidratlar yapılarında.. (C),.. (H) ve. (O) atomu bulunduran organik bileşiklerdir. Karbonhidratların formülü ( ) ile gösterilir. Nükleik asitlerin, ATP nin, hücre, bitkilerde yapısına
KARBONHİDRATLAR Karbonhidratlar yapılarında.. (C),.. (H) ve. (O) atomu bulunduran organik bileşiklerdir. Karbonhidratların formülü ( ) ile gösterilir. Nükleik asitlerin, ATP nin, hücre, bitkilerde yapısına
Hücre zarının yapısındaki yağlardan eriyerek hücre zarından geçerler.fazlalıkları karaciğerde depo edilir.
 DERS: BİYOLOJİ KONU: C.T.B(Vitaminler e Nükleik Asitler) VİTAMİNLER Bitkiler ihtiyaç duydukları bütün vitaminleri üretip, insanlar ise bir kısmını hazır alır. Özellikleri: Yapıcı, onarıcı, düzenleyicidirler.
DERS: BİYOLOJİ KONU: C.T.B(Vitaminler e Nükleik Asitler) VİTAMİNLER Bitkiler ihtiyaç duydukları bütün vitaminleri üretip, insanlar ise bir kısmını hazır alır. Özellikleri: Yapıcı, onarıcı, düzenleyicidirler.
Öğr. Gör. Dr. İlker BÜYÜK (Botanik, 10. Hafta): Fotosentez FOTOSENTEZ
 FOTOSENTEZ Elektron Koparılması ve Floresans Enerjisi Elektronlar negatif (e - ) ve protonlar pozitif (p + ) yüklüdür. Bu nedenle protonlar elektronları çekerler. Elektronlar ise, belli bir enerjiye sahiptir
FOTOSENTEZ Elektron Koparılması ve Floresans Enerjisi Elektronlar negatif (e - ) ve protonlar pozitif (p + ) yüklüdür. Bu nedenle protonlar elektronları çekerler. Elektronlar ise, belli bir enerjiye sahiptir
LYS BÝYOLOJÝ. Biyolojiye Giriþ ve Bilimsel Yöntem Canlýlarýn Temel Bileþenleri Enzimler Canlýlarýn Sýnýflandýrýlmasý
 LYS BÝYOLOJÝ Soru Çözüm Dersi Kitapçığı 1 (MF) Biyolojiye Giriþ ve Bilimsel Yöntem Canlýlarýn Temel Bileþenleri Enzimler Canlýlarýn Sýnýflandýrýlmasý Bu yayýnýn her hakký saklýdýr. Tüm haklarý bry Birey
LYS BÝYOLOJÝ Soru Çözüm Dersi Kitapçığı 1 (MF) Biyolojiye Giriþ ve Bilimsel Yöntem Canlýlarýn Temel Bileþenleri Enzimler Canlýlarýn Sýnýflandýrýlmasý Bu yayýnýn her hakký saklýdýr. Tüm haklarý bry Birey
Sunum ve Sistematik 1. ÜNİTE: CANLILARDA ENERJİ DÖNÜŞÜMÜ KONU ÖZETİ
 Sunum ve Sistematik 1. ÜNİTE: CANLILARDA ENERJİ DÖNÜŞÜMÜ KONU ÖZETİ Bu başlık altında, ünitenin en can alıcı bilgileri, kazanım sırasına göre en alt başlıklara ayrılarak hap bilgi niteliğinde konu özeti
Sunum ve Sistematik 1. ÜNİTE: CANLILARDA ENERJİ DÖNÜŞÜMÜ KONU ÖZETİ Bu başlık altında, ünitenin en can alıcı bilgileri, kazanım sırasına göre en alt başlıklara ayrılarak hap bilgi niteliğinde konu özeti
HÜCRE SOLUNUMU ve FERMENTASYON
 HÜCRE SOLUNUMU ve FERMENTASYON 1 Bakteriler yoğurt, peynir, pizza üretimi gibi mayalanma olaylarını gerçekleştirirler. Kaslarınız çok çalışırsa, oksijen yokluğundan dolayı kasılamazlar. Yediğiniz bütün
HÜCRE SOLUNUMU ve FERMENTASYON 1 Bakteriler yoğurt, peynir, pizza üretimi gibi mayalanma olaylarını gerçekleştirirler. Kaslarınız çok çalışırsa, oksijen yokluğundan dolayı kasılamazlar. Yediğiniz bütün
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU
 13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
13 HÜCRESEL SOLUNUM LAKTİK ASİT FERMANTASYONU Laktik Asit Fermantasyonu Glikozdan oksijen yokluğunda laktik asit üretilmesine LAKTİK ASİT FERMANTASYONU denir. Bütün canlılarda sitoplazmada gerçekleşir.
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ
 KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
Replikasyon, Transkripsiyon ve Translasyon. Yrd. Doç. Dr. Osman İBİŞ
 Replikasyon, Transkripsiyon ve Translasyon Yrd. Doç. Dr. Osman İBİŞ DNA replikasyonu DNA nın replikasyonu, DNA molekülünün, sakladığı genetik bilgilerin sonraki nesillere aktarılması için kendi kopyasını
Replikasyon, Transkripsiyon ve Translasyon Yrd. Doç. Dr. Osman İBİŞ DNA replikasyonu DNA nın replikasyonu, DNA molekülünün, sakladığı genetik bilgilerin sonraki nesillere aktarılması için kendi kopyasını
Can boğazdan gelir.. Deveyi yardan uçuran bir tutam ottur..
 Can boğazdan gelir.. Deveyi yardan uçuran bir tutam ottur.. 1 BESLENME BİLİMİ 2 Yaşamımız süresince yaklaşık 60 ton besin tüketiyoruz. Besinler sağlığımız ve canlılığımızın devamını sağlar. Sağlıklı bir
Can boğazdan gelir.. Deveyi yardan uçuran bir tutam ottur.. 1 BESLENME BİLİMİ 2 Yaşamımız süresince yaklaşık 60 ton besin tüketiyoruz. Besinler sağlığımız ve canlılığımızın devamını sağlar. Sağlıklı bir
YGS YE HAZIRLIK DENEMESi #6
 YGS YE HAZIRLIK DENEMESi #6 1) Canlılar soylarının devam ettirebilmek için üreyerek yeni bireyler meydana getirir. Bu üreme olaylarıyla ilgili olarak; I. Bakterinin ikiye bölünerek kendine benzer yeni
YGS YE HAZIRLIK DENEMESi #6 1) Canlılar soylarının devam ettirebilmek için üreyerek yeni bireyler meydana getirir. Bu üreme olaylarıyla ilgili olarak; I. Bakterinin ikiye bölünerek kendine benzer yeni
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur.
 Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
ÜNİTE 9. Enzimler. Amaçlar. İçindekiler. Öneriler
 ÜİTE 9 Enzimler Amaçlar Bu üniteyi çalıştıktan sonra; Enzimlerin yapısını ve enzimlerle ilgili terimleri öğrenecek, Enzimlerin isimlendirilmesini ve özgüllüğünü bilecek, Enzim aktivitesini açıklayabilecek,
ÜİTE 9 Enzimler Amaçlar Bu üniteyi çalıştıktan sonra; Enzimlerin yapısını ve enzimlerle ilgili terimleri öğrenecek, Enzimlerin isimlendirilmesini ve özgüllüğünü bilecek, Enzim aktivitesini açıklayabilecek,
1.Oksidoredüktazlar Oksidoredüktazların en önemli koenzimleri a) Nikotinamid-adenin Dinükleotidler (NAD) b) Nikotinamid-Adenin-Dinükleotid-fosfat
 1.Oksidoredüktazlar Oksidoredüktazların en önemli koenzimleri a) Nikotinamid-adenin Dinükleotidler (NAD) b) Nikotinamid-Adenin-Dinükleotid-fosfat (NADP) Prostatik grupları a) Flavinnükleotidler flavinmononükleotid
1.Oksidoredüktazlar Oksidoredüktazların en önemli koenzimleri a) Nikotinamid-adenin Dinükleotidler (NAD) b) Nikotinamid-Adenin-Dinükleotid-fosfat (NADP) Prostatik grupları a) Flavinnükleotidler flavinmononükleotid
Su ve çevrenin canlılar için uygunluğu
 Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
Su ve çevrenin canlılar için uygunluğu Su ve çevrenin canlılar için uygunluğu Yeryüzündeki yaşam su içinde ortaya çıkmış ve canlıların karalar üzerine yayılışından önceki 3 milyar yıl boyunca su içinde
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
Hücreler Enerjiyi Nasıl Elde Eder?
 Hücreler Enerjiyi Nasıl Elde Eder? MBG 111 BİYOLOJİ I Hazırlayan: Yrd.Doç.Dr. Yosun MATER Ekosistem ve Enerji Ekosistemde enerjinin akışı güneş ışığı ve ısı şeklinde gözlenir. Tam tersine canlı hücrelerde
Hücreler Enerjiyi Nasıl Elde Eder? MBG 111 BİYOLOJİ I Hazırlayan: Yrd.Doç.Dr. Yosun MATER Ekosistem ve Enerji Ekosistemde enerjinin akışı güneş ışığı ve ısı şeklinde gözlenir. Tam tersine canlı hücrelerde
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Yağ Asitlerinin Biyosentezi. Prof. Dr. Fidancı
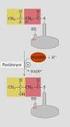 Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
ENZİMLER. Prof. Dr. Arif Altıntaş
 ENZİMLER Prof. Dr. Arif Altıntaş Enzim Biyokimyasal reaksiyonların pek çoğu protein yapısındaki organik kimyasal maddeler tarafından katalizlenir. Bu çeşit biyolojik katalizörlere Enzim adı verilir. İlk
ENZİMLER Prof. Dr. Arif Altıntaş Enzim Biyokimyasal reaksiyonların pek çoğu protein yapısındaki organik kimyasal maddeler tarafından katalizlenir. Bu çeşit biyolojik katalizörlere Enzim adı verilir. İlk
Biyokimya. Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler)
 Biyokimya Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler) Bölüm 1: Biyokimya ve önemi: 1. Biyokimya tanımı, önemi ve boyutsal
Biyokimya Biyokimyanın tanımı ve önemi Organizmanın elementer yapısı Canlılık Su Kovalent olmayan bağlar (intermoleküler etkileşimler) Bölüm 1: Biyokimya ve önemi: 1. Biyokimya tanımı, önemi ve boyutsal
LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ SAFRA ASİTLERİ
 8. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ 1. Yapısal fonksiyon görevi: Lipitler fosfolipitler başta olmak üzere hücre ve organel zarlarının yapısına girer
8. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ 1. Yapısal fonksiyon görevi: Lipitler fosfolipitler başta olmak üzere hücre ve organel zarlarının yapısına girer
ENERJİ iş yapabilme veya ortaya koyabilme kapasitesi 6 enerji şekli:
 ENERJİ SİSTEMLERİ 1 ENERJİ iş yapabilme veya ortaya koyabilme kapasitesi 6 enerji şekli: 1. Kimyasal Enerji 2. Mekanik Enerji 3. Isı Enerjisi 4. Işık Enerjisi 5. Elektrik Enerjisi 6. Nükleer Enerji Bu
ENERJİ SİSTEMLERİ 1 ENERJİ iş yapabilme veya ortaya koyabilme kapasitesi 6 enerji şekli: 1. Kimyasal Enerji 2. Mekanik Enerji 3. Isı Enerjisi 4. Işık Enerjisi 5. Elektrik Enerjisi 6. Nükleer Enerji Bu
Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar.
 Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
Kinetik ve Potansiyel Enerji Enerji iş yapabilme kapasitesidir. Kimyacı işi bir süreçten kaynaklanan enerji deyişimi olarak tanımlar. Işıma veya Güneş Enerjisi Isı Enerjisi Kimyasal Enerji Nükleer Enerji
ÜNİTE 7 : HÜCRESEL SOLUNUM
 ÜNİTE 7 : HÜCRESEL SOLUNUM Yaşam için gerekli enerjinin tümü güneşten gelir.güneşte hidrojen füzyonla helyuma dönüşür ve ışık üretilir.yeşil bitkiler güneş ışığının enerjisini fotosentezle glukozdaki kimyasal
ÜNİTE 7 : HÜCRESEL SOLUNUM Yaşam için gerekli enerjinin tümü güneşten gelir.güneşte hidrojen füzyonla helyuma dönüşür ve ışık üretilir.yeşil bitkiler güneş ışığının enerjisini fotosentezle glukozdaki kimyasal
9.Sınıf Biyoloji. Yaşam Bilimi Biyoloji. cevap anahtarı
 9.Sınıf Biyoloji 1 Yaşam Bilimi Biyoloji cevap anahtarı 1 CANLILARIN TEMEL BİLEŞENLERİ *Canlıların temel bileşenleri: Canlıların temel bileşenleri; organik ve inorganik bileşikler olmak üzere ikiye ayrılır.
9.Sınıf Biyoloji 1 Yaşam Bilimi Biyoloji cevap anahtarı 1 CANLILARIN TEMEL BİLEŞENLERİ *Canlıların temel bileşenleri: Canlıların temel bileşenleri; organik ve inorganik bileşikler olmak üzere ikiye ayrılır.
KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER
 KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER Biyokimyasal olarak önemli reaksiyon türleri Canlı hücredeki reaksiyonların çoğu, beş genel kategoriden birine uyar: 1) Fonksiyonel grup transferi 2) Oksidasyon
KİMYASAL TERMODİNAMİK VE BİYOENERJETİKLER Biyokimyasal olarak önemli reaksiyon türleri Canlı hücredeki reaksiyonların çoğu, beş genel kategoriden birine uyar: 1) Fonksiyonel grup transferi 2) Oksidasyon
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ
 7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
7. PROKARYOTLARDA GEN İFADESİNİN DÜZENLENMESİ Başlıklar 1. Prokaryotlar gen ifadesini çevre koşullarına göre düzenler 2. E. Coli de laktoz metabolizması 3. Lac operonu negatif kontrol 4. CAP pozitif kontrol
CANLILAR VE ENERJİ İLŞKİLERİ
 CANLILAR VE ENERJİ İLŞKİLERİ Besin Zincirindeki Enerji Akışı Madde Döngüleri Enerji Kaynakları ve Geri Dönüşüm Hazırlayan; Arif Özgür ÜLGER Besin Zincirindeki Enerji Akışı Bütün canlılar yaşamlarını devam
CANLILAR VE ENERJİ İLŞKİLERİ Besin Zincirindeki Enerji Akışı Madde Döngüleri Enerji Kaynakları ve Geri Dönüşüm Hazırlayan; Arif Özgür ÜLGER Besin Zincirindeki Enerji Akışı Bütün canlılar yaşamlarını devam
GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER
 GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER Mikroorganizmaların gıdalarla gelişmesi; Gıdanın karekteristik özelliğine, Gıdada bulunan m.o lara ve bunlar arası etkileşime, Çevre koşullarına bağlı
GIDALARDA MİKROBİYAL GELİŞMEYİ ETKİLEYEN FAKTÖRLER Mikroorganizmaların gıdalarla gelişmesi; Gıdanın karekteristik özelliğine, Gıdada bulunan m.o lara ve bunlar arası etkileşime, Çevre koşullarına bağlı
YGS YE HAZIRLIK DENEMESi #15
 YGS YE HAZIRLIK DENEMESi #15 1) Bir hücrede meydana gelen bölünme evrelerinden birine ait şekil yukarıdaki gibi ise; I. Diploit kromozomludur. II. Glikozu nişasta şeklinde depolar. III. Sitoplazması boğumlanma
YGS YE HAZIRLIK DENEMESi #15 1) Bir hücrede meydana gelen bölünme evrelerinden birine ait şekil yukarıdaki gibi ise; I. Diploit kromozomludur. II. Glikozu nişasta şeklinde depolar. III. Sitoplazması boğumlanma
