DrTus.com ilk ve tek tus portalı BĐYOKĐMYA ÖZET NOT
|
|
|
- Tülay Basak Akçatepe
- 6 yıl önce
- İzleme sayısı:
Transkript
1 1 BĐYOKĐMYA ÖZET NOT Vücudun başlıca enerji kaynakları karbonhidratlar, yağlar ve proteinlerdir. Bunlar diyetle alınırlar ve vücutta depolanırlar. Beslenme durumunda (yemekten sonra) üretilen enerji, vücudun acil ihtiyaçlarını karşılamak için kullanılır ve fazla enerji depolanır. Depolanan enerjiler açlık esnasında (yemek araları veya geceleyin) ihtiyaçları karşılamak için kullanılır. Kan insülin düzeyleri beslenme durumunda artarak enerjinin depolanmasını sağlarken açlıkta glukagon düzeyleri artarak depolanan enerjiyi sebestleştirir. I. METABOLĐK YAKITLAR VE DĐYET BĐLEŞENLERĐ Yakıtlar vücutta metabolize olduğunda ısı meydana gelir ve adenozin trifosfat (ATP) sentezlenir. Yakıtlar CO 2 ve H 2 O ya okside olarak enerji üretilir: a.karbonhidratlar yaklaşık 4 kcal/g üretir. b.proteinler yaklaşık 4 kcal/g üretir. c.yağlar iki kattan daha fazla enerji üretirler (9 kcal/g). d.alkol yaklaşık 7 kcal/g üretir. Yağar daha fazla redükte oldukları için daha fazla enerji verirler. Vücudun başlıca enerji kaynağı yağlardır. Yağlar yağ asitlerinden oluşur. 1
2 2 II. BESLENME VEYA EMĐLĐM DURUMU Dengeli bir yemekten sonra kanda insülin artar, glukogan azalır. Beslenme sonrası besin maddeleri - glikojen, protein, triaçilgliserol - depolanır. Đnsülin sentez reaksiyonlarında görev alır. Kas ve yağ dokusuna glukozun girişi insülin tarafından uyarılır. Diyetle alınan yağlar şilomikronlar içinde, karaciğerde sentezlenen yağlar kanda VLDL içinde taşınır. III. AÇLIK Bir yemekten sonra kan glukoz düzeyleri azaldıkça, insülin düzeyleri azalır, glukagon düzeyleri artar ve sonuçta depolanmış yakıtların kana salınımı uyarılır. Açlığın 12. saatine kadar kana glukoz sağlayan başlıca kaynak karaciğer glikojenidir. Açlığın 12. saatinden sonra kana glukoz sağlayan başlıca kaynak amino asitlerdir (glukoneogenez yoluyla). Keton cisimleri açlıkta karaciğerde sentezlenir, kas ve böbrek tarafından kullanılır. 2
3 3 IV. UZAMIŞ AÇLIK 3-5 gün açlıktan sonra vücut yakıt depolarının kullanımında değişiklikler gözlenir. Uzamış açlıkta keton cisimlerini kullanan doku: beyin Bir kişinin açlığa direnci içerdiği yağ dokusuyla orantılıdır. 3
4 4 V. ORGANĐK KĐMYANIN KISA ÖZETĐ Oksidasyon: Elektronların kaybı Redüksiyon: Elektronların kazanılması Kistik fibroziste klor iyon kanallarının proteinleri defektlidir. Bir proteinin biyolojik değerini belirleyen o proteindeki esansiyel amino asitlerin miktarıdır. 4
5 5 ASĐTLER, BAZLAR VE TAMPONLAR pk nedir? Bir asitin ayrışma sabiti olan K nın negatif logaritmasıdır. pk değeri ne kadar düşükse asit o kadar kuvvetlidir. Asitler proton veren ve bazlar proton alan bileşiklerdir. 1. Asitler, moleküllerine ayrışır. a. Hidroklorik asit (HCl) gibi güçlü asitler, tamamen ayrışır. b. Asetik asit gibi zayıf asitler sadece sınırlı bir oranda ayrışır. HA H+ + A- HA, zayıf asit ve A- onun konjuge bazıdır. Bir asitin proton taşımayan şekline konjuge baz denir. R-COOH R-COO- + H+ Bir bazın proton almış şekline konjuge asit denir. R-NH3+ R-NH2 + H+ c. Zayıf bir asitin ayrışma sabiti: K = [H+] [A-] / [HA] 2. Henderson Hasselbalch eşitliği ayrışma sabiti için düzenlenen eşitlikten türemiştir: ph = pk + log10 [A-] / [HA] pk, ayrışma sabiti olan K nın negatif logaritmasıdır. Tampon, az miktarda asit (H+) veya baz (OH-) ilave edildiğinde ph değişikliklerine direnen sulu sistemlerdir. Bir tampon sistemi zayıf asit (proton verici) ve onun konjuge bazından (proton alıcı) oluşmuştur. Örn: asetik asit ve asetat. Henderson Hasselbalch eşitliği: ph= pk + log10 [A-] / [HA] pk nın yorumu: Bir asit pk değerinin altındaki bir ph ortamında protonlanmıştır (örn. CH3-COOH), pk değerinin üstündeki bir ph ortamında ise protonunu vermiştir (örn. CH3-COO). pk değerinde ise eşit miktarda protonlanmış ve protonunu vermiş formu bulunur. Tampon sistemi oluşturan ikili: Zayıf asit ile bu asidin tuzunun karışımı Tam kanın başlıca tampon sistemleri: karbonikasit-bikarbonat + hemoglobin Tampon çözeltileri kendi pk değerlerinin ± 1 ph sınırları içinde etkili tamponlama yaparlar. Plazmanın başlıca tampon sistemleri: karbonik asit- bikarbonat + protein Asit-baz dengesinden sorumlu enzim ve kofaktörü: Karbonik anhidraz enzimi, kofaktörü çinko 5
6 6 AMĐNO ASĐTLER VE PEPTĐD BAĞLARI Amino asitler: Doğada 300 den fazla amino asit bulunmakla beraber ribozomlarda oluşan mrna nın yönettiği protein sentezinde kullanılmak üzere 20 amino asit bulunur. Diğer amino asitlerin genetik kodu yoktur; örn. Üre siklusunda veya post-translasyonel modifikasyonla oluşan amino asitler. Post-translasyonel modifikasyona örnekler: Prolin ve lizinin, hidroksiprolin ve hidroksilizine ve glutamatın gamakarboksiglutamata çevrilmesi ve fonksiyonel grupların metilasyonu, formilasyonu, asetilasyonu, prenilasyonu ve fosforilasyonu. Amino asitlerin ortak özellikleri: Amfoterik olmaları, belli ph larda bir izoelektrik noktasına sahip olmaları, nötral ph da ikili iyon yapısında olmaları, proteinlerin yapısına L-konfigürasyonunda girmeleri Dallı zincirli amino asitler: valin, lösin, izolösin Hidroksil grubu içeren amino asitler: serin, treonin, tirozin 6
7 7 Tiyo-eter bağı içeren amino asit: metionin Polar amino asitler ve özellikleri: asidik (amid formları dahil) ve bazik amino asitler, hidroksil grubu içerenler ve sistein, proteinlerin dış tarafında yer alır. Birden fazla asimetrik karbon içeren amino asitler: izolösin ve treonin Amino asitlerin hidrofilik ve hidrofobik özelliklerine göre sınıflandırılması Hidrofobik Glisin Alanin Đzolösin Lösin Metionin Fenilalanin Prolin Triptofan Valin Hidrofilik Arginin Asparagin Aspartik asit Sistein Glutamik asit Glutamin Tirozin Histidin Lizin Serin Treonin Proteinlerin yapısında yan zincirleri iyonize olan amino asitler: asidik ve bazik olanlar 7
8 8 Bir amino asitin izoelektrik noktası (pi) nedir ve nasıl hesaplanır? Amino asitte net yükün sıfır olduğu ph değeridir ve alfa-karboksil grubu ile alfa-amino grubunun pk değerlerinin toplamının yarısıdır. Asidik amino asitlerde pi değerini bulmak için karboksil gruplarının pk değeri toplanıp ikiye bölünür, bazik amino asitlerde amino gruplarının pk değeri toplanıp ikiye bölünür. Aromatik halka içeren amino asitler ve özellikleri: Fenilalanin, tirozin, triptofan ve histidin. UV ışığı absorbe ederler. Peptid bağları bir protein zincirinde her bir amino asitin à-karboksil grubuyla diğer amino asitin à-amino grubunun birleşmesidir. 8
9 9 Peptid bağları: Peptid bağları bir protein zincirinde her bir amino asitin à-karboksil grubuyla diğer amino asitin à- amino grubunun birleşmesidir. Özellikleri a. Peptid bağları kovalent yapıdadır, proteinlerin primer yapısını oluşturur. b. Peptid bağına katılan atomlar rijid, planar bir birim oluştururlar. c. Kısmi çift bağ karakterinde olduğu için, peptid bağı serbestçe rotasyon yapmaz. Bununla beraber alfakarbonuna bağlı bağlar serbestçe rotasyon yapabilir. d. Trans konfigürasyonundadır. e. Yüksüzdür fakat polardır. 9
10 10 Proteinlerin primer ve tersiyer yapısının belirlenmesinde sırasıyla neler kullanılır? Edman reaktifi ve X ışını kristallografi Tripsin ve siyanojen bromür bir proteinde hangi bağları hidroliz eder? Tripsin arginin ve lizinin karboksil tarafındaki peptid bağlarını, siyanojen bromür ise metioninin karboksil tarafındaki peptid bağını. PROTEĐN YAPISI Bir polipeptid zincirinde amino asit kalıntılarının lineer dizilimi bir proteinin üç boyutlu konfigürasyonunu belirler ve bir proteinin üç boyutlu yapısı onun fonksiyonunu belirler. Proteinlerin molekül ağırlığı Dalton birimi ile ifade edilir. Proteinin sekonder yapısından sorumlu başlıca bağ türü: hidrojen bağları 10
11 11 Alfa heliks ve beta tabakayı bozan amino asitler: prolin ve glisin Proteinlerin fonksiyonundan sorumlu olan yapı: tersiyer yapı (tersiyer yapıyı belirleyen primer yapıdır) Kuarterner yapının oluşmasında hangi bağlar rol oynamaz? Kovalent Proteinleri denatüre edici ajanlar: üre, ısı, asit ve alkaliler, SDS, ağır metaller 11
12 12 Moleküler şaperon: ısı şok proteinleri Post-translasyonel modifikasyon örneği olmayan: intronların çıkarılması, şapka eklenmesi. GLOBÜLER PROTEĐNLER: HEMOGLOBĐN VE MĐYOGLOBĐN Hem içeren moleküller Hemoglobin Sitokromlar Peroksidaz Prostaglandin sentaz Klorofil Miyoglobin Katalaz NO sentetaz Triptofan pirolaz 12
13 13 Fe2+ içeren Hem oksijen bağlayabilir. Globüler proteinler ve özellikleri: hemoglobin miyoglobin, genellikle hücre içi yerleşim gösterirler ve fonksiyonel rolleri bulunur. Miyoglobin kalp ve iskelet kasında bulunan bir hem proteinidir. Fonksiyonu kas hücresi içinde oksijeni depolamak ve egzersiz halinde ATP sentezi için bu oksijeni serbestleştirmektir. Hemoglobin yoğun olarak eritrositlerde bulunur. Başlıca fonksiyonu oksijeni akciğerlerden alarak dokulara taşımak ve dokularda oluşan CO2 ve protonları akciğerlere götürmektir. Ayrıca tampon görevi de vardır. 13
14 14 Hemoglobinin oksijene bağlanmasını etkileyen faktörler po2 ph pco2 2,3 BPG Isı 2,3 BPG artışı hangi durumda gerçekleşir? Oksijene ihtiyacın arttığı durumlarda Hemoglobinin oksijen satürasyon eğrisini sağa kaydıranlar (O2 ye afiniteyi azaltırlar): Asidoz 2,3 BPG artışı CO2 artışı Isı 14
15 15 Hemoglobinin oksijen satürasyon eğrisini sola kaydıranlar (O2 ye afiniteyi arttırırlar): Alkaloz O2 artışı CO 2,3-BPG hemoglobinin β globin zincirlerinin yüzeyindeki bazik amino asitlerle etkileşime girer. Hemoglobin F ve özelliği: 2 alfa ve 2 gama globin zincirinden oluşur, fetüste ve yeni doğanda bulunur. 2,3BPG Hb F e bağlanamaz. Oksijene afinitede doğru sıralama: miyoglobin >hemoglobin F > hemoglobin A Dokularda oluşan CO2 nin akciğerlere başlıca taşınma şekli: bikarbonat iyonları 15
16 16 Tablo: Normal yetişkin insan hemoglobinleri Hb Tipi Zincir Yapısı Total Hb fraksiyonu HbA α2β2 % 90 HbF α2γ2 <%2 HbA2 α2δ2 %2-5 HbA1c α2β2 %3-6 Protonların hemoglobindeki bağlanma bölgesi: histidin Hemoglobinopatiler Hemoglobinopatilerde: Yapısal olarak anormal hemoglobin üretimi; veya Normal hemoglobinin yetersiz miktarda sentezi; söz konusudur. Fruktozamin nedir ve kullanımı: Glikozillenmiş albümin ve 2-3 hafta önceki ortalama kan glukoz düzeylerini yansıtır. Fibröz proteinler ve özellikleri: Kollajen, elastin, keratin, tropomiyozin ve ipek fibroini. Bunlar genellikle hücre dışı yerleşim gösterirler ve yapısal fonksiyonlara sahiptir. FĐBRÖZ PROTEĐNLER Kollajen Vücutta en bol bulunan proteindir. Üçlü heliks yapıya sahiptir. Glisin, prolin ve hidroksiprolinden zengindir. Kollajen sentezinde hücre içi olaylar Preprokollajen zincirlerinin sentezi ve sinyal peptidin kaldırılması Hidroksilasyon- glikozilasyon Üçlü heliks oluşumu Uzantılarda disülfid bağların oluşumu 16
17 17 Kollajen sentezinde hücre dışı olaylar Proteolitik yıkım Kollajen oluşumu Lizil oksidasyonu Kovalent çapraz bağlar Kollajen fibrilleri arasında kovalent çapraz bağların oluşmasında görev alan amino asit: Lizin 17
18 18 En bol bulunan kollajen tipleri. Romen rakamları, Alfa1 ve Alfa2 zincirlerinin alt tiplerini göstermektedir. Kollajen türleri arasında vücutta en fazla bulunanı tip I dir. Tip Zincir Bileşimi Bulunduğu dokular I α1 (I)2 α2 (I) Deri, kemik, tendon, kan damarları, kornea II [α1(ii)]3 Kıkırdak, intervertebral disk, vitröz cisim III [α1(iii)]3 Kan damarları, fetal deri IV [α1(iv)]2α2(iv) Bazal membran ENZĐMLER Enzim, kataliz etkisi gösteren yani reaksiyonun hızını artıran proteindir. Enzimler hücre içindeki kimyasal reaksiyonları hücrenin ihtiyacına uygun olarak katalizler. Tripsin hangi enzim sınıfına aittir? Peptidaz grubuna ait olup bir hidrolazdır (su ekleyerek peptid bağlarını parçalar) Sentaz ve sentetaz arasındaki fark: sentetazlar ATP bağımlı enzimlerdir, sentaz doğrudan ATP ye gerek duymaz. Enzimlerin özellikleri Reaksiyonun denge sabitini değiştirmezler, hızını arttırırlar Reaksiyonun aktivasyon enerjisini azaltırlar Substratları ve ürünleri için spesifiktir Kofaktörlere gerek duyarlar. 18
19 19 19
20 20 Enzimin aktif bölgesi: Substrat ve kofaktörün bağlandığı bölge, genellikle polar amino asitler yer alır. Kofaktörler: Đnorganik yapıdaki metal iyonlarıdır. Koenzimler: Organik yapıdaki kofaktörlerdir (örn. B kompleks vitaminleri) Kofaktörü demir olan bazı enzimler Katalaz Peroksidaz Sit. oksidaz Triptofan pirolaz 20
21 21 Kofaktörü çinko olan bazı enzimler Karbonik anhidraz Alkol dehidrogenaz Karboksipeptidaz A ve B RNA polimeraz Alkalen fosfataz Laktat dehidrogenaz Kofaktörü bakır olan bazı enzimler Sit. oksidaz Dopamin β-hidroksilaz Lizil oksidaz Süperoksid dismutaz Tirozinaz Seruloplazmin Amin oksidaz Hidrojen gruplarını transfer eden koenzimler: * NAD+, NADP+ * FMN, FAD * Lipoik asit * Koenzim Q Hidrojenden başka diğer grupların transferinde rol oynayan koenzimler: * Şeker fosfatlar : fosfat (P) * KoA-SH : açil grubu * Tiamin pirofosfat : aldehid * Piridoksal fosfat : amino grubu * Folat koenzimleri : tek karbonlu bileşikler * Biotin : karbondioksit * Kobamid (B12) koenzimieri : alkil grupları * Lipoik asit : açil grubu Prostetik grup: Enzime sıkıca bağlanan ve ayrılmayan koenzim (örn. Karboksilaz enzimlerinin biotini, transaminazların piridoksal fosfatı) Kinazların etkisi için gerekli olan metal iyonu: magnezyum 21
22 22 Tip LDH1 LDH2 LDH3 LDH4 LDH5 Çeşitli dokularda laktat dehidrogenaz izoenzimlerinin yerleşimi. Yerleşim Miyokard, kırmızı küre Miyokard, kırmızı küre Beyin, akciğer, böbrek Akciğer, iskelet kası Karaciğer, iskelet kası Fonksiyonel plazma enzimleri: Lipoprotein lipaz, psödokolinesteraz, pıhtılaşma faktörleri Fonksiyonel olmayan plazma enzimleri: Ekzokrin sekresyonlarda bulunanlar (amilaz-lipaz) ve gerçek hücre içi enzimler (AST-ALT) Zimojenler: Proinsülin, prokollajen, pıhtılaşma faktörleri, tripsinojen, pepsinojen, kimotripsinojen, proelastaz, prokarboksipeptidaz CK1 (BB) CK2 (MB) CK3 (MM) Kreatin kinaz (CK) izoenzimlerinin çeşitli dokulardaki yerleşimi Tip Yerleşim Bağırsak, beyin, prostat Kalp kası (anormal) Đskelet kası, kalp kası (normal-anormal) Plazma alkalen fosfataz düzeylerini arttıran durumlar Karaciğer hastalıkları, Tıkanma sarılığı, Kemik hastalıkları, Kemiğin metastatik karsinoması Regan izoenzimi: plasenta kaynaklı alkalen fosfataz izoenzimidir. Serum enzimi Aminotransferazlar - Aspartat amino transferaz (AST) - Alanin amino transferaz (ALT) Amilaz, lipaz Serüloplazmin Kreatin kinaz Gama-Glutamil transpeptidaz LDH (izoenzim) Asit fosfataz Alkalen fosfataz (Đzoenzim) Klinik tanıda kullanılan başlıca serum enzimleri Başlıca kullanımı Miyokard infarktüsü Viral hepatit Akut pankreatit Wilson hastalığı Kas hastalıkları ve Ml Çeşitli (metastatik CA, alkolik) karaciğer hastalıkları MĐ Metastatik prostat karsinomu Çeşitli kemik hastalıkları, tıkayıcı karaciğer hastalıkları Serin proteazları ve özellikleri: Tripsin, kimotripsin, elastaz, plazmin, tpa, aktive pıhtılaşma faktörleri. Bu enzimler peptid bağlarını parçalar ve aktif bölgelerinde aktive olmuş serin artığı içerirler. Diizopropilfluorofosfat bu enzimleri inhibe eder. Enzimler katalitik etkilerini nasıl gerçekleştirir? Biyokimyasal reaksiyonun aktivasyon enerjisini azaltarak 22
23 23 Hız birimi: mikromol/dk Enzimle katalizlenen reaksiyonun hızını etkileyen faktörler Enzim konsantrasyonu Substrat konsantrasyonu Isı ph Kofaktörler Đnhibitörler ve ürün Michaelis-Menten kinetiği gösteren enzimler: Genellikle çift yönlü reaksiyonu katalizleyen enzimlerdir; hiperbolik kinetik gösterirler. Km: Maksimum reaksiyon hızının yarısına eşit olan substrat konsantrasyonudur. Enzimin substrata olan afinitesini gösterir. 23
24 24 Kompetitif inhibisyon özellikleri Đnhibitör ve substrat yapıca birbirine benzer, inhibitör aktif bölgeye reverzibl bağlanır Km artar Vmax değişmez. Örn. Alkol dehidrogenaz için etanol ve metanol; süksinat dehidrogenaz için malonat ve süksinat Yarışmalı inhibisyonun klinik uygulama örnekleri: Sülfonamidlerin bakterilerde PABA nın yerleşmesini inhibe etmeleri ve antibakteriyel ajan olarak etki göstermeleri, metotreksatın dihidrofolat redüktazı inhibe etmesi, dikumarolün K vitaminini inhibe etmesi Non-kompetitif inhibisyon özellikleri Đnhibitör ve substrat yapıca birbirine benzemez. Đnhibitör aktif bölge dışına reverzibl veya irreverzibl bağlanır, Km değişmez Vmax azalır. Örn. Kurşun ALA dehidrataz ve ferroşelataz enzimlerini non-kompetitif olarak inhibe eder. Ayrıca diizopropilfluorofosfat tripsini (serin proteazı) ve fluorid enolazı non-kompetitif olarak inhibe eder. Multi-enzim kompleks örnekleri Yağ asiti sentaz, Piruvat dehidrogenaz, Alfa-ketoglutarat dehidrogenaz 24
25 25 Allosterik enzimler ve özellikleri Genellikle bir metabolik yolun kontrol basamağını kataliz ederler; Aktif bölge dışında başka yere reverzibl bağlanan moleküllerle regüle edilirler, Çok sayıda alt birim içerirler, Aktive veya inhibe olabilirler, Genellikle substrat fazlalığı enzimi aktive eder, ürün fazlalığı inhibe eder, Allosterik kinetik gösterirler. Örn. Aspartat transkarbamoilaz; piruvat kinaz Enzimlerin kovalent modifikasyonu: Enzimlerin fosforilasyonu ve defosforilasyonu. Bir enzim sentezde rol oynuyorsa genellikle defosforile durumu aktiftir; bir enzim yıkımda rol oynuyorsa genellikle fosforile durumu aktiftir. Đnsülin sitrat liyaz ve fosfodiesteraz enzimlerini fosforiller ve aktive eder, diğerlerini defosforile eder. 25
26 26 Kovalent fosforilasyon-defosforilasyon ile katalitik aktiviteleri değişen enzim örnekleri Enzim Aktivite durumu Düşük Yüksek Asetil KoA karboksilaz Glikojen sentaz Piruvat dehidrogenaz HMG-KoA redüktaz Glikojen fosforilaz Sitrat liyaz Fosforilaz b kinaz HMG-KoA redüktaz kinaz Hormona duyarlı lipaz, defosforile enzim;, fosforillenmiş enzim Proteinlerde serin, treonin ve tirozindeki hidroksil gruplarına fosfat eklenir. Marfan sendromu: Fibrillin proteinindeki bir defekt sonucu gelişir. Konnektif dokuyu etkileyen ve nispeten sık görülen bir genetik hastalıktır. Klinik belirtiler değişkendir fakat, sıklıkla araknodaktilili (el ve ayak parmaklarının ince uzun olması) uzun boy, mitral valv prolapsusu ve lens dislokasyonu bulunur. OKSĐDATĐF FOSFORĐLASYON Adenozin trifosfat (ATP), enerji gerektiren olaylarda enerji transferi yapar. Glukoz, yağ asitleri, gliserol ve amino asitlerdeki karbonların büyük çoğunluğu sonunda asetil KoA ya çevrilir. ATP, bu reaksiyonlar tarafından üretilir (Şekil 3.1). Asetil KoA, trikarboksilik asit (TCA) döngüsünde okside olur. CO 2 serbestleşir ve elektronlar NAD + ve FAD ye geçerek NADH ve FADH 2 oluşur. NADH ve FADH 2, elektron transport zinciri aracılığıyla elektronlarını O 2 ye aktarır. Elektronların bu transferinden elde edilen enerji, oksidatif fosforilasyon işlemiyle ATP üretiminde kullanılır. Bir çoğu minerallerden türeyen veya vitaminlerden elde edilen kofaktörler, bu metabolik yolların reaksiyonlarını katalizleyen enzimlere yardımcı olur. 26
27 27 Asetil KoA kaynaklar Keton cisimleri Piruvat Yağ asitleri Ketojenik amino asitler Karbonhidrat, lipid ve amino asitlerin yıkımı sonucu açığa çıkan ortak son ürün: asetil KoA Besin maddelerinin oksidasyonu sonucu elektronların gittiği başlıca koenzim: NAD + ADENOZĐN TRĐFOSFATIN ÖZELLĐKLERĐ 27
28 28 ATP nin yapısında bulunanlar Adenin Riboz 3 adet fosforik asit β-n glikozidik bağ Fosfoester bağı Asit anhidrid bağlar. ATP hücre içinde Mg++ ile kompleks halde bulunur. ATP; ADP ve inorganik fosfata (Pi) veya AMP ve pirofosfata (PPi) hidroliz olabilir. ATP, ADP ve AMP adenilat kinaz reaksiyonuyla birbirlerine dönebilirler. adenilat kinaz ATP + AMP 2 ADP ELEKTRON TAŞIYICILARI Besinlerden ATP nin oluşumunda rol oynayan majör kofaktörler Besinler CO2 ve H2O ya okside oldukça elektronlar başlıca nikotinamid adenin dinükleotid (NAD+) ve flavin adenin dinükleotide (FAD) transfer olurlar. 1. NAD+, nikotinamid halkasıyla reaksiyona giren bir hidrid iyonu kabul eder. NAD+ indirgenir; substrat (RH2) okside olur; ve bir proton serbestleşir. NAD+ + RH2 NADH + H+ + R a. NAD+ sıklıkla bir hidroksil grubunun, bir ketona oksidasyonunda rol oynar. b. NAD+ nin nikotinamid halkası, niasin (nikotinik asit) halkasından ve sınırlı bir miktarda triptofan amino asitinden türemiştir. 2. FAD, iki hidrojen atomu (elektronlarıyla birlikte) kabul eder. FAD indirgenir ve substrat okside olur. FAD + RH2 FADH2+R 28
29 29 a. FAD sıklıkla bir çift bağ üreten reaksiyonlarda görev alır. R - CH2 - CH2 - R1 + FAD R - CH = CH - R1 + FADH2 b. FAD, riboflavin vitamininden türer. ATP sentezinde rol oynayan çok yüksek enerjili bileşikler Süksinil KoA Fosfoenolpiruvat 1,3-bifosfogliserat Kreatin fosfat Hidrid iyonu (2 elektron bir proton içeren hidrojen iyonu) kabul eden koenzim: NAD + ve NADP + NAD+ nin yapısında yer alanlar: adenin nükleotidi, riboz, pirofosfat, nikotinik asit Đzopren birimi içeren koenzim: Koenzim Q Protein yapıda olmayan ETZ üyesi: Koenzim Q Elektron transport zincirinin bileşenleri 29
30 30 Đndirgenmiş kofaktörler (NADH ve FADH2) elektronları, elektron transport zincirine (ETZ) aktarır. Koenzim Q hariç zincirin tüm üyeleri protein yapıdadır. Koenzim Q ve sitokrom c ETZ de hareketli bir taşıyıcı olarak fonksiyon görürler. 1. NADH dehidrogenaz kompleksi (kompleks I) içinde bulunan FMN, elektronları NADH dan alır ve onları Fe-S merkezleri içinde koenzim Q ya aktarır. FMN, riboflavine bir fosfat gurubunun bağlanmasıyla oluşur. 2. Süksinat dehidrogenaz kompleksi (kompleks II) içindeki FAD, elektronları süksinattan alarak Fe-S merkezleri içinde koenzim Q ya aktarır. 3. Koenzim Q (KoQ) elektronları H+ ile birlikte FMN den ve ayrıca Fe-S merkezleri içinde FADH2 den alır. a. FADH2, solüsyonda NAD+ ve NADH gibi serbest halde bulunmaz; enzimlere sıkıca bağlanır. b. Koenzim Q vücutta sentezlenebilir. Hidrofilik kinon bölümü ve izopren birimlerinden oluşan hidrofobik bir yan zincir içerir. Protein yapıda değildir ve bir vitaminden türememiştir. FMN içeren enzim: kompleks I (NADH dehidrogenaz) NADH nın elektronlarını aktardığı enzim: kompleks I Hangisi hem elektron hem de proton kabul eder? NAD+-NADP+ FMN-FAD, KoQ Kompleks I Kompleks II 30
31 31 4. Demir-sülfür proteinlerinde demir, inorganik sülfür atomlarıyla veya sistein artıklarının sülfür atomlarıyla ilişkidedir. Bu proteinler bir elektron transferine katılırlar. 5. Sitokromlar, koenzim Q nunindirgenmiş formundan sadece elektronları alır. a. Sitokromlar, hem grubu içeren ve görünen ışığı absorbe eden proteinlerdir. b. Mitokondride a, b ve c ile gösterilen üç sitokrom sınıfı bulunur. Sitokrom a da izopren birimi içeren hem a, sitokrom b de miyoglobin ve hemoglobinin de yapısında bulunan hem b, sitokrom c de ise sistein ile kovalent bağlanan hem c bulunur. c. Hem grubunun demiri, sitokromlar bir elektron kabul ettiğinde indirgenir. Fe3+ Fe2+ d. Hem, insanda glisin ve süksinil KoA dan sentezlenir. Bir vitaminden türememiştir. 6. Oksijen (O2) sonuçta elektron transport zincirinin sonunda elektronları alır ve H2O ya indirgenir. ELEKTRON TRANSPORT ZĐNCĐRĐ VE OKSĐDATĐF FOSFORĐLASYON ATP, elektronların NADH ve FADH2 den moleküler oksijene, elektron transport zinciri (ETZ) olarak adlandırılan bir grup elektron taşıyıcıları tarafından aktarılması esnasında üretilen enerjinin bir sonucu olarak meydana gelir. Zincirin komponentleri arasında FMN, Fe-S merkezleri, koenzim Q ve bir serisitokromlar (b, c1, c ve aa3) bulunur. Elektronların ETZ içinde taşınması ile üretilen enerji, protonların matriksten sitozolik bölgeye iç mitokondri membranı üzerinden pompalanmasında kullanılır. Sonuçta bir proton gradiyenti ve bir membran potansiyelinden meydana gelen bir elektrokimyasal gradiyent oluşur. Protonlar, ATP sentaz kompleksi içinden matrikse geritaşınırken ADP veinorganik fosfattan ATP sentezine neden olur. ATP mitokondri matriksinden sitozole ADP ile yer değiştirerek (ATP-ADP karşı taşıma sistemi) taşınır. Bir NADH nın oksidasyonu ile yaklaşık 3 ATP ve bir FADH2 nin oksidasyonu ile yaklaşık 2 ATP üretilir. 31
32 32 Elektronların ETZ içinden O2 ye transferi ile elde edilen enerji ATP üretiminde kullanıldığı için tüm işlem oksidatif fosforilasyon olarak adlandırılır. Elektron transportu ve ATP üretimi, birlikte seyreder ve birbiriyle sıkıca eşleşmiştir. NADH ve FADH2 nın oksidasyonu, ortamda ATP ye dönüşecek ADP varsa gerçekleşir (örn. ATP kullanılır ve ADP ye çevrilir). ETZ nin son enzimi: sitokrom oksidaz ETZ de irreverzibl olan basamak: sitokrom oksidaz (diğerleri reverzibl) ETZ nin hareketli iki bileşeni: KoQ ve sit c FADH2 den elektronların aktarıldığı bileşik: KoQ Okside olan her bir NADH ve FADH2 den sırasıyla yaklaşık kaç ATP sentezlenir? 3 ve 2 Đstirahat halindeki iskelet kasında oksidatif fosforilasyonun kontrolünün ADP, yoğun egzersiz halinde ise O2 ile sağlanır. ETZ nin tek irreverzibl reaksiyonu sitokrom oksidaz (Sita3 1/2 O2) Piruvattaki elektronlar ETZ ye hangi basamakta katılır? Kompleks I ETZ deki sitokromlarda hem demiri Fe3+ halinde bulunur, elektron alınca Fe2+ haline gelir. Mitokondride sentezlenen ATP stoplazmaya ne şekilde geçer? Kreatin fosfat şantı ile Mitokondri zarından geçebilmesi için taşıyıcı bir proteine ihtiyacı olan: ATP ETZ inhibitörlerinin etkisi: Elektronların oksijene geçişi inhibe olarak hem oksidasyon hem de fosforilasyon inhibedir. ATP sentazı inhibe edenler: oligomisin Adenin nükleotid taşıyıcısını inhibe edenler: atraktilozid Dimerkaprol (veya antimisina) varlığında hangi ETZ üyesi okside haldedir? Sitokrom c ve sitokrom oksidaz; diğerleri redüktedir. 32
33 33 Eşleşmeyi ayıranlar: 2,4-dinitrofenol Termogenin Anestezikler (halothan, eter) Yüksek doz aspirin Đyonoforlar (valinomisin-nigerisin) Tiroksin (fizyolojik olarak) Eşleşmeyi ayıranların özelliği: Đç mitokonri membranındaki elektrokimyasal potansiyel farkını ortadan kaldırırlar, oksidasyon olanca hızıyla devam eder, fosforilasyon durmuştur. Leber Herediter Optik Nöropati: Erkeklerde 20 yaş civarında akut veya subakut görme kaybı ile karakterize, kompleks I proteinini kodlayan mtdna daki mutasyon sonucu gelişen bir hastalıktır. ATP sentezinde rol oynayan çok yüksek enerjili bileşikler Süksinil KoA Fosfoenolpiruvat 1,3-bifosfogliserat Kreatin fosfat Hidrid iyonu (2 elektron bir proton içeren hidrojen iyonu) kabul eden koenzim: NAD+ ve NADP+ 33
34 34 KARBONHĐDRAT METABOLĐZMASI Karbonhidratların sindirimi sonucu oluşan başlıca ürün, glukozdur, fakat galaktoz ve fruktoz da bir miktar üretilir. Glukoz, enerji için hücreler tarafından okside edilen başlıca yakıttır. Bir yemek sonrası glikojene veya triaçilgliserollere çevrilir ve depolanır. Glukoz ayrıca proteoglikanlar, glikoproteinler ve glikolipidler gibi bileşiklere de çevrilir. Glukoz hücrelere girdiği zaman, çeşitli metabolik yollarda önemli bir bileşik olan glukoz 6-fosfata çevrilir. - Glukoz 6-fosfatın girdiği başlıca metabolik yol glikolizdir. Bu yolda piruvat üretilir ve NADH ve ATP elde edilir. - Glukoz 6-fosfat, glukoz 1-fosfata ve sonra UDP-glukoza çevrilerek glikojen veya proteoglikanlar gibi bileşiklerin sentezinde kullanılır. - Glukoz 6-fosfat, pentoz-fosfat yoluna da girerek NADPH (yağ asitlerinin biyosentezi gibi reaksiyonlarda kullanılır) ve riboz (nükleotid sentezinde kullanılır) üretir. Fruktoz ve galaktoz, glukozun metabolize olduğu yollardaki ara maddelere çevrilir. Glikojen hayvanlardaki karbonhidratların başlıca depo şeklidir. En büyük depolar kas ve karaciğerde bulunur. Kas glikojeni, kas kasılması için ATP elde etmede kullanılır. Karaciğer glikojeni, açlık veya egzersiz esnasında kan glukozunu korumada kullanılır. Kan glukozunun korunması karaciğerin başlıca görevidir. - Karaciğer, glikojenoliz veya glukoneogenezle kan glukozunu korur. KARBONHĐDRAT YAPISI 34
35 35 Fruktoz: Bir ketoheksozdur. Glukoz, galaktoz, mannoz: Bir aldoheksozdur. Đzomer: Kapalı formülleri aynı, açık formülleri farklı olan bileşiklerdir. Örn. Glukoz-fruktoz Epimer: Sadece bir asimetrik karbonundaki hidroksil grubunun pozisyonunun farklı olduğu stereoizomerlerdir. Örn. Glukoz-galaktoz Bir monosakkaridde anomerik karbon hangisidir? En fazla okside olabilen karbon atomuna anomerik karbon denir. Bir monosakkaridde alde-hid veya keton grubuna ait karbon anomeriktir. Bir monosakkaridde indirgeyici karbon: anomerik karbon Monosakkaridlerin birbirlerine bağlanması: hidroksil grupları aracılığı ile gerçekleşir. Monosakkaridler proteinlere hangi amino asitler üzerinden bağlanırlar: serin, treonin, asparagin 35
36 36 Glukuronik asit: Glukozun 6. karbonunun karboksilik asite oksidasyonu ile oluşur. Konjugasyon reaksiyonlarında ve glikozaminoglikanların yapısında yer alır. Sorbitol: Glukozun birinci karbonunun redüksiyonu ile oluşur. Đndirgeyici şekerler: tüm monosakkaridler, maltoz, laktoz Đndirgeyici olmayan şekerler Sorbitol Galaktitol Sükroz Trehaloz (glukoz α1-1 glukoz) 36
37 37 KARBONHĐDRATLARIN SĐNDĐRĐMĐ Nişastanın sindirimi sonucu mideye ulaşan başlıca ürün: dekstrinler (lineer veya dallı oligosakkaridler) 37
38 38 Glukozun sodyumla beraber hücre içine alındığı dokular: ince bağırsak ve böbrekler 38
39 39 GLĐKOLĐZ Glukozun aktif transportu, bir kardiyak glikozid olan ouabain (sodyum pompa inhibitörü) ve florhizin (böbrek tübüllerinde glukoz reabsorpsiyon inhibitörü) tarafından inhibe edilir. Glikoliz, glukozun piruvata çevrildiği yoldur. Vücudun tüm hücrelerinde, sitozolde gerçekleşir. Başlangıç reaksiyonlarında, bir heksoz ATP tarafından iki kez fosforillenir ve sonra iki trioz fosfata parçalanır. - Glukoz, glukoz 6-fosfata fosforillenir; bu da fruktoz 6-fosfata izomerize olur. - Fruktoz 6-fosfat, anahtar düzenleyici enzim olan fosfofruktokinaz tarafından fosforillenir. Ürün, fruktoz 1,6- bifosfat olup iki adet trioz fosfata parçalanır. Reaksiyonların ikinci bölümünde, trioz fosfatlar ATP yi oluşturur. Glikoliz sonunda ATP, NADH ve piruvat üretilir. - ATP, fosfogliserat kinaz ve piruvat kinaz tarafından katalizlenen reaksiyonlarla elde edilir. - Sitozolde üretilen NADH, doğrudan mitokondri içine giremez; bu indirgeyici eşdeğerler bir takım şant mekanizmalarıyla ATP nin elde edileceği mitokondri içine taşınırlar. - Piruvat mitokondri içine girebilir ve trikarboksilik asit (TCA) döngüsünde okside olarak ilave ATP elde edilir. - Piruvat ayrıca oksaloasetata çevrilerek TCA döngüsü ara maddelerini besler veya laktata indirgenebilir veya alanine transamine olabilir. Đnsülin GLUT4 ün sentezini uyarır. Glukoza en fazla duyarlı olan glukoz taşıyıcısı GLUT3 tür. Doku Glukoz taşıyıcıları Fonksiyonları Kolaylaştırılmış çift yönlü taşıyıcılar GLUT1 Beyin, böbrek, kolon, plasenta, eritrosit Glukoz uptake i GLUT2 Karaciğer, pankreas B hücresi, ince bağırsak, Glukozun hızlı uptake i ve salınımı böbrek GLUT3 Beyin, böbrek, plasenta Glukoz uptake i GLUT4 Kalp ve iskelet kası, yağ dokusu Glukozun insülinle uyarılmış uptake i GLUT5 Đnce bağırsak Glukoz absorpsiyonu Sodyum a bağımlı tek yönlü taşıyıcı SGLT1 Đnce bağırsak ve böbrek Bağırsak lümeninden glukozun aktif uptake i, böbreğin proksimal tübülünde konsantrasyon gradientine karşı glukozun reabsorpsiyonu 39
40 40 Glikolizde inorganik fosfatın kullanıldığı tek basamak: gliseraldehid 3-fosfat dehidrogenaz Glikolizde oksidasyon ve fosforilasyonun olduğu basamak: Gliseraldehid 3-fosfat dehidrogenaz Glikolitik yolun enzim inhibitörleri: iyodoasetat gliseraldehid 3-fosfat dehidrogenazı, fluorid enolazı inhibe ederler. 40
41 41 41
42 42 Fosfofruktokinaz 1 i aktive edenler: karaciğerde fruktoz-2,6 bifosfat, kasta AMP Fosfofruktokinaz 1 i inhibe edenler: karaciğerde glukagon, kasta ATP, sitrat, düşük ph Piruvat kinazı inhibe eden amino asit: alanin Karaciğerde glikoliz: Toklukta gerçekleşir, her üç basamak insülin tarafından aktive edilir. Bir molekülde fosfat gruplarının yerini değiştiren enzim: mutazlar (örneğin: fosfogliserat mutaz) Kinaz grubu enzimlerinden tepkime sırasında her zaman ATP sentezini sağlayan: piruvat kinaz Fosfofruktokinaz 2 ile ilgili bilgiler: karaciğerde insülin tarafından aktive edilir, fruktoz-2,6-p oluşturur, bu son bileşik fosfofruktokinaz 1 i aktive eder. Glikoliz sonunda oluşan piruvat tek bir reaksiyonla hangi bileşiklere dönüşür? Alanin, laktat, oksaloasetat, asetil KoA Glukozun her durumda tamamen okside olduğu tek doku: beyin Eritrositlerde glikoliz sonunda net üretilen bileşikler: 2 ATP, 2 laktat Anaerobik glikoliz sonunda net üretilen bileşikler: 2 ATP, 2 laktat 42
43 43 Bir mol glukozun beyinde asetil KoA ya kadar yıkımı sonunda net ATP kazancı ne kadardır? 12 mol ATP Glikolizde stoplazmada üretilen NADH lar mitokondriye ne şekilde geçer? Gliserol fosfat veya malat-aspartat şantı ile Gliserol fosfat şantını kullanan dokular: beyin ve iskelet kası Malat-aspartat şantını kullanan dokular: karaciğer, böbrek, kalp kası Bir mol glukozdan elde edilen ATP miktarı Metabolik yol Reaksiyonu katalizleyen enzim ATP üretim yeri Oluşan ATP (mol) Glikoliz Sitrik asit döngüsü Gliseraldehid 3-P dehidrogenaz 2 NADH nın solunum zincirinde oksidasyonu 4 veya 6 Fosfogliserat kinaz Substrat düzeyinde fosforilasyon 2 Piruvat kinaz Substrat düzeyinde fosforilasyon 2 Heksokinaz ve fosforuktokinaz reaksiyonlarında harcanan ATP -2 Piruvat dehidrogenaz 2 NADH nın solunum zincirinde oksidasyonu 6 Đzositrat dehidrogenaz 2 NADH nın solunum zincirinde oksidasyonu 6 alfa- ketoglutarat dehidrogenaz 2 NADH nın solunum zincirinde oksidasyonu 6 Süksinat tiokinaz Substrat düzeyinde fosforilasyon 2 Süksinat dehidrogenaz 2 FADH2 nın solunum zincirinde oksidasyonu 4 Net 6 veya 8 Malat dehidrogenaz 2 NADH nın solunum zincirinde oksidasyonu 6 Net 30 43
44 44 TCA DÖNGÜSÜ Hangisi trikarboksilik asittir? Sitrat Trikarboksilik asit (TCA) döngüsü, (sitrik asit döngüsü veya Krebs döngüsü olarak da bilinir) vücutta başlıca enerji üreten yoldur. Döngü mitokondride gerçekleşir. Besin maddeleri asetil KoA ya dönüşerek döngüyü besler ve enerji için okside olur. Döngü ayrıca amino asitlerin, yağ asitlerinin ve glukozun sentezinde de fonksiyon görür. Döngü 4-karbonlu bileşik olan oksaloasetat ile başlar, asetil KoA dan iki karbon ilave olur, CO2 halinde iki karbon dışarı çıkar ve 4-karbonlu oksaloasetat tekrar oluşur. Elektronlar döngü tarafından NAD+ ve FAD ye aktarılır. Elektronlar, elektron transport zinciri ile O2 ye aktarıldıkça oksidatif fosforilasyon işlemi tarafından ATP meydana gelir. ATP ayrıca döngünün bir reaksiyonunda substrat düzeyinde fosforilasyonla GTP den elde edilir. Döngünün reaksiyonları ikisi hariç reverzıbldır. TCA döngüsündeki irreverzibl basamaklar - Sitrat sentaz - Alfa-ketoglutarat dehidrogenaz TCA döngüsünde yüksek enerjili bileşiğin üretildiği basamak: alfa-ketoglutarat dehidrogenaz TCA döngüsünde substrat düzeyinde fosforilasyonun gerçekleştiği basamak: süksinat tiokinaz 44
45 45 TCA döngüsünde ilk oksidatif dekarboksilasyonun gerçekleştiği basamak: izositrat dehidrogenaz TCA döngüsü inhibitörleri: Akonitaz enzimini fluoroasetat, alfa-ketoglutarat dehidrogenaz enzimini arsenit, süksinat dehidrogenaz enzimini yarışmalı olarak malonat inhibe eder. TCA döngüsünde net su girişinin olduğu iki basamak: sitrat sentaz, fumaraz TCA döngüsünün kontrolü başlıca: sitrat sentaz enzimi ile gerçekleştirilir. TCA döngüsünü aktive edenler: NAD+ ADP, Ca++ TCA döngüsünü inhibe edenler Sitrat NADH ATP Süksinil KoA 45
46 46 46
47 47 Piruvat dehidrogenaz enziminin kofaktörleri: tiamin pirofosfat, lipoik asit, koenzim A, FAD, NAD+ Piruvat dehidrogenaz enziminin katalizlediği reaksiyon: Piruvat + NAD+ asetil KoA + NADH + H+ +CO2 Piruvat dehidrogenaz enzimini inhibe edenler: Asetil KoA, ATP, NADH 47
48 48 Glikojen sentezinde rol oynayan nükleotid: üridin nükleotidleri 48
49 49 Glikojen sentezinde rol oynayan enzimler: Glikojen sentaz, dallandırıcı enzim (amilo-4:6 transglikozidaz) Glikojen yıkımında rol oynayan enzimler: fosforilaz, dal koparıcı enzim Fosforilaz enziminin etkisi ile açığa çıkan glikojenin yıkım ürünü: glukoz 1-fosfat Glikojen molekülünün yıkımı ile açığa çıkan karbonhidrat birimleri: glukoz 1-fosfat (başlıca), serbest glukoz Glukagonun reseptörüne bağlanması ile ilk aktive olan enzim: adenilat siklaz camp nin aktive ettiği enzim: protein kinaz A Kas dokusunda glikojenin yıkımında rol oynayan Ca++-kalmodulin kompleksinin aktive ettiği enzim: fosforilaz kinaz b Kas dokusunda glikojenin yıkımında rol oynayan AMP nin aktive ettiği enzim: fosforilaz b Glikojen depo hastalıkları: Glikojen depo hastalıklarında, glikojen başlıca karaciğer veya kasta veya her ikisinde birikir. Enzim yetersizlikleri başlıca glikojen yıkımında veya glukoza dönüşümünde gözlenir. Karaciğer ve kasta enzimlerin farklı formları (izozimler) oluştuğu için, bir doku etkilenirken diğeri etkilenmeyebilir. Karaciğerde glikojen depo hastalıkları hepatomegaliye ve hafif hipoglisemiden karaciğer yetmezliğine kadar değişen bozukluklara neden olabilir. Kasta, devamlı egzersiz yapmadaki zorluktan kardiyo-respiratuar yetmezliğe kadar değişen derecelerde bozukluklara neden olur. 49
50 50 Glikojen depo hastalıkları Tip Etkilenen Enzim Özellikleri I Glukoz 6-fosfataz (von Gierke hastalığı) Karaciğer ve renal tübül hücreleri glikojenle doludur. Hipoglisemi, laktik asidemi, hiperürisemi, ketozis, hiperlipemi, taş bebek yüzü görünümü II Lizozomal alfa-glukozidaz (Pompe hastalığı) Fatal, lizozomlarda glikojen birikimi, kalp yetmezliği III IV V Amilo 1,6-glukozidaz (dal koparıcı) (Forbes veya Cori hastalığı) Amilo 4,6-transglukozidaz (dallandırıcı enzim) (Andersen hastalığı) Kas glikojen fosforilaz (McArdle hastalığı) Dallı polisakkarid birikimi Az dallı polisakkarid birikimi. Đlk yılda kalp veya karaciğer yetmezliğine bağlı ölüm Egzersiz toleransında azalma, kas glikojen miktarında artma, egzersiz sonrası kan laktatında azalma VI Karaciğer glikojen fosforilaz (Hers hastalığı) Karaciğer glikojen miktarında artma, hipoglisemi VII Kas-eritrosit fosfofruktokinaz (Tarui hastalığı) Tip V gibi, ayrıca hemolitik anemi VIII Fosforilaz kinaz Tip VI gibi Đnsülinin karaciğerde aktive ve inhibe ettiği enzimler sırasıyla: Glikojen sentaz ve fosforilaz 50
51 51 GLUKONEOGENEZ Glukoneogenez, karbonhidrat dışı bileşiklerden glukozun sentezidir ve başlıca karaciğer ve böbrekte meydana gelir. Glukoneogenez için başlıca prekürsörler; laktat, amino asitler (piruvat veya TCA döngüsü ara maddelerini oluşturan bileşikler), propionat (tek karbon sayılı yağ asitlerinden oluşur) ve gliseroldür (dihidroksiaseton fosfatı oluşturur). Çift karbon sayılı yağ asitleri glukoz üretmez. Glukoneogenez, glikolizde olmayan birkaç enzimatik basamak içerir; böylece glukoz, glikolizin basitçe tersine işlemesiyle elde edilmez. Piruvat karboksilaz mitokondride piruvatı, oksaloasetata çevirir. Oksaloasetat, sitozole geçen malat veya aspartata çevrilir ve sitozolde tekrar oksaloasetata çevrilir. Fosfoenolpiruvat karboksikinaz, oksaloasetatı fosfoenolpiruvata çevirir. Fosfoenolpiruvat glikoliz reaksiyonlarının tersine işlemesiyle fruktoz 1,6-bifosfata dönüşür. Fruktoz 1,6-bifosfataz, fruktoz 1,6-bifosfatı fruktoz 6-fosfata çevirir. Fruktoz 6-fosfat ise glukoz 6-fosfata çevrilir. Glukoz 6-fosfataz, glukoz 6-fosfatı kana salınan serbest glukoza çevirir. Glukoneogenez; piruvat dehidrogenaz, piruvat kinaz, fosfofruktokinaz 1 ve glukokinazın nispeten inaktif olduğu durumlarda oluşur. Bu enzimlerin düşük aktiviteleri yararlı olmayan döngülerin oluşumunu önler ve sonuçta piruvat, glukoza dönüşür. Đki mol piruvattan 1 mol glukozun sentezi için yaklaşık 6 mol ATP eşdeğerinde enerji gerekir. Glukoneogenez bölgeleri: Karaciğer ve böbrek 51
52 52 Glukoneogenez enzimleri Piruvat karboksilaz Fosfoenolpiruvat karboksikinaz Fruktoz 1,6-bifosfataz Glukoz 6-fosfataz Glukoneogenez kaynakları: Amino asitler (başlıca alanin), laktat, gliserol, propionat Laktat veya alaninden bir mol glukoz sentezi için gereken ATP miktarı: 6 mol ATP Glukagon ve kortizol tarafından sentezi indüklenen glukoneogenez enzimi: fosfoenolpiruvat karboksikinaz enzimi Karaciğerde glukoneogenez için gereken enerji nereden karşılanır? Yağ asitlerinin beta-oksidasyonundan Açlığın 24. saatinde kana glukoz sağlayan başlıca kaynak: glukoneogenez (kas dokusu proteinlerinden açığa çıkan amino asitler) Glukoz 6-fosfatın glukoza dönüştüğü organel: endoplazmik retikulum 52
53 53 53
54 54 Đnorganik fosfatın organik bir molekülün yapısına enzimatik olarak katılımı hangi metabolik yollarda gözlenir? Glikojen yıkımı Glikoliz ETZ ve oksidatif fosforilasyon Krebs döngüsü Propionil KoA nın metilmalonil KoA ya dönüşümü için gerekli koenzimler: biotin ve adenozil kobalamin PENTOZ FOSFAT YOLU (HEKSOZ MONOFOSFAT ŞANTI) Glukoz enerji üretimi için okside olabilmekte ayrıca pentoz fosfat yolu (PFY) gibi şeker metabolizmasını ilgilendiren bir yola da girebilmektedir. PFY iki aşamada gerçekleşir. Yolun irreverzibl oksidatif reaksiyonlarında, glukoz 6-fosfatın bir karbonu CO2 halinde serbestleşir; NADPH oluşur; ve ribuloz 5-fosfat üretilir. - NADPH, indirgeyici biyosentezlerde (özellikle yağ asitlerinin) ve oksidatif hasara karşı korunmada (örn. glutatyonun indirgenmesi) kullanılır. - Ribuloz 5-fosfat, nükleotid biyosentezi için riboz 5-fosfatı sağlar veya yolun oksidatif olmayan bölümüne giren pentoz fosfatları üretir. Reverzibl, oksidatif olmayan reaksiyonlarda ribuloz 5-fosfattan üretilen pentoz fosfatlar, glikolitik ara maddeler olan fruktoz 6-fosfat ve gliseraldehid 3-fosfata çevrilirler. Oksidatif olmayan reaksiyonlar reverzibl olduğu için nükleotid sentezi için glikolizin ara maddelerinden riboz 5-fosfatı elde etmek için kullanılabilirler. Pentoz fosfat yolunda üretilen bileşikler: NADPH ve riboz 5-fosfat Pentoz fosfat yolunda oksidatif ve oksidatif olmayan yolda üretilen bileşik: ribuloz 5-fosfat 54
55 55 Glukoz 6-fosfat dehidrogenaz enzimini aktive edenler: NADP+ fazlalığı ve insülin Glukoz 6-fosfat dehidrogenaz enzimini inhibe edenler: NADPH fazlalığı NADPH kullanım alanları: Sentez reaksiyonları, glutatyonun indirgenmesi, sitokrom P-450 sistemi, nötrofillerin bakterileri fagositozu esnasında, poliol yolu Psödopeptid örneği: glutatyon (gama-glutamil-sisteinil-glisin). Psödopeptid alfa pozisyonunun dışındaki diğer pozisyonlarda bulunan karboksil grubu ile amino grubu arasında oluşan peptid bağıdır. Glutatyondaki (G-SH) fonksiyonel grup: sülfidril grup (SH) Eritositleri hemolizden koruyan enzimler: Glukoz 6-fosfat dehidrogenaz, glutatyon redüktaz, glutatyon peroksidaz 55
56 56 56
57 57 Glutatyon redüktaz enziminin kofaktörü: FAD FRUKTOZ VE GALAKTOZ METABOLĐZMASI Glukoz diyetten türeyen en bol monosakkarid olmakla beraber, fruktoz ve galaktoz da başlıca sükroz ve laktozdan olmak üzere önemli miktarlarda elde edilir. Fruktoz ve galaktoz hücrelere girdikten sonra 1. karbonları fosforillenir ve glukoz metabolizmasının yollarındaki ara maddelere çevrilir. Fruktoz başlıca karaciğerde metabolize olur. Önce fruktoz 1-fosfata fosforillenir ve sonra gliseraldehid 3-fosfata fosforillenen gliseraldehide ve dihidroksiaseton fosfata parçalanır. Bu iki trioz fosfat, glikolizin ara maddeleridir. Fruktoz, sorbitolden elde edilebilir. Sorbitol ise glukozdan oluşur. Galaktoz, UDP-glukozla reaksiyona giren galaktoz 1-fosfata fosforillenir. Ürünler, glukoz 1- fosfat ve UDPgalaktozdur. UDP-galaktoz ise UDP-glukoza epimerize olur. Galaktozun glukoz parçacıklarına dönüşümü sonucu oluşan glukoz 1-fosfat ve UDP-glukoz, glukoz metabolizmasındaki ara maddelerdir. - UDP-galaktoz; glikoproteinlerin, glikolipidlerin ve proteoglikanların sentezinde kullanılır. - UDP-galaktoz meme bezinde glukozla reaksiyona girerek süt şekeri laktozu oluşturur. Galaktoz, galaktitole indirgenebilir. Riboflavin (B2 vitamini) eksikliğini araştırmada kullanılan enzim aktivitesi: eritrosit glutatyon redüktaz aktivitesi Herediter fruktoz intoleransında (aldolaz B eksikliği): sarılık ve hipoglisemi gelişir. 57
58 58 Glukozdan fruktoz oluşumunun gerçekleştiği metabolik yol: poliol yolu Aldoz redüktaz enziminin (glukozu sorbitole çevirir) bulunmadığı doku: karaciğer 58
59 59 Fruktozdan zengin diyetle beslenenlerde: hiperlipidemi ve hiperürisemi gelişir. Katarakta neden olan enzim eksiklikleri: galaktokinaz ve galaktoz 1-fosfat üridiltransferaz Klasik galaktozemide (üridiltransferaz eksikliği) görülenler: mental retardasyon, karaciğer hücre hasarı, katarakt, fankoni sendromu, hipoglisemi Galaktozdan sentezlenen bileşikler Laktoz Glikoproteinler Glikolipidler Glikozaminoglikanlar Not: Bu bileşiklerin sentezinde üridin nükleotidleri görev alır UDP-glukoz ve UDP-galaktozu birbirine dönüştüren enzim: epimeraz 59
60 60 Laktoz sentezinde görevli olan galaktozil transferaz enzimini aktive eden protein: alfa-laktalbumin PROTEOGLĐKANLAR, GLĐKOPROTEĐNLER VE GLĐKOLĐPĐDLER Proteoglikanlar, bir merkezi proteine bağlı uzun, lineer glikozaminoglikan zincirlerinden oluşmuştur. Her bir glikozaminoglikan zinciri genellikle negatif yüklü ve bir heksozamin ve bir üronik asit içeren tekrarlayan disakkarid birimlerinden oluşmuştur. Sülfat grupları sıklıkla bulunur. - Glikozaminoglikanlar, (eski adıyla mukopolisakkaritler), UDP-şekerlerden sentezlenirler. Glikoproteinler, genellikle dallı olan daha küçük polisakkarid zincirlerinden oluşmuştur. - Glikoproteinler glukoz, galaktoz ve bunların amino türevlerine ilave olarak mannoz, L- fukoz ve asetilnöraminik asit (NANA) içerir. - O-bağlı zincirlerde polisakkarid, UDP-şekerlerden bir proteindeki serin veya treonin artığına monosakkarid birimleri arka arkaya ilave oldukça büyür. - N-bağlı zincirlerde, dolikol fosfat üzerinde dallı karbonhidratlar sentezlenir ve bir proteindeki asparagin artığının amid azotuna aktarılır. Glikolipidler, sfingolipid sınıfının üyeleridir. - Karbonhidrat bölümü, seramidin hidroksimetil grubuna ve sonra zincirin indirgeyici olmayan ucuna eklenen UDP-şekerlerden sentezlenir. - N-Asetilnöraminik asit (CMP-NANA dan türemiştir) ana zincirden sıklıkla dallar oluşturur. Proteoglikanlar, glikoproteinler ve glikolipidler, endoplazmik retikulum ve golgi kompleksinde sentezlenirler; lizozomların etkisiyle yıkılırlar. Glikozaminoglikanların yapısı: amino şeker (glukozamin veya galaktozamin) ve asidik şekerden (glukuronik asit veya L-iduronik asit) oluşan tekrarlayan disakkarid birimleri Proteoglikanların yapısı: Bir proteine bağlı onlarca glikozaminoglikan birimlerinden oluşur. Proteoglikanların bulunduğu dokular: deri, kıkırdak, tendon, ligament, aorta, kornea, sinovyal sıvı, kan damarları, kalp kapakçıkları, bazal membran, mast hücreleri 60
61 61 Vücutta en bol bulunan glikozaminoglikan: kondroidin sülfat Üronik asit (asidik şeker) içermeyen GAG: keratan sülfat Sülfat içermeyen GAG: hyaluronik asit Hücre içi yerleşim gösteren ve lipid temizleyici GAG: heparin Hücre yüzeyinin bileşeni olan ve lipoprotein lipazı bağlayan GAG: heparan sülfat Aminoşekerlerin prekürsörü: glukoz N-asetilnöraminik asit (siyalik asit) içeren bileşikler: glikoprotein ve gangliozid 61
62 62 62
63 63 Asidik şekerlerin prekürsörü: glukoz Esansiyel pentozüride idrarla atılan bileşik: L-ksiluloz Mukopolisakkaridozlar hangi bileşiğin yıkımındaki bir problem sonucu gelişir? Glikozaminoglikanlar 63
64 64 Mukopolisakkaridozlar Proteoglikanlardaki oligosakkaridlerin aşırı toplanması ve ekskresyonu ile karakterize bir grup genetik hastalıktır doğumda bir gözlenir. Dermatan sülfat, heparan sülfat, kondroidin sülfat ve keratan sülfatın yıkımı etkilenmiştir. a. Glikozaminoglikanların yıkımından sorumlu bir veya daha fazla lizozomal enzimin yetersizliği söz konusudur. b. Hurler (Alfa-L-iduronidaz eksikliği) ve Sanfilippo s sendromları otozomal resesif, Hunter (iduronat sülfataz eksikliği) sendromu X e bağlı geçiş gösterir. c. Hurler sendromu korneal bulanıklık, mental retardasyon, iskelet bozuklukları (kısa boy) ve kaba yüz görünümü ile karakterizedir. Hunter sendromunda ise korneal bulanıklık yoktur fakat fiziksel deformiteler ve mental retardasyon gözlenir. d. Sanfilippo sendromu (tip III a) heparan sülfataz eksikliği ile karakterizedir. Fiziksel defektler nispeten hafif, mental retardasyon ağırdır. Glikoproteinlerin yapısı: Proteine dallı oligosakkaridlerin eklenmesi ile oluşur. Glikoproteinlerin bulunduğu yerler: tüm plazma proteinleri (albümin hariç), hormonlar (TSH, FSH, LH, hcg), lizozomal enzimler, hücre membran proteinleri, antikorlar, kan grubu belirleyicileri, hücre dışı sıvı Glikoproteinlerin karbonhidrat kısmında yer alanlar Amino şekerler Mannoz Galaktoz L-fukoz NANA (fruktoz bulunmaz) Tunikamisin N-bağlı glikoproteinlerde glikozilasyonu inhibe eder. Glikoproteinlerin sentez bölgesi: GER Dolikol ün görevi: N-bağlı glikoprotein sentezinde karbonhidrat birimlerinin GER de proteine aktarılması Glikozilasyon bölgeleri: GER ve golgi l-cell hastalığında lizozomlara gönderilecek enzimlerdeki mannoz artıkları fosforillenememekte ve sonuçta bu proteinler lizozomal vezikül içine değil hücre dışına çıkmaktadır. l-cell hastalığı iskelet bozuklukları, eklem hareketlerinde kısıtlılık, kaba yüz görünümü ve ağır psikomotor bozukluklar ile karakterizedir; genellikle 8 yaş civarında ölümle sonuçlanır. 64
65 65 KAN GLUKOZ DÜZEYLERĐNĐN KORUNMASI Kan glukoz düzeyleri, diyetin yapısı çok değişken olmasına ve normal kişinin öğünler arası ve gece yediği yemeklere rağmen çok dar aralıklarda tutulur. Bir kişi uzun süre aç dahi kalsa kan glukoz düzeyleri çok az azalır. Kan glukozunu düzenleyen başlıca hormonlar insülin ve glukagondur. Yemekten sonra, kan glukozu diyetle alınan karbonhidratlardan sağlanır. Açlıkta, karaciğer glikojenoliz ve glukoneogenez işlemleriyle kan glukoz düzeylerini korur. - Açlığın ilk birkaç saatinde, glikojenoliz kan glukoz düzeylerinin korunmasında başlıca role sahiptir. - Açlık ilerledikçe ve glikojen depoları azaldıkça, glukoneogenez kan glukozunun önemli, ek bir kaynağı haline gelir saat açlıktan sonra karaciğer glikojen depoları boşalınca, glukoneogenez kan glukozunun tek kaynağı olur. Tüm hücreler enerji için glukozu kullanırlar; açlıkta glukoz üretimi özellikle beyin ve eritrosit gibi dokular için önemlidir. Egzersiz esnasında, kan glukozu karaciğer glikojenoliz ve glukoneogenez yoluyla da korunur. 65
66 66 LĐPĐD METABOLĐZMASI * Lipidler, suda çözünmeyen bir grup heterojen bileşiktir. * Membranlar lipid içerirler; özellikle de fosfogliseroller (başlıca membran lipididir), sfingolipidler ve kolesterol. * Triaçilgliseroller diyetle elde edilir veya karaciğerde sentezlenir, vücudun başlıca enerji kaynağıdır. Kanda lipoproteinler halinde taşınır ve yağ dokusunda depolanır. * Başlıca lipoproteinler: Şilomikronlar Çok düşük dansiteli lipoproteinler (VLDL) Düşük dansiteli lipoproteinler (LDL) Yüksek dansiteli lipoproteinler (HDL) * Şilomikronlar, diyetle alınan lipidlerden bağırsakta sentezlenirler; VLDL ise karaciğerde başlıca diyetle alınan karbonhidratlardan sentezlenir. * Şilomikron ve VLDL deki triaçilgliseroller kanda lipoprotein lipaz tarafından yağ asitleri ve gliserole hidroliz olur. Yağ dokusunda, yağ asitleri triaçilgliserole çevrilir ve depolanır. IDL (ara dansiteli lipoprotein), VLDL deki bir kısım triaçilgliserolün sindiriminden sonra oluşan VLDL kalıntısıdır. IDL ya karaciğer hücreleri tarafından endositoz yoluyla alınır ve lizozomal enzimlerce sindirilir veya içindeki triaçilgliseroller kanda daha fazla yıkılarak LDL ye çevrilir. LDL, karaciğer ve periferal dokular tarafından endositozla alınır ve lizozomda sindirilir. Şilomikron kalıntıları karaciğer tarafından endositozla alınır. * Kolesterol kanda lipoproteinlerin bir bileşeni olarak taşınır. Kolesterol vücudun bir çok hücresinde sentezlenir. Anahtar düzenleyici enzim HMG KoA redüktazdır. Kolesterol hücre zarlarının bir bileşenidir. Kolesterol, karaciğerde safra tuzlarına dönüşür ve endokrin dokularda steroid hormonları oluşturur. * HDL, proteinleri (lipoprotein lipazın bir aktivatörü olan apo C dahil) şilomikronlara ve VLDL ye transfer eder. HDL ayrıca periferal dokulardan ve kanda dolaşan diğer lipoproteinlerden kolesterolü toplar. Bu kolesterol sonuçta karaciğere geri döner. * Açlık esnasında, yağ asitleri (yağ dokusu triaçilgliserol depolarından köken alan) enerji üretmek üzere okside olur. Karaciğerde yağ asitleri, kas ve böbrek gibi dokularda okside olabilen keton cisimlerine çevrilir. * Eikozanoidler (prostaglandinler, tromboksanlar, lökotrienler ve lipoksinler) poliansatüre yağ asitlerinden köken alırlar. 66
67 67 LĐPĐDLERĐN SINIFLANDIRILMASI 1. Basit lipidler: Çeşitli alkollerle yağ asitlerinin esterleridir. a. Yağlar: Yağ asitlerinin gliserolle esterleridir. b. Mumlar: Daha yüksek molekül ağırlıklı monohidrid alkollerle yağ asitlerinin esterleridir. 2. Kompleks lipidler: Bir alkol ve bir yağ asitine ilave olarak başka gruplar da içeren yağ asiti esterleridir. a. Fosfolipidler: Yağ asitleri ve bir alkole ilave olarak bir fosforik asit artığı içerirler. Örneğin, gliserofosfolipidlerde alkol, gliseroldür ve sfingolipidlerde alkol, sfingozindir. b. Glikolipidler (glikosfingolipidler): Bir yağ asiti, sfingozin ve karbonhidrat içeren lipidlerdir. c. Diğer kompleks lipidler: Sülfolipidler, aminolipidler ve lipoproteinler bu grupta yer alır. 67
68 68 3. Lipid prekürsörleri ve türevleri: a. Lipid prekürsörleri: Yağ asitleri, gliserol, steroidler, gliserol ve sterollere ilave olarak diğer alkoller, yağ aldehidleri b. Lipid türevleri: Keton cisimleri, hidrokarbonlar, yağda çözünen vitaminler ve hormonlar. Not: Yüksüz oldukları için açilgliseroller (gliseridler), kolesterol ve kolesterol esterleri nötral lipidler olarak adlandırılır. LĐPĐDLERĐN YAPISI Lipidler çeşitli yapılara sahiptir fakat ortak özellikleri suda çözünmez oluşlarıdır. Yağ asitleri alifatik karboksilik asitlerdir. Serbest halde veya gliserol ile esterleşmiş halde bulunurlar Triaçilgliseroller (trigliseridler) yağların başlıca depo şeklidir. Fosfolipidler, iki ana gruba ayrılır: 1. Fosfoaçilgliseroller (gliserofosfolipidler): Bu bileşikler fosfatidik asit türevleridir. Gliserofosfolipidlerin prekürsörü: fosfatidik asit 68
69 69 Mitokondri membranlarında bulunan başlıca fosfolipid: kardiyolipin Sfingolipidler, seramid molekülüne çeşitli grupların bağlandığı bileşikleridir. - Seramid, yağ asiti ve sfingozinin birleşimidir ve glikosfingolipidlerin de yapısında bulunur. Lesitinin parçalanması ile açığa çıkanlar: gliserol, fosforik asit, yağ asitleri, kolin Fosforik asit içeren tek sfingolipid: sfingomyelin Seramidin görevleri: Endoplazmik retikulumda serinden sentezlenir, önemli bir ikincil haberci moleküldür; programlı hücre ölümü (apoptozis), hücre siklusu ve hücre farklılaşması, ve yaşlanma dahil çeşitli yolların regülasyonunda görev alır. Gangliozidin hidrolizi ile serbestleşenler: seramid (sfingozin + yağ asiti), glukoz, galaktoz, aminoşekerler, NANA 69
70 70 Sfingomyelinin parçalanması ile açığa çıkanlar Sfingozin (serin + palmitat) Yağ asiti Fosforik asit ve kolin Glikolipidlerin prekürsörü: Seramid 70
71 71 Kolesterolde 3 adet 6 karbonlu bir halka yapısı bulunur. Çeşitli lipid bileşenlerini birbirinden ayıran yöntem: ince tabaka kromatografisi Yağ asitlerini birbirinden ayıran yöntem: gaz-likid kromatografisi Hücre zarı lipid ve proteinden oluşmuştur. MEMBRANLAR Proteinler; hormonlar gibi hücre dışındaki bileşiklerin hücre içindeki etkilerini gerçekleştirebilmeleri için taşıyıcı, enzim, reseptör ve mediatör olarak fonksiyon görürler. Hücre membranında yer alan bileşikler Fosfolipidler Kolesterol Proteinler Glikoproteinler Glikolipidler 71
72 72 Hücre membranında yer almayanlar Triaçilgliseroller Kolesterol esteri Serbest yağ asitleri Hücre membranında bulunan proteinlerin görevleri Reseptör Mediatör Enzim Transport Lipidlerin sindiriminin başladığı bölge: mide DĐYETLE ALINAN TRĐAÇĐLGLĐSEROLLERĐN SĐNDĐRĐMĐ Diyetle alınan başlıca yağ türü triaçilgliserol olup bitkisel ve hayvansal besinlerdeki yağ depolarından elde edilir. Lingual lipaz dilin dorsal yüzeyinden, gastrik lipaz mideden salgılanır. Lingual ve gastrik lipaz kısa ve orta zincirli yağ asiti içeren triaçilgliserolleri parçalayarak lipid sindirimini midede başlatır. Bu enzimlerin optimum ph sı dır ve açığa çıkan kısa ve orta zincirli yağ asitleri mide duvarından absorbe olarak portal dolaşıma geçer. Mideden asit içeriğin (kimus), kısmen sindirilmiş lipid ve proteinlerin duodenuma geçmesi duodenumdan sekretin ve kolesistokinin (CCK) sekresyonuna yol açar. Sekretin pankreastan bikarbonat salınımını, CCK ise safra kesesinden safra ve pankreastan sindirim enzimlerinin sekresyonunu uyarır. Mideden absorbe olan besin maddeleri: kısa ve orta zincirli yağ asitleri Midede düşük ph da etkili olan lipazlar: lingual lipaz, gastrik lipaz Pankreatik lipazın triaçilgliserolü parçalaması ile açığa çıkan son yıkım ürünleri: yağ asitleri ve 2-monoaçil gliserol Yeni sentezlenmiş şilomikron ve VLDL nin metabolize edilmediği doku: karaciğer Trigliseridden zengin HDL ve VLDL kalıntılarının birikmesi ile karakterize enzim eksikliği: hepatik lipaz Lipogenezden (yağ asiti sentezi) sorumlu enzim: asetil KoA karboksilaz Yağ asiti sentezinde indirgeyici eşdeğerlerin geldiği koenzim: NADPH NADPH kaynakları: pentoz fosfat yolu, malik enzim 72
73 73 Lipazlara ait özet bilgiler Enzim Kaynak Etki Bölgesi Fonksiyon Özellikleri Lingual lipaz Ağız Mide Kısa-orta zincirli yağ asitlerini içeren diyetsel TG yıkımı Gastrik lipaz Mide Mide Kısa-orta zincirli yağ asitlerini içeren diyetsel TG yıkımı Pankreatik lipaz Pankreas Đnce bağırsak Diyetsel triaçilgliserollerin yıkımı lümeni Lipoprotein lipaz Hormona duyarlı lipaz Ekstra hepatik dokular Yağhücreleri Kapiller hücre yüzeyi Yağ hüceleri (sitozol) Dolaşımdaki ŞM ve VLDL içinde bulunan TG leri yıkar Depolanmış TG lerin yıkımı Asit lipaz Çoğu dokular Lizozomlar Fagositoz esnasında alınan lipidlerden yağ asitlerini ayırır. Hepatik lipaz Karaciğer Karaciğer HDL2 deki fosfolipid ve TG leri yıkarak HDL3 e dönüşümü sağlamak, IDL yi LDL ye dönüştürmek Asite dayanıklı Asite dayanıklı Dayanıklılık için pankreatik kolipaza gerek duyar Heparin tarafından plazmaya salınır, apo CII tarafından aktifleştirilir camp bağımlı protein kinaz tarafından aktifleştirilir Asit ph da optimum Androjenler tarafından aktive, östrojenler tarafından inhibe edilir. 73
74 74 YAĞ ASĐTLERĐ VE TRĐAÇĐLGLĐSEROLÜN SENTEZĐ Lipogenez, yağ asitlerinin sentezi ve onların gliserolle esterleşerek triaçilgliserol oluşturmaları sıklıkla karaciğerde gerçekleşirken diyetle alınan karbonhidratlar başlıca karbon kaynağıdır. Yağ asitlerinin asetil KoA dan yeniden sentezi sitozolde, yağ asiti sentaz kompleksi üzerinde gerçekleşir. Başlıca glukozdan köken alan asetil KoA, asetil KoA karboksilaz tarafından malonil KoA ya çevrilir. Yağ asiti sentaz kompleksi üzerindeki büyüyen açil zincirine, malonil KoA daki üç karbondan ikisi ilave olurken biri dekarboksile olmaktadır. Her bir iki karbon ilavesiyle başlangıçta beta-keto grubu içeren büyüyen zincir, NADPH gerektiren bir seri reaksiyonla indirgenir. NADPH, pentoz fosfat yolundan veya malik enzim tarafından katalizlenen reaksiyonla elde edilir. Yağ asiti sentaz kompleksi tarafından salınan ürün palmitattır ve bir seri uzama ve desatürasyon reaksiyonu sonucu diğer yağ asitlerine dönüşebilir. Yağ açil KoA, karaciğerde gliserol 3-fosfatla birleşerek triaçilgliserolü oluşturur. Bu yolda fosfatidik asit, ara maddedir. Triaçilgliseroller, VLDL içinde paketlenerek kana salınır. Yağ asiti sentaz kompleksinin son ürünü: palmitat Yağ asiti sentezinde rol oynayan kofaktörler NADPH ATP Biotin CO2 Pantotenik asit Mangan Yağ asiti sentaz kompleksinin spesifik vitamini ve amino asiti pantotenik asit ve sistein 74
75 75 Yağ asitlerinin uzama ve desatürasyon reaksiyonlarının gerçekleştiği organel: endoplazmik retikulum Đnsanda, yağ asitlerinin doymamış hale getirilmesi: sitokrom içeren ve NADPH kullanan bir enzim tarafından katalizlenir. Asetil KoA karboksilazı aktive edenler: insülin ve sitrat Asetil KoA karboksilazı inhibe edenler: yağ asitleri, glukagon, epinefrin Triaçilgliserol sentezinin gerçekleştiği organel: endoplazmik retikulum Gliserol kinaz enzimi içermeyen dokular: kas ve yağ dokusu Đnsülinin plazma serbest yağ asitleri düzeyine etkisi: azaltıcı yöndedir. 75
76 76 76
77 77 YAĞ DOKUSUNDA TRĐAÇĐLGLĐSEROL DEPOLARININ OLUŞUMU Yağ dokusu triaçilgliserol depoları vücudun başlıca enerji kaynağıdır. Ortalama 70 kg lık bir insanda 15 kg civarında yağ vardır. Yemekten sonra, triaçilgliseroller yağ dokusu hücrelerinde depolanır. Bunlar yağ asitlerinden (lipoprotein lipaz tarafından yıkılan şilomikron ve VLDL den elde edilir) ve gliserolden (glukozdan köken alır) sentezlenir. Yağ dokusu hücrelerinde triaçilgliserollerin depolanması insülin aracılığı ile gerçekleşir. Đnsülin, yağ dokusu hücrelerinden lipoprotein lipazın sekresyonunu ve glukozun hücre içine girişini uyarır. Yağ dokusunda triaçilgliserol sentezi için gerekli bileşik: glukoz (dolayısıyla insülin) Asetil KoA nın katıldığı sentez reaksiyonları Kolesterol Keton cisimleri Yağ asitleri Sitrat KOLESTEROL VE SAFRA TUZU METABOLĐZMASI Kolesterol, başlıca karaciğer ve bağırsakta olmak üzere vücudun bir çok dokusunda sentezlenebilir. Kolesterol ve kolesterol esterleri kanda lipoproteinler içinde taşınır. Kolesterolün tüm karbonları asetil KoA dan köken alır. Kolesterol biyosentezinde anahtar ara bileşikler HMG KoA, mevalonik asit, izopentenil pirofosfat ve skualendir. Başlıca düzenleyici enzim HMG KoA redüktazdır. Karaciğerde safra tuzları, kolesterolden sterol halkasının hidroksilasyonu, yan zincirin oksidasyonu ve karboksilik asit grubunun glisin veya taurinle konjugasyonu sonucu elde edilir. 77
78 78 Safra tuzları safra kesesinde depolanır, yemek esnasında salınır ve yağların sindirimine yardımcı olur. Safra tuzlarının %95 i yeniden absorbe olur ve yeniden kullanılır. Sterol halkası parçalanamaz. Rezorbe olmayan safra tuzları halinde bütün olarak atılır. Kolesterol, dokularda kolesterol esterleri halinde depolanır. Bazı endokrin dokularda, kolesterol steroid hormonlara çevrilir. Bir kolesterol prekürsörü, vitamin D3 ün aktif formu olan 1,25-dihidroksikolekalsiferole çevrilebilir. Kolesterol sentezinin gerçekleştiği başlıca doku: karaciğer Kolesterol sentezinde kontrol basamağı: HMG-KoA mevalonat (HMG-KoA redüktaz tarafından gerçekleştirilir) Đzopren birimi içeren bileşikler Dolikol Koenzim Q Hem a Prenile proteinler Yağda çözünen vitaminler Kolesterol sentezinde oluşan ilk halka yapısı: lanosterol 78
79 79 Kolesterol sentezinin gerçekleştiği organeller: stoplazma ve ER HMG-KoA sentaz enziminin görev aldığı sentez reaksiyonları: kolesterol (stoplazmada) ve keton cisimleri (mitokondride) HMG-KoA redüktaz enzimini aktive edenler: insülin ve tiroid hormonları (tiroid hormonları kolesterol metabolizmasını da attırdığı için hipertiroidide plazma kolesterol düzeyleri azalır) HMG-KoA redüktaz enzimini inhibe edenler: mevalonat, kolesterol, safra asitleri, statinler, glukagon, glukokortikoidler Safra asiti sentezinde kontrol basamağı: 7α-hidroksilaz 7α-hidroksilaz basamağında kullanılan vitamin: C vitamini Primer safra asitleri: Kolik asit, kenodeoksikolik asit, taurokolik asit, glikokolik asit, tauro ve glikokenodeoksikolik asit Sekonder safra asitleri: deoksikolik asit, litokolik asit Enterohepatik dolaşıma katılan bileşikler: safra asitleri ve ürobilinojen 79
80 80 KAN LĐPOPROTEĐNLERĐ Kan lipoproteinleri suda çözünmeyen triaçilgliserollerin ve kolesterolün bir dokudan diğerine taşınmasında yardımcı olmaktadır. Triaçilgliserolün başlıca taşıyıcısı şilomikron ve VLDL dir. Şilomikron ve VLDL nin triaçilgliserolü kapillerlerde lipoprotein lipaz tarafından sindirilir. Oluşan yağ asitleri hücreler tarafından alınarak ya enerji için okside edilir ya da triaçilgliserole dönüştürülerek depolanır. Gliserol ise ya triaçilgliserol sentezinde kullanılır veya DHAP a çevrilerek enerji için okside olur. Şilomikron kalıntıları karaciğer hücreleri tarafından endositozla alınır ve lizozomal enzimlerce yıkılır. Ürünler, hücreler tarafından tekrar kullanılır. VLDL, IDL ye çevrilir, IDL ise ya karaciğerde lizozomal etkiyle yıkılır veya daha fazla triaçilgliserol parçalanarak LDL ye dönüşür. 80
81 81 IDL den oluşan LDL, çeşitli dokular tarafından alınarak ihtiyaçları olan kolesterolü sağlarlar. Karaciğer tarafından sentezlenen HDL, apo CII ve apo E gibi apoproteinleri şilomikron ve VLDL ye transfer eder. HDL, hücre membranlarından ve diğer lipoproteinlerden kolesterolü toplar. Kolesterol, lesitin kolesterol açil transferaz (LCAT) enzimi tarafından kolesterol esterlerine çevrilir. Bu kolesterol esterinin bir kısmı diğer lipoproteinlere aktarılır. Bu lipoproteinlerdeki veya HDL deki kolesterol esteri karaciğere taşınır ve serbest kolesterole hidroliz olarak VLDL sentezinde kullanılabilir veya safra tuzlarına çevrilebilir. Geri emilimi en az olan safra asiti: litokolik asit Safra asitlerinin plazmada bağlandığı protein: albümin Lipoproteinlerin yapısında bulunanlar: triçilgliserol,protein, kolesterol, kolesterol esteri, fosfolipid En fazla triaçilgliserol içeren lipoprotein: şilomikron En fazla kolesterol içeren lipoprotein: LDL (düşük dansiteli lipoprotein) En fazla protein ve fosfolipid içeren lipoprotein: HDL (yüksek dansiteli lipoprotein) Kan lipoproteinlerinin bileşenleri Bileşen Şilomikron VLDL IDL LDL HDL Triaçilgliserol % 85 % 55 % 26 % 10 % 8 Protein % 2 % 9 % 11 % 20 % 45 Apoprotein türü A, B, C, E B, C, E B, E B A,C, D,E Kolesterol % 1 % 7 % 8 % 10 % 5 Kolesterol ester % 2 % 10 % 30 % 35 % 15 Fosfolipid % 8 %20 % 23 % 20 % 25 Kaynak Bağırsak Karaciğer VLDL VLDL Bağırsak, Karaciğer Dansite g/ml <
82 82 Endojen sentezlenen triaçilgliserolün plazmada taşındığı lipoprotein: VLDL (çok düşük dansiteli lipoprotein) Lipoproteinlerin elektroforezle ayrılması, katoddan (- yük) anoda (+ yük) doğru sırasıyla: şilomikronlar, β lipoproteinler (LDL), pre-β-lipoproteinler (VLDL), α-lipoproteinler (HDL) Lipoproteinlerin ultrasantrifüjle dansitelerine göre ayrılması, en alttan en üste doğru: HDL, LDL, IDL, VLDL, şilomikron Kolesterol hücre içinde hangi metabolik olaylara yol açar? Hücre membranının yapısına katılma, HMG-KoA redüktazı inhibe etme, kolesterol esteri haline gelme, LDL reseptör sentezini inhibe etme Köpük hücre oluşumundan sorumlu lipoprotein: okside LDL Aterojenik protein: Apo B-100 Hem aterojenik hem de trombotik lipoprotein: Lp a Plazminojen ile yapıca benzerlik gösteren protein: apo a HDL ile diğer lipoproteinler arasında lipid alış-verişini düzenleyen protein: kolesterol ester transfer protein (apo D) Periferden kolesterol alınmasında en potent role sahip HDL: Pre-β-HDL En fazla protein içeren (oran olarak) lipoprotein: Pre-β-HDL Plazmada kolesterol esterinin oluşmasından sorumlu enzim: LCAT (lesitin kolesterol açil transferaz) Eksikliğinde plazmada serbest kolesterol/ester kolesterol oranının artmasına neden olan enzim: LCAT Hücre içinde kolesterol esterinin oluşmasından sorumlu enzim: ACAT (açil kolesterol açil transferaz) 82
83 83 Aterosklerozdan koruyucu HDL fraksiyonu: HDL-2 Antiaterojenik protein: Apo A-1 Plazma lipoproteinlerinde bulunan apoproteinlerden apo B100, apo E ve apo A1 in karaciğer hücrelerinde reseptörü vardır. 83
84 84 YAĞ DOKUSU TRĐAÇĐLGLĐSEROLLERĐNĐN SONU Açlıkta yağ asitleri ve gliserol, yağ dokusu triaçilgliserol depolarından salınır ve diğer dokular için bir yakıt kaynağı olarak kullanılır. Açlıkta insülin düşer ve glukagon yükselir. Bunun sonucunda camp-bağımlı bir mekanizmayla hormona duyarlı lipaz aktive olur. Hormona duyarlı lipaz, yağ triaçilgliserollerinin kana salınan yağ asitleri ve gliserole çevrilmesini başlatır. Yağ asitleri kanda albümine bağlı halde taşınır, çeşitli dokular tarafından alınır ve enerji için okside edilir. Karaciğerde, yağ asitleri keton cisimlerine ve gliserol glukoza çevrilir. Bu yakıt maddeleri, diğer dokular için enerji kaynağı olarak kullanılır. Yağ dokusunda hormona duyarlı lipazı inhibe edenler: insülin, prostaglandin, nikotinik asit Hormona duyarlı lipazı aktive edenler: katekolaminler, glukagon, tiroid hormonu, büyüme hormonu, ACTH, TSH, glukokortikoidler, metil ksantinler (fosfodiesterazı inhibe ederek) 84
85 85 Yağ asitlerinin hücre içine alınması: membran yağ asiti transport proteine bağlanarak sodyumla beraber hücre içine alınır. Yağ asitlerinin aktivasyonunda görev alanlar Açil KoA sentetaz (tiokinaz) KoA ATP Mg++ YAĞ ASĐTĐ OKSĐDASYONU Đnsan vücudunda en önemli enerji kaynağı olan yağ asitleri başlıca beta-oksidasyonla okside olur. Oksidasyondan önce uzun zincirli yağ asitleri aktive olarak bir karnitin taşıyıcı sistemle mitokondri içine taşınan yağ açil KoA lar oluşur. Beta-oksidasyon işlemi mitokondride gerçekleşir. FADH2 ve NADH üreten 4 basamakta yağ açil KoA dan iki karbon parçalanır ve asetil KoA olarak salınır. Bu reaksiyon serileri, bir çift zincirli yağ asiti, asetil KoA ya tamamen çevrilinceye kadar devam eder. FADH2 ve NADH, elektron transport zinciriyle ilişkiye girdiğinde veya asetil KoA daha ileri aşamaya okside olduğunda ATP elde edilir. Đskelet ve kalp kası gibi dokularda asetil KoA, TCA döngüsüne girerek CO2 ve H2O ya okside olur. Karaciğerde ise asetil KoA keton cisimlerine çevrilir. Beta-oksidasyon, oksidatif fosforilasyonu kontrol eden mekanizmalar tarafından (örn. ATP ihtiyacı) düzenlenir. Yağ asitleri ayrıca alfa ve omega-oksidasyona ve peroksizomal oksidasyona da girebilir. Uzun zincirli yağ asitlerinin stoplazmadan mitokondri içine geçişi: karnitinle birlikte olur. Karnitini oluşturan amino asitler: lizin ve metionin Karnitin ile yağ asitlerini birleştiren enzim olan karnitin palmitoil transferaz I enzimi hangisi tarafından inhibe edilir? Malonil KoA Yağ asitlerinin β-oksidasyonu hangi ikili organelde gerçekleşir: mitokondri ve peroksizomlar (çok uzun zincirli yağ asitleri için) Yağ asitlerinin β-oksidasyonuna katılanlar: yağ asitleri, FAD, H2O, NAD+, KoA 85
86 86 86
87 87 16 karbonlu satüre yağ asiti olan palmitat β-oksidasyon döngüsüne katıldığında net üretilen bileşikler: 7 FADH2, 7 NADH, 8 asetil KoA Karnitin eksikliğinde veya yağ asitlerinin beta-oksidasyon defektinde görülenler: non-ketotik hipoglisemi, dokuların yağlı infiltrasyonu, halsizlik-yorgunluk Orta zincirli açil KoA dehidrogenaz eksikliğinde görülen: dikarboksilik asidüri Peroksizomların yokluğu ile karakterize bozukluk: Zelweger sendromu Yağ asiti oksidasyonu bozuklukları: Yağ asiti oksidasyonunun bozulması; hipoglisemi, organların yağlı infiltrasyonu ve hipoketonemiye yol açar. Karnitin eksikliği ve kalıtsal karnitin palmitoiltransferaz I yetersizliğinde hipoglisemi gözlenir. Karnitin palmitoiltransferaz II yetersizliği başlıca iskelet kaslarını (güçsüzlük, nekroz, miyoglobinüri) etkiler. Dikarboksilik asidüride, mitokondrial orta zincirli açil KoA dehidrogenaz enzimi yoktur. Ketotik olmayan hipoglisemi ve C6-C10 omega-dikarboksilik asit atılımı ile karakterizedir. Refsum hastalığında alfa-oksidasyonda (peroksizomlarda) kalıtsal bir defekt ve buna bağlı fitanik asit birikimi gözlenir. Zellweger (serebrohepatorenal) sendromunda tüm dokularda peroksizomlar yoktur. Buna bağlı peroksizomlarda çok uzun zincirli yağ asitlerinin oksidasyonu bozularak beyin dokusunda C26-C38 lu polienoik asitler birikir. KETON CĐSĐMLERĐNĐN SENTEZĐ VE KULLANILMASI Keton cisimleri, asetoasetat ve β-hidroksibütirat, enerji kaynağı olarak fonksiyon görürler. Kanda yağ asiti düzeylerinin çok yükseldiği durumlarda başlıca karaciğer mitokondrisinde sentezlenirler. Yağ asitleri karaciğer hücrelerinde aktive olur ve ATP üreterek asetil KoA ya dönüşür. NADH ve ATP düzeyleri yükseldikçe, asetil KoA birikir. Asetil KoA, asetoasetil KoA ile reaksiyona girerek HMG KoA oluşur. HMG KoA ise asetoasetat oluşturmak üzere yıkılır. Asetoasetat, NADH tarafından ikinci bir keton cisimine 3-hidroksibütirata (beta-hidroksibütirat) indirgenebilir. Aseton, spontan (enzimatik olmayan) dekarboksilasyonla asetoasetattan üretilir. Karaciğer, keton cisimlerini kullanamaz çünkü asetoasetatı aktive eden tiotransferaz enziminden yoksundur. Keton cisimleri, kas ve böbrek gibi dokularda enerji kaynağı olarak kullanılırlar. Açlık esnasında (açlığın 3-5. gününden sonra) beyin de keton cisimlerini okside eder. Beta-hidroksibütirat hücre içine girerek NADH üreten bir reaksiyonla asetoasetata okside olur. Kandan doğrudan gelen veya 3-hidroksibütirat aracılığı ile elde edilen asetoasetat, süksinil KoA ile reaksiyona girerek asetoasetil KoA ya aktive olur. Asetoasetil KoA, beta-ketotiolaz tarafından 2 adet asetil KoA ya parçalanır. Asetil KoA ise TCA döngüsüne katılarak CO2 ve H2O ya okside olurken ATP elde edilir. Refsum hastalığında idrarla atılan bileşik: fitanik asit Keton cisimlerinin aktivasyonunda görevli bileşik: süksinil KoA Keton cisimlerini aktive eden enzim: KoA transferaz (tiyotransferaz, tiyoforaz) Keton cisimleri hangi bileşiğe dönüşerek TCA döngüsüne katılır? Asetil KoA Keton cisimlerinin sentezi için gerekli olan iki enzim: HMG KoA sentaz ve HMG KoA liyaz FOSFOLĐPĐD VE SFĐNGOLĐPĐD METABOLĐZMASI Fosfogliseridler ve sfingolipidler hücre zarlarının başlıca bileşenleridir. Amfipatik moleküllerdir; molekülün bir kısmı hidrofiliktir ve H2O ile ilişkidedir, diğer kısmı yağ asitlerinden köken alan hidrokarbon zincirleri içerir ve hidrofobiktir Fosfogliseridler (majör fosfolipidler); gliserol, yağ asitleri ve fosfat içerir. Fosfat grubu; kolin, serin, etanolamin veya inozitol ile esterleşmiş haldedir. Fosfogliseridler çeşitli yollarla sentezlenirler. Fosfogliseridlerin yıkımı, fosfolipazlar tarafından gerçekleştirilir. Sfingolipidler, sinir dokusundaki hücre membranlarının başlıca bileşenini oluştururlar, Bunlar arasında sfingomyelin (fosfokolin içerir), serebrozid ve gangliozidler (şeker artığı içerirler) bulunur. Sfingolipidler; serin ve palmitoil KoA dan üretilen seramidden sentezlenirler. Yıkım esnasında sfingolipidlere ait fosfokolin ve şeker birimleri lizozomal enzimler tarafından kaldırılır. Fosfolipidlerin sentezinde görevli nükleotid: sitidin nükleotidleri 87
88 88 88
89 89 Fosfatidilkolinden lizofosfatidilkolin oluşturan enzim: Fosfolipaz A2 89
90 90 90
91 91 EĐKOZANOĐDLERĐN METABOLĐZMASI Eikozanoidler (prostaglandinler, tromboksanlar, lökotrienler ve lipoksinler) poliansatüre yağ asitlerinden (örn. araşidonik asit) sentezlenirler. Bu yağ asitleri membran fosfolipidlerinden fosfolipaz A2 tarafından serbestleştirilirler. Fosfolipaz A2, glukokortikoidler tarafından inhibe edilir. Eikozanoidler biyokimyasal etkilerini G-proteinleri üzerinden gerçekleştiren lokal hormonlar olarak kabul edilir. Prostaglandin sentezi için, poliansatüre yağ asitleri halkalaşır ve siklooksijenaz enzimi tarafından oksidlenir. Siklooksijenaz, aspirin ve diğer steroid olmayan anti-inflamatuar ajanlar tarafından inhibe olur. Daha ileri oksidasyon ve düzenlemeler sonucu prostasiklinler gibi bir grup prostaglandin üretilir. Tromboksanlar, bir çeşit prostaglandinlerden üretilir. Lökotrienler ve lipoksinler, prostaglandin sentezi yolundan farklı bir yolla araşidonik asitten sentezlenirler. Lökotrien A4:Lökosit, trombosit, mast hücreleri ve kalp ve akciğer damar dokularında oluşur. Fosfolipaz A2 yi aktive edenler Bradikinin Epinefrin Trombin Anjiyotensin II PGI2 (Prostasiklin) Damar endotel hücrelerinde üretilir. Vazodilatasyon Trombosit agregasyonunu inhibe eder. TXA2 (Tromboksan A2) Başlıca trombositler tarafından üretilir. Trombosit agregasyonunu uyarır. Vazokonstruksiyon Hücre içi kalsiyum mobilizasyonu Düz kas kasılması PGF2α (Prostaglandin F2α) Bir çok dokuda üretilir. Vazokonstruksiyon Düz kas kasılması Uterus kasılmasının uyarılması Lökotrienler glutatyonla birleşerek hangi bileşik oluşur: anaflaksinin yavaş reaksiyona giren maddesi (SRS -A) PGE2 (Prostaglandin E2) Birçok dokuda özellikle böbrekte üretilir. Vazodilatasyon Düz kas gevşemesi Doğumu indüklemede kullanılır. LTC4 LTD4 LTE4 etkileri Düz kasların kasılması Bronkokonstruksiyon Vazokonstruksiyon Vasküler permeabilite artışı SRS-A komponentleri LTB4 (Lökotrien B4) etkileri PMN lökositlerin kemotaksisinde artış Lizozomal enzimlerin salınımı B lökosit adezyonu Tüm lipid depo hastalıklarında biriken ortak lipid bileşeni: seramid 91
92 92 BAZI SFINGOLIPIDOZLAR VE ÖZELLIKLERI Hastalık Enzim Eksikliği Biriken Lipid1 Klinik Semptomlar Fukozidoz α-frukozidaz Cer-Glc-Gal-GalNAc-Gal Fuc H-izoantijen Jeneralize Cer-Glc-Gal (NeucAc)-GalNAc GM1- β-galaktozidaz gangliozidoz Gal GM1 Gangliozid Tay-Sachs hastalığı Sandhoff s hastalığı Fabry s hastalığı Seramid laktozid hastalığı Metakromatik lökodistrofi Krabbe s hastalığı Gaucher s hastalığı Niemann-Pick hastalığı Farber s hastalığı Heksozaminidaz A Heksozaminidaz A ve B Cer-Glc-Gal(NeucAc) GalNAc GM2 Gangliozid Cer-Glc-Gal-Gal GalNAc+ GM2 gangliozid α- Galaktozidaz Cer-Glc-Gal Gal Seramid triheksozid Seramid laktozidaz ( β- galaktozidaz) Arilsülfataz A Cer-Glc-Gal Gal Seramid laktozid Cer-Gal OSO3 Sülfatid Serebral dejenerasyon, kas spastisitesi, kalın deri Mental retardasyon, karaciğer büyümesi, iskelet deformasyonu. Mental retardasyon, körlük, kas zayıflığı. Tay-Sachs la aynı fakat daha hızlı ilerleme Deri döküntüsü, böbrek yetmezliği, (tüm semptomlar sadece erkeklerde; X e bağlı resesif) Đlerleyici beyin hasarı, karraciğer ve dalak büyümesi Adültlerde mental retardasyon ve psikolojik bozukluklar; demyelinizasyon β- Galaktozidaz Cer GalGalaktoserebrozid Mental retardasyon; myelin yokluğu β- Glukozidaz Cer Glc Glukoserebrozid Sfingomyelinaz Seramidaz Cer P-kolin sfingomyelin Açil Sfingozin Seramid Karaciğer ve dalak büyüklüğü, uzun kemiklerin erozyonu, infantlarda mental retardayon, hayatın erken döneminde ölüm Karaciğer ve dalak büyüklüğü, mental retardasyon, hayatın erken döneminde ölüm Ses kısıklığı, dermatit, iskelet deformasyonu mental retardasyon; hayatın erken döneminde ölüm 92
93 93 Dislipidemilerin sınıflandırılması Tip Genetik Sınıflandırma Artmış Lipid Artmış Liporotein Elektroforez Yapısı I Ailesellipoproteinlipaz eksikliği,apo C II eksikliği Triaçilgliserol Hiperlipoproteinemiler Şilomikron ve VLDL Başlangıçta yoğun bant, artmış pre-beta bandı, plazma süt gibidir IIa Ailesel hiperkolesterolemi Kolesterol LDL Artmış beta- bandı IIb Triaçilgliserol ve Artmış beta- ve pre- Beta Ailesel kombine hiperlipidemi LDL ve VLDL kolesterol bandı III Triaçilgliserol ve Artmış pre beta - bandı (geniş Ailesel disbetalipoproteinemi Beta-VLDL (IDL) kolesterol beta - bandı) IV Ailesel hipertrigliseridemi Triaçilgliserol VLDL Artmış pre beta- bandı Hiperalfalipoproteinemi Kolesterol normal veya hafif yüksek HDL Artmş alfa- bandı Hipolipoproteinemiler Abetalipoproteinemi Ailesel hipobetalipoproteinemi Ailesel alfa-lipoprotein eksikliği Tangier hastalığı, Fish-eye hastalığı, Apo A-I eksikliği Açilgliseroller düşüktür HDL nin düşüklüğü veya yokluğu Şilomikron, VLDL ve LDL oluşmamıştır. LDL düzeyi normalin % Şilomikron veya VLDL oluşumunda bozulma yok; düşük LDL Triaçilgliserol transfer proteinde defekt vardır Uzun yaşam süresi Geniş beta bandı, apo C-II eksikliğine bağlı triaçilgliserol artışı. AZOT METABOLĐZMASI Azot; mide, pankreas ve bağırsak epitel hücreleri tarafından üretilen proteazların kombine etkisiyle diyetteki proteinlerin parçalanması sonucu açığa çıkan amino asitlerden elde edilmektedir (Şekil 6.1). Amino asitler bağırsak epitel hücreleri tarafından emilir, kana geçer ve vücudun diğer hücreleri tarafından alınır. Amino asitler hücreler tarafından protein sentezinde kullanılır; proteinler sürekli sentezlenirler ve yıkılırlar. Amino asitlerden azot kaldırıldıktan sonra, karbon iskeletleri enerji için okside olabilir. Amino asitlerin azotu, karaciğerde üreye çevrilir ve sonuçta böbrekler tarafından atılır. Üre, azotun başlıca atılım ürünü olmakla beraber, azot ayrıca NH4+, ürik asit ve kreatinin halinde de atılabilir. Toklukta karaciğer amino asitlerin karbonlarını, çok düşük dansiteli lipoproteinlerin (VLDL) triaçilgliserollerini oluşturan yağ asitleri ve gliserole çevirir. Açlıkta, kas proteini yıkılır ve kana amino asitler salınır. Karaciğer aminoasit karbonlarını, glukoz ve keton cisimlerine çevirir. Esansiyel amino asitler (histidin, izolösin, lösin, lizin, metionin, fenilalanin, treonin, triptofan ve valin) diyette gerekir. Arginin ve fazla miktarda histidin büyüme dönemlerinde gerekir. Esansiyel olmayan amino asitler vücutta sentezlenebilir esansiyel olmayan aminoasitin karbonları glukozdan türeyebilir. Bununla beraber, sistein sentezinde esansiyel aminoasit olan metioninden sülfür alınır. - Tirozin, 11. esansiyel olmayan aminoasittir; esansiyel aminoasit olan fenilalaninin hidroksilasyonu ile sentezlenir. Amino asitler; pürin ve pirimidin bazları, hem, kreatin, nikotinamid, serotonin, tiroksin, epinefrin, melanin ve sfingozin gibi bir çok azot içeren bileşiklerin sentezinde kullanılır. Amino asitlerin metabolize olduğu başlıca doku: karaciğer 93
94 94 94
95 95 Pepsin proteinlerde hangi bölgeyi parçalar? Dikarboksilik amino asitlerin ve aromatik halka içeren amino asitlerin amino tarafındaki peptid bağını Endopeptidazlar tripsin kimotripsin elastaz pepsin Ekzopeptidazlar Karboksipeptidaz A ve B Aminopeptidaz Tripsinojeni tripsine çeviren enzim: enterokinaz (enteropeptidaz) Bağırsakta sentezlenen enzimler: enterokinaz ve aminopeptidaz 95
96 96 Đnaktif zimojen olarak sentezlenen enzimler: pepsin, tripsin, kimotripsin, elastaz, karboksipeptidaz Pankreas enzimleri arasında zimojen formu olmayanlar: amilaz ve lipaz Amino asitlerin hücre içine alınması: Sodyumla beraber ve glutatyon üzerinden Amino asitlerin hücre içine alınmasında rol oynayan enzim: gama glutamil transferaz Sistinüride idrarla atılan amino asitler Sistein Ornitin Arginin Lizin Amino asitlerden transaminasyon reaksiyonları ile genel amino grubu toplayıcısı bileşik: alfa ketoglutarat Amino asitlerin transaminasyon, dekarboksilasyon ve deaminasyonunda görevli koenzim: pridoksal fosfat 96
97 97 Transaminasyon ile birbirine dönüşen bileşikler: glutamat-alfa-ketoglutarat; alanin-piruvat; aspartatoksaloasetat Transaminasyona katılmayan amino asitler: lizin, treonin, prolin Oksidatif deaminasyona uğrayan amino asit: glutamat Amino asitlerin amino gruplarının amonyum iyonlarına çevrildiği reaksiyon: glutamatın oksidatif deaminasyonu Glutamat dehidrogenazın bulunduğu organel ve kofaktörü: mitokondri ve NAD+ veya NADP+ 97
98 98 Pozitif azot dengesinin gerçekleştiği durumlar: büyüme dönemi, gebelik, nekahat evresi Negatif azot dengesinin gerçekleştiği durumlar: enfeksiyonlar, yanık, açlık, travma, uzun süreli hareketsizlik, diyetteki esansiyel amino asitlerin yetersizliği 98
99 99 Azot içeren bileşiklerin vücuttan başlıca atılım şekli: üre ÜRE DÖNGÜSÜ Amonyak özellikle santral sinir sistemi için çok toksiktir. Đnsanlarda çok toksik olan amonyak, toksik olmayan, suda çözünür ve böbreklerle kolaylıkla atılan üreye çevrilir. Üre sentezini başlatan enzim ve kontrol basamağı: karbamoil fosfat sentetaz I 99
100 100 Mitokondriyal formu üre sentezinde, sitoplazmik formu ise pirimidin bazlarının sentezinde rol oynayan enzim: karbamoil fosfat sentetaz Karbamoil fosfat sentetaz I enzimini aktive eden bileşik: N-asetil glutamat Üre sentezinde doğrudan amino grubu vericisi bileşikler: serbest amonyak (veya karbamoil fosfat) ve aspartat Üre sentezinde hangi bileşikte net kayıp gözlenir? Aspartat 100
101 101 Üre sentezinin gerçekleştiği organeller: mitokondri ve stoplazma Üre sentezinde harcanan enerji: 3 ATP veya 4 yüksek enerjili fosfat bağı Üre siklusu defektlerinde tedavi: proteinden fakir diyet, benzoat, fenilasetat, arginin (arginino süksinat sentetaz ve arginino süksinaz eksikliklerinde) Benzoatın detoksifikasyonunda kullanılan amino asit: glisin 101
102 102 Üre siklusu defektlerinde artmış amonyak düzeylerinin beyin için toksik olmasının nedeni: amonyakın beyinde alfa-ketoglutarat ile birleşerek glutamat oluşturması sonuçta beyinde TCA döngüsü ara maddelerinin kalmaması, glutamatın amonyak ile birleşerek glutamine dönmesi ve glutamat azalmasına bağlı olarak azalmış GABA sentezi AMĐNOASĐTLERĐN SENTEZĐ VE YIKIMI Proteinlerde bulunan 20 amino asitten 11 i esansiyel değildir çünkü vücutta sentezlenebilirler. Esansiyel olmayan amino asitlerden 10 u glukozdan türeyen karbon iskeleti içerir. Tirozin, esansiyel bir amino asit olan fenilalaninin hidroksilasyonu ile elde edilir. Sistein, esansiyel bir amino asit olan metioninden bir kükürt gurubunun serine ilave olması sonucu oluşur. Amino asitlerin karbon iskeletlerinin yıkımı sonucu elde edilen başlıca ürünler piruvat, TCA döngüsünün ara maddeleri, asetil KoA ve asetoasetattır Esansiyel amino asitler Dallı zincirliler (valin, lösin, izolösin) Aromatik halka içerenler (fenilalanin,triptofan, histidin) Lizin Treonin Metionin Yarı esansiyel amino asit: arginin Prolin veya arginin hangi amino asitin parçalanması ile oluşur? Glutamat Asparagin sentezi için gerekli olanlar: ATP-Mg, glutamin, aspartik asit, asparagin sentetaz 102
103 103 Selenosistein, birkaç ökaryotik ve prokaryotik enzimin (örn. tioredoksin redüktaz, glutatyon peroksidaz ve tiroksini triiodotironine çeviren deiyodinaz) aktif bölgesinde bulunan bir amino asittir. Posttranslasyonel modifikasyonla oluşan hidroksiprolinin tersine selenosistein, peptidlere katılmadan önceki bir işlemle oluşur. Selenyum içerir ve serinden türer. Histidinin yıkımında görevli koenzim: tetrahidrofolat 103
104 104 Saf ketojenik amino asitler: lösin ve lizin Benzoatın konjugasyonunda görev alan amino asit: glisin 104
105 105 Ornitin metbolizmasının defekti sonucu gelişen: retinanın Gyrate atrofisi KoA yı kullanarak TCA döngüsü ara maddelerine dönüşen amino asitler: valin, izolösin, metionin, treonin Homosisteinin metionine dönüşümünde rol alan vitaminler: B12 ve folat Homosistein hangi amino asitin metabolizmasında oluşur? Metionin 105
106 106 Triptofandan sentezlenen bileşikler: serotonin, melatonin, alanin, format, NAD+ nin nikotinamid bölümü, glukoz, keton cisimleri Aminoasit Metabolizmasında Çeşitli Dokuların Etkileşimleri Açlık esnasında, kas dokusundaki amino asitler başlıca alanin ve glutamin halinde kana salınırlar. Dallı zincirli amino asitler enerji üretmek üzere kasta okside olurlar. Karbonların bazıları glutamin ve alanine çevrilir. Alanin ayrıca glukoz-alanin döngüsü tarafından da üretilir. Bağırsak glutamini kandan alır ve onu alanin, sitrülin ve serbestleştirilen amonyağa çevirir. Böbrekler glutamini kandan alır ve amonyağı idrarla atarken alanin ve serini kana bırakır. Karaciğer alanin ve diğer amino asitleri kandan alır; azotu üreye ve karbonları glukoz ve keton cisimlerine çevirerek kana salar. Bunlar dokularda enerji için okside olurlar. Böylece, kas proteinindeki amino asitler diğer bir çok dokuda enerji kaynağı olarak görev görürler. Albinizmde eksik olan enzim: tirozinaz Açlık durumunda kaslardan karaciğere en fazla taşınan amino asit: alanin Böbrekte asit-baz dengesini düzenleyen amino asit: glutamin Kanda en fazla bulunan amino asitler: alanin ve glutamin 106
107 107 Beyin tarafından metabolize edilen amino asitler: dallı zincirli olanlar Folat tarafından alınan tek karbonlu bileşiklerin başlıca kaynağı: serin Folatın katıldığı sentez reaksiyonları: dtmp, pürin, serin, metilkobalamin TETRAHĐDROFOLAT, B12 VĐTAMĐNĐ VE S-ADENOZĐLMETĐONĐN Tek bir karbon atomu içeren gruplar bir bileşikten diğerine transfer edilebilirler. CO2 den daha az oksidasyon düzeyine sahip bir karbonlu gruplar tetrahidrofolat (FH4), B12 vitamini ve S- adenozilmetionin tarafından transfer edilirler (CO2, biotin tarafından transfer edilir). Folat vitamininden üretilen FH4, bir karbonlu grupları serin, glisin, histidin, formaldehid ve formattan elde eder. Bir karbonlu gruplar FH4 e bağlı halde iken oksitlenir ve indirgenir. En fazla indirgenen form metil-fh4 dür. FH4 tarafından taşınan bir karbonlu gruplar, dump ye transfer edilerek dtmp; glisine transfer edilerek serin; pürin prekürsörlerine aktarılarak pürin halkasının C2 ve C8 i oluşur. Ayrıca B12 vitaminine de aktarılabilir. B12 vitamini vücutta iki reaksiyonda görevlidir: Süksinil KoA oluşturmak üzere metilmalonil KoA nın metil grubunun düzenlenmesinde kullanılır ve 5-metil-FH4 den bir metil grubunu homosisteine transfer ederek metionin oluşturur. S-Adenozilmetionin (SAM); metionin ve ATP den elde edilir ve kreatin, fosfatidilkolin, epinefrin, melatonin ve metillenmiş polinükleotidler oluşturmak üzere çeşitli bileşiklere metil grupları transfer eder. 107
108 108 S-adenozil metioninin (SAM) katıldığı başlıca sentez reaksiyonları: Epinefrin Kreatin Melatonin Fosfatidil kolin Metilenmiş nükleotidler (örn. metil GTP) 108
109
110 110 AMĐNOASĐTLERDEN TÜREYEN ÖZEL ÜRÜNLER Amino asitler vücutta bir çok azot içeren bileşiğin sentezinde kullanılırlar. Kreatin; glisin, argininin guanidinyum grubu ve SAM in metil grubundan üretilir. - Kreatin fosfat, kreatin ve ATP den üretilir. Spontan olarak halkalaşarak kreatinine dönüşür ve idrarla atılır. Glutamatın dekarboksilasyonuyla gama-aminobutirik asit (GABA), histidinin dekarboksilasyonuyla histamin oluşur. Sfingolipidlerin sentezi için kullanılan seramid, serin ve palmitoil KoA dan üretilir. Serotonin, melatonin ve NAD+ nin nikotinamid bölümü (niasin vitamininden de türeyebilir) triptofandan türer. Tiroid hormonu, 3,4-dihidroksifenilalanin (dopa), melanin, dopamin, norepinefrin ve epinefrin; tirozinden sentezlenirler. Hem, porfirinlerin bir seri reaksiyonuyla glisin ve süksinil KoA dan üretilir. - Hem, bilirubine yıkılarak safrayla atılır. Kreatin sentezinde başlangıç ya da ara bileşik olarak yer alanlar Glisin Arginin Guanidino asetat S-adenozilmetionin Karnitin sentezine katılan amino asitler ve karnitinin görevi: lizin ve metionin; uzun zincirli yağ asitlerinin (yağ açil KoA lar) stoplazmadan mitokondri içine geçişine aracılık etme 110
111 111 Tirozinden adrenalin sentezi sırasında görülen tepkimeler: aromatik hidroksilasyon, dekarboksilasyon, β- karbonu üzerinden hidroksilasyon, transmetilasyon Norepinefrinin epinefrine dönüşümünde görevli enzim: fenil etanolamin N-metil transferaz (kortizol tarafından aktive edilir) Dopaminin yıkım ürünü: Homovanilik asit Katekolaminlerin yıkımında görevli enzimler: MAO ve KOMT Karnozin ve anserin (metilkarnozin) iskelet kasında bulunur, miyozin ATPaz aktivitesini aktive ederler. Her ikisi de bakırı şelatlar ve bakır uptake ini arttırır. Karnozin Beta-alanil ve histidinin birleşmesinden oluşur. Homokarnozin ise beyinde yüksek konsantrasyonda bulunan, histidin ile GABA dan oluşan bir dipeptiddir. 111
112 112 Spermin ve spermidin poliaminler sınıfından bileşikler olup hücre proliferasyonu ve doku büyümesinde rol oynarlar. Ornitin ve metionin amino asitlerinden sentezlenirler. Ornitinin dekarboksilasyonu ile putrescin oluşur. Spermin ve spermidini oluşturan amino asitler: ornitin ve metionin Ornitinin dekarboksilasyonu ile oluşan: putrescin Hangi amino asitlerin hidroksilasyonunda tetrahidrobiopterin ve moleküler oksijen kullanılır? Fenilalanin, tirozin, triptofan Katekolaminlerin yıkım ürünleri Dihidroksi mandelik asit Metanefrin Normetanefrin VMA Karnozin ve anserini oluşturan amino asitler: beta alanin ve histidin Glisinin katıldığı sentez reaksiyonları Kollajen Hem Pürin Kreatin Glutatyon Konjugasyon Oksalat Argininin katıldığı sentez reaksiyonları Kreatin Üre Ornitin Nitrik oksit Spermin 112
113 113 Tirozinden sentezlenenler Katekolaminler Melanin Tiroid hormonları Glukoz ve keton cisimcikleri PORFĐRĐNLER Porfirinler metal iyonlarını, özellikle Fe2+ ve Fe3+ şeklindeki demiri kolayca bağlayan siklik bileşiklerdir. Đnsanda en çok bulunan metalloporfirin hem dir. Hem; hemoglobin, miyoglobin,sitokromlar, katalaz ve triptofan pirolaz için prostetik gruptur. Hemproteinler süratle sentezlenip yıkılırlar. Örneğin her gün katabolik yıkıma uğrayan hem molekülünü yerine koymak için 6-7 g hem sentezlenir. Hem proteinlerinin turnoveri ile birlikte beraberindeki porfirinler de yıkılıp sentezlenir ve bağlı bulunan demir iyonları da bir döngü içine girer. Porfirinlerin biyosentezi: - Hem sentezinin yapıldığı başlıca yerler karaciğer (özellikle sitokrom P450 sentezlenir) ve kemik iliğidir (hemoglobin sentezinin aktif olduğu eritrosit üreten hücreler). - Porfirin sentezinde başlangıç ve son üç aşama mitokondride, ara aşamalar sitozolde gerçekleşir. Olgun eritrositlerde mitokondri olmadığı için hem üretilemez. Hem sentezinde kontrol basamağı ve kofaktörü: ALA sentaz ve B6 Đlaçların ALA sentaz aktivitesine etkisi: Bir çok ilaç, (örn. barbitüratlar, griseofulvin, sülfonamid, hekzoklorbenzen) hepatik ALA sentaz aktivitesini arttırır. Bu ilaçlar, karaciğerde bulunan mikrozomal sitokrom P450 monooksijenaz sistemi ile metabolize olurlar. Bu ilaçlara bir cevap olarak sitokrom P450 sentezi de artar. Bu durumda sitokrom P450 nin bir bileşeni olan hem tüketimi de artar. Sonuçta karaciğer hücrelerinde hem konsantrasyonu azalır. Buna bağlı olarak ALA sentaz sentezi ve dolayısıyla ALA sentezi artar. Hem sentezinin gerçekleştiği organeller: mitokondri ve stoplazma Kurşun zehirlenmesinde kanda artan bileşik: delta amino levulinik asit Hem sentezinde oluşan ilk pirol halkası: porfobilinojen Porfirialar - Porfirialar, hem sentezindeki bozuklukların neden olduğu, porfirin veya porfirin prekürsörlerinin birikimi ve fazla miktarda atılımı ile karakterize herediter (veya bazen akkiz) hastalıklardır. Porfirialar, enzim eksikliğinin kırmızı kan hücrelerinde veya karaciğerde olmasına göre eritropoetik veya hepatik olarak ayrılır. Tüm porfirialar otozomal dominant geçişlidir. Bunun tek istisnası otozomal resesif geçişli konjenital eritropoietik porfiriadır. Porfirialarda hem sentezi ile ilgili enzimlerde eksiklik olduğu için hem sentezi azalır, ara metabolitlerde birikim olur. Normalde hem, ALA sentezini baskı altında tutar, hem eksikliğinde ise ALA sentaz aktivitesinde artış gözlenir. Akut intermittant porfiria gibi ALA ve porfobilinojen birikimine neden olan porfirialar, karın ağrısı ve nöropsikiyatrik bozukluklara neden olur. Bu bileşiklerin bir veya ikisi abdominal sinirlerde ve SSS de toksik etkilere (paralizi) yol açar. Porfirin türevleri fotosensitiviteye neden olur. Porfirinler güneş ışığı ile karşılaştığında uyarılır ve moleküler oksijenle reaksiyona girerek oksijen radikalleri oluşur. Bunlar lizozomları ve diğer organelleri hasara uğratarak değişen miktarlarda deri hasarına (skarlaşma dahil) yol açar. Klinik belirtiler barbitürat gibi ilaçların kullanılmasıyla sitokrom P450 mikrozomal ilaç oksidasyon sisteminin sentezindeki artışa bağlı olarak alevlenir. Tedavide glukoz infüzyonu, intravenöz hematin (hemin okside formu) enjeksiyonu semptomları hafifletir. Hematin, ALA sentaz sentezini azaltır glukoz ise enzimi inhibe eder. Güneş ışığından kaçınmak ve β-karotenle (serbest radikal çöpçüsü) beslenmek de yararlıdır. Protoporfirine demiri ilave eden enzim: ferroşelataz Bilirubinin oluştuğu doku: RES 113
114
115 115 Hem sentezinde görev almayanlar: üroporfirin ve koproporfirin türevleri (porfirinojen türevleri ve protoporfirin IX görev alır) ALA sentaz enzimini aktive eden bileşikler: sit P450 sistemi ile metabolize olan ilaçlar (barbitüratlar, sülfonamidler, griseofulvin, heksoklorobenzen) Fotosensitivite görülmeyen porfirialar: ALA dehidrataz eksikliği ve akut intermittan porfiria Otozomal resesif geçiş gösteren porfiria: konjenital eritropoetik porfiria (diğerleri otozomal dominant) 115
116 116 En sık görülen porfiria: porfiria kutanea tarda Eritropoetik porfirialar: konjenital eritropoetik porfiria ve protoporfiria Hem oksijenaz reaksiyonunun gerçekleştiği organel ve açığa çıkanlar: ER ve Fe3+ ve CO Obstrüktif sarılığın özellikleri Plazmada konjuge bilirubin artışı 116
117 117 Đdrarda safra tuzu ve safra pigmentlerinin bulunması Kanda alkalen fosfataz kolesterol artışı Yarı ömrü en kısa olan enzimler: kontrol basamağını katalizleyen enzimler Plazma proteinlerinin yıkımı: sialik asitlerini kaybederler, reseptör aracılığı ile karaciğere alınırlar ve katepsin adlı proteazlarla parçalanırlar. Bilirubin konsantrasyonunun tayini: Bilirubin en sık olarak van den Bergh reaksiyonuyla ölçülür. Bu reaksiyon, diazotlu sülfonilik asitin bilirubinle reaksiyona girmesi ve sonuçta kırmızı renkli azodipirol oluşması ve bunun kolorimetrik olarak saptanması esasına dayanır. Fenilketonüri: Fenilketonüri (FKU), fenilalanin hidroksilaz enzimindeki bir bozukluk sonucu otozomal resesif gelişir. Amino asit metabolizması ile ilgili en sık rastlanan bozukluktur (prevalansı 1/11.000) (Şekil 6.39). Plazma fenilalanin düzeyi yüksek olan hastaların yaklaşık yarısı FKU nedeniyledir. Hiperfenilalaninemi nedenleri arasında ayrıca, herediter tirozinemi ve koenzim olan tetrahidrobiopterinin (BH4) sentez veya indirgenmesini sağlayan enzimlerde bir bozukluk (vakaların %3 ü) bulunmaktadır. Bu enzimler dihidrobiopterin (BH2) redüktaz ve BH2 sentetazdır. Bunlardaki bir mutasyon BH4 sentezini baskılar ve indirekt olarak fenilalanin konsantrasyonu artar, çünkü fenilalanin hidroksilaz, koenzim olarak BH4 ü kullanır. BH4, serotonin ve katekolaminler gibi nörotransmitterlerin sentezine yol açan reaksiyonları katalizleyen tirozin hidroksilaz ve triptofan hidroksilaz için de gereklidir. Bu durumda diyetteki fenilalanin miktarını kısıtlamanın nörotransmitterlerdeki bozukluğa bağlı olan MSS etkilerini geri çeviremeyeceği için bir yararı yoktur. 117
118 118 Proteinler çeşitli hızlarda yıkılır Bir proteinin başlangıç konsantrasyonunun yarısına, inmesi için gereken zaman o proteinin yarı ömrü olarak tanımlanır. 1. Karaciğer proteinlerinin yarı ömürleri 30 dk ila 150 saatin üzerindedir. Kısa yarı ömürlü bir çok protein prolin (P), glutamat (E), serin (S) ve treonin (T) amino asitlerinden zengin bölgeler (PEST dizisi) içerir. 2. Bir çok anahtar düzenleyici enzimin yarı ömrü kısadır. 3. Kısa ömürlü proteinler sitozolde ATP ve ubikitine gerek duyarak yıkılırlar. 4. Hücre dışı, membranla ilişkili ve uzun ömürlü proteinler ATP yi kullanmaksızın lizozomlarda yıkılırlar. 5. Dolaşımdaki proteinler oligosakkarid zincirlerindeki sialik asitini kaybederek karaciğer hücresine reseptör aracılığı ile girerler ve katepsin adlı proteazlarla lizozomlarda parçalanırlar. NÜKLEĐK ASĐTLER NÜKLEOTĐDLER Nükleik asitler (RNA ve DNA) pürin ve pirimidin bazları içerir. Pürin bazları arasında adenin (A) ve guanin (G) ve pirimidin bazları arasında sitozin (C), timin (T) ve urasil (U) bulunur. Nükleozidler pürin veya pirimidin bazlarına beta-glikozidik bağlarla bağlı bir riboz veya deoksiriboz içerirler. Nükleotidler, nükleozidlerin fosfat esterleridir. * Bir çok koenzim, nükleotid türevleridir. Pürin bazları: adenin, guanin, hipoksantin Pirimidin bazları: sitozin, timin, urasil 118
119 119 Nükleozid: baz + şeker Nükleotid: nükleozid + fosfat Nükleik asitlerin (RNA ve DNA) yapısı: nükleozid monofosfatların fosfodiester bağları ile birbirine bağlanması sonucu oluşur. 119
120 120 Pürin ve pirimidin bazları ile pentoz arasındaki bağ: β-n glikozidik bağ Pürin ve pirimidin bazları ile pentoz arasındaki bağ: β-n glikozidik bağ camp tarafından aktive edilen enzim: protein kinaz A 120
121 121 cgmp tarafından aktive edilen enzim: protein kinaz G Guanozin nükleotidlerinin görevleri: dihidrobiopterin sentezi, protein sentezi için enerji kaynağı Đnozin monofosfat (ĐMP) içindeki baz: hipoksantin UDP-şeker türevleri glukoz 1-fosfat ve galaktoz 1-fosfatın birbirine dönüşümü gibi epimerizasyon reaksiyonlarında rol alır. UDP-glukoz glikojen sentezinde glukoz donörüdür, diğer UDP-şekerler glikoproteinler ve proteoglikanların sentezine katılır. Sitozin türevleri bazı fosfogliseridlerin ve sfingomyelinin sentezinde gereklidir. 121
122 122 RNA ve DNA sentezine katılan nükleotidler ve yapısında bulunan nükleotidler: nükleozid trifosfatlar ve nükleozid monofosfatlar PÜRĐN VE PĐRĐMĐDĐN NÜKLEOTĐDLERĐNĐN METABOLĐZMASI Nükleoproteinden zengin bir diyet tüketilse dahi diyetteki pürin ve pirimidin bazları doğrudan doku nükleik asitlerine katılmaz. Đnsanda amfibolik ara maddelerden (amino asitler, riboz 5-fosfat, CO2 ve NH3) doku nükleik asitleri, ATP, NAD, FAD ve koenzim A nın yapısında bulunan pürin ve pirimidinler sentezlenir. Bazı antikanser ilaçları pürin ve pirimidin analogları olarak fonksiyon görerek DNA ya inkorpore olabilirler. Đnsanda pürin metabolizmasıyla ilgili hastalıklar arasında gut, Lesch-Nyhan sendromu, adenozin deaminaz yetersizliği ve pürin nükleozid fosforilaz yetersizliği bulunur. Pirimidin biyosentezi hastalıkları arasında ise orotik asidüriler bulunur. Pürin sentezindeki kontrol basamakları: PRPP sentaz ve PRPP glutamil aminotransferaz PRPP sentaz enzimini aktive eden: riboz 5-fosfat Pürin sentezindeki kontrol basamaklarını inhibe edenler: AMP ve GMP Pürin nükleotid sentezinde oluşan ilk nükleotid: ĐMP 122
123 123 Pürin bazlarının halka yapısını oluşturanlar: Glisinin tamamı (iki karbon ve bir azot), 2 glutaminden 2 azot, aspartattan bir azot, 2 tatrahidrofolattan iki karbon, karbondioksitten bir karbon ĐMP den AMP oluşumunu bloke eden ilaç: 6-merkaptopürin Nükleozid difosfatları deoksi haline getiren enzim ve kofaktörü: ribonükleozid redüktaz ve kofaktörü tioredoksin Pürin analogları ve klinik önemi: 6-merkapto-pürin, sitozin arabinozid, metotreksat, azaserin. Bunlar hücre siklusu inhibitörü olarak etki gösterirler ve anti-kanser ilaçlar olarak kullanılabilirler. 123
124 124 Pirimidin sentezinde kontrol basamakları: karbamoil fosfat sentetaz II ve aspartat transkarbamoilaz Karbamoil fosfat sentetaz II i aktive eden: PRPP Pirimidin bazlarının halka yapısını oluşturanlar: Aspartatın tamamı (üç karbon, bir azot), glutaminden bir azot, karbondioksitten bir karbon Pürin ve pirimidin bazlarının halka yapısını oluşturan ortak iki amino asit: aspartat ve glutamin Pürin ve pirimidin nükleotidlerinin yapısına katılan ortak dört bileşen: aspartat, glutamin, karbondioksit ve PRPP dump nin dtmp ye dönüşümünde rol oynayan koenzim: timidilat sentaz, N5-N10 metilen tetrahidrofolat, dihidrofolat redüktaz ve NADPH dump nin metilenmiş formu dtmp dir. Tioredoksin hangi bileşiğin sentezinde indirgeyici rol oynar? deoksiribonükleotidler Lesch-Nyhan sendromunda hücre içinde ve kanda artan bileşikler: hücre içinde PRPP, kanda ürik asit Pürin nükleotidlerinin yıkımında görevli enzimler: adenozin deaminaz, pürin nükleozid fosforilaz ve ksantin oksidaz Allopürinolün etkileri: Ksantin oksidazın inhibisyonu, hipoksantin anoloğu, pürin ve pirimidin sentezinin inhibisyonu, orotik asidüri Ksantin oksidaz enziminin kofaktörleri: molibden, FAD ve demir 124
125 125 Pürin nükleotidlerinin yıkım ürünü ve özelliği: ürik asit ve suda az çözünür olması Gut hastalığında primer defekt: PRPP sentaz enziminin hiper aktivitesi Hiperürisemi nedenleri Gut Lesch-Nyhan sendromu Von Gierke sendromu Böbrek yetmezliği Asidoz Lenfomalar NÜKLEĐK ASĐTLERĐN YAPISI Nükleik asitlerin monomerik birimleri nükleotidlerdir; her bir nükleotid heterosiklik bir azot bazı, bir şeker ve fosfat içerir. DNA; adenin (A), guanin (G), sitozin (C) ve timin (T) bazları içerir. RNA ise A, G, C ve timin yerine urasil (U) içerir. DNA da deoksiriboz, RNA da ise riboz bulunur. Polinükleotidler, 3,5 -fosfodiester köprüleriyle bağlı nükleozidlerden oluşmuştur. Genetik bilgi, polinükleotid zinciri boyunca yerleşmiş baz dizilerinde bulunur. DNA da, iki polinükleotid zinciri birbirlerine bazları arasındaki eşleşmelerle bağlanır (adenin timinle ve guanin sitozinle) ve bir çift heliks oluştururlar. Bir zincir 5 3 yönüne giderken diğer zincir 3 5 yönüne gider. DNA molekülleri histonlarla etkileşime girerek nükleozom iplikleri oluşturur. Bunlar sıkıca sarmalanmış yapılardır. RNA, tek bir sarmaldır fakat sarmallar kendi etrafında dönüş yaparlar ve bazlar birbiriyle eşleşir: guanin, sitozinle ve adenin, urasille. Haberci RNA (mrna), 5 ucunda bir şapka ve 3 ucunda poli (A) kuyruğa sahiptir. Ribozomal RNA (rrna)da yoğun bir baz eşleşmesi bulunur. Transfer RNA (trna), birçok olağan dışı nükleotidler ve bir antikodon içeren karanfil yaprağı yapı oluşturur. Orotik asidüri nedenleri: Ornitin transkarbamoilaz (üre siklusu enzimi) eksikliği, orotat fosforibozil transferaz ve orotidilat dekarboksilaz eksiklikleri pirimidin sentezi enzimleri), allopürinol kullanımı, Reye sendromu DNA çift sarmalında: adenin timinle, guanin sitozinle eşit miktarlarda bulunur. DNA çift sarmalı arasındaki bağ sayıları: adenin ie timin arasında iki, guanin ile sitozin arasında üç hidrojen bağı DNA çift sarmalının erime ısısı: DNA çift sarmalının %50 sinin ısı ile ayrıştığı ısı derecesine erime ısısı denir. DNA çift sarmalında guanin-sitozin miktarı ne kadar fazla ise ısıya direnç o kadar fazladır. 125
126
127 127 Denatürasyon: Alkali veya ısı DNA sarmallarının ayrılmasına yol açar fakat fosfodiester bağları koparmaz. Heliks yapısının yarısının açıldığı ısıya, DNA nın erime derecesi (melting temperature, Tm) denir. A ve T den zengin DNA, G ve C den zengin DNA ya kıyasla daha düşük ısıda denatüre olur. Hibridizasyon: DNA nın tek bir sarmalı, tamamlayıcı başka bir DNA veya RNA sarmalı ile eşleşir. DNA nın yapısında en fazla bulunan protein: Histon proteinleri Histon proteinlerinin özellikleri: arginin ve lizinden zengin bazik proteinler olması Histonlarda görülen modifikasyonlar Asetilasyon Metilasyon Fosforilasyon Kromatin, çok uzun çift sarmallı DNA moleküllerinden ve histon adı verilen bazik proteinlerden oluşur. Transkripsiyonel olarak inaktif kromatin yoğun protein içeren heterokromatindir; transkripsiyonel olarak aktif kromatin daha az protein içeren ökromatindir. Nükleozom nedir? Histon proteinleri (H1 histonu hariç) ve bunları sarmalayan DNA birimleridir. 127
128 128 Kromatin nedir? Yoğun miktarda nükleozom içeren kromozom bölgeleri Mitokondrial DNA (MtDNA): Mitokondri prokaryotlardaki gibi çembersel DNA molekülleri içerir. MtDNA bir kısım oksidatif fosforilasyon proteinlerini, 2 adet rrna ve 22 çeşit trna yı kodlar. Histon proteinleri ve nükleozom içermez. RNA nın özellikleri: Tek sarmal olması; adenin, guanin, sitozin ve urasil içermesi; riboz içermesi, baz eşleşmelerinin birebir olmaması Bazı RNA molekülleri reaksiyonların katalizörü olarak fonksiyon görürler; böylece RNA, proteinler gibi enzimatik aktiviteye sahip olabilir. Okaryotlarda hücresel RNA sınıfları ve özellikleri: rrna (4 adet, tüm RNA ların %80 i), trna (61 adet, tüm RNA ların %15 i), mrna (binlerce, tüm RNA ların %5 i), snrna (10 adet, tüm RNA ların %1 inden az) mrna özellikleri: DNA daki genetik bilgiyi alması, 5 ucunda şapka (metilenmiş GTP) ve 3 ucunda Poli A kuyruğu (200 kadar adenin nükleotidi) içermesi 128
129 129 DNA ve histon proteinlerinin sentezinin gerçekleştiği faz: S fazı trna özellikleri Amino asitleri ribozomlara taşıması En az sayıda nükleotid içermesi Modifiye bazlar içermesi Timin içermesi Antikodon halkası içermesi DNA SENTEZĐ (REPLĐKASYON) DNA sentezi işlemi olan replikasyon, ökaryotlardaki hücre döngüsünün S fazında meydana gelir ve DNA polimeraz enziminin de dahil olduğu bir protein kompleksi tarafından katalizlenir. Ebeveyn (parent) DNA nın her bir sarmalı, tamamlayıcı sarmalının sentezi için bir kalıp görevi görür. DNA polimeraz, kalıp sarmalı 3 5 yönüne doğru kopyalar ve yeni sarmalı 5 3 yönünde sentezler. Deoksiribonükleozid trifosfatlar, prekürsör olarak fonksiyon görür. DNA polimeraz, yeni bir sarmalın sentezini başlatamaz. Kısa bir RNA parçası primer olarak fonksiyon görür. Diğer protein ve enzimler ebeveyn sarmalları çözmek ve her iki sarmalın da aynı anda kopyalanması için gereklidir. Replikasyon esnasında oluşan hatalar, replikasyon kompleksiyle ilişkili enzimler tarafından düzeltilir. DNA moleküllerinde oluşan hasarlar tamir mekanizmaları tarafından düzeltilebilir. Burada hasarlı bölge kaldırılarak hasarsız sarmaldan kopyalanan bölüm yerleştirilir. DNA molekülleri rekombine olabilir. Bir moleküldeki sarmalın bir bölümü diğer moleküldeki sarmalın bir bölümüyle değiştirilebilir. Genler transpoze olabilir (bir kromozomal bölgeden diğerine hareket edebilir). DNA nın her iki sarmalının da aynı anda kalıp görevi gördüğü metabolik olay: replikasyon DNA replikasyonunun (sentezi) özellikleri: semikonservatiftir ve çift yönlüdür. 129
130 130 DNA sentezinde görevli protein ve enzimler: Helikaz Tek sarmal bağlayıcı proteinler Primaz DNA polimeraz Ribonükleaz Topoizomeraz DNA ligaz Deoksiribonükleozit trifosfatlar 130
131 131 DNA sentezinde görev alan enzimlerin etki sırası: Helikaz Primaz (DNA bağımlı RNA polimeraz) DNA polimeraz Ribonükleaz (RNA primerleri kaldırır) DNA ligaz Ökaryotlarda DNA polimeraz çeşitleri: DNA polimeraz α (seken sarmalın sentezi ve boşlukların doldurulması) DNA polimeraz δ (öncü sarmalın sentezi) DNA polimeraz β-ε (tamir) DNA polimeraz γ (mitokondrial DNA sentezi) Prokaryotlarda DNA polimeraz çeşitleri: DNA polimeraz I (görevi α ile aynı) DNA polimeraz III (görevi δ ile aynı) DNA polimeraz II (görevi β-ε ile aynı) Ökaryotlarda DNA replikasyonunda gözlenen basamaklar 1. Replikasyon başlangıcının belirlenmesi 2. dsdna nın çözülmesi (denatürasyonu) ile ssdna kalıbının oluşması 3. Replikasyon çatalının oluşması 4. DNA sentezinin başlaması ve uzama 5. Yeni sentezlenen DNA segmentinin bağlanmasıyla replikasyon kabarcıklarının oluşması 6. Kromatin yapısının oluşması 131
132 132 Topoizomerazlar ebeveyn heliksin aşırı kıvrılmasını önler. - Topoizomerazlar, DNA zincirlerini kırar ve tekrar birleştirir. - DNA giraz, kinolonlar tarafından inhibe edilen bir topoizomerazdır ve sadece prokaryotlarda bulunur. Ökaryotlarda DNA polimeraz hangisine gerek duyar? Bir RNA primere Protein DNA polimerazlar Helikazlar Topoizomerazlar DNA primaz Tek sarmal bağlayıcı protein DNA ligaz Replikasyonda rol alan proteinler Fonksiyonu Deoksinükleotid polimerizasyonu DNA sarmalının çözülmesi Helikazın indüklediği çözülme sonucu oluşan torsiyone sarmalın düzleştirilmesi RNA primerlerin sentezi dsdna nın yeniden oluşmasını önlemek Seken sarmaldaki okazaki parçalarını birleştirmek DNA daki nükleotidleri fosfodiester bağları ile birbirine bağlayan enzim: DNA polimeraz Okazaki parçaları: Seken sarmal üzerinde RNA primere bağlı küçük DNA molekülleridir. Okazaki fragmanlarının sentezlenmesini zorunlu kılan durum: Sentezin mutlaka 5 3 yönünde olması Prokaryotlarda DNA sentezini inhibe edenler: siprofloksasin, nalidiksik asit, novobiosin Baz eksizyon tamirinde DNA daki hasarlı bazı uzaklaştıran enzim: glikozilaz DNA tamir sistemlerinde önemli özellik: hasarlı nükleotid grubu ile yanındaki sağlam nükleotid uzaklaştırılır. DNA daki hasarlı bazların uzaklaştırıldığı tamir sistemi: baz eksizyon tamiri DNA tamiri - Genellikle tamir işleminde hasarlı bölge içeren DNA segmenti ile onun yanındaki sağlam nükleotid kaldırılır ve bir kalıp olarak hasarsız kardeş zinciri kullanan DNA polimerazın etkisiyle boşluk doldurulur ve yeni sentezlenen segment mevcut zincire bağlanır. - Endonükleazlar, ekzonükleazlar, bir DNA polimeraz ve bir ligaz tamir için gereklidir. Endonükleazlar molekül içindeki spesifik DNA dizisinde DNA yı keserler. Ekzonükleazlar ise molekülün terminal ucundaki nükleotidi hidroliz eder. DNA polimeraz β ve ε (tamir enzimleri) oluşan boşluğu uygun nükleotid ile doldurur. DNA ligaz iki DNA segmentini birleştirir. Endonükleaz ve ekzonükleazlar sırayla: bir polinükleotidin iç tarafındaki ve uç tarafındaki fosfodiester bağlarını parçalar. 132
133 133 Reverse transkripsiyon 1. Bir RNA kalıbından DNA sentezi, reverse transkriptaz tarafından katalizlenir. 2. Retroviruslar genetik materyel olarak RNA içerir. a. Retroviral RNA, reverse transkriptaz (RNA-bağımlı DNA polimeraz) tarafından DNA sentezi (cdna) için bir kalıp olarak fonksiyon görür. Bu enzim öncelikle RNA-DNA hibrid molekülünü sentezler. RNaz RNA sarmalını parçalar, geriye kalan DNA sarmalı kalıp fonksiyonu görür ve çift sarmallı DNA oluşur. b. Oluşan DNA, konak hücrenin genomuna (kromozomuna) yerleşebilir. DNA dan UV ışığın neden olduğu timin dimerlerinin kaldırıldığı tamir sistemi: nükleotid eksizyon tamiri Nükleotid eksizyon tamirinde gözlenen bozukluk: kseroderma pigmentozum Mismatch tamir sisteminde (uyumlu olmayan nükleotid gruplarının çıkarılması) gözlenen bozukluk: herediter nonpolipozis kolon CA Nükleotid ekzisyon veya mismatch tamirinde görevli enzimlerin etki sıraları: endonükleaz, ekzonükleaz, DNA polimeraz, DNA ligaz Telomer nedir? Kromozomların her iki ucunda genetik bilgi içermeyen DNA birimleri. Hücrenin her bölünmesinde kısalır ve azaldıkça hücre yaşlanır. 133
134 134 RNA SENTEZĐ (TRANSKRĐPSĐYON) Transkripsiyon, RNA polimeraz tarafından katalizlenen bir DNA kalıbından RNA sentezidir. RNA polimeraz, bir DNA kalıbını 3 5 yönünde kopyalar ve 5 3 yönünde tek sarmallı bir RNA molekülü sentezlenir. DNA polimerazın tersine RNA polimeraz, yeni sarmalların sentezini başlatabilir. Ökaryotlarda, transkripsiyonun primer ürünü, protein sentezine katılmadan önce modifiye olur ve düzeltilir. RNA polimeraz II tarafından üretilen ökaryotik haberci RNA nın 5 ucuna bir şapka takılır ve 3 ucuna poli(a) kuyruğu ilave olur. Đntronlar (protein kodlamayan bölümler) kaldırılır ve eksonlar (matür mrna, protein üreten bölümler) birbirine eklenir. Ökaryotik ribozomal RNA, RNA polimeraz I tarafından nükleolusta üretilir. Bu işlemde 45S prekürsör metillenir ve ribozomlarda bulunan üç rrna yı (18S, 28S ve 5.8S) oluşturmak üzere parçalanır. 5S RNA, RNA polimeraz III tarafından ayrı bir genden nükleusta üretilir. Ökaryotik transfer RNA, RNA polimeraz III tarafından 5 ve 3 uçlarından kesilen bir prekürsör olarak üretilir, intronlar kaldırılır ve eksonlar birbirine eklenir. - Normal nükleotidlerin posttranskripsiyonel modifikasyonu ile matür trna da olağan dışı nükleotidler üretilir ve bir CCA dizisi, 3 ucuna eklenir. Ökaryotik RNA, translasyon için nükleustan sitoplazmaya geçmelidir. Bakteriler nükleus içermez, dolayısıyla transkripsiyon ve translasyon eş zamanlı olarak gelişir. Bakterilerde tek bir RNA polimeraz mrna, rrna ve trna yı üretir. Bakteriyel transkriptler (örn. E. Coli dekiler) intron içermez. Telomerazın görevi: Telomer sentezi. Yaşlanma ve malignansi ile ilişkilidir. Ökaryotik hücrelerde telomeraz enziminin bulunmasını zorunlu kılan yapısal özellik: Kromozomların lineer olması RNA sentezini gerçekleştiren enzim ve kofaktörü: RNA polimeraz ve çinko Prokaryotlarda RNA polimeraz enzimi: iki alt birimden oluşur. σ faktörü ve çekirdek enzim. Her üç RNA yı da aynı enzim sentezler. RNA polimeraz enziminin DNA da bağlandığı bölge: promoter bölge (kopyalanacak bölgenin önündeki özel DNA bölgesi) Prokaryotlarda RNA sentezinin sonlanmasını sağlayan faktör: Rho faktörü (ökaryotlarda nasıl sonlandığı bilinmiyor) 134
135 135 Prokaryotlarda mrna polisistronik bir transkript halinde sentezlenir. Sistron nedir? Bir proteinin sentezinden sorumlu mrna bölgesi Ökaryotlarda kaç adet RNA polimeraz bulunur? 3 adet RNA polimeraz I:Nükleolusta 45S rrna prekürsörünü sentezler. RNA polimeraz II: Nükleusta mrna nın prekürsörü olan hnrna yı sentezler RNA polimeraz III: Nükleusta trna ve 5S rrna yı sentezler 135
136
137 137 Đntron içeren RNA: hnrna (pre-mrna) Đntron: Protein sentezinde rol oynamayan RNA bölgeleri, genellikle eksonlardan daha uzundur, kesilme (splicing) ile uzaklaştırılır., Spliceosome: Đntron-ekson kavşağında hnrna ile ilişkili small nuclear ribonükleoprotein partikülleri spliceosome u oluşturur. Ribozimler: RNA yapısındaki enzimlerdir. Örn. Ribonükleazlar, snrna (spliceosome), peptidil transferaz Post-transkripsiyonel modifikasyonlar: Đntronların kaldırılması, 5 uca şapka eklenmesi, 3 uca kuyruk eklenmesi, metilasyon PROTEĐN SENTEZĐ (mrna NIN TRANSLASYONU) Translasyon esnasında haberci RNA (mrna), üretilen proteindeki amino asitin dizilimini belirler. mrna, rrna içeren ribozomlarla birleşir. Bir çok ribozom eş zamanlı olarak tek bir mrna molekülüne bağlanarak bir polizom oluşturur. trna, amino asitleri protein sentezinin ribozomal bölgesine taşır. Her bir amino açil trna nın antikodonu, mrna daki tamamlayıcı kodonla birleşir. Bir kodon, özel bir amino asiti belirleyen mrna daki üç nükleotid dizisidir. Bir polipeptid zinciri sentezinin başlaması metionin amino asitiyle (kodon=aug) gerçekleşir. Daha sonra amino asitler, büyüyen polipeptid zincirine mrna daki kodon dizisine göre eklenir. Amino açil trna lar ve GTP, zincir uzaması için gerekli olan enerjiyi sağlar. mrna daki kodonlar 5 3 yönüne ilerlerken bir protein N-ucundan C-ucuna doğru sentezlenir. Polipeptid sentezi tamamlandığında, bir sonlanma kodonu (UGA, UAG veya UAA) polipeptid zincirinin serbestleşmesine yol açar. Ribozomların sentez bölgesi: nükleolus RNA sentez inhibitörleri: Rifampisin, aktinomisin, mitomisin, amanitin Aktinomisin D ve mitomisin DNA sarmalları ile interkalasyon yapar, böylece hem replikasyon, hem de transkripsiyon inhibe olur. Kanser kemoterapisinde kullanılırlar. Kodon nedir? mrna üzerinde 3 dizelik nükleotidlere kodon denir. Başlama kodonu: AUG (metionin trna ya spesifik) Sonlanma kodonu: UAA,UAG,UGA Mutasyonların proteinlerdeki etkisi - DNA daki mutasyonlar mrna ya kopyalanır ve böylece proteinlerin kodlanmasında değişikliklere neden olabilir. - DNA da oluşan çeşitli tipteki mutasyonların protein kodlanmasında farklı etkileri vardır. GENETĐK KOD Birinci Baz Đkinci Baz Üçüncü Baz (5 ) U C A G (3 ) Phe Ser Tyr Cys U U Phe Ser Tyr Cys C Leu Ser Term Term A Leu Ser Term Trp G Leu Pro His Arg U C Leu Pro His Arg C Leu Pro Gln Arg A Leu Pro Gln Arg G IIe Thr Asn Ser U A IIe Thr Asn Ser C IIe Thr Lys Arg A Met Thr Lys Arg G Val Ala Asp Gly U G Val Ala Asp Gly C Val Ala Glu Gly A Val Ala Glu Gly G 137
138 Nokta mutasyonları DNA daki bir baz bir diğeriyle değiştiğinde oluşur ve mrna daki kodonu değiştirir. a. Sessiz mutasyonlar bir proteinin amino asit dizisini etkilemez (örn. CGA CGG değişikliğe yol açmaz, çünkü her iki kodon da arginin için spesifiktir). b. Yanlış (missense) mutasyonlarda bir amino asit bir diğeriyle yer değiştirir (örn.cga CCA da, argininin yerine prolin geçer.) c. Saçma (nonsense) mutasyonlarda büyüyen polipeptid zinciri erkenden sonlanır (örn. CGA UGA da argininin yerine sonlanma kodonu geçmiştir). 2. Đnsersiyonlar bir baz veya bir kısım bazlar DNA ya eklendiğinde gözlenir. Normalden daha fazla amino asitli bir proteinin sentez edilmesiyle sonuçlanır. 3. Delesyonlarda bir baz veya bir kısım bazlar DNA dan kaldırılır. Normalden daha az amino asitli bir proteinin senteziyle sonuçlanır. 4. Çerçeve kayması mutasyonları eklenen veya kaldırılan baz sayısının üçün katları olmadığı durumlarda gözlenir. Okunan çerçeve kaymıştır, öyle ki mutasyonun başladığı noktanın ötesinde tamamen farklı kodon dizileri okunur. Mutasyonlar: DNA üzerinde bir nükleotidin başka bir nükleotid ile yer değiştirmesi. Örn. Tranzisyon ve transversiyon Tranzisyon: DNA da pürin pürinle veya pirimidin pirimidinle yer değiştirmesi Transversiyon: DNA da pürin pirimidinle veya pirimidin pürinle yer değiştirmesi Protein sentezinde amino asitler trna nın 3 hidroksil ucuna karboksil grupları üzerinden bağlanırlar. Amino asitlerin trna ya bağlanabilmesi için gerekenler: ATP ve aminoaçil trna sentetaz enzimi 138
139 139 DNA daki AAA nın t-rna daki antikodon karşılığı: AAA (aynısıdır) Prokaryotlarda başlama kodonu: formil metionil trna Protein sentezinin başlama kompleksinin oluşması için gerekenler Büyük ve küçük ribozomal alt birimler met. trna mrna Başlama faktörleri ATP ve GTP Protein sentezinin uzama reaksiyonlarında gerekenler peptidil transferaz uzama faktörleri 1 ve 2 GTP Amino asit taşıyan trna lar 139
140 140 Protein sentezinin sonlanması için gerekenler: sonlanma kodonu, salınım faktörü Polizom nedir? Ökaryotlarda mrna ya birden fazla ribozomun bağlanmış halidir. Operon nedir? Prokaryotlarda DNA üzerinde yapısal genler ve önündeki promoter bölgeye denir. 140
141 141 PROTEĐN SENTEZĐNĐN REGÜLASYONU Prokaryotlarda protein sentezinin regülasyonu başlıca transkripsiyonel düzeyde gerçekleşir ve bu regülasyonda operonlar olarak bilinen genetik birimler rol oynar. - Operonlar, proteinlerin bağlandığı ve RNA polimerazın bağlanmasını kolaylaştıran veya inhibe eden promoter bölgeler içerir. - RNA polimeraz, bir operonun yapısal genlerini kopyaladığı zaman, polisistronik bir mrna (örn. birden fazla polipeptid kodlayan bir mrna) üretir. Ökaryotlarda protein sentezinin regülasyonu, DNA nın modifikasyonuyla veya transkripsiyon (mrna nın işlenmesi) veya translasyon düzeyinde gelişir. - Genler hücrelerden çıkarılabilir veya yükseltgenebilir, yeniden düzenlenebilir veya modifiye edilebilir (örn. metil grubu eklenebilir). - Histonlar genlerin transkripsiyonunu baskılarlar. - DNA dizilerindeki düzenleyici elemanlar proteinlerini üreten genlerin ekspresyonunu kontrol ederler. Bunlar arasında bazal promoter (TATA kutusu başlama noktasındaki diğer diziler), arttırıcılar ve susturucular bulunur. - Đndükleyiciler, proteinlerin DNA dizisine bağlanmasına ve spesifik genlerin uyarılmasına neden olurlar. - Regülasyon, mrna oluşturmak üzere hnrna nın işlenmesi esnasında oluşur ve transkripsiyon için alternatif başlama bölgeleri, intronların kaldırılması için alternatif bağlama bölgeleri, poli(a) kuyruğunun eklenmesi için alternatif poliadenilasyon bölgeleri kullanılır. - Proteinlerin sentezi translasyon düzeyinde regüle edilebilir. Operatör nedir? Prokaryotlarda repressör molekülün promoter bölgede bağlandığı yerdir. Repressör operatöre bağlanarak promoter bölgeye RNA polimerazın bağlanmasını önler. Dolayısıyla protein sentezi baskılanır. Hangi bölgedeki mutasyon devamlı protein sentezine neden olur? operatör Đndükleyici nedir? Repressör moleküle bağlanarak onu inhibe eden dolayısıyla protein sentezinin uyarılmasını sağlayan moleküldür. 141
142 142 Steroid hormon reseptörlerine bağlanan koaktivatörlerde histonlar histon asetiltransferaz enzimi ile lizil artıkları üzerinden asetillenir, pozitif yükleri ve dolayısıyla negatif yüklü DNA ya bağlanma afiniteleri azalır. Sonuçta nükleozomun yapısı bozulur, transkripsiyon faktörleri devreye girer ve gen ekspresyonu başlar. Histon deasetilasyonu ise ters etkiye sahiptir. Puromisin in etkisi : Tirozin taşıyan trna anoloğudur. Hem prokaryot hem de ökaryotlarda amino açil trna nın A bölgesine bağlanmasını inhibe eder. Sikloheksimid in etkisi: Ökaryotlarda peptidil transferazın inhibisyonu Eritromisinin etkisi: Prokaryotlarda translokasyonun inhibisyonu Kloramfenikolün etkisi: Prokaryotlarda peptidil transferazın inhibisyonu Onkosüpressör bir genin delesyonu sonucu oluşan bir kanser: retinoblastoma Onkojen ve proto-onkojenler: Kansere neden olan genlere onkojen, normal hücrelerde bulunan onkojenlere protoonkojen adı verilir. Proto-onkojenler viral enfeksiyonlarla, proto-onkojendeki mutasyonla, promoter insersiyonu ve kromozom translokasyonu ile aktive olur. Onkojenler kansere neden olan genlerdir. Normal hücrelerdeki karşılıkları olan proto-onkojenler normal büyüme ve gelişmede rol oynarlar. Şayet onkojenler değiştirilişe veya yanlış yorumlanırsa kanser gelişebilir. Birçok onkojenler büyüme faktörleriyle ilişkili proteinleri kodlar. Bazı onkojen ürünleri nükleusa girer ve genleri aktive eder. Onkojen teorisine göre virüsler iki şekilde kansere neden olurlar: 1) Proto-onkojenlerin anormal veya ilave kopyalarını hücre içine yerleştirmek; 2) Bu genlerin ekspresyonunu düzenleyen bölgelere güçlü promoterleri yerleştirmek. Kanser ayrıca hücre büyümesinin süpressörleri olarak etki eden proteinleri üreten genlerdeki değişiklikler sonucu da gelişebilir. Streptomisinin etkisi: Prokaryotlarda mrna nın hatalı okunmasını sağlamak Streptomisinin etkisi: Prokaryotlarda mrna nın hatalı okunmasını sağlamak Rifampisinin etkisi: Prokaryotlarda RNA polimerazı inhibe etmek Bakterilerde protein sentezinin irreverzibl inhibitörü: Aminoglikozidler (örn. Streptomisin). Kloramfenikol, tetrasiklin, eritromisin, klindamisin protein sentezini reverzibl inhibe ederler. Hidroksiüre hematolojik malignansilerde kullanılan antineoplastik ilaçtır. Antiretroviral (örn. HIV) ajan olarak da kullanılır. Ribonükleotid redüktaz enzimini inhibe ederek DNA sentezini baskılar. cdna sentezini gerçekleştiren enzim: reverse transkriptaz. Retrovirüsler RNA virüsü olup RNA bağımlı DNA polimeraz aktivitesine sahip olan bu enzimi içerirler. Sonuçta cdna sentezi gerçekleşir, konakçı genomuna girerek virüs proteinleri sentezlenir. Rekombinant DNA tekniği ile ilaç olarak üretilen molekül: protein Adriamisinin etki mekanizması: topoizomeraz inhibitörü Mitomisinin etki mekanizması: DNA sarmallarıyla interkalasyon Prob: DNA veya RNA daki spesifik bir parçayı belirlemek için kullanılan bir molekül. Sık kullanılan problar cdna molekülleri, tanımlanmış sentetik oligodeoksinükleotidler veya spesifik proteinlere karşı geliştirilmiş antikorlardır. Southern blotting nedir ve kullanım alanı: DNA izole edilir, restriksiyon endonükleazlarla parçalara ayrılır, kesilmiş parçalara agaroz jelde elektroforez uygulanır sonra nitrosellülöz membrana aktarılır, membran üzerine radioaktif prob yerleştirilir ve sonunda otomatik radyografisi çekilir. Southern blotting anormal genleri belirlemek, virüs integrasyonunu göstermek ve prenatal tanı (örn. Orak hücre anemisi, Huntington chorea, Duchenne muscular dystrofi) amacıyla kullanılır. Gen amplifikasyonunda kullanılan teknik: PCR (Polimeraz chain reaction) PCR da kullanılan enzim: Taq polimeraz Northern blotting spesifik RNA yı göstermek için kullanılır. Agaroz jelden nitrosellülöz filtreye RNA transfer edilir ve uygun bir probla belirlenir. Western blotting proteinleri (nükleik asitleri değil) belirler. Proteinler dokudan izole edilir ve elektroforez uygulanır. Ayrılmış proteinler nitrosellülöz membrana aktarılır, uygun bir radioaktif antikorla problanarak belirlenir. VĐTAMĐNLER 142
143 143 Vitaminler, çeşitli biyokimyasal reaksiyonların yürümesi için az miktarda gereken organik besin maddeleridir. Vitaminler vücutta sentezlenemez, bu nedenle diyetle alınmalıdır. Yağda veya suda çözünür oluşlarına göre vitaminler sınıflandırılır. C vitamini hariç suda çözünen vitaminler, B kompleks vitaminlerinin üyeleridir ve enzimlerin kofaktörleridir. Tiamin, alfa-keto asitlerin oksidatif dekarboksilasyonunda ve pentoz fosfat yolunun önemli bir enzimi olan transketolazın bir kofaktörüdür. Riboflavin ve niasin, oksidasyon-redüksiyon reaksiyonlarında önemli kofaktörlerdir. - Riboflavin, flavoprotein enzimlerinde (flavin mononükleotid ve flavin adenin dinükleotid) prostetik grup olarak bulunur., - Niasin, bir çok dehidrogenaz enzimlerinin kofaktörü olan NAD+ ve NADP+ nin yapısında bulunur Pantotenik asit, koenzim A da ve bir çok önemli reaksiyonda açil gruplarının taşınmasında rol oynayan açil taşıyıcı proteinde bulunur. Piridoksal fosfat, transaminazlar dahil amino asit metabolizması ile ilgili çeşitli enzimlerin kofaktörüdür. Biotin, çeşitli karboksilaz enzimlerinin kofaktörüdür. Bunlar arasında lipogenezde hız sınırlayıcı bir enzim olan asetil KoA karboksilaz ve glukoneogenezde önemli olan piruvat karboksilaz bulunur. B12 ve folik asit, çeşitli farklı fonksiyonlara sahip olmakla beraber nükleik asit sentezinde bir karbonlu birimlerin sağlanmasında rol oynarlar. Askorbik asit suda çözünen bir antioksidandır ve bir çok metal kofaktörün indirgenmiş halde tutulmasını sağlar. Yağda çözünen vitaminler apolar, hidrofobik moleküllerdir ve izopren türevleridir. Bağırsaktan etkili bir şekilde absorbe olabilmeleri için normal yağ emiliminin olması gerekir. Bu mekanizmada bir defekt olursa eksiklik semptomları gelişebilir. A vitamini (retinol) sadece diyette değil bitkilerdeki provitaminde (Beta-karoten) de bulunur. Retinol ve retinoik asit genler üzerinden etkili olurken retinal, görmede kullanılır. D vitamini, bir steroid prohormondur ve aktivitesi kalsitriol adı verilen türevi üzerinden gerçekleştirilir. Kalsiyum ve fosfat metabolizmasının regülasyonunda kullanılır ve diyetteki yokluğu rikets ve osteomalasiye yol açar. E vitamini (tokoferol), vücuttaki en önemli antioksidandır ve membranların lipid fazına etkilidir, toksik radikallerin etkilerine karşı koruyucudur. Poliansatüre yağların alımı arttıkça tokoferol gerekliliği de artar. K vitamini, çeşitli pıhtılaşma faktörlerinin (örn. II, VII, IX ve X) sentezinde gereklidir. - Pıhtılaşma faktörü protein prekürsörleri üzerinde bulunan glutamat artıklarının karboksillenmesinde, kofaktör olarak fonksiyon görür. - Dikumarol (varfarin) türü bileşiklerle SUDA ERĐYEN VĐTAMĐNLER B kompleks vitaminleri enzimatik reaksiyonlarda kofaktördür. Đnsan beslenmesi için esansiyel olan B vitaminleri: (1) tiamin (Bı vitamini), (2) riboflavin (B2 vitamini), (3) niasin (nikotinik asit, nikotinamid) (B3 vitamini), (4) pantotenik asit (B5 vitamini), (5) B6 vitamini (piridoksin, piridoksal, piridoksamin), (6) biyotin, (7) B12 vitamini (kobalamin), ve (8) folik asit (pteroilglutamik asit) - Suda çözünür oluşlarından dolayı bu vitaminlerin fazlalıkları idrarla atılır, nadiren toksik düzeylerde birikirler. Kobalamin hariç sınırlı miktarda depolanırlar. 143
144 144 Alkolün bağırsaklardan emilimini önlediği vitamin: tiamin Alkoliklerde gözlenen Wernicke ensefalopatisi hangi vitamin eksikliğine bağlı gelişir? Tiamin Ketoasitlerin oksidatif dekarboksilasyonunda gerekli olan vitamin: tiamin pirofosfat 144
145 145 Riboflavin eksikliğini araştırmada kullanılan enzim: eritrosit glutatyon redüktaz Oksidasyon-redüksiyon reaksiyonlarında kullanılan vitaminler: riboflavin ve niasin Triptofandan NAD+ sentezinde kullanılan vitamin: Piridoksal fosfat Pellegra semptomlarının geliştiği durumlar: Niasin eksikliği Vitamin B6 eksikliği Karsinoid sendrom Hartnup sendromu Diyette lösin fazlalığı Đzoniazid kullanımı Pantotenik asitin yapısı: β-alanin ve pantoik asit Koenzim A nın yapısına katılanlar: Pantotenik asit, tioetanolamin, adenin, riboz, fosfor 145
146 146 Piridoksal fosfatın (B6 vitamini) rol oynadığı reaksiyonlar: amino asitlerin transaminasyon, dekarboksilasyon ve deaminasyon reaksiyonları, ALA sentaz, sistationin sentaz ve sistationaz reaksiyonları, kas glikojen fosforilaz reaksiyonu B6 vitamini eksikliğinde idrarla atılan bileşik: ksanturenik asit Aktif formu fosfat içeren vitaminler: tiamin, riboflavin, niasin, pantotenik asit, piridoksal ve vitamin B12 Aktif formu adenozin monofosfat türevi içeren vitaminler: riboflavin, niasin, pantotenik asit, vitamin B12 Vücutta sentezlenebilen vitaminler: niasin, biotin, D vitamini, K vitamini Karboksilasyon reaksiyonlarında görevli olan vitamin: biotin Biotin eksikliğinde idrarla atılan bileşikler: laktat ve propionat Yapısında kobalt (eser element) içeren vitamin: B12 Suda çözünen vitaminler arasında önemli miktarlarda depolanan tek vitamin: B12 vitamini 146
147 147 B12 vitamininin görev aldığı reaksiyonlar: metilmalonil KoA süksinil KoA (kofaktör: adenozil kobalamin; yer: mitokondri); homosistein metionin (kofaktör: metilkobalamin; yer: stoplazma) Bağırsaklardan emilimi için pankreas bikarbonat sekresyonuna gerek duyulan vitamin: B12 Vitamin B12 eksikliğinde görülenler: metilmalonik asidüri, metil malonik asit birikimi, myelin kılıfının kesintiye uğraması ve sinir iletiminde aksamalar, homosistinüri, megaloblastik anemi Folik asitin kimyasal yapısı hangisidir? Pteridin + PABA + glutamik asit Metotreksatın etki mekanizması: dihidrofolat redüktazı inhibe eder ve güçlü anti-kanser ilaçtır. 147
148 148 Aktif formu vücuda alındığı şekli ile etkili olan vitaminler: askorbik asit ve biotin C vitamininin katıldığı reaksiyonlar: Kollajen sentezi (prolil hidroksilaz basamağı) Katekolamin sentezi (dopamin β-hidroksilaz basamağı) Safra asiti sentezi (7α-hidroksilaz basamağı) Tirozinin yıkımı Demirin emilimi, böbreküstü bezi hormonlarının sentezi Antioksidan YAĞDA ÇÖZÜNEN VĐTAMĐNLER Yağda çözünen vitaminler apolar, hidrofobik moleküllerdir ve tümü izopren türevleridir. Vücutta yeterli miktarda sentezlenemezler ve bu nedenle diyetle alınmalıdırlar. Sadece normal yağ emilimi gerçekleştiğinde absorbe olabilirler. Absorbe olduktan sonra kanda lipoproteinler içinde veya spesifik bağlayıcı proteinlere bağlı halde taşınırlar. Başlangıçta sadece bir vitamin oldukları düşünülüyor ise de D vitamini gerçekte bir prohormondur. A vitamini prekürsörü: β karoten Karaciğerde depolanan ve teratojenik özelliğe sahip olan vitamin: A vitamini A vitamini türevlerinin fonksiyonları: retinol üremeden, retinal görmeden, retinoik asit büyüme ve farklılaşmadan sorumludur. 148
149 149 Düşük oksijen basıncında antioksidan etki gösteren vitamin: A vitamini Retinol bağlayıcı protein sentezi enfeksiyonlarda azalır (negatif akut faz reaktanı). Sonuçta dolaşımdaki vitamin A azalır ve immün yanıt daha da bozulur. 149
150 150 Hangi vitamin bir prohormon olarak fonksiyon gösterir? D vitamini Yağda çözünen vitaminler arasında en toksik olanı: D vitamini Hangisi D3 vitaminidir? Kolekalsiferol D vitamininin etkileri: Kemikten kalsiyum ve fosfatın rezorpsiyonu, bağırsaklardan kalsiyum ve fosfatın geri emilimi, böbrekten kalsiyumun geri emilimi 1α-hidroksilaz (böbrekte bulunur) üzerine etkili olan bileşikler: kalsiyum düşüklüğü, fosfat düşüklüğü ve parathormon fazlalığı enzimi aktive eder, kalsitriol (1,25-dihidroksikolekalsiferol) fazlalığı inhibe eder. Böbrek hastalıklarında oral D vitamini alınması niçin etkili olmayabilir? D vitamininin hidroksilasyonu ve aktivasyonu böbrekte gerçekleşir. Kalsitriol fazlalığında 25 hidroksi vitamin D3 hangi bileşiğe dönüşür? Böbrekte 24 hidroksilaz tarafından inaktif bir metabolit olan 24,25-dihidroksi vitamin D3 e dönüşür. Yüksek oksijen basıncında antioksidan etkili vitamin: E vitamini Glutatyon peroksidaz (kofaktörü selenyum) ile sinerjik etki gösteren vitamin: E vitamini 150
151 151 Poliansatüre yağ asitlerini peroksidasyondan koruyan vitamin: E vitamini Abetalipoproteinemide eksikliği gözlenen vitamin: E vitamini (şilomikron ve VLDL içinde kanda taşınır) Eksikliğinde yeni doğanlarda hemolitik anemiye neden olan vitamin: E vitamini Vitamin K eksikliğinde, protein üzerinde oluşumu gerçekleşmeyen amino asit: Gama-karboksiglutamat Eksikliğinde osteoporoza ve kanamaya eğilimi arttıran vitamin: K vitamini Bazı pıhtılaşma faktörlerinin ve bir kemik proteini olan osteokalsinin karboksilasyonunda rol oynayan vitamin: K vitamini HORMONLAR 151
152 152 * Hücreler arası haberleşme insan yaşamı için çok önemlidir ve başlıca sinir ve endokrin sistemler tarafından sağlanır. * Endokrin bezler, etki edecekleri diğer dokulara kan yoluyla giden hormonlar üretir. * Hormonların moleküler düzeyde etkileri reseptörlerle gerçekleşir. * Polipeptid hormonlar ve epinefrin, hücre membranındaki reseptörlerle reaksiyona girerek hücreiçi bileşiklerin (ikincil haberciler) yapı ve konsantrasyonunda bir değişikliğe yol açarlar. Sonuçta hormondan gelen dış uyaran, hücre içi etkilere neden olur. * Steroid hormonlar (ayrıca tiroid hormonu, 1,25-dihidroksikolekalsiferol ve retinoik asit) hücre membranını geçer ve hücre içi reseptörlere bağlanır. Sonuçta hormon-reseptör kompleksi DNA ya bağlanır ve fizyolojik etkilere sahip olan proteinleri üretecek genleri aktive veya inaktive eder. * Hormonlar sıklıkla kimyasal habercilerin bir zinciri gibi davranır. Örneğin, hipotalamus tarafındanüretilen bir hormon, ön hipofizi uyararak çeşitli hormonların salınmasına yol açar. Bunlar da endokrin bezden hedef hücreler üzerinde etkili olacak diğer bir hormonu üretir. Steroid hormonların sentezinde kontrol basamakları: star (steroid akut regülatuar protein) ve desmolaz (mitokondrial yan zincir parçalayıcı enzim) enzimi ACTH kortizol biyosentezinde hangi basamakta etkili olur? Kolesterol pregnenolon HORMONLARIN SENTEZĐ Bir amino asit, bir hormon olarak fonksiyon gören bir bileşiğe çevrilebilir (örn.epinefrin, tiroid hormonu) veya bir grup, amino asitler peptid bağlarıyla birleşerek bir polipeptid hormonu oluştururlar (örn. insülin, prolaktin). Steroid çekirdeği çeşitli hormonları üretmek üzere biyokimyasal olarak değişikliğe uğrayabilir (örn. progesteron, kortizol). Böbrek üstü bezinde sentezlenen en potent glukokortikoid: kortizol Sadece zona glomerulozada bulunan enzim: 18 hidroksilaz (aldosteron sentaz) 152
153 153 Östrojen sentezine özgü hidroksilaz: aromataz Böbrek üstü bezinde sentezlenen en potent mineralokortikoid: aldosteron 21 karbonlu hormononlar: pregnenolon, progesteron, kortizol, aldosteron ve bunların sentezinde yer alan ara bileşikler 19 karbonlu hormonlar: androjenler 18 karbonlu olup aromatik halkaya sahip hormonlar: östrojenler Estriol sentezinde görevli enzim ve bulunduğu doku: 16α-hidroksilaz ve fetal karaciğer Kadında over Theca hücreleri androstenedion ve testesteron kaynağıdır. Bunlar aromataz enzimi ile granuloza hücrelerinde sırasıyla estron ve estrodiole çevrilir. Progesteron bir miktar estradiol de üreten korpus luteum tarafından üretilir ve salınır. Önemli miktarda estrojenler androjenlerin periferal aromatizasyonu ile üretilir. Aromataz aktivitesi adipoz hücrelerinde, karaciğerde, deride ve diğer dokularda bulunur. HORMON ETKĐSĐNĐN GENEL MEKANĐZMALARI Hormonlar hücre içinde veya hücre membranında bulunan reseptörlerle etkileşime girerler. Hücreler bir çok hormonla karşılaşırlar. Bilinen bir hormonun bir hücrede etki yapıp yapamayacağı hücrenin ilişkili reseptörleri içerip içermediğine bağlıdır. 153
154 154 Polipeptid bir hormon olan insülin, hücre membranındaki insülin reseptörlerine bağlanarak tirozin artığı üzerinde reseptörün kendisini fosforillemesine neden olur. Ve sonra hücre içi proteinler fosforillenerek hücresel cevapla sonuçlanan bir seri olaylar başlar. Genellikle diğer polipeptid hormonlar ve epinefrin ikincil habercil aracılığıyla etki gösterir. Hormon (ilk habercil) hücre membranındaki reseptörlerle reaksiyona girerek ikincil habercil olarak bilinen bileşiklerin (örn. siklik AMP (camp), siklik GMP (cgmp), inozitol trifosfat (IP3), diaçilgliserol (DAG) ve Ca2+) hücre içi konsantrasyonunu değiştirir. Bu ikincil haberciler hormondan gelen dış uyaranın hücre içi etkilere yol açmasını sağlarlar. Steroid ve tiroid hormonlar, 1,25-DHC ve retinoik asit hücre membranını geçerek genleri aktive veya inaktive eden kompleksler oluşturur. ETKĐ MEKANĐZMALARINA GÖRE HORMONLARIN SINIFLANDIRILMASI I. Hücre içi reseptörlere bağlanan hormonlar Androjenler Kalsitriol (1,25(OH)2-D3) Östrojenler Glukokortikoidler Mineralokortikoidler Progestinler Retinoik asit Tiroid hormonları (T3 ve T4) II. Hücre yüzey reseptörlerine bağlanan hormonlar A. Đkincil habercisi camp olanlar 1. Adenilat siklazı uyaranlar Glukagon ß Adrenerjik katekolaminler Adrenokortikotropik hormon (ACTH) Paratiroid hormon (PTH) Tiroid stimülan hormon (TSH) Antidiüretik hormon (ADH) Kalsitonin Human koryonik gonadotropin (hcg) Kortikotropin releasing hormon (CRH) Follikül stimülan hormon (FSH) Luteinize edici hormon (LH) Melanosit stimülan hormon (MSH) 2. Adenilat siklazı inhibe edenler Anjiyotensin II Alfa2-Adrenerjik katekolaminler Somatostatin Asetilkolin B. Đkincil habercisi cgmp olanlar Atrial natriüretik peptid (ANP) Nitrik oksit (NO) C. Đkincil habercisi kalsiyum veya fosfatidilinozitol (veya her ikisi) olanlar Asetilkolin (muskarinik) α1-adrenerjik katekolaminler Anjiyotensin II Antidiüretik hormon (ADH) Kolesistokinin Gastrin Gonadotropin releasing hormon (GnRH) Oksitosin Platelet-kökenli büyüme faktörü (PDGF) Substance P Tirotropin-releasing hormon (TRH) 154
155 155 D. Đkincil habercisi bir kinaz veya fosfataz şelalesi olanlar Koryonik somatomammotropin Epidermal büyüme faktörü (EGF) Eritropoietin Büyüme hormonu (GH) Đnsülin Đnsülin-benzeri büyüme faktörleri (IGF-I, IGF-II) Prolaktin (PRL) Böbrek üstü bezinde sentezlenen en potent androjen: testosteron Böbrek üstü bezinde en fazla sentezlenen androjen: DHEA Testosteronu dihidrotestosterona çeviren enzim: 5α-redüktaz Androjenlerden östrojen sentezinde rol alan enzim: aromataz Fertil dönemdeki kadında başlıca östrojen formu: estradiol (E2) Gebelik dönemindeki başlıca östrojen formu: estriol (E3) Menopozal dönemde bulunan başlıca östrojen formu: estron (E1) Tirozin kinaz reseptörleri üzerinden etkili olan hormonlar: intrensek tirozin kinaz üzerinden etkili olanlar (insülin, ĐGF, epidermal büyüme faktörü), solubl tirozin kinaz (Tyk-2, JAK-STAT) üzerinden etkili olanlar (büyüme hormonu, prolaktin, eritropoetin, sitokinler) Đnsülin, EGF ve IGF-I hücre yüzeyindeki bir reseptöre bağlanarak iç yüzeyde lokalize tirozin artıkları üzerinde reseptörün ß subünitlerinin (membran boyunca uzama gösterir) kendilerini fosforillemesine neden olur. (Đntrensek tirozin kinaz aktivitesi) Büyüme hormonu, prolaktin, eritroprotein ve sitokinler hücre yüzeyindeki reseptörüne bağlanınca stoplazmik tirozin kinaz (Tyk-2, Jak1 veya Jack2) aktive olur. Bu kinazlar sitoplazmik proteinleri fosforiller. Nitrik oksit stoplazmadaki ve atrial natriüretik peptid (ANP) (hücre membranındaki) guanilat siklazı aktive ederek cgmp yi üretir. 155
156
157 157 Hangi hormon reseptörüne bağlanınca fosfolipaz C enzimi aktive olur? Kasılmaya neden olan hormonlar. Sonuçta fosfatidil inozitol 4,5-bifosfat parçalanır. Diaçilgliserolün aktive ettiği enzim: protein kinaz C Đnozitol trifosfatın etkisi: hücre içi kalsiyum depolarından kalsiyumun serbestleştirilmesi 157
158 158 Hücre içi reseptörlere bağlanarak etkili olan hormonlar: steroid yapılı hormonlar, kalsitriol, retinoik asit, tiroid hormonları Hücre içi reseptörlere bağlanarak etkili olan hormonların ortak özelliği: lipofilik olmaları ve hücre membranlarını taşıyıcı kullanmadan geçebilmeleri HORMON DÜZEYLERĐNĐN REGÜLASYONU Homeostazı sürdürmek için veya menstrüel siklus gibi fizyolojik işlemleri tekrarlamak için hormon düzeyleri regüle edilmelidir. Sinyal iletiminde birincil mesajcı olanlar: hormonlar (örn. Östrojen, epinefrin) Vazopressinin (ADH) etkileri: Böbrekte distal ve toplayıcı tübüllerden suyun geri emilimi ve damar düz kaslarında kasılma Oksitosinin etkileri: Uterus kontraksiyonu ve süt bezlerinde miyoepitelyal hücrelerde kontraksiyon Prolaktinin etkileri: TRH salınımını uyarır, dopamin baskılar. Meme dokusunda süt proteinlerinin ve süt şekerinin sentezini uyarır. SPESĐFĐK HORMONLARIN ETKĐLERĐ Hormon üreten dokular arasında hipotalamus, ön ve arka hipofiz, adrenal korteks ve medulla, gonadlar, tiroid ve paratiroid bezleri, kalp, beyin, gastrointestinal sistem şekil hücreleri ve pankreas bulunur. Luteinizan hormonun (LH) etkileri: Ovülasyonu sağlamak, korpus luteumdan progesteron ve estradiol sentezini uyarmak, testiste leydig hücrelerinden testosteron sentezini uyarmak. Follikül stimulan hormonun etkileri: Overlerden estradiol sentezini uyarmak, testiste sertoli hücrelerinden androjen bağlayıcı protein sentezini uyarmak Kortizolün etkileri: Glukoneogenez, glikojenez, lipoliz(ekstremitelerde), lipogenez (diğer dokularda), fizyolojik dozlarda protein ve RNA metabolizmasında artış (anabolizan etki), yüksek dozlarda katabolizan etki, antiinflamatuar cevap ve immünsüpresyon (T lenfositlerde parçalanma) 158
159
160 160 Tiroid hormonlarının etkileri: Fizyolojik dozlarda protein sentezinde artış, yüksek dozlarda yıkım, bazal metabolik hızda artma, lipoliz, kolesterol sentezinin uyarılması, LDL metabolizmasının uyarılması (kan kolesterol düzeyinin azalması), vitaminlerin kullanımının uyarılması Büyüme hormonunun etkileri: Glukoneogenez, glikojenez, lipoliz, protein sentezinin uyarılması, kasta dokusunda glukoz uptake inin azalması, büyüme. Aldosteron sentezini uyaranlar: Potasyum yüksekliği ve anjiotensin II Anjiotensin II nin etkileri: Arteriollerde vazokonstruksiyon sonucu kan basıncında artış, renin salınımının inhibisyonu, aldosteron üretiminin uyarılması ve sonuçta sodyum retansiyonu, hacim artışı ve kan basıncında artış Renin salınımını inhibe edenler Artmış kan basıncı Ayaktan oturur duruma geçmek Tuz yüklemesi β- adrenerjik antagonistler Prostaglandin inhibitörleri Potasyum Vazopressin Anjiyotensin II Besinlerin kullanımını düzenleyen hormonlar 1.Bağırsak hormonları a. Gastrin, gastrik antrum ve duodenumdan salınır; gastrik asit ve mide sekresyonunu uyarır. b. Kolesistokinin (CCK), duodenum ve jejunumdan salınır; safra kesesinin kontraksiyonunu ve pankreatik enzimlerin sekresyonunu uyarır. Ayrıca mide düz kasını gevşetir, pilor spazmı yapar ve midenin boşalmasını geciktirir. c. Sekretin, duodenum ve jejunumdan salınır; pankreastan bikarbonat sekresyonunu uyarır d. Gastrik inhibitör polipeptid (GĐP), ince bağırsaktan salınır; salınımı oral glukoz alınınca artar; insülinin, salınımını arttırır, gastrik asit sekresyonunu inhibe eder. 160
161 161 e. Vazoaktif intestinal polipeptid (VĐP), pankreastan salınır; düz kasları gevşetir ve pankreastan bikarbonat sekresyonunu uyarır. f. Bradikinin plazma, bağırsak ve diğer dokularda oluşur; hipotansiyonla sonuçlana vazodilatasyona yol açar.đnsülin ve Đnsülin ve glukagonun etkileri Đnsülin Beslenme durumunda yükselir Yakıt depolarını arttırır: glikojen ve triaçilgliserol Uyardığı metabolik olaylar Karaciğer ve kasta glikojen sentezi Karaciğerde TG sentezi ve VLDL ye dönüşüm Yağ dokusunda TG in depolanması Kas ve yağ hücrelerine glukozun transportu Protein sentezi ve büyüme Glukagon Açlıkta yükselir Kanda mevcut yakıtları arttırır (glukoz ve yağ asitleri) Uyardığı metabolik olaylar Karaciğerde fakat kasta değil glikojen yıkımı Glukoneogenez Yağ dokusunda lipoliz Đnsülin ve glukagon tarafından indüklenen ve baskılanan enzimler Insülin tarafından (toklukta) indüklenen ve glukagon tarafından (açlıkta) baskılanan enzimler Glukokinaz Sitrat liyaz Asetil KoA karboksilaz HMG-KoA redüktaz Piruvat kinaz Fosfofruktokinaz 1 Fosfofruktokinaz 2 Glukagon tarafından (açlıkta) indüklenen ve insülin tarafından (toklukta) baskılanan enzimler Glukoz 6-fosfataz Fosfoenolpiruvat karboksikinaz (PEPCK) Fruktoz-l,6-bifosfataz Đnsülin tarafından fosforilasyon durumu ve aktivitesi değiştirilen enzimler Enzim Aktivitede değişiklik Mekanizma camp metabolizması Fosfodiesteraz Artma Fosforilasyon Protein kinaz A Azalma Düzenleyici ve katalitik alt birimlerin ilişkisi Glikojen Metabolizması Glikojen sentaz Artma Defosforilasyon Fosforilaz sentaz Azalma Defosforilasyon Fosforilaz Azalma Defosforilasyon Glikoliz ve Glukoneogenez Piruvat dehidrogenaz Artma Defosforilasyon Piruvat kinaz Artma Defosforilasyon Fosfofruktokinaz 2 Artma Defosforilasyon Fruktoz 2,6-bifosfataz Azalma Defosforilasyon Lipid metabolizması Sitrat liyaz Artma Fosforilasyon Asetil KoA karboksilaz Artma Defosforilasyon HMG-KoA redüktaz Artma Defosforilasyon Hormona duyarlı lipaz Azalma Defosforilasyon 161
162 162 PLAZMA PROTEĐNLERĐ, ĐMMÜNOGLOBÜLĐNLER VE KAN KOAGÜLASYONU * Plazma, çeşitli fonksiyonlara sahip bir çok protein içerir. * Plazma proteinlerinin birçoğu karaciğerde sentezlenir ve glikozile durumdadır. * Albümin, başlıca plazma proteinidir ve glikozile değildir. Đntra-vasküler osmotik basıncı sağlar ve ilaçlar ve bilirubin gibi bir çok ligandı bağlar. * Haptoglobülin, ekstrakorpüsküler hemoglobini bağlayarak böbreklerden atılımını önler. * Transferrin, demiri bağlayarak kullanılacağı bölgeye taşır. * Ferritin, hücre içi demirin depo şeklidir. * Serüloplazmin, önemli miktarda bakır içerir. * Wilson hastalığı ve Menkes hastalığı bakır metabolizmasındaki bozukluklar sonucu gelişmektedir. * Alfa1-antitripsin, plazmanın başlıca serin proteaz inhibitörüdür; özellikle nötrofil elastazı inhibe etmektedir. Yetersizliği, amfizeme ve karaciğer hastalığına yol açabilmektedir. * Alfa2-makroglobülin, bir çok proteazları nötralize eden ve bazı sitokinleri spesifik organlara hedefleyen başlıca plazma proteinidir. * Đmmunoglobülinler, vücudun savunma mekanizmasında kilit bir role sahiptir; bu proteinlerin bazı önemli özellikleri anlatılacaktır. * Hemostaz ve trombozis; pıhtılaşma faktörlerinin, trombositlerin ve kan damarlarının rol oynadığı kompleks işlemlerdir. I. PLAZMA PROTEĐNLERĐ Plazma proteinlerinin özellikleri: Albümin hariç tümü glikoprotein yapıdadır, karaciğerde sentezlenir (immünoglobülinler hariç), kan ve dokular arasındaki sıvı dağılımını belirler, belirli yarı ömnürleri vardır, bazıları akut faz reaktanıdır, GER deki ribozomlarda sentezlenir. Plazma proteinleri arasında en fazla negatif yük içeren protein: prealbümin ve albümin KANIN BAŞLICA FONKSĐYONLARI 1. Solunum- akciğerlerden dokulara oksijenin ve dokulardan akciğere CO2 nin transportu 2. Beslenme- absorbe edilen besin maddelerinin transportu 3. Ekskresyon-metabolik atık ürünlerin uzaklaştırılması için böbrekler, akciğerler, deri bağırsaklara transportu ve 4. Asit-baz dengesi 5. Su dengesi- dolaşımdaki sıvı ve doku sıvısı arasında su değişiminin regülasyonu 6. Vücut ısısının regülasyonu 7. Savunma- beyaz küre ve antikorlarla infeksiyonlara karşı koyma 8. Hormonların transportu- metabolizmanın regülasyonu 9. Metabolitlerin transportu 10. Koagülasyon Negatif akut faz reaktanları: Prealbümin, albümin, transferin, retinol bağlayıcı protein Pozitif akut faz reaktanları: α1-antitripsin, α1-asitglikoprotein, haptoglobülin, seruloplazmin, fibrinojen, C3, C4, CRP 162
163 163 Bazı plazma proteinleri ve fonksiyonları Protein Akut faz özelliği Yorum Prealbümin Neg AFR Beslenmenin takibi Albümin Neg AFR Bir çok hastalıkta azalır, genel taşıyıcı protein Elektroforezde alfa1bölgesinde bulunan proteinler alfa1-antitripsin AFR Eksikliği amfizem ve siroz alfa1-asit glikoprotein AFR Fonksiyonu bilinmiyor alfa1-lipoprotein (Apo-A) alfa1-fetoprotein Lipid taşıyıcısı Fetal protein, artışı nöral tüp defekti Elektroforezde alfa2- bölgesinde bulunan proteinler Haptoglobülin AFR Hemoglobini bağlar, hemolizde azalır alfa2-makroglobülin Nefrotik sendromda yükselir Serüloplazmin AFR Wilson hastalığında azalır, bakır içerir Elektroforezde beta-bölgesinde bulunan proteinler Transferrin Neg AFR Demir taşır, hipokromik anemide artar Hemopeksin Beta-Lipoprotein (Apo B) Hem bağlar, hemolizde azalır. Lipid taşıyıcısı C4 AFR Kompleman faktörü C3 AFR Kompleman faktörü Beta2-Mikroglobülin Renal tubül fonksiyonu değerlendirilmesi Fibrinojen AFR Fibrin prekürsörü Elektroforezde gama- bölgesinde bulunan proteinler IgG IgA IgM C-reaktif protein AFR++ Đmmün reaksiyonlarda antikor artışı B-hücre tümörlerinde monoklonal artış Nonspesifik fakat en duyarlı AFR dir. Inflamatuar olayların takibinde kulanılır. 163
164 164 Prealbüminin (transtiretin) özellikleri: Karaciğerde sentezlenir, tiroksin (serum düzeyinin % 10 kadarını) ve retinol bağlayıcı protein olarak fonksiyon gösterir, yarı ömrü 48 saat kadardır, beslenmenin takibinde kullanılır. Albümin ve özellikleri: Plazmanın başlıca proteini, globüler protein, tüm vücut sıvılarında en bol bulunan protein, karbonhidrat içermez, kolloid osmotik basıncın başlıca sağlayıcısıdır, karaciğerde sentezlenir, sentezi onkotik basınç ve protein alımı ile kontrol edilir, sitokinler sentezini azaltır, yarı ömrü gün kadardır, plazmanın genel taşıyıcı proteinidir. α1-antitripsin ve özellikleri: Karaciğerde sentezlenir, plazmanın başlıca serin proteaz inhibitörüdür, eksikliğinde amfizem ve siroz gelişir, protein elektroforezinde α1-bandının % 90 ını oluşturur. Alfa-fetoprotein ve özellikleri: Fetüsün yolk kesesinde ve karaciğerinde üretilir, gebeliğin 13. haftasında pik yapar ve sonra azalmaya başlar, gebelerde artışı açık nöral tüp defektlerinde ve fetal distres durumlarında gözlenir, tümör belirteci olarak hepatosellüler karsinomaların ve germ-hücre tümörlerinin araştırılmasında kullanılır. Haptoglobülin ve özellikleri: Hemoglobini bağlayan immünoglobülin benzeri plazma proteinidir, hemolizde azalır, pozitif akut faz reaktanıdır. α2-makroglobülin ve özellikleri: Yüksek molekül ağırlıklı plazma proteaz inhibitörüdür, fibrinolitik/koagülasyon sisteminin regülasyonunda, büyüme hormonu ve çinko gibi moleküllerin taşınmasında rol oynar. Hemolizde azalır. Serüloplazmin: Bakır içeren ve ferroksidaz aktivitesine sahip bir proteindir. Demir ve bakır metabolizmasında rol oynayan bir α2-globülindir. Düşük dansiteli lipoproteini (LDL) okside ettiği için kardiyovasküler hastalıklar için bağımsız risk faktörü olabildiği gösterilmiştir. Geç dönemde yükselen pozitif akut faz reaktanıdır ve Wilson hastalığında azalır. Plazmada bakırı bağlayan proteinler: seruloplazmin ve albümin 164
165 165 Transferrin: Plazmanın başlıca demir taşıyan proteinidir, negatif akut faz reaktanıdır. Plazmadaki miktarı demir bağlama kapasitesini yansıtır. Transferrin ölçümü kimyasal yöntemle ölçülen total demir bağlama kapasitesinden daha doğru sonuçlar verir. 1 mg transferrin 1.25 mcg demir bağlar. Demir eksikliği anemilerinde ve yüksek östrojen düzeylerinde (örn. Gebelik ve oral kontraseptif kullanımı) artar, inflamasyonda azalır. Hemopeksin: Hem bağlar ve hemolizde azalır. Hemosiderin: Ferritinin demir içeren kısmen parçalanmış formudur. Aşırı demir depoları oluştuğunda gözlenir. Demire spesifik histolojik boyalarla (örn. Prusya mavisi) saptanabilir. Đdrarda bulunması intravasküler hemolizle ilişkilidir. Fibrinojen: Karaciğerde sentezlenen ve suda çözünen bir plazma glikoproteinidir. Nedeni açıklanamayan kanamaların araştırılmasında kullanılır. Artmış fibrinojen düzeyleri arteriyel trombotik olaylara yol açabilir. Akut faz reaktanıdır. β2-mikroglobülin: Klas I MHC antijenlerinin hafif zinciri olan düşük molekül ağırlıklı bir proteindir. Tüm nükleuslu hücrelerde bulunduğu ve tamamen reabsorbe olduğu ve proksimal tübüllerde katabolize olduğu için proksimal tübüler fonksiyonun ve immün aktivasyonun bir markırı olarak kullanılır. Serum düzeyleri hematolojik malignansilerde (örn. Multiple myeloma) artar ve prognozu yansıtır. Đdrar düzeylerindeki artış tübüler fonksiyonu yansıtır. C-reaktif protein: CRP pentraksin protein ailesinin (serum amiloid P olarak da bilinir) bir üyesidir. Bu ismi almasının nedeni pnömokok hücre duvarındaki polisakkaridin C fraksiyonuna bağlanması iledir. Hepatik sekresyonu interlökin 6 gibi sitokinlere cevap olarak uyarılır. CRP nin immün cevabın oluşmasında bir role sahip olduğuna inanılır. CRP kompleman sistemini aktive eder, Fc reseptörlerine bağlanır, bazı mikroorganizmalar için opsonin olarak fonksiyon gösterir. Yüksek duyarlılıklı CRP ölçümleri vasküler inflamasyonun ve kardiyovasküler riskin değerlendirilmesinde yararlıdır. Sedimantasy on hızı ile iyi bir korelasyon gösterir fakat daha erken yükselir ve daha erken düşer. En erken yükselen akut faz proteini olup inflamasyonda, infeksiyonda, travma ve doku nekrozunda, malignansilerde ve otoimmün hastalıklarda artar. PLAZMA ĐMMÜNOGLOBÜLĐNLERĐ Đmmünoglobülinler ve özellikleri: Đmmünoglobülinler yabancı antijenleri tanıyan ve bağlayan antikor olarak fonksiyon gösteren bir grup plazma proteinidir. Birbirlerine disülfid bağlarla bağlı iki hafif ve iki ağır zincirden oluşur. Đki tür hafif zincir (κ ve λ) ve beş tür ağır zincir (γ, α, µ, δ ve ε) Ağır ve hafif zincirlerin N-terminal amino asit dizilimi (değişken bölge) oldukça değişken olup antijen bağlama bölgeleri içerir (Fab). Zincirlerin geri kalan kısımlarındaki amino asit dizilimi (sabit bölge) bir immünoglobülin sınıfı içinde aynıdır. Antijenin immünoglobülinlere bağlanması non-kovalent bağlarla gerçekleşir. Đmmünoglobülin sınıfları arasında özgüllüğü belirleyen ağır zincirlerdeki amino asit dizilimidir (primer yapı). Plazmadaki miktarları en yüksekten en düşüğe göre sıralandığında beş sınıf immünoglobülin bulunur: IgG, IgA, IgM, IgD ve IgE. IgG: Fonksiyonları arasında sekonder cevapta ana antikor, bakteri fagositozunda opsonizasyon, kompleman fiksasyonu, bakteri toksinleri ve virüslerin nötralize edilmesi bulunur. 165
166 166 Plasentayı geçen tek immünoglobülin. Total serum immünoglobülin konsantrasyonunun %70-80 ini oluşturur. Multiple myelomada belirlenen en sık ağır zincir tipidir. Kronik veya rekürren infeksiyonlarda, otoimmün hastalıklarda artar. IgA: Sekresyonlarda bulunan başlıca immünoglobülin tipi. Bakteri ve virüslerin müköz membranlara yapışmasını önler. Multiple myelomada ikinci en sık görülen monoklonal immünoglobülin tipidir. Kolostrum ve sütteki maternal kaynaklı sekretuar IgA infantları GĐS infeksiyonlarından korumaktadır. Đmmünoglobülin IgG IgA IgM IgD IgE Đmmünoglobülinlerin başlıca fonksiyonları Başlıca Fonksiyonları Sekonder cevapta ana antikor. Bakterilerin fagositozunda onları opsonize eder. Bakteri harabiyetini arttıran komplemanı fikse eder. Bakteriyel toksinleri ve virüsleri nötralize eder. Plasentayı geçer. Sekretuar Ig A, bakteri ve virüslerin müköz membranlara yapışmasını önler. Komplemanı fikse etmez. Bir antijene karşı primer cevapta üretilir. Komplemanı fikse eder. Plasentayı geçmez. B hücrelerinin yüzeyinde antijen reseptörü Belli değil. Serumda olduğu kadar B hücrelerinin yüzeyinde de bulunur. Antijenle (allerjenle) karşılaştıktan sonra mast hücreleri ve bazofillerden mediatörlerin salınımına neden olarak erken dönem hipersensitiviteye aracılık eder. Eozinofillerden enzimleri salarak infeksiyonlara karşı korur. Komplemanı fikse etmez. Helmint infeksiyonlarına karşı konağı korur. IgD: Serumda ve membrana bağlı halde bulunur. Membrana bağlı IgD B hücre yüzeylerinde bulunur ve antijen tanınmasında fonksiyon gösterir. HEMOSTAZ VE TROMBOZ Hemostaz, bir kesi yerinden kanamanın durmasıdır; tromboz ise kan damarlarını döşeyen endotelin hasara uğraması veya kaldırılması (örn. aterosklerotik plağın rüptürü) durumunda ortaya çıkar. Bu işlemler kan pıhtılaşması (koagülasyon) olarak karşımıza çıkar ve trombosit agregatlarının oluşması ve çözünmesi işleminde kan damarları, trombosit kümelenmesi ve plazma proteinleri rol oynar. IgE: Mast hücrelerinin ve bazofillerin yüzeyinde bulunur ve bunlardan mediatör salınımına neden olarak hipersensitiviteye aracılık eder. Eozinofillerden enzimleri salarak infeksiyonlara karşı korur. Helmintlere karşı immünitede görev alır. IgM: Antijene cevapta üretilen ilk immünoglobülin tipi. Kompleman aktivatörüdir. Soğuk-reaktif antikorların çoğu IgM tipindedir. Fetüste üretilebilir ve plasentayı geçmez. Kord kanında veya doğumun hemen sonrasında serumda bulunması konjenital infeksiyon tanısında yararlıdır. Klasik romatoid faktörler (RF) IgG ye karşı geliştirilmiş IgM otoantikorlarıdır. IgM konsantrasyonlarındaki selektif artış infeksiyona bir cevabı gösterir. Monoklonal artışlar Waldenström makroglobülinemide gözlenir. Koagülasyon şelalesinin başlaması: Subendotelyal dokudaki doku faktörünün kanla teması ve faktör VII yi aktive etmesi ile başlar. Protrombini trombine çeviren faktörler: Bunlara protrombinaz kompleksi de denir ve faktör Xa, faktör Va, fosfolipidler ve kalsiyumdan oluşur. Faktör Pıhtılaşma faktörlerinin nümerik sistemi Ortak Đsim I Fibrinojen Bu faktörler genellikle kendi isimleriyle adlandırılır II Protrombin III IV Doku faktörü Ca2+ Bu faktörler genellikle koagülasyon faktörleri olarak kabul edilmez V Proakselerin, labil faktör, akseleratör globülin VII Prokonvertin VIII Antihemofilik faktör A IX Antihemofilik faktör B, Christmas faktör X Stuart-Prower faktör XI Plazma tromboplastin antesedan XII Hageman faktör XIII Fibrin stabilize edici faktör Not: Faktör VI yoktur 166
167 167 Kan pıhtılaşması esnasında fibrinojeni fibrine çeviren enzim: trombin Faktör XIIIa: Fibrin polimerlerindeki glutamin ve lizin arasında kovalent çapraz bağlar oluşturur. Koagülasyon şelalesinin inhibisyonu: Başlıca fizyolojik inhibitör doku faktörü yolu inhibitörüdür. Ayrıca antitrombin III (FXa ve trombini inhibe eder), protein C ve S sistemi de görev alır. Fibrinoliz: Plazminojen dolaşımda fibrine tutunur ve doku plazminojen aktivatör tarafından fibrini parçalayan plazmine dönüşür. Ayrıca ürokinaz ve streptokinaz (rekombinant olarak üretilir) da plazminojen aktivatörüdür. Trombositlerin kan damarlarında açığa çıkan kollajene bağlanması: yüzeylerindeki GP Ia-IIa reseptörleri ile gerçekleşir. Bu bağlanmada von Willebrand faktör rol oynar. von Willebrand faktör: Endotel hücrelerinde sentezlenerek plazmaya salınan bir glikoproteindir, FVIII i stabilize eder ve kollajen ve subendotele bağlanır. Trombositler, vwf ye trombosit yüzeyinde bulunan bir glikoprotein kompleksi (GP Ib-IX) ile bağlanır 167
168 168 Faktör XII Faktör XI Faktör IX Faktör VII Faktör X Faktör II Faktör VIII Faktör V Doku faktörü (Faktör III) Faktör 1 Faktör XIII Protein C Protein S Trombomodulin Koagülasyonda rol oynayan proteinlerin fonksiyonları Serin proteazların zimojenleri Damar hasarı bölgesinde negatif yüklü yüzeye bağlanır; yüksek molekül ağırlıklı kininojen ve kallikrein tarafından aktive edilir. Faktör Xlla tarafından aktive edilir. Ca2+ varlığında faktör Xla tarafından aktive edilir. Ca2+varlığında trombin tarafından aktive edilir. Tenaz kompleksi (Ca2+, faktör VIIIa ve IXa) ve doku faktörü ve Ca2+ varlığında faktör VIIIa tarafından aktive olmuş trombositlerin yüzeyinde aktive olur. Aktive olmuş trombositlerin yüzeyinde protrombinaz kompleksi (Ca2+, faktör Va ve Xa) tarafından aktive olur. (Faktör II, VII, IX ve X; gama-karboksiglutamat içeren zimojenlerdir.) Kofaktörler Trombin tarafından aktive edilir; faktör VIIIa, faktör IXa tarafından faktör X un aktivasyonunda bir kofaktördür Trombin tarafından aktive edilir; faktör Va, faktör Xa tarafından protrombinin aktivasyonunda kofaktördür Hasarlı veya uyarılmış endotel hücrelerinin yüzeyinde bulunan bir glikoproteindir; faktör VIIa için bir kofaktör olarak fonksiyon görür Fibrinojen Fibrin pıhtısı oluşturmak üzere trombin tarafından parçalanır Tiyol bağımlı transglutaminaz Ca2+ varlığında trombin tarafından aktive edilir, kovalent çapraz bağlarla fibrin pıhtısını stabilize eder Düzenleyici proteinler Trombomoduline bağlı trombin tarafından aktive protein C ye çevrilir; sonra faktör VIIIa ve Va yı parçalar Protein C nin kofaktörü olarak fonksiyon görür; her iki protein de Gla (gama-karboksiglutamat) artıkları içerir Endotel hücrelerinin yüzeyinde bulunan bir proteindir; trombine bağlanarak protein C yi aktive eder 168
169 169 Fibrinojenin trombosit yüzeylerine tutunması: GP IIb-IIIa kompleksi (fibrinojen reseptörü) ile gerçekleşir. Bazı tümör belirleyicileri ve yükseldiği kanser türleri Karsinoembriyonik antijen (kolon, akciğer, göğüs, pankreas), alfa-fetoprotein (karaciğer), human koryonik gonadotropin (trofoblast), prostat spesifik antijen (prostat), kalsitonin (tiroid medüller karsinoma), CA 19-9 (tüm gastrointestinal kanser formları özellikle pankreas CA), CA 125 (over kanseri), CA 15-3 (metastatik göğüs kanseri) CA (metastatik göğüs kanseri) CA 72-4 (gastrik karsinoma) Asemptomatik kişilerin taranması Malign ve benign durumların ayırımı Tedavi ve rekürrensin takibi Sınıflandırma ve evreleme Tedavi Tümör belirleyicilerinin uygulamaları 169
170 170 SIVI ELEKTROLĐT DENGESĐ VE MĐNERALLER Đnsan vücudu büyük oranda sudan oluşmuştur. Vücutta su üç bölümde bulunur: hücre içi, interstisiyel ve damar içi. Elektrolitler, moleküllerinin solüsyonda iyonlara ayrıştığı maddelerdir. Đnsan vücudunda bulunan başlıca elektrolitler pozitif yüklü katyonlar (sodyum, potasyum, kalsiyum ve magnezyum) veya negatif yüklü anyonlardır (klor, bikarbonat, fosfat, sülfat, proteinler ve laktat gibi bir kısım organik asitler). Vücuttaki elektro nötraliteyi sürdürmek için toplam katyon konsantrasyonu, anyonlarınkine eşit olmalıdır. Vücutta elektrolitlerin fonksiyonları: osmotik basıncın sürdürülmesi ve suyun dağılımı, ph nın uygun düzeyde tutulması, kalp ve diğer kasların fonksiyonunun düzenlenmesi, oksidasyon-redüksiyon (elektron transferi) reaksiyonları, enzimlerin kofaktörleri oluşu. Su ve elektrolitlerin regülasyonu başlıca hormonal ve böbrekler yoluyla sağlanır. Mineraller iki kısma ayrılır: makromineraller ve mikromineraller. Bazı önemli minerallerin özellikleri özet halinde sunulmuştur. Vücut sıvı bölümlerinin bileşimi Sıvı bölümü % Toplam vücut suyu Başlıca katyonlar Başlıca anyonlar Protein konsantrasyonu Intrasellüler K, Mg PO4 Çok yüksek Intravasküler Na, K, Ca Cl, HCO3 Yüksek Đnterstisiyel Na, K, Ca Cl, HCO3 Çok düşük Osmolalite ve hacim düzenleyicileri Faktör Uyaran Etki Susama Antidiüretik-Hormon (ADH) Renin-Anjiyotensin- Aldosteron Atrial Natriüretik Hormon (ANH) Osmolalitenin %1 artması; volümün >%5 azalması Osmolalitenin %1 artması; volümün >%5 azalması Volümde azalma; idrarda elektrolit azalması Atriyal kan basıncında artma Su alımını arttırır, osmolaliteyi azaltır Böbreklerden su reabsorpsiyonunu arttırır, osmolaliteyi azaltır Kan basıncında artma; serum Na artar (hafif), serum K ve H azalır; idrar Na azalır, idrar K ve H artar Đdrar Na artar, kan hacmi azalır; aldosteron azalır 170
171 171 MĐNERALLER Fizyolojik ve biyokimyasal fonksiyonlar için gereklidir Mineraller iki gruba ayrılır: (1) makromineraller: 100 mg/gün den daha fazla miktarlarda gerek duyulur. (2) mikromineraller (eser elementler): 100 mg/gün den daha az miktarlarda gerek duyulurlar. Genellikle mineraller absorpsiyonları için bir taşıyıcıya gerek duyarlar. Absorpsiyon nadiren tam olur; diğer besinlerden ve diyetteki diğer bileşiklerden etkilenir (örn. çift değerli katyonları bağlayan oksalatlar ve fitatlar). Transport ve depolamada özel proteinlere gerek duyar. Ekskresyon feçesle, idrarla ve terle gerçekleşir. Aşırı mineral alımı toksik semptomlara yol açar. Semptomlar arasında genellikle kusma, diyare ve irritabilite bulunur. Mineral ihtiyaçları uygun miktarlarda alınan çeşitli türden tahıl ürünleri, meyveler, yeşil yapraklı sebzeler, et ve süt ürünleri ile karşılanır. Çeşitli moleküllerin hücre içi ve dışı konsantrasyonları tablo 11.3 te gösterilmiştir. Bazı moleküllerin hücre içi ve dışı ortalama konsantrasyonları Madde Hücre Dışı Sıvı Hücre Đçi Sıvı Na+ 140 mmol/l 10 mmol/l K+ 4 mmol/l 140 mmol/l Ca2+ (serbest) 2.5 mmol/l 0.1 mmol/l Mg mmol/l 30 mmol/l Cl- 100 mmol/l 4 mmol/l HCO3-27 mmol/l 10 mmol/l PO43-2 mmol/l 60 mmol/l Glukoz 5. 5 mmol/l 0-1 mmol/l Protein 2 g/dl 16 g/dl HÜCRE VE DOKU BĐYOKĐMYASI Hücre, biyolojinin başlıca yapısal ve fonksiyonel birimidir. Bir hücre yaşamın bağımsız olarak sürdürebilen en basit birimdir. Vücutta bir çok kimyasal reaksiyonlar hücre içinde meydana gelir, Vücudun çeşitli dokuları farklı biyokimyasal fonksiyonlara sahiptir. Bu fonksiyonlar fizyolojik durumlarda (örn, açlık, beslenme, egzersiz) değişir. HÜCRE BĐYOKĐMYASI Hücrenin bileşimi 1. Hücrelerin % 90 ı sudur. Geriye kalan moleküllerin ise: - % 50 protein - % 25 karbonhidrat - % 15 nükleik asit 171
172 172 - % 10 lipid - % 10 diğerleri 2. Element olarak hücre bileşimi: - % 60 hidrojen - % 25 oksijen - % 10 karbon - % 5 nitrojen 3. Ökaryotlar, prokaryotlardan (bakteri hücreleri) daha kompleks bir yapıya sahiptirve aralarında farklılıklar vardır. a. Ökaryotların bir nükleusu ve stoplazmalarında bir membranla çevriliorganelleri vardır; prokaryotlarda ise yoktur. b. Prokaryotlarda DNA tüm hücre içinde yüzer haldedir; ökaryotlarda isenükleusla sınırlıdır. c. Prokaryotlar ortadan bölünerek, ökaryotlar ise mitozla çoğalırlar. d. Ortalama olarak ökaryotik hücreler prokaryotik hücrelerden 10 kat dahabüyüktür. e. Enerji metabolizması prokaryotlarda plazma membranına bağlıoksidatif enzimlerle ökaryotlarda ise mitokondrideki oksidatif enzimlerlegerçekleştirilir. f. Ökaryotların DNA sı prokaryotların DNA sından daha komplekstir. g. Prokaryotlarda hücre iskeleti bulunmaz, ökaryotlarda ise bulunur. h. Prokaryotlar, şeker ve amino asitlerden oluşan peptidoglikan yapısında birhücre duvarına sahiptir. Ökaryotik hücreler ise peptidoglikan yapıda olmayanbir hücre zarı içerirler. Hücrelerin %90 ı: sudur. Hücrenin kuru ağırlığı baz alındığında en fazla bulunan organik komponent ve element: protein ve karbon Granüllü endoplazmik retikulum üzerindeki poliribozomlarda sentezlenen proteinler: Sekretuar Golgi cisimciği Plazma zarı Endoplazmik retikulum Salgı granülleri Lizozomal enzimler Serbest ribozomlarda sentezlenen proteinler Hücre içi Nükleer Mitokondri Peroksizom Katepsinler: Hücre içinde bulunan proteolitik enzimlerdir. Hücre organelleri 1. Plazma membranı taşıyıcılar ve reseptörler içerir. Hücrelerin içinden ve dışından moleküllerin transportunu, hücreler arası adezyonu ve haberleşmeyi ve hücrenin bütünlüğünü sağlar. Markırı: Na+-K+ATP az, 5 -Nükleotidaz ve adenilat siklaz 2. Endoplazmik retikulum (ER) protein ve lipidlerin sentezini ve ksenobiyotiklerin oksidasyonunu (sitokrom P450) organize eder. Ribozomların bağlanması sonucu granüllü endoplazmik retikulum (GER) oluşurken ribozomsuz ER, düz endoplazmik retikulum (DER) olarak adlandırılır. Hücre dışına sekrete edilecek proteinler GER de, hücre içinde kalacaklar ise ribozomlarda sentezlenir. Bazı dokularda (örn. iskelet kası) ER da kalsiyum iyonları depolanır ve gerektiğinde salınır. Markırı: Glukoz 6-fosfataz 3. Golgi kompleksi proteinleri işler ve sınıflandırır. Ayrıca glikozilasyon ve sülfatasyon reaksiyonları burada gerçekleşir. Markırı: Galaktozil transferaz 172
173 Mitokondride sitrik asit döngüsü ve oksidatif fosforilasyon reaksiyonları meydana gelir. Aerobik hücrelerde mitokondri ATP nin üretildiği başlıca organeldir. Diğer membranöz yapıların (örn. lizozom, golgi) aksine mitokondri sadece daha önceden mevcut mitokondrinin bölünmesiyle üretilir; her bir mitokondri kendine ait DNA, RNA ve ribozomları içerir. Markır: Glutamat dehidrogenaz 5. Nükleus kromozomların bulunduğu ve DNA nın yönettiği RNA sentezinin (transkripsiyon) yapıldığı bölgedir. Nükleus, nükleer bir zarfla çevrilidir. Bölünme halinde olmayan hücre nükleusu kromatin (DNA ve protein bileşimi) ile doludur. Nükleolusta ribozomal RNA yı kodlayan genlerin bir çok kopyasını içeren DNA bulunur. Ribozomal RNA nükleolusta sentezlenir. Markırı: DNA 6. Ribozom protein sentezi bölgesidir (mrna nın proteine translasyonu). Markırı: RNA 7. Lizozomlar protein, polisakkarid, nükleik asit ve lipidlerin yıkım reaksiyonlarını katalizleyen hidrolaz enzimlerini içerir. Markırı: asit fosfataz 8. Peroksizom bazı yağ asiti ve amino asitlerin yıkımı, hidrojen peroksitin üretimi ve yıkımı reaksiyonlarında rol oynar. Markırı: katalaz ve ürik asit oksidaz 9. Hücre iskeleti mikroflamentleri, mikrotübülleri ve ara filamentleri içerir. Hücrenin şeklini sabitler, sitoplazmayı organize eder ve hareketi sağlar. Markırı: spesifik enzim markırı yoktur 10.Sitozol glikoliz, yağ asiti sentezi ve pentoz fosfat yolu enzimlerini içerir. Markırı: laktat dehidrogenaz 173
174 174 DOKULARIN BĐYOKĐMYASAL FONKSĐYONLARI Dokuların fonksiyonlarını ağızdan başlayarak böbrekte sonlandıracak şekilde inceleyeceğiz. Çeşitli dokuların ve organların başlıca biyokimyasal fonksiyonlarını ve bazı faktörlerin (fiziksel, kimyasal, infeksiyon, diyet ve mutasyonlar) bu fonksiyonlara etkilerini gözden geçireceğiz. Lizozim: Eksternal sekresyonlarda bulunan (makrofajlarda bol bulunur) ve bazı bakteri hücre duvarlarındaki N- asetilmuramik asit ve N-asetil-D-glukozamin arasındaki bağı parçalayan enzimdir. Laktoferrin: Anne sütünde, ekzokrin sekresyonlarda bulunan ve inflamasyon esnasında nötrofil granüllerinden salınan demir bağlayıcı proteindir, demiri bağlayarak bazı bakterilerin büyümesini inhibe edebilir. Antibakteriyel, antiviral, antifungal, anti-inflamatuar, antioksidan ve immünomodülatör aktivitelere sahiptir. Ekto-enzimler: Plazma membranının dış bölümünde bulunan enzimlerdir. Örn: alkalen fosfataz, 5 -nükleotidaz Hücre membranlarındaki spesifik iyon kanalları: Sodyum, potasyum, kalsiyum ve klor iyonları için özeldir. Çölyak hastalığında kullanılan tanı testleri Endomisial antikorlar Retikülin antikoru Doku transglutaminaz antikoru Gliadin antikoru Kolerada üretilen enterotoksin: adenilat siklazı aktive eder, üretilen camp bağırsak hücrelerine sodyumun aktif transportunu önler, sonuçta bağırsak lümeninde su toplanır ve şiddetli diyare gelişir. Kolera toksini, stimülatör G proteininin α altbirimine ADP-ribozu bağlayarak bu alt birimin GTPaz aktivitesini inhibe eder. Alkolizm ve yağlı karaciğer: Alkol karaciğerde metabolize olarak bol miktarda NADH üretilir, NAD+ azalır. NAD+ deki azalma yağ asitlerinin beta-oksidasyonunu azaltır, karaciğerde yağ asitleri birikir. Kronik alkoliklerde beslenme bozulur, apo B100 sentezi azalır, VLDL sentezlenemez, triaçilgliseroller karaciğerde birikir. Detoksifikasyonda rol oynayan bileşikler PAPS (fosfoadenozin fosfosülfat) Metionin Glisin Glutatyon Glukuronik asit Alkolizm 1) Etanolün oksidasyonu karaciğerde oluşan reaksiyonlarla NADH üretir. 2) Besin almaksızın etanol içilmesi (NADH) / (NAD+) oranının artışına yol açar ve sonuçta: - Piruvatın laktata dönüşümü artarak laktik asidoz gelişir. - Glukoneogenez inhibe olarak hipoglisemi gözlenir. - Artmış gliserol 3-fosfat düzeyleri yağ dokusu triaçilgliserollerin kaynaklanan yağ asitleri ile birleşerek VLDL sentezinde artış olur. Kanda artmış VLDL düzeyleri hiperlipidemiye yol açar. Kronik alkolizmde karaciğerde protein sentezi azalır. Bu nedenle VLDL sekresyonu azalarak yağlı karaciğer gelişir. En sık görülen glikolitik yol enzim eksikliği: piruvat kinaz Beyaz ırkta en sık görülen enzim eksikliği: glukoz 6-fosfat dehidrogenaz 174
175 175 Serbest oksijen radikallerini zararsız hale getirmede rol oynayan enzimler Glukoz 6-fosfat dehidrogenaz Glutatyon redüktaz Glutatyon peroksidaz Süperoksid dismutaz Katalaz Süperoksid dismutazın kofaktörleri: Stoplazmik formu bakır ve çinko, mitokondrial formu mangan Serbest oksijen radikallerinin oluşumu ve bunlara karşı hücresel savunma Oksijen, hayat için esansiyeldir. Bununla beraber O2 nin elektron yapısı, bir elektron alarak indirgenmesine ve hücre hasarına neden olabilen oksijen radikallerinin oluşumuna yol açar. Bir radikal, dış orbitalinde eşleşmemiş elektron içeren oldukça reaktif bir moleküldür. Bu molekül kendi dış yörüngesini tamamlamak için diğer bir molekülden bir elektron kaldırarak bir dizi reaksiyonlar başlatır. O2 ye elektronların transferi sırasıyla süperoksid anyonu (O2-), kısmen indirgenmiş hidrojen peroksid (H2O2) ve serbest hidroksil radikali (OH-) oluşumuna neden olur. Oksijenin suya indirgenmesindeki bu ara maddelerden en tehlikelisi hidroksil radikali olup lipid peroksidasyonuna ve diğer toksik radikallerin oluşumuna neden olur. Hidrojen peroksidin kendisi bir serbest radikal değildir fakat Fenton veya Haber-Weiss reaksiyonlarıyla Fe2+ veya Cu+ varlığında hidroksil radikaline çevrilir. Hücre içi oksijen radikallerinin başlıca kaynağı mitokondrial elektron transport zinciridir. Toksik oksijen parçacıkları ayrıca peroksizomlarda, endoplazmik retikulumda ve makrofajlarda fagositoz esnasında da oluşur. Bu radikallerin zararlı etkilerini önlemede süperoksid dismutaz, katalaz, glutatyon peroksidaz enzimleri ve vitamin E, C ve β-karoten rol oynar. 175
176 176 2H2O2 2H2O + O2 tepkimesini gerçekleştiren enzim: katalaz Nitrik oksitin etkileri Vazodilatasyon kan basıncının regülasyonu makrofajların bakterisidal ve tümorisidal etkilerine aracılık etme beyinde nörotransmitter trombosit adezyon ve agregasyonunun inhibisyonu Nitrik oksid (NO) kan damarlarının düz kaslarını gevşeten ve bir çok diğer önemli biyolojik fonksiyonlara (vazodilatasyon, trombosit adezyon ve agregasyonunun inhibisyonu, nörotransmitter, kan basıncı regülasyonu, makrofajların bakterisidal ve tümörosidal etkilerine aracılık etme) sahip bir bileşiktir. Argininden NO sentaz aracılığı ile sitozolde sentezlenir. NO sentaz çok kompleks bir enzimdir ve 5 kofaktör kullanır: NADPH, FAD, FMN, hem ve tetrahidrobiopterin. NO ayrıca gliseril trinitrat gibi vazodilatatörlerden köken alan nitritten de sentezlenir Đdrarla atılan endojen sülfatın kaynağı amino asit: sistein 176
Referans:e-TUS İpucu Serisi Biyokimya Ders Notları Sayfa:368
 21. Aşağıdakilerden hangisinin fizyolojik ph'de tamponlama etkisi vardır? A) CH3COC- / CH3COOH (pka = 4.76) B) HPO24- / H2PO-4 (pka = 6.86) C) NH3/NH+4(pKa =9.25) D) H2PO-4 / H3PO4 (pka =2.14) E) PO34-/
21. Aşağıdakilerden hangisinin fizyolojik ph'de tamponlama etkisi vardır? A) CH3COC- / CH3COOH (pka = 4.76) B) HPO24- / H2PO-4 (pka = 6.86) C) NH3/NH+4(pKa =9.25) D) H2PO-4 / H3PO4 (pka =2.14) E) PO34-/
BİYOKİMYADA METABOLİK YOLLAR DERSİ VİZE SINAV SORULARI ( ) (Toplam 4 sayfa olup 25 soru içerir) (DERSİN KODU: 217)
 BİYOKİMYADA METABOLİK YOLLAR DERSİ VİZE SINAV SORULARI (05.11.2012) (Toplam 4 sayfa olup 25 soru içerir) (DERSİN KODU: 217) Adı Soyadı: A Fakülte No: 1- Asetil KoA, birçok amaçla kullanılabilir. Aşağıdakilerden
BİYOKİMYADA METABOLİK YOLLAR DERSİ VİZE SINAV SORULARI (05.11.2012) (Toplam 4 sayfa olup 25 soru içerir) (DERSİN KODU: 217) Adı Soyadı: A Fakülte No: 1- Asetil KoA, birçok amaçla kullanılabilir. Aşağıdakilerden
Sitrik Asit Döngüsü. (Trikarboksilik Asit Döngüsü, Krebs Döngüsü)
 Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
Sitrik Asit Döngüsü (Trikarboksilik Asit Döngüsü, Krebs Döngüsü) Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Ünversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı, Le>oşa, KKTC Sir Hans
Beslenmeden hemen sonra, artan kan glikoz seviyesi ile birlikte insülin hormon seviyesi de artar. Buna zıt olarak glukagon hormon düzeyi azalır.
 Seçmeli Ders: Dokular ve Organlar Arası Metabolik İlişkiler 1.HAFTA Normal metabolizmada aktif olan günlük akış; Yaşamak için gerekli olan enerji akışı, dışardan alınan gıdalardan elde edilir. Kullanılan
Seçmeli Ders: Dokular ve Organlar Arası Metabolik İlişkiler 1.HAFTA Normal metabolizmada aktif olan günlük akış; Yaşamak için gerekli olan enerji akışı, dışardan alınan gıdalardan elde edilir. Kullanılan
Hücre Solunumu: Kimyasal Enerji Eldesi
 Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
Hücre Solunumu: Kimyasal Enerji Eldesi Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. Organik moleküllerin atomları enerji depolamaya müsaittir. Hücreler enzimler aracılığı ile organik
DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI TRİGLİSERİTLERİN SENTEZİ
 9. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI Palmitoleik ve oleik asitlerin sentezi için palmitik ve stearik asitler hayvansal organizmalardaki çıkş maddeleridir.
9. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI DOYMAMIŞ YAĞ ASİTLERİNİN OLUŞMASI Palmitoleik ve oleik asitlerin sentezi için palmitik ve stearik asitler hayvansal organizmalardaki çıkş maddeleridir.
25.03.2015. 1. Glukoz - 6 Fosfataz enzim eksikliğinde hangi glikojen depo hastalığı oluşur?
 1. Glukoz - 6 Fosfataz enzim eksikliğinde hangi glikojen depo hastalığı oluşur? a. Tıp II - Pompe hastalığı b. Tip III - Forbes - Cori Hastalığı c. Tip I- Von Gierke Hastalığı d.tıp V- Mc Ardle Hastalığı.
1. Glukoz - 6 Fosfataz enzim eksikliğinde hangi glikojen depo hastalığı oluşur? a. Tıp II - Pompe hastalığı b. Tip III - Forbes - Cori Hastalığı c. Tip I- Von Gierke Hastalığı d.tıp V- Mc Ardle Hastalığı.
Notlarımıza iyi çalışan kursiyerlerimiz soruların çoğunu rahatlıkla yapılabileceklerdir.
 Biyokimya sınavı orta zorlukta bir sınavdı. 1-2 tane zor soru ve 5-6 tane eski soru soruldu. Soruların; 16 tanesi temel bilgi, 4 tanesi ise detay bilgi ölçmekteydi. 33. soru mikrobiyolojiye daha yakındır.
Biyokimya sınavı orta zorlukta bir sınavdı. 1-2 tane zor soru ve 5-6 tane eski soru soruldu. Soruların; 16 tanesi temel bilgi, 4 tanesi ise detay bilgi ölçmekteydi. 33. soru mikrobiyolojiye daha yakındır.
Solunumda organik bileşikler karbondioksite yükseltgenir ve absorbe edilen oksijen ise suya indirgenir.
 Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Solunum bütün aktif hücrelerde oksijenin absorbe edilmesi ve buna eşdeğer miktarda karbondioksitin salınması şeklinde sürekli olarak devam eden bir prosestir. Solunumda organik bileşikler karbondioksite
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu)
 Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
Yağ Asitlerinin Metabolizması- I Yağ Asitlerinin Yıkılması (Oksidasyonu) Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Yağ Asitleri Uzun karbon zincirine sahip
GLİKOJEN METABOLİZMASI
 METABOLİZMASI DİLDAR KONUKOĞLU TIBBİ BİYOKİMYA 8.4.2015 DİLDAR KONUKOĞLU 1 YAPISI Alfa-[1,6] glikozid Alfa- [1-4] glikozid bağı yapısal olarak D-glukozdan oluşmuş dallanmış yapı gösteren homopolisakkarittir.
METABOLİZMASI DİLDAR KONUKOĞLU TIBBİ BİYOKİMYA 8.4.2015 DİLDAR KONUKOĞLU 1 YAPISI Alfa-[1,6] glikozid Alfa- [1-4] glikozid bağı yapısal olarak D-glukozdan oluşmuş dallanmış yapı gösteren homopolisakkarittir.
LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ SAFRA ASİTLERİ
 8. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ 1. Yapısal fonksiyon görevi: Lipitler fosfolipitler başta olmak üzere hücre ve organel zarlarının yapısına girer
8. Hafta: Lipit Metabolizması: Prof. Dr. Şule PEKYARDIMCI LİPİTLERİN ORGANİZMADAKİ GÖREVLERİ 1. Yapısal fonksiyon görevi: Lipitler fosfolipitler başta olmak üzere hücre ve organel zarlarının yapısına girer
Enzimler. Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO
 Enzimler Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO Enzimler Biyokimyasal olayların vücutta yaşam ile uyumlu bir şekilde gerçekleşmesini sağlayan katalizörlerdir. Katalitik RNA moleküllerinin
Enzimler Yrd.Doç.Dr.Funda GÜLCÜ BULMUŞ Fırat Üniversitesi SHMYO Enzimler Biyokimyasal olayların vücutta yaşam ile uyumlu bir şekilde gerçekleşmesini sağlayan katalizörlerdir. Katalitik RNA moleküllerinin
Yağ Asitlerinin β Oksidayonu. Prof. Dr. Fidancı
 Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
Yağ Asitlerinin β Oksidayonu Prof. Dr. Fidancı Yağ Asitlerinin Beta Oksidasyonu Yağ asitlerinin enerji üretimi amacı ile yıkımında (yükseltgenme) en önemli yol β oksidasyon yoldudur. β oksidasyon yolu
Enzimlerin Yapısı. Enzimler biyokatalizörlerdir,
 Enzimler biyokatalizörlerdir,, Prof. Dr. Muhsin KONUK H 2 O 2 H 2 O + ½ O 2 A.E = 18.16 kkal/mol Kollaidal platin A.E= 11.71 kkal/mol Katalaz A.E = 1.91 kkal/mol Enzimlerin Yapısı Basit enzimler: Pepsin,
Enzimler biyokatalizörlerdir,, Prof. Dr. Muhsin KONUK H 2 O 2 H 2 O + ½ O 2 A.E = 18.16 kkal/mol Kollaidal platin A.E= 11.71 kkal/mol Katalaz A.E = 1.91 kkal/mol Enzimlerin Yapısı Basit enzimler: Pepsin,
METABOLİZMA REAKSİYONLARI. Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV
 METABOLİZMA REAKSİYONLARI Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV METABOLİZMA Canlı sistemde maddelerin uğradığı kimyasal değişikliklerin hepsine birden metabolizma, bu değişiklikleri meydana
METABOLİZMA REAKSİYONLARI Hazırlayanlar Prof. Dr. Ayşe CAN Prof.Dr. Nuriye AKEV METABOLİZMA Canlı sistemde maddelerin uğradığı kimyasal değişikliklerin hepsine birden metabolizma, bu değişiklikleri meydana
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın
 İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın Mitokondri, ökaryotik organizmanın farklı bir organeli Şekilleri küremsi veya uzun silindirik Çapları 0.5-1 μm uzunlukları 2-6 μm Sayıları
İstanbul Tıp Fakültesi Tıbbi Biyoloji ABD Prof. Dr. Filiz Aydın Mitokondri, ökaryotik organizmanın farklı bir organeli Şekilleri küremsi veya uzun silindirik Çapları 0.5-1 μm uzunlukları 2-6 μm Sayıları
Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı
 YAĞ ASİTLERİNİN OKSİDASYONU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPOSİTLERDEN MOBİLİZASYONU ATGL; adiposit triaçilgliserol lipaz, HSL; hormona duyarlı
YAĞ ASİTLERİNİN OKSİDASYONU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPOSİTLERDEN MOBİLİZASYONU ATGL; adiposit triaçilgliserol lipaz, HSL; hormona duyarlı
TEST 1. Hücre Solunumu. 4. Aşağıda verilen moleküllerden hangisi oksijenli solunumda substrat olarak kullanılamaz? A) Glikoz B) Mineral C) Yağ asidi
 1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
1. Termometre Çimlenen bezelye tohumlar Termos Çimlenen bezelye tohumları oksijenli solunum yaptığına göre yukarıdaki düzenekle ilgili, I. Termostaki oksijen miktarı azalır. II. Termometredeki sıcaklık
Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir.
 METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
METABOLİZMA ve ENZİMLER METABOLİZMA Hücrelerde gerçekleşen yapım, yıkım ve dönüşüm olaylarının bütününe metabolizma denir. A. ÖZÜMLEME (ANABOLİZMA) Metabolizmanın yapım reaksiyonlarıdır. Bu tür olaylara
Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol)
 hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
hücre solunumu Hücre solunumu ve fermentasyon enerji veren katabolik yollardır. (ΔG=-686 kcal/mol) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 0 + enerji (ATP + ısı) Hücre solunumu karbonhidratlar, yağlar ve protein
21.11.2008. I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI.
 Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
Hazırlayan: Sibel ÖCAL 0501150027 I. Koenzim A nedir? II. Tarihsel Bakış III. Koenzim A nın yapısı IV. Asetil-CoA nedir? V. Koenzim A nın katıldığı reaksiyonlar VI. Eksikliği 1 2 Pantotenik asit (Vitamin
Hücresel Enerji Sistemleri. Prof. Dr. Fadıl ÖZYENER
 Hücresel Enerji Sistemleri I-II Prof. Dr. Fadıl ÖZYENER Metabolizma Vücudun temel işlevlerini devam ettirebilmek için kullanılan enerji miktarıdır. Enerji değişimi içeren tepkimeler; Katabolik: Enerji
Hücresel Enerji Sistemleri I-II Prof. Dr. Fadıl ÖZYENER Metabolizma Vücudun temel işlevlerini devam ettirebilmek için kullanılan enerji miktarıdır. Enerji değişimi içeren tepkimeler; Katabolik: Enerji
METABOLİZMA. Prof. Dr. Arif ALTINTAŞ
 METABOLİZMA Prof. Dr. Arif ALTINTAŞ altintas@veterinary.ankara.edu.tr Canlı organizmaların özelliği olarak Metabolizma Canlıların yapı taşlarının devamlı yapım, yıkım ve değişim içinde bulunması ve bu
METABOLİZMA Prof. Dr. Arif ALTINTAŞ altintas@veterinary.ankara.edu.tr Canlı organizmaların özelliği olarak Metabolizma Canlıların yapı taşlarının devamlı yapım, yıkım ve değişim içinde bulunması ve bu
ayxmaz/biyoloji Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H
 Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Adı: 1.Aşağıda verilen atomların bağ yapma sayılarını (H) ekleyerek gösterin. C N O H 2.Radyoaktif izotoplar biyologları için önemlidir? Aşağıda radyoakif maddelerin kullanıldığı alanlar sıralanmıştır.bunlarla
Kolesterol Metabolizması. Prof. Dr. Fidancı
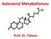 Kolesterol Metabolizması Prof. Dr. Fidancı Kolesterol oldukça önemli bir biyolojik moleküldür. Membran yapısında önemli rol oynar. Steroid hormonların ve safra asitlerinin sentezinde öncül maddedir. Diyet
Kolesterol Metabolizması Prof. Dr. Fidancı Kolesterol oldukça önemli bir biyolojik moleküldür. Membran yapısında önemli rol oynar. Steroid hormonların ve safra asitlerinin sentezinde öncül maddedir. Diyet
BİYOİNORGANİK KİMYA 5. HAFTA
 BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
BİYOİNORGANİK KİMYA 5. HAFTA ESER ELEMENTLER İnsan vücudunda en yüksek oranda bulunan element oksijendir. İkincisi ise karbondur. İnsan vücudunun kütlesinin %99 u sadece 6 elementten meydana gelir. Bunlar:
OKSİJENLİ SOLUNUM
 1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
1 ----------------------- OKSİJENLİ SOLUNUM ----------------------- **Oksijenli solunum (aerobik): Besinlerin, oksijen yardımıyla parçalanarak, ATP sentezlenmesine oksijenli solunum denir. Enzim C 6 H
BĠYOKĠMYA DOÇ. DR. MEHMET KARACA
 BĠYOKĠMYA DOÇ. DR. MEHMET KARACA TANIMLAR GLĠKOLĠZ: (LĠZ LEZYON (LYSIS), YIKAMA, PARÇALAMA ANLAMINDADIR). Glikoliz hücrede sitozolde gerçekleģir. Glikoliz olayı hem aerobik hem de anaerobik organizmalarda
BĠYOKĠMYA DOÇ. DR. MEHMET KARACA TANIMLAR GLĠKOLĠZ: (LĠZ LEZYON (LYSIS), YIKAMA, PARÇALAMA ANLAMINDADIR). Glikoliz hücrede sitozolde gerçekleģir. Glikoliz olayı hem aerobik hem de anaerobik organizmalarda
(Anaplerotik Reaksiyonlar)
 5. Hafta: Karbohidrat Metabolizması Prof. Dr. Şule PEKYARDIMCI TCA ARA ÜRÜNLERİNİN ANABOLİK İŞLEMLERDE KULLANILMASI (Anaplerotik Reaksiyonlar) Sitrik asit döngüsü, aerobik organizmalarda amfibolik bir
5. Hafta: Karbohidrat Metabolizması Prof. Dr. Şule PEKYARDIMCI TCA ARA ÜRÜNLERİNİN ANABOLİK İŞLEMLERDE KULLANILMASI (Anaplerotik Reaksiyonlar) Sitrik asit döngüsü, aerobik organizmalarda amfibolik bir
ENZİMLERİN GENEL ÖZELLİKLERİ - II. Doç Dr. Nurzen SEZGİN
 ENZİMLERİN GENEL ÖZELLİKLERİ - II Doç Dr. Nurzen SEZGİN bstrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate
ENZİMLERİN GENEL ÖZELLİKLERİ - II Doç Dr. Nurzen SEZGİN bstrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate Enzyme substrate
GLİKOLİZİN KONTROLU Prof. Dr. İzzet Hamdi Öğüş
 GLİKOLİZİN KONTROLU Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Üniversitesi Tıp Fakültesi Biyokimya Anabilim Dalı, Le>oşa, KKTC GLİKOLİZİN ALLOSTERİK DÜZENLENMESİ Metabolik düzenleme: Bütün
GLİKOLİZİN KONTROLU Prof. Dr. İzzet Hamdi Öğüş hamdiogus@gmail.com Yakın Doğu Üniversitesi Tıp Fakültesi Biyokimya Anabilim Dalı, Le>oşa, KKTC GLİKOLİZİN ALLOSTERİK DÜZENLENMESİ Metabolik düzenleme: Bütün
III-Hayatın Oluşturan Kimyasal Birimler
 III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
III-Hayatın Oluşturan Kimyasal Birimler MBG 111 BİYOLOJİ I 3.1.Karbon:Biyolojik Moleküllerin İskeleti *Karbon bütün biyolojik moleküllerin omurgasıdır, çünkü dört kovalent bağ yapabilir ve uzun zincirler
Enzimler ENZİMLER ENZİMLER ENZİMLER İSİMLENDİRME ENZİMLER
 Enzimler Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Vücuttaki tüm reaksiyonlar, tüm işlem sonunda kendileri değişmeden reaksiyonların hızını artıran protein katalizörler olan enzimler
Enzimler Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Vücuttaki tüm reaksiyonlar, tüm işlem sonunda kendileri değişmeden reaksiyonların hızını artıran protein katalizörler olan enzimler
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
BİY 471 Lipid Metabolizması-I. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 471 Lipid Metabolizması-I Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Lipoproteinler Türev lipidler: Glikolipidler Lipoproteinler Lipoproteinler, lipidlerin proteinlerle oluşturdukları komplekslerdir.
BİY 471 Lipid Metabolizması-I Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Lipoproteinler Türev lipidler: Glikolipidler Lipoproteinler Lipoproteinler, lipidlerin proteinlerle oluşturdukları komplekslerdir.
ORGANİK BİLEŞİKLER Karbon Dünyası
 ORGANİK BİLEŞİKLER Canlı Organizmalarda bulunan büyük ve karışık yapılı moleküller yani makromoleküllerdir Makromoleküllerin hepsinde karbon vardır. Karbon Dünyası Makromoleküller birbirlerine kovalent
ORGANİK BİLEŞİKLER Canlı Organizmalarda bulunan büyük ve karışık yapılı moleküller yani makromoleküllerdir Makromoleküllerin hepsinde karbon vardır. Karbon Dünyası Makromoleküller birbirlerine kovalent
AMİNO ASİTLER. Yrd. Doç. Dr. Osman İBİŞ
 AMİNO ASİTLER Yrd. Doç. Dr. Osman İBİŞ Proteinler, tüm hücrelerde ve hücrelerin tüm bölümlerinde en çok bulunan biyolojik makromoleküllerdir ve canlının kuru ağırlığının % 50 veya daha fazlasını kapsarlar.
AMİNO ASİTLER Yrd. Doç. Dr. Osman İBİŞ Proteinler, tüm hücrelerde ve hücrelerin tüm bölümlerinde en çok bulunan biyolojik makromoleküllerdir ve canlının kuru ağırlığının % 50 veya daha fazlasını kapsarlar.
LİPOPROTEİN METABOLİZMASI. Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı
 LİPOPROTEİN METABOLİZMASI Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı Lipoprotein Nedir? 1- Lipidler Hidrofobik lipidler çekirdekte (Trigliserit, Kolesterol esterleri)
LİPOPROTEİN METABOLİZMASI Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı Lipoprotein Nedir? 1- Lipidler Hidrofobik lipidler çekirdekte (Trigliserit, Kolesterol esterleri)
Aminoasitler proteinleri oluşturan temel yapı taşlarıdır. Amino asitler, yapılarında hem amino grubu (-NH2) hem de karboksil grubu (-COOH) içeren
 AMİNO ASİTLER Aminoasitler proteinleri oluşturan temel yapı taşlarıdır. Amino asitler, yapılarında hem amino grubu (-NH2) hem de karboksil grubu (-) içeren bileşiklerdir. Amino asitler, hem bir asidik
AMİNO ASİTLER Aminoasitler proteinleri oluşturan temel yapı taşlarıdır. Amino asitler, yapılarında hem amino grubu (-NH2) hem de karboksil grubu (-) içeren bileşiklerdir. Amino asitler, hem bir asidik
YAĞ ASİTLERİNİN OKSİDASYONU
 YAĞ ASİTLERİNİN KSİDASYNU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPSİTLERDEN MBİLİZASYNU Adrenalin Glukagon İnsülin reseptör Adenilat siklaz G protein ATP
YAĞ ASİTLERİNİN KSİDASYNU Prof.Dr. Yeşim ÖZKAN G.Ü. Eczacılık Fakültesi Biyokimya Anabilim Dalı YAĞ ASİTLERİNİN ADİPSİTLERDEN MBİLİZASYNU Adrenalin Glukagon İnsülin reseptör Adenilat siklaz G protein ATP
Midede etkin enzim Pepsin Ürün; Albumoz ve pepton Barsakta etkili enzimler Tripsin Kimotripsin Elaztaz Karboksipeptidaz, Aminopeptidaz Dipeptidaz,
 PROTEİN SİNDİRİMİ Polipeptit zincirini oluşturan amino asitler arasındaki peptit bağlarının hidrolizi; proteoliz Proteinlerin sindirimi midede başlar ve barsakta tamamlanır. Midede etkin enzim Pepsin Ürün;
PROTEİN SİNDİRİMİ Polipeptit zincirini oluşturan amino asitler arasındaki peptit bağlarının hidrolizi; proteoliz Proteinlerin sindirimi midede başlar ve barsakta tamamlanır. Midede etkin enzim Pepsin Ürün;
BİY 315 Lipid Metabolizması-II. Yrd. Doç. Dr. Ebru SAATÇİ Güz Yarı Dönemi
 BİY 315 Lipid Metabolizması-II Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Yağ Asidi Oksidasyonu Besinlerin sindirimi sonucu elde edilen yağlar, bağırsaktan geçerek lenf sistemine ulaşır ve bu
BİY 315 Lipid Metabolizması-II Yrd. Doç. Dr. Ebru SAATÇİ 2008-2009 Güz Yarı Dönemi Yağ Asidi Oksidasyonu Besinlerin sindirimi sonucu elde edilen yağlar, bağırsaktan geçerek lenf sistemine ulaşır ve bu
Amino Asitler. Amino asitler, yapılarında hem amino grubu ( NH 2 ) hem de karboksil grubu ( COOH) içeren bileşiklerdir.
 Amino Asitler Amino asitler, yapılarında hem amino grubu ( NH 2 ) hem de karboksil grubu ( COOH) içeren bileşiklerdir. 1 Fizyolojik ph da, amino asitlerin amino grubu proton taşır ve pozitif yüklüdür;
Amino Asitler Amino asitler, yapılarında hem amino grubu ( NH 2 ) hem de karboksil grubu ( COOH) içeren bileşiklerdir. 1 Fizyolojik ph da, amino asitlerin amino grubu proton taşır ve pozitif yüklüdür;
Biyolojik Oksidasyon. Yrd.Doç.Dr.Filiz Bakar Ateş
 Biyolojik Oksidasyon Yrd.Doç.Dr.Filiz Bakar Ateş Canlı hücreler, dışarıdan aldıkları kimyasal veya fiziksel enerjiyi, geliştirdiği bir sistemle, ATP ile taşınan biyolojik enerjiye çevirirler; ATP yi kullanarak
Biyolojik Oksidasyon Yrd.Doç.Dr.Filiz Bakar Ateş Canlı hücreler, dışarıdan aldıkları kimyasal veya fiziksel enerjiyi, geliştirdiği bir sistemle, ATP ile taşınan biyolojik enerjiye çevirirler; ATP yi kullanarak
Yağ Asitlerinin Biyosentezi. Prof. Dr. Fidancı
 Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
Yağ Asitlerinin Biyosentezi Prof. Dr. Fidancı Yağ asitlerinin sentezi özellikle karaciğer ve yağ dokusu hücrelerinde iki şekilde gerçekleşir. Bu sentez şekillerinden biri yağ asitlerinin, hücrenin sitoplazma
Prof. Dr. Şule PEKYARDIMCI
 13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
13. Hafta: Vitaminler ve Koenzimler: Vitamin tanımı, vitaminlerin görevleri, vitaminlerin sınıflandırılmaları, koenzim tanımı, önemli vitaminler, suda çözünen vitaminler, yağda çözünen vitaminler, vitaminlerin
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir.
 Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
Canlıların yapısına en fazla oranda katılan organik molekül çeşididir. Deri, saç, tırnak, boynuz gibi oluşumların temel maddesi proteinlerdir. Proteinlerin yapısında; Karbon ( C ) Hidrojen ( H ) Oksijen
6. glikolizde enerji kazanım hesaplamalarında; Substrat düzeyinde -ATP üretimi yaklaşık yüzde kaç hesaplanır? a. % 0 b. % 2 c. % 10 d. % 38 e.
 www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
www.lisebiyoloji.com ayxmaz/biyoloji Test Çoktan Seçmeli 1. Hangi terim moleküllerin parçalanması ile açığa çıkan enerjinin depolandığı metabolik yolları ifade eder? a. anabolik yollar b. Katabolik yollar
Metabolizma. Metabolizmaya giriş. Metabolizmaya giriş. Metabolizmayı tanımlayacak olursak
 Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
Metabolizma Yaşamak için beslenmek zorundayız. Çünkü; Besinlerden enerji elde ederiz ve bu enerji; Hücresel faaliyetleri sürdürmemiz, Hareket etmemiz, Taşınım olaylarını gerçekleştirebilmemiz, Vücut sıcaklığını
TIBBİ BİYOLOJİ YAĞLARIN VE PROTEİNLERİN OKSİDASYONU
 TIBBİ BİYOLOJİ YAĞLARIN VE PROTEİNLERİN OKSİDASYONU Yağların Oksidasyonu Besinlerle alınan yağlar ince bağırsakta safra asidi tuzları ile önce emülsiyonlaşarak küçük damlacıklar haline getirilir. Sonra
TIBBİ BİYOLOJİ YAĞLARIN VE PROTEİNLERİN OKSİDASYONU Yağların Oksidasyonu Besinlerle alınan yağlar ince bağırsakta safra asidi tuzları ile önce emülsiyonlaşarak küçük damlacıklar haline getirilir. Sonra
Kolesterol Metabolizması. Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D.
 Kolesterol Metabolizması Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Steroidler Steroidlerin yapı taşı birbirine yapışık 4 halkalı karbon iskelehdir, bu yapı
Kolesterol Metabolizması Yrd. Doç. Dr. Bekir Engin Eser Zirve Üniversitesi EBN Tıp Fakültesi Tıbbi Biyokimya A.B.D. Steroidler Steroidlerin yapı taşı birbirine yapışık 4 halkalı karbon iskelehdir, bu yapı
LİPOPROTEİN METABOLİZMASI. Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı
 LİPOPROTEİN METABOLİZMASI Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı Lipoprotein Nedir? 1- Lipidler Hidrofobik lipidler çekirdekte (Trigliserit, Kolesterol esterleri)
LİPOPROTEİN METABOLİZMASI Prof.Dr. Yeşim ÖZKAN Gazi Üniversitesi Eczacılık Fakültesi Biyokimya Anabilim Dalı Lipoprotein Nedir? 1- Lipidler Hidrofobik lipidler çekirdekte (Trigliserit, Kolesterol esterleri)
GLİKOJEN FOSFORİLAZ HAZIRLAYAN: HATİCE GÜLBENİZ ( ) Prof. Dr. Figen ERKOÇ GAZİ EĞİTİM FAKÜLTESİ GAZİ ÜNİVERSİTESİ
 GLİKOJEN FOSFORİLAZ HAZIRLAYAN: HATİCE GÜLBENİZ (050559016) Prof. Dr. Figen ERKOÇ GAZİ EĞİTİM FAKÜLTESİ GAZİ ÜNİVERSİTESİ Karaciğer ve kas glikojeninin kana ve kas dokusuna glukoz sağlamak üzere kısmen
GLİKOJEN FOSFORİLAZ HAZIRLAYAN: HATİCE GÜLBENİZ (050559016) Prof. Dr. Figen ERKOÇ GAZİ EĞİTİM FAKÜLTESİ GAZİ ÜNİVERSİTESİ Karaciğer ve kas glikojeninin kana ve kas dokusuna glukoz sağlamak üzere kısmen
METABOL ZMA. Metabolizmanın amacı nedir?
 METABOL ZMA Canlıda olu an ve devam eden fiziksel ve kimyasal olayların tümüne birden metabolizma adı verilmektedir Ara metabolizma, katabolizma ve anabolizma olmak üzere iki faz içerir; bu iki faz arasındaki
METABOL ZMA Canlıda olu an ve devam eden fiziksel ve kimyasal olayların tümüne birden metabolizma adı verilmektedir Ara metabolizma, katabolizma ve anabolizma olmak üzere iki faz içerir; bu iki faz arasındaki
AMİNO ASİTLER. COO - H 3 N + C a H R
 AMİNO ASİTLER AMİNO ASİTLER H 3 N + C a H R a-amino Asit (AA) Yapılarında Amino (-NH 3 + ) grubu Karboksil (- ) grubu Yan zincir ( R ) taşıyan organik bileşiklerdir (a-amino karboksilik asitler) Kısa zincirli
AMİNO ASİTLER AMİNO ASİTLER H 3 N + C a H R a-amino Asit (AA) Yapılarında Amino (-NH 3 + ) grubu Karboksil (- ) grubu Yan zincir ( R ) taşıyan organik bileşiklerdir (a-amino karboksilik asitler) Kısa zincirli
BİYOKİMYA II EK NOT. Ortak biyokimyasal tepkimeler
 BİYOKİMYA II EK NOT Dr. NaĢit ĠĞCĠ Ortak biyokimyasal tepkimeler Ġndirgenme-yükseltgenme (redüksiyon-oksidasyon, redoks) tepkimeleri de biyokimya açısından çok önemli tepkimelerdir. Basitçe, elektron kaybı
BİYOKİMYA II EK NOT Dr. NaĢit ĠĞCĠ Ortak biyokimyasal tepkimeler Ġndirgenme-yükseltgenme (redüksiyon-oksidasyon, redoks) tepkimeleri de biyokimya açısından çok önemli tepkimelerdir. Basitçe, elektron kaybı
DÖNEM II DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 24 ARALIK MART 2019)
 2018-2019 DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 24 ARALIK 2018 01 MART 2019) DERSLER TEORİK PRATİK TOPLAM Anatomi 26 5X2 36 Fizyoloji 22 4X2 30 Histoloji ve Embriyoloji 12 6X2 24 Tıbbi Biyokimya
2018-2019 DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 24 ARALIK 2018 01 MART 2019) DERSLER TEORİK PRATİK TOPLAM Anatomi 26 5X2 36 Fizyoloji 22 4X2 30 Histoloji ve Embriyoloji 12 6X2 24 Tıbbi Biyokimya
Hücreler Enerjiyi Nasıl Elde Eder?
 Hücreler Enerjiyi Nasıl Elde Eder? MBG 111 BİYOLOJİ I Hazırlayan: Yrd.Doç.Dr. Yosun MATER Ekosistem ve Enerji Ekosistemde enerjinin akışı güneş ışığı ve ısı şeklinde gözlenir. Tam tersine canlı hücrelerde
Hücreler Enerjiyi Nasıl Elde Eder? MBG 111 BİYOLOJİ I Hazırlayan: Yrd.Doç.Dr. Yosun MATER Ekosistem ve Enerji Ekosistemde enerjinin akışı güneş ışığı ve ısı şeklinde gözlenir. Tam tersine canlı hücrelerde
AZOTLU BİYOMOLEKÜLLERİN METABOLİZMASI. Protein Metabolizması Doç. Dr. A. Eser ELÇİN
 AZOTLU BİYOMOLEKÜLLERİN METABOLİZMASI Protein Metabolizması Doç. Dr. A. Eser ELÇİN Proteinler Makromoleküldür. Karbon, Hidrojen, Oksijen, Azot ve Kükürt içerir. Azot %16 sını içerir. Anorganik azottur.
AZOTLU BİYOMOLEKÜLLERİN METABOLİZMASI Protein Metabolizması Doç. Dr. A. Eser ELÇİN Proteinler Makromoleküldür. Karbon, Hidrojen, Oksijen, Azot ve Kükürt içerir. Azot %16 sını içerir. Anorganik azottur.
ORGANİZMANIN ÖNEMLİ METABOLİK DURUMLARI
 ORGANİZMANIN ÖNEMLİ METABOLİK DURUMLARI Metabolizma durumları Memelilerde ana hatları ile en az iki metabolizma durumu önemlidir. Bunların birincisi besin maddelerinin kana emildiği beslenme (rezorpsiyon),
ORGANİZMANIN ÖNEMLİ METABOLİK DURUMLARI Metabolizma durumları Memelilerde ana hatları ile en az iki metabolizma durumu önemlidir. Bunların birincisi besin maddelerinin kana emildiği beslenme (rezorpsiyon),
Sfingozin türevi membran lipidleri
 Dr. Suat Erdoğan Sfingozin türevi membran lipidleri Sfingolipidler Sfingomyelin Glikolipidler Kolesterol ve Steroidler Bu tür lipidler gliserol içermezler Yapıda bir amino alkol olan sfingozin bulunur
Dr. Suat Erdoğan Sfingozin türevi membran lipidleri Sfingolipidler Sfingomyelin Glikolipidler Kolesterol ve Steroidler Bu tür lipidler gliserol içermezler Yapıda bir amino alkol olan sfingozin bulunur
OKSİDATİF FOSFORİLASYON. Prof. Dr. Yeşim ÖZKAN
 OKSİDATİF FOSFORİLASYON Prof. Dr. Yeşim ÖZKAN Canlı organizmalarda; Biyosentez Aktif Transport Hareket gibi süreçlerde enerjiye ihtiyaç vardır. Bu enerji tüketilen yiyeceklerden sağlanmaktadır. Enerji
OKSİDATİF FOSFORİLASYON Prof. Dr. Yeşim ÖZKAN Canlı organizmalarda; Biyosentez Aktif Transport Hareket gibi süreçlerde enerjiye ihtiyaç vardır. Bu enerji tüketilen yiyeceklerden sağlanmaktadır. Enerji
Canlı hücrelerin bilinen kimyasal yapı taşları
 anlı hücrelerin bilinen kimyasal yapı taşları rganik maddeler a) Karbonhidratlar b) Proteinler, amino asitler ve peptitler c) Enzimler d) Lipidler e) Nükleotidler ve nükleik asitler f) Vitaminler İnorganik
anlı hücrelerin bilinen kimyasal yapı taşları rganik maddeler a) Karbonhidratlar b) Proteinler, amino asitler ve peptitler c) Enzimler d) Lipidler e) Nükleotidler ve nükleik asitler f) Vitaminler İnorganik
DÖNEM II DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 25 ARALIK 02 MART 2018)
 2017-2018 DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 25 ARALIK 02 MART 2018) DERSLER TEORİK PRATİK TOPLAM Anatomi 26 5X2 31 Biyofizik 4-4 Fizyoloji 22 5X2 27 Histoloji ve Embriyoloji 12 6X2 18 Tıbbi
2017-2018 DERS YILI SİNDİRİM VE METABOLİZMA DERS KURULU ( 25 ARALIK 02 MART 2018) DERSLER TEORİK PRATİK TOPLAM Anatomi 26 5X2 31 Biyofizik 4-4 Fizyoloji 22 5X2 27 Histoloji ve Embriyoloji 12 6X2 18 Tıbbi
MİNERALLER. Dr. Diyetisyen Hülya YARDIMCI
 MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
MİNERALLER Dr. Diyetisyen Hülya YARDIMCI MİNERALLER İnsan vücudunun yaklaşık %4-5 i minareldir.bununda yarıya yakını Ca, ¼ ü fosfordur. Mg, Na, Cl, S diğer makro minerallerdir. Bunların dışında kalanlar
6. BÖLÜM MİKROBİYAL METABOLİZMA
 6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
6. BÖLÜM MİKROBİYAL METABOLİZMA 1 METABOLİZMA Hücrede meydana gelen tüm reaksiyonlara denir Anabolizma: Basit moleküllerden kompleks moleküllerin sentezlendiği enerji gerektiren reaksiyonlardır X+Y+ENERJİ
PÜRİN VE PİRİMİDİN METABOLİZMASI
 PÜRİN VE PİRİMİDİN METABOLİZMASI Nükleotidlerin vücuda alınımı Nükleotidler, nükleik asitlerin yapı taşları olarak besinlerde bulunur. Hücre içeren besinlerle alınan nükleik asitler, mide enzimlerinden
PÜRİN VE PİRİMİDİN METABOLİZMASI Nükleotidlerin vücuda alınımı Nükleotidler, nükleik asitlerin yapı taşları olarak besinlerde bulunur. Hücre içeren besinlerle alınan nükleik asitler, mide enzimlerinden
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur.
 Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
Kloroform, eter ve benzen gibi organik çözücülerde çözünen bunun yanı sıra suda çözünmeyen veya çok az çözünen organik molekül grubudur. Yağların suda çözünmemesi canlılığın devamı içi önemlidir. Çünkü
ENDOTEL VE BİYOKİMYASAL MOLEKÜLLER
 ENDOTEL VE BİYOKİMYASAL MOLEKÜLLER Endotel Damar duvarı ve dolaşan kan arasında tek sıra endotel hücresinden oluşan işlevsel bir organdır Endotel en büyük endokrin organdır 70 kg lik bir kişide, kalp kitlesix5
ENDOTEL VE BİYOKİMYASAL MOLEKÜLLER Endotel Damar duvarı ve dolaşan kan arasında tek sıra endotel hücresinden oluşan işlevsel bir organdır Endotel en büyük endokrin organdır 70 kg lik bir kişide, kalp kitlesix5
Suda çözünebilen nişasta molekülleri pityalin (amilaz) enzimiyle küçük moleküllere parçalanır.
 CANLILARDA ENERJİ Besinlerin Enerjiye Dönüşümü Besin öğeleri: Karbonhidratlar, yağlar, proteinler, vitaminler, mineraller Besin maddelerindeki bu öğelerin vücut tarafından kullanılabilmesi için sindirilmesi
CANLILARDA ENERJİ Besinlerin Enerjiye Dönüşümü Besin öğeleri: Karbonhidratlar, yağlar, proteinler, vitaminler, mineraller Besin maddelerindeki bu öğelerin vücut tarafından kullanılabilmesi için sindirilmesi
Kaynak kitap: Biyokimya (Nobel Tıp Kitabevi). Karbonhidrat Metabolizması (12. Bölüm).
 METABOLİZMA DİLİMİ BİYOKİMYA ANABİLİM DALI DERSLERİ HEDEFLER: Bu dilim derslerinin sonunda öğrenci: Vücudun yaşam için gerekli enerjiyi sağladığı reaksiyonları bilmeli Aerobik ve anaerobik koşullarda enerji
METABOLİZMA DİLİMİ BİYOKİMYA ANABİLİM DALI DERSLERİ HEDEFLER: Bu dilim derslerinin sonunda öğrenci: Vücudun yaşam için gerekli enerjiyi sağladığı reaksiyonları bilmeli Aerobik ve anaerobik koşullarda enerji
Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler
 Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler proteindir. Katalitik aktiviteleri doğal protein konformasyonunun
Enzimler Enzimler metabolizma reaksiyonlarını hızlandıran moleküllerdir. Katalitik RNA moleküllerinin küçük bir grubu hariç, bütün enzimler proteindir. Katalitik aktiviteleri doğal protein konformasyonunun
MİTOKONDRİ Doç. Dr. Mehmet GÜVEN
 MİTOKONDRİ Doç.. Dr. Mehmet GÜVENG Hemen hemen bütün b ökaryotik hücrelerde ve ökaryotik mikroorganizmalarda bulunur. Eritrositlerde, bakterilerde ve yeşil alglerde mitokondri yoktur. Şekilleri (küremsi
MİTOKONDRİ Doç.. Dr. Mehmet GÜVENG Hemen hemen bütün b ökaryotik hücrelerde ve ökaryotik mikroorganizmalarda bulunur. Eritrositlerde, bakterilerde ve yeşil alglerde mitokondri yoktur. Şekilleri (küremsi
Canlının yapısında bulunan organik molekül grupları; o Karbonhidratlar o Yağlar o Proteinler o Enzimler o Vitaminler o Nükleik asitler ve o ATP
 Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
Tamamı karbon ( C ) elementi taşıyan moleküllerden oluşan bir gruptur. Doğal organik bileşikler canlı vücudunda sentezlenir. Ancak günümüzde birçok organik bileşik ( vitamin, hormon, antibiyotik vb. )
En basit şekerlerdir. ll aldehid veya ketonlu türevleri olarak tanımlanır.
 En basit şekerlerdir. Monosakkaritler polihidroksilli illi alkollerin ll aldehid veya ketonlu türevleri olarak tanımlanır. Glukoz ve fruktoz gibi monosakaritler bunlara örnek verilebilir. Monosakkarit
En basit şekerlerdir. Monosakkaritler polihidroksilli illi alkollerin ll aldehid veya ketonlu türevleri olarak tanımlanır. Glukoz ve fruktoz gibi monosakaritler bunlara örnek verilebilir. Monosakkarit
ÇİSEM İLGİN ( ) LÜTFİYE ALAÇAM ( ) Prof. Dr. Figen ERKOÇ GAZİ ÜNİVERSİTESİ
 HAZIRLAYLANLAR ÇİSEM İLGİN (040559015) LÜTFİYE ALAÇAM (040559003) ZEYNEP HALICI (040559014) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ ÜNİVERSİTESİ 1 TRANSAMİNAZLAR Transaminazlar veya Aminotransferazlar
HAZIRLAYLANLAR ÇİSEM İLGİN (040559015) LÜTFİYE ALAÇAM (040559003) ZEYNEP HALICI (040559014) Prof. Dr. Figen ERKOÇ Gazi Eğitim Fakültesi GAZİ ÜNİVERSİTESİ 1 TRANSAMİNAZLAR Transaminazlar veya Aminotransferazlar
METABOLİZMA. Dr. Serkan SAYINER
 METABOLİZMA Dr. Serkan SAYINER serkan.sayiner@neu.edu.tr Genel Bakış Canlı organizmalar, kendilerini yenilemek, gelişmek ve üremek için kimyasal maddelere gereksinim duyarlar. Çünkü organizmanın tamamı
METABOLİZMA Dr. Serkan SAYINER serkan.sayiner@neu.edu.tr Genel Bakış Canlı organizmalar, kendilerini yenilemek, gelişmek ve üremek için kimyasal maddelere gereksinim duyarlar. Çünkü organizmanın tamamı
HÜCRE MEMBRANLARINDAN TAŞINMA
 2. Hafta : HücreYapısı ve Hücre Zarından Madde Taşınması Prof. Dr. Şule Pekyardımcı Organizmanın en önemli özellikleri (hareket, büyüme, üreme ve metabolizma) membranlarla ilişkilidir. Tüm hücre ve organellerde
2. Hafta : HücreYapısı ve Hücre Zarından Madde Taşınması Prof. Dr. Şule Pekyardımcı Organizmanın en önemli özellikleri (hareket, büyüme, üreme ve metabolizma) membranlarla ilişkilidir. Tüm hücre ve organellerde
Yağ ihtiyacı nereden karşılanır?
 Besinde Lipitler Besinsel Yağlar 1. Trigliseritler (%90) 2. Kolesterol (serbest ya da yağ asitlerine bağlı halde) 3. Serbest Yağ Asitleri 4. Fosfolipitler 5. Yağda Çözünen Vitaminler (A,D,E,K) Suda çözünmezler
Besinde Lipitler Besinsel Yağlar 1. Trigliseritler (%90) 2. Kolesterol (serbest ya da yağ asitlerine bağlı halde) 3. Serbest Yağ Asitleri 4. Fosfolipitler 5. Yağda Çözünen Vitaminler (A,D,E,K) Suda çözünmezler
METABOLİK DEĞİŞİKLİKLER VE FİZİKSEL PERFORMANS
 METABOLİK DEĞİŞİKLİKLER VE FİZİKSEL PERFORMANS Aerobik Antrenmanlar Sonucu Kasta Oluşan Adaptasyonlar Miyoglobin Miktarında oluşan Değişiklikler Hayvan deneylerinden elde edilen sonuçlar dayanıklılık antrenmanları
METABOLİK DEĞİŞİKLİKLER VE FİZİKSEL PERFORMANS Aerobik Antrenmanlar Sonucu Kasta Oluşan Adaptasyonlar Miyoglobin Miktarında oluşan Değişiklikler Hayvan deneylerinden elde edilen sonuçlar dayanıklılık antrenmanları
Organik Bileşikler. Karbonhidratlar. Organik Bileşikler YGS Biyoloji 1
 Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
Organik Bileşikler YGS Biyoloji 1 Hazırladığımız bu yazıda; organik bileşikler ve organik bileşiklerin yapısını, canlılarda bulunan organik bileşikleri ve bunların görevlerini, kullanım alanlarını, canlılar
Hücre. 1 µm = 0,001 mm (1000 µm = 1 mm)!
 HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
Metabolizma. Prof. Dr. Arif ALTINTAŞ Ankara Üniver. Veteriner Fakültesi Biyokimya Anabilim Dalı
 Metabolizma Prof. Dr. Arif ALTINTAŞ Ankara Üniver. Veteriner Fakültesi Biyokimya Anabilim Dalı Metabolik Yol Haritası Enerji Metabolizması Her makromolekül küçük alt moleküllere ayrılır: Karbonhidratlar
Metabolizma Prof. Dr. Arif ALTINTAŞ Ankara Üniver. Veteriner Fakültesi Biyokimya Anabilim Dalı Metabolik Yol Haritası Enerji Metabolizması Her makromolekül küçük alt moleküllere ayrılır: Karbonhidratlar
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon
 Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
Canlılarda Enerjitik Olaylar, Fotosentez ve Kemosentez, Aerobik Solunum ve Fermantasyon SOLUNUM İki çeşit solunum vardır HÜCRE DIŞI SOLUNUM: Canlıların dış ortamdan O 2 alıp, dış ortama
ENZİM KATALİZİNİN MEKANİZMALARI
 ENZİMLER 3. Hafta Ders Konuları 1) Enzim Katalizinin Mekanizmaları -Kovalan Kataliz -Yakınlığa (proximity) bağlı kataliz -Asit-Baz katalizi -Metal iyon katalizi 2) Enzimlerin Regülasyonu -Allosterik Regülasyon
ENZİMLER 3. Hafta Ders Konuları 1) Enzim Katalizinin Mekanizmaları -Kovalan Kataliz -Yakınlığa (proximity) bağlı kataliz -Asit-Baz katalizi -Metal iyon katalizi 2) Enzimlerin Regülasyonu -Allosterik Regülasyon
ELEKTRON TRANSPORT ZİNCİRİ VE OKSİDATİF FOSFORİLASYON. Doç.Dr.REMİSA GELİŞGEN
 ELEKTRON TRANSPORT ZİNCİRİ VE OKSİDATİF FOSFORİLASYON Doç.Dr.REMİSA GELİŞGEN OKSİDATİF FOSFORİLASYON Metabolik yakıt maddelerinin (glukoz, yağ asidleri, amino asidler gibi elektron vericileri) enzim katalizli
ELEKTRON TRANSPORT ZİNCİRİ VE OKSİDATİF FOSFORİLASYON Doç.Dr.REMİSA GELİŞGEN OKSİDATİF FOSFORİLASYON Metabolik yakıt maddelerinin (glukoz, yağ asidleri, amino asidler gibi elektron vericileri) enzim katalizli
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ
 HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
HÜCRE SOLUNUMU: KİMYASAL ENERJİ ELDESİ Güneş: Temel enerji kaynağı!!! Güneş ışığı bitkiler ve diğer organizmalar için temel enerji kaynağıdır. 2 Katabolik yollar Hücreler, enzimler aracılığı ile, potansiyel
PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER
 PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER Öncelikle, protein sentezinin yapılabilmesi için aşağıdakilerin mutlaka mevcut olması gerekmektedir: DNA Aktifleyici enzimler Üç çeşit RNA (mrna, trna, rrna) Ribozomlar
PROTEİN SENTEZİ ENZİMLER ve VİTAMİNLER Öncelikle, protein sentezinin yapılabilmesi için aşağıdakilerin mutlaka mevcut olması gerekmektedir: DNA Aktifleyici enzimler Üç çeşit RNA (mrna, trna, rrna) Ribozomlar
Prof.Dr.Gül ÖZYILMAZ
 Prof.Dr.Gül ÖZYILMAZ ENZİMLER; Tüm canlıların yapısında bulunan, Esas olarak proteinden oluşmakla beraber, organik-inorganik maddeleri de bünyesinde barındıran, Biyokimyasal tepkimeleri gerçekleştiren
Prof.Dr.Gül ÖZYILMAZ ENZİMLER; Tüm canlıların yapısında bulunan, Esas olarak proteinden oluşmakla beraber, organik-inorganik maddeleri de bünyesinde barındıran, Biyokimyasal tepkimeleri gerçekleştiren
Karbohidratlar. Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu
 Karbohidratlar Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Karbohidratlar, insan diyetinin en önemli kısmını oluştururlar Karbonhidratlar q Doğada en bol bulunan organik moleküllerdir.
Karbohidratlar Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu q Karbohidratlar, insan diyetinin en önemli kısmını oluştururlar Karbonhidratlar q Doğada en bol bulunan organik moleküllerdir.
Karbohidratlar 02.04.2012. Karbonhidratlar. Sınıflandırılması q. Sınıflandırılması. q Karbohidratlar, insan diyetinin en önemli kısmını oluştururlar
 q Karbohidratlar, insan diyetinin en önemli kısmını oluştururlar Karbohidratlar Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu Karbonhidratlar q Doğada en bol bulunan organik moleküllerdir.
q Karbohidratlar, insan diyetinin en önemli kısmını oluştururlar Karbohidratlar Yrd.Doç.Dr. Ahmet GENÇ Sağlık Hizmetleri Meslek Yüksekokulu Karbonhidratlar q Doğada en bol bulunan organik moleküllerdir.
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER
 CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
CANLILARIN YAPISINDA BULUNAN TEMEL BİLEŞENLER Canlıların yapısında bulunan moleküller yapısına göre 2 ye ayrılır: I. İnorganik Bileşikler: Bir canlı vücudunda sentezlenemeyen, dışardan hazır olarak aldığı
Karbohidratlar. Karbohidratların sınıflandırılması. Monosakkaritler
 Karbohidratlar Yeryüzünde en çok bulunan organik molekül grubudur, (CH 2 O) n genel formülüyle ifade edilebilirler. Genelde suda çözünürler, Güneş ışığının fotosentez yapan organizmalar tarafından tutulmasıyla
Karbohidratlar Yeryüzünde en çok bulunan organik molekül grubudur, (CH 2 O) n genel formülüyle ifade edilebilirler. Genelde suda çözünürler, Güneş ışığının fotosentez yapan organizmalar tarafından tutulmasıyla
ÜNİTE 7:HÜCRESEL SOLUNUM
 ÜNİTE 7:HÜCRESEL SOLUNUM Hücreler iş yapabilmek için enerjiye gereksinim duyarlar. Enerji ekosisteme güneş enerjisi yoluyla gelir ve ototrof canlılar sayesinde güneş enerjisi besinlerdeki kimyasal bağ
ÜNİTE 7:HÜCRESEL SOLUNUM Hücreler iş yapabilmek için enerjiye gereksinim duyarlar. Enerji ekosisteme güneş enerjisi yoluyla gelir ve ototrof canlılar sayesinde güneş enerjisi besinlerdeki kimyasal bağ
HÜCRE FİZYOLOJİSİ Hücrenin fiziksel yapısı. Hücre membranı proteinleri. Hücre membranı
 Hücrenin fiziksel yapısı HÜCRE FİZYOLOJİSİ Hücreyi oluşturan yapılar Hücre membranı yapısı ve özellikleri Hücre içi ve dışı bileşenler Hücre membranından madde iletimi Vücut sıvılar Ozmoz-ozmmotik basınç
Hücrenin fiziksel yapısı HÜCRE FİZYOLOJİSİ Hücreyi oluşturan yapılar Hücre membranı yapısı ve özellikleri Hücre içi ve dışı bileşenler Hücre membranından madde iletimi Vücut sıvılar Ozmoz-ozmmotik basınç
Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı
 Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı Canlılarda Enerji Dönüşümleri Canlılarda Solunum: Enerjinin Açığa Çıkışı Canlı hücrede gerçekleşen tüm metabolik olaylar enerji gerektirir. Hayvanlar
Biyoloji Canlılarda Solunum Enerjinin Açığa Çıkışı Canlılarda Enerji Dönüşümleri Canlılarda Solunum: Enerjinin Açığa Çıkışı Canlı hücrede gerçekleşen tüm metabolik olaylar enerji gerektirir. Hayvanlar
LİPOPROTEİNLER. Lipoproteinler; Lipidler plazmanın sulu yapısından dolayı sınırlı. stabilize edilmeleri gerekir. kanda lipidleri taşıyan özel
 LİPOPROTEİNLER LİPOPROTEİNLER Lipidler plazmanın sulu yapısından dolayı sınırlı olarak çözündüklerinden, taşınmaları için stabilize edilmeleri gerekir. Lipoproteinler; komplekslerdir. kanda lipidleri taşıyan
LİPOPROTEİNLER LİPOPROTEİNLER Lipidler plazmanın sulu yapısından dolayı sınırlı olarak çözündüklerinden, taşınmaları için stabilize edilmeleri gerekir. Lipoproteinler; komplekslerdir. kanda lipidleri taşıyan
Karbohidrat Metabolizması Dr. Akın Yeşilkaya
 Karbohidrat Metabolizması Dr. Akın Yeşilkaya Akdeniz Üniversitesi Tıp Fakültesi Biyokimya Anabilim Dalı Dersin İçeriği Karbohidratların önemi Karbohidratların sindirimi ve emilimi Karbohidratların metabolizması
Karbohidrat Metabolizması Dr. Akın Yeşilkaya Akdeniz Üniversitesi Tıp Fakültesi Biyokimya Anabilim Dalı Dersin İçeriği Karbohidratların önemi Karbohidratların sindirimi ve emilimi Karbohidratların metabolizması
İal-biyoloji METABOLİZMA/SOLUNUM. 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir?
 METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
METABOLİZMA/SOLUNUM 1.Metabolizma ölçümünde dikkate edilecek koşullar nelerdir? 2.Solunum evrelerinde elektron vericiler (giren madde) ve elektron alıcıları (son) yazınız Evreler Elektron vericiler Elektron
