TEBLİĞ TASLAĞI VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞI
|
|
|
- Kudret Neftçi
- 7 yıl önce
- İzleme sayısı:
Transkript
1 Türkiye İlaç ve Tıbbi Cihaz Kurumundan: TEBLİĞ TASLAĞI VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞI BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Tebliğin amacı; vücut dışında (in-vitro) kullanılan tıbbi tanı cihazlarının, temel özellikleri ile uyum içerisinde tasarımı ve imal edilmesi ile üreticilerin bu temel özellikleri karşılamalarına yardımcı olmak ve Türkiye ile birlikte Avrupa Birliği üye ülkeleri arasında yeniden gözden geçirme faaliyetlerinin tutarlılığını sağlamak için, ortak teknik özelliklerini belirlemektir. Kapsam MADDE 2 (1) Bu tebliğ; Vücut Dışında Kullanılan (İn Vitro) Tıbbî Tanı Cihazları Yönetmeliği EK-II nin (A) listesindeki cihazların ortak teknik özelliklerini kapsar. Dayanak MADDE 3 (1) Bu Tebliğ, 09/01/2007 tarih ve sayılı Resmî Gazete de yayımlanan Vücut Dışında Kullanılan (İn Vitro) Tıbbî Tanı Cihazları Yönetmeliğine dayanılarak hazırlanmıştır. Tanımlar MADDE 4 (1) Bu Tebliğde geçen; a) Analitik duyarlılık: Aranan hedef markırın kesin olarak tespit edilebildiği en düşük miktarı olan saptama limitini, b) Analitik özgüllük: Yöntemin sadece aranan hedef markırı belirleyebilme yeteneğini, c) Doğrulama analizi: analizinde reaktif bulunan bir sonucun doğrulanması için kullanılan analizi, ç) Erken HIV sero-konversiyon örnekleri: p24 antijen ve / veya HIV RNA pozitif olan, tüm antikor tarama testleri ile saptanamayan ve doğrulama analizleri ile şüpheli veya negatif sonuç veren örnekleri, d) Gerçek negatif: Hedef markır için negatif olduğu bilinen ve cihaz tarafından negatif tanımlanan örneği, e) Gerçek pozitif: Hedef markır için pozitif olduğu bilinen ve cihaz tarafından pozitif tanımlanan örneği, f) HIV sero-konversiyon örnekleri: p24 antijen ve / veya HIV RNA pozitif olan, tüm antikor tarama testleri ile saptanan ve doğrulama analizleri ile pozitif veya belirsiz sonuç veren örnekleri, g) Hızlı test: otomatik prosedür içermeyen ve hızlı sonuç vermek üzere tasarlanmış olan, tek veya az sayıda örnekte kullanılan kalitatif veya yarı kantitatif in vitro tıbbi tanı cihazları ğ)nükleik asit çoğaltma (amplifikasyon) teknikleri (NAT): Bir hedef dizisinin çoğaltılması, sinyalinin güçlendirilmesi yada hibridizasyon ile nükleik asitlerin saptanması ve/veya miktarlarının belirlenmesi için kullanılan testleri, h)tanısal duyarlılık: Hedef markır varlığında cihazın pozitif sonuç verme olasılığını, ı)tanısal özgüllük: Hedef markır yokluğunda cihazın negatif sonuç verme olasılığını, i)tutarlılık (robustness): Normal kullanım süresince güvenilirliğinin gösterilmesinin sağlayan tutarlılık, analitik bir işlemin yöntem parametrelerindeki küçük, fakat öngörülen değişkenlerden etkilenmeme kapasitesini, j) Tüm sistem hata oranı: Tüm sürecin imalatçı tarafından belirtildiği şekilde uygulandığında ortaya çıkan hata sıklığını,
2 k)virüs tiplendirme analizi: Primer enfeksiyon tanısı veya tarama için kullanılmayan, pozitif olduğu bilinen örneklerin tiplendirilmesi için yapılan analizi, l)yalancı negatif: Hedef markır için pozitif olduğu bilinen ancak cihaz tarafından negatif tanımlanan örneği, m)yalancı pozitif: Hedef markır için negatif olduğu bilinen ancak cihaz tarafından pozitif tanımlanan örneği, n)yönetmelik: Vücut Dışında Kullanılan (İn Vitro) Tıbbî Tanı Cihazları Yönetmeliğini, ifade eder. İKİNCİ BÖLÜM Yönetmeliğin EK-II/A listesindeki ürünler için ortak teknik özellikler MADDE 5 (1) İnsan örneklerinde, HIV enfeksiyonu (HIV 1 ve 2), HTLV I ve II ve Hepatit B, C, D nin markırlarının saptanması, doğrulanması ve miktar ölçümü için kullanılan reaktif ve reaktif ürünlerinin performans değerlendirmesine yönelik ortak teknik özellikler aşağıdaki genel ilkeleri sağlar. a) veya tanısal testler olarak piyasaya arz edilen virüs enfeksiyonlarını tespit etmeye yönelik cihazlar tablo 1 de öngörülmüş olan duyarlılık ve özgüllük gerekliliklerini karşılar. analizleri için ayrıca bu maddenin birinci fıkrasının (ı) bendine bakınız. b) İmalatçı tarafından, serum veya plazmadan farklı olarak idrar, tükürük vücut sıvılarını test etmek için tasarlanan cihazlar, serum veya plazma testlerinde duyarlılık ve özgüllük için belirtilen ortak teknik özellikler ile ilgili aynı gereklilikleri karşılar. Performans değerlendirmesinde, aynı bireylerden alınan örnekler, hem onaylanacak testlerde hem de serum veya plazma analizlerinde test edilir. c) İmalatçı tarafından, kişisel test cihazı olarak tasarlanan cihazlar; profesyonel kullanım amaçlı cihazlardaki duyarlılık ve özgüllük için belirtilen ortak teknik özellikler ile ilgili aynı gereklilikleri karşılar. Performans değerlendirmesinin ilgili bölümleri uygun son kullanıcılar tarafından yürütülerek veya tekrarlanarak, cihazın çalışması ve kullanma talimatları geçerli kılınır. ç) Tüm performans değerlendirmeleri, en son teknolojik yeniliklere sahip olan kullanımdaki bir cihaz ile doğrudan karşılaştırılarak yapılmalıdır. Karşılaştırma için kullanılan cihaz, performans değerlendirmesi sırasında piyasada bulunuyor ise bu cihazda CE işareti bulunmalıdır. d) Değerlendirme sırasında uyumsuz sonuçlar belirlendi ise, bu sonuçlar; 1) Uyumsuz örneğin ileri test sistemleriyle değerlendirilmesi, 2) Alternatif yöntem veya markır kullanılması, 3) Hastanın klinik durumunun ve tanısının yeniden gözden geçirilmesi, 4) Takip örneklerinin test edilmesi yöntemler uygulanarak mümkün olduğunca çözüme kavuşturulur. e) Performans değerlendirmeleri Türkiye ve/veya Avrupa popülasyonuna eşdeğer bir popülasyon üzerinde yapılmalıdır. f) Performans değerlendirmesinde kullanılan pozitif örnekler, söz konusu hastalıkların farklı evreleri, farklı antikor paternlerini, farklı genotipleri, farklı alt tipleri, mutantları vb. yansıtacak şekilde seçilir. g) Gerçek pozitifler ve sero-konversiyon örnekleri ile duyarlılık aşağıdaki şekilde değerlendirilir: 1) Sero-konversiyon sırasındaki tanısal test duyarlılığı geçerli ve güncel teknolojiye uygun olur. Onaylanmış kuruluş ya da üretici firma tarafından yapılmış olan aynı ya da ek sero-konversiyon panellerinin ileri test sonuçları, ilk performans değerlendirme verilerini doğrulamalıdır (Tablo 1 e bakınız). Sero-konversiyon panelleri, negatif kan örneği ile başlamalı ve kısa aralıklı kan örneklerini içermelidir. 2) HBsAg ve anti-hbc testleri hariç, kan taramaya yönelik cihazların CE işareti alabilmesi için tüm gerçek pozitif örnekleri doğru tanımlaması gerekir (tablo 1). HBsAg ve anti-hbc testleri için yeni cihaz en az geçerliliği gösterilmiş olan mevcut kullanımdaki cihaza eşdeğer bir performansa sahip olmalıdır. (5 inci maddenin birinci fıkrasının (ç) bendine bakınız.)
3 3) HIV testleri ile ilgili olarak; tüm HIV sero-konversiyon örnekleri pozitif olarak tanımlanmalıdır ve en az 40 erken HIV sero-konversiyon örneği test edilmelidir. Sonuçların, geçerli ve güncel teknoloji cihaz ile elde edilen sonuçlara uyumlu olması gerekir. ğ) analizlerinin performans değerlendirmesi, 25 pozitif (nadir görülen enfeksiyonlarda mevcut olması halinde) aynı güne ait taze serum ve / veya plazma örneğini içermelidir. (örnek alma işleminden itibaren en fazla bir gün) h) Performans değerlendirmesinde kullanılan negatif örnekler, testin kullanım amacına uygun kan bağışçıları, yatarak tedavi gören hastalar ve hamile kadınlar hedef popülasyonunu yansıtacak şekilde tanımlanır. ı) analizlerinin performans değerlendirmeleri için (Tablo 1), en az iki kan bağış merkezinden bağışçı popülasyonları incelenir ve ilgili popülasyonlar, ilk kez kan veren bağışçıları dışarıda bırakmayacak şekilde seçilmiş olan ardışık kan bağışlarından oluşturulur. i) Ekteki tablolarda aksi belirtilmedikçe, cihazlar, kan bağış örneklerinde en az % 99,5 oranında bir özgüllüğe sahip olmalıdır. Özgüllük, hedef markerin negatif olduğu kan bağışçılarındaki tekrarlayan reaktif (yalancı pozitif) sonuçların sıklığı kullanılarak hesaplanır. j) Cihazlar; performans değerlendirmesinin bir parçası olarak, potansiyel girişime yol açabilecek maddelerin etkisini belirlemek üzere değerlendirilir. Potansiyel girişime yol açabilecek maddeler bir ölçüde reaktifin yapısına ve analizin konfigürasyonuna bağlı olacak şekilde değerlendirilmelidir. Her bir yeni cihaz için temel gerekler kapsamında ihtiyaç duyulan risk analizinin bir parçası olarak, Potansiyel girişime yol açabilecek maddeler tanımlanmalıdır. Bu tanımlamada örneğin; 1) İlişkili enfeksiyonları temsil eden örnekler, 2) Multipar (birden fazla gebelik geçirmiş) kadınlardan veya romatoid faktörü pozitif hastalardan alınan örnekler, 3) Rekombinant antijenler için ekspresyon sisteminin bileşenlerine karşı oluşan insan antikorlarını (anti-e.coli veya anti-maya, vs.) içeren örnekler yer alabilir. k) İmalatçı tarafından serum ve plazma ile kullanılmak üzere tasarlanan cihazların performans değerlendirmesinde serum/plazma eşdeğerliğinin gösterilmesi zorunludur. Bu, 25 pozitif ve 25 negatif olmak üzere en az 50 bağışçı örneği için gösterilir. l) Plazma ile kullanılmak üzere tasarlanan cihazlar için performans değerlendirmesinde, imalatçının cihazla kullanım için belirttiği bütün antikoagulanları kullanarak cihazın performansı doğrulanmalıdır. Bu, 25 pozitif ve 25 negatif olmak üzere en az 50 bağışçı örneği için gösterilir. m) Risk analizinin bir parçası olarak, yalancı negatif sonuçlara yol açan tüm sistem hata oranı, düşük pozitif örneklerde yapılan tekrar analizlerinde belirlenir. n) Eğer Ek II Liste A da yer alan yeni bir in vitro tıbbi tanı cihazı spesifik olarak ortak teknik özellikler kapsamında yer almıyorsa, ilgili bir cihaza ait ortak teknik özellikler dikkate alınır. İlgili cihazlar aynı ya da benzer kullanım amacına sahip olma ya da benzer riskler taşıma farklı gerekçeler zemininde tanımlanabilir. (2) HIV antikor/antijen kombine testlerine ilişkin ek gereklilikler; a) Tek p24 antijeni tespitine yönelik beyan içeren, Anti HIV ve p24 antijen tespitine yönelik HIV antikor/ antijen kombine testleri, p24 antijeni için analitik duyarlılık kriteri de dahil olmak üzere Tablo 1 ve Tablo 5 e uygun olmalıdır. b) Tek p24 antijeni tespitine yönelik beyan içermeyen, Anti HIV ve p24 antijen tespitine yönelik HIV antikor/ antijen kombine testleri, p24 antijeni için analitik duyarlılık kriteri hariç Tablo 1 ve Tablo 5 e uygun olmalıdır. (3) Nükleik asit çoğaltma (amplifikasyon) teknikleri (NAT) için ek gereklilikler; a) Hedef dizi çoğaltma analizlerinde her bir test örneği için internal kontrol güncel ve geçerli teknolojik özellikleri yansıtır. Bu kontrol, mümkün olduğunca ekstraksiyon, çoğaltma/hibridizasyon ve saptama tüm süreç boyunca kullanılmalıdır. b) NAT analizleri için analitik duyarlılık veya saptama limiti % 95 pozitif eşik değeri olarak ifade edilir. Bu değer, Dünya Sağlık Örgütü standardı veya kalibre edilmiş referans örnekler uluslararası referans materyallerinin seri dilüsyonlarının test çalışmalarında % 95 pozitif sonuç verdiği durumdaki analit konsantrasyonudur.
4 c) Genotip saptaması uygun primer veya prob tasarım validasyonuyla gösterilmeli ve ayrıca belirlenmiş genotip örnekleri test edilerek geçerli kılınmalıdır. ç) Kantitatif NAT analizlerinin sonuçları, var ise uluslararası standartlara veya kalibre edilmiş referans materyallerine göre izlenebilir olmalı ve mümkünse belirli uygulama alanlarında yararlanılan uluslararası birimlerle ifade edilmelidir. d) NAT testleri sero-konversiyon döneminden önceki antikor negatif örneklerde virüs tespit etmek için kullanılabilir. İmmün komplekslerdeki bağlı virüsler serbest virüslerle karşılaştırıldığında (örneğin santrifüj basamağı sırasında) farklı davranış gösterebilirler. Bu nedenle tutarlılık çalışmalarına antikor negatif (sero-konversiyon öncesi) örneklerin dahil edilmesi önemlidir. e) Tutarlılık çalışmaları süresince, olası taşınarak bulaşmanın araştırılmasına yönelik en az 5 kez ardışık yüksek pozitif ve negatif örneklerle çalışılmalıdır. Yüksek pozitif örnekler, doğal olarak yüksek virüs titreleri olan örneklerden oluşmalıdır. f) Yalancı negatif sonuçlara yol açan tüm sistem hata oranı, düşük pozitif örnekler test edilerek belirlenmelidir. Düşük pozitif örnekler, % 95 pozitif eşik virüs konsantrasyonunun 3 misline eşdeğer bir virüs konsantrasyonunu içermelidir. g) NAT yöntemlerine ilişkin performans değerlendirme i Tablo 2 de belirtilmiştir. (4) İnsan örneklerinde sadece immünolojik analizler için HIV enfeksiyonu (HIV 1 ve 2), HTLV I ve II, Hepatit B,C,D markırlarının saptanması, doğrulanması ve miktar tayini amacıyla kullanılan reaktif ve reaktif ürünlerinin imalatçı tarafından salıverilme testleri için ortak teknik özellikler: a) İmalatçının salıverilme test i, her lotun ilgili antijenleri, epitopları ve antikorları tutarlı olarak belirlediğini garanti etmelidir. b) analizleri için, imalatçının, lot salıverilme testleri, ilgili analit için en az 100 negatif örneği içermelidir. (5) ABO kan grubu sistemi ABO1 (A), ABO2 (B), ABO3 (A, B); Rh kan grubu sistemi RH1 (D), RH2 (C), RH3 (E), RH4 (c), RH5(e); Kell kan grubu sistemi KEL1 (K) kan grubu antijenlerinin tespitine yönelik reaktif ve reaktif ürünlerinin performans değerlendirmesine ilişkin ortak teknik özellikler aşağıdaki genel ilkeleri sağlamalıdır. a)tüm performans değerlendirmeleri, en geçerli ve güncel teknolojik yeniliklere sahip olan kullanımdaki bir cihaz ile doğrudan karşılaştırılarak yapılmalıdır. Karşılaştırma için kullanılan cihaz performans değerlendirmesi sırasında piyasada bulunuyor ise bu cihazda CE işareti bulunmalıdır. b)değerlendirmenin bir bölümünde uyumsuz sonuçlar belirlendi ise, bu sonuçlar; 1)uyumsuz örneğin ileri test sistemleriyle değerlendirilmesi, 2)alternatif bir metot kullanılması, yöntemler uygulanarak mümkün olduğunca çözüme kavuşturulmalıdır. c)performans değerlendirmeleri Türkiye ve/veya Avrupa popülasyonuna eşdeğer bir popülasyon üzerinde yapılmalıdır. ç)performans değerlendirmesinde kullanılan pozitif örnekler varyant ve zayıf antijen ifadesini yansıtacak şekilde seçilmelidir. d) Cihazlar; performans değerlendirmesinin bir parçası olarak, potansiyel girişime yol açabilecek maddelerin etkisini belirlemek üzere değerlendirilir. Potansiyel girişime yol açabilecek maddeler bir ölçüde reaktifin yapısına ve analizin konfigürasyonuna bağlı olacak şekilde değerlendirilmelidir. Her bir yeni cihaz için temel gerekler kapsamında ihtiyaç duyulan risk analizinin bir bölümü olarak, hatalı sonuca yol açabilecek etkenler tanımlanmalıdır. e) Plazma ile kullanılmak üzere tasarlanan cihazlar için performans değerlendirmesi, üreticinin cihazla kullanım için belirttiği bütün antikoagulanları kullanarak cihazın performansını doğrulamalıdır. Bu, 25 pozitif ve 25 negatif olmak üzere en az 50 bağışçı örneği için gösterilir. f) ABO kan grubu sistemi AB01 (A), AB02 (B), ABO3 (A, B); Rh kan grubu sistemi RH1 (D), RH2 (C), RH3 (E), RH4 (c), RH5(e); Kell kan grubu sistemi KEL1 (K) kan grubu antijenlerinin tespit edilmesi için reaktif ve reaktif ürünlerinin performans değerlendirmesine ilişkin Tablo 9 da belirtilmiştir. (6) ABO kan grubu sistemi AB01 (A), AB02 (B), ABO3 (A, B); Rh kan grubu sistemi RH1 (D), RH2 (C), RH3 (E), RH4 (c), RH5(e); Kell kan grubu sistemi KEL1 (K)
5 kan grubu antijenlerinin tespitine yönelik reaktif ve reaktif ürünlerinin imalatçı tarafından salıverilme testleri için ortak teknik özellikleri aşağıdaki genel ilkeleri sağlamalıdır. a) İmalatçının salıverilme test i, her lotun ilgili antijenleri, epitopları ve antikorları tutarlı olarak belirlediğini garanti etmelidir. b) İmalatçı için lot salıverilme test gereklilikleri Tablo 10 da belirtilmiştir. (7) Kan taraması için Varyant Creutzfeldt Jakob hastalığı (vcjd) testlerine ilişkin ortak teknik özellikler, Tablo 11 de belirtilmiştir. ÜÇÜNCÜ BÖLÜM Çeşitli ve Son Hükümler Uyumlaştırılan AB Mevzuatı MADDE 6 (1) Bu tebliğ AB mevzuatına uyum sağlamak amacıyla; a) 2009/886/EC sayılı AB Komisyon Kararına, b) 2009/886/ECsayılı AB Komisyon Kararının tarihli Düzeltici Kararına, c) 2011/869/EU sayılı AB Komisyon Kararına, paralel olarak hazırlanmıştır. Atıf MADDE 7 (1) Daha önce diğer düzenlemelerde 07/04/2005 Tarihli ve Sayılı Resmi Gazetede yayımlanan Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliğine yapılan atıflar, bu tebliğe yapılmış sayılır. Yürürlükten Kaldırılan Tebliğ MADDE 8 (1) 07/04/2005 Tarihli ve Sayılı Resmi Gazetede yayımlanan Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği yürürlükten kaldırılmıştır. Yürürlük MADDE 9 (1) Bu tebliğ yayımlandığı tarih itibarı ile yürürlüğe girer. Yürütme MADDE 10 (1) Bu tebliğ hükümlerini Türkiye İlaç ve Tıbbi Cihaz Kurumu yürütür.
6 Tanısal duyarlılık Pozitif örnekler 400 HIV HIV-2 40 non-b alt tipi şekilde; her bir alt tip en az 3 örnek ile temsil edilmek kaydıyla mevcut tüm HIV/1 alt tipleri Tablo 1 Analizleri: anti-hiv 1 ve 2, anti-htlv I ve II, anti-hcv, HBsAg, anti-hbc Anti-HIV-1/2 Anti-HTLV-I/II Anti-HCV HBsAg Anti-HBc 300 HTLV - I 100 HTLV - II 400 (pozitif örnek) Enfeksiyonun farklı evreleri ve farklı antikor paternlerini yansıtan örnekler içerecek şekilde. Genotip 1-4: > 20 örnek (her bir genotipe ait) (genotip 4 için non-a alt tipleri de içerecek şekilde) Genotip 5: > 5 örnek Genotip 6: mevcut ise 400 (Alt-tipler de içerecek şekilde) 400 (Diğer HBVmarkırlarının değerlendirilmesini içerecek şekilde) Sero-konversiyon panelleri 20 panel 10 ek panel (Onaylanmış Kuruluş ya da üreticide) Mevcut olduğunda tanımlanacaktır 20 panel 10 ek panel (Onaylanmış Kuruluş ya da üreticide) 20 panel 10 ek panel (Onaylanmış Kuruluş ya da üreticide) Analitik duyarlılık Standartlar IU/ml (HBsAg, alt tip adw2, genotip A için İkinci Uluslararası Standart, NIBSC Kodu: 00/588) Mevcut olduğunda tanımlanacaktır Özgüllük Rastgele donörler (ilk defa bağışta bulunanları içerecek şekilde) Yatarak tedavi gören hastalar Potansiyel olarak çapraz reaksiyon veren kan örnekleri (RF+, ilgili virüsler, hamile kadınlar vs.)
7 Tablo 2 HIV1, HCV, HBV, HTLV I/II için NAT analizleri (kalitatif ve kantitatif; moleküler tiplendirme dışı) HIV1 HCV HBV HTLV I/II Kabul i NAT Kalitatif Kantitatif Kalitatif Duyarlılık Saptama limiti Analitik duyarlılığın saptanması (IU/ml; WHO standartları ya da kalibre referans materyallerine göre tanımlanmış) Genotip / alt tip saptanması / sayısal ölçüm verimliliği EP validasyon rehberine göre 1 : sınır konsantrasyon değeri içinde birkaç dilüsyon serisi; en az 24 tekrar örneğinde istatistiksel analiz (örn. Probit analizi); %95 eşik değerinin hesaplanması. Her alt tip için en az 10 örnek (mümkün olduğunca) Saptama limiti: Kalitatif testlerdeki ; Sayısal ölçüm limiti: kalibre referans materyallerinin (yarım log 10 ya da altı) dilüsyonları, alt, üst sayısal ölçüm limitlerinin tanımlanması, kesinlik, doğruluk, lineer ölçüm aralığı, dinamik aralık. Farklı konsantrasyonlarda tekrarlanabilirliğin gösterilmesi. Tüm ilgili genotip / alt tiplere ait dilüsyon serileri, terci- hen, mümkün oldu-ğunca referans materyalleri EP validasyon rehberine göre 1 : sınır konsantrasyon değeri içinde birkaç dilüsyon serisi; en az 24 tekrar örneğinde istatistiksel analiz (örn. Probit analizi); %95 eşik değerinin hesaplanması. Her alt tip için en az 10 örnek (mümkün olduğunca) Kantitatif HIV kantitatifteki Kalitatif EP validasyon rehberine göre 1 : sınır konsantrasyon değeri içinde birkaç dilüsyon serisi; en az 24 tekrar örneğinde istatistiksel analiz (örn. Probit analizi); %95 eşik değerinin hesaplanması. Mümkün olduğunca kalibre genotip referans materyalleri Kantitatif Kalitatif Kantitatif HIV kantitatifteki EP validasyon rehberine göre 1 :sınır konsantrasyon değeri içinde birkaç dilüsyon serisi; en az 24 tekrar örneğinde istatistiksel analiz (örn. Probit analizi); %95 eşik değerinin hesaplanması. Mümkün olduğunca kalibre genotip referans materyalleri HIV kantitatifteki 1 Avrupa Farmakopi Rehberi Notlar: Yalancı negatif sonuçlara yol açan tüm sistem hata oranı kabul kriteri, 99/100 analizin pozitif olmasıdır. Kantitatif NAT lar için, kullanıcıların rutin durumlarını yansıtacak şekilde (örn.örnekler önceden seçilmemeli) en az 100 örnek üzerinde çalışma yapılmalıdır. Başka bir NAT sistemi ile karşılaştırmalı sonuçlar paralellik oluşturmalıdır. Kalitatif NAT lar için, tanısal duyarlılık çalışması en az 10 sero konversiyon paneli kullanılarak yapılmalıdır. Başka bir NAT sistemi ile karşılaştırmalı sonuçlar paralellik oluşturmalıdır.
8 HIV1 HCV HBV HTLV I/II Kabul i Kantitatif Kantitatif Kantitatif NAT Kalitatif Kantitatif Kalitatif Tanısal özgüllük için negatif örnekler Potansiyel çapraz reaktif markırlar Tutarlılık Hücre kültürü süpernatanları (nadir HIV-1 alt tiplerinin yerine geçebilir) EP validasyon rehberine göre 2 : mümkün olduğunca kalibre genotip referans materyalleri; in vitro transkriptler de bir seçenek olabilir. Uygun yöntemlerle sayısal olarak belirlenmiş transkriptler ya da plazmidler kullanılabilir. EP validasyon rehberine göre 2 : mümkün olduğunca kalibre genotip referans materyalleri; in vitro transkriptler de bir seçenek olabilir. HIV kantitatifteki Kalitatif EP validasyon rehberine göre 2 : mümkün olduğunca kalibre genotip referans materyalleri; in vitro transkriptler de bir seçenek olabilir. HIV kantitatifteki Kalitatif EP validasyon rehberine göre 2 : mümkün olduğunca kalibre genotip referans materyalleri; in vitro transkriptler de bir seçenek olabilir. 500 kan donörü 100 kan donörü 500 kan donörü 500 kan donörü 500 bireysel kan bağışı Uygun analiz tasarım kanıtı (örn. sekans karşılaştırması) ve / veya en az 10 insan retrovirüs (örn. HTLV) - pozitif örneğin test edilmesiyle Kalitatif testlerdeki Kalitatif testlerdeki Analizlerin tasarımı ve / veya en az 10 insan flavivirüs (örn. HGV, YFV) - pozitif örneğin test edilmesiyle Analizlerin tasarımı ve / veya en az 10 diğer DNA virüs pozitif örneklerin test edilmesiyle Analizlerin tasarımı ve / veya en az 10 insan retrovirüs (örn. HIV-) pozitif örneğin test edilmesiyle HIV kantitatifteki
9 HIV1 HCV HBV HTLV I/II Kabul i Kantitatif Kantitatif Kantitatif NAT Kalitatif Kantitatif Kalitatif Çaprazkontamin-asyon Inhibisyon Yalancı negatif sonuçlara yol açan tüm sistem hata oranı Yüksek pozitif (doğal olarak var olduğu bilinen) ve negatif örneklerin ardışık test edildiği en az 5 çalışma Tercihen tüm NAT prosedürü süresince çalışılan internal kontrol 3 x % 95 pozitif eşik değer konsantrasyonunda virüs içeren en az 100 örnek Yüksek pozitif (doğal olarak var olduğu bilinen) ve negatif örneklerin ardışık test edildiği en az 5 çalışma Tercihen tüm NAT prosedürü süresince çalışılan internal kontrol 3 x % 95 pozitif eşik değer konsantrasyonunda virüs içeren en az 100 örnek HIV kantitatifteki Kalitatif Yüksek pozitif (doğal olarak var olduğu bilinen) ve negatif örneklerin ardışık test edildiği en az 5 çalışma Tercihen tüm NAT prosedürü süresince çalışılan internal kontrol 3 x % 95 pozitif eşik değer konsantrasyonunda virüs içeren en az 100 örnek HIV kantitatifteki Kalitatif Yüksek pozitif (doğal olarak var olduğu bilinen) ve negatif örneklerin ardışık test edildiği en az 5 çalışma Tercihen tüm NAT prosedürü süresince çalışılan internal kontrol 3 x % 95 pozitif eşik değer konsantrasyonunda virüs içeren en az 100 örnek HIV kantitatifteki 99/100 pozitif analiz
10 Tanısal duyarlılık Pozitif örnekler Sero konversiyon panelleri Tablo 3 Hızlı Testler: anti-hiv 1 ve 2, anti-hcv, HBsAg, anti-hbc, anti-htlv I ve II Anti-HIV ½ Anti-HCV HBsAg Anti-HBc Anti HTLV I/II Kabul i Tanısal özgüllük Negatif örnekler 1000 kan bağışı 1000 kan bağışı 1000 kan bağışı 1000 kan bağışı 1000 kan bağışı % 99 (anti-hbc: 200 klinik örnek 200 klinik örnek 200 klinik örnek 200 klinik örnek 200 klinik örnek % 96) Gebe kadınlardan alınan 200 örnek Potansiyel girişime yol açabilecek 100 örnek Gebe kadınlardan alınan 200 örnek Potansiyel girişime yol açabilecek 100 örnek Gebe kadınlardan alınan 200 örnek Potansiyel girişime yol açabilecek 100 örnek Potansiyel girişime yol açabilecek 100 örnek Gebe kadınlardan alınan 200 örnek Potansiyel girişime yol açabilecek 100 örnek
11 Tanısal duyarlılık Analitik duyarlılık Tanısal özgüllük Tablo 4 Anti-HIV 1 ve 2, anti-htlv I ve II, anti-hcv ve HBsAg için doğrulama analizleri / ek analizler Anti-HIV doğrulama analizi Pozitif örnekler 200 HIV-1 ve 100 HIV - 2 Sero-konversiyon panelleri Standartlar Enfeksiyonun farklı evreleri ve farklı antikor paternlerini yansıtan örnekleri içerecek şekilde 15 sero-konversiyon paneli / düşük titreli paneller Anti-HTLV doğrulama analizi 200 HTLV- I ve 100 HTLV- II HCV ek analizler HBsAg doğrulama analizi Kabul i 300 HCV (pozitif örnekler) 300 HBsAg Pozitif (ya da belirsiz) olarak doğru tanımlama, negatif olmaması Enfeksiyonun farklı evreleri ve farklı antikor paternlerini yansıtan örnekleri içerecek şekilde Genotip 1-4: > 20 örnek (her bir genotipe ait) (genotip 4 için non-a alt tipleri de dahil) Genotip 5: > 5 örnek Genotip 6: mevcut ise 15 sero-konversiyon paneli / düşük titreli paneller Enfeksiyonun farklı evrelerinden örnekleri içerecek şekilde 20 yüksek pozitif örnek (> 26 IU/ml); eşik değeri aralığında 20 örnek 15 sero-konversiyon paneli / düşük titreli paneller HBsAg, alt tip adw2, genotip A için İkinci Uluslararası Standart, NIBSC Kodu: 00/588 Negatif örnekler 200 kan bağışı 200 kan bağışı 200 kan bağışı Mümkünse tarama analizlerinin performans değerlendirmesinden 10 yalancı pozitif örnek 2 Gebe kadınları da içeren 200 klinik örnek Gebe kadınları da içeren 200 klinik örnek Gebe kadınları da içeren 200 klinik örnek Yalancı pozitif sonuç olmaması / 2 nötralizasyon olmaması Diğer doğrulama analizlerinde sonuçları belirsiz çıkan örnekleri içerecek şekilde potansiyel girişime yol açabilecek 50 örnek Diğer doğrulama analizlerinde sonuçları belirsiz çıkan örnekleri içerecek şekilde potansiyel girişime yol açabilecek 50 örnek Diğer doğrulama analizlerinde sonuçları belirsiz çıkan örnekleri içerecek şekilde potansiyel girişime yol açabilecek 50 örnek Potansiyel girişime yol açabilecek 50 örnek 2 Kabul kriteri HBsAg doğrulama analizi için nötralizasyon olmaması.
12 Tanısal duyarlılık Pozitif örnekler 50 HIV-1 Ag-pozitif örnek Tablo 5 HIV 1 antijen HIV-1 antijen analizleri Değişik HIV-1 alt tipleri ve HIV-2 dahil 50 hücre kültürü süpernatanı Sero-konversiyon panelleri 20 sero-konversiyon paneli / düşük titreli paneller Analitik duyarlılık Standartlar HIV-1 p24 Antijeni, Birinci Uluslararası Referans reaktifi, NIBSC kodu: 90/636 2 IU/ml Tanısal özgüllük 200 kan bağışı 200 klinik örnek Potansiyel girişime yol açabilecek 50 örnek Kabul i Doğru tanımlama (nötralizasyondan sonra) Nötralizasyondan sonra % 99.5 Tablo 6 Serotipleme ve genotipleme analizleri: HCV HCV serotipleme ve genotipleme testleri Tanısal duyarlılık Pozitif örnekler 200 (pozitif örnek) Enfeksiyonun farklı evreleri ve farklı antikor paternlerini yansıtan örnekler içerecek şekilde. Genotip 1-4: > 20 örnek (her bir genotipe ait) (genotip 4 için non-a alt tipleri de içerecek şekilde) Genotip 5: > 5 örnek Genotip 6: mevcut ise Kabul i Serotipleme ve genotipleme arasında % 95 uyum Genotipleme ve sekanslama arasında > % 95 uyum Tanısal özgüllük Negatif örnekler 100
13 Tanısal duyarlılık Pozitif örnekler 100 aşılanmış 100 doğal enfekte kişi Tablo 7 HBV markırları: anti-hbs, anti HBc IgM, anti-hbe, HBeAg Anti-HBs Anti-HBc IgM Anti-HBe HBcAg Kabul i 200 Enfeksiyonun değişik evrelerinden (akut / kronik vb) örnekler dahil 200 Enfeksiyonun değişik evrelerinden (akut / kronik vb) örnekler dahil 200 Enfeksiyonun değişik evrelerinden (akut / kronik vb) örnekler dahil % 98 Sero-konversiyon panelleri 10 takip ya da anti-hbs sero-konversiyonu Analitik duyarlılık Standartlar WHO Birinci Uluslararası Referans Materyali 1977; NIBSC, İngiltere Tanısal özgüllük Negatif örnekler 500 Kabul i sadece akut enfeksiyon evrelerinden örneklere uygulanmalıdır. Mevcut olduğunda 200 kan bağışı 200 kan bağışı HBe Referenzantigen 82: PEI Almanya 200 kan bağışı Anti HBs: < 10 miu/ml % 98 Klinik örnek içerecek şekilde Potansiyel girişime yol açabilecek 50 örnek 200 klinik örnek Potansiyel girişime yol açabilecek 50 örnek 200 klinik örnek Potansiyel girişime yol açabilecek 50 örnek 200 klinik örnek Potansiyel girişime yol açabilecek 50 örnek
14 Tanısal duyarlılık Pozitif örnekler Tablo 8 HDV markırları: anti-hdv, anti-hdv IgM, delta antijen Anti-HDV Anti-HDV IgM Delta antijen Kabul i 100 HBV markırları tanımlanmış örnek 50 HBV markırları tanımlanmış örnek 10 HBV markırları tanımlanmış örnek % 98 Tanısal özgüllük Negatif örnekler 200 Klinik örnekler içerecek şekilde 200 Klinik örnekler içerecek şekilde 200 Klinik örnekler içerecek şekilde % potansiyel girişime yol açabilecek örnek 50 potansiyel girişime yol açabilecek örnek 50 potansiyel girişime yol açabilecek örnek
15 Özgüllük Tablo 9 ABO, Rh ve Kell kan grubu sistemlerinde kan grubu antijenleri Önerilen metot başına test sayısı Piyasaya ilk kez çıkacak bir ürün için test edilmesi gereken toplam örnek sayısı Yeni bir formülasyon ya da iyi tanımlanmış reaktiflerin kullanımı için test edilmesi gereken toplam örnek sayısı Anti-ABO1 (anti-a), anti-abo2 (anti-b), anti ABO3 (anti-a, B) Anti-RH1 (anti-d) Anti-RH2 (anti-c), anti-rh4 (anti-c), anti-rh (anti-e) Anti-RH5 (anti-e) Anti-KEL1 (anti-k) Kabul i: Yukarıdaki reaktiflerin tamamı, cihazın iddia edilen reaktivitesine göre kabul edilebilir bir performansla geçerliliği gösterilmiş olan reaktiflerle karşılaştırılabilir analiz sonuçları göstermelidir. Geçerliliği gösterilmiş olan reaktifler için, uygulamanın ya da kullanımın değiştirildiği ya da genişletildiği durumlarda, yukarıda 1. kolonda verilmiş olan şartlar uyarınca daha ileri testler yapılmalıdır. Anti-D reaktiflerinin performans değerlendirmesi, ürünün amaçlanan kullanımına göre, zayıf RH1 (D) ve parsiyel RH1 (D) örnek yelpazesi ile yapılacak testleri içerir. Nitelikler: Klinik örnekler: Neonatal örnekler: ABO örnekleri: zayıf D : test popülasyonunun %10 u > %2 test popülasyonu > %40 A, B pozitifler > %2 RH1(D)pozitifler
16 Tablo 10 ABO, Rh ve Kell grup sistemlerindeki kan grubu antijenlerinin belirlenmesine yönelik reaktif ve reaktif ürünleri için lot salıverilme i 1. Test reaktifleri Kan grubu reaktifleri Her bir reaktif için özgüllük test şartları Test edilecek minimum kontrol hücresi sayısı Pozitif reaksiyonlar Negatif reaksiyonlar A1 A2B Ax B 0 Anti-ABO1 (anti-a) ( ) 2 2 B A1B A1 0 Anti-ABO2 (anti-b) A1 A2 Ax B 0 Anti-ABO3 (anti-a, B) R1r R2r Zayıf D r r r r rr Anti-RH1 (anti-d) ( ) R1R2 R1r r r R2R2 r r rr Anti-RH2 (anti-c) R1R2 R1r r r R1R1 Anti-RH4 (anti-c) R1R2 R2r r r R1R1 r r rr Anti-RH 3 (anti-e) R1R2 R2r r r R2R2 Anti-RH5 (anti-e) Kk kk Anti-KEL1 (anti-k) 4 3 Yalnızca bu antijenlere karşı reaktivitenin iddia edildiği durumlarda önerilen teknikler ile. Not: Poliklonal reaktifler, özgüllüğü doğrulamak ve istenmeyen kontaminant antikorların varlığını ekarte etmek için daha geniş bir hücre paneline karşı mutlaka test edilmelidir.
17 Kabul i: Her bir reaktif lotu, önerilen bütün teknikler ile performans değerlendirme verilerinden edinilen sonuçlara uygun olarak, net şekilde pozitif veya negatif sonuçları göstermek zorundadır 2. Kontrol materyalleri (eritrositler) Yukarıdaki listede yer alan ve kan gruplama reaktiflerinin kontrolünde kullanılan eritrositlerin fenotipi, geçerliliği gösterilmiş bir cihaz kullanılarak doğrulanmalıdır.
18 Tablo 11 Kan taraması için Varyant Creutzfeldt Jakob hastalığı (vcjd) testleri Analitik duyarlılık Materyal Örnek sayısı Kabul i vcjd li beyin ile yoğunlaştırılmış insan plazması (WHO referans numarası NHBY0/0003) NHBYO/0003 Sayılı WHO materyalinin üç dilüsyonunun her birinden 24 tekrar örneği (1 x 10 4, 1 x 10 5, 1 x 10 6 ) 1 x 10 4 de saptanan 24 tekrar örneğinin 23 ü vcjd li dalak ile yoğunlaştırılmış insan plazması (%10 dalak homojenatı-nibsc referans numarası NHSY0/0009) NHBYO/0009 Sayılı NIBSC materyalinin üç dilüsyonunun her birinden 24 tekrar örneği (1 x 10, 1 x 10 2, 1 x 10 3 ) Tanısal duyarlılık A) Uygun hayvan modellerinden örnek En az 10 örnek olması kaydı ile mümkün olduğunca en fazla sayıda örnek B) Bilinen klinik vcjd li insanlardan En az 10 örnek olması kaydı ile mümkün alınan örnek olduğunca en fazla sayıda örnek Sadece 10 örneğin mevcut olmadığı durumlarda: - Test edilen örnek sayısı, 6-9 arasında olacaktır - Mevcut tüm örnekler test edilecektir 1 x 10 da saptanan 24 tekrar örneğinin 23 ü % 90 % 90 En fazla bir yalancı negatif sonuç Analitik özgüllük Tanısal özgüllük Potansiyel olarak çapraz reaksiyon gösteren kan örnekleri Bovin spongiform ensefalopati (BSE) ile karşılaşmanın az olduğu bölgelerden normal insan plazma örnekleri En az % 99.5
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.
 Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.Sayı: 25779 Amaç Madde 1 Bu Tebliğin amacı; vücut dışında (in-vitro) kullanılan
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.Sayı: 25779 Amaç Madde 1 Bu Tebliğin amacı; vücut dışında (in-vitro) kullanılan
I. Analitik duyarlılık ve özgüllük II. Klinik duyarlılık ve özgüllük III. Kesinlik tekrarlanabilirlik IV. Doğruluk V. Doğrusallık (lineerite)
 SORU 1 IVD/CE belgesi olan kantitatif HBV DNA PCR testi satın alma aşamasında yöntem doğrulama (verifikasyon) yapmak istiyorsunuz. Hangi parametreleri mutlaka kontrol etmek isterseniz? I. Analitik duyarlılık
SORU 1 IVD/CE belgesi olan kantitatif HBV DNA PCR testi satın alma aşamasında yöntem doğrulama (verifikasyon) yapmak istiyorsunuz. Hangi parametreleri mutlaka kontrol etmek isterseniz? I. Analitik duyarlılık
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER)
 VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
VERİFİKASYON. Dr. Tijen ÖZACAR. Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR
 VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
TLERDE SEROLOJİK/MOLEK HANGİ İNCELEME?) SAPTANMASI
 * VİRAL V HEPATİTLERDE TLERDE SEROLOJİK/MOLEK K/MOLEKÜLER LER TESTLER (NE ZAMANHANG HANGİ İNCELEME?) *VİRAL HEPATİTLERDE TLERDE İLAÇ DİRENCİNİN SAPTANMASI *DİAL ALİZ Z HASTALARININ HEPATİT T AÇISINDAN
* VİRAL V HEPATİTLERDE TLERDE SEROLOJİK/MOLEK K/MOLEKÜLER LER TESTLER (NE ZAMANHANG HANGİ İNCELEME?) *VİRAL HEPATİTLERDE TLERDE İLAÇ DİRENCİNİN SAPTANMASI *DİAL ALİZ Z HASTALARININ HEPATİT T AÇISINDAN
NAT Yöntem onayı. Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD
 NAT Yöntem onayı Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Yöntem onayı (minimum) Doğruluk Ticari test (Verifikasyon) Tekrarlanabilirlik (intra-,inter-assay) Doğrusallık
NAT Yöntem onayı Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Yöntem onayı (minimum) Doğruluk Ticari test (Verifikasyon) Tekrarlanabilirlik (intra-,inter-assay) Doğrusallık
TRANSFÜZYON MERKEZİ HASTALARDA KULLANILAN MİKROBİYOLOJİK TARAMA TESTLERİ TALİMATI
 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM : Bu talimat transfüzyon merkezinde
1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM : Bu talimat transfüzyon merkezinde
Kan Hizmetleri Genel Müdürlüğü
 Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 05 Kasım Nepton, Serkan www.kanver.org www.kizilay.org.tr GÜVENLİ KAN BAĞIŞÇISINA ULAŞIMDA NAT TARAMA TESTİ UYGULAMALARI Uzm. Dr.
Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 05 Kasım Nepton, Serkan www.kanver.org www.kizilay.org.tr GÜVENLİ KAN BAĞIŞÇISINA ULAŞIMDA NAT TARAMA TESTİ UYGULAMALARI Uzm. Dr.
IV. KLİMUD Kongresi, Kasım 2017, Antalya
 IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 HCV Tanısında Cut off/ Sinyal (S/CO)/TV) Değerlerinin Tanısal Geçerliliklerinin Değerlendirilmesi TÜLİN DEMİR¹, DİLARA YILDIRAN¹, SELÇUK KILIǹ, SELÇUK
IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 HCV Tanısında Cut off/ Sinyal (S/CO)/TV) Değerlerinin Tanısal Geçerliliklerinin Değerlendirilmesi TÜLİN DEMİR¹, DİLARA YILDIRAN¹, SELÇUK KILIǹ, SELÇUK
Moleküler Testlerde Yöntem Geçerliliğinin Sınanması. Dr. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD
 Moleküler Testlerde Yöntem Geçerliliğinin Sınanması Dr. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD 8. Ulusal Moleküler ve Tanısal Mikrobiyoloji Kongresi 2014 Laboratuvarda
Moleküler Testlerde Yöntem Geçerliliğinin Sınanması Dr. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD 8. Ulusal Moleküler ve Tanısal Mikrobiyoloji Kongresi 2014 Laboratuvarda
MİKROBİYOLOJİK TARAMA TEST ÇALIŞILMA ESASLARI VE BAĞIŞÇI POZİTİFLİĞİNE YAKLAŞIM
 TRF.PR.05 11.04.2012 01.02.2016 01 1/5 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM
TRF.PR.05 11.04.2012 01.02.2016 01 1/5 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM
VİRAL ENFEKSİYONLARDA ALGORİTMALAR
 VİRAL ENFEKSİYONLARDA ALGORİTMALAR PANEL: TRANSFÜZYON VE VİRAL ENFEKSİYONLAR Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu,XII 3-7 Kasım 2009 Uzm.Dr.A.Esra KARAKOÇ S.B.Ankara EAH, Tıbbi Mikrobiyoloji
VİRAL ENFEKSİYONLARDA ALGORİTMALAR PANEL: TRANSFÜZYON VE VİRAL ENFEKSİYONLAR Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu,XII 3-7 Kasım 2009 Uzm.Dr.A.Esra KARAKOÇ S.B.Ankara EAH, Tıbbi Mikrobiyoloji
Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri. Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya
 Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya Dünyada 130-170 milyon kişi hepatit C virüsü (HCV) ile infekte Her yıl 3-4 milyon
Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya Dünyada 130-170 milyon kişi hepatit C virüsü (HCV) ile infekte Her yıl 3-4 milyon
Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları
 HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HPV Moleküler Tanısında Güncel Durum. DNA bazlı Testler KORAY ERGÜNAY 1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ
 1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ HPV Moleküler Tanısında Güncel Durum DNA bazlı Testler KORAY ERGÜNAY Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Viroloji Ünitesi HPV tanısı... Sitolojik/Patolojik
1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ HPV Moleküler Tanısında Güncel Durum DNA bazlı Testler KORAY ERGÜNAY Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Viroloji Ünitesi HPV tanısı... Sitolojik/Patolojik
Yöntem ve Test Seçimine Yaklaşım. Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR
 Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
TANIMLAR. Dr. Neriman AYDIN. Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 TANIMLAR Dr. Neriman AYDIN Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı In-vitro tanı Sürekli doğru sonuç Amaca uygun Zamanında Uygun maliyet In-vitro tanı elemanları Kitler
TANIMLAR Dr. Neriman AYDIN Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı In-vitro tanı Sürekli doğru sonuç Amaca uygun Zamanında Uygun maliyet In-vitro tanı elemanları Kitler
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı:
 Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması. Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Testler farklı amaçlarla uygulanabilir: - Tanı, tarama, doğrulama,
Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Testler farklı amaçlarla uygulanabilir: - Tanı, tarama, doğrulama,
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ
 VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
BOS, idrar, doku, diğer doku ve sıvılarda (DDS) Kalitatif testler (pozitif / negatif sonuç) Kantitatif testler (miktar belirten; viral yük)
 Klinik Viroloji Laboratuvarı testleri: 1. Serolojik testler: Serum veya plazmada antijen ve/veya antikor araştırılması 2. Serum dışı örneklerde (BOS, sürüntü örnekleri, idrar, doku, diğer sıvı örnekleri;
Klinik Viroloji Laboratuvarı testleri: 1. Serolojik testler: Serum veya plazmada antijen ve/veya antikor araştırılması 2. Serum dışı örneklerde (BOS, sürüntü örnekleri, idrar, doku, diğer sıvı örnekleri;
Kan Bankacılığında tarama testlerin tarama
 Kan Bankacılığında tarama testlerinde güncel durum Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Temel tarama testleri İmmunoassay temelli testler Enzim immunoassay
Kan Bankacılığında tarama testlerinde güncel durum Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Temel tarama testleri İmmunoassay temelli testler Enzim immunoassay
Viral Hepatitler. Hepatit A Virus. Viral Hepatitler- Tarihsel Bakış. Hepatit Tipleri. Hepatit A Klinik Özellikler
 Viral Hepatitler- Tarihsel Bakış Viral Hepatitler İnfeksiyöz Viral hepatitler A NANB E Enterik yolla geçen Dr. Ömer Şentürk Serum B D C F, G, TTV,? diğerleri Parenteral yolla geçen Hepatit Tipleri A B
Viral Hepatitler- Tarihsel Bakış Viral Hepatitler İnfeksiyöz Viral hepatitler A NANB E Enterik yolla geçen Dr. Ömer Şentürk Serum B D C F, G, TTV,? diğerleri Parenteral yolla geçen Hepatit Tipleri A B
WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır.
 WEİL FELİX TESTİ WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır. Riketsiyöz tanısında çapraz reaksiyondan faydalanılır bu nedenle riketsiyaların çapraz reaksiyon
WEİL FELİX TESTİ WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır. Riketsiyöz tanısında çapraz reaksiyondan faydalanılır bu nedenle riketsiyaların çapraz reaksiyon
TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV
 TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV Doç. Dr. Mustafa GÜL Kahramanmaraş Sütçü İmam Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Sunum Planı Transfüzyonla
TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV Doç. Dr. Mustafa GÜL Kahramanmaraş Sütçü İmam Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Sunum Planı Transfüzyonla
VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞINA İLİŞKİN UYUM TABLOSU
 AVRUPA BİRLİĞİ MEVZUATINA UYUM TABLOSU VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞINA İLİŞKİN UYUM TABLOSU Commission Decision 2009/886/EC of 27 November 2009
AVRUPA BİRLİĞİ MEVZUATINA UYUM TABLOSU VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞINA İLİŞKİN UYUM TABLOSU Commission Decision 2009/886/EC of 27 November 2009
VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI
 KLİMUD BÖLGE TOPLANTILARI VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI KLİMUD Klinik Viroloji Çalışma Grubu A B Fekal-oral bulaşma Kronikleşmez E Parenteral bulaşma Kronikleşir C D HBV - Olgu 56 yaşında olgunun
KLİMUD BÖLGE TOPLANTILARI VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI KLİMUD Klinik Viroloji Çalışma Grubu A B Fekal-oral bulaşma Kronikleşmez E Parenteral bulaşma Kronikleşir C D HBV - Olgu 56 yaşında olgunun
Prediktör Testler ve Sıradışı Serolojik Profiller. Dr. Dilara İnan Isparta
 Prediktör Testler ve Sıradışı Serolojik Profiller Dr. Dilara İnan 04.06.2016 Isparta Hepatit B yüzey antijeni (HBsAg) HBV yüzeyinde bulunan bir proteindir; RIA veya EIA ile saptanır Akut ve kronik HBV
Prediktör Testler ve Sıradışı Serolojik Profiller Dr. Dilara İnan 04.06.2016 Isparta Hepatit B yüzey antijeni (HBsAg) HBV yüzeyinde bulunan bir proteindir; RIA veya EIA ile saptanır Akut ve kronik HBV
P z o itif Nega g ti a f
 Platelia Aspergillus Ag, serum örneklerinde aspergillus galaktomannan antijenini saptayan bir enzyme immun assay testidir. Test invaziv aspergillozis tanısında kullanılmaktadır. Kit prospektüsünde kalibratör
Platelia Aspergillus Ag, serum örneklerinde aspergillus galaktomannan antijenini saptayan bir enzyme immun assay testidir. Test invaziv aspergillozis tanısında kullanılmaktadır. Kit prospektüsünde kalibratör
Akut ve Kronik Hepatit Tanısında Serolojik ve Moleküler Yöntemler Atipik Profiller
 Akut ve Kronik Hepatit Tanısında Serolojik ve Moleküler Yöntemler Atipik Profiller Dr Güle Çınar Ankara Üniversitesi Tıp Fakültesi Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları ABD Etkenler HAV HBV HCV
Akut ve Kronik Hepatit Tanısında Serolojik ve Moleküler Yöntemler Atipik Profiller Dr Güle Çınar Ankara Üniversitesi Tıp Fakültesi Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları ABD Etkenler HAV HBV HCV
ANALİTİK YÖNTEMLERİN DEĞERLENDİRİLMESİ. Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004
 ANALİTİK YÖNTEMLERİN DEĞERLENDİRİLMESİ Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Laboratuvarlarda yararlanılan analiz yöntemleri performans kalitelerine göre üç sınıfta toplanabilir: -Kesin yöntemler
ANALİTİK YÖNTEMLERİN DEĞERLENDİRİLMESİ Doç.Dr. Mustafa ALTINIŞIK ADÜTF Biyokimya AD 2004 1 Laboratuvarlarda yararlanılan analiz yöntemleri performans kalitelerine göre üç sınıfta toplanabilir: -Kesin yöntemler
Mikrobiyolojide Moleküler Tanı Yöntemleri. Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D
 Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
artus BK Virus QS-RGQ Kit
 artus BK Virus QS-RGQ Kit Performans Özellikleri artus BK Virus QS-RGQ Kit, Versiyon 1, 4514363 Testi gerçekleştirmeden önce www.qiagen.com/products/artusbkvirusrgpcrkit.aspx adresinde yeni elektronik
artus BK Virus QS-RGQ Kit Performans Özellikleri artus BK Virus QS-RGQ Kit, Versiyon 1, 4514363 Testi gerçekleştirmeden önce www.qiagen.com/products/artusbkvirusrgpcrkit.aspx adresinde yeni elektronik
HIV TANISINDA YENİLİKLER
 HIV/AIDS KURSU HIV TANISINDA YENİLİKLER Dr. Mert Ahmet KUŞKUCU İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Dünya Sağlık Örgütü Verileri (2016) YILLARA GÖRE HIV (+) SAPTANAN VAKA SAYISI
HIV/AIDS KURSU HIV TANISINDA YENİLİKLER Dr. Mert Ahmet KUŞKUCU İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Dünya Sağlık Örgütü Verileri (2016) YILLARA GÖRE HIV (+) SAPTANAN VAKA SAYISI
21 gün. 21 gün. 21 gün. Tüm programlar için kullanılabilir. Tüm programlar için kullanılabilir. Tüm programlar için kullanılabilir.
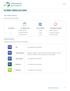 2014 Yükleme Takvimi Yükleme takvimi aşağıdaki gibidir: Test Yükleme Test Yükleme Açılış Pencere Dönemi Sonuç Bildirim Son Günü 1 26 Mart, Çarşamba 16 Nisan, Çarşamba 2 25 Haziran, Çarşamba 16 Temmuz,
2014 Yükleme Takvimi Yükleme takvimi aşağıdaki gibidir: Test Yükleme Test Yükleme Açılış Pencere Dönemi Sonuç Bildirim Son Günü 1 26 Mart, Çarşamba 16 Nisan, Çarşamba 2 25 Haziran, Çarşamba 16 Temmuz,
IV. KLİMUD Kongresi, Kasım 2017, Antalya
 IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 4. Kuşak HIV ELISA Sinyal/cut-off Değerleri ile Hatalı Pozitiflik İlişkisinin Değerlendirilmesi Tülin Demir 1, Süleyman Yalçın 1, Selçuk Kılıç2 1 Sağlık
IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 4. Kuşak HIV ELISA Sinyal/cut-off Değerleri ile Hatalı Pozitiflik İlişkisinin Değerlendirilmesi Tülin Demir 1, Süleyman Yalçın 1, Selçuk Kılıç2 1 Sağlık
İÜ ONKOLOJİ ENSTİTÜSÜ KALİTE KONTROL ve TEST KALİBRASYON PROSEDÜRÜ
 Sayfa No : 1 / 6 1. Amaç Tıbbi Biyokimya Laboratuvarında rastgele ve sistematik hataları önlemek, doğru ve güvenilir test sonuçları elde etmek için iç ve dış kalite kontrol yöntemleri, bakım-kalibrasyonu
Sayfa No : 1 / 6 1. Amaç Tıbbi Biyokimya Laboratuvarında rastgele ve sistematik hataları önlemek, doğru ve güvenilir test sonuçları elde etmek için iç ve dış kalite kontrol yöntemleri, bakım-kalibrasyonu
VİRAL HEPATİTLER 5. Sınıf Entegre Ders. Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU
 VİRAL HEPATİTLER 5. Sınıf Entegre Ders Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU Kronik Viral Hepatitler Sporadik Enfeksiyon ENDER HBV HCV HDV Ulusal Aşılama Programı Erişkinlerin Sorunu HFV, HGV,
VİRAL HEPATİTLER 5. Sınıf Entegre Ders Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU Kronik Viral Hepatitler Sporadik Enfeksiyon ENDER HBV HCV HDV Ulusal Aşılama Programı Erişkinlerin Sorunu HFV, HGV,
Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı
 Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı Deniz Gökengin Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Cinsel yolla bulaşan enfeksiyonlar Gonore Klamidyal
Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı Deniz Gökengin Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Cinsel yolla bulaşan enfeksiyonlar Gonore Klamidyal
Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay. Dr. Dilek Çolak
 Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay Dr. Dilek Çolak İmmün Yanıt C. Macrophage A. Pathogen B. B cells D. Macrophage E. Macrophage F. T cell G. B cell H. Memory B cells I. Plasma
Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay Dr. Dilek Çolak İmmün Yanıt C. Macrophage A. Pathogen B. B cells D. Macrophage E. Macrophage F. T cell G. B cell H. Memory B cells I. Plasma
EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU
 EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Aşağıdakilerden hangisi transfüzyon reaksiyonlarından biri değildir? A) Akut hemolitik transfüzyon reaksiyonu B) Akut normovolemik hemodilüsyon
EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Aşağıdakilerden hangisi transfüzyon reaksiyonlarından biri değildir? A) Akut hemolitik transfüzyon reaksiyonu B) Akut normovolemik hemodilüsyon
BELGELER. Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD
 BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) Tıbbi laboratuvarlar için uluslar arası kalite standardı 4. bölüm
BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) Tıbbi laboratuvarlar için uluslar arası kalite standardı 4. bölüm
CROSS-MATCH & DAT Testler/Problemler
 CROSS-MATCH & DAT Testler/Problemler Hazırlayan: Prof. Dr. Birol GÜVENÇ Çukurova Üniversitesi Tıp Fakültesi Balcalı Hastanesi Bölge Kan Merkezi Sunan: Dr. S. Haldun BAL UludağÜniversitesi Tıp Fakültesi
CROSS-MATCH & DAT Testler/Problemler Hazırlayan: Prof. Dr. Birol GÜVENÇ Çukurova Üniversitesi Tıp Fakültesi Balcalı Hastanesi Bölge Kan Merkezi Sunan: Dr. S. Haldun BAL UludağÜniversitesi Tıp Fakültesi
Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon)
 Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon) Kaynaklar Mikrobiyolojik prosedürleri doğrulama / geçerli kılmaya ilişkin aşağıdaki uluslararası kaynaklar önerilir
Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon) Kaynaklar Mikrobiyolojik prosedürleri doğrulama / geçerli kılmaya ilişkin aşağıdaki uluslararası kaynaklar önerilir
artus HCV QS-RGQ Kit Performans Özellikleri Ocak 2014 Sample & Assay Technologies Saptama limiti (LOD) Versiyon yönetimi
 artus HCV QS-RGQ Kit Performans Özellikleri artus HCV QS-RGQ Kit, Versiyon 1, 4518363, 4518366 Versiyon yönetimi Bu belge artus HCV QS-RGQ Kit Performans Özellikleri, Versiyon 1, R1 belgesidir. Testi gerçekleştirmeden
artus HCV QS-RGQ Kit Performans Özellikleri artus HCV QS-RGQ Kit, Versiyon 1, 4518363, 4518366 Versiyon yönetimi Bu belge artus HCV QS-RGQ Kit Performans Özellikleri, Versiyon 1, R1 belgesidir. Testi gerçekleştirmeden
Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları
 HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
TRANSFÜZYON MERKEZİ STANDART İŞLETİM PROSEDÜRÜ
 KOD:YÖN.PRS 34 YAY.TAR:27.03.2014 REV.TAR: REV.NO: SAYFA :1 / 5 1.AMAÇ: Bölge Kan Merkezinden temin edilen kan ve bileşenlerinin, transfüzyon için cross-match (çapraz karşılaştırma) ve gerek duyulan diğer
KOD:YÖN.PRS 34 YAY.TAR:27.03.2014 REV.TAR: REV.NO: SAYFA :1 / 5 1.AMAÇ: Bölge Kan Merkezinden temin edilen kan ve bileşenlerinin, transfüzyon için cross-match (çapraz karşılaştırma) ve gerek duyulan diğer
SINIR DEĞERLER NE ÖNERİLİR? Düzen Laboratuvarlar Grubu
 SEROLOJİK TANIDA SINIR DEĞERLER NASIL DEĞERLENDİRİLİR? NE ÖNERİLİR? Dr. Tutku TANYEL Dr. Tutku TANYEL Düzen Laboratuvarlar Grubu Şüpheli ilişkimin üzerinden 5 gün geçti acaba ne testi yaptırsam HIV bulaşıp
SEROLOJİK TANIDA SINIR DEĞERLER NASIL DEĞERLENDİRİLİR? NE ÖNERİLİR? Dr. Tutku TANYEL Dr. Tutku TANYEL Düzen Laboratuvarlar Grubu Şüpheli ilişkimin üzerinden 5 gün geçti acaba ne testi yaptırsam HIV bulaşıp
Dünyada 350 milyonun üzerindeki hepatit B taşıyıcısının %50 sinden fazlasında infeksiyon perinatal yolla kazanılmıştır.
 GİRİŞ Dünyada 350 milyonun üzerindeki hepatit B taşıyıcısının %50 sinden fazlasında infeksiyon perinatal yolla kazanılmıştır. HBeAg pozitif annelerden bebeğe bulaş oranı % 90 dır. Perinatal olarak kazanılan
GİRİŞ Dünyada 350 milyonun üzerindeki hepatit B taşıyıcısının %50 sinden fazlasında infeksiyon perinatal yolla kazanılmıştır. HBeAg pozitif annelerden bebeğe bulaş oranı % 90 dır. Perinatal olarak kazanılan
Prof Dr Davut Albayrak. Ondokuz mayıs Üniversitesi Tıp Fakültesi KAN MERKEZİ VE ÇOCUK HEMATOLOJİ BÖLÜMÜ SAMSUN KMTD KURS-2012
 Prof Dr Davut Albayrak Ondokuz mayıs Üniversitesi Tıp Fakültesi KAN MERKEZİ VE ÇOCUK HEMATOLOJİ BÖLÜMÜ SAMSUN KMTD KURS-2012 KAN GRUBU ANTİJENLERİ Kan grubu kırmızı kan hücrelerinin üzerinde bulunan ve
Prof Dr Davut Albayrak Ondokuz mayıs Üniversitesi Tıp Fakültesi KAN MERKEZİ VE ÇOCUK HEMATOLOJİ BÖLÜMÜ SAMSUN KMTD KURS-2012 KAN GRUBU ANTİJENLERİ Kan grubu kırmızı kan hücrelerinin üzerinde bulunan ve
Hepatit B Hasta Takibi Nasıl Yapılmalı?
 Hepatit B Hasta Takibi Nasıl Yapılmalı? Yrd. Doç. Dr. Kaya Süer Yakın Doğu Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Sunum Planı Giriş HBsAg Pozitifliği Kronik Hepatit
Hepatit B Hasta Takibi Nasıl Yapılmalı? Yrd. Doç. Dr. Kaya Süer Yakın Doğu Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Sunum Planı Giriş HBsAg Pozitifliği Kronik Hepatit
PERSONEL YARALANMALARI İZLEM TALİMATI
 Hazırlayan Kontrol eden Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Direktörü Hastane Yöneticisi 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden sağlık
Hazırlayan Kontrol eden Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Direktörü Hastane Yöneticisi 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden sağlık
Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme;
 Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme; o Hangi durumlarda bağışçıdan kan alınacağı, o Bağışçının seçilmesi, bağışçının reddi, bağışçıdan kan
Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme; o Hangi durumlarda bağışçıdan kan alınacağı, o Bağışçının seçilmesi, bağışçının reddi, bağışçıdan kan
PERSONEL YARALANMALARI İZLEM TALİMATI
 Sayfa No 1 / 5 Hazırlayan İnceleyen Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Temsilcisi Başhekim 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden
Sayfa No 1 / 5 Hazırlayan İnceleyen Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Temsilcisi Başhekim 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden
Prof Dr Davut Albayrak Ondokuz mayıs üniversitesi Tıp Fakültesi Kan merkezi Ve çocuk hematoloji BD -Samsun
 Prof Dr Davut Albayrak Ondokuz mayıs üniversitesi Tıp Fakültesi Kan merkezi Ve çocuk hematoloji BD -Samsun İNDİREKT COOMBS TESTİ ANTİKOR ARANAN PLAZMA + %5 LİK YIKANMIŞ KIRMIZI KAN HÜCRESİ EKLE FAB UÇLARI
Prof Dr Davut Albayrak Ondokuz mayıs üniversitesi Tıp Fakültesi Kan merkezi Ve çocuk hematoloji BD -Samsun İNDİREKT COOMBS TESTİ ANTİKOR ARANAN PLAZMA + %5 LİK YIKANMIŞ KIRMIZI KAN HÜCRESİ EKLE FAB UÇLARI
Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık
 Doç. Dr. Onur POLAT Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık personeli gibi hastalardan bulaşabilecek
Doç. Dr. Onur POLAT Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık personeli gibi hastalardan bulaşabilecek
Laboratuvar Tıbbında İzlenebilirlik
 Laboratuvar Tıbbında İzlenebilirlik Medikal Metroloji Çalıştayı TÜBİTAK-UME, İstanbul Dr. Diler Aslan Pamukkale Üniversitesi 13 Şubat 2013, İstanbul İçerik Adlandırma,Tanım, kavram, sektör, segment: Tıbbi
Laboratuvar Tıbbında İzlenebilirlik Medikal Metroloji Çalıştayı TÜBİTAK-UME, İstanbul Dr. Diler Aslan Pamukkale Üniversitesi 13 Şubat 2013, İstanbul İçerik Adlandırma,Tanım, kavram, sektör, segment: Tıbbi
EĞİTİM SONRASI BAŞARI ÖLÇME FORMU
 EĞİTİM SONRASI BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Transfüzyon tarihindeki önemli buluşu (ABO antijenleri tanımı) ile Nobel ödülü alan bilim adamı kimdir? a. Robert Cook b. Anthony Van Löwenhook
EĞİTİM SONRASI BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Transfüzyon tarihindeki önemli buluşu (ABO antijenleri tanımı) ile Nobel ödülü alan bilim adamı kimdir? a. Robert Cook b. Anthony Van Löwenhook
Belge No: Yayın Tarihi: Güncelleme Tarihi: Güncelleme No: Sayfa No: EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ
 EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama - 0 - EKÖ/YÖN 20 19.08.2009-1 2/5 1. AMAÇ Bu yönergenin amacı; çalışanların iş kazası sonucu yaralanmalarında bildirimin
EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama - 0 - EKÖ/YÖN 20 19.08.2009-1 2/5 1. AMAÇ Bu yönergenin amacı; çalışanların iş kazası sonucu yaralanmalarında bildirimin
EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI
 EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI Nilgün Kaşifoğlu, Tercan Us, Nazmiye Ülkü Koçman, Yurdanur Akgün Eskişehir Osmangazi Üniversitesi Tıp Fakültesi
EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI Nilgün Kaşifoğlu, Tercan Us, Nazmiye Ülkü Koçman, Yurdanur Akgün Eskişehir Osmangazi Üniversitesi Tıp Fakültesi
Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği. Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD
 Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD Akut ve kronik HBV enf da seroloji Akut Hep B de HBe Ag,
Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD Akut ve kronik HBV enf da seroloji Akut Hep B de HBe Ag,
TARAMA VE DOĞRULAMA TESTLERİ
 TARAMA VE DOĞRULAMA TESTLERİ Ortalama 450 (± %10) ml (~ 250 ml plazma + ~ 200 ml eritrosit) Yaklaşık hematokrit %36-37 Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu 2 Ulusal Kan Merkezleri ve Transfüzyon
TARAMA VE DOĞRULAMA TESTLERİ Ortalama 450 (± %10) ml (~ 250 ml plazma + ~ 200 ml eritrosit) Yaklaşık hematokrit %36-37 Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu 2 Ulusal Kan Merkezleri ve Transfüzyon
Eylül 2015 artus HSV-1/2 QS-RGQ Kiti: Performans Özellikleri
 Eylül 2015 artus HSV-1/2 QS-RGQ Kiti: Performans Özellikleri artus HSV-1/2 QS-RGQ Kiti, Versiyon 1 4500363 Testi gerçekleştirmeden önce www.qiagen.com/products/artushsv- 12pcrkitce.aspx adresinde yeni
Eylül 2015 artus HSV-1/2 QS-RGQ Kiti: Performans Özellikleri artus HSV-1/2 QS-RGQ Kiti, Versiyon 1 4500363 Testi gerçekleştirmeden önce www.qiagen.com/products/artushsv- 12pcrkitce.aspx adresinde yeni
KULLANICI TARAFINDAN TESTİN DOĞRULANMASI (VERİFİKASYON) Dr. Murat Öktem Düzen Laboratuvarlar Grubu
 KULLANICI TARAFINDAN TESTİN DOĞRULANMASI (VERİFİKASYON) Dr. Murat Öktem Düzen Laboratuvarlar Grubu Kaynaklar CLSI EP5-A2: Evaluation of Precision Performance of Quantitative Measurement Methods (2004)
KULLANICI TARAFINDAN TESTİN DOĞRULANMASI (VERİFİKASYON) Dr. Murat Öktem Düzen Laboratuvarlar Grubu Kaynaklar CLSI EP5-A2: Evaluation of Precision Performance of Quantitative Measurement Methods (2004)
T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ. SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006
 T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006.. GENELGE 2006/128 Günümüzde kan transfüzyonu uygulamalarının mesleki usul ve
T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006.. GENELGE 2006/128 Günümüzde kan transfüzyonu uygulamalarının mesleki usul ve
GEBELİK VE VİRAL HEPATİTLER. Uz. Dr. Funda Şimşek Okmeydanı Eğitim Hastanesi İnfeksiyon Hast. ve Kli. Mikr.Kliniği
 GEBELİK VE VİRAL HEPATİTLER Uz. Dr. Funda Şimşek Okmeydanı Eğitim Hastanesi İnfeksiyon Hast. ve Kli. Mikr.Kliniği GEBELİK VE VİRAL HEPATİTLER Uz.Dr.Funda Şimşek SSK Okmeydanı Eğitim Hastanesi İnfeksiyon
GEBELİK VE VİRAL HEPATİTLER Uz. Dr. Funda Şimşek Okmeydanı Eğitim Hastanesi İnfeksiyon Hast. ve Kli. Mikr.Kliniği GEBELİK VE VİRAL HEPATİTLER Uz.Dr.Funda Şimşek SSK Okmeydanı Eğitim Hastanesi İnfeksiyon
BELGELER. Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD
 BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) A global quality standart for medical laboratories 4. bölüm -
BELGELER Dr. A. Arzu Sayıner Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Belgeler - 1 ISO 15189, 2003 (2009 da revizyon) A global quality standart for medical laboratories 4. bölüm -
Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı. Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi
 Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi Akut Hepatit B ve Kronik Hepatit Aktivasyonunun Ayrımı Neden AHB ve KHB-A karışır? Neden AHB ve KHB-A
Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi Akut Hepatit B ve Kronik Hepatit Aktivasyonunun Ayrımı Neden AHB ve KHB-A karışır? Neden AHB ve KHB-A
Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi. Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş
 Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş Giriş Hemodiyaliz hastalarında enfeksiyon önemli mortalite nedenleri arasındadır Hepatit C
Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş Giriş Hemodiyaliz hastalarında enfeksiyon önemli mortalite nedenleri arasındadır Hepatit C
(13-01-2005 tarih ve 25699 sayılı R.G.)
 GIDA MADDELERĐNDE OKRATOKSĐN A SEVĐYESĐNĐN RESMĐ KONTROLÜ ĐÇĐN NUMUNE ALMA METOTLARI TEBLĐĞĐ (Tebliğ No: 2004/47) (13-01-2005 tarih ve 25699 sayılı R.G.) Amaç Madde 1- Bu Tebliğin amacı okratoksin A seviyesinin
GIDA MADDELERĐNDE OKRATOKSĐN A SEVĐYESĐNĐN RESMĐ KONTROLÜ ĐÇĐN NUMUNE ALMA METOTLARI TEBLĐĞĐ (Tebliğ No: 2004/47) (13-01-2005 tarih ve 25699 sayılı R.G.) Amaç Madde 1- Bu Tebliğin amacı okratoksin A seviyesinin
Kronik Hepatit B li Hastanın Güncel Tedavisi
 Kronik Hepatit B li Hastanın Güncel Tedavisi Prof. Dr. Reşat Özaras İstanbul Üniversitesi, Cerrahpaşa Tıp Fakültesi, Enfeksiyon AD. rozaras@yahoo.com Genel Bakış HBV Enfeksiyonunda Neredeyiz? Eradikasyon
Kronik Hepatit B li Hastanın Güncel Tedavisi Prof. Dr. Reşat Özaras İstanbul Üniversitesi, Cerrahpaşa Tıp Fakültesi, Enfeksiyon AD. rozaras@yahoo.com Genel Bakış HBV Enfeksiyonunda Neredeyiz? Eradikasyon
Tıbbi Cihaz Klinik Araştırmaları
 Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Tedavi Ne Zaman Yapılmalı Ne Zaman Yapılmamalı?
 Tedavi Ne Zaman Yapılmalı Ne Zaman Yapılmamalı? Dr. Ziya Kuruüzüm DEÜTF Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Hepatit Akademisi 2015: Temel Bilgiler 22-25.01.2015, Kolin Otel, Çanakkale Sunum
Tedavi Ne Zaman Yapılmalı Ne Zaman Yapılmamalı? Dr. Ziya Kuruüzüm DEÜTF Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD Hepatit Akademisi 2015: Temel Bilgiler 22-25.01.2015, Kolin Otel, Çanakkale Sunum
KRONİK HEPATİT B OLGUSU
 KRONİK HEPATİT B OLGUSU DR DURU MISTANOĞLU ÖZATAĞ KÜTAHYA SAĞLIK BİLİMLERİ ÜNİVERSİTESİ TIP FAKÜLTESİ ENFEKSİYON HASTALIKLARI VE KLİNİK MİKROBİYOLOJİ ABD OLGU 44 yaşında, kadın 2014 yılında eşi akut hepatit
KRONİK HEPATİT B OLGUSU DR DURU MISTANOĞLU ÖZATAĞ KÜTAHYA SAĞLIK BİLİMLERİ ÜNİVERSİTESİ TIP FAKÜLTESİ ENFEKSİYON HASTALIKLARI VE KLİNİK MİKROBİYOLOJİ ABD OLGU 44 yaşında, kadın 2014 yılında eşi akut hepatit
TÜRK GIDA KODEKSİ GIDA İLE TEMAS EDEN AKTİF VE AKILLI MADDE VE MALZEMELER TEBLİĞİ (TEBLİĞ NO: 2017/Taslak)
 Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ GIDA İLE TEMAS EDEN AKTİF VE AKILLI MADDE VE MALZEMELER TEBLİĞİ (TEBLİĞ NO: 2017/Taslak) Amaç MADDE 1 (1) Bu Tebliğin amacı; gıda ile temas eden
Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ GIDA İLE TEMAS EDEN AKTİF VE AKILLI MADDE VE MALZEMELER TEBLİĞİ (TEBLİĞ NO: 2017/Taslak) Amaç MADDE 1 (1) Bu Tebliğin amacı; gıda ile temas eden
AKILICI LABORATUVAR KULLANIMI TEST İSTEM PROSEDÜRÜ
 DOKUMAN BL.PR. 03 İLK YAYIN 16.11.2018 SAYFA 1/ 7 Revizyon Nedeni: 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını
DOKUMAN BL.PR. 03 İLK YAYIN 16.11.2018 SAYFA 1/ 7 Revizyon Nedeni: 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını
HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi
 HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi Prof Dr Ali Ağaçfidan İstanbul Tıp Fakültesi, Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı İnsan retrovirusları
HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi Prof Dr Ali Ağaçfidan İstanbul Tıp Fakültesi, Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı İnsan retrovirusları
EV TİPİ FIRINLARIN VE ASPİRATÖRLERİN ENERJİ ETİKETLEMESİNE DAİR TEBLİĞ
 14 Ocak 2015 ÇARŞAMBA Resmî Gazete Sayı : 29236 TEBLİĞ Bilim, Sanayi ve Teknoloji Bakanlığından: EV TİPİ FIRINLARIN VE ASPİRATÖRLERİN ENERJİ ETİKETLEMESİNE DAİR TEBLİĞ (SGM-2015/8) Amaç MADDE 1 (1) Bu
14 Ocak 2015 ÇARŞAMBA Resmî Gazete Sayı : 29236 TEBLİĞ Bilim, Sanayi ve Teknoloji Bakanlığından: EV TİPİ FIRINLARIN VE ASPİRATÖRLERİN ENERJİ ETİKETLEMESİNE DAİR TEBLİĞ (SGM-2015/8) Amaç MADDE 1 (1) Bu
Kan Hizmetleri Genel Müdürlüğü
 Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 10 Mart 2016 www.kanver.org www.kizilay.org.tr KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015 NAT TARAMA TESTİ UYGULAMALARI VE ÖNEMİ KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015
Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 10 Mart 2016 www.kanver.org www.kizilay.org.tr KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015 NAT TARAMA TESTİ UYGULAMALARI VE ÖNEMİ KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015
Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD
 Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HÇ, 28 yş, E, Memur 2010 yılı ocak ayında kan bağışı sırasında sarılık olduğu söyleniyor. Başvuru sırasında bazen halsizlik ve
Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HÇ, 28 yş, E, Memur 2010 yılı ocak ayında kan bağışı sırasında sarılık olduğu söyleniyor. Başvuru sırasında bazen halsizlik ve
ANTİBİYOTİK DUYARLILIK TEST SİSTEMLERİNİN VERİFİKASYONU
 ANTİBİYOTİK DUYARLILIK TEST SİSTEMLERİNİN VERİFİKASYONU Yrd.Doç.Dr. Murat TELLİ Adnan Menderes Üniversitesi tıp Fakültesi Tıbbi Mikrobiyoloji A.D. Çalışma Planı Verifikasyon planı Kabul kriterleri Çalışmada
ANTİBİYOTİK DUYARLILIK TEST SİSTEMLERİNİN VERİFİKASYONU Yrd.Doç.Dr. Murat TELLİ Adnan Menderes Üniversitesi tıp Fakültesi Tıbbi Mikrobiyoloji A.D. Çalışma Planı Verifikasyon planı Kabul kriterleri Çalışmada
Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması. Prof. Dr. Yaşar BAYINDIR BUHASDER-2017
 Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması Prof. Dr. Yaşar BAYINDIR BUHASDER-2017 ABD: Solid Organ Nakli 26.034 organ nakli (Ocak-Eylül 2017 arası) 4.491 (%17) canlı verici 21.543 (%83)
Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması Prof. Dr. Yaşar BAYINDIR BUHASDER-2017 ABD: Solid Organ Nakli 26.034 organ nakli (Ocak-Eylül 2017 arası) 4.491 (%17) canlı verici 21.543 (%83)
BİYOİSTATİSTİK Sağlık Alanına Özel İstatistiksel Yöntemler Dr. Öğr. Üyesi Aslı SUNER KARAKÜLAH
 BİYOİSTATİSTİK Sağlık Alanına Özel İstatistiksel Yöntemler Dr. Öğr. Üyesi Aslı SUNER KARAKÜLAH Ege Üniversitesi, Tıp Fakültesi, Biyoistatistik ve Tıbbi Bilişim AD. Web: www.biyoistatistik.med.ege.edu.tr
BİYOİSTATİSTİK Sağlık Alanına Özel İstatistiksel Yöntemler Dr. Öğr. Üyesi Aslı SUNER KARAKÜLAH Ege Üniversitesi, Tıp Fakültesi, Biyoistatistik ve Tıbbi Bilişim AD. Web: www.biyoistatistik.med.ege.edu.tr
CMV lab.tanı Hangi test, ne zaman, laboratuvar sonucunun klinik anlamı?
 CMV lab.tanı Hangi test, ne zaman, laboratuvar sonucunun klinik anlamı? Maternal inf.tanısı Fetal inf.tanısı Yenidoğan inf.tanısı Bir test sonucunun doğru yorumlanabilmesi, testin tanı doğruluğunun bilinmesi
CMV lab.tanı Hangi test, ne zaman, laboratuvar sonucunun klinik anlamı? Maternal inf.tanısı Fetal inf.tanısı Yenidoğan inf.tanısı Bir test sonucunun doğru yorumlanabilmesi, testin tanı doğruluğunun bilinmesi
2. Kapsam 2.1. Sağlık hizmet sunucularındaki acil ve yoğun bakım üniteleri dışındaki birimlerden istenen test istemlerini kapsar.
 AKILCI LABORATUVAR KULLANIMI AKILCI TEST İSTEMİ PROSEDÜRÜ 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını arttırmak
AKILCI LABORATUVAR KULLANIMI AKILCI TEST İSTEMİ PROSEDÜRÜ 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını arttırmak
25 Ağustos 2014 PAZARTESİ. Resmî Gazete. Sayı : (Mükerrer) YÖNETMELİK. Gıda, Tarım ve Hayvancılık Bakanlığından:
 25 Ağustos 2014 PAZARTESİ Resmî Gazete Sayı : 29099 (Mükerrer) YÖNETMELİK Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ PESTİSİTLERİN MAKSİMUM KALINTI LİMİTLERİ YÖNETMELİĞİ BİRİNCİ BÖLÜM
25 Ağustos 2014 PAZARTESİ Resmî Gazete Sayı : 29099 (Mükerrer) YÖNETMELİK Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ PESTİSİTLERİN MAKSİMUM KALINTI LİMİTLERİ YÖNETMELİĞİ BİRİNCİ BÖLÜM
Kronik Hepatitlerin serolojik ve moleküler tanısı Doç. Dr. Kenan Midilli
 Kronik Hepatitlerin serolojik ve moleküler tanısı Doç. Dr. Kenan Midilli İÜ Cerrahpaşa Tıp Fakültei Tıbbi Mikrobiyoloji Anabilim Dalı Hepadnaviridae ailesi Orthohepadnavirus cinsi semisirküler (relaxed),
Kronik Hepatitlerin serolojik ve moleküler tanısı Doç. Dr. Kenan Midilli İÜ Cerrahpaşa Tıp Fakültei Tıbbi Mikrobiyoloji Anabilim Dalı Hepadnaviridae ailesi Orthohepadnavirus cinsi semisirküler (relaxed),
Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi
 Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi 1 Eyvah iğne battı, ne yapmalıyım? 2 İş Kazası İş kazalarını %98
Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi 1 Eyvah iğne battı, ne yapmalıyım? 2 İş Kazası İş kazalarını %98
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ
 TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ Amaç MADDE 1- Kozmetik ürünlerin üreticileri tarafından raf ömürleri belirlenirken
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ Amaç MADDE 1- Kozmetik ürünlerin üreticileri tarafından raf ömürleri belirlenirken
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı. Rehberler Es lig inde Hasta Yo netimi
 Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji
 Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Sunum Kapsamı HCV tanımı HCV enfeksiyonunun seyri Epidemiyoloji HCV genotiplerinin önemi, dağılımı Laboratuvarımızdaki
Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Sunum Kapsamı HCV tanımı HCV enfeksiyonunun seyri Epidemiyoloji HCV genotiplerinin önemi, dağılımı Laboratuvarımızdaki
TEBLİĞ. a) 29/12/2011 tarihli ve 28157 üçüncü mükerrer sayılı Resmî Gazete de yayımlanan Türk Gıda Kodeksi Yönetmeliğine dayanılarak,
 14 Şubat 2014 CUMA Resmî Gazete Sayı : 28913 Gıda, Tarım ve Hayvancılık Bakanlığından: TEBLİĞ TÜRK GIDA KODEKSİ KİLO VERME AMAÇLI ENERJİSİ KISITLANMIŞ GIDALAR TEBLİĞİ (TEBLİĞ NO: 2014/3) Amaç MADDE 1 (1)
14 Şubat 2014 CUMA Resmî Gazete Sayı : 28913 Gıda, Tarım ve Hayvancılık Bakanlığından: TEBLİĞ TÜRK GIDA KODEKSİ KİLO VERME AMAÇLI ENERJİSİ KISITLANMIŞ GIDALAR TEBLİĞİ (TEBLİĞ NO: 2014/3) Amaç MADDE 1 (1)
MADDE 2 (1) Bu Yönetmelik, gıdaların mikrobiyolojik kriterleri ile gıda işletmecilerinin uyması ve uygulaması gereken kuralları kapsar.
 TÜRK GIDA KODEKSİ MİKROBİYOLOJİK KRİTERLER YÖNETMELİĞİ Yetki Kanunu: 5996 Yayımlandığı R.Gazete: 29.12.2011-28157 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı;
TÜRK GIDA KODEKSİ MİKROBİYOLOJİK KRİTERLER YÖNETMELİĞİ Yetki Kanunu: 5996 Yayımlandığı R.Gazete: 29.12.2011-28157 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı;
MADDE 4 (1) 5996 sayılı Kanunun 3 üncü maddesindeki tanımlara ilave olarak ikinci fıkrada yer alan tanımlar da geçerlidir.
 Resmi Gazete Sayısı: 29899 TÜRK GIDA KODEKSİ PESTİSİTLERİN MAKSİMUM KALINTI LİMİTLERİ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; tüketicinin yüksek
Resmi Gazete Sayısı: 29899 TÜRK GIDA KODEKSİ PESTİSİTLERİN MAKSİMUM KALINTI LİMİTLERİ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; tüketicinin yüksek
Kronik Viral Hepatit B Mikrobiyolojik Laboratuvar Tanı Yönetimi. Selda Erensoy Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 Kronik Viral Hepatit B Mikrobiyolojik Laboratuvar Tanı Yönetimi Selda Erensoy Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Hepatit B de virolojik göstergeler HBsAg anti-hbc anti-hbs
Kronik Viral Hepatit B Mikrobiyolojik Laboratuvar Tanı Yönetimi Selda Erensoy Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Hepatit B de virolojik göstergeler HBsAg anti-hbc anti-hbs
MESGEMM İSG/Mevzuat/Yönetmelikler
 MESGEMM İSG/Mevzuat/Yönetmelikler İçindekiler Birinci Bölüm - Amaç, Kapsam, Dayanak ve Tanımlar Madde 1 Amaç Madde 2 Kapsam Madde 3 Dayanak Madde 4 Tanımlar İkinci Bölüm - Teftiş Yetkisi ve İşin Durdurulması
MESGEMM İSG/Mevzuat/Yönetmelikler İçindekiler Birinci Bölüm - Amaç, Kapsam, Dayanak ve Tanımlar Madde 1 Amaç Madde 2 Kapsam Madde 3 Dayanak Madde 4 Tanımlar İkinci Bölüm - Teftiş Yetkisi ve İşin Durdurulması
BAĞIMSIZ VE ÜRÜNLERE ENTEGRE SALMASTRASIZ DEVİRDAİM POMPALARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2011/15)
 Resmi Gazete Tarihi: 23.09.2011 Resmi Gazete Sayısı: 28063 BAĞIMSIZ VE ÜRÜNLERE ENTEGRE SALMASTRASIZ DEVİRDAİM POMPALARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2011/15) Amaç MADDE
Resmi Gazete Tarihi: 23.09.2011 Resmi Gazete Sayısı: 28063 BAĞIMSIZ VE ÜRÜNLERE ENTEGRE SALMASTRASIZ DEVİRDAİM POMPALARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2011/15) Amaç MADDE
ANTİGLOBULİN TESTLER. Dr. Güçhan ALANOĞLU
 ANTİGLOBULİN TESTLER Dr. Güçhan ALANOĞLU Tanımlar İnsan nsan globulinlerine karşı oluşan antikorlara Anti-Human Globulinler (AHG, AHG, antikorlara karşı gelişen en anti-antikor) antikor) Bu u antikorların
ANTİGLOBULİN TESTLER Dr. Güçhan ALANOĞLU Tanımlar İnsan nsan globulinlerine karşı oluşan antikorlara Anti-Human Globulinler (AHG, AHG, antikorlara karşı gelişen en anti-antikor) antikor) Bu u antikorların
ELEKTRİK MOTORLARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2012/2)
 7 Şubat 2012 SALI Resmî Gazete Sayı : 28197 TEBLİĞ Bilim, Sanayi ve Teknoloji Bakanlığından: ELEKTRİK MOTORLARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2012/2) Amaç MADDE 1 (1)
7 Şubat 2012 SALI Resmî Gazete Sayı : 28197 TEBLİĞ Bilim, Sanayi ve Teknoloji Bakanlığından: ELEKTRİK MOTORLARI İLE İLGİLİ ÇEVREYE DUYARLI TASARIM GEREKLERİNE DAİR TEBLİĞ (SGM-2012/2) Amaç MADDE 1 (1)
GAZİANTEP ÜNİVERSİTESİ - KALİTE YÖNETİM SİSTEMİ Doküman No: HTRF-T22-P01
 Sayfa: 1/6 Revizyonun Açıklaması Madde No - - KAPSAM: Transfüzyon Merkezi Hazırlayanlar Murat ORULLUOĞLU Transfüzyon Merk. Sor. Tekn. Gülay YABA Kalite Yönetim Birimi Kontrol Funda BATMAZOĞLU Kalite Koordinatörü
Sayfa: 1/6 Revizyonun Açıklaması Madde No - - KAPSAM: Transfüzyon Merkezi Hazırlayanlar Murat ORULLUOĞLU Transfüzyon Merk. Sor. Tekn. Gülay YABA Kalite Yönetim Birimi Kontrol Funda BATMAZOĞLU Kalite Koordinatörü
