In Vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir Türkçe 4 I
|
|
|
- Murat Abacı
- 6 yıl önce
- İzleme sayısı:
Transkript
1 B MAX StaphSR In Vitro Diyagnostik Kullanım İçindir P0207(01) BD MAX System ile kullanım içindir Türkçe 4 I KULLANIM AMACI BD MAX System'da gerçekleştirilen BD MAX StaphSR testi, nazal kolonizasyon riski altında olan hastalardan elde edilen nazal swablarda Staphylococcus aureus (SA) DNA ve metisiline dirençli Staphylococcus aureus (MRSA) DNA'nın doğrudan saptanması ve ayrıştırılmasında kullanılan otomatik kalitatif in vitro diyagnostik bir testtir. Bu testte, MRSA/SA DNA'sının amplifikasyonunda gerçek zamanlı polimeraz zincir reaksiyonu (PCR) ve amplifiye DNA'nın saptanmasında florojenik, hedefe özel hibridizasyon probları kullanılır. BD MAX StaphSR testinin, sağlık bakımı ortamlarında MRSA ve SA enfeksiyonlarının önlenmesine ve kontrolüne yardımcı olması amaçlanmıştır. MRSA veya SA enfeksiyonlarına tanı koyması veya MRSA/SA enfeksiyonları konusunda tedaviye rehberlik yapması veya tedaviyi izlemesi amaçlanmamıştır. Negatif bir sonuç nazal kolonizasyonu önlemez. Eş zamanlı kültürler epidemiyolojik tipin belirlenmesi amacıyla organizmaların elde edilmesi veya daha ileri duyarlılık testleri için gereklidir. PROSEDÜRÜN ÖZETİ VE AÇIKLAMASI Staphylococcus aureus, klinik belirtileri püstülden sepsis ve ölüme kadar değişen kan dolaşımı enfeksiyonları ve ameliyat bölgesi enfeksiyonları gibi nozokomiyal enfeksiyonların başlıca nedenidir 1. Sıklıkla sağlıklı bireylerin burnunda veya cildinde bulunur (asemptomatik taşıyıcılar). Staphylococcus aureus enfeksiyonlarının tedavisi daha önceden etkili olan antimikrobiyal ajanlara dirençli suşların ortaya çıkmasıyla önemli bir konu haline gelmiştir. Metisiline dirençli Staphylococcus aureus suşları sıklıkla sağlık bakımı ortamlarında bulunur; bazı sağlık tesislerindeki Kuzey Amerika hastanelerinde hastaneden kapılan Staphylococcus aureus izolatlarının %60'ına yakınını temsil eder. 2,3 Hastane ortamlarında MRSA, sağlık çalışanlarının kontamine ellerinden hastadan hastaya bulaşabilir. Sağlık bakımı ortamında MRSA ile kolonizasyonun risk faktörleri arasında hastanede uzun süre kalma, MRSA ile enfekte hastalara yakın olma, çok sayıda ve uzun süreli geniş spektrumlu antibiyotik tedavisi kullanma ve MRSA taşıma vardır. MRSA enfeksiyonu MRSA kolonili hastalarda yüksektir. Staphylococcus aureus cerrahi bölge enfeksiyonlarının (SSI) başlıca sebeplerinden biridir. SSI nin %20 56 sından sorumludur ve bunlar arasında MRSA, izolatların %57 sini temsil edebilir. 4 Her iki patojenle ilişkili mortalite oranı %5 ila %22 arasında değişmektedir. 4,5 SSI'li çoğu hastada, Staphylococcus aureus enfeksiyonu endojen kaynaklıdır. 4,6 Staphylococcus aureus ve MRSA'yı saptamak için kullanılan geleneksel teknikler, kültür basamaklarını ve saf kolonilerin izolasyonunu gerektirir ve bunları Staphylococcus aureus'u saptamak için aglütinasyon testi ve ya oksasilin duyarlılık testi, metisiline direnç (meca geni) saptanması ya da MRSA'yı saptamak için penisilin bağlayıcı protein (PBP 2a) saptanması yer alır. Bu geleneksel yöntemler kullanıldığında Staphylococcus aureus ve MRSA durumunu çözümlemek için, 48 saatten fazla medyan süreyle minimum 24 saat gerekmektedir. Staphylococcus aureus enfeksiyonları ile ilişkili morbidite ve mortalitenin artması, kayıp meca suşlarının ortaya çıkması ve yeni bir metisiline dirençli genin (mecc geni) yayılmasına rağmen, Staphylococcus aureus ve MRSA'nın günler yerine saatler içerisinde saptanıp ayrıştırılabilmesi mevcut uygulamalara göre bir avantaj sunmakta ve hastaların daha etkili bir şekilde tedavi edilmesine olanak sağlamaktadır. Bir nazal örnek alınır ve önerilen swab kullanılarak laboratuvara gönderilir (Gerekli Fakat Sağlanmamış Ekipman ve Malzemeler bölümüne bakın). Swab, BD MAX StaphSR Sample Buffer Tube'e yerleştirilir. Hücreleri swab'dan tampona bırakmak için Örnek Tampon Tüpü vortekslenir. Örnek Tampon Tüpü BD MAX System'a yerleştirilince buradaki otomatik prosedür oluşur: Bakteriyel hücreler lizise uğratılır; DNA manyetik boncuklardan ekstrakt ve konsantre edilir; son olarak da, varsa, genetik hedefleri amplifiye etmek için kullanılan SA'ya ve MRSA'ya spesifik primerlerin bulunduğu elüsyona uğratılmış DNA alikotu PCR reaktiflerine eklenir. Bu testte de Örnek İşleme Kontrolü vardır. İnhibitör maddeler ve cihaz kaynaklı yetersizlik veya reaktif hatası işlemini izlemek için Örnek İşleme Kontrolü Ekstraksiyon tüpünde kalır ve ekstraksiyon, konsantrasyon ve amplifikasyon adımlarını uygular. BD MAX System'a klinik örnek, BD MAX Unitized Reagent Strip (Ünitelendirilmiş Reaktif Stripi) ve BD MAX PCR Cartridge'i (Kartuş) yüklendikten sonra operatör müdahalesi gerekmez. BD MAX System örnek lizisi, DNA ekstraksiyonu ve konsantrasyonu, reaktif rehidrasyonu, nükleik asit amplifikasyonu ve gerçek zamanlı polimeraz zincir reaksiyonu (PCR) kullanılarak hedef nükleik asit sekansının saptanmasını otomatik olarak gerçekleştirir. Amplifiye hedefler, sönmüş floroforlarla etiketlenmiş hidroliz problarıyla algılanır. Sinyallerin amplifikasyonu, saptanması ve yorumlanması BD MAX System tarafından otomatik olarak yapılır. 1
2 PROSEDÜR İLKELERİ BD MAX System, hücre lizisi ve DNA ekstraksiyonu gerçekleştirmek üzere litik ve ekstraksiyon reaktiflerinin bir kombinasyonunu kullanır. Yüksek bir sıcaklıkta enzimatik hücre lizisi sonrasında serbest kalan nükleik asitler manyetik afinite boncuklarıyla yakalanır. Bağlı nükleik asitlerin bulunduğu boncuklar yıkanır ve nükleik asitler Elüsyon Tamponunda ısıyla elüsyona uğratılır. Elüsyona uğratılmış DNA, Nötralizasyon Tamponuyla nötralize edilir ve PCR reaktiflerinin rehidrasyonu için Ana Karışım Tüpüne aktarılır. Rekonstitüsyon yapılmış amplifikasyon reaktifi BD MAX PCR Cartridge'e dağıtılır. BD MAX PCR Cartridge'deki mikrovalfler PCR başlamadan önce buharlaşma ve amplikon kontaminasyonunu önlemek için sistem tarafından mühürlenir. Amplifiye DNA hedefleri bir uçta söndürücü kısım ve öteki uçta bir floresan raportör boya (florofor) ile etiketlenmiş hidroliz (TaqMan) problarıyla saptanır. Farklı floroforlarla etiketlenmiş problar; SCCmec sağ uç bileşkesindeki (MREJ) belirli bir amplikonun, metisiline dirençli meca ve mecc genlerinin, ısıya dayanıklı Staphylococcus aureus nükleazını kodlayan nuc geninin ve Örnek İşleme Kontrolü amplikonlarının BD MAX System'daki dört farklı optik kanalında saptanmasında kullanılır: MREJ amplikonları FAM kanalında, meca ve mecc amplikonları ROX kanalında, nuc amplikonları VIC kanalında, Örnek İşleme Kontrolü amplikonları da Cy5.5 kanalında algılanır. Problar doğal durumundayken florofor floresanı söndürücüye yakınlığı nedeniyle söndürülür. Ancak hedef DNA varlığında problar tamamlayıcı sekanslarına hibridize olur ve DNA polimerazın, DNA şablonu boyunca yeni oluşan iplikçiği sentezlerken 5 3 ekzonükleaz aktivitesi ile hidrolize uğrar. Bunun sonucunda floroforlar söndürücü moleküllerden ayrılır ve floresan yayılır. BD MAX StaphSR testi için kullanılan dört optik kanalda saptanan floresan miktarı doğrudan hidrolize uğrayan, karşılık gelen prob miktarıyla orantılıdır. BD MAX System bu sinyalleri her amplifikasyon döngüsünün sonunda ölçer ve verileri sonuç sağlamak üzere yorumlar. REAKTİFLER REF İçindekiler Miktar BD MAX StaphSR Master Mix (Ana Karışım) (B7) Polimeraz, nükleotidler ve spesifik moleküler problar ve primerlerle birlikte Örnek İşleme Kontrolüne spesifik 24 test moleküler prob içeren kurutulmuş PCR Master Mix. BD MAX StaphSR Unitized Reagent Strip (Ünitelendirilmiş Reaktif Stripi) Örnek işleme ve DNA ekstraksiyonu için gerekli tüm sıvı reaktifler ve tek kullanımlık pipet uçları içeren 24 test Ünitelendirilmiş Reaktif Stripi. BD MAX StaphSR Extraction Tube (Ekstraksiyon Tüpü) (B8) DNA manyetik afinite boncukları, Akromopeptidaz ve Örnek İşleme Kontrolü içeren kuru ekstraksiyon reaktifi 24 test BD MAX StaphSR Sample Buffer Tube (Örnek Tamponu Tüpü) 24 test Septum Kapakları 25 GEREKLİ FAKAT SAĞLANMAMIŞ EKİPMAN VE MALZEMELER BD BBL CultureSwab Liquid Stuart tek veya çift swab (Becton Dickinson katalog no veya ), Copan (Venturi) Transystem* Liquid Stuart tek veya çift swab (Copan, katalog no. 141C veya 139C) VWR Multi-Tube Vortexer (VWR katalog no ) NALGENE Cryogenic Vial Holder (VWR, katalog no ) Tek kullanımlık eldivenler, pudrasız Steril makas (isteğe bağlı) Steril Gazlı Bez Kronometre veya süre ölçer BD MAX PCR Cartridges (BD MAX PCR Kartuşları) (BD Diagnostic Systems katalog no ) 2
3 UYARILAR VE ÖNLEMLER BD MAX StaphSR testi in vitro Diagnostik Kullanım içindir. Bu ürün sadece BD MAX System'da kullanılabilir. Son kullanma tarihi geçmiş reaktifler ve/veya malzemeleri kullanmayın. Varışıyla birlikte dış kartonu mühürleyen etiket bozulmuşsa kiti kullanmayın. Koruyucu poşetler geldiklerinde açık veya yırtıksa reaktifleri kullanmayın. Reaktifleri reaktif poşetleri içinde kurutucu yoksa veya açılmışsa kullanmayın. Reaktif poşetlerinden kurutucuyu çıkarmayın. Reaktiflerin koruyucu poşetini her kullanımdan sonra fermuar şeklinde kapanan mühürle hemen kapatın. Mühürlemeden önce varsa poşetlerdeki fazla havayı giderin. Reaktifleri ısıya ve neme karşı koruyun. Neme uzun süre maruziyet ürün performansına etki edecektir. Reaktifleri folyo bozulmuş veya hasarlıysa kullanmayın. Farklı poşetler ve/veya kitler ve/veya lotlardan reaktifleri karıştırmayın. Kontaminasyon oluşacağından ve test sonuçlarını olumsuz etkileyebileceğinden kapakları birbirleriyle değiştirmeyin veya tekrar kullanmayın. Ünitelendirilmiş Reaktif Stripleri uygun sıvı dolması için kontrol edin (sıvıların tüplerin alt kısmında olmasını sağlayın) (bkz. Şekil 1). Tüm pipet uçlarının var olduğundan emin olmak için Ünitelendirilmiş Reaktif Striplerini kontrol edin (bkz. Şekil 1). Ana Karışım ve Ekstraksiyon Tüpü barkod okunabilirliği bozulabileceğinden kimyasal solüsyonları kullanırken dikkatli davranın. Bu testin düzgün yapılması için uygun laboratuvar tekniği şarttır. Testin yüksek analitik duyarlılığı nedeniyle tüm malzeme ve reaktiflerin saflığını korumak için büyük dikkat gösterilmelidir. Laboratuvarın aynı genel alanında diğer PCR testlerinin yapıldığı durumlarda BD MAX StaphSR testi, test için gereken herhangi bir ek reaktif ve BD MAX System'ın kontamine olmamasına dikkat edilmelidir. Her zaman reaktiflerin mikrobiyal ve deoksiribonükleaz (DNase) kontaminasyonunu önleyin. Reaktifler ve kartuşlar kullanılmadan önce eldivenler değiştirilmelidir. Ortamın amplikonlar tarafından kontaminasyonunu önlemek için, kullandıktan sonra BD MAX PCR Cartridges'ı parçalarına ayırmayın. BD MAX PCR Cartridges mühürleri kontaminasyonu önleyecek şekilde tasarlanmıştır. Çapraz kontaminasyon riskinin en aza indirilmesi için laboratuvarda rutin olarak çevrenin izlenmesi gerekmektedir. BD MAX Microfluidic Cartridges (Mikrofluidik Kartuşları) en çok 2 çalışma için kullanılabilir. BD MAX StaphSR testinin önerilen süre aralıklarının dışına çıkması geçersiz sonuçlara neden olabilir. Belirtilen süreler içinde yapılmayan testler tekrarlanmalıdır. Yerel, eyalet, bölgesel ve/veya federal yönetmelikler veya sertifikasyon sağlayan kurumların gereklilikleri veya kılavuz ilkelere göre ek kontroller test edilebilir. Örnekleri her zaman bulaşıcı olabilirlermiş gibi ve CLSI Belgesi M29 da 7 ve Biosafety in Microbiological and Biomedical Laboratories de tanımlandığı şekilde güvenli laboratuvar prosedürlerine göre kullanın. 8 Tüm reaktifleri kullanırken koruyucu giysiler ve tek kullanımlık eldivenler kullanın. Testi yaptıktan sonra ellerinizi iyice yıkayın. Ağzınızla pipetlemeyin. Örneklerin veya kit reaktiflerinin kullanıldığı yerlerde sigara içmeyin ve bir şey yemeyin, içmeyin ve çiğnemeyin. Kullanılmamış reaktifleri ve atığı yerel, eyalet, bölgesel ve/veya federal yönetmeliklere göre atın. Ek uyarılar, önlemler ve prosedürler için BD MAX System Kullanıcı Kılavuzuna 11 bakın. SAKLAMA VE STABİLİTE Örnekler taşıma sırasında 2 C ile 25 C arasında tutulmalıdır. Donmaya veya aşırı sıcağa maruz kalmaya karşı koruyun. Örnekler test yapılmadan önce 25 ± 2 C'de 48 saate kadar, 2 8 C'de de 120 saate kadar (5 gün) saklanabilir. BD MAX StaphSR testi reaktifleri ve bileşenleri 2 25 C'de belirtilen son kullanma tarihine kadar stabildir. Son kullanma tarihi geçmiş bileşenleri kullanmayın. BD MAX StaphSR Master Mix ve Extraction Tubes mühürlenmiş poşetlerde sağlanır. Ürünü nemden korumak için açtıktan hemen sonra tekrar mühürleyin. Reaktif tüpleri, poşetin ilk açılışından ve tekrar mühürlenmesinden sonra 2 25 C'de 14 güne kadar stabildir. Rekonstitüsyon Yapılmamış Ekstraksiyon ve Ana Karışım reaktif tüpleri koruyucu poşetinden çıkarıldıktan sonra 5 saate kadar 2 25 C sıcaklıkta stabildir. KULLANIM TALİMATLARI Örnek Toplama/Taşıma Önerilen swab taşıma cihazının kullanılması (Gerekli Fakat Sağlanmamış Ekipman ve Malzemeler bölümüne bakın), nazal örnekler kurumsal ve laboratuvar standardı çalışma prosedürlerine ve/veya aşağıdakilere göre toplanmalıdır: 1. Swab'ları iki damla (yaklaşık 50 µl) steril fizyolojik salinle nemlendirin veya kuru olarak kullanın. 2. Swab'ları dikkatle hastanın burun deliğine yerleştirin [swab ucu burun kanadının kenarından 2,5 cm (1 inç) mesafeye kadar yerleştirilmelidir]. 3. Swab'ları ikinci burun deliğinde 5 kez mukozayla yuvarlayın. 3
4 4. Aynı swab'ları ikinci burun deliğine yerleştirin ve 2. ve 3. adımları tekrarlayın. 5. Swab'ları kendi taşıma tüpüne yerleştirin. 6. Taşıma tüpünü etiketleyin. 7. Swab'ları laboratuvara kurum ve laboratuvarın çalışma prosedürlerine göre taşıyın. (Saklama ve Stabilite bölümüne bakın). Örnek Hazırlama NOT: Test edilecek her örnek ve her Harici Kontrol için bir (1) Örnek Tampon Tüpü, bir (1) Septum Kapağı, bir (1) Ana Karışım (B7), bir (1) Ekstraksiyon Tüpü (B8) ve bir (1) Reaktif Stripi gereklidir. NOT: BD MAX StaphSR testini yapmadan önce klinik örneklerden kültür alma ayrıntıları için Klinik Örneklerden Kültür Alınması bölümüne bakın. 1. Örnek ve çalıştırılacak harici kontrol sayısına karşılık gelen Örnek Tampon Tüpü sayısını koruyun. 2. Barkodların net olduğundan, üzerine yazılmadığından veya etiketlenmediğinden emin olarak her Örnek Tampon Tüpünü uygun hasta kimliğiyle etiketleyin. 3. Örnek Tampon Tüpünün kapağını çıkarın. 4. Örnek taşıma tüpünden swab'ı çıkarıp karşılık gelen Örnek Tampon Tüpüne yerleştirin. 5. Swab'ı tüp kenarına yakın olarak sapından tutun (kontaminasyon riskini en aza indirmek için steril gazlı bez kullanın). Swab'ı, Örnek Tampon Tüpünün en dibinden yaklaşık bir (1) cm kaldırın ve kırmak için tüpün kenarına doğru bükerek kırın. Alternatif yöntem: sapı kesmek için steril bir makas kullanın. 6. Örnek Tampon Tüpünü bir septum kapağıyla kapatın. 7. Örnek Tampon Tüpünü NALGENE Kriyojenik Flakon Tutucuya yerleştirin ve Çoklu Tüp Vorteksleyici ile bir (1) dakika boyunca maksimum hızda vorteksleyin. Çoklu Tüp Vorteksleyici ile aynı anda en çok 24 örnek vortekslenebilir. BD MAX System'ın Çalışması NOT: Ayrıntılı talimat için BD MAX System Kullanıcı Kılavuzuna 11 bakın (Çalıştırma bölümü). NOT: BD MAX StaphSR testine ilişkin testler, yukarıdaki vorteksleme adımından hemen sonra yapılmalıdır (Örnek Hazırlama, Adım 7). Yeniden test etmek gerekirse örnekleri yeniden vorteksleyin. 1. BD MAX System'ın gücünü açın (daha önce yapılmadıysa) ve <user name> (kullanıcı adı) ve <password> (şifre) girerek oturum açın. 2. Reaktifler ve kartuşlar kullanılmadan önce eldivenler değiştirilmelidir. 3. BD MAX StaphSR kitinden gerekli sayıda Ünitelendirilmiş Reaktif Stripi çıkarın. Her Ünitelendirilmiş Reaktif Stripini, tüm sıvıların tüplerin alt kısmında olmasını sağlayacak şekilde sert bir yüzeye hafifçe vurun. 4. Gerekli sayıda Ekstraksiyon Tüpü/Tüpleri ve Ana Karışım Tüpü/Tüplerini koruyucu poşetlerinden çıkarın. Fazla havayı çıkarın ve poşetleri fermuar şeklinde kapanan mühür ile kapatın. 5. Test edilecek her örnek için bir (1) Ünitelendirilmiş Reaktif Stripi BD MAX System Rack'e, Raf A Pozisyon 1 ile başlayarak yerleştirin. 6. Bir (1) Ekstraksiyon Tüpünü (beyaz folyo) Şekil 1'de gösterildiği gibi her Ünitelendirilmiş Reaktif Stripinde Pozisyon 1 içine tıklatarak oturun. 7. Bir (1) Ana Karışım Tüpünü (yeşil folyo) Şekil 1'de gösterildiği gibi her Ünitelendirilmiş Reaktif Stripinde Pozisyon 2 içine tıklatarak oturun. Ek bileşen tüpleri Atık Haznesi Pipet Uçları #1 #2 #3 Lizis Tüpü Ekstraksiyon Tüpü StaphSR Master Mix (Ana Karışım) Elüsyon Tamponu Yıkama Tamponu Nötralizasyon Tamponu Şekil 1: BD MAX StaphSR Master Mix ve Extraction Tubes'ü Ünitelendirilmiş Reaktif Striplerine tıklatarak oturtun. 8. Run (Çalıştır) simgesine tıklayın ve barkodu tarayıcıyla tarayarak veya manuel giriş yaparak (lot izlenebilirliği için) BD MAX StaphSR testi için kit lot numarasını girin. NOT: Adım 8'i her yeni kit lotu kullanıldığında tekrarlayın. 9. Worklist'te (Çalışma Listesi) gezinin. Aşağı açılan menüyü kullanarak <BD MAX StaphSR 55> öğesini seçin. 10. Çalışma Listesine Örnek Tampon Tüpü Kimliği, Hasta Kimliği ve Erişim Numarasını (varsa) barkodu tarayıcıyla tarayarak veya manuel olarak girin. 4
5 11. Aşağı açılan menüden uygun kit lot numarasını seçin (dış kutuda bulabilirsiniz). 12. Geriye kalan tüm Örnek Tampon Tüpleri için adım 9 11'i tekrarlayın. 13. Örnek Tampon Tüplerini adım 5 ila 7'de belirtildiği gibi ilgili Ünitelendirilmiş Reaktif Striplerine karşılık gelen BD MAX System Rack'ler içine yerleştirin. NOT: Örnek Tampon Tüplerini, 1D barkod etiketleri dışarıya bakacak şekilde (böylece örnek kaydedilirken Örnek Tampon Tüpleri daha kolay taranabilir) örnek rafına/raflarına yerleştirin. 14. BD MAX System'a gerekli sayıda BD MAX PCR Cartridge yerleştirin (bkz. Şekil 2). Her kartuş toplam 24 örnek için 12 adede kadar örneklik 2 çalışmayı alır. BD MAX System her çalışma için PCR Kartuşunda pozisyon ve sırayı otomatik olarak seçer. BD MAX PCR Cartridges tüm şeritler kullanılıncaya dek birden fazla kullanılabilir. BD MAX PCR Cartridges'ın kullanımını maksimuma çıkarmak için, Sample Mode'u kullanarak, şerit atamaları için Worklist (Çalışma listesi) sekmesinin altında Run Wizard'ı (Sihirbazı Yürüt) seçin. Daha fazla ayrıntı için BD MAX System Kullanıcı Kılavuzuna bakın. 15. Rafı/rafları BD MAX System'a yükleyin (Şekil 3). Şekil 2: BD MAX PCR Cartridge'leri yükleyin. Taraf A Taraf B Şekil 3: Rafı/Rafları BD MAX System'a yükleyin. 5
6 16. BD MAX System kapağını kapatın ve işleme başlamak için <Start> (Başlat) öğesine tıklayın. 17. Çalışma sonunda, sonuçları hemen kontrol edin veya Örnek Tampon Tüplerini 2 8 C'de 5 güne kadar VEYA 25 ± 2 C'de sonuçlar kontrol edilinceye kadar maksimum 48 saat saklayın. NOT: Bir çalışma sırasında bir septum kapağı hasar görmüşse örneği saklamadan önce kapağı yenisiyle değiştirin. NOT: Hazırlanmış BD MAX StaphSR Sample Buffer Tube leri, örnek, Örnek Tampon Tüpüne eklendikten sonra 2 8 C'de maksimum 120 saat (5 gün) VEYA 25 ± 2 C'de maksimum 36 saat saklanabilir. Belirsiz (IND), Çözümlenmemiş (UNR) veya Eksik (INC) sonuç elde edildiğinde veya bir Harici Kontrol hatası oluştuğunda bu zaman çerçevesi içinde hazırlanmış Örnek Tampon Tüpünden bir test tekrarı yapılmalıdır ( Tekrar Test Prosedürü bölümüne bakın). KALİTE KONTROLÜ Kalite kontrolü prosedürleri test performansını izler. Laboratuvarlar test kontrol malzemelerinin sayısı, türü ve sıklığını yerel, bölgesel, eyalet, federal ve/veya ülke yönetmelikleri veya sertifika sağlayan kurumların kılavuz ilkeleri veya gerekliliklerine göre belirlemelidir. Genel Kalite Kontrolü rehberliği için CLSI MM3 ve EP12 bölümlerine bakabilirsiniz. 9,10 1. Harici Kontrol malzemelerini BD sağlamaz. BD MAX System yazılımında örnek test sonucunu yorumlamak amacıyla Harici Pozitif veya Negatif Kontroller kullanılmaz. Harici Kontroller hasta örnekleriymiş gibi ele alınır. (Harici Kontrol test sonuçlarının yorumlanması için Sonuçların Yorumlanması bölümündeki tabloya bakın.) 2. Bir (1) Harici Pozitif Kontrol ve bir (1) Harici Negatif Kontrol her bir laboratuvar düzeninde BD MAX System'da yeterli işlem doğrulama elde edilinceye kadar en azından günlük olarak çalışılmalıdır. Kontrol testinin azaltılmış sıklığı ilgili yönetmeliklere uygun olmalıdır. 3. Harici Pozitif Kontrol, önemli reaktif hatalarını izlemek üzere tasarlanmıştır. Harici Negatif Kontrol hedef nükleik asitlerle reaktif veya çevresel kontaminasyonu (veya taşımayı) saptamak üzere tasarlanmıştır. 4. Tüm analitik sürecin etkinliğini izlemek için, yerel, eyalet ve/veya federal yönetmelikler veya sertifikasyon sağlayan kurumların gereklilikleri veya kılavuz ilkelerine göre kontrol suşları test edilmelidir. 5. Kullanıcının laboratuvar kalite kontrolü programı için en uygun kontrolü seçmesini mümkün kılmak üzere çeşitli türlerde Harici Kontroller önerilir. a. Harici Negatif Kontrol: Ticari olarak temin edilebilir kontrol malzemesi [örn. Staphylococcus epidermidis suşu (ATCC 12228)] veya negatif olduğu bilinen önceden karakterize edilen örnek. BD, kontrol preparatının sonucu olarak kontaminasyon potansiyelini azaltmak için Harici Negatif Kontrol'ün Harici Pozitif Kontrol'den önce hazırlanmasını önerir. b. Harici Pozitif Kontrol: Piyasada bulunan kontrol malzemeleri [örn. referans MRSA suşu (ATCC 43300), ve metisiline duyarlı Staphylococcus aureus suşu (örn. ATCC 29213)] veya pozitif olduğu bilinen önceden karakterize edilen örnek. Harici Kontrol süspansiyonlarının hazırlanması için, izolatları salin solüsyonda 0,5 McFarland (~1 X 10 8 CFU/mL) turbiditede yeniden süspanse edin. ~1,0 X 10 4 CFU/mL nihai süspansiyon elde edecek şekilde salin içinde seri dilüsyonlar gerçekleştirin. Seyreltilmiş bakteriyel süspansiyona bir swab daldırın, fazla sıvıyı çıkarın ve swab'ı karşılık gelen Örnek Tampon Tüpüne yerleştirin. Örnek gibi işleme koyun ve test edin (Örnek Hazırlama ve BD MAX System'ın Çalışması bölümlerine bakın). 6. Tüm Harici Kontroller beklenen sonuçları vermeli (Harici Pozitif Kontrol için pozitif, Harici Negatif Kontrol için negatif) ve hiç başarısız harici kontrol olmamalıdır (Çözümlenmemiş veya Belirsiz sonuçlar). 7. Pozitif test sonucu veren bir Harici Negatif Kontrol örnek işleme ve/veya kontaminasyon olayına işaret eder. Karışma ve/veya kontaminasyondan kaçınmak için örnek işleme tekniğini gözden geçirin. Negatif sonuç veren bir Harici Pozitif Kontrol, bir örnek işleme/hazırlama sorununa işaret eder. Örnek işleme/hazırlama tekniğini gözden geçirin. 8. Çözümlenmemiş, Belirsiz veya Eksik test sonucu veren bir Harici Kontrol, bir reaktif veya BD MAX System hatasına işaret eder. BD MAX System monitörünü herhangi bir hata mesajı açısından kontrol edin. Uyarı ve hata kodlarının yorumlanması için BD MAX System Kullanıcı Kılavuzunda 11 Sistem Hata Özeti bölümüne bakın. Sorun devam ederse açılmamış bir poşetten reaktifler kullanın veya yeni bir test kiti kullanın. 9. Her Ekstraksiyon Tüpü bir sentetik hedef DNA dizisi içeren bir plazmit olan bir Örnek İşleme Kontrolü içerir. Örnek İşleme Kontrolü, örnek işleme adımları sırasında DNA yakalama, yıkama ve DNA elüsyonunun etkinliğini ve ayrıca PCR analizi sırasında amplifikasyonu ve saptamanın etkinliğini izler. Örnek İşleme Kontrolü sonucu kabul kriterlerini karşılayamazsa, örnek sonucu Çözümlenmemiş olarak rapor edilir; ancak, tüm pozitif (POS) test kiti sonuçları rapor edilir ve hiçbir hedef NEG olarak adlandırılmaz. Çözümlenmemiş bir sonuç örnekle ilişkili inhibisyonun veya reaktif hatasının bir sonucudur. Çözümlenmemiş olarak bildirilen herhangi bir örneği Tekrar Test Prosedürü bölümüne göre tekrarlayın. 6
7 SONUÇLARIN YORUMLANMASI Sonuçlar, BD MAX System monitöründe Results (Sonuçlar) penceresinde Results (Sonuçlar) sekmesinde bulunur. BD MAX System yazılımı otomatik olarak test sonuçlarını yorumlar. Bir test sonucu hedef ve Örnek İşleme Kontrolünün amplifikasyon durumu temelinde [SA NEG, MRSA NEG (negatif)], [SA POS, MRSA POS (MRSA pozitif)], [SA POS, MRSA NEG (SA pozitif)] veya [SA UNR, MRSA UNR (Çözümlenmemiş)] olarak belirtilebilir. IND (Belirsiz) veya INC (Eksik) sonuçlar BD MAX System hatasından kaynaklanır. Sonuçlar aşağıdaki karar algoritmasını temel alır (Tablo 1): Bildirilen Test Sonucu SA POS MRSA POS SA POS MRSA NEG SA NEG MRSA NEG SA UNR MRSA UNR IND INC Tablo 1: BD MAX StaphSR Assay Sonuç Yorumlama Sonucun Yorumlanması MRSA DNA saptandı SA DNA saptandı; MRSA DNA saptanmadı SA ve MRSA DNA saptanmadı Çözümlenmemiş inhibitör örnek veya reaktif hatası; hedef veya Örnek İşleme Kontrolü amplifikasyonu yok BD MAX System hatası nedeniyle belirsiz sonuç (Uyarı veya Hata Kodlarıyla a ) Eksik Çalışma (Uyarı veya Hata Kodlarıyla a ) a Uyarı ve hata kodlarının yorumlanması için BD MAX System Kullanıcı Kılavuzunun 11 Sorun Giderme bölümüne bakın. SA POS, MRSA POS (MRSA DNA saptandı) Hem MREJ (Staphylococcus aureus spesifik) hem de meca veya mecc hedefi için floresan sinyali saptanmıştır ve Nadir durumlarda MRSA'da nuc geninin olmayabileceği gösterildiğinden, nuc geni hedefi saptanabilmiş veya saptanamamış olabilir 12 ve MRSA hedef amplifikasyonu bu kontrolü devre dışı bıraktığından Örnek İşleme Kontrolü de yok sayılmaktadır. SA POS, MRSA NEG (SA DNA saptandı; MRSA DNA saptanmadı) Floresan sinyali sadece nuc geni hedefi için saptandı (SA suşunu belirtir) veya MREJ sekansının yokluğunda nuc geni ve meca veya mecc hedefi için floresan sinyali saptanmıştır (SA olmayan metisiline dirençli bakteri suşunun eş kolonizasyonuyla varlık gösteren SA suşunun bir göstergesidir) veya Floresan sinyali nuc geni ve MREJ hedefleri için saptandı (boş kaset varyantı belirtir) veya Floresan sinyali sadece MREJ hedefi için saptandı (Staphylococcus aureus boş kaset varyantını belirtir). MREJ Staphylococcus aureus türlerine spesifiktir; bu nedenle de SA suşu belirtir. Boş kaset varyantı için SA POS, MRSA NEG sonucunun elde edilmesi amacıyla nuc geninin saptanması gerekli değildir; SA hedef amplifikasyonu bu kontrolü devre dışı bıraktığından Örnek İşleme Kontrolü de yok sayılmaktadır. SA NEG, MRSA NEG (SA ve MRSA DNA saptanmadı) BD MAX StaphSR testi tarafından hiçbir hedef (nuc, meca, mecc ve MREJ hedefleri) için floresan sinyali saptanmadı ve Örnek İşleme Kontrolü için floresan sinyali saptandı veya Yalnızca meca veya mecc geni için floresan sinyali saptanmıştır [meca ve mecc genleri Staphylococcus aureus türlerine özgü değildir ve diğer bakteri cinslerinde (örn. Staphylococcus epidermidis) bulunabilir]. SA UNR, MRSA UNR (Çözümlenmemiş sonuç) Floresan sinyali nuc geni, meca, mecc veya MREJ hedefleri için saptanmadı ve Floresan sinyali Örnek İşleme Kontrolü için saptanmadı (İnhibitör örnek veya reaktif hatası). IND (Belirsiz sonuç) Uyarı veya Hata Kodlarıyla BD MAX System hatası. Uyarı ve hata kodlarının yorumlanması için BD MAX System Kullanıcı Kılavuzunda 11 Sorun Giderme bölümüne bakın. INC (Eksik çalışma) Uyarı veya Hata Kodlarıyla BD MAX System hatası. Uyarı ve hata kodlarının yorumlanması için BD MAX System Kullanıcı Kılavuzunda 11 Sorun Giderme bölümüne bakın. TEKRAR TEST PROSEDÜRÜ NOT: BD MAX System'daki Örnek Tampon Tüpü'nde yalnızca tek bir tekrar testine yetecek hacim bulunmaktadır. 25 ± 2 C sıcaklıkta saklanan Örnek Tampon Tüpleri için yukarıda bulunan Örnek Hazırlama bölümündeki adımlardan sonraki 36 saat içerisinde gerçekleştirilmelidir. Farklı olarak, 2 8 C sıcaklıkta saklanan Örnek Tampon Tüpleri için yukarıda bulunan Örnek Hazırlama bölümündeki adımlardan sonraki 120 saat (5 gün) içerisinde yapılmalıdır. NOT: Yeni örnekler tekrar örneklerle aynı çalışmada test edilebilir. 7
8 ÇÖZÜMLENMEMİŞ SONUÇ Çözümlenmemiş sonuçlar, örnekle ilişkili inhibitör madde veya reaktif hatası, uygun hedef veya Örnek İşleme Kontrolü amplifikasyonunu önlerse alınabilir. Örnekler, yukarıda tanımlanan zaman dilimlerinde ilgili Örnek Tampon Tüpleriyle tekrarlanabilir. Örnekleri bir (1) dakika boyunca vorteksleyin ve BD MAX System'ın Çalışması bölümünü izleyerek tekrar başlayın. BELİRSİZ SONUÇ Belirsiz sonuçlar, bir Sistem hatası olması durumunda alınabilir. Örnekler, yukarıda tanımlanan zaman dilimlerinde ilgili Örnek Tampon Tüpleriyle tekrarlanabilir. Örnekleri bir (1) dakika boyunca vorteksleyin ve BD MAX System'ın Çalışması bölümünü izleyerek tekrar başlayın. Uyarı veya hata kodu mesajlarının yorumlanması için BD MAX Kullanıcı Kılavuzuna 11 (Sorun Giderme bölümü) bakın. EKSİK SONUÇ Eksik sonuçlar, sonlandırma uyarısı veya hata kodu durumunda ya da Örnek Hazırlama veya PCR beklenen zaman noktalarına ulaşmadığı durumda alınabilir. Eksik sonuçlar çalışmaya veya şeride uygulanabilir. Örnekler, yukarıda tanımlanan zaman dilimlerinde ilgili Örnek Tampon Tüpleriyle tekrarlanabilir. Örnekleri bir (1) dakika boyunca vorteksleyin ve BD MAX System'ın Çalışması bölümünü izleyerek tekrar başlayın. Uyarı veya hata kodu mesajlarının yorumlanması için BD MAX Kullanıcı Kılavuzuna 11 (Sorun Giderme bölümü) bakın. HARİCİ KONTROL HATASI Harici Kontroller test edildiklerinde beklenen sonuçlar vermelidir. Örneklerin hatalı bir Harici Kontrol sonucu nedeniyle tekrarlanması gerekirse, Örnek Tampon Tüplerinden taze hazırlanmış Harici Kontroller ile birlikte yukarıda tanımlanan zaman çerçeveleri içinde tekrarlanmaları gerekir. Örnekleri bir (1) dakika boyunca vorteksleyin ve BD MAX System'ın Çalışması bölümünü izleyerek tekrar başlayın. KLİNİK ÖRNEKLERDEN KÜLTÜR ALINMASI Antimikrobiyal duyarlılık veya epidemiyolojik tip belirleme amacıyla, Örnek Hazırlama prosedürünü gerçekleştirmeden önce (Streak-Plate yöntemi kullanılarak) veya Örnek Hazırlama prosedüründen sonra (Enrichment Broth yöntemi kullanılarak) klinik örnekler toplama cihazlarından (swab) kültür alabilir. İlk PCR çalışmasından hemen sonra, swab'lar 2 8 C sıcaklıkta 36 saat, kültür alınmadan önce, hastane prosedürlerine göre Örnek Tampon Tüplerinde saklanabilir. PROSEDÜRÜN KISITLI OLDUĞU ALANLAR Bu ürün, Gerekli Fakat Sağlanmamış Ekipman ve Malzemeler bölümünde listelenin örnek toplama ve taşıma cihazları kullanılarak toplanan nazal swab örnekleriyle kullanılmak üzere tasarlanmıştır. Sıvı Amies tekli veya çiftli taşıma cihazının kullanıldığı BD MAX StaphSR testinin performansı belirlenmemiştir. Bu ürün sadece BD MAX System ile kullanılmalıdır. Yanlış test sonuçlarının nedeni uygunsuz örnek toplama, işleme veya saklama, teknik hata, örnek karışması veya örnekteki organizma sayısının testin analitik duyarlılığının altında olması olabilir. Hatalı sonuçları önlemek için prospektüs talimatı ve BD MAX System Kullanıcı Kılavuzuna 11 dikkatle uymak gereklidir. Tarama belirli bir zamanda kolonizasyon durumunu gösterir. Kolonizasyon hastanın aldığı tedavi (örn. dekolonizasyon rejimi), hastanın durumu (örn. geçici SA veya MRSA kolonizasyonu) veya yüksek riskli ortamlara maruz kalma (örn., SA veya MRSA taşıyıcısıyla temas ve/veya uzun süreli hastanede yatma) gibi durumlarla değişebilir. Kolonizasyon durumu kurumsal politikalara göre izlenmelidir. BD MAX StaphSR pozitif bir sonuç DNA varlığında devam edebileceğinden eradikasyon tedavisi başarısızlığını kesin olarak göstermez. Daha önceki bir pozitif test sonucundan sonraki negatif bir sonuç eradikasyon tedavisi başarısını gösterebilir veya aralıklı kolonizasyon nedeniyle olabilir. Pozitif bir test sonucu, mutlaka canlı organizma bulunduğu anlamına gelmez. Pozitif bir sonuç SA veya MRSA DNA varlığını gösterir. BD MAX StaphSR testi, eş zamanlı olarak SCCmec kasetinde taşınan meca veya mecc genini ve SCCmec kaseti ve orfx geni (MREJ) bileşkesinde yer alan Staphylococcus aureus spesifik sekansı saptar. BD MAX StaphSR testi Staphylococcus aureus spesifik nuc genini de saptar. BD MAX StaphSR testi, bugüne kadar BD tarafından test edilen dünya çapındaki suşların %98'den fazlasını oluşturarak, MRSA suşlarında yerleşen (farklı SSCmec/MREJ türlerine ait) meca ve mecc öğelerinin çoğunu temsil eden i, ii, iii, iv, v, vi, vii, ix, xiii, xiv ve xxi MREJ genotiplerini saptamak üzere tasarlanmıştır. BD MAX StaphSR testinin diğer MREJ genotiplerini saptama kabiliyeti bilinmemektedir. BD MAX StaphSR testi, Sınırda Oksasiline Dirençli Staphylococcus aureus'u (BORSA) MRSA olarak bildirmez (yalnızca SA olarak bildirir). BORSA suşlarındaki oksasilin direnci mekanizması meca veya mecc genine değil, artan β laktamaz üretimine bağlıdır. BORSA suşları nadir görülür. BD MAX StaphSR testinin modifiye Staphylococcus aureus'un (MOD-SA) saptanmasındaki performansı, bu suşlar değerlendirilmediğinden bilinmemektedir. MOD-SA suşundaki oksasilin direnci mekanizması, penisilini bağlayan proteinlerin oksasiline olan afinitesindeki değişiklik nedeniyledir. MOD-SA suşları nadir görülür. BD MAX StaphSR testi, metisiline dirençli koagülaz negatif Staphylococcus (MRCoNS) ve boş kaset metisiline duyarlı SA varyantı içeren eş kolonizasyon sergilemiş nazal örneğin test edilmesi esnasında yanlış bir pozitif MRSA sonucu meydana getirir. MRCoNS ve boş kaset metisiline duyarlı SA ile eş kolonizasyon görülmesi nadirdir. Tüm PCR tabanlı in vitro diyagnostik testlerde olduğu gibi testin LoD altında çok düşük hedef düzeyleri saptanabilir ama sonuçlar tekrar edilemeyebilir. Tobramisin BD MAX StaphSR testinde inhibisyona neden olabilir (Daha fazla ayrıntı için İnterferans Yapan Maddeler bölümüne bakın). 8
9 Yanlış negatif sonuçlar örneklerin yetersiz toplanması, taşınması veya saklanması sonucunda nükleik asit kaybı veya yetersiz bakteriyel hücre lizisi nedeniyle oluşabilir. Örnek İşleme Kontrolü teste PCR amplifikasyonu inhibitörleri içeren örneklerin tanımlanmasına yardımcı olmak üzere, bir bütün halinde reaktif entegrasyonu ve test sisteminin kontrolü olarak eklenmiştir. Örnek İşleme Kontrolü nükleik asidin örneklerin yetersiz toplanması, taşınması veya saklanması nedeniyle kaybedilip kaybedilmediğini veya bakteriyel hücrelerin yetersiz lizise uğrayıp uğramadığını belirtmez. Karma bir kültürde yüksek konsantrasyonlarda MRSE bulunduğunda, MRSA veya SA'nın saptanması değişkenlik gösterir. MRSE rekabeti 1: 1 x 10 2 lik MRSA:MRSE oranında ve 1: 1 x 10 5 lik SA:MRSE oranında gözlenmiştir. Karma bir kültürde yüksek konsantrasyonlarda MSSA bulunduğunda, MRSA'nın saptanması değişkenlik gösterir. MSSA rekabeti 1: 1 x 10 3 lük MRSA:MSSA oranında gözlenmiştir. BD MAX StaphSR testi sonuçları bazen geçersiz örnek işleme kontrolü nedeniyle çözümlenmemiş olabilir veya cihaz arızası nedeniyle belirsiz veya eksik olabilir ve son sonuçların elde edilmesinde gecikmeye neden olabilecek şekilde tekrar test yapılmasını gerektirebilir. Primer veya prob bağlayıcı bölgelerdeki mutasyonlar veya polimorfizmler yeni veya bilinmeyen MRSA veya SA varyantlarının saptanmasını etkileyebilir ve BD MAX StaphSR testi ile yanlış negatif bir sonuç verebilir. Tüm in vitro diyagnostik testlerde olduğu gibi pozitif ve negatif prediktif değerler prevalansa yüksek ölçüde bağlıdır. BD MAX StaphSR testi performansı prevalansa ve test edilen popülasyona göre değişebilir. BD MAX StaphSR testi için BD MAX System'a ait dört (4) optik kanalın kullanılması gerekir; FAM kanalı ( nm), ROX kanalı ( nm), VIC kanalı (530/565 nm) ve Cy5.5 kanalı (680/715 nm). Kalan optik kanalın performansını bu test gerçekleştirmez. BEKLENEN DEĞERLER BD MAX StaphSR testi klinik çalışmasında, örnek ve PCR düzeylerinde uyumlu örneklerden, 3 farklı coğrafi bölgede bildirilebilir toplam sonuç elde edilmiş ve Doğrudan ve Zenginleştirilmiş kültür ile karşılaştırılmıştır. Çalışma popülasyonu yatan hasta ve ayakta tedavi edilen hasta kategorileri şeklinde gruplandırılmıştır. BD MAX StaphSR testi ile belirlendiği şekliyle pozitif vakaların sayısı ve yüzdesi Tablo 2'de sunulmuştur. Tablo 2: Hasta Grubuna göre Uyumlu Klinik Deney Katılım Özeti Grup Toplam Örnek Sayısı a Pozitif MRSA Sayısı Pozitif SA Sayısı Yatan Hasta Ayakta Tedavi Edilen Hasta Toplam a a Uyumlu PCR sonuçlarına göre toplam örnek sayısı. Pozitif MRSA Yüzdesi %10,2 (172/1.683) %3,9 (28/710) %8,4 (200/2.393) Pozitif SA Yüzdesi %32,4 (545/1.683) %25,6 (182/710) %30,4 (727/2.393) PERFORMANS ÖZELLİKLERİ Klinik Performans BD MAX StaphSR testinin klinik performans özellikleri çok merkezli (3) bir prospektif araştırma çalışmasında belirlenmiştir. Çalışmaya üç (3) araştırma merkezi katılmıştır. Çalışmaya katılmak için hastaların, kurum politikaları doğrultusunda MRSA veya SA testlerine uygun olmaları gerekmiştir. Klinik tesis politikalarına göre hedeflenmiş tarama için uygunluk gereklilikleri arasında verilenlerle sınırlı olmamak üzere şunlar vardı: sağlık hizmeti veren belirli bir sisteme kabul edilen hastalar; Yoğun Bakım Ünitesine kabul edilen hastalar; Yoğun Bakım Ünitesine aktarılan hastalar; elektif cerrahi öncesindeki hastalar ve uzun dönemli bakım tesislerinden kabul edilen hastalar. Çalışmaya önceden kayıtlı hastalara ait örnekler dahil edilmemiştir. Karşılaştırmalı Referans Yöntem doğrudan kültürden oluşur zenginleştirilmiş kültürle tamamlanır. Zenginleştirilmiş kültür analizi, doğrudan kültürle MRSA veya SA ile ilgili negatif olan tüm örnekler için tamamlanmıştır. Kanlı Agarda (BA) alt kültür oluşturmuş selektif (Staphylococcus aureus) kromojenik ortamda varsayılan Staphylococcus aureus kolonileri gözlemlendi. Tanımlama bir aglütasyon testi ile yapılırken metisilin direnci Sefoksitin diski (30 μg) difüzyon duyarlılık testiyle doğrulandı. MRSA veya SA başlangıç yöntemiyle doğrulanmadığında %6,5 NaCl ile Trypticase Soy Broth (%6,5 NaCl ile TSB) içinde zenginleştirme uygulandı. Turbid TSB %6,5 NaCl soya, ek kromojenik ortam ve Kanlı Agar plaklarını inoküle etmek için kullanıldı; MRSA doğrulaması yukarıda tanımlandığı şekilde yapıldı. BD MAX StaphSR Assay ile Elde Edilen ve Referans Yöntemle Karşılaştırmalı Sonuçlar Çalışmaya toplamda örnek kaydedilmiştir. Bunlardan 94 örnek, protokol kriterlerine göre uyumsuz olarak kabul edilmiş ve tam uyumlu dört (4) öde bildirilemeyen nihai PCR sonuçları elde edilmiştir. BD MAX StaphSR testinin Referans Yöntemle karşılaştırmalı klinik performansının belirlenmesinde toplam örnek sonucu kullanılmıştır (Tablo 3-6). Referans Yöntemiyle (Doğrudan/Zenginleştirilmiş kültür) karşılaştırıldığında BD MAX StaphSR testi MRSA'nın %93,1'ini pozitif örnek, MRSA'nın %97,8'ini de negatif örnek olarak tanımlamıştır (Tablo 3 ve 4). Test edilen popülasyon için bu durum %99,5 Negatif Prediktif Değer (NPV), %75,5 Pozitif Prediktif Değere (PPV) karşılık gelmektedir. 9
10 Tablo 3: BD MAX StaphSR Assay ile MRSA İçin Elde Edilen Sonuçların Referans Yöntemle Karşılaştırılması Tüm Tesisler Referans Yöntem MRSA Pozitif Negatif Toplam Pozitif a 197 BD MAX StaphSR Assay Negatif 11 a Toplam Duyarlılık: %93,1 (149/160) (%95 CI: %88,1, %96,1) Özgüllük: %97,8 (2.145/2.193) (%95 CI: %97,1, %98,3) PPV: %75,5 (%95 CI: %70,0, %80,5) NPV: %99,5 (%95 CI: %99,1, %99,7) a Referans Yöntem ve BD MAX StaphSR testi arasında, diskordan sonuçları olan örneklerde daha fazla araştırma yapılmıştır. Referans Yöntemin tekrarlanmasından sonra, 48 MRSA Yanlış Pozitif BD MAX StaphSR örneğinden 11 tanesinin de pozitif olduğu anlaşılmıştır. Referans Yöntemin tekrarlanmasından sonra, 11 MRSA Yanlış Negatif BD MAX StaphSR örneğinden 5 tanesinin de negatif olduğu anlaşılmıştır. Tablo 4: BD MAX StaphSR Assay ile MRSA için Elde Edilen ve Referans Yöntem Karşılaştırmalı Tesis Performansları Klinik Tesisler Prevalans a Duyarlılık (%95 CI) b Özgüllük (%95 CI) b Tesis 1 %4,3 (41/960) Tesis 2 %5,8 (38/650) Tesis 3 %10,6 (81/765) Genel %6,7 (160/2.375 c ) a Yalnızca referans yönteme dayalı prevalans b Güven aralığı c örnek referans yöntemle uyumludur %92,7 (38/41) (%80,6, %97,5) %86,8 (33/38) (%72,7, %94,2) %96,3 (78/81) (%89,7, %98,7) %93,1 (149/160) (%88,1, %96,1) %99,0 (909/918) (%98,1, %99,5) %98,6 (584/592) (%97,4, %99,3) %95,5 (652/683) (%93,6, %96,8) %97,8 (2.145/2.193) (%97,1, %98,3) Referans Yöntemle (Doğrudan/Zenginleştirilmiş kültür) karşılaştırıldığında BD MAX StaphSR testi SA'nın %92,0'ını pozitif örnek, SA'nın %93,2'sini de negatif örnek olarak tanımlamıştır (Tablo 5 ve 6). Test edilen popülasyon için bu durum %96,9 NPV ve %83,8 PPV karşılık gelmektedir. Tablo 5: BD MAX StaphSR Assay ile SA İçin Elde Edilen Sonuçların Referans Yöntemle Karşılaştırılması Tüm Tesisler BD MAX StaphSR Assay Referans Yöntem SA Pozitif Negatif Toplam Pozitif a 714 Negatif 52 a Toplam Duyarlılık: %92,0 (599/651) (%95 CI: %89,7, %93,9) Özgüllük: %93,2 (1.587/1.702) (%95 CI: %92,0, %94,3) PPV: %83,8 (%95 CI: %81,3, %86,1) NPV: %96,9 (%95 CI: %96,0, %97,6) a Referans Yöntem ve BD MAX StaphSR testi arasında, diskordan sonuçları olan örneklerde daha fazla araştırma yapılmıştır. Referans Yöntemin tekrarlanmasından sonra, 115 SA Yanlış Pozitif BD MAX StaphSR örneğinden 28 tanesinin de pozitif olduğu anlaşılmıştır. Referans Yöntemin tekrarlanmasından sonra, 52 SA Yanlış Negatif BD MAX StaphSR örneğinden 23 tanesinin de negatif olduğu anlaşılmıştır Tablo 6: BD MAX StaphSR Assay ile SA için Elde Edilen ve Referans Yöntem Karşılaştırmalı Tesis Performansları Klinik Tesisler Prevalans a %95 CI ile duyarlılık b %95 CI ile özgüllük b Tesis 1 %27,2 (261/960) Tesis 2 %27,5 (179/650) Tesis 3 %27,8 (213/765) Genel %27,5 (653/2.375 c ) a Yalnızca referans yönteme dayalı prevalans b Güven aralığı c örnek referans yöntemle uyumludur %90,0 (235/261) (%85,8, %93,1) %91,5 (162/177) (%86,5, %94,8) %94,8 (202/213) (%91,0, %97,1) %92,0 (599/561) (%89,7, %93,9) %96,3 (672/698) (%94,6, %97,4) %90,9 (412/453) (%88,0, %93,3) %91,3 (503/551) (%88,6, %93,4) %93,2 (1.587/1.702) (%92,0, %94,3) 10
11 BD MAX StaphSR Assay ile Elde Edilen Sonuçların Doğrudan Kültürle Karşılaştırılması Çalışmaya toplamda örnek kaydedilmiştir. Bunlardan 54 örnek, protokol kriterlerine göre uyumsuz olarak kabul edilmiş ve tam uyumlu altı (6) örnekte bildirilemeyen nihai PCR sonuçları elde edilmiştir. BD MAX StaphSR testinin Doğrudan Kültürle karşılaştırmalı pozitif ve negatif yüzde benzerliğinin belirlenmesinde toplam örnek sonucu kullanılmıştır (Tablo 7 10). Doğrudan Kültürle karşılaştırıldığında, BD MAX StaphSR testinde MRSA pozitif örneklerin %96,5'i ve MRSA negatif örneklerin %97,2'si tanımlanmıştır (Tablo 7 ve 8). Tablo 7: BD MAX StaphSR Assay ile MRSA İçin Elde Edilen Sonuçların Doğrudan Kültürle Karşılaştırılması Tüm Tesisler Doğrudan Kültür Pozitif Negatif Toplam Pozitif BD MAX StaphSR Negatif Toplam Pozitif Yüzde Benzerlik: %96,5 (137/142) (%95 CI: %92,0, %98,5) Negatif Yüzde Benzerlik: %97,2 (2.186/2.249) (%95 CI: %96,4, %97,8) Tablo 8: BD MAX StaphSR Assay ile MRSA için Elde Edilen ve Doğrudan Kültür Karşılaştırmalı Tesis Performansları Klinik Tesisler %95 CI'ya sahip Pozitif Yüzde Benzerlik a %95 CI'ya sahip Negatif Yüzde Benzerlik a Tesis 1 Tesis 2 Tesis 3 Genel a Güven aralığı %100 (35/35) (%90,1, %100) %93,5 (29/31) (%79,3, %98,2) %96,1 (73/76) (%89,0, %98,6) %96,5 (137/142) (%92,0, %98,5) %98,7 (912/924) (%97,7, %99,3) %98,0 (587/599) (%96,5, %98,9) %94.6 (687/726) (%92,7, %96,0) %97,2 (2.186/2.249) (%96,4, %97,8) Doğrudan Kültürle karşılaştırıldığında, BD MAX StaphSR testinde SA pozitif örneklerin %95,1'i ve SA negatif örneklerin %91'u tanımlanmıştır (Tablo 9 ve 10). Tablo 9: BD MAX StaphSR Assay ile SA İçin Elde Edilen Sonuçların Doğrudan Kültürle Karşılaştırılması Tüm Tesisler Doğrudan Kültür Pozitif Negatif Toplam Pozitif BD MAX StaphSR Negatif Toplam Pozitif Yüzde Benzerlik: %95,1 (564/593) (%95 CI: %93,1, %96,6) Negatif Yüzde Benzerlik: %91,0 (1.637/1.798) (%95 CI: %89,6, %92,3) Tablo 10: BD MAX StaphSR Assay ile SA için Elde Edilen ve Doğrudan Kültür Karşılaştırmalı Tesis Performansları a Güven aralığı Klinik Tesisler %95 CI'ya sahip Pozitif Yüzde Benzerlik a %95 CI'ya sahip Negatif Yüzde Benzerlik a Tesis 1 Tesis 2 Tesis 3 Genel %93,0 (213/229) (%89,0, %95,7) %94,9 (149/157) (%90,3, %97,4) %97,6 (202/207) (%94,5, %99,0) %95,1 (564/593) (%93,1, %96,6) %93,4 (682/730) (%91,4, %95,0) %88,6 (419/473) (%85,4, %91,1) %90,1 (536/595) (%87,4, %92,2) %91,0 (1.637/1.798) (%89,6, %92,3) BD MAX StaphSR testi ile test edilen, örnek ve PCR düzeyinde uyumlu nazal swab örneğinden 17'si (%0,7) ilk testin sonunda Çözümlenmemiş olarak bildirilmiştir. Tekrarlanan testin sonunda Çözümlenmemiş Oranı %0,1'dir (3/2.399) (Tablo 11). Tablo 11: Çözümlenmemiş Oranlar Başlangıçta Çözümlenmemiş Oranlar %0,7 (17/2.399) a (%95 CI: %0,4, %1,1) a Uyumlu örnekler ve BD MAX StaphSR testi sonuçlarına göre toplam sayı Tekrar Sonrasında Çözümlenmemiş Oranlar %0,1 (3/2.399) (%95 CI: %0, %0,4) 11
12 BD MAX StaphSR testi ile test edilen aynı nazal swab örneğinden 14'ü (%0,6) başlangıçta Belirsiz olarak bildirilmiştir. Tekrar sonrası hiçbir sonuç Belirsiz olarak kalmamıştır (iki örnek tekrar test edilmemiştir). Sekiz (8) örnek (%0,3) başlangıçta Eksik olarak bildirilmiştir. Tekrar sonrası hiçbir sonuç Eksik olarak kalmamıştır (tek bir örnek tekrar test edilmemiştir). Boş Kaset Varyantları Bir örneğin BD MAX StaphSR testi ile MRSA pozitif olarak tanımlanması için, hem MREJ hem de meca veya mecc için pozitif sonuç elde edilmesi gereklidir (nuc geni zorunlu değildir). MREJ taşıyan ancak meca veya mecc geni taşımayan bir örnek metisiline duyarlı olamayacağından MRSA negatiftir. Bu durum, mecaveya mecc geni SCCmec kasetinden çıkarıldığında meydana gelir ancak sağ uç fragman (MREJ) kalır ve pozitif MREJ sonucu verir. Bu örnek türü bazen boş kaset varyantı olarak adlandırılır. meca ve mecc genlerini saptama kabiliyeti BD MAX StaphSR testinin bu varyantı SA POS; MRSA NEG olarak doğru bir şekilde ayrıştırıp tanımlamasına olanak sağlar. Klinik performans belirleme işlemine dahil edilen uygun öden (Tablo 3) toplam 10 tanesi boş kaset profiline uymakta ve bu örnekler sayesinde meca veya mecc gen saptaması olmaksızın MREJ saptanabilmektedir. 10 örneğin tümünün Referans Yönteme göre gerçek negatif MRSA ve gerçek pozitif SA oldukları doğrulanmıştır. Analitik Duyarlılık BD MAX StaphSR testi için analitik duyarlılık (Saptama Sınırı veya LoD) şu şekilde saptanmıştır: pozitif örnekler, kültürlerden hazırlanan ve miktarları kültürlerden belirlenen çok çeşitli MRSA veya MSSA bakteri süspansiyonlarına swab'ların batırılmasıyla hazırlanmıştır. Test edilen suşlar, 5 SCCmec türüne (I, II, III, IV ve XI) karşılık gelen 11 MREJ genotipini (i, ii, iii, iv, v, vi, vii, ix, xiii, xiv ve xxi) temsil eden 11 MRSA suşu ile 2 MSSA suşudur. Swab'lar daha sonra simüle nazal matrikse yerleştirilmiştir. Her bir MRSA ve MSSA suşu, 3 farklı BD MAX StaphSR testi üretim lotunu kullanan 2 farklı operatör tarafından konsantrasyon başına 24 replikat olacak şekilde test edilmiştir. Tüm replikatların en az %95'inin pozitif çıktığı en düşük konsantrasyon olarak tanımlanan analitik duyarlılık (LoD), MRSA suşlarının saptanmasında 71 ila 454 CFU/swab aralığında (Tablo 12) ve MSSA suşlarının saptanmasında 174 ila 211 CFU/swab aralığında (Tablo 13) değişkenlik göstermiştir. Tablo 12: BD MAX StaphSR Assay ile MRSA Genotiplerini Saptama Sınırı MRSA Suşu MREJ Genotipi SCCmec türü a LoD Konsantrasyonu [CFU/swab (%95 Cl b )] 1 Tür i I 91 (55, 150) 2 Tür ii II 110 (68, 176) 3 Tür iii III 181 (102, 322) 4 Tür iv III 81 (48, 136) 5 Tür v IV 128 (74, 224) 6 Tür vi ND c 454 (246, 839) 7 Tür vii II 269 (134, 538) 8 Tür ix ND c 199 (111, 356) 9 Tür xiii ND c 71 (41, 121) 10 Tür xiv ND c 96 (57, 163) 11 Tür xxi d XI 108 (64, 183) a SCCmec türü, iki farklı tipleme yöntemi olduklarından MREJ türüyle ilişkili değildir. b Cl: Güven Aralıkları c ND = belirlenmedi d mecc içeren MRSA suşları (meca LGA251 suşu olarak da bilinir) Tablo 13: BD MAX StaphSR Assay ile MSSA Saptama Sınırı a Cl: Güven Aralıkları MSSA Suşu LoD Konsantrasyonu [CFU/swab (%95 Cl a )] (88, 346) (104, 429) Analitik Dahil Olma Analitik dahil etme çalışması, bir dizi MRSA ve MSSA suşları kullanılarak, coğrafi çıkışı, MREJ genotipi (vahşi tür ve mutant), SCCmec türü, Puls Alan Jel Elektroforezi (PFGE) türü, temporal çeşitlilik ve duyarlılık paterni dikkate alınarak gerçekleştirilmiştir. Bu çalışmada kamu koleksiyonlarından ve iyi karakterize edilmiş klinik izolatlardan örnek Vankomisine Dirençli Staphylococcus aureus (VRSA) ve Vankomisin Ara Staphylococcus aureus (VISA) suşları dahil olmak üzere 27 ülkeden yetmiş yedi (77) suş ve 16 ülkeden 51 MSSA suşu dahil edilmiştir. BD MAX StaphSR testinde, düşük bakteri yükünde (2 3 x LoD) test etme durumunda i, ii, iii, iv, v, vi, vii, ix, xiii, xiv ve xxi MREJ türleri saptanmıştır. BD MAX StaphSR testi I, II, III, IV, V, VI, VII, VIII ve XI MRSA SCCmec türleri ve 2 3 x LoD'da 100 ila 800, ve MRSA PFGE tipleri USA saptamıştır. Vankomisine ek direnç gösteren tüm MRSA suşları da (VRSA ve VISA) saptanmıştır. BD MAX StaphSR testi, test edilmiş meca boş kaset varyantları da dahil 51 MSSA suşunun tümünü saptamıştır. 12
13 İyi Karakterize Edilmiş bir Karşılaştırma Suşu Panelinin Değerlendirilmesi İyi karakterize edilmiş karşılaştırma suşu panelini kullanarak BD MAX StaphSR testinin analitik performansını değerlendirmek için ek bir analitik çalışma gerçekleştirilmiştir: 2 3 x LoD konsantrasyonunda test edilen PFGE tipleri USA 100 to 800, 1.000, PFGE tipi IV/IBERIAN ve mecc varyantı da (meca içeren Staphylococcus aureus suşu LGA251) dahil yüksek ve düşük oksasilin minimum inhibitör konsantrasyonlarıyla (MIC) 17 MRSA suşunun on yedisi (17) SA POS, MRSA POS sonuçlarını göstermiştir CFU/swab'da test edilen 4 BORSA suşunun (Sınırda Oksasiline Dirençli Staphylococcus aureus) dördü (4) SA POS, MRSA NEG sonuçlarını göstermiştir CFU/swab'da test edilen 5 MSSA suşunun beşi (5) SA POS, MRSA NEG sonuçlarını göstermiştir CFU/swab'da test edilen 1 Metisiline Dirençli Staphylococcus epidermidis (MRSE) suşunun biri (1) negatif bir sonuç (SA NEG, MRSA NEG) göstermiştir. Analitik Özgüllük BD MAX StaphSR testi, MRSA ve SA saptamaları amacıyla testin özgüllüğünü belirtmek için BD MAX System'ı kullanarak hedef olmayan organizmaların ve MSSA suşlarının üst düzeyini kapsayan örneklerde gerçekleştirilmiştir CFU/swab'daki 15 boş kaset varyantı MSSA suşunun on beşi (15) SA POS, MRSA NEG sonuçlarını vermiştir CFU/mL (3x10 5 CFU/swab'da test edilen Cryptococcus neoformans hariç) konsantrasyonda test edilen stafilokoksik olmayan çeşitli türlere ait 57 suşun elli yedisi (57) negatif sonuçlar (SA NEG, MRSA NEG) vermiştir. 28 türü temsil eden kırk beş (45) Koagülaz Negatif stafilokoksik suşu (CoNS) ve Koagülaz Pozitif stafilokoksik suşu (CoPS) BD MAX StaphSR testi ile 0,5 McFarland konsantrasyonunda test edilmiştir. Test edilen 45 suşun kırk beşi (45) negatif sonuçlar (SA NEG, MRSA NEG) göstermiştir CFU/swab'daki yüksek konsantrasyonda test edilen 50 MSSA suşunun ellisi (50) SA POS, MRSA NEG sonuçlarını vermiştir. 12 farklı viral türde temsil edilen on yedi (17) virüs 10 5 PFU/mL'de test edilmiştir. 17 virüsün hepsi negatif sonuçlar (SA NEG, MRSA NEG) vermiştir. İnterferans Yapan Maddeler Burun deliklerinde kullanılabilen veya nazal swab örneklerinde bulunan yirmi dokuz (29) mikroorganizma ve kimyasal madde, BD MAX StaphSR testi ile olası bir interferans bakımından değerlendirilmiştir (Tablo 14). 2 3 x LoD'deki MRSA negatif örnek ve MRSA pozitif örnekler, örnek alma bölgesi veya nazal swab örneğinde bulunması olası her bir bileşik veya mikroorganizmanın en yüksek miktarı ile test edilmiştir. Sonuçlarda, 4,5 x 10-3 g/swab konsantrasyonunda test edildiğinde BD MAX StaphSR testinde inhibisyon sergileyen Tobramisin dışında, mikroorganizmalar veya kimyasal maddelerle bildirilebilecek bir interferans olmadığı görülmüştür. Tablo 14: BD MAX StaphSR Assay ile Test Edilen Endojen ve Eksojen Maddeler Madde Sonuç a Madde Sonuç a Müsin, sığır çene altı bezlerinden NI Rhinocort aqua* NI Deksametazon Sodyum Fosfat Oftalmik Solüsyon Zicam* Damlamayan Sıvı* Nazal NI USP, %0,1 Deksametazon Fosfat Eşdeğeri Jel* Uç Konjesyon Tahliyesi* NI Chloraseptic* NI Flutikazon Propiyonat NI Taro-Mupirocin, Mupirocin Merhem USP, %2 NI Luffeel* NI Dayanıklı Dristan* Nazal Buhar NI Staphylococcus epidermidis NI Neo-Synephrine* NI Micrococcus luteus NI Equate* Nazal Sprey Dekonjestan NI Enterococcus faecium NI Beconase AQ* NI Enterococcus faecalis NI Flunisolid Nazal Solüsyon USP, %0,025 NI Escherichia coli NI Nasacort* AQ NI Corynebacterium flavescens NI Nasonex* NI Moraxella catarrhalis NI Relenza* NI Staphylococcus hominis subsp hominis NI Tobramisin I Haemophilus influenzae NI Kan NI Streptococcus pneumoniae NI Flumist* NI a NI: BD MAX StaphSR testi ile bildirilebilir interferans yoktur. I: BD MAX StaphSR testi ile bildirilebilir interferans. Mikrobiyal Kompetitif İnhibitör Etki Potansiyel mikrobiyal inhibitör etki aşağıdakilerle değerlendirilmiştir: düşük konsantrasyondaki (1 2 x LoD) MRSA veya MSSA ile eş zamanlı olarak verildiğinde artan MRSE konsantrasyonu ve düşük konsantrasyondaki (1 2 x LoD) MRSA ile eş zamanlı olarak verildiğinde artan MSSA konsantrasyonu. Sonuçlar: 1: 1 x 10 2 lik MRSA:MRSE oranında MRSE rekabetini göstermiştir. 1: 1 x 10 5 lik MSSA:MRSE oranında MRSE rekabetini göstermiştir. 1: 1 x 10 3 lük MRSA:MSSA oranında MSSA rekabetini göstermiştir. 13
In Vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir Türkçe 4 U I
 MAX MRSA XT 443461 In Vitro Diyagnostik Kullanım İçindir P0205(01) BD MAX System ile kullanım içindir 2016-06 Türkçe 4 U I KULLANIM AMACI BD MAX System'da gerçekleştirilen BD MAX MRSA XT testi, nazal kolonizasyon
MAX MRSA XT 443461 In Vitro Diyagnostik Kullanım İçindir P0205(01) BD MAX System ile kullanım içindir 2016-06 Türkçe 4 U I KULLANIM AMACI BD MAX System'da gerçekleştirilen BD MAX MRSA XT testi, nazal kolonizasyon
BD GeneOhm MRSA ACP Lizis Kiti
 REF 441638 100 Test P0071(03) _TR Tarih: 2014-09 İÇİNDEKİLER KULLANIM AMACI... 3 İŞLEMİN ÖZETİ VE AÇIKLAMASI... 3 AYIRAÇLAR... 3 ÖNLEMLER... 3 SAĞLANAN MATERYALLER... 4 SAKLAMA, MUAMELE VE STABİLİTE...
REF 441638 100 Test P0071(03) _TR Tarih: 2014-09 İÇİNDEKİLER KULLANIM AMACI... 3 İŞLEMİN ÖZETİ VE AÇIKLAMASI... 3 AYIRAÇLAR... 3 ÖNLEMLER... 3 SAĞLANAN MATERYALLER... 4 SAKLAMA, MUAMELE VE STABİLİTE...
BD GeneOhm MRSA ACP Testi Amplifikasyon Kiti
 Testi Amplifikasyon Kiti REF 441637 REF 441639 48 Test 200 Test P0057(02)_TR Tarih : 2014-09 P0057(02)_TR - 2 - İÇİNDEKİLER TÜRKÇE... 4 KULLANIM AMACI... 4 ÖZET VE AÇIKLAMA... 4 İŞLEMİN PRENSİBİ... 4 AYIRAÇLAR...
Testi Amplifikasyon Kiti REF 441637 REF 441639 48 Test 200 Test P0057(02)_TR Tarih : 2014-09 P0057(02)_TR - 2 - İÇİNDEKİLER TÜRKÇE... 4 KULLANIM AMACI... 4 ÖZET VE AÇIKLAMA... 4 İŞLEMİN PRENSİBİ... 4 AYIRAÇLAR...
RTA DNA qpcr Probe Master Mix
 RTA DNA qpcr Probe Master Mix Kullanma Kılavuzu Yayın Tarihi -- 2012-01 DNA'nın gerçek zamanlı tayini ve miktar ölçümü için Yalnızca profesyonel kullanım için REF 09030025 25 test 09030100 100 test 09030500
RTA DNA qpcr Probe Master Mix Kullanma Kılavuzu Yayın Tarihi -- 2012-01 DNA'nın gerçek zamanlı tayini ve miktar ölçümü için Yalnızca profesyonel kullanım için REF 09030025 25 test 09030100 100 test 09030500
BD MAX MRSA assay
 BD MAX MRSA assay 442953 Sadece İn vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir P0133(06) 2014-11 Türkçe KULLANIM AMACI BD MAX System'de (BD MAX Sistemi) gerçekleştirilen BD MAX
BD MAX MRSA assay 442953 Sadece İn vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir P0133(06) 2014-11 Türkçe KULLANIM AMACI BD MAX System'de (BD MAX Sistemi) gerçekleştirilen BD MAX
MAX Extended Enteric Bacterial Panel
 MAX Extended Enteric Bacterial Panel 443812 In Vitro Diyagnostik Kullanım İçindir P0221(02) BD MAX System ile kullanım içindir 2017-06 Türkçe 4 I KULLANIM AMACI BD MAX System'da gerçekleştirilen BD MAX
MAX Extended Enteric Bacterial Panel 443812 In Vitro Diyagnostik Kullanım İçindir P0221(02) BD MAX System ile kullanım içindir 2017-06 Türkçe 4 I KULLANIM AMACI BD MAX System'da gerçekleştirilen BD MAX
BD MAX Enteric Parasite Panel 442960 In Vitro Diyagnostik Kullanım İçindir BD MAX Sistemi ile kullanım içindir
 BD MAX Enteric Parasite Panel 442960 In Vitro Diyagnostik Kullanım İçindir BD MAX Sistemi ile kullanım içindir P0195(04) 2015-04 Türkçe KULLANIM AMACI BD MAX Sistemi üzerinde gerçekleştirilen BD MAX Enteric
BD MAX Enteric Parasite Panel 442960 In Vitro Diyagnostik Kullanım İçindir BD MAX Sistemi ile kullanım içindir P0195(04) 2015-04 Türkçe KULLANIM AMACI BD MAX Sistemi üzerinde gerçekleştirilen BD MAX Enteric
BD MAX CT/GC 442969 Sadece İn Vitro Diagnostik Kullanım İçindir.
 BD MAX CT/GC 442969 Sadece İn Vitro Diagnostik Kullanım İçindir. P0039(01) BD MAX System ile kullanılmak için tasarlanmıştır 2014-12 Türkçe 0086 KULLAM AMACI BD MAX CT/GC testi BD MAX System üzerinde uygulandığı
BD MAX CT/GC 442969 Sadece İn Vitro Diagnostik Kullanım İçindir. P0039(01) BD MAX System ile kullanılmak için tasarlanmıştır 2014-12 Türkçe 0086 KULLAM AMACI BD MAX CT/GC testi BD MAX System üzerinde uygulandığı
Sadece İn vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir Türkçe 4 I
 MAX MRSA 442953 Sadece İn vitro Diyagnostik Kullanım İçindir P0133(07) BD MAX System ile kullanım içindir 2016-10 Türkçe 4 I KULLANIM AMACI BD MAX System de (BD MAX Sistemi) gerçekleştirilen BD MAX MRSA
MAX MRSA 442953 Sadece İn vitro Diyagnostik Kullanım İçindir P0133(07) BD MAX System ile kullanım içindir 2016-10 Türkçe 4 I KULLANIM AMACI BD MAX System de (BD MAX Sistemi) gerçekleştirilen BD MAX MRSA
Değişiklik Geçmişi MAX MDR-TB P0228(04) Türkçe. Revizyon Bölümler Değişiklik Özeti
 MAX MDR-TB 443878 P0228(04) 2018-08 Türkçe Değişiklik Geçmişi Revizyon Bölümler Değişiklik Özeti 02 Tümü Basılı ambalaj ekini elektronik ambalaj ekine çevirin. 03 İçindekiler İçindekiler ekle Tablo 3 ve
MAX MDR-TB 443878 P0228(04) 2018-08 Türkçe Değişiklik Geçmişi Revizyon Bölümler Değişiklik Özeti 02 Tümü Basılı ambalaj ekini elektronik ambalaj ekine çevirin. 03 İçindekiler İçindekiler ekle Tablo 3 ve
RTA JEL / PZR Saflaştırma Kiti
 RTA JEL / PZR Saflaştırma Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 DNA parçalarının agaroz jelden geri kazanımı ve PZR ürünlerinin saflaştırılması için Yalnızca profesyonel kullanım için REF 09009050
RTA JEL / PZR Saflaştırma Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 DNA parçalarının agaroz jelden geri kazanımı ve PZR ürünlerinin saflaştırılması için Yalnızca profesyonel kullanım için REF 09009050
MAX Enteric Parasite Panel
 MAX Enteric Parasite Panel 442960 In Vitro Diyagnostik Kullanım İçindir P0219(01) BD MAX Sistemi ile kullanım içindir 2016-05 Türkçe 4 I KULLANIM AMACI BD MAX Sistemi üzerinde gerçekleştirilen BD MAX Enteric
MAX Enteric Parasite Panel 442960 In Vitro Diyagnostik Kullanım İçindir P0219(01) BD MAX Sistemi ile kullanım içindir 2016-05 Türkçe 4 I KULLANIM AMACI BD MAX Sistemi üzerinde gerçekleştirilen BD MAX Enteric
BD GeneOhm MRSA Testi
 REF 441242 REF 441244 200 Test 48 Test DOPS03-09-V3TR2 Türkçe Tarih: 2009-02 İçindekiler Türkçe Kullanım amacı ---------------------------------------------------------------------------------------------------------
REF 441242 REF 441244 200 Test 48 Test DOPS03-09-V3TR2 Türkçe Tarih: 2009-02 İçindekiler Türkçe Kullanım amacı ---------------------------------------------------------------------------------------------------------
BD GeneOhm StaphSR testi
 testi REF 441253 REF 441252 200 Test 48 Test P0036(02)_TR Tarih: 2014-09 İçindekiler Kullanım amacı --------------------------------------------------------------------------------------------------------------------------------
testi REF 441253 REF 441252 200 Test 48 Test P0036(02)_TR Tarih: 2014-09 İçindekiler Kullanım amacı --------------------------------------------------------------------------------------------------------------------------------
Listeria Monocytogenes Real time PCR Tespit Kiti
 Listeria Monocytogenes Real time PCR Tespit Kiti Protokol PD LM00 0 50 Reaksiyon REŞİT GALİP CADDESİ 74-7 06700 ÇANKAYA, ANKARA, TÜRKİYE T +90 32 447 22 79 / 80 F +90 32 447 22 07 W www.bmlabosis.com İnternal
Listeria Monocytogenes Real time PCR Tespit Kiti Protokol PD LM00 0 50 Reaksiyon REŞİT GALİP CADDESİ 74-7 06700 ÇANKAYA, ANKARA, TÜRKİYE T +90 32 447 22 79 / 80 F +90 32 447 22 07 W www.bmlabosis.com İnternal
QMS LAMOTRIGINE. İmmün testi. Simgelerin Açıklamaları LAMOTRİGİN KALİBRATÖRLERİ 0373787
 0155199-E-TR November, 2014 QMS LAMOTRIGINE İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu
0155199-E-TR November, 2014 QMS LAMOTRIGINE İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu
In Vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir Türkçe
 MAX CT/GC 442969 In Vitro Diyagnostik Kullanım İçindir P0212(04) BD MAX System ile kullanım içindir 2017-06 Türkçe 4 0086 I KULLAM AMACI BD MAX CT/GC testi BD MAX System üzerinde uygulandığı şekilde, Chlamydia
MAX CT/GC 442969 In Vitro Diyagnostik Kullanım İçindir P0212(04) BD MAX System ile kullanım içindir 2017-06 Türkçe 4 0086 I KULLAM AMACI BD MAX CT/GC testi BD MAX System üzerinde uygulandığı şekilde, Chlamydia
Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan
 Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan ekstraselluler matriks içinde, birbirlerine yapışarak meydana getirdikleri
Biyofilmler; mikroorganizmaların, biyotik veya abiyotik yüzeylere adhezyonu sonrasında oluşturdukları glikokaliks olarak da adlandırılan ekstraselluler matriks içinde, birbirlerine yapışarak meydana getirdikleri
QMS TOPIRAMAT. İmmün testi. Simgelerin Açıklamaları TOPIRAMATE KONTROLLERİ 0374181 1-3
 0155241-C October, 2014 QMS TOPIRAMAT İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu prospektüste
0155241-C October, 2014 QMS TOPIRAMAT İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu prospektüste
QMS LAMOTRIGINE. İmmün testi. Simgelerin Açıklamaları LAMOTRİGİN KONTROLLERİ 0374090
 0155206-D-TR October, 2014 QMS LAMOTRIGINE İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu prospektüste
0155206-D-TR October, 2014 QMS LAMOTRIGINE İmmün testi Bu Quantitative Microsphere System (QMS) prospektüsü kullanım öncesinde dikkatle okunmalıdır. Prospektüste verilen talimatlar uygulanmalıdır. Bu prospektüste
BD GeneOhm Lizis Kiti
 BD GeneOhm Lizis Kiti REF 441243 P0015(03)_TR Türkçe Tarih: 2014-10 İçindekiler Türkçe... 3 Kullanım Amacı... 3 Ayıraçlar... 3 Önlemler... 3 Sağlanan materyaller... 3 Saklama, muamele ve stabilite... 3
BD GeneOhm Lizis Kiti REF 441243 P0015(03)_TR Türkçe Tarih: 2014-10 İçindekiler Türkçe... 3 Kullanım Amacı... 3 Ayıraçlar... 3 Önlemler... 3 Sağlanan materyaller... 3 Saklama, muamele ve stabilite... 3
Protokolü PD S Reaksiyon
 Salmonella sp. Real time PCR Tespit Kiti Protokolü PD S00 0 50 Reaksiyon REŞİT GALİP CADDESİ 74-7 06700 ÇANKAYA, ANKARA, TÜRKİYE T +90 32 447 22 79 / 80 F +90 32 447 22 07 www.bmlabosis.com İnternal Pozitif
Salmonella sp. Real time PCR Tespit Kiti Protokolü PD S00 0 50 Reaksiyon REŞİT GALİP CADDESİ 74-7 06700 ÇANKAYA, ANKARA, TÜRKİYE T +90 32 447 22 79 / 80 F +90 32 447 22 07 www.bmlabosis.com İnternal Pozitif
In Vitro Diyagnostik Kullanım İçindir. P0167(03) 2014-07 Türkçe. BD MAX Sistemi ile kullanım içindir
 In Vitro Diyagnostik Kullanım İçindir 443461 BD MAX Sistemi ile kullanım içindir P0167(03) 2014-07 Türkçe KULLANIM AMACI BD MAX Sistemi'nde gerçekleştirilen BD MAX MRSA XT testi, nazal kolonizasyon riski
In Vitro Diyagnostik Kullanım İçindir 443461 BD MAX Sistemi ile kullanım içindir P0167(03) 2014-07 Türkçe KULLANIM AMACI BD MAX Sistemi'nde gerçekleştirilen BD MAX MRSA XT testi, nazal kolonizasyon riski
M50 otomatik tanımlama Ve duyarlılık testi
 BD Phoenix M50 otomatik tanımlama Ve duyarlılık testi Performans Tanımlama Tanımlama için 45 kromojenik ve florojenik sübstrat kullanılır. Cihazdaki inkübasyon ve deteksiyon sürecinde ek reaktif eklenmesi
BD Phoenix M50 otomatik tanımlama Ve duyarlılık testi Performans Tanımlama Tanımlama için 45 kromojenik ve florojenik sübstrat kullanılır. Cihazdaki inkübasyon ve deteksiyon sürecinde ek reaktif eklenmesi
In Vitro Diyagnostik Kullanım İçindir BD MAX System ile kullanım içindir Türkçe 4 I
 MAX CT/GC/TV 442970 In Vitro Diyagnostik Kullanım İçindir P0185(03) BD MAX System ile kullanım içindir 2017-01 Türkçe 4 I KULLAM AMACI BD MAX CT/GC/TV testi, BD MAX System kullanılarak gerçekleştirildiği
MAX CT/GC/TV 442970 In Vitro Diyagnostik Kullanım İçindir P0185(03) BD MAX System ile kullanım içindir 2017-01 Türkçe 4 I KULLAM AMACI BD MAX CT/GC/TV testi, BD MAX System kullanılarak gerçekleştirildiği
BRCA 1/2 DNA Analiz Paneli
 FAST-BRCA Sequencing Kit BRCA 1/2 DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR... 3 5
FAST-BRCA Sequencing Kit BRCA 1/2 DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR... 3 5
RTA Kandan Genomik DNA İzolasyon Kiti
 RTA Kandan Genomik DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-05 IVD İnsan kan örneklerinden in vitro tanı amaçlı genomik nükleik asit izolasyon ve saflaştırması için In vitro tanı amaçlı
RTA Kandan Genomik DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-05 IVD İnsan kan örneklerinden in vitro tanı amaçlı genomik nükleik asit izolasyon ve saflaştırması için In vitro tanı amaçlı
DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER
 DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER 1. Vankomisin Vankomisin, Nocardia Orientalis in (eskiden Streptomyces orientalis olarak bilinen) belli suşlarından elde edilen amfoterik
DİRENÇLİ BAKTERİ ENFEKSİYONLARINA KARŞI KULLANILAN ANTİBİYOTİKLER 1. Vankomisin Vankomisin, Nocardia Orientalis in (eskiden Streptomyces orientalis olarak bilinen) belli suşlarından elde edilen amfoterik
Prof.Dr. Meltem Yalınay Çırak Gazi Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji A.D. SALGINLARIN İZLENMESİ VE MOLEKÜLER
 SALGIN ARAŞTIRMASINDA MOLEKÜLER MİKROBİYOLOJİ LABORATUVARININ ROLÜ Prof.Dr. Meltem Yalınay Çırak Gazi Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji A.D. SALGINLARIN İZLENMESİ VE MOLEKÜLER
SALGIN ARAŞTIRMASINDA MOLEKÜLER MİKROBİYOLOJİ LABORATUVARININ ROLÜ Prof.Dr. Meltem Yalınay Çırak Gazi Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji A.D. SALGINLARIN İZLENMESİ VE MOLEKÜLER
attomol apo B-100 quicktype
 attomol apo B-100 quicktype İnsan apolipoprotein B-100 (apo B-3500 mutasyonu) gen inde 10708G>A geçiş tespitine yönelik kit Sadece in vitro diagnostik kullanım içindir! 20 tespit sipariş numarası: 1015
attomol apo B-100 quicktype İnsan apolipoprotein B-100 (apo B-3500 mutasyonu) gen inde 10708G>A geçiş tespitine yönelik kit Sadece in vitro diagnostik kullanım içindir! 20 tespit sipariş numarası: 1015
VERİFİKASYON. Dr. Tijen ÖZACAR. Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR
 VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
Check-Direct CPE Screen for BD MAX. Rektal sürüntülerde Enterobakterilerden karbapenemaz genlerinin tespiti ve ayrıştırılması
 Kullanım kılavuzu Check-Direct CPE Screen for BD MAX Rektal sürüntülerde Enterobakterilerden karbapenemaz genlerinin tespiti ve ayrıştırılması Versiyon 1.4 Yayın tarihi: 11.08.2016 18-0051 24 İçindekiler
Kullanım kılavuzu Check-Direct CPE Screen for BD MAX Rektal sürüntülerde Enterobakterilerden karbapenemaz genlerinin tespiti ve ayrıştırılması Versiyon 1.4 Yayın tarihi: 11.08.2016 18-0051 24 İçindekiler
Mitokondrial DNA Analiz Paneli
 FAST-mtDNA Sequencing Kit Mitokondrial DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR...
FAST-mtDNA Sequencing Kit Mitokondrial DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR...
Protokolü PD S001 01. 50 Reaksiyon
 Salmonella sp. Real time PCR Tespit Kiti Protokolü PD S001 01 50 Reaksiyon REAKSİYON PRENSİPLERİ Reaksiyon Bileşenleri: qpcr Master Mix (PMM) Hedef probe Mix (HPM) Zenginleştirilmiş gıda ürünleri kültüründen
Salmonella sp. Real time PCR Tespit Kiti Protokolü PD S001 01 50 Reaksiyon REAKSİYON PRENSİPLERİ Reaksiyon Bileşenleri: qpcr Master Mix (PMM) Hedef probe Mix (HPM) Zenginleştirilmiş gıda ürünleri kültüründen
Enfeksiyon odaklarından izole edilen Gram negatif ve Gram pozitif bakterilerde antimikrobiyal duyarlılık sonuçları
 Enfeksiyon odaklarından izole edilen Gram negatif ve Gram pozitif bakterilerde antimikrobiyal duyarlılık sonuçları Doç. Dr. Gönül Şengöz 13 Haziran 2015 KAYIP DİLLERİN FISILDADIKLARI SERGİSİ-İSTANBUL Antimikrobiyal
Enfeksiyon odaklarından izole edilen Gram negatif ve Gram pozitif bakterilerde antimikrobiyal duyarlılık sonuçları Doç. Dr. Gönül Şengöz 13 Haziran 2015 KAYIP DİLLERİN FISILDADIKLARI SERGİSİ-İSTANBUL Antimikrobiyal
Tüberküloz laboratuvarında kalite kontrol
 Tüberküloz laboratuvarında kalite kontrol Prof. Dr. Aydan Özkütük Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Sunum planı Kalite gereklilikleri Yöntem geçerli kılma İç Kalite Kontrol
Tüberküloz laboratuvarında kalite kontrol Prof. Dr. Aydan Özkütük Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Sunum planı Kalite gereklilikleri Yöntem geçerli kılma İç Kalite Kontrol
REAKSİYON PRENSİPLERİ
 REAKSİYON PRENSİPLERİ Reaksiyon Bileşenleri: qpcr Master Mix (PMM) Hedef probe Mix (HPM) Zenginleştirilmiş gıda ürünleri kültüründen izole edilen DNA örneği Polimerase Chain Reaction (PCR): Son yıllarda
REAKSİYON PRENSİPLERİ Reaksiyon Bileşenleri: qpcr Master Mix (PMM) Hedef probe Mix (HPM) Zenginleştirilmiş gıda ürünleri kültüründen izole edilen DNA örneği Polimerase Chain Reaction (PCR): Son yıllarda
Enzimlerinin Saptanmasında
 Gram Negatif Bakterilerde Karbapenemaz Enzimlerinin Saptanmasında OXA-48 K-Se T, Blue-Carba Test ve PCR Testlerinin Etkinliğinin Karşılaştırılması Ayham Abulaila, Fatma Erdem, Zerrin Aktaş, Oral Öncül
Gram Negatif Bakterilerde Karbapenemaz Enzimlerinin Saptanmasında OXA-48 K-Se T, Blue-Carba Test ve PCR Testlerinin Etkinliğinin Karşılaştırılması Ayham Abulaila, Fatma Erdem, Zerrin Aktaş, Oral Öncül
GIDA KAYNAKLI HASTALIKLAR. Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır.
 GIDA KAYNAKLI HASTALIKLAR Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır. Gıda Enfeksiyonu: Patojen bir m.o ile kontamine olmuş bir gıdanın yenmesi sonucu oluşan
GIDA KAYNAKLI HASTALIKLAR Gıda orijinli hastalıklar gıda zehirlenmesi gıda enfeksiyonu olarak 2 ana gruba ayrılır. Gıda Enfeksiyonu: Patojen bir m.o ile kontamine olmuş bir gıdanın yenmesi sonucu oluşan
1.5 Kalite Kontrol Bölüm Fiziksel Kalite Kriterleri Bölüm Mikrobiyolojik Kalite Kriterleri Mikrobiyal Kontaminasyon
 1.5 Kalite Kontrol Günümüzde gıda mikrobiyolojisi laboratuarlarında yaygın olarak ticari dehidre formülasyonlardan hazırlanan besiyerleri veya kullanıma hazır besiyerleri kullanılmaktadır. Kullanıma hazır
1.5 Kalite Kontrol Günümüzde gıda mikrobiyolojisi laboratuarlarında yaygın olarak ticari dehidre formülasyonlardan hazırlanan besiyerleri veya kullanıma hazır besiyerleri kullanılmaktadır. Kullanıma hazır
Avian Flu Screening&Typing H5, H7
 REF V-34-50R VER 04.03.08 Avian Flu Screening&Typing H5, H7 Kullanılan Semboller REF Liste Numarası 2-8 C/ -20 C de saklayın RUO Sadece Araştırma Kullanımı için Dikkat! LOT Lot Numarası VER Versiyon Son
REF V-34-50R VER 04.03.08 Avian Flu Screening&Typing H5, H7 Kullanılan Semboller REF Liste Numarası 2-8 C/ -20 C de saklayın RUO Sadece Araştırma Kullanımı için Dikkat! LOT Lot Numarası VER Versiyon Son
Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon)
 Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon) Kaynaklar Mikrobiyolojik prosedürleri doğrulama / geçerli kılmaya ilişkin aşağıdaki uluslararası kaynaklar önerilir
Klinik Mikrobiyoloji Testlerinde Doğrulama (verifikasyon) ve Geçerli Kılma (validasyon) Kaynaklar Mikrobiyolojik prosedürleri doğrulama / geçerli kılmaya ilişkin aşağıdaki uluslararası kaynaklar önerilir
BD MAX SİSTEMİ VE KARBAPENEMAZ ÜRETEN ENTEROBACTERIACEAE'NIN HIZLI SAPTANMASI
 BD MAX SİSTEMİ VE KARBAPENEMAZ ÜRETEN ENTEROBACTERIACEAE'NIN HIZLI SAPTANMASI Dr. Feriha Çilli Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Gram olumsuz bakterilerde GSBL enzimlerinin
BD MAX SİSTEMİ VE KARBAPENEMAZ ÜRETEN ENTEROBACTERIACEAE'NIN HIZLI SAPTANMASI Dr. Feriha Çilli Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Gram olumsuz bakterilerde GSBL enzimlerinin
RTA Viral DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2010-05
 RTA Viral DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2010-05 IVD In vitro tanı amaçlı insan plazma ve serum örneklerinden viral nükleik asit izolasyon ve saflaştırılması için In vitro tanı amaçlı
RTA Viral DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2010-05 IVD In vitro tanı amaçlı insan plazma ve serum örneklerinden viral nükleik asit izolasyon ve saflaştırılması için In vitro tanı amaçlı
PROSEDÜRÜN ÖZETİ VE AÇIKLAMASI
 BD MAX StaphSR Assay İn Vitro Diyagnostik Kullanım İçindir BD MAX Sistemi ile kullanım içindir REF: 44349 P0082(0) 203-06 Türkçe KULLANIM AMACI BD MAX Sistemi'nde gerçekleştirilen BD MAX StaphSR Assay,
BD MAX StaphSR Assay İn Vitro Diyagnostik Kullanım İçindir BD MAX Sistemi ile kullanım içindir REF: 44349 P0082(0) 203-06 Türkçe KULLANIM AMACI BD MAX Sistemi'nde gerçekleştirilen BD MAX StaphSR Assay,
MAIA Pesticide MultiTest
 MAIA Pesticide MultiTest GIDALARDA PESTİSiT KALINTILARI İÇİN AB MAKSİMUM KALINTI LİMİTLERİ İLE UYUMLU ÇOKLU KALINTI TARAMA TESTİ Microplate Acetylcholinesterase Inhibition Assay (MAIA) katı veya sıvı gıda
MAIA Pesticide MultiTest GIDALARDA PESTİSiT KALINTILARI İÇİN AB MAKSİMUM KALINTI LİMİTLERİ İLE UYUMLU ÇOKLU KALINTI TARAMA TESTİ Microplate Acetylcholinesterase Inhibition Assay (MAIA) katı veya sıvı gıda
Kistik Fibrozis DNA Analiz Paneli
 FAST-CFTR Sequencing Kit Kistik Fibrozis DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR...
FAST-CFTR Sequencing Kit Kistik Fibrozis DNA Analiz Paneli Dizi Analizi Amaçlı Kullanım İçin KULLANIM KILAVUZU İÇİNDEKİLER 1 GİRİŞ... 3 2 KİT İÇERİĞİ... 3 3 SAKLAMA... 3 4 GEREKLİ MATERYAL VE CİHAZLAR...
BIONEER MARKA ACCUPOWER EBV QUANTATIVE PCR KİTİ PROTOKOLÜ
 BIONEER MARKA ACCUPOWER EBV QUANTATIVE PCR KİTİ PROTOKOLÜ Kullanılan Ekipmanlar : - Bioneer Marka ExiPrep16 Plus Model Tam Otomatik Nükleik Asit Ekstraksiyon Sistemi - Bioneer Marka ExiPrep Viral DNA/RNA
BIONEER MARKA ACCUPOWER EBV QUANTATIVE PCR KİTİ PROTOKOLÜ Kullanılan Ekipmanlar : - Bioneer Marka ExiPrep16 Plus Model Tam Otomatik Nükleik Asit Ekstraksiyon Sistemi - Bioneer Marka ExiPrep Viral DNA/RNA
Performans Özellikleri
 Performans Özellikleri QIAamp DSP DNA FFPE Tissue Kiti, Sürüm 1 60404 Sürüm yönetimi Bu belge, QIAamp DSP DNA FFPE Tissue Kiti Performans Özellikleri, Sürüm 1, R3 belgesidir. Testi gerçekleştirmeden önce
Performans Özellikleri QIAamp DSP DNA FFPE Tissue Kiti, Sürüm 1 60404 Sürüm yönetimi Bu belge, QIAamp DSP DNA FFPE Tissue Kiti Performans Özellikleri, Sürüm 1, R3 belgesidir. Testi gerçekleştirmeden önce
QIAsymphony SP Protokol Sayfası
 QIAsymphony SP Protokol Sayfası PC_AXpH_HC2_V1_DSP protokolü Kullanım Amacı İn vitro diagnostik kullanım içindir. Bu protokol QIAsymphony SP ve QIAsymphony DSP AXpH DNA Kiti kullanılarak PreservCyt Solüsyonunda
QIAsymphony SP Protokol Sayfası PC_AXpH_HC2_V1_DSP protokolü Kullanım Amacı İn vitro diagnostik kullanım içindir. Bu protokol QIAsymphony SP ve QIAsymphony DSP AXpH DNA Kiti kullanılarak PreservCyt Solüsyonunda
Saf Enterobakteri kolonilerinden karbapenemaz genlerinin tespiti ve ayrıştırılması
 Kullanım kılavuzu Check-Direct CPE for BD MAX Saf Enterobakteri kolonilerinden karbapenemaz genlerinin tespiti ve ayrıştırılması Versiyon 1.5 Yayın tarihi: 11.08.2016 18-0082 24 İçindekiler Kullanım amacı...
Kullanım kılavuzu Check-Direct CPE for BD MAX Saf Enterobakteri kolonilerinden karbapenemaz genlerinin tespiti ve ayrıştırılması Versiyon 1.5 Yayın tarihi: 11.08.2016 18-0082 24 İçindekiler Kullanım amacı...
attomol HLA-B*27 Sadece in vitro diagnostik kullanım içindir! 1.Giriş 2. Genel Açıklamalar
 attomol HLA-B*27 HLA-B*27 in tespitine yönelik kit (Doku tiplemesi için kullanmayın!) Sadece in vitro diagnostik kullanım içindir! 40 tespit sipariş numarası: 1030 1.Giriş İnsan lökosit antijenleri(hla)
attomol HLA-B*27 HLA-B*27 in tespitine yönelik kit (Doku tiplemesi için kullanmayın!) Sadece in vitro diagnostik kullanım içindir! 40 tespit sipariş numarası: 1030 1.Giriş İnsan lökosit antijenleri(hla)
QIAsymphony SP Protokol Sayfası
 Şubat 2017 QIAsymphony SP Protokol Sayfası circdna_2000_dsp_v1 ve circdna_4000_dsp_v1 Bu belge QIAsymphony circdna_2000_dsp_v1 ve circdna_4000_dsp_v1 Protokol Sayfası, Versiyon 1, R1 belgesidir. Sample
Şubat 2017 QIAsymphony SP Protokol Sayfası circdna_2000_dsp_v1 ve circdna_4000_dsp_v1 Bu belge QIAsymphony circdna_2000_dsp_v1 ve circdna_4000_dsp_v1 Protokol Sayfası, Versiyon 1, R1 belgesidir. Sample
Emrah Salman, Zeynep Ceren Karahan Ankara Üniversitesi Tıp Fakültesi. Tıbbi Mikrobiyoloji Anabilim Dalı
 Emrah Salman, Zeynep Ceren Karahan Ankara Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Antibiyotik kullanımına bağlı ishal etkeni olan Clostridium difficile, nozokomiyal diyarenin en sık
Emrah Salman, Zeynep Ceren Karahan Ankara Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Antibiyotik kullanımına bağlı ishal etkeni olan Clostridium difficile, nozokomiyal diyarenin en sık
QIAsymphony DSP Dolaşan DNA Kiti
 QIAsymphony DSP Dolaşan DNA Kiti Şubat 2017 Performans Özellikleri 937556 Sample to Insight İçindekiler Performans Özellikleri... 4 Temel performans... 4 Çalışma kesinliği... 5 2 ml ve 4 ml protokollerinin
QIAsymphony DSP Dolaşan DNA Kiti Şubat 2017 Performans Özellikleri 937556 Sample to Insight İçindekiler Performans Özellikleri... 4 Temel performans... 4 Çalışma kesinliği... 5 2 ml ve 4 ml protokollerinin
EUCAST tarafından önerilen rutin iç kalite kontrol Sürüm 3.1, geçerlilik tarihi
 EUCAST tarafından önerilen rutin iç kalite kontrol Sürüm.1, geçerlilik tarihi 11.0.01 Escherichia coli Pseudomonas aeruginosa Staphylococcus aureus Enterococcus faecalis Streptococcus pneumoniae Haemophilus
EUCAST tarafından önerilen rutin iç kalite kontrol Sürüm.1, geçerlilik tarihi 11.0.01 Escherichia coli Pseudomonas aeruginosa Staphylococcus aureus Enterococcus faecalis Streptococcus pneumoniae Haemophilus
Değerlendirme kılavuzu
 Değerlendirme kılavuzu Antimikrobik duyarlılık testine yönelik EUCAST disk difüzyon yöntemi Sürüm 3.0 Ocak 2014 EUCAST değerlendirme kılavuzu slayt gösterisinde yapılan değişiklikler Sürüm Sürüm 3.0 Nisan
Değerlendirme kılavuzu Antimikrobik duyarlılık testine yönelik EUCAST disk difüzyon yöntemi Sürüm 3.0 Ocak 2014 EUCAST değerlendirme kılavuzu slayt gösterisinde yapılan değişiklikler Sürüm Sürüm 3.0 Nisan
Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması
 Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması Aycan Gundogdu, Ph.D. Erciyes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim
Komplike deri ve yumuşak doku enfeksiyonu etkeni çoklu dirençli patojenlerin bakteriyofaj duyarlılıklarının araştırılması Aycan Gundogdu, Ph.D. Erciyes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim
TANIMLAR. Dr. Neriman AYDIN. Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 TANIMLAR Dr. Neriman AYDIN Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı In-vitro tanı Sürekli doğru sonuç Amaca uygun Zamanında Uygun maliyet In-vitro tanı elemanları Kitler
TANIMLAR Dr. Neriman AYDIN Adnan Menderes Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı In-vitro tanı Sürekli doğru sonuç Amaca uygun Zamanında Uygun maliyet In-vitro tanı elemanları Kitler
Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması
 Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması Melisa Akgöz 1, İrem Akman 1, Asuman Begüm Ateş 1, Cem Çelik 1, Betül Keskin 1, Büşra Betül Özmen
Çocuk ve Yetişkin Üriner Escherichia coli İzolatlarında Plazmidik Kinolon Direnç Genlerinin Araştırılması Melisa Akgöz 1, İrem Akman 1, Asuman Begüm Ateş 1, Cem Çelik 1, Betül Keskin 1, Büşra Betül Özmen
RTA Bakteriden Genomik DNA İzolasyon Kiti
 RTA Bakteriden Genomik DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 IVD Bakteri örneklerinden genomik nükleik asit izolasyonu ve saflaştırılması için In vitro tanı amaçlı kullanım için Yalnızca
RTA Bakteriden Genomik DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 IVD Bakteri örneklerinden genomik nükleik asit izolasyonu ve saflaştırılması için In vitro tanı amaçlı kullanım için Yalnızca
RTA Viral Nükleik Asit İzolasyon Kiti
 RTA Viral Nükleik Asit İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-10 IVD In vitro tanı amaçlı insan serum veya plazma (EDTA) örneklerinden viral DNA ve RNA izolasyon ve saflaştırılması amacıyla
RTA Viral Nükleik Asit İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-10 IVD In vitro tanı amaçlı insan serum veya plazma (EDTA) örneklerinden viral DNA ve RNA izolasyon ve saflaştırılması amacıyla
artus HCV QS-RGQ Kit Performans Özellikleri Ocak 2014 Sample & Assay Technologies Saptama limiti (LOD) Versiyon yönetimi
 artus HCV QS-RGQ Kit Performans Özellikleri artus HCV QS-RGQ Kit, Versiyon 1, 4518363, 4518366 Versiyon yönetimi Bu belge artus HCV QS-RGQ Kit Performans Özellikleri, Versiyon 1, R1 belgesidir. Testi gerçekleştirmeden
artus HCV QS-RGQ Kit Performans Özellikleri artus HCV QS-RGQ Kit, Versiyon 1, 4518363, 4518366 Versiyon yönetimi Bu belge artus HCV QS-RGQ Kit Performans Özellikleri, Versiyon 1, R1 belgesidir. Testi gerçekleştirmeden
BIOKITS RAPID 3-D Fındık Test Kat. No E
 BIOKITS RAPID 3-D Fındık Test Kat. No. 902087E Test etmeden önce lütfen talimatları dikkatle okuyun. Giriş ve Kullanım amacı BIOKITS RAPID 3-D Fındık Test birbirinden faklı 3 tespit çizgisi ile tasarlanmıştır
BIOKITS RAPID 3-D Fındık Test Kat. No. 902087E Test etmeden önce lütfen talimatları dikkatle okuyun. Giriş ve Kullanım amacı BIOKITS RAPID 3-D Fındık Test birbirinden faklı 3 tespit çizgisi ile tasarlanmıştır
Mikrobiyolojide Moleküler Tanı Yöntemleri. Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D
 Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
Mikrobiyolojide Moleküler Tanı Yöntemleri Dr.Tuncer ÖZEKİNCİ Dicle Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D 1 Enfeksiyonun Özgül Laboratuvar Tanısı Mikroorganizmanın üretilmesi Mikroorganizmaya
RTA Plazmid DNA İzolasyon Kiti
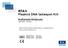 RTA Plazmid DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 Bakteri örneklerinden plazmid DNA izolasyonu ve saflaştırılması için Yalnızca profesyonel kullanım için REF 09007050 50 test 09007100
RTA Plazmid DNA İzolasyon Kiti Kullanma Kılavuzu Yayın Tarihi - 2011-12 Bakteri örneklerinden plazmid DNA izolasyonu ve saflaştırılması için Yalnızca profesyonel kullanım için REF 09007050 50 test 09007100
Tissue_LC_200_V7_DSP ve Tissue_HC_200_V7_DSP (QIAsymphony DSP DNA Mini Kiti için kullanıcı açısından doğrulanmıştır)
 Ağustos 2015 QIAsymphony SP Protokol Sayfası Tissue_LC_200_V7_DSP ve Tissue_HC_200_V7_DSP (QIAsymphony DSP DNA Mini Kiti için kullanıcı açısından doğrulanmıştır) Bu belge Kit Versiyonu 1 için Tissue_LC_200_V7_DSP
Ağustos 2015 QIAsymphony SP Protokol Sayfası Tissue_LC_200_V7_DSP ve Tissue_HC_200_V7_DSP (QIAsymphony DSP DNA Mini Kiti için kullanıcı açısından doğrulanmıştır) Bu belge Kit Versiyonu 1 için Tissue_LC_200_V7_DSP
artus BK Virus QS-RGQ Kit
 artus BK Virus QS-RGQ Kit Performans Özellikleri artus BK Virus QS-RGQ Kit, Versiyon 1, 4514363 Testi gerçekleştirmeden önce www.qiagen.com/products/artusbkvirusrgpcrkit.aspx adresinde yeni elektronik
artus BK Virus QS-RGQ Kit Performans Özellikleri artus BK Virus QS-RGQ Kit, Versiyon 1, 4514363 Testi gerçekleştirmeden önce www.qiagen.com/products/artusbkvirusrgpcrkit.aspx adresinde yeni elektronik
Kromozom, DNA ve Gen. Allel Segregasyonu. DNA çift sarmalı. Hastalık yapan mutasyonlar protein fonksiyonunu bozar. Hastalık yapan mutasyonlar
 Temel Genetik Kavramlar DNA izolasyon yöntemleri Kromozom, DNA ve Gen Hücre Nukleus Kromozomlar Gen Prof.Dr.Uğur ÖZBEK Protein DNA çift sarmalı Allel Segregasyonu Şeker Fosfat omurga Bazlar Baz çifti A
Temel Genetik Kavramlar DNA izolasyon yöntemleri Kromozom, DNA ve Gen Hücre Nukleus Kromozomlar Gen Prof.Dr.Uğur ÖZBEK Protein DNA çift sarmalı Allel Segregasyonu Şeker Fosfat omurga Bazlar Baz çifti A
HPV Moleküler Tanısında Güncel Durum. DNA bazlı Testler KORAY ERGÜNAY 1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ
 1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ HPV Moleküler Tanısında Güncel Durum DNA bazlı Testler KORAY ERGÜNAY Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Viroloji Ünitesi HPV tanısı... Sitolojik/Patolojik
1.ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ HPV Moleküler Tanısında Güncel Durum DNA bazlı Testler KORAY ERGÜNAY Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD Viroloji Ünitesi HPV tanısı... Sitolojik/Patolojik
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı:
 Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER)
 VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
Nilgün Çerikçioğlu Marmara Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 Nilgün Çerikçioğlu Marmara Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Kandolaşımı Enfeksiyonları %10 Kandidemi Ölüm hızı : % 50 (YBÜ) Erken tanı (?), tedavinin önemi Etken: Candida allbicans
Nilgün Çerikçioğlu Marmara Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Kandolaşımı Enfeksiyonları %10 Kandidemi Ölüm hızı : % 50 (YBÜ) Erken tanı (?), tedavinin önemi Etken: Candida allbicans
HASTA BAŞI TEST CİHAZI (glukometre) Uz.Dr.Fatma ÇORCU BARAN
 HASTA BAŞI TEST CİHAZI (glukometre) Uz.Dr.Fatma ÇORCU BARAN Glukometre Nedir? Hastanenin servis katlarında sağlık çalışanlarının veya ev kullanıcılarının da kullandığı küçük cep tipi elektronik cihazlardır.
HASTA BAŞI TEST CİHAZI (glukometre) Uz.Dr.Fatma ÇORCU BARAN Glukometre Nedir? Hastanenin servis katlarında sağlık çalışanlarının veya ev kullanıcılarının da kullandığı küçük cep tipi elektronik cihazlardır.
GRAM POZİTİF BAKTERİ ANTİBİYOGRAMLARI
 GRAM POZİTİF BAKTERİ ANTİBİYOGRAMLARI Dr. Özlem KURT AZAP 26 Kasım 2008 Genel Kurallar Tek koloniden yapılan pasaj seçici olmayan besiyerinde (kanlı agar...) bir gece inkübe edilir Benzer morfolojideki
GRAM POZİTİF BAKTERİ ANTİBİYOGRAMLARI Dr. Özlem KURT AZAP 26 Kasım 2008 Genel Kurallar Tek koloniden yapılan pasaj seçici olmayan besiyerinde (kanlı agar...) bir gece inkübe edilir Benzer morfolojideki
Laboratuvar Gereçleri Listesi QIAsymphony SP
 Şubat 2017 Laboratuvar Gereçleri Listesi QIAsymphony SP QIAsymphony DSP Dolaşan DNA Kiti ve QIAsymphony SP (yazılım versiyonu 4.0 ve yazılım versiyonu 4.1; laboratuvar gereçleri paketi SOW-516-6) ile kullanılabilecek
Şubat 2017 Laboratuvar Gereçleri Listesi QIAsymphony SP QIAsymphony DSP Dolaşan DNA Kiti ve QIAsymphony SP (yazılım versiyonu 4.0 ve yazılım versiyonu 4.1; laboratuvar gereçleri paketi SOW-516-6) ile kullanılabilecek
Maymun Çiçek Virüsü (Monkeypox) VEYSEL TAHİROĞLU
 Maymun Çiçek Virüsü (Monkeypox) VEYSEL TAHİROĞLU insanlarda ölümcül hastalığa neden olabilir; her ne kadar genellikle çok daha az ciddi olsa da insan çiçek virüsü hastalığına benzer. Maymun çiçek virüsü
Maymun Çiçek Virüsü (Monkeypox) VEYSEL TAHİROĞLU insanlarda ölümcül hastalığa neden olabilir; her ne kadar genellikle çok daha az ciddi olsa da insan çiçek virüsü hastalığına benzer. Maymun çiçek virüsü
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ SÜRÜM 1.
 TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ SÜRÜM 1.0 Amaç MADDE 1- (1) Kozmetik ürünlerin üreticileri tarafından raf ömürleri
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ SÜRÜM 1.0 Amaç MADDE 1- (1) Kozmetik ürünlerin üreticileri tarafından raf ömürleri
ETKEN BELİRLEMEDE KLASİK YÖNTEMLER, MOLEKÜLER YÖNTEMLER. Doç. Dr. Gönül ŞENGÖZ 9 Mayıs 2014
 ETKEN BELİRLEMEDE KLASİK YÖNTEMLER, MOLEKÜLER YÖNTEMLER Doç. Dr. Gönül ŞENGÖZ 9 Mayıs 2014 DM ve diyabetik ayak «1960 yılından sonra doğan her iki kadından biri 100 yaşını görecektir.» Age and Ageing Toplumda
ETKEN BELİRLEMEDE KLASİK YÖNTEMLER, MOLEKÜLER YÖNTEMLER Doç. Dr. Gönül ŞENGÖZ 9 Mayıs 2014 DM ve diyabetik ayak «1960 yılından sonra doğan her iki kadından biri 100 yaşını görecektir.» Age and Ageing Toplumda
Klinik Örneklerden İzole Edilen E.coli Suşlarının Kümülatif Antibiyotik Duyarlılıklarının Belirlenmesi
 Klinik Örneklerden İzole Edilen E.coli Suşlarının Kümülatif Antibiyotik Duyarlılıklarının Belirlenmesi Mine Aydın Kurç,Özge Tombak,Dumrul Gülen,Hayati Güneş,Aynur Eren Topkaya Antibiyotik duyarlılık raporlarının
Klinik Örneklerden İzole Edilen E.coli Suşlarının Kümülatif Antibiyotik Duyarlılıklarının Belirlenmesi Mine Aydın Kurç,Özge Tombak,Dumrul Gülen,Hayati Güneş,Aynur Eren Topkaya Antibiyotik duyarlılık raporlarının
Genişlemiş Spektrumlu Beta-Laktamaz Üreten Gram Negatif Kan İzolatları: Karbapenemlere Duyarlılık ve Fenotipik/Genotipik Direnç Mekanizmaları
 Genişlemiş Spektrumlu Beta-Laktamaz Üreten Gram Negatif Kan İzolatları: Karbapenemlere Duyarlılık ve Fenotipik/Genotipik Direnç Mekanizmaları 1. ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ 12-16 KASIM 2011, ANTALYA
Genişlemiş Spektrumlu Beta-Laktamaz Üreten Gram Negatif Kan İzolatları: Karbapenemlere Duyarlılık ve Fenotipik/Genotipik Direnç Mekanizmaları 1. ULUSAL KLİNİK MİKROBİYOLOJİ KONGRESİ 12-16 KASIM 2011, ANTALYA
RT-PCR. (reverse transckripsiyon-polimeraz zincir reaksiyonu) Dr Gülnur Güler
 RT-PCR (reverse transckripsiyon-polimeraz zincir reaksiyonu) Dr Gülnur Güler RT-PCR (reverse transckripsiyon-polimeraz zincir reaksiyonu) mrna ekspresyon seviyelerini belirlemek için sensitiv bir metod
RT-PCR (reverse transckripsiyon-polimeraz zincir reaksiyonu) Dr Gülnur Güler RT-PCR (reverse transckripsiyon-polimeraz zincir reaksiyonu) mrna ekspresyon seviyelerini belirlemek için sensitiv bir metod
Çok ilaca dirençli Mycobacterium tuberculosis izolatlarının hızlı tespitinde nitrat redüktaz testinin değerlendirilmesi: Çok merkezli bir çalışma
 Çok ilaca dirençli Mycobacterium tuberculosis izolatlarının hızlı tespitinde nitrat redüktaz testinin değerlendirilmesi: Çok merkezli bir çalışma Ahmet Yılmaz Çoban 1, Berika Taştekin 1, Meltem Uzun 2,
Çok ilaca dirençli Mycobacterium tuberculosis izolatlarının hızlı tespitinde nitrat redüktaz testinin değerlendirilmesi: Çok merkezli bir çalışma Ahmet Yılmaz Çoban 1, Berika Taştekin 1, Meltem Uzun 2,
Yoğun Bakımlarda İnfeksiyon Kontrolü: Haricen Klorheksidin Uygulanmalı mı?
 Yoğun Bakımlarda İnfeksiyon Kontrolü: Haricen Klorheksidin Uygulanmalı mı? Dr. Funda YETKİN İnönü Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Sunum Planı Klorheksidin
Yoğun Bakımlarda İnfeksiyon Kontrolü: Haricen Klorheksidin Uygulanmalı mı? Dr. Funda YETKİN İnönü Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Sunum Planı Klorheksidin
Direnç hızla artıyor!!!!
 Direnç hızla artıyor!!!! http://www.cdc.gov/drugresistance/about.html Yoğun Bakım Üniteleri (YBÜ) Fizyolojik bakımdan stabil olmayan hastaların yaşam fonksiyonlarının düzeltilmesi Altta yatan hastalığın
Direnç hızla artıyor!!!! http://www.cdc.gov/drugresistance/about.html Yoğun Bakım Üniteleri (YBÜ) Fizyolojik bakımdan stabil olmayan hastaların yaşam fonksiyonlarının düzeltilmesi Altta yatan hastalığın
OXA-48 in Saptanmasına Yönelik İzotermal Rekombinaz Polimeraz Amplifikasyon Yöntemine Dayalı Bir Hızlı Moleküler Test Formatının Geliştirilmesi
 OXA-48 in Saptanmasına Yönelik İzotermal Rekombinaz Polimeraz Amplifikasyon Yöntemine Dayalı Bir Hızlı Moleküler Test Formatının Geliştirilmesi Mert Ahmet Kuşkucu, Gökhan Aygün, Asiye Karakullukçu, Nergiz
OXA-48 in Saptanmasına Yönelik İzotermal Rekombinaz Polimeraz Amplifikasyon Yöntemine Dayalı Bir Hızlı Moleküler Test Formatının Geliştirilmesi Mert Ahmet Kuşkucu, Gökhan Aygün, Asiye Karakullukçu, Nergiz
SAĞLIK ÇALIŞANLARININ ENFEKSİYON RİSKLERİ
 SAĞLIK ÇALIŞANLARININ ENFEKSİYON RİSKLERİ Sağlık hizmeti veren, Doktor Ebe Hemşire Diş hekimi Hemşirelik öğrencileri, risk altındadır Bu personelin enfeksiyon açısından izlemi personel sağlığı ve hastane
SAĞLIK ÇALIŞANLARININ ENFEKSİYON RİSKLERİ Sağlık hizmeti veren, Doktor Ebe Hemşire Diş hekimi Hemşirelik öğrencileri, risk altındadır Bu personelin enfeksiyon açısından izlemi personel sağlığı ve hastane
Grieshaber Sklerotomi Adaptörleri Tek Kullanımlık
 Oftalmik Cerrahi için Dünyanın en hassas cihazları Oftalmik Cerrahi için Dünyanın en hassas cihazları Grieshaber Sklerotomi Adaptörleri Tek Kullanımlık Grieshaber Sklerotomi Adaptörleri Tek Kullanımlık
Oftalmik Cerrahi için Dünyanın en hassas cihazları Oftalmik Cerrahi için Dünyanın en hassas cihazları Grieshaber Sklerotomi Adaptörleri Tek Kullanımlık Grieshaber Sklerotomi Adaptörleri Tek Kullanımlık
J Popul Ther Clin Pharmacol 8:e257-e260;2011
 SİTOMEGALOVİRUS (CMV) Prof. Dr. Seyyâl ROTA Gazi Ü.Tıp Fakültesi LOW SYSTEMIC GANCICLOVIR EXPOSURE AND PREEMPTIVE TREATMENT FAILURE OF CYTOMEGALOVIRUS REACTIVATION IN A TRANSPLANTED CHILD J Popul Ther
SİTOMEGALOVİRUS (CMV) Prof. Dr. Seyyâl ROTA Gazi Ü.Tıp Fakültesi LOW SYSTEMIC GANCICLOVIR EXPOSURE AND PREEMPTIVE TREATMENT FAILURE OF CYTOMEGALOVIRUS REACTIVATION IN A TRANSPLANTED CHILD J Popul Ther
WaveLight FS200 Hızlı Başlangıç Kılavuzu
 Bu, ayrıntılı Kullanma Kılavuzunun yerini almamaktadır. WaveLight FS200 Kullanıcı Kılavuzunu Adım 1 Ana Şalter Acil-Laser - Emisyonu-Durdurma - Şalteri Şalter Lazerin Çalıştırılması Ana ünitenin sağ tarafındaki
Bu, ayrıntılı Kullanma Kılavuzunun yerini almamaktadır. WaveLight FS200 Kullanıcı Kılavuzunu Adım 1 Ana Şalter Acil-Laser - Emisyonu-Durdurma - Şalteri Şalter Lazerin Çalıştırılması Ana ünitenin sağ tarafındaki
KAN DOLAŞIMI İNFEKSİYONLARI VE DAPTOMİSİN
 KAN DOLAŞIMI İNFEKSİYONLARI VE DAPTOMİSİN Dr. Kaya Süer Yakın Doğu Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Mikrobiyoloji Anabilim Dalı Kan dolaşımı enfeksiyonlarının tanımı Primer (hemokültür
KAN DOLAŞIMI İNFEKSİYONLARI VE DAPTOMİSİN Dr. Kaya Süer Yakın Doğu Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Mikrobiyoloji Anabilim Dalı Kan dolaşımı enfeksiyonlarının tanımı Primer (hemokültür
KULLANMA TALİMATI. Etkin madde: 1 g da 3,00 mg tobramisin Yardımcı maddeler: Klorobutanol hemihidrat, vazelin sıvı, petrolatum (beyaz yumuşak parafin)
 TOBRASED % 0.3 steril göz merhemi Göze uygulanır. KULLANMA TALİMATI Etkin madde: 1 g da 3,00 mg tobramisin Yardımcı maddeler: Klorobutanol hemihidrat, vazelin sıvı, petrolatum (beyaz yumuşak parafin) Bu
TOBRASED % 0.3 steril göz merhemi Göze uygulanır. KULLANMA TALİMATI Etkin madde: 1 g da 3,00 mg tobramisin Yardımcı maddeler: Klorobutanol hemihidrat, vazelin sıvı, petrolatum (beyaz yumuşak parafin) Bu
attomol lactose intolerance C>T quicktype
 attomol lactose intolerance -13910C>T quicktype İnsan laktase-genine karşı -13910C>T geçiş tespitine yönelik mutasyon testi Sadece in vitro diagnostik kullanım içindir! 20 tespit sipariş numarası: 1045
attomol lactose intolerance -13910C>T quicktype İnsan laktase-genine karşı -13910C>T geçiş tespitine yönelik mutasyon testi Sadece in vitro diagnostik kullanım içindir! 20 tespit sipariş numarası: 1045
Bimes Biyomedikal Sistemler ve Sağlık Hizmetleri Tic. Ltd. Şti Çetin Emeç Bulvarı 6. Cad. 64/4 06460 A.Öveçler ANKARA Tel: (0 312) 473 17 83 Fax: (0
 3M PETRİFİLM SELECT E.KOLİ SAYIM PLAKALARI 3M Petrifilm Select E.Koli Sayım Plakaları, E.koli tespiti için dizayn edilmiştir. Basit bir tek testle 24 saat içerisinde sonuçlar elinize ulaşabilmektedir.
3M PETRİFİLM SELECT E.KOLİ SAYIM PLAKALARI 3M Petrifilm Select E.Koli Sayım Plakaları, E.koli tespiti için dizayn edilmiştir. Basit bir tek testle 24 saat içerisinde sonuçlar elinize ulaşabilmektedir.
 Kateter İnfeksiyonlarında Mikrobiyoloji Doç. Dr. Deniz Akduman Karaelmas Üniversitesi it i Tıp Fakültesi İnfeksiyon hastalıkları ve Klinik Mikrobiyoloji A.D Kateter infeksiyonlarında etkenler; kateter
Kateter İnfeksiyonlarında Mikrobiyoloji Doç. Dr. Deniz Akduman Karaelmas Üniversitesi it i Tıp Fakültesi İnfeksiyon hastalıkları ve Klinik Mikrobiyoloji A.D Kateter infeksiyonlarında etkenler; kateter
İZOLASYON ÖNLEMLERİ TALİMATI
 İZOLASYON ÖNLEMLERİ TALİMATI SDÜDHF/TBH/TLM/62/YT-13.01.2015/REVNO-00 1. AMAÇ 1.1. Tanımlanmış veya şüphe edilen bulaşıcı hastalığı olan veya epidemiyolojik olarak önemli bir patojenle enfekte veya kolonize
İZOLASYON ÖNLEMLERİ TALİMATI SDÜDHF/TBH/TLM/62/YT-13.01.2015/REVNO-00 1. AMAÇ 1.1. Tanımlanmış veya şüphe edilen bulaşıcı hastalığı olan veya epidemiyolojik olarak önemli bir patojenle enfekte veya kolonize
KOLONİZASYON. DR. EMİNE ALP Erciyes Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D.
 KOLONİZASYON DR. EMİNE ALP Erciyes Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D. KOLONİZASYON Mikroorganizmanın bir vücut bölgesinde, herhangi bir klinik oluşturmadan
KOLONİZASYON DR. EMİNE ALP Erciyes Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D. KOLONİZASYON Mikroorganizmanın bir vücut bölgesinde, herhangi bir klinik oluşturmadan
Minimum Bakterisidal. Prof.Dr.Ayşe Willke Topcu Mart 2010, Aydın
 Minimum Bakterisidal Konsantrasyon (MBC) Prof.Dr.Ayşe Willke Topcu Mart 2010, Aydın Antimikrobik Tedavinin Başarısı Esas olarak konak defans mekanizmasına bağlıdır Konak antibiyotikle etkisi azalmış mikroorganizmayı
Minimum Bakterisidal Konsantrasyon (MBC) Prof.Dr.Ayşe Willke Topcu Mart 2010, Aydın Antimikrobik Tedavinin Başarısı Esas olarak konak defans mekanizmasına bağlıdır Konak antibiyotikle etkisi azalmış mikroorganizmayı
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ
 VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
KALİTE SİZSİNİZ. Uzm. Dr. Özgür APPAK Prof. Dr. A. Aydan ÖZKÜTÜK Prof. Dr. Nuran ESEN Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.
 KALİTE SİZSİNİZ Uzm. Dr. Özgür APPAK Prof. Dr. A. Aydan ÖZKÜTÜK Prof. Dr. Nuran ESEN Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D Sunum Planı Güvenlik raporlama sistemi Laboratuvar süreçleri
KALİTE SİZSİNİZ Uzm. Dr. Özgür APPAK Prof. Dr. A. Aydan ÖZKÜTÜK Prof. Dr. Nuran ESEN Dokuz Eylül Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji A.D Sunum Planı Güvenlik raporlama sistemi Laboratuvar süreçleri
