TRANSFÜZYONLA BULAŞAN
|
|
|
- Onur Akdarı
- 10 yıl önce
- İzleme sayısı:
Transkript
1 TRANSFÜZYONLA BULAŞAN AN ENFEKSİYONLAR (I) TÜRKİYE VE DÜNYADA D ZORUNLU TESTLERDE ALGORİTMALAR Uzm.Dr.Rukiye BERKEM S.B Ankara Eğitim E ve Araştırma rma Hastanesi IV. Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kongresi Aralık k 2011
2 ZORUNLU TESTLERDE ALGORİTMALAR Transfüzyon tıbbt bbının önemli önceliklerden biri kan güvenlig venliğinin inin sağlanmas lanmasıdır. Ülkelerin kan bağış ğışlarında uyguladığı zorunlu testler ülkeden ülkeye farklılıklar klar göstermektedir. Gelişmi miş ülkeler maliyet etkinlik çalışmaları sonuçlar larına göre g bazı ileri ve özgül l testleri tarama stratejilerinde uygulamaya koymuşlard lardır. r.
3 ZORUNLU TESTLERDE ALGORİTMALAR Gelişmekte olan ülkelerde ise; Bölgesel epidemiyolojik veriler, Tarama laboratuarlarının n kapasitesi, Yöntemlerin özellikleri, Kanın n taranmasına na ayrılan bütçe, b Sağlık k alanındaki ndaki öncelikler dikkate alınarak, en iyi tarama stratejileri oluşturulmal turulmalı, risk takibi ile birlikte maliyet etkinlik çalışmaları yapılarak uygun stratejiler geliştirilmeye çalışılmalıdır.
4 TÜRKİYE DE ZORUNLU TESTLERDE ALGORİTMALAR Ülkemizde uygulanan mikrobiyolojik tarama testleri HBsAg, anti-hcv, anti-hiv 1/2 Sifiliz
5 TÜRKİYE DE ZORUNLU TESTLERDE ALGORİTMALAR Mikrobiyolojik tarama testleri İlgili antijen ve/veya antikorun gösterilmesi g esasına dayanır. Her çalışma için i in negatif ve pozitif kontrolleri içeren kitler halinde temin edilmelidir. Bu testlerin asgari ve mutlak çalışma koşulu, üretici firma talimatlarına uygun olarak kontrollerin doğru sonuç vermesidir. Bu testlerin, zayıf f pozitif bir dışd kontrolü de içermeleri önerilmektedir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
6 TÜRKİYE DE ZORUNLU TESTLERDE ALGORİTMALAR Mikrobiyolojik tarama testlerinin çalışılmasında Sağlık k Bakanlığı tarafından onaylanmış test kitleri kullanılmal lmalı, Testler üreticinin talimatlarına göre g çalışılmalı, Kitler 9 Ocak 2007 tarih ve sayılı resmi gazetede yayımlanm mlanmış olan invitro (vücut dışıd ışında kullanılan) lan) tıbbi t tanı cihazları yönetmeliği ne uygun olarak üretilmiş olmalı, Ulusal Kan ve Kan Ürünleri Rehberi 2011
7 Mikrobiyolojik tarama testlerinin çalışılmasında HBsAg, anti-hcv ve anti-hiv 1/2 viral göstergeleri EIA yöntemleri y Sifiliz taramasında Lesitin bazlı bir antijen içeren i kardiyolipin testi (RPR/VDRL) Treponema pallidum hemaglütinasyon (TPHA) yöntemine dayalı bir test EIA testi kullanılmaktad lmaktadır.
8 Mikrobiyolojik tarama testlerinin çalışılmasında HBsAg nin taranmasında nda kullanılan lan kitlerin duyarlılığı ığı 0.5 IU/mL nin altında olmalıdır. HIV 1/2 antikorlarını araştıran ran kitler HIV subtip O duyarlılığı ığına da sahip olmalıdır.
9 MİKROBİYOLOJİK K TARAMA TESTLERİNDE STANDARTLAR Mikrobiyolojik tarama testlerinin çalışılmasında Üretici bu yönetmeliy netmeliğe e uygun şekilde, yetkili makam tarafından verilmiş eksiksiz bir kalite sistem sertifikasına ve bu kapsamda yer alan her reaktif için i in tüm t m kontrol sonuçlar larını içeren bir belgeye sahip olmalı, Uluslar arası standartlara göre g bunların n aynı zamanda kan bağışı ve kan bağış ğışçısı taraması yönünden nden uygunluğu üretici tarafından beyan edilmeli, Onaylanmış kuruluşlarca; larca; geçerlili erliliği i onaylanmış ve belgelenmiş olmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
10 Tarama testlerinde tekrarlayan reaktiviteye bakılmas lması İlk test sonucu reaktif değilse, Bağış ğışlanan kanın n aranan gösterge g yönünden nden negatif olduğu u kabul edilir. Bağış ğışlanan kan transfüzyon için i in veya bileşenlere enlere ayrılmak için i in kullanılabilir. labilir.
11 Tarama testlerinde tekrarlayan reaktiviteye bakılmas lması İlk test sonucu reaktifse, Bağış ğışlanan kanın n aranan gösterge g yönünden nden başlang langıçta reaktif olduğu kabul edilir. Bağış ğışçı kan örneği, ilk test için i in kullanılan lan aynı test kiti ile yeniden iki kez çalışılmalıdır.
12 Tarama testlerinde tekrarlayan reaktiviteye bakılmas lması İlk test sonucu reaktifse, Tekrar edilen testlerin her ikisi de reaktif değilse ilse; Ünitenin aranan gösterge g yönünden y nden negatif olduğu u kabul edilir, Ünite transfüzyon için i in veya bileşenlere enlere ayrılmak için i in kullanılabilir, labilir, Bağış ğışçı tekrar kan bağışı ğışında bulunabilir.
13 Tarama testlerinde tekrarlayan reaktiviteye bakılmas lması Tekrar edilen testlerin her ikisi veya en az birisi reaktif ise, sonuç tekrarlayan reaktif olarak kabul edilir; Ünite transfüzyon veya bileşenlere enlere ayrılmak için i in kullanılamaz, lamaz, Kan bağış ğışçısı geçici ret kapsamına alınır, Bağış ğışçının n bilgilendirilmesinden önce tekrarlayan reaktif sonucun doğrulama yöntemleri y kullanılarak larak doğrulanmas rulanması gerekir, Doğrulanm rulanmış enfeksiyon tespit edilen kan bağış ğışçıları kalıcı ret kapsamına alınır.
14 MİKROBİYOLOJİK K DOĞRULAMA TESTLERİ İÇİN N ULUSAL ALGORİTMA Tekrarlayan reaktif tarama testi Kan örneklerini doğrulama laboratuarına gönderg Önceden tekrarlayan reaktif kaydı var mım kontrol et. Bağış ğışçyı ait ürünleri bloke et. Doğrulama test sonuçlar ları POZİTİF Bağış ğışçıyla görüşerek kan bağışı ğışını reddet. Yeni bir örnekle bağış ğışçı/sonuç bağlant lantısını doğrula NEGATĐF İstenirse bağış ğışçıyı bilgilendir. Bağış ğışçıyı aktif hale getir. Ancak bağış ğışçı kaydına tekrarlayan reaktif olarak not düşd BELĐRS RSĐZ (Đndeterminate) Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. En uzun pencere dönemi d sonunda testleri tekrarla Ulusal Kan ve Kan Ürünleri Rehberi 2011
15 MİKROBİYOLOJİK K DOĞRULAMA TESTLERİ İÇİN N ULUSAL ALGORİTMA Önceden tekrarlayan reaktif sonucu olan bağış ğışçıda tekrarlayan reaktif tarama testi Kan örneklerini doğrulama laboratuarına gönderg Bağış ğışçıya ait ürünleri bloke et Doğrulama test sonuçlar ları POZİTİF Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. Yeni bir örnekle bağış ğışçı/sonuç bağlant lantısını doğrula NEGATİF Bağış ğışçıyı bilgilendir ve kan bağışı ğışını reddet. BELİRS RSİZ (İndeterminate) Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. Doğrulama laboratuarı gerekli görürse g rse en uzun pencere dönemi d sonunda testleri tekrarla Ulusal Kan ve Kan Ürünleri Rehberi 2011
16 Tarama testlerinde tekrarlayan reaktiviteye bakılmas lması Bağış ğışçı kayıtlar tlarının n incelenmesi, Bağış ğışçıya ait ürünlerin bloke edilmesi, Bağış ğışçının n tıbbi t değerlendirmesi, erlendirmesi, bilgilendirilmesi, danış ışmanlık k verilmesi, ilgili sağlık k kuruluşlar larına yönlendirme y yapılmas lması, Tutarsız z sonuçlar varsa önceden belirlenmiş kriterlere göre g kan bağış ğışçısının n tekrar kan bağışı ğışına uygunluk yönünden y nden değerlendirilmesi erlendirilmesi önemlidir.
17 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Kan bağış ğışçısında viral enfeksiyonun serolojik kanıtının n bulunduğundan undan söz s edebilmek için i in tarama testinde elde edilen tekrarlayan reaktif sonucun daha spesifik serolojik testlerle doğrulanmas rulanması gerekir.
18 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Doğrulama testleri RIBA WB NAT Yüksek duyarlılık k ve özgüllükte ek ELISA testleri Bu kural HBV, HCV, HIV antijen ve antikor tarama testlerinin tümüt için in geçerlidir. erlidir. Doğrulama laboratuarları bu virüsler için i in rutin olarak uyguladıklar kları ek testleri içeren i algoritmalara sahip olmalıdırlar.
19 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Viral enfeksiyonların n prevalansının n normal popülasyondan daha düşük d k olduğu u kan bağış ğışçılarında hatalı pozitif test sonuçlar larına yüksek y oranlarda rastlanmaktadır. r. Asemptomatik bireylerde, enfeksiyonla ilgili herhangi bir bulgusu bulunmayanlarda ve ilk kez test yapılanlarda bu durum dikkat çekicidir.
20 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması HBsAg ELISA testinin doğrulanmas rulanmasında nda nötralizasyon testi kullanılmal lmalıdır. Nötralizasyon testi ile doğrulanmayan HBsAg EIA sonucunda kan bağış ğışçısı HBV enfeksiyonu yönünden y nden tekrar değerlendirilmelidir. erlendirilmelidir. Bağış ğışçının n enfeksiyon dönemi, d anti-hbc (anti-hbc total ve anti-hbc IgM) ve HBe antijen/antikor (HBeAg/anti-HBe) HBe) testleri ile belirlenebilir.
21 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması HCV de tekrarlayan reaktif bulunan örnekler, Strip immunoblot testler (LIA), Rekombinant immunoblot (RIBA) testler Sonuçlar: Pozitif, Belirsiz (indeterminate) Negatif
22 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Pozitif sonuç: HCV antikorunun pozitif olduğunu unu gösterir. g Ancak anti-hcv HCV nin varlığı geçirilmi irilmiş veya geçirilmekte olan enfeksiyonlar arasında ayırım m yaptırmaz, Bu bağış ğışçıların n virüsün n ve karaciğer hastalığı ığının n varlığı yönünden nden tıbbi t değerlendirme erlendirme ve danış ışmanlığa a ihtiyaçlar ları vardır. r.
23 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Negatif sonuç: anti-hcv HCV nin negatif olduğunu unu gösterir. g Enfeksiyonun erken dönemlerinde d anti-hcv hatalı negatif sonuç verirken, virüsle karşı şılaşmadan 1-21 hafta sonra HCV RNA tespit edilebilir. Az sayıda hasta da serokonversiyon aylarca gecikebilir. Bazı kişilerde ilerde HCV enfeksiyonu iyileştikten sonra anti-hcv tespit edilebilen düzeylerin d altına iner. Kronik HCV enfeksiyonu olan ve immünosupresif hastalarda anti-hcv sürekli s negatiftir ve HCV RNA enfeksiyonun tek göstergesi g olabilir.
24 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Belirsiz (indeterminate) sonuç: anti-hcv sonucunun belirlenemediğini ini gösterir. Yakın n zamanda enfekte olmuş ve serokonversiyon aşamasa amasındaki hastalarda ve HCV ile kronik enfeksiyonu bulunan bireylerde bu sonuç elde edilebilir. Bu sonuç aynı zamanda hatalı tarama testi sonucunu da gösterebilir. g
25 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması Reaktif sifiliz tarama test sonuçlar larının TPHA, Floresan Treponema pallidum Antikor testi İmmunoblot testleri ile doğrulanmas rulanması gerekir.
26 Test sonuçlar larının n değerlendirilmesi erlendirilmesi ve yorumlanması İdeal doğrulama testleri Tarama testleri kadar duyarlı Tarama testlerinden çok daha özgül l olmalıdır. Halen kullanılmakta lmakta olan bazı tarama testleri, doğrulama testlerinden daha duyarlıdır. r. Uyumsuz veya doğrulanmam rulanmamış sonuçlara bağlı sorunlarda kalıcı bir çözüm m için i in önerilen ulusal algoritma uygulanmalıdır.
27 Özel Durumlar Ülkemizde HIV Doğrulama test sonuçlar larının sorumluluğu, u, Sağlık k Bakanlığı tarafından onaylanmış referans laboratuarına verilmiştir. Doğrulama laboratuarına, tarama testi hakkında bilgi verilmelidir, doğrulamada kullanılan lan testler tarama testleri kadar duyarlı ve farklı bir test olmalıdır. Kan hizmet birimleri, sonuçlar için i in tarama testi pozitif, doğrulama testi pozitif, negatif veya belirsiz şeklinde kayıt t tutmalıdır. Doğrulama test sonuçlar ları ile bağış ğışçının n tarama test sonuçlar ları birlikte gösterilmelidir. g Ulusal Kan ve Kan Ürünleri Rehberi 2011
28 KODLAMA İSİM İLK 2 HARF SOYADI İLK 2 HARF, BABA ADI İLK 2 HARF, DOĞUM TARİHİ YILININ SON 2 RAKAMI
29 Özel Durumlar Kan Hizmet Birimleri tarama testlerinin kalite ve güvenilirliği i için i in standartlar uygulamalıdır: Hem reaktif hem de test yöntemlerini y kapsayan günlük k içi kalite kontrol programı izlenmeli ve kayıtlar tları tutulmalıdır. Yeni parti kitlerin kabul öncesi denenmesi ek bir kalite güvence g önlemi olarak uygulanmalıdır. Akredite bir laboratuardan dışd kalite kontrol örnekleri temin edilmeli ve dış kalite kontrol programı uygulanıp kayıtlar tları tutulmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
30 Özel Durumlar Kan Hizmet Birimleri tarama testlerinin kalite ve güvenilirliği i için i in standartlar uygulamalıdır: Tüm m yeni yöntemler y ve yöntem y değişiklikleri iklikleri uygulamaya konmadan önce doğrulanmal rulanmalı, kontrol edilmeli ve kayıtlar tları tutulmalıdır. Enfeksiyon göstergelerine g ilişkin tarama testlerindeki tekrarlayan reaktif sonuçlar ile doğrulanm rulanmış pozitif sonuçlar ların n hemovijilans sisteminin bir parças ası olarak Sağlık k Bakanlığı ığı na bildirimi yapılmal lmalı ve izlenmelidir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
31 Anti-HIV testinin kalite kontrolü Alınan tüm t m kan veya kan bileşenleri, enleri, HIV-1 1 tip O gibi nadir tipleri de içerecek şekilde HIV-1 1 ve HIV-2 ye yönelik y antijen ve/veya antikorları güvenilir biçimde imde saptayacak, onaylanmış bir testle taranmalıdır. r. HIV enfeksiyonunu doğrulamak için; i in; Western blot (WB) testleri, Rekombinant/line immunoblot testleri Ulusal bir algoritma ile kullanılmal lmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
32 Anti-HIV testinin kalite kontrolü Kuşkulu anti-hiv testlerinin yorumlanmasında nda HIV antijen testleri ve NAT ın n kullanılmas lması yararlı olabilir. Pozitif çıkan bir doğrulama testi, ilk kan örneğinden 2-44 hafta sonra alınacak yeni bir kan örneği i ile tekrarlanmalıdır. r.
33 Anti-HIV testinin kalite kontrolü Kontrol edilecek parametre Kalite koşulu Kontrol sıkls klığı Kontrolü yürüten anti-hiv 1/2 tarama duyarlılığı ığı zayıf f pozitif örneğin saptanması* Her çalışma Tarama lab. *Zayıf f pozitif kontrol serumu mümkm mkünse üretici firma tarafından sağlanm lanmış olmalıdır. Ancak menşei ei üretici firmadan farklı olmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
34 Anti-HIV testinin kalite kontrolü Kontrol edilecek parametre Kalite koşulu Kontrol sıkls klığı Kontrolü yürüten anti-hiv 1/2 tarama duyarlılığı ığı zayıf f pozitif örneğin saptanması* Her çalışma Tarama lab. *Zayıf f pozitif kontrol serumu mümkm mkünse üretici firma tarafından sağlanm lanmış olmalıdır. Ancak menşei ei üretici firmadan farklı olmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
35 HbsAg testinin kalite kontrolü Tüm m kan veya kan bileşenleri, enleri, Hepatit B yüzey y antijenini (HBsAg) en az 0.5 IU/mL düzeyinde saptayabilecek, onaylanmış bir testle taranmalıdır. r. HBsAg reaktivitesinin doğrulanmas rulanması, özgül nötralizasyon testi ile yapılmal lmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
36 HbsAg testinin kalite kontrolü Bağış ğışçının n enfeksiyon dönemi, d anti-hbc (anti-hbc total ve anti-hbc IgM) ve HBe antijen/antikor (HBeAg/anti-HBe) HBe) testleri ile belirlenebilir.
37 HbsAg testinin kalite kontrolü Kontrol edilecek parametre Kalite koşulu Kontrol sıkls klığı Kontrolü yürüten HbsAg tarama testi 0.5 IU/mL standardının n saptanması Her çalışma Tarama lab. Ulusal Kan ve Kan Ürünleri Rehberi 2011
38 Anti-HCV testinin kalite kontrolü Tüm m kan veya kan bileşenleri, enleri, Hepatit C virus antijeni ve/veya antikorunu (anti-hcv) güvenilir g biçimde imde saptayacak, onaylanmış bir testle taranmalıdır. r. HCV enfeksiyonunu doğrulamak için; i in; immunoblot testler gibi özgül l yöntemleri y içereceki ulusal bir algoritma kullanılmal lmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
39 Anti-HCV testinin kalite kontrolü HCV antijen ve genomunun gösterilmesine yönelik y duyarlı testler, bağış ğışçıdaki enfeksiyon durumunun doğrulanmas rulanmasında nda yararlı olabilir.
40 Anti-HCV testinin kalite kontrolü Kontrol edilecek parametre Kalite koşulu Kontrol sıkls klığı Kontrolü yürüten anti-hcv tarama duyarlılığı ığı zayıf f pozitif örneğin saptanması* Her çalışma Tarama lab. *Zayıf f pozitif kontrol serumu mümkm mkünse üretici firma tarafından sağlanm lanmış olmalıdır. Ancak menşei ei üretici firmadan farklı olmalıdır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
41 Sifiliz testinin kalite kontrolü Kan bağış ğışçılarında sifiliz taramasının n gerekliliği konusunda tartış ışmalar sürmektedir, s Bu test, cinsel yolla geçen en hastalıklar için in riskli davranış ışların n bir göstergesi g olarak kullanılabilir, labilir, Halen birçok ülkede uygulanmaktadır.
42 Sifiliz testinin kalite kontrolü Çoğu u merkez, manuel veya otomatize bir sistemde; Lesitin bazlı bir antijen içereni kardiyolipin testi Treponema pallidum hemaglütinasyon (TPHA) yöntemine dayalı bir test ELISA testi kullanmaktadır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
43 Sifiliz testinin kalite kontrolü Reaktif sifiliz tarama test sonuçlar larının; n; TPHA, Floresan Treponema pallidum Antikor testi (FTA), İmmunoblot testleri ile doğrulanmas rulanması gerekir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
44 Sifiliz testinin kalite kontrolü Kontrol edilecek parametre Kalite koşulu Kontrol sıkls klığı Kontrolü yürüten Lesitin bazlı reagen ve TPHA reagenleri zayıf f pozitif örneğin saptanması Her çalışmanın başlang langıcında nda ve sonunda Tarama lab. Ulusal Kan ve Kan Ürünleri Rehberi 2011
45 Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesi Kan bağış ğışçılarının n tarama testlerinde elde edilen tekrarlayan reaktif sonuçlar ların n ek testlerle doğrulanmas rulanması ve kan bağış ğışçılarının n bilgilendirilmesi gerekmektedir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
46 Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesi Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesinin amaçlar ları: 1) Enfeksiyonu bulunan kan bağış ğışçılarını ilgili sağlık k birimlerine yönlendirmek, y 2) Enfeksiyonu bulunan kan bağış ğışçılarının n tekrar kan bağışı ğışında bulunmalarını önlemek, 3) Belirsiz (indeterminate) veya çelişkili sonuçlar ları bulunan ve geçici ret alan kan bağış ğışçılarını ilgili test sonuçlar ları yönünden nden takip etmek ve aydınlatmak.
47 Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesi HBV için in tekrarlayan reaktiflik durumunda bağış ğışçı bilgilendirilir. HCV ve HIV için in tekrarlayan reaktif örneklerin pozitifliği i doğruland rulandığında, bağış ğışçı ile görüşülmeli g ve bağış ğışçı-test sonucu bağlant lantısını doğrulamak için i in yeni bir serum örneği i alınmal nmalıdır.
48 Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesi Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesinin yazılı olarak mektupla,, mektubun doğrudan kan bağış ğışçısına ulaşaca acağından emin olunarak ya da yüzyy zyüze ze görüşme g ile yapılmas lması önerilmektedir. Ulusal Kan ve Kan Ürünleri Rehberi nde belirtilen biçimde; imde; Doğrulama testi pozitif tespit edilen bağış ğışçı,, Kan Hizmet Birimi tarafından (Form 1) e e göre g yazılı olarak bilgilendirilir. Yönlendirme; ; hizmet biriminin bulunduğu İlin Sağlık Müdürlüğü tarafından belirlenen, konu ile ilgili eğitim e almış uzman hekimlerin bulunduğu, u, bağış ğışçının n takip ve tedavisinin yürütülebileceği i bir sağlık k kurumuna yapılır. Ulusal Kan ve Kan Ürünleri Rehberi 2011
49 Kan bağış ğışçısının n test sonuçlar ları konusunda bilgilendirilmesi Form 1. KAN BAĞIŞCISI MİKROBM KROBİYOLOJİK K TEST POZİTİFL FLİĞİ BİLDİRİM M FORMU Sayın Bağış ğışçılarımızdan sağlanan kanlar, yapılan tarama testleri sonucu enfeksiyon etkenlerinin bulunmadığı tespit edildiğinde, inde, kullanıma sunulmaktadır.tarama testlerinde pozitiflik saptandığı takdirde ise, söz s konusu kan imha edilmekte ve hastaya kullanılmamakta, lmamakta, ilgili bağış ğışçımız bilgilendirilmektedir. /.../.../... tarihinde bağış ğışladığınız z... numaralı kandan alınan numune ile yapılan testlerde pozitiflik saptanmış ıştır. Size, konu ile ilgili ayrınt ntılı bilgi verebilmemiz için i in en yakın n zamanda...kan Merkezi ne müracaat m etmenizi rica ederiz. Konu hakkında bilgilendirilecek, gerekli ise test tekrarınız z ve/veya doğrulama testleriniz için i in ileri tetkiklerinizin yapılabilece labileceği i sağlık k kuruluşlar larına yönlendirileceksiniz. y Kan Bağışı ğışına gösterdig sterdiğiniz iniz ilgi ve duyarlılık k için i in teşekk ekkür r eder, sağlıkl klı günler dileriz. Ulusal Kan ve Kan Ürünleri Rehberi 2011 syf:265 *Kan Bağoşcısı mikrobiyolojik test pozitifliğinin inin bildiriminde bu formun kullanımı zorunludur.
50 Kan Hizmet Biriminin Yapması Gerekenler Kan Hizmet Birimi, doğrulanm rulanmış HIV, HBV veya HCV enfeksiyonu olan bir bağış ğışçının n pencere döneminde iken bağış yapması durumunda, bu kandan üretilen ve potansiyel olarak enfeksiyöz olan kan bileşenlerini enlerini alan hasta veya hastaların belirlenip izlenmesi ve kendilerini tedavi eden doktorun konuyla ilgili bilgilendirilmesi işlemini i başlat latır. Bu bağış ğışlar son bir yılly llık zaman diliminde yapılm lmış olan bağış ğışları kapsar. Ulusal Kan ve Kan Ürünleri Rehberi 2011
51 Kan Hizmet Biriminin Yapması Gerekenler Mikrobiyolojik tarama testleri tekrarlayan reaktif bulunan kan bağış ğışları bloke edilmeli, transfüzyonda ve ürün n yapımında kullanılmamal lmamalıdır. Kan bağış ğışçısının n dosyasına tekrarlayan reaktivite kaydedilmeli, bağış ğışçı geçici ret kapsamına alınmal nmalıdır. Doğrulama testlerinin veya ek testlerin sonuçlar larına göre g kan bağış ğışçısının n kalıcı reddine karar verilebilir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
52 Kan Hizmet Biriminin Yapması Gerekenler Doğrulama testleri negatif sonuçlan lanır r ya da ek test sonuçlar ları arasında tutarsızl zlık oluşursa; ursa; Tekrarlayan reaktif sonucun hatalı pozitif bir test sonucu olma olasılığı ığı vardır. r. Bu durumda kan bağış ğışçısının n belli bir süre s sonra testleri tekrarlanarak kan bağışı yapıp p yapamayacağı konusunda karar verilmesi gerekir. Ulusal Kan ve Kan Ürünleri Rehberi 2011
53 Kan Hizmet Biriminin Yapması Gerekenler İlk tarama örneği i ile takip örneği i arasında geçmesi gereken süre s İngiltere standartlarına na göre g en az 12 haftadır. Amerika standartları bu süreyi s HIV için i in sekiz hafta ve HCV için i in altı hafta olarak bildirmektedir. Nötralizasyon testi ile doğrulanamayan reaktif HBs Ag sonucu ya da tutarsız z HBsAg, HBV DNA ve anti-hbc sonuçlar ları bulunan kan bağış ğışçılarının n tekrar kan örneklerinin altınc ncı ayda alınmas nması önerilmektedir.
54 Kan Hizmet Biriminin Yapması Gerekenler Kan bağış ğışçısından alınan tekrar kan örneğinde tarama testleri reaktif değilse, ek testler de negatif sonuç verirse kişiden iden tekrar kan bağışı alınabilir. Ancak bağış esnasında nda da testlerin tekrarlanması ve böylece b iki seri negatif test sonucu bulunması gerekli görülmektedir. g Bu konularda ulusal test algoritmalarının belirlenmesine ihtiyacımız z vardır. r.
55 Dünya Sağlık Örgütü (DSÖ) DSÖ Ö nün n rehberleri ve önerilerinin üye ülkelerin hiçbirinde kanuni bağlay layıcılığıığı yoktur; ancak AB mevzuatına göre g üye ülkelerin kendi mevzuatlarını oluştururken DSÖ Ö nün n tavsiyelerini göz g önünde nde bulundurmalı gerekmektedir. DSÖ tüm ülkelerde tam kan ve aferez bağış ğışları için in zorunlu tarama testleri olarak HBsAg, anti-hcv, anti-hiv 1/2 ve sifiliz tarama testlerinin kullanılmas lmasını önermektedir.
56 Dünya Sağlık Örgütü (DSÖ) Tarama için i in kullanılacak lacak testler; HIV-1 1 ve HIV-2: HIV antikorları veya HIV antijen-antikor antikor kombine testleri, Hepatit B: Hepatit B yüzey y antijeni (HBsAg) taraması, Hepatit C: HCV antikorları veya HCV antijen-antikor antikor kombine testleri, Sifiliz (Treponema pallidum): Non spesifik antikorlar (lipoidal antijenler için) i in) veya özgül (spesifik) treponemal antikorlar olmalıdır.
57 Dünya Sağlık Örgütü (DSÖ) Sıtma, Chagas hastalığı veya HTLV gibi enfeksiyonlar için i in ise tarama testleri, epidemiyolojik kanıtlara dayalı olmalı ve ulusal sağlık k otoritesi tarafından karar verilmelidir. Taramada kullanılacak lacak testlerin duyarlılıklar kları ve özgüllükleri yüksek y olmalı,, en az %99.5 duyarlılık k sınırına s na sahip olmalıdır.
58 Dünya Sağlık Örgütü (DSÖ) HBsAg, anti-hcv ve anti-hiv 1/2 viral göstergeleri g EIA/CLIA yöntemleri HIV 1/2 antikorlarını araştıran ran kitler HIV subtip O duyarlılığı ığına da sahip olmalıdır. Sifiliz taramasında ise non-spesifik (VDRL veya RPR) lesitin bazlı bir antijen içeren i kardiyolipin testi veya treponemal antikorların n kullanıld ldığı yüksek duyarlılık k ve özgüllüğe e sahip spesifik testler Treponema pallidum hemaglütinasyon (TPHA) yöntemine y dayalı bir test veya EIA testi kullanılmal lmalıdır.
59 DSÖ Ö nün n Tarama ve Doğrulama Testleri Algoritması
60 DSÖ Ö nün n Zorunlu Testler için i in Önerileri Virüs HIV Tarama marker Anti-HIV (1,2,0) Anti-HIV (1,2,0) Test EIA/CLIA Hızlı EIA (Rapid) Partikül l agg. HIV p-24 p Ag EIA/CLIA HIV RNA NAT Öneriler Önerilen En etkili testler Ag/Ab kombine testlerdir. Özel durumlarda kullanılabilir. labilir. Ag/Ab kombine testlerinin bir parças ası ise önerilmektedir. Maliyet/etkinliğe e göre g değerlendirilmelidir. erlendirilmelidir. HBsAg EIA/CLIA Önerilen Hepatit B HBsAg Anti-HBc Hızlı EIA (Rapid) Partikül l agg. EIA/CLIA Özel durumlarda kullanılabilir. labilir. HBV nin prevalansının n yüksek y olduğu ülkelerde önerilmemektedir. HBV DNA NAT Maliyet/etkinliğe e göre g değerlendirilmelidir. erlendirilmelidir. Anti-HCV EIA/CLIA Önerilen Hepatit C Anti-HCV HCV Ag Hızlı EIA (Rapid) EIA/CLIA Özel durumlarda kullanılabilir. labilir. Ag/Ab kombine testlerinin bir parças ası ise önerilmektedir. HCV RNA NAT Maliyet/etkinliğe e göre g değerlendirilmelidir. erlendirilmelidir. Sifiliz T. Pallidum Ab. Lipoidal Ag Ab. Partikül l agg. (TPHA) EIA VDRL RPR Önerilen Sifilizin yüksek y insidansı bulunan ülkelerde düşünülebilir.
61 Avrupa Konseyi Önerileri Avrupa Konseyi önerilerinin AB ye bağlı ülkelerde hukuki bağlay layıcılığıığı yoktur ancak birliğe e bağlı ülkelerde göz g önünde nde bulundurulmaları gerekir. Direktiflerin ise hukuki bağlay layıcılığıığı vardır r ve üye ülkelerin kanunlarına na aktarılmalar lmaları gerekmektedir. Zorunlu tarama testleri olarak en az HBsAg, anti-hcv, anti-hiv 1/2 tarama testlerinin kullanılmas lmasını önermektedir. Daha önce bu grupta yer alan Sifiliz tarama testi Ek serolojik tarama testleri kapsamına alınm nmıştır.
62 Avrupa Konseyi Önerileri Zorunlu serolojik tarama testleri En az aşağıa ğıda yer alan testleri içermelidir: i HIV-1 1 tip O gibi nadir tipleri de içerecek i şekilde HIV-1 1 ve HIV-2 ye yönelik y antikorlar (anti-hiv HIV-1 1 ve anti-hiv HIV-2), Hepatit C virus antikoru (anti-hcv), Hepatit B yüzey y antijenini (HBsAg) en az 0.5 IU/mL düzeyinde saptayabilecek bir test.
63 Avrupa Konseyi Önerileri. Zorunlu serolojik testlerin kalite kontrolü Kontrol edilecek parametre anti-hiv 1/2 tarama duyarlılığı ığı anti-hcv tarama duyarlılığı ığı HbsAg tarama testi Kalite koşulu zayıf f pozitif örneğin saptanması* zayıf f pozitif örneğin saptanması* 0.5 IU/mL standardının saptanması Kontrol sıkls klığı Her plak/çal alışma Her plak/çal alışma Her plak/çal alışma *Zayıf f pozitif kontrol serumu mümkm mkünse üretici firma tarafından sağlanm lanmış olmalıdır. Ancak menşei ei üretici firmadan farklı olmalıdır. Zorunlu serolojik tarama testlerini çalışan laboratuarlar düzenli d bir dışd kalite kontrol programına katılmal lmalıdır.
64 Avrupa Konseyi Önerileri Doğrulama testleri HIV veya HCV enfeksiyonunu doğrulamak için i in güncel g yaklaşı şım; Alternatif ELISA testleri, Western blot veya rekombinan immunoblot testleri gibi yöntemleri içerecek i ulusal bir algoritmanın kullanılmas lmasıdır. Kuşkulu antikor test sonuçlar larının yorumlanmasında nda antijen testleri ve NAT ın n kullanılmas lması yararlı olabilir.
65 Avrupa Konseyi Önerileri Doğrulama testleri Pozitif çıkan bir doğrulama testi, ilk kan örneğinden hafta sonra alınacak yeni bir kan örneği i ile tekrarlanmalıdır. r. HBsAg reaktivitesinin doğrulanmas rulanması, özgül nötralizasyon testi ile yapılmal lmalıdır. Bağış ğışçının n enfeksiyon dönemi, d anti-hbc (anti-hbc total ve anti-hbc IgM) ve HBe antijen/antikor (HBeAg/anti-HBe) HBe) testleri ile belirlenebilir.
66 MİKROBİYOLOJİK K DOĞRULAMA TESTLERİ İÇİN N ALGORİTMA Tekrarlayan reaktif tarama testi Kan örneklerini doğrulama laboratuarına gönderg Önceden tekrarlayan reaktif kaydı var mım kontrol et. Bağış ğışçyı ait ürünleri bloke et. Doğrulama test sonuçlar ları POZİTİF Bağış ğışçıyla görüşerek kan bağışı ğışını reddet. Yeni bir örnekle bağış ğışçı/sonuç bağlant lantısını doğrula NEGATĐF İstenirse bağış ğışçıyı bilgilendir. Bağış ğışçıyı aktif hale getir. Ancak bağış ğışçı kaydına tekrarlayan reaktif olarak not düşd BELĐRS RSĐZ (Đndeterminate) Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. En uzun pencere dönemi d sonunda testleri tekrarla
67 MİKROBİYOLOJİK K DOĞRULAMA TESTLERİ İÇİN N ALGORİTMA Önceden tekrarlayan reaktif sonucu olan bağış ğışçıda tekrarlayan reaktif tarama testi Kan örneklerini doğrulama laboratuarına gönderg Bağış ğışçıya ait ürünleri bloke et Doğrulama test sonuçlar ları POZİTİF Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. Yeni bir örnekle bağış ğışçı/sonuç bağlant lantısını doğrula NEGATİF Bağış ğışçıyı bilgilendir ve kan bağışı ğışını reddet. BELİRS RSİZ (İndeterminate) Bağış ğışçıyla görüşerek g kan bağışı ğışını reddet. Doğrulama laboratuarı gerekli görürse g rse en uzun pencere dönemi d sonunda testleri tekrarla
68 İNGİLTERE KAN TRANSFÜZYON MERKEZLERİNİN ZORUNLU TARAMA TESTLERİNDEK NDEKİ ALGORİTMASI İngiltere de kan bağış ğışlarına uygulanan testler zorunlu testler ve ek testler olmak üzere iki grupta sınıflandırılmıştır. Zorunlu testler Klinik kullanımı olan tüm t m kan bağış ğışları ve kan ürünlerinin kullanımına na izin verilebilmesi için i in Sağlık k Otoritesinin zorunlu tuttuğu u testlerdir. HBsAg, anti-hiv 1 ve 2, anti-hcv, HCV NAT, anti-htlv I/II ve sifiliz antikorları.
69 İNGİLTERE KAN TRANSFÜZYON MERKEZLERİNİN N ZORUNLU TARAMA TESTLERİNDEK NDEKİ ALGORİTMASI Reaktif çıkan tüm t örnekler ilk testte kullanılan lan test yönteminin y aynısı ile tekrar iki kez çalışılmalıdır. Eğer tekrar uygulanan testler reaktif değilse, kan ve bunlardan elde edilen ürünlerin kullanımına na izin verilebilir ve bu ürünler stoklanır. MĐKROBĐYOLOJĐK K TARAMA TESTĐ REAKTĐF;BA F;BAŞLANGIÇTA REAKTĐF Bağış ğışçıya ait kanı ve bundan hazırlanan tüm t m kan bileşenlerini enlerini karantinaya al TEKRAR TESTLERĐ TEKRAR TESTLERĐNDEN BĐRĐB REAKTĐFSE; TEKRARLAYAN REAKTĐF Kan ve kan bileşenlerini enlerini transfüzyon için i in uygun değildir ildir şeklinde etiketle Kan bağış ğışçısının n kaydına işaret i koy REAKTĐF F DEĞĐ ĞĐL ĐMMÜNOHEMATOLOJĐK TESTLER TAMAM STOK ĐÇĐN SERBESTLEŞTĐR HER ĐKĐ TEKRAR TESTĐ NON REAKTĐF F (REAKTĐF DEĞĐ ĞĐL) KAN ÖRNEĞĐNĐ DOĞRULAMA LABORATUVARINA ARINA GÖNDERG POZĐTĐF F SONUÇ Kan bağış ğışçısının n kaydına kalıcı ret gir. Kan bağış ğışçısı nı bilgilendir; danış ışmanlık k ve yönlendirme y sağla NEGATĐF F VEYA INDETERMINATE SONUC Ulusal algoritmaya gore akışı takip et
70 İNGİLTERE KAN TRANSFÜZYON MERKEZLERİNİN ÇELİŞKİLİ YADA BELİRS RSİZ Z TEST SONUÇLARINDA TEKRAR BAĞIŞA A KABUL İÇİN N ALGORİTMASI Mikrobiyolojik tarama testi tekrarlayan reaktif Doğrulama Lab.testleri negatif veya belirsiz (indeterminate) Đlk (indeks) bağış ğışdan 12 hafta sonra tekrar kan alınır Mikrobiyolojik tarama testleri kan merkezinde çalışılır NEGATİF POZĐTĐF Alternatif (ikinci) mikrobiyolojik tarama testi NEGATİF POZĐTĐF Doğrulama laboratuarı Doğrulama laboratuarı Doğrulama laboratuarı BELİRS RSİZ** POZİTİF* BELİRS RSİZ ** POZİTİF* BELİRS RSİZ ** POZİTİF* NEGATİF NEGATİF NEGATİF BAĞIŞ ALINMAZ; BAĞIŞÇI I KAYDI TEKRAR BAĞIŞ ĐÇĐN N UYGUN HALE GETĐRĐLĐR. R. BAĞIŞ ALINDIĞINDA INDA TARAMA TESTLERĐ VE ALTERNATĐF F (ĐKĐNC( NCĐ) TARAMA TESTĐ TEKRARLANIR. TÜMÜT NEGATĐFSE BAĞIŞ KULLANILIR *: dosyaya kayıt; kalıcı red; bilgilendir, danış ışmanlık k ver **: dosyaya kayıt; takip
71 Tarama Testlerinin Özellikleri Serolojik taramada kullanılan lan test kitlerinin duyarlılıklar kları her geçen en gün g arttırılmakta ve performansları geliştirilmektedir. Antijen ve antikorun birlikte bakıld ldığı antijen-antikor antikor kombo testler özellikle tanısal yönden y akut enfeksiyonu tespit etmede yararlıdır. r.
72 Tarama Testlerinin Özellikleri HIV antijen antikor kombo testlerin pencere dönemini 3-55 gün g kısalttığı, HCV de ise bu testlerle sağlanan pencere dönemindeki d kısalmank salmanın 26 gün g olduğu u yapılan çalışmalar da bildirilmektedir. Antijen antikor kombo testlerin kan bankacılığı ığında kullanılmalar lmaları durumunda doğrulama algoritmaları buna göre g düzenlenmelidir. d NAT ın n kullanıld ldığı ülkelerde bu testlerin kullanımına na ihtiyaç bulunmadığı ığı,, ancak NAT yapılm lmıyorsa enfeksiyonun epidemiyolojisine göre g kullanılmalar lmalarının kan güvenlig venliğine ine önemli katkılar sağlayabilece layabileceği bildirilmektedir.
73 Tarama Testlerinin Özellikleri Kan bankalarında nda kullanımı onaylanmış HIV-1 ve HCV NAT tarama testlerinin yanında nda ikili (HIV-1/HCV) ve üçlü (HIV-1/HCV/HBV) NAT tarama testleri de vardır. r. MP NAT tarama testleri ile pencere dönemindeki kısalma k HIV-1 1 RNA ile antikor testlerine göre g gün, g, HIV-1 1 p24 antijen testine göre g gün, g HCV NAT ile gündür.
74 Tarama Testlerinin Özellikleri Almanya, Fransa, İngiltere gibi birçok Avrupa Birliği ülkesi, ABD, Kanada, Yeni Zelanda, Avustralya gibi birçok ülkede HIV ve HCV NAT kan bağış ğışlarında zorunlu testler kapsamına girmiştir. Japonya da bunların n yanı sıra HBV NAT zorunlu testler kapsamındad ndadır, 1999 da 500 lük k plazma havuzlarında başlanan HBV NAT taramaları bugün 20 lik havuzlarda sürds rdürülmektedir. HBV enfeksiyonunun yüksek y endemisite gösterdig sterdiği Japonya da 50 örneklik plazma havuzlarında denenen multipleks NAT ile tek başı şına HBsAg taramasından daha yüksek y duyarlılığ ığa a ulaşı şıldığı bildirilmiştir.
75 Anti-HBc Tarama Testi HBV enfeksiyonunun düşük d k prevalans gösterdig sterdiği Almanya, ABD, Kanada gibi birçok ülkede anti-hbc taraması kanın n viral güvenlig venliği yönünden nden ek bir zorunlu testtir. Anti-HBc HBc nin tarama testlerine eklenmesi HBV enfeksiyonu yönünden y nden kan güvenlig venliğini ini arttırmakla rmakla birlikte anti-hbc taramasında kullanılan lan kitlerin özgüllüğünün n yeterli olmaması tutarsız z sonuçlara neden olmaktadır.
76 Anti-HBc Tarama Testi Başlang langıçta anti-hbc reaktif örneklerin yalnızca % 32 sinde tekrarlayan reaktivite elde edilmektedir. Nonspesifik anti-hbc reaktif tespit edilen bağış ğışçıların n reddedilmesi gereksiz olarak sağlıkl klı kan bağış ğışçılarının n kaybına yol açabilmektedir. a abilmektedir. Anti-HBc reaktivitesinin geçirilmi irilmiş HBV enfeksiyonunun göstergesi g olarak doğrulanmas rulanmasını sağlayan bir test ve algoritma henüz önerilmemiştir.
77 Anti-HBc Tarama Testi Japonya anti-hbc pozitif kan bağış ğışçılarının anti-hbs titresi 200 miu/ml nin üzerinde ve HBV DNA negatifse bağış ğışları kabul etmektedir. İngiltere de piercing, akupunktur v.s. yaptıran bağış ğışçılar için i in uygulanacak ret süresi s sonrası bu bağış ğışçılara anti-hbc testi uygulanmakta ve sonuçlar ları negatif olan bağış ğışlar kabul edilmekte anti-hbc HBc si pozitif olan bağış ğışlar anti-hbs açısından test edilmekte anti-hbs düzeyi d <100 IU/L olanlar kabul edilmemekte, >100 IU/L olanların n ise güvenli g olarak kabul edilebileceği i belirtilmektedir.
78 Anti-HBc Tarama Testi DSÖ ise HBV enfeksiyonunun yüksek y prevalans gösterdiği ülkelerde anti-hbc taramasının n kan bağış ğışçılarının n yüksek y oranlarda reddine yol açabileceğini ini belirterek rutin tarama testi olarak kullanılmas lmasını önermemektedir. Anti-HBc testini taramada kullanan ülkelerin ise tüm t m anti-hbc pozitif bağış ğışlara anti-hbs testi uygulamasını ve anti-hbs düzeyinin d >100 miu/ml olanların n klinik kullanım m için i in uygun olduğunu unu belirtmektedir.
79 Anti-HBc Tarama Testi Avrupa Birliğinin inin Rehberinde ise seçilmi ilmiş bağış ğışçılar için i in anti-hbc testinin uygulandığı ülkelerde; Doğrulamada ulusal bir algoritmanın uygulanmasını ve anti-hbs ve NAT gibi destekleyici testlerin uygulanmasının Yerel olarak bağış ğışçı kabulünü ilişkin kararları etkileyebileceği i belirtilmektedir.
80 DÜNYADA UYGULANMAKTA OLAN ZORUNLU TARAMA TESTLERİ DSÖ AVRUPA BİRLİĞİ TÜRKİYE İNGİLTERE ABD KANADA AVUSTURALYA ZORUNLU TESTLER HBsAg anti-hcv anti-hiv 1/2 Sifiliz HBsAg anti-hcv anti-hiv 1/2 HBsAg anti-hcv anti-hiv 1/2 Sifiliz HBsAg anti-hcv anti-hiv 1/2 anti-htlv 1/2 Sifiliz HBsAg Anti-HBc anti-hcv anti-hiv 1/2 anti-htlv 1/2 Sifiliz NAT HIV-1 NAT HCV HBsAg anti-hcv anti-hiv 1/2 Sifiliz anti-htlv 1/2 Batı Nil Virüsü CMV HBsAg anti-hcv anti-hiv 1/2 Anti-HTLV 1/2 Sifiliz EK TESTLER Sıtma Chagas HTLV 1/2 Sifiliz HTLV 1/2 anti-hbc - Sıtma Chagas Batı Nil Virüs CMV anti-hbc Sıtma Chagas Batı Nil Virüs CMV Chagas Chagas CMV YÖNTEMLER EIA/CLIA Rapid IA Partikül l agg. HIV p24 Ag HCV Ag NAT HBV,HCV,HIV EIA TPHA/EIA NAT (HCV,HIV) EIA RPR/VDRL TPHA/EIA EIA TPHA/EIA NAT HCV, WNV EIA/CLIA TPHA NAT HBV,HCV,HIV WNV EIA/CLIA TPHA NAT HCV,HIV WNV EIA/CLIA NAT HBV,HCV,HIV
81 SONUÇ Ülkemizde ve diğer ülkelerde kan güvenlig venliğini ini arttırmak rmak için i in kullanılan lan zorunlu tarama testleri ve test yöntemleri y farklılıklar klar göstermektedir. Ülkemizde uygulanmakta olan zorunlu tarama testleri DSÖ Ö nün n ve Avrupa Kan Transfüzyon Komitesinin önerdiği i zorunlu testlerdir.
82 SONUÇ Tarama testlerinde kullanılacak lacak kalite standartları, testlerin geçerlili erliliği i ve test yöntemleri, y reaktivite tespit edildiğinde inde tekrarlayan reaktiviteye bakılmas lması, tekrarlayan reaktif sonuçlar ların n doğrulanmas rulanması için in kullanılacak lacak test yöntemleri y için i in ulusal algoritmamız oluşturulmu turulmuş ve kullanılmaya lmaya başlanm lanmıştır. Tekrarlayan reaktif ve doğrulanm rulanmış test sonuçlar larında bağış ğışçının n bilgilendirilmesi ve yönlendirilmesi y için i in yapılmas lması gerekenler de ulusal rehberimizde tanımlanm mlanmıştır.
83 TEŞEKK EKKÜR R EDERİM
TRANSFÜZYON MERKEZİ HASTALARDA KULLANILAN MİKROBİYOLOJİK TARAMA TESTLERİ TALİMATI
 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM : Bu talimat transfüzyon merkezinde
1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM : Bu talimat transfüzyon merkezinde
MİKROBİYOLOJİK TARAMA TEST ÇALIŞILMA ESASLARI VE BAĞIŞÇI POZİTİFLİĞİNE YAKLAŞIM
 TRF.PR.05 11.04.2012 01.02.2016 01 1/5 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM
TRF.PR.05 11.04.2012 01.02.2016 01 1/5 1.AMAÇ.Hastalara ait kan örneklerinde yapılması gereken mikrobiyolojik testleri, bu testlerin çalışma yöntemlerini ve kalite kontrol gereklerini belirlemektir.. 2.KAPSAM
VİRAL ENFEKSİYONLARDA ALGORİTMALAR
 VİRAL ENFEKSİYONLARDA ALGORİTMALAR PANEL: TRANSFÜZYON VE VİRAL ENFEKSİYONLAR Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu,XII 3-7 Kasım 2009 Uzm.Dr.A.Esra KARAKOÇ S.B.Ankara EAH, Tıbbi Mikrobiyoloji
VİRAL ENFEKSİYONLARDA ALGORİTMALAR PANEL: TRANSFÜZYON VE VİRAL ENFEKSİYONLAR Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu,XII 3-7 Kasım 2009 Uzm.Dr.A.Esra KARAKOÇ S.B.Ankara EAH, Tıbbi Mikrobiyoloji
BİLDİKLERİMİZ. Transfüzyonla bulaşan mikroorganizmalar. Zorunlu tarama testleri. Tarama testlerinin güvenilirliği
 KAN BANKACILIĞI VE KLİNİK MİKROBİYOLOJİ Ramazan ULUHAN Rukiye BERKEM Pınar ZARAKOLU-KÖŞKERKÖŞKER Yüce AYHAN Nil Banu PELİT 2 BİLDİKLERİMİZ Transfüzyonla bulaşan mikroorganizmalar Zorunlu tarama testleri
KAN BANKACILIĞI VE KLİNİK MİKROBİYOLOJİ Ramazan ULUHAN Rukiye BERKEM Pınar ZARAKOLU-KÖŞKERKÖŞKER Yüce AYHAN Nil Banu PELİT 2 BİLDİKLERİMİZ Transfüzyonla bulaşan mikroorganizmalar Zorunlu tarama testleri
Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması. Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Testler farklı amaçlarla uygulanabilir: - Tanı, tarama, doğrulama,
Anti-HIV Pozitif Bulunan Hastada Kesin Tanı Algoritması Doç. Dr. Kenan Midilli İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Testler farklı amaçlarla uygulanabilir: - Tanı, tarama, doğrulama,
TLERDE SEROLOJİK/MOLEK HANGİ İNCELEME?) SAPTANMASI
 * VİRAL V HEPATİTLERDE TLERDE SEROLOJİK/MOLEK K/MOLEKÜLER LER TESTLER (NE ZAMANHANG HANGİ İNCELEME?) *VİRAL HEPATİTLERDE TLERDE İLAÇ DİRENCİNİN SAPTANMASI *DİAL ALİZ Z HASTALARININ HEPATİT T AÇISINDAN
* VİRAL V HEPATİTLERDE TLERDE SEROLOJİK/MOLEK K/MOLEKÜLER LER TESTLER (NE ZAMANHANG HANGİ İNCELEME?) *VİRAL HEPATİTLERDE TLERDE İLAÇ DİRENCİNİN SAPTANMASI *DİAL ALİZ Z HASTALARININ HEPATİT T AÇISINDAN
Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları
 HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı
 Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı Deniz Gökengin Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Cinsel yolla bulaşan enfeksiyonlar Gonore Klamidyal
Cinsel Yolla Bulaşan Enfeksiyonlarda Tanı Deniz Gökengin Ege Üniversitesi Tıp Fakültesi Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı Cinsel yolla bulaşan enfeksiyonlar Gonore Klamidyal
IV. KLİMUD Kongresi, Kasım 2017, Antalya
 IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 HCV Tanısında Cut off/ Sinyal (S/CO)/TV) Değerlerinin Tanısal Geçerliliklerinin Değerlendirilmesi TÜLİN DEMİR¹, DİLARA YILDIRAN¹, SELÇUK KILIǹ, SELÇUK
IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 HCV Tanısında Cut off/ Sinyal (S/CO)/TV) Değerlerinin Tanısal Geçerliliklerinin Değerlendirilmesi TÜLİN DEMİR¹, DİLARA YILDIRAN¹, SELÇUK KILIǹ, SELÇUK
TARAMA VE DOĞRULAMA TESTLERİ
 TARAMA VE DOĞRULAMA TESTLERİ Ortalama 450 (± %10) ml (~ 250 ml plazma + ~ 200 ml eritrosit) Yaklaşık hematokrit %36-37 Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu 2 Ulusal Kan Merkezleri ve Transfüzyon
TARAMA VE DOĞRULAMA TESTLERİ Ortalama 450 (± %10) ml (~ 250 ml plazma + ~ 200 ml eritrosit) Yaklaşık hematokrit %36-37 Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kursu 2 Ulusal Kan Merkezleri ve Transfüzyon
Kan Hizmetleri Genel Müdürlüğü
 Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 05 Kasım Nepton, Serkan www.kanver.org www.kizilay.org.tr GÜVENLİ KAN BAĞIŞÇISINA ULAŞIMDA NAT TARAMA TESTİ UYGULAMALARI Uzm. Dr.
Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 05 Kasım Nepton, Serkan www.kanver.org www.kizilay.org.tr GÜVENLİ KAN BAĞIŞÇISINA ULAŞIMDA NAT TARAMA TESTİ UYGULAMALARI Uzm. Dr.
TR0802.15-01/001 Türkiye de Kan Tedarik Sisteminin Güçlendirilmesi Teknik Destek Projesi
 Bu proje Avrupa Birliği ve Türkiye Cumhuriyeti tarafından finanse edilmektedir Türkiye 2008 Ulusal IPA (Katılım Öncesi Mali Yardım) Programı TR0802.15-01/001 Türkiye de Kan Tedarik Sisteminin Güçlendirilmesi
Bu proje Avrupa Birliği ve Türkiye Cumhuriyeti tarafından finanse edilmektedir Türkiye 2008 Ulusal IPA (Katılım Öncesi Mali Yardım) Programı TR0802.15-01/001 Türkiye de Kan Tedarik Sisteminin Güçlendirilmesi
Kan Bankacılığında tarama testlerin tarama
 Kan Bankacılığında tarama testlerinde güncel durum Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Temel tarama testleri İmmunoassay temelli testler Enzim immunoassay
Kan Bankacılığında tarama testlerinde güncel durum Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Temel tarama testleri İmmunoassay temelli testler Enzim immunoassay
Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları
 HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HEPATİT B TESTLERİ Hepatit B Virüs Testleri: Hepatit serolojisi, Hepatit markırları Hepatit B virüs enfeksiyonu insandan insana kan, semen, vücut salgıları ile kolay bulaşan yaygın görülen ve ülkemizde
HIV TANISINDA YENİLİKLER
 HIV/AIDS KURSU HIV TANISINDA YENİLİKLER Dr. Mert Ahmet KUŞKUCU İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Dünya Sağlık Örgütü Verileri (2016) YILLARA GÖRE HIV (+) SAPTANAN VAKA SAYISI
HIV/AIDS KURSU HIV TANISINDA YENİLİKLER Dr. Mert Ahmet KUŞKUCU İ.Ü. Cerrahpaşa Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Dünya Sağlık Örgütü Verileri (2016) YILLARA GÖRE HIV (+) SAPTANAN VAKA SAYISI
IV. KLİMUD Kongresi, Kasım 2017, Antalya
 IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 4. Kuşak HIV ELISA Sinyal/cut-off Değerleri ile Hatalı Pozitiflik İlişkisinin Değerlendirilmesi Tülin Demir 1, Süleyman Yalçın 1, Selçuk Kılıç2 1 Sağlık
IV. KLİMUD Kongresi, 08-12 Kasım 2017, Antalya 1 4. Kuşak HIV ELISA Sinyal/cut-off Değerleri ile Hatalı Pozitiflik İlişkisinin Değerlendirilmesi Tülin Demir 1, Süleyman Yalçın 1, Selçuk Kılıç2 1 Sağlık
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.
 Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.Sayı: 25779 Amaç Madde 1 Bu Tebliğin amacı; vücut dışında (in-vitro) kullanılan
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları İçin Ortak Teknik Özellikler Tebliği (Tebliğ No: 2005/1) R.G.Tarih: 07.04.2005 R.G.Sayı: 25779 Amaç Madde 1 Bu Tebliğin amacı; vücut dışında (in-vitro) kullanılan
WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır.
 WEİL FELİX TESTİ WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır. Riketsiyöz tanısında çapraz reaksiyondan faydalanılır bu nedenle riketsiyaların çapraz reaksiyon
WEİL FELİX TESTİ WEİL-FELİX TESTİ NEDİR NASIL YAPILIR? Weil Felix testi Riketsiyozların tanısında kullanılır. Riketsiyöz tanısında çapraz reaksiyondan faydalanılır bu nedenle riketsiyaların çapraz reaksiyon
Mikrobiyoloji Laboratuvarında Karşılaşılan Sorunlar
 Sürekli Tıp Eğitimi / Sürekli Mesleki Gelişim Etkinlikleri Kapsamında 2012 yılı KLİMUD İzmir Toplantıları Klinik Mikrobiyoloji Uzmanının Sorumluluğunda Kan Hizmet Birimleri Mikrobiyoloji Laboratuvarında
Sürekli Tıp Eğitimi / Sürekli Mesleki Gelişim Etkinlikleri Kapsamında 2012 yılı KLİMUD İzmir Toplantıları Klinik Mikrobiyoloji Uzmanının Sorumluluğunda Kan Hizmet Birimleri Mikrobiyoloji Laboratuvarında
CMV EBV HHV-8 Dengue v. Parvovirüs B19 HAV HEV Leishmania spp Kene kaynaklı ansefalit v. Sarı humma
 MALİYET ETKİLİLİK YÖNÜYLE TARAMA TESTİ ALGORİTMALARI Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Transfüzyon ile bulaşan etkenler HBV HCV HIV T. Pallidum Plasmodium
MALİYET ETKİLİLİK YÖNÜYLE TARAMA TESTİ ALGORİTMALARI Dr. Rüçhan Yazan Sertöz Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Transfüzyon ile bulaşan etkenler HBV HCV HIV T. Pallidum Plasmodium
Prediktör Testler ve Sıradışı Serolojik Profiller. Dr. Dilara İnan Isparta
 Prediktör Testler ve Sıradışı Serolojik Profiller Dr. Dilara İnan 04.06.2016 Isparta Hepatit B yüzey antijeni (HBsAg) HBV yüzeyinde bulunan bir proteindir; RIA veya EIA ile saptanır Akut ve kronik HBV
Prediktör Testler ve Sıradışı Serolojik Profiller Dr. Dilara İnan 04.06.2016 Isparta Hepatit B yüzey antijeni (HBsAg) HBV yüzeyinde bulunan bir proteindir; RIA veya EIA ile saptanır Akut ve kronik HBV
VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI
 KLİMUD BÖLGE TOPLANTILARI VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI KLİMUD Klinik Viroloji Çalışma Grubu A B Fekal-oral bulaşma Kronikleşmez E Parenteral bulaşma Kronikleşir C D HBV - Olgu 56 yaşında olgunun
KLİMUD BÖLGE TOPLANTILARI VİRÜS ENFEKSİYONLARDA LABORATUVAR TANISI KLİMUD Klinik Viroloji Çalışma Grubu A B Fekal-oral bulaşma Kronikleşmez E Parenteral bulaşma Kronikleşir C D HBV - Olgu 56 yaşında olgunun
21 gün. 21 gün. 21 gün. Tüm programlar için kullanılabilir. Tüm programlar için kullanılabilir. Tüm programlar için kullanılabilir.
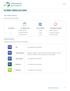 2014 Yükleme Takvimi Yükleme takvimi aşağıdaki gibidir: Test Yükleme Test Yükleme Açılış Pencere Dönemi Sonuç Bildirim Son Günü 1 26 Mart, Çarşamba 16 Nisan, Çarşamba 2 25 Haziran, Çarşamba 16 Temmuz,
2014 Yükleme Takvimi Yükleme takvimi aşağıdaki gibidir: Test Yükleme Test Yükleme Açılış Pencere Dönemi Sonuç Bildirim Son Günü 1 26 Mart, Çarşamba 16 Nisan, Çarşamba 2 25 Haziran, Çarşamba 16 Temmuz,
SINIR DEĞERLER NE ÖNERİLİR? Düzen Laboratuvarlar Grubu
 SEROLOJİK TANIDA SINIR DEĞERLER NASIL DEĞERLENDİRİLİR? NE ÖNERİLİR? Dr. Tutku TANYEL Dr. Tutku TANYEL Düzen Laboratuvarlar Grubu Şüpheli ilişkimin üzerinden 5 gün geçti acaba ne testi yaptırsam HIV bulaşıp
SEROLOJİK TANIDA SINIR DEĞERLER NASIL DEĞERLENDİRİLİR? NE ÖNERİLİR? Dr. Tutku TANYEL Dr. Tutku TANYEL Düzen Laboratuvarlar Grubu Şüpheli ilişkimin üzerinden 5 gün geçti acaba ne testi yaptırsam HIV bulaşıp
Hepatit C virüs enfeksiyonunun laboratuar testleri:
 HEPATİT C TESTLERİ Hepatit C virüs enfeksiyonunun laboratuar testleri: * Anti HCV ve * HCV RNA PCR dır. Bu testler hepatit C hastası olup olmadığınızı, hepatit C taşıyıp taşımadığınızı, kronik hepatit
HEPATİT C TESTLERİ Hepatit C virüs enfeksiyonunun laboratuar testleri: * Anti HCV ve * HCV RNA PCR dır. Bu testler hepatit C hastası olup olmadığınızı, hepatit C taşıyıp taşımadığınızı, kronik hepatit
MİKROBİYOLOJİK TARAMA SİSTEMLERİ VE MEKANİZMALARI. Dr. Nafiz KOÇAK GATA Haydarpaşa Eğt.Hst.
 MİKROBİYOLOJİK TARAMA SİSTEMLERİ VE MEKANİZMALARI Dr. Nafiz KOÇAK GATA Haydarpaşa Eğt.Hst. Mikrobiyolojik donör tarama testleri Transfüzyonla bulaşan enfeksiyonlar yönünden bağışlanan kanların taranması,
MİKROBİYOLOJİK TARAMA SİSTEMLERİ VE MEKANİZMALARI Dr. Nafiz KOÇAK GATA Haydarpaşa Eğt.Hst. Mikrobiyolojik donör tarama testleri Transfüzyonla bulaşan enfeksiyonlar yönünden bağışlanan kanların taranması,
HIV TANISINDA YENİLİKLER
 HIV TANISINDA YENİLİKLER Uzm.Dr. Tülin DEMİR Ülkemizde güncel durum 1985 yılı-mayıs 2016 tarihi itibari ile; Doğrulama testi (+) tespit edilerek bildirimi yapılan toplam vaka sayısı= 12 542 2015 yılı
HIV TANISINDA YENİLİKLER Uzm.Dr. Tülin DEMİR Ülkemizde güncel durum 1985 yılı-mayıs 2016 tarihi itibari ile; Doğrulama testi (+) tespit edilerek bildirimi yapılan toplam vaka sayısı= 12 542 2015 yılı
Akut Hepatit C: Bir Olgu Sunumu. Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa
 Akut Hepatit C: Bir Olgu Sunumu Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa Olgu 24 yaşında erkek hasta 6. sınıf tıp öğrencisi Ortopedi polikliniğine başvurmuş Rutin
Akut Hepatit C: Bir Olgu Sunumu Uz.Dr.Sevil Sapmaz Karabağ İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Manisa Olgu 24 yaşında erkek hasta 6. sınıf tıp öğrencisi Ortopedi polikliniğine başvurmuş Rutin
GAZİANTEP ÜNİVERSİTESİ - KALİTE YÖNETİM SİSTEMİ Doküman No: HTRF-T22-P01
 Sayfa: 1/6 Revizyonun Açıklaması Madde No - - KAPSAM: Transfüzyon Merkezi Hazırlayanlar Murat ORULLUOĞLU Transfüzyon Merk. Sor. Tekn. Gülay YABA Kalite Yönetim Birimi Kontrol Funda BATMAZOĞLU Kalite Koordinatörü
Sayfa: 1/6 Revizyonun Açıklaması Madde No - - KAPSAM: Transfüzyon Merkezi Hazırlayanlar Murat ORULLUOĞLU Transfüzyon Merk. Sor. Tekn. Gülay YABA Kalite Yönetim Birimi Kontrol Funda BATMAZOĞLU Kalite Koordinatörü
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ
 VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
VİRUS HASTALIKLARINDA TANI YÖNTEMLERİ Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı, Viroloji Ünitesi Viral Enfeksiyonlar... Klinik
Viral Hepatitler. Hepatit A Virus. Viral Hepatitler- Tarihsel Bakış. Hepatit Tipleri. Hepatit A Klinik Özellikler
 Viral Hepatitler- Tarihsel Bakış Viral Hepatitler İnfeksiyöz Viral hepatitler A NANB E Enterik yolla geçen Dr. Ömer Şentürk Serum B D C F, G, TTV,? diğerleri Parenteral yolla geçen Hepatit Tipleri A B
Viral Hepatitler- Tarihsel Bakış Viral Hepatitler İnfeksiyöz Viral hepatitler A NANB E Enterik yolla geçen Dr. Ömer Şentürk Serum B D C F, G, TTV,? diğerleri Parenteral yolla geçen Hepatit Tipleri A B
TRANSFÜZYON MERKEZİ STANDART İŞLETİM PROSEDÜRÜ
 KOD:YÖN.PRS 34 YAY.TAR:27.03.2014 REV.TAR: REV.NO: SAYFA :1 / 5 1.AMAÇ: Bölge Kan Merkezinden temin edilen kan ve bileşenlerinin, transfüzyon için cross-match (çapraz karşılaştırma) ve gerek duyulan diğer
KOD:YÖN.PRS 34 YAY.TAR:27.03.2014 REV.TAR: REV.NO: SAYFA :1 / 5 1.AMAÇ: Bölge Kan Merkezinden temin edilen kan ve bileşenlerinin, transfüzyon için cross-match (çapraz karşılaştırma) ve gerek duyulan diğer
Belge No: Yayın Tarihi: Güncelleme Tarihi: Güncelleme No: Sayfa No: EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ
 EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama - 0 - EKÖ/YÖN 20 19.08.2009-1 2/5 1. AMAÇ Bu yönergenin amacı; çalışanların iş kazası sonucu yaralanmalarında bildirimin
EKÖ/YÖN 20 19.08.2009-1 1/5 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama - 0 - EKÖ/YÖN 20 19.08.2009-1 2/5 1. AMAÇ Bu yönergenin amacı; çalışanların iş kazası sonucu yaralanmalarında bildirimin
PERSONEL YARALANMALARI İZLEM TALİMATI
 Hazırlayan Kontrol eden Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Direktörü Hastane Yöneticisi 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden sağlık
Hazırlayan Kontrol eden Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Direktörü Hastane Yöneticisi 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden sağlık
Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri. Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya
 Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya Dünyada 130-170 milyon kişi hepatit C virüsü (HCV) ile infekte Her yıl 3-4 milyon
Hepatit C Virüsü: Tanıda Serolojik ve Moleküler Yöntemlerin Yeri Üner Kayabaş İnönü Üniversitesi Tıp Fakültesi Malatya Dünyada 130-170 milyon kişi hepatit C virüsü (HCV) ile infekte Her yıl 3-4 milyon
PERSONEL YARALANMALARI İZLEM TALİMATI
 Sayfa No 1 / 5 Hazırlayan İnceleyen Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Temsilcisi Başhekim 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden
Sayfa No 1 / 5 Hazırlayan İnceleyen Onaylayan Enfeksiyon Kontrol Komitesi Kalite Yönetim Temsilcisi Başhekim 1.AMAÇ Hasta kanı ve/veya diğer vücut sıvıları ile parenteral veya mukoza yoluyla temas eden
Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme;
 Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme; o Hangi durumlarda bağışçıdan kan alınacağı, o Bağışçının seçilmesi, bağışçının reddi, bağışçıdan kan
Transfüzyon merkezinde süreçlerin işleyişine yönelik yazılı düzenleme bulunmalıdır. Yazılı düzenleme; o Hangi durumlarda bağışçıdan kan alınacağı, o Bağışçının seçilmesi, bağışçının reddi, bağışçıdan kan
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER)
 VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
VERİFİKASYON (SEROLOJİ, MOLEKÜLER TESTLER) Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının
VERİFİKASYON. Dr. Tijen ÖZACAR. Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR
 VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
VERİFİKASYON Dr. Tijen ÖZACAR Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD - İZMİR TANIM Ticari veya laboratuvarda geliştirilmiş bir testin, laboratuvardaki performansının ölçülerek dökümante
TARAFLARDAN BEKLEDİKLER
 Dr. Mahmut TOKAÇ Sağlık k Bakanlığı İlaç ve Eczacılık k Genel MüdürüM İn vivo ve in vitro BY/BE çalışmaları başvuru dosyalarının, n, yürürly rlükte olan 27 Mayıs s 1994 tarih ve 21942 sayılı Farmasötik
Dr. Mahmut TOKAÇ Sağlık k Bakanlığı İlaç ve Eczacılık k Genel MüdürüM İn vivo ve in vitro BY/BE çalışmaları başvuru dosyalarının, n, yürürly rlükte olan 27 Mayıs s 1994 tarih ve 21942 sayılı Farmasötik
KAN BAĞIŞÇILARINDA HBV, HCV, HIV TARAMA TESTLERİNİN DOĞRULANMASI: TARAMA TESTLERİNİN POZİTİF PREDİKTİVİTESİ VE DOĞRULAMA TESTLERİNİN MALİYETİ
 TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ KAN BAĞIŞÇILARINDA HBV, HCV, HIV TARAMA TESTLERİNİN DOĞRULANMASI: TARAMA TESTLERİNİN POZİTİF PREDİKTİVİTESİ VE DOĞRULAMA TESTLERİNİN MALİYETİ
TÜRKİYE CUMHURİYETİ ANKARA ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ KAN BAĞIŞÇILARINDA HBV, HCV, HIV TARAMA TESTLERİNİN DOĞRULANMASI: TARAMA TESTLERİNİN POZİTİF PREDİKTİVİTESİ VE DOĞRULAMA TESTLERİNİN MALİYETİ
Gebelerde Toxoplasma gondii Seropozitifliğinin Değerlendirilmesinde İstenen Testlerin Önerilen Tanı Algoritmasına Uygunluğunun Değerlendirilmesi
 Gebelerde Toxoplasma gondii Seropozitifliğinin Değerlendirilmesinde İstenen Testlerin Önerilen Tanı Algoritmasına Uygunluğunun Değerlendirilmesi Dr.Hilal GÜREL Ankara Numune Eğitim ve Araştırma Hastanesi
Gebelerde Toxoplasma gondii Seropozitifliğinin Değerlendirilmesinde İstenen Testlerin Önerilen Tanı Algoritmasına Uygunluğunun Değerlendirilmesi Dr.Hilal GÜREL Ankara Numune Eğitim ve Araştırma Hastanesi
TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV
 TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV Doç. Dr. Mustafa GÜL Kahramanmaraş Sütçü İmam Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Sunum Planı Transfüzyonla
TRANSFÜZYONLA BULAŞAN HASTALIKLAR TARAMA TESTİYAPILANLAR: HEPATİTLER VE HIV Doç. Dr. Mustafa GÜL Kahramanmaraş Sütçü İmam Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı 1 Sunum Planı Transfüzyonla
CLOSTRIDIUM DIFFICILE ENFEKSİYONUNDA GLUTAMAT DEHİDROGENAZ VE TOKSİN A/B TESTLERİNİN TANI DEĞERİ VE MALİYET ETKİNLİĞİ
 CLOSTRIDIUM DIFFICILE ENFEKSİYONUNDA GLUTAMAT DEHİDROGENAZ VE TOKSİN A/B TESTLERİNİN TANI DEĞERİ VE MALİYET ETKİNLİĞİ Dr. Zahide Doyuk Bektaş Sağlık Bakanlığı Marmara Ünv. Pendik Eğitim Arş. Hastanesi
CLOSTRIDIUM DIFFICILE ENFEKSİYONUNDA GLUTAMAT DEHİDROGENAZ VE TOKSİN A/B TESTLERİNİN TANI DEĞERİ VE MALİYET ETKİNLİĞİ Dr. Zahide Doyuk Bektaş Sağlık Bakanlığı Marmara Ünv. Pendik Eğitim Arş. Hastanesi
Transplantasyon Öncesi Verici ve Alıcının İnfeksiyon Yönünden Taranması. Dr. Filiz Günseren AÜTF Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları AD
 Transplantasyon Öncesi Verici ve Alıcının İnfeksiyon Yönünden Taranması Dr. Filiz Günseren AÜTF Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları AD Transplantasyon Öncesi Alıcı ve Vericilerin İnfeksiyon
Transplantasyon Öncesi Verici ve Alıcının İnfeksiyon Yönünden Taranması Dr. Filiz Günseren AÜTF Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları AD Transplantasyon Öncesi Alıcı ve Vericilerin İnfeksiyon
TEBLİĞ TASLAĞI VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞI
 Türkiye İlaç ve Tıbbi Cihaz Kurumundan: TEBLİĞ TASLAĞI VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞI BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE
Türkiye İlaç ve Tıbbi Cihaz Kurumundan: TEBLİĞ TASLAĞI VÜCUT DIŞINDA KULLANILAN TIBBİ TANI CİHAZLARI İÇİN ORTAK TEKNİK ÖZELLİKLER TEBLİĞİ TASLAĞI BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE
EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU
 EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Aşağıdakilerden hangisi transfüzyon reaksiyonlarından biri değildir? A) Akut hemolitik transfüzyon reaksiyonu B) Akut normovolemik hemodilüsyon
EĞİTİM ÖNCESİ BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Aşağıdakilerden hangisi transfüzyon reaksiyonlarından biri değildir? A) Akut hemolitik transfüzyon reaksiyonu B) Akut normovolemik hemodilüsyon
Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı. Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi
 Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi Akut Hepatit B ve Kronik Hepatit Aktivasyonunun Ayrımı Neden AHB ve KHB-A karışır? Neden AHB ve KHB-A
Akut ve Kronik Hepatit B Aktivasyonunun Ayrımı Dr. Murat Kutlu Pamukkale Üniversitesi Tıp Fakültesi Akut Hepatit B ve Kronik Hepatit Aktivasyonunun Ayrımı Neden AHB ve KHB-A karışır? Neden AHB ve KHB-A
TRANSFÜZYON MERKEZİ HEMOVİJİLANS(İSTENMEYEN CİDDİ ETKİ VE OLAYLARIN BİLDİRİMİ )VE İZLENEBİLİRLİK TALİMATI
 1.AMAÇ.. Kan bağışçısı veya alıcılarda ortaya çıkan istenmeyen ciddi etki ve olaylar ile kan bağışçılarının epidemiyolojik takibinin sağlandığı işlemlerin bütününü tanımlamaktır. 2.KAPSAM : Bu talimat
1.AMAÇ.. Kan bağışçısı veya alıcılarda ortaya çıkan istenmeyen ciddi etki ve olaylar ile kan bağışçılarının epidemiyolojik takibinin sağlandığı işlemlerin bütününü tanımlamaktır. 2.KAPSAM : Bu talimat
P z o itif Nega g ti a f
 Platelia Aspergillus Ag, serum örneklerinde aspergillus galaktomannan antijenini saptayan bir enzyme immun assay testidir. Test invaziv aspergillozis tanısında kullanılmaktadır. Kit prospektüsünde kalibratör
Platelia Aspergillus Ag, serum örneklerinde aspergillus galaktomannan antijenini saptayan bir enzyme immun assay testidir. Test invaziv aspergillozis tanısında kullanılmaktadır. Kit prospektüsünde kalibratör
BOS, idrar, doku, diğer doku ve sıvılarda (DDS) Kalitatif testler (pozitif / negatif sonuç) Kantitatif testler (miktar belirten; viral yük)
 Klinik Viroloji Laboratuvarı testleri: 1. Serolojik testler: Serum veya plazmada antijen ve/veya antikor araştırılması 2. Serum dışı örneklerde (BOS, sürüntü örnekleri, idrar, doku, diğer sıvı örnekleri;
Klinik Viroloji Laboratuvarı testleri: 1. Serolojik testler: Serum veya plazmada antijen ve/veya antikor araştırılması 2. Serum dışı örneklerde (BOS, sürüntü örnekleri, idrar, doku, diğer sıvı örnekleri;
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı. Rehberler Es lig inde Hasta Yo netimi
 Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
Enfeksiyon Bakıs Ac ısı ile Biyolojik Ajan Kullanımı Rehberler Es lig inde Hasta Yo netimi Uz.Dr. Servet ÖZTÜRK Fatih Sultan Mehmet Eğitim ve Araştırma Hastanesi Enfeksiyon Hastalaıkları ve Klinik Mikrobiyoloji
EĞİTİM SONRASI BAŞARI ÖLÇME FORMU
 EĞİTİM SONRASI BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Transfüzyon tarihindeki önemli buluşu (ABO antijenleri tanımı) ile Nobel ödülü alan bilim adamı kimdir? a. Robert Cook b. Anthony Van Löwenhook
EĞİTİM SONRASI BAŞARI ÖLÇME FORMU KATILIMCI: GÖREV YERİ: 1. Transfüzyon tarihindeki önemli buluşu (ABO antijenleri tanımı) ile Nobel ödülü alan bilim adamı kimdir? a. Robert Cook b. Anthony Van Löwenhook
Yöntem ve Test Seçimine Yaklaşım. Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR
 Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
Yöntem ve Test Seçimine Yaklaşım Dr. Alpay Özbek Mikrobiyoloji ve Klinik Mikrobiyoloji AD. Dokuz Eylül Üni. Tıp Fak. İZMİR Literatür Tanı Rehberleri Kongre İyileştirme Ğereksinimi Uzman Klinisyen İsteği
DELİCİ KESİCİ ALET YARALANMALARI VE ALINMASI GEREKEN ÖNLEMLER
 DELİCİ KESİCİ ALET YARALANMALARI VE ALINMASI GEREKEN ÖNLEMLER Hastanelerde Hastaneler enfeksiyon etkenleri bakımından zengin ortamlar Sağlık personeli kan yolu ile bulaşan hastalıklar açısından yüksek
DELİCİ KESİCİ ALET YARALANMALARI VE ALINMASI GEREKEN ÖNLEMLER Hastanelerde Hastaneler enfeksiyon etkenleri bakımından zengin ortamlar Sağlık personeli kan yolu ile bulaşan hastalıklar açısından yüksek
Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji
 Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Sunum Kapsamı HCV tanımı HCV enfeksiyonunun seyri Epidemiyoloji HCV genotiplerinin önemi, dağılımı Laboratuvarımızdaki
Dr. Funda Şimşek SB Okmeydanı EAH Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Sunum Kapsamı HCV tanımı HCV enfeksiyonunun seyri Epidemiyoloji HCV genotiplerinin önemi, dağılımı Laboratuvarımızdaki
TRANSFÜZYON MERKEZİ ÇALIŞMA PROSEDÜRÜ
 AMAÇ: Özel Vitale Hastanesi Kan merkezinde kan ürünlerinin hazırlanması, kan merkezi kan grubu bakma, kan merkezi cross match testi uygulama, kan torbasına kan alma gibi spesifik işlerin tanımlanması yanında
AMAÇ: Özel Vitale Hastanesi Kan merkezinde kan ürünlerinin hazırlanması, kan merkezi kan grubu bakma, kan merkezi cross match testi uygulama, kan torbasına kan alma gibi spesifik işlerin tanımlanması yanında
Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması. Prof. Dr. Yaşar BAYINDIR BUHASDER-2017
 Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması Prof. Dr. Yaşar BAYINDIR BUHASDER-2017 ABD: Solid Organ Nakli 26.034 organ nakli (Ocak-Eylül 2017 arası) 4.491 (%17) canlı verici 21.543 (%83)
Alıcı ve Vericinin Böbrek Transplantasyonuna Hazırlanması Prof. Dr. Yaşar BAYINDIR BUHASDER-2017 ABD: Solid Organ Nakli 26.034 organ nakli (Ocak-Eylül 2017 arası) 4.491 (%17) canlı verici 21.543 (%83)
2. Kapsam 2.1. Sağlık hizmet sunucularındaki acil ve yoğun bakım üniteleri dışındaki birimlerden istenen test istemlerini kapsar.
 AKILCI LABORATUVAR KULLANIMI AKILCI TEST İSTEMİ PROSEDÜRÜ 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını arttırmak
AKILCI LABORATUVAR KULLANIMI AKILCI TEST İSTEMİ PROSEDÜRÜ 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını arttırmak
MEVZUAT HİZMET KALİTE STANDARTLARI, HUKUKSAL SORUNLAR DR.YÜCE AYHAN
 MEVZUAT HİZMET KALİTE STANDARTLARI, VE HUKUKSAL SORUNLAR DR.YÜCE AYHAN KAN VE KAN ÜRÜNLERİ KANUNU Kanun no:5624 Resmi Gazete :02.05.2007/26510 KAN VE KAN ÜRÜNLERİ KANUNU Genel Esaslar Madde 3-c Kan, kan
MEVZUAT HİZMET KALİTE STANDARTLARI, VE HUKUKSAL SORUNLAR DR.YÜCE AYHAN KAN VE KAN ÜRÜNLERİ KANUNU Kanun no:5624 Resmi Gazete :02.05.2007/26510 KAN VE KAN ÜRÜNLERİ KANUNU Genel Esaslar Madde 3-c Kan, kan
AKILICI LABORATUVAR KULLANIMI TEST İSTEM PROSEDÜRÜ
 DOKUMAN BL.PR. 03 İLK YAYIN 16.11.2018 SAYFA 1/ 7 Revizyon Nedeni: 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını
DOKUMAN BL.PR. 03 İLK YAYIN 16.11.2018 SAYFA 1/ 7 Revizyon Nedeni: 1. Amaç 1.1. Prosedürün amacı, sağlık hizmet sunucularında, hastaya doğru tanı konulmasını sağlamak ve test sonuçlarının klinik yararlılığını
EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI
 EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI Nilgün Kaşifoğlu, Tercan Us, Nazmiye Ülkü Koçman, Yurdanur Akgün Eskişehir Osmangazi Üniversitesi Tıp Fakültesi
EPSTEIN-BARR VİRUS ENFEKSİYONLARI TANISINDA ELISA VE İMMUNOBLOT TESTLERİNİN KARŞILAŞTIRILMASI Nilgün Kaşifoğlu, Tercan Us, Nazmiye Ülkü Koçman, Yurdanur Akgün Eskişehir Osmangazi Üniversitesi Tıp Fakültesi
ENFEKSİYON RİSKİNİ AZALTMA YÖNTEMLERİ. Prof.Dr.Halis Akalın Uludağ Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Enfeksiyon Hastalıkları AD
 ENFEKSİYON RİSKİNİ AZALTMA YÖNTEMLERİ Prof.Dr.Halis Akalın Uludağ Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Enfeksiyon Hastalıkları AD Yıllık Bireysel Riskler Yüksek(>1:100): Suçiçeği bulaşı, anneden
ENFEKSİYON RİSKİNİ AZALTMA YÖNTEMLERİ Prof.Dr.Halis Akalın Uludağ Üniversitesi Tıp Fakültesi Mikrobiyoloji ve Enfeksiyon Hastalıkları AD Yıllık Bireysel Riskler Yüksek(>1:100): Suçiçeği bulaşı, anneden
HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi
 HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi Prof Dr Ali Ağaçfidan İstanbul Tıp Fakültesi, Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı İnsan retrovirusları
HIV/AIDS ve Diğer Retrovirus İnfeksiyonları,laboratuvar tanısı ve epidemiyolojisi Prof Dr Ali Ağaçfidan İstanbul Tıp Fakültesi, Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dalı İnsan retrovirusları
Kan Merkezimize Başvuran Donörlerin 10 Yıllık Tarama Sonuçlarının Değerlendirilmesi
 JOPP Derg (3):13-141, 2013 doi:10.222/jopp.2013.13 Araştırma Kan Merkezimize Başvuran Donörlerin 10 Yıllık Tarama Sonuçlarının Değerlendirilmesi Evaluation of 10-Year Screening Test Results in Blood Donors
JOPP Derg (3):13-141, 2013 doi:10.222/jopp.2013.13 Araştırma Kan Merkezimize Başvuran Donörlerin 10 Yıllık Tarama Sonuçlarının Değerlendirilmesi Evaluation of 10-Year Screening Test Results in Blood Donors
Akut Hepatit C Tedavisi. Dr. Dilara İnan Akdeniz ÜTF, İnfeksiyon Hastalıkları ve Kl. Mikr AD, Antalya
 Akut Hepatit C Tedavisi Dr. Dilara İnan Akdeniz ÜTF, İnfeksiyon Hastalıkları ve Kl. Mikr AD, Antalya HCV DSÖ verilerine göre tüm dünya nüfusunun %3 ü (yaklaşık 170 milyon kişi) HCV ile infekte. İnsidans;
Akut Hepatit C Tedavisi Dr. Dilara İnan Akdeniz ÜTF, İnfeksiyon Hastalıkları ve Kl. Mikr AD, Antalya HCV DSÖ verilerine göre tüm dünya nüfusunun %3 ü (yaklaşık 170 milyon kişi) HCV ile infekte. İnsidans;
HCV ENFEKSİYONU SEROLOJİ VE NÜKLEİK ASİT TESTLERİNİN KLİNİK KULLANIMI
 HCV ENFEKSİYONU SEROLOJİ VE NÜKLEİK ASİT TESTLERİNİN KLİNİK KULLANIMI Dr. Ali KAYA Mersin Ü. Tıp Fak. Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HCV enfeksiyonu - tanı Klinik tanı Klinik bulgular
HCV ENFEKSİYONU SEROLOJİ VE NÜKLEİK ASİT TESTLERİNİN KLİNİK KULLANIMI Dr. Ali KAYA Mersin Ü. Tıp Fak. Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HCV enfeksiyonu - tanı Klinik tanı Klinik bulgular
HIV ENFEKSİYONUNUN İMMÜNOLOJİ LABORATUARINDA TAKİBİ
 HIV ENFEKSİYONUNUN İMMÜNOLOJİ LABORATUARINDA TAKİBİ Doç. Dr. Gülderen Yanıkkaya Demirel Yeditepe Üniversitesi Tıp Fakültesi İmmunoloji Anabilim Dalı Bşk Yeditepe Universitesi Hastanesi, Doku Tipleme Laboratuvarı
HIV ENFEKSİYONUNUN İMMÜNOLOJİ LABORATUARINDA TAKİBİ Doç. Dr. Gülderen Yanıkkaya Demirel Yeditepe Üniversitesi Tıp Fakültesi İmmunoloji Anabilim Dalı Bşk Yeditepe Universitesi Hastanesi, Doku Tipleme Laboratuvarı
T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ. SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006
 T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006.. GENELGE 2006/128 Günümüzde kan transfüzyonu uygulamalarının mesleki usul ve
T.C. SAĞLIK BAKANLIĞI TEDAVİ HİZMETLERİ GENEL MÜDÜRLÜĞÜ SAYI: B100THG100004/5190 KONU:Tam Kan kullanımı 23240 * 12.12.2006.. GENELGE 2006/128 Günümüzde kan transfüzyonu uygulamalarının mesleki usul ve
HBV Reaktivasyonunda Rehber Önerileri
 HBV Reaktivasyonunda Rehber Önerileri Dr. Orhan YILDIZ Erciyes Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D. e-mail: [email protected] Lok AS, et al. Hepatology.
HBV Reaktivasyonunda Rehber Önerileri Dr. Orhan YILDIZ Erciyes Üniversitesi Tıp Fakültesi İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D. e-mail: [email protected] Lok AS, et al. Hepatology.
Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD
 Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HÇ, 28 yş, E, Memur 2010 yılı ocak ayında kan bağışı sırasında sarılık olduğu söyleniyor. Başvuru sırasında bazen halsizlik ve
Yrd.Doç.Dr. Özgür Günal Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji AD HÇ, 28 yş, E, Memur 2010 yılı ocak ayında kan bağışı sırasında sarılık olduğu söyleniyor. Başvuru sırasında bazen halsizlik ve
Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay. Dr. Dilek Çolak
 Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay Dr. Dilek Çolak İmmün Yanıt C. Macrophage A. Pathogen B. B cells D. Macrophage E. Macrophage F. T cell G. B cell H. Memory B cells I. Plasma
Klinik Mikrobiyoloji de Enzimli İmmün Deney Enzyme Immuno Assay Dr. Dilek Çolak İmmün Yanıt C. Macrophage A. Pathogen B. B cells D. Macrophage E. Macrophage F. T cell G. B cell H. Memory B cells I. Plasma
BİRİNCİ BASAMAKTA AKILCI LABORATUVAR KULLANIMI
 BİRİNCİ BASAMAKTA AKILCI LABORATUVAR KULLANIMI Doç. Dr. Ayşe Palanduz Aile Hekimliği Anabilim Dalı DERS PLANI TARİH DERS 07.09.2015 Sağlık Hizmetlerinin Basamaklandırılması ve Birinci Basamak Sağlık Hizmetleri
BİRİNCİ BASAMAKTA AKILCI LABORATUVAR KULLANIMI Doç. Dr. Ayşe Palanduz Aile Hekimliği Anabilim Dalı DERS PLANI TARİH DERS 07.09.2015 Sağlık Hizmetlerinin Basamaklandırılması ve Birinci Basamak Sağlık Hizmetleri
Kan Yoluyla Bulaşan Enfeksiyonlardan Korunma ve Riskli Yaralanmaların İzlenmesi
 Kan Yoluyla Bulaşan Enfeksiyonlardan Korunma ve Riskli Yaralanmaların İzlenmesi Sağlık Çalış ışanlarında Enfeksiyon Riski Kan yoluyla bulaşan hastalıklar Sağlık çalış ışanlarında majör bulaş kaynağı kanla
Kan Yoluyla Bulaşan Enfeksiyonlardan Korunma ve Riskli Yaralanmaların İzlenmesi Sağlık Çalış ışanlarında Enfeksiyon Riski Kan yoluyla bulaşan hastalıklar Sağlık çalış ışanlarında majör bulaş kaynağı kanla
TRANSFÜZYON EKİBİ VE HASTANE TRANSFÜZYON KOMİTELERİ. Uz Dr Nil Banu PELİT
 TRANSFÜZYON EKİBİ VE HASTANE TRANSFÜZYON KOMİTELERİ Uz Dr Nil Banu PELİT Tarihçe Bock AV. Use and abuse of blood transfusion. N Engl J Med. 1936 ; 215: 421-425. Fantus B. The therapy of Cook Country Hospital
TRANSFÜZYON EKİBİ VE HASTANE TRANSFÜZYON KOMİTELERİ Uz Dr Nil Banu PELİT Tarihçe Bock AV. Use and abuse of blood transfusion. N Engl J Med. 1936 ; 215: 421-425. Fantus B. The therapy of Cook Country Hospital
Yrd. Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD. Viroloji Ünitesi
 Hepatit C enfeksiyonlarında yeni bir laboratuvar testi: HCV kor (özyapı) antijeni Yrd. Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD. Viroloji Ünitesi Hepatit
Hepatit C enfeksiyonlarında yeni bir laboratuvar testi: HCV kor (özyapı) antijeni Yrd. Doç. Dr. Koray Ergünay MD PhD Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji AD. Viroloji Ünitesi Hepatit
Akreditasyon Sertifikası Eki (Sayfa 1/5) Akreditasyon Kapsamı
 Akreditasyon Sertifikası Eki (Sayfa 1/5) Tıbbi Laboratuar Adresi :Tunus Cad. No:95 Kavaklıdere 06680 ANKARA / TÜRKİYE Tel : 0 312 468 70 10 Faks : 0 312 427 78 74 E-Posta : [email protected] Website
Akreditasyon Sertifikası Eki (Sayfa 1/5) Tıbbi Laboratuar Adresi :Tunus Cad. No:95 Kavaklıdere 06680 ANKARA / TÜRKİYE Tel : 0 312 468 70 10 Faks : 0 312 427 78 74 E-Posta : [email protected] Website
Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık
 Doç. Dr. Onur POLAT Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık personeli gibi hastalardan bulaşabilecek
Doç. Dr. Onur POLAT Travmalı hastaya müdahale eden sağlık çalışanları, hasta kanı ve diğer vücut salgıları ile çalışma ortamında karşılaşma riski bulunan diğer sağlık personeli gibi hastalardan bulaşabilecek
Kan Hizmetleri Genel Müdürlüğü
 Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 10 Mart 2016 www.kanver.org www.kizilay.org.tr KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015 NAT TARAMA TESTİ UYGULAMALARI VE ÖNEMİ KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015
Kan Hizmetleri Genel Müdürlüğü Sunum Tarihi: 10 Mart 2016 www.kanver.org www.kizilay.org.tr KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015 NAT TARAMA TESTİ UYGULAMALARI VE ÖNEMİ KAN HİZMETLERİ GENEL MÜDÜRLÜĞÜ 2015
İstanbul Bölgesi Kan Donörlerinde HBsAg, Anti-HCV ve Anti-HIV Seroprevalansı
 Araştırma İstanbul Bölgesi Kan Donörlerinde HBsAg, Anti-HCV ve Anti-HIV Seroprevalansı Özlem ALTUNTAŞ AYDIN, Hayat KUMBASAR KARAOSMANOĞLU, Asuman KÖKREK, M. Emirhan IŞIK, Özcan NAZLICAN Haseki Eğitim ve
Araştırma İstanbul Bölgesi Kan Donörlerinde HBsAg, Anti-HCV ve Anti-HIV Seroprevalansı Özlem ALTUNTAŞ AYDIN, Hayat KUMBASAR KARAOSMANOĞLU, Asuman KÖKREK, M. Emirhan IŞIK, Özcan NAZLICAN Haseki Eğitim ve
Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi
 Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi 1 Eyvah iğne battı, ne yapmalıyım? 2 İş Kazası İş kazalarını %98
Eyvah iğne battı! Ne yapmalıyım? Acil Uzm. Dr. Esra Kadıoğlu Giresun Üniversitesi Prof. Dr. İlhami Özdemir Eğitim ve Araştırma Hastanesi 1 Eyvah iğne battı, ne yapmalıyım? 2 İş Kazası İş kazalarını %98
İMMUNSUPRESE HASTALARDA PROFİLAKSİ
 İMMUNSUPRESE HASTALARDA PROFİLAKSİ DR GÜLE ÇINAR AYDIN AFYONKARAHİSAR DEVLET HASTANESİ Hematolojik malignitesi olan hastalarda KC disfonksiyonu kemoterapinin sık görülen ve önemli bir komplikasyonu! Major
İMMUNSUPRESE HASTALARDA PROFİLAKSİ DR GÜLE ÇINAR AYDIN AFYONKARAHİSAR DEVLET HASTANESİ Hematolojik malignitesi olan hastalarda KC disfonksiyonu kemoterapinin sık görülen ve önemli bir komplikasyonu! Major
Akut Hepatit B ve Kronik Hepatit B Reaktivasyonu Ayrımı. Dr. Şafak Kaya SBÜ Gazi Yaşargil SUAM Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji
 Akut Hepatit B ve Kronik Hepatit B Reaktivasyonu Ayrımı Dr. Şafak Kaya SBÜ Gazi Yaşargil SUAM Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji HBV Neden Önemli? Dünyada yaklaşık 400 milyon kişi HBV ile
Akut Hepatit B ve Kronik Hepatit B Reaktivasyonu Ayrımı Dr. Şafak Kaya SBÜ Gazi Yaşargil SUAM Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji HBV Neden Önemli? Dünyada yaklaşık 400 milyon kişi HBV ile
MİKROBİYOLOJİ LABORATUVAR HİZMETLERİ
 MİKROBİYOLOJİ LABORATUVAR HİZMETLERİ Laboratuvarda çalışılan tüm testleri içeren test rehberi bulunmalıdır. Test rehberi; Örneklerin çalışılma zamanını, Örnek türünü, Ön hazırlık işlemi gerektiren testlere
MİKROBİYOLOJİ LABORATUVAR HİZMETLERİ Laboratuvarda çalışılan tüm testleri içeren test rehberi bulunmalıdır. Test rehberi; Örneklerin çalışılma zamanını, Örnek türünü, Ön hazırlık işlemi gerektiren testlere
HIV infeksiyonu tanısında doğru algoritmalar. Prof. Dr. Gülden ÇELİK Yeditepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı
 HIV infeksiyonu tanısında doğru algoritmalar Prof. Dr. Gülden ÇELİK Yeditepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı HIV ile infeksiyonun tanısı Erişkinlerde ve 18 aydan büyük çocuklarda:
HIV infeksiyonu tanısında doğru algoritmalar Prof. Dr. Gülden ÇELİK Yeditepe Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı HIV ile infeksiyonun tanısı Erişkinlerde ve 18 aydan büyük çocuklarda:
Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği. Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD
 Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD Akut ve kronik HBV enf da seroloji Akut Hep B de HBe Ag,
Hepatit B de atipik serolojik profiller HBeAg-antiHBe pozitifliği Dr. H. Şener Barut Gaziosmanpaşa Üniversitesi Enfeksiyon Hastalıkları ve KM AD Akut ve kronik HBV enf da seroloji Akut Hep B de HBe Ag,
Korunma Yolları (Üniversal Önlemler)
 Doç. Dr. Onur POLAT Korunma Yolları (Üniversal Önlemler) İlk kez 1987 yılında ABD de hastalık kontrol merkezleri (CDC) tarafından HIV bulaşmasını önlemek amacıyla önerilen yöntemler Üniversal Önlemler
Doç. Dr. Onur POLAT Korunma Yolları (Üniversal Önlemler) İlk kez 1987 yılında ABD de hastalık kontrol merkezleri (CDC) tarafından HIV bulaşmasını önlemek amacıyla önerilen yöntemler Üniversal Önlemler
Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi. Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş
 Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş Giriş Hemodiyaliz hastalarında enfeksiyon önemli mortalite nedenleri arasındadır Hepatit C
Hemodiyaliz olgularında hepatit enfeksiyonu ve önlenmesi Dr Hayriye Sayarlıoğlu, KSÜ, Nefroloji, Kahramanmaraş Giriş Hemodiyaliz hastalarında enfeksiyon önemli mortalite nedenleri arasındadır Hepatit C
Hepatit C ile Yaşamak
 Hepatit C ile Yaşamak NEDİR? Hepatit C kan yoluyla bulaşan Hepatit C virüsünün(hcv) neden olduğu bir karaciğer hastalığıdır. 1 NEDİR? Hepatit C virüsünün birçok türü (genotipi ) bulunmaktadır. Ülkemizde
Hepatit C ile Yaşamak NEDİR? Hepatit C kan yoluyla bulaşan Hepatit C virüsünün(hcv) neden olduğu bir karaciğer hastalığıdır. 1 NEDİR? Hepatit C virüsünün birçok türü (genotipi ) bulunmaktadır. Ülkemizde
ÇALIŞAN SAĞLIĞI BİRİMİ İŞLEYİŞİ Hastanesi
 KİHG/İŞL-005 19.08.2009 07.08.2012 2 1/8 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama 11.11.2009 1 Belge içeriğinde ve belge numarasında değişiklik yapılması 07.08.2012 2 Komite, başlık,
KİHG/İŞL-005 19.08.2009 07.08.2012 2 1/8 GÜNCELLEME BİLGİLERİ Güncelleme Tarihi Güncelleme No Açıklama 11.11.2009 1 Belge içeriğinde ve belge numarasında değişiklik yapılması 07.08.2012 2 Komite, başlık,
İmmünyetmezlikli Konakta Viral Enfeksiyonlar
 İmmünyetmezlikli Konakta Viral Enfeksiyonlar Dr. Dilek Çolak 10 y, erkek hasta Olgu 1 Sistinozis Böbrek transplantasyonu Canlı akraba verici HLA 2 antijen uyumsuz 2 Olgu 1 Transplantasyon öncesi viral
İmmünyetmezlikli Konakta Viral Enfeksiyonlar Dr. Dilek Çolak 10 y, erkek hasta Olgu 1 Sistinozis Böbrek transplantasyonu Canlı akraba verici HLA 2 antijen uyumsuz 2 Olgu 1 Transplantasyon öncesi viral
AFYON BÖLGESİ KAN DONÖRLERİNDE VİRAL ENFEKSİYON ETKENLERİNİN ARAŞTIRILMASI
 ARAŞTIRMA Cilt 58, No 2, S : 61-66 Türk Hij Den Biyol Derg 2001 AFYON BÖLGESİ KAN DONÖRLERİNDE VİRAL ENFEKSİYON ETKENLERİNİN ARAŞTIRILMASI Mustafa ALTINDİŞ 1 Funda KOÇOĞLU 2 ÖZET Ülkemizde kan merkezlerinde
ARAŞTIRMA Cilt 58, No 2, S : 61-66 Türk Hij Den Biyol Derg 2001 AFYON BÖLGESİ KAN DONÖRLERİNDE VİRAL ENFEKSİYON ETKENLERİNİN ARAŞTIRILMASI Mustafa ALTINDİŞ 1 Funda KOÇOĞLU 2 ÖZET Ülkemizde kan merkezlerinde
Dr. Gökay GÖK Ege Bölge Kan Merkezi Müdürü. izmirbkm.org.tr
 Kan ve Kan Ürünleri Kanunu nun 5. Yılı: Yazılanlar ve Uygulananlar Dr. Gökay GÖK Ege Bölge Kan Merkezi Müdürü TÜRK KIZILAYI EGE BÖLGE KAN MERKEZİ TÜRK KIZILAYI FAALİYET ALANLARI Afet Hizmetleri Sağlık
Kan ve Kan Ürünleri Kanunu nun 5. Yılı: Yazılanlar ve Uygulananlar Dr. Gökay GÖK Ege Bölge Kan Merkezi Müdürü TÜRK KIZILAYI EGE BÖLGE KAN MERKEZİ TÜRK KIZILAYI FAALİYET ALANLARI Afet Hizmetleri Sağlık
CROSSMATCH (ÇAPRAZ KARŞILAŞTIRMA TESTİ)
 CROSSMATCH (ÇAPRAZ KARŞILAŞTIRMA TESTİ) Dr. İhsan Karadoğan V. Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kongresi 18-22 Kasım 2012 Antalya 1111 1111 1111 1111 UYGULAMA BASİT YORUM SON DERECE KARMAŞIK
CROSSMATCH (ÇAPRAZ KARŞILAŞTIRMA TESTİ) Dr. İhsan Karadoğan V. Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kongresi 18-22 Kasım 2012 Antalya 1111 1111 1111 1111 UYGULAMA BASİT YORUM SON DERECE KARMAŞIK
Hematolog bakış açısıyla hemovijilansın transfüzyon güvenliğini artırmadaki rolü
 Hematolog bakış açısıyla hemovijilansın transfüzyon güvenliğini artırmadaki rolü 28.10.2017 12. Ulusal Aferez Kongresi Dr. Neslihan Andıç Eskişehir Osmangazi Üniversitesi Erişkin Hematoloji BD Sunum planı
Hematolog bakış açısıyla hemovijilansın transfüzyon güvenliğini artırmadaki rolü 28.10.2017 12. Ulusal Aferez Kongresi Dr. Neslihan Andıç Eskişehir Osmangazi Üniversitesi Erişkin Hematoloji BD Sunum planı
ÖRNEK KABUL VE SONUÇ VERME GÜNÜ LİSTESİ. ÖRNEK KABUL GÜN ve SAATİ
 TEST ADI ÖRNEK KABUL GÜN ve SAATİ SONUÇ VERME GÜN ve SAATİ KÜLTÜRLER Boğaz Kültürü 3 gün sonra İdrar Kültürü 3 gün sonra Balgam Kültürü 4 gün sonra Kan Kültürü 7 gün sonra Dışkı Kültürü 4 gün sonra Diğer
TEST ADI ÖRNEK KABUL GÜN ve SAATİ SONUÇ VERME GÜN ve SAATİ KÜLTÜRLER Boğaz Kültürü 3 gün sonra İdrar Kültürü 3 gün sonra Balgam Kültürü 4 gün sonra Kan Kültürü 7 gün sonra Dışkı Kültürü 4 gün sonra Diğer
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı:
 Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
Klinik Mikrobiyoloji Laboratuarında Validasyon ve Verifikasyon Kursu 12 Kasım 2011 Cumartesi Salon C (BUNIN SALONU) Kursun Amacı: Katılımcılara; klinik mikrobiyoloji laboratuarlarında doğru, geçerli ve
Araştırma. Demet Çelebİ*, Özgür Çelebİ**, Ülkü Altoparlak***, Ahmet Nezih Kök**** GİRİŞ
 Türk Mikrobiyol Cem Derg 42(4):37-4, 202 doi:0.5222/tmcd.202.37 Araştırma Kan Donörlerinde HBsAg, Anti-HCV, Anti-HIV, Sifiliz Seroprevalansı ve Macro-ELISA Sonuçlarının Optik Dansite Değerleri ile Doğrulama
Türk Mikrobiyol Cem Derg 42(4):37-4, 202 doi:0.5222/tmcd.202.37 Araştırma Kan Donörlerinde HBsAg, Anti-HCV, Anti-HIV, Sifiliz Seroprevalansı ve Macro-ELISA Sonuçlarının Optik Dansite Değerleri ile Doğrulama
VİRAL HEPATİTLER 5. Sınıf Entegre Ders. Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU
 VİRAL HEPATİTLER 5. Sınıf Entegre Ders Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU Kronik Viral Hepatitler Sporadik Enfeksiyon ENDER HBV HCV HDV Ulusal Aşılama Programı Erişkinlerin Sorunu HFV, HGV,
VİRAL HEPATİTLER 5. Sınıf Entegre Ders Prof. Dr. Fadıl VARDAR Prof. Dr. Sema AYDOĞDU Kronik Viral Hepatitler Sporadik Enfeksiyon ENDER HBV HCV HDV Ulusal Aşılama Programı Erişkinlerin Sorunu HFV, HGV,
KAN YOLUYLA BULAŞAN ENFEKSİYONLAR
 KAN YOLUYLA BULAŞAN ENFEKSİYONLAR Prof. Dr. Oğuz KARABAY BU sunularda UHESA sunularından yararlanmıştır. UHESA ya ve eğitmenlerine teşekkürü borç biliriz. 1 Sunum Özeti BU derste verilmek İstenenler!!!
KAN YOLUYLA BULAŞAN ENFEKSİYONLAR Prof. Dr. Oğuz KARABAY BU sunularda UHESA sunularından yararlanmıştır. UHESA ya ve eğitmenlerine teşekkürü borç biliriz. 1 Sunum Özeti BU derste verilmek İstenenler!!!
