KARBOKSİLLİ ASİTLER. İsimlendirilmeleri CH 3 CH C OH CH 3 CH CH COOH
|
|
|
- Duygu Güçlü
- 7 yıl önce
- İzleme sayısı:
Transkript
1 İsimlendirilmeleri Karbonil grubuna bir hidroksil bağlanması ile oluşan yapıya karboksil grubu, bu grubu taşıyan -CH yapısındaki bileşiklere ise karboksilli asitler denir. KABKSİLLİ ASİTLE CH Karboksilli asit Birden fazla karboksil grubu içeren bileşiklere di, tri vb. karboksilli asitler, karboksil grubundan başka halojen içerenlere haloasitler, amino grubu içerenlere aminoasitler vb. isimler verilir. CH 3 CH CH 2 1 CH 2 CH 3 2-Metilbütan-1,4-dioik asit 4 Alifatik karboksilli asitlerden birçoğu doğal kaynaklardan elde edilmiş ve özel isimler verilmiştir. Bu isimlerin çoğunluğu geleneksel sistemde de kullanılır. HCH Formik asit CH 3 CH Asetik asit IUPAC sisteminde alifatik karboksilli asitler, molekülün karboksil karbonunun da dahil olduğu en uzun zincir esas alınarak isimlendirilir; söz konusu zincir hidrokarbon gibi isimlendirilip, bu ismin sonuna oik asit eki getirilir. Cl α CH 3 CH C H CH 3 CH CH CH 3 2 α-kloropropiyonik asit 2-Kloropropanoik asit 1 Krotonik asit 2-Bütenoik asit Sikloalifatik, aromatik ve heterosiklik karboksilli asitlerin isimlendirilmesinde ise, karboksil grubunun bağlı olduğu ana yapının ismine karboksilik asit kelimeleri eklenir. Konumlar rakamlarla gösterilir. α CH β 1 CH 4 β-naftoik asit Naftalen-2-karboksilik asit 2 1 N İzonikotinik asit Piridin-4-karboksilik asit 1
2 Alifatik bileşiklerde numaralandırmaya karboksil grubu karbonundan başlanır. Siklik bileşiklerde, halka sistemleri belirlenmiş kurallara göre numaralandırılır; ancak karboksil grubuna ya ilk numara verilir ya da en küçük numara verilecek yön izlenir. Karboksil grubu isimlendirme bakımından öncelikli bir grupdur. Bu nedenle poli fonksiyonel bileşikler, karboksil grubuna göre isimlendirilirler Cl CH 2 CH CH 3-Kloro-2-metilpropanoik asit CH 3 H H CH 2 CCH 2 CH CH 3 3,4-Dihidroksi-3-metilbütanoik asit Karboksil grubundaki hidroksilin çıkması ile kalan -C- yapısındaki kısma açil grubu adı verilir. Açil grubları geleneksel sistemde de, IUPAC sisteminde de türedikleri asidin isminin sonundaki ik ekinin yerine il eki getirilerek isimlendirilirler. CCH NH C 2 Elde Edilmeleri 1. Nitrillerin hidrolizi Hidroliz işlemi genellikle sıcakta, hidroklorik, sülfürik ve bazen fosforik asit gibi mineral asitler veya alkali hidroksitlerin katalizörlüğündeğ yürütülür. H 2 S 4, ısı H 2 S 4, ısı 2-Benzoil amino naftalen 1-Asetilnaftalen 2. ksidasyon eaksiyonları ksidasyon işlemi, krom trioksit-sülfürik asit, potasyum permanganat, nitrik asit vb. ajanlarla yapılabilir. Aldehitlerin oksidasyonlarında, özellikle molekülde oksidasyona hassas başka grubların bulunması halinde gümüş oksit tercih edilir. (CH 3 ) 3 CCHC(CH 3 ) 3 CH 2 H 2-tert-butil-3,3-dimetil-1-butanol K 2 Cr 2 7 H 2, H 2 S 4 K 2 Cr 2 7 CH H 2 S 4, H 2 Furfural Furan-2-karbaldehit (CH 3 ) 3 CCHC(CH 3 ) 3 CH 2-tert-butil-3,3-dimetilbutanoik asit Furoik asit CH Furan-2-karboksilik asit 2
3 Metil grubu içeren aromatik bileşiklerde, bu grup okside edilerek karboksil haline dönüştürülür. eaksiyonun alifatik karboksilli asitlerin sentezlerinde uygulanması sınırlı olmakla beraber bazı örnekleri bulunmaktadır. **** CH 3 CH CH 3 N 2 3-Metoksi-4-nitrotoluen 1. KMn 4, H - 2. H CH 3 N 2 3-Metoksi-4-nitrobenzoik asit -2 veya ısı 3. Grignard bileşiklerinin karbon dioksitle reaksiyonu Polarlaşan C atomuna Grignard bileşiğinin metil grubu hücum eder. luşan ara ürünün HBr veya HCl gibi asitlerle muamelesi ile asetik asit elde edilir. x oksidasyon oksidasyon oksidasyon ısı Fiziksel Özellikleri Normal şartlarda küçük moleküllü alifatik karboksilli asitler sıvı, diğer bütün asitler katıdır. Karbonil grubunda karbon-oksijen arasında kuvvetli bir dipol bağı vardır, hidroksil grubundaki oksijen-hidrojen bağı da alkollerdekinden daha kuvvetle polarize olur. Karboksilli asitlerde hidrojen bağları çok kuvvetlidir. Bu nedenle erime ve kaynama derecelerinin aynı sayıda karbon içeren alkol, eter ve hidrokarbonlardan çok daha yüksektir. H 2-Metil-1-büten 2-Bütanon 2-Bütanol Propanoik asit H 31 0 C 80 0 C 99 0 C C 3
4 Karboksil grubunun bütün atomları ve radikal grubunun bağlanma atomu, karbonil karbonu ve hidroksil oksijeninin orbital düzenleri nedeni ile aynı düzlem üzerinde yer alır; bağ açıları 120 civarındadır. Formik asit : : C H Formik asitte karbon ve her iki oksijen sp 2 hibriti oluşturur. Asetik asitte hidrojen bağı. Asetik asitin elektrostatik potansiyel haritası δ- δ δ δ - Asetik asitte çekim kuvvetleri, bir molekülün oksijeni ile diğer molekülün -H grubunun protonundan kaynaklanır. Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu Asetik asitin H grubunun hidrojen atomu düşük elektron yoğunluğu bölgesindedir ve asidiktir (pka~5). Nükleofilik açil sübstitüsyon reaksiyonları ile karboksilik asit türevlerine dönüştürülür. Asetat (etanoat) iyonunun elektrostatik potansiyel haritası Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu Karbondioksit (-C - 2 ) grubunun her iki oksijen atomu yüksek elektron yoğunluğu bölgesindedir. Karbonil oksijeninden dolayı bazik veya nükleofilik davranış gösterir. Sodyum stereat uzun hidrokarbon zincirinin bir ucunda polar, iyonik karboksilat grubuna sahiptir. Bu karboksilat grubu hidrofiliktir ve su moleküllerine hidrojen bağı ile bağlanarak molekülü çözünür hale getirme eğilimi gösterir. Hidrokarbon zinciri hidrofobiktir. Sodyum stereat suya bırakıldığında misel adı verilen küresel yığınlar oluşur. - CH 3 (CH 2 ) 16 CNa Sodyum stereat (Sodyum oktadekanoat) 4
5 Deterjanlar, sabunlar gibi, misel davranışıyla temizleme özelliği gösteren maddelerdir. Karboksilli asit molekülleri su molekülleri ile de etkileşebildiklerinden küçük moleküllü alifatik asitler suda çok çözünürler. Çözünürlük alkil zincirinin uzamasına bağlı olarak azalır. Kimyasal Özellikleri 1. Asitlik I. İçerdiği karbonil grubu nedeniyle -H bağı zayıflar. CH C - H II. Karboksilat iyonundaki rezonans H in ortama kolayca bırakılmasını sağlar. Karboksilik asitin 3 rezonans formu vardır. III. İndüktif Etki: Halojenler, hidroksil, siyano, karboksil ve metoksil gibi indüktif yolla elektron çekici gruplar (-I), karboksilli asitin asitliğini artırmaktadır. İndüktif etki mesafe arttıkça azalır. -N 2 >-S 2 >-CN>-CH>-CH> -C>F>Cl>Br>I>-CH 3 >-H> -SH > -C 6 H 5 > -C=CH > -CH=CH 2 >-CH 3 Nükleofillere karşı etkinlik sırası; Açil klorürler, kararlılığı en az etkinlikleri en fazla olan asit türevleridir. Nükleofilik Açil Sübstitüsyon 2. Karboksilli asitler, kalsiyum oksit, baryum oksit, alkali hidroksitler veya piperidin, piridin gibi organik bazlar karşısında ısıtıldıklarında, termal dekompozisyon sonucu dekarboksilasyona uğrarlar. 5
6 3. Isıtıldıkları zaman iki molekül asitten bir molekül su çıkarak, asit anhidritleri oluşur. eaksiyonun iki değişik asitle uygulanmasından karışım anhidritler elde edilebilir. 4. Tiyonil klorür ve fosforlu klorlama ajanları ile ısıtıldıklarında, karboksil hidroksili yerine klor sübstitüsyonu olur ve asit klorürleri oluşur. Diğer fosforlu halojenleme ajanları ile de benzer ürünler elde edilebilir. ısı asit anhidrit Trietilamin veya asit klorür HCl 5. Ester sentezi- Fisher Esterleşmesi Karboksilli asitler, alkol ve fenollerle ısıtıldığında esterler oluşur. Genellikle sülfürik asit, hidroklorik asit, fosforik asit ve p-toluensulfonik asit gibi katalizörler karşısında, sıcakta çalışılır. CH 2 H 'CH asitten CH 2 C' alkolden H 2 CH 3 H CH 3 CHCH 2 CH 3 H C H C CH 3 H 2 H 2 S 4 sek-bütil alkol Benzoik asit CH 3 CH H 2 S 4 Metil benzoat CH 3 CCHCH 2 CH 3 CH 3 H 2 sek-bütil asetat 6. Karboksilli asitler, katalitik hidrojenasyona, sodyum bor hidrür, sodyum hidrür ve diğer alışılmış laboratuar hidrojenleme ajanlarına karşı dirençli bileşiklerdir. ş Sadece lityum aluminyum hidrürle yavaşça redüklenerek alkollere dönüşürler. baz baz ısı ısı baz Açil klorür Asit anhidrit Ester Amit Karboksilat 6
7 KABKSİLLİ ASİT TÜEVLEİ KABKSİLLİ ASİT TÜEVLEİ ESTELE ESTELE Karboksilli asit esterleri, alkollerin veya fenollerin açillenmesi, diğer bir ifade ile karboksil grubundaki hidroksilin bir alkoksi veya fenoksi grubu ile yer değiştirmesi sonucu oluşan bileşiklerdir. ksijen içeren heterosiklik halkalarda, oksijene komşu konumda bir karbonil bulunması halinde, halka içi ester oluşur; bu tip bileşiklere lakton adı verilir. İsimlendirilmeleri Esterler,oluştukları alkol veya fenole ait radikalin ismine, asidin isminden ik asit çıkarılıp sonuna -at eki getirilerek isimlendirilirler. C' Ester H H C C C H Lakton CH 3 CC 2 H 5 Asetik asitten gelen kısım Etilasetat etanolden gelen kısım Büyük ve karmaşık moleküllü bileşiklerin isimlendirilmeleri ana yapılarına göre yapılıp, ester grubu ana yapının isminin başında, sübstitüent ismi gibi belirtilebilir; bu durumda ester grubu açil grubunun ismine oksi eki getirilerek gösterilir. CCH 2 CH 2 CHCH 3 Cl Siklopentil γ-klorovaleryanat Siklopentil 4-kloropentanoat 4-Kloropentanoiloksisiklopentan CC 2 H N Etil izonikotinat Etil piridin-4-karboksilat CH 3 CH 2 C Siklobutil propanoat Siklobutil etil karboksilat 7
8 CH 3 CCH 2 CH 2 CH(CH 3 ) 2 3-Metilbütil asetat Muzun özgün kokusu Elde Edilmeleri 1. Esterlerin elde edilmelerinde en çok kullanılan yöntem, alkol veya fenollerin karboksilli asitlerle esterleştirilmeleridir. eaksiyon tersinir özelliktedir; oluşan suyun ortamdan uzaklaştırılması, ş ortama katalitik miktarda derişik sülfürik asit ilave edilmesi ester oluşumunu kolaylaştırır. 2. Alkollerin esterleştirme işlemi, asit klorürleri ile gerçekleşir. eaksiyonda oluşan hidrojen klorürün tutulması için alkali hidroksitlerin sulu çözeltileri, piridin, N,N-dimetilanilin vb. bazik ajanlar karşısında çalışılabilir (Schotten-Baumann reaksiyonu). N 2 (CH 3 ) 2 CHCH 2 H CCl N 2 piridin N 2 CCH 2 CH(CH 3 ) 2 N 2 izobütil alkol 3,5-dinitrobenzoil klorür izobütil 3,5-dinitrobenzoat CCl 'H C' HCl piridin 3. Alkoller asit anhidritleri ile de kolaylıkla esterleştirilebilirler; reaksiyonda katalizör olarak derişik sülfürik asit, susuz çinko klorür, asetil klorür, sodyum asetat veya alkali hidroksitler kullanılabilir. 4. Karboksilli asitlerin sodyum, potasyum, baryum, kalsiyum veya gümüş tuzları ile halojenli bileşiklerin reaksiyonları sonucunda da esterler oluşur; reaksiyon genellikle sıcakta yürütülür. C 'H C' CH CNa ' X C' NaX 8
9 5. Esterlerde alkol değişmesi; C' ''H C'' ' H Fiziksel Özellikleri Birçok ester doğal olarak bulunur. Esterler özel ve hoş kokulu maddelerdir. Meyve ve çiçeklerin kokulu yağlarının önemli bir kısmını oluştururlar. 3-Metilbütil asetat gıdalarda meyve aroması üretiminde kullanılır. Normalşartlarda küçük moleküllü alifatik esterler sıvı, diğerleri katıdır. Suda genellikle az çözünürler, organik çözücülerde çözünürler. Metil etanoatın elektrostatik potansiyel haritası Karboksilik asit Açil klorür Asit anhidrit Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu Karbonilin oksijen atomu yüksek elektron yoğunluğu bölgesindedir. Ester Amit Kimyasal Özellikleri 1. Sulu ortamda hidroliz olarak, kendilerini oluşturan asit ve alkollere ayrışırlar. Asit ve alkaliler ile ısı reaksiyonu hızlandırır. Mekanizması; ısı 9
10 2. Sıvı amonyak veya derişik amonyak çözeltisi ile amitleri verirler. Primer ve sekonder aminlerle ısıtıldıklarında ise sübstitüe amitler oluşur. 3. Esterler, alkollü ortamda metalik sodyum (Bauveault-Blanc reaksiyonu), lityum aluminyum hidrür ve katalizör karşısında hidrojenle redüklenerek alkollere dönüşürler. C' NH 3 CNH ' 2 H Amonyak C' H 2 N'' CNH'' ' H Primer amin Mekanizması; 4. rganometalik bileşiklerin esterlerin karbonil grubuna katıldığında da öncelikle ketonlar elde edilir. luşan bu keton bileşiğine ortamda bulunan grignard bileşiği ile tekrar reaksiyona girerek tersiyer alkoller elde edilir. KABKSİLLİ ASİT TÜEVLEİ ANHİDİTLE baz 10
11 Karboksilli asit anhidritleri, iki molekül karboksilli asitten bir molekül su çıkması ile oluşmuş (C) 2 genel yapısında bileşiklerdir. Aynı asidin iki molekülünden su çıkışı ile oluşan anhidritlere basit anhidritler, farklı iki asitten oluşan anhidritlere ise karışım anhidritler denir. C ' C Dibazik asitler, intermoleküler su çıkışı ile siklik yapıda anhidrit oluştururlar. Genellikle kullanılan ve anhidrit tabirinin çağrıştırdığı bileşikler, basit ya da siklik anhidritlerdir. (CH 2 )n CH 2 C CH 2 C siklik anhidrit İsimlendirilmeleri Anhidritler, türedikleri asit veya asitlerin isimlerine anhidrit kelimesi eklenerek isimlendirilirler. (CH 3 C) 2 Asetik anhidrit (CH 3 CHCH 2 CH 2 C) 2 Cl 4-Kloropentanoik anhidrit CH 3 CH 3 CH 2 C C Asetik propanoik anhidrit Elde Edilmeleri 1. Karboksilli asit anhidritlerinin elde edilmeleri için klasik yöntem, asitlerin sodyum, potasyum veya gümüş tuzlarının açillenmesidir. eaksiyon oda sıcaklığında yürür. Bu yöntemle de hem basit, hem de karışım anhidritler elde edilebilir. CNa CCl C NaCl 2. Asitlerin asit klorürleri ile açillenmesi, anhidritlerinin elde edilmeleri için en iyi yöntemdir. Bu yöntemde genellikle sıcakta ve piridin karşısında çalışılır. Farklı asit ve asit halojenürü kullanarak karışık anhidritlerin sentezi yapılabilir. CH CCl HCl 3. Isıtıldıkları zaman iki molekül asitten bir molekül su çıkarak, asit anhidritleri oluşur. eaksiyonun iki değişik asitle uygulanmasından karışım anhidritler elde edilebilir. ısı asit anhidrit 11
12 3. Esterler çinko klorür karşısında asit klorürleri ile ısıtıldıklarında, kullanılan ester ve asit klorürü cinsine bağlı olarak basit veya karışım anhidritler oluşur. C CCl C Cl Fiziksel Özellikleri Normal şartlarda küçük moleküllü asit anhidritleri sıvı, diğerleri katı halde bulunur. Sıvıların kaynama dereceleri, türedikleri asitlerinkinden daha yüksektir. Genellikle karakteristik kokulu ve tahriş edici i maddelerdir. di rganik çözücülerde çözünürler. Etanoik anhidritin elektrostatik potansiyel haritası Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu Kimyasal Özellikleri 1. Alkoller asit anhidritleri ile de kolaylıkla esterleştirilebilirler; reaksiyonda katalizör olarak derişik sülfürik asit, susuz çinko klorür, asetil klorür, sodyum asetat veya alkali hidroksitler kullanılabilir. Bu reaksiyon kullanılan alkol primer veya sekonder ise kolay yürür ve ürün esterdir. Tersiyer alkollerde ise alken oluşur. C 'H C' CH 2.Suluortamdayadahavanın rutubetiile türedikleri asitlere dönüşürler. C H 2 2CH 3. Aminlerin açillenmesi Primer ve sekonder aminler asit anhidrit gibi açilleme ajanları ile N-sübstitüe amitleri elde edilir. CH 3 C CH 3 C HN' CN' N,N-disübstitüe amit 12
13 4. Friedel-Crafts açilasyonu, Karboksilik asit anhidritleri, alüminyum klorürlü ortamda aromatik halkayı açillerler. CC AlCl 3 C CH baz CH3 CH 3 CCCH 3 AlCl 3 CH 3 CCH 3 Anizol Asetik anhidrit p-metoksiasetofenon 5. Peroksitlerle oksitlendiklerinde perasit, lityum aluminyum hidrürle veya katalizör karşısında hidrojenle redüklendiklerinde önce aldehit, daha ileri redüksiyon sonucunda ise alkollere dönüşürler. (C) 2 H CH H 2 perasit (C) 2 2 H 2 CH H 2 KABKSİLLİ ASİT TÜEVLEİ ASİT HALJENÜLEİ Karboksilli asit halojenürleri, karboksil grubundaki hidroksilin bir halojen ile yer değiştirmesi ile oluşmuş -CX genel yapısında bileşiklerdir. İsimlendirilmeleri İsimleri, ik asit yada oik asit ekleri ile biten asitlerden türeyen asit halojenürleri, içerdikleri açil grubunun ismine halojen ismi ve -ür eklenerek isimlendirilirler. CH 3 CCl ClCH 2 CCl CH 3 CHCH 2 CH 2 CCl Cl Asetil klorür Kloroasetil klorür 4-Kloropentanoil klorür 13
14 Karboksilik asit şeklinde bitenlerin halojenürleri ise, içerdikleri ana yapının ismine, karbonil sözcüğü, halojen ismi ve -ür eklenerek isimlendirilirler. CCl Siklopentan karbonilklorür Kompleks yapılarda, ya da molekülde isimlendirme bakımından asit halojenüründen daha öncelikli grupların bulunması halinde, grup ismin başında, haloformil (kloroformil-, bromoformilgibi) şeklinde, sübstitüent gibi yazılır. CCl 2 1 CH 2-Kloroformilsiklopentan karboksilik asit Elde Edilmeleri 1.Asit klorürlerinin elde edilmelerinde en çok uygulanan yöntem, asitlerin tiyonil klorür ile piridin gibi bir baz varlığında ısıtılmasıdır. Bu reaksiyonda karboksilik asitler yerine bunların tuzları, esterler veya anhidritleri de kullanılabilir. CH SCl 2 CCl S 2 HCl CNa SCl 2 CCl S 2 NaCl C' SCl ' 2 CCl S 2 Cl (C) 2 SCl 2 2 CCl S 2 2.Karboksilli asitlerin, asit klorürü haline dönüştürülmelerinde fosfor triklorür, fosfor pentaklorür veya fosfor oksiklorürden de yararlanılabilir. 3 CH PCl 3 CCl H 3 P 3 CH PCl 5 CCl PCl 3 Fiziksel Özellikleri Asit halojenürleri normal şartlarda genellikle sıvı maddelerdir. Erime ve kaynama dereceleri, türedikleri asitlerden çok daha düşüktür. Çoğunlukla tahriş edici kokuya sahiptirler. rganik çözücülerde çözünürler. Kimyasal bakımdan çok aktif bileşiklerdir; reaksiyonlarının çoğunluğu ekzotermik ve şiddetlidir. Etil klorürün elektrostatik potansiyel haritası Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu 14
15 Zayıf rezonans kararlılığı.. - Cl Cl Açil klorürlerdeki rezonans kararlılığı karboksilik asitlerin diğer türevlerindeki kadar değildir. Karbon-klor bağı uzun bir bağdır. Klorun 3p orbitali ile karbonil grubunun π orbitalinin örtüşmesi zayıftır. Bu nedenle klorun elektron çiftlerinin π sistemi içindeki delokalizasyonu zayıf olur. Bir açil klorürün karbonil grubu, klor atomunun elektron verme etkisinden daha çok, elektron çekici indüktif etkisini hisseder. Bu durum, açil klorürün karbonil karbonunu diğer karboksilik asit türevlerine göre nükleofilik etkilere daha istekli hale getirir. Kimyasal Özellikleri 1. Sulu ortamda veya havanın rutubetinden etkilenerek parçalanır ve karboksilli asitlere dönüşürler. CCl H 2 CH HCl 2. Karboksilli asitler veya tuzları asit klorürleri ile açillenmesi, anhidritlerinin elde edilmeleri için en iyi yöntemdir. Bu yöntemde genellikle sıcakta ve piridin karşısında çalışılır. Farklı asit ve asit halojenürü kullanarak karışık anhidritlerin sentezi yapılabilir. CH CCl HCl 3. Aromatik bileşiklerin Friedel-Crafts açilleme tepkimesi: Açil klorürleri ve karboksilik asit anhidritleri, alüminyum klorürlü ortamda aromatik halkayı açillerler. l Mekanizması; yavaş Hem karbon, hem de oksijen, azot, kükürt vb. heteroatomlar üzerinden açilleme yapabilirler. hızlı 15
16 4. Asit halojenürleri, amonyak ve primer ya da sekonder aminlerle de soğukta, kolaylıkla reaksiyon verirler; amitler meydana gelir. CCl 2 NH 3 CNH 2 NH 4 Cl - CCl 2 'NH 2 CNH' 'NH 3 Cl - 5. Peroksitlerle oksitlendiklerinde perasit, lityum aluminyum hidrürle veya katalizör karşısında hidrojenle redüklendiklerinde önce aldehit, daha ileri redüksiyon sonucunda ise alkollere dönüşürler. CCl H 2 2 CH HCl perasit CCl H 2 CH HCl KABKSİLLİ ASİT TÜEVLEİ AMİTLE baz Amonyak veya primer ya da sekonder aminlerin açillenmesi, diğer bir ifade ile karboksil grubundaki hidroksilin, bir amonyak veya primer ya da sekonder amin artığı ile yer değiştirmesi sonucu oluşmuş -CNH 2 genel yapısında bileşiklere amit denir. Amitler, azot üzerinde bir veya iki tane radikal taşıyabilirler veya nonsübstitüe olabilirler. Azota bağlanan bu gruplar, birbirinin aynı veya farklı, alifatik, sikloalifatik, aromatik yada heterosiklik yapıda olabilirler. NH 2 NH N 2 Nonsübstitüe amit Monosübstitüe amit Disübstitüe amit 16
17 İsimlendirilmeleri Nonsübstitüe amitler, türedikleri asitin isminin sonundaki ik asit yada oik asit eki kaldırılıp, yerine amit kelimesi getirilerek isimlendirilirler. Sübstitüe amitlerde, ismin başında - sübstitüentin azot üzerinde olduğunu göstermek için -Nharfi ve daha sonra sübstitüentlerin isimleri yazılır. CH 3 CNH 2 CH 3 CNHCH 3 CH 3 CN(CH 3 ) 2 CNH 2 (CH 3 ) 2 CHCH 2 CNH 2 Benzamit CH 3 CH 2 CH 2 CNCH CH 3 3-Metilbütanamit CH 3 CH 3 N-izopropil-N-metil-bütanamit Asetamit N-Metilasetamit N,N-Dimetilasetamit Elde Edilmeleri 1. Karboksilli asitlerin amonyum veya amin tuzları pirolize edildiklerinde, bir denge reaksiyonu ile amit haline dönüşürler. eaksiyon, karboksilli asitlerin amonyak veya aminlerle ısıtılması suretiyle de yürütülebilir. CH NH 3 C - NH 4 CNH 2 H 2 CH NH 2 CNH Anilin H 2 N-Fenilbenzamit 2. Aminlerin açillenmesi Primer ve sekonder aminler asit anhidrit gibi açilleme ajanları ile N-sübstitüe amitler elde edilir. CH 3 C CH 3 C HN' CN' N,N-disübstitüe amit Amonyak, primer ve sekonder aminler asit klorürler gibi açilleme ajanları ile amitler elde edilirler. CCl 2 NH 3 CNH 2 NH 4 Cl - Nonsübstitüe amit 3. Sıvı amonyak veya derişik amonyak çözeltisi ile amitleri verirler. Primer ve sekonder aminlerle ısıtıldıklarında ise sübstitüe amitler oluşur. C' NH 3 CNH ' 2 H Amonyak CCl 2 NH 3 CNH 2 NH 4 Cl Benzoilklorür Benzamit C' H 2 N'' CNH'' ' H Primer amin 17
18 Fiziksel Özellikleri Normal şartlarda formamit sıvı, diğer bütün nonsübstitüe amitler -kuvvetli intermoleküler etkileşmeler nedeni ilekatıdır. Küçük moleküllü mono ve di sübstitüe amitler, intermoleküler etkileşmelerin azalmış olması nedeni ile sıvıdır. Alifatik amitlerden ilk beş tanesi suda çözünür. Sıvı amitler organik bileşikler için çok iyi çözücüdürler. Özellikle N,N-dimetil formamit, birçok sentez çalışmasında çözücü olarak kullanılmaktadır. Etanamit elektrostatik potansiyel haritası Çok etkili rezonans kararlılığı N' 2 N' 2 - Kırmızı: Yüksek elektron yoğunluğunu Mavi: Düşük elektron yoğunluğunu Azottan elektron verilmesi amit karbonilini kararlı kılar ve nükleofilik atakların hızını azaltır. Nükleofiller, molekülün elektrofilik kısmına atak yapar. Kimyasal Özellikleri 1. Asit ve alkali hidroksitlerin sulu çözeltileri ile ısıtıldıklarında hidroliz olurlar; asit hidrolizde karboksilli asit ve amonyum tuzu, alkali hidrolizde karboksilli asit tuzu ve amonyak oluşur. 2. Amidlerin redüksiyonu Azot üzerinde en az bir hidrojen bulunan amidlerin redüksiyonu sonucu aminler elde edilirler. ısı 18
19 CH 2 Cl NaCN CH 2 CN H 2 H 2S 4 CH 2 CH Benzil klorür Benzil siyanür Fenil asetik asit H H 1.NaCN CH 3 C(CH 2 ) 2 CH 3 H 2. H 3C(CH 2 ) 2 CH 2 3 HCl CH 3 C(CH 2 ) 2 CH 3 CN CH 2-Pentanon 2-Siyano-2-pentanol 2-Hidroksi-2- metilpentanoik asit 1 3 CH 2 CH SCl 2 1 CH 3 CH 3 3 CH 2 CCl 3-Metoksifenil asetik asit 3-Metoksifenil asetil klorür CH 2 CCl CH 2 NH 2 CH 2 CNHCH 2 C 6 H 5 Fenil asetil klorür Benzil amin N-Benzilfenilasetamit CH 3 CH CCl FCH 2 CCH 2 CH 3 H 2 NH 3 FCH 2 CNH 2 C 2 H 5 H K 2 Cr 2 7 H 2, H 2 S 4 SCl 2 Etil floroasetat Amonyak Floroasetamit Etanol Toluen Benzoik asit Benzoil klorür etileter =Alkil, vinil, aril CC 2 H 5 Primer alkol Sekonder alkol Tersiyer alkol CH 3 CHCH 2 CH 3 Cl 2-Klorobütan CCH 3 Metilbenzoat 1. Mg, dietil eter 2. C 2 CH 3 CHCH 2 CH 3 3. H 3 CH 2 C 2 H 5 MgBr 2-Metilbütanoik asit 1. dietil eter C 2. H 3 H C 2 H 5 C 2 H 5 3-Fenil-3-hidroksipentan (3-Fenil-3-pentanol) Tersiyer alkol Karboksilli asit Primer alkol 19
20 20
İsimlendirilmeleri. Karbonil grubuna bir hidroksil bağlanması ile oluşan yapıya karboksil grubu, bugrubu. karboksilli asitler denir.
 KARBKSİLLİ ASİTLER İsimlendirilmeleri Karbonil grubuna bir hidroksil bağlanması ile oluşan yapıya karboksil grubu, bugrubu taşıyan R-CH yapısındaki bileşiklere ise karboksilli asitler denir. RCH Karboksilli
KARBKSİLLİ ASİTLER İsimlendirilmeleri Karbonil grubuna bir hidroksil bağlanması ile oluşan yapıya karboksil grubu, bugrubu taşıyan R-CH yapısındaki bileşiklere ise karboksilli asitler denir. RCH Karboksilli
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
AROMATİK BİLEŞİKLERİN NİTROLANMASI
 Elektrofilik Aromatik Sübstitüsyon Elektrofil parçacığa atak sonucunda arenyum iyonu oluşumu: AMATİK BİLEŞİKLEİN NİTLANMASI Uzm. Ecz. Dilan KNYA Proton kaybı ile sübstitüsyon ürününün elde edilmesi: Nitrolama
Elektrofilik Aromatik Sübstitüsyon Elektrofil parçacığa atak sonucunda arenyum iyonu oluşumu: AMATİK BİLEŞİKLEİN NİTLANMASI Uzm. Ecz. Dilan KNYA Proton kaybı ile sübstitüsyon ürününün elde edilmesi: Nitrolama
ÜNİTE 15 Organik Kimya - II Heteroatomlu Bileşikler
 ÜİTE 15 rganik Kimya - II eteroatomlu Bileşikler Amaçlar Bu üniteyi çalıştıktan sonra; eteroatom kavramını, eteroatom içeren bileşiklerin önemini, eteroatom içeren bileşiklerin reaksiyonlarını, eteroatom
ÜİTE 15 rganik Kimya - II eteroatomlu Bileşikler Amaçlar Bu üniteyi çalıştıktan sonra; eteroatom kavramını, eteroatom içeren bileşiklerin önemini, eteroatom içeren bileşiklerin reaksiyonlarını, eteroatom
FONKSİYONLU ORGANİK BİLEŞİKLER I
 FNKSİYNLU GANİK BİLEŞİKLE rganik bileşiklerde, bileşiğin temel kimyasal ve fiziksel özelliklerini belirleyen ve formülleri yazıldığında tanınmalarını sağlayan atom gruplarına fonksiyonel gruplar denir.
FNKSİYNLU GANİK BİLEŞİKLE rganik bileşiklerde, bileşiğin temel kimyasal ve fiziksel özelliklerini belirleyen ve formülleri yazıldığında tanınmalarını sağlayan atom gruplarına fonksiyonel gruplar denir.
2.ORGANİK MOLEKÜLLERDE FONKSİYONEL GRUPLAR VE İSİMLEMDİRMELER
 BÖLÜM II 2.ORGANİK MOLEKÜLLERDE FONKSİYONEL GRUPLAR VE İSİMLEMDİRMELER Fonksiyonel gurup: Fonksiyonel gurup, bir molekülün kimyasal anlamda en aktif olan kısımları olarak tanımlanabilir. Bu tanıma göre
BÖLÜM II 2.ORGANİK MOLEKÜLLERDE FONKSİYONEL GRUPLAR VE İSİMLEMDİRMELER Fonksiyonel gurup: Fonksiyonel gurup, bir molekülün kimyasal anlamda en aktif olan kısımları olarak tanımlanabilir. Bu tanıma göre
AROMATİK BİLEŞİKLER
 AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
AROMATİK BİLEŞİKLER AROMATİK HİDROKARBONLAR BENZEN: (C 6 H 6 ) Aromatik moleküllerin temel üyesi benzendir. August Kekule (Ogüst Kekule) benzen için altıgen formülü önermiştir. Bileşik sınıfına sistematik
Mekanizma;
 4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
Birbiri ile ikili bağla bağlanmış karbon ve. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
 ALDEHİT ve KETNLAR Birbiri ile ikili bağla bağlanmış karbon ve oksijene (C=) karbonil grubu denir. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
ALDEHİT ve KETNLAR Birbiri ile ikili bağla bağlanmış karbon ve oksijene (C=) karbonil grubu denir. Karbonil grubu, aldehit, keton, karboksilli asit, ester, amid vb. fonksiyonel grubun çatısını oluşturur.
Organik Bileşiklerin Sınıflandırılması - Alkanlar. Prof. Dr. Arif ALTINTAŞ
 Organik Bileşiklerin Sınıflandırılması - Alkanlar Prof. Dr. Arif ALTINTAŞ Organik Bileşiklerin Sınıflandırılması idrokarbonlar yapılarında ve bulunduran bileşiklerdir. Genel olarak 2 grupta incelenebilir:
Organik Bileşiklerin Sınıflandırılması - Alkanlar Prof. Dr. Arif ALTINTAŞ Organik Bileşiklerin Sınıflandırılması idrokarbonlar yapılarında ve bulunduran bileşiklerdir. Genel olarak 2 grupta incelenebilir:
ALKOLLER ve ETERLER. Kimya Ders Notu
 ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
ALKOLLER ve ETERLER Kimya Ders Notu ALKOLLER Alkan bileşiklerindeki karbon zincirinde H atomlarından biri yerine -OH grubunun geçmesi sonucu oluşan organik bileşiklere alkol adı verilir. * Genel formülleri
KİMYA-IV. Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu)
 KİMYA-IV Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu) Alkoller Bir alkil grubuna (R-) bir hidroksil (-OH) grubunun bağlanmasıyla oluşan yapılardır. Genel formülleri R-OH şeklindedir. Alkollerin
KİMYA-IV Alkoller, Eterler ve Karbonil Bileşikleri (6. Konu) Alkoller Bir alkil grubuna (R-) bir hidroksil (-OH) grubunun bağlanmasıyla oluşan yapılardır. Genel formülleri R-OH şeklindedir. Alkollerin
ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 3. YAZILI
 / / Adı Soyadı : Numara : ÖĞRETİM YL. DÖNEM 1. SNF / KİMYA DERSİ / 3. YAZL Soru Puan 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 TOPLAM 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 100 1. X: 3 NH Y:3 N 3
/ / Adı Soyadı : Numara : ÖĞRETİM YL. DÖNEM 1. SNF / KİMYA DERSİ / 3. YAZL Soru Puan 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 TOPLAM 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 100 1. X: 3 NH Y:3 N 3
Bölüm 11 Alkoller ve Eterler. Alkollerin Yapısı. Sınıflandırma. Hidroksil (-OH) fonksiyonel grubu Oksijen sp 3 melezleşmiştir. =>
 Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
Aromatik nitro bileşiklerinin sentezlerinde aşağıdaki yollardan faydalanılabilir.
 1.1.1. Nitrolama ve Aromatik Nitro Bileşikleri Farmasötik önemi olan kimyasal maddeler arasında aromatik nitro bileşikleri (Ar-NO 2) önemli bir yer tutmaktadır. Nitro (-NO 2) grubu ilaç etken maddelerinin
1.1.1. Nitrolama ve Aromatik Nitro Bileşikleri Farmasötik önemi olan kimyasal maddeler arasında aromatik nitro bileşikleri (Ar-NO 2) önemli bir yer tutmaktadır. Nitro (-NO 2) grubu ilaç etken maddelerinin
AMİNLER SEKONDER AMİN
 AMİNLER (ALKİLLENMİŞ AMONYAK) AMİNLER (RNH 2 )PRİMER AMİN TERSİYER AMİN(R 3 N) SEKONDER AMİN R 2 NH Aminler Alkillenmiş Amonyak olarak tanımlanır. Azot Atomuna bağlı 2 tane H atomu varsa(bir tane alkil
AMİNLER (ALKİLLENMİŞ AMONYAK) AMİNLER (RNH 2 )PRİMER AMİN TERSİYER AMİN(R 3 N) SEKONDER AMİN R 2 NH Aminler Alkillenmiş Amonyak olarak tanımlanır. Azot Atomuna bağlı 2 tane H atomu varsa(bir tane alkil
Bolum 11&12 Eterler, Epoksitler, Sülfitler
 Bolum 11&12 Eterler, Epoksitler, Sülfitler Giriş Eter Formülü R--R (R ve R alkil veya aril). Simetrik ve asimetrik olabilir Örnekler: C 3 C 3 C 3 2 Yapı ve Polarite Eğik moleküler geometri ksijen sp 3
Bolum 11&12 Eterler, Epoksitler, Sülfitler Giriş Eter Formülü R--R (R ve R alkil veya aril). Simetrik ve asimetrik olabilir Örnekler: C 3 C 3 C 3 2 Yapı ve Polarite Eğik moleküler geometri ksijen sp 3
verilmiştir. Form aldehit alifatik aldehit aromatik aldehit O O R R
 Dr. ilmi NAMLI -ALDEİT VE KETNLA ALDEİT VE KETNLA rganik kimyanın belki de en önemli fonksiyonel grubu olan karbonil grubunu içeren önemli iki bileşiği aldehitler ve ketonlardır. karbonil Bu fonksiyonel
Dr. ilmi NAMLI -ALDEİT VE KETNLA ALDEİT VE KETNLA rganik kimyanın belki de en önemli fonksiyonel grubu olan karbonil grubunu içeren önemli iki bileşiği aldehitler ve ketonlardır. karbonil Bu fonksiyonel
4. Asetilen katımı: Aldehit ve ketonlara
 4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
4. Asetilen katımı: Aldehit ve ketonlara asetilen veya terminal asetilenik grup içeren alkinler katılarak alkinil bileşiklerini yaparlar. Metil etil ketona asetilen katılması ile sedatif-hipnotik bir ilaç
³DQ ³HQ (WDQ (WHQ 3URSDQ 3URSHQ % WDQ % WHQ
 En az ndan bir adet karbon-karbon çift ba içeren hidrokarbonlara denir. Bu bile iklerin di er bir ismi ise dir.alkenlerin genel formülleri Alkenlerde çift ba bir adet kuvvetli sigma ba ile sigma ba na
En az ndan bir adet karbon-karbon çift ba içeren hidrokarbonlara denir. Bu bile iklerin di er bir ismi ise dir.alkenlerin genel formülleri Alkenlerde çift ba bir adet kuvvetli sigma ba ile sigma ba na
10. H F Bileşiğinin sistematik adı nedir?
 MÜEDİSLİK KÜLTESİ KİMY MÜEDİSLİĞİ ÖLÜMÜ GİK KİMY DESİ DÖEM SIVI 19.01.2012 o: dı ve Soyadı: Öğretim Programı: ÖÖ ( ) ; İÖ ( ) Öğretim Üyesi: asan Seçen ( ) ; amdullah Kılıç ( ) Toplam 34 soru vardır. 125
MÜEDİSLİK KÜLTESİ KİMY MÜEDİSLİĞİ ÖLÜMÜ GİK KİMY DESİ DÖEM SIVI 19.01.2012 o: dı ve Soyadı: Öğretim Programı: ÖÖ ( ) ; İÖ ( ) Öğretim Üyesi: asan Seçen ( ) ; amdullah Kılıç ( ) Toplam 34 soru vardır. 125
T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER
 T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER ALKOL, ETER VE EPOKSİTLER: YAPILARI VE FİZİKSEL ÖZELLİKLERİ Alkoller, doymuş bir karbon atomuna bağlı bir hidroksil (-OH)
T.W.Graham Solomons ORGANİK KİMYA 7. Basımdan çeviri. ALKOLLER, ETERLER, EPOKSİTLER ALKOL, ETER VE EPOKSİTLER: YAPILARI VE FİZİKSEL ÖZELLİKLERİ Alkoller, doymuş bir karbon atomuna bağlı bir hidroksil (-OH)
A M İ N L E R
 A M İ N L E Bir azot atomuna bağlı bir, iki veya üç tane radikal taşıyan, amonyak molekülündeki hidrojenlerin radikallerle değişmesi ile oluşmuş bileşiklere amin denir. NH 3 Amonyak -N Alkilamin CH 3 NH
A M İ N L E Bir azot atomuna bağlı bir, iki veya üç tane radikal taşıyan, amonyak molekülündeki hidrojenlerin radikallerle değişmesi ile oluşmuş bileşiklere amin denir. NH 3 Amonyak -N Alkilamin CH 3 NH
ORGANİK KİMYA. Prof.Dr. Özlen Güzel Akdemir. Farmasötik Kimya Anabilim Dalı
 ORGANİK KİMYA Prof.Dr. Özlen Güzel Akdemir Farmasötik Kimya Anabilim Dalı Ders sunumlarına erişim için : http://aves.istanbul.edu.tr/oguzel/dokumanlar 2018-2019 EĞİTİM-ÖĞRETİM YILI ORGANİK KİMYA DERS PLANI
ORGANİK KİMYA Prof.Dr. Özlen Güzel Akdemir Farmasötik Kimya Anabilim Dalı Ders sunumlarına erişim için : http://aves.istanbul.edu.tr/oguzel/dokumanlar 2018-2019 EĞİTİM-ÖĞRETİM YILI ORGANİK KİMYA DERS PLANI
KİMYA-IV. Yrd. Doç. Dr. Yakup Güneş
 KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
KİMYA-IV Yrd. Doç. Dr. Yakup Güneş Organik Kimyaya Giriş Kimyasal bileşikler, eski zamanlarda, elde edildikleri kaynaklara bağlı olarak Anorganik ve Organik olmak üzere, iki sınıf altında toplanmışlardır.
Alkoller, Eterler ve Tiyoller
 Alkoller, Eterler ve Tiyoller Alkoller (R- OH) Alkoller, OH (hidroksil) fonksiyonel grubu taşıyan organik bileşiklerdir (alkil veya aril grubuna bağlı hidroksil) Metanol (CH 3 OH) en basit alkoldür Chemistry,
Alkoller, Eterler ve Tiyoller Alkoller (R- OH) Alkoller, OH (hidroksil) fonksiyonel grubu taşıyan organik bileşiklerdir (alkil veya aril grubuna bağlı hidroksil) Metanol (CH 3 OH) en basit alkoldür Chemistry,
KARBOKSİLLİ ASİTLER#2
 KARBOKSİLLİ ASİTLER#2 ELDE EDİLME TEPKİMELERİ KİMYASAL ÖZELLİKLERİ KULLANIM ALANLARI ELDE EDİLME TEPKİMELERİ 1. Birincil (primer) alkollerin ya da aldehitlerin yükseltgenmesiyle elde edilir. Örnek: İzobütil
KARBOKSİLLİ ASİTLER#2 ELDE EDİLME TEPKİMELERİ KİMYASAL ÖZELLİKLERİ KULLANIM ALANLARI ELDE EDİLME TEPKİMELERİ 1. Birincil (primer) alkollerin ya da aldehitlerin yükseltgenmesiyle elde edilir. Örnek: İzobütil
6. Deney Hidrokarbonların Belirlenmesi
 6. Deney Hidrokarbonların Belirlenmesi Genel Prensipler Yapıları ve kimyasal davranışları esas alındığında, hidrokarbonlar üç kategoriye ayrılabilir. Doymuş Alifatik Hidrokarbonlar: Tüm karbon atomlarının
6. Deney Hidrokarbonların Belirlenmesi Genel Prensipler Yapıları ve kimyasal davranışları esas alındığında, hidrokarbonlar üç kategoriye ayrılabilir. Doymuş Alifatik Hidrokarbonlar: Tüm karbon atomlarının
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ
 ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
ALKOL ELDE EDİLME TEPKİMELERİ ALKOL KİMYASAL ÖZELLİKLERİ Alkollerin Elde Edilme Yöntemleri 1. Alkil Halojenürlerin Bazlarla Tepkimesi: Alkil halojenürlerin seyreltik NaOH ya da KOH gibi bazlarla ısıtılması
Aminler. amonyak. Primer sekonder tersiyer
 Aminler & Amitler Aminler Aminler amonyak molekülünün organik türevleridirler amonyaktaki hidrojenler alkil grupları ile yer değiş;rmiş;r Aminler bazik özellik gösterirler doğada bulunan en önemli organik
Aminler & Amitler Aminler Aminler amonyak molekülünün organik türevleridirler amonyaktaki hidrojenler alkil grupları ile yer değiş;rmiş;r Aminler bazik özellik gösterirler doğada bulunan en önemli organik
KARBOKSİLLİ ASİT TÜREVLERİ-I
 KARBOKSİLLİ ASİT TÜREVLERİ-I KARBOKSİLLİ ASİT VE TÜREVLERİ (OH grubunun kopması ile oluşan bileşikler) Su ile etkileştiğinde karboksil asit oluşumuna neden olan organik bileşiklere karboksilik asit türevleri
KARBOKSİLLİ ASİT TÜREVLERİ-I KARBOKSİLLİ ASİT VE TÜREVLERİ (OH grubunun kopması ile oluşan bileşikler) Su ile etkileştiğinde karboksil asit oluşumuna neden olan organik bileşiklere karboksilik asit türevleri
26/02. azota yapılan tek veya çift bir bağ ile [2] 26/06. azot içeren bir heterosiklik halka tarafından [2] 26/08.. N - Vinil - pirolidin [2]
![26/02. azota yapılan tek veya çift bir bağ ile [2] 26/06. azot içeren bir heterosiklik halka tarafından [2] 26/08.. N - Vinil - pirolidin [2] 26/02. azota yapılan tek veya çift bir bağ ile [2] 26/06. azot içeren bir heterosiklik halka tarafından [2] 26/08.. N - Vinil - pirolidin [2]](/thumbs/93/113321405.jpg) Uluslararası Patent Sınıflandırması C Sınıfı4 24/00 En az birinin, oksijen içeren heterosiklik halka tarafından bitirildiği ve herbirinin sadece bir adet karbon - karbon çift bağına sahip olduğu, bir ya
Uluslararası Patent Sınıflandırması C Sınıfı4 24/00 En az birinin, oksijen içeren heterosiklik halka tarafından bitirildiği ve herbirinin sadece bir adet karbon - karbon çift bağına sahip olduğu, bir ya
KİMYA-IV. Alkenler (3. Konu)
 KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BİLEŞİKLERİN ADLANDIRILMASI. Bileşikleri isimlendirmek için elementlerin ve bazı köklerin değerliklerinin ve isimlerinin bilinmesi gerekir.
 BİLEŞİKLERİN ADLANDIRILMASI Bileşikleri isimlendirmek için elementlerin ve bazı köklerin değerliklerinin ve isimlerinin bilinmesi gerekir. Bileşiklerin İsimlendirilmesi: 1.METAL-AMETAL(İYONİK ) BİL. İSİMLENDİRİLMESİ
BİLEŞİKLERİN ADLANDIRILMASI Bileşikleri isimlendirmek için elementlerin ve bazı köklerin değerliklerinin ve isimlerinin bilinmesi gerekir. Bileşiklerin İsimlendirilmesi: 1.METAL-AMETAL(İYONİK ) BİL. İSİMLENDİRİLMESİ
lması *Bisiklik -Alkenler -Alkinlerin -Alkil halojenürlerin -Aminlerin adlandırılmas -Esterlerin adlandırılmas *Benzen ve türevlerinin t kuralı
 16.05.2010 1 16.05.2010 2 -Alkanların ve sikloalkanların adlandırılmas lması *Bisiklik bileşiklerin iklerin adlandırılmas lması -Alkenler ve sikloalkenlerin adlandırılmas lması -Alkinlerin adlandırılmas
16.05.2010 1 16.05.2010 2 -Alkanların ve sikloalkanların adlandırılmas lması *Bisiklik bileşiklerin iklerin adlandırılmas lması -Alkenler ve sikloalkenlerin adlandırılmas lması -Alkinlerin adlandırılmas
Bu bilgiler ışığında yukarıdaki C atomlarının yükseltgenme basamaklarını söyleyelim:
 Organik Bileşiklerde C atomunun Yükseltgenme Basamağının Bulunması Yükseltgenme basamağı, C'a bağlı atomların elektronegatifliğine göre değişmektedir. C'un başlangıçta yükseltgenme basamağını 0 gibi düşünelim.
Organik Bileşiklerde C atomunun Yükseltgenme Basamağının Bulunması Yükseltgenme basamağı, C'a bağlı atomların elektronegatifliğine göre değişmektedir. C'un başlangıçta yükseltgenme basamağını 0 gibi düşünelim.
HİDROKARBONLAR HİDROKARBONLAR 2. AROMATİK 1. ALİFATİK HİDROKARBONLAR HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) DOYMAMIŞ
 HİDROKARBONLAR HİDROKARBONLAR HİDROKARBONLAR 1. ALİFATİK HİDROKARBONLAR 2. AROMATİK HİDROKARBONLAR DOYMUŞ HİDROKARBONLAR DOYMAMIŞ HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) BİTİŞİK İKİ HALKALI (NAFTALİN)
HİDROKARBONLAR HİDROKARBONLAR HİDROKARBONLAR 1. ALİFATİK HİDROKARBONLAR 2. AROMATİK HİDROKARBONLAR DOYMUŞ HİDROKARBONLAR DOYMAMIŞ HİDROKARBONLAR TEK HALKALI (BENZEN VE TÜREVLERİ) BİTİŞİK İKİ HALKALI (NAFTALİN)
HİDROKARBONLAR ve ALKİNLER. Kimya Ders Notu
 HİDROKARBONLAR ve ALKİNLER Kimya Ders Notu HİDROKARBONLAR ve ALKiNLER Karbon atomları arasında en az bir üçlü bağ içerdiklerinden doymamış hidrokarbonlardır. Üçlü bağdan biri sigma, diğerleri pi bağıdır.
HİDROKARBONLAR ve ALKİNLER Kimya Ders Notu HİDROKARBONLAR ve ALKiNLER Karbon atomları arasında en az bir üçlü bağ içerdiklerinden doymamış hidrokarbonlardır. Üçlü bağdan biri sigma, diğerleri pi bağıdır.
Alkinler (Asetilenler)
 Organik-İnorganik Kimya Alkinler (Asetilenler) ALKİNLER (ASETİLENLER) Genel formülleri C n H 2n-2 şeklinde olan ve yapılarında en az bir üçlü bağ içeren bileşiklerdir. Bu bileşiklere, moleküllerindeki
Organik-İnorganik Kimya Alkinler (Asetilenler) ALKİNLER (ASETİLENLER) Genel formülleri C n H 2n-2 şeklinde olan ve yapılarında en az bir üçlü bağ içeren bileşiklerdir. Bu bileşiklere, moleküllerindeki
ORGANİK KİMYA ÖZET ÇÖZÜMLERİ TEST - 1
 RGANİK KİMYA ÖZET ÇÖZÜMLERİ TEST - 1 1. Alkanlar, parafinler olarakta adlandırılırlar. lefinler ise alkenlerdir. 5. ( ) 2 C( ) 2 bileşiğinin UPAC adı: 1 C 2 3 4 5 6 2.5 dimetil 2 hekzen dir. 2. Siklo alkenlerin
RGANİK KİMYA ÖZET ÇÖZÜMLERİ TEST - 1 1. Alkanlar, parafinler olarakta adlandırılırlar. lefinler ise alkenlerdir. 5. ( ) 2 C( ) 2 bileşiğinin UPAC adı: 1 C 2 3 4 5 6 2.5 dimetil 2 hekzen dir. 2. Siklo alkenlerin
POLİMER KİMYASI -2. Prof. Dr. Saadet K. Pabuccuoğlu
 POLİMER KİMYASI -2 Prof. Dr. Saadet K. Pabuccuoğlu Polimerize Olabilirlik Nedir? Bir monomerin polimerize olabilirliği termodinamik ve kinetik düşüncelere bağlıdır. Termodinamikçe uygun olan her monomer,
POLİMER KİMYASI -2 Prof. Dr. Saadet K. Pabuccuoğlu Polimerize Olabilirlik Nedir? Bir monomerin polimerize olabilirliği termodinamik ve kinetik düşüncelere bağlıdır. Termodinamikçe uygun olan her monomer,
T.C. Ölçme, Seçme ve Yerleştirme Merkezi
 T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 25 HAZİRAN 2016 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
T.C. Ölçme, Seçme ve Yerleştirme Merkezi LİSANS YERLEŞTİRME SINAVI-2 KİMYA TESTİ 25 HAZİRAN 2016 CUMARTESİ Bu testlerin her hakkı saklıdır. Hangi amaçla olursa olsun, testlerin tamamının veya bir kısmının
ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI
 / / Adı Soyadı : Numara : ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI Soru Puan BAŞARILAR 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 TOPLAM 100 1. Açık formülü olan bileşiğin genel
/ / Adı Soyadı : Numara : ÖĞRETİM YILI 2. DÖNEM 12. SINIF / KİMYA DERSİ / 1. YAZILI Soru Puan BAŞARILAR 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 TOPLAM 100 1. Açık formülü olan bileşiğin genel
KİMYA-IV. Aromatik Hidrokarbonlar (Arenler) (5. Konu)
 KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
Oksidasyon ve Redüksiyon Reaksiyonları Oksidasyon Reaksiyonları
 1.1.1. Oksidasyon ve Redüksiyon Reaksiyonları 1.1.1.1. Oksidasyon Reaksiyonları Bir organik molekülün oksidasyonu, oksijen miktarının artışı veya hidrojen miktarının azalması olarak tanımlanabilir. Başka
1.1.1. Oksidasyon ve Redüksiyon Reaksiyonları 1.1.1.1. Oksidasyon Reaksiyonları Bir organik molekülün oksidasyonu, oksijen miktarının artışı veya hidrojen miktarının azalması olarak tanımlanabilir. Başka
Ayırma ve Đzolasyon Teknikleri : Ekstraksiyon
 3. Deney Ayırma ve Đzolasyon Teknikleri : Ekstraksiyon Sentezlerde istenen ürünü yan ürünlerden, fazla miktardaki veya tepkimeye girmemiş başlangıç bileşiklerinden, safsızlıklardan ve çözeltiden ayırmak
3. Deney Ayırma ve Đzolasyon Teknikleri : Ekstraksiyon Sentezlerde istenen ürünü yan ürünlerden, fazla miktardaki veya tepkimeye girmemiş başlangıç bileşiklerinden, safsızlıklardan ve çözeltiden ayırmak
ALKENLER; ÇALIŞMA SORULARI
 ALKENLER; ÇALIŞMA SORULARI SORU 1.) 1 büten ve 2 büten için cis ve trans izomeri yazmak mümkün müdür? SORU 2.) Aşağıda verilen bileşikleri IUPAC metoduna göre adlandırınız. A) CH2 = C = CH CH3 B) CH3 CH
ALKENLER; ÇALIŞMA SORULARI SORU 1.) 1 büten ve 2 büten için cis ve trans izomeri yazmak mümkün müdür? SORU 2.) Aşağıda verilen bileşikleri IUPAC metoduna göre adlandırınız. A) CH2 = C = CH CH3 B) CH3 CH
EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö)
 EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö) 200620105028 KONU BAŞLIKLARI 1)AMİNLERİN ADLANDIRILMASI 2)GABRİEL SENTEZİ AMİNLERİN ADLANDIRILMASI Aminler amonyaktaki bir, iki
EBRU TEKİN BALIKESİR ÜNİVERSİTESİ FEN EDEBİYAT FAKÜLTESİ KİMYA BÖLÜMÜ(İ.Ö) 200620105028 KONU BAŞLIKLARI 1)AMİNLERİN ADLANDIRILMASI 2)GABRİEL SENTEZİ AMİNLERİN ADLANDIRILMASI Aminler amonyaktaki bir, iki
12-B. 31. I. 4p II. 5d III. 6s
 -B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
-B.. 4p. 5d. 6s Baş kuantum sayısı n, açısal kuantum sayısı olmak üzere yukarıda verilen orbitallerin enerjilerinin karşılaştırılması hangisinde doğru verilmiştir? A) == B) >> C) >> D) >> E) >> ÖLÇME,
ORGANİK KİMYA H C C C C C C C C H H H H H H H H H (H 3 C CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3 )
 ORGANİK KİMYA Organik maddeler Organik kimya, karbon bileşiklerinin kimyasıdır; hücrenin kuru ağırlığının yarısından daha fazlasını karbon ( C ) elementi oluşturur. Organik maddelerin molekülleri, genellikle
ORGANİK KİMYA Organik maddeler Organik kimya, karbon bileşiklerinin kimyasıdır; hücrenin kuru ağırlığının yarısından daha fazlasını karbon ( C ) elementi oluşturur. Organik maddelerin molekülleri, genellikle
veya Monoalkoller OH grubunun bağlı olduğu C atomunun komşu C atomlarına bağlı olarak primer, sekonder ve tersiyer olmak üzere sınıflandırılabilirler:
 ALKLLE Genel formülleri: n 2n+2 ( n 2n+1 = ) Fonksiyonel grupları: Alkollerin sistematik adlandırmasında en uzun zincirdeki atomuna göre alkan adının sonuna ol eki getirilir. Yapısında 1 tane grubu bulunduran
ALKLLE Genel formülleri: n 2n+2 ( n 2n+1 = ) Fonksiyonel grupları: Alkollerin sistematik adlandırmasında en uzun zincirdeki atomuna göre alkan adının sonuna ol eki getirilir. Yapısında 1 tane grubu bulunduran
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
HİDROKARBONLAR ve ALKANLAR. Kimya Ders Notu
 HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
HİDROKARBONLAR ve ALKANLAR Kimya Ders Notu HİDROKARBONLAR ve ALKANLAR ALKANLAR Hidrokarbon zincirinde C atomları birbirine tek bağ ile bağlanmışlardır ve tüm bağları sigma bağıdır. Moleküllerindeki C atomları
KİMYA-IV. Alkenler (3. Konu)
 KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
KİMYA-IV Alkenler (3. Konu) Alkenler (Olefinler) En az bir tane C=C çift bağı içeren hidrokarbonlara alkenler veya olefinler denir. Alkenler doymamış yapıda hidrokarbonlar olup, katalizörler eşliğinde
HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö
 BALIKESİR ÜNİVERSİTESİ 2008-2009 2009 EĞİE ĞİTİM ÖĞRETİM M YILI BAHAR DÖNEMİ ORGANİK K SENTEZ DERSİ ÖDEVİ HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö 200610105034 FRİEDEL EDEL-CRAFTS REAKSİYONLARI Friedel-Crafts
BALIKESİR ÜNİVERSİTESİ 2008-2009 2009 EĞİE ĞİTİM ÖĞRETİM M YILI BAHAR DÖNEMİ ORGANİK K SENTEZ DERSİ ÖDEVİ HAZIRLAYAN: Defne GÖKMENG FEF/Kimya 1.Ö 200610105034 FRİEDEL EDEL-CRAFTS REAKSİYONLARI Friedel-Crafts
$e"v I)w ]/o$a+ s&a; %p,{ d av aa!!!!aaa!a!!!a! BASIN KİTAPÇIĞI 00000000
![$ev I)w ]/o$a+ s&a; %p,{ d av aa!!!!aaa!a!!!a! BASIN KİTAPÇIĞI 00000000 $ev I)w ]/o$a+ s&a; %p,{ d av aa!!!!aaa!a!!!a! BASIN KİTAPÇIĞI 00000000](/thumbs/29/13231412.jpg) BASIN KİTAPÇIĞI 00000000 AÇIKLAMA 1. Bu kitapç kta Lisans Yerle tirme S nav - Kimya Testi bulunmaktad r.. Bu test için verilen toplam cevaplama süresi 5 dakikadır.. Bu kitapç ktaki testlerde yer alan her
BASIN KİTAPÇIĞI 00000000 AÇIKLAMA 1. Bu kitapç kta Lisans Yerle tirme S nav - Kimya Testi bulunmaktad r.. Bu test için verilen toplam cevaplama süresi 5 dakikadır.. Bu kitapç ktaki testlerde yer alan her
Yapısında yalnızca C ve H u bulunduran bileşiklere hidrokarbon adı verilir.
 HİDROKARBONLAR Yapısında yalnızca C ve H u bulunduran bileşiklere hidrokarbon adı verilir. Alifatik Hidrokarbonlar Düz zincirli veya dallanmış olabilir. Doymuş hidrokarbonlar : Alifatik hidrokarbonlar
HİDROKARBONLAR Yapısında yalnızca C ve H u bulunduran bileşiklere hidrokarbon adı verilir. Alifatik Hidrokarbonlar Düz zincirli veya dallanmış olabilir. Doymuş hidrokarbonlar : Alifatik hidrokarbonlar
POLİMER KİMYASI -13. Prof. Dr. Saadet K. Pabuccuoğlu
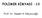 POLİMER KİMYASI -13 Prof. Dr. Saadet K. Pabuccuoğlu İlerleme: Başlama adımında oluşan iyon çifti (karbokatyon negatif yüklü karşıt iyonu) diğer monomer birimlerini katarak büyüme gerçekleşir. veya Bazı
POLİMER KİMYASI -13 Prof. Dr. Saadet K. Pabuccuoğlu İlerleme: Başlama adımında oluşan iyon çifti (karbokatyon negatif yüklü karşıt iyonu) diğer monomer birimlerini katarak büyüme gerçekleşir. veya Bazı
1.Evrende ve Dünyada Elementler. 2.Elementler Nasıl Elde Edilir? 3.Alaşımlar 6 Ekim İstanbul'un Kurtuluşu. 4.Hidrojen. 5.Alkaliler ve Toprak Alkaliler
 KASIM EKİM EYLÜL Öğretim Yılı: 0 05 Okulu: Özel Asfa Fen Lisesi ÜNİTELENDİRİLMİŞ YILLIK PLAN Dersin Adı: KİMYA Sınıflar: A SÜRE.ÜNİTE: ELEMENTLER KİMYASI.. Hafif elementlerin olusumunu, evrenin baslangıcı
KASIM EKİM EYLÜL Öğretim Yılı: 0 05 Okulu: Özel Asfa Fen Lisesi ÜNİTELENDİRİLMİŞ YILLIK PLAN Dersin Adı: KİMYA Sınıflar: A SÜRE.ÜNİTE: ELEMENTLER KİMYASI.. Hafif elementlerin olusumunu, evrenin baslangıcı
Örnek : 3- Bileşiklerin Özellikleri :
 Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Bileşikler : Günümüzde bilinen 117 element olmasına rağmen (92 tanesi doğada bulunur) bu elementler farklı sayıda ve şekilde birleşerek ve etkileşerek farklı kimyasal özelliklere sahip milyonlarca yani
Ödevleri teslim ederken bu soru sayfası da verilmek zorundadır.
 12. BÖLÜM: ARENLERİN REAKSİYONLARI: ELEKTROFİLİK AROMATİK YER DEĞİŞTİRME TEPKİMELERİ (ÖDEV TESLİM TARİHİ 13/03/2017) 1) Aşağıda verilen tepkimelerin ana organik ürününü yazınız. 2) aşağıda verilen bileşiği
12. BÖLÜM: ARENLERİN REAKSİYONLARI: ELEKTROFİLİK AROMATİK YER DEĞİŞTİRME TEPKİMELERİ (ÖDEV TESLİM TARİHİ 13/03/2017) 1) Aşağıda verilen tepkimelerin ana organik ürününü yazınız. 2) aşağıda verilen bileşiği
KİMYA-IV. Aromatik Hidrokarbonlar (Arenler) (5. Konu)
 KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
KİMYA-IV Aromatik Hidrokarbonlar (Arenler) (5. Konu) Aromatiklik Kavramı Aromatik sözcüğü kokulu anlamına gelir. Kimyanın ilk gelişme evresinde, bilinen hidrokarbonların çoğu kokulu olduğu için, bu bileşikler
BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031
 BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031 Organik kimyada bilinen ilk tepkimelerden (metod) biridir. Bu reaksiyonun mucidi bilim adamı, Viktor Grignard, bu tepkime sayesinde 1912 Kimya Nobel ödülünün
BALİKESİR ÜNİVERSİTESİ MERVE USTA 200510105031 Organik kimyada bilinen ilk tepkimelerden (metod) biridir. Bu reaksiyonun mucidi bilim adamı, Viktor Grignard, bu tepkime sayesinde 1912 Kimya Nobel ödülünün
Atomlar ve Moleküller
 Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
Atomlar ve Moleküller Madde, uzayda yer işgal eden ve kütlesi olan herşeydir. Element, kimyasal tepkimelerle başka bileşiklere parçalanamayan maddedir. -Doğada 92 tane element bulunmaktadır. Bileşik, belli
ERKAN ALTUN
 2008-200 2009 EĞİTİM M VE ÖĞRETİM M YILI 200610105003 ERKAN ALTUN RGANİK K SENTEZLER SCHMİDTH REAKSİYNLARI Hidrojen azidin elektrofillerle (karbonil bileşikleri,tersiyer ikleri,tersiyer alkoller,alkenler
2008-200 2009 EĞİTİM M VE ÖĞRETİM M YILI 200610105003 ERKAN ALTUN RGANİK K SENTEZLER SCHMİDTH REAKSİYNLARI Hidrojen azidin elektrofillerle (karbonil bileşikleri,tersiyer ikleri,tersiyer alkoller,alkenler
Molekülde bulunan OH grubunun sayısına göre 2 ye ayrılırlar:
 FONKSİYONEL GRUPLAR ALKOLLER Hidrokarbonlardaki hidrojen unun bir ya da farklı C daki birkaçının çıkarılıp yerine OH kökünün bağlanmasıyla oluşan bileşiklerdir. Genel formülü R OH dır. Molekülde bulunan
FONKSİYONEL GRUPLAR ALKOLLER Hidrokarbonlardaki hidrojen unun bir ya da farklı C daki birkaçının çıkarılıp yerine OH kökünün bağlanmasıyla oluşan bileşiklerdir. Genel formülü R OH dır. Molekülde bulunan
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI
 BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
BENZENİN NİTROLANMASINDA GRAFİTİN KATALİZÖR OLARAK ETKİSİNİN ARAŞTIRILMASI AMACIMIZ: Günümüz kimya endüstrisinde ideal katalizörler ekonomik olan, bol bulunan, geri kazanılan ve tepkime mekanizmasında
Bileşikteki atomların cinsini ve oranını belirten formüldür. Kaba formül ile bileşiğin molekül ağırlığı hesaplanamaz.
 BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
BİLEŞİKLER Birden fazla elementin belirli oranlarda kimyasal yollarla bir araya gelerek, kendi özelligini kaybedip oluşturdukları yeni saf maddeye bileşik denir. Bileşikteki atomların cins ve sayısını
Doç. Dr. Mutlu AYTEMİR
 Organik Kimya Hücre Bilimleri I 2008 Doç. Dr. Mutlu AYTEMİR Eczacılık Fakültesi Farmasötik Kimya ABD mutlud@hacettepe.edu.tr http://yunus.hacettepe.edu.tr/~mutlud ALKOLLER İSİMLENDİRİLMELERİ Alkoller,
Organik Kimya Hücre Bilimleri I 2008 Doç. Dr. Mutlu AYTEMİR Eczacılık Fakültesi Farmasötik Kimya ABD mutlud@hacettepe.edu.tr http://yunus.hacettepe.edu.tr/~mutlud ALKOLLER İSİMLENDİRİLMELERİ Alkoller,
ASİTLER- BAZLAR. Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur.
 ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ASİTLER- BAZLAR SUYUN OTONİZASYONU: Suyun kendi kendine iyonlaşmasına Suyun Otonizasyonu - Otoprotoliz adı verilir. Suda oluşan H + sadece protondur. H 2 O (S) H + (suda) + OH - (Suda) H 2 O (S) + H +
ÜNİVERSİTEYE HAZIRLIK 12. SINIF OKULA YARDIMCI SORU BANKASI KİMYA ORGANİK KİMYA SORU BANKASI
 ÜNİVERSİTEYE HAZIRLIK 2. SINIF KULA YARDIMCI SRU BANKASI RGANİK KİMYA SRU BANKASI KİMYA ÜNİVERSİTEYE HAZIRLIK 2. SINIF KULA YARDIMCI SRU BANKASI SUNU Sevgili Öğrenciler, ISBN 978 605 2273 84 5 Dizgi ÇAP
ÜNİVERSİTEYE HAZIRLIK 2. SINIF KULA YARDIMCI SRU BANKASI RGANİK KİMYA SRU BANKASI KİMYA ÜNİVERSİTEYE HAZIRLIK 2. SINIF KULA YARDIMCI SRU BANKASI SUNU Sevgili Öğrenciler, ISBN 978 605 2273 84 5 Dizgi ÇAP
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ
 KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
KARBON ve CANLILARDAKİ MOLEKÜL ÇEŞİTLİLİĞİ Karbonun önemi Hücrenin % 70-95ʼ i sudan ibaret olup, geri kalan kısmın çoğu karbon içeren bileşiklerdir. Canlılığı oluşturan organik bileşiklerde karbon atomuna
PROBLEM 1.1 a ) Örnek Çözüm b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s
 PROBLEM 1.1 b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s 2 3p 4 ) ç ) 14 Si; 1s 2 2s 2 2p 6 3s 2 3p 2 (Değerlik elektronları:
PROBLEM 1.1 b ) 9 F; 1s 2 2s 2 2p 5 (Değerlik elektronları: 2s 2 2p 5 ) c ) 16 S; 1s 2 2s 2 2p 6 3s 2 3p 4 (Değerlik elektronları: 3s 2 3p 4 ) ç ) 14 Si; 1s 2 2s 2 2p 6 3s 2 3p 2 (Değerlik elektronları:
Kimya.12 3.Ünite Konu Özeti
 Kimya.12 3.Ünite Konu Özeti 1. ORGANĠK REDOKS TEPKĠMELERĠ 2. YER DEĞĠġTĠRME (SÜBSTĠTÜSYON) TEPKĠMELERĠ 3. KATILMA TEPKĠMELERĠ 4. AYRILMA (ELĠMĠNASYON) TEPKĠMELERĠ 5. KONDENZASYON TEPKĠMELERĠ Hazırlayan
Kimya.12 3.Ünite Konu Özeti 1. ORGANĠK REDOKS TEPKĠMELERĠ 2. YER DEĞĠġTĠRME (SÜBSTĠTÜSYON) TEPKĠMELERĠ 3. KATILMA TEPKĠMELERĠ 4. AYRILMA (ELĠMĠNASYON) TEPKĠMELERĠ 5. KONDENZASYON TEPKĠMELERĠ Hazırlayan
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ)
 ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
ANADOLU ÜNİVERSİTESİ ECZACILIK FAKÜLTESİ FARMASÖTİK KİMYA ANABİLİMDALI GENEL KİMYA II DERS NOTLARI (ORGANİK KİMYAYA GİRİŞ) Hazırlayan: Doç. Dr. Yusuf ÖZKAY 1. Organik bileşik kavramının tarihsel gelişimi
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BUADA ÖZET BİLGİ VEİLMİŞTİ. DAHA AYINTILI BİLGİ İÇİN VEİLEN KAYNAK KİTAPLAA BAKINIZ. KAYNAKLA 1) P. Volhardt, N. Schore; rganic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E. Craine,
BUADA ÖZET BİLGİ VEİLMİŞTİ. DAHA AYINTILI BİLGİ İÇİN VEİLEN KAYNAK KİTAPLAA BAKINIZ. KAYNAKLA 1) P. Volhardt, N. Schore; rganic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E. Craine,
Oksidasyon ve redüksiyon reaksiyonu aynı anda yürür. Dr.Ecz. Serap YILMAZ
 ksijen miktarı artar Dr.Ecz. Serap YILMAZ ksidasyon ksijen miktarının artışı, hidrojen miktarının azalması (=) bağ oluşumu (deshidrojenasyon) ksijen reaktifinin doymamış bağlara katımı yerine fonksiyonlu
ksijen miktarı artar Dr.Ecz. Serap YILMAZ ksidasyon ksijen miktarının artışı, hidrojen miktarının azalması (=) bağ oluşumu (deshidrojenasyon) ksijen reaktifinin doymamış bağlara katımı yerine fonksiyonlu
HİDROLİZ REAKSİYONLARI
 İDLİZ EAKSİYNLAI İDLİZ EAKSİYNLAI İDLİZ su ile parçalanma demektir. (Su kullanılarak bağın kopması) Su ile parçalanabilen organik moleküller: Karboksilik Asit Türevleri (Amidler, Asit Klorürleri, Esterler,
İDLİZ EAKSİYNLAI İDLİZ EAKSİYNLAI İDLİZ su ile parçalanma demektir. (Su kullanılarak bağın kopması) Su ile parçalanabilen organik moleküller: Karboksilik Asit Türevleri (Amidler, Asit Klorürleri, Esterler,
HİDROLİZ REAKSİYONLARI
 İDLİZ EAKSİYNLAI İDLİZ EAKSİYNLAI İDLİZ su ile parçalanma demektir. (Su kullanılarak bağın kopması) Su ile parçalanabilen organik moleküller: Karboksilik Asit Türevleri (Amidler, Asit Klorürleri, Esterler,
İDLİZ EAKSİYNLAI İDLİZ EAKSİYNLAI İDLİZ su ile parçalanma demektir. (Su kullanılarak bağın kopması) Su ile parçalanabilen organik moleküller: Karboksilik Asit Türevleri (Amidler, Asit Klorürleri, Esterler,
Doymuş Hidrokarbonlar (ALKANLAR)
 Doymuş Hidrokarbonlar (ALKANLAR) Organik bileşikler Alifatik Bileşikler Aromatik bileşikler Halkalı bileşikler Karbosiklik (C, H) Heterosiklik (C, H...N, O) Karbosiklik (C, H) Heterosiklik (C, H...N, O)
Doymuş Hidrokarbonlar (ALKANLAR) Organik bileşikler Alifatik Bileşikler Aromatik bileşikler Halkalı bileşikler Karbosiklik (C, H) Heterosiklik (C, H...N, O) Karbosiklik (C, H) Heterosiklik (C, H...N, O)
ORGANİK BİLEŞİKLER. Prof. Dr. Arif ALTINTAŞ
 ORGANİK BİLEŞİKLER Prof. Dr. Arif ALTINTAŞ ORGANİK KİMYA-ORGANİK BİLEŞİK ORGANİK KİMYA NEDİR? Organik kimya temel olarak karbon ve hidrojen elementi içeren bileşikleri inceleyen bir bilim dalıdır. Saç,
ORGANİK BİLEŞİKLER Prof. Dr. Arif ALTINTAŞ ORGANİK KİMYA-ORGANİK BİLEŞİK ORGANİK KİMYA NEDİR? Organik kimya temel olarak karbon ve hidrojen elementi içeren bileşikleri inceleyen bir bilim dalıdır. Saç,
Bolum 18 Karboksilik Asitler ve Türevleri
 Bolum 18 Karboksilik Asitler ve Türevleri Giriş Karbonil (-=) and hidroksil (-H) on the same carbon is karboksil grubu. karboksil grubu is usually written -H. alifatik asitler -H a bağlı bir alkil içerir.
Bolum 18 Karboksilik Asitler ve Türevleri Giriş Karbonil (-=) and hidroksil (-H) on the same carbon is karboksil grubu. karboksil grubu is usually written -H. alifatik asitler -H a bağlı bir alkil içerir.
Kimyasal Bağ. Atomları birarada tutan kuvvetlere kimyasal bağ denir
 Kimyasal Bağlar Kimyasal Bağ Atomları birarada tutan kuvvetlere kimyasal bağ denir İyonik bağ Kovalent bağ Polar Kovalent bağ Apolar Kovalent bağ Metalik bağ Lewis bağ teorisi Kimyasal bağlanma için atomun
Kimyasal Bağlar Kimyasal Bağ Atomları birarada tutan kuvvetlere kimyasal bağ denir İyonik bağ Kovalent bağ Polar Kovalent bağ Apolar Kovalent bağ Metalik bağ Lewis bağ teorisi Kimyasal bağlanma için atomun
5-AROMATİK BİLEŞİKLER.
 5-AROMATİK BİLEŞİKLER. Organik kimyada çok geç tanınan, yapısı ve reaktifliği çok geç anlaşılan bileşiklerdir. İlk önce kimyacıların karşısına çıkan C6H5- temel yapısını içeren moleküller anlaşılmakta
5-AROMATİK BİLEŞİKLER. Organik kimyada çok geç tanınan, yapısı ve reaktifliği çok geç anlaşılan bileşiklerdir. İlk önce kimyacıların karşısına çıkan C6H5- temel yapısını içeren moleküller anlaşılmakta
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR
 BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
BURADA ÖZET BİLGİ VERİLMİŞTİR. DAHA AYRINTILI BİLGİ İÇİN VERİLEN KAYNAK KİTAPLARA BAKINIZ. KAYNAKLAR 1) P. Volhardt, N. Schore; Organic Chemistry-Structure and Function, Sixth Edition. 2) H. Hart, L. E.
ORGANĠK BĠLEġĠKLER. 2. ÜNİTE 6. Bölüm
 ORGANĠK BĠLEġĠKLER 2. ÜNİTE 6. Bölüm Organik ve Anorganik BileĢiklerin Ayırt Edilmesi Kimya bilimi temelde organik ve anorganik olmak üzere ikiye ayrılır. * Karbonun oksitleri (CO, CO 2 ) * Karbonatlar
ORGANĠK BĠLEġĠKLER 2. ÜNİTE 6. Bölüm Organik ve Anorganik BileĢiklerin Ayırt Edilmesi Kimya bilimi temelde organik ve anorganik olmak üzere ikiye ayrılır. * Karbonun oksitleri (CO, CO 2 ) * Karbonatlar
amonyak primer amin sekonder amin tersiyer amin
 DENEY 9-Bölüm 1 AMĐNLE VE DĐAZONYUM BĐLEŞĐKLEĐ Genel Prensipler Aminler amonyak üzerindeki hidrojenlerin organik gruplar ile değiştirilmesi sonucu türetilen organik bazlardır. Değiştirilen hidrojenlerin
DENEY 9-Bölüm 1 AMĐNLE VE DĐAZONYUM BĐLEŞĐKLEĐ Genel Prensipler Aminler amonyak üzerindeki hidrojenlerin organik gruplar ile değiştirilmesi sonucu türetilen organik bazlardır. Değiştirilen hidrojenlerin
Bölüm 11 Alkoller ve Eterler. Alkollerin Yapısı. Sınıflandırma. Hidroksil (-OH) fonksiyonel grubu Oksijen sp 3 melezleşmiştir. =>
 Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
Bölüm 11 Alkoller ve Eterler Alkollerin Yapısı idroksil (-) fonksiyonel grubu ksijen sp 3 melezleşmiştir. 2 Sınıflandırma Primer(Birincil): ın bağlandığı karbon sadece bir adet karbona bağlı. Sekonder(Đkincil):
KİMYA-IV. Alkinler (4. Konu)
 KİMYA-IV Alkinler (4. Konu) Alkinler (Asetilenler) En az bir tane karbon-karbon üçlü bağı içeren hidrokarbonlara alkinler veya asetilenler denir. C C 2 Alkinler Yalnızca bir tane karbon-karbon üçlü bağı
KİMYA-IV Alkinler (4. Konu) Alkinler (Asetilenler) En az bir tane karbon-karbon üçlü bağı içeren hidrokarbonlara alkinler veya asetilenler denir. C C 2 Alkinler Yalnızca bir tane karbon-karbon üçlü bağı
ASİT-BAZ VE ph. MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN. Yrd. Doç. Dr. Atilla Evcin Afyonkarahisar Kocatepe Üniversitesi 2006
 ASİT-BAZ VE ph MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Asitler ve bazlar günlük yaşantımızda sıkça karşılaştığımız kavramlardan biridir.insanlar, her nekadar asetil salisilik asit ve
ASİT-BAZ VE ph MÜHENDİSLİK KİMYASI DERS NOTLARI Yrd. Doç. Dr. Atilla EVCİN Asitler ve bazlar günlük yaşantımızda sıkça karşılaştığımız kavramlardan biridir.insanlar, her nekadar asetil salisilik asit ve
2+ 2- Mg SO 4. (NH 4 ) 2 SO 4 (amonyum sülfat) bileşiğini katyon ve anyonlara ayıralım.
 KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
KONU: Kimyasal Tepkimeler Dersin Adı Dersin Konusu İYONİK BİLEŞİKLERİN FORMÜLLERİNİN YAZILMASI İyonik bağlı bileşiklerin formüllerini yazmak için atomların yüklerini bilmek gerekir. Bunu da daha önceki
Bileşiğin basit formülünün bulunması (moleküldeki C, H, O, X atomlarının oranından, veya molekül ağırlığından)
 1 SPEKTROSKOPİ PROBLEMLERİ Ref. e_makaleleri, Enstrümantal Analiz, Kütle Spektrometre Uygulamaları Molekül yapısı bilinmeyen bir organik molekülün yapısal formülünün tayin edilmesi istendiğinde, başlangıç
1 SPEKTROSKOPİ PROBLEMLERİ Ref. e_makaleleri, Enstrümantal Analiz, Kütle Spektrometre Uygulamaları Molekül yapısı bilinmeyen bir organik molekülün yapısal formülünün tayin edilmesi istendiğinde, başlangıç
Soygazların bileşik oluşturamamasının sebebi bütün orbitallerinin dolu olmasındandır.
 KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
KİMYASAL BAĞLAR Kimyasal bağ, moleküllerde atomları birarada tutan kuvvettir. Bir bağın oluşabilmesi için atomlar tek başına bulundukları zamankinden daha kararlı (az enerjiye sahip) olmalıdırlar. Genelleme
Biochemistry Chapter 4: Biomolecules. Hikmet Geçkil, Professor Department of Molecular Biology and Genetics Inonu University
 Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
Biochemistry Chapter 4: Biomolecules, Professor Department of Molecular Biology and Genetics Inonu University Biochemistry/Hikmet Geckil Chapter 4: Biomolecules 2 BİYOMOLEKÜLLER Bilim adamları hücreyi
İLAÇ METABOLİZMASI (BİYOTRANSFORMASYON)
 İLAÇ METABLİZMASI (BİYTRASFRMASY) Prof. Dr. Gülgün Ayhan-Kılcıgil İlaçların, organizmada çeşitli enzimlerin etkisiyle kimyasal değişikliklere uğramasına metabolizma veya biyotransformasyon, biyotransformasyon
İLAÇ METABLİZMASI (BİYTRASFRMASY) Prof. Dr. Gülgün Ayhan-Kılcıgil İlaçların, organizmada çeşitli enzimlerin etkisiyle kimyasal değişikliklere uğramasına metabolizma veya biyotransformasyon, biyotransformasyon
Kullanılacak Kimyasal Miktarı. 1.9g (10mmol) 10mL 1g (25mmol) 2.5g (20mmol) 5-10mL Uygun miktarda. Dimetil sülfat [Dietil eter] H 2 SO 4
![Kullanılacak Kimyasal Miktarı. 1.9g (10mmol) 10mL 1g (25mmol) 2.5g (20mmol) 5-10mL Uygun miktarda. Dimetil sülfat [Dietil eter] H 2 SO 4 Kullanılacak Kimyasal Miktarı. 1.9g (10mmol) 10mL 1g (25mmol) 2.5g (20mmol) 5-10mL Uygun miktarda. Dimetil sülfat [Dietil eter] H 2 SO 4](/thumbs/62/47181423.jpg) Preparatın Adı: Anisol (Fenil metil eter) Deney Konusu: Eterleşme Tepkimeleri Denel Organik Kimya Kitabındaki Sayfa No: 432 Fenol NaOH Dimetil sülfat [] H 2 SO 4 NaCl Preparatın Adı: Asetofenon Deney Konusu:
Preparatın Adı: Anisol (Fenil metil eter) Deney Konusu: Eterleşme Tepkimeleri Denel Organik Kimya Kitabındaki Sayfa No: 432 Fenol NaOH Dimetil sülfat [] H 2 SO 4 NaCl Preparatın Adı: Asetofenon Deney Konusu:
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ
 ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
ÖĞRENME ALANI : MADDE VE DEĞİŞİM ÜNİTE 4 : MADDENİN YAPISI VE ÖZELLİKLERİ E BİLEŞİKLER VE FRMÜLLERİ (4 SAAT) 1 Bileşikler 2 Bileşiklerin luşması 3 Bileşiklerin Özellikleri 4 Bileşik Çeşitleri 5 Bileşik
www.kimyahocam.com HİDROKARBONLAR I ÖRNEK 1
 İDROKARBONLAR Yalnızca karbon (C) ve hidrojen () elementlerinden oluşan bileşiklere hidrokarbon denir. Karbon elementinin atom numarası 6 dır. Elektron dizilişi, 1s 2 2s 2 2p 2 olup değerlik elektron say
İDROKARBONLAR Yalnızca karbon (C) ve hidrojen () elementlerinden oluşan bileşiklere hidrokarbon denir. Karbon elementinin atom numarası 6 dır. Elektron dizilişi, 1s 2 2s 2 2p 2 olup değerlik elektron say
KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü
 KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 13 Asitler ve
KİM-118 TEMEL KİMYA Prof. Dr. Zeliha HAYVALI Ankara Üniversitesi Kimya Bölümü Bu slaytlarda anlatılanlar sadece özet olup ayrıntılı bilgiler ve örnek çözümleri derste verilecektir. BÖLÜM 13 Asitler ve
