EAU TESTİS KANSERİ KILAVUZU
|
|
|
- Onur Bucak
- 10 yıl önce
- İzleme sayısı:
Transkript
1 EAU TESTİS KANSERİ KILAVUZU P. Albers (başkan), W. Albrecht, F. Algaba, C. Bokemeyer, G. Cohn-Cedermark, A. Horwich, M. P. Laguna, Avrupa Üroloji Derneği 2008 Çeviri: Üroonkoloji Derneği 1
2 İÇİNDEKİLER: 1. GİRİŞ 1.1. Yöntem 2. PATOLOJİK SINIFLANDIRMA 3. TANI 3.1. Fizik muayene 3.2. Testisin görüntülenmesi 3.3. Serum tümör belirleyicileri 3.4. İnguinal eksplorasyon ve orşiektomi 3.5. Organ koruyucu cerrahi 3.6. Testisin patolojik incelenmesi 3.7. Karsinoma in situ (Tin) tanı ve tedavisi 3.8. Tarama 4. EVRELEME 4.1. Tanıda kullanılan araçlar 4.2. Serum tümör belirleyicileri. Orşiektomi sonrası yarı-ömür kinetikleri 4.3. Retroperitoneal, mediastenal, supraklaviküler lenf düğümleri ve organlar 4.4. Evreleme ve prognostik sınıflamalar 4.5. Prognostik risk faktörleri 5. FERTİLİTEYE ETKİ VE FERTİLİTEYLE İLİŞKİLİ KONULAR 6. TESTİS KANSERİ TANI VE EVRELEME KILAVUZU 7. TEDAVİ: EVRE 1 GERM HÜCRELİ TÜMÖRLER 7.1. Evre 1 Seminom İzlem Adjuvan kemoterapi Adjuvan radyoterapi Retroperitoneal lenf düğümü diseksiyonu (RPLDD) Riske göre tedavi 7.2. Evre I seminom tedavi kılavuzu 7.3. Evre I seminom dışı germ hücreli tümör (SDGHT) İzlem Birincil kemoterapi 2
3 Riske göre tedavi Retroperitoneal lenf düğümü diseksiyonu (RPLDD) 7.4. Yüksek (ısrarlı) serum tümör belirleyicileriyle birlikte olan KE1S 7.5. Evre I SDGHT tedavi kılavuzu 8. TEDAVİ: METASTATİK GERM HÜCRELİ TÜMÖRLER 8.1. Düşük hacimli metastatik hastalık (evre II A/B) Evre IIA/B seminom Evre IIA/B SDGHT 8.2. İlerlemiş metastatik hastalık Birincil kemoterapi 8.3. Tekrar evreleme ve ileri tedavi Tekrar evreleme Rezidü tümör rezeksiyonu İkincil cerrahi sonrası pekiştirme kemoterapisi 8.4. Nüks eden veya tedaviye dirençli hastalıkta sistemik kurtarma tedavisi Seminom Seminom dışı Geç nüks (birinci basamak tedavinin tamamlanmasından 2 yıl sonra) 8.5. Kurtarma cerrahisi 8.6. Beyin metastazlarının tedavisi 8.7. Metastatik germ hücreli tümör tedavi kılavuzu 9. SAĞALTIM AMAÇLI TEDAVİ SONRASI TAKİP 9.1. Genel bilgiler 9.2. Seminom dışı evre 1 tümörlerde takip İzlem sırasında takip Sinir koruyucu RPLDD sonrası takip Adjuvan kemoterapi sonrası takip 9.3. Evre 1 seminomda takip Radyoterapi sonrası takip İzlem sırasında takip Adjuvan kemoterapi sonrası takip 9.4. Evre II ve ilerlemiş (metastatik) hastalıkta takip 10. TESTİS STROMA TÜMÖRLERİ 3
4 10.1. Giriş Yöntem Sınıflama Leydig hücreli tümörler Epidemiyoloji Leydig hücreli tümörlerin patolojisi Tanı Tedavi Takip Sertoli hücreli tümörler Epidemiyoloji Sertoli hücreli tümörlerin patolojisi Sınıflandırma Tanı Tedavi Takip Granuloza hücreli tümör Tekoma/fibroma grup tümörler Diğer seks kord/gonadal stroma tümörleri Germ hücresi ve seks kord/gonadal stroma içerikli tümörler (gonadoblastoma) Testisin diğer tümörleri Ovaryan epitelyal tip tümörler Toplayıcı kanallar ve rete testis tümörleri Spesifik olmayan stroma tümörleri (benin ve malin) 11. KAYNAKLAR Germ hücreli tümörler Germ hücre dışı tümörler 4
5 Çeviri Notu: Kılavuzda yer alan bazı tıbbi terimler ve tercümede kullanılan Türkçe karşılıkları aşağıda yazıdaki kullanım sırasıyla verilmiştir. incidence: cure: curative: surveillance: primary: frozen section: stage: classification: marker: WHO: invasion: mixed: specific: sensitive: negative predictive value: predict: survival: involvement: extension: relaps: proliferation: secondary: salvage: grade: consolidation: insidans sağaltım sağaltım amaçlı izlem birincil dondurulmuş kesit evre sınıflama belirleyici DSÖ yayılım karışık özgül duyarlı negatif öngörücü değer tahmin, öngörü sağkalım tutulum uzanım nüks, hastalık tekrarı çoğalma ikincil kurtarma derece pekiştirme 5
6 1. GİRİŞ Testis kanseri erkek neoplazmlarının %1-1.5 ini, tüm ürolojik tümörlerin ise %5 ini teşkil eder ve Batı toplumlarında her erkekte yılda 3-6 yeni olgu görülmektedir (1,2). Özellikle Kuzey Avrupa ülkelerinde 1970 ve 1980 li yıllarda testis kanseri insidansında artış gözlenmiştir. Son 30 yıl içinde Kuzey Amerika, Avrupa ve Okyanusya daki sanayileşmiş ülkelerin çoğunda testis kanseri insidansında artış eğilimi görülürken, komşu ülkelerde şaşırtıcı derecede farklı insidans oranları görülebilmektedir (3)A.B.D de 1973 ile 1998 arası Surveillance Epidemiology and End Results Program verileri beyaz erkeklerde sadece seminom riskinde devam eden bir artış göstermektedir (4). Tanı anında olguların sadece %1-2 kadarı çift taraflıdır. Histolojik tipler değişkenlik göstermekle beraber germ hücreli tümörlerin belirgin hakimiyeti vardır (1). İnsidansın en yüksek olduğu yaşlar seminom dışı tümörler için 20 ile 30 yaş arası, saf seminom için ise 30 ile 40 yaş arasıdır. Ailesel olgular özellikle kardeşler arasında görülebilmektedir. Testis kanseri olan hastalarda genetik değişiklikler tarif edilmiştir. Germ hücreli tümörlerin tüm histolojik tiplerinde 12. kromozomun kısa kolunun izokromozomu (i(12p) özgül bir genetik belirleyici olarak tarif edilmiştir. İntratübüler germ hücreli neoplazi (testiküler intraepitelyal neoplazi, Tin) aynı kromozomal değişiklikleri gösterir ve testiküler Tin olgularının %66 sında p53 bölgesi değişiklikleri bulunmuştur (6). Tin ve germ hücre neoplazisinin gelişimine neden olan olay muhtemelen fetal germ hücrelerinin pluripotent düzenlenmelerinde oluşan bozukluklardır (bu bozukluklar M2A, C-KIT ve OCT4/NANOG gibi özgül belirleyiciler ile saptanabilir). Seminom ve embryonal karsinom gelişiminde bazı çakışmaların olduğu genom-wide expression analizi ile gösterilebilmekte ayrıca bazı atipik seminomlarda alfa-fetoprotein (AFP) mrna sı saptanabilmektedir (7,8). Testiküler tümörlerin gelişimi için epidemiyolojik risk faktörleri kriptorşidizm yada inmemiş testis öyküsü, Klinefelter sendromu, aile öyküsünde birinci derece akrabalarda (kardeş, baba) testiküler tümör bulunması, karşı taraf testiste tümör yada TIN varlığı ve infertilite olarak sıralanabilir (9-14). Uzun boylu olmak germ hücreli kanser ile ilişkilendirilmiş olmakla beraber bu bulguyu doğrulayan ileri çalışmalara ihtiyaç vardır (15). Günümüzde testis tümörleri mükemmel sağaltım oranları göstermektedir. Bu durumu etkileyen ana etkenler tanı anında dikkatli bir evrelendirme, kemoterapi kombinasyonlarına dayanan erken ve uygun tedavinin gerekli durumlarda radyoterapi ve cerrahi tedavinin de 6
7 eklenmesi ile uygulanması, çok sıkı izlem ve kurtarma tedavileridir. Son on yılda tanı ve tedavinin başlanmasındaki gecikmeler azalmıştır (16). Testiküler kanserlerin tedavisinde tedavi merkezinin seçimi çok önemlidir. Erken evreler referans olmayan merkezlerde başarıyla tedavi edilebilmesine rağmen nüks oranları daha yüksektir (17). Klinik çalışmalarda kötü prognozlu, seminom dışı germ hücreli tümörlerin toplam sağkalım oranları tedavi edilen hasta sayısı ile ilişkili bulunmuştur (5 hastanın altında daha kötü sağkalım) (18) Yöntem Bu kılavuz daha önce yayınlanan kılavuzların geliştirilmesiyle oluşturulmuştur. Bir önceki EAU Kılavuzu 2005 yılında derleme makale olarak yayınlanmış (19) ve Mart 2006 da EAU üyelerine dağıtılmıştı. Şu anki kılavuza testiküler stromal tümörler ile ilgili bir bölüm eklenmiştir. Bu kılavuz üroloji, medikal onkoloji, radyoterapi ve patoloji uzmanlarından oluşan bir takım tarafından hazırlanmıştır. Kılavuz Ekim 2007 tarihine kadar germ hücreli ve germ hücre dışı tümörlerle ilgili yayınlanan çalışmaların taranarak gözden geçirilmesi ile oluşturulmuştur. Ek olarak meta analiz çalışmalarında elde edilen veriler, Cochrane bulguları ve European Germ Cell Cancer Collaborative Group tarafından Kasım 2006 Amsterdam Toplantısında yapılan öneriler ve diğer mevcut kılavuzlardan yararlanılmıştır (20-26). Mümkün olan her durumda kaynaklar kanıta dayalı tıp (KDT) prensiplerine uygun isimlendirilmiştir. Bu kılavuzda yer alan öneriler kanıt derecesine göre tanımlanmıştır (27). 2. PATOLOJİK SINIFLANDIRMA Önerilen patolojik sınıflama (Dünya Sağlık Örgütü nün [DSÖ] 2004 sınıflamasından değişiklik yapılarak oluşturulmuştur) aşağıda gösterilmiştir (28) 1. Germ hücreli tümörler İntratübüler germ hücreli neoplazi Seminom (sinsisyotrofoblastik hücreli olgular dahil) Spermatositik seminom (sarkomatoz içerik varsa belirtilir) Embriyonal karsinom Yol sak tümörü Koryokarsinom 7
8 Teratom (matür, immatür, malin içerikli) Birden fazla histolojik tipi olan tümörler (her tip % olarak belirtilir) 2. Seks kord/gonadal stromal tümörler Leyding hücreli tümör Malin Leyding hücreli tümör Sertoli hücreli tümör - lipidden zengin tip - sklerozan - kalsifiye büyük hücreli Malin Sertoli hücreli tümör Granüloza hücreli tümör - erişkin tip - jüvenil tip Tekoma/fibroma grubu tümörler Diğer seks kord/gonadal stromal tümörler - tam diferansiye olmamış - karışık Germ hücreli ve seks kord/gonadal stromal yapıları beraber içeren tümörler (gonadoblastoma) 3. Çeşitli özgül olmayan stromal tümörler - Ovaryan epitelyal tümörler - Toplayıcı duktuslar ve rete testis tümörleri - Özgül olmayan stroma tümörleri (benin veya malin) 3. TANI 3.1. Fizik muayene Testis kanseri genellikle genç erkekleri hayatın üçüncü ve dördüncü on yılında etkiler. Normalde skrotum içinde ağrısız tek taraflı kitle olarak ortaya çıkar (29). Olguların yaklaşık %20 sinde ilk semptom skrotal ağrıdır ve testiküler kanser hastalarının %27 sinde bölgesel ağrı görülebilir (1). 8
9 Bazen skrotal travma sonucu testiküler kitlenin varlığı fark edilir. Jinekomasti olguların %7 sinde görülür ve seminom dışı tümörlerde daha sıktır. Bel ve sırt ağrısı olguların %11 inde görülür (16). Testis tümörünün ortaya çıkmasında önce testis boyutlarında küçülme görülebilir (30). Olguların %10 kadarında testis tümörü orşidoepididimiti taklit eder ve bu nedenle doğru tanının konulması gecikebilir (1,2). Şüpheli durumlarda ultrasonografi yapılmalıdır. Fizik muayene kitlenin özelliklerinin belirlenmesini sağlar ve supraklaviküler lenf düğümü, batın içi kitle, jinekomasti gibi eşlik edebilecek bulguların saptanabilmesi için mutlaka genel muayene ile beraber yapılmalıdır. Skrotum içi kitle olan tüm olgularda mutlaka doğru tanı ortaya konulmalıdır (31) Testisin görüntülenmesi Günümüzde tanısal ultrason testiküler kitlenin varlığının kesinleştirilmesi ve karşı taraf testisin incelenmesi amacıyla kullanılır. Skrotal ultrasonun tanı koymada duyarlılığı hemen hemen % 100 dür ve kitlenin testisin kendisinden mi yoksa testis dışından mı kaynaklandığının belirlenmesinde önemli rolü vardır (32). Ultrasonografi ucuz bir testtir ancak testiküler tümörün varlığı klinik olarak belirgin ise yapılması gereksizdir (33). Ele gelen testiküler kitlesi olmayan ancak retroperitoneal veya organ metastazları olan veya insan koryonik gonadotropin (hcg) veya AFP serum düzeyi yükselmiş genç erkeklerde testis ultrasonu yapılmalıdır (34-37). Riskli hastaların takibinde karşı testisin ultrason ile izlenmesi önerilmektedir (38). Magnetik rezonans görüntüleme (MRG) tümör tanısında ultrasona göre daha yüksek duyarlılık ve özgüllüğe sahiptir (39-41) ve bazı durumlarda seminom ve seminom dışı tümörlerin ayrımını yapabilir. Skrotumun MRG incelemesi %100 duyarlılık ve % özgüllük sağlamasına rağmen (42) yüksek maliyeti nedeniyle tanı amaçlı kullanılması önerilmez Serum tümör belirleyicileri Serum tümör belirleyicileri prognostik olarak önem taşırlar ve tanı ve evrelemede rol alırlar (43). Aşağıdaki belirleyiciler ölçülmelidir: AFP (yolk kesesi hücrelerince salgılanırlar) hcg (trofoblast ekspresyonunu gösterir) 9
10 Laktat dehidrogenaz (LDH) (doku yıkımının belirleyicisidir) metastazı olan hastalarda önerilir. Genel olarak testis kanserlerinin %51 inde bu belirleyicilerde yükseklik vardır (16,29). AFP seminom dışı germ hücreli tümörlerin (SDGHT) %50-70 inde, hcg ise %40-60 ında yüksek bulunur. SDGHT lerin %90 ında AFP ve/veya hcg yüksekliği bulunur. Seminomlarda ise tanı anında veya hastalığın seyri sırasında %30 a kadar oranlarda hcg yüksekliği görülür (44,45). Laktat dehidrogenaz daha az özgül bir belirleyicidir ve tümör hacmiyle doğru orantılıdır. İleri evre hastaların %80 inde yükselebilir (44). Tümör belirleyicilerin yüksek olmamasının tümör tanısını ortadan kaldırmadığı akılda tutulmalıdır. Üstünde çalışılan diğer tümör belirleyicileri arasında saf seminom hastalarının takibinde değerli olabilecek plasental alkalen fosfataz (PLAP) vardır. Belirli merkezlerde sitogenetik ve moleküler belirleyiciler bulunmakta ancak bunlar günümüzde araştırma amaçlı olarak kullanılmaktadır. AFP, hcg ve LDH (ilerlemiş tümörlerde) mutlaka, PLAP ise isteğe bağlı olarak ölçülmelidir İnguinal eksplorasyon ve orşiektomi Testiste kitleden şüphelenilen her hastada inguinal eksplorasyon yapılmalı ve testis tunikasıyla birlikte dışarı alınmalıdır. Tümör bulunması durumunda hemen spermatik kord internal inguinal halka seviyesinden ayrılarak orşiektomi yapılmalıdır. Eğer tanı kesin değilse testiküler biyopsi alınarak dondurulmuş kesit histolojik inceleme yapılmalıdır. Yaygın hastalıkta yada yaşamı tehdit eden metastazların varlığı halinde güncel uygulamada hemen kemoterapi başlanabilir ve orşiektomi hastanın klinik durumu düzelene kadar geciktirilebilir Organ koruyucu cerrahi Karşı testiste tümör olmayan olgularda organ koruyucu cerrahi indikasyonu olmamasına rağmen, gerekli önlemler alınmak şartıyla bazı özel olgularda uygulanabilir. Eş zamanlı çift taraflı testis tümörlerinde, farklı zamanlı karşı taraf tümörlerde ve soliter testis tümöründe ameliyat öncesi serum testosteron düzeyi normalse ve bu olgularda tümör hacmi testiküler hacmin %30 undan daha az ise cerrahi prensiplere uyularak organ koruyucu cerrahi uygulanabilir. Bu olgularda ilişkili Tin oranları yüksek olması nedeniyle (%82 ye ulaşan oranlarda) geride kalan testis dokusu 20 Gy dozda adjuvan radyoterapi ile tedavi edilmelidir (46). 10
11 Radyoterapi sonrası infertilite gelişecektir ve tek testisin radyoterapisi sonrası uzun dönmede Leyding hücre yetmezliği riski de artmıştır (47). Baba olmak isteyen fertil hastalarda radyoterapi geciktirilebilir. Organ koruyucu cerrahi seçeneği hasta ile dikkatli şekilde tartışılmalı ve cerrahi deneyimli bir merkezde uygulanmalıdır (48, 49) Testisin patolojik incelenmesi Patolojik incelemede gerekli şartlar: Makroskopik özellikler: boyut, testis boyutu, tümörün en büyük boyutu ve epididim, spermatik kord ve tunika vajinalisin makroskopik özellikleri. Örnekleme: (eğer varsa) normal makroskopik parankim ve şüphelenilen alanlardaki albuginea ve epididimi de kapsayacak şekilde en büyük tümör çapının her santimetresi için 1cm² lik kesitler. Spermatik kordun en azından bir proksimal ve bir distal kesiti ve şüpheli tüm bölgeleri. Mikroskopik özellikler ve tanı: DSÖ 2004 e (28) göre histolojik tip (her bir bileşen ayrı ayrı belirtilir ve yüzde olarak tahmini miktar verilir). - Peri-tümöral venöz ve/veya lenfatik yayılımın varlığı yada yokluğu. - Albuginea, tunika vajinalis, rete testis, epididim yada spermatik kord yayılımının varlığı yada yokluğu. - Tümör olmayan parenkimde intratübüler germ hücre neoplazisi (Tin) olup olmadığı. TNM 2002ye göre pt kategorisi (Tablo 1). İmmünohistokimyasal çalışmalar: Seminom ve karışık germ hücreli tümörde, AFP, hcg. Şüphede kalınan olgularda önerilen immünohistokimyasal belirteçler: Seminomda: sitokeratinler (CAM 5.2), PLAP, c-kit İntratübüler germ hücre noeplazisinde: PLAP, c-kit Diğer önerilen belirteçler: kromogranin A (CgA), Ki-1 (MIB-1) 3.7. Karsinoma in situ (Tin) tanı ve tedavisi 11
12 Karşı testiste Tin olmadığının gösterilmesi karşı testis biyopsisi savunulmaktadır (50). Bu bazı ülkelerde rutin uygulanmasına rağmen, TIN insidansının ve karşı taraf testiste eş zamanlı tümör insidansının düşük olması (sırasıyla %9 a kadar ve yaklaşık %2.5) (58, 59), TIN tedavisinin morbiditesi ve eş zamanlı tümörlerin çoğunun tanı anında düşük evrede oluşları karşı testis biyopsilerinin rutin uygulanması önerisini tartışılır kılmaktadır (54-56). Karşı tarafta TIN varlığının tüm olgularda belirlenmesinin gerekliliği hakkında bir fikir birliği oluşturmak hala oldukça zordur. Yine de karşı taraf testi biyopsisi testis hacmi 12 ml den az, kriptorşidizm öyküsü olan ve 40 yaşın altındaki hastalar gibi karşı taraf testiste Tin için yüksek risk grubunda olan hastalara teklif edilmelidir (52, 57-59). Duyarlılığı arttırmak amacıyla çift biyopsi tercih edilir. TIN tanısı konulduğunda seçilecek tedavi lokal radyoterapidir (her biri 2 Gy lik fraksiyonlar halinde toplam 20 Gy). Bu uygulama infertiliteye yol açacağı için tedavi başlamadan önce hastalar dikkatlice aydınlatılmalıdır (52, 60). İnfertiliteye ek olarak radyoterapi sonrası uzun dönemde Leydig hücre fonksiyonu ve testosteron üretimi de bozulabilir (47). Çocuk sahibi olmak isteyen fertil hastalarda radyoterapi ertelenebilir Tarama Tarama programlarının avantajını gösteren herhangi bir çalışma bulunmamasına rağmen evre ve prognozun erken tanı ile doğrudan ilişkili olduğu gösterilmiştir. Klinik risk faktörlerinin varlığında bu kişilerin kendi kendilerin muayene etmeleri önerilir. 4. EVRELEME Metastatik yada gizli hastalığın saptanması için serum tümör belirleyicilerin yarı ömürlerine göre serum düzeylerindeki değişiklikler hesaplanmalı, lenf düğümleri lenf yolları boyunca taranmalı ve organ metastazları araştırılmalıdır. Sonuç olarak yapılması zorunlu değerlendirmeler şunlardır: Orşiektomi sonrası tümör belirleyicilerinin yarı-ömür kinetikleri Retroperitoneal ve supraklavikuler lenf düğümlerinin ve karaciğerin durumu Mediastinal lenf düğümü tutulumu ve akciğer metastazlarının varlığı veya yokluğu 12
13 Şüpheli semptom varlığında beyin ve kemiklerin durumunun değerlendirilmesi Tanıda kullanılan araçlar Elimizde bulunan mevcut testler şunlardır: Ardışık kan örneklemesi Akciğer filmi Abdominopelvik ve toraks bilgisayarlı tomografisi (BT) Abdominal ve retroperitoneal ultrason, magnetik rezonans görüntüleme (MRG) Pozitron emisyon tomografi (PET) taraması Klinik şüpheye göre seçilecek diğer özgül testler 4.2. Serum tümör belirleyicileri. Orşiektomi sonrası yarı-ömür kinetikleri AFP nin yarı ömrü 5-7 gün, hcg nin ise yaklaşık 2-3 gündür (44). Bu nedenle orşiektomi sonrası yarı-ömür kinetiklerinin belirlenmesi için tümör belirleyicilerinin serum düzeylerine tekrar bakılmalıdır. Klinik evre I hastalarda tümör belirleyici serum düzeyleri normalleşinceye kadar takip edilmelidir. Orşiektomi sonrası tümör belirleyici düzeyleri hastanın International Germ Cell Cancer Collaborative Group un (IGCCCG) risk sınıflamasına göre sınıflanabilmesi için önemlidir. Orşiektomi sonrası serum tümör belirleyicilerin yüksek kalması mikroskopik veya makroskopik metastatik hastalığa işaret edebilirken tümör belirleyicilerin orşiektomi normal seviyeye düşmesi tümör metastazı olmadığını kesin olarak göstermez. Kemoterapi sırasında tümör belirleyici düzeyleri düşmelidir, belirleyicilerin yüksek kalması kötü prognostik anlam taşır Retroperitoneal, mediastinal, supraklaviküler lenf düğümleri ve organlar Retroperitoneal ve mediastinal lenf düğümleri en iyi bilgisayarlı tomografi (BT) ile değerlendirilir.supraklaviküler lenf düğümleri için en iyi yöntem fizik muayenedir. BT retroperitondaki lenf düğümleri için %70-80 duyarlılığa sahiptir. Doğruluk oranı lenf düğümlerinin boyutu ile bağımlıdır. Hedef bölgelerde bulunan metastatik lenf düğümlerini belirlemek amacıyla 3 mm lik kesitler alındığında duyarlılık ve negatif öngörücü değer artmaktadır (61). Bu oranlar evre I ve II için biraz daha düşüktür (62, 63) ve aşağı evreleme 13
14 oranları %25 ile 30 arasında değişmektedir (64). Yeni nesil BT cihazlarının da duyarlılığı arttırabildiği gösterilememiştir. Magnetik rezonans görüntüleme (MRG) retroperitoneal lenf düğümlerindeki büyümenin belirlenmesinde BT ile benzer sonuç vermektedir (65). MRG kullanımının dezavantajları yüksek maliyeti ve her yerde kolay ulaşılabilir olmamasıdır. Yine de MRG BT veya ultrasonun kesin sonuç veremediği durumlarda (65), damar içi kontrast allerjisi nedeniyle BT nin kontrendike olduğu durumlarda veya hasta veya doktorun radyasyon dozu ile ilgili endişelerinin olması durumunda faydalı olabilir. MRG isteğe bağlı bir testtir ve günümüzde testis tümörlerinin evrelemesinde sistematik olarak kullanım indikasyonu yoktur. Akciğer grafisi toraks incelemesi için rutin testtir. Retroperitoneal ve pelvik BT nin negatif olduğu seminomlu olgularda anteroposterior ve lateral akciğer grafisi toraks incelemesi için tek başına yeterlidir (66). Göğüs BT toraks ve mediyastinal lenf düğümlerinin değerlendirilmesinde en duyarlı yöntemdir (66). SDGHT hastalarında %10 a kadar oranlarda radyolojik olarak görülebilmesi mümkün olmayan küçük subplöral nodüller bulunabilmesi nedeniyle toraks BT önerilmelidir (1). BT nin duyarlılığı yüksek ancak özgüllüğü düşüktür (65). SDGHT hastalarının tümünde ve pozitif batın BT olan seminomlarda toraks BT incelemesi mutlaka yapılmalıdır (66). Testis kanseri evrelemesinde florodeoksiglukoz-pozitron emisyon tomografisi (FDG-PET) kullanımını destekleyecek yeterli kanıt yoktur. Ancak seminomlarda kemoterapiden en az 4 hafta sonra rezidüel kitlesi olan hastalarda izlem yada aktif tedavi kararı verilmesi amacıyla önerilir (67-70). Beyin ya da spinal BT, kemik sintigrafisi yada karaciğer ultrasonu, bu organlarda metastaz şüphesi olduğunda yapılmalıdır. Kafa BT ve MRG SDGHT hastalarında yaygın akciğer metastazı olması durumunda önerilir. Tablo 1 de evreleme için önerilen testler gösterilmiştir. Tablo 1: Tanı anında evreleme için önerilen testler Test B Derece Öneri C Derece Öneri Serum tümör belirleyicileri Alfa-feto protein hcg LDH (tüm ilerlemiş tümörlerde) Abdominopelvik BT Tüm hastalar Ergenlik çağında zayıf hasta Akciğer grafisi Seminom a Toraks BT SDGHT Testis ultrasonu Klinik şüphe ve tanı sırasında 14
15 palpasyonla normal skrotum MRG Abdominal BT nin karasız kaldığı durumlar PET b Seminomda rezidü kitlelerin takibi Diğer Klinik şüphe varsa a Eğer abdominopelvik BT negatif ise Tüm hastalar b Günümüzde tanı sırasında PET incelemesi indikasyonu yoktur 4.4. Evreleme ve prognostik sınıflamalar Bu kılavuzda önerilen evreleme sistemi UICC nin (International Union Against Cancer) 2002 TNM sistemidir (Tablo 2) (71). Bu sistemin içeriği şöyledir: Hastalığın anatomik yaygınlığının belirlenmesi Serum tümör belirleyici düzeyleri ve orşiektomi sonrası hcg, AFP ve LDH nin en düşük seviyeleri (S kategorisi) Bölgesel lenf düğümlerinin açıkça tanımlanması Lenf düğümü boyutuna göre N sınıfında bazı değişiklikler Tablo 2: TNM Sınıflandırması (UICC, 2002, 6.baskı) pt Primer tümör 1 ptx Primer tümör değerlendirilemiyor pt0 Primer tümör bulgusu yok (örneğin testiste histolojik skar) ptis İntratübüler germ hücreli neoplazi (carcinoma in situ) pt1 Tümör testis ve epididime sınırlı vasküler/lenfatik yayılım yok: tümör tunika albugineaya yayılmış olabilir ancak tunika vaginalise yayılım yok. pt2 Tümör testis ve epididime sınırlı vasküler/lenfatik yayılım var veya tunika albugineayı aşmış ve tunika vaginalis tutulumu oluşmuş. pt3 Tümör spermatik korda yayılmıştır (vasküler/lenfatik yayılım var veya yok) pt4 Tümör skrotuma yayılmıştır (vasküler/lenfatik yayılım var veya yok) N Bölgesel lenf düğümleri klinik Nx Bölgesel lenf düğümleri değerlendirilemiyor N0 Bölgesel lenf düğümlerinde metastaz yok N1 En büyük boyutu 2 cm veya daha az tek lenf düğümü veya hiçbirinin en büyük 15
16 boyutu 2 cm den büyük olmayan birden çok lenf düğümü metastazı N2 En büyük boyutu 2 ile 5 cm arası tek lenf düğümü metastazı veya an az biri 2 cm den büyük ancak 5 cm den küçük birden çok lenf düğümü metastazı N3 En büyük çapı 5 cm den büyük lenf düğümü metastazı pn Patolojik pnx Bölgesel lenf düğümleri değerlendirilemiyor pn0 Bölgesel lenf düğümlerinde metastaz yok pn1 En büyük boyutu 2 cm veya daha küçük ve 5 veya daha az sayıda hiçbirinin en büyük boyutu 2 cm den fazla olmayan lenf düğümüm metastazı pn2 En büyük boyutu 2 cm den büyük ancak 5 cm den küçük veya hiçbiri 5 cm den büyük olmayan 5 adetten daha fazla sayıda lenf düğümü metastazı, veya tümörün lenf düğümü dışına uzanım gösterdiğine dair bulgu olması pn3 En büyük boyutu 5 cm den büyük lenf düğümü metastazı M Uzak metastaz Mx Uzak metastaz değerlendirilemiyor M0 Uzak metastaz yok M1 Uzak metastaz var M1a Bölgesel olmayan lenf düğümleri yada akciğer metastazı M1b Diğer bölgeler S Serum tümör belirleyicileri Sx Serum tümör belirleyici sonuçları elde yok veya çalışılmamış S0 Serum tümör belirleyicileri normal sınırlarda LDH (U/l) hcg (miu/ml) AFP (ng/ml) S1 <1,5 x N ve <5000 ve <1000 S2 1,5 - veya veya S3 >10 x N veya >50000 veya >10000 N: LDH için normalin üst sınırını gösterir. 1 ptis ve pt4 gibi sınıflandırma için sınıflandırma için radikal orşeiktominin her zaman gerekli olmadığı durumlar hariç, primer tümörün uzanımı radikal orşiektomi sonrası sınıflandırılır; bakınız pt4. Diğer durumlarda radikal orşiektomi yapılmamışsa Tx kullanılır. 16
17 2002 TNM sınıflandırmasına göre evre 1 testis kanseri aşağıdaki alt evrelere ayrılmaktadır: Evre 1A pt1 N0 M0 S0 Evre 1B pt2, pt3 veya pt4 N0 M0 S0 Evre 1S Herhangi bir pt/tx N0 M0 S1-3 Evre 1A hastalar testis ve epididimde sınırlı birincil tümörleri olan, mikroskopik incelemede tümör hücrelerinin mikroskopik vasküler veya lenfatik yayılım yapmadığı, klinik muayene veya görüntülemede metastaz bulgusu olmayan ve orşiektomi sonrası serum tümör belirleyicileri normal sınırlar içinde olan hastalardır. Klinik evre I hastalarda serum tümör belirleyicilerinin düşüşü normal sınırlara ulaşılıncaya değin takip edilmelidir. Evre 1B hastalar daha fazla bölgesel yayılım gösteren birincil tümörü olan ancak metastaz bulgusu olmayan hastalardır. Evre 1S hastalar orşiektomi sonrası tümör belirleyicilerinin serum düzeylerindeki yükseklik devam eden (ve genellikle artan) hastalardır ki bu durum subklinik metastatik hastalığın (veya karşı testiste ikinci bir germ hücre tümörü olasılığının) göstergesidir. Orşiektomi sonrası tümör belirleyici seviyeleri beklenen yarı ömürlere uygun olarak düşüş gösteriyorsa normal düzeylere ulaşılıncaya kadar hasta takip edilir. Topluma dayalı geniş serilerde seminom hastalarının %75-80 ni, SDGHT hastalarının ise %55 i tanı anında evre I hastalığa sahiptir (72,73). Gerçek evre IS hastalık (orşiektomi sonrası yüksek veya yükselen serum tümör belirleyicileri) seminom dışı hastaların %5 inde bulunur. Evre IS hastalara evreleme amaçlı RPLDD yapılması durumunda bunların hemen hemen tamamında patolojik evre II hastalık olduğu görülecektir (pn+) (1,2,5,72). IGCCCG 1997 yılında metastatik testis tümöründe bazı bağımsız klinik olumsuz faktörleri kullanarak prognostik faktörlere dayalı bir evreleme sistemi tanımladı. TNM Sınıflamasına dahil edilen ve bu sistemde histoloji, birincil tümörün yerleşim yeri, metastazların yeri ve kemoterapi öncesi tümör belirleyicilerin serum düzeyi kullanılarak hastalar iyi orta ve kötü prognoza sahip olarak sınıflandırılır (Tablo 3) (74). Tablo 3: Metastatik germ hücreli tümörlerde prognoza bağlı evreleme sistemi (International Germ Cell Cancer Collaborative Group) İyi prognoz grubu Seminom dışı Aşağıdaki kriterlerin hepsi sağlanmalı: 17
18 Hastaların %56 sı 5 yıllık ilerlemesiz sağkalım: %89 5 yıllık sağkalım: %92 Seminom Hastaların %90 ı 5 yıllık ilerlemesiz sağkalım: %82 5 yıllık sağkalım: %86 Orta prognoz grubu Seminom dışı Hastaların %28 i 5 yıllık ilerlemesiz sağkalım: %75 5 yıllık sağkalım: %80 Seminom Hastaların %10 u 5 yıllık ilerlemesiz sağkalım: %67 5 yıllık sağkalım: %72 Kötü prognoz grubu Seminom dışı Hastaların %16 sı 5 yıllık ilerlemesiz sağkalım: %41 5 yıllık sağkalım: %48 Seminom Hiçbir seminom kötü prognozlu olarak sınıflandırılmamıştır Testis veya retroperitoneal primer Akciğer dışı organ tutulumu yok AFP < 1000 ng/ml hcg < 5000 miu/l LDH< 1,5 x normal Aşağıdaki kriterlerin hepsi sağlanmalı: Herhangi bir primer yerleşim alanı Akciğer dışı organ tutulumu yok Normal AFP Herhangi bir hcg değeri Herhangi bir LDH değeri Aşağıdaki kriterlerin hepsi sağlanmalı: Testis veya retroperitoneal primer Akciğer dışı organ tutulumu yok AFP > 1000 ve <10000 ng/ml veya hcg > 5000 ve <50000 miu/l veya LDH> 1,5 ve <10 x NÜS Aşağıdaki kriterlerden herhangi biri: Herhangi bir primer yerleşim alanı Akciğer dışı organ tutulumu var Normal AFP Herhangi bir hcg değeri Herhangi bir LDH değeri Aşağıdaki kriterlerden herhangi biri: Mediastinal primer Akciğer dışı organ tutulumu var AFP > ng/ml veya hcg > miu/l veya veya LDH > 10 x NÜS NÜS: Normalin üst sınırı 4.5. Prognostik risk faktörleri Evre I seminomda tümör boyutu (> 4 cm) ve rete testise tümör yayılımı çoklu analizde nüksün öngörüsü için en önemli faktörler olarak belirlenmiştir (20). Seminom-dışı evre I hastalıkta gizli metastatik hastalığın öngörüsünde en önemli faktör birincil tümörüm kan veya lenf damarlarına yayılımıdır (lenfatik ve vasküler yayılım). Proliferasyon oranı ve embriyonal karsinom oranı vasküler yayılımın artı veya eksi öngörü değerini iyileştiren ek faktörlerdir (75,76). 18
19 Evre I de anlamlı prognostik patolojik risk faktörleri ve metastatik hastalık için klinik risk faktörleri Tablo 4 de sıralanmıştır. Tablo 4: Testis kanserinde gizli metastatik hastalık için prognostik faktörler Patolojik (evre I için) Histopatolojik tip Seminom için Tümör boyutu (> 4 cm) Rete testise yayılım Seminom-dışı için Tümör içinde veya peri-tümöral vasküler/lenfatik yayılım Proliferasyon oranı > %70 Embriyonal kanser oranı > %50 Klinik (metastatik hastalık için) Birincil yerleşim yeri Tümör belirleyicilerinde yükselme Akciğer-dışı organ metastazı olması 5. FERTİLİTEYE ETKİ VE FERTİLİTEYLE İLİŞKİLİ KONULAR Testis tümörü olan hastalarda sperm bozukluğu nadir değildir. Uygulanacak kemoterapi de fertiliteye zarar verir. Üreme çağındaki hastalara tedavi öncesi, hatta orşiektomi öncesi fertilite değerlendirmesi (testosteron, lutenizan hormon (LH) ve folikül stimulizan hormon (FSH) düzeyleri) ve sperm analizi ile birlikte sperm dondurulması teklif edilmelidir. Sperm dondurulması orşiektomi öncesi veya sonrasında olabilir ancak kemoterapi öncesi yapılmalıdır (47, 77-83). Çift taraflı orşiektomi yada TIN tedavisi sonrası düşük testosteron düzeyi olan hastalara hayat boyu dışardan testosteron verilmesi önerilir (84). Daha detaylı bilgi için EAU Erkek İnfertilitesi Kılavuzuna başvurunuz. 6. TESTİS KANSERİ TANI VE EVRELEME KILAVUZU 19
20 1. Testis ultrasonu mutlaka yapılmalıdır (Öneri derecesi: B). 2. Tanı ve bölgesel yayılımın belirlenmesi (pt Evresi) için orşiektomi ve testisin patolojik incelemesi gereklidir (B Derece Öneri). Yaygın metastazlara bağlı olarak hayatı tehdit eden bir durumun varlığında kemoterapi orşiektomiden önce başlanmalıdır. 3. Tümör belirleyicilerinin serum düzeyleri (AFP, hcg ve metastatik hastalıkta LDH) orşiektomi öncesi ve sonrası evreleme ve prognozun belirlenmesi amacıyla belirlenmelidir (Öneri derecesi B) 4. Testis kanserinde retroperitoneal, mediyastinal ve supraklaviküler lenf düğümlerinin durumu ve organ metastazlarının varlığı belirlenmelidir. Seminomda abdominal lenf düğümlerinde tutulum yoksa toraks BT incelemesi gerekli değildir (Öneri derecesi: B). 7. TEDAVİ: EVRE 1 GERM HÜCRELİ TÜMÖRLER 7.1. Evre 1 Seminom Modern evreleme yöntemlerinden sonra, evre 1 seminomu olan hastaların %15-20 sinde genellikle retroperiton yerleşimli subklinik metastatik hastalık bulunmaktadır ve bu durum hastalarda tek başına orşiektomi sonrası nüks oluşumuna sebep olur (85) İzlem Son on yılda çeşitli prospektif randomize olmayan izlem çalışmaları yapılmıştır. Bu çalışmalardan en genişi Kanada da yapılmış olup 1550 den fazla hastayı içermektedir (86). Bundan önce yayınlanan dört çalışmanın meta-analizinde 5 yıllık nükssüz sağkalım oranı %82.3 olarak bulunmuştur. Princess Margaret Hastanesi serisinde (n = 1559) seçilmemiş hastalarda genel nüks oranı %16.8 dir. Hesaplanan 5 yıllık nüks oranları %15-20 aralığında olup nükslerin büyük çoğunluğu ilk olarak diyafragma altı lenf düğümlerinde saptanmaktadır (85,87-89). İzlem sırasında nüks eden seminom hastaları için IGCCCG sınıflamasına göre doz ayarlaması yapılarak kemoterapi uygulanması seçilebilecek bir tedavidir. Ancak nüks eden hastaların %70 inde nüks sırasında hastalığın düşük hacimli olması nedeniyle tek başına radyoterapi uygun tedavi seçeneğidir. Kurtarma radyoterapisi sonrası bu hastaların sadece %20 kadarında tekrar nüks nedeniyle kurtarma kemoterapisine ihtiyaç görülür. Evre I seminomda deneyimli merkezler tarafından izlem tedavisi için genel kansere özgü sağkalım oranı % arasında bildirilmiştir (88,89). İzlem protokolünün en önemli dezavantajı daha yoğun takip ihtiyacıdır. Özellikle retroperiton bölgesinin orşiektomi sonrası en az 5 yıl boyunca sık tekrarlanan görüntüleme yöntemleriyle incelenmektedir. Buna karşılık adjuvan radyoterapi sonrası diyafragma altında nüks görülme sıklığı çok düşüktür. 20
21 İzlem sırasında nükslerin yaklaşık %20 si orşiektomiden 4 yıl sonra görülür (88). İzlem tedavisinin maliyet analizi radyoterapininki ile karşılaştırıldığında izlemin daha pahalı olduğunu göstermektedir (90) ancak hesaplamalar takip takvimlerine bağlı olarak değişebilmektedir (91,92) Adjuvan kemoterapi MRC ve European Organization for Research and Treatment of Cancer (EORTC) tarafından beraber gerçekleştirilen bir siklus karboplatin ile adjuvan radyoterapinin karşılaştırıldığı çalışmada (MRC TE19 çalışması, EORTC çalışması) ortanca 4 yıllık takip sonrası nüks oranı, nükse kadar geçen süre ve sağkalım oranları açısından tedaviler arasında fark olmadığı gösterilmiştir (93). Bu nedenle evre 1 seminom tedavisinde adjuvan karboplatin tedavisi, radyoterapi ve izleme alternatif bir seçenektir (88,89,93). İki kür adjuvan karboplatin relaps oranını %1-3 daha azaltıyor gibi görünmektedir, fakat daha çok deneyim ve uzun dönem gözlemlere gereksinim vardır Adjuvan radyoterapi Seminom hücreleri radyasyona son derece duyarlıdır. Para-aortik (PA) alana veya hokey sopası alanına (para-aortik ve aynı taraf ilyak düğümler) ılımlı dozda (toplam Gy) adjuvan radyoterapi uygulaması nüks oranını %1-3 e düşürür (98-101). Modern radyoterapi uygulamaları sonrasında hemen hemen tüm olgularda nüksler ilk oluşum yeri radyasyon uygulanan bölgenin dışındadır (diyafram üstü lenf düğümleri veya akciğerler) (98-101). Fossa ve arkadaşların geniş randomize Medical Research Council (MRC) çalışmasının sonuçlarına dayanarak evre 1, T1-T3 testis seminomu olan ve lenfatik drenajı bozulmamış hastalara, paraaortik alan radyoterapisi standart tedavi olarak önerilmiştir (98,99). Para-aortik alana radyoterapi uygulaması sonrası geleneksel köpek bacağı bölgesine göre akut toksisite oranı daha düşük ve ilk 18 ay içinde sperm sayıları daha yüksektir. Diğer taraftan ilyak lenf düğümlerinde nüks oranı yalnızca para-aortik bölgeye radyoterapi uygulandığında %2 (tamamı sağ tarafta) köpek bacağı şeklinde radyoterapi uygulandığında ise %0 dır. Nüks gelişme ihtimali olan bir diğer bölge sol böbrek hilusudur. Para-aortik radyasyon primer tümörün yerine göre planlanmalıdır. Evre 1 seminomda diyafram üstü lenf düğümlerine adjuvan radyoterapi uygulaması indikasyonu yoktur. Dozla ilgili olarak MRC evre 1 seminom radyoterapisinde 20 Gy e karşın 30 Gy para-aortik radyasyon uygulamasının karşılaştırıldığı büyük randomize bir çalışmayı yakın zamanda 21
22 tamamlamış ve her iki dozun nüks oranları açısından benzer sonuçlar verdiğini göstermiştir (99). Radyasyona bağlı uzun dönem ciddi toksisite görülme oranı %2 den azdır. Hastaların %5 inde orta şiddette kronik gastrointestinal yan etkiler, %60 ında orta şiddette akut gastrointestinal toksisite görülmektedir (98). Adjuvan radyoterapideki temel endişe uygulanan radyasyona bağlı ikincil germ hücre dışı malinite gelişmesi riskini arttırmasıdır ( ). Karşı taraf testisin saçılan radyasyon etkisinden korunması amacıyla skrotum siperi faydalı olabilir (105). Şu an, evre 1 seminomlardaki adjuvan radyoterapinin oluşturduğu uzun dönem risklerin değerlendirmesi daha önceki tedavi yöntemlerindeki daha büyük alanlar, daha yüksek dozlar ve/veya alklilleyici kemoterapi kullanımı nedeniyle zordur Retroperitoneal lenf düğümü diseksiyonu (RPLDD) Evre 1 seminomda radyoterapi ve RPLDD i karşılaştıran prospektif randomize olmayan bir çalışmada birincil tedavi olarak RPLDD uygulana grupta retroperitoneal nükslerin daha sık gelişme (%9,5) eğiliminde olduğu görülmüştür. Bu nedenle evre 1 seminom tedavisinde RPLDD önerilmemelidir (94) Riske göre tedavi Tümör boyutunun >4 cm ve rete testis yayılımı kriterleri kullanılarak evre 1 seminomlu hastalar gizli metastatik hastalık açısından düşük ve yüksek risk gruplarına ayrılabilir. Her iki risk faktörünü birden olan ve olmayan hastalarda gizli metastatik hastalık olma riski sırasıyla %32 ve %12 dir. Bu risk faktörleri yalnızca retrospektif çalışmaların meta-analizleriyle ortaya konulmuştur (20). Bu risk faktörlerine dayanan prospektif bir çalışmada (risk faktörü yok: izlem; her iki risk faktörü de var: 2 kür karboplatin AUC 7) riske dayalı yaklaşımın uygulanabilirliği gösterilmiştir. Sınırlı takip zamanına dayanan erken veriler risk faktörü olmayan hastalarda 5 yılda %6 nüks riski vardır. Karboplatin ile tedavi edilen yüksek riskli hastalarda nüks oranı %3.3 olarak gerçekleşmiştir (95) Evre I seminom tedavi kılavuzu 1. İzlem (uygun imkanlar varsa ve hasta uyumluysa) (Öneri derecesi: B) 2. Karboplatin tabanlı kemoterapi(1 kür, AUC 7) radyoterapiye ve izleme alternatif olarak önerilebilir. (A derece öneri) 3. Toplam 20 Gy dozda paraaortik bölgeye veya hokey sopası şeklinde adjuvan radyoterapi (A derece öneri) 7.3. Evre I seminom dışı germ hücreli tümör (SDGHT) 22
23 Klinik evre 1 (KE1) hastaların %30 unda subklinik metastaz vardır ve orşiektomi sonrası sadece izlem ile bu hastalarda nüks gelişecektir İzlem Klinik evreleme ve takip yöntemlerindeki gelişmeler ve sisplatin tabanlı kemoterapi ile etkin kurtarma tedavisi ve kemoterapi sonrası cerrahinin uygulanabilmesi, KE1 SDGHT hastalarında orşiektomi sonrası hastaların sadece yakın takip edildiği çalışmaların yapılmasına yol açmıştır. En geniş izlem çalışmalarında nüks oranı %30 civarında olup, nükslerin %80 ilk 12 ayda, %12 si ikinci yılda ve %6 sı üçüncü yılda olmakta 4. ve 5. yıllarda %1 e düşmekte, takip eden yıllarda ise daha da düşük oranlara inmektedir ( ). Nüks olan hastaların %35 inde nüks sırasında serum tümör belirleyicileri normal seviyelerdedir. Nükslerin %60 kadarı retroperitonda olmaktadır. Çok yakın izleme rağmen nüks olan hastaların %11 inde nüks yüksek hacimli hastalık şeklinde ortaya çıkmaktadır. İzlem çalışmalarında bildirilen nüks oranlarının RPLDD ile evrelenen hastalarla karşılaştırıldığında (110) beklenenden düşük gibi görünmesi muhtemelen yüksek riskli hastalara izlem önerilmemesi ile açıklanabilir. Genel kansere özgü sağkalım verilerine bakıldığında, riske göre ayrım yapılmamış klinik evre I seminom dışı hastalara uyumlu olmaları ve beklenen nüks oranları ve kurtarma tedavisi konusunda bilgilendirmek şartıyla izlem konusunda deneyimli merkezlerde izlem önerilebilir Birincil kemoterapi Yüksek riskli hastalarda (yaklaşık %50 nüks riski olan) birincil tedavi olarak iki kür bleomisin, etoposid ve sisplatin (PEB) kemoterapisi veren birkaç çalışma yayınlanmıştır ( ). Bazılarında ortanca takip süresi neredeyse 8 yıl olan (112) ve 200 den fazla hasta içeren bu çalışmalarda çok düşük uzun dönem toksisite ile birlikte sadece %2.7 lik nüks oranı bildirilmiştir. İki siklüs sisplatin tabanlı adjuvan kemoterapinin infertilite ve cinsel aktivite üzerine olumsuz bir etkisi yok gibi görünmektedir (118). Birincil kemoterapi sonrası yavaş büyüyen retroperitoneal teratom ve kemoterpiye dirençli geç kanser nüksü akılda bulundurulmalıdır (119). Birincil kemoterapi sonrası retroperitonun uzun dönem tekrarlayan görüntüleme ile takibinin gerekliliği henüz kesin değildir. İzlem, RPLDD ve birincil kemoterapinin karşılaştırıldığı maliyet analizi çalışmalar muhtemelen takip yoğunluğu ve 23
24 kullanılan yöntemlerin fiyatlandırılmasındaki değişiklikler nedeniyle farklı sonuçlar göstermiştir (120). Takip BT lerinin düşük sıklıkta uygulanması durumunda (örneğin seminom dışı KE 1 için etkin bir takip yöntemi olduğu gösterilen) takip maliyeti önemli oranda azaltılabilmektedir (121) Riske göre tedavi Riske göre tedavi günümüzde risk faktörlerinden vasküler yayılıma dayanmaktadır. KE1 SDGHT hastalarının öngörülen nüks riskine göre sınıflandırılması akla yatkın bir seçenektir çünkü çeşitli çalışmalarda riske göre gruplama yaklaşımı ve mevcut tedavi seçeneklerinin kullanılması ile hastalarda benzer sağkalım ve %100 e yakın sağaltım oranları gösterilmiştir ( , ). Bu nedenle KE1 SDGHT hastalarında riske dayalı tedavi diğer seçeneklerle benzer etkinlik gösteren bir alternatiftir. Vasküler yayılımı olan hastalar 2 kür sisplatin, etoposide ve bleomisin (PEB) adjuvan kemoterapisi ile tedavi edilmeleri, vasküler yayılımı olmayanların ise izleme ile takip edilmeleri önerilmektedir. Diğer tedavi seçenekleri yalnızca hasta veya doktor riske göre tedaviyi kabul etmezse yada buna karşı şartlar söz konusu ise düşünülmelidir. Bu nedenle tedavi kararı alınırken hasta ile tedavinin avantajları ve dezavantajları, hastanın kendisi ile ve tedavinin uygulanacağı merkez ile ilgili koşullar ayrıntılı bir şekilde tartışılmalı ve tedavi seçimi buna göre yapılmalıdır Retroperitoneal lenf düğümü diseksiyonu (RPLDD) Risk değerlendirmesi yapılmaksızın RPLDD uygulaması durumunda hastaların %30 unda retroperitoneal lenf düğümü metastazı (PE 2 hastalık) bulunmaktadır (94, 125, 126). RPLDD ile metastaz bulunmayan PE1 hastaların yaklaşık %10 unda uzak bölgelerde nüks olmaktadır (76, 110, ). İzlem ile takip edilen KE1 SDGHT hastalarında nüksün öngörüsünde ve RPLDD sonrası PE 2 hastalık saptanması veya PE 1 hastalarda nüks gelişmesinin öngörüsünde en önemli etmen birincil tümör içinde veya komşuluğunda tümör hücrelerinin vasküler yayılımıdır (76,106,110,129,130). Vasküler yayılım çok belirgin bir parametre olup, uzman heyeti tarafından merkezi inceleme yapılmayan durumlarda dahi klinik kullanımı mümkündür (122,129). Çok faktörlü analizde vasküler yayılım evre için en iyi öngörücü olarak belirlenmiştir. Vasküler yayılım olmamasının negatif öngörücü değeri %77 dir ve düşük riskli ve uyumlu hastalarda izleme olanak sağlar (76). 24
25 KE1 hastaların yaklaşık %50-70 kadarında vasküler yayılım bulunmamaktadır ve bu hastalarda izlem sırasında nüks riski %15-20 dir. KE1 ve vasküler yayılımı olan hastalarda ise nüks riski %50 dir. PE1 hastalarda ise vasküler yayılım olmayan ve olan hastalarda nüks riski sırasıyla %10 ve %30 kadardır (122,129,131,132). KE1 olmasına rağmen PE2 olan hastalar RPLDD sonrası yalnızca izlem ile takip edilirse yaklaşık %30 unda nüks görülmekte ve nüks genellikle karın ve pelvis dışında olacaktır. Nüks riski rezeke edilen retroperitoneal hastalığın miktarı ile ilişkilidir ( ). PE2 hastalarda RPLDD sonrası adjuvan iki kür (yada daha fazla) sisplatin tabanlı kemoterapi verilirse nüks oranı teratom nüksü de dahil olmak üzere %2 nin altına düşmektedir (110,130,136). Uygun şekilde yapılmış sinir koruyucu RPLDD sonrasında nüks oranı çok düşük (%2 den az), ejakülasyon bozuklukları veya diğer ciddi yan etkilerin görülme oranı da oldukça azdır (130,133,134). RPLDD sonrası takip, orşiektomi sonrası izlem ile takibe göre, batın BT incelemelerine ihtiyacın azalması nedeniyle çok daha kolay ve ucuzdur (130). Laparoskopik RPLDD tecrübeli ellerde açık yönteme alternatif bir evreleme yöntemi olabilir, fakat henüz standart yöntem olarak önerilemez ( ). RPLDD ile bir kür PEB kemoterapisinin randomize karşılaştırıldığı bir çalışmada adjuvan kemoterapi ile 2 yıllık hastalıksız sağkalım anlamlı derecede yükselmiş ve %99.41 (güven aralığı (CI) [%95.87, %99.92]) olarak bulunmuş, cerrahide ise bu rakam %92.37 (CI [%87.21, %95.5]). Aradaki fark ise %7.04 dür CI [%2.52, %11.56]. Tümör nüksü için cerrahi ve kemoterapi karşılaştırıldığında cerrahinin tehlike oranı (hazard ratio) 7.937, CI [1.808, 34.48]. Bu nedenle risk faktörlerine göre düzenlenmemiş hastalarda nüks oranları açısından bir kür adjuvan PEB tedavisi RPLDD dan üstündür (141) Yüksek (ısrarlı) serum tümör belirleyicileriyle birlikte olan KE1S Orşiektomi sonrası serum tümör belirleyicileri, AFP ve hcg için beklenen yarılanma sürelerine uygun olarak düşüp düşmedikleri netleşene değin yakından takip edilmelidir. Orşiektomi sonrası tümör belirleyicilerinin düzeyinin yükselmesi hastada artık hastalık olduğunu gösterir. Bu hastalara RPLDD yapılması durumunda %87 sinde retroperitonda patolojik lenf düğümleri görülür (142). Başta yapılmadıysa karşı testis ultrasonla incelenmelidir. Gerçek KE1S hastaların tedavisi halen tartışmalıdır. Bu hastalar birincil kemoterapi sonrası KE1B hastalarda olduğu gibi 3 kür birincil PEB kemoterapisi ve takip ile (143) veya 25
26 RPLDD ile tedavi edilebilir (120). Vasküler yayılım olan KE1S hastaların büyük çoğunluğu için eninde sonunda zaten kemoterapi gerektiği için vasküler yayılım varlığı birincil kemoterapi indikasyonunu güçlendirir Evre I SDGHT tedavi kılavuzu KE1 Vasküler yayılıma dayandırılan riske göre tedaviler veya izlem önerilen tedavi seçenekleridir (Öneri derecesi: B) KE1A (pt1, vasküler tutulum yok); düşük risk 1. Eğer hasta istekli ve uyumlu olabilecekse, uzun dönem (en az 5 yıl) yakın izlem önerilmelidir (B derece öneri) 2. Düşük riskli hasta eğer izleme istekli değilse adjuvan kemoterapi veya sinir koruyucu RPLDD diğer seçeneklerdir. Eğer RPLDD nodal tutulum (PN+) gösterirse iki kür PEB kemoterapi verilmelidir (A derece öneri) KE1B (pt2-pt4); yüksek risk 1. İki kür birincil BEP kemoterapisi önerilmektedir (B Derecesinde öneri) Hasta adjuvan kemoterapi istemiyorsa izlem veya sinir koruyucu RPLDD diğer seçeneklerdir. Eğer RPLDD sonrası patolojik evre II hastalık bulunursa ek kemoterapi düşünülmelidir (A derece öneri) 8. TEDAVİ: METASTATİK GERM HÜCRELİ TÜMÖRLER Metastatik germ hücreli tümörlerin tedavisi aşağıdakilere dayanır: Birincil tümörün histolojisi IGCCCG tarafından 5202 seminom-dışı ve 660 seminom hastasının verilerine dayanarak tarif edilen prognostik gruplar (Tablo 3) (144) Düşük hacimli metastatik hastalık (evre II A/B) Evre IIA/B seminom Evre II A/B seminomda standart tedavi radyoterapidir. Evre IIA ve IIB de uygulanacak radyasyon dozu sırasıyla 30 Gy ve 36 Gy dir. Standart radyasyon alanına PA bölgesi genişletilerek aynı taraf ilyak alanda dahil edilmiştir (hokey sopası). Evre IIB de lateral sınırlar metastatik lenf düğümlerini cm emniyet sınırı ile içermelidir. Bu teknik evre IIA 26
27 ve IIB de sırasıyla %95 ve %96oranında 6 yıllık nükssüz sağkalım sağlar. Genel sağkalım hemen hemen %100 dür (60,88). Radyoterapi görmek istemeyen Evre IIB hastalarda 3 kür PEB veya 4 kür EP (iyi prognozda) şeklinde kemoterapi de bir seçenektir. Tekli karboplatin standart PEB kemoterapisine alternatif değildir (145) Evre IIA/B SDGHT İleri evre SDGHT de tedavinin kemoterapiyle başlaması konusunda genel bir görüş birliği vardır. Buna istisna oluşturan tek grup olan yüksek serum tümör belirleyicileri olmayan evre II SDGHT hastalarda birincil RPLDD veya izlem diğer tedavi seçenekleridir (146,147). Belirleyicilerin yüksek olmadığı Evre II A/B çok nadirdir ve metastatik diferansiye teratomu veya saf embryonal karsinomu gösterebilir. Yüksek tümör belirleyicili Evre II A/B SDGHT, tümör belirleyicilerin düzeyine göre IGCCCG iyi veya orta prognoz grubu olarak tedavi edilmelidir (iyi prognoz grubunda 3, kötü prognoz grubunda ise 4 kür PEB kemoterapisi ve takiben rezidüel kitle rezeksiyonu) (148,149). Hastaların yaklaşık %30 unda kemoterapi sonrası tam remisyon sağlanamazsa ve rezidü kitle rezeksiyonu gerekir. Birincil kemoterapi istemeyen hastalar için birincil sinir koruyucu RPLDD ve patolojik incelemede metastaz saptanması durumunda (pii A/B) adjuvan kemoterapi (2 kür PEB) tedavisi uygulanabilir. Birincil kemoterapi ve birincil RPLDD benzer sonuçlar sağlar ancak yan etkileri ve toksisiteleri farklıdır. Bu nedenle seçilecek tedaviye hasta ile beraber karar vermek uygundur (150). Her iki yaklaşımla da kür oranı %98 e yakındır (136, ) İlerlemiş metastatik hastalık Birincil kemoterapi İleri hastalıkta birincil tedavi seçeneği IGCCCG risk sınıflandırması göz önünde bulundurularak (Tablo 3 e bakınız) 3 yada 4 kür PEB kemoterapisidir (Tablo 5). İleri hastalıkta bu rejimin sisplatin, vinblastin ve bleomisin (PVB) rejiminden üstün olduğu kanıtlanmıştır ( ). Üç günlük uygulamanın 5 günlük uygulamayla eşit etkinlikte olmakla birlikte toksisitesinin daha fazla olduğunu gösteren veriler mevcuttur (160). Tablo 3: PEB rejimi (her 3 haftada bir) 27
28 İlaç PEB Sisplatin 20 mg/m inci günler* Etoposid 100 mg/m 2, 1.-5.inci günler Bleomisin 30 mg, 1, 8 ve 15. günler PEB= sisplatin, etoposid, bleomisin *Hidrasyonla beraber IGCCCG ye göre iyi prognozlu hastalarda (144) standart tedavi 3 kür PEB veya bleomisinin kontrendike olduğu durumlarda 4 kür PE uygulamasıdır (144, ). Tedavi doz azaltılması olmadan 22 günlük aralıklarla verilmelidir. Kemoterapinin ertelenmesi ancak ateş, nötrofil sayısının <1.000/µ yada trombosit sayısının < /µ olması halinde kabul edilebilir. Granulosit koloni stimule edici faktör (G-CSF) gibi hemotopoetik büyüme faktörü profilaktik uygulanımı için bir indikasyon yoktur. Ancak kemoterapi sırasında iltahabi bir komplikasyon olursa sonraki sikluslar için profilaktik G-CSF önerilir (161,164). IGCCCG ye göre orta prognozlu hastalar içinde 5 yıllık sağkalım oranı yaklaşık %80 olan bir hasta grubu olarak tanımlanmaktadır. Elimizde bulunan veriler standart tedavinin 4 kür PEB uygulaması olduğunu desteklemektedir (144,165). İyi prognozlu gruba göre genellikle daha kötü prognoza sahip olmaları nedeniyle bu hastalar EORTC nin PEB ile PEB + paklitaksel tedavisini karşılaştıran çalışması gibi prospektif çalışmalara dahil edilebilirler (165). Kötü prognozlu hastalar için standart tedavi 4 kür PEB uygulamasıdır. Dört kür PEI (sisplatin, etoposid, ifosfamid) tedavisi de aynı etkiye sahiptir ancak daha toksiktir (166,167). Beş yıllık ilerlemesiz sağkalım %45-50 arasındadır. Randomize bir çalışmada yüksek doz kemoterapinin kötü prognoz grubunda avantajı olmadığı görülmüştür. Ancak, tümör belirleyicilerindeki düşüş yavaş olan hastalar daha kötü prognozlu bir alt grup oluşturabilirler (168).. Eşleştirmeli karşılaştırma çalışmalarında daha iyi sağkalım oranları bulunması nedeniyle (169,170) bu hastalar yüksek doz kemoterapinin değerini araştıran prospektif randomize çalışmalara dahil edilmelidir. Bu nedenle bu kötü prognostik kriterlere uyan hastaların referans merkezlerine sevk edilmeleri gerekir. Genel durumu bozuk (Karnofsky performans durumu <%50), yaygın karaciğer tutulumu ve yaygın akciğer tutulumu olan hastalara tedavi değişikliği için genel öneri bulunmamaktadır Tekrar evreleme ve ileri tedavi Tekrar evreleme 28
29 İki kür kemoterapinin bitiminden sonra görüntüleme çalışmaları ve tümör belirleyicilerinin bakılması ile yeniden değerlendirme yapılır. Belirleyicinin düşmesi ve tümörün sabit yada geriliyor olması durumunda halinde kemoterapi tamamlanır (başlangıç evresine göre 3 veya 4 kür) (144,171,172). Belirleyicilerin düşmesi, fakat metastazların büyümesi halinde, lokal tümör büyümesine bağlı bir aciliyet olmadıkça başlangıç tedavisinin sonlanması sonrası tümörün rezeksiyonu zorunludur (173). Erken tedavi değişikliği indikasyonu yalnızca iki kür kemoterapi sonrasında tümör belirleyicilerde artma olan hastalarda vardır. Bu hastalar genellikle yeni ilaç çalışmaları için adaydırlar (169,174). Tedavi sonrası belirleyiciler normal düzeye inmeyen ancak düşük düzeyde artmadan seyreden hastalar takibe alınarak belirleyici düzeylerinin normale inip inmeyeceği gözlenir. Kurtarma kemoterapisi indikasyonu yalnızca belirleyici yüksekliği görüldüğünde vardır (175,176) Rezidü tümör rezeksiyonu Seminomda, rezidü kitlenin boyutu ne olursa olsun rezeke edilmez ancak görüntüleme araştırmaları ve tümör belirleyicileri ile kontrol edilir ( ). FDG-PET, seminom tedavisi sonrası rezidü kitlelerde yüksek prognostik değer taşır. Üç cm den büyük rezidü kitlesi olan hastalarda bu rezidü kitlelerin canlılığı ile ilgili daha fazla bilgi edinebilmek amacıyla FDG-PET yapılmalıdır. Üç cm den küçük rezidü kitlesi olan hastalarda FDG-PET yapılması isteğe bağlıdır (184). İlerleme durumunda kurtarma kemoterapisi yapılır ve gerekirse buna cerrahi ve radyoterapi eklenir ( ). Kemoterapi sonrası tam remisyon olan seminom dışı olgularda (görüntülenebilen tümör yok) rezidü tümörün rezeksiyonu indikasyonu yoktur ( ). Görüntülenebilen herhangi bir rezidü kitle varsa ve belirleyiciler normale düşmüşse cerrahi rezeksiyon indikasyonu vardır. Bir cm den küçük rezidü kitlesi olan hastalarda dahi rezidü kanser veya teratom riski vardır (196). Retroperitoneal hastalığın ısrar ettiği durumlarda kemoterapinin tamamlanmasından itibaren 4-6 hafta içinde tüm birincil metastaz alanları tamamen rezeke edilmelidir. Eğer teknik olarak mümkün ise sinir koruyucu işlem yapılmalıdır (190, ) PEB tedavisi sonrası rezidüel kitlelerin ancak %10 nu canlı kanser dokusu, %50 si matür teratom ve %40 ı nekrotik-fibrotik doku içerir. Henüz PET dahil hiçbir görüntüleme yöntemi veya prognostik model seminom dışı tümörlerde rezidü kitlenin histolojik yapısını öngörememektedir. Bu nedenle rezidüel kitle rezeksiyonu zorunludur ( , ). 29
30 Cerrahinin sınırı hastanın nüks riski ve yaşam kalitesi konuları ile ilişkilidir (198). Mümkün olduğunca tüm kitle rezeke edilmelidir, çünkü yaşayan tümör varlığı halinde tam rezeksiyon post-operatif kemoterapiden daha yararlıdır (214). Değişik organlarda histoloji farklılık gösterebilir (206) İkincil cerrahi sonrası pekiştirme kemoterapisi Nekroz yada matür teratomun rezeksiyonu sonrasında ek tedavi gerekmez. Canlı karsinom yada immatür teratomun tam rezeksiyonu sonrasında 2 kür adjuvan sisplatin tabanlı kemoterapi bazı alt grup hastalara verilebilir (örneğin IGCCCG kötü prognoz grubu, bu uygulamanın dezavantajı hastanın artan dozlarda bleomisin almasıdır) (214). Kitlenin tam rezeksiyonu sonrası kitle içinde canlı tümör oranı <%10 ise ilerde oluşabilecek nükslerin önlenmesi amacıyla adjuvan kemoterapi uygulaması faydasızdır. İkincil ve üçüncül kemoterapi sonrası rezeksiyon spesimeninde canlı karsinom bulunması prognozun kötü seyredeceğini gösterir. Böyle bir durumda post-operatif kemoterapi indikasyonu yoktur ve zaten prognozu iyileştirici etkisi yoktur (202,207) Nüks eden veya tedaviye dirençli hastalıkta sistemik kurtarma tedavisi Seminom İlk kemoterapi sonrası nüks olan hastalarda sisplatin tabanlı kombinasyon kurtarma kemoterapisi, hastaların %50 sinde uzun dönem remisyon sağlar (215). Tercih edilen rejimler; 4 siklüs PEI/VIP (sisplatin, etoposid, ifosfamid), 4 siklüs TIP (paklitaksel, ifosfamid, sisplatin) yada 4 kür VeIP dir (vinblastin, ifosfamid, vinblastin). Halen klasik doz sisplatin tabanlı kombinasyon tedavisinin ilk kurtarma tedavisi olarak yeterli olup olmadığı ve ilk kurtarma kemoterapisinin yüksek doz kemoterapi olarak verilmesinin gerekliliğini belirlemek olanaksızdır (216). Bu nedenle bu tür nadir görülen hastaların klinik çalışmalara dahil edilmeleri ve deneyimli merkezlerde tedavi edilmeleri çok önemlidir Seminom dışı İlk kemoterapi sonrası standart kurtarma tedavisi 4 siklüs PEI/VIP, 4 kür TIP veya 4 siklüs VeIP şeklinde uygulanabilir (Tablo 6). Klasik dozda kurtarma kemoterapisi hastaların %15-40 ında risk faktörlerine de bağlı olarak, uzun dönem remisyon sağlar ( ). Kurtarma tedavisine cevapta prognostik göstergeler: primer tümörün yeri ve histolojisi 30
31 ilk tedaviye cevap remisyonun süresi nükste AFP ve hcg düzeyleri VeIP ile kurtarma tedavisinin muhtemelen klasik doz sisplatin tabanlı kombinasyon rejiminden üstünlüğü yoktur ( ). Klasik dozda kombinasyon rejimlerinin 3 ajandan daha fazla ilaçla kullanımı tedavi başarısını arttırmaksızın toksisiteyi arttırır (220). Kötü prognostik faktörlerin varlığına bağlı olarak ilk sisplatin tabanlı kemoterapi sonrası uygulanan kurtarma tedavisi sonuçları tatmin edici değildir (176,221). Bazı faz II çalışmalar ilk kurtarma tedavisinde yüksek doz kemoterapi kullanılmasının sağkalımda %10 luk bir kazanç elde edildiğini gösterse de diğer çalışmalarda bu kazanç gösterilememiştir ( ). Randomize IT94 çalışmasında iyi risk grubundaki hastalarda yüksek doz kemoterapinin herhangi bir avantajı belirlenememiştir (227). Bu nedenle iyi risk grubundaki hastalara klasik doz kurtarma tedavisi önerilmelidir. Bazı faz II çalışmalarda ve bir retrospektif eşleştirilmiş çiftler analizinde erken yoğunlaştırma veya ilk kurtarma tedavisinin yüksek dozda yapılmasının kötü prognozlu grubun sağkalımında düzelme sağladığı görülmüştür (218, ) (KDT IIB) Son dönemde taksol ve gemsitabinin dirençli germ hücreli tümörlerin tedavisinde aktif oldukları gösterilmiştir, her iki ilaç da sisplatinle sinerjistik etkilidir ( ). Ancak kurtarma tedavisinde en iyi yöntemin belirlenebilmesi amacıyla bu hastalar çok merkezli çalışmalara dahil edilmek amacıyla deneyimli merkezlere sevk edilmelidir (216). Tablo 6: Standart PEI/VIP, TIP ve VeIP kemoterapisi PEI/VIP Doz Siklüs süresi Sisplatin* 20 mg/m 2, günler 21 gün Etoposid mg/m 2, günler Ifosfamid** 1,2 g/m 2, günler TIP Doz Siklüs süresi Paklitaksel 250 mg/m 2 1. gün 24 saat devamlı infüzyon Ifosfamid** 1.5 g/m günler Sisplatin* 25 mg/m günler 31
32 VeIP Doz Siklüs süresi Vinblastin 0.11 mg/kg, günler 21 gün Ifosfamid** 1,2 g/m 2, günler Sisplatin* 20 mg/m 2, günler PEI/VIP = sisplatin, eposid, ifosfamid; TIP = paklitaksel, ifosfamid, sisplatin; VeIP = vinblastin, ifosfamid, sisplatin. *Hidrasyon ile ** Mesna koruması ile Geç nüks (birinci basamak tedavinin tamamlanmasından 2 yıl sonra) Geç nüks, herhangi bir hastanın metastatik hastalık nedeniyle kemoterapi uygulanmasından 2 yıldan daha fazla bir süre sonra nüks etmesi şeklinde tanımlanır. Teknik olarak mümkün olması durumunda geç nükslü tüm hastalar tümör belirleyici düzeyleri ne olursa olsun tüm diferansiye olmamış germ hücreli tümör, matür teratom ve ikincil germ hücre dışı kanser dokularının tamamen rezeke edilmesi amacıyla derhal radikal cerrahi ile tedavi edilmelidir ( ). Eğer tüm lezyonların rezeksiyonu mümkün olamıyorsa bu dokulardan biyopsi alınarak histolojik değerlendirme yapılmalı ve bu değerlendirme sonucuna göre kurtarma kemoterapisine başlanmalıdır. Hastanın kurtarma kemoterapisine cevap vermesi durumunda mümkün olan zamanda ikincil cerrahi yapılmalıdır. Rezeke edilemeyen ancak lokalize dirençli hastalıkta radyoterapi düşünülmelidir. Mortalite oranlarını düşük tutmak amacıyla geç nüksler sadece bu hastaların tedavisinde deneyimli merkezlerde tedavi edilmelidir (235) Kurtarma cerrahisi Kurtarma kemoterapisi sonrasında rezidüel tümörler belirleyicilerin normale dönmesi yada bir platoya ulaşmasını takiben 4-6 hafta içinde rezeke edilmelidir. Kurtarma tedavisi sonrasında belirleyici yükselmesi yada diğer kemoterapi seçeneklerin olmadığı durumda eğer tüm tümörün rezeksiyonu mümkün görünüyorsa rezidü tümör rezeksiyonu (son umut cerrahisi) düşünülebilir (yaklaşık %25 uzun süreli sağkalım elde edilebilir) (176,200,208,211, ) Beyin metastazlarının tedavisi Beyin metastazları sistemik nüks veya nadiren izole nüks olarak görülür. İlk tanıda beyin metastazı olan hastalarda uzun süreli sağkalım kötüdür (%30-40), fakat nüks olarak beyin metastazı gelişen hastalarda daha da kötüdür (5 yıllık sağkalım %2-5) (246,247). Kemoterapi 32
33 bu durumlarda ilk tedavidir ve kemoterapiye tam cevap olsa bile pekiştirme radyoterapisinin uygulanmasını destekleyen bazı veriler vardır (248). Israrlı tekil metastazlarda sistemik duruma, primer tümörün histolojisine ve metastazın yerine bağlı olarak cerrahi yapılabilir Metastatik germ hücreli tümör tedavi kılavuzu 1. Tümör hacmi düşük, serum belirleyici düzeyi yükselmiş Evre IIA/B SDGHT iyi veya orta prognozlu ilerlemiş SDGHT e benzer şekilde 3 veya 4 kür PEB ile tedavi edilmelidir. Belirleyicilerin yüksek olmadığı Evre II tümörler RPLDD ile veya yakın izlem ile tedavi edilebilirler. 2. İyi prognostik gruptaki metastatik SDGHT de ( Evre IIC) birincil tedavi seçeneği 3 kür BEP tir. (A derece öneri). 3. Orta veya kötü prognostik gruptaki metastatik SDGHT de birincil tedavi seçeneği 4 kür PEB tir. (A derece öneri). 4. SDGHT de kemoterapi sonrası rezidü kitle rezeksiyonu indikasyonu görüntülenebilen rezidü tümör varlığında ve serum tümör belirleyicileri seviyesi normal veya normale düşüyorsa vardır.(b derece öneri). 5. N3M1 hastalıktan daha düşük evrede metastatik seminom ilk olarak radyoterapi ile tedavi edilebilir. Gerektiğinde kemoterapi aynı prognostik gruptaki SDGHT ile benzer rejimlerin kullanılmasıyla kurtarma tedavisi şeklinde kullanılabilir (A derece öneri). 6. İlerlemiş seminom (N3 yada M1) SDGHT ile aynı prensiplere bağlı kalınarak birincil kemoterapi ile tedavi edilmelidir (A derece öneri). 9. SAĞALTIM AMAÇLI TEDAVİ SONRASI TAKİP 9.1. Genel bilgiler Takipte kullanılacak testler aşağıdaki prensiplerle sadık kalmalıdır (249): A. Muayene ve yapılacak testler arasındaki süreler nüks riskinin en fazla olduğu zaman ve tümörün doğal seyri dikkate alınarak belirlenmelidir. B. Testler nüksün en sık olduğu bölgelere yönelik olmalı ve yüksek pozitif ve negatif öngörücü değere sahip olmalıdır. C. Nüks olması durumunda nüksün sağaltımını sağlayacak, yaşam süresini uzatacak veya semptomları giderecek tedavi mevcut olmalıdır. Erken tedavi tümör nüksüne bağlı semptomların ortaya çıkmasından sonra verilen tedavi ile karşılaştırıldığında daha başarılı sonuçlar sağlamalıdır. D. Aynı karsinojenlere maruz kalan yada epidemiyolojik olarak artmış risk belirtisi olan birincil veya diğer dokularda gelişebilen ikincil kanserlerin artan riski, testlerin seçiminde yol gösterici olmalıdır. 33
34 Tedavinin malin ve malin olmayan komplikasyonları da dikkate alınmalıdır. Testlerin yapılacağı süre ve sıklıklar bu risklerin özellikleri de dikkate alınarak hazırlanmalı ve yüksek pozitif ve negatif öngörücü değere sahip olmalıdır. Tüm evrelerdeki testis tümörlerinin takibinde kullanılacak inceleme ve protokoller genel olarak aşağıdaki bilgiler dikkate alınarak seçilmelidir. Sağaltım amaçlı tedavi sonrası nükslerin büyük çoğunluğu ilk 2 yıl içinde olur; bu nedenle izlem bu dönemde daha sıkı ve yoğun olmalıdır. Geç nüksler 5 yıldan sonra da gelişebilir, be nedenle yaşam boyu yıllık takip savunulabilir. RPLDD sonrası retroperitonda nüks nadirdir, en sık nüks yeri ise göğüs bölgesidir. Yaygın hastalığın tam remisyonundan sonra hastaların izlenmesinde göğüs grafisinin değeri son zamanlarda sorgulanmaktadır (250,251). Göğüs BT nin göğüs grafisinden daha yüksek öngörücü değeri vardır (251). Tedavi sonuçları hastalık yükü ile ilişkilidir, bu nedenle hastalığın, semptomlar gelişmeden önce saptanması amacıyla yoğun takip stratejisi akla yatkındır. Kemoterapi veya radyoterapi sonrası uzun dönemde ikincil kanser gelişimi riski mevcuttur Seminom dışı evre 1 tümörlerde takip Klinik evre 1 SDGHT hastaların yaklaşık %5 inde orşiektomi sonrası tümör belirleyicileri yükselir ve %25-30 kadarında ilk iki yıl içinde nüks saptanır (5,112,129,132,151, ). Takip protokolu 3 olası tedavi şemasından hangisinin seçilmiş olduğuna göre değişir; İzlem Sinir koruyucu RPLDD Adjuvan kemoterapi İzlem sırasında takip 34
35 İzlem politikasının sonuçları operasyon öncesi dikkatli evreleme yapılması ve takibin uygulanış şekline bağlıdır. Bekle ve gör politikasında olguların %30 unda nüks görülecektir. Bu nükslerin, %80 i ilk 12 ayda görülürken yaklaşık %12 si de ikinci yılda görülür. Ortanca nüks zamanı 6 aydır (aralık: 1-62 ay), fakat yıllık %4 oranında olmak üzere 3-5 yıl sonra hatta daha da geç nüks görülebilir (107,108). Nüks genelde retroperitonda olur; yaklaşık %20 hastada retroperiton metastazı varken, %10 da mediasten ve akciğer metastazları görülür (256). Bazen tek gösterge artmış tümör belirleyicileridir. MRC tarafından yılda 2 kez ve beş kez BT uygulamasını karşılaştıran bir randomize çalışma tamamlanarak yayınlanmış ve bu çalışmada izlem sırasında BT sıklığının düşürülerek orşiektomi sonrası 3. ve 12. aylarda yapılması önerilmiştir. Bu çalışmaya 414 hasta katılmış ve çalışmanın gücü, orta veya kötü prognoz grubundaki bir hastanın metastaz yapmış nüks ile yakalanmasının %3 olasılığını dışlayacak şekilde belirlenmiştir. Nüks saptama oranı 2 BT ile %15, 5 BT ile ise %20 olup bu hastaların %1.6 sında orta veya kötü prognoz özellikleri olduğu görülmüştür. Hastaların yalnızca %10 nunda yüksek risk özellikleri (vasküler yayılım) vardır. Özet olarak bu randomize çalışma klinik evre I seminom dışı hastalarda minimum takip için 1. seviye kanıt oluşturmaktadır (121). Önerilen takip programı (Tablo 7) görüntüleme için minimum gereksinimleri içermekte ve diğer izlem testleri içinde önerileri eklemektedir. Tablo 7 : Evre 1 seminom dışı tümörlerde izlem için önerilen takip programı. Yöntem Yıllar Fizik Muayene 3 ayda bir 3 ayda bir Yılda 2 Yılda 1 Tümör belirleyicisi 3 ayda bir 3 ayda bir Yılda 2 Yılda 1 Akciğer grafisi Yılda 2 Yılda 2 Yılda 2 Yılda 1 Abdominopelvik BT Yılda 2 (3. ve 12. ayda) BT = Bilgisayarlı tomografi Sinir koruyucu RPLDD sonrası takip 35
36 Uygun şekilde yapılmış RPLDD sonrası retroperitoneal nüks çok nadirdir. RPLDD retroperitoneal lenf düğümlerini nüks sahası olmaktan çıkarırken, tekrarlayan batın BT gerekliliğini de ortadan kaldırır. ABD intergroup verileri patolojik evre 1 hastalarında 7/264 retroperitoneal nüks bildirir (ve 20 akciğer nüksü). Yedi hastanın 4 ünde tümör belirleyicileri yükselmemiştir (257). Indiana serisinde; 559 hastada sadece bir nüks bildirilmiştir (258). Nüks olduğunda genellikle göğüs, boyun veya cerrahi sahanın kenarında görülmektedir. Akciğer nüksleri hastaların %10-12 sinde görülürken, bunların %90 ı RPLDD den sonra ilk iki yıl içinde izlenir (73,259). Ancak RPLDD sonrası düşük retroperitoneal nüks oranına ancak özelleşmiş merkezlerde uygulanan ameliyatlarla ulaşılabilinmektedir. RPLDD ile tek kür PEB in karşılaştırıldığı Alman randomize çalışmasında bu durum ortaya konulmuş ve yüksek saha içi nüks (13 nüksten 7 si) bulunmuştur (141). Tablo 8 de önerilen minimum takip şeması verilmiştir. Tablo 8: Evre 1 SDGHT için RPLDD veya adjuvan kemoterapi sonrası önerilen takip şeması Yöntem Yıl Fizik muayene 3 ayda bir 3 ayda bir Yılda iki Yılda bir Tümör Belirleyicileri 3 ayda bir 3 ayda bir Yılda iki Yılda bir Akciğer grafisi Yılda iki Yılda iki Abdominopelvik BT Yılda bir Yılda bir BT = Bilgisayarlı tomografi Adjuvan kemoterapi sonrası takip Uzun takip süreli prospektif çalışmalarda %3 gibi düşük nüks oranı bildirilmiştir (112,113,252,253). Bir kür PEB ile RPLDD nun karşılaştırıldığı randomize bir çalışmada adjuvan kemoterapi ile nüks oranı %1 olarak bulunmuştur (174 de 2 hasta: 1 inde tümör belirleyici nüksü, diğerinde ise retroperitonda matür teratom) (141). Retroperitonun uzun dönem tekrarlayan incelemelerle değerlendirilmesinin gerekliliği halen net değildir. Adjuvan kemoterapi sonrası retroperitonda geç, yavaş büyüyen teratoma riski göz önüne alınarak batın BT nin yapılması yine de gereklidir (Tablo 8). 36
37 9.3. Evre 1 seminomda takip Seminom hastalarının büyük kısmı (%70-80) tanı anında klinik evre 1 hastalık taşırlar (88). Hastaların %15-20 sinde radyolojik olarak retroperitonda lenf düğümü tutulumu ve %5 inde de uzak metastaz vardır (88). Nüks oranları, orşiektomi sonrası seçilen tedaviye bağlı olarak, %1 ile %20 arasında değişir. Hastaların sadece %30 unda tanı anında veya takiplerde hcg de yükselme saptanır. Bu nedenle tümör belirleyicilerin ölçülmesi takip için güvenilir bir test değildir (260). Orşiektomi sonrası evre 1 seminom için tedavi seçenekleri; radyoterapi, izlem ve adjuvan kemoterapidir. Yüksek radyoterapi ve kemoterapi duyarlılığından dolayı hangi tedavi seçilirse seçilsin, nüks durumunda dahi % 100 gibi bir başarı oranı yakalanabilmektedir. Değişik tedavilerin maliyetleri ve beklenen yan etkileri birbirlerinden farklıdır (90,261,262) Radyoterapi sonrası takip Retroperiton bölgesine veya hokey sopası alanına sınırlı düşük doz (20-24 Gy) radyoterapi %99 a ulaşan 5-10 yıllık genel sağkalım oranı sağlar (98,100,263,264). Nüks oranı %1-2 dir ve geç nüksler da tariflenmiş olmasına rağmen (267), en sık tedaviden sonraki ilk 18 ayda ortaya çıkar (98,101,262,265,266). Nüks alanı genelde diyafram üstü lenf düğümleri, mediyasten, akciğerler ve kemiklerdir. Hastaların küçük bir kesiminde nüks inguinal ve eksternal ilyak düğümlerde gelişir (88). Radyoterapinin yan etkileri arasında bozulmuş spermatogenez, gastrointestinal semptomlar (peptik ülser) ve ikincil kanser gelişmesi vardır (262,268,269). Hastaların %50 sinde orta dereceli (1.-2. derece) tokisisite görülür (263). Takip şeması tablo 9 da verilmiştir. 37
38 Tablo 9: Evre I seminomda orşiektomiden sonra radyoterapi veya kemoterapi için önerilen minimum takip şeması Yöntem Yıl Fizik muayene 3 ayda bir 3 ayda bir Yılda iki Yılda bir Tümör Belirleyicileri 3 ayda bir 3 ayda bir Yılda iki Yılda bir Akciğer grafisi Yılda iki Yılda iki Yılda bir Yılda bir Abdominopelvik BT Yılda iki Yılda iki Yılda bir Yılda bir BT = Bilgisayarlı tomografi İzlem sırasında takip Beş yıl için hesaplanan nüks riski %6 ile (düşük risk hastalar) %20 arasında değişmektedir (95, ). Artmış ölüm riski yoktur. Ortanca nüks zamanı 12 ile 16 ay arsında değişmektedir ancak nükslerin %29 u daha sonra gelişebilir (88,275). Nüksler olguların %822sinde PA lenf düğümlerinde görülür, ancak pelvik ve inguinal lenf düğümleri ve akciğerlerde de nüks gelişebilir (88, ). Yüksek nüks oranı ve sıklıkla nükslerin geç gelişmesi nedeniyle en az 5 yıl yakın ve aktif takip zorunludur (281) (Tablo 9 a bakınız) Adjuvan kemoterapi sonrası takip Evre 1 seminom hastalarında, bir veya iki kür karboplatin tabanlı kemoterapi etkili bir alternatiftir. Nüks oranı %1.9 ile 4.5 arasındadır. Tedavi genellikle iyi tolere edilir ve sadece hafif akut ve orta dönem toksisiteye yol açar (282,283). Nüks ve sağkalım için uzun dönem veri mevcut değildir (Bkz Tablo 9) Evre II ve ilerlemiş (metastatik) hastalıkta takip Hastalığın lenf düğümü (N) evresi ne kadar ileriyse nüks olasılığı da o kadar yüksektir (136). Genellikle tanı anındaki tümör hacmi SDGHT de hastanın prognozunu belirler (284). Evre II SDGHT de uygulanan tedavi şekli ne olursa olsun, nükslerin erken saptanması şartıyla %97 ye ulaşan mükemmel sağkalım oranları sağlamıştır (146,147,152). İleri evre metastatik germ hücreli tümörlerde, hastalığın yaygınlığı tedaviye cevap ve sağkalım ile ilişkilidir. Hastalığın yaygınlığı ile ilgili olarak sisplatin tabanlı kemoterapi ve cerrahinin beraber uygulanması (agresif çoklu yaklaşım) %65-85 arası sağkalım oranları 38
39 sağlayabilmektedir (284,285). Kemoterapiye tam yanıt oranları %50-60 arasında olup (284), hastaların %20-30 u ise kemoterapi sonrası cerrahiyle hastalıksız hale getirilebilmiştir (286). İlerlemiş SDGHT de en önemli başarısızlık nedenleri şu şekilde sıralanabilir (284,287,288): Kemoterapiye tam yanıt vermeyen yüksek hacimli hastalık, Kemoterapi sonrası cerrahiyle çıkarılamayan teratom varlığı, Kemoterapiye dirençli germ hücre dışı elemanların varlığı veya gelişmesi ki bu durum olguların %8.2 sini oluşturur. Tablo 10: İlerlemiş SDGHT ve seminom için önerilen minimum takip şeması. Yöntem Yıl Daha sonra Fizik muayene 3 ayda bir 3 ayda bir Yılda iki Yılda bir Tümör Belirleyicileri 3 ayda bir 3 ayda bir Yılda iki Yılda bir Akciğer grafisi 3 ayda bir 3 ayda bir Yılda iki Yılda bir Abdominopelvik BT ab Yılda iki Yılda iki Yılda bir Yılda bir Toraks BT bc Lüzum halinde Lüzum halinde Lüzum halinde Lüzum halinde Beyin BT d Lüzum halinde Lüzum halinde Lüzum halinde Lüzum halinde BT = Bilgisayarlı tomografi a Retroperitonda teratom olması durumunda abdominal BT en az yılda bir yapılmalıdır. b Kemoterapi sonrası değerlendirmede > 3 cm kitle bulunması durumunda uygun BT incelemesi kitlenin daha sonra küçülmeye devam ettiğinden emin olunması için 2 ve 4 ay sonra tekrar edilmelidir. Eğer ulaşılabiliyorsa FDG-PET yapılmalıdır. c Toraks BT indikasyonu akciğer grafisinde anormallik saptanana hastalarda ve akciğer rezeksiyonu yapılmış hastalarda vardır. d Baş ağrısı, fokal nörolojik bulgusu veya herhangi bir merkezi sinir sistemi semptomu olan hastalarda 39
40 10. TESTİS STROMA TÜMÖRLERİ Giriş Testisin stromal tümörleri nadirdir ve erişkin testis tümörlerinin yalnızca %2-4 ünü oluştururlar. Bununla beraber yalnızca Leydig hücreli ve Sertoli hücreli tümörlerin klinik önemi vardır. Bugüne kadar bu tümörlerle ilgili yayınlanmış öneri olmaması nedeniyle EAU Testiküler Kanser Çalışma Grubu bu tümörlerin EAU Germ Hücreli Tümör Kılavuzuna eklenmesine karar vermiştir. Tanı ve tedavi için öneriler yalnızca Leydig ve Sertoli Hücreli tümörler için yapılmıştır Yöntem Leydig hücreli (eş adı: interstisiyel hücreli tümör) ve sertoli hücreli tümör (eş adı: androblastoma) için yapılan Medline taramasında yaklaşık 850 makale bulunmuştur. Klinik verisi olmayan laboratuar çalışmaları, kadın ve pediatrik hastalar ve hayvan çalışmaları hariç tutulunca 371 makale ve özet gözden geçirilmiştir. İki kez basımlar ve kesin olmayan histoloji yada klinik takipte kaybedilen bilgi olan makaleler de dışlanmıştır. Geri kalan 285 makalenin büyük kısmı olgu sunumudur. Yalnızca birkaçı 10 un üzerinde olgu içermekte ve bunların da pek çoğu patoloji literatüründe yer almaktadır.bu nedenle stromal tümörlerin gerçek insidansı bilinmemekte ve metastatik tümörlerin oranı takriben verilebilmektedir. Buna rağmen, testiküler stromal tümörlerin ameliyat öncesi şüpheli semptomları ve metastaz için yüksek risk taşıyan tümörlerin özellikleri yeterli şekilde belirlenmiş olduğundan (kanıt düzeyi IIA ve IIB) tanı ve cerrahi yaklaşım için öneriler yapılabilmiştir. Ancak bildirilen olguların genellikle takip verilerinin olmayışı ve seçilen tedavi ne olursa olsun metastatik tümörlerin ölümcül seyri nedeniyle uygun takip önerileri verilmemiştir. Yayınların her biri kanıta dayalı tıp kategorilerine göre değerlendirilmiştir (Bkz. Yukarı) Leydig hücreli tümör klinik verileri için yapılan literatür taramasında yetişkinlerde 480 den fazla tümörü içeren 193 makale bulunmuştur. Bunların içinde (1-3) 3 makale toplam 90 hastayı içeren en büyük serilerdir. Seksen hasta için 2 yıldan uzun takip süresi vardır. Sertoli hücreli tümör klinik verileri için yapılan literatür taramasında yetişkinlerde 260 den fazla tümörü içeren 93 makale bulunmuştur. Bunların içinde (4-6) 3 makale (aynı gruptan) toplam 80 hastayı içeren serilerdir. Kırktan az sayıda hasta için 2 yıldan fazla takip verileri vardır. 40
41 10.3. Sınıflama Testisin germ hücreli olmayan tümörleri, seks kord/gonadal stromal tümörler ve çeşitli nonspesifik tümörleri içermektedir. Testiküler tümörlerin farklı histolojik alt grupları DSÖ 2004 sınıflandırmasına göre tanımlanmıştır (7) Leydig hücreli tümörler Epidemiyoloji Leydig hücreli tümörler erişkin testis tümörlerin yaklaşık %1-3 nü (2,8) ve bebek ve çocukluk çağı tümörlerinin %3 ünü oluşturur (8). Tümör yetişkinlerde en sık 3. ve 6. on yıl arasında görülür ve bu aralıkta her on yıllık dönem için benzer insidans söz konusudur. İnsidansın yüksek görüldüğü diğer dönem ise çocukluk çağında 3 ve 9. yaşlar arası dönmedir. Leydig hücreli tümörlerin %3 ü çift taraflıdır (2). Nadiren Klinefelter sendromlu hastalarda da gelişir (8) Leydig hücreli tümörlerin patolojisi Leydig hücreli tümörler seks kord/gonadal stromal tümörlerin en sık görülen tipidir. Histopatolojik olarak iyi sınırlı ve çapları genellikle 5 cm e kadardır. Tümör solid yapıda, sarı - açık kahverengi arası renktedir ve olguların %30 unda hemoraji ve/veya nekroz içerir. Mikroskopik olarak poligonal bazen Reinke kristalleri olan eozinofilik sitoplazmalı, düzgün nükleuslu solid düzenlenmiş ve kapiller stromalı hücrelerden oluşur. Hücreler vimentin, protein S100, steroid hormon, kalretinin ve sitokeratin (fokal) salgılarlar (7). Leydig hücreli tümörlerin %10 nu malindir ve bunlar aşağıdaki parametreleri gösterirler; Büyük boyut (>5cm) Sitolojik atipi Artmış mitotik aktivite (her 10 luk büyütme alanında >3) Artmış MIB-1 salınımı (%18.6 ya karşılık benin tümörlerde %1.2) Nekroz Vasküler yayılım (9) İnfiltratif sınırlar Testis parankiminden dışarı uzanım 41
42 DNA anöploidi (1,10) Tanı Hastalarda testiste ağrısız kitle nedeniyle başvurur yada kitle raslantısal olarak ultrasonda saptanır. Hastaların %80 e yakın kısmında yüksek östrojen ve östrodiol ve düşük testesteron seviyeleri, artmış LH ve FSH düzeyi gibi hormonal bozukluklar bildirilmiştir (11,12). Diğer taraftan testiküler germ hücreli tümör belirleyicileri AFP, HCG, LDH ve PLAP her zaman negatiftir. Hastaların yaklaşık %30 unda jinekomasti vardır (13,14). Tümörlerin %3 ü çift taraflıdır (2). Leydig hücreli tümörler adrenogenital sendroma bağlı gelişen ve sıklıkla çift taraflı olan multinoduler tümör benzeri lezyonlardan ayrılmalıdır (15). Tanı amaçlı değerlendirmede hormonlar (en azından testesteron, LH ve FSH, eğer sonuç alınamazsa ek olarak östrojen, östradiol, progesteron ve kortizol), her iki testis ultrasonu ve göğüs ve batın BT yapılmalıdır. Ultrasonda iyi sınırlı, küçük, hipervasküler hipoekoik lezyonlar görülebilir ancak görünüm değişkendir ve germ hücreli tümörlerden ayırım mümkün değildir (16,17). Tüm yayınlanmış olgu sunumlarında metastatik tümörlerin oranı %10 dur. Uzun takipli 3 büyük seride toplam 83 olgudan 18 inde metastatik tümör bulunmuştur (%21.7) (1-3). Malinite için histopatolojik belirtiler yukarıda sıralanmıştır (Bkz ) (1,10). Ek olarak yaşlı hastalarda malin potansiyel taşıyan tümör olasılığı daha fazladır Tedavi Küçük hacimli semptom vermeyen testis tümörleri genellikle germ hücreli tümörlerle karışır ve inguinal orşiektomi yapılır. Küçük parenkim içinde yerleşik lezyonlarda histolojik tanı elde edilene değin organ koruyucu girişim önerilmektedir. Özellikle jinekomasti veya hormonal bozukluklara bağlı semptomları olan hastalarda germ hücre dışı tümör olasılığı düşünülmeli ve hemen orşiektomiden kaçınılmalıdır (18). Dondurulmuş kesitte yada parafin histolojide germ hücreli tümör saptanırsa diğer testis normalse orşiektomi önerilir. Malin histolojik bulguların olduğu stromal tümörlerde, özellikle yaşlı hastalarda, orşiektomi ve retroperitoneal lenfadenektomi metastazların önlenmesi için önerilir (19). Malin histolojik bulgular olmadığında orşiektomi sonrası hastaya uygun izlem protokolu önerilir (Spesifik tümör belirleyicileri olmadığı için BT ile takip en uygun seçenek olabilir). Lenf düğümleri, akciğer, karaciğer yada kemik metastazı yapmış olan tümörler kemoterapi yada radyasyona iyi cevap vermez ve sağkalım kötüdür (18). 42
43 Takip Tedaviye bağımlı olmaksızın bildirilen olgularda takip verilerinin olmayışı ve metastatik tümörlerin ölümcül olması nedeniyle uygun takip için öneriler verilememektedir Sertoli hücreli tümörler Epidemiyoloji Sertoli hücreli tümörler testis tümörlerinin %1 inden azını oluşturur. Tanıda ortalama yaş 45 dir ve nadiren 20 yaşın altında görülür (4,20). Bu tümörler nadiren androjen yetmezliği sendromu ve Peutz-Jeghers sendromu olan hastalarda gelişir Sertoli hücreli tümörlerin patolojisi Tümör iyi sınırlı, sarı, açık kahverengi yada beyaz renklidir ve ortalama çapı 3.5 cm dir (4). Mikroskopik olarak eozinofilik vakuollu soluk sitoplazmalı hücrelerden oluşur. Nükleuslar düzgün sınırlı olup çentiklidir ve inklüzyonlar olabilir. Hücreler tübüler yada solid düzende olabilir, kord şeklinde yada retiform yapı mümkündür. Stroma düzenli ve kapillerdir, fakat bazen sklerozan yapı ön planda olabilir. Hücreler vimentin, sitokeratin, inhibin (%40) ve S- 100 proteini salgılar (%30) (4). Malin tümör oranı %10-%22 arasındadır ve 50 den az malin olgu bildirilmiştir (23-25). Malin Sertoli tümör belirtileri: Büyük boyut (>5cm) Nükleolu olan pleomorfik nükleus Artmış mitotik aktivite (her 10 luk büyütme alanında >3) Nekroz Vasküler yayılım Sınıflandırma Üç alt tipi tanımlanmıştır (20): Klasik sertoli hücreli tümör (4) Karakteristik kalsifikasyonları olan kalsifiye büyük hücre formu (5,21) Nadir sklerozan form (6,22) 43
44 Tanı Hastalarda testiste ağrısız kitle nedeniyle başvurur yada kitle raslantısal olarak ultrasonda saptanır. (26). Klasik Sertoli hücreli tümörlerin çoğu tek taraflı ve unifokaldir. Hormonal bozukluklar sık değildir ancak bazen jinekomasti görülür (4). Testiküler tümör belirleyiciler AFP, HCG, LDH ve PLAP her zaman negatiftir. Tanı için yapılacak değerlendirmede tümör belirleyicileri, hormonlar (en azından testesteron, LH ve FSH, eğer sonuç alınamazsa ek olarak östrojen, östradiol, progesteron ve kortizol), her iki testis ultrasonu ve göğüs ve batın BT yapılmalıdır. Sertoli hücreli tümörler ultrasonda genel olarak hipoekoiktir, fakat değişik görünümler olabilir ve bu nedenle germ hücreli tümörlerden güvenli şekilde ayrımı yapılamaz (20). Yalnızca büyük kalsifiye hücreli form kalsifikasyona bağlı parlak ekojenik odaklarla karakteristik görüntü verir (27,28). Büyük kalsifiye hücreli formu genç erkeklerde görülür ve genetik sendromlarla ilişkilidir (Carney sendromu (29) ve Peutz-Jegher sendromu (30)) yada olguların %40 ında endokrin bozukluklarla beraberdir. %44 ü eş zamanlı veya farklı zamanlı olarak çift taraflıdır ve %28 i multifokalite gösterir (24). Metastatik tümör karakteristikleri yukarıda tanımlanmıştır (24,25). Ancak, histopatolojik olarak malin olarak tanımlanan hastaların (tüm bildirilen tümörlerin %18.8 i) yalnızca %7 sinde takiplerde metastaz gelişmiştir. En uzun izlem süresi olan en büyük seride hastaların %7.5 i tanı anında malin olarak sınıflandırılmıştır ve %11.7 sinde uzun dönemde metastaz gelişmiştir (4). Genel olarak hastalar genellikle ileri yaştadır ve tümörlerin hemen hemen tamamı muayenede ele gelir ve birden fazla malinite belirtisi taşır (4). Büyük hücreli sklerozan form %20 ye kadar oranlarda malindir. Metastatik hastalık riski açısından erken ve geç başlayan tipleri arasında değişik risk oranları olduğuna dair bazı ipuçları vardır (%5.5 e karşın %23) (20). Nadir görülen sklerozan alt tipinde metastaz oluşumu da sık görülmez Tedavi Küçük hacimli semptom vermeyen testis tümörleri genellikle germ hücreli tümörlerle karışır ve inguinal orşiektomi yapılır. Küçük parenkim içinde yerleşik lezyonlarda histolojik tanı elde edilene değin organ koruyucu girişim önerilmektedir. Özellikle jinekomasti veya hormonal bozukluklara bağlı semptomları olan hastalarda yada ultrasonda tipik görünüm olması 44
45 durumunda (kalsifikasyonlar, küçük iyi sınırlı tümörler) organ koruyucu cerrahi tercih düşünülmelidir. Kesin patolojik sonuç non-stromal tümör (örneğin germ hücreli) olarak belirlenirse ikincil orşiektomi yapılır. Organ koruyucu cerrahi, kalan testis parenkimi endokrin (ve stromal tümörlerde ekzokrin) fonksiyon için yeterli olması durumunda mantıklı olacaktır. Malin histolojik bulguların olduğu stromal tümörlerde, özellikle yaşlı hastalarda, orşiektomi ve retroperitoneal lenfadenektomi metastazların önlenmesi için önerilir (19). Malin histolojik bulgular olmadığında orşiektomi sonrası hastanın özelliklerine göre biçimlendirilen izlem protokolu önerilir (özgün tümör belirleyicileri olmadığı için BT ile takip en uygun yöntem olabilir). Lenf düğümü, akciğer, karaciğer yada kemik metastazı yapmış olan tümörler kemoterapi yada radyasyona iyi cevap vermez ve sağkalım kötüdür Takip Tedaviye bağımlı olmaksızın bildirilen olgularda takip verilerinin olmayışı ve metastatik tümörlerin ölümcül olması nedeniyle uygun takip için öneriler verilememektedir Granuloza hücreli tümör Nadir bir tümördür ve juvenil ve yetişkin olmak üzere iki tipi vardır. Juvenil tip benindir. En sık doğumsal testis tümördür ve tüm ergenlik öncesi testis neoplazmlarının %6.6 sını oluşturur. Bu tümör tipi için kistik görünüm karakteristiktir (31). Yetişkin tipte ortalama görülme yaşı 44 dür. Tipik morfoloji homojen, sarı-gri renkli mikro-foliküler ve Call-Exner cisimcikleri içeren uzamış hücrelerin oluşturduğu tümör görüntüsüdür. Malin tümörler olguların %20 sini oluşturur. Genellikle 7 cm den büyüktür. Vasküler yayılım ve nekroz malin davranışı düşündüren özelliklerdir (32) Tekoma/fibroma grup tümörler Bunlar çok nadir görülen ve benin özellikte tümörlerdir (7) Diğer seks kord/gonadal stroma tümörleri Seks kord/gonadal stromal tümörler tam farklılaşmamış yada karışık formlarda olabilir. 45
46 Tam farklılaşmamış seks kord/gonadal stromal tümörlerle ilgili sınırlı deneyim vardır ve bu tümörlerde metastaz rapor edilmemiştir (7). Karışık form tümörlerde tüm histolojik öğeler rapor edilmelidir. Bununla beraber tümörün klinik davranışını en yaygın yada en saldırgan öğenin davranışı yansıtır (33) Germ hücresi ve seks kord/gonadal stroma içerikli tümörler (gonadoblastoma) Eğer germ hücreleri yuva (nest) şeklinde diziliş gösteriyor ve tümörün geri kalan kısmı seks kord/gonadal stroma tarafından oluşturuluyorsa gonadoblastoma terimi kullanılır. En sık gonadal disgenez ile birlikte cinsiyetin belirsiz (ambiguous genitalia) olduğu olgularda görülür ve olguların %40 ında çift taraflıdır. Prognoz germinal içeriğin yayılarak büyümesi ile ilişkilidir (34). Farklı öğelerin dağınık görüldüğü olgularda germinal hücrelerin neoplastik durumu ile ilgili şüpheler vardır ve bazı yazarlar germinal hücrelerin neoplastik olmaktan çok tümör dokusu içinde sıkışmış durumda olduklarını savunurlar (35) Testisin diğer tümörleri Ovaryan epitelyal tip tümörler Bu tümörler overin epitelyal tümörlerine benzerlik gösterirler. Bazen müsinöz maddeleri de içeren kistik görünüm gözlenebilir. Mikroskopik olarak bu tümörler overdeki karşılıklarıyla aynı görünümdedir ve gelişmeleri overdeki değişik alt tiplere benzerlik gösterir. Bazı Brenner tipleri malin olabilir (7) Toplayıcı kanallar ve rete testis tümörleri Bu tümörler çok nadirdir. Benin (adenom) ve malin (adenokarsinom) olgular bildirilmiştir ve lokal yayılım gösteren malin tiplerde mortalite oranı %56 dır (18) Spesifik olmayan stroma tümörleri (benin ve malign) Bu tümörler çok nadirdir ve yumuşak doku sarkomaları ile benzer özellikler, prognoz ve tedavi şekline sahiptir. 46
47 11. KAYNAKLAR Germ hücreli tümörler 1. Richie JP. Neoplasms of the testis. In: Walsh PC et al., eds. Campbell s Urology. 7th edn. Philadelphia:WB Saunders, 1997: Schottenfeld D, Warshauer ME, Sherlock S, Zauber AG, Leder M, Payne R. The epidemiology of testicular cancer in young adults. Am J Epidemiol 1980;112(2): EBM III. =Abstract 3. Huyghe E, Matsuda T, Thonneau P. Increasing incidence of testicular cancer worldwide: a review. J Urol 2003;170(1):5-11. EBM III. t=abstract 4. McGlynn KA, Devesa SS, Sigurdson AJ, Brown LM, Tsao L, Tarone RE. Trends in the incidence oftesticular germ cell tumours in the United States. Cancer 2003;97(1): EBM III- IIb. dopt=abstract 5. Bosl GJ, Motzer RJ. Testicular germ-cell cancer. N Engl J Med 1997;337(4): =Abstract 6. Kuczyk MA, Serth J, Bokemeyer C, Jonassen J, Machtens S, Werner M, Jonas U. Alterations of the p53 tumour suppressor gene in carcinoma in situ of the testis. Cancer 1996;78(9): EBM IIb. opt=abstract 7. Looijenga LH, Gillis AJ, Stoop H, Hersmus R, Oosterhuis JW. Relevance of micrornas in normal and malignant development, including human testicular germ cell tumours. Int J Androl 2007;30(4): ; iscussion &ordinalpos=8&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 8. Reuter VE. Origins and molecular biology of testicular germ cell tumors. Mod Pathol 2005;18(Suppl 2):S &ordinalpos=42&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocS um 9. Osterlind A, Berthelsen JG, Abildgaard N, Hansen SO, Hjalgrim H, Johansen B, Munck-Hansen J, Rassmussen LH. Risk of bilateral testicular germ cell tumours in Denmark: J Natl Cancer Inst 1991;83(19): EBM IIa. =Abstract 10. Moller H, Prener A, Skakkebaek NE. Testicular cancer, cryptorchidism, inguinal hernia, testicularatrophy and genital malformations: case-control studies in Denmark. Cancer Causes Control 1996;7(2): EBM IIa. =Abstract 47
48 11. Dieckmann KP, Pichlmeier U. The prevalence of familial testicular cancer. Cancer 1997;80(10): EBM IIb. =Abstract 12. Forman D, Oliver RT, Brett AR, Marsh SG, Moses JH, Bodmer JG, Chilvers CE, Pike MC. Familial testicular cancer: a report of the UK family register, estimation of risk and a HLA class 1 sib-pair analysis. Br J Cancer 1992;65(2): EBM IIb. =Abstract 13. Weestergaard T, Olsen JH, Frisch M, Kroman N, Nielsen JW, Melbye M. Cancer risk in fathers and brothers of testicular cancer patients in Denmark. A population based study. Int J Cancer 1996;66(5): EBM IIb. opt=abstract 14. Dieckmann KP, Loy V, Buttner P. Prevalence of bilateral germ cell tumours and early detection based on contralateral testicular intra-epithelial neoplasia. Br J Urol 1993;71(3): EBM IIa. =Abstract 15. Dieckmann KP, Pichlmeier U. Is risk of testicular cancer related to the body size? Eur Urol 2002;42(6): EBM III. t=abstract 16. Wanderas EH, Tretli S, Fossa SD. Trends in incidence of testicular cancer in Norway Eur J Cancer 1995;31A(12): EBM III. =Abstract 17. Jones A, Fergus JN, Chapman J, Houghton L. Is surveillance for stage I germ cell tumours of the testis appropiate outside a specialist centre? BJU Int 1999;84(1): EBM III Collette L, Sylvester RJ, Stenning SP, Fossa SD, Mead GM, de Wit R, de Mulder PH, Ney Lallemand E, Kaye SB. Impact of the treating institution on survival of patients with poor-prognosis nonseminoma.european Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Collaborative Group and the Medical Research Council Testicular Working Party. J Natl Cancer Inst 1999;91(10): EBM III Albers P, Albrecht W, Algaba F, Bokemeyer C, Cohn-Cedermark G, Horwich A, Klepp O, Laguna MP, Pizzocaro G. Guidelines on testicular cancer. Eur Urol 2005;48(6): &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 20. Warde P, Specht L, Horwich A, Oliver T, Panzarella T, Gospodarowicz M, von der Maase H. Prognostic factors for relapse in stage I seminoma managed by surveillance: a pooled analysis. J Clin Oncol 2002;20(22): EBM IIa Shelley MD, Burgon K, Mason MD. Treatment of testicular germ-cell cancer: a cochrane evidence based systematic review. Cancer Treat Rev 2002;28(5): Krege S, Souchon R, Schmoll HJ; German Testicular Cancer Study Group. Interdisciplinary consensus on diagnosis and treatment of testicular germ cell tumours: result of an update conference on evidencebased medicine (EBM). Eur Urol 2001;40(4): Deutsche Krebsgesellschaft: Leitlinie zur Diagnostik und Therapie von Hodentumouren auf Grundlage evidenzbasierter Medizin (EBM). Souchon R, Schmoll HJ, Krege S, for the German Testicular Cancer Study Group (eds). Qualitätsicherung in der Onkologie. 1st ed. München-Bern-Wien-New York- 48
49 Zuckschwerdt, [German Cancer Society: Evidence-based guideline for the assessment and treatment of testicular tumours] [German]. 24. The Royal College of Radiologists Clinical Oncology Network in partnership with Scottish Intercollegiate Network Guidelines on the management of adult testicular germ cell tumours. Clin Oncol (R Coll Radiol) 2000;12(5):S173-S Diagnostiek en behandeling van kiemceltumouren van de testis. Richtlijnen Nederlandse Vereniging voor urologie. No 14. [Diagnosis and treatment of testicular germ cell tumours. Dutch Urological Society guidelines] [Dutch] 26. Segal R, Lukka H, Klotz LH, Eady A, Bestic N, Johnston M; Cancer Care Ontario Practice Guidelines Initiative Genitourinary Cancer Disease Site Group. Surveillance programs for early stage nonseminomatous testicular cancer: a practice guideline. Can J Urol 2001;8(1): US Department of Health & Human Services. Public Health Service, Agency for Healthcare Research and Quality 1992: WHO histological classification of testis tumours. In: Eble JN, Sauter G, Epstein JI, Sesterhenn IA, eds. Pathology & Genetics. Tumours of the urinary system and male genital organs. Lyons: IARC Press, 2004: 218, EBM III. 29. Germa-Lluch JR, Garcia del Muro X, Maroto P, Paz-Ares L, Arranz JA, Guma J, Alba E, Satre J, Aparicio J, Fernandez A, Barnadas A, Terrassa J, Saenz A, Almenar D, Lopez-Brea M, Climent MA, Sanchez MA, Lasso de la Vega R, Berenguer G, Perez X; Spanish Germ-Cell Cancer Group (GG). Clinical pattern and therapeutic esults achieved in 1490 patients with germ-cell tumours of the testis: the experience of the Spanish Germ-Cell Cancer Group (GG). Eur Urol 2002;42(6): EBM III Skakkebaek NE. Possible carcinoma-in-situ of the testis. Lancet 1972;2(7776): EBM III. ttp:// bstract 31. Richie JP, Birnholz J, Garnick MB. Ultrasonography as a diagnostic adjunct for the evaluation of masses in the scrotum. Surg Gynecol Obstet 1982;154(5): EBM III Doherty FJ. Ultrasound of the nonacute scrotum. In: Raymond HW et al. eds. Seminars in Ultrasound, CT and MRI. New York: WB Saunders, 1991: Comiter CU, Benson CJ, Capelouto CC, Kantoff P, Shulman L, Richie JP, Loughlin KR. Nonpalpable intratesticular masses detected sonographically. J Urol 1995;154(4): EBM III. 4 &ordinalpos=2&itool=entrezsystem2.pentrez.pubmed.pubmed_resultspanel.pubmed_rvdocsum 34. Friedrich M, Claussen CD, Felix R. Immersion ultrasound of testicular pathology. Radiology 81;141(1): Glazer HS, Lee JKT, Melson GL, McClennan BL. Sonographic detection of occult testicular neoplasm. ARJ Am J Roentgenol 1982;138(4): = bstract 36. Bockrath JM, Schaeffer AJ, Kiess MS, Nieman HL. Ultrasound Identification of impalpable testicle tumour. J Urol 1983;130(2): Shawker TH, Javadpour N, O Leary T, Shapiro E, Krudy AG. Ultrasonographic detection of burnedout primary testicular germ cell tumours in clinically normal testes. J Ultrasound Med 1983;2(10): &ordinalpos=4&itool=entrezsystem2.pentrez.pubmed.pubmed_resultspanel.pubmed_rvdocsum 49
50 38. Lenz S, Giwercman A, Skakkebaek NE, Bruun E, Frimodt-Moller C. Ultrasound in detection of early neoplasia of the testis. Int J Androl 1987;10(1): EBM III. = bstract 39. Thurnher S, Hricak H, Carroll PR, Pobiel RS, Filly RA. Imaging the testis: comparison between MR imaging and US. Radiology 1988;167(3): = bstract 40. Mattrey RF. Magnetic resonance imaging of the scrotum. Semin Ultrasound CT MR 1991;12(2): Rholl KS, Lee JKT, Ling D, Heiken JP, Glazer HS. MR imaging of the scrotum with a high resolution urface coil. Radiology 1987;163(1): EBM IIa Johnson JO, Mattrey RF, Phillipson J. Differentiation of seminomatous from nonseminomatous testicular tumours by MRI. AJR Am J Roentgenol 1990;154(3): = bstract 43. Klein EA. Tumour markers in testis cancer. Urol Clin North Am 1993;20(1): &ordinalpos=2&itool=entrezsystem2.pentrez.pubmed.pubmed_resultspanel.pubmed_rvdocsum 44. Peyret C. Tumeurs du testicule. Synthèse et recommandations en onco-urologie. Prog Urol 1993;2: [Testicular tumours. Summary of onco-urological recommendations.] [French] 45. Javadpour N. The role of biologic markers in testicular cancer. Cancer 1980;45(7 Suppl): Heidenreich A, Weissbach L, Holth W, Albers P, Kliesch S, Kohrmann KU, Dieckmann KP. German Testicular Cancer Study Group. Organ sparing surgery for malignant germ cell tumour of the testis. J Urol 2001;166(6): EBM IIb Petersen PM, Giwercman A, Daugaard G, Rorth M, Petersen JH, Skakkebaek NE, Hansen SW, von der Maase H. Effect of graded testicular doses of radiotherapy in patients treated for carcinoma-in-situ in the testis. J Clin Oncol 2002;20(6): EBM IIb Heidenreich A, Holtl W, Albrecht W, Pont J, Engelmann UH. Testis-preserving surgery in bilateral testicular germ cell tumours. Br J Urol 1997;79(2): EBM IIb Weissbach L. Organ preserving surgery of malignant germ cell tumours. J Urol 1995;153(1):90-3.EBM IIb. opt=abstract 50. Dieckmann KP, Loy V. Prevalence of contralatral testicular intraepithelial neoplasia in patients with testicular germ cell neoplasms. J Clin Oncol 1996;14(12): EBM IIa-IIb Von der Maase H, Rorth M, Walbom-Jorgensen S, Sorensen BL, Christophersen IS, Hald T, Jacobsen GK, Berthelsen JG, Skakkebaek NE. Carcinoma-in-situ of contralateral testis in patients with testicular germ cell cancer: study of 27 cases in 500 patients. Br Med J (Clin Res Ed) 1986; 293(6559): EBM IIa Harland SJ, Cook PA, Fossa SD, Horwich A, Mead GM, Parkinson MC, Roberts JT, Stenning SP. Intratubular germ cell neoplasia of contralateral testis in testicular cancer: defining a high risk group. J Urol 1998;160(4): EBM IIa. 50
51 53. Giwercman A, Bruun E, Frimotd-Muller C, Skakkebaek NE. Prevalence of carcinoma in situ and other histopathological abnormalities in testes of men with a history of cryptorchidism. J Urol1989;142(4): EBM IIb Tabernero J, Paz-Ares L, Salazar R, Lianes P, Guerra J, Borras J, Villavicencio H, Leiva O, Cortes- Funes H. Incidence of contralateral germ cell testicular tumours in South Europe: report of the experience at 2 Spanish university hospitals and review of the literature. J Urol 2004;171(1): EBM III Herr HW, Sheinfeld J. Is biopsy of the contralateral testis necessary in patients with germ cell tumors? J Urol 1997;158(4): opt 56. Albers P, Goll A, Bierhoff E, Schoeneich G, Muller SC. Clinical course and histopathologic risk factor assessment in patients with bilateral testicular germ cell tumours. Urology 1999;54(4): Heidenreich A, Moul JW. Contralateral testicular biopsy procedure in patients with unilateral testis cancer: is it indicated? Sem Urol Oncol 2002;20(4): EBM III or IIb Dieckmann KP, Kulejewski M, Pichlmeier U, Loy V. Diagnosis of contralateral testicular intraepithelial neoplasia (TIN) in patients with testicular germ cell cancer: systematic two-site biopsies are more sensitive than a single random biopsy. Eur Urol 2007:51(1): EBM IIb &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 59. Kliesch S, Thomaidis T, Schütte B, Puhse G, Kater B, Roth S, Bergmann M. Update on the diagnostic safety for detection of testicular intraepithelial neoplasia (TIN). APMIS 2003;111(1): &ordinalpos=19&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 60. Classen J, Dieckmann K, Bamberg M, Souchon R, Kliesch S, Kuehn M, Loy V; German Testicular Cancer Study Group. Radiotherapy with 16 Gy may fail to eradicate testicular intraepithelial neoplasia: preliminary communication of a dose-reduction trial of the German Testicular Cancer Study Group. Br J Cancer 2003;88(6): EBM IIb &query_hl=1 61. Leibovitch I, Foster RS, Kopecky KK, Donohue JP. Improved accuracy of computerized tomography based clinical staging in low stage nonseminomatous germ cell cancer using size criteria of retroperitoneal lymph nodes. J Urol 1995;154(5): EBM III Jing B, Wallace S, Zornoza J. Metastases to retroperitoneal and pelvic lymph nodes: computed tomography and lymphangiography. Radiol Clin North Am 1982;20(3): &ordinalpos=24&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 63. Husband JE, Barrett A, Peckham MJ. Evaluation of computed tomography in the management of testicular teratoma. Br J Urol 1981;53(2): EBM III &ordinalpos=26&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 64. Swanson DA. Role of retroperitoneal lymphadenectomy (RLDN) when patients with nonseminomatous germ cell testicular tumours are at high risk of needing lymph node surgery plus chemotherapy. In: 51
52 Donohue JP, ed. Lymph Node Surgery in Urology. International Society of Urology Reports. Oxford: Isis Medical Media, 1995: Ellis JH, Blies JR, Kopecky KK, Klatte EC, Rowland RG, Donohue JP. Comparison of NMR and CT imaging in the evaluation of metastatic retroperitoneal lymphadenopathy from testicular carcinoma. J Comput Assist Tomogr 1984;8(4): See WA, Hoxie L. Chest staging in testis cancer patients: imaging modality selection based upon risk assessment as determined by abdominal computerized tomography scan results. J Urol 1993;150(3): EBM III Cremerius U, Wildberger JE, Borchers H, Zimny M, Jakse G, Gunther RW, Buell U. Does positron emission tomography using 18-fluoro-2-deoxyglucose improve clinical staging of testicular cancer? Results of a study in 50 patients. Urology 1999;54(5): EBM IIb Albers P, Bender H, Yilmaz H, Schoeneich G, Biersack HJ, Mueller SC. Positron emission tomography in the clinical staging of patients with Stage I and II testicular germ cell tumours. Urology 1999;53(4): EBM IIb De Santis M, Becherer A, Bokemeyer C, Stoiber F, Oechsle K, Sellner F, Lang A, Kletter K, Dohmen BM, Dittrich C, Pont J. 2-18fluoro-deoxy-D-glucose positron emission tomography is a reliable predictor for viable tumor in postchemotherapy seminoma: an update of the prospective multicentric SEMPET trial. J Clin Oncol 2004;22(6): EBM IIb. Pubmed_ResultsPanel.Pubmed_RVDocSum 70. Spermon JR, De Geus-Oei LF, Kiemeney LA, Witjes JA, Oyen WJ. The role of (18)fluoro-2- deoxyglucose positron emission tomography in initial staging and re-staging after chemotherapy for testicular germ cell tumours. BJU Int, 2002;89(6): EBM IIb Sobin LH, Wittekind Ch, eds. UICC: TNM classification of malignant tumours. 6th edn. Wiley-Liss, Zagars GK. Management of stage I seminoma: radiotherapy. In: Horwich A, ed. Testicular Cancer: Investigation and Management. London: Chapman & Hall Medical, 1999: Klepp O, Flodgren P, Maartman-Moe H, Lindholm CE, Unsgaard B, Teigum H, Fossa SD, Paus E. Early clinical stages (CS1, CS1Mk+ and CS2A) of non-seminomatous testis cancer. Value of pre- and storchidectomy serum tumour marker information in prediction of retroperitoneal lymph node metastases. Swedish-Norwegian Testicular Cancer Project (SWENOTECA). Ann Oncol 1990;1(4): EBM IIb. =Abstract 74. International Germ Cell Cancer Collaborative Group. International Germ Cell Consensus Classification: a prognostic factor-based staging system for metastatic germ cell cancers. J Clin Oncol 1997;15(2): EBM Ia, IIa, IIb, III. =Abstract 75. Bokemeyer C, Schmoll HJ. Treatment of clinical stage I testicular cancer and a possible role for new biological prognostic parameters. J Cancer Res Clin Oncol 1996;122: Albers P, Siener R, Kliesch S, Weissbach L, Krege S, Sparwasser C, Schulze H, Heidenreich A, de Riese W, Loy V, Bierhoff E, Wittekind C, Fimmers R, Hartmann M; German Testicular Cancer Study Group. Risk factors for relapse in clinical stage I nonseminomatous testicular germ cell tumours: results of the German Testicular Cancer Study Group Trial. J Clin Oncol 2003;21(8): EBM IIa-Ib. =Abstract 77. Petersen PM, Giwercman A, Skakkebaek NE, Rorth M. Gonadal function in men with testicular cancer. Semin Oncol 1998;25(2): EBM III. 52
53 78. De Santis M, Albrecht W, Holtl W, Pont J. Impact of cytotoxic treatment on long-term fertility in patients with germ-cell cancer. Int J Cancer 1999;83(6): EBM III Jacobsen KD, Fossa SD, Bjoro TP, Aass N, Heilo A, Stenwig AE. Gonadal function and fertility in patients with bilateral testicular germ cell malignancy. Eur Urol 2002;42(3): EBM III Kliesch S, Behre HM, Jurgens H, Nieschlag E. Cryopreservation of semen from adolescent patients with malignancies. Med Pediatr Oncol 1996;26(1): EBM IV Giwercman A, von der Maase H, Rorth M, Skakkebaek NE. Semen quality in testicular tumour and CIS in the contralateral testis. Lancet 1993;341(8841): EBM IV. =Abstract 82. Kliesch S, Bergmann M, Hertle L, Nieschlag E, Behre HM. Semen parameters and testicular pathology in men with testicular cancer and contralateral carcinoma in situ or bilateral testicular malignancies. Hum Reprod 1997;12(12): EBM IV. =Abstract 83. Spermon JR, Kiemeney LA, Meuleman EJ, Ramos L, Wetzels AM, Witjes JA. Fertility in men with testicular germ cell tumours. Fertil Steril 2003;79(Suppl 3): EBM III Nieschlag E, Behre HM. Pharmacology and clinical use of testosterone. In: Nieschlag E, Behre HM, eds. Testosterone-Action, deficiency, substitution. Berlin Heidelberg-New York: Springer, 1999: EBM Ib-IV. 85. Sternberg CN. The management of stage I testis cancer. Urol Clin North Am 1998 Aug;25(3): EBM IIb. =Abstract&itool=iconabstr 86. Groll RJ, Warde P, Jewett MA. A comprehensive systematic review of testicular germ cell tumor surveillance. Crit Rev Oncol Hematol 2007;64(3): &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 87. Chung P, Parker C, panzarella T, Gospodarowicz MK, Jewett S, Milosevic MF, Catton CN, Bayley AJ, Tew-George B, Moore M, Sturgeon JF, Warde P. Surveillance in stage I testicular seminoma-risk of late relapse. Can J Urol 2002;9(5): EBM III. &itool=iconabstr 88. Warde P, Jewett MAS. Surveillance for stage I testicular seminoma. Is it a good option? Urol Clin North Am 1998;25(3): &itool=iconabstr 89. Aparicio J, Garcia del Muro X, Maroto P, Paz-Ares L, Alba E, Saenz A, Terrasa J, Barnadas A, Almenar D, Arranz JA, Sanchez M, Fernandez A, Sastre J, Carles J, Dorca J, Guma J, Yuste AL, Germa JR; Spanish Germ Cell Cancer Cooperative Group (GG). Multicenter study evaluating a dual policy of postorchidectomy surveillance and selective adjuvant single-agent carboplatin for patients with clinical stage I seminoma. Ann Oncol 2003;14(6): t=abstract&itool=iconabstr 90. Sharda N, Kinsella T, Ritter M. Adjuvant radiation versus observation: a cost analysis of alternate management schemes in earlystage testicular seminoma. J Clin Oncol 1996;14(11): EBM IIb. 53
54 =Abstract&itool=iconabstr 91. Francis R, Bower M, Brunstrom G, Holden L, Newlands ES, Rustin GJS, Seckl MJ. Surveillance for stage I testicular germ cell tumours: results and cost benefit analysis of management options. Eur J Cancer 2000;36(15): EBM III. &itool=iconabstr 92. Warde P, Gospodarowicz M, Panzarella T, Catton C, Sturgeon J, Moore M, Jewett M. Issues in the management of stage I testicular seminoma. Int J Radiat Oncol Biol Phys 1997;39:S Oliver RT, Mason MD, Mead GM, von der Maase H, Rustin GJ, Joffe JK, de Wit R, Aass N, Graham JD, Coleman R, Kirk SJ, Stenning SP; MRC TE19 collaborators and the EORTC collaborators. Radiotherapy versus single-dose carboplatin in adjuvant treatment of stage I seminoma: a randomised trial. Lancet 2005;23-29;366(9482): &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 94. Warszawski N, Schmucking M. Relapses in early-stage testicular seminoma: radiation therapy versus retroperitoneal lymphadenectomy. Scan J Urol Nephrol 1997;31(4): EBM III. &itool=iconabstr 95. Heidenreich A, Albers P, Hartmann M, Kliesch S, Kohrmann KU, Krege S, Lossin P, Weissbach L; German Testicular Cancer Study Group. Complications of primary nerve sparing retroperitoneal lymph node dissection for clinical stage I nonseminomatous germ cell tumours of the testis: experience of the German Testicular Cancer Study Group. J Urol 2003;169(5): EBM III. &itool=iconabstr 96. Aparicio J, Germà JR, García del Muro X, Maroto P, Arranz JA, Sáenz A, Barnadas A, Dorca J, Gumà J, Olmos D, Bastús R, Carles J, Almenar D, Sánchez M, Paz-Ares L, Satrústegui JJ, Mellado B, Balil A, López- Brea M, Sánchez A; The Second Spanish Germ Cell Cancer Cooperative Group. Risk-adapted management for patients with clinical stage I seminoma: the Second Spanish Germ Cell Cancer Cooperative Group study. J Clin Oncol 2005;23(34): EBM IIa 98&ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 97. Schoffski P, Höhn N, Kowalski R, Classen J, Meisner C, Fechner G, Dieckmann K, Winkler C, Bamberg M. Health-related quality of life (QoL) in patients with seminoma stage I treated with either adjuvant radiotherapy (RT) or two cycles of carboplatinum chemotherapy (CT): Results of a randomized phase III trial of the German Interdisciplinary Working Party on Testicular Cancer. ASCO Annual Meeting Proceedings. Part 1. J Clin Oncol 2007;25(Suppl 18S): f8201eb61a7010VgnVCM100000ed730ad1RCRD&vmview=abst_detail_view&confID=47&abstractI D= Fossa SD, Horwich A, Russell JM, Roberts JT, Cullen MH, Hodson NJ, Jones WG, Yosef H, Duchesne GM, Owen JR, Grosch EJ, Chetiyawardana AD, Reed NS, Widmer B, Stenning SP. Optimal planning target volume for stage I testicular seminoma: a Medical Research Council randomized trial. J Clin Oncol 1999;17(4):1146. EBM Ib. =Abstract&itool=iconabstr 99. Jones WG, Fossa SD, Mead GM, Roberts JT, Sokal M, Naylor S, Tenning SP. A randomized trial of two radiotherapy schedules in the adjuvant treatment of stage I seminoma (MRC TE 18). Eur J Cancer 2001;37(Suppl 6):S157, abstract 572. EBM Ib Melchior D, Hammer P, Fimmers R, Schuller H, Albers P. Long term results and morbidity of paraaortic compared with paraaortic and iliac adjuvant radiation in clinical stage I seminoma. Anticancer Res 2001;21(4B): EBM III. &itool=iconabstr 101. Livsey JE, Taylor B, Mobarek N, Cooper RA, Carrington B, Logue PJ. Patterns of relapse following radiotherapy for stage I seminoma of the testis: implications for followup. Clin Oncol (R Coll Radiol) 2001;13(4): EBM III. &itool=iconabstr 54
55 102. Van Leeuwen FE, Stiggelbout AM, van den Belt-Dusebout AW, Noyon R, Eliel MR, van Kerkhoff EH, Delemarre JF, Somers R. Second cancer risk following testicular cancer: a follow-up study of 1909 patients. Clin Oncol 1993;11(3): &itool=iconabstr 103. Travis LB, Curtis RE, Storm H, Hall P, Holowaty E, Van Leeuwen FE, Kohler BA, Pukkala E, Lynch CF, Andersson M, Bergfeldt K, Clarke EA, Wiklund T, Stoter G, Gospodarowicz M, Sturgeon J, Fraumeni JF Jr, Boice JD Jr. Risk of second malignant neoplasms among long-term survivors of esticular cancer. J Natl Cancer Inst 1997;89(19): EBM III. &itool=iconabstr 104. Horwich A, Bell J. Mortality and cancer incidence following treatment for seminoma of the testis. Radiother Oncol 1994;30(3): EBM III. &itool=iconabstr 105. Bieri S, Rouzaud M, Miralbell R. Seminoma of the testis: is scrotal shielding necessary when radiotherapy is limited to the para-aortic nodes? Radiother Oncol 1999;50(3): EBM IIb. &itool=iconabstr 106. Freedman LS, Parkinson MC, Jones WG, Oliver RT, Peckham MJ, Read G, Newlands ES, Williams CJ. Histopathology in the prediction of patients with stage I testicular teratoma treated by orchidectomy alone. Lancet 1987;2(8554): &itool=iconabstr 107. Read G, Stenning SP, Cullen MH, Parkinson MC, Horwich A, Kaye SB, Cook PA. Medical Research Council prospective study of surveillance for stage I testicular teratoma. J Clin Oncol 1992;10(11): EBM IIb. &itool=iconabstr 108. Colls BM, Harvey VJ, Skelton L, Frampton CM, Thompson PI, Bennett M, Perez DJ, Dady PJ, Forgeson GV, Kennedy IC. Late results of surveillance of clinical stage I nonseminoma germ cell testicular tumours: 17 years experience in a national study in New Zealand. Br J Urol Int 1999;83(1): EBM IIb. &itool=iconabstr 109. Oliver RT, Ong J, Shamash J, Ravi R, Nagund V, Harper P, Ostrowski MJ, Sizer B, Levay J, Robinson A, Neal DE, Williams M; Anglian Germ Cell Cancer Group. Long-term follow-up of Anglian Germ Cell Cancer Group surveillance versus patients with Stage 1 nonseminoma treated with adjuvant chemotherapy. Urology 2004;63(3): EBM III &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 110. Klepp O, Olsson AM, Henrikson H, Aass N, Dahl O, Stenwig AE, Persson BE, Cavallin-Stahl E, Fossa SD, Wahlqvist L. Prognostic factors in clinical stage I nonseminomatous germ cell tumours of the testis: multivariate analysis of a prospective multicenter study. J Clin Oncol 1990;8(3): EBM IIa. &itool=iconabstr 111. Kakiashvili D, Anson-Cartwright L, Sturgeon JF, Warde PR, Chung P, Moore M, Wang L, Azuero J, Jewett MA. Non risk-adapted surveillance management for clinical stage I nonseminomatous testis tumors. J Urol 2007;177:278 (abstract 835) Cullen MH, Stenning SP, Parkinson MC, Fossa SD, Kaye SB, Horwich AH, Harland SJ, Williams MV, Jakes R. Short-course adjuvant chemotherapy in high-risk stage I nonseminomatous germ cell tumours of the testis: a Medical Research Council report. J Clin Oncol 1996;14(4): EBM III. &itool=iconabstr 113. Oliver RTD, Raja MA, Ong J, Gallagher CJ. Pilot study to evaluate impact of a policy of adjuvant chemotherapy for high risk stage I malignant teratoma on overall relapse rate of stage I cancer patients. J Urol 1992;148(5): EBM III. 55
56 &itool=iconabstr 114. Studer UE, Fey MF, Calderoni A. Adjuvant chemotherapy after orchidectomy in high risk patients with clinical stage I nonseminomatous testicular cancer. Eur Urol 1993;23(4): EBM IIb. &itool=iconabstr 115. Bohlen D, Borner M, Sonntag RW, Fey MF, Studer UE. Long-term results following adjuvant chemotherapy in patients with clinical stage I testicular nonseminomatous malignant germ cell tumours with high risk factors. J Urol 1999;161(4): EBM III. &itool=iconabstr 116. Pont J, Albrecht W, Postner G, Sellner F, Angel K, Holtl W. Adjuvant chemotherapy for high risk linical stage I nonseminomatous testicular germ cell cancer: long-term results of a prospective trial. J Clin Oncol 1996;14(2): EBM IIa. =Abstract&itool=iconabstr 117. Chevreau C, Mazerolles C, Soulié M, Gaspard MH, Mourey L, Bujan L, Plante P, Rischmann P, Bachaud JM, Malavaud B. Long-term efficacy of two cycles of PEB regimen in high-risk stage I nonseminomatous testicular germ cell tumors with embryonal carcinoma and/or vascular invasion. Eur Urol 2004;46(2): EBM III &ordinalpos=21&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RV DocSum 118. Bohlen D, Burkhard FC, Mills R, Sonntag RW, Studer UE. Fertility and sexual function following orchidectomy and 2 cycles of chemotherapy for stage I high risk nonseminomatous germ cell cancer. J Urol 2001;165(2): EBM III. &itool=iconabstr 119. Baniel J, Foster RS, Gonin R, Messemer JE, Donohue JP, Einhorn LH. Late relapse of testicular cancer. J Clin Oncol 1995;13(5): EBM III Baniel J, Roth BJ, Foster RS, Donohue JP. Cost and risk benefit considerations in the management of clinical stage I nonseminomatous testicular tumours. Ann Surg Oncol 1996;3(1): &itool=iconabstr 121. Rustin GJ, Mead GM, Stenning SP, Vasey PA, Aass N, Huddart RA, Sokal MP, Joffe JK, Harland SJ, Kirk SJ; National Cancer Research Institute Testis Cancer Clinical Studies Group. Randomized trial of two or five computed tomography scans in the surveillance of patients with stage I nonseminomatous germ cell tumors of the testis: Medical Research Council Trial TE08, ISRCTN the National Cancer Research Institute Testis Cancer Clinical Studies Group. J Clin Oncol 2007;25(11): EBM Ib &ordinalpos=2&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 122. Klepp O, Dahl O, Flodgren P, Stierner U, Olsson AM, Oldbring J,Nilsson S, Daehlin L, Tornblom M, Smaland R, Starkhammar H, Abramsson L, Wist E, Raabe N, Edekling T, Cavallin-Stahl E. Riskadapted treatment of clinical stage 1 non-seminoma testis cancer. Eur J Cancer 1997;33(7): EBM IIa. &itool=iconabstr 123. Ondrus D, Matoska J, Belan V. Prognostic factors in clinical stage I nonseminomatous germ cell testicular tumours: rationale for different risk-adapted treatment. Eur Urol 1998;33(6): EBM IIa, IIb =Abstract&itool=iconabstr 124. Maroto P, García del Muro X, Aparicio J, Paz-Ares L, Arranz JA, Guma J, Terrassa J, Barnadas J, Dorta J, Germà-Lluch JR. Multicentre risk-adapted management for stage I non-seminomatous germ cell tumours. Ann Oncol 2005;16(12): EBM III. 56
57 &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 125. Spermon JR, Roeleveld TA, van der Poel HG, Hulsbergen-van de Kaa CA, Ten Bokkel-Huinink WW, van de Vijver M, Witjes JA, Horenblas S. Comparison of surveillance and retroperitoneal lymph node dissection in stage I nonseminomatous germ cell tumours. Urology 2002;59(6): EBM III. t =Abtract&itool=iconabstr Hendry WF, Norman A, Nicholls J, Dearnaley DP, Peckham MJ, Horwich A. Abdominal relapse in stage 1 nonseminomatous germ cell tumours of the testis managed by surveillance or with adjuvant chemotherapy. BJU Int 2000;86(1): EBM III. &itool=iconabstr Pizzocaro G, Salvioni R, Zanoni F. Unilateral lymphadenectomy in intraoperative stage I nonseminomatous testis cancer. J Urol 1985;134(3): EBM III. &itool=iconabstr Donohue JP, Thornhill JA, Foster RS, Rowland RG, Bihrle R. Retroperitoneal lymphadenectomy for clinical stage A testis cancer ( ): modifications of technique and impact on ejaculation. J Urol 1993;149(2): EBM III. &itool=iconabstr Lashley DB, Lowe BA. A rational approach to managing stage I nonseminomatous germ cell cancer. Urol Clin North Am 1998;25(3): &itool=iconabstr 130. Foster RS, Roth BJ. Clinical stage I nonseminoma: surgery versus surveillance. Semin Oncol 1998;25(2): &itool=iconabstr 131. Kratzik C, Holtl W, Albrecht W et al. Risk adapted management for NSGCT stage I: long-term results of a multicenter study. J Urol 1996;155:547A. (Abstract) Ondrus D, Goncalves F, Kausitz J, Mat'oska J, Belan V. The value of prognostic factors in the management of stage I nonseminomatous germ cell testicular tumours (NSGCTT). Neoplasma 1996;43(3): &itool=iconabstr 133. Donohue JP, Thornhill JA, Foster RS, Rowland RG, Bihrle R. Clinical stage B nonseminomatous germ cell testis cancer: the Indiana University experience using routine primary retroperitoneal lymph node dissection. Eur J Cancer 1995;31A(10): EBM III. =Abstract&itool=iconabstr 134. Richie JP, Kantoff PW. Is adjuvant chemotherapy necessary for patients with stage 1B testicular cancer? J Clin Oncol 1991;9(8): &itool=iconabstr 135. Pizzocaro G, Monfardini S. No adjuvant chemotherapy in selected patients with pathological stage II nonseminomatous germ cell tumours of the testis. J Urol 1984;131(4): EBM IIa. &itool=iconabstr 136. Williams SD, Stablein DM, Einhorn LH, Muggia FM, Weiss RB, Donohue JP, Paulson DF, Brunner KW, Jacobs EM, Spaulding JT. Immediate adjuvant chemotherapy versus observation with treatment at relapse in pathological stage II testicular cancer. N Engl J Med 1987;317(23): EBM Ib. &itool=iconabstr 137. Bianci G, Beltrami P, Giusti G. Unilateral laparoscopic lymph node dissection for clinical stage I nonseminomatous germ cell testicular neoplasm. Eur Urol 1998;33(2): EBM III. &itool=iconabstr 57
58 138. Rassweiler JJ, Frede T, Lenz E, Seemann O, Alken P. Long-term experience with laparoscopic retroperitoneal lymph node dissection in the management of low-stage testis cancer. Eur Urol 2000;37(3): EBM III. &itool=iconabstr 139. Janetschek G, Hobisch A, Peschel R, Hittmair A, Bartsch G. Laparoscopic retyroperitoneal lymph node dissection for clinical stage I non-seminomatous testicular carcinoma: long-term outcome. J Urol 2000;163(6): EBM III. &itool=iconabstr 140. LeBlanc E, Caty A, Dargent D, Querleu D, Mazeman E. Extraperitoneal laparoscopic para-aortic lymph node dissection for early stage nonseminomatous germ cell tumours of the testis with introduction of a nerve sparing technique: description and results. J Urol 2001;165(1): EBM III. &itool=iconabstr 141. Albers P, Siener R, Krege S, Schmelz H, Dieckmann K, Heidenreich A, Kwasny P, Pechoel M, Lehmann J, Fimmers R, Hartmann M. One course of adjuvant PEB chemotherapy versus retroperitoneal lymph node dissection in patients with stage I non-seminomatous germ-cell tumours (NSGCT): Results of the German Prospective Multicenter Trial (Association of Urological Oncology [AUO]/German testicular cancer study group [GTCSG] Trial 01-94). ASCO Annual Meeting Proceedings. Part I. J Clin Oncol 2006;24(18S): f8201eb61a7010VgnVCM100000ed730ad1RCRD&vmview=abst_detail_view&confID=40&abstractI D= Pizzocaro G, Nicolai N, Salvioni R. Marker positive clinical stage I non seminomatous germ cell tumours (NSGCT) of the testis: which primary therapy? J Urol 1996;155(Suppl):328A Davis BE, Herr HW, Fair WR, Bosl GJ. The management of patients with nonseminomatous germ cell tumours of the testis with serologic disease only after orchidectomy. J Urol 1994;152(1): EBM III. &itool=iconabstr 144. International Germ Cell Collaborative Group. International Germ Cell Consensus Classification: a prognostic factor-based staging system for metastatic germ cell cancers. J Clin Oncol 1997;15(2): EBM Ia, IIa, IIb, III Krege S, Boergermann C, Baschek R, Hinke A, Pottek T, Kliesch S, Dieckmann KP, Albers P, Knutzen Weinknecht S, Schmoll HJ, Beyer J, Ruebben H; German Testicular Cancer Study Group (GTCSG) Single agent carboplatin for CS IIA/B testicular seminoma. A phase II study of the German Testicular Cancer Study Group (GTCSG). Ann Oncol 2006;17(2): EBM IIb. 23&ordinalpos=15&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 146. Frohlich MW, Small EJ. Stage II nonseminomatous testis cancer: the roles of primary and adjuvant chemotherapy. Urol Clin North Am 1998;25(3): Baniel J, Donohue JP. Cost and risk benefit considerations in low stage (I and II) nonseminomatous testicular tumours. AUA Update Series 1997;26: Kondagunta GV, Sheinfeld J, Mazumdar M, Mariani TV, Bajorin D, Bacik J, Bosl GJ, Motzer RJ. Relapse-free and overall survival in patients with pathologic stage II nonseminomatous germ cell cancer treated with etoposide and cisplatin adjuvant chemotherapy. J Clin Oncol 2004;1;22(3): EBM III &ordinalpos=14&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 149. Steiner H, Müller T, Gozzi C, Akkad T, Bartsch G, Berger AP. Two cycles of cisplatin-based chemotherapy for low-volume retroperitoneal stage II nonseminomatous germ cell tumours. BJU Int 2006;98(2): EBM IIb. 58
59 &ordinalpos=2&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 150. Weissbach L, Bussar-Maatz R, Fletchner H, Pichlmeier U, Hartmann M, Keller L. RPLND or primary chemotherapy in clinical stage IIA/B nonseminomatous germ cell tumours. Results of a prospective multicenter trial including quality of life assessment. Eur Urol 2000;37(5): Sternberg CN. Role of primary chemotherapy in stage I and low-volume stage II nonseminomatous germ-cell testis tumours. Urol Clin North Am 1993;20(1): EBM IIb Horwich A, Norman A, Fisher C, Hendry WF, Nicholls J, Dearnaley DP. Primary chemotherapy for stage II nonseminomatous germ cell tumours of the testis. J Urol 1994;151(1): EBM III Donohue JP, Thornhill JA, Foster RS, Bihrle R, Rowland RG, Einhorn LH. The role of retroperitoneal lymphadenectomy in clinical stage B testis cancer: the Indiana University Experience (1965 to 1989). J Urol 1995;153(1): EBM III. Abstract 154. Motzer RJ, Sheinfeld J, Mazumdar M, Bajorin DF, Bosl GJ, Herr H, Lyn P, Vlamis V. Etoposide and cisplatin adjuvant therapy for patients with pathological stage II germ cell tumours. J Clin Oncol 1995;13(11): EBM IIb Hartlapp JH, Weissbach L, Bussar-Maatz R. Adjuvant chemotherapy in nonseminomatous testicular tumour stage II. Int J Androl 1987;10(1): Logothetis CJ, Swanson DA, Dexeus F, Chong C, Ogden S, Ayala AG, von Eschenbach AC, Johnson DE, Samuels ML. Primary chemotherapy for clinical stage II nonseminomatous germ cell tumours of the testis: a follow-up of 50 patients. J Clin Oncol 1987;5(6): EBM IIb Saxman S, Finch D, Gonin R, Einhorn LH. Long-term follow-up of a phase III study of three versus four cycles of bleomycin, etoposide and cisplatin in favorable-prognosis germ-cell tumours: the Indiana University Experience. J Clin Oncol 1998;16(2): EBM Ib de Wit R, Stoter G, Kaye SB, Sleijfer DT, Jones WG, ten Bokkel Huinink WW, Rea LA, Collette L, Sylvester R. Importance of bleomycin in combination chemotherapy for good-prognosis testicular nonseminoma: a randomized study of the European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group. J Clin Oncol 1997;15(5): EBM Ib Horwich A, Sleijfer DT, Fossa SD, Kaye SB, Oliver RT, Cullen MH, Mead GM, de Wit R, de Mulder PH, Dearnaley DP, Cook PA, Sylvester RJ, Stenning SP. Randomized trial of bleomycin, etoposide and isplatin compared with bleomycin, etoposide and carboplatin in good-prognosis metastatic nonseminomatous germ cell cancer: a multi-institutional Medical Research Council/European Organization for Research and Treatment of Cancer trial. J Clin Oncol 1997;15(5): EBM Ib Abstract 160. De Wit R, Roberts JT, Wilkinson PM, de Mulder PH, Mead GM, Fossa SD, Cook P, de Pryck L, Stenning S, Collette L. Equivalence of three or four cycles of bleomycin, etoposide, and cisplatin chemotherapy and of a 3- or 5- day schedule in good-prognosis germ cell cancer: a randomized study of the European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group and the Medical research Council. J Clin Oncol 2001;19(6): EBM Ib. 59
60 Bokemeyer C, Kuczyk MA, Köhne H, Einsele H, Kynast B, Schmoll HJ. Hematopoetic growth factors and treatment of testicular cancer: biological interactions, routine use and dose intensive chemotherapy. Ann Hematol 1996;72(1):1-9. EBM IIa Xiao H, Mazumdar M, Bajorin DF, Sarosdy M, Vlamis V, Spicer J, Ferrara J, Bosl GJ, Motzer RJ. Longterm follow-up of patients with good-risk germ cell tumours treated with etoposide and cisplatin. J Clin Oncol 1997;15(7): EBM III. =Abstract 163. Culine S, Kerbrat P, Kramar A, Théodore C, Chevreau C, Geoffrois L, Bui NB, Pény J, Caty A, Delva R, Biron P, Fizazi K, Bouzy J, Droz JP; Genito-Urinary Group of the French Federation of Cancer Center (GETUG T93BP). Refining the optimal chemotherapy regimen for good-risk metastatic nonseminomatous germ-cell tumors: a randomized trial of the Genito-Urinary Group of the French Federation of Cancer Centers (GETUG T93BP). Ann Oncol. 2007;18(5): EBM IB &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum Fossa SD, Kaye SB, Mead GM, Cullen M, de Wit R, Bodrogi I, van Groeningen CJ, de Mulder PH, Stenning S, Lallemand E, de Pryck L, Collette L. Filgastrim during combination chemotherapy of patients with poor prognosis metastatic germ cell malignancy. European Organization for Research and Treatment of Cancer, Genito-Urinary Group, and the Medical Research Council Testicular Cancer Working Party. J Clin Oncol 1998;16(2): EBM IIa De Wit R, Stoter G, Sleijfer DT, Neijt JP, ten Bokkel Huinink WW, de Pryck L, Collette L, Sylvester R. Four cycles of PEB vs four cycles of VIP in patients with intermediate-prognosis metastatic testicular on-seminoma: a randomized study of the EORTC Genitourinary Tract Cancer Cooperative Group. European Organization for Research and Treatment of Cancer. Br J Cancer 1998;78(6): EBM Ib De Witt R, Louwerens M, de Mulder PH, Verweij J, Rodenhuis S, Schornagel J. Management of intermediate-prognosis germ-cell cancer: results of a phase I/II study of Taxol-PEB. Int J Cancer 1999;83(6): EBM III Nichols CR, Catalano PJ, Crawford ED, Vogelzang NJ, Einhorn LH, Loehrer PJ. Randomized comparison of cisplatin and etoposide and either bleomycin or ifosfamide in treatment of advanced disseminated germ cell tumours: and Eastern Cooperative Oncology Group, Southwest Oncology Group, and Cancer and Leukaemia Group B Study. J Clin Oncol 1998;16(9): EBM Ib Motzer RJ, Nichols CJ, Margolin KA, Bacik J, Richardson PG, Vogelzang NJ, Bajorin DF, Lara PN Jr, Einhorn L, Mazumdar M, Bosl GJ. Phase III randomized trial of conventional-dose chemotherapy with or without high-dose chemotherapy and autologous hematopoietic stem-cell rescue as first-line treatment for patients with poor-prognosis metastatic germ cell tumors. J Clin Oncol 2007;25(3): EBM Ib &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 169. Motzer RJ, Mazumdar M, Bajorin DF, Bosl GJ, Lyn P, Vlamis V. High-dose carboplatin, etoposide, and cyclophosphamide with autologous bone marrow transplantation in first-line therapy for patients with poor-risk germ cell tumours. J Clin Oncol 1997;15(7): EBM IIb. 60
61 170. Bokemeyer C, Kollmannsberger C, Meisner C, Harstrick A, Beyer J, Metzner B, Hartmann JT, Schmoll HJ, Einhorn L, Kanz L, Nichols C. First-line high-dose chemotherapy compared with standard-dose PEB/VIP chemotherapy in patients with advanced germ cell tumours: a multivariate and matched-pair analysis. J Clin Oncol 1999;17(11): EBM IIb Gerl A, Clemm C, Lamerz R, Mann K, Wilmanns W. Prognostic implications of tumour marker analysis in non-seminomatous germ cell tumours with poor prognosis metastatic disease. Eur J Cancer 1993;29A(7): EBM IIa Murphy BA, Motzer RJ, Mazumdar M, Vlamis V, Nisselbaum J, Bajorin D, Bosl GJ. Serum tumour markers decline is an early predictor of treatment outcome in germ cell tumour patients treated with cisplatin and ifosfamide salvage chemotherapy. Cancer 1994;73(10): EBM IIa Andre F, Fizazi K, Culine S, Droz J, Taupin P, Lhomme C, Terrier-Lacombe M, Theodore C. The growing teratoma syndrome: results of therapy and long-term follow-up of 33 patients. Eur J Cancer 2000;36(11): EBM III De Wit R, Collette L, Sylvester R, de Mulder PH, Sleyfer DT, ten Bokkel Huinink WW, Kaye SB, van Oosterom AT, Boven E, Stoter G. Serum alpha-fetoprotein surge after the initiation of chemotherapy for non-seminomatous testicular cancer has and adverse prognostic significance. Br J Cancer 1998;78(10): EBM IIb Zon RT, Nichols C, Einhorn LH. Management strategies and outcomes of germ cell tumour patients with very high human chorionic gonadotropin levels. J Clin Oncol 1998;16(4): EBM III Fossa AD, Stenning SP, Gerl A, Horwich A, Clark PI, Wilkinson PM, Jones WG, Williams MV, Oliver RT, Newlands ES, Mead GM, Cullen MH, Kaye SB, Rustin GJ, Cook PA. Prognostic factors in patients progressing after cisplatin-based chemotherapy for malignant non-seminomatous germ cell tumours. Br J Cancer 1999;80(9): EBM IIb. t Abstract 177. Fossa SD, Borge L, Aass N, Johannessen NB, Stenwig AE, Kaalhus O. The treatment of advanced metastatic seminoma: experience in 55 cases. J Clin Oncol 1987;5(7): EBM III Herr HW, Bosl G. Residual mass after after chemotherapy for seminoma: changing concepts of management. J Urol 1987;137(6): EBM III Hofmockel G, Gruss A, Theiss M. Chemotherapy in advanced seminoma and the role of postcytostatic retroperitoneal lymph node dissection. Urol Int 1996;57(1): EBM III Kamat MR, Kulkarni JN, Tongoankar HB, Ravi R. Value of retroperitoneal lymph node dissection in advanced testicular seminoma. J Surg Oncol 1992;51(1): EBM III Loehrer PJ Sr, Birch R, Williams SD, Greco FA, Einhorn LH. Chemotherapy of metastatic seminoma: the SouthEastern Cancer Study Group Experience. J Clin Oncol 1987;5(8): EBM III Motzer R, Bosl G, Heelan R, Fair W, Whitmore W, Sogani P, Herr H, Morse M. Residual mass: an indication for further therapy in patients with advanced seminoma following systemic chemotherapy. J 61
62 Clin Oncol 1987;5(7): EBM III Peckham MJ, Horwich A, Hendry WF. Advanced seminoma treatment with cisplatinum based combination chemotherapy or carboplatin (JM8). Br J Cancer 1985;52(1):7-13. EBM III De Santis M, Becherer A, Bokemeyer C, Stoiber F, Oechsle K, Sellner F, Lang A, Kletter K, Dohmen BM, Dittrich C, Pont J. 2-18fluoro-deoxy-D-glucose positron emission tomography is a reliable predictor for viable tumor in postchemotherapy seminoma: an update of the prospective multicentric SEMPET trial. J Clin Oncol 2004;22(6): EBM IIb &ordinalpos=1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 185. Duchesne GM,Stenning SP, Aass N, Mead GM, Fossa SD, Oliver RT, Horwich A, Read G, Roberts IT, Rustin G, Cullen MH, Kaye SB, Harland SJ, Cook PA. Radiotherapy after chemotherapy for metastatic seminoma a diminishing role. Eur J Cancer 1997;33(6): EBM III Bamberg M, Classen J. Stellenwert der Strahlentherapie von Residualtumouren nach Chemotherapie matastasierter Seminome. Strahlenther Onkol 1998;174(8): [German] [Significance of radiotherapy for residual tumours following chemotherapy for metastatic seminoma] Puc H, Heelan R, Mazumdar M, Herr H, Scheinfeld J, Vlamis V, Bajorin DF, Bosl GJ, Mencel P, Motzer RJ. Management of residual mass in advanced seminoma: results and recommendations from Memorial Sloan Kettering Cancer Center. J Clin Oncol 1996;14(2): EBM IV Herr HW, Sheinfeld J, Puc HS, Heelan R, Bajorin DF, Mencel P, Bosl GJ, Motzer RJ. Surgery for a postchemotherapy residual mass in seminoma. J Urol 1997;157(3): EBM III Mosharafa AA. Foster RS, Leibovich BC, Bihrle R, Donahue JP. Is the post-chemotherapy resection of seminomatous elements associated with higher acute morbidity? J Urol 2002;167:172, abstract 692. EBM III Kuczyk M, Machtens S, Stief C, Jonas U. Management of the post-chemotherapy residual mass in patients with advanced stage non-seminomatous germ cell tumours (GCT). Int J Cancer 1999;83(6): EBM III Fossa SD, Ous S, Lien HH, Stenwig AE. Post-chemotherapy lymph node histology in radiologically normal patients with metastatic nonseminomatous testicular cancer. J Urol 1989;141(3): EBM IIb Toner GC, Panicek DM, Heelan RT, Geller NL, Lin SY, Bajorin D, Motzer RJ, Scher HI, Herr HW, Morse MJ et al. Adjunctive surgery after chemotherapy for nonseminomatous germ cell tumours: recommendations for patient selection. J Clin Oncol 1990;8(10): EBM IIb Donohue JP, Rowland RG, Kopecky K, Steidle CP, Geier G, Ney KG, Einhorn L, Williams S, Loehrer P. Correlation of computerized tomographic changes and histological findings in 80 patients having radical retroperitoneal lymph nodedissection after chemotherapy for testis cancer. J Urol 1987;137(6): EBM III. 62
63 194. Richie JP. The surgical management of advanced abdominal disease. Semin Urol 1984;2(4): Stomper PC, Fung CY, Socinski MA, Jochelson MS, Garnick MB, Richie JP. Detection of retroperitoneal metastases in early-stage nonseminomatous testicular cancer: analysis of different CT criteria. Am J Roentgenol 1987;149(6): EBM III Carver BS, Shayegan B, Serio A, Motzer RJ, Bosl GJ, Sheinfeld J. Long-term clinical outcome afterpostchemotherapy retroperitoneal lymph node dissection in men with residual teratoma. J Clin Oncol 2007;25(9): &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 197. Aprikian AG, Herr HW, Bajorin DF, Bosl GJ. Resection of post-chemotherapy residual masses and limited retroperitoneal lymphadenectomy in patients with metastatic testicular nonseminomatous germ cell tumours. Cancer 1994;74(4): EBM IIa Herr HW. Does necrosis on frozen-section analysis of a mass after chemotherapy justify a limited etroperitoneal resection in patients with advanced testis cancer? Br J Urol 1997;80(4): EBM IIa Hendry WF, A Hern RP, Hetherington JW, Peckham MJ, Dearnaley DP, Horwich A. Para-aortic ymphadenectomy after chemotherapy for metastatic non-seminomatous germ cell tumours: prognostic value and therapeutic benefit. Br J Urol 1993;71(2): Wood DP, Herr HW, Heller G, Vlamis V, Sogani PC, Motzer RJ, Fair WR, Bosl GJ. Distribution of etroperitoneal metastases after chemotherapy in patients with nonseminomatous germ cell tumours J Urol 1992;148(6): EBM IIb. Abstract 201. Baniel J, Foster RS, Rowland RG, Bihrle R, Donohue JP. Complications of post-chemotherapy retroperitoneal lymph node dissection. J Urol 1995;153(3 Pt 2): EBM III Hartmann JT, Schmoll HJ, Kuczyk MA, Candelaria M, Bokemeyer C. Post-chemotherapy resection of residual masses from metastatic non-seminomatous germ cell tumours. Ann Oncol 1997;8(6): EBM III Rabbani F, Goldenberg SL, Gleave ME, Paterson RF, Murray N, Sullivan LD. Retroperitoneal ymphadenectomy for post-chemotherapy residual masses: is a modified dissection and resection of the residual mass sufficient? Br J Urol 1998;81(2): EBM III Tekgul S, Özen HA, Celebi I, Ozgu I, Ergen A, Demircin M, Remzi D. Postchemotherapeutic surgery for metastatic testicular germ cell tumours: results of extended primary chemotherapy and limited surgery. Urology 1994;43(3): EBM III Steyerberg EW, Keizer HJ, Fossa SD, Sleijfer DT, Toner GC, Schraffordt Koops H, Mulders PF, Messemer JE, Ney K, Donohue JP et al. Prediction of residual retroperitoneal mass histology after chemotherapy for metastatic nonseminomatous germ cell tumour: multivariate analysis of individual patient data from six study groups. J Clin Oncol 1995;13(5): EBM IIb. 63
64 206. Hartmann JT, Candelaria M, Kuczyk MA, Schmoll HJ, Bokemeyer C. Comparison of histological results from the resection of residual masses at different sites after chemotherapy for metastatic nonseminomatous germ cell tumours. Eur J Cancer 1997;33(6): EBM III Stenning SP, Parkinson MC, Fisher C, Mead GN, Cook PA, Fossa SD,Horwich A, Jones WG, Newlands ES, Oliver RT, Stenwig AE, Wilkinson PM. Post-chemotherapy residual masses in germ cell tumour patients: content, clinical features and prognosis. Medical Research Council Testicular Tumour Working Party. Cancer 1998;83(7): EBM III Weinknecht S, Hartmann M, Weissbach L. Bei welchen markerpositiven patienten mit keimzelltumouren ist die residualtumourresektion sinnvoll? Urologe A 1998;37(6): EBM III. [German] [In which marker positive germ-cell tumour patients is residual tumour resection useful?] Hendry WF, Norman AR, Dearnaley DP, Fisher C, Nicholls J, Huddart RA, Horwich A. Metastatic nonseminomatous germ cell tumours of the testis: results of elective and salvage surgery for patients with residual retroperitoneal masses. Cancer 2002;94(6): EBM III Sheinfeld J. The role of adjunctive post-chemotherapy surgery for nonseminomatous germ-cell tumours: current concepts and controversies. Sem Urol Oncol 2002;20(4): EBM III Foster RS, Donohue JP. Can retroperitoneal lymphadenectomy be omitted in some patients after chemotherapy? Urol Clin North Am 1998;25(3): EBM III Steyerberg EW, Kaiser HJ, Habbema JD. Prediction models of the histology of residual masses after chemotherapy for metastatic testicular cancer. ReHiT Study Group. Int J Cancer 1999;83(6): EBM III Vergouwe Y, Steyerbeg EW, De Wit R, Roberts JT, Keizer HJ, Collette L, Stenning SP, Habbema JD. External validity of a prediction rule for residual mass histology in testicular cancer: an evaluation for good prognosis patients. Br J Cancer 2003;88(6): EBM III Fizazi K, Tjulandin S, Salvioni R, Germa-Lluch JR, Bouzy J, Ragan D, Bokemeyer C, Gerl A, Flechon A, de Bono JS, Stenning S, Horwich A, Pont J, Albers P, De Giorgi U, Bower M, Bulanov A, Pizzocaro G, Aparicio J, Nichols CR, Theodore C, Hartmann JT, Schmoll HJ, Kaye SB, Culine S, Droz JP, Mahe C. Viable malignant cells after primary chemotherapy for disseminated nonseminomatous germ cell tumours: prognostic factors and role of postsurgery chemotherapy-results from an international study group. J Clin Oncol 2001;19(10): EBM III Miller KD, Loehrer PJ, Gonin R, Einhorn LH. Salvage chemotherapy with vinblastine, ifosfamide and cisplatin in recurrent seminoma. J Clin Oncol 1997;15(4): EBM IIb Beyer J, Bokemeyer C, Schmoll HJ. [Salvagetherapie rezidivierter und refraktärer Hodentumouren.] Onkologe 1998;4: [German] [Salvage chemotherapy for relapsed and refractory germ cell tumours] 217. Loehrer PJ, Gonin R, Nichols CR, Weathers T, Einhorn LH. Vinblastine plus iofosfamide plus cisplatin as nitial salvagetherapy in recurrent germ cell tumour. J Clin Oncol 1998;16(7): EBM IIb. 64
65 218. Beyer J, Rick O, Siegert W, Bokemeyer C. Salvage chemotherapy in relapsed germ cell tumours. World J Urol 2001;19(2): EBM IIb Schmoll HJ, Beyer J. Prognostic factors in metastatic germ cell tumours. Semin Oncol 1998;25(2): EBM III Kaye SB, Mead GM, Fossa SD, Cullen M, de Wit R, Bodrogi I, van Groeningen C, Sylvester R, Collette L, Stenning S, de Pryck L, Lallemand E, de Mulder P. Intensive induction-sequential chemotherapy with BOP/VIP-B compared with treatment with PEB/EP for poor prognosis metastatic germ celltumour: a randomized Medical Research Council/European Organization for Research and Treatment of Cancer study. J Clin Oncol 1998;16(2): EBM IIb Beyer J, Schmoll HJ. [Prognosefaktoren bei metastasierten seminomatösen und nichtseminomatösen Hodentumouren.] Onkologe 1998;4: [German] [Prognostic factors in metastatic seminoma and non-seminoma germ-cell tumours] 222. Beyer J, Stenning S, Gerl A, Fossa S, Siegert W. High-dose versus onventional-dose chemotherapy as a first-salvage treatment in patients with non-seminomatous germ-cell umours: a matched pair analysis. Ann Oncol 2002;13(4): EBM IIb Bhatia S, Abonour R, Porcu P, Seshadri R, Nichols CR, Cornetta K, Einhorn LH. High-dose chemotherapy as inital salvage chemotherapy in patients with relapsed testicular cancer. J Clin Oncol 2000;18(19): EBM IIb Rosti G, Pico JL, Wandt H et al. High-dose chemotherapy (HDC) in the salvage treatment of patients failling first-line platinum chemotherapy for advanced germ cell tumours (GCT): first results of a prospective randomised trial of the European Group for Blood and Marrow Transplantation (EBMT): IT- 94 study. Proc Ann Soc Clin Oncol 2002;21:180a, abstract 716. EBM Ib Kondagunta GV, Bacik J, Donadio A, Bajorin D, Marion S, Sheinfeld J, Bosl GJ, Motzer RJ. Combination of paclitaxel, ifosfamide, and cisplatin is an effective second-line therapy for patients with relapsed testicular germ cell tumors. J Clin Oncol 2005;23(27): &ordinalpos=15&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 226. Mead GM, Cullen MH, Huddart R, Harper P, Rustin GJ, Cook PA, Stenning SP, Mason M; MRC Testicular Tumour Working Party. A phase II trial of TIP (paclitaxel, ifosfamide and cisplatin) given as second-line (post-peb) salvage chemotherapy for patients with metastatic germ cell cancer: a medical research council trial. Br J Cancer 2005;93(2): &ordinalpos1&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 227. Pico JL, Rosti G, Kramar A, Wandt H, Koza V, Salvioni R, Theodore C, Lelli G, Siegert W, Horwich A, Marangolo M, Linkesch W, Pizzocaro G, Schmoll HJ, Bouzy J, Droz JP, Biron P; Genito-Urinary Group of the French Federation of Cancer Centers (GETUG-FNCLCC), France; European Group for Blood and Marrow Transplantation (EBMT). A randomised trial of high-dose chemotherapy in the salvage treatment of patients failing first-line platinum chemotherapy for advanced germ cell tumours. Ann Oncol 2005;16(7): EBM Ib &ordinalpos=4&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 228. Lorch A, Kollmannsberger C, Hartmann JT, Metzner B, Schmidt-Wolf IG, Berdel WE, Weissinger F, Schleicher J, Egerer G, Haas A, Schirren R, Beyer J, Bokemeyer C, Rick O; German Testicular Cancer Study Group. Single versus sequential high-dose chemotherapy in patients with relapsed or refractory germ cell tumors: a prospective randomized multicenter trial of the German Testicular Cancer Study 65
66 Group. J Clin Oncol 2007;25(19): &ordinalpos=13&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 229. Motzer RJ, Mazumdar M, Sheinfeld J, Bajorin DF, Macapinlac HA, Bains M, Reich L, Flombaum C, Mariani T, Tong WP, Bosl GJ. Sequential dose-intensive paclitaxel, ifosfamide, carboplatin, and etoposide salvage therapy for germ cell tumor patients. J Clin Oncol 2000;18(6): EBM IIb &ordinalpos=24&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 230. Vaena DA, Abonour R, Einhorn LH. Long-term survival after high-dose salvage chemotherapy for germ cell malignancies with adverse prognostic variables. J Clin Oncol 2003;21(22): EBM III &ordinalpos=6&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 231. Reinhorn LH, Rajhavan D, Kindlen H. A phase I trial of gemcitabine plus paclitaxel combination therapy in patients with refractory advanced germ cell tumours. Proc ASCO 1999;18:207A (abstract 796). EBM IIa Motzer JR, Sheinfeld J, Mazumdar M, Bains M, Mariani T, Bacik J, Bajorin D, Bosl GJ. Paclitaxel, ifosfamide, and cisplatin second-line therapy for patients with relapsed testicular germ cell cancer. J Clin Oncol 2000;18(12): EBM IIb Bokemeyer C, Gerl A, Schoffski P, Harstrick A, Niederle N, Beyer J, Casper J, Schmoll HJ, Kanz L. Gemcitabine in patients with relapse or cisplatin refractory testicular cancer. J Clin Oncol 1999;17(2): EBM IIa George DW, Foster RS, Hromas RA, Robertson KA, Vance GH, Ulbright TM, Gobbett TA, Heiber DJ, Heerema NA, Ramsey HC, Thurston VC, Jung SH, Shen J, Finch DE, Kelley MR, Einhorn LH. Update on late relapse of germ cell tumor: a clinical and molecular analysis. J Clin Oncol 2003;21(1): EBM III &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 235. Lipphardt ME, Albers P. Late relapse of testicular cancer. World J Urol 2004;22(1): &ordinalpos=2&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 236. Tiffany P, Morse MJ, Bosl G, Vaughan ED Jr, Sogani PC, Herr HW, Whitmore WF Jr. Sequential excision of residual thoracic and retroperitoneal masses after chemotherapy for stage III germ cell tumours. Cancer 1986;57(5): EBM III Cassidy J, Lewis CR, Kaye SB, Kirk D. The changing role of surgery in metastatic non-seminomatous germcell tumour. Br J Cancer 1992;65(1): Coogan CL, Foster RS, Rowland RG, Bihrle R, Smith ER Jr, Einhorn LH, Roth BJ, Donohue JP. Postchemotherapy retroperitoneal lymph node dissection is effective therapy in selected patients with elevated tumour markers after primary chemotherapy alone. Urology 1997;50(6): EBM III Eastham JA, Wilson TG, Russell C, Ahlering TE, Skinner DG. Surgical resection in patients with nonseminomatous germ cell tumour who fail to normalize serum tumour markers after chemotherapy. Urology 1994;43(1): EBM III. 66
67 Gerl A, Clemm C, Schmeller N, Hentrich M, Lamerz R, Wilmanns W. Late relapse of germ cell tumours after cisplatin-based chemotherapy. Ann Oncol 1997;8(1): EBM III Kisbenedek L, Bodrogi I, Szeldeli P, Baki M, Tenke P, Horti J. Results of salvage retroperitoneal lymphadenectomy (RLA) in the treatment of patients with nonseminomatous germ cell tumours remaining marker positive after inductive chemotherapy. Int Urol Nephrol 1995;27(3): EBM III Murphy BR, Breeden ES, Donohue JP, Messemer J, Walsh W, Roth BJ, Einhorn LH. Surgical salvage of chemorefractory germ cell tumours. J Clin Oncol 1993;11(2): EBM III Nichols C. Treatment of recurrent germ cell tumours. Semin Surg Oncol 1999;17(4): Ravi R, Ong J, Oliver RT, Badenoch DF, Fowler CG, Hendry WF. Surgery as salvage therapy in chemotherapy-resistant nonseminomatous germ cell tumours. Br J Urol 1998;81(6): EBM III Albers P, Ganz A, Hanning E, Miersch WD, Muller SC. Salvage surgery of chemorefractory germ cell tumours with elevated tumour markers. J Urol, 2000;164(2): EBM III Fossa SD, Bokemeyer C, Gerl A, Culine S, Jones WG, Mead GM, Germa-Luch JR, Pont J, Schmoll HJ, Tjulandin S. Treatment outcome of patients with brain metastases from malignant germ cell tumours. Cancer 1999;85(4): EBM IIa Bokemeyer C, Nowak P, Haupt A et al. Treatment of brain metastases in patients with testicular cancer. J Clin Oncol 1997;15(4): EBM III. = Absract 248. Hartmann JT, Bamberg M, Albers P et al. Multidiciplinary treatment and prognosis of patients with central nervous metastases (CNS) from testicular germ cell tumour (GCT) origin. Proc Ann Soc Clin ncol 2003;22:400, abstract EBM III Edelman MJ, Meyers FJ, Siegel D. The utility of follow-up testing after curative cancer therapy. J Gen Intern Med 1997;12(5): Rathmell AJ, Brand IR, Carey BM, Jones WG. Early detection of relapse after treatment for metastatic germ cell tumour of the testis: an exercise in medical audit. Clin Oncol (R Coll Radiol) 1993;5(1): EBM III Gietema JA, Meinardi MT, Sleifer DT, Hoekstra HJ, van der Graaf WT. Routine chest X-rays have no additional value in the detection of relapse during routine follow-up of patients treated with chemotherapy for disseminated non-seminomatous testicular cancer. Ann Oncol 2002;13(10): EBM III Pont J, Albrecht W, Postner G, Sellner F, Angel K, Holtl W. Adjuvant chemotherapy for high risk clinical stage I nonseminomatous testicular germ cell cancer: long-term results of a prospective trial. J Clin Oncol 1996;14(2): EBM IIa. &itool=iconabstr 67
68 253. Bohlen D, Borner M, Sonntag RW, Fey MF, Studer UE. Long-term results following adjuvant chemotherapy in patients with clinical stage I testicular nonseminomatous malignant germ cell tumours with high risk factors. J Urol 1999;161(4): EBM III. &itool=iconabstr 254. Tjan-Heijnen VCG, Oosterhof GON, de Wit R, de Mulder PHM. Treatment of germ cell tumours: state of the art. Eur J Surg Oncol 1997;23(2): Lowe BA. Surveillance versus nerve-sparing retroperitoneal lymphadenectomy in stage I germ cell tumours. Urol Clin North Am 1993;20(1): EBM IIb Gels ME, Hoekstra HJ, Sleijfer DT, Marrink J, de Bruijn HW, Molenaar WM, Freling NJ, Droste JH, Schraffordt Koops H. Detection of recurrence in patients with clinical stage I nonseminomatous testicular germ cell tumours and consequences for further follow-up: a single-center 10-year experience. J Clin Oncol 1995;13(5): EBM III McLeod DG, Weiss RB, Stablein DM, Muggia FM, Paulson DF, Ellis JH, Spaulding JT, Donohue JP. Staging relationships and outcome in early stage testicular cancer: a report from the Testicular Cancer Intergroup Study. J Urol 1991;145(6): EBM IIa Donohue JP, Thornhill JA, Foster RS, Rowland RG, Bihrle R. Primary retroperitoneal lymph node dissection in clinical stage A non-seminomatous germ cell testis cancer: review of the Indiana University Experience Br J Urol 1993;71(3): EBM III Schmoll HJ, Weissbach L. [Diagnostik und Therapie von Hodentumouren.] Interdisziplinäre Konsensus-Konferenz, Halle (Saale), [German] EBM IIa, IIb, III. [Diagnosis and therapy for germcell tumours] 260. McCaffrey JA, Bajorin DF, Motzer RJ. Risk assessment for metastatic testis cancer. Urol Clin North Am 1998;25(3): Buchholz TA, Walden TL, Prestidge BR. Cost-effectiveness of post-treatment surveillance after radiation therapy for early stage seminoma. Cancer 1998;82(6): EBM III Tana S, Cerrotta A, Gardani G, Palazzi M, Pizzocaro G. Post surgical policy in stage I testicular seminoma: cost and benefit of prophylactic irradiation in a long-term experience. Tumouri 997;83(6): EBM III Sultanem K, Souhami L, Benk V, Bahary JP, Roman T, Shenouda G, Freeman C. Para-aortic irradiation only appears to be adequate treatment for patients with stage I seminoma of the testis. Int J Radiat Oncol Biol Phys 1998;40(2): EBM III Kiricuta IC, Sauer J, Bohndorf W. Omission of the pelvic irradiation in stage I testicular seminoma: a study of postorchidectomy paraaortic radiotherapy. Int J Radiat Oncol Biol Phys 1996;35(2): EBM IIb Warde P, Gospodarowicz MK, Panzarella T, Catton CN, Sturgeon JF, Moore M, Goodman P, Jewett MA. Stage I testicular seminoma: results of adjuvant irradiation and surveillance. J Clin Oncol 1995;13(9): EBM III. 68
69 Fossa SD, Aass N, Kaalhus O. Radiotherapy for testicular seminoma stage I: treatment results and longterm post-irradiation morbidity in 365 patients. Int J Radiat Oncol Biol Phys 1989;16(2): EBM III. =Abstract 267. Baniel J, Foster RS, Einhorn LH, Donohue JP. Late relapse of clinical stage I testicular cancer. J Urol 1995;154(4): EBM III Stein ME, Leviov M, Drumea K, Moshkovitz B, Nativ O, Milstein D, Sabo E, Kuten A. Radiationinduced tumours in irradiated stage I testicular seminoma: results of a 25-year follow-up ( ). J Surg Oncol 1998;67(1): EBM III Akimoto T, Takahashi I, Takahashi M, Yamakawa M, Hayakawa K, Mitsuhashi N, Niibe H. Long-term outcome of postorchidectomy radiation therapy for stage I and II testicular seminoma. Anticancer Res 1997;17(5B): EBM III Von der Maase H, Specht L, Jacobsen GK, Jakobsen A, Madsen EL, Pedersen M, Rorth M, Schultz H. Surveillance following orchidectomy for stage I seminoma of the testis. Eur J Cancer 1993;29A(14): EBM III Horwich A, Alsanjari N, A Hern, Nicholls J, Dearnaley DP, Fisher C. Surveillance following orchidectomy for stage I testicular seminoma. Br J Cancer 1992;65(5): EBM III Germá Lluch JR, Climent MA, Villavicencio H, Gomez de Segura G, Blanco R, Mercedes A, de Andres L, Sole Balcells FJ. Treatment of stage I testicular tumours. Br J Urol 1993;71(4): EBM III Warde P, Gospodarowicz MK, Goodman PJ, Sturgeon JF, Jewett MA, Catton CN, Richmond H, Thomas GM, Duncan W, Munro AJ. Results of a policy of surveillance in stage I testicular seminoma. Int J Radiat Oncol Biol Phys 1993;27(1): EBM III Allhoff EP, Liedke S, de Riese W, Stief C, Schneider B. Stage I seminoma of the testis: adjuvant radiotherapy or surveillance? Br J Urol 1991;68(2): EBM IIb Fosså SD, Chen J, Schonfeld SJ, McGlynn KA, McMaster ML, Gail MH, Travis LB. Risk of contralateral testicular cancer: a population-based study of 29,515 U.S. men. J Natl Cancer Inst 2005;97(14): EBM III &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 276. Wierecky J, Kollmannsberger C, Boehlke I, Kuczyk M, Schleicher J, Schleucher N, Metzner B, Kanz L, Hartmann JT, Bokemeyer C. Secondary leukemia after first-line high-dose chemotherapy for patients with advanced germ cell cancer. J Cancer Res Clin Oncol 2005;131(4): EBM III &ordinalpos=4&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 277. Nuver J, Smit AJ, Sleijfer DT, van Gessel AI, van Roon AM, van der Meer J, van den Berg MP, Hoekstra HJ, Sluiter WJ, Gietema JA. Left ventricular and cardiac autonomic function in survivors of testicular cancer. Eur J Clin Invest 2005;35(2): EBM III. 69
70 &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 278. Huddart RA, Norman A, Shahidi M, Horwich A, Coward D, Nicholls J, Dearnaley DP. Cardiovascular disease as a long-term complication of treatment for testicular cancer. J Clin Oncol 2003;21(8): EBM III &ordinalpos=10&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSu m 279. van den Belt-Dusebout AW, Nuver J, de Wit R, Gietema JA, ten Bokkel Huinink WW, Rodrigus PT, Schimmel EC, Aleman BM, van Leeuwen FE. Long-term risk of cardiovascular disease in 5-year survivors of testicular cancer. J Clin Oncol 2006;24(3): EBM III &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 280. Haugnes HS, Aass N, Fosså SD, Dahl O, Klepp O, Wist EA, Svartberg J, Wilsgaard T, Bremnes RM. Components of the metabolic syndrome in long-term survivors of testicular cancer. Ann Oncol 2007;18(2): EBM III &ordinalpos=2&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 281. Huddart RA, Joffe JK. Preferred treatment for stage I seminoma: a survey of Canadian radiation oncologists. Clin Oncol (R Coll Radiol) 2006;18(9): &ordinalpos=3&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_RVDocSum 282. Kre ge S, Kalund G, Otto T, Goepel M, Rubben H. Phase II study: adjuvant single-agent carboplatin therapy for clinical stage I seminoma. Eur Urol 1997;31(4): EBM IIb Dieckmann KP, Krain J, Kuster J, Bruggeboes B. Adjuvant carboplatin treatment for seminoma clinical stage I. J Cancer Res Clin Oncol 1996;122(1): EBM IIb Bukowski RM. Management of advanced and extragonadal germ-cell tumours. Urol Clin North Am 1993;20(1): Fair W, Dalbagni G, Machele Donat S, Theodorescu D. Evaluation and follow-up of patients with urologic cancer. AUA Office of Education Publications 9958 PG, Pizzocaro G. Non-seminomatous germ-cell tumours (NSGCT) of the testis: diagnosis and management, stage by stage. Eur Urol Update Series 1997;6: Sheinfeld J, Bajorin DF, Solomon M. Management of postchemotherapy residual masses in advanced germ cell tumours. Urol Clin North Am 1997;3: Little JS, Foster RS, Ulbright TM, Donohue JP. Unusual neoplasms detected in testis cancer patients undergoing postchemotherapy retroperitoneal lymphadenectomy. J Urol 1994;152(4): EBM III. 70
71 11.1. Germ hücresi dışı tümörler 1. Cheville JC, Sebo TJ, Lager DJ, Bostwick DG, Farrow GM. Leydig cell tumour of the testis: a clinicopathologic, DNA content, and MIB-1 comparison of nonmetastasizing and metastasizing tumours. Am J Surg Pathol 1998;22(11): EBM IIA Kim I, Young RH, Scully RE. Leydig cell tumours of the testis. A clinicopathological analysis of 40 cases and review of the literature. Am J Surg Pathol 1985;9(3): EBM III. Pubmed_ResultsPanel.Pubmed_RVDocSum 3. Matveev BP, Gurarii LL. [Leydig-cell tumours of the testis.] Urol Nefrol (Mosk) 1997;(4): [Russian] EBM III Young RH, Koelliker DD, Scully RE. Sertoli cell tumours of the testis, not otherwise specified: a clinicopathologic analysis of 60 cases. Am J Surg Pathol 1998;22(6): EMB III Proppe KH, Scully RE. Large-cell calcifying Sertoli cell tumour of the testis. Am J Clin Pathol 1980;74(5): EMB III Zukerberg LR, Young RH, Scully RE. Sclerosing Sertoli cell tumour of the testis. A report of 10 cases. Am J Surg Pathol 1991;15(9): EMB III WHO histological classification of testis tumours. In: Eble JN, Sauter G, Epstein JI, Sesterhenn IA, eds. Pathology & Genetics. Tumours of the urinary system and male genital organs. Lyon: IARC Press, 2004: 218, EBM III. 8. Ulbright TM, Amin MB, Young RH. Tumours of the testis, adnexia, spermatic cord and scrotum. AFIP EBM III. 9. Cheville JC, Sebo TJ, Lager DJ, Bostwick DG, Farrow GM. Leydig cell tumour of the testis: a clinicopathologic, DNA content, and MIB-1 comparison of non-metastasizing and metastasizing tumours. Am J Surg Pathol 1998;22(11): EBM III McCluggage WG, Shanks JH, Arthur K, Banerjee SS. Cellular proliferation and nuclear ploidy assessments augment established prognostic factors in predicting malignancy in testicular Leydig cell tumours. Histopathology 1998;33(4): EBM III Mineur P, de Cooman S, Hustin J, Verhoeven G, de Hertogh E. Feminizing testicular Leydig cell tumour: hormonal profile before and after unilateral orchidectomy. J Clin Endocrinol Metab 1987;64(4): EBM IIB. = Reznik Y, Rieu M, Kuhn JM, Mandard JC, Bottet P, Lemonnier D, Bekka S, Mahoudeau J. Luteinizing hormone regulation by sex steroids in men with germinal and Leydig cell tumours. Clin Endocrinol (Oxf) 1993;38(5): EBM IIB Bercovici JP, Nahoul K, Tater D, Charles JF, Scholler R. Hormonal profile of Leydig cell tumours with gynecomastia. J Clin Endocrinol Metab 1984;59(4): EBM III Haas GP, Pittaluga S, Gomella L, Travis WD, Sherins RJ, Doppman JL, Linehan WL, Robertson C. Clinical occult Leydig cell tumour presenting with gynecomastia. J Urol 1989;142(5): EBM III. = Ruthgers JL, Young RH, Scully RE. The testicular tumour of the adrenogenital syndrome. A report of six cases and review of the literature on testicular masses in patients with adrenocortical disorders. Am J Surg Pathol 1988;12(7): EBM III. 71
72 Maizlin ZV, Belenky A, Kunichezky M, Sandbank J, Strauss S. Leydig cell tumours of the testis: gray scale and color Doppler sonographic appearance. J Ultrasound Med 2004;23(7): EBM III Ponce de Leon Roca J, Algaba Arrea F, Bassas Arnau L, Villavicencio Mavrich H. [Leydig-cell tumours of the testis.] Arch Esp Urol 2000;53(6): [Spanish] EBM III Wegner HE, Dieckmann KP, Herbst H, Andresen R, Miller K. Leydig cell tumour comparison of results of radical and testis sparing surgery in a single center. Urol Int 1997;59(3): EBM IIB Mosharafa AA, Foster RS, Bihrle R, Koch MO, Ulbright TM, Einhorn LH, Donohue JP. Does retroperitoneal lymph node dissection have a curative role for patients with sex cord-stromal testicular tumours? Cancer 2003;98(4): EBM III Giglio M, Medica M, De Rose AF, Germinale F, Ravetti JL, Carmignani G. Testicular Sertoli cell tumours and relative sub-types. Analysis of clinical and prognostic features. Urol Int 2003;70(3): Review. EBM III. = Plata C, Algaba F, Andujar M, Nistal M, Stocks P, Martinez JL, Nogales FF. Large cell calcifying Sertoli cell tumour of the testis. Histopathology 1995;26(3): EBM III Anderson GA. Sclerosing Sertoli cell tumour of the testis: a distinct histological subtype. J Urol 1995;154(5): Review. EBM III Jacobsen GK. Malignant Sertoli cell tumours of the testis. J Urol Pathol 1993;1: EBM III. 24. Kratzer SS, Ulbright TM, Talerman A, Srigley JR, Roth LM, Wahle GR, Moussa M, Stephens JK, Millos A, Young RH. Large cell calcifying Sertoli cell tumour of the testis: contrasting features of six malignant and six benign tumours and a review of the literature. Am J Surg Pathol 1997;21(11): EBM III Henley JD, Young RH, Ulbright TM. Malignant Sertoli cell tumours of the testis: a study of 13 examples of a neoplasm frequently misinterpreted as seminoma. Am J Surg Pathol 2002;26: EBM III. 26. Grabrilove JL, Freiberg EK, Leiter E, Nicolis GL. Feminizing and non-feminizing Sertoli cell tumour. J Urol 1980;124(6): Gierke CL, King BF, Bostwick DG, Choyke PL, Hattery RR. Large-cell calcifying Sertoli cell tumour of the testis: appearance at sonography. AJR Am J Roentgenol 1994;163(2): EBM III Chang B, Borer JG, Tan PE, Diamond DA. Large-cell calcifying Sertoli cell tumour of the testis: case report and review of the literature. Urology 1998;52(3): EBM III Washecka R, Dresner MI, Honda SA. Testicular tumours in Carney s complex. J Urol 2002;167(3): EBM III Young S, Gooneratne S, Straus FH, Zeller WP, Bulun SE, Rosenthal IM. Feminizing Sertoli cell tumours in boys with Peutz-Jeghers syndrome. Am J Surg Pathol 1995;19(1): EBM III Kaplan GW, Cromie WJ, Kelalis PP, Silber I, Tank ES Jr. Gonadal stromal tumours: a report of the prepuberal testicular tumours registry. J Urol 1986;136(1 Pt 2): EBM III
73 32. Al-Bozom IA, El-Faqih SR, Hassan SH, El-Tiraifi AE, Talic RF. Granulosa cell tumour of the adult type. A case report and review of the literature of a very rare testicular tumour. Arch Pathol Lab Med 2000;124(10): EBM III Perito PE, Ciancio G, Civantos F, Politano VA. Sertoli-Leydig cell testicular tumour. case report and review of sex cord/gonadal stromal tumour histogenesis. J Urol 1992;148(3): EBM III Scully RE. Gonadoblastoma. A review of 74 cases. Cancer 1970;25(6): EBM III Ulbright TM, Srigley JR, Reuter VE, Wojno K, Roth LM, Young RH. Sex-cord-stromal tumours of the testis with entrapped germ cells: a lesion mimicking unclassified mixed germ cell sex cord-stromal tumours. Am J Surg Pathol 2000;24(4): EBM III
5. SINIF DERS NOTLARI TESTİS TÜMÖRLERİ. Doç. Dr. Yaşar BOZKURT
 Epidemiyoloji: 5. SINIF DERS NOTLARI TESTİS TÜMÖRLERİ Doç. Dr. Yaşar BOZKURT Testis tümörleri 100.000 erkekte 6-11 oranında görülen genç erişkin erkeklerde en sık görülen kanserdir. Büyük çoğunluğu ( %96)
Epidemiyoloji: 5. SINIF DERS NOTLARI TESTİS TÜMÖRLERİ Doç. Dr. Yaşar BOZKURT Testis tümörleri 100.000 erkekte 6-11 oranında görülen genç erişkin erkeklerde en sık görülen kanserdir. Büyük çoğunluğu ( %96)
DOÇ.DR.YAŞAR BOZKURT
 DOÇ.DR.YAŞAR BOZKURT Epidemiyoloji: Testis tümörleri 100.000 erkekte 6-11 oranında görülen ve genç erişkin erkeklerde en sık görülen kanserdir. Büyük çoğunluğu ( %96) germ hücre tümörleridir. İlk tanı
DOÇ.DR.YAŞAR BOZKURT Epidemiyoloji: Testis tümörleri 100.000 erkekte 6-11 oranında görülen ve genç erişkin erkeklerde en sık görülen kanserdir. Büyük çoğunluğu ( %96) germ hücre tümörleridir. İlk tanı
EVRE I SEMİNOM DIŞI TÜMÖRLERE YAKLAŞIM
 EVRE I SEMİNOM DIŞI TÜMÖRLERE YAKLAŞIM Dr. Ahmet BİLİCİ İstanbul Medipol Üniversitesi, Tıp Fakültesi Tıbbi Onkoloji B.D. 16.12.2018 Giriş Testis tümörlerinin %30 unu oluşturur %70 i erken evre olarak tanı
EVRE I SEMİNOM DIŞI TÜMÖRLERE YAKLAŞIM Dr. Ahmet BİLİCİ İstanbul Medipol Üniversitesi, Tıp Fakültesi Tıbbi Onkoloji B.D. 16.12.2018 Giriş Testis tümörlerinin %30 unu oluşturur %70 i erken evre olarak tanı
Evre I Seminom Dışı Testis Tümörlerinde (NSGHT) Tedavi
 Evre I Seminom Dışı Testis Tümörlerinde (NSGHT) Tedavi Prof. Dr. Abdurrahman IŞIKDOĞAN Dicle Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı III. Tıbbi Onkoloji Kongresi / 25 Mart 2010 / ANTALYA Testisin
Evre I Seminom Dışı Testis Tümörlerinde (NSGHT) Tedavi Prof. Dr. Abdurrahman IŞIKDOĞAN Dicle Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı III. Tıbbi Onkoloji Kongresi / 25 Mart 2010 / ANTALYA Testisin
Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi
 Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Testis tümörleri Erkeklerdeki kanserlerin %1 i Yıllık %3-6 artış Avrupa da her yıl 24.000 yeni vak a Testis Tümör Epidemiyolojisi İnsidans dünya genelinde
Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Testis tümörleri Erkeklerdeki kanserlerin %1 i Yıllık %3-6 artış Avrupa da her yıl 24.000 yeni vak a Testis Tümör Epidemiyolojisi İnsidans dünya genelinde
GERM HÜCRELİ TÜMÖRLER İnteraktif Olgu Sunumu Dr BENGÜ DEMİRAĞ
 GERM HÜCRELİ TÜMÖRLER İnteraktif Olgu Sunumu Dr BENGÜ DEMİRAĞ Haziran 1999 erkek Başvuru Ekim 2014 2 aydır sağ testiste şişlik. Bitlis. Karın ağrısı ve şişlik ile Ankara ya sevk. Ankara da Üroloji AD da
GERM HÜCRELİ TÜMÖRLER İnteraktif Olgu Sunumu Dr BENGÜ DEMİRAĞ Haziran 1999 erkek Başvuru Ekim 2014 2 aydır sağ testiste şişlik. Bitlis. Karın ağrısı ve şişlik ile Ankara ya sevk. Ankara da Üroloji AD da
TESTİS TÜMÖRLERİ. Dr. Tahsin Turunç. Başkent Üniversitesi Tıp Fakültesi Üroloji AD Adana Uygulama ve Araştırma Merkezi
 TESTİS TÜMÖRLERİ Dr. Tahsin Turunç Başkent Üniversitesi Tıp Fakültesi Üroloji AD Adana Uygulama ve Araştırma Merkezi EPİDEMİYOLOJİ Erkeklerde tüm kanserlerin %1 i %2-3 bilateral Genç erişkinlerde en sık
TESTİS TÜMÖRLERİ Dr. Tahsin Turunç Başkent Üniversitesi Tıp Fakültesi Üroloji AD Adana Uygulama ve Araştırma Merkezi EPİDEMİYOLOJİ Erkeklerde tüm kanserlerin %1 i %2-3 bilateral Genç erişkinlerde en sık
SEMİNOM-DIŞI TESTİS TÜMÖRLERİNİN TEDAVİSİNDE RADYOTERAPİ. Doç. Dr. Mert Saynak
 SEMİNOM-DIŞI TESTİS TÜMÖRLERİNİN TEDAVİSİNDE RADYOTERAPİ Doç. Dr. Mert Saynak Clinical Radiation Oncology, Third Edition OLGU 30 yaşında bir hentbol oyuncusu, Migren tanısı var Son maçı esnasında
SEMİNOM-DIŞI TESTİS TÜMÖRLERİNİN TEDAVİSİNDE RADYOTERAPİ Doç. Dr. Mert Saynak Clinical Radiation Oncology, Third Edition OLGU 30 yaşında bir hentbol oyuncusu, Migren tanısı var Son maçı esnasında
Testis Germ Hücreli Kanser. Prof.Dr.Necdet Üskent
 Testis Germ Hücreli Kanser Primer Tedavi Standartları ve Prensipleri Prof.Dr.Necdet Üskent Artan İnsidans, Azalan Mortalite İnsidans Erkek Malinitelerinin %1 Görülme Oranı/100.000 Mortalite 15-35 yaş aralığı
Testis Germ Hücreli Kanser Primer Tedavi Standartları ve Prensipleri Prof.Dr.Necdet Üskent Artan İnsidans, Azalan Mortalite İnsidans Erkek Malinitelerinin %1 Görülme Oranı/100.000 Mortalite 15-35 yaş aralığı
Prof. Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi
 Prof. Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Seminom GHTT in %60 ı Seminom dur Ayrıca %10 kadar da mix tümörler içinde yer alırlar Tanı anında %75-80 i Evre I Diğer türlere göre daha iyi prognozlu
Prof. Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Seminom GHTT in %60 ı Seminom dur Ayrıca %10 kadar da mix tümörler içinde yer alırlar Tanı anında %75-80 i Evre I Diğer türlere göre daha iyi prognozlu
Nonseminamatöz Germ Hücreli Testis Tümörlerinde Güncel Tedaviler. Dr. Işıl Somalı DEÜ Onkoloji Enstitüsü UKK 2013
 Nonseminamatöz Germ Hücreli Testis Tümörlerinde Güncel Tedaviler Dr. Işıl Somalı DEÜ Onkoloji Enstitüsü UKK 2013 2007 yılı, 29 yaşında VAKA Sol testis tm nedeniyle, sol inguinal orşiektomi (Kasım 2007)
Nonseminamatöz Germ Hücreli Testis Tümörlerinde Güncel Tedaviler Dr. Işıl Somalı DEÜ Onkoloji Enstitüsü UKK 2013 2007 yılı, 29 yaşında VAKA Sol testis tm nedeniyle, sol inguinal orşiektomi (Kasım 2007)
TESTİS KANSERİ.
 TESTİS KANSERİ www.uroonkoloji.org ÜROONKOLOJİ DERNEĞİ TESTİS TÜMÖRLERİ Testis tümörleri nadir görülmekle birlikte, 15-35 yaş arası erkeklerde en sık görülen malign tümördür. Erkekteki tüm malign tümörlerin
TESTİS KANSERİ www.uroonkoloji.org ÜROONKOLOJİ DERNEĞİ TESTİS TÜMÖRLERİ Testis tümörleri nadir görülmekle birlikte, 15-35 yaş arası erkeklerde en sık görülen malign tümördür. Erkekteki tüm malign tümörlerin
DİFERANSİYE TİROİD KANSERİ
 DİFERANSİYE TİROİD KANSERİ RİSK GRUPLARINA GÖRE TEDAVİ-TAKİP Dr.Nuri ÇAKIR Gazi Ü Tıp Fak Endokrinoloji ve Metabolizma B.D 35.Türkiye Endokrinoloji ve Metabolizma HastalıklarıKongresi 15-19 Mayıs 2013-Antalya
DİFERANSİYE TİROİD KANSERİ RİSK GRUPLARINA GÖRE TEDAVİ-TAKİP Dr.Nuri ÇAKIR Gazi Ü Tıp Fak Endokrinoloji ve Metabolizma B.D 35.Türkiye Endokrinoloji ve Metabolizma HastalıklarıKongresi 15-19 Mayıs 2013-Antalya
Lokal İleri Evre Küçük Hücreli Dışı Akciğer Kanseri Tedavisi
 Lokal İleri Evre Küçük Hücreli Dışı Akciğer Kanseri Tedavisi Lokal ileri evre akciğer kanserli olgularda cerrahi tedavi, akciğer rezeksiyonu ile birlikte invaze olduğu organ ve dokuların rezeksiyonunu
Lokal İleri Evre Küçük Hücreli Dışı Akciğer Kanseri Tedavisi Lokal ileri evre akciğer kanserli olgularda cerrahi tedavi, akciğer rezeksiyonu ile birlikte invaze olduğu organ ve dokuların rezeksiyonunu
Hodgkin lenfoma tedavisinde Radyoterapinin Rolü. Dr. Görkem Aksu Kocaeli Tıp Fakültesi Radyasyon Onkolojisi AD
 Hodgkin lenfoma tedavisinde Radyoterapinin Rolü Dr. Görkem Aksu Kocaeli Tıp Fakültesi Radyasyon Onkolojisi AD 15-30 yaş arası ve > 55 yaş olmak üzere iki dönemde sıklık artışı (+) Erkek ve kadınlarda en
Hodgkin lenfoma tedavisinde Radyoterapinin Rolü Dr. Görkem Aksu Kocaeli Tıp Fakültesi Radyasyon Onkolojisi AD 15-30 yaş arası ve > 55 yaş olmak üzere iki dönemde sıklık artışı (+) Erkek ve kadınlarda en
Tanı: Metastatik hastalık için patognomonik bir radyolojik. Tek veya muitipl nodüller iyi sınırlı veya difüz. Göğüs Cerrahisi Hasan Çaylak
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
Kemoterapi sonrası artık kitlelerin tedavisi. Dr. Haluk Özen, Hacettepe Universitesi
 Kemoterapi sonrası artık kitlelerin tedavisi Dr. Haluk Özen, Hacettepe Universitesi Testis Tümörleri: Tedavi edilebilen kanser modeli DüĢük evre Kür oranı %100 e yakındır Ġleri evre %85-90 uzun süreli
Kemoterapi sonrası artık kitlelerin tedavisi Dr. Haluk Özen, Hacettepe Universitesi Testis Tümörleri: Tedavi edilebilen kanser modeli DüĢük evre Kür oranı %100 e yakındır Ġleri evre %85-90 uzun süreli
ERKEN EVRE SEMİNOM OLGUSU
 ERKEN EVRE SEMİNOM OLGUSU Dr. Mustafa ERMAN Hacettepe Kanser Enstitüsü İzmir, Kasım 2014 36 y, E Aralık 2009 da sol orşiektomi Markerlar ve CT normal Patoloji: Klasik seminom, tm 2,5 cm. Tm testis içine
ERKEN EVRE SEMİNOM OLGUSU Dr. Mustafa ERMAN Hacettepe Kanser Enstitüsü İzmir, Kasım 2014 36 y, E Aralık 2009 da sol orşiektomi Markerlar ve CT normal Patoloji: Klasik seminom, tm 2,5 cm. Tm testis içine
ALFA FETOPROTEİN (TÜMÖR BELİRLEYİCİSİ)
 ALFA FETOPROTEİN (TÜMÖR BELİRLEYİCİSİ) Diğer adı ve kısaltma: α fetoprotein, AFP. Kullanım amacı: Primer karaciğer, testis ve over kanserlerinin araştırılması ve tedaviye alınan cevabın izlenmesi amacıyla
ALFA FETOPROTEİN (TÜMÖR BELİRLEYİCİSİ) Diğer adı ve kısaltma: α fetoprotein, AFP. Kullanım amacı: Primer karaciğer, testis ve over kanserlerinin araştırılması ve tedaviye alınan cevabın izlenmesi amacıyla
İnsidental kanser. Dr. Ali İlker Filiz Haydarpaşa Sultan Abdülhamid Eğitim ve Araştırma Hastanesi Genel Cerrahi Kliniği
 İnsidental kanser Dr. Ali İlker Filiz Haydarpaşa Sultan Abdülhamid Eğitim ve Araştırma Hastanesi Genel Cerrahi Kliniği Tanım Preoperatif tanı yöntemleriyle saptanamayan, ancak benign hastalıklar nedeniyle
İnsidental kanser Dr. Ali İlker Filiz Haydarpaşa Sultan Abdülhamid Eğitim ve Araştırma Hastanesi Genel Cerrahi Kliniği Tanım Preoperatif tanı yöntemleriyle saptanamayan, ancak benign hastalıklar nedeniyle
Kökten Tedavi Sonrası PSA Nüksü. Dr. M. Gökhan Toktaş İstanbul Eğitim ve Arş. Hastanesi Üroloji Kliniği
 Kökten Tedavi Sonrası PSA Nüksü Dr. M. Gökhan Toktaş İstanbul Eğitim ve Arş. Hastanesi Üroloji Kliniği Epidemiyoloji Kökten tedavi sonrası 1/3 hastada PSA nüksü olur ABD de yılda yeni 200.000 PCa var Bunların
Kökten Tedavi Sonrası PSA Nüksü Dr. M. Gökhan Toktaş İstanbul Eğitim ve Arş. Hastanesi Üroloji Kliniği Epidemiyoloji Kökten tedavi sonrası 1/3 hastada PSA nüksü olur ABD de yılda yeni 200.000 PCa var Bunların
Ulusal Akciğer Kanseri Kongresi İleri Evre Küçük Hücreli Dışı Akciğer Kanserlerinde Neoadjuvan Tedavi Sonrası Pulmoner Rezeksiyon Sonuçlarımız
 Ulusal Akciğer Kanseri Kongresi İleri Evre Küçük Hücreli Dışı Akciğer Kanserlerinde Neoadjuvan Tedavi Sonrası Pulmoner Rezeksiyon Sonuçlarımız Dr.Levent Alpay Süreyyapaşa Egitim vearaştırma Hastanesi Mart
Ulusal Akciğer Kanseri Kongresi İleri Evre Küçük Hücreli Dışı Akciğer Kanserlerinde Neoadjuvan Tedavi Sonrası Pulmoner Rezeksiyon Sonuçlarımız Dr.Levent Alpay Süreyyapaşa Egitim vearaştırma Hastanesi Mart
AKCİĞER KANSERİ TANISI KONULDUKTAN SONRA NE YAPILIR HASTA NASIL TAKİP VE İDARE EDİLİR
 AKCİĞER KANSERİ TANISI KONULDUKTAN SONRA NE YAPILIR HASTA NASIL TAKİP VE İDARE EDİLİR Akciğer kanseri olmak her şeyin sonu değildir. Bu hastalığı yenmek için mutlaka azimli, inançlı ve sabırlı olmanız
AKCİĞER KANSERİ TANISI KONULDUKTAN SONRA NE YAPILIR HASTA NASIL TAKİP VE İDARE EDİLİR Akciğer kanseri olmak her şeyin sonu değildir. Bu hastalığı yenmek için mutlaka azimli, inançlı ve sabırlı olmanız
Cerrahi Dışı Tedaviler
 KÖTÜ HUYLU YUMUŞAK DOKU TÜMÖRLERİ Cerrahi Dışı Tedaviler Dr.Selami ÇAKMAK GATA Haydarpaşa Eğitim Hastanesi 50 den fazla yumuşak doku sarkomu tipi Kaynaklandığı doku, Klinik gidişat, Görülme yaşı, Agresifliği,
KÖTÜ HUYLU YUMUŞAK DOKU TÜMÖRLERİ Cerrahi Dışı Tedaviler Dr.Selami ÇAKMAK GATA Haydarpaşa Eğitim Hastanesi 50 den fazla yumuşak doku sarkomu tipi Kaynaklandığı doku, Klinik gidişat, Görülme yaşı, Agresifliği,
İNVAZİF MESANE KANSERİNDE ORGAN KORUYUCU TEDAVİLER METASTATİK MESANE KANSERİNİN TEDAVİSİ
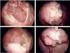 İNVAZİF MESANE KANSERİNDE ORGAN KORUYUCU TEDAVİLER METASTATİK MESANE KANSERİNİN TEDAVİSİ Dr.Cavit Can Eskişehir Osmangazi Ün. Tıp Fak. Üroloji AD Organ Koruyucu Tedaviler Transüretral rezeksiyon Parsiyel
İNVAZİF MESANE KANSERİNDE ORGAN KORUYUCU TEDAVİLER METASTATİK MESANE KANSERİNİN TEDAVİSİ Dr.Cavit Can Eskişehir Osmangazi Ün. Tıp Fak. Üroloji AD Organ Koruyucu Tedaviler Transüretral rezeksiyon Parsiyel
2016 by American Society of Clinical Oncology. Amerikan Klinik Onkoloji Cemiyeti (ASCO) İnvaziv Servikal Kanser Yönetimi
 2016 by American Society of Clinical Oncology Amerikan Klinik Onkoloji Cemiyeti (ASCO) İnvaziv Servikal Kanser Yönetimi Servikal kanserin tedavisi hastalığın evresine göre belirlenmektedir. Tedavi konizasyon,,
2016 by American Society of Clinical Oncology Amerikan Klinik Onkoloji Cemiyeti (ASCO) İnvaziv Servikal Kanser Yönetimi Servikal kanserin tedavisi hastalığın evresine göre belirlenmektedir. Tedavi konizasyon,,
LOKAL ILERI REKTUM TÜMÖRLERINDE
 LOKAL ILERI REKTUM TÜMÖRLERINDE NEOADJUVAN KıSA DÖNEM VE UZUN DÖNEM KEMORADYOTERAPI SONRASı HAYAT KALITESI DEĞERLENDIRILMESI SORUMLU ARAŞTIRMACI: Prof.Dr.ESRA SAĞLAM YARDIMCI ARAŞTIRMACI: Dr. ŞÜKRAN ŞENYÜREK
LOKAL ILERI REKTUM TÜMÖRLERINDE NEOADJUVAN KıSA DÖNEM VE UZUN DÖNEM KEMORADYOTERAPI SONRASı HAYAT KALITESI DEĞERLENDIRILMESI SORUMLU ARAŞTIRMACI: Prof.Dr.ESRA SAĞLAM YARDIMCI ARAŞTIRMACI: Dr. ŞÜKRAN ŞENYÜREK
Osteosarkom Tedavisinde Neoadjuvan Tedavi. Dr. Bülent Yalçın 5. Türk Tıbbi Onkoloji Kongresi, Mart 2014 Susesi Otel, Antalya
 Osteosarkom Tedavisinde Neoadjuvan Tedavi Dr. Bülent Yalçın 5. Türk Tıbbi Onkoloji Kongresi, 19-23 Mart 2014 Susesi Otel, Antalya Osteosarkoma-1 Nadir tümörler (2-3/100.000), Çalışma yapmak zor (çok merkezli,
Osteosarkom Tedavisinde Neoadjuvan Tedavi Dr. Bülent Yalçın 5. Türk Tıbbi Onkoloji Kongresi, 19-23 Mart 2014 Susesi Otel, Antalya Osteosarkoma-1 Nadir tümörler (2-3/100.000), Çalışma yapmak zor (çok merkezli,
XVII. ULUSAL KANSER KONGRESİ
 XVII. ULUSAL KANSER KONGRESİ İnteraktif Olgu Sunumu KEMİK TÜMÖRLERİ . 17 yaşında bayan hasta. 2.5 yıldır sol bacakda yürürken ağrı Enfeksiyon ve dolaşım bozukluğu tedavisi uygulanmış. Son 6 aydır ağrı
XVII. ULUSAL KANSER KONGRESİ İnteraktif Olgu Sunumu KEMİK TÜMÖRLERİ . 17 yaşında bayan hasta. 2.5 yıldır sol bacakda yürürken ağrı Enfeksiyon ve dolaşım bozukluğu tedavisi uygulanmış. Son 6 aydır ağrı
MEME KANSERİNDE GÖRÜNTÜLEME YÖNTEMLERİ
 MEME KANSERİNDE GÖRÜNTÜLEME YÖNTEMLERİ Dr. Filiz Yenicesu Düzen Laboratuvarı Görüntüleme Birimi Meme Kanserinde Tanı Yöntemleri 1. Fizik muayene 2. Serolojik Testler 3. Görüntüleme 4. Biyopsi Patolojik
MEME KANSERİNDE GÖRÜNTÜLEME YÖNTEMLERİ Dr. Filiz Yenicesu Düzen Laboratuvarı Görüntüleme Birimi Meme Kanserinde Tanı Yöntemleri 1. Fizik muayene 2. Serolojik Testler 3. Görüntüleme 4. Biyopsi Patolojik
Küçük Hücreli Akciğer Kanserlerinde Radyoterapi. Dr. Meltem Serin
 Küçük Hücreli Akciğer Kanserlerinde Radyoterapi Dr. Meltem Serin Sınırlı hastalıkta radyoterapi Yaygın hastalıkta radyoterapi Sınırlı hastalıkta radyoterapi Torakal radyoterapide tartışmalı konular Proflaktik
Küçük Hücreli Akciğer Kanserlerinde Radyoterapi Dr. Meltem Serin Sınırlı hastalıkta radyoterapi Yaygın hastalıkta radyoterapi Sınırlı hastalıkta radyoterapi Torakal radyoterapide tartışmalı konular Proflaktik
Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım. Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi
 Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi okült (gizli, saklı, bilinmeyen, anlaşılmaz) okült + kanser primeri bilinmeyen
Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi okült (gizli, saklı, bilinmeyen, anlaşılmaz) okült + kanser primeri bilinmeyen
Dr. A. Nimet Karadayı. Hastanesi, Patoloji Kliniği
 Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
ULUSAL ENDOKRİN CERRAHİ KONSENSUS KONFERANSI
 ULUSAL ENDOKRİN CERRAHİ KONSENSUS KONFERANSI TİROİD NODÜLÜNDE AMELİYAT ENDİKASYONLARI Tüm tiroid nodülleri ameliyat endikasyonudur Nodülün hızlı büyümesi (6 ayda çapın > %20) İİAB gerektirmeksizin ameliyat
ULUSAL ENDOKRİN CERRAHİ KONSENSUS KONFERANSI TİROİD NODÜLÜNDE AMELİYAT ENDİKASYONLARI Tüm tiroid nodülleri ameliyat endikasyonudur Nodülün hızlı büyümesi (6 ayda çapın > %20) İİAB gerektirmeksizin ameliyat
Dr. Zeynep Özsaran. E.Ü.T.F. Radyasyon Onkolojisi AD
 Dr. Zeynep Özsaran E.Ü.T.F. Radyasyon Onkolojisi AD Son cümle: Geçmiş yıllarda yapılan randomize çalışmalarda endometrium kanserinde RT nin rolü tanımlanmıştı Ancak eksternal RT nin yeri yüksek risk faktörlü
Dr. Zeynep Özsaran E.Ü.T.F. Radyasyon Onkolojisi AD Son cümle: Geçmiş yıllarda yapılan randomize çalışmalarda endometrium kanserinde RT nin rolü tanımlanmıştı Ancak eksternal RT nin yeri yüksek risk faktörlü
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi
 Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
Evre III KHDAK nde Radyoterapi
 Evre III KHDAK nde Radyoterapi Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. 20. UKK, 2013, Antalya Evre III Alt Grupları IIIA 0 : N2 tutulumu yok (T3N1, T4N0-1) IIIA 1 : Rezeksiyon spesimeninde
Evre III KHDAK nde Radyoterapi Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. 20. UKK, 2013, Antalya Evre III Alt Grupları IIIA 0 : N2 tutulumu yok (T3N1, T4N0-1) IIIA 1 : Rezeksiyon spesimeninde
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri. Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı
 Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
PRİMER GASTRİK LENFOMA OLGUSU DR SİNAN YAVUZ
 PRİMER GASTRİK LENFOMA OLGUSU DR SİNAN YAVUZ A C I B A D E M Ü N İ V E R S İ T E S İ T I P F A K Ü L T E S İ İ Ç H A S T A L I K L A R I A N A B İ L İ M D A L I A C I B A D E M A D A N A H A S T A N E
PRİMER GASTRİK LENFOMA OLGUSU DR SİNAN YAVUZ A C I B A D E M Ü N İ V E R S İ T E S İ T I P F A K Ü L T E S İ İ Ç H A S T A L I K L A R I A N A B İ L İ M D A L I A C I B A D E M A D A N A H A S T A N E
PEDİATRİK HODGKİN LENFOMA DR. CEM ÖNAL BAŞKENT ÜNİVERSİTESİ RADYASYON ONKOLOJISI A.D.
 PEDİATRİK HODGKİN LENFOMA DR. CEM ÖNAL BAŞKENT ÜNİVERSİTESİ RADYASYON ONKOLOJISI A.D. Vaka 16y, K. Şikayet: sol boyunda 6 aydır var olan şişlikte giderek artış olmuş. Şişlik sayısında artış mevcut. Fizik
PEDİATRİK HODGKİN LENFOMA DR. CEM ÖNAL BAŞKENT ÜNİVERSİTESİ RADYASYON ONKOLOJISI A.D. Vaka 16y, K. Şikayet: sol boyunda 6 aydır var olan şişlikte giderek artış olmuş. Şişlik sayısında artış mevcut. Fizik
TÜRK ÜROLOJĠ DERNEĞĠ KUZEY MARMARA ġubesġ AYLIK BĠLĠMSEL TOPLANTI OLGU SUNUMU
 TÜRK ÜROLOJĠ DERNEĞĠ KUZEY MARMARA ġubesġ AYLIK BĠLĠMSEL TOPLANTI OLGU SUNUMU Üroonkoloji Konseyi Olgu sunusu eģliğinde algoritmanın gözden geçirilmesi OLGU 1 20 yaģında erkek hasta 1 aydır sol testiste
TÜRK ÜROLOJĠ DERNEĞĠ KUZEY MARMARA ġubesġ AYLIK BĠLĠMSEL TOPLANTI OLGU SUNUMU Üroonkoloji Konseyi Olgu sunusu eģliğinde algoritmanın gözden geçirilmesi OLGU 1 20 yaģında erkek hasta 1 aydır sol testiste
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ. Dr. Derin KÖSEBAY
 ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
Akciğer Kanserinde Evreleme SONUÇ ALGORİTMİ
 Akciğer Kanserinde Evreleme SONUÇ ALGORİTMİ Doç. Dr. Tuncay Göksel Ege Ü.T.F. Göğüs Hast. A.D. SONUÇ Konuşması Yöntemi Toraks Derneği Akciğer ve Plevra Maligniteleri Rehberi 2006 + Kurs Konuşmaları Prognozu
Akciğer Kanserinde Evreleme SONUÇ ALGORİTMİ Doç. Dr. Tuncay Göksel Ege Ü.T.F. Göğüs Hast. A.D. SONUÇ Konuşması Yöntemi Toraks Derneği Akciğer ve Plevra Maligniteleri Rehberi 2006 + Kurs Konuşmaları Prognozu
Prof.Dr.Bülent Soyupak Dr.Alper Eken TESTİS TÜMÖRLERİ
 Prof.Dr.Bülent Soyupak Dr.Alper Eken TESTİS TÜMÖRLERİ Testis tümörleri nadir görülmekle birlikte, 15-35 yaş arası erkeklerde en sık görülen malign tümördür. Erkekteki tüm malign tümörlerin %1-2 sini kapsar.
Prof.Dr.Bülent Soyupak Dr.Alper Eken TESTİS TÜMÖRLERİ Testis tümörleri nadir görülmekle birlikte, 15-35 yaş arası erkeklerde en sık görülen malign tümördür. Erkekteki tüm malign tümörlerin %1-2 sini kapsar.
TESTİS KANSERİNDE TÜMÖR MARKERLARI Tanı, Tedavi ve Takipteki Yeri. Dr. Mert BAŞARAN İ.Ü. ONKOLOJİ ENSTİTÜSÜ
 TESTİS KANSERİNDE TÜMÖR MARKERLARI Tanı, Tedavi ve Takipteki Yeri Dr. Mert BAŞARAN İ.Ü. ONKOLOJİ ENSTİTÜSÜ Testis Tümöründe Markerlar Kullanımı Kanıtlanmış Markerlar AFP hcg LDH Kullanımı Kanıtlanmamış
TESTİS KANSERİNDE TÜMÖR MARKERLARI Tanı, Tedavi ve Takipteki Yeri Dr. Mert BAŞARAN İ.Ü. ONKOLOJİ ENSTİTÜSÜ Testis Tümöründe Markerlar Kullanımı Kanıtlanmış Markerlar AFP hcg LDH Kullanımı Kanıtlanmamış
PROF.DR. KADİR BAYKAL GATA HAYDARPAŞA EĞİTİM HASTANESİ ÜROLOJİ KLİNİĞİ
 PROF.DR. KADİR BAYKAL GATA HAYDARPAŞA EĞİTİM HASTANESİ ÜROLOJİ KLİNİĞİ Lokalize prostat Ca: 1-radikal prostatektomi 2- radyoterapi RP sonrası rezidü PSA olmaması gerekir. PSA nın total olarak ortadan kaldırılmasından
PROF.DR. KADİR BAYKAL GATA HAYDARPAŞA EĞİTİM HASTANESİ ÜROLOJİ KLİNİĞİ Lokalize prostat Ca: 1-radikal prostatektomi 2- radyoterapi RP sonrası rezidü PSA olmaması gerekir. PSA nın total olarak ortadan kaldırılmasından
İnvaziv Mesane Kanserinde Radikal Sistektomi + Lenfadenektomi, Neoadjuvan ve Adjuvan Kemoterapi. Dr. Öztuğ Adsan
 İnvaziv Mesane Kanserinde Radikal Sistektomi + Lenfadenektomi, Neoadjuvan ve Adjuvan Kemoterapi Dr. Öztuğ Adsan Radikal Sistektomi Radikal sistektomi pelvik lenfadenektomi ile birlikte kasa invaze ve
İnvaziv Mesane Kanserinde Radikal Sistektomi + Lenfadenektomi, Neoadjuvan ve Adjuvan Kemoterapi Dr. Öztuğ Adsan Radikal Sistektomi Radikal sistektomi pelvik lenfadenektomi ile birlikte kasa invaze ve
Karaciğer Metastazlarının Cerrahi Tedavisi. Dr. Orhan Bilge İ.Ü. İst. Tıp Fakültesi Genel Cerrahi ABD
 Karaciğer Metastazlarının Cerrahi Tedavisi Dr. Orhan Bilge İ.Ü. İst. Tıp Fakültesi Genel Cerrahi ABD Kolon tümörlü olguların %40-50 sinde karaciğer metastazı gelişir ; % 15-25 senkron (primer tm ile /
Karaciğer Metastazlarının Cerrahi Tedavisi Dr. Orhan Bilge İ.Ü. İst. Tıp Fakültesi Genel Cerrahi ABD Kolon tümörlü olguların %40-50 sinde karaciğer metastazı gelişir ; % 15-25 senkron (primer tm ile /
AKCİĞER KANSERİ AKCİĞER KANSERİNE NEDEN OLAN FAKTÖRLER
 AKCİĞER KANSERİ Akciğer kanseri; akciğerlerde anormal hücrelerin kontrolsüz olarak çoğalması sonucu ortaya çıkar. Kanser hücreleri akciğerlere, komşu dokulara veya vücudun diğer bölgelerine yayılabilir.
AKCİĞER KANSERİ Akciğer kanseri; akciğerlerde anormal hücrelerin kontrolsüz olarak çoğalması sonucu ortaya çıkar. Kanser hücreleri akciğerlere, komşu dokulara veya vücudun diğer bölgelerine yayılabilir.
HİPOFARİNKS KANSERİ DR. FATİH ÖKTEM
 HİPOFARİNKS KANSERİ DR. FATİH ÖKTEM Nadirdir!!! Üst aerodijestif sistem malinitelerinin % 5-10 u, tüm malinitelerin ise %0.5 i hipofarinks kanserleridir. Kötü seyirlidir!!! İleri evrede başvurmaları ve
HİPOFARİNKS KANSERİ DR. FATİH ÖKTEM Nadirdir!!! Üst aerodijestif sistem malinitelerinin % 5-10 u, tüm malinitelerin ise %0.5 i hipofarinks kanserleridir. Kötü seyirlidir!!! İleri evrede başvurmaları ve
MESANE KORUYUCU YAKLAŞIM. Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D.
 MESANE KORUYUCU YAKLAŞIM Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. Kanser tedavisinde multidisipliner organ koruyucu yaklaşım: Meme kanseri Anal kanal kanseri Larinks kanseri Prostat kanseri
MESANE KORUYUCU YAKLAŞIM Dr. Deniz Yalman Ege Ü.T.F. Radyasyon Onkolojisi A.D. Kanser tedavisinde multidisipliner organ koruyucu yaklaşım: Meme kanseri Anal kanal kanseri Larinks kanseri Prostat kanseri
TÜMÖR GÖSTERGELERİ. Dr. Sezai Vatansever İ.Ü. İstanbul Tıp Fakültesi
 TÜMÖR GÖSTERGELERİ Dr. Sezai Vatansever İ.Ü. İstanbul Tıp Fakültesi Tümör Göstergesi Tümör göstergeleri klinik, radyolojik, patolojik incelemenin dışında özel tahlil gerektirten moleküler ya da dokuya
TÜMÖR GÖSTERGELERİ Dr. Sezai Vatansever İ.Ü. İstanbul Tıp Fakültesi Tümör Göstergesi Tümör göstergeleri klinik, radyolojik, patolojik incelemenin dışında özel tahlil gerektirten moleküler ya da dokuya
Düşük Riskli Diferansiye Tiroid Kanserlerinde RAİ Tedavisi
 Düşük Riskli Diferansiye Tiroid Kanserlerinde RAİ Tedavisi 14.04.2017 Dr. Ebru YILMAZ İstanbul Üniveristesi İstanbul Tıp Fakültesi Nükleer Tıp Anabilim Dalı Neden evreleme yapıyoruz? Prognostik bilgi Hastalık
Düşük Riskli Diferansiye Tiroid Kanserlerinde RAİ Tedavisi 14.04.2017 Dr. Ebru YILMAZ İstanbul Üniveristesi İstanbul Tıp Fakültesi Nükleer Tıp Anabilim Dalı Neden evreleme yapıyoruz? Prognostik bilgi Hastalık
HODGKIN DIŞI LENFOMA
 HODGKIN DIŞI LENFOMA HODGKIN DIŞI LENFOMA NEDİR? Hodgkin dışı lenfoma (HDL) veya Non-Hodgkin lenfoma (NHL), vücudun savunma sistemini sağlayan lenf bezlerinden kaynaklanan kötü huylu bir hastalıktır. Lenf
HODGKIN DIŞI LENFOMA HODGKIN DIŞI LENFOMA NEDİR? Hodgkin dışı lenfoma (HDL) veya Non-Hodgkin lenfoma (NHL), vücudun savunma sistemini sağlayan lenf bezlerinden kaynaklanan kötü huylu bir hastalıktır. Lenf
Yasemin Giles* (Senyurek), Fatih Tunca*, Harika Boztepe**, Faruk Alagöl**, Tarık Terzioglu*, MD, Serdar Tezelman*
 PRİMER OLARAK SANTRAL LENF DİSEKSİYONU YAPILMAMIŞ OLAN PAPİLLER TİROİD KANSERLİ HASTALARDA UZUN DÖNEM SONUÇLAR: RUTİN DİSEKSİYONDAN BEKLENEN İYİLEŞME Yasemin Giles* (Senyurek), Fatih Tunca*, Harika Boztepe**,
PRİMER OLARAK SANTRAL LENF DİSEKSİYONU YAPILMAMIŞ OLAN PAPİLLER TİROİD KANSERLİ HASTALARDA UZUN DÖNEM SONUÇLAR: RUTİN DİSEKSİYONDAN BEKLENEN İYİLEŞME Yasemin Giles* (Senyurek), Fatih Tunca*, Harika Boztepe**,
Merkel Hücreli Karsinom
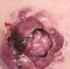 Merkel Hücreli Karsinom Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği IV. DOD Dermatoloji Gündemi, 3-6 Eylül 2015, Eskişehir Merkel Hücreli Karsinom
Merkel Hücreli Karsinom Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği IV. DOD Dermatoloji Gündemi, 3-6 Eylül 2015, Eskişehir Merkel Hücreli Karsinom
TPOG İSKİP Merkez Çalışma Kodu: Hasta TC Kimlik No Hasta İsim, Soyadı. Gönüllü Bilgilendirilmiş Onam Formu. Sayın Anne Babalar,
 TPOG İSKİP 2011 Gönüllü Bilgilendirilmiş Onam Formu Sayın Anne Babalar, Bu bir klinik araştırma çalışmasıdır. Klinik araştırmalar sadece bu çalışmaya katılmayı seçen hastaların dahil edildiği protokollerdir.
TPOG İSKİP 2011 Gönüllü Bilgilendirilmiş Onam Formu Sayın Anne Babalar, Bu bir klinik araştırma çalışmasıdır. Klinik araştırmalar sadece bu çalışmaya katılmayı seçen hastaların dahil edildiği protokollerdir.
TTOD MEME KANSERİ GÜNCELLEME KURSU 13-14 HAZİRAN 2015 İSTANBUL 08:25-08:30 Açılış 08:00-08:30 Pratiği değiştiren çalışmalar. (salonda kahvaltı ile)
 TTOD MEME KANSERİ GÜNCELLEME KURSU 13-14 HAZİRAN 2015 İSTANBUL 08:25-08:30 Açılış 08:00-08:30 Pratiği değiştiren çalışmalar. (salonda kahvaltı ile) 1. Gün 1. Oturum: Meme kanserine giriş, Patoloji ve Alt
TTOD MEME KANSERİ GÜNCELLEME KURSU 13-14 HAZİRAN 2015 İSTANBUL 08:25-08:30 Açılış 08:00-08:30 Pratiği değiştiren çalışmalar. (salonda kahvaltı ile) 1. Gün 1. Oturum: Meme kanserine giriş, Patoloji ve Alt
ERKEK GENİTAL SİSTEMİ. Webmaster tarafından yazıldı. Pazartesi, 12 Ocak 2009 11:39 - Son Güncelleme Perşembe, 15 Ocak 2009 09:19
 1) Çocuklarda en sık görülen testis tümörü aşağıdakilerden hangisidir? (1998 NİSAN) a) Klasik seminom b) Teratom c) Yolk sak tümörü d) Kariokarsinom e) Spermatositik seminom Testisde en sık görülen tümör
1) Çocuklarda en sık görülen testis tümörü aşağıdakilerden hangisidir? (1998 NİSAN) a) Klasik seminom b) Teratom c) Yolk sak tümörü d) Kariokarsinom e) Spermatositik seminom Testisde en sık görülen tümör
Dr Şükrü DİLEGE VKV Koç Üniversitesi Tıp Fakültesi ve Amerikan Hastanesi Göğüs Cerrahisi Bölümü
 Dr Şükrü DİLEGE VKV Koç Üniversitesi Tıp Fakültesi ve Amerikan Hastanesi Göğüs Cerrahisi Bölümü KHDAK nin en tartışmalı grubu Evre IIIA-N2 N2 ALT GRUPLARI ALTGRUPLAR TANIM SIKLIK IIIA-1 IIIA-2 IIIA-3 IIIA-4
Dr Şükrü DİLEGE VKV Koç Üniversitesi Tıp Fakültesi ve Amerikan Hastanesi Göğüs Cerrahisi Bölümü KHDAK nin en tartışmalı grubu Evre IIIA-N2 N2 ALT GRUPLARI ALTGRUPLAR TANIM SIKLIK IIIA-1 IIIA-2 IIIA-3 IIIA-4
OVER KANSERİNİN SİSTEMİK TEDAVİSİNDE ÇELİŞKİLER. Prof. Dr. Nil MOLİNAS MANDEL İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Medikal Onkoloji
 OVER KANSERİNİN SİSTEMİK TEDAVİSİNDE ÇELİŞKİLER Prof. Dr. Nil MOLİNAS MANDEL İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Medikal Onkoloji Over Kanseri FIGO Evrelemesi Evre Tanımlama Sıklık Sağkalım
OVER KANSERİNİN SİSTEMİK TEDAVİSİNDE ÇELİŞKİLER Prof. Dr. Nil MOLİNAS MANDEL İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Medikal Onkoloji Over Kanseri FIGO Evrelemesi Evre Tanımlama Sıklık Sağkalım
Türk Üroloji Dergisi: 31 (4): ,
 TARTIŞMALI OLGU: ÜROONKOLOJİ/Urooncology Nil MOLİNAS*, Haluk ONAT**, Fuat DEMİRELLİ*, Ferruh ZORLU***, Cüneyt İŞERİ****, Levent TÜRKERİ***** * İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Medikal Onkoloji
TARTIŞMALI OLGU: ÜROONKOLOJİ/Urooncology Nil MOLİNAS*, Haluk ONAT**, Fuat DEMİRELLİ*, Ferruh ZORLU***, Cüneyt İŞERİ****, Levent TÜRKERİ***** * İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Medikal Onkoloji
OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI. Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı
 OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı Malign mikst müllerian tümör Diğer isimleri Malign mikst mezodermal
OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı Malign mikst müllerian tümör Diğer isimleri Malign mikst mezodermal
Vaka Eşliğinde Güncel Pratik Yaklaşım: Oligometastatik Meme Kanserine Yaklaşım. Prof. Dr. Feyyaz ÖZDEMİR K.T.Ü Tıbbi Onkoloji B.D.
 Vaka Eşliğinde Güncel Pratik Yaklaşım: Oligometastatik Meme Kanserine Yaklaşım Prof. Dr. Feyyaz ÖZDEMİR K.T.Ü Tıbbi Onkoloji B.D. S A, 32 yaşında, Öğretmen, Trabzon Şikayeti: Karın ağrısı Hikayesi: 6 yıl
Vaka Eşliğinde Güncel Pratik Yaklaşım: Oligometastatik Meme Kanserine Yaklaşım Prof. Dr. Feyyaz ÖZDEMİR K.T.Ü Tıbbi Onkoloji B.D. S A, 32 yaşında, Öğretmen, Trabzon Şikayeti: Karın ağrısı Hikayesi: 6 yıl
Dr. MANSUR DAĞGÜLLİ Üroloji ABD
 Dr. MANSUR DAĞGÜLLİ Üroloji ABD Tanım İnfertilite, cinsel yönden aktif ve kontrasepsiyon uygulamayan bir çiftin bir yıl içerisinde gebelik elde edememesi durumudur (WHO). Epidemiyoloji Çiftlerin yaklaşık
Dr. MANSUR DAĞGÜLLİ Üroloji ABD Tanım İnfertilite, cinsel yönden aktif ve kontrasepsiyon uygulamayan bir çiftin bir yıl içerisinde gebelik elde edememesi durumudur (WHO). Epidemiyoloji Çiftlerin yaklaşık
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ
 MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim
 Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim Murat Özdemir, Özer Makay, Tevfik Demir*, Berk Göktepe, Kamil Erözkan, Barış Bingül**, Yeşim Ertan**, Hüsnü Buğdaycı***, Gökhan İçöz, Mahir Akyıldız
Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim Murat Özdemir, Özer Makay, Tevfik Demir*, Berk Göktepe, Kamil Erözkan, Barış Bingül**, Yeşim Ertan**, Hüsnü Buğdaycı***, Gökhan İçöz, Mahir Akyıldız
EAU kılavuzu NCCN Dr. Şeref Başal GATA Üroloji AD
 KILAVUZLAR NE DİYOR D? EAU kılavuzu NCCN Dr. Şeref Başal GATA Üroloji AD EAU KılavuzuK Radikal prostatektomi (RP) Endikasyonları Düşük ve orta riskli lokalize prostat kanserli hastalar (ctb-t2 ve Gleason
KILAVUZLAR NE DİYOR D? EAU kılavuzu NCCN Dr. Şeref Başal GATA Üroloji AD EAU KılavuzuK Radikal prostatektomi (RP) Endikasyonları Düşük ve orta riskli lokalize prostat kanserli hastalar (ctb-t2 ve Gleason
Küçük Hücrelidışı Akciğer Kanseri- Yeni Evreleme
 Küçük Hücrelidışı Akciğer Kanseri- Yeni Evreleme Dr.Alper Çelikten Yedikule Göğüs Hastalıkları ve Göğüs Cerrahisi Eğitim ve Araştırma Hastanesi 1. Göğüs Cerrahisi Kliniği Akciğer ve Plevral Tümörlerin
Küçük Hücrelidışı Akciğer Kanseri- Yeni Evreleme Dr.Alper Çelikten Yedikule Göğüs Hastalıkları ve Göğüs Cerrahisi Eğitim ve Araştırma Hastanesi 1. Göğüs Cerrahisi Kliniği Akciğer ve Plevral Tümörlerin
Varikoselde en iyi tedavi hangisi? Prof.Dr.Önder YAMAN Ankara Üniversitesi Tıp Fakültesi Üroloji A.B.D
 Varikoselde en iyi tedavi hangisi? Prof.Dr.Önder YAMAN Ankara Üniversitesi Tıp Fakültesi Üroloji A.B.D Arena resmi koyalım Sunu Planı Varikosel tanımı ve pato-fizolojisi Varikosel testisi etkiler mi? Varikosel
Varikoselde en iyi tedavi hangisi? Prof.Dr.Önder YAMAN Ankara Üniversitesi Tıp Fakültesi Üroloji A.B.D Arena resmi koyalım Sunu Planı Varikosel tanımı ve pato-fizolojisi Varikosel testisi etkiler mi? Varikosel
Mide Tümörleri Sempozyumu
 Mide Tümörleri Sempozyumu Lokal İleri Hastalıkta Neoadjuvan Radyoterapi ve İORT Prof. Dr. Ahmet KİZİR İ.Ü. Onkoloji Enstitüsü 17 Aralık 2004 İstanbul Neoadjuvan Radyoterapi Amaç : Lokal ileri hastalıkla
Mide Tümörleri Sempozyumu Lokal İleri Hastalıkta Neoadjuvan Radyoterapi ve İORT Prof. Dr. Ahmet KİZİR İ.Ü. Onkoloji Enstitüsü 17 Aralık 2004 İstanbul Neoadjuvan Radyoterapi Amaç : Lokal ileri hastalıkla
Vücutta dolaşan akkan sistemidir. Bağışıklığımızı sağlayan hücreler bu sistemle vücuda dağılır.
 HODGKIN LENFOMA HODGKIN LENFOMA NEDİR? Hodgkin lenfoma, lenf sisteminin kötü huylu bir hastalığıdır. Lenf sisteminde genç lenf hücreleri (Hodgkin ve Reed- Sternberg hücreleri) çoğalır ve vücuttaki lenf
HODGKIN LENFOMA HODGKIN LENFOMA NEDİR? Hodgkin lenfoma, lenf sisteminin kötü huylu bir hastalığıdır. Lenf sisteminde genç lenf hücreleri (Hodgkin ve Reed- Sternberg hücreleri) çoğalır ve vücuttaki lenf
 LOKOREJYONAL REKÜREN ve UZAK METASTAZ SONRASI SİSTEMİK TEDAVİ Dr.Mehmet Aliustaoğlu Lokal nüks: Aynı taraf göğüs duvarında hastalığın görülmesi Bölgesel nüks: Genellikle aksiler veya supraklivikular ve
LOKOREJYONAL REKÜREN ve UZAK METASTAZ SONRASI SİSTEMİK TEDAVİ Dr.Mehmet Aliustaoğlu Lokal nüks: Aynı taraf göğüs duvarında hastalığın görülmesi Bölgesel nüks: Genellikle aksiler veya supraklivikular ve
mrcc Tedavisinde Olgular Eşliğinde Tartışma
 mrcc Tedavisinde Olgular Eşliğinde Tartışma Doç.Dr.Adnan Şimşir - Yaklaşım,Risk Grupları Ege Üniversitesi Tıp Fakültesi Üroloji ABD Prof.Dr.İbrahim Cüretlibatır - Sitoredüktif Cerrahi Ege Üniversitesi
mrcc Tedavisinde Olgular Eşliğinde Tartışma Doç.Dr.Adnan Şimşir - Yaklaşım,Risk Grupları Ege Üniversitesi Tıp Fakültesi Üroloji ABD Prof.Dr.İbrahim Cüretlibatır - Sitoredüktif Cerrahi Ege Üniversitesi
LENFATİK VE İMMÜN SİSTEM HANGİ ORGANLARDAN OLUŞUR?
 LENFOMA NEDİR? Lenfoma, diğer grup onkolojik hastalıklar içinde yaşamın uzatılması ve daha kaliteli yaşam sağlanması ve hastaların kurtarılmaları açısından daha fazla başarı elde edilmiş bir hastalıktır.
LENFOMA NEDİR? Lenfoma, diğer grup onkolojik hastalıklar içinde yaşamın uzatılması ve daha kaliteli yaşam sağlanması ve hastaların kurtarılmaları açısından daha fazla başarı elde edilmiş bir hastalıktır.
Beyin tümörü, beyni oluşturan üç bölgeden birinden -beyin, beyincik ve beyin sapıkaynaklanabilir.
 BEYİN TÜMÖRÜ BEYİN TÜMÖRÜ NEDİR? Beyin tümörü beyinde anormal hücrelerin çoğalması sonucu gelişen bir kitledir. Bazı beyin tümörleri iyi huylu (örneğin meningiom), bazıları ise kötü huylu kitlelerdir.
BEYİN TÜMÖRÜ BEYİN TÜMÖRÜ NEDİR? Beyin tümörü beyinde anormal hücrelerin çoğalması sonucu gelişen bir kitledir. Bazı beyin tümörleri iyi huylu (örneğin meningiom), bazıları ise kötü huylu kitlelerdir.
Beslenme desteğinde hangi içerik kime, ne zaman, hangi yolla uygulansın?
 Beslenme desteğinde hangi içerik kime, ne zaman, hangi yolla uygulansın? Dr. Beste Atasoy Marmara Üniversitesi Tıp Fakültesi Radyasyon Onkolojisi Anabilim Dalı & Sağlık Bakanlığı-Marmara Üniversitesi Pendik
Beslenme desteğinde hangi içerik kime, ne zaman, hangi yolla uygulansın? Dr. Beste Atasoy Marmara Üniversitesi Tıp Fakültesi Radyasyon Onkolojisi Anabilim Dalı & Sağlık Bakanlığı-Marmara Üniversitesi Pendik
AMELİYAT SONRASI TAKİP/ NÜKSTE NE YAPALIM? Dr. Meral Mert
 AMELİYAT SONRASI TAKİP/ NÜKSTE NE YAPALIM? Dr. Meral Mert AMELİYAT SONRASI TAKİP n Ameliyat sonrası evreleme; - TNM sınıflaması kullanılmakla beraber eksiklikleri var; post-op kalsitonin- CEA ölçümü, CEA
AMELİYAT SONRASI TAKİP/ NÜKSTE NE YAPALIM? Dr. Meral Mert AMELİYAT SONRASI TAKİP n Ameliyat sonrası evreleme; - TNM sınıflaması kullanılmakla beraber eksiklikleri var; post-op kalsitonin- CEA ölçümü, CEA
Böbrek Tümörlerinin Prognostik Kategorizasyonu
 Böbrek Tümörlerinin Prognostik Kategorizasyonu Dr. Özgür Yaycıoğlu Başkent Üniversitesi Tıp Fakültesi Üroloji A.D Adana Uygulama ve Araştırma Merkezi Ürolojik Cerrahi Derneği Böbrek Tümörü ve BPH Toplantısı,
Böbrek Tümörlerinin Prognostik Kategorizasyonu Dr. Özgür Yaycıoğlu Başkent Üniversitesi Tıp Fakültesi Üroloji A.D Adana Uygulama ve Araştırma Merkezi Ürolojik Cerrahi Derneği Böbrek Tümörü ve BPH Toplantısı,
Evre I Seminom İzlem. Dr. Haluk Özen Hacettepe Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı
 Evre I Seminom İzlem Dr. Haluk Özen Hacettepe Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı Klinik Evre I Seminoma Tedavi alternatifleri İzlem Adjuvant Radyasyon tedavisi Adjuvant Kemoterapi Kür tedavi
Evre I Seminom İzlem Dr. Haluk Özen Hacettepe Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı Klinik Evre I Seminoma Tedavi alternatifleri İzlem Adjuvant Radyasyon tedavisi Adjuvant Kemoterapi Kür tedavi
Erken Evre Over Kanserlerinde Lenfadenektominin önemi. Dr. Aykut Tuncer
 Erken Evre Over Kanserlerinde Lenfadenektominin önemi Dr. Aykut Tuncer Erken Evre Over Kanserlerinde Lenfadenektominin önemi Sunum Planı Over kanseri prevelansı, evrelere göre sağkalım, yayılım yolları
Erken Evre Over Kanserlerinde Lenfadenektominin önemi Dr. Aykut Tuncer Erken Evre Over Kanserlerinde Lenfadenektominin önemi Sunum Planı Over kanseri prevelansı, evrelere göre sağkalım, yayılım yolları
Mesane Kanseri Olgu Tartışmaları Dr. Sümer Baltacı
 Mesane Kanseri Olgu Tartışmaları Dr. Sümer Baltacı Ankara Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı ÜOD/2009 Olgu 1 55 y Hematüri USG: Mesanede perivezikal uzanımı olmayan 1.5 4 cm çaplı tümörler
Mesane Kanseri Olgu Tartışmaları Dr. Sümer Baltacı Ankara Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı ÜOD/2009 Olgu 1 55 y Hematüri USG: Mesanede perivezikal uzanımı olmayan 1.5 4 cm çaplı tümörler
Multipl Myeloma da PET/BT. Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD
 Multipl Myeloma da PET/BT Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD İskelet sisteminin en sık görülen primer neoplazmı Radyolojik olarak iskelette çok sayıda destrüktif lezyon ve yaygın
Multipl Myeloma da PET/BT Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD İskelet sisteminin en sık görülen primer neoplazmı Radyolojik olarak iskelette çok sayıda destrüktif lezyon ve yaygın
29 yaşında erkek aktif şikayeti yok. sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması. üzerine hasta polikliniğimize başvurdu
 29 yaşında erkek aktif şikayeti yok Dış merkezde yapılan üriner sistem ultrasonografisinde insidental olarak sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması üzerine hasta polikliniğimize
29 yaşında erkek aktif şikayeti yok Dış merkezde yapılan üriner sistem ultrasonografisinde insidental olarak sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması üzerine hasta polikliniğimize
Adrenokortikal Karsinom Tek merkezin 10 yıllık deneyimi
 Adrenokortikal Karsinom Tek merkezin 10 yıllık deneyimi Erman Alçı, Özer Makay, Adnan Şimşir*, Yeşim Ertan**, Ayşegül Aktaş, Timur Köse***, Gökhan İçöz, Mahir Akyıldız Ege Üniversitesi Hastanesi, Genel
Adrenokortikal Karsinom Tek merkezin 10 yıllık deneyimi Erman Alçı, Özer Makay, Adnan Şimşir*, Yeşim Ertan**, Ayşegül Aktaş, Timur Köse***, Gökhan İçöz, Mahir Akyıldız Ege Üniversitesi Hastanesi, Genel
İnmemiş Testis ve İnguinal Herni. PANEL: Görseller Eşliğinde Vaka Tartışmaları
 İnmemiş Testis ve İnguinal Herni PANEL: Görseller Eşliğinde Vaka Tartışmaları DR.CEVPER ERSÖZ ÜROLOJİ ANABİ L İ M DALI Vaka 1 18 aylık, erkek çocuk Ailesi sağ yumurtalığının yukarıda olduğunu ifade ediyor
İnmemiş Testis ve İnguinal Herni PANEL: Görseller Eşliğinde Vaka Tartışmaları DR.CEVPER ERSÖZ ÜROLOJİ ANABİ L İ M DALI Vaka 1 18 aylık, erkek çocuk Ailesi sağ yumurtalığının yukarıda olduğunu ifade ediyor
Dr. Mehmet TÜRKELİ A.Ü.T.F İç Hastalıkları A.D Medikal Onkoloji B.D 5. Türk Tıbbi Onkoloji Kongresi Mart 2014-Antalya
 Dr. Mehmet TÜRKELİ A.Ü.T.F İç Hastalıkları A.D Medikal Onkoloji B.D 5. Türk Tıbbi Onkoloji Kongresi 19 23 Mart 2014-Antalya VAKA-1 S.B. 43 Yaş, Bayan, Erzurum Şikayeti: Çarpıntı, terleme, Hikayesi: Haziran
Dr. Mehmet TÜRKELİ A.Ü.T.F İç Hastalıkları A.D Medikal Onkoloji B.D 5. Türk Tıbbi Onkoloji Kongresi 19 23 Mart 2014-Antalya VAKA-1 S.B. 43 Yaş, Bayan, Erzurum Şikayeti: Çarpıntı, terleme, Hikayesi: Haziran
Prostat kanserinde hormonal tedavi ve komplikayonları
 Prostat kanserinde hormonal tedavi ve komplikayonları Dr Haluk ONAT Anadolu Sağlık k Merkezi Hastansei Medikal Onkoloji Gebze, Kocaeli Prostat kanseri Hormonal tedavi Metastatik hastalıkta hormonal tedavi
Prostat kanserinde hormonal tedavi ve komplikayonları Dr Haluk ONAT Anadolu Sağlık k Merkezi Hastansei Medikal Onkoloji Gebze, Kocaeli Prostat kanseri Hormonal tedavi Metastatik hastalıkta hormonal tedavi
Papiller Tiroid Karsinomunda Santral Lenf Nodu Diseksiyonu
 Papiller Tiroid Karsinomunda Santral Lenf Nodu Diseksiyonu 7. Ulusal Endokrin Cerrahi Kongresi Prof. Dr. Serdar Özbaş Nisan 2015 / Antalya Papiller Tiroid Karsinomunda Santral Lenf Nodu Diseksiyonu Serdar
Papiller Tiroid Karsinomunda Santral Lenf Nodu Diseksiyonu 7. Ulusal Endokrin Cerrahi Kongresi Prof. Dr. Serdar Özbaş Nisan 2015 / Antalya Papiller Tiroid Karsinomunda Santral Lenf Nodu Diseksiyonu Serdar
Laparoskopik RPLND. Monique Gueudet-Bornstein. Brass Band. New Orleans 1998.
 Laparoskopik RPLND Monique Gueudet-Bornstein. Brass Band. New Orleans 1998. Laparoskopik RPLND L-RPLND rasyoneli Endikasyonlar Teknik Komplikasyonlar Operatif data Onkolojik sonuçlar Yaşam kalitesi Laparoskopik
Laparoskopik RPLND Monique Gueudet-Bornstein. Brass Band. New Orleans 1998. Laparoskopik RPLND L-RPLND rasyoneli Endikasyonlar Teknik Komplikasyonlar Operatif data Onkolojik sonuçlar Yaşam kalitesi Laparoskopik
AZ DİFERANSİYE TİROİD KANSERLERİ. Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM
 AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
ERKEN TEK DOZ İNTRAVEZİKAL İNSTİLASYON
 ERKEN TEK DOZ İNTRAVEZİKAL İNSTİLASYON TAM DEĞERİNİ BİLİYOR MUYUZ? Doç. Dr. Mustafa KAPLAN Trakya Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı-Edirne m 2 Erken tek doz intravezikal instilasyonun amacı
ERKEN TEK DOZ İNTRAVEZİKAL İNSTİLASYON TAM DEĞERİNİ BİLİYOR MUYUZ? Doç. Dr. Mustafa KAPLAN Trakya Üniversitesi Tıp Fakültesi Üroloji Anabilim Dalı-Edirne m 2 Erken tek doz intravezikal instilasyonun amacı
GEBELİK VE MEME KANSERİ
 GEBELİK VE MEME KANSERİ Doç. Dr. Ramazan YILDIZ Gazi Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı, 27 Kasım 2014, Ankara Gebelikte Kanser Gebelikte kanser insidansı % 0.07-0.1 arasında Gebelik
GEBELİK VE MEME KANSERİ Doç. Dr. Ramazan YILDIZ Gazi Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı, 27 Kasım 2014, Ankara Gebelikte Kanser Gebelikte kanser insidansı % 0.07-0.1 arasında Gebelik
OLGU SUNUMU. Dr. Ömer Fatih ÖLMEZ Medipol Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilimdalı
 OLGU SUNUMU Dr. Ömer Fatih ÖLMEZ Medipol Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilimdalı Vaka Takdimi HY 56 yaş, erkek, maden mühendisi Şikayet: Kemik ağrısı ve kilo kaybı Hikaye: 1 aydır ağrı kesicilere
OLGU SUNUMU Dr. Ömer Fatih ÖLMEZ Medipol Üniversitesi Tıp Fakültesi Tıbbi Onkoloji Bilimdalı Vaka Takdimi HY 56 yaş, erkek, maden mühendisi Şikayet: Kemik ağrısı ve kilo kaybı Hikaye: 1 aydır ağrı kesicilere
KÜRATİF TEDAVİ SONRASI PSA YÜKSELMESİNE NASIL YAKLAŞALIM? Doç. Dr. Bülent Akduman Zonguldak Karaelmas Üniversitesi Tıp Fakültesi Üroloji A.D.
 KÜRATİF TEDAVİ SONRASI PSA YÜKSELMESİNE NASIL YAKLAŞALIM? Doç. Dr. Bülent Akduman Zonguldak Karaelmas Üniversitesi Tıp Fakültesi Üroloji A.D. PSA nın tanımı Prostate Specific Antigen PSA yı hasta nasıl
KÜRATİF TEDAVİ SONRASI PSA YÜKSELMESİNE NASIL YAKLAŞALIM? Doç. Dr. Bülent Akduman Zonguldak Karaelmas Üniversitesi Tıp Fakültesi Üroloji A.D. PSA nın tanımı Prostate Specific Antigen PSA yı hasta nasıl
Metastatik Prostat Kanserinde Tedavi. Dr. Deniz Tural Bakırköy Dr. Sadi Konuk Eğitim ve Araştırma Hastanesi Tıbbi Onkoloji
 Metastatik Prostat Kanserinde Tedavi Dr. Deniz Tural Bakırköy Dr. Sadi Konuk Eğitim ve Araştırma Hastanesi Tıbbi Onkoloji Ders Planı İnsidans ve mortalite Hormona duyarlı metastatik prostat ca Hormona
Metastatik Prostat Kanserinde Tedavi Dr. Deniz Tural Bakırköy Dr. Sadi Konuk Eğitim ve Araştırma Hastanesi Tıbbi Onkoloji Ders Planı İnsidans ve mortalite Hormona duyarlı metastatik prostat ca Hormona
İleri Evre Testis Tümörleri Kemoterapi Sonrası Cerrahi. Dr. Cemil Uygur
 İleri Evre Testis Tümörleri Kemoterapi Sonrası Cerrahi Dr. Cemil Uygur TEDAVİ KONSEPTİ GERM HÜCRELİ TÜMÖRLER: DİFERANSİASYON BOZUKLUĞU GERM HÜCRELİ TÜMÖR KLASİFİKASYONU GERM CELL (STEM) ITGCN EC/YS totipotentir.
İleri Evre Testis Tümörleri Kemoterapi Sonrası Cerrahi Dr. Cemil Uygur TEDAVİ KONSEPTİ GERM HÜCRELİ TÜMÖRLER: DİFERANSİASYON BOZUKLUĞU GERM HÜCRELİ TÜMÖR KLASİFİKASYONU GERM CELL (STEM) ITGCN EC/YS totipotentir.
SERVİKS KANSERİNDE RADYOTERAPİ
 SERVİKS KANSERİNDE RADYOTERAPİ Prof. Dr. Sait Okkan İ.Ü. Cerrahpaşa Tıp Fakültesi Radyasyon Onkolojisi Anabilim Dalı Adana, 2004 Erken Evre Serviks Kanseri Tedavi Seçenekleri * Cerrahi * Radyoterapi *
SERVİKS KANSERİNDE RADYOTERAPİ Prof. Dr. Sait Okkan İ.Ü. Cerrahpaşa Tıp Fakültesi Radyasyon Onkolojisi Anabilim Dalı Adana, 2004 Erken Evre Serviks Kanseri Tedavi Seçenekleri * Cerrahi * Radyoterapi *
AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ. Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi
 AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi Nöroendokrin tümörlerde 2004 WHO sınıflaması Tümör Tipi Tipik Karsinoid Atipik Karsinoid Büyük Hücreli nöroendokrin
AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi Nöroendokrin tümörlerde 2004 WHO sınıflaması Tümör Tipi Tipik Karsinoid Atipik Karsinoid Büyük Hücreli nöroendokrin
Proflaktik santral disekisyon: Yeni bir tartışma alanı. Ashok R. Shaha, MD. Çeviren: Dr. Yalın İşcan*, Dr. Yasemin Giles* * İÜTF Genel Cerrahi ABD
 Proflaktik santral disekisyon: Yeni bir tartışma alanı Ashok R. Shaha, MD Çeviren: Dr. Yalın İşcan*, Dr. Yasemin Giles* * İÜTF Genel Cerrahi ABD SURGERY dergisinin Aralık sayısı American Society of Endocrine
Proflaktik santral disekisyon: Yeni bir tartışma alanı Ashok R. Shaha, MD Çeviren: Dr. Yalın İşcan*, Dr. Yasemin Giles* * İÜTF Genel Cerrahi ABD SURGERY dergisinin Aralık sayısı American Society of Endocrine
