TÜRKĐYE CUMHURĐYETĐ ANKARA ÜNĐVERSĐTESĐ TIP FAKÜLTESĐ
|
|
|
- Canan Meric
- 7 yıl önce
- İzleme sayısı:
Transkript
1 TÜRKĐYE CUMHURĐYETĐ ANKARA ÜNĐVERSĐTESĐ TIP FAKÜLTESĐ KEMĐĞĐN DEV HÜCRELĐ TÜMÖRLERĐNDE HĐSTOPATOLOJĐK PROGNOSTĐK KRĐTERLERĐN BELĐRLENMESĐ VE DOKU MĐKROARREY BLOKLARI ÜZERĐNDE ĐMMÜNHĐSTOKĐMYASAL CD117 Ki 67, c-myc VE p53 EKSPRESYONLARININ PROGNOZLA ĐLĐŞKĐSĐNĐN ARAŞTIRILMASI DR. HATĐCE GERMEN ÜNVERDĐ PATOLOJĐ ANABĐLĐM DALI TIPTA UZMANLIK TEZĐ TEZ DANIŞMANI PROF. DR. NURAL ERDOĞAN Bu tez Ankara Üniversitesi Rektörlüğü araştırma Fonu tarafından HPD Proje numarası ile desteklenmiştir. ANKARA
2 ÖNSÖZ Tezimin tüm aşamalarında büyük katkısı ve desteği olan tez danışmanım Prof. Dr. Nural ERDOĞAN ve Uzm. Dr. Gülşah KAYGUSUZ a, Patoloji Anabilim Dalında asistanlık eğitimim boyunca emeği geçen tüm değerli hocalarıma, tez vakalarının temininde yardımcı olan sayın Prof. Dr. Selim EREKUL ve Prof. Dr. Yener SAĞLIK a, kesitlerin ve immünhistokimyasal boyaların yapılması aşamalarında yardımlarını esirgemeyen tüm patoloji ve immünpatoloji laboratuvar çalışanlarına, çalışmanın istatiksel değerlendirilmesinin yapılmasında emeği geçen Zeynep Bıyıklı ya, desteklerini hiç esirgemeyen başta sevgili eşim ve annem olmak üzere tüm aileme teşekkür ederim. 2
3 3
4 ĐÇĐNDEKĐLER Sayfa No: KABUL VE ONAY SAYFASI...i ÖNSÖZ... ii ĐÇĐNDEKĐLER... iii SĐMGELER VE KISALTMALAR...vi TABLOLAR DĐZĐNĐ... vii ŞEKĐLLER VE RESĐMLER DĐZĐNĐ... viii 1. GĐRĐŞ VE AMAÇ GENEL BĐLGĐLER Kemik Yapısı ve Organizasyonu Normal Kemik Histolojisi Organik Bölüm Đnorganik Bölüm Kemik Dokunun Hücreleri Kompakt Kemik Dokusu ve Yapısı Periyosteum Endosteum Spongiyöz Kemik Dokusu (Trabeküllü Kemik) ve Yapısı Kemik Histogenezi (Kemik Oluşumu)...8 4
5 Đntramembranöz Kemik Oluşumu Kondral Kemik Oluşumu Kemikte Onarım (Kemiğin Rejenerasyonu) KemikTümörleri Tümör ve tümör benzeri lezyonlarının değerlendirilmesi Hasta yaşı Lezyonun kemikteki yerleşimi Labaratuvar çalışmaları ve radyografik değerlendirme Kemik tümörlerinin sınıflandırılması Dev Hücreli Kemik Tümörü (Osteoklastoma) Tanım Sıklık Cinsiyet Yaş Lokalizayon Semptom Radyolojik Bulgular Makroskopik bulgular Histopatolojik bulgular
6 Histogenezis Tanı Tümörün Prognozu Tedavi ve Prognoz MATERYAL-METOD Olgu Seçimi ve Doku Mikarrey Blokların Hazırlanması Klinik Đnceleme Đmmünhistokimyasal Đnceleme TMA Bloklarında Doku Silindirlerinin Değerlendirilmesi Đstatistiksel Değerlendirme BULGULAR Klinik Bulgular Đmmünhistokimayasal Bulgular TARTIŞMA SONUÇLAR ÖZET SUMMARY KAYNAKLAR
7 7
8 SĐMGELER VE KISALTMALAR DĐZĐNĐ TMA: Doku Mikroarrey (Tissue microarray) DHT: Dev Hücreli Tümör IHK: Đmmünhistokimya H.E: Hematoksilen Eozin ER: Endoplazmik Retikulum ALP: Alkalen fosfataz WHO: Dünya sağlık örgütü (World Health Organization) ER: Östrojen Reseptörü MMP: Matriks Metallo Proteinaz AC: Akciğer 8
9 TABLOLAR DĐZĐNĐ Sayfa No: Tablo 1: Kemik lezyonlarının yerleşim yerleri...15 Tablo 2: Kemik tümörlerinin sınıflandırılması...18 Tablo 3: Đmmünhistokimyasal antikorların özellikleri...32 Tablo 4: Tümörün lokalizasyonlara göre dağılımı...35 Tablo 5: Semptomlara göre vakaların dağılımı...36 Tablo 6: Tümörün klinik evreye göre dağılımı...36 Tablo 7: Tümörde total p53 skoru dağılımı...37 Tablo 8: Tümörde total CD117 skor dağılımı...38 Tablo 9: Tümörde total c-myc skor dağılımı
10 ŞEKĐL VE RESĐMLER DĐZĐNĐ Sayfa No: Şekil 1: Kemik dokusunda kanaliküller içinde osteositin yerleşimi...5 Şekil 2: Kompakt ve spongiyöz kemiğin şematik görünümü...7 Şekil 3: DHT ün Cinsiyet ve Yaşa Göre dağılımı...20 Şekil 4: DHT ün Lokalizasyona Göre dağılımı...21 Resim 1: Howship lakünasına yerleşmiş osteoklast...6 Resim 2: Enkondral kemikleşme...10 Resim 3: Kırık bölgesinde oluşmuş yeni kıkırdak doku...11 Resim 4: TMA blok...40 Resim 5: H.E ve ĐHK boyalı lamlar...40 Resim 6: HE boyalı kesitler...40 Resim 7: Ki 67 boyanması...41 Resim 8: p53 boyanması...41 Resim 9: CD117 boyanması...42 Resim 10: c-myc boyanması
11 1. GĐRĐŞ VE AMAÇ Kemik tümörlerinde güncel WHO klasifikasyonuna göre neoplazilerin büyük bir bölümü benign ya da malign olarak sınıflandırılmaktadır. Bu iki kategori arasında keskin bir sınır bulunmamakla birlikte bazı tümörler (dev hücreli tümörler ve iyi differansiye kartilaginöz tümörler) borderline ya da intermediate karakter sergilemektedir. Malign kemik tümörlerinin büyük bir kısmı de novo meydana gelmektedir. Fakat benign kemik tümörlerinin bir kısmı iskelet sistemi lezyonları ile (Paget hastalığı, kondromatozis, osteokondromatozis, fibröz displazi ve osteofibröz displazi gibi) birlikte olabilmektedir. Đskelet sistemi tümörleri prezentasyon paternlerine göre sabittir. Dikkate alınması gereken önemli parametreler hasta yaşı, lezyonun lokalizasyonu, kemikte tutulan spesifik bölge (epifiz, metafiz, diafiz, korteks, medulla, periost), radyolojik görüntü ve mikroskopik görüntüdür. Kemik tümörlerinin tanısı konulurken mutlaka ilk dört parametre dikkate alınmalıdır. Dev hücreli tümör (DHT) (osteoklastoma) tüm kemik tümörlerinin %4-5 ini, benign primer kemik tümörlerinin ise %20 sini oluşturmaktadır yaşlar en sık görüldüğü yaşlar olmakla birlikte vakaların %10-15 inde 2. dekadda görülmektedir. Çok nadir olarak ise 10 yaşın altındaki çocuklarda immatür iskelet sisteminde de görülebilmektedir. Yapılan geniş serili çalışmalarda çok az kadın predominansı görülmüştür. Irk farklılığı bulunmamakla birlikte bazı coğrafik farklılıklar bulunmaktadır. Benign ancak lokal agresif seyreden dev hücreli tümör muhtemelen histiyofibroblastik elemanlardan köken almaktadır ve multinükleer dev hücreler ile stromal hücrelerden meydana gelmektedir. Bu tümörü diğer iskelet sistem lezyonlarından 11
12 (neoplastik-non-neoplastik) ayıran en önemli özellik çok sayıda dev hücrelerin bulunmasıdır. Bu kolay tanınabilir histolojik görüntüsüne rağmen DHT ın klinik, topografik ve anatomo-radyografik tanısı oldukça zordur. En önemlisi ise sonucu tam olarak belirlenemeyen lokal agresif seyirli olması ve çok nadir olarak malign transformasyon göstermesidir. Histogenezi net olarak bilinmeyen ve agresif davranabilen DHT ün lokal rekürrens veya metastaz potansiyelini öngörmekte kullanılabilecek güvenilir prognostik parametrelere ihtiyaç duyulmaktadır. Literatürde, prognostik kriterleri belirlemek üzere kısıtlı vaka serileri üzerinde yapılmış çok az sayıda çalışma bulunmaktadır. Bu çalışmada klinik takipli olgularda histopatolojik özellikler yanı sıra Doku Mikroarrey (TMA) ve Đmmünhistokimya (ĐHK) (CD117, Ki67, c-myc, p53) yöntemleri kullanarak prognozla ilişkili olabilecek kriterlerin araştırılması planlanmıştır. 12
13 2. GENEL BĐLGĐLER 2.1 Kemik Yapısı ve Organizasyonu Kemikler iskelet sisteminin en önemli yapı taşı olmakla birlikte kaslarla beraber vücut hareketini sağlamaktadırlar. Kemik dokusu organizmadaki diğer dokularda olduğu gibi hücreler, lifler ve temel maddeden oluşmaktadır. Ancak yapısındaki kalsiyumdan ötürü sertleşmiş bir destek dokusu olma özelliğini kazanmıştır. Sertliğinden dolayı kafatasıyla beyin, omurgayla omuriliği, göğüs kafesiyle başta kalp olmak üzere hayati önemi olan organları çevreleyerek korumaya almaktadır. Bunlar dışında metabolik önemi olan kalsiyum deposu olması ve kan hücrelerinin yapıldığı kemik iliğini içermesi, kemiğin destek dokusu olması dışında da önemli rolleri olduğunu ortaya koymaktadır. Kemik dokusu metabolik, endokrin ve mekanik koşullara çok duyarlı bir dokudur. Bu nedenle aktif doku olma özelliğini taşımaktadır (1, 2). Kemik, kompakt ve spongiyöz olmak üzere iki ayrı komponentten oluşmaktadır. Kompakt kemik sıkıca birbiri içine geçmiş, boşluk içermeyen bir doku olmasına karşın spongiyöz kemik gevşek, labirent veya bol boşluklu bir dokudur. Spongiyöz kemikteki bu boşluklar kemik iliği ile doludur (1, 2). Uzun kemiklerin iki uç tarafına veya eklemlerinin bulunduğu bölgeye epifiz, bunların arasında yer alan uzun bölgeye diyafiz adı verilir. Metafiz kemik oluşumunda rol oynar ve ince kompakt kemikle kaplı spongiyöz kemik dokusundan yapılmıştır. Diyafiz bölümü ise kompakt kemik dokusundan oluşur ve diyafizin ortasında kemik iliği bulunur (1, 2, 3). Kemikler periyosteum adı verilen ve osteojenik (kemik oluşturabilme) aktivitesi olan bağ dokusuyla çevrilidir. Diyafizdeki kemik iliği kavitesinde ve spongiyöz kemikteki boşlukların etrafında endosteum adı verilen ince bir bağ dokusu bulunmaktadır (3). Kemik dokusu kıkırdağın aksine bol damarlıdır. Ancak martiksinin sert olması nedeni ile diffüzyona elverişli değildir ve dokunun beslenmesi, içinde kemik hücreleri 13
14 bulunan kanaliküllerle olmaktadır. Hücreler sitoplazmik uzantılarıyla birbirleri ve komşu damarlarla ilişki kurarak metabolizmayı sağlarlar (3). 2.2 Normal Kemik Histolojisi Kemik matriksi organik ve inorganik bölümlerden oluşmaktadır Organik Bölüm Bu bölüm paralel ve belirli aralıklarla aralarında porlar bırakacak şekilde yerleşen kollajen lifler (Tip I), protein ve glikozaminoglikanlardan oluşmaktadır. Lifler arasında hidroksiapatit kristalleri bulunmaktadır (1, 2, 3) Đnorganik Bölüm Kemik kuru ağırlığının yaklaşık %50'sini oluşturur. Bu maddelerin başında kalsiyum, fosfat, magnezyum ve sitrat gelir. Kalsiyum ve fosfat hidroksiapatit kristalleri şeklindedir ve kemik kollajenlerinin yanında amorf madde ile birlikte içiçe organize olmuştur. Bu kristaller, kemikte kollajenlerle birlikte kemik sertliğini ve dayanıklılığını sağlar Kemik Dokunun Hücreleri Kemik dokusunda osteoprogenitör hücre, osteoblast, osteosit, osteoklast olmak üzere 4 tip hücre bulunmaktadır: Osteoprogenitör Hücreler Mezenşim kökenli osteoprogenitör hücreler kemiğin ana hücrelerini oluşturmaktadır. Genellikle soluk boyanan nükleuslu, asidofilik sitoplazmalı hücreler olup endosteumda, periyosteumun iç katında ve Havers kanallarında bulunurlar. Bu hücreler mitozla olgun kemik hücrelerine farklılaşır ve kemik büyümesinde, 14
15 zedelenmesi veya kırık tamirinde aktif hale gelerek bölünürler ve osteoblastlara dönüşürler (1, 4) Osteoblastlar Kemik matriksi yapımından sorumlu hücrelerdir. Kübik-alçak prizmatik olan bu hücreler iri nükleusludur ve sitoplazmaları koyu bazofiliktir. Golgi ve endoplazmik retikulumları (ER) iyi gelişmiştir. Osteoblastlar birbirleriyle kısa çıkıntılarla ilişkidedir. Kuvvetli alkalen fosfataz (ALP) ve PAS pozitif reaksiyon verirler. ALP hem matriksde bulunan hem de kalsifikasyonda rol alan önemli bir enzimdir. Enzim, fosfatın hidroliziyle lokal inorganik fosfat konsantrasyonunu arttırmakta ve bunun kalsiyum iyonlarıyla birleşmesi sonucu kalsiyum tuzları halinde dokuya çökmesini sağlamaktadır. Organizmada kemik yapım hızı kandaki ALP enzimi seviyesine bakılarak ölçülebilmektedir (1,4 ) Osteositler Olgun kemik hücresi adını da alan osteositler lakünalar içine yerleşmiştir ve kemiğin esas hücrelerini oluşturmaktadır. Gelişimlerini tamamlamış olduklarından sentez yapamazlar. Bu nedenle granüllü ER ve golgileri azalmıştır. Sitoplazma bazofilisi de daha azdır. En tipik özellikleri lakünalar arası teması sağlayan kanaliküller içinde seyreden uzantılarıdır (Şekil 1). Osteositlerin kalsiyumun kemiklerden kana verilmesi ve kalsiyum konsantrasyonunu düzenleme gibi önemli metabolik rolleri de vardır (1, 4). Şekil 1. Kemik dokusunda kanaliküller içinde osteositin yerleşimi (1) 15
16 Osteoklastlar Howship lakünası adı verilen boşluklarda yerleşmiş olan bu hücreler kemikte yıkımı veya kemik rezorbsiyonunu gerçekleştirmektedir (Resim 1). 2 den 50 ye kadar değişen sayılarda nükleusları bulunan, asidofilik ve vakuole sitoplazmalı, µm çapında çok büyük hücrelerdir. Hücrelerin çok sayıda lizozomları, mitokondrileri ve iyi gelişmiş golgi kompleksleri vardır. Osteoklastların kemiğe bitişik yüzlerinde hücre yüzeyinin genişletilmesinde rol oynayan fırçamsı kenarları bulunur. Mononükleer fagositer sisteme ait hücrelerdir ancak aktif fagositoz yapmazlar. Osteoklastlar içerdikleri kollagenaz ve diğer proteolitik enzimlerle kemiği rezorbe ederler ve eritilen kemik dokusunu uzantılarla hücre içine alılar (1, 4). Resim 1: Howship lakünasına yerleşmiş osteoklast (1) 2.3 Kompakt Kemik Dokusu ve Yapısı Kompakt kemik havers kanalları etrafında 3-7 µm kalınlıktaki lamellerden, hücrelerden ve sert bir matriksten oluşmaktadır. Đçine osteosit yerleşmiş olan ve boşluk içermeyen kanaliküller dallıdır. Bu kanaliküller aracılığı ile Havers sisteminde en içten dış lamele kadar temas sağlanır. Enine bir kesitte bu Havers sistemi konsantrik halkalar şeklinde görülür ve bu görünüme osteon adı verilir. Havers kanalı Volkmann Kanalları denen yan dallarla kemik iliği ve periyosteumla bağlantı kurar. Sert bir matrikse sahip olan kemik dokusunda diffüzyon olmadığından kanal ve kanaliküllerle kemiğin dışından 16
17 içine doğru ilişki kurulur, bu şekilde metabolizma için gerekli maddeler damar ve kanaliküllerle hücrelere kadar ulaşır (Şekil 2) (1, 4) Periyosteum Eklem yüzleri dışında kemiği dıştan çevreleyen ve bağ dokusundan (kollajen ve elastik lifler) yapılı bu doku, kemiğin desteklenmesi, beslenmesi, gelişimi ve tamiri olaylarında büyük önem taşımaktadır. Kollajen özelliğindeki Sharpey lifleri matriks içine doğru ilerleyerek periyosteumu kemiğe bağlar. Bunlar dış esas lameller ile ara lamellere kadar uzanabilirler. Bol damar içerir periosteumun dış tabaka ve iç tabaka olmak üzere iki tabakası bulunur (1). Şekil 2. Kompakt ve spongiyöz kemiğin şematik görünümü (1) 17
18 Endosteum Bu tabaka kemik iliği kavitesini ve kompakt kemiğin kanal sistemlerini çevreleyen ince bir retiküler bağ dokusudur. Bu tabaka hem kemik dokuyu hem de hemopoetik hücreleri yapabilme özelliğine sahiptir Spongiyöz Kemik Dokusu (Trabeküllü Kemik) ve Yapısı Kompakt kemiğe benzemekle birlikte trabeküler lamelden yoksundur. Bu nedenle histolojik olarak enine kesitte sirküler lamel görülmez. Buna karşılık kemik iliği ile dolu boşluklu petek gibi bir dokusu vardır (Şekil 2). Özellikle uzun kemiklerin epifizindeki spongiyöz doku basıncın veya kuvvetin geldiği yönde düzenlenmiştir. Böylece yapı çok daha sağlam bir hale gelmektedir (1) Kemik Histogenezi (Kemik Oluşumu) Đntramembranöz ve enkondral olmak üzere 2 tür kemikleşme vardır. Đntramembranöz kemikleşme bağ dokusunun, enkondral kemikleşme ise kıkırdak dokunun katılımıyla oluşmaktadır. Her iki tipte de ilk oluşan primer kemik (olgunlaşmamış) dokusudur. Bu primer kemik kalıcı değildir ve yerini olgun lamelli kemik dokuya bırakmaktadır (1, 2, 3) Đntramembranöz Kemik Oluşumu Bağ dokusu tarafından oluşturulan bu kemikleşme kafatasında görülmektedir. Kemiğin gelişimi mezenşim hücrelerinin damarlar etrafında toplanması ve çoğalması ile başlar. Mezenşim hücreleri osteoblastlara dönüşür ve bu hücreler hücrelerarası madde ve lif sentezini de yaparak osteositlere farklılaşır. Bu bölgeye kemikleşme merkezi denir. Oluşan kemik spongiyöz (trabeküler) yapıdadır ve osteoid doku adını alır. Damar çevresindeki osteoblastların osteositlere dönüşerek boşalttıkları yerlere arkadan yeni hücrelerin gelmesiyle olayda devamlılık sağlanmaktadır. Trabeküller büyür, çoğalır ve anastomozlaşarak spongiyöz kemik dokusu şekillenmiş olur. Trabeküllerarası boşluklardaki bağ dokusu da hemapoetik dokuya dönüşmektedir (1, 2). 18
19 Kondral Kemik Oluşumu Đntrakartilagenöz kemikleşme de denen bu tür kemikleşme hyalin kıkırdaktan oluşmaktadır. Kondral kemikleşme perikondral ve enkondral olmak üzere 2 tiptir Perikondral Kemikleşme Kıkırdak yüzeyindeki mezenşimal hücreler osteoblastlara dönüşür ve bu bölgede tabakalaşma yapar. Daha sonra bu hücreler ara maddeyi salgılayarak osteosit haline dönüşür ve bu olayı kalsifikasyon izler. Sonuçta ise diyafizin ortasında ve daha sonra da uçlara doğru gelişen ve kıkırdağı çevreleyen bir perikondral kemik dokusu ortaya çıkar. Kemikleşme tamamlandıktan sonra perikondriyum periyosteum adını alır. Bu kemik kompakt yapıdadır ve bu yolla kemiğin enine büyümesi sağlanır (1, 2 ) Enkondral Kemikleşme Uzun kemiklerin şekillenmesini ve uzunlamasına büyümesini sağlayan bu tür kemikleşmede kıkırdak hücreleri önemlidir. Bu tür kemikleşme esas olarak kıkırdak hücrelerinin özellikle uzun kemiklerin diyafiz bölgesinde birtakım değişimleri şeklinde olmaktadır. Kıkırdak hücrelerinde görülen farklılaşmalar neticesinde doku, dinlenme zonu, proliferasyon zonu, hipertrofi zonu, kalsifikasyon zonu, kemikleşme zonu gibi birtakım bölgelere ayrılmaktadır (Resim 2) (1, 2 ). Proliferasyon zonunda kıkırdak hücreleri kemik uzun eksenine doğru dizilirler. Çoğalma diyafiz ortalarında durur. Bundan sonra hücreler sitoplazmalarında madde depolamaya başlarlar ve büyürler (hipertrofi zonu). Buradaki hücrelerde alkalen fosfataz enzimi artmıştır ve bu enzimin dışarı çıkmasıyla kalsifikasyon başlar. Kalsifikasyondan sonra osteoklastlar rezorbsiyona başlar. Rezorbsiyon sonucu ortaya çıkan boşluklara periyosteumdan gelen osteoprogenitör hücreler yerleşir ve osteoblastlara dönüşür. Osteoblastlar kavitelerin yüzeyine yerleşerek kemik matriksini yaparlar daha sonra da osteosit haline dönüşürler. Matriks de ileride kalsifiye olur (3). 19
20 Resim 2: Enkondral kemikleşme (1) Havers lamel sistemi osteoklastların çevre dokuyu eriterek açtıkları kovukların anastomozlaşmasıyla oluşur. Bunların içi kemik iliği, bağ dokusu ve osteoklastlarca dolmuştur. Bağ dokusunda yer alan hücreler osteoblastlara farklılaşarak kanal duvarına dizilirler ve Havers'in en dış lamelini yaparlar. Sürekli olan bu olay ile periferden merkeze doğru konsentrik tertiplenmiş lamel tabakası ortaya çıkar (osteon) (3). Sonuç olarak perikondral kemikleşme perikondriyumun osteojenik aktivitesiyle, enkondral kemikleşme ise kondrositlerin çoğalması ve bu hücrelerdeki bir takım değişiklerle meydana gelmektedir. Kemik bir yandan devamlı olarak yapılırken bir yandan da osteoklastlarca yıkıma uğratılmakta ve bu iki olayın uyumu ile kemik normal yapısını korumaktadır (3). 2.6 Kemikte Onarım (Kemiğin Rejenerasyonu) Organizmada hasar gören dokular belirli oranda kendisini yenileyebilmektedir. Kemik dokusu da bunlardan biridir. Kemik kırıklarında, kırık bölgesinde yeni bir kemik dokusu oluşabilir ve doku tamamen eski fonksiyonuna kavuşabilir. Kırık meydana geldiğinde kemikte ve çevre zedelenmiş dokuda inflamasyon başlamaktadır. Ortama gelen nötrofiller ve makrofajlar hasarlı dokuyu ortadan kaldırır ve doku fibroblastların çoğaldığı, neovaskülarüzasyonun başladığı fibröz doku halini alır. Kırık yeri kallus denen kıkırdak dokuya dönüşür. Bu arada kırık bölgesindeki periyosteum ve 20
21 endosteumun osteoblastları çoğalarak burada bir hücre katı oluştururlar. Daha sonra enkondral kemikleşmede olduğu gibi primer kemik oluşur. Olgunlaşmamış bu kemik dokusu yavaş yavaş ortadan kalkar ve yerini sekonder yani esas kemik dokuya bırakır (Resim 3) (3). Resim 3: Kırık bölgesinde oluşmuş yeni kıkırdak doku (1) 2.7. Kemik Tümörleri Primer kemik tümörlerine çok sık rastlanmamakla birlikte ABD istatistiklerine göre yılda 10 milyonda 10 kişide görülmektedir (5). Benign kemik tümörleri arasında en sık rastlananlar histiyositik fibroma, ekzositoz, kondroma, dev hücreli kemik tümörü, osteoid osteoma ve fibröz displazi gelmektedir. Malign tümörler arasında ise en sık görülenler osteosarkom, plazmositom, kondrosarkom, Ewing sarkom, malign fibröz histiyositom, lenfoma ve kordomadır. Vasküler tümörler, admantinoma, sinir ve yağ dokusundan köken alan tümörler ise oldukça nadirdir. Tümör benzeri lezyonlar içinde kemik kistleri, histiyositozis X ve anevrizmal kemik kisti görülmektedir (5, 6). Kemik tümörleri ve tümor benzeri lezyonlarının, anatomik yerleşimleri, kökenleri, klinik sunumları ve davranışları belirgin farklılık gösterdiğinden sıklıkla tanı ve tedavi güçlüğü oluşturmaktadırlar. Kas-iskelet sisteminin herhangi bir bölgesinde yerleşebilir; kemik, kıkırdak, fibröz doku, kemik iliği, lenfoid doku, sinir ve kan damarları dahil herhangi bir dokudan köken alabilir ve her yaşta görülebilir. Normal dokulara hasar verebilir, dayanılmaz ağrı, şişlik, ciddi sakatlık ve patolojik kırık gibi şikayet ve bulgulara yol açabilir ya da normal dokuları çok az etkileyip sessiz kalabilir. 21
22 Doğal seyirlerine bakıldığı zaman bazı lezyonlar kendi kendine rezorbe olurken, bazıları yoğun tedaviye rağmen hızlı şekilde yayılıp ölüme yol açabilir. Bu farklılıklara rağmen iyi ve kötü huylu tümörler ve tümör benzeri lezyonlar benzer klinik ve radyolojik bulgular gösterebilir (7). Kemik tümörlerinin sınıflandırılması ve tiplendirilmesinde tümörün morfolojik görüntüsü yanında klinik, radyolojik, makroskopik, prognostik ve terapatik natürü gibi özellikleri de göz önünde bulundurulmalıdır. Tüm bu özellikler içerisinde histolojik özellikler en önemli parametreyi oluşturmaktadır. Mesela parosteal osteosarkom histolojik özellikleri dışında klinik, radyolojik ve prognostik özelliklerinin benzer olması nedeni ile klasik osteosarkomdan, Ewing sarkom, primer lenfomadan ayrılmalıdır. Kemiğin tümöral lezyonlarını değerlendiriken tüm kemik lezyonlarını ayırıcı tanıya koymak yerine hastanın ve lezyonun özelliğine göre birkaç seçeneğe indirgemek tanı ve tedavi için daha faydalı olabilir. Bu lezyonları değerlendiriken karşılaşılan en önemli sorun hangi lezyonların takip edileceği, hangi lezyonlarda daha ileri tetkik ve biopsiye ihtiyaç olduğunun belirlenmesidir (6) Kemiğin tümör ve tümör benzeri lezyonlarının değerlendirilmesi Kemiğin tümör ve tümör benzeri lezyonlarının değerlendirilmesi diğer hastalıkların değerlendirilmesine benzer. Đyi bir hikaye, tam bir fizik muayene ve radyografilerin iyi incelenmesi ile değerlendirmeye başlanır. Değerlendirmede önemli olan noktalar; hastanın yaşı, lezyonun nasıl tespit edildiği, lezyonun kemikteki yerleşimi, lezyonun radyografik görünümü ve lezyonun sayısıdır (6, 8, 9). 22
23 2.7.2 Hasta yaşı Pek çok kemik lezyonun görüldüğü belli yaş aralıkları mevcuttur. Eozinofilik granülom ve myelom birbirine çok benzer radyografik bulgular verse de, eozinofilik granülom genelde beş yaşın altında görülürken, myelom daha çok 30 ve daha ileri yaşların hastalığıdır. Hastaları yaşlarına göre dört gruba ayırmak mümkündür. Birinci grup; hayatın ilk sekiz yılı, ikinci grup; sekiz yaştan fizislerin kapandığı döneme kadar olan süre, üçüncü grup; fizislerin kapandığı geç ergenlik döneminden 40 yaşa kadar olan süre, dördüncü grup ise 40 yaş sonrasını oluşturmaktadır (6). Birinci grupta sık görülen lezyonlar; osteomyelit, eozinofilik granülom ve metastatik Wilm s tümörüdür. Basit ve anevrizmal kemik kisti ile non-ossifying fibrom da görülebilen lezyonlar arasındadır. Đkinci grupta basit ve anevrizmal kemik kisti, nonossifying fibrom, osteomyelit, osteosarkom, Ewing sarkom, enkondrom, kondroblastom ve kondromikzoid fibrom sık görülür. Osteofibröz displazi, fibröz displazi, osteoblastom da görülebilecek lezyonlardır. Üçüncü grupta en sık dev hücreli tümör, Ewing sarkom, osteosarkom, dördüncü grupta ise en sık metastatik kemik lezyonları ve myelom görülmektedir. Hiperparatiroidiye bağlı brown tümör oldukça nadirdir. Kemiğin malign fibröz histiyositom ve fibrosarkom gibi radyolusen özellikli primer tümörleri oldukça nadirdir ve 40 yaş üzerinde görülebilir (6) Lezyonun kemikteki yerleşimi Lezyonun kemikteki yerleşimi diyafizyel, metafizyel, epifizyel ya da bu bölgelerin kesişmesi şeklinde olabileceği gibi kortikal ya da medüller de olabilir (Tablo 1). Epifizde yerleşen ve tamamen intramedüller olan lezyon osteomyelit, kondroblastom veya ileri yaşta dejeneratif kist olabilir. Hemen tüm kemik tümörleri metafizyel yerleşimli olabileceğinden bu yerleşim yeri tanıya yardımcı olmayabilir. Basit kemik kisti ve enkondromlar 10 yaş altında epifize hemen komşu metafizyel bölgede santral yerleşimli olarak görülürken daha ileri yaşlarda metafizyel-diyafizyel bölgeye doğru 23
24 yerleşir. Diğer kemik lezyonları ekzantrik yerleşimlidir. Osteosarkom en sık görülen malign kemik tümörüdür ve sıklıkla metafizde yerleşir (5). Büyüme plakları açık hastalarda metafiz ve epifizde yerleşen radyolüsen lezyonların ayırıcı tanısında osteomyelit ve malign tümörler akla gelmelidir. Çünkü büyüme plağı tümörlere karşı doğal bariyer olarak kabul edilir. Büyüme plakları kapalı hastalarda ise dev hücreli tümör ve kondroblastom metafizyo-epifizyel yerleşim gösterir. Ewing sarkomu nadiren epifizyel yerleşim gösterse de genelde metafizyel yerleşimlidir. Uzun kemiklerin diyafizi nadir yerleşim bölgelerinden biridir. Osteofibröz displazi, adamantinoma özellikle tibia ve fibulanın diyafizinde görülür. Ewing sarkom, osteoid osteoma, malign fibröz histiyositom ve eozinofilik granülom da diyafizyel yerleşebilir. Metastatik lezyonlar ise sıklıkla metafizyo-diyafizyel bileşkede yerleşir (6). Tablo 1. Kemik lezyonlarının yerleşim yerleri Epifiz Diyafiz Metafizyo-diyafizer Metafiz - Dev hücreli tümör - Kondroblastom - Enfeksiyon -Malign fibröz histiyositom -Myelom -Ewing sarkom -Osteoid osteom -Non-ossifying fibrom -Osteoblastom -Kondromigzoid fibrom -Osteosarkom -Osteokondrom -Anevrizmal kemik kisti -Non-ossifying fibrom -Eozinofilik granülom -Kondromigzoid fibrom -Osteom -Kondrosarkom -Enkondrom -Fibrosarkom -Parosteal osteosarkom -Dev hücreli tümör -Basit kemik kisti 24
25 2.7.4 Labaratuvar çalışmaları ve radyografik değerlendirme Kemik tümörlerinde tanısal veya prognostik önemi olan çok az test vardır. Artmış beyaz küre ve eritrosit sedimentasyon hızı genelde enfeksiyon belirtisi olsa da Ewing sarkomu gibi hastalıklarda da görülebilir. ALP metastatik kemik tümörü ya da Paget hastalığında yükselebilir. Multiple myelomlu hastalarda serum ve idrar protein elektroforeziyle monoklonal pik görülebilir (6, 10). Kemik lezyonun değerlendirmesinde en önemli görüntüleme yöntemi direk grafidir. Direk grafilerin incelenmesinde önemli noktalar; lezyonla kemik arasındaki sınır ve kemiğin lezyona karşı gösterdiği reaksiyondur. Küçük hücrelerce oluşturulan lezyonlar (Ewing sarkomu, eozinofilik granülom, osteomyelit) hızlı bir şekilde kemiğin yerini alır ve kemikle lezyon arasında belirgin bir sınır göstermez. Bu tür sınıra geniş geçiş bölgesi adı verilir ve güve yeniği şeklinde görülebilir. Bu lezyonlar korteksi harap ederek yumuşak dokuya yayılır ve kırığa yol açabilir. Yavaş büyüyen lezyonlar kemiğin hastalığa karşı cevap oluşturabilmesine olanak tanır ve kemik hasarını kısıtlar. Bu tür lezyonlarda belirgin veya jeografik sınır görülür ve dar geçiş bölgesi olarak adlandırılır. Oldukça yavaş büyüyen lezyonlarda sklerotik sınır görülürken, iyi huylu fakat nispeten daha hızlı büyüyen lezyonlarda sklerotik sınır görülmez (6, 11, 12). Kemik korteksi kırılıp periosta açıldığı zaman periost reaksiyonu oluşturur. Periost reaksiyonunun tipi lezyonun karakteri hakkında fikir verir ve kabaca iki gruba ayrılabilir: Sürekli olan ve sürekli olmayan periost reaksiyonu. Sürekli veya solid tip periost reaksiyonu yavaş büyüyen lezyonlarda görülür ve periostun lezyona kapsül oluşturabilecek zamanı vardır. Bu lezyonlar %90-95 oranında iyi huyludur. Osteoid osteom ve eozinofilik granülom bu tip reaksiyona yol açar. Daha hızlı büyüyen lezyonlar ise periosta yeterli zaman bırakmadıkları için sürekli olmayan periost reaksiyonu oluştururlar. Osteomyelit, osteosarkom, kondrosarkom, fibrosarkom, lenfoma, lösemi ve kemik metastazları sürekli olmayan periost reaksiyonu oluşturur (6, 10, 11). Belirgin sınırları olan ve sürekli periost reaksiyonu ile sınırlandırılan lezyonlar genelde yavaş büyüyen iyi huylu lezyonlarken, belirgin sınırları olmayan ve sürekli 25
26 olmayan tip periost reaksiyonu ile sınırlanmış lezyonlar hızlı büyüyen ve olası kötü huylu lezyonlardır. Osteomyelit ve anevrizmal kemik kisti ise istisna olarak aggresif radyolojik görünüme neden olabilir (6, 10, 12). Direk grafiler dışında bilgisayarlı tomografi, manyetik rezonans görüntüleme, anjiografi, radyonüklid kemik sintigrafisi, positron emisyon tomografi kemik tümörlerinin tanısında önemli yer tutmaktadır (6, 12). Biopsi tanının son basamağı, tedavinin ilk basamağı olmalıdır. Biopsi sadece lezyona ad koymak için yapılmamalıdır (6, 9). Biopsi seçenekleri ince iğne aspirasyonu, trokar veya açık biopsidir. Herhangi bir biopside alınan dokuyu temsil edebilecek nitelikte yeterli doku alınmalı, dokular mümkün olduğunca az travmatize edilmeli, ekstremite uzun aksına parallel ve mümkün olduğunca en kısa longitudinal insizyonlar kullanılmalıdır (6, 10). Tümörde ekstraosseöz yumuşak dokuya yayılım varsa biopsi buradan alınmalıdır. Böylece hem periferde diagnostik malign hücrelerin bol olması tanıyı kolaylaştırır hem de kemiğin içine girme sonucu oluşabilecek patolojik kırık ihtimali ortadan kalkar (12). Kapalı biopsinin komplikasyonu çok azsa da maksimum tanı değeri %80 dir. Tanı için yeterli doku örneği alınmayabilir. Açık biopsi ile yeterli doku almak daha kolaydır ancak morbiditesi daha fazla olan girişimlerdir. Biopsi öncesi tanı ve evrelendirme çalışmaları lokalize benign tümör lehine ise eksizyonel biopsi tercih edilir (12, 13). Her kemik lezyonunda biopsi gerekli değildir. Lezyonun klinik görünümü tanı için yeterli ise, cerrahi tedaviye gerek yoksa veya ayırıcı tanıda yer alan lezyonların hiçbirinde cerrahi tedaviye gerek yoksa bu lezyonlarda biopsi yapılmayabilir. Böyle durumlarda tedavi seçeneği periyodik olarak izlemdir. Bu lezyonlar basit kemik kisti, non-ossifying fibrom ve enkondromlardır. Ilk başta 6-12 haftada bir radyografik takip önerilirken, eğer lezyonda değişiklik yoksa daha uzun aralıklarla takip edilebilir (6, 12). 26
27 2.7.5 Kemik tümörlerinin sınıflandırılması Kemik tümörleri 2002 de yapılmış WHO sınıflamasına gore kategorize edilmektedir (Tablo 2). Bu tümörler differansiasyonlarına göre benign, düşük gradeli malign ve yüksek gradeli malign olmak üzere üç kategoride sınıflandırılmıştır (5). Bunlar dışında etyolojisi net olarak bilinmeyen ancak kemik tümörlerinden ayırıcı tanısı gereken tümör benzeri lezyonlar bulunmaktadır. Bunlar; kemik kistleri, anevrizmal kemik kisti, müköz kist, progresif telenjiektatik osteolizis, histiyositozis X, primer hiperparatiroidizme eşlik eden osteozis, dev hücreli reperatif granülom, tümör benzeri periosteal ossifikasyondur. 27
28 Tablo 2. Kemik tümörlerinin Sınıflandırılması Differansiasyon Benign Düşük-gradeli malign tümörler Yüksek-gradeli malign tümörler -Fibröz ve histiyositik -Histiyositik fibroma -Benign fibroma histiyositoma -Dev hücreli tümör -Desmoid fibrom -Grade I-II fibrosarkom -Grade III-IV fibrosarkom -Malign fibrözhistiyositom -Kartiloginöz -Ekzositoz -Epifizyal Displazi -Kondroma -Kondroblastoma -Kondromikzoid fibroma -Grade I-II santral kondrosarkom -Periferal Kondrosarkom -Periosteal kondrasarkom -Clear-cell kondrosarkom -Fibrokartiloginöz mezenkimoma -Grade III santral kondrosarkom -Mezenkimal kondrosarkom -Osseoz -Hematopoetik -Osteoma -Osteoid osteoma -Osteoblastom -Fibröz displazi -Osteofibröz displazi -Parestoal osteosarkom -Periosteal osteosarkom -Low-grade santral osteosarkom -Klasik osteosarkom -Hemorajik osteosarkom -Small-cell osteosarkom -Osteosarkomatozis -Lenfoma -Plazmostoma -Lösemi -Vasküler -Hemanjioma -Lenfanjioma -Low-grade hemanjioendotelioma -Hemanjioperisitoma -High-grade hemanjioendotelioma -Hemanjioperisitoma -Nervous -Nörinoma -Nörofibroma -Ewing Sarkom? -Adipö -Lipoma -Lipsarkom -Miks -Adamantinoma? -Malign mezenkimoma -Notokordal -Kordoma 28
29 2.8 Dev Hücreli Kemik Tümörü (Osteoklastoma) Tanım Santral yerleşimli kemik tümörü olan DHT, histiyo-fibroblastik elemanlardan köken aldığı düşünülen ve dev hücreler ile karakterli bir tümör grubunu oluşturmaktadır yılında Jaffe ve ark. tarafından tanımlanmış ve çok sayıda multinükleer osteoklast benzeri dev hücrelerin varlığı nedeniyle osteoklastoma adı verilmiştir (13, 14, 15). Bu tümörü diğer iskelet sistemi tümörlerinden (benign-malign) ayıran en önemli özellik çok sayıda dev hücrelerin bulunmasıdır. Tümörün en önemli özelliği ise biyolojik davranışının net olarak bilinmemesidir. Benign ancak lokal agresif olduğu bilinen bu tümörelerde nadir de olsa malignite riski bulunmaktadır. Malign tümörler içinde en çok fibrosarkom, osteosarkom, malign fibröz histiyositoma dönüştüğü bildirilmiştir. Sarkomatöz transformasyon tümörün bulunduğu alanda görülebildiği gibi buna komşu bir sarkomatöz tümöre ait bir alanda da görülebilir. Ancak ransformasyon genellikle radyasyon terapisine sekonder görülmektedir (5, 15). Literatürde nadir olarak multisentrik DHT de bildirilmiştir. Ancak bu durumda primer hiperparatiroidizm ekarte edilmelidir (16) Sıklık Odukça nadir görülmektedir. Tüm primer kemik tümörlerinin %5 ini, primer benign kemik tümörlerinin %20 sini oluşturur (17, 18, 19). Sarkomatöz diferansiasyon ise tüm DHT ün %5 inden azında görülmektedir Cinsiyet Kadın ve erkekte birbirine benzer oranlarda görülmekle birlikte literatürlerde çok az bir oranda kadın predominansı (%52,5) bildirilmiştir (Şekil 3) (19, 20). 29
30 Şekil 3. DHT ün Cinsiyet ve Yaşa Göre Dağılımı Yaş Karakteristik olarak genç erişkinlerde, epifiz plağı kapandıktan sonra görülür. Vakaların çoğunda yaşları arasında saptanır. Sıklığın ve yaşları arasında da arttığı bilinmektedir (Şekil 3) (15, 20). Püberteden önce kartilaj dokunun hala büyümeye devam etmesi ve epifiz plağının kapanmaması nedeni ile daha seyrek olarak görülmektedir. 50 yaş sonrası ise oldukça nadirdir (21) Lokalizasyon Vakaların %90 ında uzun kemiklerde ve meta-epifiziyal segmentte görülmektedir (19). Püberteden önce büyüme plağı kapanmadan ortaya çıkarsa metafizde yerleşim göstermektedir Tümörün en sık görüldüğü meta-epifiziyel bölge distal femur ve proksimal tibiadır (Şekil 4). Vakaların yarısından çoğunda tümör diz bölgesinde yerleşmektedir. Bunun dışında distal radius, proksimal femur, distal tibia, proksimal humerus görülen diğer lokalizasyonlardır. Nadir olarak ise distal humerus, proksimal radius ve ulna, proksimal fibula, distal ulnada görülmektedir. El kemiklerinde %1,7, ayak kemiklerinde %1,2 gibi çok nadir oranda bidirilmekle birlikte bu bölgelerde daha çok epifiziyel yerleşimlidir (22). Fakat kemik boyutu küçük olduğundan diafizede yayılım göstermektedir (15). 30
31 Uzun kemikler dışında DHT sakrum, pelvis (ileum, iskium, pubis), vertebra ve tarsus gibi kısa ve düz kemiklerde de görülebilmektedir. Vakaların % 2 sinde DHT baş ve boyunda yerleşim gösterir (23). Temporal, sfenoid ve etmoid kemikler en sık tutulan kemiklerdir. Parieta-oksipital kemik, maksilla ve zigomatik kemikler çok daha nadir oranda tutulmaktadır (24). Kraniumda da DHT görülebilmekle birlikte bu durum Paget hastalığına sekonder olarak ortaya çıkmaktadır. Şekil 4. DHT ün Lokalizasyona Göre Dağılımı Semptom Ana semptom ağrıdır. Eklem aralığına yakın yerleşimli tümörlerde kartilaj dokunun veya sinovial membranın ayrılmasına bağlı olarak fonksiyon kaybı ve eklem aralığında efüzyon görülebilmektedir. Yüzeyel ve küçük çaplı kemiklerde (proksimal tibia, distal radius ve ulna, fibula, metekarp ve falankslarda) kemiğin genişlemesine bağlı olarak tümör dışarıdan görülebilir hale gelmektedir. Korteksi ince kemiklerde 31
32 mikrofraktür ve patolojik fraktür daha sık meydana gelmektedir. Tümörün aşırı büyüdüğü durumlarda ise çevre yumuşak dokuda şişlik, peritümöral ödem, yüzeyel venöz ağda tıkanıklığa sebep olmaktadır (5, 15) Radyolojik Bulgular Radyolojik görüntüsü oldukça karakteristiktir. Direk grafilerde genellikle eksantrik, meta-epifiziyal yerleşimli, sirküler genişleme paternine sahip ve çevre yumuşak dokuda radiotransparan bir görüntü veren tümör olarak izlenmektedir. Kortikal ve süngerimsi kemikte osteolitik lezyon oluşturmaktadır. Osteolizis homojendir, ossifikasyon ve kalsifikasyon içermez. Tümör genellikle yakınındaki eklem kartilajına yayılım gösterir. Korteks genellikle erken dönemde diffüz olarak tutulur. Radius, ulna ve fibula gibi küçük çaplı tubuler kemiklerde tümör meta-epifiziyal bölgeyi aşarak diafize ulaşabilir. Tümör çevresindeki osteogenetik reaksiyona bağlı olarak gelişen osteoid doku matür değildir ve kolayca resorbe olabilir. Bu alanda tümör ince bir tabaka olan periosta yayılım gösterir ve radyolojik olarak bu alan radyoopasite verir. Patolojik fraktür meydana geldiğinde ise bu alanda kallus dokusu oluşur. Hızlı büyüme ve aggresif gelişim paternini destekleyen bir takım radyolojik görüntüler de mevcuttur. Osteolitik bölge hızlı bir şekilde büyüyor, süngerimsi kemik ve çevre yumuşak dokuya ulaşıyorsa tümör aggresif gelişim gösteriyor demektir. Radyografik olarak Enneking in benign tümör sınıflamasına göre DHT 3 kategoride incelenmektedir (5, 25, 26): 1. Sakin (Quiescent) radyografik görünüş: Kortikal kemik bütünlüğünü korumuş ve incedir. Osteolizis iyi sınırlıdır ve peritümöral hiperosteozis ile arasında keskin ve ince bir sınır mevcuttur. Tümörun oluşmasından uzun zaman geçmesine rağmen büyük değildir. Çevrede bulunan ekleme invazyon göstermez. Bu karakterdeki tümörler daha nadirdir ve stage 1-2 kabul edilmektedir. 32
33 2. Aktif radyografik görünüş: En karakteristik ve sık görülen formdur. Korteks oldukça incelmiştir. Tümör periosteumu daraltmış ve kemik dışına yayılım göstermiştir. Osteolizis düzensiz sınırlıdır. Bazı tümörlerde çevre eklem kartilajına ulaşım görülebilir. Stage 2 tümör olarak bilinmektedir. 3. Agresif radyografik görünüş: Korteks tümör ile tamamen parçalanmıştır. Tümör aggresif gelişim göstererek çevre yumuşak dokuya, epifiz ve eklem kartilajına ulaşmıştır. Radyoopasite vermez. Nadir olarak izlenir ve stage 3 tümörü ifade eder. Bazı vakalarda tümör osteolizisi çevre kemiklere ulaşabilmektedir (fibuladan proksimal veya distal tibiaya, ulnadan distal radiusa gibi). Bu durum tümörün kapsül, liagament veya sinoviyal membranı geçtiğinde ortaya çıkmaktadır Makroskopik bulgular Makroskopik olarak tümör kompakt, açık kahve ya da kahve kırmızı renkli, parankimatöz, yumuşak ve düzgün yüzeyli olarak karşımıza çıkar. Tümör komşuluğunda görülebilir bir kalsifikasyon ya da kemikleşme bulunmaz. Süngerimsi kemik, meduller kanal, periost ve incelmiş korteks ile tümör arasında keskin bir sınır bulunmakla birlikte fibröz ya da hiperostatik bir demarkasyon hattı bulunmaz (20). Genellikle doku uniform değildir. Tümör içinde dallanmış vasküler yapılar, regrese sekonder fibrotik alanlar ve lipid akümülasyonuna bağlı sarı renkli alanlar bulunabilir. Bazen oldukça hemorajik görünümlü alanlar içeren tümörde kanın akümülasyonuna bağlı süngerimsi alanlar dikkati çeker. Gri sarı renkli nekrotik alanlar bazen daha kuru görünümlü olabilir. Hemorojik ve nekrotik orijinli kistik kaviteler de izlenebilir (5). Aktif formda periostta iyi sınırlı bir lezyon olarak izlenen tümör, agresif formda periostta sınırlanmaz, ekspansifdir ve yumuşak doku ve kas dokusuna multiple uzantılar gösterir. Makroskopik olarak zor izlenen bir psödokapsüle sahiptir. Tümörün eklem 33
34 kapsülüne, ligamentlere, sinovial menbranlara ve eklemi oluşturan diğer kemiklere penetre olduğu makroskopik olarak izlenebilir Histopatolojik bulgular Histolojik olarak DHT iki hücre tipi içermektedir: multinükleer dev hücreler (osteoklast) ve prolifere hücre proliferasyonunu oluşturan neoplastik stromal hücreler (27). Tek nükleuslu stromal hücreler yuvarlak, oval ya da spindle karakterdedir. Nükleus oval ya da yuvarlak, hiperkromatik veya vezikülerdir. Bir veya birden fazla nükleol bulunabilir. Hücrelerde pleomorfizm ve polimorfizm görülebilir. 10 BBA da 2-20 kadar mitoz bulunabilir. Ancak atipik mitoz görülmez. Atipik mitoz varlığı sarkoma differansiasyonu düşündürmelidir (28). ĐHK sal olarak Tip 1 ve Tip3 Kollagen, Paratiroid hormon reseptörü, lizozim, alfa 1-antitripsin ve S100 pozitifliği izlenebilir (5, 20, 29, 30). Dev hücreler geniş vakuole sitoplazmalı, arasında değişen nükleusa sahip hücreler özelliğindedir. Nükleuslar genellikle hücrenin santralinde yerleşim gösterir ve stromal hücrelerde izlenen nükleuslar ile benzer özelliktedir. Histokimyasal olarak asit fosfataz ve diğer hidrolitik enzimler ile ĐHK sal olarak lizozim, alfa1-antitripsin, alfa1- antikimotipsin, diğer histiyositik markerlar, kalsitonin reseptörü, ER, MMP ile boyanma gösterebilir (29, 30, 31). Stromal hücreler arasında ince ve seyrek olarak kollajen ve retiküler lifler izlenebilir. Sayıca artmış kan adamarları geniş sinüzoidler oluşturabilir ve bunlar içinde dev hücreler izlenebilir. Psödokapsül altında yerleşimli venüller içerisinde neoplastik dokuya rastlanabilir (20, 31). Tümörde nadir olarak regresyon bildirilmiştir. Tümörün geçici elenmenti olan dev hücreler genellikle piknotik nükleus içerir. Tümörün tamamı nekroze gidebilir. Fibröz doku oluşturarak skar dokusu meydana getirebilir. DHT de osteolitik aktivite daha belirgin olmakla birlikte tümörün periferinde ve periost altında ince bir osteoid doku da bulunabilir. Bu osteoid doku tümör hücreleri tarafından periferal peritümöral 34
35 dokudan meydana getirilir. Tümör içerisinde sık sık difüz ve interstisyel kanama meydana gelebilir ve anevrizmal kemik kistinde olduğu gibi kanla dolu kaviteler oluşabilir. Kanamaya ve nekroze sekonder köpüksü hücre akümülasyonu, kolesterol yarıkları ve hemosiderin granülleri bulunabilir (5, 29). Histolojik olarak tümörün tanınabilmesi ve sarkomatöz differansiasyonun olup olmadığının araştırılması amacı ile farklı lokalizasyonlardan çok sayıda örneklerin alınması gerekmektedir (28, 31). Tümörlerin bir kısmının maligniteye dönüşme riski ve bu riskin tümöre ait spesifik bir alandan gelişebileceği göz önünde bulundurulduğunda çok sayıda biopsinin farklı lokaliazsyonlardan alınması gerektiğinin önemi ortya çıkmaktadır (20). Jaffe ve Linchtenstein a göre DHT aggresif davranışa göre üç histolojik grade e ayrılmaktadır. Ancak bu gradeleme sistemi tümörün klinik davranışı ile korele olmadığından kullanılmamaktadır. Bu nedenle DHT ün transforme olabileceği sarkomdan ayrılması önemlidir. Sarkomatöz differansiasyon fibrosarkom, osteosarkom veya malign fibröz histiyositomaya olmaktadır (5, 13, 29) Histogenezis Yapılan son çalışmalarda ve elektron mikroskopik incelemelerde stromal hücrelerin fibroblastik ve histiyositik olmak üzere iki hücre tipinden köken alındığı saptanmıştır. Bu nedenle de tümörün histiyo-fibroblastik hücrelerden geliştiği bilinmektedir (20, 31). Dev hücreler stromal hücrelerin birleşmesinden meydana gelmektedir. Bazı çaılşmalarda ise dev hücrelerin transforme monositlerden köken aldığını savunulmaktadır (15). Bu dev hücreleri normal osteoklastlardan veya diğer iskelet sistem lezyonlarında görülebilen dev hücrelerden ayırmada histokimyasal ya da elektron mikroskopik bir özellik bulunmamaktadır (31, 32). 35
36 Tanı Tanı klinik ve radyolojik veriler eşliğinde hastanın yaşı ve tümörün yerleşim yeri de göz önünde bulundurularak yapılmalıdır. DHT ler arasında büyüme kartilajını ve metafizi de tutan tümörler bulunmaktadır. Metafiziyel yerleşimli bir tümörde büyüme kartilajı hala sağlam olarak görülüyor ise DHT tanısı verilirken dikkatli olunmalıdır. Büyüme kartilajı sağlam, tümör epifiz ve metafizi tutuyor ise tümörün kondroblastom olma ihtimali yüksektir. Post pübertal dönemde kartilaj görünmüyorsa, osteolitik tümör epifiz ve metafizde ise radyografik olarak tümörün kondroblastoma, kronik abse, hiperparatiroidizme sekonder gelişen Brown tümör, kondrosarkom, fibrosarkom, osteolitik osteosarkom, epitelyal metastaz ve soliter plazmositom gibi diğer osteolitik lezyonlardan ayrılması gerekmektedir (5, 32, 33). Radyografik ayırıcı tanı Kondrosarkomada osteolitik alan iyi bir sınırla çevreden ayrılmıştır. Kenarda ince bir hiperostozis alanı ve intratümöral kalsifikasyon ve ossifikasyon bulunur. Kemik korteksini inceltmez, kalınlaştırır. Hiperparatiroidizme sekonder gelişen Brown tümör eğer soliter ve epifizde yerleşimli (genellikle meta-diafizel yerleşimlidir) ise radyografik olarak DHT ile benzer görüntü sergiler. Ancak tümörü çevreleyen kemik tipik olarak laküner osteoporoz meydana getirir (33). Santral kondrosarkomda korteks ayrılmış veya kalınlaşmıştır. Đntratümöral radyoopasite ve periostta osteogenetik reaksiyon mevcuttur. Epifizyal bölgede görülebilecek kondrosarkomun şeffaf hücreli varyantı radyografik olarak DHT ile karışabilir. Fibrosarkom invaziv karakter sergiler ve sınırları düzensizdir. Buna rağmen radyografik ayırım mümkün değildir. DHT ün sarkomatöz differansiasyonundan da ayırım zordur. Ayırım hastanın hikayesi, hastaya ait daha önceki radyogramlar ve 36
37 histolojik olarak daha önceki veya aynı zamanda bulunan DHT varlığı ile yapılmalıdır (5, 33). Osteolitik osteosarkom radyografik olarak DHT ile karışmamakla birliktre nadir görülen formu olan hemorajik osteosarkom DHT den ayrımı güç bir radyografik görüntü oluşturabilir. Epitelyal metastaz erken evrede düzensiz sınırların bulunması ve korteks düzensizliği yapması sebebiyle DHT ile benzer radyografik görüntü oluşturabilir. Soliter plazmositom düzensiz sınırların ve ekpansif gelişim paterninin bulunması nedeni ile radyografik olarak DHT ile benzer örüntüye sahip olabilir (33). Histolojik ayırıcı tanı Histolojik olarak DHT ün, hiperparatiroidizme sekonder gelişen Brown tümörden ayırımı oldukça güçtür. Ayrıca oldukça kanamalı DHT ler anevrizmal kemik kisti ile hemen hemen benzer morfolojik özellikler içerir (32, 34). Tiroid, pankreas ve akciğer gibi organlara ait karsinomlar seyrek olmamakla birlikte benzer görünüm sergileyebilir. Çok nadir olarak ise kondroblastom, histiyositik fibrom, osteoblastom ve benign fibröz histiyositom benzer morfolojik görüntü içerebilir(33) Tümörün Prognozu Tümörün gidişatı değişken ve belirsizdir. Ancak gidişat tümörün histolojik görüntüsü ile orantılı olarak değişmektedir. Agresif histolojik görüntüye sahip bir tümör daha hızlı ilerleyebilmektedir. Bununla birlikte tipik bir DHT görüntüsüne sahip bir tümör daha hızlı ve agresif gelişim paternine sahip olabilir. Sonuç olarak DHT yavaş büyüyüp yıllarca sessiz kalabilirken, birkaç haftada invaziv bir karakter sergileyebilmektedir (20, 28). Tümörün rekürrensi eğer inkomplet bir eksizyonel cerrahi uygulanmış ise cerrahiden sonra 3 yıl içinde gerçekleşmektedir. Nadir vakalarda rekürrens 3 yıldan fazla sürede ortaya çıkmaktadır. DHT aynı zamanda yumuşak dokuya doğru da gelişim 37
38 gösterebilmektedir. Ekstraskletal rekürrens ise daha çok cerrahi yara bölgesinde ve greftin yerleştirildiği alanda sıklıkla kemikleşme şeklinde ortaya çıkmaktadır (5). %1-2 vakada DHT AC metastazı yapabilmektedir. Metastatik tümör histolojik olarak primer tümör ile aynı görüntüdedir. Metastazlar genellikle yavaş gelişim gösterir ve survivi kısaltmaz. Nadir olarak ise popliteal ve inguinal bölge gibi yerlere lenf nodu metastazı yapabilmektedir (35, 36, 37). Benign DHT den sekonder malign DHT gelişimi nadir olarak görülmekle birlikte (tüm DHT lerin %5 inden az) ilk defa Hutter ve Dahlin tarafından sarkomatöz büyüme olarak tanımlanmıştır (38, 39). Malign transformasyon genellikle primer tümöre uygulanan radyasyon terapisi sonrası gelişmektedir. Literatürde birkaç vaka gibi çok daha nadir olarak ise cerrahi tedavi sonrasında görüldüğü bildirilmiştir (40). Sarkomatöz differansiasyon 3 şekilde ortaya çıkmaktadır (32, 38): 1. Tedavi edilmemiş DHT ün spontan transformasyonu: Nadir olarak görülmekle birlikte demonstre etmek zordur. 2. Opere edilmiş ancak radyasyon almamış lokal rekürrensli DHT den: Nadir olarak ortaya çıkar, ancak iyi tanımlanmıştır. 3. Opere edilmiş ve radyasyon almış DHT den: En sık görülen formdur. Sekonder olarak sarkom gelişen olguların yaklaşık yarısında görülmektedir Tedavi ve Prognoz Yakın geçmişe kadar DHT %40 kadar yüksek oranlarda lokal rekürrens gösteren intralezyonel eksizyon (küretaj) ile tedavi edilmekteydi. Ancak bu yöntem tümör evrelemesine imkan vermediği gibi lokal adjuvanların kullanılmasını da engellemekteydi. Küretaj ve birlikte kullanılan adjuvan terapi (fenol ve metilmetakrilat) ile rekürrens riski %10 lara düşmüştür. DHT de son zamanlarda kullanılan temel tedavi yöntemi cerrahi eksizyondur (26, 41). Đntralezyonal eksizyon (küretaj) ya da en-blok rezeksiyon lokal yayılımlı tümörlere uygulanmaktadır (35). En-blok rezeksiyonun en büyük dezavantajı rezeke edilen segment eğer diz, dirsek gibi alanlar ise yapılan cerrahi 38
39 yöntemin kompleks rekonstrüksiyon gerektirebilmesi ve önemli fonksiyonel defisit oluşturabilmesidir (42). Lokal rekürrens riski lezyonun aggresivitesi ile orantılıdır (26). Serilerde lokal rekürrens riski sessiz tümörlerde %7, aktif tümörlerde %26 ve aggressif tümörlerde %41 olarak bulunmuştur. Multiple lokal rekürrens gösteren tümörlerde metastaz da sık görülmektedir (35). Agresif davranış sergileyen ve yaygın deri infiltrasyonu olan tümörlerde tedavi amputasyon olmalıdır (26). Đntralezyonel eksizyonun endike olduğu durumlar stage 1,2 ve bazı grade 3 tümörler ile biyolojik ve mekanik olarak hareketi sağlayabilecek, rekonstrüksiyona izin verecek bölgelerde oluşan tümörlerde olmaktadır. Eğer tümör kortikal duvarı inceltmiş ise uygulanılacak tedavi en blok eksizyon olmalıdır (41, 43). En blok rezeksiyon stage 3 ve yaygın tümörlerde uygulanmaktadır. Daha çok ise distal radius, el ve ayak tubular kemiklerde, proksimal fibula ve ilium gibi kemiklere yapılmaktadır. Eklem kapsülü ve ligamentler ile çevre yumuşak dokuya invazyon gösteren tümörlere de uygulanabilmektedir. Marjinal ve geniş eksizyondan sonra lokal rekürrens insidansı neredeyse sıfıra inmektedir (41, 43). En-blok rezeksiyon stage 2 ve 3 vakalarda tercih edilmelidir. Bu tedavi şekli hastalığı genellikle tam olarak eradike eder, çok düşük nüks oranlarına sahiptir. Ancak hastanın fonksiyonel kapasitesini olumsuz etkiler. Komplikasyon gelişim riski geniş rezeksiyon sonrası intralezyonel eksizyona oranla daha yüksek olmaktadır (18, 42). Vertebral lokalizasyonlu tümörlerde küretaj ve internal osteosentezden sonra radyasyon terapisinin uygulanması lokal rekürrensi azaltmaktadır (44). Pulmoner metastaz cerrahi uygulamadan sonra radyasyon terapisi ile tedavi edilmelidir. Kemoterapi efektif olmamaktadır. Bu şekilde olan tümörler başarı ile tedavi edilse bile nadir vakalarda ilerlemekte ve sonuç ölüm olabilmektedir (37,45). 39
40 Sarkomlar ise geniş ya da radikal cerrahiyi takiben kemoterapi ile tedavi edilmektedir. Kemoterapi sonrası survive %20 lere çıkmaktadır. DHT de lokal rekürrens ya da metastaz cerrahiden en fazla 3 yıl kadar sonra ortaya çıkmaktadır. Bu nedenle ilk 3 yılda primer tümör lokalizasyonu ve akciğerler mutlaka belli aralıklar ile takip edilmelidir (44). Sonu ölüm ile biten tümörlerin çoğu genellikle vertebra ve sakroiliak eklem gibi inoperable tümörler, kontrol edilemeyen akciğer metastazı yapan tümörler ve sarkoma differansiasyon gösteren tümörlerde olmaktadır. Böyle vakalarda bile radyasyon terapisinin kullanılması ile ölüm oranları %5 kadar azaltılabilmiştir (42). 40
41 3. MATERYAL-METOD 3.1. Olgu Seçimi ve Doku Mikroarrey (TMA) Blokların Hazırlanması Bu çalışmada yılları arasında, Ankara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı nda raporlanmış 25 vakaya ait, yılları arasında, Erekul Patoloji Laboratuarında raporlanmış 34 vakaya ait, amputasyon, tümör rezeksiyonu ve kemik küretaj materyalleri ile Ankara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı nda 2000 yılında raporlanmış DHT metastazı bulunduran 1 adet akciğer wedge rezeksiyon materyali incelenmiştir. Küçük doku içeren, geniş nekrozlu ve kanamalı, 2 doku silindiri almaya yetecek canlı tümör hücresi içermeyen materyaller çalışmaya dahil edilmemiştir. Böylece toplam 60 olgu değerlendirilmiştir. Olguların H.E boyalı kesitleri ışık mikroskobi ile yeniden incelenmiş ve her vaka için tümörlü alanlar cam kalemi ile çizilerek işaretlenmiştir. Tümörlü alanları çizilmiş bu H.E boyalı kesitler ile olguların parafin blokları eşleştirilmiştir. Mikroarrey işlemi için bu tümörlü bloklar verici blokları, normal parafin bloklardan daha yüksek ve daha enli hazırlanmış, normal parafinden farklı olarak 57 derecede eriyen plastik parafin ile doldurulmuş bloklar alıcı blokları olarak kullanılmıştır. Alıcı blok düzgün bir yüzey elde edilene kadar tıraşlanmış ve daha sonra Beecher Instruments Microarrey ile alıcı blokta 1mm çap ve 3-4mm yükseklik gösteren kuyular açılmıştır. Her bir kuyuya verici bloktan alınan tümörlü doku yerleştirildikten sonra, her bir doku silindiri arasında 2mm mesafe kalacak şekilde, aynı sıra ile işleme devam edilmiştir. Olgular her bir sırada bir kontrol dokusu ve bir TMA bloğunda 6 sıra, her bir sırada 11 doku silindiri bulunacak şekilde hazırlanmış haritalara göre yerleştirilmiştir. Bu şekilde bir blokta toplam 66 doku silindiri elde edilmiştir. Tüm vakalardan alınan 2 şerli tümörlü doku silindiri ve kontrol dokularına ait silindirler 2 adet TMA bloğu ile gösterilmiştir. Bu TMA bloklarından 4 mikron kalınlığında kesitler alınmış, birer kesit H.E boyanmış, diğer kesitler ĐHK sal boyamalarda kullanılmıştır. 41
42 3.2. Klinik Đnceleme DHT vakalarından 54 ünün klinik bilgisine ulaşılabilmiştir. Vakaların yaş, cinsiyet, şikayet, şikayet süresi, tümör lokalizasyonu, yapılan cerrahi müdahale, nüks olup olmadığı gibi klinik bilgileri kaydedilmiştir Đmmünhistokimyasal Đnceleme Kullanılan antikorların özellikleri Kullanılan antikorların klonları, dilüsyonları, Pretreatment yöntemleri ve ticari kaynakları Tablo 3 de belirtilmektedir. Tablo 3: Đmmünhistokimyasal antikorların özelllikleri Antikor Klon Dilüsyon Pretreatment Ticari Kaynak P53 DO-7+BP :200 Cell Condition Standart Neomarkers Ki67 SP6 1:200 Cell Condition Mild Lab Vision CD117 T595 1:400 Cell Condition standart Novocastra c-myc 9E11 1:400 Cell Condition standart Novocastra Kullanılan Kontroller ĐHK sal boyamalarda CD117 için gastrointestinal stromal tümör ve mast hücreleri, c-myc için kolon, vajen yassı hücreli karsinomu ve lenf nodülü, p53 için prostat karsinomu, Ki 67 için lenf nodülü pozitif kontrol dokular olarak kullanılmıştır. 42
43 Đmmünhistokimyasal boyama Ventana i-view DAB Detection kiti kullanılmış; Ki67, p53, CD117 Ventana Benchmark ĐHK otomatik boyama makinesi ile c-myc için Ventana Benchmark XD ĐHK otomatik boyama makinesi ile boyanmıştır Đmmünhistokimyasal boyanmaların değerlendirilmesi: Đmmünhistokimyasal markerların boyanma şekilleri: Tüm markerlar için tümörün her iki komponentindeki (dev hücreler ve stromal hücreler) boyanma ayrı ayrı değerlendirilmiştir. p53 ve Ki67 için her iki komponenti oluşturan hücrelerdeki nükleer boyanma, CD117 için dev hücreler ve stromal hücrelerdeki sitoplazmik veya membranöz boyanma, c-myc için dev hücreler ve stromal hücrelerdeki perinükleer dot-like boyanma spesifik boyanma olarak kabul edilmiştir. Tüm vakalar için boyanma şiddeti ayrı ayrı değerlendirilmiştir Đmmünhistokimyasal markerların boyanma skorları Her bir immünhistokimyasal marker için boyanma skoru boyanma yaygınlığına ve şiddetine göre tüm doku silindirlerine tek tek yüzde verildikten sonra, literatür bilgileri eşliğinde gruplanarak skor verilmiştir. Buna göre; CD117 ve p53 boyanması, dev hücre ve stromal hücrelerde boyanma yaygınlığı dikkate alınarak ayrı ayrı değerlendirilmiş, 0-3 arasında skorlanmıştır (0:negatif, 1: %10 hücre, 2: %11-50 hücre, 3:% hücre). Dev hücre ve stromal hücre ekspresyon skorları toplanarak, CD117 ve p53 için total boyanma skoru elde edilmiştir. c-myc ekspresyonu, boyanma şiddeti ve yaygınlığı dikkate alınarak değerlendirilip skorlanmıştır. Boyanma şiddeti (hafif:1, orta:2 ve şiddetli:3) ve boyanma yaygınlığı (negatif:0, %20 hücre:1, %21-50 hücre:2, % hücre:3) ayrı ayrı skorlanmış ve bu skorların toplamı ile c-myc için total boyanma skoru elde edilmiştir. Ki67 ekspresyonu, 100 stromal hücre sayılarak her vaka için ayrı ayrı değerlendirilmiştir. 43
44 3.4. TMA Bloklarında Doku Silindirlerinin Değerlendirilmesi ĐHK sal markerlar değerlendirilirken her bir doku silindirinin boyanma şekli ve skoru kaydedilmiştir. Đstatistiksel inceleme aşamasında her vaka için alınan iki doku silindirinden en yüksek boyanma skoruna sahip olan dikkate alınmıştır. Đki doku silindirinin 2 sinin de uygun olmadığı, doku silindirinin tümüyle nekroz içermesi veya kesit sırasında dökülmesi gibi durumlarda o vaka değerelendirmeden çıkartılmıştır Đstatistiksel Değerlendirme Verilerin istatistiksel değerlendirmeleri SPSS 9.0 for Windows bilgisayar programında gerçekleştirilmiştir. Yaş, cinsiyet, lokalizasyon, semptom, klinik evre, tedavi prosedürü, nüks oranları, ortalama takip süreleri ve ĐHK sal markerlar ile boyanma gibi kategorik değişkenlerin değerlendirmesinde Kruskal Wallis, Spearman, Pearson korelasyon ya da Mann-Whitney testi kullanılmıştır. 44
45 4. BULGULAR 4.1. Klinik Bulgular: Çalışma grubunda yer alan 60 vakadan 54 ünün yaş, 55 inin cinsiyet, 53 ünün tümör lokalizasyonu, 42 sinin semptom, 27 sinin klinik evre, 42 sinin takip süresi ve 37 sinin nüks bilgisine ulaşılabilmiştir. Yaşları bilinen 54 vakanın 26 sının erkek (%47,3), 29 unun ise kadın (%52,7) olduğu saptanmıştır. Erkek: Kadın oranı 0,9 olarak bulunmuştur. Vakaların yaş ortalaması 33,33 (15-65 yaş) olarak belirlenmiştir. 59 vakanın primer tümör, 1 vakanın ise akciğer metastazı olduğu gözlenmiştir. Tümör lokalizasyonu açısından değerlendirildiğinde olguların femur (n:15), tibia (n:10), radius (n:7), humerus (n:5), fibula (n:4), vertebra (n:2), falanks (n:1), kosta (n:1), malleol (n:1), olekranon (n:1), patella (n:1), sakrum (n:1), paranazal sinüs (n:1), sternum (n:1), ulna (n:1) ve AC de kitle (n:1) yerleşimli olduğu belirlenmiştir (Tablo 4). Tablo 4: Tümörün Lokalizasyonlara Göre Dağılımı Tümör Lokalizasyonu Femur %25 (n: 15) Tibia %16,7 (n: 10) Radius %11,7 (n:7) Humerus %8,3 (n:5) Fibula %6,7 (n:4) Vertebra %3,3 (n:2) AC kitle, Falanks, Kosta, Malleol, Olekranon, Patella, Sakrum, Sinüs, Sternum, Ulna %1,7 (n:1) 45
46 Klinik seyri bilinen 42 hastada en sık semptom sırasıyla ağrı (%54,8), ağrı+kitle (%16,7), ağrı+patolojik kırık (%16,7), ağrı+his kaybı (%2,4) ve patolojik kırık (%2,4) olarak tesbit edilmiş; 3 hastanın (%7,1) asemptomatik olduğu belirlenmiştir (Tablo 5). Tablo 5: Semptomlara göre vakaların dağılımı Semptom Asemptomatik %7,1 (n: 3) Ağrı %54,8 (n: 23) Ağrı+Kitle %16,7 (n: 7) Ağrı+Patolojik Kırık %16,7 (n: 7) Ağrı+His Kaybı %2,4 (n: 1) Patolojik Kırık %2,4 (n: 1) 25 hastada klinik evre (stage) bilgisine ulaşılabilmiş buna göre; 15 hasta (%60) Evre 3, 6 hasta (%24) Evre 2 ve 4 hasta (%16) Evre 1 şeklinde evrelendirilmiştir. Tablo 6: Tümörün Klinik Evreye Göre Dağılımı Klinik Evre Evre 1 %16 (n: 4) Evre 2 %24 (n: 6) Evre 3 %60 (n: 15) 46
47 Hastaların ortalama klinik takip süresi 45,98 ay (2-146 ay), nüks oranı %16,2 (6/37 hasta) bulunmuştur. 4.2 Đmmünhistokimyasal Bulgular: TMA bloklarında 2 vakada, teknik nedenlerle inceleme yapılamamıştır. p53 ekspresyonu 23 vakada (%29,7) tesbit edilmiştir. p53 boyanması 21 vakada (%36,1) sadece dev hücre komponentinde, 15 vakada (%25,8) ise sadece stromal hücre komponentinde görülmüştür. Total skor Tablo 7 de belirtilmiştir. Tablo 7: Tümörde total p53 skoru dağılımı Skor 0 %60,3 (n: 35) Skor 1 %12,1 (n: 7) Skor 2 %10,3 (n: 6) Skor 3 %6,9 (n: 4) Skor 4 %6,9 (n: 4) Skor 5 %1,7 (n: 1) Skor 6 %1,7 (n: 1) CD117 reaktivitesi 11 vakada (%19) görülmüştür. 11 vakada (%19) sadece dev hücre komponentinde, 1 vakada (%1,7) ise sadece stromal hücre komponentinde saptanmıştır. Dev hücre ve stromal hücrelerdeki total boyanma skoru Tablo 8 de belirtilmiştir. 47
48 Tablo 8: Tümörde total CD117 skor dağılımı Skor 0 %81 (n: 47) Skor 1 %5,2 (n:3) Skor 2 %6,9 (n: 4) Skor 3 %6,9 (n: 4) c-myc ekspresyonu 48 vakada (%82,8) saptanmıştır. Tümörde c-myc yaygınlık ve şiddeti toplanarak elde edilen total skoru Tablo 9 da gösterimiştir. Tablo 9: Tümörde total c-myc skoru dağılımı Skor 0 %17,2 (n:10) Skor 2 %20,7 (n:12) Skor 3 %1,7 (n:1) Skor 4 %6,9 (n:4) Skor 5 %39,7 (n:23) Skor 6 %13,8 (n:8) Olgularda Ki67 immünreaktivitesi ile belirlenen proliferasyon indeksi ortalama %12,66 (4-50) bulunmuştur. 48
49 Ki67 boyanması ile nüks ve klinik evre arasında istatistiksel bir ilişki bulunamamıştır. Ki67 indeksi ile p53 ekspresyonu arasında istatistiksel olarak anlamlı bir ilişki bulunmuş, (p:0.007, r: 0,351 Pearson correlation test) ancak aynı korelasyon Ki67 indeksi ile CD117 ve c-myc ekspresyonu arasında bulunmamıştır. c-myc boyanma skoru ile p53 skoru arasında (p:0.000, r:0,446, Pearson correlation test) ve CD117 skoru arasında pozitif bir korelasyon saptanmıştır (p:0.014, r:0,320, Pearson correlation test). p53 boyanma skoru ile CD117 boyanması arasında pozitif bir korelasyon saptanmıştır (p:0.008, r:0,344, Pearson correlation test). Klinik evre ve nüks ile p53, CD117 ve c-myc ekspresyonu arasında ilişki bulunamamıştır (p>0.05, Spearman s test). Ancak c-myc skorunun 1 birim artışında nüks riskinin 1,53 oranında artmış olduğu saptanmıştır. Nüks ile yaş, cinsiyet, tümör lokalizasyonu ve semptomlar gibi klinik parametreler arasında ilişki bulunmamıştır.. 49
50 Resim 4: TMA bloklar Resim 5: H.E ve ĐHK boyalı lamlar Resim 6: HE boyalı kesitler 50
51 Resim 7: Ki 67 boyanması Resim 8: p53 boyanması 51
52 Resim 9: CD117 boyanması Resim 10: c-myc boyanması 52
53 5. TARTIŞMA DHT kemiğin nadir görülen bir tümörü olup tüm primer kemik tümörlerinin %5-8 ini oluşturmaktadır (17). Kadınlarda erkeklere oranla biraz daha fazla görülmekte ve pik insidansını 2. ve 3. dekadda göstermektedir (27). Çalışma serimizde literatürler ile uyumlu olarak E/K oranı 0,9, vakaların yaş ortalaması 33,33 (15-65 yaş) olarak bulunmuştur. Distal femur ve proksimal tibia en sık tutulan lokalizasyondur. Tümör genellikle uzun kemiklerin meta-epifiziyal bölgesine yerleşmektedir (5). Çalışmamızdaki vakalar tümör lokalizasyonu açısından değerlendirildiğinde; olguların %25 i femur, %16,7 si tibia, %11,7 si radius, daha az oranlarda ise humerus, fibula, vertebra, falanks, kosta, malleol, olekranon, patella, sakrum, paranazal sinüs, sternum ve ulna yerleşimli olduğu belirlenmiştir. Tümörün en önemli özelliğinden biri biyolojik davranışının net olarak bilinmemesidir. Benign ancak lokal agresif olduğu bilinen bu tümörlerde nadir de olsa malignite riski bulunmaktadır (15, 31). Çalışmamızdaki vakalardan 59 u primer kemik tümörü, bir vaka AC metastazı özelliğindedir. Lokal agresif davranan, multipl rekürrens gösteren ve daha agresif görünüşlü tümörlerin AC metastazı açısından daha fazla risk taşıdığı bilinmektedir (15, 17, 19). Serimizde nüks bilgisine ulaşılan 37 vakadan sadece 6 sında (%16,2) nüks olduğu tespit edilmiştir. Bu vakalardan üçünde küretaj ve otogreftleme tedavi yöntemi olarak uygulanmıştır. Nüks bulunan diğer 3 vakada tedavi yöntemi bilinmemektedir. Nüksün olduğu vakalarda tümörün lokalizasyonları sakrum, proksimal femur, vertebra, distal femur (2 vaka) ve proksimal tibiadır. Gupta ve ark. nın yaptığı bir çalışmada ise nüks oranı %36,1 olarak bulunmuştur (19). Đki çalışma arasındaki bu anlamlı fark çalışmamızdaki vakaların bir kısmının nüks bilgisine ulaşılabilmesine, bunlar arasında da çok az nüks vaka olmasına ve Gupta ve ark nın yaptığı çalışmada geniş bir seri ve bu seride daha fazla nüks vaka olmasına bağlanmıştır. Lokal rekürrens riski pelvis ve sakrum yerleşimli tümörlerde diğer yerleşim yerlerine göre daha fazla oranda görülmektedir (46). Bunun nedeni ise tümörün yerleşim yerinin kompleks olması, klinik olarak geç bulgu vermesi ve cerrahi olarak tam çıkarılamamasından kaynaklanmaktadır (46). 53
54 Semptom açısından değerlendirildiğinde ise vakaların %54,8 i (n: 23) ağrı şikayeti ile başvurmuştur. Sonra ağrı ve kitle, ağrı ve patolojik kırık, ağrı ve his kaybı ve patolojik kırık en sık karşılaşılan semptom olmuştur. Gupta ve ark nın 470 vakalık seride yaptığı çalışmada da en sık karşılaşılan semptom ağrı ve kitle olmuştur (19). Daha önce literatürde yapılan çok az sayıda, çok az seri ile yapılan çalışmalarda; Ki67 proliferasyon indeksi, p53, CD117 ve c-myc ekspresyonlarının kemiğin dev hücreli tümörlerinde tümörün biyolojik davranışı ve nüks varlığı ile ilişkili olduğuna dair sonuçlar bulunmaktadır (17, 40, 47, 48, 49, 50, 51). Serimizde Ki67 ile dev hücrelerde boyanma izlenmemiş, stromal hücrelerde boyanmanın bulunduğu saptanmıştır. Ki67 ile yapılmış diğer çalışmalarda da dev hücrelerde boyanmanın bulunmadığı görülmüştür (48). Çalışmamızda Ki67 immünreaktivitesi ile belirlenen proliferasyon indeksi ortalama %12,66 (4-50) bulunmuştur. Antal ve ark nın yaptıkları 50 vakalık bir çalışmada ise grade I tümörlerde Ki67 proliferasyon indeksi %7,5, grade II tümörlerde %13 ve grade III tümörlerde %14 bulunmuştur (17). Çalışmamızda nüks bulunan vakalarda sakrum yerleşimli tümörde Ki67 ile %50 kuvvetli, proksimal femur yerleşimli tümörde %40 kuvvetli, L4 vertebra ve proksimal tibia yerleşimli tümörde %5 kuvvetli, distal femurda yerleşimli tümörlerde %20 ve %10 proliferasyon indeksi saptanmıştır. Daha öncede belirtildiği gibi sakrum yerleşimli tümörler lokalizasyonları nedeni ile daha agresif seyirli olabilmektedir. Bizim çalışmamamızda yer alan sakral tümörde de literatür ile uyumlu olarak proliferasyon indeksi %50 gibi yüksek oranlarda bulunmuş ve bu vakada nüks bulunduğu saptanmıştır (46). AC metastazı özelliğindeki tümörde Ki67 proliferasyon indeksi %20 olarak belirlenmiştir. Cai ve ark. multipl ve bilateral AC metastazı gösteren DHT bulunan bir olguda metastatik tümörde Ki67 ve p53 ile sadece stromal hücrelerde %20 oranında boyanma tespit etmişlerdir (49). Antal ve ark nın yaptıkları bir çalışmada Ki67 boyanması ile nüks ve klinik evre arasında ilişki saptanırken, çalışmamızda istatistiksel bir ilişki bulunamamıştır (17). Osaka ve ark. 2 akciğer metastazı bulunan 5 vakalık bir seride malign transformasyon gösteren hücrelerin p53 ile boyandığını ve bu hücrelerin Ki67 ile de pozitif boyanma gösterdiğini belirtmişlerdir (47). Çalışmamızda da Ki67 indeksi ile p53 ekspresyonu 54
55 arasında istatistiksel olarak anlamlı bir ilişki bulunmuştur (p:0.007, r: 0,351 Pearson correlation test). Ancak aynı korelasyon Ki67 indeksi ile CD117 ve c-myc ekspresyonu arasında bulunamamıştır. Daha önceki çalışmalarda p53 ekspresyonunun varlığı da rekürrens ve metastaz ile ilişkili bulunmuştur (40, 42, 47, 49, 52). Oda ve ark. klinik takipli 103 DHT olgusundan sadece ikisinde AC metastazı geliştiğini saptamışlar ve bunlarda ĐHK sal ve moleküler yöntemler ile p53 antikoru çalışmışlardır. p53 ile sadece bir vakada metastatik lezyonda ĐHK sal olarak boyanmanın, PCR yöntemi ile de nokta mutasyonunun bulunduğunu tespit etmişlerdir (40). Masui ve ark. da 47 vakalık serilerinde 6 vakada stromal hücrelerde p53 ekspresyonunu izlemişler ve bunlardan 3 ünde AC metastazı, 4 ünde rekürrens bulunduğunu saptamışlardır (42). Cai ve ark. multipl ve bilateral AC metastazı bulunan bir vakada mononükleer hücrelerde p53 ile %20 oranında boyanmanın bulunduğunu tespit etmişlerdir (49). Çalışmamızda nüks ve metastatik vaka sayısının az olması nedeni ile böyle bir ilişki bulunamamıştır. Ancak nüks bulunan sakrum yerleşimli tümörde, nüks bulunan diğer tümörlere göre biraz daha fazla oranda p53 boyanması bulunduğu görülmüştür. Bununla birlikte çalışmamızda Ki67 indeksi ile p53 ekspresyonu arasında istatistiksel olarak anlamlı bir ilişki bulunmuştur (p:0.007, r: 0,351 Pearson correlation test). Tümör rekürrens ve metastazı ile ilşkili olduğu düşünülen bir diğer marker da CD117 dir. DHT lerde CD117 ile yapılmış sınrlı sayıda çalışma bulunmaktadır. Bunlardan biri Gattei ve ark nın yaptığı çalışmadır. Bu çalışmada indirekt immünflorasan yöntemi kullanılarak kemik iliğinde preosteoklastik mononükleer hücrelerde, kemikteki multinükleer osteoklastik hücrelerde ve DHT de c-kit ekspresyonunun bulunduğu saptanmıştır (53). Yamazaki ve ark. ise prekürsör hücrelerdeki osteoklast differansiasyonunu, c-kit bağımlı ve bağımsız olmak üzere (daha çok c-kit bağımlı) ortaya çıktığını savunmuşlardır (54). Bunu takip eden çalışma ise 55
56 Haydon ve ark nın yaptığı çalışmadır. Buna göre çalışmaya alınan 10 DHT vakasında da kuvvetli c-kit boyanmasının bulunduğu saptanmıştır. Sekans analizinde ise bu 10 vakadan 2 sinde c-kit geninde mutasyon bulunduğu görülmüştür (55). Tüm bu çalımalar sonucunda c-kit in osteoklast differansiasyonu ile ortaya çıktığı sonucuna varılmıştır. Son çalışmalardan biri ise Ramos ve ark. nın yaptığı çalışmadır. Bu çalışmada 35 DHT vakası kullanılmış, bunlarda 1:25 ve 1:50 antikor dilüsyonlarında stromal hücrelerde boyanma izlenirken, dev hücrelerde boyanma bulunmadığı görülmüştür. Ancak 1:100 ve 1:200 dilüsyonlarda c-kit boyanmasının bulunmadığı saptanmıştır (56). Çalışmaların neticesinde c-kit ekspresyonunun, tümörün fonksiyonel aktivitesini göstermediği ve c-kit boyanmasının antikor konsantrasyonuna bağımlı olduğu belirtilmiştir. Bu nedenle de c- kit gen ekspresyon analizi ve immünblotting yöntemlerinin DHT lerde c-kit varlığını göstermede daha sensitif yöntemler olduğu sonucuna varılmıştır. Çalışmamaızda ise CD117 reaktivitesi 11 vakada (%19) görülmüştür. 11 vakada (%19) dev hücre komponentinde, 1 vakada hem dev hücre hem stromal hücrelerde (%1,7) boyanma saptanmıştır. Nüks gösteren vakalardan ise sadece sakrum yerleşimli tümörde dev hücre komponentinde boyanma bulunduğu izlenmiştir. CD117 ile Ki67 ekspresyonu, klinik evre ve nüks arasında bir ilişki göstermezken, CD117 ile c-myc boyanma skoru (p:0.014, r:0,320, Pearson correlation test) ve p53 boyanma skoru (p:0.008, r:0,344, Pearson correlation test) arasında bir ilişki bulunduğu saptanmıştır. Çalışmamızda kullandığımız diğer bir marker ise c-myc antikorudur. C-myc 8. kromozomda yerleşen bir proto-onkogendir. C-myc geni başka bir transkripsiyon faktörü olan max ı kodlamaktadır. C-myc amplifikasyonu ilk kez insan promyelositik lösemide yüksek seviyelerde saptanmıştır. Daha sonra ise bazı karsinomalarda, nöroblastomada, glioblastomada ve bazı mezenşimal tümörlerde de bulunduğu belirtilmiştir (Gamberi G). Gamberi ve ark. 45 vakalık DHT (32 primer, 13 AC metastazı) serilerinde ĐHK sal c-myc antikoru çalışmışlar ve in-situ hibridizasyon yöntemiyle mrna ve 56
57 protein analizini gerçekleştirmişlerdir. Buna göre metastatik vakaların %69 unda, hastalıksız yaşayan vakaların %16 sında c-myc mrna ekspresyonunun bulunduğunu saptamışlardır. C-myc protein overekspresyonunu ise AC metastazı bulunan vakaların %54 ünde ve hastalıksız yaşayan vakaların %26 sında tespit etmişlerdir. ĐHK sal olarak AC metastazı bulunan vakaların %62 sinde, hastalıksız yaşayan vakaların %21 inde c- myc boyanmasının bulunduğunu izlemişlerdir. Sonuçta c-myc overekspresyonunun metastatik yayılımda ve prognozda önemli role sahip olduğu kanaatine varılmıştır (51). Aynı zamanda mononükleer hücreler ve dev hücrelerin her ikisinin birden c-myc pozitifliği göstermesi, dev hücrelerin mononükleer hücreler ile aynı histogenetik yapıya sahip olduğu görüşünü düşündürmüştür (51) Oda ve ark nın yaptıkları çalışmada rekürrens gösteren iki vakadan birinde rekürrens gösteren tümörde c-myc pozitifliği görülmüştür (40). Çalışmamızda ise c-myc boyanma skoru ile p53 skoru arasında (p:0.000, r:0,446, Pearson correlation test) ve CD117 skoru arasında pozitif bir korelasyon saptanmıştır (p:0.014, r:0,320, Pearson correlation test). Klinik evre ve nüks ile c-myc ekspresyonu arasında ilişki bulunamamıştır (p>0.05, Spearman s test). Ancak c-myc skorunun 1 birim artışında nüks riskinin 1,53 oranında artmış olduğu saptanmıştır. Sonuçta çalışmamızda p53, CD117 ve c-myc ekspresyonlarının birbiriyle ilişkili olduğu bulunmuş; ancak nüksü öngörmedikleri sonucuna varılmıştır. Nüks bilgisine ulaşılan ve nüks gösteren vaka sayısının az olması, sonuçlarımızın literatürdeki sonuçlarla uyumsuzluğunun bir başka nedeni olabilir. c-myc protein ekspresyonu ve nüks arasındaki pozitif uyum, nüks vaka sayısının daha fazla olduğu serilerde kromojenik in situ hibridizasyon gibi daha sensitif yöntemlerle c-myc amplifikasyonunun araştırılması yolunda umut vaat etmektedir. Serimizde sınırlı sayıda metastatik vaka yer aldığından, primer ve metastatik tümörler arasında söz konusu immunhistokimyasal markerların ekspresyon profili karşılaştırılamamıştır. Serimizde yer alan Ki67 indeksi yüksek olgularda p53 ekspresyonunun da buna paralel olarak arttığı belirlenmiştir. 57
58 6. SONUÇLAR Çalışmada toplam 60 vaka değerlendirmeye alınmış, ancak 2 vaka teknik nedenlerle değerlendirilememiştir. Cinsiyetleri bilinen 54 vakanın 26 sı erkek (%47,3), 29 u kadındır (%52,7). Erkek: Kadın oranı 0,9 olarak bulunmuştur. Vakaların yaş ortalaması 33,33 (15-65 yaş) dür. 59 vaka primer tümör, 1 vaka akciğer metastazı özelliğindedir. Primer tümörlerde en sık yerleşim yeri femurdur (%28,3). Vakalar arasında en sık karşılaşılan semptom ağrıdır (%54,8). Küretaj+greftleme en sık kullanılan tedavi yöntemi (%13,3) olmuştur. Nüks bilgisine ulaşılan 37 vakadan 6 sında (%16,2) nüks saptanmıştır. Vakaların ortalama takip süresi 45,98 ay (2-146 ay) olarak bulunmuştur. p53 ekspresyonu 23 vakada (%29,7) tesbit edilmiştir. P53 boyanması 21 vakada (%36,1)sadece dev hücre komponentinde, 15 vakada (%25,8) ise sadece stromal hücre komponentinde görülmüştür. CD117 reaktivitesi 11 vakada (%19) görülmüştür. 11 vakada (%19) dev hücre komponentinde, 1 vakada (%1,7) stromal hücre komponentinde saptanmıştır. c-myc ekspresyonu 48 vakada (%82,8) saptanmıştır. Olgularda Ki67 immünreaktivitesi ile belirlenen proliferasyon indeksi ortalama %12,66 (4-50) bulunmuştur. Ki67 boyanması ile nüks ve klinik evre arasında istatistiksel bir ilişki bulunamamıştır. 58
59 Ki67 indeksi ile p53 ekspresyonu arasında istatistiksel olarak anlamlı bir ilişki bulunmuş, (p:0.007, r: 0,351 Pearson correlation test) ancak aynı korelasyon Ki67 indeksi ile CD117 ve c-myc ekspresyonu arasında bulunmamıştır. c-myc boyanma skoru ile p53 skoru arasında (p:0.000, r:0,446, Pearson correlation test) ve CD117 skoru arasında pozitif bir korelasyon saptanmıştır (p:0.014, r:0,320, Pearson correlation test). p53 boyanma skoru ile CD117 boyanması arasında pozitif bir korelasyon saptanmıştır (p:0.008, r:0,344, Pearson correlation test). Klinik evre ve nüks ile p53, CD117 ve c-myc ekspresyonu arasında ilişki bulunamamıştır (p>0.05, Spearman s test). Ancak c-myc skorunun 1 birim artışında nüks riskinin 1,53 oranında artmış olduğu saptanmıştır. Nüks ile yaş, cinsiyet, tümör lokalizasyonu ve semptomlar gibi klinik parametreler arasında ilişki bulunmamıştır. 59
60 7. ÖZET Kemiğin Dev Hücreli Tümörlerinde Histopatolojik Prognostik Kriterlerin Belirlenmesi ve Doku Mikroarrey Blokları Üzerinde Đmmünhistokimyasal CD117, Ki67, c-myc ve p53 Ekspresyonlarının Prognozla Đlişkisinin Araştırılması Giriş: DHT tüm kemik tümörlerinin %4-5 ini, benign primer kemik tümörlerinin ise %20 sini oluşturmaktadır. En sık 2. ve 3. dekadda görülmektedir. Benign ancak lokal agresif seyreden DHT ün histiyo-fibroblastik elementlerden köken aldığı ve multinükleer dev hücreler ile neoplastik stromal hücrelerden meydana geldiği düşünülmektedir. Benign olmasına karşın bu tümör tam olarak belirlenemeyen lokal agresif seyirli olma ve çok nadir olarak malign transformasyon gösterebilme özelliğine sahiptir. Histogenezi net olarak bilinmeyen DHT ün lokal rekürrens veya metastaz potansiyelini öngörmekte kullanılabilecek güvenilir prognostik parametrelere ihtiyaç duyulmaktadır. Literatürde, prognostik kriterleri belirlemek üzere kısıtlı vaka serileri üzerinde yapılmış çok az sayıda çalışma bulunmaktadır. Bu çalışmada klinik takipli 60 vakada (59 vakada primer tümör, 1 vaka AC metastazı) histopatolojik özellikler yanı sıra doku mikroarrey ve ĐHK yöntemleri kullanarak CD117, Ki67, c-myc ve p53 ekspresyonları ve bunların prognozla ilişkileri araştırılmıştır. Materyal ve Metod: yılları arasında, Ankara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı nda değerlendirilen 26 vaka ve yılları arasında Erekul Patoloji Laboratuarında değerlendirilen 34 vakanın oluşturduğu toplam 60 vaka bu çalışmaya dahil edilmiştir. Beecher Instruments Microarrey cihazı yardımıyla her vaka için 1mm çaplı 2 kor biyopsi alınmış ve toplam 2 adet TMA bloğu elde edilmiştir. TMA blokları içerisine pozitif ve negatif kontrol olabilecek diğer dokular da yerleştirilmiştir. TMA bloklarından 4 mikron kalınlığında kesitler alınmış, bu kesitlerden birer örnek H&E ile boyanmış, diğer kesitler üzerinde ĐHK incelemesi yapılmıştır. Ventana otomatik immünboyama cihazı ile CD117, Ki67, c-myc ve p53 antikorları kullanılarak ĐHK incelemesi yapılmıştır. 60
61 Bulgular: CD117, Ki67, c-myc ve p53 ekspresyonları ile tümör nüksü ya da diğer klinik parametreler arasında istatistiksel bir ilişki bulunamamıştır. Ancak c-myc reaktivitesinin, nüks oranı ile paralel bir artış gösterdiği saptanmıştır. P53, CD117 ve c- myc ekspresyonları arasında pozitif korelasyon bulunmuştur. Ki67 ile belirlenen proliferasyon indeksinin, p53 eksprese eden vakalarda yüksek oranda olduğu tesbit edilmiştir. Sonuçlar: Daha önce literatürde yapılan çok az sayıda çalışmada; Ki67 proliferasyon indeksi, p53, CD117 ve c-myc ekspresyonlarının kemiğin dev hücreli tümörlerinde tümörün biyolojik davranışı ve nüks varlığı ile ilişkili olduğuna dair sonuçlar bulunmaktadır. Aksine bu çalışmada p53, CD117 ve c-myc ekspresyonlarının birbiriyle ilişkili olduğu bulunmuş; ancak nüksü öngörmek açısından prediktif olmadıkları sonucuna varılmıştır. Nüks bilgisine ulaşılan ve nüks gösteren vaka sayısının az olması, sonuçlarımızın literatürdeki sonuçlarla uyumsuzluğunun bir başka nedeni olabilir. c-myc protein ekspresyonu ve nüks arasındaki pozitif uyum, nüks vaka sayısının daha fazla olduğu serilerde kromojenik in situ hibridizasyon gibi daha sensitif yöntemlerle c-myc amplifikasyonunun araştırılması yolunda umut vaat etmektedir. Serimizde sınırlı sayıda metastatik vaka yer aldığından, primer ve metastatik tümörler arasında söz konusu immünmarkerların ekspresyon profili karşılaştırılamamıştır. Serimizde yer alan Ki67 indeksi yüksek olgularda p53 ekspresyonunun da buna paralel olarak arttığı belirlenmiştir. 61
62 8. SUMMARY Histopathological and prognostic criteria in giant cell tumor of bone, and the relationship between the prognosis and immunohistochemical expression of CD117, Ki67, c-myc and p53 on tissue microarray blocks. The giant cell tumour of bone (GCT) is a locally aggressive intraosseous neoplasm of obscure biological behaviour. Although well defined in clinical, radiological and histological terms, detailed information on its biological development is still relatively unclear. The tumoral tissue consists of two cell types: neoplastic stromal cells and multinuclear giant cells. GCT usually behaves as a benign tumor, but has a significant tendency to recur locally and rarely may result in the development of lung metastases. Rarely, GCT may transform into a high-grade sarcoma. A few prognostic markers have been reported to predict the clinical outcome of GCT patients, so is needed to find the predictive parameters those can be implicated in its potential aggressiveness. In this study, we aimed to analyse the histopathological features and the expression patterns of CD117, p53, Ki67, c-myc of 60 cases of GCT, using tissue microarray and immunohistochemical methods. There was no statistically significant correlation between the expression of CD117, Ki67, c-myc and p53 with recurrence, as well as other clinical parameters. But, we determined a tendency of increase between c-myc reactivity and the recurrence. We also found a positive correlation between the reactivity of p53, CD117 and c-myc. We observed that the proliferation index determined by Ki67 immunostaining was high in p53 positive tumors. 62
63 9. KAYNAKLAR 1. Blue histology-skeletal Tissues-Bone. School of Anatomy and Human Biology- The University Western Australia 2. Włodarski K, Galus R. The histophysiology of fracture healing. Ortop Traumatol Rehabil Sep 30;2(3): Crofton PM. Bone and bone turnover. Endocr Dev. 2009;15: Epub 2009 Mar 3. Review. 4. Maquis ME, Lord E, Bergeron E, Drevelle O, Park H, Cabana F, Senta H, Faucheux N. Bone cells-biomaterials interactions. Front Biosci.2009 Jan 1:14: Campanacci M. Bone and Soft Tissue Tumors 1990, Bologna Ayvaz M. Aksoy C. Kemiğin tümör ve tümör benzeri lezyonlarına yaklaşım. Hacettepe Tıp Dergisi 2006; 37: Weinstein SL., Buckwalter JA. Turek s orthopedics principles and their application. 5 th ed. Baltimore, Maryland, USA, Springfeld DS,. Radolucaent lesions of the extremities. J Am Acad Orthop Surg 1994; 2: Peabody TD, Gibbs CP, Simon MA. Current concepts rewiev. Ewvaluation and staging of musculoskeletal neoplasms. J Bone Joint Surg Am 1998; 80: Pahade J, Sekhar A, Shetty SK. Imaging of malignant skeletal tumors. Cancer Treat Res. 2008;143: Review 11. Erlemann R. MRI morphology of bone tumors and tumor-like lesions.] Radiologe Jul Carrasco CH, Wallace S, Richli WR. Percutaneous skeletal biopsy. Cardiovasc and Intervent Radiol 1991; 14:
64 13. Jaffe HL, Lichtenstein L, Portis RB (1940) Giant cell tumor of bone.its pathologic appearance, grading, supposed variants and treatment. Arch Pathol 30: Feigenberg SJ, Marcus RB Jr, Zlotecki RA, Scarborough MT, Enneking WF. Whole-lung radiotherapy for giant cell tumors of bone with pulmonary metastases. Clin Orthop Relat Res 2002; 401: Haque AU, Moatasim A. Giant cell tumor of bone: a neoplasm or a reactive condition? Int J Clin Exp Pathol Jan 1;1(6): Hoch B, Inwards C, Sundaram M, Rosenberg AE. Multicentric giant cell tumor of bone. Clinicopathologic analysis of thirty cases. J Bone Joint Surg Am Sep;88(9): Antal I., Sapi Z., Szendröi M. The prognostik significance of DNA cytophotometry and proliferation index (Ki 67) in giant cell tumors of bone. Int Ortho. (1999) 23: Güngör Ş., Arıkan M., Karakaş A. Stage 2 ve 3 kemiğin dev hücreli tümörlerinde kısa dönem tedavi sonuçları. Acta Oncol Turcica, Cilt:37, No.1-2, Gupta R., Seethalakshmi V., Jambhekar NA., Prabhudesai S., Merchant N., Puri A., Agarwal M. Clinicicopathologic pofile of 470 giant cell tumors of bone from a cancer hospital western india. Annals of Diagnostic Pathology 12 (2008) Willüng M., Engels C., Jesse N., Werner M., Delling G.,.Keiser E. The nature of giant cell tumor of bone. J.Cancer Res Clin Oncol : Puri A, Agarwal MG, Shah M, Jambhekar NA, Anchan C, Behle S. Giant cell tumor of bone in children and adolescents. J Pediatr Orthop Sep;27(6): Unni KK. Dahlin s bone tumours: general aspects and data on 1187 cases. 5th edition. Philadelphia: Lippincott-Raven, 1996: Saleh EA, Taibah AK, Naguib M, Aristegui M, Vassallo G. Giant-cell tumour of the lateral skull base: a case report. Otolaryngol Head Neck Surg 1994; 111:
65 24. Sethi A, Passey JC, Mrig S, Sareen D, Sharma P. Giant cell tumour of the zygoma: An extremely unusual neolasm. Acta Oto-Laryngologica, 126(3): , Enneking WF. (1983) Musculoskeletal tumor surgery. Churchill Livingstone, New York 26. Faisham W, Zulmi W, Halim A, Biswal BM, Mutum S. Aggressive giant cell tumour of bone. Singapore Med J 2006; 47(8): Balke M, Schremper L, Gebert C, Ahrens H. Giant cell tumour of bone: treatment and outcome of 214 cases. J Cancer Res Clin Oncol 2008; Brimo F, Aziz M, Rosen G, Turcotte R, Nahal A. Malignancy in giant cell tumour of bone: is there a reproducible histological threshold? A study of three giant cell tumours with worrisome features. Histopathology Dec; 51(6): Salerno M, Avnet S, Alberghini M, Giunti A, Baldini N.Histogenetic characterization of giant cell tumor of bone. Clin Orthop Relat Res Sep;466(9): Epub 2008 Jun Folpe AL., Morris RJ., Weiss SW. Soft tissues giant cell tumor of low malignant potential: a proposal fort he reclassification of malignant giant cell tumor of soft parts. Mod Pathol Sep; 12 (9): Werner M. Giant cell tumour of bone: morphological, biological and histogenetical aspects. Int Orthop Dec;30(6): Epub 2006 Sep 30. Review 32. Gong LH, Sun XQ, Meng SQ, Huang XY. Giant cell tumor of bone and malignancies in giant cell tumor: a clinicopathologic analysis] Zhonghua Bing Li Xue Za Zhi May;38(5): Lang S. Differential diagnosis of giant cell-rich lesions of bone] Pathologe Nov;29 Suppl 2: Iltar S, Alemdaroğlu KB, Karalezli N, Irgit K, Caydere M, Aydoğan NH. A case of an aneurysmal bone cyst of a metatarsal: review of the differential diagnosis and treatment options. J Foot Ankle Surg Jan-Feb;48(1):74-9. Review 65
66 35. Rock MG. Curettage of giant cell tumour of bone. Factors influencing local recurrences and metastasis. Chir Organi Mov 1990;75: Kamer S, Anacak Y, Savaş R, Doğanavşargil B, Haydaroğlu A. Giant cell tumor of the bone with an asymptomatic huge solitary lung metastasis; case presentation and literature review. J BUON Jan-Mar;11(1): Seethalakshmi Viswanathan, Jambhekar NA. Metastatic Giant Cell Tumor of Bone: Are There Associated Factors and Best Treatment Modalities? Clin Orthop Relat Res Jul Hutter RV, Worcester JN, Francis KC, Foote FW, Stewart FW. Benign and malignant giant-cell tumours of bone. Clinicopathological analysis of the natural history of the disease. Cancer 1962; 15; Dahlin DC, Cupps RE, Johnson EW, Jr. Giant-cell tumour: a study of 195 cases. Cancer 1970; 25; Oda Y, Sakamoto A, Saito T, Matsuda S, Tanaka K, Iwamoto Y. Secomdary malignanat giant-cell tumour of bone: molecular abnormalities of p53and H-ras gene correlated with malignant transformation. Histopathology 2001: 39; Lackman RD, Hosalkar HS, Ogilvie CM, Torbert JT, Fox EJ.Intralesional curettage for grades II and III giant cell tumors of bone.clin Orthop Relat Res Sep;438: Masui F, Ushigome S, Fujii K Giant cell tumor of bone: a clinicopathologic study of prognostic factors. Pathol Int Sep;48(9): Nishida J, Shimamura T.. Methods of reconstruction for bone defect after tumor excision: a review of alternatives.med Sci Monit Aug;14(8):RA Review 66
67 44. Abdelrahman M, Bassiony AA, Shalaby H, Assal MK. Cryosurgery and Impaction Subchondral Bone Graft for the Treatment of Giant Cell Tumor Around the Knee. HSS J Jul Thomas DM, Skubitz KM.Giant cell tumour of bone. Curr Opin Oncol Jul;21(4): Review 46. Leggon R., Zlotecki R., Reith John., Scarborough M. Giant cell tumor of the pelvis and sacrum. Clinical Orthopaedics and Related Research : Osaka S., Sugita H., Osaka E., Yoshida Y., Ryu J. Clinical and immunhistochemical characteristics of benign giant cell tumor of bone with pulmanary metastases: case series. Journal of Orthopaedic surgery 2004;12 (1): Rousseau MA., Handra A., Jean L., Lazennec Y., Catonne Y., Saillant G. Metachronous multicentric giant cell tumor of bone in the lower limb. Case report and Ki67 immunhistochemistry study. Virchows Arch (2004) 445: Cai G., Ramdall R., Garcia R., Levine P. Pulmonary metastasis of giant cell tumor of the bone diagnosed by fine needle aspiration biopsy. Diagnostic Cytopathology 2007; 35: Matsubayashi S., Nakashimo M., Kumagai K. Immunhistochemical analyses of betacatenin and cyclin D1 expression in giant cell tumor of bone (GCTB). A possible role of Wnt pathway in GCTB tumorigenesis. Pathol Res and Prac Gamberi G., Benassi M., Böhling T., Ragazzini P. Prognostic relevance of c-myc gene expression in giant cell tumor of bone. J Ortho Res. 1998; 16: Krober S., Greschniok A., Bohm P., Kaiserling E. Giant cell tumor of bone. Morphological, immunhistochemical, morphometric and DNA flow cytometric findings. Verh Dtsch Ges Pathol. 1998;82:
68 53. Gattei V., Aldinucci D., Quinn JM. Human osteoclasts and preosteoclast cells Express functional c-kit receptors and interact with osteoblast and stromal cells via membrane-bound stem cell factor. Cell Growth Differ. 1996;7: Yamazaki H, Kunisada T, Yamane T. Presence of osteoclast precursors in colonies cloned in the presence of hematopoetic colony-stimulating factors. Exp Heatol. 2001; 29: Haydon RC, Deyrup A, Ishikawa AR. Upregulation of c-kit in giant cell tumor of the bone: possible therapeutic target using STI-571. Paper presented at Orthopedic Research Society and Musculoskeletal Tumor Society Meeting; Ramos R, Helen M, Kanetsky P. Giant cell tumor. Inquiry into immunhistochemical expression of CD117, Microphtalmia Transcription Factor, Tartrate-Resistant Acid Phosphatase and HAM-56. Arch POathol Lab Med- Vol129, March
Organizmanın en sert dokusudur. Kemik dokusunun hücreler arası maddesinin içinde kollajen teller ve inorganik elemanlar bulunur. İnorganik elemanlar
 KEMİK DOKUSU Organizmanın en sert dokusudur. Kemik dokusunun hücreler arası maddesinin içinde kollajen teller ve inorganik elemanlar bulunur. İnorganik elemanlar hidroksiapatit kristalleri olarak tanımlanır.
KEMİK DOKUSU Organizmanın en sert dokusudur. Kemik dokusunun hücreler arası maddesinin içinde kollajen teller ve inorganik elemanlar bulunur. İnorganik elemanlar hidroksiapatit kristalleri olarak tanımlanır.
SERT DOKUNUN SULU (KĠSTĠK) LEZYONU. Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011
 SERT DOKUNUN SULU (KĠSTĠK) LEZYONU Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011 OLGU 9 Y, K Sağ humerus proksimali 2 yıl önce kırık Doğal iyileşmeye bırakılmış
SERT DOKUNUN SULU (KĠSTĠK) LEZYONU Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011 OLGU 9 Y, K Sağ humerus proksimali 2 yıl önce kırık Doğal iyileşmeye bırakılmış
Göğüs Cerrahisi Alkın Yazıcıoğlu. Journal of Clinical and Analytical Medicine Göğüs Cerrahisi
 Mediastenin Nadir Görülen Tümörleri Tüm mediastinal kitlelerin %10 dan azını meydana getiren bu lezyonlar mezenkimal veya epitelyal kökenli tümörlerden oluşmaktadır. Journal of linical and nalytical Medicine
Mediastenin Nadir Görülen Tümörleri Tüm mediastinal kitlelerin %10 dan azını meydana getiren bu lezyonlar mezenkimal veya epitelyal kökenli tümörlerden oluşmaktadır. Journal of linical and nalytical Medicine
ÜNİTE 7. Kemik Dokusu. Amaçlar
 ÜNİTE 7 Kemik Dokusu Amaçlar Bu üniteyi çalıştıktan sonra, Kemik dokusunun yapısını ve özelliklerini, Kemik oluşumunu, Kemik dokusunun fonksiyonlarını öğrenmiş olacaksınız. İçindekiler Giriş Kemik Yapısı
ÜNİTE 7 Kemik Dokusu Amaçlar Bu üniteyi çalıştıktan sonra, Kemik dokusunun yapısını ve özelliklerini, Kemik oluşumunu, Kemik dokusunun fonksiyonlarını öğrenmiş olacaksınız. İçindekiler Giriş Kemik Yapısı
Pediatrik kemik tümörlerinde radyolojik tanı
 Pediatrik kemik tümörlerinde radyolojik tanı Dr. Zeynep Yazıcı Uludağ Üniversitesi, Bursa Kemik tümörleri Tüm kemik tümörlerinin %42 si: İlk 20 yaşta Çoğu: Belirli bir yaşta görülme eğiliminde D Resnick,
Pediatrik kemik tümörlerinde radyolojik tanı Dr. Zeynep Yazıcı Uludağ Üniversitesi, Bursa Kemik tümörleri Tüm kemik tümörlerinin %42 si: İlk 20 yaşta Çoğu: Belirli bir yaşta görülme eğiliminde D Resnick,
SIK KARŞILAŞILAN KAS İSKELET LEZYONLARINDA AYIRICI TANI
 SIK KARŞILAŞILAN KAS İSKELET LEZYONLARINDA AYIRICI TANI Dr. İbrahim ADALETLİ İ.Ü. Cerrahpaşa Tıp Fakültesi Radyoloji AD. Pediatrik Radyoloji Bilim Dalı Olgu 1 Tanınız nedir? 1- Enkondrom 2- Non ossifaying
SIK KARŞILAŞILAN KAS İSKELET LEZYONLARINDA AYIRICI TANI Dr. İbrahim ADALETLİ İ.Ü. Cerrahpaşa Tıp Fakültesi Radyoloji AD. Pediatrik Radyoloji Bilim Dalı Olgu 1 Tanınız nedir? 1- Enkondrom 2- Non ossifaying
ELİN YUMUŞAK DOKU TÜMÖRLERİ
 ELİN YUMUŞAK DOKU TÜMÖRLERİ Çoğunlukla selim karakterde olan bu tümörlerin sadece % 1-2 si habistir. Sinovial kistler, tendon kılıfının dev hücreli tümörü, lipom, enkondrom sık görülen selim oluşumlardır.
ELİN YUMUŞAK DOKU TÜMÖRLERİ Çoğunlukla selim karakterde olan bu tümörlerin sadece % 1-2 si habistir. Sinovial kistler, tendon kılıfının dev hücreli tümörü, lipom, enkondrom sık görülen selim oluşumlardır.
Dr. Recep Savaş Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir
 Dr. Recep Savaş Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir SİSTEMATİK DEĞERLENDİRME Yorumlama dıştan içe veya içten dışa doğru yapılmalı TORAKS DUVARI Kostalar Sternum Klavikula Torasik vertebralar
Dr. Recep Savaş Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir SİSTEMATİK DEĞERLENDİRME Yorumlama dıştan içe veya içten dışa doğru yapılmalı TORAKS DUVARI Kostalar Sternum Klavikula Torasik vertebralar
HABİS KEMİK TÜMÖRLERİNDE ORTOPEDİK CERRAHİ YAKLAŞIM. Prof.Dr.Murat HIZ İ.Ü.Cerrahpaşa Tıp Fakültesi Ortopedi ve Travmatoloji A.B.D.
 HABİS KEMİK TÜMÖRLERİNDE ORTOPEDİK CERRAHİ YAKLAŞIM Prof.Dr.Murat HIZ İ.Ü.Cerrahpaşa Tıp Fakültesi Ortopedi ve Travmatoloji A.B.D. Habis Kemik Tümörleri Nadir görülen tümörler olmasına rağmen ( tüm kanserlerin
HABİS KEMİK TÜMÖRLERİNDE ORTOPEDİK CERRAHİ YAKLAŞIM Prof.Dr.Murat HIZ İ.Ü.Cerrahpaşa Tıp Fakültesi Ortopedi ve Travmatoloji A.B.D. Habis Kemik Tümörleri Nadir görülen tümörler olmasına rağmen ( tüm kanserlerin
Radyolüsent Görüntü Veren Odontojenik Tümörler Dr.Zuhal Tuğsel
 Radyolüsent GörüntG ntü Veren Odontojenik TümörlerT Dr.Zuhal Tuğsel Ameloblastoma Odontojenik epitelden kökenli yavaş büyüyen, iyi huylu bir tümördür. Herhangi bir yaşta görülür, literatürde sözü edilen
Radyolüsent GörüntG ntü Veren Odontojenik TümörlerT Dr.Zuhal Tuğsel Ameloblastoma Odontojenik epitelden kökenli yavaş büyüyen, iyi huylu bir tümördür. Herhangi bir yaşta görülür, literatürde sözü edilen
Kemik dokusu, yapısı ve işlevi. Dr. Kutay Engin Özturan
 Kemik dokusu, yapısı ve işlevi Dr. Kutay Engin Özturan Kemik dokusunun görevleri Mekanik destek ve çatı Hayati organların korunması Mineral depolanması ve homestazisi Kemik iliği için ev sahipliği Hareket
Kemik dokusu, yapısı ve işlevi Dr. Kutay Engin Özturan Kemik dokusunun görevleri Mekanik destek ve çatı Hayati organların korunması Mineral depolanması ve homestazisi Kemik iliği için ev sahipliği Hareket
İSKELET YAPISI VE FONKSİYONLARI
 İSKELET YAPISI VE FONKSİYONLARI 1- Vücuda şekil vermek 2- Kaslara bağlantı yeri oluşturmak ve hareketlerin yapılmasına olanaksağlamak 3- Vücut ağırlığını taşımak 4- Vücudun yumuşak kısımlarını korumak
İSKELET YAPISI VE FONKSİYONLARI 1- Vücuda şekil vermek 2- Kaslara bağlantı yeri oluşturmak ve hareketlerin yapılmasına olanaksağlamak 3- Vücut ağırlığını taşımak 4- Vücudun yumuşak kısımlarını korumak
Sternum korpusunda (en çok)
 GÖĞÜS DUVARI TÜMÖRLERİ PROF. DR. REFİK ÜLKÜ D.Ü Tıp Fak Göğüs Cerrahisi Tüm primer tümörler arasında %1-1.5 Malign primer göğüs duvarı tümörleri, tüm kanser hastaları arasında %0.04 Göğüs duvarı malign
GÖĞÜS DUVARI TÜMÖRLERİ PROF. DR. REFİK ÜLKÜ D.Ü Tıp Fak Göğüs Cerrahisi Tüm primer tümörler arasında %1-1.5 Malign primer göğüs duvarı tümörleri, tüm kanser hastaları arasında %0.04 Göğüs duvarı malign
Çocukluk çağı Kemik Tümörlerinde Radyoloji
 Çocukluk çağı Kemik Tümörlerinde Radyoloji Dr.Hakan Gençhellaç. Trakya Üniversitesi Tıp Fakültesi Radyoloji Ana Bilim Dalı, Çocuk Radyolojisi Bilim Dalı Türk Radyoloji Derneği 36. ULUSAL RADYOLOJİ KONGRESİ
Çocukluk çağı Kemik Tümörlerinde Radyoloji Dr.Hakan Gençhellaç. Trakya Üniversitesi Tıp Fakültesi Radyoloji Ana Bilim Dalı, Çocuk Radyolojisi Bilim Dalı Türk Radyoloji Derneği 36. ULUSAL RADYOLOJİ KONGRESİ
Prof Dr Sergülen Dervişoğlu. Kemik tümörleri Kemiğin tümör benzeri lezyonları
 Prof Dr Sergülen Dervişoğlu Kemik tümörleri Kemiğin tümör benzeri lezyonları Kemik tümörleri Ekip çalışması Ortopedist Radyolog Patolog Onkolog ( Medikal/Radyasyon) Klinik anamnez Tanıda çok önemli Yaş
Prof Dr Sergülen Dervişoğlu Kemik tümörleri Kemiğin tümör benzeri lezyonları Kemik tümörleri Ekip çalışması Ortopedist Radyolog Patolog Onkolog ( Medikal/Radyasyon) Klinik anamnez Tanıda çok önemli Yaş
FTR 207 Kinezyoloji I. Eklemlerin Temel Yapısı ve Fonksiyonu II. yrd.doç.dr. emin ulaş erdem
 FTR 207 Kinezyoloji I Eklemlerin Temel Yapısı ve Fonksiyonu II yrd.doç.dr. emin ulaş erdem EKLEMLERDEKİ BAĞ DOKUSUNU OLUŞTURAN BİYOLOJİK MATERYALLER Eklemlerdeki bağ dokusunu oluşturan biyolojik materyallerin
FTR 207 Kinezyoloji I Eklemlerin Temel Yapısı ve Fonksiyonu II yrd.doç.dr. emin ulaş erdem EKLEMLERDEKİ BAĞ DOKUSUNU OLUŞTURAN BİYOLOJİK MATERYALLER Eklemlerdeki bağ dokusunu oluşturan biyolojik materyallerin
Akciğer Karsinomlarının Histopatolojisi
 Akciğer Karsinomlarının Histopatolojisi Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Akciğer karsinomlarının gelişiminde preinvaziv epitelyal lezyonlar; Akciğer karsinomlarının gelişiminde
Akciğer Karsinomlarının Histopatolojisi Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Akciğer karsinomlarının gelişiminde preinvaziv epitelyal lezyonlar; Akciğer karsinomlarının gelişiminde
Kemik tümörleri ve tümör benzeri lezyonları, sıklıkla tanı ve tedavi güçlüğüyle
 DERLEME Hacettepe T p Dergisi 2006; 37:124-131 Kemi in tümör ve tümör benzeri lezyonlar na yaklafl m Mehmet Ayvaz 1, M. Cemalettin Aksoy 2 1 Uzman Dr., Hacettepe Üniversitesi Tıp Fakültesi Ortopedi ve
DERLEME Hacettepe T p Dergisi 2006; 37:124-131 Kemi in tümör ve tümör benzeri lezyonlar na yaklafl m Mehmet Ayvaz 1, M. Cemalettin Aksoy 2 1 Uzman Dr., Hacettepe Üniversitesi Tıp Fakültesi Ortopedi ve
PROF. DR. OKTAY ARDA
 PROF. DR. OKTAY ARDA 2 BAĞ DOKUSU? OLUŞUR HÜCRELER LİFLER ARA MADDE 3 KEMİK ÖZELL BİR BAĞ DOKUSUDUR 4 KEMİĞİN DİĞER BAĞ DOKULARINDAN FARKI ARA MADDESİ YAPISI 5 KEMİK ARA MADDESİ KALSİFİYE SERT DİFÜZYON
PROF. DR. OKTAY ARDA 2 BAĞ DOKUSU? OLUŞUR HÜCRELER LİFLER ARA MADDE 3 KEMİK ÖZELL BİR BAĞ DOKUSUDUR 4 KEMİĞİN DİĞER BAĞ DOKULARINDAN FARKI ARA MADDESİ YAPISI 5 KEMİK ARA MADDESİ KALSİFİYE SERT DİFÜZYON
Adrenalde sık ve nadir görülen lezyonlar. Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD
 Adrenalde sık ve nadir görülen lezyonlar Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD Feokromositoma Kromafin hücrelerden köken alır 2 tip hücre içerir:kromafin hücreler ve sustentaküler
Adrenalde sık ve nadir görülen lezyonlar Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD Feokromositoma Kromafin hücrelerden köken alır 2 tip hücre içerir:kromafin hücreler ve sustentaküler
Destekleme Koruma Hareket. Kemik dokusunun Fonksiyonları. Mineral depolama (Ca, P) Kan yapımı Enerji depolama (kemiklerdeki sarı kemik iliği)
 KEMİK DOKUSU Destekleme Koruma Hareket Kemik dokusunun Fonksiyonları Mineral depolama (Ca, P) Kan yapımı Enerji depolama (kemiklerdeki sarı kemik iliği) Hücrelerarası madde (matriks) I. Organik maddeler
KEMİK DOKUSU Destekleme Koruma Hareket Kemik dokusunun Fonksiyonları Mineral depolama (Ca, P) Kan yapımı Enerji depolama (kemiklerdeki sarı kemik iliği) Hücrelerarası madde (matriks) I. Organik maddeler
HİSTOLOJİ. DrYasemin Sezgin
 HİSTOLOJİ DrYasemin Sezgin HİSTOLOJİ - Canlı vücudunu meydana getiren hücre, doku ve organların çıplak gözle görülemeyen (mikroskopik) yapılarını inceleyen bir bilim koludur. - Histolojinin sözlük anlamı
HİSTOLOJİ DrYasemin Sezgin HİSTOLOJİ - Canlı vücudunu meydana getiren hücre, doku ve organların çıplak gözle görülemeyen (mikroskopik) yapılarını inceleyen bir bilim koludur. - Histolojinin sözlük anlamı
Böbrek kistleri olan hastaya yaklaşım
 Böbrek kistleri olan hastaya yaklaşım Dr. Ayşegül Örs Zümrütdal Başkent Üniversitesi-Nefroloji Bilim Dalı 20/05/2011-ANTALYA Böbrek kistleri Genetik ya da genetik olmayan nedenlere bağlı olarak, Değişik
Böbrek kistleri olan hastaya yaklaşım Dr. Ayşegül Örs Zümrütdal Başkent Üniversitesi-Nefroloji Bilim Dalı 20/05/2011-ANTALYA Böbrek kistleri Genetik ya da genetik olmayan nedenlere bağlı olarak, Değişik
Tanı: Metastatik hastalık için patognomonik bir radyolojik. Tek veya muitipl nodüller iyi sınırlı veya difüz. Göğüs Cerrahisi Hasan Çaylak
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
XVII. ULUSAL KANSER KONGRESİ
 XVII. ULUSAL KANSER KONGRESİ İnteraktif Olgu Sunumu KEMİK TÜMÖRLERİ . 17 yaşında bayan hasta. 2.5 yıldır sol bacakda yürürken ağrı Enfeksiyon ve dolaşım bozukluğu tedavisi uygulanmış. Son 6 aydır ağrı
XVII. ULUSAL KANSER KONGRESİ İnteraktif Olgu Sunumu KEMİK TÜMÖRLERİ . 17 yaşında bayan hasta. 2.5 yıldır sol bacakda yürürken ağrı Enfeksiyon ve dolaşım bozukluğu tedavisi uygulanmış. Son 6 aydır ağrı
BİRİNCİL KEMİK KANSERİ
 BİRİNCİL KEMİK KANSERİ KONDROSARKOM (KS) PROF. DR. LEVENT ERALP Ortopedi ve Travmatoloji Uzmanı İÇİNDEKİLER Kondrosarkom Nedir? KS dan kimler etkilenir? Bulgular nelerdir? KS tipleri nelerdir? Risk faktörleri
BİRİNCİL KEMİK KANSERİ KONDROSARKOM (KS) PROF. DR. LEVENT ERALP Ortopedi ve Travmatoloji Uzmanı İÇİNDEKİLER Kondrosarkom Nedir? KS dan kimler etkilenir? Bulgular nelerdir? KS tipleri nelerdir? Risk faktörleri
KIKIRDAK ve KEMİK DOKUSU. Prof. Dr. Levent ERGÜN
 KIKIRDAK ve KEMİK DOKUSU Prof. Dr. Levent ERGÜN Kıkırdak Dokusu Yumuşak dokulardan oluşmuş organlara (burun, gırtlak, hava borusu, akciğerler, kulak kepçesi) desteklik sağlar. Eklem yüzlerini örterek kayganlık
KIKIRDAK ve KEMİK DOKUSU Prof. Dr. Levent ERGÜN Kıkırdak Dokusu Yumuşak dokulardan oluşmuş organlara (burun, gırtlak, hava borusu, akciğerler, kulak kepçesi) desteklik sağlar. Eklem yüzlerini örterek kayganlık
KEMİK DOKU HİSTOLOJİSİ DERS NOTLARI - 1
 KEMİK DOKU HİSTOLOJİSİ DERS NOTLARI - 1 KEMİK DOKUSU Vücudun en sert dokusudur. Destek dokular arasında gerçek anlamda destekleme görevi yapan doku budur. Vücut ve organları için; 1.Destek ve koruma, 2.Kalsiyum
KEMİK DOKU HİSTOLOJİSİ DERS NOTLARI - 1 KEMİK DOKUSU Vücudun en sert dokusudur. Destek dokular arasında gerçek anlamda destekleme görevi yapan doku budur. Vücut ve organları için; 1.Destek ve koruma, 2.Kalsiyum
Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi
 Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi 1 Öğrenme hedefleri Metastazların genel özellikleri Görüntüleme Teknikleri Tedavi sonrası metastaz takibi Ayırıcı tanı 2 Metastatik Hastalık Total
Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi 1 Öğrenme hedefleri Metastazların genel özellikleri Görüntüleme Teknikleri Tedavi sonrası metastaz takibi Ayırıcı tanı 2 Metastatik Hastalık Total
Tiroid bezinde ender bir mezenkimal tümör. Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı
 Tiroid bezinde ender bir mezenkimal tümör Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 10-10 - 2015 ANKARA Ülkemizin başı sağ olsun Değerli Hocamızı saygıyla anıyoruz Prof.
Tiroid bezinde ender bir mezenkimal tümör Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 10-10 - 2015 ANKARA Ülkemizin başı sağ olsun Değerli Hocamızı saygıyla anıyoruz Prof.
MEME PATOLOJİSİ SLAYT SEMİNERİ
 MEME PATOLOJİSİ SLAYT SEMİNERİ Prof. Dr. Şahsine Tolunay Uludağ Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 17.10.2015 OLGU 43 yaşında kadın 2 çocuğu var Sol memede ağrı ve kitle yakınması mevcut
MEME PATOLOJİSİ SLAYT SEMİNERİ Prof. Dr. Şahsine Tolunay Uludağ Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 17.10.2015 OLGU 43 yaşında kadın 2 çocuğu var Sol memede ağrı ve kitle yakınması mevcut
NEOPLAZİ D R. Y A S E M İ N S E Z G İ N. yasemin sezgin
 NEOPLAZİ D R. Y A S E M İ N S E Z G İ N yasemin sezgin Neoplazi Yeni bir doku oluşmasını ifade eder. Oluşan bu kitleye neoplazm denir. Aslen şişlik anlamına gelen tümör deyimi de neoplazm anlamında kullanılmaktadır.
NEOPLAZİ D R. Y A S E M İ N S E Z G İ N yasemin sezgin Neoplazi Yeni bir doku oluşmasını ifade eder. Oluşan bu kitleye neoplazm denir. Aslen şişlik anlamına gelen tümör deyimi de neoplazm anlamında kullanılmaktadır.
Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm
 BAZAL HÜCRELİ KARSİNOM Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm Nadiren met. yapar fakat tedavisiz bırakıldığında invazif davranış göstermesi,lokal invazyon,
BAZAL HÜCRELİ KARSİNOM Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm Nadiren met. yapar fakat tedavisiz bırakıldığında invazif davranış göstermesi,lokal invazyon,
Spinal Tümörler Prof. Dr. E. Turgut TALI Gazi Üniversitesi Tıp Fakültesi Radyoloji A. D. Nöroradyoloji B. D.
 Spinal Tümörler Prof. Dr. E. Turgut TALI Gazi Üniversitesi Tıp Fakültesi Radyoloji A. D. Nöroradyoloji B. D. [email protected] Kemik tümörlerinin %5 i Gençlerde benign, adultta malign Primer < sekonder
Spinal Tümörler Prof. Dr. E. Turgut TALI Gazi Üniversitesi Tıp Fakültesi Radyoloji A. D. Nöroradyoloji B. D. [email protected] Kemik tümörlerinin %5 i Gençlerde benign, adultta malign Primer < sekonder
Deri Tümörleri Pratik Ders İçeriği
 Deri Tümörleri Pratik Ders İçeriği Deri Tümörleri DSÖ(2006) sınıflaması Yassı Hücreli Karsinom Bazal Hücreli Karsinom Bazoskuamoz Karsinom Melanositik Dermal Nevus Melanom DSÖ DERİ TÜMÖRLERİ SINIFLAMASI
Deri Tümörleri Pratik Ders İçeriği Deri Tümörleri DSÖ(2006) sınıflaması Yassı Hücreli Karsinom Bazal Hücreli Karsinom Bazoskuamoz Karsinom Melanositik Dermal Nevus Melanom DSÖ DERİ TÜMÖRLERİ SINIFLAMASI
AZ DİFERANSİYE TİROİD KANSERLERİ. Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM
 AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK
 KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK 1 2 Lokomotor sistemi oluşturan yapılar içinde en fazla stres altında kalan kıkırdaktır. Eklem kıkırdağı; 1) Kan damarlarından, 2) Lenf kanallarından, 3) Sinirlerden yoksundur.
KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK 1 2 Lokomotor sistemi oluşturan yapılar içinde en fazla stres altında kalan kıkırdaktır. Eklem kıkırdağı; 1) Kan damarlarından, 2) Lenf kanallarından, 3) Sinirlerden yoksundur.
GELİŞİMSEL KALÇA DİSPLAZİSİ PROGNOZU VE GÖRÜNTÜLEME. Dr. Öznur Leman Boyunağa Gazi Üniversitesi Tıp Fakültesi Pediatrik Radyoloji Bilim Dalı
 GELİŞİMSEL KALÇA DİSPLAZİSİ PROGNOZU VE GÖRÜNTÜLEME Dr. Öznur Leman Boyunağa Gazi Üniversitesi Tıp Fakültesi Pediatrik Radyoloji Bilim Dalı Doğal seyir & Prognoz Tedavi edilmezse uzun dönemde ekstremite
GELİŞİMSEL KALÇA DİSPLAZİSİ PROGNOZU VE GÖRÜNTÜLEME Dr. Öznur Leman Boyunağa Gazi Üniversitesi Tıp Fakültesi Pediatrik Radyoloji Bilim Dalı Doğal seyir & Prognoz Tedavi edilmezse uzun dönemde ekstremite
KRANİYOFASİYAL YAPININ BÜTÜN OLARAK DEĞERLENDİRİLMESİ. Prof. Dr. Hatice Gökalp
 KRANİYOFASİYAL YAPININ BÜTÜN OLARAK DEĞERLENDİRİLMESİ Prof. Dr. Hatice Gökalp KAFATASI KAFA KAİDESİ MAKSİLLA MANDİBULA Kartilajın doku oluşumudur kartilajdan kemik oluşmasıdır Undiferansiye mezenşimal
KRANİYOFASİYAL YAPININ BÜTÜN OLARAK DEĞERLENDİRİLMESİ Prof. Dr. Hatice Gökalp KAFATASI KAFA KAİDESİ MAKSİLLA MANDİBULA Kartilajın doku oluşumudur kartilajdan kemik oluşmasıdır Undiferansiye mezenşimal
LENFOİD SİSTEM DR GÖKSAL KESKİN ARALIK-2014
 LENFOİD SİSTEM DR GÖKSAL KESKİN ARALIK-2014 Lenfoid Sistem Lenfositlerin, mononükleer fagositlerin ve diğer yardımcı rol oynayan hücrelerin bulunduğu, yabancı antijenlerin taşınıp yoğunlaştırıldığı, Antijenin
LENFOİD SİSTEM DR GÖKSAL KESKİN ARALIK-2014 Lenfoid Sistem Lenfositlerin, mononükleer fagositlerin ve diğer yardımcı rol oynayan hücrelerin bulunduğu, yabancı antijenlerin taşınıp yoğunlaştırıldığı, Antijenin
Göğüs Cerrahisi Sedat Gürkok. Göğüs Cerrahisi. Journal of Clinical and Analytical Medicine
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Soliter Pulmoner Nodül Tanım: Genel bir tanımı olmasa da 3 cm den küçük, akciğer parankimi ile çevrili, beraberinde herhangi patolojinin eşlik
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Soliter Pulmoner Nodül Tanım: Genel bir tanımı olmasa da 3 cm den küçük, akciğer parankimi ile çevrili, beraberinde herhangi patolojinin eşlik
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER
 MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 25. Ulusal Patoloji Kongresi 14-17
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 25. Ulusal Patoloji Kongresi 14-17
SELİM KEMİK TÜMÖRLERİ ve KEMİĞİN TÜMÖRE BENZEYEN LEZYONLARI
 SELİM KEMİK TÜMÖRLERİ ve KEMİĞİN TÜMÖRE BENZEYEN LEZYONLARI PROF. DR. MURAT HIZ İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Ortopedi ve Travmatoloji A.D. Tümör = Neoplazm Bir veya birden fazla dokunun
SELİM KEMİK TÜMÖRLERİ ve KEMİĞİN TÜMÖRE BENZEYEN LEZYONLARI PROF. DR. MURAT HIZ İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi Ortopedi ve Travmatoloji A.D. Tümör = Neoplazm Bir veya birden fazla dokunun
Adrenal lezyonların görüntüleme bulguları. Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul
 Adrenal lezyonların görüntüleme bulguları Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul Öğrenme hedefleri Adrenal bez kitlelerinin BT ile değerlendirilmesinde temel prensip ve bulguları öğrenmek
Adrenal lezyonların görüntüleme bulguları Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul Öğrenme hedefleri Adrenal bez kitlelerinin BT ile değerlendirilmesinde temel prensip ve bulguları öğrenmek
Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D
 Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D 03.11.2016 Olgu 22 yaşında, kadın hasta Bacakta nodüler lezyon Son 1 yıl içinde farkediyor. Özgeçmiş: Özellik yok. Klinik ön tanı: Yumuşak doku sarkomu?
Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D 03.11.2016 Olgu 22 yaşında, kadın hasta Bacakta nodüler lezyon Son 1 yıl içinde farkediyor. Özgeçmiş: Özellik yok. Klinik ön tanı: Yumuşak doku sarkomu?
KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK
 KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK 1 Dik postürü oluşturan rijit dokuyu kemikler oluşturmaktadır. Kemik, hareket sistemi için esas olan kaldıraç sistemini ve desteği oluşturmasının yanında iç organları ve
KİNEZYOLOJİ ÖĞR.GÖR. CİHAN CİCİK 1 Dik postürü oluşturan rijit dokuyu kemikler oluşturmaktadır. Kemik, hareket sistemi için esas olan kaldıraç sistemini ve desteği oluşturmasının yanında iç organları ve
Dr. A. Nimet Karadayı. Hastanesi, Patoloji Kliniği
 Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
Kötü Huylu Yumuşak Doku Tümörleri. Tanım, sınıflama, hastaya ilk yaklaşım. Dr. Serkan BİLGİÇ
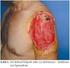 Kötü Huylu Yumuşak Doku Tümörleri Tanım, sınıflama, hastaya ilk yaklaşım Dr. Serkan BİLGİÇ İskelet dışı bağ dokusundan kaynaklanan mezodermal kökenli nadir malignitelerdir. Tanım Görülme Sıklığı Tüm kanser
Kötü Huylu Yumuşak Doku Tümörleri Tanım, sınıflama, hastaya ilk yaklaşım Dr. Serkan BİLGİÇ İskelet dışı bağ dokusundan kaynaklanan mezodermal kökenli nadir malignitelerdir. Tanım Görülme Sıklığı Tüm kanser
OLGU. 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle
 OLGU 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle Meme USG; Sağ memeyi bütünüyle dolduran, düzgün sınırlı, içerisinde yer yer kistik alanların ve kalsifikasyonların izlendiği, yoğun vasküler sinyal
OLGU 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle Meme USG; Sağ memeyi bütünüyle dolduran, düzgün sınırlı, içerisinde yer yer kistik alanların ve kalsifikasyonların izlendiği, yoğun vasküler sinyal
Sistinozis ve Herediter Multiple Ekzositoz Birlikteliği
 Sistinozis ve Herediter Multiple Ekzositoz Birlikteliği Aysun Karabay Bayazıt, Bahriye Atmış, Deniz Kör, Neslihan Önenli Mungan, Ali Anarat Çukurova Üniversitesi Tıp Fakültesi, Çocuk Nefroloji ve Çocuk
Sistinozis ve Herediter Multiple Ekzositoz Birlikteliği Aysun Karabay Bayazıt, Bahriye Atmış, Deniz Kör, Neslihan Önenli Mungan, Ali Anarat Çukurova Üniversitesi Tıp Fakültesi, Çocuk Nefroloji ve Çocuk
Kemik Doku. Prof.Dr.Ümit Türkoğlu
 Kemik Doku Prof.Dr.Ümit Türkoğlu 1 Kemik Dokusu İskelet sistemi başlıca işlevleri: Mekanik destek Hareket için kasların yapışma yerlerini sağlama Medüllasında yer alan, hemapoetik sistem elemanı kemik
Kemik Doku Prof.Dr.Ümit Türkoğlu 1 Kemik Dokusu İskelet sistemi başlıca işlevleri: Mekanik destek Hareket için kasların yapışma yerlerini sağlama Medüllasında yer alan, hemapoetik sistem elemanı kemik
SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU
 SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU Ezgi Işıl Turhan 1, Nesrin Uğraş 1, Ömer Yerci 1, Seçil Ak 2, Berrin Tunca 2, Ersin Öztürk
SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU Ezgi Işıl Turhan 1, Nesrin Uğraş 1, Ömer Yerci 1, Seçil Ak 2, Berrin Tunca 2, Ersin Öztürk
Anatomik Sistemler. Hastalıklar Bilgisi Ders-2 İskelet-Kas-Sinir Sistemleri
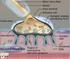 Anatomik Sistemler Hastalıklar Bilgisi Ders-2 İskelet-Kas-Sinir Sistemleri Anatomik Sistem İskelet Sistemi İskeletin Görevleri Vücuda şekil verir. Vücuda destek sağlar. Göğüs kafes ve kafatası kemikleri
Anatomik Sistemler Hastalıklar Bilgisi Ders-2 İskelet-Kas-Sinir Sistemleri Anatomik Sistem İskelet Sistemi İskeletin Görevleri Vücuda şekil verir. Vücuda destek sağlar. Göğüs kafes ve kafatası kemikleri
Multipl Myeloma da PET/BT. Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD
 Multipl Myeloma da PET/BT Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD İskelet sisteminin en sık görülen primer neoplazmı Radyolojik olarak iskelette çok sayıda destrüktif lezyon ve yaygın
Multipl Myeloma da PET/BT Dr. N. Özlem Küçük Ankara Üniv. Tıp Fak. Nükleer Tıp ABD İskelet sisteminin en sık görülen primer neoplazmı Radyolojik olarak iskelette çok sayıda destrüktif lezyon ve yaygın
VÜCUDUN TEMEL PARÇALARI. 1) Baş-boyun 2)Gövde 3)Ekstremiteler (Kollar ve bacaklar)
 VÜCUDUN TEMEL PARÇALARI 1) Baş-boyun 2)Gövde 3)Ekstremiteler (Kollar ve bacaklar) 1)BAŞ a)yüz b)kranium (Kafatası) 2) GÖVDE a)toraks (Göğüs kafesi) b)karın 3) EKSTREMİTELER a)üst ekstremiteler b)alt ekstremiteler
VÜCUDUN TEMEL PARÇALARI 1) Baş-boyun 2)Gövde 3)Ekstremiteler (Kollar ve bacaklar) 1)BAŞ a)yüz b)kranium (Kafatası) 2) GÖVDE a)toraks (Göğüs kafesi) b)karın 3) EKSTREMİTELER a)üst ekstremiteler b)alt ekstremiteler
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri. Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı
 Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
KOLOREKTAL POLİPLER. Prof. Dr. Mustafa Taşkın
 KOLOREKTAL POLİPLER Prof. Dr. Mustafa Taşkın -Polip,mukozal örtülerden lümene doğru gelişen oluşumlara verilen genel isimdir. -Makroskopik ve radyolojik görünümü tanımlar. -Sindirim sisteminde en çok kolonda
KOLOREKTAL POLİPLER Prof. Dr. Mustafa Taşkın -Polip,mukozal örtülerden lümene doğru gelişen oluşumlara verilen genel isimdir. -Makroskopik ve radyolojik görünümü tanımlar. -Sindirim sisteminde en çok kolonda
Kıkırdak Doku Kemik Doku
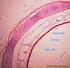 Atatürk Üniversitesi Veteriner Fakültesi Histoloji Embriyoloji Anabilim Dalı Kıkırdak Doku Kemik Doku Doç. Dr. Nejdet ŞİMŞEK Kıkırdak Doku Destek dokulardandır Burun, gırtlak, hava borusu, akciğerler,
Atatürk Üniversitesi Veteriner Fakültesi Histoloji Embriyoloji Anabilim Dalı Kıkırdak Doku Kemik Doku Doç. Dr. Nejdet ŞİMŞEK Kıkırdak Doku Destek dokulardandır Burun, gırtlak, hava borusu, akciğerler,
Kemik iliği yapısı Miyeloretiküler Bağ Dokusu
 Kemik iliği yapısı Miyeloretiküler Bağ Dokusu Doç. Dr. Sinan Özkavukcu Histoloji-Embriyoloji AD Öğretim Üyesi Üremeye Yardımcı Tedavi ve Eğitim Merkezi Laboratuvar Sorumlusu Kemik İliği Kemik iliği çok
Kemik iliği yapısı Miyeloretiküler Bağ Dokusu Doç. Dr. Sinan Özkavukcu Histoloji-Embriyoloji AD Öğretim Üyesi Üremeye Yardımcı Tedavi ve Eğitim Merkezi Laboratuvar Sorumlusu Kemik İliği Kemik iliği çok
DOKU. Dicle Aras. Doku ve doku türleri
 DOKU Dicle Aras Doku ve doku türleri Doku Bazı özel görevler üstlenmiş hücre topluluklarıdır. Bir doku aynı yönde özelleşmiş hücre ve hücreler arası maddelerin bir araya gelmesiyle oluşmuştur. İntrauterin
DOKU Dicle Aras Doku ve doku türleri Doku Bazı özel görevler üstlenmiş hücre topluluklarıdır. Bir doku aynı yönde özelleşmiş hücre ve hücreler arası maddelerin bir araya gelmesiyle oluşmuştur. İntrauterin
FTR 207 Kinezyoloji I. Eklemlerin Temel Yapısı ve Fonksiyonu. yrd.doç.dr. emin ulaş erdem
 FTR 207 Kinezyoloji I Eklemlerin Temel Yapısı ve Fonksiyonu yrd.doç.dr. emin ulaş erdem GİRİŞ İki ya da daha fazla kemiğin pivot noktasına ya da kavşağına eklem denir. Vücudun hareketi kemiklerin bireysel
FTR 207 Kinezyoloji I Eklemlerin Temel Yapısı ve Fonksiyonu yrd.doç.dr. emin ulaş erdem GİRİŞ İki ya da daha fazla kemiğin pivot noktasına ya da kavşağına eklem denir. Vücudun hareketi kemiklerin bireysel
KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI
 KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI AMAÇ Kanser ön ya da kesin tanılı hastalarda radyolojik algoritmayı belirlemek ÖĞRENİM HEDEFLERİ Kanser riski olan hastalara doğru radyolojik tetkik
KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI AMAÇ Kanser ön ya da kesin tanılı hastalarda radyolojik algoritmayı belirlemek ÖĞRENİM HEDEFLERİ Kanser riski olan hastalara doğru radyolojik tetkik
29 yaşında erkek aktif şikayeti yok. sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması. üzerine hasta polikliniğimize başvurdu
 29 yaşında erkek aktif şikayeti yok Dış merkezde yapılan üriner sistem ultrasonografisinde insidental olarak sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması üzerine hasta polikliniğimize
29 yaşında erkek aktif şikayeti yok Dış merkezde yapılan üriner sistem ultrasonografisinde insidental olarak sağ sürrenal lojda yaklaşık 3 cm lik solid kitlesel lezyon saptanması üzerine hasta polikliniğimize
NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ
 NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ Dinç Süren 1, Mustafa Yıldırım 2, Vildan Kaya 3, Ruksan Elal 1, Ömer Tarık Selçuk 4, Üstün Osma 4, Mustafa Yıldız 5, Cem
NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ Dinç Süren 1, Mustafa Yıldırım 2, Vildan Kaya 3, Ruksan Elal 1, Ömer Tarık Selçuk 4, Üstün Osma 4, Mustafa Yıldız 5, Cem
Endometrial stromal tümörler
 Endometrial stromal tümörler WHO-2014 sınıflamasında neler değişti? Dr. Şennur İlvan İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji AD Endometrial stromal tümör (1966) Endometrial stromal nodül Low grade endometrial
Endometrial stromal tümörler WHO-2014 sınıflamasında neler değişti? Dr. Şennur İlvan İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji AD Endometrial stromal tümör (1966) Endometrial stromal nodül Low grade endometrial
TÜLAY AKSARAY TECİMER 4 MAYIS 2013
 TÜLAY AKSARAY TECİMER 4 MAYIS 2013 Langerhans hücreli histiyositoz(lhh) Castleman Hastalığı (CH) Kimura Hastalığı Kikuchi Fujimoto -Histiyositik nekrotizan lenfadenit Rosai-Dorfman hastalığı Tanım Langerhans
TÜLAY AKSARAY TECİMER 4 MAYIS 2013 Langerhans hücreli histiyositoz(lhh) Castleman Hastalığı (CH) Kimura Hastalığı Kikuchi Fujimoto -Histiyositik nekrotizan lenfadenit Rosai-Dorfman hastalığı Tanım Langerhans
Omurga-Omurilik Cerrahisi
 Omurga-Omurilik Cerrahisi BR.HLİ.017 Omurga cerrahisi, omurilik ve sinir kökleri ile bu hassas sinir dokusunu saran/koruyan omurga üzerinde yapılan ameliyatları ve çeşitli girişimleri içerir. Omurga ve
Omurga-Omurilik Cerrahisi BR.HLİ.017 Omurga cerrahisi, omurilik ve sinir kökleri ile bu hassas sinir dokusunu saran/koruyan omurga üzerinde yapılan ameliyatları ve çeşitli girişimleri içerir. Omurga ve
İskelet ve kemik çeşitleri nelerdir?
 On5yirmi5.com İskelet ve kemik çeşitleri nelerdir? İskelet ve kemik çeşitleri nelerdir? Yayın Tarihi : 16 Kasım 2012 Cuma (oluşturma : 1/4/2017) A. İSKELET ÇEŞİTLERİ Hayvanların çoğunda, vücuda destek
On5yirmi5.com İskelet ve kemik çeşitleri nelerdir? İskelet ve kemik çeşitleri nelerdir? Yayın Tarihi : 16 Kasım 2012 Cuma (oluşturma : 1/4/2017) A. İSKELET ÇEŞİTLERİ Hayvanların çoğunda, vücuda destek
Basit Guatr. Yrd.Doç.Dr. Okan BAKINER
 Basit Guatr Yrd.Doç.Dr. Okan BAKINER Amaç Basit (nontoksik) diffüz ve nodüler guatrı öğrenmek, tanı ve takip prensiplerini irdelemek. Öğrenim hedefleri 1.Tanım 2.Epidemiyoloji 3.Etiyoloji ve patogenez
Basit Guatr Yrd.Doç.Dr. Okan BAKINER Amaç Basit (nontoksik) diffüz ve nodüler guatrı öğrenmek, tanı ve takip prensiplerini irdelemek. Öğrenim hedefleri 1.Tanım 2.Epidemiyoloji 3.Etiyoloji ve patogenez
MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR?
 MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR? Dr. Nebil BAL Başkent Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Adana Arş ve Uyg Mrk 1 Malign Melanoma Deri Mukozal 2 Malign Melanoma Biyopsi
MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR? Dr. Nebil BAL Başkent Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Adana Arş ve Uyg Mrk 1 Malign Melanoma Deri Mukozal 2 Malign Melanoma Biyopsi
Osteoporoz Rehabilitasyonu
 Osteoporoz Rehabilitasyonu OSTEOPOROZ Kemik kitlesinde azalma, kemik mikroyapısında bozulma sonucu kemik kırılganlığının artması olarak tanımlanır. Kemik yaşayan, dengeli bir şekilde oluşan yıkım ve yapım
Osteoporoz Rehabilitasyonu OSTEOPOROZ Kemik kitlesinde azalma, kemik mikroyapısında bozulma sonucu kemik kırılganlığının artması olarak tanımlanır. Kemik yaşayan, dengeli bir şekilde oluşan yıkım ve yapım
Meme Olgu Sunumu. Gürdeniz Serin. Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı. 3 Kasım Antalya
 Meme Olgu Sunumu 3 Kasım 2016 Antalya Gürdeniz Serin Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Olgu 35 yaşında kadın Sağ meme de kitle Özgeçmişinde: SLE - Renal Tx Radyoloji Mamografi: Sağ
Meme Olgu Sunumu 3 Kasım 2016 Antalya Gürdeniz Serin Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Olgu 35 yaşında kadın Sağ meme de kitle Özgeçmişinde: SLE - Renal Tx Radyoloji Mamografi: Sağ
KEMİĞİN DEV HÜCRELİ LEZYONLARINDA HÜCRE SİKLUS PROTEİNLERİNİN (SİKLİN D1, SİKLİN D3, P21, P27) VE Ki-67 NİN DEĞERLENDİRİLMESİ
 T.C. ÇUKUROVA ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI KEMİĞİN DEV HÜCRELİ LEZYONLARINDA HÜCRE SİKLUS PROTEİNLERİNİN (SİKLİN D1, SİKLİN D3, P21, P27) VE Ki-67 NİN DEĞERLENDİRİLMESİ Dr. AYŞE GÖKDEMİR
T.C. ÇUKUROVA ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI KEMİĞİN DEV HÜCRELİ LEZYONLARINDA HÜCRE SİKLUS PROTEİNLERİNİN (SİKLİN D1, SİKLİN D3, P21, P27) VE Ki-67 NİN DEĞERLENDİRİLMESİ Dr. AYŞE GÖKDEMİR
YARA İYİLEŞMESİ. Yrd.Doç.Dr. Burak Veli Ülger
 YARA İYİLEŞMESİ Yrd.Doç.Dr. Burak Veli Ülger YARA Doku bütünlüğünün bozulmasıdır. Cerrahi ya da travmatik olabilir. Akut Yara: Onarım süreci düzenli ve zamanında gelişir. Anatomik ve fonksiyonel bütünlük
YARA İYİLEŞMESİ Yrd.Doç.Dr. Burak Veli Ülger YARA Doku bütünlüğünün bozulmasıdır. Cerrahi ya da travmatik olabilir. Akut Yara: Onarım süreci düzenli ve zamanında gelişir. Anatomik ve fonksiyonel bütünlük
Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları ABD, Medikal Onkoloji BD Güldal Esendağlı
 Sağlık Bakanlığından Muaf Hekimin Ünvanı - Adı Soyadı Aydın Aytekin Bildiriyi Sunacak Kişi Ünvanı - Adı Soyadı Rafiye Çiftçiler Bildiriyi Sunacak Kişi Kurumu Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları
Sağlık Bakanlığından Muaf Hekimin Ünvanı - Adı Soyadı Aydın Aytekin Bildiriyi Sunacak Kişi Ünvanı - Adı Soyadı Rafiye Çiftçiler Bildiriyi Sunacak Kişi Kurumu Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları
Tiroidin en sık görülen benign tümörleri foliküler adenomlardır.
 GİRİŞ: Tiroidin en sık görülen benign tümörleri foliküler adenomlardır. Foliküler adenomlar iyi sınırlı tek lezyon şeklinde olup, genellikle adenomu normal tiroid dokusundan ayıran kapsülleri vardır. Sıklıkla
GİRİŞ: Tiroidin en sık görülen benign tümörleri foliküler adenomlardır. Foliküler adenomlar iyi sınırlı tek lezyon şeklinde olup, genellikle adenomu normal tiroid dokusundan ayıran kapsülleri vardır. Sıklıkla
Hücre. 1 µm = 0,001 mm (1000 µm = 1 mm)!
 HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
HÜCRE FİZYOLOJİSİ Hücre Hücre: Tüm canlıların en küçük yapısal ve fonksiyonel ünitesi İnsan vücudunda trilyonlarca hücre bulunur Fare, insan veya filin hücreleri yaklaşık aynı büyüklükte Vücudun büyüklüğü
TİROİD (GUATR) CERRAHİSİ HAKKINDA SIK SORULAN SORULAR FR-HYE-04-301-08
 TİROİD (GUATR) CERRAHİSİ HAKKINDA SIK SORULAN SORULAR FR-HYE-04-301-08 Tiroid bezi boyun ön tarafında yerleşmiş olup, nefes, yemek borusu ve ana damarlarla yakın komşuluk gösterir. Kelebek şeklinde olup
TİROİD (GUATR) CERRAHİSİ HAKKINDA SIK SORULAN SORULAR FR-HYE-04-301-08 Tiroid bezi boyun ön tarafında yerleşmiş olup, nefes, yemek borusu ve ana damarlarla yakın komşuluk gösterir. Kelebek şeklinde olup
OLGU SUNUMU. Prof. Dr. Yeşim Gürbüz
 OLGU SUNUMU Prof. Dr. Yeşim Gürbüz HİKAYE 48 yaşında bayan hasta, 2 senedir nefes darlığı olan hasta dahiliyeye başvurmuş, Tiroit palpasyonunda sol lopta 3x2 cm boyutunda kitle ele gelmiş, MNG tanısı
OLGU SUNUMU Prof. Dr. Yeşim Gürbüz HİKAYE 48 yaşında bayan hasta, 2 senedir nefes darlığı olan hasta dahiliyeye başvurmuş, Tiroit palpasyonunda sol lopta 3x2 cm boyutunda kitle ele gelmiş, MNG tanısı
Klinik ve Radyolojik Değerlendirme 4
 Klinik ve Radyolojik Değerlendirme 4 Prof.Dr. Kıvanç Kamburoğlu Ankara Üniversitesi Diş Hekimliği Fakültesi Ağız, Diş ve Çene Radyolojisi Ana Bilim Dalı Rezolüsyona bağlı olarak farklı tekniklerde alınmış
Klinik ve Radyolojik Değerlendirme 4 Prof.Dr. Kıvanç Kamburoğlu Ankara Üniversitesi Diş Hekimliği Fakültesi Ağız, Diş ve Çene Radyolojisi Ana Bilim Dalı Rezolüsyona bağlı olarak farklı tekniklerde alınmış
Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim
 Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim Murat Özdemir, Özer Makay, Tevfik Demir*, Berk Göktepe, Kamil Erözkan, Barış Bingül**, Yeşim Ertan**, Hüsnü Buğdaycı***, Gökhan İçöz, Mahir Akyıldız
Paratiroid Kanserinde Yönetim İzmir den Üç Merkezli Deneyim Murat Özdemir, Özer Makay, Tevfik Demir*, Berk Göktepe, Kamil Erözkan, Barış Bingül**, Yeşim Ertan**, Hüsnü Buğdaycı***, Gökhan İçöz, Mahir Akyıldız
Benign ve Malign Kemik Lezyonlarını Değerlendirmede Bilgisayarlı Tomografinin Değeri
 DERLEME DOI:10.4274/nts.2016.003 Nuclear Medicine Seminars / Nükleer Tıp Seminerleri 2016;1:15-20 Benign ve Malign Kemik Lezyonlarını Değerlendirmede Bilgisayarlı Tomografinin Değeri The Value of Computed
DERLEME DOI:10.4274/nts.2016.003 Nuclear Medicine Seminars / Nükleer Tıp Seminerleri 2016;1:15-20 Benign ve Malign Kemik Lezyonlarını Değerlendirmede Bilgisayarlı Tomografinin Değeri The Value of Computed
PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ
 PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ Dr. Nimet Karadayı Dr.Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi Patoloji Kliniği Lenf nodları metastatik malignitelerde en
PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ Dr. Nimet Karadayı Dr.Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi Patoloji Kliniği Lenf nodları metastatik malignitelerde en
GÖĞÜS DUVARI TÜMÖRLERİ. PROF. DR. REFİK ÜLKÜ D.Ü Tıp Fak Göğüs Cerrahisi
 GÖĞÜS DUVARI TÜMÖRLERİ PROF. DR. REFİK ÜLKÜ D.Ü Tıp Fak Göğüs Cerrahisi Primer göğüs duvarı tümörleri göğüs kafesindeki, kemik,kıkırdak ve yumuşak dokulardan kaynaklanabilen, benign veya malign, geniş
GÖĞÜS DUVARI TÜMÖRLERİ PROF. DR. REFİK ÜLKÜ D.Ü Tıp Fak Göğüs Cerrahisi Primer göğüs duvarı tümörleri göğüs kafesindeki, kemik,kıkırdak ve yumuşak dokulardan kaynaklanabilen, benign veya malign, geniş
oporoz Tanı ve Tedavi Prensipleri
 Osteoporoz Tanı ve Tedavi oporoz Tanı ve Tedavi Prensipleri Prensipleri Dr. Ümit İNCEBOZ Balıkesir Üniversitesi Tıp Fakültesi Kadın Hastalıkları ve Doğum AD Dr. Ümit İNCEBOZ Balıkesir Üniversitesi Tıp
Osteoporoz Tanı ve Tedavi oporoz Tanı ve Tedavi Prensipleri Prensipleri Dr. Ümit İNCEBOZ Balıkesir Üniversitesi Tıp Fakültesi Kadın Hastalıkları ve Doğum AD Dr. Ümit İNCEBOZ Balıkesir Üniversitesi Tıp
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ. Dr. Derin KÖSEBAY
 ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
RADYOLOJİ RADYODİAGNOSTİK ANABİLİM DALI-DÜTF- DİYARBAKIR
 NÖRORADYOLOJİ NÖRORADYOLOJİDE GÖRÜNTÜLEME YÖNTEMLERİ ve GİRİŞİMSEL RADYOLOJİ RADYODİAGNOSTİK ANABİLİM DALI-DÜTF- DİYARBAKIR Dr. Faysal EKİCİ İNCELEME YÖNTEMLERİ DİREKT GRAFİLER BİLGİSAYARLI TOMOGRAFİ MANYETİK
NÖRORADYOLOJİ NÖRORADYOLOJİDE GÖRÜNTÜLEME YÖNTEMLERİ ve GİRİŞİMSEL RADYOLOJİ RADYODİAGNOSTİK ANABİLİM DALI-DÜTF- DİYARBAKIR Dr. Faysal EKİCİ İNCELEME YÖNTEMLERİ DİREKT GRAFİLER BİLGİSAYARLI TOMOGRAFİ MANYETİK
Sinir Kılıfı Tümörleri. Doç. Dr. Halil KIYICI 2016
 Sinir Kılıfı Tümörleri Doç. Dr. Halil KIYICI 2016 Sinir Sistemi Merkezi (santral) sinir sistemi (MSS): beyin ve omurilikten oluşur kafatası - omurga kemikleri ve kemik altındaki pia örtüsüyle kaplıdır
Sinir Kılıfı Tümörleri Doç. Dr. Halil KIYICI 2016 Sinir Sistemi Merkezi (santral) sinir sistemi (MSS): beyin ve omurilikten oluşur kafatası - omurga kemikleri ve kemik altındaki pia örtüsüyle kaplıdır
Yaşlanmaya Bağlı Oluşan Kas ve İskelet Sistemi Patofizyolojileri. Sena Aydın 0341110011
 Yaşlanmaya Bağlı Oluşan Kas ve İskelet Sistemi Patofizyolojileri Sena Aydın 0341110011 PATOFİZYOLOJİ Fizyoloji, hücre ve organların normal işleyişini incelerken patoloji ise bunların normalden sapmasını
Yaşlanmaya Bağlı Oluşan Kas ve İskelet Sistemi Patofizyolojileri Sena Aydın 0341110011 PATOFİZYOLOJİ Fizyoloji, hücre ve organların normal işleyişini incelerken patoloji ise bunların normalden sapmasını
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi
 Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
Selim kemik tümörleri: Sınıflama, klinik ve radyolojik özellikler, biyopsi. Bülent Erol, Nadir Aydemir
 TOTBİD Dergisi Türk Ortopedi ve Travmatoloji Birliği Derneği TOTBİD Dergisi 2013; 12:490 500 doi: 10.14292/totbid.dergisi.2013.57 DERLEME Selim kemik tümörleri: Sınıflama, klinik ve radyolojik özellikler,
TOTBİD Dergisi Türk Ortopedi ve Travmatoloji Birliği Derneği TOTBİD Dergisi 2013; 12:490 500 doi: 10.14292/totbid.dergisi.2013.57 DERLEME Selim kemik tümörleri: Sınıflama, klinik ve radyolojik özellikler,
VÜCUDUMUZDA SISTEMLER. Destek ve Hareket
 VÜCUDUMUZDA SISTEMLER Destek ve Hareket DESTEK VE HAREKET SİSTEMİ Vücudun hareket etmesini sağlamak Vücutta bulunan organlara destek sağlamak Destek ve Hareket Sistemi İskelet Sistemi Kaslar Kemikler Eklemler
VÜCUDUMUZDA SISTEMLER Destek ve Hareket DESTEK VE HAREKET SİSTEMİ Vücudun hareket etmesini sağlamak Vücutta bulunan organlara destek sağlamak Destek ve Hareket Sistemi İskelet Sistemi Kaslar Kemikler Eklemler
Polipte Kanser. Dr.Cem Terzi. Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi
 Polipte Kanser Dr.Cem Terzi Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi Polip ve polipoid karsinoma POLİP Epitelyal yüzeyden kaynaklanan çıkıntı HİSTOLOJİK POLİP TİPLERİ
Polipte Kanser Dr.Cem Terzi Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi Polip ve polipoid karsinoma POLİP Epitelyal yüzeyden kaynaklanan çıkıntı HİSTOLOJİK POLİP TİPLERİ
BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ. Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi
 BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi 61 y/ K Sol parotiste kitle Makroskopi: 2.3x2.2x0.7 cm ölçülerinde kirli beyaz-kahverengi, kesitinde
BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi 61 y/ K Sol parotiste kitle Makroskopi: 2.3x2.2x0.7 cm ölçülerinde kirli beyaz-kahverengi, kesitinde
FİBRİNOJEN DEPO HASTALIĞI. Yrd.Doç.Dr. Güldal YILMAZ Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı Ankara
 FİBRİNOJEN DEPO HASTALIĞI Yrd.Doç.Dr. Güldal YILMAZ Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı Ankara H. K., 5 yaşında, Kız çocuğu Şikayet: Karında şişlik Özgeçmiş: 8 aylıkken karında
FİBRİNOJEN DEPO HASTALIĞI Yrd.Doç.Dr. Güldal YILMAZ Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı Ankara H. K., 5 yaşında, Kız çocuğu Şikayet: Karında şişlik Özgeçmiş: 8 aylıkken karında
Tanı Olgularda ayrıntılı bir anemnezin ardından dikkatli bir fizik muayene ve rutin laboratuvar incelemeleri
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Göğüs Duvarı Tümörleri Primer göğüs duvarı tümörleri yumuşak doku, kemik ve kıkırdak kaynaklı olabilir. Primer malign göğüs duvarı tümörlerinin
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Göğüs Duvarı Tümörleri Primer göğüs duvarı tümörleri yumuşak doku, kemik ve kıkırdak kaynaklı olabilir. Primer malign göğüs duvarı tümörlerinin
TRD KIŞ OKULU KURS 2, Gün 3. Sorular
 TRD KIŞ OKULU KURS 2, Gün 3 Sorular SORU 1 Romatoid artrit ile psöryatik artritin birbirinde ayırt edilmesinde EN ÖNEMLİ radyografik özellik hangisidir? a. Uniform eklem aralığı daralmasının varlığı veya
TRD KIŞ OKULU KURS 2, Gün 3 Sorular SORU 1 Romatoid artrit ile psöryatik artritin birbirinde ayırt edilmesinde EN ÖNEMLİ radyografik özellik hangisidir? a. Uniform eklem aralığı daralmasının varlığı veya
ÖN ÇAPRAZ BAĞ ZEDELENMELERİ
 ÖN ÇAPRAZ BAĞ ZEDELENMELERİ Diz eklemi çepeçevre bağlarla desteklenen ve cildin altında kaslarla çevrili olmadığı için de travmaya son derece açık olan bir eklemdir. Diz ekleminde kayma, menteşe ve dönme
ÖN ÇAPRAZ BAĞ ZEDELENMELERİ Diz eklemi çepeçevre bağlarla desteklenen ve cildin altında kaslarla çevrili olmadığı için de travmaya son derece açık olan bir eklemdir. Diz ekleminde kayma, menteşe ve dönme
Karsinoid Tümörler Giriş Sınıflandırma: Göğüs Cer rahisi rahisi Göğüs Cer Klinik:
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Karsinoid Tümörler Giriş Ender görülen akciğer tümörleridirler Rezeksiyon uygulanan akciğer tümörlerinin %0,4- %3 ünü oluştururlar Benign-malign
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Karsinoid Tümörler Giriş Ender görülen akciğer tümörleridirler Rezeksiyon uygulanan akciğer tümörlerinin %0,4- %3 ünü oluştururlar Benign-malign
MENİSKÜS ZEDELENMELERİ
 MENİSKÜS ZEDELENMELERİ Diz eklemi uyluk (femur) ve kaval (tibia) kemikleri arasında kusursuz bir uyum içinde çalışır. Bu uyumun sağlanmasında, diz içerisinde yer alan menisküs denilen yarım ay şeklindeki
MENİSKÜS ZEDELENMELERİ Diz eklemi uyluk (femur) ve kaval (tibia) kemikleri arasında kusursuz bir uyum içinde çalışır. Bu uyumun sağlanmasında, diz içerisinde yer alan menisküs denilen yarım ay şeklindeki
