Salk Bakanlndan: 13 mart 2002 tarihli sayl resmi gazetede yaynlanmtr. Tbbi Cihaz Yönetmelii
|
|
|
- Mehmed Albayrak
- 6 yıl önce
- İzleme sayısı:
Transkript
1 Salk Bakanlndan: 13 mart 2002 tarihli sayl resmi gazetede yaynlanmtr. Tbbi Cihaz Yönetmelii BRNC BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeliin amac; insan salnda dorudan veya dolayl olarak kullanlan tbbî cihaz ve aksesuarlarnn tamas gereken temel gereklerin belirlenmesine, tasarmna, üretimine, datmna, piyasaya arzna, hizmete sunulmasna, kullanlmasna, snflandrlmasna, denetlenmesine ve tbbî cihaz ve aksesuarlarnn kullanm srasnda hastalarn, uygulayclarn, kullanclarn ve üçüncü kiilerin salk ve güvenlii açsndan ortaya çkabilecek tehlikelere kar korunmalarn salayacak ekilde piyasaya sunulmasna ilikin usul ve esaslar düzenlemektir. Kapsam Madde 2 Bu Yönetmelik; kamu kurum ve kurulular ile gerçek ve tüzel kiilerin, tbbî cihaz ve aksesuarlarnn tasarm, üretimi, datm, piyasaya arz, hizmete sunulmas ve kullanm ile ilgili bütün faaliyetlerini kapsar. nsan kan türevini, ilevinin bir parças olarak içeren tbbî cihazlar da bu Yönetmelik kapsamndadr. Tbbî cihaz, ilevini yerine getirebilmek için tbbî ürün ile birlikte kullanlyor ise, tbbî ürün kendisi ile ilgili mevzuat kapsamnda; tbbî cihaz da bu Yönetmelik kapsamnda deerlendirilir. Tbbî cihaz, tbbî ürün veya ilaç ile kombine halde tek bir ürün olarak kullanlyor ve tek kullanmlk ise, tbbî ürün veya ilaç kabul edilerek ilgili mevzuat kapsamnda deerlendirilir. Ancak; a) In vitro tbbî tan cihazlar, b) nsan vücuduna yerletirilebilir aktif tbbî cihazlar, c) Tbbî ürünler, d) Kozmetik ürünleri, e) nsan kan türevleri hariç olmak üzere; insan kan, kan ürünleri, insan kaynakl plazma veya kan hücreleri ile insan hücresi, dokusu, nakil organlar veya bunlardan üretilen ürünler, f) Cansz hayvan dokular ve cansz hayvan dokularndan üretilen ürünleri içeren cihazlar hariç olmak üzere, hayvan kökenli doku ve hücreler, g) Ürünün esas kullanm amacna bal olarak kiisel koruma cihazlar, bu Yönetmelik kapsam dndadr. Hukukî Dayanak Madde 3 Bu Yönetmelik; 29/6/2001 tarihli ve 4703 sayl Ürünlere likin Teknik Mevzuatn Hazrlanmas ve Uygulanmasna Dair Kanunun 4 üncü maddesine, 7/5/1987 tarihli ve 3359 sayl Salk Hizmetleri Temel Kanununun 3 üncü maddesinin (k) bendi ile 9 uncu maddesinin (c) bendine 13/12/1983 tarihli ve 181 sayl Salk Bakanlnn Tekilat ve Görevleri Hakknda Kanun Hükmünde Kararnamenin 43 üncü maddesine dayanlarak hazrlanmtr. Tanmlar Madde 4 Bu Yönetmelikte geçen; a) Kanun: 29/6/2001 tarihli ve 4703 sayl Ürünlere likin Teknik Mevzuatn Hazrlanmas ve Uygulanmasna Dair Kanunu, b) Bakanlk: Salk Bakanln, c) Müstearlk: D Ticaret Müstearln, d) Komisyon: Avrupa Birlii Komisyonunu, e) Temel Gerekler: Tbbî cihaz ve aksesuarlarnn; insan sal, can ve mal güvenlii, hayvan ve bitki yaam ve sal, çevre ve tüketicinin korunmas açsndan sahip olmas gereken asgarî güvenlik koullarn, f) Üretici: Bu Yönetmelie uygun olarak piyasada hazr bulunan tbbî cihaz ve aksesuarlarn, hastasna uygun hale getirip kullanma hazrlayan kiiler hariç olmak üzere; bir tbbî cihaz üreten, slah eden veya buna adn, ticarî markasn veyahut ayrt edici iaretini koymak suretiyle kendini üretici olarak tantan gerçek veya tüzel kiiyi; üreticinin Türkiye dnda olmas halinde ise, üretici tarafndan yetkilendirilen temsilciyi ve/veya
2 ithalatçy; ayrca, tbbî cihazn tedarik zincirinde yeralan ve faaliyetleri, tbbî cihazn güvenliine ilikin özelliklerini etkileyen gerçek veya tüzel kiiyi, g) Datc: Tbbî cihazn tedarik zincirinde yeralan ve faaliyetleri, tbbî cihazn güvenliine ilikin özelliklerini etkilemeyen gerçek veya tüzel kiiyi, h) Standart: Üzerinde mutabakat salanm olan, kabul edilmi bir kurulu tarafndan onaylanan, mevcut artlar altnda en uygun seviyede bir düzen kurulmasn amaçlayan, ortak ve tekrar eden kullanmlar için tbbî cihazn özellikleri, ileme ve üretim yöntemleri, bunlarla ilgili terminoloji, sembol, ambalajlama, iaretleme, etiketleme ve uygunluk deerlendirmesi ilemleri hususlarndan biri veya birkaçn belirten ve uyulmas ihtiyarî olan düzenlemeyi, ) Uyumlatrlm Standart: Bu Yönetmelik ile ilgili olan ve Avrupa Birlii tarafndan belirlenmi standartlara uygun olarak Türk Standartlar Enstitüsü tarafndan uyumlatrlarak kabul edilen ve Bakanlkça her yl listesi tebliler halinde yaymlanan ulusal standartlar, i) Tbbî Cihaz: nsanda kullanldklarnda aslî fonksiyonunu, farmakolojik, kimyasal, immünolojik veya metabolik etkiler ile salamayan; fakat, fonksiyonunu yerine getirirken bu etkiler tarafndan desteklenebilen ve insan üzerinde bir hastaln, yaralanmann, sakatln tans, tedavisi, izlenmesi ve kontrol altnda tutulmas, hafifletilmesi veya maduriyetin giderilmesi, anatomik veya fizyolojik bir ilevin aratrlmas, deitirilmesi veya yerine baka bir ey konulmas, doum kontrolü veya sadece ilaç uygulamak amacyla üretilmi, tek bana veya birlikte kullanlabilen, amaçlanan ilevini yerine getirebilmesi için gerekiyorsa bilgisayar yazlm ile de kullanlan ve cansz hayvanlarn dokularndan da elde edilen ürünler dahil olmak üzere, her türlü araç, alet, cihaz, aksesuar veya dier malzemeleri (bundan sonra, "cihaz" olarak anlacaktr), j) Aksesuar: Kendi bana cihaz saylmayan ve fakat, cihaz ile birlikte kullanlmak amacyla üretilen parçay veya parçalar, k) Ismarlama Üretilen Cihaz: Toplu üretime tâbi olan ve uygulayc hekimin isteklerine göre uyarlanan cihazlar hariç olmak üzere; uzman hekimin reçetesine istinaden belirli bir hastada kullanlmak amacyla üretilen parçay veya parçalar veyahut, uzman hekimin sorumluluunda belirli bir hastada kullanlmak üzere sipari edilen cihazlar, l) nsan Kan Türevi: nsan vücudu üzerindeki etkisini entegral parças olarak içinde bulunduu bir cihaz ile salayan, insan kan ve plazmasndan türetilen tbbî ürünleri, m) Klinik Aratrma Cihaz: Konusunda uzman hekim veya klinik aratrma yapmaya yetkili kii tarafndan yeterli klinik ortamda insan üzerinde yaplacak klinik aratrmalarda kullanlmak üzere tasarlanan cihaz veya cihazlar, n) n Vitro Tbbî Tan Cihaz: Genel laboratuvar kullanmna yönelik cihazlar, özellikleri bakmndan üreticileri tarafndan bilhassa in vitro inceleme amaçl kullanlmyorlar ise, in vitro tbbî tan cihaz deildir. Üreticinin sadece, fizyolojik veya patolojik durum veya kaltmsal anomalilerle ilgili bilgi edinmek veya güvenlik seviyesini ve muhtemel kullanclara uygunluunu tespit etmek veya tedavi edici tedbirleri izlemek için tek bana veya birlikte kullanlmasna baklmakszn, insan vücudundan alnan kan ve doku balarn da içeren numunelerin incelenmesinde in vitro kullanmay amaçlad, ayraç (reaktif), ayraç ürünü, kalibratör, kontrol materyali, kit, araç, gereç, ekipman veya sistem olan bütün tbbî cihazlar ve vakumlu özellie sahip olsun veya olmasn, üreticileri tarafndan özellikle, in vitro tbbî tan incelemesi için insan vücudundan alnan örneklerin konulmas ve muhafaza edilmesi amacyla kullanlan numune kaplarn, o) Onaylanm Kurulu: Test, muayene ve/veya belgelendirme kurulular arasndan, bu Yönetmelik çerçevesinde uygunluk deerlendirme faaliyetinde bulunmak üzere, Kanunda, bu Yönetmelikte ve 17/1/2002 tarihli ve sayl Resmî Gazete de yaymlanan Uygunluk Deerlendirme Kurulular ile Onaylanm Kurululara Dair Yönetmelikte belirtilen esaslar çerçevesinde yetkilendirilen kamu veya özel kuruluu, ö) Beyan Edilen Amaç: Üretici tarafndan cihazn etiketinde, kullanm klavuzunda veya tantm broüründe belirtilen kullanm amac ile ilgili bilgileri, p) Piyasaya Arz: Klinik aratrma cihazlar hariç olmak üzere; cihazn, yeni veya yenilenmi olmasna baklmakszn, tedarik veya kullanm amacyla bedelli veya bedelsiz olarak ilk defa piyasada yer almas için yaplan faaliyeti, r) Hizmete Sunmak: Bir cihazn, kullanm amacna uygun olarak, piyasada ilk defa son kullancnn kullanmna hazr hale getirilmesini, s) CE Uygunluk areti: Üreticinin, bu Yönetmelikten doan yükümlülüklerini yerine getirdiini ve cihaz ve aksesuarlarnn ilgili bütün uygunluk deerlendirme ilemlerine tâbi tutulduunu gösteren iareti, ) Danma Komisyonu: Bakanln gerektiinde, klinik aratrma konusunda veya tbbî ve teknik konularda oluturaca danma komisyonunu,
3 t) Uygunluk Deerlendirmesi: Cihaz ve aksesuarlarnn, bu Yönetmelik hükümlerine uygunluunun test ve muayene edilmesine ve/veya belgelendirilmesine ilikin her türlü faaliyeti, u) Tasarm-nceleme Sertifikas: Onaylanm kuruluun, cihaz ve aksesuarlarnn tasarmnn bu Yönetmelik hükümlerine uygunluuna karar vermesi halinde üreticiye verecei belgeyi, ü) Tip-nceleme Sertifikas: Onaylanm kuruluun, üretim numunesinin bu Yönetmelik hükümlerine uygunluuna karar vermesi halinde üreticiye verecei belgeyi, v) Tip ncelemesi: Onaylanm kurulu tarafndan, üretim numunesinin bu Yönetmelik hükümlerine uygunluunun incelenmesi ve deerlendirilmesi ilemini, y) Tip Dorulamas: Onaylanm kuruluun, cihaz test ederek, cihazn tip-inceleme sertifikasnda tanmlanan tipe ve bu Yönetmelik hükümlerine uygunluunu beyan ve garanti eden ilemini, ifade eder. KNC BÖLÜM Temel Gerekler, Standartlar, Snflandrma, stisnaî Durumlarla lgili Kararlar, Uygunluk Deerlendirme lemleri ve CE aretlemesi Temel Gerekler Madde 5 Üretici, cihazn kullanm amacn da dikkate almak suretiyle cihaz ile ilgili olarak EK-I de belirtilen temel gereklere uymak zorundadr. Üretici tarafndan cihazla birlikte, hastalara, kullanclara ve uygulayclara yönelik olarak verilmesi gereken EK-I/13 de belirtilen bilgiler, kullanm klavuzlar, etiketler ve dier açklamalar, Türkçe ve tercihan ngilizce veya Franszca veyahut Almanca dillerinden birinde olmak üzere, en az iki dilde hazrlanm olmaldr. Standartlara Uyum Madde 6 Standartlara uyum; Avrupa ve Türk Farmakopelerinin ilgili standartlarna, özellikle cerrahi iplikler ve ilaç ihtiva eden cihazlarn ilaçla etkileimine ilikin standartlara ve uyumlatrlm standartlara uygunluktur. Birinci fkrada belirtilen standartlara uygun olarak üretilen cihazlar bakmndan, EK-I de belirtilen temel gereklerin yerine getirildii kabul edilir. Üretici veya ithalatç, uyumlatrlm standartlarn temel gerekleri tam olarak karlamadn tespit ettii takdirde, durumu Bakanla bildirir; Bakanlk, bu bilgileri Müstearlk kanalyla Komisyona iletir. Snflandrma Madde 7 Cihazlar, tasarm ve üretiminden kaynaklanan potansiyel risk durumu ve insan sal açsndan yaratabilecekleri tehlike seviyelerine göre, I., IIa., IIb., ve III. Snf olarak dört snfa ayrlr. Snflandrma, EK-IX da belirlenen esaslara göre yaplr. Snflandrma kurallarnn uygulanmasyla ilgili olarak, üretici ve onaylanm kurulu arasnda ortaya çkabilecek ihtilaflar, Bakanlk tarafndan çözümlenir. Bakanlk, cihazn piyasaya arzndan sonra tespit edilen olumsuzluklara ilikin olarak bu Yönetmeliin 17 nci maddesindeki uyar sisteminde öngörülen bilgiler ve teknik gelimeler nda, gerektiinde snflandrmann esaslarn yeniden düzenler.,stisnaî Durumlarla,lgili Kararlar Madde 8 Bakanlk; a) Cihaz ile ilgili EK-IX da belirtilen snflandrma kurallarnn uygulanmas srasnda bir karar verilmesi gerektiinde, b) Cihazn, EK-IX hükümlerinden farkl bir ekilde, baka bir snf içinde yer almas gerektiinde, c) Cihazn veya cihaz grubunun uygunluunun deerlendirilmesi srasnda, bu Yönetmeliin 9 uncu maddesinde belirtilen yöntemlerden farkl bir yöntemin tespiti gerektiinde, gerekli tedbirleri ve karar alr ve bu kararn, gerekçeleriyle birlikte Müstearlk kanalyla Komisyona bildirir. Uygunluk Deerlendirme,/lemleri Madde 9 Uygunluk deerlendirme ilemlerinde aada belirtilen hususlar dikkate alnr: a) Ismarlama üretilen cihazlar ve klinik aratrma cihazlar hariç olmak üzere; üretici, uygunluk deerlendirmesine ilikin olarak aada belirtilen ilemleri yerine getirir: 1) I. Snf cihazlarda CE iaretini ilitirmek için, sadece EK-VII de belirlenen ilemi takip eder ve uygunluk beyan düzenler. 2) IIa. Snf cihazlarda CE iaretini ilitirmek için; i) Tam kalite güvence sistemiyle ilgili olarak EK-II de belirlenen uygunluk beyan ilemini, EK-II nin 4 üncü maddesini hariç tutarak veya,
4 ii) EK-VII de belirlenen uygunluk beyan ile ilgili ilemle birlikte EK-IV de belirlenen tip dorulama ilemini veya üretim kalite güvencesiyle ilgili EK-V de belirlenen uygunluk beyan ilemini veya ürün kalite güvencesiyle ilgili EK-VI da belirlenen uygunluk beyan ilemini, takip eder. 3) IIb. Snf cihazlarda CE iaretini ilitirmek için; i) Tam kalite güvence sistemiyle ilgili olarak EK-II de belirlenen uygunluk beyan ilemini EK-II deki 4 üncü maddeyi hariç tutarak veya, ii) EK-III de belirlenen tip incelemesi ile birlikte EK-IV de belirlenen tip dorulama ilemini veya üretim kalite güvencesiyle ilgili EK-V de belirlenen uygunluk beyan ilemini veya ürün kalite güvencesiyle ilgili EK- VI da belirlenen uygunluk beyan ilemini, takip eder. 4) III. Snf cihazlarda CE iaretini ilitirmek için; i) Tam kalite güvence sistemiyle ilgili olarak EK-II de belirlenen uygunluk beyan ilemini veya, ii) EK-III de belirlenen tip incelemesiyle birlikte EK-IV de belirtilen tip dorulama ilemini veya üretim kalite güvencesiyle ilgili EK-V de belirtilen uygunluk beyan ilemini, takip eder. b) Ismarlama üretilen cihazlar için, EK-VIII de belirlenen ilemi takip ederek, bu EK deki beyan düzenler. Ismarlama üretilen cihazlarn bir listesini Bakanla verir. c) Üretici ve/veya onaylanm kurulu, üretimin ara aamasnda, bu Yönetmelie uygun olarak yaplan deerlendirme ve dorulama sonuçlarn, cihazn uygunluk beyan ilemi srasnda göz önünde bulundurur. d) Üretici, EK-III, EK-IV, EK-VII ve EK-VIII de belirlenen ilemleri balatma konusunda ülke içindeki yetkili temsilcisini görevlendirir. e) Uygunluk deerlendirme ileminde, onaylanm kuruluun yer almas gerektii durumlarda, üretici veya yetkili temsilcisi bu i için onaylanm kurululardan birini seçer. f) Onaylanm kurulu, seçilen ilem çerçevesinde uygunluu onaylamak için gerekli olan bilgi ve belgeleri bavuru sahibinden ister. g) Onaylanm kurulularca EK-II ye ve EK-III e uygun olarak alnan kararlar, en fazla be yl süre ile geçerlidir. Ancak, onaylanm kurulu ile üretici arasnda imzalanan sözlemede belirlenen süre içerisinde yaplan müracaat üzerine, kararn geçerlilik süresi, sonraki be yllk süreler için uzatlr. h) Bu maddenin (a) bendinde belirlenen yöntemler ile ilgili kaytlar ve yazmalar, Türkçe ve tercihan ngilizce veya Franszca veyahut Almanca dillerinden birinde olmak üzere, en az iki dilde yazlr. ) Bakanlk gerektiinde, bu maddenin (a) bendinde belirlenen ilemler uygulanmam olan ve fakat, kullanlmasnn saln korunmasnda yardmc olaca, hakl bir talep üzerine belirlenen bireysel cihazlarn ülke içinde piyasaya arzna ve hizmete sunulmasna izin verebilir. CE,/aretlemesi Madde 10 CE iaretinin ilitirilmesinde, aadaki hususlar dikkate alnr: a) Ismarlama üretilen cihazlar ve klinik aratrma amaçl cihazlar dnda kalan bütün cihazlar, piyasaya arz edilecekleri zaman, CE iaretini ve EK-II, EK-IV, EK-V ve EK-VI da belirtilen ilemlerin uygulanmasndan sorumlu onaylanm kuruluun kimlik numarasn tamak zorundadrlar. b) EK-XII de belirtilen CE iareti, kolayca görülebilir, okunabilir ve silinmeyecek bir ekilde cihaza ve/veya sterilliini koruyan ambalajna, kullanm klavuzuna ve mümkünse, d ambalajn üzerine ilitirilir. c) CE iaretinin anlam veya ekli konusunda yanl anlamaya yol açabilecek iaret veya ibare ilitirmek yasaktr. Baka bir iaret, ancak CE iaretinin görülmesini ve okunmasn engellemeyecek biçimde, cihazn üzerine, ambalajnn üzerine veya kullanm klavuzuna konulabilir. Ayrca, CE iaretinin ilitirilmesi ve kullanlmas konusunda, 17/1/2002 tarihli ve sayl Resmî Gazete de yaymlanan "CE" Uygunluk aretinin Ürüne litirilmesine ve Kullanlmasna Dair Yönetmelik hükümlerine de uyulmas zorunludur. ÜÇÜNCÜ BÖLÜM Sistem ve lem Paketleri çin Özel Yöntemler, Serbest Dolam ve Klinik Aratrmalar Sistem ve,/lem Paketleri,çin Özel Yöntemler Madde 11 Bu Yönetmeliin 9 uncu maddesi dnda kalan cihaz sistemleri ile ilem paketleri hakknda aadaki hususlara uyulmas gerekir:
5 a) Bir ilem paketi veya bir cihaz sistemi halinde piyasaya arz amacyla, üreticileri tarafndan beyan edilen kullanm artlarna ve amacna uygun olarak CE iareti tayan cihazlar bir araya getiren bütün gerçek ve tüzel kiiler; 1) Üreticilerin talimatlarna uygun olarak, cihazlarn karlkl uyumasnn salandn ve bir araya getirme ileminin bu talimatlara göre gerçekletirilmi olduunu, 2) Sistem ve ilem paketinin ambalajlanmasnn gerçekletirildiini ve üreticinin talimatlarn da içeren bilgiler ile birlikte kullanclara sunulduunu, 3) ç kontrol ve denetimlerinin uygun yöntemlerle yapldn, belirten bir beyan düzenlerler. Yukarda belirtilen artlarn yerine getirilmemesi durumunda; sistem veya ilem paketinin, CE iareti tamayan cihazlarla birlemesi veya seçilmi cihaz kombinasyonunun gerçek kullanm amacyla uyumlu olmamas hallerinde olduu gibi, sistem, ilem paketi ve cihaz kombinasyonu komple bir cihaz olarak ilem görür ve bu Yönetmeliin 9 uncu maddesinin ilgili hükümleri uygulanr. b) Bu maddenin (a) bendinde iaret edilen cihaz sistemini veya ilem paketini veyahut kullanm öncesinde steril edilecek ekilde üreticilerin planlam olduu dier CE iaretli cihazlar piyasaya arz için steril eden gerçek veya tüzel kii, kendi isteine göre EK-IV de veya EK-V de veyahut EK-VI da belirtilen ilemlerden birini takip eder. EK-IV ün veya EK-V in veyahut EK-VI nn uygulanmas ve onaylanm kuruluun müdahalesi, sterilizasyonun teminiyle ilgili yöntemler ile snrldr. Gerçek veya tüzel kii yapm olduu sterilizasyon ilemini, üreticinin talimat dorultusunda yaptn belirten bir beyan düzenler. c) Bu maddenin (a) ve (b) bentlerinde belirtilen cihazlar, ilave bir CE iareti tamazlar. Bu cihazlar, piyasaya birlikte arz edildikleri cihazlarn üreticisi tarafndan verilen bilgileri içeren ve EK-I/13 de belirtilen bilgileri tarlar. Bu maddenin (a) ve (b) bentlerinde iaret edilen beyan, Bakanla sunulmak üzere be yl süreyle saklanr. Serbest Dola/m Madde 12 Bakanlk, kullanm amac çerçevesinde piyasaya arz edilen, usulüne uygun olarak kurulan, korunan, kullanlan ve bu Yönetmelik hükümlerine uygun olan cihazlarn piyasaya arzn ve/veya hizmete sunulmasn engellemez. Aada belirtilen cihazlar için CE iareti aranmaz: a) Bu Yönetmeliin 13 üncü maddesinde ve EK-VIII de belirtilen artlara uygun olan klinik aratrma cihazlar, b) Bu Yönetmeliin 9 uncu maddesinin (b) bendinde belirtilen ve EK-VIII deki artlara uygun olarak smarlama üretilen cihazlar. Bu maddenin (b) bendinde sözüedilen ve smarlama üretilen IIa., IIb. ve III. Snf cihazlar, EK-VIII de belirtilen beyana sahip olmaldr. Bu Yönetmelik hükümlerine uygun olmayan cihazlarn, Yönetmelik hükümleri yerine getirilinceye kadar piyasaya arz edilemeyeceini ve hizmete sunulamayacan açk bir ekilde gösteren bir iaret tamalar kaydyla, ticarî fuarlar ve sergilerde gösterimi Bakanlkça engellenmez. Klinik Ara/trmalar Madde 13 Üretici veya üreticinin Türkiye dnda olmas durumunda onun yetkili temsilcisi, klinik aratrma cihazlar için EK-VIII de belirtilen beyan ve yaplacak klinik aratrma hakkndaki gereken bilgiyi Bakanla verir. Bakanlk, halk sal ve kamu yarar bakmndan III. Snf cihazlar ve IIa. veya IIb. Snflara dahil olan implant ve uzun süreli kullanlan invaziv cihazlar ile ilgili aratrma plann deerlendirerek kararn, altm gün içinde üreticiye bildirir. Bununla birlikte, ilgili danma komisyonunun sözkonusu aratrma plan hakknda olumlu görü vermesi halinde, altm günlük sürenin bitimini beklemeden üreticiye klinik aratrmay balatma izni verebilir. Bu maddenin ikinci fkrasnda belirtilen cihazlar dndaki cihazlar sözkonusu olduunda ise, ilgili danma komisyonunun aratrma plan ile ilgili olarak olumlu görü vermesi halinde, üreticilere hemen klinik aratrma balatmalar için izin verilebilir. Klinik aratrmalar, EK-X da belirtilen hükümlere göre yürütülür ve üretici, EK-X un nci kknda belirtilen raporu, Bakanla vermek üzere hazr bulundurur. Bakanlk gerektiinde, klinik aratrmalar bakmndan halk saln ve kamu yararn korumaya yönelik gerekli ve uygun tedbirleri alr.
6 Klinik aratrma, CE iareti tayan cihazlar kullanlarak cihazn ilgili uygunluk deerlendirme beyannda belirtilen amaç için yaplyorsa, bunun için sadece EK-X un ilgili hükümleri uygulanr. DÖRDÜNCÜ BÖLÜM Onaylanm Kurulu ve Danma Komisyonlar Onaylanm/ Kurulu/ Madde 14 Onaylanm kurulu, aada belirtilen hususlar dorultusunda Bakanlk tarafndan yetkilendirilir ve faaliyette bulunur: a) Bu Yönetmeliin 9 uncu maddesinde belirtilen görevleri ve kendilerine verilmi özel görevleri yerine getirebilecek kurulular Bakanla müracaat ederler. b) Onaylanm kurulularn belirlenmesinde, EK-XI de belirtilen artlara uygunluk aranr. Bu konuyla ilgili olarak, Bakanlkça yaymlanacak teblilerde yer alan uyumlatrlm standartlarda belirtilen artlar tayan kurulularn EK-XI deki artlara uygun olduu kabul edilir. c) Bakanlk, onaylanm kuruluun bu maddenin (b) bendinde belirtilen artlara uymadn tespit ettii takdirde, onaylamay geçersiz klar ve bu kararn, Resmî Gazete de yaymlar ve ayrca Komisyona bildirir. d) Onaylanm kurulu ile üretici, deerlendirme ve dorulama ilemlerinin tamamlanmas için gereken süreyi ortaklaa belirler. e) Talep halinde onaylanm kurulu, bu Yönetmelik kapsamna giren cihaz ve aksesuarlarla ilgili olarak yapt faaliyetler hakknda Bakanla bilgi verir. f) Onaylanm kurulu tarafndan, bu Yönetmeliin ilgili hükümlerine üretici tarafndan uyulmadnn tespit edilmesi veya bir belgenin ibraz edilmemesi hallerinde; üretici tarafndan uygun düzeltici tedbirler alnncaya ve sözkonusu artlara uygunluk temin edilinceye kadar, orantllk ilkesini gözönünde bulundurarak verilen belgeyi askya alr veya iptal eder veyahut snrlamalara tâbi tutar. Belgenin askya alnmas veya iptal edilmesi veyahut snrlamalara tâbi tutulmas durumlarnda veya yetkili otoritenin müdahalesinin gerekli görüldüü hallerde, onaylanm kurulu Bakanla bilgi verir ve Bakanlk da durumu Komisyona bildirir. g) Talep halinde onaylanm kurulu, bütçe belgeleri de dahil olmak üzere, EK-XI de öngörülen artlara uygunluun denetlemesini salayacak bütün bilgi ve belgeleri Bakanla verir. Onaylanm kuruluun seçiminde ve faaliyetlerinde, bu madde ve EK-XI de belirlenen asgarî kriterler ile birlikte, Kanun ve Uygunluk Deerlendirme Kurulular ile Onaylanm Kurululara Dair Yönetmelik hükümleri de uygulanr. Dan/ma Komisyonlar Madde 15 Bakanlk, cihazlar ve standartlar konusunda, bünyesinde bulunan teknik düzenleme ve danma komisyonlar yetersiz kaldnda, yeni danma komisyonlar oluturabilir. Danma komisyonlarnn oluturulmas, çalma usûl ve esaslar ile görev, yetki ve sorumluluklar, bu Yönetmeliin yaymlanmasndan itibaren bir yl içinde Bakanlkça çkarlacak Yönerge ile belirlenir. BEPNC BÖLÜM Kayt ve Uyar Sistemi, Koruma Önlemleri, Denetim ve Yaptrmlar Kayt Sistemi Madde 16 Bakanlk, piyasaya arz edilmi olan cihazlar ve bu cihazlarn piyasaya arzndan sorumlu kiilerin kaytlarn, aada belirtilen esaslara ve verilere göre standart bir formata uygun olarak tutar ve takip eder: a) Cihaz kendi adyla piyasaya arz eden üretici ve bu Yönetmeliin 11 inci maddesinde belirtilen faaliyetlerde bulunan gerçek veya tüzel kii, Yönetmeliin 9 uncu maddesinin (a) ve (b) bentlerinde belirtilen ilemlere uygun olarak, iletme adresini ve cihazla ilgili gerekli bilgileri Bakanla bildirir. b) Cihaz kendi adyla piyasaya arz eden üretici ülke snrlar dnda ise, yetkili temsilcisini Bakanla bildirir. Yetkili temsilci, irket merkezinin adresini ve cihazla ilgili gerekli bilgileri Bakanla bildirir. c) Bakanlk, bütün IIb. Snf ve III. Snf cihazlar için, ayet bu cihazlar iç piyasada hizmete sunuluyorsa, cihazlarn etiketi ve kullanm klavuzu ile birlikte sözkonusu cihazla ilgili tantc bilgileri de talep eder. d) Yurt dndan kullanlm olarak ithal edilen ve iç piyasaya arz edilmek istenen cihazlarn, iç piyasaya arz edilmeden önce bu Yönetmeliin temel gereklerini yerine getirmesi art aranr. Bu cihazlarn kaytlar da Bakanlkça tutulur. e) Bakanlk, bu maddenin (a) ve (c) bentleriyle ilgili olarak, talep olmas halinde Müstearlk kanalyla Komisyona bilgi verir ve ayrca, gerektiinde Komisyondan bilgi ister. f) Bu Yönetmelik ile ilgili düzenleyici veriler, yetkili kurulularn bu Yönetmelik çerçevesindeki görevlerini yerine getirmelerini temin etmek için onlarn ulaabilecei bir Avrupa Veri Bankasnda saklanr. Veri Bankas, aada belirtilen unsurlardan oluur:
7 1) Bu maddede düzenlenen üreticinin ve cihazn kaydyla ilgili veriler, 2) Ek II ve VII de öngörülen yönteme uygun olarak verilen, deitirilen, ikame edilen, askya alnan, iptal edilen veya reddedilen belgeler ile ilgili veriler. Uyar Sistemi Madde 17 Cihazn piyasaya arz edilmesinden sonra tespit edilen olumsuzluklara ilikin uyar sistemi öyledir: a) Bakanlk, I., IIa., IIb. veya III. Snf bir cihaza bal olan ve aada belirtilen olaylar ile ilgili olarak bilgisine sunulan verilerin, bu Yönetmelik hükümlerine uygun ekilde deerlendirilmesi için gerekli tedbirleri alr. Bunlar: 1) Cihazn özelliklerinin ve/veya performansnn bozulmas veya sapmas, hastann veya kullancnn salk durumunda ciddi bozulmaya veya ölüme yol açabilecek veya yol açm olan kullanm klavuzu ve etiketteki yetersizlikler, 2) Ayn tip cihazlarn üreticisi tarafndan cihazn piyasadan sistematik olarak geri çekilmesine yol açan ve bu bendin (1) numaral alt bendinde belirlenen sebepler için bir cihazn özelliklerine ve performansna bal teknik ve tbbî sebepler. b) Üretici veya üreticinin Türkiye dnda olmas durumunda onun yetkili temsilcisi, hekim veya salk kurum ve kurulular, bu maddenin (a) bendinin (1) numaral alt bendinde belirtilen durumlar hakknda Bakanl bilgilendirmek zorundadrlar. Bakanlk, hekim veya salk kurum ve kurulularndan gelen bildirimlerle ilgili olarak cihazn üreticisinin veya üreticinin Türkiye dnda olmas durumunda onun yetkili temsilcisinin bu durumdan haberdar olmas için gerekli bütün tedbirleri alr. c) Bakanlk gerekirse, üretici veya üreticinin Türkiye dnda olmas durumunda onun yetkili temsilcisi ile birlikte, konuyu yerinde inceler ve deerlendirme sonucundan, bu Yönetmeliin 18 inci maddesindeki hususlar sakl kalmak kaydyla, Müstearlk kanalyla Komisyona bilgi verir. Korumaya,li/kin Tedbirler Madde 18 Bakanlk; bu Yönetmeliin 12 nci maddesinin ikinci fkrasnda belirtilen ve EK-VIII e uygun ekilde smarlama üretilen cihazlar hariç olmak üzere; beyan edilen amaca uygun olan cihazlarn kullanmnn hasta, kullanc, uygulayc veya üçüncü kiilerin salk ve güvenlii açsndan tehlike oluturduunu tespit ettiinde, bu cihazlarn piyasaya arzn engellemek, piyasadan çekilmesini salamak, hizmete sunulmasn yasaklamak veya kstlamak için gereken bütün tedbirleri alr ve aadaki hususlar da gözönünde bulundurarak, alnan tedbirleri Müstearlk kanalyla Komisyona bildirir. a) Bu Yönetmeliin 5 inci maddesindeki temel gereklerin ihlâli, b) Bu Yönetmeliin 6 nc maddesindeki standartlarn yanl uygulanmas, c) Standartlarn kendisinden kaynaklanan eksiklikler. Bu Yönetmelie uygun olmayan bir cihaz CE iareti tadnda, Bakanlk, iareti kullanana kar gerekli tedbirleri alr ve Müstearlk kanalyla Komisyon a bilgi verir. Usûlsüz Olarak,li/tirilmi/ CE,/areti Madde 19 CE iaretinin usulsüz olarak cihaza ilitirilmi olduunun tespit edilmesi halinde, bu Yönetmeliin 18 inci madde hükümleri sakl kalmak kaydyla; üretici veya üreticinin Türkiye dnda olmas durumunda yetkili temsilcisi, Bakanlkça belirlenen artlar çerçevesinde, ihlâle son vermek zorundadr. hlâlin devam halinde Bakanlk, cihazn piyasaya arzn kstlayc veya yasaklayc gerekli bütün tedbirleri alr ve cihazn piyasadan çekilmesini salar. Red veya Snrlama Kararlar Madde 20 Bakanlkça, bu Yönetmeliin uygulanmas srasnda cihazn piyasaya arzna, hizmete sunulmasna ve klinik aratrmalarna yönelik red veya snrlayc nitelikteki veyahut cihazlarn piyasadan çekilmesine ilikin olarak alnan herhangi bir kararda, karara esas alnan gerekçeler açkça belirtilir. Birinci fkrada belirtilen bütün kararlar için alnacak tedbirin aciliyeti, fikir alverii suretiyle deerlendirme yaplmasna imkan veriyor ise, üretici veya üreticinin Türkiye dnda olmas durumunda yetkili temsilcisi, görüünü önceden belirtme hakkna sahiptir. Cihaz veya cihazlara ilikin red veya snrlama veyahut piyasadan çekilmesi i ve ilemleri ile ilgili olarak ayrca, 17/1/2002 tarihli ve sayl Resmî Gazete de yaymlanan Ürünlerin Piyasa Gözetimi ve Denetimine Dair Yönetmelik hükümleri de uygulanr. Dier Mevzuata Uyum ALTINCI BÖLÜM Çeitli Hükümler
8 Madde 21 Cihaz, CE iaretinin ilitirilmesini öngören baka mevzuatn da konusuna giriyor ise, ilgili dier mevzuat hükümlerine de uymak zorundadr. Bununla birlikte, ilgili dier mevzuat hükümlerinden bir veya daha fazlas bir geçi dönemi boyunca üreticiye uygulama konusunda bir seçme hakk tanyor ise CE iareti sadece, üreticinin uygulamay seçtii mevzuat hükümlerine uygunluu gösterir. Bu durumda, hangi mevzuatn uyguland, cihazla birlikte verilen belgelerde, uyar, etiket veya kullanm klavuzunda belirtilir. Gizlilik Madde 22 Bakanlk, onaylanm kurulu ve bu Yönetmeliin uygulanmasna katlan bütün taraflar, görevlerini yerine getirirken temin ettikleri bütün bilgilerin gizliliini salarlar. Ancak, gizlilik mahiyetini haiz bu bilgiler, kamu salnn ve düzeninin gerektirdii hallerde, adlî ve ilgili üst mercilerin talebi üzerine ve Bakanla bilgi verilmek suretiyle açklanabilir. Hüküm Bulunmayan Haller Madde 23 Bu Yönetmelikte hüküm bulunmayan hallerde, Kanunun ve ilgili dier mevzuatn hükümleri uygulanr. YEDNC BÖLÜM Son Hükümler Aykr Davran/lar Hakknda Uygulanacak Hükümler Madde 24 Bu Yönetmelik hükümlerine aykr davranan ve faaliyet gösterenler hakknda Kanun, 1/3/1926 tarihli ve 765 sayl Türk Ceza Kanunu ve ilgili dier mevzuat hükümleri uygulanr. Uyumla/trlan Avrupa Birlii Mevzuat Madde 25 Bu Yönetmelik, Avrupa Birlii nin tbbî cihazlar ile ilgili mevzuatna uyum salanmas amacyla; a) 93/42/EEC sayl Tbbî Cihazlar Direktifi ile bu Direktifte deiiklik yapan Direktife, b) 98/79/EEC sayl Vücut Dnda Tan Amaçl Kullanlan Tbbî Cihazlar Direktifine, c) 2000/70/EEC sayl nsan Kan veya Plazmasnn Stabil Türevlerini htiva Eden Tbbî Cihazlar Hakkndaki Direktife, paralel olarak hazrlanmtr. Yürürlük Madde 26 Bu Yönetmelik, yaym tarihinden itibaren 18 ay sonra yürürlüe girer. Yürütme Madde 27 Bu Yönetmelik hükümlerini Salk Bakan yürütür. EK-I TEMEL GEREKLER I.GENEL GEREKLER 1) Cihazlar; beyan edilen amaç ve artlara uygun olarak kullanldnda, ortaya çkabilecek tehlikeler, hastaya salad faydaya göre makûl ve kabul edilebilir nitelikte olmal ve cihazlar, hastalarn güvenlii, klinik artlar, kullanc ve üçüncü kiilerin saln ve güvenliini bozmayacak ve yüksek seviyede koruyacak ekilde tasarlanmal ve üretilmelidir. 2) Üretici, cihazlarn tasarm ve üretiminde, genel olarak benimsenen teknik yöntemleri ve çözümleri gözönünde bulundurarak, güvenlik prensiplerine uymal ve aada belirtilen hususlar uygulamaldr: - Tehlikeleri mümkün olduu kadar azaltmak veya ortadan kaldrmak için güvenli tasarm ve üretim yapmaldr, - Tehlikelerin önlenememesi halinde gerekli alarm ve ikaz önlemlerini alnmaldr, - Kabul edilen koruma tedbirlerinin yetersizliine bal olarak kalan tehlikeler kullancya bildirilmelidir. 3) Cihaz, üretici tarafndan öngörülen performansa ulamal ve bu Yönetmeliin 4 üncü maddesinin (i) bendinde belirtilen ilevlerin biri veya birden fazlasna uygun olabilecek bir tarzda tasarlanmal, üretilmeli ve ambalajlanmaldr. 4) Cihazn üretici tarafndan belirtilen kullanm süresi boyunca, normal artlar altnda kullanm srasnda ortaya çkabilecek olumsuzluklar; cihazn bu EK in 1 inci, 2 nci ve 3 üncü kknda belirtilen özellikleri, performans ve klinik artlar deitirecek, hastann, kullancnn ve üçüncü kiilerin salk ve güvenliini bozacak nitelikte olmamaldr. 5) Cihazlar, üreticiden temin edilen kullanm klavuzunda verilen bilgilere uygun ekilde nakledildiinde ve depolandnda, öngörülen kullanm süresince özellikleri ve performans olumsuz yönde etkilenmeyecek ekilde tasarlanm, üretilmi ve paketlenmi olmaldr.
9 6) Cihazn istenmeyen yan etkileri, cihazdan beklenen performanslara nazaran deerlendirildiinde kabul edilebilir bir risk tekil etmelidir. II. TASARIM VE ÜRETM BAKIMINDAN GEREKLER 7) Kimyasal, fiziksel ve biyolojik özellikler: 7.1. Cihazlar, bu EK in "Genel Gerekler" inde belirtilen özellikleri ve performans garanti edecek ekilde, özellikle aadaki hususlar göz önünde bulundurularak, tasarlanmal ve üretilmelidir. - Kullanlacak malzemenin seçiminde, toksik ve alev alma özellii, - Cihazlarn beyan edilen amac gözönüne alnarak, kullanlan malzeme ile biyolojik doku, hücre ve vücut svlar arasndaki uyum Cihazlar; hasta, kullanc ve tayc için, kalnt ve kontaminantlar yönünden tehlikeleri asgariye indirecek ekilde ve cihazn kullanm amacna uygun olarak tasarlanmal, üretilmeli ve paketlenmelidir. Cihazn doku ile maruz kalma süresine ve sklna, maruz kalan dokulara özellikle dikkat edilmelidir Cihazlar, normal kullanmlar srasnda veya rutin ilemler uygulanrken temas ettikleri malzemeler, maddeler ve gazlar ile güvenli ekilde kullanlabilecek tarzda tasarlanmal ve üretilmelidir. Cihaz, tbbî bir ürünü vermek için tasarlanm ise, ilgili ürünlere ait önlemler ve kstlamalara göre tasarlanm ve üretilmi olmal ve her ikisinin de performanslar kullanm amacna uygun olarak sürdürülmelidir Tek bana kullanldnda tbbî ürün olarak deerlendirilen bir madde, bir cihazn tamamlayc bir parças olarak kullanldnda ve bu fonksiyonu ile insan vücuduna etki ettiinde, maddenin güvenilirlii, kalitesi ve kullanlabilirlii tbbî ürünlerle ilgili yönetmeliklerde tanmlanan uygun metotlar ile kyaslanmak suretiyle cihazn beyan edilen amac hesaba katlarak deerlendirilmelidir. Bir cihaz, bütünün bir parças olarak bir insan kan türevi ihtiva ediyorsa, onaylanm kurulu bu türevin kalitesi ve güvenilirlii için Bakanlktan bilimsel görü isteyecektir. Bu türevin cihazn bir parças olarak kullanll, cihazn belirtilen amac dikkate alnarak tetkik edilir. Kamu salnn temini açsndan, Bakanlk, insan kan türevini piyasaya arzndan sorumlu kiiden balkn ve/veya bitmi ürünün her bir serisinden bir Devlet laboratuvar veya Bakanln bu amaç için tayin ettii bir laboratuvarda test edilmesi için numune alnarak kendisine teslim etmesini isteyebilir. Ancak bunun için söz konusu serinin Avrupa Birlii üyesi ülkelerden birinde daha önceden incelenmemi ve onaylanm özelliklere uygunluunun beyan edilmemi olmas gerekir. Ayrca, Bakanlk sözkonusu incelemelerin, numunenin alnmasndan itibaren en geç altm gün içerisinde tamamlanmasn temin eder Cihazlar, kendisinden szan maddelerin meydana getirebilecei tehlikeleri asgariye indirebilecek ekilde tasarlanmal ve üretilmelidir Cihaz ve cihazn kullanlaca çevre artlar göz önüne alnarak, cihazn içine istenmeden giren maddelere bal tehlikeleri asgariye indirecek tarzda tasarlanmal ve üretilmelidir. 8) Enfeksiyon ve mikrobiyolojik kontaminasyon: 8.1. Cihazlar ve üretim ilemleri; hastann, uygulaycnn ve üçüncü kiilerin enfeksiyon tehlikesini mümkün olduunca azaltacak veya ortadan kaldracak ekilde tasarlanm olmaldr. Tasarm kolayca uygulanabilmeli ve varsa kullanm srasnda hastann cihazdan veya cihazn hastadan kontaminasyonunu asgariye indirmelidir Hayvan kökenli dokular, kullanm amacna uygun denetimden ve veteriner kontrolünden geçmi hayvanlardan salanmaldr. Onaylanm kurulular, hayvanlarn corafi kökenine ait bilgileri saklamaldr. Hayvan kökenli hücrelerin ve maddelerin ilenmesi, korunmas, test edilmesi ve kullanm en uygun güvenlik artlarnda yaplmaldr. Özellikle, virüsler ve dier bulac ajanlar ile ilgili güvenlik ve üretim ilemleri srasnda virüslerin inaktivasyonu veya geçerli eliminasyon metodlarnn uygulanmas ile salanmaldr Steril cihazlar, bir kullanmlk ambalajlarda piyasaya arz edildiinde, depolama ve nakil aamalarnda, koruyucu ambalaj açlncaya veya bozuluncaya kadar steril kalmasn salayacak uygun yöntemlere göre tasarlanmal, üretilmeli ve paketlenmelidir Steril cihazlar geçerli ve uygun bir metodla üretilmi ve steril edilmi olmaldr Sterilizasyonu gereken cihazlar, usûlüne uygun olarak kontrol edilmi ortamlarda üretilmelidir (örnein, çevre artlar gibi) Steril olmayan cihazlarn ambalajlama sistemleri; cihazn öngörülen temizlik düzeyini koruyacak ekilde ve ayet cihazlar kullanmdan önce steril edilecek ise, mikrobiyolojik kontaminasyon tehlikesini asgariye indirecek ekilde olmaldr. Ambalajlama sistemi üretici tarafndan belirtilen sterilizasyon metodu ile sterilizasyona uygun olmaldr.
10 8.7. Cihazn ambalaj ve/veya etiketi özde veya benzer olan ve gerek steril ve gerekse steril olmayan artlarda satlan cihazlar ayrt edecek ekilde olmaldr. 9) Yapm ve çevresel özellikler: 9.1. Cihaz, bir baka cihaz veya ekipmanla kombine halde kullanlacaksa, balant sistemleri dahil tüm kombinasyon, cihazn belirlenmi performansn garanti etmeli ve azaltmamaldr. Kullanma yönelik kstlamalar etiket veya kullanm klavuzunda belirtilmelidir Cihaz, aada belirtilen tehlikeleri ortadan kaldracak veya bunun mümkün olmad hallerde asgariye indirecek tarzda tasarlanmal ve üretilmelidir. - Boyutsal ve ergonomik özellikler ile hacim/basnç oran dahil fiziksel özelliklerine bal yaralanma tehlikesi. - Manyetik alan, harici elektriksel etkiler, elektrostatik dearj, basnç, s veya basnç ve ivmedeki deiiklikler gibi tahmini çevre koullarna bal tehlikeler. - Uygulanan tedavi veya klinik aratrmalar srasnda normal olarak kullanlan dier cihazlarla karlkl etkileim tehlikeleri. - Herhangi bir ölçüm ve kontrol mekanizmasnn geçerliliini yitirdii veya kullanlan malzemenin yalanmas, ypranmas sonucu bakm ve ayarlamann mümkün olmad durumlarda (implantlarda olduu gibi) ortaya çkan tehlikeler Cihaz, normal kullanm srasnda ve en basit hatal durumda dahi yanma veya patlama tehlikesini asgariye indirecek ekilde tasarlanmal ve üretilmelidir. Özellikle, cihazn parlayc, patlayc veya yanc maddelerle birlikte kullanm gerektiinde, bu hususlara dikkat edilmelidir. 10) Ölçüm fonksiyonlu cihazlar: Ölçüm fonksiyonlu cihazlar, cihazn öngörülen amac hesaba katlarak, yeterli hassasiyeti salayacak ve uygun ölçüm hassasiyet snrlar içinde kalacak ekilde tasarlanmal ve üretilmelidir. Hassasiyet limitleri üretici tarafndan belirlenmelidir Ölçme, izleme ve gösterge skalas cihazn beyan edilen amac hesaba katlarak ergonomik prensiplere göre tasarlanmaldr Ölçüm fonksiyonlu cihazla gerçekletirilen ölçümler, uyumlatrlm standartlara uygun kanunî birimlerle ifade edilmelidir. 11) Radyasyona kar koruma: Genel olarak: Cihazlarn tasarmnda ve üretiminde; radyasyona maruz kalan hastalar, kullanclar ve üçüncü kiiler üzerinde oluabilecek etkiyi asgariye indirecek ekilde gerekli tedbirler alnmaldr. Bununla birlikte cihaz, tedavi ve tehis için belirtilen uygun dozlarn uygulanmasn kstlamayacak ekilde tasarlanmal ve üretilmelidir stenen radyasyon: Emisyonla ilgili risklerin önemi göz önünde bulundurularak, belirli bir tbbî amaç bakmndan radyasyonlarn tehlikeli düzeylere çkmasn salayacak ekilde tasarlanm cihazlar söz konusu olduunda, kullanc için emisyonlar kontrol etme imkan salanmaldr. Bu cihazlar, ilgili daimi deiken parametrelerin tolerans ve yeniden üretilebilirliini salayacak ekilde tasarlanmal ve üretilmelidir Cihaz görülebilir ve/veya görülmeyen potansiyel radyasyon tehlikesi oluturduunda, sesli veya görsel ikaz sistemleriyle donatlm olmaldr stenmeyen radyasyon: Cihaz, hastalarn, kullanclarn ve üçüncü kiilerin, istenmeyen radyasyon emisyonuna maruz kalmasn mümkün olduunca asgariye indirecek ekilde tasarlanmal ve üretilmelidir Kullanm klavuzlar: Radyasyon yayan cihazlarn kullanm klavuzlar, yaylan radyasyonun nitelii, hasta ve kullancnn korunmasna yönelik önlemler ve hatal kullanmdan saknma yollar ile cihazn yerletirilmesinden kaynaklanan tehlikelerin ortadan kaldrlmas hakknda ayrntl bilgi içermelidir yonlatrc radyasyon: yonlatrc radyasyon yayan cihazlar, mümkün olduu kadar, yaylan radyasyonun nitelik, nicelik ve geometrisini beyan edilen amaca göre düzenlenebilmesini ve kontrol edilebilmesini salayacak ekilde tasarlanmal ve üretilmelidir Radyodiagnostik amaçl iyonlatrc radyasyon yayan cihazlar, hastann ve kullancnn radyasyona maruz kalmasn asgariye indirerek, öngörülen tbbî amaca uygun görüntü ve/veya çktnn kalitesini salayacak ekilde tasarlanmal ve üretilmelidir.
11 Radyoterapi amaçl iyonlatrc radyasyon yayan cihazlar, uygulanan dozun, n tipinin ve enerjisinin, gerektiinde n kalitesinin güvenilir bir gözlem ve kontrolüne olanak salayacak ekilde tasarlanmal ve üretilmelidir. 12) Bir enerji kaynayla donatlm veya balantl cihazlar için gerekler: Programlanabilen elektronik sistemler içeren cihazlar, öngörülen kullanma uygun olarak bu sistemlerin sürekliliini, güvenilirliini ve performansn salayacak ekilde tasarlanmaldr. Sistemde herhangi bir hata olutuunda, muhtemel tehlikeleri asgariye indirecek veya ortadan kaldracak uygun araçlarla donatlmaldr Hasta güvenliinin dahili enerji kaynana bal olduu durumlarda cihaz, güç kaynann durumunu gösteren bir gereçle donatlmaldr Hasta güvenliinin harici enerji kaynana bal olduu durumlarda cihaz, enerji kaynann kesilmesi durumunda sinyal veren bir alarm sistemiyle donatlmaldr Bir hastann bir veya birden fazla sayda klinik parametrelerini izleme amaçl cihazlar, hastann ölümüne veya salk durumunun ciddi bozulmasna yol açabilen durumlarda, kullancy uyaran uygun alarm sistemleriyle donatlmaldr Cihazlar, ayn çevrede bulunan dier cihaz veya ekipmanlarn çalmasn etkileyebilecek elektromanyetik alan yaratma riskini asgariye indirilebilecek ekilde tasarlanmal ve üretilmelidir Elektriksel tehlikelere kar koruma: Cihazlar, doru kurulmak kaydyla normal kullanm srasnda ve tek hatal durumda bile hiçbir elektriksel ok riski oluturmayacak ekilde tasarlanmal ve üretilmelidir Mekanik ve ssal tehlikelere kar koruma: Cihazlar, dayankllk, stabilite, hareketli parçalar ve benzerlerinden kaynaklanan mekanik tehlikelerden kullanc ve hastay koruyacak ekilde tasarlanmal ve üretilmelidir Cihazlar, titreimleri belirlenmi performansn bir parças olmadkça, özellikle kaynakta, titreimleri snrlayc araçlar ve teknik gelimeler gözönüne alnarak, cihazn titreimlerinden kaynaklanan tehlikeleri asgariye indirecek ekilde tasarlanmal ve üretilmelidir Cihazlar, çkardklar sesler belirlenmi performansn bir parças deilse, özellikle kaynakta, çkard sesi snrlayc araçlar ve teknik gelimeler göz önüne alnarak, cihazn çkard sesten kaynaklanan tehlikeleri asgariye indirecek ekilde tasarlanmal ve üretilmelidir Kullanc tarafndan elle kullanlmas gereken terminaller ile elektrik, gaz, hidrolik ve pnömatik enerji kaynaklarna balantlar, muhtemel riskleri asgariye indirecek ekilde tasarlanmal ve üretilmelidir Is salama veya belirli slara erime amaçl parçalar ve alanlar hariç olmak üzere, cihazlarn el deen ksmlar ve bunlarn çevreleri normal kullanm artlarnda tehlike yaratacak s seviyesine ulamamaldr Maddelerin verilmesinde veya enerji temininde hasta için oluabilecek tehlikelere kar koruma: Hastaya maddelerin verilmesine veya enerji teminine yönelik cihazlar, kullancnn ve hastann güvenliini garanti etmek için uygun ak hznn salanaca ve yeterli hassasiyette sürdürülebilecei ekilde tasarlanmal ve üretilmelidir Cihazlar, ak hzndaki düzensizlikleri önleyen ve/veya gösteren gereçlerle donatlmaldr. Cihazlar, enerji ve/veya madde kaynandan gelen enerjinin kazara tehlikeli seviyeye gelmesini önleyici uygun sistemle donatlmaldr Kontrol ve gösterge fonksiyonlar, cihazlar üzerinde açkça belirtilmelidir. Cihazn üzerinde ileyi için gerekli bilgiler veya ileyi ve ayarlama parametreleri bir görüntüleme sistemi yardmyla belirtildiinde, bu bilgiler kullanc tarafndan ve gerektiinde hasta tarafndan anlalr olmaldr. 13) Üretici tarafndan verilen bilgiler: Her bir cihazn beraberinde, kullanclarn eitim düzeyi ve bilgi seviyesi göz önüne alnarak, güvenli bir kullanm salayan ve üreticiyi belirten bilgiler yer almaldr. Bu bilgiler kullanm klavuzunda ve etiket üzerinde detayl olarak verilmelidir. Cihazn güvenli kullanmn salamak için gereken bilgiler, cihazn üzerinde ve/veya her bir parçasnn ambalaj üzerinde veya gerektiinde, ticarî ambalaj üzerinde de bulunmaldr. Her bir parçann ayr ayr ambalajlanmas mümkün deil ise, bu bilgiler bir veya birkaç cihazn broüründe yeralmaldr. Her cihazn ambalajnda kullanm klavuzu bulunmaldr. I. ve IIa. Snfta tanmlanan cihazlarn kullanm klavuzu olmadan güvenli kullanm mümkün ise, kullanm klavuzu bulunmayabilir Bu bilgiler gerektiinde sembol eklinde olabilir. Sembol ve tantc renkler uyumlatrlm standartlara uygun olmaldr. Standard bulunmayanlar için sembol ve renkler cihazla birlikte verilen dokümanlarda açklanmaldr.
12 13.3. Etikette bulunmas gereken bilgiler: (a) Üreticinin ad veya ticarî ad ve adresi; ithal cihazlar için gerektiinde, bu Yönetmeliin 16 nc maddenin (a) ve (b) bendi hükmünde belirtildii ekilde ithalatç firmann ad veya ticarî ad ve adresi de etiket üzerinde yer alacaktr, (b) Ambalajn içerii ve cihazn tantlmas için kullancya gerekli bilgiler, (c) Gerektiinde, "STERL" ibaresi, (d) Gerektiinde, seri numaras, batch code, lot numaras, (e) Gerektiinde, ay ve yl olarak son kullanma tarihi, (f) Gerektiinde, "bir kullanmlk" olduu ibaresi, (g) Cihaz sipari üzerine yaplm ise, "smarlama üretilen cihazdr" ibaresi, (h) Klinik aratrma amaçl cihazlarda "klinik aratrmaya mahsustur " ibaresi, (i) Özel depolama ve/veya kullanm artlar, (j) Özel kullanm klavuzu, (k) kazlar ve/veya alnacak önlemler, (l) Aktif cihazlar için (e) kkndan ayr olarak, seri numaras içerisinde belirtilecek üretim tarihi, (m) Gerektiinde, sterilizasyon metodu, (n) Radyoaktif madde içeren tayc kap ve cihazlar ile ilgili olarak Türkiye Atom Enerjisi Kurumu ndan alnacak izin belgesi, (o) Cihazn bir insan kan türevi ihtiva etmesi durumunda bunu belirtir ibare, aranr Cihazn kullanm amac kullanc tarafndan kolaylkla anlalamyorsa, üretici cihazn kullanm amacn etikette ve/veya kullanm klavuzunda açkça belirtmelidir Gerektiinde ve mümkünse; ayn seri içindeki cihaz ve bileenlerinden kaynaklanabilecek herhangi bir potansiyel tehlikeye sebep olabilecek bütün durumlar kullanm klavuzunda açkça belirtilmelidir Gerektiinde, kullanm klavuzu aadaki bilgileri içermelidir: (a) Bu EK in 13.3 üncü kknda belirtilen (d) ve (e) bendi dndaki tüm ayrntlar, (b) Bu EK in 3 üncü kknda belirtilen performans ve istenmeyen yan etkiler, (c) Cihazn beyan edilen amacna uygun olarak çaltrlmas için, dier cihazlarla veya donanmlarla birlikte yerletirilmesi veya balanmas gerekiyorsa, güvenli bir bütünlüü salamak amacyla gerekli olan bütün özellikler ve yeterli bilgiler, (d) Cihazn iyi yerletirilip yerletirilmediini ve güvenli bir ekilde ileyip ilemediini dorulamak ve cihazn güvenlii ile sürekli olarak iyi ilemesini salamak amac ile yaplmas gereken ayarlama ve bakm ilemlerinin skln ve niteliini veren bilgileri dorulayc gerekli bütün bilgiler, (e) Gerektiinde, cihazn implantasyonuna bal oluabilecek ciddi tehlikelerden kaçnmay salayan bilgiler, (f) Spesifik tedavi veya aratrma srasnda cihazdan kaynaklanan karlkl etkileim tehlikeleriyle ilgili bilgiler, (g) Steriliteyi salayan ambalajn bozulmas halinde ve gerektiinde yeniden sterilizasyon metodlarnn uygulanmasna ait gerekli bilgiler, (h) Cihaz yeniden kullanlacak ise; temizlenmesi, dezenfekte edilmesi ve yeniden sterilizasyonu gerekiyorsa, sterilizasyon metodu dahil gerekli yöntemlere ilikin bilgilendirmeler ve yeniden kaç kez kullanlabileceine ilikin bilgiler, Cihazn kullanlmadan önce steril edilmesi gerekiyorsa, üretici tarafndan verilen temizleme ve sterilizasyon ile ilgili talimatlar doru ekilde uygulandnda, cihaz bu EK in "Genel Gerekler"ini halen karlyor olmaldr, (i) Cihaz kullanma hazr olmadan önce, gerekli bütün manüplasyon veya ileyile ilgili bilgiler, (j) Tbbî amaçl radyasyon yayc cihazlarda; radyasyonun dalm, younluu, tipi ve nitelii hakknda detayl bilgiler, Kullanm klavuzu ayn zamanda, salk meslek mensuplarn ve hastalar, kontrendikasyonlar ve alnacak tedbirler konusunda bilgilendirilmesine yarayacak ayrntlar da içermelidir. Bu ayrntlar özellikle aadaki hususlar kapsamaldr. (k) Cihazn performansnda deiiklik olduunda alnacak önlemler, (l) Manyetik alanlarda, harici elektriksel etkilerde, elektrostatik dearjda, basnç veya basnç deiimlerinde, ivme ve termik ateleme kaynaklarnda, önceden tahmin edilebilen çevre koullarnda meydana gelebilecek deiikliklere maruz kalma durumunda alnacak tedbirler,
13 (m) laç vermeye yönelik cihazlar üzerinde, uygulanacak olan tbbî ürün veya ürünlerin seçimindeki kstlamalar dahil olmak üzere, uygulanacak ürünle ilgili gerekli bütün bilgiler, (n) Cihazn imhas srasnda meydana gelebilecek, özel veya beklenmeyen tehlikelere kar alnacak tedbirler, (o) Bu EK in 7.4 üncü kkna göre, bir entegre parça olarak uygulanacak tbbî maddeler, (p) Ölçüm fonksiyonlu cihazlarn doruluk derecesinin bildirilmesi. 14) Temel gereklere uygunluk deerlendirilmesi, bu EK in 6 nc kknda olduu gibi, klinik verilere dayanmay gerektiriyor ise, bu veriler EK-X a göre oluturulmaldr. EK-II UYGUNLUK BEYANI (TAM KALTE GÜVENCE SSTEM ) 1) Üretici, cihazlarn tasarm, üretimi ve nihaî kontrolleri için, bu EK in 3 üncü kknda belirtilen onaylanan kalite sisteminin uygulanmasn salar; ayrca, kontrol ve denetim hususunda, bu EK in 3.3 üncü, 4 üncü ve 5 inci kknda öngörülen ilemlere tâbidir. 2) Uygunluk Beyan (The Decleration of Conformity) bu EK in 1 inci kknda belirtilen zorunluluklar yerine getiren üreticinin, sözkonusu ürünlerin bu Yönetmelik hükümlerine uygun olduunu temin ve beyan ettiini gösteren ilemdir. Buna göre üretici, bu Yönetmeliin 10 uncu maddesine uygun olarak CE iaretini basar, yazl bir uygunluk beyan hazrlar. Bu beyan imal edilen cihazlarn saysn içerir ve üretici tarafndan muhafaza edilir. 3) Kalite Sistemi: 3.1. Üretici, kalite sisteminin deerlendirilmesi için onaylanm kurulua bavurur. Bu bavuru aadaki hususlar içerir: - Üreticinin ad ve adresi, kalite sistemi içinde yeralan dier bütün üretim yerlerinin ad ve adresleri, - leme esas cihaz veya cihaz snfyla ilgili bütün bilgiler, - Ayn cihazlar hakknda baka bir onaylanm kurulua bavuru yaplmadna dair yazl beyan, - Kalite sistemi hakknda belgeler, - Üreticinin, onaylanan kalite sisteminin gereklerini yerine getirme taahhüdü, - Onaylanan kalite sisteminin eksiksiz ve etkili olarak sürdürüleceine dair üretici taahhüdü, - Cihazlarn üretimlerinden itibaren elde edilen verilerinin gözden geçirilmesi amacyla bir sistem oluturulmas, bu sistemin güncelletirilmesi ve gerekli düzeltici faaliyetlerin uygulanmasna dair üretici taahhüdü. Bu taahhüt, üreticinin aadaki durumlar konusunda yetkilileri hemen bilgilendirme zorunluluunu kapsar: i. Bir cihazn özelliklerinin ve/veya performansnn bozulma veya sapmas, hastann veya kullancnn salk durumunda ciddi bozulmaya veya ölüme yol açabilecek veya yol açm olan kullanma klavuzunda ve etiketteki bilgilendirme ile ilgili yetersizlikler. ii. (i) alt paragrafnda belirtilen hususlarda, ayn tip cihazn üreticisi tarafndan sistematik olarak geri çekilmesine yol açan ve cihazn performansna veya özelliklerine bal tbbî ve teknik sebepler Kalite Sistemi Uygulamas; tasarmdan nihaî kontrole kadar bütün aamalarda, cihazlarn bu Yönetmelik hükümlerine uygun olduunu garanti etmelidir. Kalite sistemi için, üretici tarafndan benimsenen bütün artlar, gerekler ve unsurlar, kaliteye ilikin kaytlar, yaplan iler, planlar, programlar, yazl, sral ve sistematik bir ekilde bir belgede yer almaldr. Bu belge aadaki hususlar kapsar: a) Üreticinin kalite hedefleri, b) letmenin organizasyon yaps, cihazn tasarm ve kalitesi konusunda yetkililerin ve çalanlarn sorumluluklar ve yetkileri, Uygun olmayan cihazlarn kontrolü dahil, cihazlarn ve tasarmlarnn istenen kalitede olmas için kalite sisteminin etkin ileyiini kontrol etmeyi salayan metodlar, c) Cihazlarn tasarmn kontrol etmeyi ve denetlemeyi salayan ilemler ise: - Öngörülen deiiklikler dahil, cihazn genel tanm, - Bu Yönetmeliin 6 nc maddesinde belirtilen standartlar tamamen uygulanmad zaman, cihazlara uygulanan temel gereklere uymak için benimsenen çözümlerin tanm gibi, uygulanacak olan standartlar ve risk analizlerinin sonuçlar dahil tasarm özelliklerini, - Cihazlarn tasarm esnasnda kullanlacak olan sistematik ilemler ve yöntemler gibi, tasarm incelemesi ve kontrolünün teknikleri,
14 - Cihazn, amacna uygun olarak ileyebilmesi için baka bir cihaza/cihazlara balanmas gerekiyorsa, üretici tarafndan belirtilen özellikleri tayan bu cihaz/cihazlarn baka bir cihaza balanmas durumunda temel gereklere uygun olduunun kant, - EK-I/7.4 de bahsedilen ve cihazn, bir bütünün parças olarak bir insan kan türevi veya bir maddeyi ihtiva edip etmediini gösteren bir ifade ve cihazn belirtilen amacn dikkate alarak, bu çerçevede, insan kan türevi veya maddenin kullanllnn, kalitesinin ve güvenilirliliinin tayin edilmesi için gereken test sonuçlarna ait veriler, - EK-X da belirtilen klinik veriler, - Etiket ve kullanm klavuzu örnei, d) Üretim aamasndaki denetim ve kalite güvencesi teknikleri; - Sterilizasyon ve satn alma konusunda uygulanacak ilemler, yöntemler ve ilgili belgeler, - Üretimin her aamasnda kullanlan çizimlerden, uygulanan özelliklerden veya dier ilgili belgelerden hareketle cihazn tanmlanmas ilemi, e) Üretimden önce, üretim esnasnda ve üretimden sonra yaplan deney ve incelemeler ile ilgili bilgilerin, bunlarn hangi sklkla yaplaca, kullanlan test cihazlar ve test cihazlarnn kalibrasyonu ile ilgili kaytlarn geriye doru izlenmesi mümkün olmaldr Onaylanm kurulu, kalite sisteminin bu EK in 3.2 nci kknda belirtilen gereklere uygun olup olmadn saptamak için denetimini yapar. Kalite sisteminde gerekli uyumlatrlm standartlarn uygulanp uygulanmad kontrol eder. Deerlendirme ekibinde en az bir üyenin, ilgili teknoloji hakknda deerlendirme deneyimi olmaldr. Deerlendirme ileminde üretim yöntemini kontrol etmek için üretici ve gerektiinde üreticinin tedarikçisi ve/veya üreticinin yüklenicisi de yerinde denetlenir. Karar, denetim sonuçlar ve açklamal deerlendirmeyle birlikte üreticiye tebli edilir Üretici, kalite sisteminin ve cihaz çeidinin önemli deiikliklerine ilikin bütün tasarlar hakknda, kalite sistemini onaylayan onaylanm kurulua bilgi verir. Onaylanm kurulu, teklif edilen deiiklikleri deerlendirir ve kalite sistemindeki bu deiikliklerin bu EK in 3.2 nci kknda belirtilen gereklere uyup uymadn inceler ve kararn üreticiye tebli eder. Bu karar, denetimin sonuçlarn ve açklamal deerlendirmeyi de kapsar. 4) Cihaz Tasarmnn ncelenmesi: 4.1. Üretici, bu EK in 3 üncü kknda belirtilen gereklere ilave olarak, bu EK in 3.1 inci kkna göre üretimini planlad cihazn tasarm dosyasn incelemek üzere onaylanm kurulua verir Cihazn, bu EK in 3.2 nci kknn (c) bendinde tanmland gibi, bu Yönetmeliin gereklerine uygunluunu deerlendirmek için gerekli belgeleri içeren bavuru sözkonusu cihazn tasarmn, üretimini ve performansn tanmlar Onaylanm kurulu bavuruyu inceler ve cihaz bu Yönetmelik hükümlerine uygun ise, bavuru sahibine Tasarm-nceleme Sertifikas (EC Design-Examination Certificate) verir. Sertifika; inceleme sonuçlarn, geçerlilik artlarn, onaylanan tasarmn tanmnda gerekli verileri ve gerektiinde cihazn amacn da kapsar. Onaylanm kurulu, bu Yönetmeliin gereklerine uygunluun deerlendirilmesi amacyla bavuru srasnda ilave kantlar ve deneyler isteyebilir. EK-I/7.4 ün birinci paragrafnda bahsedilen cihazlar söz konusu olduunda, onaylanm kurulu bu bölümde bahsedilen durum hakknda bir karar almadan önce Bakanla danr. Onaylanm kurulu, kararn verirken bu danmada ifade edilen görülere ilave olarak gerekli deerlendirmesini belirtir ve nihaî kararn Bakanla iletir. EK-I/7.4 ün ikinci paragrafnda bahsedilen cihazlar sözkonusu olduunda, cihaz ile ilgili belgelere Bakanln bilimsel görüü de dahil edilmelidir. Onaylanm kurulu kararn verirken Bakanln görüüne ilave olarak kendi gerekli deerlendirmesini belirtir. Payet, Bakanln bilimsel görüü olumlu deil ise, onaylanm kurulu, sertifikay teslim etmez Tasarm deiiklikleri durumunda, bu Yönetmeliin temel gereklerine uygunluunun ortaya konmas halinde, Tasarm-nceleme Sertifikasn veren onaylanm kurulutan ilave bir onay alnmaldr. Bavuru sahibi, onaylanan tasarm ile ilgili bütün deiiklikleri onaylanm kurulua bildirir. Tasarm-nceleme Sertifikasna ilave olarak "ek onay formu" alr. 5) Denetim: 5.1. Denetimin amac, üreticinin, onaylanan kalite sisteminin gereklerini tam olarak yerine getirmesini salamaktr.
15 5.2. Üretici, onaylanm kuruluun gerekli bütün denetimleri yapmasna izin verir ve ona, gereken bütün bilgileri temin eder. Bunlar: - Kalite sistemine ilikin belgeler, - Kalite sisteminin tasarma ilikin bölümünde öngörülen deney ve analiz sonuçlar gibi veriler, - Kalite sisteminin üretime ilikin bölümünde öngörülen denetim raporlar, test verileri, kalibrasyon verileri, ilgili personelin nitelikleri hakkndaki raporlar gibi veriler Onaylanm kurulu, üreticinin onaylanan kalite sistemine uymasn salamak amacyla periyodik olarak denetim ve deerlendirme yapar, üreticiye deerlendirme raporu verir Ayrca, onaylanm kurulu, üreticiye beklenmeyen ziyaretler yapabilir. Bu ziyaretlerde gerekli görür ise, kalite sisteminin iyi ilediini denetlemek için deneyler yapar veya yaptrabilir. Üreticiye bir denetim raporu ve eer deney yaplmsa deney raporu verilir. 6) darî Hükümler: 6.1. Üretici, cihazn son üretim tarihinden itibaren en az 5 yllk bir süre boyunca gerektiinde yetkililere ibraz edilmek üzere u belgeleri saklar: - Uygunluk beyan, - Bu EK in 3.1 inci kknda belirtilen belgeler, - Bu EK in 3.4 üncü kknda belirtilen deiiklikler, - Bu EK in 4.2 nci kknda belirtilen belgeler, - Bu EK in 3.3 üncü, 4.3 üncü, 4.4 üncü, 5.3 üncü, 5.4 üncü kknda belirtilen onaylanm kurulu kararlar ve raporlar Bu EK in 4 üncü kknda belirtilen ileme tâbi olan cihazlarda teknik belgelerin saklanmas zorunluluu, üretici veya üreticinin Türkiye de olmad takdirde yetkili temsilcisine, yetkili temsilci yurt içinde bulunmad durumda cihaz piyasaya arzdan sorumlu kiiye ve EK-I/ 13.3 ün (a) bendinde belirtilen üretici veya ithalatçya aittir. 7) IIa. ve IIb. Snf Cihazlar için Uygulama: Bu EK in 4 ncü kk hariç olmak üzere, Yönetmeliin 9 uncu maddesinin (a) bendinin (2) numaral ve (3) numaral alt bentlerine uygun olan IIa. ve IIb. Snfndaki cihazlara uygulanr. 8) nsan kan türevi ihtiva eden cihazlara yönelik uygulama: nsan kan türevi ihtiva eden cihazlardan her bir serinin üretiminin tamamlanmas üzerine, üretici, onaylanm kuruluu cihaz serisinin piyasaya arz konusunda bilgilendirir ve Devlet laboratuar veya Bakanlk ça belirlenen baka bir laboratuar tarafndan cihaz içinde kullanlan insan kan türevi serisinin piyasaya arz ile ilgili olarak verilen resmî sertifikay onaylanm kurulua gönderir. EK-III TP NCELEMES 1) Tip incelemesi; onaylanm kuruluun üretim numunesinin bu Yönetmelik hükümlerine uygunluunu belgelemesi ilemidir. 2) Bavuru dilekçesi u hususlar içerir: - Üreticinin ad ve adresi; bavuru, yetkili temsilci tarafndan yaplmsa yetkili temsilcinin ad ve adresi, - Bu Yönetmelik hükümlerinde tip olarak tanmlanan cihazn tantc numunesinin uygunluk deerlendirmesi için bu EK in 3 üncü kknda istenilen belgeler gerekir. Bavuru sahibi onaylanm kurulua vermek üzere bir tip numunesi hazrlar. Onaylanm kurulu gerektiinde baka numuneler de isteyebilir. - Cihaz ile ilgili numune hakknda baka bir onaylanm kurulua bavuru yaplmadna dair yazl beyan. 3) Verilen belgeler; tasarm, üretim ve cihaz performanslarnn anlalmasn salamal ve aadaki hususlar içermeli: - Planlanan deiiklikleri de içermek üzere, tipin genel bir tanm, - Tasarm çizimleri, öngörülen üretim metodlar özellikle sterilizasyon konusunu ve tasarmn önemli parçalarn, aksesuarlarn, devrelerini gösteren ayrntl ema, - Cihazn çalmas, çizim ve emalarn anlalmas için gerekli tanm ve açklamalar, - Bu Yönetmeliin 6 nc maddesinde belirtilen standartlardan tam veya ksmen uygulananlarn bir listesi ile bu standartlar uygulanmad taktirde, bu Yönetmeliin temel gereklerine uyum salayan çözümlerin tanm, - Uygulanan risk analizleri, inceleme, teknik testler ve tasarm hesaplamalar gibi sonuçlar,
16 - Cihazn kullanm amac dikkate alnarak, EK-I/7.4 de belirtilen bir madde veya insan kan türevinin bir bütünün parças olarak cihazn yapsnda yer alp almadna ilikin beyan ve bu madde veya kan türevinin güvenilirlii, kalitesi ve kullanlln tayin etmek için yaplan testlere ait veriler, - EK-X da belirtilen klinik veriler, - Etiket ve gerekiyor ise kullanm klavuzu örnei. 4) Onaylanm kurulu: 4.1. braz edilen belgelerin, tipe uygunluunu ve tipin de belgelere uygun olarak üretilip üretilmediini, bu Yönetmeliin 6 nc maddesinde belirtilen standartlarn uygulanabilir hükümlerine uyulup uyulmadn inceler, deerlendirir ve deerlendirme sonuçlarn kaydeder Bu Yönetmeliin 6 nc maddesinde belirtilen standartlarn uygulanmad cihazlar için üreticinin tavsiye ettii çözümlerin ve bu Yönetmeliin temel gereklerinin yerine getirilip getirilmediini dorulamak için uygun inceleme ve testleri yapar veya yaptrr. Payet, cihazn kullanl amacna uygun olarak ileyebilmesi için baka cihaz veya cihazlara balanmas gerekiyorsa, üretici tarafndan belirtilen özelliklere sahip cihazlara balandnda temel gereklere uygunluunu da kantlamaldr Üreticinin halen yürürlükte olan ilgili standartlar seçmesi halinde, bu standartlarn gerçekten uygulanp uygulanmadn deerlendirmek için gerekli inceleme ve testleri yapar veya yaptrr Gerekli denetim ve testlerin uygulanaca yeri bavuru sahibi ile birlikte belirler. 5) Onaylanm kurulu, bu Yönetmelik hükümlerini yerine getiren üreticiye Tip-nceleme Sertifikasn (EC Type-Examination Certificate) verir. Sertifika, üreticinin ad ve adresini, tefti sonuçlarn, geçerlilik artlarn ve onaylanan tip tanmlanmas için gerekli verileri içerir. Belgenin ilgili bölümleri sertifikaya eklenir ve bir kopyas onaylanm kurulu tarafndan saklanr. EK-I/7.4 ün birinci paragrafnda belirtilen cihazlar sözkonusu olduunda, onaylanm kurulu, bu bölümde belirtilen hususlar için bir karar vermeden önce, tbbî ürün ile ilgili olarak Bakanla danr. EK-I/7.4 ün ikinci paragrafnda bahsedilen cihazlar sözkonusu olduunda, cihazla ilgili belgelere Bakanln bilimsel görüü de dahil edilmelidir. Onaylanm kurulu kararn verirken, Bakanln görüüne ilave olarak, kendi gerekli deerlendirmesini belirtecektir. Payet, Bakanln bilimsel görüü uygun deilse, onaylanm kurulu sertifikay vermeyebilir. Onaylanm kurulu, danlan kuruluun görüleri dorultusunda nihaî kararn verir ve Bakanla bildirir. 6) Bavuru sahibi onaylanan üründe yaplan bütün önemli deiiklikleri, Tip-nceleme Sertifikas veren onaylanm kurulua bildirmek zorundadr. Tasarm deiiklikleri bu Yönetmeliin temel gereklerine uygunluu ve ürünün kullanm için belirtilen artlar etkiliyorsa, bu deiiklikler için Tip-nceleme Sertifikasn veren onaylanm kurulutan ek onay alnmaldr. Bavuru sahibi, gerektiinde, ilk Tip-nceleme Sertifikasna ilave olarak ek onay alr. 7) darî hükümler: 7.1. Dier onaylanm kurulular Tip-nceleme Sertifikalar ve/veya bunlarn eklerinden bir kopya alabilir. Sertifikann ekleri, üreticinin bilgisi dahilinde, gerekçeli talep üzerine dier onaylanm kurululara verilir Üretici veya üreticinin Türkiye de olmamas halinde yetkili temsilcisi, son cihazn üretiminden sonra en az 5 yl boyunca teknik belgelerle birlikte Tip-nceleme Sertifikas ve bunlarn tamamlayc ek belgelerinin bir kopyasn saklar Yurtiçinde üretici veya yetkili temsilcisi bulunmadnda, teknik belgeleri Bakanla verme yükümlülüü, ilgili cihazn piyasaya sürülmesinden sorumlu kiiye ve EK-I/13.3 ün (a) kknda belirtilen üreticiye veya ithalatçya aittir. EK-IV TP DORRULAMASI 1) Tip dorulamas; üreticinin veya yetkili temsilcinin, bu EK in 4 üncü kknda açklanan ilemlere tâbi olan cihazlarn Tip-nceleme Sertifikasnda tanmlanan tipe uyduunu ve bunlarla ilgili Yönetmelik hükümlerine uygun olduunu beyan ve garanti ettii ilemdir. 2) Üretici, üretilen cihazlarn, bu Yönetmelik hükümlerine ve Tip-nceleme Sertifikasnda tanmlanan tipin bütün özelliklerine tamamen uygun olmas için üretim yöntemiyle ilgili gerekli tedbirleri alr. Üretime balamadan önce, üretici, üretim ilemlerini açklayan belgeleri, özellikle sterilizasyon konusunu, gerekirse tüm rutin ilemleri, homojen üretim salamak için önceden kabul edilmi hükümleri, gerekirse de Tip-nceleme Sertifikasnda ve Yönetmeliin bu tip ile ilgili hükümlerine uygunluunu gösteren belgeleri de hazrlamaldr. Üretici, uygunluk beyan düzenlemeli ve 10 uncu maddeye göre CE iaretini kullanmaldr.
17 Ayrca steril durumda piyasaya arz edilen cihazlar için ve sadece üretim ileminin steril koullarda salanmas ve sürdürülmesi amacyla üretici EK-V in 3 üncü ve 4 üncü klarnn hükümlerini uygulamaldr. 3) Üretici, cihazlarn üretimlerinden sonra elde edilen verilerin gözden geçirilmesi amacyla bir sistem oluturulmas, bu sistemin güncelletirilmesi ve gerekli düzeltici faaliyetlerin uygulanmas sorumluluunu almaldr. Bu yükümlülük üreticinin aada belirtilen durumlardan bilgisi olduu andan itibaren yetkili makamlar haberdar etme zorunluluunu da içerir: i. Bir cihazn özelliklerinin ve/veya performansnn bozulma veya sapmas, hastann veya kullancnn salk durumunda ciddi bozulmaya veya ölüme yol açabilecek veya yol açm olan kullanma klavuzunda ve etiketteki bilgilendirmeyle ilgili yetersizlikler, ii. (i) alt paragrafnda belirtilen hususlarda, ayn tip cihazn üreticisi tarafndan sistematik olarak geri çekilmesine yol açan ve cihazn performansna veya özelliklerine bal tbbî ve teknik sebepler. 4) Onaylanm kurulu, üreticinin seçtii yönteme istinaden ya, bu EK in 5 inci kknda belirtildii gibi her bir cihaz test ve kontrol ederek veya 6 nc kknda belirtildii gibi ürünlerin istatistiksel dorulamasn yaparak, Yönetmeliin öngördüü gereklerin yerine getirilip getirilmediini dorulamak amacyla uygun test ve incelemeleri gerçekletirir. Yukarda bahsedilen kontroller sterilizasyonu salamak amacyla tasarlanm üretim ilemlerine uygulanmaz. 5) Her bir cihazn test ve kontroller ile dorulanmas: 5.1. Her cihaz ayr ayr incelenir. Bu Yönetmeliin 6 nc maddesinde öngörülen ilgili Standartlarda belirlenen uygun testler veya edeer testler yaplr. Gerekirse, Tip-nceleme Sertifikasnda tanmlanan tip ve bunlara uygulanacak Yönetmelik hükümlerine göre dorulama yaplr Onaylanm kurulu, onaylanan her bir cihaza kendi kimlik numarasn basar veya bastrr ve gerçekletirilen bütün testler ile ilgili uygunluk sertifikas (Certificate of Conformity) düzenler. 6) statistiksel dorulama: 6.1. Üretici, cihazn üzerine seri numaras koymaldr Her seriden örnekleme metodu ile numune alnr. Bu numuneler, Yönetmeliin 6 nc maddesinde öngörülen ilgili standartlarda tanmlanan, uygun testlerle ayr ayr incelenir veya benzer testler gerektiinde, serinin kabul veya reddedildiini tespit etmek amacyla kendilerine uygulanan Yönetmeliin gerekleriyle Tip- nceleme Sertifikasnda tanmlanan Tip in cihazlara uygunluunu dorulamak için edeer testler gerçekletirilir Cihazn istatistiksel kontrolü %3 ilâ % 7 aras uygunsuzluk yüzdesi ile birlikte %5 kabul olasln karlayan uygun kalite limitini salayan örnekleme sistemine dayanlarak yaplr. Bu örnekleme metodu, sözkonusu cihaz kategorisinin özel nitelii gözönünde bulundurularak, Yönetmeliin 6 nc maddesinde öngörülen ilgili standartlara göre oluturulur Eer seri kabul edilirse, onaylanm kurulu her bir cihazn üzerine kendi kimlik numarasn basar veya bastrr ve gerçekletirilen testler ile ilgili uygunluk sertifikas düzenler. Uygun seri cihazlar uygun olmayan örnekleme cihazlar haricinde piyasaya arz edilebilir. Eer bir seri reddedilirse, onaylanm kurulu bu serinin piyasaya arzn engellemek için gerekli tedbirleri alr. Serinin sklkla reddedilmesi durumunda, onaylanm kurulu istatistiksel dorulamaya ara verebilir. Üretici, onaylanm kuruluun sorumluluu altnda, üretim ilemleri srasnda onaylanm kuruluun kimlik numarasn basabilir. 7) darî hükümler: Üretici veya üreticinin Türkiye de olmamas halinde, yetkili temsilcisi cihazn son üretim tarihinden itibaren en az 5 yl süreyle yetkililere ibraz etmek üzere aadaki belgeleri saklar: - Uygunluk beyan, - Bu EK in 2 nci kknda belirtilen belgeler, - Bu EK in 5.2 inci ve 6.4 üncü kknda belirtilen belgeler, - Gerektiinde, EK-III de belirtilen Tip-nceleme Sertifikas. 8) IIa. Snf cihazlar için uygulama: Bu EK, Yönetmeliin 9 uncu maddesinin (a/2) bendine uygun olarak, aada belirtilen istisnalar göz önünde bulundurulmak suretiyle, IIa. Snf cihazlara uygulanabilir Bu EK in 1 inci ve 2 nci klarnn uygulanmad durumda üretici, IIa. Snf ürünlerini EK-VII nin 3 üncü kknda belirtilen teknik belgelere uygun olarak ürettiini ve kendilerine uygulanan bu Yönetmelik gereklerine cevap verdiini, uygunluk beyan ile açklar ve garanti eder.
18 8.2. EK-VII nin 3 üncü kknda belirtilen teknik belgeleri bulunan IIa. Snf ürünlerin onaylanm kuruluça gerçekletirilen uygunluk dorulamas bu EK in 1 inci, 2 nci, 5 inci ve 6 nc klar hariç tutularak yaplr. 9) nsan kan türevi ihtiva eden cihazlara yönelik uygulama: nsan kan türevi ihtiva eden cihazlarda, her bir cihaz serisinin üretiminin tamamlanmas ve 6 nc maddeye göre tetkik edilmesi söz konusu olduunda, üretici, onaylanm kuruluu bu cihaz serisinin piyasaya arz konusunda bilgilendirir ve ayrca, Devlet laboratuar veya Bakanlkça belirlenen bir baka laboratuvar tarafndan cihazda kullanlan insan kan türevi serisinin piyasaya arz ile ilgili olarak düzenledii resmî sertifikay onaylanm kurulua gönderir. EK-V TP UYGUNLUK BEYANI (ÜRETM KALTE GÜVENCES) 1) Üretici, üretim için onaylanan kalite sistemini uygulayarak sözkonusu cihazlarn nihaî kontrollerini bu EK in 3 üncü kknda belirtildii gibi yapar; ayrca, bu EK in 4 üncü kknda belirtilen denetime tâbidir. 2) Uygunluk beyan; bu EK in 1 inci kknda belirtilen gerekleri yerine getiren üreticinin, sözkonusu ürünleri Tip-nceleme Sertifikasnda belirtilen tipe ve bu Yönetmelik hükümlerine uygunluunu garanti eden ve bildiren ilemdir. Üretici, Yönetmeliin 10 uncu maddesine uygun olarak CE iaretini ilitirir ve bir uygunluk beyan hazrlar. Bu beyan, üretilen cihazlardan seçilen "numuneleri tanmlayan bir numara"y kapsamal ve üretici tarafndan saklanmaldr. 3) Kalite Sistemi: 3.1. Üretici, kalite sisteminin deerlendirilmesi için onaylanm kurulua bavurur. Bu bavuru unlar içerir: - Üreticinin ad ve adresi, - leme esas cihaz veya cihaz snf ile ilgili bütün bilgiler, - Ayn cihazlar hakknda baka bir onaylanm kurulua bavuru yaplmadna dair yazl beyan, - Kalite sistemi belgeleri, - Onaylanan kalite sisteminin bütün gerekleri yerine getirme taahhüdü, - Onaylanan kalite sisteminin eksiksiz ve etkili ekilde sürdürülmesi taahhüdü, - Gerektiinde, onaylanan tipe ilikin teknik belge ve Tip-nceleme Sertifikalarnn bir örnei, - Cihazlarn üretimlerinden sonra elde edilen verilerinin gözden geçirilmesi amacyla, bir sistem oluturulmas, bu sistemin güncelletirilmesi ve gerekli düzeltici faaliyetlerin uygulanmasna ilikin üretici taahhüdü. Bu taahhüt, üreticinin aadaki durumlardan yetkilileri hemen bilgilendirmesi zorunluluunu da kapsar: i. Hastann veya kullancnn salk durumunda ciddi bozulmaya veya ölüme yol açabilecek veya yol açm olan cihazn özelliklerindeki ve/veya performansndaki bozukluklar veya sapmalar ile kullanma klavuzunda ve etiketteki bilgilendirmeyle ilgili yetersizlikler. ii. (i) alt paragrafnda belirtilen hususlarda, ayn tip cihazn üretimcisi tarafndan sistematik olarak geri çekilmesine yol açan ve cihazn performansna veya özelliklerine bal tbbî ve teknik sebepler Kalite sisteminin uygulanmas ürünlerin Tip-nceleme Sertifikasnda belirtilen tipe uygunluunu salamaldr. Kalite sistemi için üretici tarafndan benimsenen bütün hükümler, gerekler ve unsurlar, kaliteye ilikin kaytlar, yaplan iler, planlar, programlar gibi yazl, sral ve sistematik ekilde bir belgede yer almal ve kalite konusunda yöntemlerin ve politikalarn ayn tarzda yorumlanmasna imkan vermelidir. Bu belge, özellikle aadaki tanmlar içerir: a) Üreticinin kalite hedefleri, b) letmenin organizasyon yaps, cihazn üretimi konusunda organizasyon yetkililerinin ve çalanlarnn sorumluluk ve yetkileri, kalite sisteminin etkili ekilde ilemesini kontrol etmek için yöntemler ve uygun olmayan cihazlarn engellenmesi dahil, istenen kalitede ürün salama kapasitesi, c) Üretim aamasnda kalite güvencesi ve kontrol teknikleri: - Sterilizasyon ve satn alma konusunda uygulanacak ilemler, yöntemler ve ilgili belgeler, - Üretimin her aamasnda kullanlan çizimlerden, uygulanan özelliklerden veya dier ilgili belgelerden yararlanarak cihazn tanmlanmas ilemi,
19 d) Üretimden önce, üretim esnasnda ve üretimden sonra yaplan deney ve incelemeler ile ilgili bilgiler, bunlarn hangi sklkla yaplaca, kullanlan test cihazlar ve test cihazlarnn kalibrasyonu ile ilgili kaytlarn geriye doru izlenmesi mümkün olmaldr Onaylanm kurulu, kalite sisteminin bu EK in 3.2 nci kknda belirtilen gereklere uygun olup olmadn saptamak için denetim yapar. Kalite sisteminde gerekli Uyumlatrlm Standartlarn uygulanp uygulanmad kontrol eder. Deerlendirme ekibinde en az bir üyenin, ilgili teknoloji hakknda deerlendirme deneyimi olmaldr. Deerlendirme ileminde üretim yöntemini kontrol etmek için üretici ve gerektiinde, üreticinin tedarikçisi de yerinde denetlenir. Karar, denetim sonuçlar ve açklamal deerlendirmeyle birlikte üreticiye tebli edilir Üretici, kalite sisteminin önemli deiikliklerine ilikin bütün tasarlardan, kalite sistemini onaylayan onaylanm kurulua bilgi verir. Onaylanm kurulu, teklif edilen deiiklikleri deerlendirir ve kalite sistemindeki bu deiikliklerin bu EK in 3.2 nci kknda belirtilen gereklere uyup uymadn inceler. Sözkonusu bilgilerin alnmasndan sonra, kontrol sonuçlarn ve açklamal deerlendirmeyi içeren karar üreticiye tebli edilir. 4) Denetim: 4.1. Denetimin amac, üreticinin, onaylanan kalite sisteminin gereklerini tam olarak yerine getirmesini salamaktr Üretici, onaylanm kuruluun gerekli tüm teftileri gerçekletirmesine izin verir ve kurulua aadaki bilgiler de dahil olmak üzere gerekli bütün bilgileri temin eder; - Kalite sistemine ilikin belgeler, - Kalite sisteminin üretime ilikin bölümünde öngörülen tefti raporlar, test verileri, kalibrasyon verileri, ilgili personelin nitelikleri hakkndaki raporlar gibi veriler Onaylanm kurulu, üreticinin onaylanan kalite sistemine uymasn salamak amacyla periyodik olarak tefti ve deerlendirme yapar, üreticiye deerlendirme raporu verir Ayrca, onaylanm kurulu, üreticiye beklenmeyen ziyaretler yapabilir. Bu ziyaretlerde gerekli görürse, kalite sisteminin iyi ilediini denetlemek için test yapar veya yaptrabilir. Üreticiye bir denetim raporu ve eer test yaplmsa, test raporu verilir. 5) darî Hükümler: Üretici, cihazn son üretim tarihinden itibaren en az 5 yl süreyle yetkililere ibraz etmek üzere aadaki belgeleri saklar: - Uygunluk beyan, - Bu EK in 3.1 inci kknda belirtilen kalite sistemi belgeleri, - Bu EK in 3.4 üncü kknda belirtilen deiiklikler, - Bu EK in 3.1 inci kknda belirtilen Tip-nceleme Sertifikasnn bir örnei ve onaylanm tipe ilikin teknik belgeler, - Bu EK in 4.3 üncü ve 4.4 üncü kknda belirtilen onaylanm kuruluun karar ve raporlar, - Gerektiinde EK-III de belirtilen Tip-nceleme Sertifikas. 6) IIa. Snf Cihazlar çin Uygulama: Bu EK, Yönetmeliin 9 uncu maddesinin (a/2) bendine uygun olarak aadaki istisnaî durum göz önünde tutulmak suretiyle IIa. Snf cihazlara uygulanr. Bu EK in 2 nci, 3.1 inci ve 3.2 nci klarnn uygulanmad durumlarda üretici, IIa. Snf cihazlarn EK- VII nin 3 üncü kknda belirtilen teknik belgelere uygun olarak ürettiini ve kendilerine uygulanan bu Yönetmelik gereklerine cevap verdiini, uygunluk beyan ile açklar ve garanti eder. 7) nsan kan türevi ihtiva eden cihazlara yönelik uygulama: nsan kan türevi ihtiva eden cihazlarda, her bir cihaz serisinin üretiminin tamamlanmas üzerine üretici, onaylanm kuruluu bu cihaz serisinin piyasaya arz konusunda bilgilendirir ve Devlet Laboratuvar veya Bakanlkça belirlenen bir baka laboratuvar tarafndan cihazda kullanlan insan kan türevi serisinin piyasaya arz ile ilgili olarak verilen resmî sertifikay onaylanm kurulua gönderir. EK-VI ÜRÜN KALTE GÜVENCES UYGUNLUK BEYANI 1) Üretici, üretim için onaylanan kalite sistemini uygulayarak sözkonusu cihazlarn nihaî kontrollerini, bu EK in 3 üncü kknda belirtildii gibi yapar; ayrca, bu EK in 4 üncü kknda belirtilen denetime tâbidir.
20 Ayrca, steril olarak piyasaya verilecek cihazlar için, sadece steriliteyi salamak ve devam ettirmek amacna yönelik üretim yöntemlerinde üretici, EK-V in 3 üncü ve 4 üncü klarndaki hükümleri uygular. 2) Uygunluk beyan; bu EK in 1 inci kknda belirtilen gerekleri yerine getiren üreticinin, sözkonusu cihazlar Tip-nceleme Sertifikasnda belirtilen tipe ve bu Yönetmelik hükümlerine uygunluunu garanti eden ve bildiren ilemdir. Üretici, bu Yönetmeliin 10 uncu maddesine uygun olarak CE iaretini ilitirir ve bir uygunluk beyan hazrlar. Bu beyan, üretilen cihazlardan seçilen "numuneleri tanmlayan bir numara"y kapsamal ve üretici tarafndan saklanmaldr. CE iareti, bu EK de belirtilen ilemleri uygulayan onaylanm kuruluun kimlik numaras ile birlikte yer alr. 3) Kalite Sistemi: 3.1. Üretici, kalite sisteminin deerlendirilmesi için ilgili onaylanm kurulua bavurur. Bavuru aadaki hususlar içerir: - Üreticinin ad ve adresi, - leme esas cihaz veya cihaz snf ile ilgili bütün bilgiler, - Ayn ürün için, baka bir onaylanm kurulua bavuruda bulunulmadn belirten yazl bir beyan, - Kalite sistemi hakkndaki belgeler, - Üreticinin, onaylanan kalite sisteminin gereklerini yerine getirme taahhüdü, - Onaylanan kalite sisteminin eksiksiz ve etkili bir ekilde sürdürülmesine ilikin üretici taahhüdü, - Gerektiinde, onaylanan tipe ait teknik belgenin ve Tip-nceleme Sertifikasnn bir örnei, - Cihazlarn üretimlerinden sonra elde edilen verilerinin gözden geçirilmesi amacyla, bir sistem oluturulmas, bu sistemin güncelletirilmesi ve gerekli düzeltici faaliyetlerin uygulanmasna dair üretici taahhüdü. Bu taahhüt, üreticinin aadaki olaylardan, yetkilileri hemen bilgilendirmesi zorunluluunu da kapsar: i. Bir cihazn özelliklerinin ve/veya performansnn bozulmas veya sapmas, hastann veya kullancnn salk durumunda ciddi bozulmaya veya ölüme yol açabilecek veya yol açm olan kullanma klavuzunda ve etiketteki bilgilendirmeyle ilgili yetersizlikler. ii. (i) alt paragrafnda belirtilen hususlarda, ayn tip cihazn üreticisi tarafndan sistematik olarak yenilenmesine yol açan ve cihazn performansna veya özelliklerine bal tbbî ve teknik sebepler Kalite sistemi çerçevesinde, her cihaz veya serinin numunesi incelenir ve Tip-nceleme Sertifikasnda belirtilen tipe ve bu Yönetmelik hükümlerine uygunluunu denetlemek için, Yönetmeliin 6 nc maddesinde öngörülen standartlarda belirtilen uygun testlerden veya edeerindeki deneylerden geçirilir. Üretici tarafndan benimsenen bütün unsurlar, gerekler ve hükümler, yazl bilgiler ve ilemlerin sistematik olarak ele alnd ve uygun ekilde sraland bir belgede yer almaldr. Kalite sistemi hakkndaki bu belge, programlarn, planlarn, yaplan ilemlerin ve kaliteye ilikin kaytlarn ayn tarzda açklamasn salar. Bu belge, özellikle aadaki tanmlar içerir: - Kalitenin hedefleri, organizasyonun yaps, cihaz kalitesi konusunda organizasyonda çalanlarnn sorumluluk ve yetkileri, - Üretimden sonra yaplan kontroller ve testler. (Test donanmnn yeterli kalibrasyonunun, geriye doru izlenmesi mümkün olmaldr), - Kalite sisteminin etkin olarak ilemesini izleme metotlar, - Tefti raporlar, deney verileri, standart veriler, ilgili personelin nitelii hakkndaki raporlar gibi kaliteye ait kaytlar. Yukardaki incelemeler, üretimin, sterilizasyon yaplan aamalarnda uygulanmaz Onaylanm kurulu, kalite sisteminin bu EK in 3.2 nci kknda belirtilen gereklere uygun olup olmadn saptamak için denetimini yapar. Kalite sisteminde gerekli Uyumlatrlm Standartlarn uygulanp uygulanmadn kontrol eder. Deerlendirme ekibinde en az bir üyenin, ilgili teknoloji hakknda deerlendirme deneyimi olmaldr. Deerlendirme ileminde üretim yöntemini kontrol etmek için üretici ve gerektiinde, üreticinin tedarikçisi de yerinde denetlenir. Karar, denetim sonuçlar ve açklamal deerlendirmeyle birlikte üreticiye tebli edilir Üretici, kalite sisteminin önemli deiikliklerine ilikin bütün tasarlarndan, kalite sistemini onaylayan onaylanm kurulua bilgi verir. Onaylanm kurulu teklif edilen deiiklikleri deerlendirir ve kalite sistemindeki bu deiikliklerin bu EK in 3.2 nci kknda belirtilen gereklere uyup uymadn inceler ve kontrol sonuçlar ile açklamal deerlendirmelerin de yer ald karar üreticiye tebli eder. 4) Denetim:
21 4.1. Denetimin amac, üreticinin onaylanan kalite sisteminin gereklerini hatasz olarak yerine getirmesini garanti etmektir Üretici, onaylanm kuruluu test ve depolama yerlerinin teftii konusunda yetkili klar ve kurulua aadaki bilgilerde dahil olmak üzere gerekli bütün bilgileri eksiksiz olarak temin eder; - Kalite sistemi bilgileri, - Teknik belgeler, - Tefti raporlar ve test verileri, kalibrasyon verileri, ilgili personelin nitelikleri hakknda raporlar gibi kaliteye ait kaytlar Onaylanm kurulu, üreticinin kalite sistemini uyguladn garanti etmek amacyla, periyodik olarak tefti ve deerlendirme yapar ve üreticiye deerlendirme raporu verir lgili onaylanm kurulu üreticiye beklenmeyen ziyaretler yapabilir. Bu ziyaretlerde, gerekli görürse kalite sisteminin iyi ilediini ve ürünün bu Yönetmelik gereklerine uygunluunu denetlemek için deneyler yapabilir veya yaptrabilir. Bu amaçla, onaylanm kurulu bitmi cihazn bir numunesini yerinde alr, kontrol eder ve Yönetmeliin 6 nc maddesinde öngörülen standartlarda tanmlanan testlerden geçirir veya edeer testleri uygular. Kontrol edilen bir veya birden fazla cihaz örneinin uygun olmad durumda, onaylanm kurulu gerekli tedbirleri alr. Onaylanm kurulu, üreticiye bir denetim raporu ve eer test yaplmsa, test raporu verir. 5) darî Hükümler: Üretici, son cihazn üretiminden itibaren en az 5 yl süreyle yetkililere ibraz etmek üzere aadaki belgeleri saklar: - Uygunluk beyan, - Bu EK in 3.1 inci kknda belirtilen Tip-nceleme Sertifikasnn bir örnei ve onaylanm tip ile ilgili teknik belgeleri, - Bu EK in 3.4 üncü kknda belirtilen deiiklikleri, - Bu EK in 3.4 üncü kknn ikinci paragrafnda ve yine bu EK in 4.3 üncü ile 4.4 üncü kknda belirtilen onaylanm kurulu karar ve raporlar, - Gerektiinde, EK-III de belirtilen uygunluk sertifikasn. 6) IIa. Snf Cihazlar çin Uygulama: Bu EK, Yönetmeliin 9 uncu maddesinin (a/2) bendine uygun olarak, aadaki istisnai durum göz önünde tutulmak suretiyle, IIa. Snf cihazlara uygulanr. Üretici, bu EK in 2 nci, 3.1 inci ve 3.2 nci kknn uygulanmad durumlarda, IIa. Snf cihazlarn EK- VII nin 3 üncü kknda belirtilen teknik belgelere uygun olarak ürettiini ve kendilerine uygulanan bu Yönetmelik gereklerine cevap verdiini, uygunluk beyan ile açklar ve garanti eder. EK-VII UYGUNLUK BEYANI 1) Uygunluk Beyan; bu EK in 2 nci kknda belirtilen yükümlülükleri ve ölçme fonksiyonu bulunan cihazlar ile steril olarak piyasaya arz edilen cihazlar için bu EK in 5 inci kknda belirtilen yükümlülükleri yerine getiren üretici veya üreticinin Türkiye de olmad zaman yetkili temsilcisinin, bu yükümlülükleri yerine getirdiini ve sözkonusu cihazlarn bu Yönetmeliin hükümlerine uygunluunu gösteren ilemdir. 2) Üretici bu EK in 3 üncü kknda açklanan teknik belgeyi hazrlamaldr. Üretici veya üreticinin Türkiye de olmad zaman yetkili temsilcisi uygunluk beyan ile birlikte bu teknik belgeyi en son cihazn üretildii tarihten itibaren en az 5 yl süreyle yetkililerin denetimi için saklar. Üretici ve yetkili temsilcinin yurtiçinde bulunmad durumlarda, bu teknik belgeleri saklama zorunluluu, cihaz piyasaya arz eden gerçek veya tüzel kiilere aittir. 3) Bu teknik belge, Yönetmelikte belirtilen uyulmas gereken artlar tayan cihazn, uygunluunun deerlendirilmesini salamaldr. Bu belge aadaki hususlar içerir: - Cihaz ve cihaz üzerinde yaplmas düünülen her türlü deiiklii de kapsayan genel bir tanm, - Tasarm çizimleri, öngörülen üretim metodlar, cihazn önemli parçalar, aksesuarlar, devreleri gibi özellikleri gösteren ayrntl ema, - Cihazn kullanm, plan ve emalarnn anlalmas için gerekli tanm ve açklamalar, - Bu Yönetmeliin 6 nc maddesinde öngörülen standartlardan tam veya ksmen uygulananlarn bir listesi ve risk analizi sonuçlar,
22 Bu Yönetmeliin 6 nc maddesinde öngörülen standartlara uyulmad takdirde, bu Yönetmeliin temel gereklerine uyum salayan çözümlerin tanmlar, - Piyasaya steril olarak arz edilen cihazlar için kullanlan metodlarn tanm, - Uygulanan kontroller ile tasarm hesaplamalar gibi sonuçlar; cihazn planland gibi kullanm için baka bir cihaza/cihazlara balanmas gerekiyor ise, özellikleri üretici tarafndan belirlenmi olan bu tip cihaz/cihazlara balanan cihazn Yönetmelikte belirtilen temel gereklere uyduunu kantlayan belgeler, - Test raporlar ve gerektiinde EK-X a göre hazrlanm klinik veriler, - Etiket ve kullanm klavuzu. 4) Üretici, cihazla ilgili doal durumlar ve riskleri gözönünde bulundurarak, bunlar düzeltici gerekli çalmalar yapabilmesi için, uygun yöntemler gelitirmeli ve üretim sonrasnda cihazlarn kullanmndan elde edilen deneyimleri gözden geçirecek sistematik güncel bir yöntem oluturmal ve bu çalmalar sürdürmelidir. Ayrca, üretici aadaki durumlar hemen Bakanla bildirmelidir: i. Cihazn özellikleri veya performansnda herhangi bir hata veya bozukluk olmas, bunun yannda etiketleme ve kullanm klavuzundaki herhangi bir yetersizlik sebebiyle hastann veya kullancnn ölümüne yol açabilecek/açan, veya hastann salk durumunda ciddi bir bozulmaya sebep olabilecek/olmu olan durumlar, ii. (i) alt paragrafnda belirtilen hususlarda, ayn tip cihazn üreticisi tarafndan sistematik olarak yenilenmesine yol açan ve cihazn performansna veya özelliklerine bal tbbî ve teknik sebepler. 5) Üretici, steril olarak piyasaya arz edilen cihazlar ile I. Snfta yeralan ölçme fonksiyonlu cihazlar ile ilgili olarak, sadece bu EK de belirtilen artlara deil, ayn zamanda EK-IV de, EK-V de ve EK-VI da belirtilen ilemlerden birine uygun hareket etmelidir. Yukarda belirtilen eklerin uygulanmas ve onaylanm kuruluun müdahalesi; - Steril olarak piyasaya arz edilen cihazlarda, sadece steril artlarn sürdürülmesi ve güvenilirliiyle ilgili üretim konular, - Ölçüm fonksiyonlu cihazlarda, sadece ölçüm fonksiyonu bulunan ürünün uygunluuyla ilgili üretim konular, ile snrldr. Ayrca bunlara, bu EK in 6 nc kknn ikinci paragraf uygulanr. 6) IIa. Snf Cihazlara Yönelik Uygulama: Bu EK, Yönetmeliin 9 uncu maddesinin (a/2) bendine uygun olarak aadaki istisnaî durum göz önünde tutulmak suretiyle, IIa. Snf ürünlere uygulanabilir. Bu EK hükümleri; EK-IV de, EK-V de ve EK-VI da belirtilen ilemlerle birlikte uygulandnda, ilgili eklerde belirtilen uygunluk beyan tek bir beyan ile yaplr. Bu EK i esas alan beyan ile ilgili olarak üretici, üretim tasarmnn bu Yönetmelik hükümlerini karladn beyan ve garanti eder. EK-VIII ÖZEL AMAÇLI CHAZLARA LPKN BEYAN 1) Üretici veya üreticinin Türkiye de olmamas halinde yetkili temsilcisi, smarlama üretilen cihazlar ve klinik aratrma cihazlar için bu EK in 2 nci kknda belirtilen bilgileri içeren bir beyan hazrlar. 2) Bu beyan aadaki bilgileri kapsar: 2.1. Ismarlama üretilen cihazlar için; - Cihaz tanmlayc bilgiler, - Yalnzca belirli hastalar tarafndan kullanlacan belirten ve bu hastann adn da içeren rapor, - Reçeteyi yazan konusunda uzman hekim ad ile ilgili kliniin ad, - lgili tbbî reçetede belirtilmi olan cihazn önemli özellikleri, - Söz konusu cihazn EK-I de belirtilen temel gereklere uygunluunu ve bu gerekleri tam olarak karlamad durumlarda, bunlar sebebiyle birlikte açklayan bir rapor EK-X da belirtilen klinik aratrma cihazlar için; - Cihaz tanmlayc bilgiler, - Cihazlarn amacn, bilimsel, teknik veya tbbî özelliklerini, kullanm alann ve saysn belirten bir aratrma plan, - lgili danma komisyonunun görüleri ve bu görülerle ilgili detayl açklamalar, - Aratrmadan sorumlu enstitünün, hekimin veya yetkili uzman personelin ad, - Aratrmalarn yapld yer, balama tarihi ve çalma plan, - Cihazn, aratrmalar kapsamndaki konular dnda kalan temel gereklere uygunluu ve bu konularla ilgili olarak, hastann güvenlii ve salnn korunmas amacyla alnm olan tedbirleri belirten belge.
23 3) Üretici ayn zamanda Bakanla gerektiinde sunmak üzere: 3.1. Ismarlama üretilen cihazn, bu Yönetmeliin gereklerini tadn belgeleyen, tasarm, üretimi ve beklenen performans dahil, elde edilen performansn açklayan belge paketini hazr bulundurmakla yükümlüdür. Üretici birinci paragrafta belirtilen belgeye göre üretilmi olan cihazn üretim yöntemini gerçekletirici bütün tedbirleri alr Klinik aratrma cihazlarna ilikin belge paketi aadaki bilgileri içermelidir: - Cihazn genel tanm, - Tasarm çizimleri, özellikle sterilizasyon metodu ve cihazn önemli parçalar, aksesuarlar, devreleri gibi emalarn da içeren üretim metodlar, - Cihazn kullanm, plan ve emalarnn anlalmas için gerekli tanm ve açklamalar, - Bu Yönetmeliin 6 nc maddesinde öngörülen standartlardan tam veya ksmen uygulananlarn bir listesi ve risk analizi sonuçlar ile, bu maddede öngörülen standartlara uyulmad takdirde, bu Yönetmeliin temel gereklerine uyum salayan çözümlerin tanmlar, - Uygulanan kontroller ile tasarm hesaplamalar gibi sonuçlar. Üretici yukarda belirtilen belgeye göre üretilmi olan cihazn üretim yöntemini gerçekletirici bütün tedbirleri alr. Üretici bu tedbirlerin etkinliinin deerlendirilmesini veya gerektiinde denetimini kabul ve taahhüt eder. 4) Bu EK te öngörülen bilgi ve belgeler en az 5 yl süreyle saklanmaldr. EK-IX SINIFLANDIRMA KURALLARI I. TANIMLAR: 1) Snflandrma kurallarnda yeralan tanmlar: 1.1. Süre esas göre cihazlar: - Geçici süreli: Normalde 60 dakikadan az bir sürede ve devaml kullanlmas amaçlanan cihazlar. - Ksa süreli: Normalde 30 günden az ve sürekli kullanlmas amaçlanan cihazlar. - Uzun süreli: Normalde 30 günden fazla ve sürekli kullanlmas amaçlanan cihazlar nvaziv Cihazlar: Bu cihazlar, vücut açklndan veya vücut yüzeyini geçerek vücudun iç ksmna ksmen veya tamamen yerletirilen cihazlardr. - Vücut Açkl: Göz yuvasnn d yüzeyini de içeren vücuttaki herhangi bir doal açklk veya kalc olarak açlm yapay açklktr. - Cerrahi nvaziv Cihaz: Bu tip cihazlar, bir cerrahi müdahale sonucu vücut yüzeyini geçerek vücudun iç ksmna yerletirilen cihazlardr. Bu Yönetmeliin amacna uygun olarak tanmlanan ve yukarda belirtilen cihazlardan ayr olarak, vücudun mevcut girileri haricindeki bir yere cerrahi operasyonla yerletirilerek kullanlan cihazlar da cerrahi invaziv cihazlar olarak tanmlanr. - mplant Cihazlar: Cerrahi müdahale ile, bütünüyle insan vücuduna veya göz yüzeyine veya deri yüzeyine yerletirilen ve yerletirme ileminden sonra yerinde kalan cihazlardr. nsan vücuduna cerrahi operasyonla ksmen taklan ve ilemden sonra en az 30 gün yerinde kalmas öngörülen cihazlar da implant cihazlar olarak tanmlanr Tekrar Kullanlabilir Cerrahi Aletler: Bunlar hiçbir aktif tbbî cihaz ile balants olmakszn, kesme, delme, dikme, birletirme, skma, çekme, tutturma veya benzeri cerrahi ilemleri yapmak için kullanlan ve bu ilemler tamamlandktan sonra tekrar kullanlabilen tbbî cihazlardr Aktif Tbbî Cihazlar: Bunlar, insan vücudunun doal olarak oluturduu enerji haricinde herhangi bir elektrik enerjisi veya güç kaynayla ve bu enerjinin dönüümüyle çalan cihazlardr. Tbbî cihaz ile hasta arasnda enerjinin, maddelerin ve dier elementlerin, belirli bir deiime yol açmakszn, geçiini salayan cihazlar ise, aktif tbbî cihaz saylmaz Aktif Tedavi Edici Cihazlar: Bunlar; bir hastaln, yarann veya sal bozan faktörlerin etkisini azaltmak veya tedavisini gerçekletirmek üzere tek bana veya dier tbbî cihazlarla birlikte, biyolojik yaplar veya fonksiyonlar destekleyen, deitiren, yenileyen veya yeniden düzenleyen cihazlardr Tehis Amaçl Aktif Cihazlar: Bunlar, hastalk veya doutan gelen ekil bozukluklar, salk durumunu ve fizyolojik fonksiyonlar tanmlama, tehis, izleme ve tedavi etmek amacyla bilgi salamak için tek bana veya baka tbbî cihazlarla bileik olarak kullanlan aktif tbbî cihazlardr.
24 1.7. Merkezî Dolam Sistemi: Bu Yönetmelik amac çerçevesinde, kalp ve kalbe giri-çk yapan atar ve toplar damar sistemi aadaki damarlar içerir: Arteriae pulmonalis, aorta ascendens, arteriae coronariae, arteria carotis communis, arteria carotis externa, arteria carotis interna, arteriae cerebralis, truncus brachicephalicus, venae cordis, venae pulmonalis, vena cava süperior ve vena cava inferior Merkezî Sinir Sistemi: Bu Yönetmelik amac çerçevesinde merkezî sinir sistemi beyin, beyincik ve omurilii içerir. II. UYGULAMA KURALLARI: 2) Uygulama Kurallar: 2.1. Snflandrma kurallarnn uygulanmas, cihazlarn amaçlarna göre deiir Eer cihaz dier bir cihaz ile beraber kullanlacak ise, snflandrma kural her cihaza ayr ayr uygulanr. Aksesuarlar ise, beraber kullanldklar cihazlardan ayr olarak snflandrlr Cihazn kullanmn etkileyen veya cihaz çaltran yazlm da ayn snfa girer Payet cihaz, vücudun belirli bir bölümünde tek bana veya esas olarak kullanlmayacak ise, en kritik kullanma göre snflandrlr Payet ayn cihaza üreticisi tarafndan, cihazn performansna bal olarak birden fazla kural uygulanabiliyor ise, cihaz bunlardan en yüksek snflandrma kapsamndaki en kat kural çerçevesinde deerlendirilir. III. SINIFLANDIRMA: 1) nvaziv Olmayan Cihazlar: 1.1. Kural 1: Bütün invaziv olmayan cihazlar, aadaki kurallardan birine girmedikçe I. Snf içinde yer alrlar Kural 2: Kann, vücut svlarnn veya dokularnn alnp verilmesi veya saklanmas, sv veya gazlarn vücuda infüzyonu, verilmesi veya uygulanmas amacna yönelik bütün invaziv olmayan cihazlar; - Payet, IIa. Snftaki veya daha yüksek bir snftaki aktif tbbî cihazlara balanabiliyor ise, - Payet, kann veya dier vücut svlarnn alnp verilmesi veya saklanmas veya organlar, organ parçalarnn veya vücut dokularnn saklanmas amacna yönelik ise, IIa. Snfta yer alr. Dier bütün durumlarda I. Snfa girerler Kural 3: Kann, dier vücut svlarnn veya vücuda infüzyonu amaçlanan dier svlarn kimyasal veya biyolojik bileimlerini düzenleyen tüm invaziv olmayan cihazlar IIb. Snfa girerler. Ancak tedavi; gazn veya snn filtrasyonu, santrifüjü veya deiimi temeline dayanyor ise, bu durumda IIa. Snfa girerler Kural 4: Yaral ciltle temas eden tüm invaziv olmayan cihazlar; - Salglarn emilimi veya basklanmas için mekanik bariyer olarak kullanlyorsa I. Snfa girerler. - Esas olarak derms tabakasnn tahribat sonucu oluan yaralarda kullanlmas öngörülen ve sadece ikincil olarak iyilemeyi salayan cihazlar IIb. Snfa girerler. - Esas olarak yarann mikro çevresini iyiletirme amaçl cihazlar dahil, dier bütün durumlarda kullanlan cihazlar IIa. Snfa girerler. 2) nvaziv cihazlar: 2.1. Kural 5: Bunlar cerrahi invaziv cihazlar dndaki ve baka aktif tbbî cihazlarla birlemeksizin vücut girileri ile uyumlu cihazlardr. - Geçici kullanm öngörülenler I. Snfa girerler. - Ksa süreli kullanm amaçl cihazlar IIa. Snfa girerler. Ancak, I. Snfta yeralan ve yutaa kadar olan az boluu içinde, kulak zarna kadar olan kulak kanal veya nazal bolukta kullanlanlar hariçtir. - Uzun süreli kullanm amaçl cihazlar IIb. Snfa girerler. Ancak, IIa. Snfta yeralan, mukoz zarlardan emilmeye uygun olmayan ve yutaa kadar olan az boluu içinde, kulak zarna kadar olan kulak kanal veya nazal bolukta kullanlanlar hariçtir. Cerrahi invaziv cihazlar haricinde, IIa. Snf veya daha üst bir snfa giren bir aktif tbbî cihaz ile balantl olarak kullanm öngörülen, vücut girileri ile uyumlu bütün invaziv cihazlar IIa. Snfa girerler Kural 6: Bütün geçici kullanml cerrahi invaziv cihazlar IIa. Snfa girerler:
25 - Temelde kalpte veya merkezî dolam sistemindeki bir bozukluu vücudun bu bölümleriyle dorudan temasa girerek tehis eden, izleyen ve düzelten cihazlar III. Snfa girerler. - Tekrar kullanlabilir cerrahi cihazlar I. Snfa girerler. - yonlatrc radyasyon formunda enerji salamaya yarayan cihazlar IIb. Snfa girerler. - Biyolojik etkiye sahip ve tamam ya da büyük bir çounluu absorbe edilen cihazlar IIb. Snfa girerler. - Payet, bu invaziv cihazlar bir serbest brakma mekanizmas araclyla, ilaçlar vermeye elverili ve uygulama ekli tehlike oluturuyor ise, IIb. Snfa girerler Kural 7: Aadaki durumlar dnda ksa süreli kullanm için olan bütün cerrahi invaziv cihazlar IIa. Snfa girerler: - Kalpteki veya merkezî dolam sistemindeki bir bozukluu vücudun bu ksmlar ile temas etmek suretiyle tehis eden, izleyen ve düzelten cihazlar III. Snfa girerler. - Özellikle merkezî sinir sistemi ile dorudan temas etmek suretiyle kullanlan cihazlar III. Snfa girerler. - yonlatrc radyasyon formunda enerji salayan cihazlar IIb. Snfa girerler. - Biyolojik etkisi olan veya tamam veyahut büyük bir çounluu absorbe edilen cihazlar III. Snfa girerler, - Di içine yerletirilenler hariç, vücutta kimyasal deiime urayan veya ilaç vermede kullanlan cihazlar IIb. Snfa girerler Kural 8: Aadaki durumlar dnda, bütün implant cihazlar ve uzun süre etkili cerrahi invaziv cihazlar IIb. Snfa girerler. - Dilere yerletirilen ve tutuculuu dilerle ve/veya dieti dokusuyla salanan cihazlar IIa. Snfa girerler. - Kalp, merkezî dolam sistemi veya merkezî sinir sistemiyle dorudan temas edecek ekilde kullanlan cihazlar III. Snfa girerler. - Biyolojik etkileri olan veya tamam veyahut büyük bir çounluu absorbe edilen cihazlar III. Snfa girerler. - Di içine yerletirilenler hariç, vücutta kimyasal deiime urayan veya ilaç vermede kullanlan cihazlar III. Snfa girerler. 3) Aktif cihazlara uygulanan ek kurallar: 3.1. Kural 9: Enerji verme veya enerji dönüümünü salamaya yönelik tüm aktif tedavi edici cihazlar IIa. Snfa girerler. Ancak yaps, younluu ve enerji uygulama yeri gözönüne alndnda, insan vücudunda enerji alp vermede veya enerji dönüümünü salamada potansiyel bir risk oluturuyor ise IIb. Snfa girerler. IIb. Snfda yeralan aktif tedavi edici cihazlarn performanslarn izleyen ve kontrol eden cihazlar veya bu cihazlarn performanslarn dorudan etkilemeye yönelik aktif tbbî cihazlar da IIb. Snfna girerler Kural 10: IIa. Snfa giren tehis amaçl aktif cihazlar; - Gözle görülebilir bir spektrumda hasta vücudunu aydnlatmak için kullanlan cihazlar hariç, insan vücudu tarafndan absorbe edilecek enerjiyi salayan cihazlar, - Radyofarmasötiklerin canl dokulardaki dalmn görüntülemede kullanlan cihazlar, - Hayati fizyolojik fonksiyonlarn dorudan tehisi veya izlenmesine olanak salayan cihazlar. Ancak, IIb. Snfa giren, merkezî sinir sistemi faaliyetleri, solunum ve kalp fonksiyonlarndaki deiiklikler gibi hastann durumunda ani tehlike yaratacak yapdaki deiiklikleri izlemeye yönelik olanlar hariç, -yonlatrc radyasyon yayan cihazlar ve giriimsel radyolojik tehis ve tedavi amaçl cihazlar ve bu cihazlar kontrol ve izlemeye yönelik veya bunlarn performansn dorudan etkileyen aktif cihazlar IIb. Snfa girerler Kural 11: laçlar, vücut svlarn ve dier maddeleri vücuda veren veya alan tüm aktif cihazlar IIa. Snfa girerler. Ancak verili ekli, vücudun ilgili bölümü ve verilen maddelerin özellii gözönüne alndnda, bu ilem potansiyel bir risk oluturuyor ise IIb. Snfa girerler Kural 12: Dier bütün aktif cihazlar I. Snfa girerler. 4) Özel Kurallar: 4.1. Kural 13: Ayr olarak kullanldnda, tbbî ürün olarak deerlendirilen ve cihazn insan üzerindeki etkisini destekleyici aktivite gösteren bir maddeyi bir iç parça olarak ihtiva eden bütün cihazlar III. Snfa girerler. nsan kan türevini bir bütünün parças olarak içeren tüm cihazlar III. Snf kapsam içerisindedir.
26 4.2. Kural 14: Doum kontrolü veya cinsel temasla geçen hastalklarn bulamasn engellemek amacyla kullanlan bütün cihazlar IIb. Snfa girerler. Ancak, implant veya uzun süreli invaziv cihaz olmas halinde, III. Snfa girerler Kural 15: Kontakt lensleri dezenfekte etmeye, temizlemeye, durulamaya ve gerektiinde nemlendirmeye yarayan cihazlar IIb. Snfa girerler. Özellikle tbbî cihazlar dezenfekte etmeye yarayan cihazlar IIa. Snfa girerler. Bu kural kontakt lensler dndaki tbbî cihazlar fiziksel etkiyle temizleyen dier ürünlere uygulanmaz Kural 16: Özellikle X-ray tehis görüntülerini kaydetme amacyla kullanlan aktif olmayan cihazlar IIa. Snfa girerler Kural 17: Sadece salam deri ile temas amaçlanan cihazlar hariç, hayvan dokular veya ölü doku parçalar kullanlarak üretilen bütün cihazlar III. Snfa gireler. 5) Kural 18: Dier kurallardan farkl olarak kan torbalar, IIb. Snfa girerler. EK-X KLNK DERERLENDRME 1) Genel Hükümler: 1.1. Genel bir kural olarak, EK-I in 1 inci ve 3 üncü klarnda belirtilen performans ve özellikler ile ilgili artlarn uygunluunun tasdiki, özellikle implant cihazlar ve III. Snfta yeralan cihazlar için, cihazn normal artlardaki kullanm ve yan etkilerinin deerlendirilmesi klinik verilere dayandrlmaldr. lgili uyumlatrlm standartlar göz önüne alnarak, uygun olan yerlerde, klinik verinin yeterlilii aadaki hususlara dayandrlr; Kullanlan teknikler ile cihazn tasarm amacna yönelik güncel bilimsel literatürlere olduu kadar mümkün ise, bu literatürlerin eletirel bir deerlendirmesini içeren bir rapora veya, Bu EK in 2 nci kkna uygun olarak gerçekletirilenler dahil, yaplm klinik aratrma sonuçlarna Bu Yönetmeliin 22 nci maddesi gereince, bütün veriler gizli kalmaldr. 2) Klinik Aratrmalar: 2.1. Klinik aratrmann amac; - Cihazn normal kullanm koullarndaki performansnn EK-I in 3 üncü kkna göre uygunluunun deerlendirilmesi, - Normal kullanm koullarndaki olas istenmeyen herhangi bir yan etkiyi ve bu etkinin cihazn amaçlanan performansyla kyaslandnda kabul edilebilir bir risk oluturup- oluturmadnn deerlendirmesidir Etik Deerlendirmeler; Klinik aratrmalar, 1964 de Finlandiya nn Helsinki ehrinde yaplan 18 inci Dünya Tp Asamblesi nde kabul edilen ve son düzenlemeleri 1989 da Hong Kong daki 41 inci Dünya Tp Asamblesi nde yaplan, "Helsinki Bildirgesi ne göre gerçekletirilmelidir. Bu Bildirge, insan saln korumaya yönelik bütün tedbirlerin Helsinki Bildirgesi çerçevesinde ele alnmas hükmünü içerir. Bu Bildirge, klinik deerlendirme gereinin ilk ortaya çkndan, dorulayc çalma sonuçlarnn yaymlanmasna kadar her aamay içerir Metodlar; Klinik aratrmalar, güncelliini koruyan bilimsel ve teknik bilgileri yanstan bir plana göre uygulanmal ve üreticinin cihaza ilikin iddialarn dorulayc veya reddedici ekilde belirlenmelidir. Bu aratrmalar, sonuçlarn bilimsel geçerliliini garantileyen yeterli sayda gözlem içermelidir Aratrmalar gerçekletirmek için kullanlan metodlar incelenen cihaza uygun olmaldr Klinik aratrmalar cihazn normal koullarda kullanmna benzer artlarda yaplmaldr Cihazn, performansn ve güvenilirliini salayanlar da dahil, uygun bütün parçalar ve bunlarn hasta üzerindeki etkisi incelenmelidir Bu Yönetmeliin 17 nci maddesinde belirlenen bütün olumsuz durumlar Bakanla eksiksiz olarak bildirilmeli ve kaydettirilmelidir Aratrmalar, ilgili hekim veya konusunda uzman tarafndan uygun bir ortamda yaplmaldr. lgili hekim veya konusunda uzman yetkili kii cihaza ilikin teknik ve klinik verilere sahip olmaldr Yazlan rapor, klinik aratrma süresince toplanan bütün verilerin eletirel bir deerlendirilmesini içermeli ve sorumlu ilgili hekim veya dier yetkili personel tarafndan imzalanmaldr. EK-XI
27 ONAYLANMIP KURULUPUN SEÇMNE LPKN ASGARÎ ÖZELLKLER Onaylanm kuruluun seçiminde, Kanun, Uygunluk Deerlendirme Kurulular ile Onaylanm Kurululara Dair Yönetmelik ve bu Yönetmelik hükümlerinin yannda ayrca, aada belirtilen asgarî özellikler gözetilir: 1) Onaylanm kuruluun yöneticisi ile deerlendirme ve dorulama ilemini yürüten elemanlar, ayn zamanda denetimlerini yaptklar cihazlar tasarlayan, üreten, temin eden, yerletiren veya kullanan kiiler veya bu kiilerin yetkili temsilcileri olamazlar. Bu kiiler cihazlarn tasarmna, pazarlanmasna, temin edilmesine dorudan katlmamal veya bu faaliyetlerde görev alan taraflar temsil etmemelidir. Bu hususlar üretici ile kurum arasndaki teknik bilgi alveriini engellemez. 2) Onaylanm kurulu ve ilgili elemanlar, tbbî cihazlar alannda yeterli bilgiye sahip olmal, deerlendirme ve dorulama ilemlerini meslekî etik kurallar içinde gerçekletirmeli ve özellikle dorulama sonuçlarndan çkar salayacak kiilerin ve gruplarn denetim sonuçlarn etkileyebilecek tüm basklarndan ve parasal yönlendirmelerden uzak olmaldrlar. Onaylanm kurulular görevlendirildikleri uygunluk deerlendirme faaliyetlerinin bir ksmn, sözleme yaparak bir yüklenici/taeron kurulua yaptrabilirler. Onaylanm kurulu faaliyetlerinin tamamn yüklenici/taerona devredemez. Yüklenici/taeron kurulu da, Onaylanm kuruluun kendisiyle yapm olduu sözleme konusu faaliyetleri bir baka kurulua devredemez. Onaylanm kurulu yüklenici kurulu ile dorudan bir sözleme ilikisi içinde olmal ve sözleme yapaca yüklenici/taeron bu Yönetmeliin ve özellikle bu EK in hükümlerini yerine getirdiini garantilemelidir. Onaylanm kurulu, yüklenicinin/taeronun niteliklerinin deerlendirilmesi ile ilgili belgeleri ve sürdürdüü çalmalarla ilgili bütün dier belgeleri gerektiinde Bakanla sunmak üzere saklar. Yaplan bütün ilemlerden onaylanm kurulu sorumludur ve uygunluk belgesi onaylanm kurulu tarafndan verilir. 3) Onaylanm kurulu EK-II ile EK-VI arasndaki eklerden birine göre kendisine verilen görevi yapmaya veya kendi sorumluluu altnda yaptrmaya yetkin olmaldr. Onaylanm kurulu, deerlendirme ve onaylama faaliyetlerinin gerektirdii teknik ve idarî ilemleri yürütmesi için gerekli personel ve teknik imkanlara sahip olmaldr. Ayrca, kuruluun istenen dorulama ilemi için gereken donanma da sahip ve bu Yönetmelik hükümlerini, özellikle EK-I de düzenlenen artlar göz önünde bulundurarak, kurum içerisinde, bildirdii cihazn tbbî ilerlii ve performansn deerlendirebilecek yeterli deneyime ve bilgiye sahip yeterli sayda uzman personelin olmas gerekir. 4) Onaylanm kuruluun ilgili personeli: -Tayin edildii deerlendirme ve dorulama ilemlerinin tamamn kapsayan meslekî eitime, -Yapt denetimlerle ilgili kurallar hakknda yeterli bilgi ve tecrübeye, -Yapm olduu denetimleri gösteren sertifikalar, kaytlar ve raporlar düzenleme becerisine, sahip olmaldr. 5) Onaylanm kurulu, tarafszln garanti etmelidir. Ücretler, yaplan denetimlerin saysna veya sonuçlarna bal olmamaldr. 6) Onaylanm kurulu, kendisine verilen yetkilere istinaden yapt her türlü ilem ile ilgili olarak hukukî sorumluluu üstlenmelidir. 7) Bu Yönetmelik hükümlerine göre, onaylanm kuruluun personeli, görevi sebebiyle örendii her türlü bilgileri yetkili idarî ve adlî mercilerin talepleri olmas hali dnda, meslekî sr olarak saklamaldr.
28 CE uygunluk iareti "CE" harflerinden oluur. EK-XII CE UYGUNLUK PARET - Eer iaret büyültülür veya küçültülür ise, yukardaki çizim içinde gösterilen oranlar deimemelidir. - CE iareti harfleri, ayn tarz ve dikey boyutlarda olmaldr. Dikey boyut, 5 milimetreden küçük olamaz. Bu minimal boyut, küçük boyutlu cihazlar için zorunlu deildir. - CE iaretinin ilitirilmesinde, Kanun ve "CE" Uygunluk aretinin litirilmesine ve Kullanlmasna Dair Yönetmelik hükümleri uygulanr.
Elektromanyetik Uyumluluk Yönetmelii (89/336/AT)
 Sanayi ve Ticaret Bakanlndan: Elektromanyetik Uyumluluk Yönetmelii (89/336/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak, Tan+mlar Amaç Madde 1 Bu Yönetmeliin amac; radyokomünikasyon ile telekomünikasyon ve elektrikli
Sanayi ve Ticaret Bakanlndan: Elektromanyetik Uyumluluk Yönetmelii (89/336/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak, Tan+mlar Amaç Madde 1 Bu Yönetmeliin amac; radyokomünikasyon ile telekomünikasyon ve elektrikli
Belirli Gerilim Snrlar Dahilinde Kullanlmak Üzere Tasarlanm Elektrikli Teçhizat ile lgili Yönetmelik (73/23/AT)
 Belirli Gerilim Snrlar Dahilinde Kullanlmak Üzere Tasarlanm Elektrikli Teçhizat ile lgili Yönetmelik (73/23/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak, Tanmlar Amaç : Madde 1 Bu Yönetmeliin amac; Yönetmelik
Belirli Gerilim Snrlar Dahilinde Kullanlmak Üzere Tasarlanm Elektrikli Teçhizat ile lgili Yönetmelik (73/23/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak, Tanmlar Amaç : Madde 1 Bu Yönetmeliin amac; Yönetmelik
Asansör Yönetmelii ( 95/16/AT ) BRNC BÖLÜM Amaç, Kapsam, Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli"in amac; mar Kanunu ve buna ba"l imar
 Asansör Yönetmelii ( 95/16/AT ) BRNC BÖLÜM Amaç, Kapsam, Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli"in amac; mar Kanunu ve buna ba"l imar yönetmeliklerine göre in'a edilen binalarda, insan ve yük ta'masnda
Asansör Yönetmelii ( 95/16/AT ) BRNC BÖLÜM Amaç, Kapsam, Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli"in amac; mar Kanunu ve buna ba"l imar yönetmeliklerine göre in'a edilen binalarda, insan ve yük ta'masnda
Dilek GÖKCEK. İzmir 2014
 1 Dilek GÖKCEK İzmir 2014 2 Piyasa Gözetimi ve Denetimi TİTCK ürün grupları Kurumumuz sorumluluğundaki PGD ye tabi ürünler Tıbbi Cihazlar -Genel Tıbbi Cihazlar Kozmetikler İlaçlar -Vücuda Yerleştirilebilir
1 Dilek GÖKCEK İzmir 2014 2 Piyasa Gözetimi ve Denetimi TİTCK ürün grupları Kurumumuz sorumluluğundaki PGD ye tabi ürünler Tıbbi Cihazlar -Genel Tıbbi Cihazlar Kozmetikler İlaçlar -Vücuda Yerleştirilebilir
e) İnsan kanı türevleri hariç olmak üzere; insan kanı, kan ürünleri, insan kaynaklı plazma veya kan hücreleri ile insan hücresi, dokusu, nakil
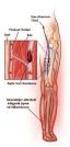 CE İŞARETİ (MEDİKAL) TIBBİ CİHAZ YÖNETMELİĞİ Avrupa Birliği Komisyonu 93/42/EEC numaralı Tıbbi Cihaz Direktifinde, gelişen pazar ve teknoloji koşulları ile direktifte net olmayan, üye ülkeler arasında
CE İŞARETİ (MEDİKAL) TIBBİ CİHAZ YÖNETMELİĞİ Avrupa Birliği Komisyonu 93/42/EEC numaralı Tıbbi Cihaz Direktifinde, gelişen pazar ve teknoloji koşulları ile direktifte net olmayan, üye ülkeler arasında
TIBBÎ CİHAZ YÖNETMELİĞİ. BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar
 Sağlık Bakanlığından: TIBBÎ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbî
Sağlık Bakanlığından: TIBBÎ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbî
TIBBİ CİHAZLARIN ONAY PROSEDÜRLERİ
 TIBBİ CİHAZLARIN ONAY PROSEDÜRLERİ Tıbbi Cihaz Yönetmeliği I. Bölüm - Amaç ve Kapsam (Madde 1) - Dayanak (Madde 2 - Tanımlar (Madde 3) II. Bölüm - Piyasaya Arz ve Hizmet Sunumu (Madde 4) - Temel Gerekler
TIBBİ CİHAZLARIN ONAY PROSEDÜRLERİ Tıbbi Cihaz Yönetmeliği I. Bölüm - Amaç ve Kapsam (Madde 1) - Dayanak (Madde 2 - Tanımlar (Madde 3) II. Bölüm - Piyasaya Arz ve Hizmet Sunumu (Madde 4) - Temel Gerekler
Tıbbi Cihaz Yönetmeliği Sağlık Bakanlığından
 Tıbbi Cihaz Yönetmeliği Sağlık Bakanlığından BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbi cihaz
Tıbbi Cihaz Yönetmeliği Sağlık Bakanlığından BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbi cihaz
Tıbbi Cihaz Klinik Araştırmaları
 Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Tıbbi Cihaz Klinik Araştırmaları Tıbbi Cihaz Onaylanmış Kuruluş ve Klinik araştırmalar Daire Başkanlığı İçerik: Tıbbi cihaz nedir? Neden klinik araştırması yapmak zorundayız? Tıbbi cihaz klinik araştırması
Eczacılar ve Eczaneler Hakkında Yönetmelikte Değişiklik Yapılmasına Dair Yönetmelik bugün sayılı Resmi Gazete'de yayımlandı
 Eczac?lar ve Eczaneler Hakk?nda Yönetmelikte De?i?iklik Yap?lmas?na Dair Yönetmelik bugün 29667 say?l? Resmi Gazete'de yay?mland? Say? : 29667 28 Mart 2016 PAZARTES? Resmî Gazete YÖNETMEL?K Türkiye?laç
Eczac?lar ve Eczaneler Hakk?nda Yönetmelikte De?i?iklik Yap?lmas?na Dair Yönetmelik bugün 29667 say?l? Resmi Gazete'de yay?mland? Say? : 29667 28 Mart 2016 PAZARTES? Resmî Gazete YÖNETMEL?K Türkiye?laç
Tıbbi Cihaz Yönetmeliği
 Tıbbi Cihaz Yönetmeliği BĐRĐNCĐ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbî cihaz ve aksesuarlarının
Tıbbi Cihaz Yönetmeliği BĐRĐNCĐ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbî cihaz ve aksesuarlarının
Kişisel Koruyucu Donanımlarla İlgili Onaylanmış Kuruluşların Görevlendirilmesine Dair Tebliğ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanımlar
 Kişisel Koruyucu Donanımlarla İlgili Onaylanmış Kuruluşların Görevlendirilmesine Dair Tebliğ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanımlar Amaç Madde 1 Bu Tebliğin amacı, 09.02.2004 tarih ve 25368
Kişisel Koruyucu Donanımlarla İlgili Onaylanmış Kuruluşların Görevlendirilmesine Dair Tebliğ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanımlar Amaç Madde 1 Bu Tebliğin amacı, 09.02.2004 tarih ve 25368
Basnçl ekipmanlar Yönetmelii ( 97/23/AT ) B"R"NC" BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanmlar
 Sanayi ve Ticaret Bakanlndan: Amaç ve Kapsam Basnçl ekipmanlar Yönetmelii ( 97/23/AT ) B"R"NC" BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanmlar Madde 1 Bu Yönetmelik; maksimum izin verilebilen PS basnc 0,5
Sanayi ve Ticaret Bakanlndan: Amaç ve Kapsam Basnçl ekipmanlar Yönetmelii ( 97/23/AT ) B"R"NC" BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanmlar Madde 1 Bu Yönetmelik; maksimum izin verilebilen PS basnc 0,5
kapsamında faaliyet gösteren uygunluk değerlendirme kuruluşu ya da onaylanmış kuruluşların aşağıda belirtilen şartları taşıması gerekir;
 Uygunluk Değerlendirme Kuruluşları ile Onaylanmış Kuruluşlara Dair Yönetmelik BİRİNCİ BÖLÜM Amaç ve Kapsam, Hukuki Dayanak ve Tanımlar Amaç ve kapsam Madde 1- Bu Yönetmelik; bir teknik düzenleme kapsamında
Uygunluk Değerlendirme Kuruluşları ile Onaylanmış Kuruluşlara Dair Yönetmelik BİRİNCİ BÖLÜM Amaç ve Kapsam, Hukuki Dayanak ve Tanımlar Amaç ve kapsam Madde 1- Bu Yönetmelik; bir teknik düzenleme kapsamında
8.MÜKEMMELL ARAYI SEMPOZYUMU 17 Nisan 2007 / zmir
 8.MÜKEMMELL ARAYI SEMPOZYUMU 17 Nisan 2007 / zmir Betül Faika SÖNMEZ Sa*l+k Bakanl+*+ Temel Sa*l+k Hiz.Gen. Md. Kalite E*itim ve Koor. Birimi Daire Ba3kan+ SA LIK HZMETNDE ARTAN TALEP Kaliteli, düük maliyette
8.MÜKEMMELL ARAYI SEMPOZYUMU 17 Nisan 2007 / zmir Betül Faika SÖNMEZ Sa*l+k Bakanl+*+ Temel Sa*l+k Hiz.Gen. Md. Kalite E*itim ve Koor. Birimi Daire Ba3kan+ SA LIK HZMETNDE ARTAN TALEP Kaliteli, düük maliyette
YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ
 9 Ocak 2007 SALI Resmî Gazete Sayı : 26398 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
9 Ocak 2007 SALI Resmî Gazete Sayı : 26398 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
ASMOLEN UYGULAMALARI
 TURGUTLU TULA VE KREMT SANAYCLER DERNE ASMOLEN UYGULAMALARI Asmolen Ölçü ve Standartlar Mart 2008 Yayn No.2 1 ASMOLEN UYGULAMALARINDA DKKAT EDLMES GEREKL HUSUSLAR Döeme dolgu tulas, kil veya killi topran
TURGUTLU TULA VE KREMT SANAYCLER DERNE ASMOLEN UYGULAMALARI Asmolen Ölçü ve Standartlar Mart 2008 Yayn No.2 1 ASMOLEN UYGULAMALARINDA DKKAT EDLMES GEREKL HUSUSLAR Döeme dolgu tulas, kil veya killi topran
Kiisel Koruyucu Donanm Yönetmelii BRNC BÖLÜM Amaç, Kapsam, Hukuki Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli#in amac; insan sa#l# ve güvenli#inin
 Kiisel Koruyucu Donanm Yönetmelii BRNC BÖLÜM Amaç, Kapsam, Hukuki Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli#in amac; insan sa#l# ve güvenli#inin korunmas amacyla kullanlan ki)isel koruyucu donanmlarn
Kiisel Koruyucu Donanm Yönetmelii BRNC BÖLÜM Amaç, Kapsam, Hukuki Dayanak ve Tanmlar Amaç Madde 1 Bu Yönetmeli#in amac; insan sa#l# ve güvenli#inin korunmas amacyla kullanlan ki)isel koruyucu donanmlarn
GIDA İLE TEMAS EDEN MADDE VE MALZEME ÜRETEN İŞLETMELERİN KAYIT İŞLEMLERİ İLE İYİ ÜRETİM UYGULAMALARINA DAİR YÖNETMELİK BİRİNCİ BÖLÜM
 GIDA İLE TEMAS EDEN MADDE VE MALZEME ÜRETEN İŞLETMELERİN KAYIT İŞLEMLERİ İLE İYİ ÜRETİM UYGULAMALARINA DAİR YÖNETMELİK Amaç BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar MADDE 1 (1) Bu Yönetmeliğin amacı,
GIDA İLE TEMAS EDEN MADDE VE MALZEME ÜRETEN İŞLETMELERİN KAYIT İŞLEMLERİ İLE İYİ ÜRETİM UYGULAMALARINA DAİR YÖNETMELİK Amaç BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar MADDE 1 (1) Bu Yönetmeliğin amacı,
Piyasa Gözetimi ve Denetimi Uygulamaları
 Tüketicinin Korunması ve Piyasa Gözetimi Genel Müdürlüğü Piyasa Gözetimi ve Denetimi Uygulamaları Elif DOĞAN Gümrük ve Ticaret Denetmeni SUNUM İÇERİĞİ TANIMLAR PİYASA GÖZETİMİ VE DENETİMİNE İLİŞKİN USUL
Tüketicinin Korunması ve Piyasa Gözetimi Genel Müdürlüğü Piyasa Gözetimi ve Denetimi Uygulamaları Elif DOĞAN Gümrük ve Ticaret Denetmeni SUNUM İÇERİĞİ TANIMLAR PİYASA GÖZETİMİ VE DENETİMİNE İLİŞKİN USUL
YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ
 9 Ocak 2007 SALI Resmî Gazete Sayı : 26398 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
9 Ocak 2007 SALI Resmî Gazete Sayı : 26398 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ. Resmi Gazete: BİRİNCİ BÖLÜM. Amaç, Kapsam, Dayanak ve Tanımlar. Amaç
 Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ Resmi Gazete:9.1.2007-26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı
Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ Resmi Gazete:9.1.2007-26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı
KISA VADE MEVZUAT UYUMU
 T.C. SAĞLIK BAKANLIĞI AVRUPA BİRLİĞİ KOORDİNASYON DAİRESİ BAŞKANLIĞI KISA VADE MEVZUAT UYUMU SAĞLIK BAKANLIĞI TARAFINDAN ULUSAL PROGRAM ÇERÇEVESİNDE GERÇEKLEŞTİRİLEN BİRİNCİ BASKI ANKARA Eylül 2002 T.C.
T.C. SAĞLIK BAKANLIĞI AVRUPA BİRLİĞİ KOORDİNASYON DAİRESİ BAŞKANLIĞI KISA VADE MEVZUAT UYUMU SAĞLIK BAKANLIĞI TARAFINDAN ULUSAL PROGRAM ÇERÇEVESİNDE GERÇEKLEŞTİRİLEN BİRİNCİ BASKI ANKARA Eylül 2002 T.C.
Tel Halatların, Zincirlerin ve Kancaların Belgelendirilmesi ve İşaretlenmesi ile İlgili Yönetmelik (73/361/AT) ( R.G 01.07.
 Tel Halatların, Zincirlerin ve Kancaların Belgelendirilmesi ve İşaretlenmesi ile İlgili Yönetmelik (73/361/AT) ( R.G 01.07.2003/25155 ) BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin
Tel Halatların, Zincirlerin ve Kancaların Belgelendirilmesi ve İşaretlenmesi ile İlgili Yönetmelik (73/361/AT) ( R.G 01.07.2003/25155 ) BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin
Yönetmelik. Sanayi ve Ticaret Bakanlığından : Ölçü ve Ölçü Aletlerinin Metrolojik Kontrolleri İçin Genel Esaslara Dair Yönetmelik (71/316/AT)
 RESMİ GAZETE tarih 03 / 06 / 2002 sayı 24774 Yönetmelik Sanayi ve Ticaret Bakanlığından : Ölçü ve Ölçü Aletlerinin Metrolojik Kontrolleri İçin Genel Esaslara Dair Yönetmelik (71/316/AT) BİRİNCİ BÖLÜM Amaç,
RESMİ GAZETE tarih 03 / 06 / 2002 sayı 24774 Yönetmelik Sanayi ve Ticaret Bakanlığından : Ölçü ve Ölçü Aletlerinin Metrolojik Kontrolleri İçin Genel Esaslara Dair Yönetmelik (71/316/AT) BİRİNCİ BÖLÜM Amaç,
Türk Gıda Kodeksi Gıda Maddeleri ile Temasta Bulunan Madde ve Malzemeler Tebliği (Tebliğ No: 2002/ 32 )
 Resmi gazete tarih sayı : 22 Nisan 2002-24734 Tarım ve Köyişleri Bakanlığı ve Sağlık Bakanlığından: Türk Gıda Kodeksi Gıda Maddeleri ile Temasta Bulunan Madde ve Malzemeler Tebliği (Tebliğ No: 2002/ 32
Resmi gazete tarih sayı : 22 Nisan 2002-24734 Tarım ve Köyişleri Bakanlığı ve Sağlık Bakanlığından: Türk Gıda Kodeksi Gıda Maddeleri ile Temasta Bulunan Madde ve Malzemeler Tebliği (Tebliğ No: 2002/ 32
TIBBİ CİHAZ YÖNETMELİĞİ. Resmi Gazete: BİRİNCİ BÖLÜM. Amaç, Kapsam, Dayanak ve Tanımlar
 TIBBİ CİHAZ YÖNETMELİĞİ Resmi Gazete:9.1.2007-26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbi
TIBBİ CİHAZ YÖNETMELİĞİ Resmi Gazete:9.1.2007-26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı; insan sağlığında doğrudan veya dolaylı olarak kullanılan tıbbi
TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM
 7 Haziran 2011 SALI Resmî Gazete YÖNETMELİK Sayı : 27957 Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı;
7 Haziran 2011 SALI Resmî Gazete YÖNETMELİK Sayı : 27957 Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı;
DOKUZ EYLÜL ÜNVERSTES MÜHENDSLK FAKÜLTES METALURJ VE MALZEME MÜHENDSL BÖLÜMÜ BTRME PROJES YÜRÜTME YÖNERGES
 BTRME PROJES YÜRÜTME YÖNERGES 1. AMAÇ ve KAPSAM Madde 1: Bitirme projesi dersinde örencilerin önceki derslerde edindikleri bilgi ve becerileri kullanarak karmak bir sistemi, sistem bileenini veya süreci
BTRME PROJES YÜRÜTME YÖNERGES 1. AMAÇ ve KAPSAM Madde 1: Bitirme projesi dersinde örencilerin önceki derslerde edindikleri bilgi ve becerileri kullanarak karmak bir sistemi, sistem bileenini veya süreci
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ HAFTA
 İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 1. HAFTA İLAÇ Hastalıkların teşhisi, tedavisi, profilaksisi (hastalıktan korunma) cerrahi girişimlerin kolaylaştırılması ve
İLAÇ, KOZMETİK ÜRÜNLER İLE TIBBİ CİHAZLARDA RUHSATLANDIRMA İŞLEMLERİ ECZ 961 1. HAFTA İLAÇ Hastalıkların teşhisi, tedavisi, profilaksisi (hastalıktan korunma) cerrahi girişimlerin kolaylaştırılması ve
BANKALARIN KRED LEMLERNE LKN YÖNETMELKTE DEKLK YAPILMASINA LKN YÖNETMELK TASLAI
 Bankacılık Düzenleme ve Denetleme Kurumundan: BANKALARIN KRED LEMLERNE LKN YÖNETMELKTE DEKLK YAPILMASINA LKN YÖNETMELK TASLAI MADDE 1 01/11/2006 tarihli ve 26333 sayılı Resmi Gazete de yayımlanarak yürürlüe
Bankacılık Düzenleme ve Denetleme Kurumundan: BANKALARIN KRED LEMLERNE LKN YÖNETMELKTE DEKLK YAPILMASINA LKN YÖNETMELK TASLAI MADDE 1 01/11/2006 tarihli ve 26333 sayılı Resmi Gazete de yayımlanarak yürürlüe
YAYINA HAZIRLAYAN ERKAN KARAARSLAN
 YAYINAHAZIRLAYAN ERKANKARAARSLAN 1 i İç Kontrol Mevzuatı ii TEMMUZ/2012 iii İç Kontrol Mevzuatı iv ÇNDEKLER 1. KAMUMALÎYÖNETMVEKONTROLKANUNU 1 2. ÇKONTROLVEÖNMALÎKONTROLELKNUSULVEESASLAR 13 3. STRATEJGELTRMEBRMLERNNÇALIMAUSULVEESASLARI
YAYINAHAZIRLAYAN ERKANKARAARSLAN 1 i İç Kontrol Mevzuatı ii TEMMUZ/2012 iii İç Kontrol Mevzuatı iv ÇNDEKLER 1. KAMUMALÎYÖNETMVEKONTROLKANUNU 1 2. ÇKONTROLVEÖNMALÎKONTROLELKNUSULVEESASLAR 13 3. STRATEJGELTRMEBRMLERNNÇALIMAUSULVEESASLARI
SU ÜRÜNLERİ YETİŞTİRİCİLİĞİ YÖNETMELİĞİ
 SU ÜRÜNLERİ YETİŞTİRİCİLİĞİ YÖNETMELİĞİ Organik Su Ürünleri Yetiştiriciliği Madde 16 - Organik su ürünleri yetiştiriciliği projeleri ile ilgili işlemler bu Yönetmeliğin ilgili maddelerine uygun olarak
SU ÜRÜNLERİ YETİŞTİRİCİLİĞİ YÖNETMELİĞİ Organik Su Ürünleri Yetiştiriciliği Madde 16 - Organik su ürünleri yetiştiriciliği projeleri ile ilgili işlemler bu Yönetmeliğin ilgili maddelerine uygun olarak
TIPTA TEDAVİ AMACIYLA KULLANILAN İYONLAŞTIRICI RADYASYON KAYNAKLARINI İÇEREN TESİSLERE LİSANS VERME YÖNETMELİĞİ
 TIPTA TEDAVİ AMACIYLA KULLANILAN İYONLAŞTIRICI RADYASYON KAYNAKLARINI İÇEREN TESİSLERE LİSANS VERME YÖNETMELİĞİ Resmi Gazete Tarih/Sayı: 21.07.1996/21997 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak,Tanımlar Amaç
TIPTA TEDAVİ AMACIYLA KULLANILAN İYONLAŞTIRICI RADYASYON KAYNAKLARINI İÇEREN TESİSLERE LİSANS VERME YÖNETMELİĞİ Resmi Gazete Tarih/Sayı: 21.07.1996/21997 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak,Tanımlar Amaç
KİŞİSEL KORUYUCU DONANIMLARIN İŞYERLERİNDE KULLANILMASI HAKKINDA YÖNETMELİK
 KİŞİSEL KORUYUCU DONANIMLARIN İŞYERLERİNDE KULLANILMASI HAKKINDA YÖNETMELİK BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı, işyerindeki risklerin önlenmesinin veya
KİŞİSEL KORUYUCU DONANIMLARIN İŞYERLERİNDE KULLANILMASI HAKKINDA YÖNETMELİK BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı, işyerindeki risklerin önlenmesinin veya
YÖNETMELİK. R.G. Tarihi: 09.01.2007 R.G. Sayısı: 26398
 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ R.G. Tarihi: 09.01.2007 R.G. Sayısı: 26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ R.G. Tarihi: 09.01.2007 R.G. Sayısı: 26398 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı; insan sağlığında
Makina Emniyeti Yönetmelii (98/37/AT)
 Sanayi ve Ticaret Bakanlndan: Makina Emniyeti Yönetmelii (98/37/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak ve Tan(mlar Amaç Madde 1- Bu Yönetmeliin amac, gerektii gibi kurulduunda, bakm yapldnda ve kendinden
Sanayi ve Ticaret Bakanlndan: Makina Emniyeti Yönetmelii (98/37/AT) BRNC BÖLÜM Amaç, Kapsam, Dayanak ve Tan(mlar Amaç Madde 1- Bu Yönetmeliin amac, gerektii gibi kurulduunda, bakm yapldnda ve kendinden
SOSYAL GÜVENLK KURMUNUN YAPISI VE LEY. Sosyal Güvenlik Kurumu Bakanl Strateji Gelitirme Bakan Ahmet AÇIKGÖZ
 SOSYAL GÜVENLK KURMUNUN YAPISI VE LEY Sosyal Güvenlik Kurumu Bakanl Strateji Gelitirme Bakan Ahmet AÇIKGÖZ KURUMUN AMACI ve GÖREVLER' Sosyal sigortalar ile genel salk sigortas bakmndan kiileri güvence
SOSYAL GÜVENLK KURMUNUN YAPISI VE LEY Sosyal Güvenlik Kurumu Bakanl Strateji Gelitirme Bakan Ahmet AÇIKGÖZ KURUMUN AMACI ve GÖREVLER' Sosyal sigortalar ile genel salk sigortas bakmndan kiileri güvence
ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN
 8027 ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı R. Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur
8027 ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı R. Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur
Mali Yönetim ve Denetim Dergisinin May s-haziran 2008 tarihli 50. say nda yay nlanm r.
 HURDAYA AYRILAN VARLIKLARIN MUHASEBELELMELER VE YAPILAN YANLILIKLAR Ömer DA Devlet Muhasebe Uzman info@omerdag.net 1.G Kamu idarelerinin kaytlarnda bulunan tarlar ile maddi duran varlklar doalar gerei
HURDAYA AYRILAN VARLIKLARIN MUHASEBELELMELER VE YAPILAN YANLILIKLAR Ömer DA Devlet Muhasebe Uzman info@omerdag.net 1.G Kamu idarelerinin kaytlarnda bulunan tarlar ile maddi duran varlklar doalar gerei
ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN
 8027 ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı Resmî Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur
8027 ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı Resmî Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur
2012 2013 E T M ve Ö RET M YILI ÖRGÜN ve YAYGIN E T M KURUMLARI ÇALI MA TAKV M
 2012 2013 ETM ve ÖRETM YILI ÖRGÜN ve YAYGIN ETM KURUMLARI ÇALIMA TAKVM SIRA NO ÇALIMA KONULARI TARH 1. Okul Öncesi Ve lköretim Okullar 1. Snf Örencilerinin Eitim- Öretime Hazrlanmalar ( Bamsz Anaokullar
2012 2013 ETM ve ÖRETM YILI ÖRGÜN ve YAYGIN ETM KURUMLARI ÇALIMA TAKVM SIRA NO ÇALIMA KONULARI TARH 1. Okul Öncesi Ve lköretim Okullar 1. Snf Örencilerinin Eitim- Öretime Hazrlanmalar ( Bamsz Anaokullar
T.C. İZMİR VALİLİĞİ ALİAĞA İLÇE MİLLÎ EĞİTİM MÜDÜRLÜĞÜ HİZMET STANDARTLARI. Sıra Hizmet Standardı Olan Birimler Sayı
 T.C. İZMİR VALİLİĞİ ALİAĞA İLÇE MİLLÎ EĞİTİM MÜDÜRLÜĞÜ HİZMET STANDARTLARI Sıra Hizmet Standardı Olan Birimler Sayı 1 Özel Öğretim Kurumları Bölümü 92 2 Atama Bölümü 1 3 Basın Yayın Bölümü 4 4 Eğitim Öğretim
T.C. İZMİR VALİLİĞİ ALİAĞA İLÇE MİLLÎ EĞİTİM MÜDÜRLÜĞÜ HİZMET STANDARTLARI Sıra Hizmet Standardı Olan Birimler Sayı 1 Özel Öğretim Kurumları Bölümü 92 2 Atama Bölümü 1 3 Basın Yayın Bölümü 4 4 Eğitim Öğretim
ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN
 ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı R. Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur : Tertip
ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN Kanun Numarası : 4703 Kabul Tarihi : 29/6/2001 Yayımlandığı R. Gazete : Tarih : 11/7/2001 Sayı : 24459 Yayımlandığı Düstur : Tertip
Kamu Görevlileri Sendikalar Kanunu Kapsamna Giren Kurum ve Kurulularn Girdikleri Hizmet Kollarnn Belirlenmesine likin Yönetmelik
 Kamu Görevlileri Sendikalar Kanunu Kapsamna Giren Kurum ve Kurulularn Girdikleri Hizmet Kollarnn Belirlenmesine likin Yönetmelik Resmi Gazete Tarih ve Says: 07.09.2001-24516 BRNC BÖLÜM Amaç, Kapsam, Dayanak
Kamu Görevlileri Sendikalar Kanunu Kapsamna Giren Kurum ve Kurulularn Girdikleri Hizmet Kollarnn Belirlenmesine likin Yönetmelik Resmi Gazete Tarih ve Says: 07.09.2001-24516 BRNC BÖLÜM Amaç, Kapsam, Dayanak
TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM. Amaç, Kapsam, Dayanak ve Tanımlar
 Resmi Gazete Tarihi: 07.06.2011 Resmi Gazete Sayısı: 27957 TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı; tıbbi cihaz ve aksesuarlarının
Resmi Gazete Tarihi: 07.06.2011 Resmi Gazete Sayısı: 27957 TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı; tıbbi cihaz ve aksesuarlarının
T.C. SAĞLIK BAKANLIĞI
 T.C. SAĞLIK BAKANLIĞI TEMEL SAĞLIK HİZMETLERİ GENEL MÜDÜRLÜĞÜ Piyasa Gözetimi, Denetimi ve Temizlik Ürünleri Şubesi Oyuncak Mayıs 2012 Oyuncaklar Hakkında Yönetmelik 17.05.2002 tarihli ve 24758 sayılı
T.C. SAĞLIK BAKANLIĞI TEMEL SAĞLIK HİZMETLERİ GENEL MÜDÜRLÜĞÜ Piyasa Gözetimi, Denetimi ve Temizlik Ürünleri Şubesi Oyuncak Mayıs 2012 Oyuncaklar Hakkında Yönetmelik 17.05.2002 tarihli ve 24758 sayılı
T.C KÜLTÜR VE TURZM BAKANLII Strateji Gelitirme Bakanl!"! (1. sayfa) ZEYLNAME
 (1. sayfa) ZEYLNAME Türkiye Kültür Portal! Altyap!s!n!n Oluturulmas! ve Portal Uygulama Yaz!l!mlar!n!n Temin Edilmesi ihalesi 03/07/2009 Cuma gününe ertelenmitir. Teknik :artnamenin 6.(2). Maddesi Portal
(1. sayfa) ZEYLNAME Türkiye Kültür Portal! Altyap!s!n!n Oluturulmas! ve Portal Uygulama Yaz!l!mlar!n!n Temin Edilmesi ihalesi 03/07/2009 Cuma gününe ertelenmitir. Teknik :artnamenin 6.(2). Maddesi Portal
"GDO Yönetmeliði" tamam:gdo'suza GDO'suz demek yasak!.
 "GDO Yönetmeliði" tamam:gdo'suza GDO'suz demek yasak!. GDO Yönetmeliði Resmi Gazete de yayýnlandý. Üreticileri ve tüketicileri büyük tehdit altýna sokacak yönetmenliði yayýnlýyoruz. Tarým ve Köyiþleri
"GDO Yönetmeliði" tamam:gdo'suza GDO'suz demek yasak!. GDO Yönetmeliði Resmi Gazete de yayýnlandý. Üreticileri ve tüketicileri büyük tehdit altýna sokacak yönetmenliði yayýnlýyoruz. Tarým ve Köyiþleri
TEBLİĞ SAĞLIK BAKANLIĞININ ÖZEL İZNİNE TABİ MADDELERİN İTHALAT DENETİMİ TEBLİĞİ (ÜRÜN GÜVENLİĞİ VE DENETİMİ: 2017/4)
 30 Aralık 2016 CUMA Resmî Gazete Sayı : 29934 (Mükerrer) Ekonomi Bakanlığından: TEBLİĞ SAĞLIK BAKANLIĞININ ÖZEL İZNİNE TABİ MADDELERİN İTHALAT DENETİMİ TEBLİĞİ (ÜRÜN GÜVENLİĞİ VE DENETİMİ: 2017/4) Amaç
30 Aralık 2016 CUMA Resmî Gazete Sayı : 29934 (Mükerrer) Ekonomi Bakanlığından: TEBLİĞ SAĞLIK BAKANLIĞININ ÖZEL İZNİNE TABİ MADDELERİN İTHALAT DENETİMİ TEBLİĞİ (ÜRÜN GÜVENLİĞİ VE DENETİMİ: 2017/4) Amaç
Türkiye de özel sa l k kurulu lar nda bir tutundurma faaliyeti olarak reklam n hukuki boyutu üzerine bir ara t rma
 ABMYO Dergisi. 23, (2011) (99-108) Türkiye de özel salk kurulularnda bir tutundurma faaliyeti olarak reklamn hukuki boyutu üzerine bir aratrma Özet 1 stanbul Aydn Üniversitesi, Sosyal Bilimler Enstitüsü,
ABMYO Dergisi. 23, (2011) (99-108) Türkiye de özel salk kurulularnda bir tutundurma faaliyeti olarak reklamn hukuki boyutu üzerine bir aratrma Özet 1 stanbul Aydn Üniversitesi, Sosyal Bilimler Enstitüsü,
YÖNETMELİK. MADDE 2 (1) Bu Yönetmelik kamu, üniversite ve özel sektör ikinci ve üçüncü basamak sağlık kurumlarını kapsar.
 6 Nisan 2011 ÇARŞAMBA Resmî Gazete Sayı : 27897 Sağlık Bakanlığından: YÖNETMELİK HASTA VE ÇALIŞAN GÜVENLİĞİNİN SAĞLANMASINA DAİR YÖNETMELİK BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1
6 Nisan 2011 ÇARŞAMBA Resmî Gazete Sayı : 27897 Sağlık Bakanlığından: YÖNETMELİK HASTA VE ÇALIŞAN GÜVENLİĞİNİN SAĞLANMASINA DAİR YÖNETMELİK BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1
IN VITRO TIBBİ TANI CİHAZLARI YÖNETMELİĞİ. Resmi Gazete Tarihi: 14/10/2003. Resmi Gazete Sayısı: Sağlık Bakanlığından BİRİNCİ BÖLÜM
 IN VITRO TIBBİ TANI CİHAZLARI YÖNETMELİĞİ Resmi Gazete Tarihi: 14/10/2003 Resmi Gazete Sayısı: 25259 Sağlık Bakanlığından BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 -Bu Yönetmeliğin
IN VITRO TIBBİ TANI CİHAZLARI YÖNETMELİĞİ Resmi Gazete Tarihi: 14/10/2003 Resmi Gazete Sayısı: 25259 Sağlık Bakanlığından BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 -Bu Yönetmeliğin
TÜRK GIDA KODEKSİ YÖNETMELİĞİ. BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar
 Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1- (1) Bu Yönetmeliğin amacı; gıda ve gıda ile temas eden madde ve malzemelere
Gıda, Tarım ve Hayvancılık Bakanlığından: TÜRK GIDA KODEKSİ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1- (1) Bu Yönetmeliğin amacı; gıda ve gıda ile temas eden madde ve malzemelere
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU HİZMET SUNUMUNDA YER ALAN KOZMETİK ÜRÜNLERE İLİŞKİN KILAVUZ
 TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU HİZMET SUNUMUNDA YER ALAN KOZMETİK ÜRÜNLERE İLİŞKİN KILAVUZ Amaç MADDE 1-24.03.2005 tarihli ve 5324 sayılı Kozmetik Kanunu ile bu Kanuna istinaden hazırlanan ve 23.05.2005
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU HİZMET SUNUMUNDA YER ALAN KOZMETİK ÜRÜNLERE İLİŞKİN KILAVUZ Amaç MADDE 1-24.03.2005 tarihli ve 5324 sayılı Kozmetik Kanunu ile bu Kanuna istinaden hazırlanan ve 23.05.2005
Sanayi ve Ticaret Bakanlıından: Sanayi Mallarının Satı Sonrası Hizmetleri Hakkında Yönetmelik Amaç Madde 1 Bu Yönetmeliin amacı, ekli listede yer
 Sanayi ve Ticaret Bakanlıından: Sanayi Mallarının Satı Sonrası Hizmetleri Hakkında Yönetmelik Amaç Madde 1 Bu Yönetmeliin amacı, ekli listede yer alan malların kullanım ömürleri ile satı sonrası montaj,
Sanayi ve Ticaret Bakanlıından: Sanayi Mallarının Satı Sonrası Hizmetleri Hakkında Yönetmelik Amaç Madde 1 Bu Yönetmeliin amacı, ekli listede yer alan malların kullanım ömürleri ile satı sonrası montaj,
T.C. YALOVA ÜNİVERSİTESİ Strateji Geliştirme Daire Başkanlığı. İÇ KONTROL ve RİSK YÖNETİMİ 1 İÇ İÇ KONTROL
 T.C. YALOVA ÜNİVERSİTESİ Strateji Geliştirme Daire Başkanlğ İÇ KONTROL ve RİSK YÖNETİMİ 1 İÇ İÇ KONTROL EYLÜL 2015 1-) İç Kontrol Nedir? Üniversite varlklarnn korunmas, kurumsal ve yasal düzenlemelere
T.C. YALOVA ÜNİVERSİTESİ Strateji Geliştirme Daire Başkanlğ İÇ KONTROL ve RİSK YÖNETİMİ 1 İÇ İÇ KONTROL EYLÜL 2015 1-) İç Kontrol Nedir? Üniversite varlklarnn korunmas, kurumsal ve yasal düzenlemelere
T.C. M LLÎ E T M BAKANLI I Talim ve Terbiye Kurulu Ba kanl YANGIN E T M KURS PROGRAMI
 T.C. MLLÎ ETM BAKANLII Talim ve Terbiye Kurulu Bakanl YANGIN ETM KURS PROGRAMI ANKARA 2012 1 KURUMUN ADRES : KURUCUSUNUN ADI : PROGRAMIN ADI : Yangn Eitimi Kurs Program PROGRAMIN DAYANAI : 5580 sayl Özel
T.C. MLLÎ ETM BAKANLII Talim ve Terbiye Kurulu Bakanl YANGIN ETM KURS PROGRAMI ANKARA 2012 1 KURUMUN ADRES : KURUCUSUNUN ADI : PROGRAMIN ADI : Yangn Eitimi Kurs Program PROGRAMIN DAYANAI : 5580 sayl Özel
Vücuda Yerleştirilebilir Aktif Tıbbî Cihazlar Yönetmeliği
 Vücuda Yerleştirilebilir Aktif Tıbbî Cihazlar Yönetmeliği R.G.Tarihi: 12.03.2002 R.G.Sayısı: 24693 BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında
Vücuda Yerleştirilebilir Aktif Tıbbî Cihazlar Yönetmeliği R.G.Tarihi: 12.03.2002 R.G.Sayısı: 24693 BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği
 Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği Tarih: 14.10.2003 Sayı: 25259 BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; vücut dışında (in-vitro)
Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği Tarih: 14.10.2003 Sayı: 25259 BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; vücut dışında (in-vitro)
Yönetmelikler Devlet Bakanlığından : Teknik Mevzuatın ve Standartların Türkiye ile Avrupa Birliği Arasında Bildirimine Dair Yönetmelik BİRİNCİ BÖLÜM
 Yönetmelikler Devlet Bakanlığından : Teknik Mevzuatın ve Standartların Türkiye ile Avrupa Birliği Arasında Bildirimine Dair Yönetmelik BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanımlar Amaç Madde 1
Yönetmelikler Devlet Bakanlığından : Teknik Mevzuatın ve Standartların Türkiye ile Avrupa Birliği Arasında Bildirimine Dair Yönetmelik BİRİNCİ BÖLÜM Amaç, Kapsam, Hukuki Dayanak, Tanımlar Amaç Madde 1
4703 SAYILI, ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN
 4703 SAYILI, ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN (11.7.2001 Tarih ve 24459 Sayılı Resmi Gazetede yayımlanmış olup; 11.1. 2002 tarihinde yürürlüğe girmiştir) Amaç
4703 SAYILI, ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN (11.7.2001 Tarih ve 24459 Sayılı Resmi Gazetede yayımlanmış olup; 11.1. 2002 tarihinde yürürlüğe girmiştir) Amaç
4703 Sayılı Ürünlere İlişkin Teknik Mevzuatın Hazırlanması ve Uygulanmasına Dair Kanun
 4703 Sayılı Ürünlere İlişkin Teknik Mevzuatın Hazırlanması ve Uygulanmasına Dair Kanun BİRİNCİ BÖLÜM Amaç, Kapsam ve Tanımlar Amaç Madde 1-Bu Kanunun amacı; ürünlerin piyasaya arzı, uygunluk değerlendirmesi,
4703 Sayılı Ürünlere İlişkin Teknik Mevzuatın Hazırlanması ve Uygulanmasına Dair Kanun BİRİNCİ BÖLÜM Amaç, Kapsam ve Tanımlar Amaç Madde 1-Bu Kanunun amacı; ürünlerin piyasaya arzı, uygunluk değerlendirmesi,
DOAL GAZ PYASASI KANUNU (ELEKTRK PYASASI KANUNUNDA DEKLK YAPILMASI VE DOAL GAZ PYASASI HAKKINDA KANUN)
 DOAL GAZ PYASASI KANUNU (ELEKTRK PYASASI KANUNUNDA DEKLK YAPILMASI VE DOAL GAZ PYASASI HAKKINDA KANUN) Kanun No. : 4646 Kabul Tarihi : 18/4/2001 Yay&m Tarihi : 2/5/2001 tarih ve 24390 Sayl Resmi Gazete
DOAL GAZ PYASASI KANUNU (ELEKTRK PYASASI KANUNUNDA DEKLK YAPILMASI VE DOAL GAZ PYASASI HAKKINDA KANUN) Kanun No. : 4646 Kabul Tarihi : 18/4/2001 Yay&m Tarihi : 2/5/2001 tarih ve 24390 Sayl Resmi Gazete
Madde 3 Bu Yönetmelik, 4857 sayılı İş Kanununun 78 inci maddesine göre düzenlenmiştir.
 TİTREŞİM YÖNETMELİĞİ Resmi Gazete: 23 Aralık 2003-25325 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı, işçilerin mekanik titreşime maruz kalmaları sonucu ortaya çıkabilecek
TİTREŞİM YÖNETMELİĞİ Resmi Gazete: 23 Aralık 2003-25325 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı, işçilerin mekanik titreşime maruz kalmaları sonucu ortaya çıkabilecek
cerrahi bir müdahale ile insan vücuduna, doğal bir vücut girişine veya boşluğuna yerleştirilen ve yerleştirildiği yerde kalması gereken aktif tıbbî ci
 Vücuda Yerleştirilebilir Aktif Tıbbî Cihazlar Yönetmeliği R.G. Tarihi:12.03.2002 R.G. Sayısı:24693 Sağlık Bakanlığından: BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin
Vücuda Yerleştirilebilir Aktif Tıbbî Cihazlar Yönetmeliği R.G. Tarihi:12.03.2002 R.G. Sayısı:24693 Sağlık Bakanlığından: BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1- Bu Yönetmeliğin
Bilecik İli Kamu Hastaneleri Birliği Genel Sekreterliği Mali Hizmetler Başkanlığı Klinik Mühendislik Hizmetleri Birimi
 Amaç: SAĞLIK TESİSLERİNİN TIBBİ CİHAZLAR PIYASA GÖZETİM VE DENETİM (PGD) VE OLUMSUZ OLAY BİLDİRİMİNE İLİŞKİN TALİMAT (Rev.2) Genel Sekreterliğimize bağlı sağlık tesislerinde kullanılan tıbbi cihazlara
Amaç: SAĞLIK TESİSLERİNİN TIBBİ CİHAZLAR PIYASA GÖZETİM VE DENETİM (PGD) VE OLUMSUZ OLAY BİLDİRİMİNE İLİŞKİN TALİMAT (Rev.2) Genel Sekreterliğimize bağlı sağlık tesislerinde kullanılan tıbbi cihazlara
SONRADAN KONTROL VE RİSKLİ İŞLEMLERİN KONTROLÜ YÖNETMELİĞİ
 SONRADAN KONTROL VE RİSKLİ İŞLEMLERİN KONTROLÜ YÖNETMELİĞİ Başbakanlık (Gümrük Müsteşarlığı) tan:27.10.2008 tarih ve 27037 sayılı R.G. Amaç BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar MADDE 1 (1) Bu
SONRADAN KONTROL VE RİSKLİ İŞLEMLERİN KONTROLÜ YÖNETMELİĞİ Başbakanlık (Gümrük Müsteşarlığı) tan:27.10.2008 tarih ve 27037 sayılı R.G. Amaç BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar MADDE 1 (1) Bu
RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ
 Türkiye Atom Enerjisi Kurumundan: RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ Resmi Gazete: 31.7.2010-27658 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 -(1) Bu Yönetmeliğin
Türkiye Atom Enerjisi Kurumundan: RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ Resmi Gazete: 31.7.2010-27658 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 -(1) Bu Yönetmeliğin
Resmi Gazete: Salı, Sayı: (Asıl)
 Titreşim Yönetmeliği Resmi Gazete:23.12.2003 Salı, Sayı: 25325 (Asıl) Çalışma ve Sosyal Güvenlik Bakanlığından: BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı, işçilerin
Titreşim Yönetmeliği Resmi Gazete:23.12.2003 Salı, Sayı: 25325 (Asıl) Çalışma ve Sosyal Güvenlik Bakanlığından: BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı, işçilerin
MADDE 2 (1) Bu Yönetmelik, gıdaların mikrobiyolojik kriterleri ile gıda işletmecilerinin uyması ve uygulaması gereken kuralları kapsar.
 TÜRK GIDA KODEKSİ MİKROBİYOLOJİK KRİTERLER YÖNETMELİĞİ Yetki Kanunu: 5996 Yayımlandığı R.Gazete: 29.12.2011-28157 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı;
TÜRK GIDA KODEKSİ MİKROBİYOLOJİK KRİTERLER YÖNETMELİĞİ Yetki Kanunu: 5996 Yayımlandığı R.Gazete: 29.12.2011-28157 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı;
Konu : Sağlık Bakanlığının Özel İznine Tabi Maddelerin İthalat Denetimi Tebliği (Ürün Güvenliği ve Denetimi: 2017/4) hk.
 Ankara, 30 Aralık 2016, Cuma Sirküler 2016 / 447 Konu : Sağlık Bakanlığının Özel İznine Tabi Maddelerin İthalat Denetimi Tebliği (Ürün Güvenliği ve Denetimi: 2017/4) hk. Sayın Üyemiz; 30 Aralık 2016 Tarihli
Ankara, 30 Aralık 2016, Cuma Sirküler 2016 / 447 Konu : Sağlık Bakanlığının Özel İznine Tabi Maddelerin İthalat Denetimi Tebliği (Ürün Güvenliği ve Denetimi: 2017/4) hk. Sayın Üyemiz; 30 Aralık 2016 Tarihli
VÜCUDA YERLEŞTİRİLEBİLİR AKTİF TIBBİ CİHAZLAR YÖNETMELİĞİ
 VÜCUDA YERLEŞTİRİLEBİLİR AKTİF TIBBİ CİHAZLAR YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında kullanılan vücuda yerleştirilebilir
VÜCUDA YERLEŞTİRİLEBİLİR AKTİF TIBBİ CİHAZLAR YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; insan sağlığında kullanılan vücuda yerleştirilebilir
TGK-ÖZEL TIBBĐ AMAÇLI DĐYET GIDALAR TEBLĐĞĐ (Tebliğ No: 2001/42) (R.G /24620)
 TGK-ÖZEL TIBBĐ AMAÇLI DĐYET GIDALAR TEBLĐĞĐ (Tebliğ No: 2001/42) (R.G. 24.12.2001/24620) Değişiklik :Yayımlandığı R.Gazete 31.08.2003-25215 Amaç Madde 1 Bu Tebliğin amacı, özel tıbbi amaçlı diyet gıdaların
TGK-ÖZEL TIBBĐ AMAÇLI DĐYET GIDALAR TEBLĐĞĐ (Tebliğ No: 2001/42) (R.G. 24.12.2001/24620) Değişiklik :Yayımlandığı R.Gazete 31.08.2003-25215 Amaç Madde 1 Bu Tebliğin amacı, özel tıbbi amaçlı diyet gıdaların
tarih ve sayılı Resmi Gazetede yayınlanan Yönetmelik ile
 5.7.2012 tarih ve 28344 sayılı Resmi Gazetede yayınlanan Yönetmelik ile YÜRÜRLÜKTEN KALDIRILMIŞTIR. Sağlık Bakanlığından: KAMU SAĞLIK HİZMETLERİNDE İYONLAŞTIRICI RADYASYON KAYNAKLARI İLE ÇALIŞAN PERSONELİN
5.7.2012 tarih ve 28344 sayılı Resmi Gazetede yayınlanan Yönetmelik ile YÜRÜRLÜKTEN KALDIRILMIŞTIR. Sağlık Bakanlığından: KAMU SAĞLIK HİZMETLERİNDE İYONLAŞTIRICI RADYASYON KAYNAKLARI İLE ÇALIŞAN PERSONELİN
Bu maddenin yürürlüe girdii tarih itibarıyla bu Kanuna göre kurulan serbest bölgelerde faaliyette bulunmak üzere ruhsat almı mükelleflerin;
 ! "! # $% & % & ' &! ' ( )* +$' #,*,-. / - Gecici Madde 3 Bu maddenin yürürlüe girdii tarih itibarıyla bu Kanuna göre kurulan serbest bölgelerde faaliyette bulunmak üzere ruhsat almı mükelleflerin; a)
! "! # $% & % & ' &! ' ( )* +$' #,*,-. / - Gecici Madde 3 Bu maddenin yürürlüe girdii tarih itibarıyla bu Kanuna göre kurulan serbest bölgelerde faaliyette bulunmak üzere ruhsat almı mükelleflerin; a)
BÜLTEN. KONU: Mükelleflerin zahat (Özelge) Taleplerinin Cevaplandırılmasına Dair Yönetmelik Yayınlanmıtır.
 Kültür Mah. 1375 Sk. No:25 Cumhuruiyet hanı K:5 35210 Alsancak - zmir-turkey Tel : + 90 232 464 16 16.. Fax: + 90 232 421 71 92. e-mail : info@psdisticaret.com..tr BÜLTEN SAYI :2010-044 Tarih: 31.08.2010
Kültür Mah. 1375 Sk. No:25 Cumhuruiyet hanı K:5 35210 Alsancak - zmir-turkey Tel : + 90 232 464 16 16.. Fax: + 90 232 421 71 92. e-mail : info@psdisticaret.com..tr BÜLTEN SAYI :2010-044 Tarih: 31.08.2010
YÖNETMELİK ÇALIŞANLARIN TİTREŞİMLE İLGİLİ RİSKLERDEN KORUNMALARINA DAİR YÖNETMELİK. BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar
 22 Ağustos 2013 PERŞEMBE Resmî Gazete Sayı : 28743 Çalışma ve Sosyal Güvenlik Bakanlığından: YÖNETMELİK ÇALIŞANLARIN TİTREŞİMLE İLGİLİ RİSKLERDEN KORUNMALARINA DAİR YÖNETMELİK Amaç BİRİNCİ BÖLÜM Amaç,
22 Ağustos 2013 PERŞEMBE Resmî Gazete Sayı : 28743 Çalışma ve Sosyal Güvenlik Bakanlığından: YÖNETMELİK ÇALIŞANLARIN TİTREŞİMLE İLGİLİ RİSKLERDEN KORUNMALARINA DAİR YÖNETMELİK Amaç BİRİNCİ BÖLÜM Amaç,
Tıbbi Cihazlarda Klinik Araştırmalar ve Yeni Gereklilikler IPTS Dr. Ali Sait SEPTİOĞLU
 Tıbbi Cihazlarda Klinik Araştırmalar ve Yeni Gereklilikler IPTS 2016 Dr. Ali Sait SEPTİOĞLU Sağlık Sektörü Sağlık Hizmeti Sunumunda Bileşenler Tıbbi gereçler Vücuda yerleştirilebilir aktif tıbbi cihazlar,
Tıbbi Cihazlarda Klinik Araştırmalar ve Yeni Gereklilikler IPTS 2016 Dr. Ali Sait SEPTİOĞLU Sağlık Sektörü Sağlık Hizmeti Sunumunda Bileşenler Tıbbi gereçler Vücuda yerleştirilebilir aktif tıbbi cihazlar,
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ
 TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ Amaç MADDE 1- Kozmetik ürünlerin üreticileri tarafından raf ömürleri belirlenirken
TÜRKİYE İLAÇ VE TIBBİ CİHAZ KURUMU KOZMETİK ÜRÜNLERİN STABİLİTESİNE VE AÇILDIKTAN SONRA KULLANIM SÜRESİNE İLİŞKİN KILAVUZ Amaç MADDE 1- Kozmetik ürünlerin üreticileri tarafından raf ömürleri belirlenirken
Biyosidal Ürün Üretim Yerleri Mevzuatı ve Kaliteye Katkısı. Dr. Hüseyin İLTER Daire Başkanı
 Biyosidal Ürün Üretim Yerleri Mevzuatı ve Kaliteye Katkısı Dr. Hüseyin İLTER Daire Başkanı İÇERİK İmalat Tesisi, Birimleri ve Genel Özellikleri Dokümantasyon, Personel Eğitimi ve Sağlık Kontrolü İmalat
Biyosidal Ürün Üretim Yerleri Mevzuatı ve Kaliteye Katkısı Dr. Hüseyin İLTER Daire Başkanı İÇERİK İmalat Tesisi, Birimleri ve Genel Özellikleri Dokümantasyon, Personel Eğitimi ve Sağlık Kontrolü İmalat
Kanun. Svlatrlm Petrol Gazlar (LPG) Piyasas Kanunu ve Elektrik Piyasas Kanununda Deiiklik Yaplmasna Dair Kanun
 Kanun Svlatrlm Petrol Gazlar (LPG) Piyasas Kanunu ve Elektrik Piyasas Kanununda Deiiklik Yaplmasna Dair Kanun Kanun No. 5307 Kabul Tarihi : 2.3.2005 BRNC KISIM Genel Hükümler BRNC BÖLÜM Amaç, Kapsam ve
Kanun Svlatrlm Petrol Gazlar (LPG) Piyasas Kanunu ve Elektrik Piyasas Kanununda Deiiklik Yaplmasna Dair Kanun Kanun No. 5307 Kabul Tarihi : 2.3.2005 BRNC KISIM Genel Hükümler BRNC BÖLÜM Amaç, Kapsam ve
4703 sayılı ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN. (11/07/2001 tarihli ve 24459 sayılı Resmi Gazete)
 4703 sayılı ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN (11/07/2001 tarihli ve 24459 sayılı Resmi Gazete) BİRİNCİ BÖLÜM Amaç, Kapsam ve Tanımlar Amaç MADDE 1- Bu Kanunun
4703 sayılı ÜRÜNLERE İLİŞKİN TEKNİK MEVZUATIN HAZIRLANMASI VE UYGULANMASINA DAİR KANUN (11/07/2001 tarihli ve 24459 sayılı Resmi Gazete) BİRİNCİ BÖLÜM Amaç, Kapsam ve Tanımlar Amaç MADDE 1- Bu Kanunun
YÖNETMELİK. Türkiye Atom Enerjisi Kurumundan: RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ
 YÖNETMELİK Türkiye Atom Enerjisi Kurumundan: RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı, radyasyon
YÖNETMELİK Türkiye Atom Enerjisi Kurumundan: RADYASYON GÜVENLİĞİ DENETİMLERİ VE YAPTIRIMLARI YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 (1) Bu Yönetmeliğin amacı, radyasyon
BÜLTEN Tarih: 02.06.2008
 Kültür Mah. 1375 Sk. No:25 Cumhuruiyet hanı K:5 35210 Alsancak - zmir-turkey Tel : + 90 232 464 16 16.. Fax: + 90 232 421 71 92. e-mail : info@psdisticaret.com..tr BÜLTEN Tarih: 02.06.2008 SAYI :2008-046
Kültür Mah. 1375 Sk. No:25 Cumhuruiyet hanı K:5 35210 Alsancak - zmir-turkey Tel : + 90 232 464 16 16.. Fax: + 90 232 421 71 92. e-mail : info@psdisticaret.com..tr BÜLTEN Tarih: 02.06.2008 SAYI :2008-046
EGE ÜNİVERSİTESİ TEHLİKELİ ATIK YÖNERGESİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar
 Amaç EGE ÜNİVERSİTESİ TEHLİKELİ ATIK YÖNERGESİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Madde 1- Bu Yönergenin amacı, Ege Üniversitesi Rektörlüğü sorumluluk alanı içinde bulunan eğitim, öğretim,
Amaç EGE ÜNİVERSİTESİ TEHLİKELİ ATIK YÖNERGESİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Madde 1- Bu Yönergenin amacı, Ege Üniversitesi Rektörlüğü sorumluluk alanı içinde bulunan eğitim, öğretim,
! "#$%& " !"# "# $ % &' ()%%*+,#-.,# % /# #0/.0&/ 1 %. '%% & &%%'% /!2!0 #
 ! "#$%& " '(! "#$%& "!"#!"# "# $ % &' ()%%*+,#-.,# % /# #0/.0&/ 1 %. '%% & &%%'% /!2!0 # )*+ $, "- (.,/ 0..1)2#$,# &%& 0! #. # #. &&/& %# -$ 1. $.1 3 - ' # % # 1/% & & 2%% &#&&% '% /!2% &%&& #,# '%' #
! "#$%& " '(! "#$%& "!"#!"# "# $ % &' ()%%*+,#-.,# % /# #0/.0&/ 1 %. '%% & &%%'% /!2!0 # )*+ $, "- (.,/ 0..1)2#$,# &%& 0! #. # #. &&/& %# -$ 1. $.1 3 - ' # % # 1/% & & 2%% &#&&% '% /!2% &%&& #,# '%' #
ELEKTRK MÜHENDSLER ODASI MESLEK Ç SÜREKL ETM MERKEZ YÖNETMEL
 ELEKTRK MÜHENDSLER ODASI MESLEK Ç SÜREKL ETM MERKEZ YÖNETMEL Amaç Madde 1: Bu Yönetmeliin amacı; meslekteki bilimsel, teknolojik gelimelerle ve uygulama alanları ile ilgili olarak Üye Mühendislere verilecek
ELEKTRK MÜHENDSLER ODASI MESLEK Ç SÜREKL ETM MERKEZ YÖNETMEL Amaç Madde 1: Bu Yönetmeliin amacı; meslekteki bilimsel, teknolojik gelimelerle ve uygulama alanları ile ilgili olarak Üye Mühendislere verilecek
YÖNETMELİK Sanayi ve Ticaret Bakanlığından: SANAYİ VE TİCARET BAKANLIĞI PİYASA GÖZETİMİ VE DENETİMİ YÖNETMELİĞİ
 16 Mays 2008 CUM Resmî Gazete Say : 26878 YÖNETMELİK Sanayi ve Ticaret Bakanlğndan: SNYİ VE TİCRET BKNLIĞI PİYS GÖZETİMİ VE DENETİMİ YÖNETMELİĞİ BİRİNCİ BÖLÜM maç Kapsam Dayanak ve Tanmlar maç MDDE 1 (1)
16 Mays 2008 CUM Resmî Gazete Say : 26878 YÖNETMELİK Sanayi ve Ticaret Bakanlğndan: SNYİ VE TİCRET BKNLIĞI PİYS GÖZETİMİ VE DENETİMİ YÖNETMELİĞİ BİRİNCİ BÖLÜM maç Kapsam Dayanak ve Tanmlar maç MDDE 1 (1)
Online Bilimsel Program Yönetici K lavuzu
 Online Bilimsel Program Yönetici Klavuzu Bu belgedeki bilgiler, ekiller ve program ilevi önceden haber verilmeksizin deitirilebilir. Tersi belirtilmedikçe, burada örnek olarak ad geçen kiiler, adresler,
Online Bilimsel Program Yönetici Klavuzu Bu belgedeki bilgiler, ekiller ve program ilevi önceden haber verilmeksizin deitirilebilir. Tersi belirtilmedikçe, burada örnek olarak ad geçen kiiler, adresler,
T.C. KÜLTÜR VE TUR ZM BAKANLI I * NE A T SÖZLE*ME TASARISI
 T.C. KÜLTÜR VE TURZM BAKANLII Strateji Gelitirme Bakanl!"! Emek Ek Hizmet Binas! Data ve Enerji Kablolamas! *NE AT SÖZLE*ME TASARISI Götürü Bedel Hizmet Al!m! Sözlemesi KN (hale Kayt Numaras): 2010/45966
T.C. KÜLTÜR VE TURZM BAKANLII Strateji Gelitirme Bakanl!"! Emek Ek Hizmet Binas! Data ve Enerji Kablolamas! *NE AT SÖZLE*ME TASARISI Götürü Bedel Hizmet Al!m! Sözlemesi KN (hale Kayt Numaras): 2010/45966
Kpss 2014 E?itim Bilimleri Dvd Seti
 KPSS Ö?retmen Adaylar? Görüntülü E?itim Seti 58 DVD + Rehberlik Kitab? GÜNCEL Kpss E?itim Bilimleri Dvd Seti Tüm Dersler Kpss 2014 E?itim Bilimleri Dvd Seti Kpss 2014 E?itim Bilimleri Dvd Seti 58 Dvd Derecelendirme:Henüz
KPSS Ö?retmen Adaylar? Görüntülü E?itim Seti 58 DVD + Rehberlik Kitab? GÜNCEL Kpss E?itim Bilimleri Dvd Seti Tüm Dersler Kpss 2014 E?itim Bilimleri Dvd Seti Kpss 2014 E?itim Bilimleri Dvd Seti 58 Dvd Derecelendirme:Henüz
Yönetmelikler Sağlık Bakanlığından: Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar
 Yönetmelikler Sağlık Bakanlığından: Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; vücut dışında (in-vitro)
Yönetmelikler Sağlık Bakanlığından: Vücut Dışında Kullanılan Tıbbî Tanı Cihazları Yönetmeliği BİRİNCİ BÖLÜM Amaç, Kapsam, Hukukî Dayanak ve Tanımlar Amaç Madde 1 Bu Yönetmeliğin amacı; vücut dışında (in-vitro)
BAYINDIRLIK LER BRM FYAT ANALZLERNDEK GÜCÜ VERMLLKLERNN RDELENMES. M.Emin ÖCAL, Ali TAT ve Ercan ERD Ç.Ü., naat Mühendislii Bölümü, Adana / Türkiye
 ISSN 1019-1011 Ç.Ü.MÜH.MM.FAK.DERGS CLT.19 SAYI.2 Aral,k December 2004 Ç.Ü.J.FAC.ENG.ARCH. VOL.19 NO.2 BAYINDIRLIK LER BRM FYAT ANALZLERNDEK GÜCÜ VERMLLKLERNN RDELENMES M.Emin ÖCAL, Ali TAT ve Ercan ERD
ISSN 1019-1011 Ç.Ü.MÜH.MM.FAK.DERGS CLT.19 SAYI.2 Aral,k December 2004 Ç.Ü.J.FAC.ENG.ARCH. VOL.19 NO.2 BAYINDIRLIK LER BRM FYAT ANALZLERNDEK GÜCÜ VERMLLKLERNN RDELENMES M.Emin ÖCAL, Ali TAT ve Ercan ERD
Oyuncaklar Konusunda Faaliyet Gösterecek Onaylanmış Kuruluşlara Dair Tebliğ. Tarih: 28.02.2004 Sayı: 25387
 Oyuncaklar Konusunda Faaliyet Gösterecek Onaylanmış Kuruluşlara Dair Tebliğ Tarih: 28.02.2004 Sayı: 25387 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak, Genel Esaslar ve Tanımlar Amaç Madde 1 Bu Tebliğin amacı,
Oyuncaklar Konusunda Faaliyet Gösterecek Onaylanmış Kuruluşlara Dair Tebliğ Tarih: 28.02.2004 Sayı: 25387 BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak, Genel Esaslar ve Tanımlar Amaç Madde 1 Bu Tebliğin amacı,
KİŞİSEL KORUYUCU DONANIM KULLANIMI (Kişisel Koruyucu Ekipmanlar)
 KİŞİSEL KORUYUCU DONANIM KULLANIMI (Kişisel Koruyucu Ekipmanlar) İÇERİK KKE LERİN GENEL ÖZELLİKLERİ KAFA KORUMA GÖZ KORUMA KULAK KORUMA SOLUNUM KORUMA EL KORUMA AYAK KORUMA DÜŞÜŞ ENGELLEYİCİLER VÜCUT KORUMA
KİŞİSEL KORUYUCU DONANIM KULLANIMI (Kişisel Koruyucu Ekipmanlar) İÇERİK KKE LERİN GENEL ÖZELLİKLERİ KAFA KORUMA GÖZ KORUMA KULAK KORUMA SOLUNUM KORUMA EL KORUMA AYAK KORUMA DÜŞÜŞ ENGELLEYİCİLER VÜCUT KORUMA
TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM
 7 Haziran 2011 SALI Resmî Gazete Sayı : 27957 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı;
7 Haziran 2011 SALI Resmî Gazete Sayı : 27957 YÖNETMELİK Sağlık Bakanlığından: TIBBİ CİHAZ YÖNETMELİĞİ BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç ve kapsam MADDE 1 (1) Bu Yönetmeliğin amacı;
Miktar kısıtlamaları ve tarifeler yerini teknik engellere bırakıyor
 1/50 2/50 Tarife engelleri (Gümrük vergileri, miktar kısıtlamaları vb.) Tarife dışı engeller (Standartların, mevzuatın farklılığı, uygunluk değerlendirme prosedürlerindeki farklılıklar) Miktar kısıtlamaları
1/50 2/50 Tarife engelleri (Gümrük vergileri, miktar kısıtlamaları vb.) Tarife dışı engeller (Standartların, mevzuatın farklılığı, uygunluk değerlendirme prosedürlerindeki farklılıklar) Miktar kısıtlamaları
İŞ SAĞLIĞI VE GÜVENLİĞİ KURULLARI HAKKINDA YÖNETMELİK (7 Nisan 2004/25426 R.G.) BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak
 Amaç İŞ SAĞLIĞI VE GÜVENLİĞİ KURULLARI HAKKINDA YÖNETMELİK (7 Nisan 2004/25426 R.G.) BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak Madde 1 Bu Yönetmelik, iş sağlığı ve güvenliği ile ilgili çalışmalarda bulunmak
Amaç İŞ SAĞLIĞI VE GÜVENLİĞİ KURULLARI HAKKINDA YÖNETMELİK (7 Nisan 2004/25426 R.G.) BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak Madde 1 Bu Yönetmelik, iş sağlığı ve güvenliği ile ilgili çalışmalarda bulunmak
İŞYERLERİNDE ACİL DURUMLAR HAKKINDA YÖNETMELİK TASLAĞI
 Çalışma ve Sosyal Güvenlik Bakanlığından: İŞYERLERİNDE ACİL DURUMLAR HAKKINDA YÖNETMELİK TASLAĞI BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı, işyerlerinde acil
Çalışma ve Sosyal Güvenlik Bakanlığından: İŞYERLERİNDE ACİL DURUMLAR HAKKINDA YÖNETMELİK TASLAĞI BİRİNCİ BÖLÜM Amaç, Kapsam, Dayanak ve Tanımlar Amaç MADDE 1 - (1) Bu Yönetmeliğin amacı, işyerlerinde acil
