GASTROİNTESTİNAL STROMAL TÜMÖRLERDE AYIRICI TANI
|
|
|
- Eren Abacı
- 10 yıl önce
- İzleme sayısı:
Transkript
1 T.C. TRAKYA ÜNİVERSİTESİ TIP FAKÜLTESİ TIBBİ PATOLOJİ ANABİLİM DALI Tez Yöneticisi Prof. Dr. Filiz ÖZYILMAZ GASTROİNTESTİNAL STROMAL TÜMÖRLERDE AYIRICI TANI (Uzmanlık Tezi) Dr. Beril GÜLER EDİRNE
2 TEŞEKKÜR Uzmanlık eğitimim süresince destek ve katkılarını esirgemeyen ve tez çalışmamda derin bir özveri ile beni yönlendiren Sayın Hocam Prof. Dr. Filiz ÖZYILMAZ a, bilgi ve tecrübeleri ile eğitimime katkı sağlayan Sayın Hocalarım Prof. Dr. A. Kemal KUTLU, Doç. Dr. Şemsi ALTANER, Doç. Dr. Ömer Yalçın, Doç. Dr. Ufuk USTA, Yrd. Doç Dr. Fulya ÖZ PUYAN a, teknik ve immünohistokimyasal çalışmalarda yardımcı olan Biyolog Muzaffer TUDAN a ve diğer teknisyen arkadaşlarıma, istatistiksel analizlerdeki katkılarından dolayı Halk Sağlığı AD. ndan Yrd. Doç. Dr. Burcu TOKUÇ a, zorlu asistanlık sürecinde dostluklarından güç aldığım asistan arkadaşlarıma, Patoloji Anabilim Dalı mızın diğer tüm çalışanlarına en içten teşekkürlerimi sunarım. 2
3 İÇİNDEKİLER GİRİŞ VE AMAÇ... 1 GENEL BİLGİLER... 3 TANIM... 3 TARİHÇE... 3 GASTROİNTESTİNAL STROMAL TÜMÖRLERİN HÜCRESEL KÖKENİ... 4 EPİDEMİYOLOJİ... 7 LOKALİZASYON... 8 KLİNİK BULGULAR... 8 MAKROSKOPİK BULGULAR MİKROSKOPİK BULGULAR TANIYA YARDIMCI YÖNTEMLER YENİ GELİŞMELER PROGNOZ TEDAVİ GEREÇ VE YÖNTEMLER BULGULAR TARTIŞMA SONUÇLAR ÖZET SUMMARY KAYNAKLAR EKLER 3
4 SİMGE VE KISALTMALAR BBA : Büyük Büyütme Alanı DOG1 : Diagnosis on Gastrointestinal Stromal Tümör 1 = Discovered on GIST 1 Gİ : Gastrointestinal GİS : Gastrointestinal Sistem GİST : Gastrointestinal Stromal Tümör HE : Hemotoksilen + Eozin ICC : Interstitial Cells of Cajal İHK : İmmünohistokimya PDGFRα : Platelet Derived Growth Factor α PKC Ө : Protein Kinaz C Theta SMA : Smooth Muscle Actin 4
5 GİRİŞ VE AMAÇ Gastrointestinal stromal tümörler (GİST), gastrointestinal sistemin en sık mezenkimal tümörleridir. KIT (CD117, c-kit) pozitif iğsi veya epiteloid mezenkimal neoplazmlar olarak tanımlanan bu tümörler, genellikle orta yaş ve üzeri erişkinlerde izlenir, primer yerleşim yerleri ise gastrointestinal (Gİ) kanal, omentum veya mezenterdir (1-4). İnterstisyel Cajal hücrelerinden orijin alan bu tümörler, reseptör tirozin kinaz aktivitesini etkileyen KIT veya PDGFRα (platelet derived growth factor α) mutasyonlarına sahiptir ve konvansiyonel tedaviye cevap vermezler. Tümör yerleşim yeri ve morfolojik bulguları gastrointestinal stromal tümör tanısı ile uyumlu olan vakalarda kesin tanı için, CD117 immünohistokimyasal belirtecinin pozitifliği altın standarttır. Ancak özellikle PDGFRα mutant olgular başta olmak üzere, bazı tümörlerde c-kit ekspresyonu gösterilemeyebilir. Bu nedenle, günümüzde gastrointestinal stromal tümör tanısını desteleyebilecek, yeni antikorlara ihtiyaç duyulmaktadır (1,2). Gastrointestinal stromal tümörlerin klinik seyirleri asemptomatik, rastlantısal olarak yakalanan küçük boyutlu olgulardan, büyük boyutlu, çok hızlı ilerleyen, malign davranış gösteren vakalara kadar uzanan geniş bir spektrum gösterir. Hastalık progresyonunun öngörülebilmesi ve prognoz tahmini için mevcut tüm histopatolojik bulguların ayrıntılı değerlendirilmesi gerekmektedir (1-3). Çalışmamızda, gastrointestinal stromal tümörlerin DOG1 (discovered on GİST 1), PDGFRα, CD117, CD34, Vimentin, SMA (smooth muscle actin), S-100, Desmin, Ki67, Bcl2 antikorlarının boyanma özellikleri ile, tanının spesifikleştirilmesi ve ayırıcı tanıda belirlenebilecek yardımcı yeni bir algoritm düzenlenmesi hedeflenmiştir. Aynı zamanda gastrointestinal stromal tümör vakalarının risk kategorizasyonu ve prognostik özellikleri 1
6 birlikte değerlendirilerek, klinik davranışın belirlenebilmesinde ipucu olabilecek bulgular saptanmaya çalışılmıştır. 2
7 GENEL BİLGİLER TANIM Gastrointestinal stromal tümörler, gastrointestinal sistemin en sık görülen mezenkimal tümörüdür. Asemptomatik, rastlantısal olarak yakalanan küçük boyutlu olgulardan, büyük boyutlu, çok hızlı ilerleyen, malign davranış gösteren vakalara kadar uzanan geniş bir klinik spektrumda yer alarak, konvansiyonel kemoterapiye güçlü rezistans gösterirler. Çoğunda, tirozin kinaz reseptörleri olan, c-kit (CD117) veya PDGFRα kodlayan aktive gen mutasyonları görülür. TARİHÇE Gastrointestinal stromal tümörler tanımlandığı ilk yıllarda, primer olarak barsak duvarında yerleşim gösteren heterojen bir mezenkimal tümör grubu olarak tariflendi. Bu konuda ki kapsamlı ilk çalışma Golden ve Stout tarafından 1941 de yayınlanmıştır. Bu çalışmada tanımlanan serideki tümörlerin myofibriller içeren, bona fide düz kas hücre tümörleri olduğu ve leiomyom veya leiomyosarkoma dönüşüm gösterdiği iddia edilmiştir (5). Martin ve ark yılında, midede yerleşim gösteren ve düz kas hücre orijinli nadir altı vakayı intramural myoid tümöler olarak isimlendirmişlerdir. İki yıl sonra, Stout midedeki düz kas hücreli tümörlerden oluşan büyük bir vaka grubu ile yaptığı çalışmada leiomyoblastom tanısını tariflemiştir. Bu tanımlamadan sonra, omentum ve mezenterde dahil olmak üzere, gastrointestinal sistemin (GİS) herhangi bir yerinde gelişim gösteren, iğsi veya epiteloid hücreli tümörler için birçok isimlendirme yapılmıştır (6). 3
8 Elektron mikroskopi ve immünohistokimyasal (İHK) analizlerin keşfinden sonra, Mazur ve Clark 1983 de çoğu hiçbir diferansiyasyon göstermeyen bu tümörleri tanımlamada ilk kez stromal tümör terimini kullandılar (6). Herrera ve ark. (7) 1984 te, otonomik nöronal diferansiyasyon gösteren olguları pleksosarkom olarak isimlendirmiştir. Bu tümörler de daha sonra gastrointestinal otonomik sinir tümörleri (Gastrointestinal Autonomic Nerve Tumors: GANT) olarak adlandırılmıştır (8). Gastrointestinal stromal tümörlerin 1990 ların sonuna doğru, barsak pacemaker hücreleri olan interstisyel Cajal hücreleri (ICC) ile benzer morfolojik, immünofenotipik ve genetik karakteristik özelliklere sahip olduğu gösterilmiştir. Bu hücreler immünofenotipik ve ultrastrüktürel olarak hem düz kas, hem de nöronal diferansiyasyon göstererek, peristalstizm regülasyonunu sağlamaktadır. GİST lerin çoğu, aynı zamanda ICC ler için de immünohistokimyasal belirleyici olan c-kit onkoproteinini eksprese etmektedir (9). Objektif tanımlama kriterlerinin henüz tanımlanmadığı yıllarda bu tümörlerin sınıflandırmasındaki karmaşa, 1998 de hücre orijininin belirlenmesi ve tümörün histolojik, ultrastrüktürel, immünohistokimyasal özelliklerinin anlaşılması ile aydınlığa kavuşmuştur (5). GASTROİNTESTİNAL STROMAL TÜMÖRLERİN HÜCRESEL KÖKENİ Tartışmalı İnterstisyel Cajal Hücre Orijini Cajal 1889 ve 1893 yılları arasında, primitif nöronlar olarak sınıfladığı yeni bir hücre tipi tarifleyerek çeşitli makalelerde yayınladı. Bu hücre tipi barsağın villuslarının stromasında, Auerbach pleksusunda, derin muskuler pleksusta, sirküler müsküler tabakada ve pankreasın kan damarları ile asinusları çevresinde bulunmaktaydı. Cajal ın ilk tarifinin ardından, bu hücreler değişik isimlendirmelerle tanımlandılar; células simpáticas intersticiales (sempatik interstisyal hücreler, 1891); células simpáticas (sempatik hücreler, 1892); neuronas intersticiales células (sempatik interstisyal nöronlar); veya intersticiales simpáticas (interstitial hücreler, ). Daha sonra Dogiel bu hücreleri Cajal ın hücreleri olarak isimlendirmiştir. Keşfinden 100 yıl sonra da günümüzde hala İnterstisyal Cajal Hücreleri tanımı kullanılmaktadır (10). Aynı zamanda, bu hücrelerin orijini önemli tartışmalara neden oldu. Cajal da dahil olmak üzere bazı araştırmacılar, bu hücrelerin nöron olduğunu düşünürken, Kölliker ve Dogiel ise bu hücreleri fibroblast olarak sınıfladı (10). Uzun yıllar süren tartışmaların 4
9 ardından, bu alandaki en önemli gelişme ICC lerin tirozin kinaz reseptörünü eksprese ettiğinin keşfi ile oldu (11). Bu sayede, musküler tabakadaki bu hücreler morfolojik olarak benzedikleri diğer hücrelerden, histokimyasal olarak ayırt edilebildi ve bu hücrelerin dokulardaki dağılımları sağlıklı bir şekilde öğrenildi (12,13). İmmünohistokimyasal (İHK) tekniklerin kullanıma girmesi ile beraber ise, ICC lerin orijini daha detaylı olarak araştırılabildi. Bu yöntem ile anöral eksplantlarda c-kit ekspresyonunun saptanması, ICC lerin memelilerde nöral krest orijinli olmadığını düşündürdü (14). Diğer yandan, düz kas hücrelerinde de c-kit ekspresyonun gösterilmesi ile ICC lerin düz kas hücreleri gibi benzer mezoderm orijinden kaynaklandığı gösterildi (15, 16). Ancak sirküler müsküler tabakada yerleşen ICC lerin, nöral krest hücrelerinden diferansiye olan ICC prekürsörleri, glia ve nöronların kaynağı olan ventral nöral tüpten [(VENT hücreleri),(17) geliştiğinin gösterilmesiyle, ICC lerin önemli bir alt kümesinin nöral orijinli olabileceği kabul edildi. Önemli bir nokta olarak, ince barsaktaki derin muskuler pleksusta (DMP) lokalize ICC ler gibi tüm ICC ler c-kit eksprese etmeyebilirler (18,19). Dahası, ICC ler dışında, mast hücreleri, melanositler, nöronlar ve glia gibi c-kit eksprese eden çok çeşitli hücre tipleri mevcuttur (20). Bu nedenle, belirli hücrelerin ICC ailesine ait olduğunu kanıtlamak için, ultrastriktürel analizlere ihtiyaç vardır. ICC lerin ultrastriktürel karakteristikleri tanımlanmış ve ICC tanımlamasında altın standart olarak özetlenmiştir (21-23). Ultrastrüktürel olarak bu hücrelerde, parsiyel bazal lamina, çok sayıda intermediyal filaman, koyu boyanan sitoplazma, çok sayıda granüllü endoplazmik retikulum, sublamellar kaveoller, oval katlantılı nükleus ve miyozin filaman yokluğu mevcuttur (24). Günümüzde çok çeşitli immünohistokimyasal belirteçlerin de yardımı ile farklı ekspresyon çeşitleri ve paternlerinin gösterilmesi sonucunda ICC lerin, nöral veya müsküler yönde diferansiasyon gösterebilen, GİS te yavaş dalga peristaltizminde nörotransmisyonu sağlayan, kök hücrelerden gelişmiş özel hücre grubu olduğu kabul edilmektedir (10,25). Cajal ın, intestinal kanalın değişik bölgelerinde tespit ettiği, dar sitoplazmalı, küçük, fusiform ve trianguler yapıda, anastomoz proçesleri içeren hücreler, ICC olarak tanımlandı. Klasik olarak, Meissner pleksusu (submusküler konnektif dokuda lokalize) ve Auerbach pleksusu (longitudinal ve sirküler düz kas fiberleri arasında lokalize) dışında, Cajal üç tane daha pleksus tanımladı: derin müsküler, periglandüler ve intravillöz pleksuslar (Şekil 1) (10). 5
10 ICC; İnterstisyel Cajal hücreleri, DMP; Derin müsküler pleksus, SMP; Submukozal pleksus, SM; Submukoza, CM; Sirküler kas, IM; İntra müsküler, MP; Multipolar, MY; myenterik pleksus, LM; Longitudinal kas. Şekil 1. İnterstisyel Cajal hücreleri ağı organizasyon şeması (10) Günümüzde ICC lerin, özefagustan anorektuma kadar tüm gastrointestinal kanalda bulunduğunu biliyoruz. Ancak bu hücrelerin GİS te bulundukları bölgeye göre yerleşim gösterdiği tabakalarda farklılıklar vardır. ICC ler özefagus, gastrik kardiya ve fundusta muskularis propriada yerleşim gösterirken, myenterik pleksus veya submukozada bulunmazlar. Gastrik nonfundik korpus, pilor ve barsaklarda ise myenterik pleksusta yerleşirler. Submukozal ICC ler, ince ve kalın barsakta görülürler (Şekil 2) (26). A B Şekil 2. Barsak submukozasında Cajal hücrelerinde (ok) CD117 pozitivitesi, (İmmünohistokimya A: x100, B: x200 ). 6
11 Cajal hücreleri aynı zamanda gastrointestinal sistemin dışında da lokalize olabilir. Bazı histolojistler golgi tekniği ile, dilin seröz glandlarında veya miyokardda bu hücreleri saptamışlardır (10). Ayrıca modern teknikler kullanılarak, ICC lerin üst üriner kanal (27), üretra (28), miyometrium (29), uterus, fallop tüpü (30) ve plasenta (31) gibi bir çok lokalizasyondaki varlığı gösterilmiştir. Cajal Hücrelerinin Fizyolojik Fonksiyonu Kas fiberleri ve nöral ağ ile birlikte, GİS te barsak motilitesinde kritik rolü olan, ICC ler mezenkimal hücrelerin üçüncü popülasyonudur. Yavaş dalga depolarizasyonu meydana getirirler (24). Üç major fonksiyonları vardır (26, 32): a) Gİ kaslarda pacemaker rolüne sahiptirler, b) Elektriksel olayların aktif yayılımını kolaylaştırırlar, c) Nörotransmisyona aracılık ederler ve mekanoreseptör görevi görürler. Bu hücrelerin anormalliklerinde motilite hastalıkları görülebilir veya GİST e neden olabilirler (26). Ailesel GİST lerde veya nörofibromatozisli hastalarda, tüm Gİ kanalda özellikle myenterik pleksus çevresinde, sıklıkla fokal veya diffüz ICC hiperplazisi görülür (26). Literatürde KIT mutasyonu olmaksızın, ICC hiperplazisi gösteren, pediatrik gruptaki bir olguda, kronik idyopatik intestinal psödo-obstrüksiyon bildirilmiştir (33). Daha yeni bir gelişme olarak da, intestinal psödo-obstrüksiyon mevcut olan bazı vakalarda, c-kit-pozitif ICC lerin total veya totale yakın yokluğu gösterilmiştir (34-37). C-kit reseptör blokajı ise, barsak motilitesinde çeşitli dengesizliklerle sonuçlanır (38). Piebaldizm hastalarında görülen, inaktive KIT mutasyonu, hayat boyu konstipasyona neden olmaktadır (39,40). EPİDEMİYOLOJİ Gastrointestinal stromal tümörler relatif olarak nadir tümörlerdir. Surveillance, Epidemiology and results (SEER) verilerine göre GİST ler, gastrik kanserlerin %2.2 sini, ince barsak kanserlerinin %13,9 unu, tüm kolorektal kanserlerin ise %0.1 ini oluşturmaktadırlar (41).Tüm malign mezenkimal tümörlerin %5-10 unu oluşturmaktadır (42). İzlanda da yılları arasında yapılan bir çalışmada, insidansı milyonda 11 vaka olarak bulunmuştur (43). İsviçre deki yıllık insidansı milyonda 14.5 olarak tahmin edilmektedir (44). ABD deki istatistiklere göre de benzer oranlar saptanmıştır ki, yılda yaklaşık 4000 yeni vaka beklenmektedir (45). Fletcher (41) ın risk grupları esas alınarak 7
12 yapılan sınıflamaya göre prevelans oranları: çok düşük risk grubu için milyonda 22.2, düşük risk grubu için milyonda 51.9, intermediate risk grubu için milyonda 24.2 ve yüksek risk grubu için milyonda 22.2 olarak bildirilmiştir (44). İnsidans ile coğrafi yerleşim, maruziyet ya da ırk arasında herhangi bir ilişki gösterilememiştir (46). Bu tümörler sıklıkla, orta yaş ve yaşlı bireylerde görülmektedir. Primer etkilenen yaş grubu 6. ve 8. dekatlardır (1,2,47). Vakaların %75 i 50 yaş üstüdür (median yaş, 58) (48). Ancak konjenital tümörler olarak karşılaşılabildiği gibi, genç yaşlarda da izlenebilirler (47). Çalışmaların çoğunda vakaların görülme sıklığı ve cinsiyet arasında istatistiksel olarak korelasyon olmadığı saptanmış iken, bazı çalışmalarda erkeklerde biraz daha sık görüldüğü belirtilmiştir (48,49). LOKALİZASYON Gastrointestinal stromal tümörler, gastrointestinal kanalın herhangi bir yerinde gelişebilmekle birlikte en sık midede (%50-70) gelişim gösterirler. Daha sonra ise sıklık sırasına göre jejunum ve ileum %20-40, duodenum %5 ve kolorektumda <%5 oranında görülürler (3,45,50-52). Kolorektal lezyonların çoğu rektumda görülür (5). Düşük oranlarda özefagus, appendiks vermiformis, safra kesesi ve pankreasta da görülebilirler (53-55). Bu tümörler barsak duvarının tüm katlarında gelişebilir ancak en sık submukoza veya muskularis propriadan köken alırlar. Bazı tümörler ise Gİ kanalın serozal yüzlerinde ektramural yerleşim gösterirler. Bu lokalizasyondaki tümörler oldukça büyük boyutlara ulaşıp çevre dokuya ve komşu organlara yayılım gösterebilirler (1). Ayrıca primer tümör Gİ kanal dışında retroperiton veya abdomende (omentum veya mezenter gibi) izlenebilir ve GİS dışı stromal tümörler olarak isimlendirilirler(56,57). Armed Forces Institute of Pathology (AFIP) tarafından yayınlanan 1008 GİST vakası içeren seride GİS dışı yerleşim oranı %6.7 olarak belirtilmiştir (42). Nadiren uterus, over, rektovajinal septum, vajen gibi yerleşim yerleri de bildirilmiştir (58,59). KLİNİK BULGULAR Gastrointestinal stromal tümörlerde klinik bulgular; tümörün Gİ kanalda yerleşim yeri, tümör boyutu ve organ duvarındaki lokalizasyonu ile ilişkilidir (1). 8
13 İkiyüz seksensekiz primer GİST vakasının alındığı bir çalışmada, tümörlerin %69 u semptomatik iken, %21 i cerrahi sırasında rastlantısal olarak görülmüş, geri kalan %10 u ise otopsi sırasında saptanmıştır (44). Benign tümörler, genellikle küçük boyutlarda olmaları nedeniyle çoğunlukla asemptomatiktir ve başka bir nedenle yapılan cerrahi girişimler sırasında insidental olarak saptanırlar. Ancak bazı benign tümörler de Gİ kanama ve abdominal ağrı gibi semptomlara yol açabilir (1). Hem benign hem de malign tümörlerde görülen Gİ kanamanın nedeni, tümörün Gİ kanal lümenine projeksiyonu sonucunda görülen ülserasyonlardır (3). Daha az sıklıkla görülen diğer klinik semptomlar ise mide bulantısı, kusma, kilo kaybı ve abdominal kitledir (1). Yerleşim yerlerine göre karşılaşılabilecek potansiyel klinik semptolar Tablo 1 de özetlenmiştir. Tablo 1. Yerleşim yerlerine göre gastrointestinal stromal tümör semptomları TÜMÖR YERLEŞİM YERİ Özefagus Mide Duodenum İnce barsak Anorektal KLİNİK SEMPTOM Disfaji, odinofaji, göğüs ağrısı, hematemez Bulantı, kusma, kilo kaybı, şişkinlik Biliyer obstrüksiyon Melena, tıkanıklık, perforasyon Rektal tuşede palpabl kitle Bazı GİST vakaları ise, diğer sarkomlar gibi çevre dokuya invaze olmak yerine, komşu dokuların yerini alarak büyüdükleri (ekspansif büyüme) için semptomatik olmadan önce büyük boyutlara ulaşabilirler (60). Bulgular ve semptomlar endoskopi ve biyopsi yapılmasına sebep olabilir. Ancak endoskopik biyopside GİST tanısı verilmesi güçtür ve genellikle vakalar mezenkimal tümör tanısı alırlar. Şayet biyopsi derin alınabilmişse veya neoplazm üzerindeki mukozayı infiltre etmiş ise, bazı vakalarda, spesifik histolojik tanı verilebilmektedir. Endoskopik biyopsi materyallerinde ve hatta frozen kesitlerde GİST vakalarında benign-malign ayrımını yapmak güçtür ve zorunlu değildir. Baryum kontrast, bilgisayarlı tomografi (BT) ve endoskopik ultrasonu (EUS) içeren radyografik görüntüleme yöntemleri, bu neoplazmların tanısında sıklıkla kullanılır (61). Radyolojik görüntüler spesifik değildir ama gastrik mural büyük kitlelerin çoğunluğu GİST tir (42). Endoskopik ultrason, GİST tanısında önemli bir yere sahiptir. EUS un 9
14 submukozal lezyon ile bası arasındaki ayrımı yapmakta duyarlılığı %92, özgüllüğü ise %100 olarak bulunmuştur. Malign GİST tanısında endoskopik ultrasonun sensitivitesi % arasında değişmektedir (62,63). Özellikle 3 cm in üzerindeki, düzensiz sınırlı, heterojen eko yapısında, ortasında nekrotik alanı telkin edecek şekilde anekoik boşluklar bulunan kitleler daha çok malign lehine değerlendirilmektedir (64). Bununla birlikte, nadiren bazı tümörlere ince iğne aspirasyon sitolojisi ile tanı konabilir. Ancak bu teknikle benign-malign ayrımı genellikle mümkün değildir (65). MAKROSKOPİK BULGULAR Gastrointestinal stromal tümörlerin çoğu ince bir psödokapsülle çevrili, çevre normal dokuyu basıya uğratan iyi sınırlı lezyonlardır. Tek nodül, plak veya multipl nodüler lezyonlar şeklinde gelişim gösterebilirler. Geniş tabanlı, intraluminal polipoid şekilde de görülebilirler. Bu tümörler endofitik veya ekzofitik paternde büyüyebilirler. Tümörler bu iki paternde de lobuler yapıda olabilir. Tümörün üzerini örten mukoza intakt veya ülsere olabilir. GİST lerin kesit yüzü, düz kas tümörlerinin karakteristiği olan, dışa doğru kabarma eğilimi ve helozonik görünümden yoksundur. Buna karşılık kesit yüzleri et kıvamında-solid ya da yama şeklinde hemoraji, nekroz veya kistik dejenerasyon alanları içeren granüler görünümde, pembe renkli ve gevrek kıvamlıdır. Kompleks kistik kitleler ve multinodüler peritoneal ekilme izlenebilir. Tümör boyutu 0.5 cm den, 45cm e kadar değişen ölçülerde olabilmektedir. Ortalama boyut 6cm dir. Büyük tümörlerde, masif hemorajik nekroz sonucu oluşan kistik formasyonda, sadece kistlerin cidarlarında canlı tümöral doku izlenebilir. Bu durumda tümörler kompleks kistik kitle görünümünü alır (1-3,5,52). MİKROSKOPİK BULGULAR Gastrointestinal stromal tümörler komplet, inkomplet veya mikst olmak üzere, miksoid, nöral, ganglionik pleksus fenotipi gibi çok çeşitli diferansiasyon spektrumları gösterirler. Günümüzde immünohistokimyasal çalışmaların yardımıyla, GİST hücrelerinin, multipotansiyel mezenkimal kök hücrelerle yakından ilişkili olduğu açıklığa kavuşmuştur. Bu nedenle GİST ler çok çeşitli histolojik paternler içerebilirler. Aynı zamanda sellülarite oranları da, tümörden tümöre ya da tümörün değişik odaklarında farklılıklar gösterebilir. Hücresel pleomorfizm ise, GİST lerde nadir görülen bir bulgu olup, genellikle fokal alanlarda izlenebilir. Diffüz pleomorfizm, GİST lerde beklenen bir bulgu değildir ve mikroskopik mevcudiyetinde öncelikle ayırıcı tanıdaki diğer mezenkimal tümörler ekarte edilmelidir. Bazı 10
15 yazarlar bu çok çeşitli histolojik bulguların prognostik önem taşıdığını vurgulamaktadır (6,41,66,67). Gastrointestinal stromal tümörler histomorfolojik görünümlerine göre iğsi, epiteloid ve mikst hücreli tip olarak gruplandırılabilir (1,41,45,50,68). İğsi hücreli komponent, storiform (girdapsı), palizatlanan (çit şeklinde) veya fishbone (balıksırtı) paternde gözlenebilir. Nukleusların görünümü tipik olarak, uzun, mermi veya puro şeklinde, bir ucu künt, bir ucu sivridir. Bazı tümör hücreleri geniş sitoplazmalıdır. Hyalinizasyon alanları görülebilir (2). Epiteloid hücreli tip, sıkıca bir araya gelmiş poligonal hücrelerden oluşmaktadır. Bu tümörler aynı zamanda alveolar paternde gelişim gösteren küçük hücre adaları da içermektedir. Hücreler genellikle uniform görünümde olmakla birlikte, bizar veya multinükleer hücreler karakteristik olarak izlenebilir (2,52,68). Pleomorfik hücreli tip, stromal tümörlerin küçük bir kısmında, fokal şiddetli pleomorfizmin mevcut olduğu hücrelerden oluşmaktadır (2). Mikst hücreli tümörlerde ise, hem iğsi hücreli komponent, hem de epiteloid morfolojide ki tümör hücreleri bir arada bulunur (2). Son çalışmalarda GİST lerin, Gİ sistemdeki lokalizasyonlarına göre histolojik tip farklılığı vurgulanmış ve tümör sınıflaması buna göre yapılmıştır (2). Özefageal Gastrointestinal Stromal Tümörler Özefageal GİST ler nadir görülür ve çoğu malign tümörlerdir (69). Erkeklerde daha sık görülür ve hastalar genellikle disfaji ile prezente olur. Bu tümörler tipik olarak distal özefagusta yerleşir ve özefagogastrik bileşkeyi tutabilirler (1). İntramural tümör veya polipoid kitle olarak gelişim gösterebilirler (69). Makroskopik olarak yumuşak kıvamlı, kesit yüzleri heterojen ve sıklıkla santral nekroz ve/veya kistik değişiklik gösterirler. Tipik olarak yüksek sellülariteye sahiptirler. Orta derece atipi içerirler. Mitotik aktivite değişken olmakla beraber, çoğunda 50 BBA (büyük büyütme alanı) da, 5 ten fazla mitotik figür izlenir (1). İğsi hücre paterninde görülebilir veya epiteloid diferansiyasyon alanları içerebilirler. Nükleer palizatlanmalar gösteren hücre adaları ve miksoid değişiklikler görülebilir. Bazı tümörler nöral diferansiyasyon gösterirler (69). Az sayıdaki vakada koagülatif nekroz ve mukozal invazyon bildirilmiştir (1). 11
16 Gastrik Gastrointestinal Stromal Tümörler Mide, GİST lerin en sık lokalizasyon bölgesidir. Genellikle benign davranış sergilerler. Antral GİST lerle kıyaslandığında, fundik ve gastroözefageal GİST lerde malignensi sıklığı daha yüksektir (2). Gastrik GİST ler relatif olarak spesifik olan, iki morfolojik subtip gösterirler. Birinci tip sellüler iğsi hücreli stromal tümördür. Bu tip, monoton görünümde uniform nükleuslu, perinükleer vakuoller içeren, belirgin palizatlanma gösteren iğsi hücre fasikülleri ile karakterizedir. Hyalinizasyon ve miksoid dejenerasyon sıktır. Mitotik aktivite düşüktür. Diğer tip olan epiteloid GİST ler ise, gastrik GİST lerin çoğunluğunu teşkil eder. Bu tümörler belirgin berrak sitoplazmalı, sitoplazmik perinükleer vakualizasyon gösteren yuvarlak epiteloid hücrelerden oluşur. Bu tümör hücreleri fasiküller yerine, adalar ve tabakalar halinde dizilim gösterir. Hücreler perivasküler alan yerleşimli olma eğilimindedirler. Mitoz sayısı 50 BBA da 5 i geçmediği sürece, midedeki epiteloid GİST lerin çoğu benigndir (70). Trupiano ve ark. (71) ı gastrik GİST leri hücre tipi ve davranışına göre şöyle sınıflamaktadır; -Benign iğsi hücreli GİST -Malign iğsi hücreli GİST -Benign epiteloid hücreli GİST -Malign epiteloid hücreli GİST -Benign mikst hücreli GİST -Malign mikst hücreli GİST Hem iğsi, hem de epiteloid hücrelerin varlığında, tümörün %75 inden fazlasını oluşturan, baskın hücre tipi bildirilir. Bu kriterin sağlanamadığı tümörler mikst tümörler olarak sınıflandırılırlar (2). Benign iğsi hücreli gastrik GİST ler; soluk veya eozinofilik sitoplazmalı, uniform iğsi hücreli, yüksek sellülariteye sahip tümörlerdir. Sıkışık hücreler fasiküler, helozonik, storiform veya palizatlanan yapıda ya da herhangi bir patern oluşturmadan dizilim gösterebilir. Uniform soluk nüveler nükleolden yoksundur ve iyi dağılmış kromatin yapısı ile, düzgün nükleer sınırlara sahiptirler. Mitotik aktivite 50 BBA da 2 veya daha azdır. Perinükleer vakuoller bulunabilir (2). Bu vakuoller fiksasyon artefaktına bağlı olarak görülmektedir ve frozen kesitlerde izlenemez (1). Tümör hücreleri arasında genellikle hyalinize veya kalsifiye stroma görülür. Perivasküler tümör adalarını ayıran asellüler materyal gölcükleri ile likefaktif nekroz alanları izlenebilir (71). 12
17 Benign epiteloid gastrik GİST ler; mide yerleşiminde en sık görülen tiptir. Bu tümörler pür veya baskın olarak, adalar ve tabakalar oluşturan epiteloid hücrelerden oluşur. Tümör hücreleri eozinofilik, amfofilik veya berrak geniş sitoplazmalara sahiptir (2). Sadece hemotoksilen-eozin (HE) kesitlerde seçilebilen, frozen kesitlerde ve ultrastrüktürel çalışmalarda izlenemeyen, periferal sitoplazmik berraklaşma eşliğinde, nükleus komşuluğunda, sitoplazmik eozinofilik kondanse rim görülebilir (1). Nukleus genellikle yuvarlak olup, küçük nukleol içerir. Ama dağınık multinükleer dev hücreler veya bizar nükleuslu hücreler de görülebilir. Mitotik figür nadirdir. Stromada hyalinizasyon ve kalsifikasyon izlenebilir (71). Vasküler yapıların zenginliği nöroendokrin veya glomus benzeri görünüm oluşturabilir (2). Malign iğsi hücreli gastrik GİST ler, benign iğsi hücreli gastrik GİST lere kıyasla daha büyük tümör boyutuna sahiptir, daha sellüler nitelikte ve yüksek nükleositoplazmik orana sahip hücrelerden oluşur. Sitoplazma eozinofilik, bazofilik veya amfofilik görülebilir. Nukleuslar pleomorfik ve sıklıkla veziküler görünümdedir. Benign iğsi hücreli tiplerde görülen ve tipik olan perinükleer vakuoller bu tipte izlenmez. Tümörde nekroz alanları sıktır. Tümör hücreleri storiform veya fasiküler paternde dizilebilir. Bazı tümörler belirgin nükleer palizatlanma gösterir. Mitoz sıklıkla 50 BBA da 10 dan fazladır. Muskularis mukoza ve bazal mukozal glandlar arasında tümör hücre infiltrasyonu olarak tanımlanan mukozal invazyon görülebilir (2). Malign epiteloid gastrik GİST lerde; hücreler, oldukça dar sitoplazmalı ve belirgin olarak sıkışık dizilim gösterirler. Bu özellikleri dolayısıyla küçük büyütmede yüksek sellüler görünüme sahiptirler. Tümörün değişik alanlarında farklı hücresel paternleri görmek mümkündür. Hücreler, asit mukopolisakkaritten zengin miksoid stromada, geniş adalar veya küçük asinus benzeri yapı oluşturan gruplar halinde dizilebilir. Benign formlarının aksine, nukleuslar daha hiperkromatiktir ve genellikle monoton görünümdedirler. Nadiren malign epiteloid tümörler diffüz pleomorfizm gösterebilirler. Mitotik aktivite derecesi, benign formlarla benzer olabilir. Bu nedenle, mitoz sayısı çok yüksek olmadığı sürece, mitotik parametre yalnız başına benign ve malign epiteloid gastrik stromal tümör ayrımında kullanılamaz. Bu nedenle munis görünümlü epiteloid tip gastrik GİST lerde, çok sayıda örnekleme yapılarak, malignite belirleyicisi olan yüksek atipi, yüksek mitoz ve nekrozun varlığı araştırılmalıdır (1). Uzun süre takipli, 1765 gastrik GİST vakasını kapsayan geniş bir çalışmada ise sekiz histolojik subtip tanımlanmıştır (68); 13
18 Sklerozan iğsi hücreli GİST; yaygın ekstrasellüler kollajen içeren, hücreden fakir tümörlerdir. İğsi hücreler atipi içermez, mitotik aktivite düşüktür ve sıklıkla kalsifikasyon izlenir. Genellikle küçük lezyonlar olmakla birlikte, %13 ü 10 cm den büyüktür. Palizatlanan ve vakuole iğsi hücreli GİST; nükleer palizatlanma ve perinükleer vakuolizasyon içeren, sellüler nitelikte, tombul, uniform iğsi hücrelerden oluşan tümörlerdir. Sınırlı atipi içerirler ve mitotik aktivite nadiren 50 BBA nda, 10 u geçer. Hipersellüler iğsi hücreli GİST; sıkışık gruplar oluşturan, diffüz tabakalar halinde gelişim gösteren, uniform iğsi hücrelerden oluşurlar. Hafif atipi, nükleer palizatlanma ve perinükleer vakuolizasyon içerirler. Mitotik aktivite nadiren 50 BBA nda, 15 i geçer. Sarkomatöz iğsi hücreli GİST; diffüz atipi içeren iğsi veya oval hücrelerden oluşur. Miksoid stroma ile ayrılmış, tümör hücre yığınları görülür. Mitotik aktivite 50 BBA nda, 20 den fazladır. Tümörlerin nerdeyse hepsi 5 cm den büyüktür. Sklerozan epiteloid GİST; diffüz kollajenöz matrikste, sinsityal patern gösteren, belirsiz hücre sınırlarına sahip, koheziv, uniform, poligonal hücrelerden oluşan tümörlerdir. Multinükleasyon ve düşük mitoz oranı karakteristiktir. Diskoheziv paternli epiteloid GİST; dar interstisyel matriks içinde, geniş sitoplazmalı, hücre sınırları belirgin, diskoheziv paternde, büyük poligonal hücrelerden oluşurlar. Multinükleasyon, fokal atipi görülebilir. Mitoz oranı düşüktür. Hipersellüler epiteloid GİST; iyi sınırlı, birbirlerine yaslanmış epiteloid hücrelerden oluşurlar. Nükleer atipi mevcuttur ve diskoheziv epiteloid GİST lere kıyasla, yüksek nükleo/sitoplazmik orana sahiptirler. Mitotik aktivite nadiren 50 BBA nda 10 dan fazladır. Sarkomatöz epiteloid GİST; uniform nükleuslu, belirgin nukleollü, yüksek nükleo/sitoplazmik orana sahip epiteloid ve yuvarlak hücrelerden oluşurlar. Mitotik aktivite dikkat çekici oranda yüksektir (50 BBA nda 20 den fazla). Benign İnce Barsak Gastrointestinal Stromal Tümörleri: Klasik olarak benign ince barsak GİST leri, 5 cm den küçük boyutlu, geniş eozinofilik sitoplazmalı, sitolojik olarak munis, uniform iğsi hücrelerden oluşan tümörlerdir. Düşük dereceli sellülariteye sahiptirler. Tipik olarak, fibrovasküler septalar ile ayrılmış hücre grupları nedeniyle organoid büyüme paterni gösterirler. Skenoid fiber olarak adlandırılan, 14
19 eozinofilik kollajen globüller karakteristiktir ve genellikle çok sayıdadır. Mitotik figürler 50 BBA nda 5 ten azdır. Tümör nekrozu ve mukozal invazyon belirgin değildir (1,72). Malign İnce Barsak Gastointestinal Stromal Tümörleri Malign ince barsak GİST lerinin çoğu, iğsi hücrelerin, yüksek sellüler proliferasyonundan oluşur ve benign formlarına göre sitolojik atipi baskındır. Nukleuslar büyük ve kaba kromatinlidir. Mitotik figürler 50 BBA da, 5 ten fazladır. Tipik olarak tümör hücreleri, benign tümörlerdeki uniform organoid büyüme paterninin aksine, uzun fasiküller halinde düzenlenmiştir. Skenoid fiber azdır veya hiç izlenmez. Malign ince barsak GİST lerinin çoğu, en azından fokal odaklarda olmak üzere, tümör hücre nekrozu ya da mukozal invazyon veya her ikisini de gösterirler. Neoplazmın %25 inden fazlasını, epiteloid komponentin oluşturduğu tümörler genellikle maligndir (1,73). İnce barsak GİST lerinin çoğu midedekilerden farklı olarak, kolaylıkla benign veya malign olarak klasifiye edilebilirler. Sadece nadir ince barsak GİST leri belirsiz malignensi kategorisine uyar (1). Kolonik Gastrointestinal Stromal Tümörler Özefagus ayrı tutulursa, kolon Gİ kanalda GİST lerin en az görüldüğü bölgedir. Bununla birlikte, birkaç çalışmada önemli sayıda vaka raporlanmıştır (45,74,75). Histolojik olarak, benign kolonik GİST ler son derece nadirdir (1). Örneğin, Miettinen ve ark. (75) nın (75) bir çalışmasında, 37 kolonik GİST ten 23 ü, klinik olarak malign davranış sergilerken sadece 4 ü, insidental olarak saptanmış, küçük boyutlu, serozal protrüzyon gösteren polipoid kitleler olup, nadir mitotik figüre ve skeinoid fiber sahip, nekroz içermeyen, atipisiz iğsi hücrelerden oluşan tümörlerdir. Kolon yerleşimli GİST ler, diğer yerleşim bölgelerindeki GİST lerle karşılaştırıldığında, yüksek sellülarite gösteren iğsi hücreli tümörlerden, şiddetli pleomorfik sarkomlara kadar çok çeşitli ve heterojen bir grup oluştururlar. Morfolojik olarak hafiften şiddetliye, çok değişken sitolojik atipi kriterlerini içermelerine rağmen, kolonik GİST lerin çoğu klinik davranış olarak maligndir. Çoğu hastada tanı anında metastaz mevcuttur ve prognoz kötüdür (74,75). Miettinen ve ark. (75) nın bir çalışmasında, 1 cm veya daha büyük boyutlu, 50 BBA nda 5 ten fazla mitoz içeren kolonik GİST li hastaların neredeyse tümü, 15 aylık median sürvi ile hastalık nedenli kaybedilmiştir. Ancak aynı seride, 1 cm den büyük boyutlu, 50 BBA da 5 veya daha az mitoz içeren tümöre sahip vakalarda hastalıksız sağkalım 15
20 izlenmekle birlikte, bu kategorideki bazı hastalarda hızlı fatal gidişat görülmüştür. Tworek ve ark. (74) nın çalışmasında, muskularis propriada infiltratif büyüme paterni, mukozal invazyon ve yüksek mitoz oranının (50 BBA nda 5 ten fazla mitotik figür), metaztaz ve ölüm ile yüksek korelasyon gösterdiği saptanmıştır. Koagülatif nekroz ve yüksek sellülarite ise kötü prognozda minör kriter olarak değerlendirilmiştir (1) (Tablo 2). Tablo 2. Kolonik gastrointestinal stromal tümörlerde risk karşılaştırılması (1) Özellik Düşük-Risk GİST Yüksek-Risk GİST Muskularis propria infiltrasyonu Yok Mevcut Mitoz 5/50 BBA >5/50 BBA Mukozal invazyon Yok Mevcut Sellülarite Düşük Orta-Yüksek Tümör nekrozu Yok Sıklıkla mevcut GİST; Gastrointestinal stromal tümör, BBA; Büyük büyütme alanı. Anorektal Gastrointestinal Stromal Tümörler Anorektal GİST ler, diğer bölgelerdeki GİST lerle benzer ışık mikroskopik, immünohistokimyasal ve moleküler özellikler gösterirler (76). Eski bilgilere göre, tüm anorektal GİST lerin histolojik özelliklerine bakılmaksızın malign olduğu kabul edilirdi (77). Ancak son çalışmalar göstermiştir ki, tüm anorektal GİST ler klinik olarak malign değildir ve benign formları malignden ayırt etmek için Tablo 3 te bildirilen özellikler kullanılmaktadır (1,76,78,79). Tablo 3. Anorektal gastrointestinal stromal tümörlerde risk karşılaştırılması (1) Özellik Düşük-Risk GİST Yüksek-Risk GİST Boyut <2 cm >5 cm Mitoz 5/50 BBA >5/50 BBA Sellülarite Düşük Orta-Yüksek Kalsifikasyon Sık Yok GİST; Gastrointestinal stromal tümör, BBA; Büyük büyütme alanı. 16
21 Anorektal GİST ler submukozal bölgeden ziyade, daha sıklıkla muskularis propriadan köken alırlar. Submukozal kaynaklı olanlar polipoid kitle halinde gelişerek, nadiren mukozal invazyon yapabilirler. Anorektal GİST ler, yüksek sellülariteye sahip, demetler oluşturan, relatif olarak uniform, uzun, iğsi nüveli ve sıklıkla belirgin nükleer palizatlanma gösteren tümörlerdir. Gastrik GİST lerden farklı olarak, anorektal GİST lerde çok nadiren baskın epiteloid morfoloji görülebilir (1). TANIYA YARDIMCI YÖNTEMLER İmmünohistokimyasal Özellikler Literatürde yayınlanan, immünohistokimyasal GİST bulguları son 25 yıldır gelişim göstermektedir. İlk çalışmalarda myoid ve nöral antijenlerin ekspresyonları üzerine odaklanılmıştır, ancak sonuçlar uyumsuz bulunmuştur. Daha sonra denenen, bir hematopoetik kök hücre belirleyicisi olan CD34 ün, tüm yerleşim bölgelerindeki GİST lerin çoğunda eksprese edildiği saptanmıştır (80-82). Ancak son birkaç yılda, tüm bölgelerdeki GİST ler için en sensitif immünohistokimyasal belirleyicinin CD117 (c-kit) olduğu anlaşılmıştır (83,84). Proto-onkogen c-kit in (kromozom 4) ürünü olan KIT, bir transmembran büyüme faktörüdür. Bir tirozin kinaz reseptör üyesi olarak, ailenin platelet kökenli büyüme faktörü (PDGFR) ve diğer reseptörleri ile yakından ilişkilidir. KIT hemotopoetik progenitör, mast, germ ve interstisyal Cajal hücrelerinde eksprese edilir. Stem-cell factor (SCF) olarak bilinen ligantı ile KIT reseptör aktivasyonu, proliferasyon, adezyon, apoptoz ve diferansiyasyonu içeren onkogenez kaskadını başlatır (25). C-kit GİST lerin %95 inden fazlasında eksprese edilmektedir (83,84). Bunun yanı sıra, intra-abdominal lokalizasyona sahip olabilen anjiosarkom, metastatik melanom, berrak hücreli sarkom ve Ewing sarkom/primitif nöroektodermal tümörlerde de CD117 pozitifliği görülebilir. Ayrıca seminom, mastositom ve granülositik sarkom gibi diğer birçok neoplazmda da bu antijen ile pozitif reaksiyon saptanmıştır. Dolayısıyla bu immünohistokimyasal belirleyici GİST ler için spesifik değildir. Ancak günümüzde hala morfolojik tanı ile birlikte, altın standart İHK sal seçenektir (85). Gastrointestinal stromal tümörlerde CD117 nin boyanma paterni genellikle kuvvetli, diffüz ve pansitoplazmiktir. Ancak özellikle epiteloid morfolojideki bazı tümörlerde membranöz boyanma ve bununla birlikte perinükleer dot-like (golgi zone patern) boyanma görülebilir. İmmünreaktivite bazı vakalarda yamalı tarzda olabilir. Böyle vakaların küçük 17
22 biyopsi materyallerinde yanlış negatiflikler saptanabilir (1). Ticari olarak sağlanabilen farklı klonlar ve farklı boyama metodları da yanlış pozitif ve yanlış negatif sonuçlara neden olabilir (2). Gastrointestinal stromal tümörlerin yaklaşık %5 i CD117 negatiftir. Bu tümörlerin genellikle epiteloid sitomorfolojide, mide veya omentum/periton yerleşimli ve PDGFRα mutasyonu içeren vakalardır. Enteresan olarak belirtilmelidir ki, c-kit immünohistokimyasal reaksiyonu bulunmayan GİST lerin, yaklaşık %20 sinde KIT mutasyonu mevcuttur (5). Buna göre İHK sal olarak c-kit negatif GİST ler, KIT mutasyon negatifliğini göstermemektedir. GİST lerin küçük bir grubunda ise hem KIT, hem de PDGFRα mutasyonu gösterilemez. Bu grup GİST wild type olarak tanımlanmıştır (1). Wild tip GİST ler genellikle İHK sal olarak c-kit pozitif olmalarına rağmen, moleküler düzeyde imatinib tedavisine beklenen yanıtı vermezler (85). Gastrointestinal stromal tümörler için ilk tanımlanmış belirleyici olan CD34, bir hematopoetik progenitör hücre antijenidir ve endotelyal hücreler, fibroblast alt tipleri ve bu hücre tipleriyle ilişkili birçok tümörde pozitif olarak saptanabilmektedir. Tüm GİST lerin %40-82 inde CD34 pozitifliği mevcuttur ve bu parametre tümörün c-kit negatif veya pozitifliği ile ilişkili değildir (1,5,25,41,43,52,68,86-90). Özefagus ve rektum yerleşimli GİST lerde, gastrik ve ince barsak yerleşimli olanlara göre daha sık CD34 pozitifliği görülür (25). ICC yönünde diferansiyasyon uyarısı almış kök hücrenin tümör olma yolundaki ilk uyarıyı alma zamanı, tümörün davranışını belirleyen önemli bir noktadır. Buna ilaveten malign davranışlı GİST ler, benignlere oranla daha yüksek oranda CD34 ekspresyonu göstermektedirler. Bu özellik malign GİST lerin, ICC yönünde diferansiyasyon uyarısı almış daha primitif özelliğe sahip kök hücreden geliştiğini destekleyen bir bulgudur (91). Gastrointestinal stromal tümörlerin yaklaşık %30 u SMA, kalponin ve h-caldesmon gibi kas belirleyicileri eksprese ederler (86). CD34 immünreaktivitesinin aksine özellikle gastrik ve ince barsak tümörlerinde SMA pozitifliği görülür. Hem CD34, hem de SMA pozitifliği gösteren bir GİST olgusunda, bu belirteçlerin pozitif olduğu alanların, birbirinden farklı odaklar olduğu özellikle vurgulanarak, aynı primitif hücrenin farklı iki yönde diferansiasyonuna delil olarak gösterilmektedir (25). Çizgili kasa özgü intermediate filaman proteini olan desmin, özefageal tümörlerde relatif olarak daha sık pozitif olmakla birlikte, tüm bölgelerdeki GİST lerde desmin pozitifliği oldukça nadirdir (25). Epiteloid tiplerde daha belirgin desmin ekspresyonu görülebilir (2). 18
23 Enteresan olarak, imatinib mesilat tedavisi, nadir GİST vakalarında desmin ekspresyonunu arttırabilir (86). Gastrointestinal stromal tümörlerde S100 protein ekspresyonu oldukça nadirdir. Olguların sadece %5 inde fokal S100 immünreaktivitesi görülebilir. Diğer bölgelerdeki GİST lere göre, ince barsak tümörlerinde S100 ekspresyonu daha sıktır (90). Bu tümörler nörofilaman protein ve glial fibriller asidik protein gibi diğer nöral antijenlerle genellikle negatiftir. Kök hücrelerin çoğunda bulunan, tip VI intermediate filaman protein olan nestin, GİST lerin çoğunda eksprese edilir. Ancak Gİ schwannomlar gibi, diğer Gİ mezenkimal tümörlerdede nestin pozitifliği gösterirler (92,93). Bcl2 ekspresyonu GİST lerin %80 inde görülür (2). Çoğu mezenkimal tümörlerde olduğu gibi, GiST lerde vimentin ile pozitif reaksiyon gösterirler (25). Ayrıca GİST lerin küçük bir kısmı, fokal sitokeratin 8 ve 18 immünreaktivitesi gösterirler ki, bu durum epiteloid GİST ve karsinom ayırıcı tanısında karmaşa yaratması açısından önemlidir (92). Keratin 18 pozitifliği malign GİST lerde daha sık rastlanır. Ancak bu tümörlerde keratin 7, 13, 14, 17, 19, 20 negatiftir (45). Gen Analizleri Klinikopatolojik farklılıklarına rağmen, GİST lerin çoğu, KIT veya PDGFRA nın mutasyona (onkojenik mutasyon) uğrayarak, otonomik fonksiyon kazanmasını içeren benzer genetik profillere sahiptirler (94). Genetik haritada KIT ve PDGFRα kromozom 4q12 lokusunda yerleşmektedir ve muhtemelen gen duplikasyonlarında aynı gen ailesinden gelişim göstermektedirler. Her iki gen de, tip III reseptör tirozin kinaz ailesinden olan, büyük ölçüde homolog transmembran glikoproteinleri kodlamaktadır. Bu glikoprotein ailesinin moleküler yapısı, beş immünglobulin benzeri lup içeren ekstrasellüler (EC) bölge ile iki parçadan oluşan sitoplazmik tirozin kinaz bölgesi (TK1 ve TK2) içeren, jukstamembran (JM) alandan oluşmaktadır (Şekil 3). TK1 adenozin trifosfat (ATP) bağlanma bölgesi olup, hidrofilik kinaz ek ile, TK1 e tutunan TK2 fosfotransferaz bölgesidir. Ekstrasellüler ve sitoplazmik domainler tranmembran bölge ile birbirine bağlanır (95,96). Tirozin kinaz reseptörleri normalde ligandları (SCF ve PDGF: platelet derived growth factor) ile bağlanarak aktive olurlar. Bu ligandlar yukarıda sözü edilen reseptörlerin EC domain lerine bağlanarak, reseptörün dimerizasyonunu sağlar ve bu sayede sitoplazmik TK domain lerindeki tirozinler fosforillenir. Tirozinlerin fosforilasyon kaskadı, Ras/MAP kinaz, Rac/Rho-JNK, PI3K/AKT ve SKF/STAT gibi sinyal ağlarını içeren, çok sayıda sinyal 19
24 molekülünün ve sinyal transdüksiyon aktivasyon yolağının akışına neden olur (95). KIT ligand yokluğunda, KIT kinaz aktivite inhibisyonu JM domain ile kontrol edilir (97). Tirozin kinaz aktivasyonu; hücrede proliferasyon, apoptoz, kemotaksis, adezyon gibi önemli fonksiyonları düzenler ve değişik hücre tiplerinde gelişim ve onarım için kritik öneme sahiptir. Bu hücreler hematopoetik hücreler, mast hücreleri, melanositler, gametositler ve gastrointestinal sistem mobilitesi ile otonomik nöral tranmisyon migrasyonundan sorumlu ICC lerdir (95). PDGFRα; Platelet derived growth factor α, L; Ligand, P; Protein Şekil 3. Reseptör tirozin kinaz aktivasyon şeması (95) 20
25 İmmünofenotipik, ultrastrüktürel ve hücre sinyal benzerliklerine dayanarak, GİST lerin, GİST patogenezinde ilk basamak olduğuna inanılan, c-kit pozitif ICC progenitör hücrelerin KIT veya PDGFRα somatik mutasyonları ile oluştuğuna inanılmaktadır (84,94). İlginç olarak ailesel GİST olgularında, tümör dışı alanlarda, poliklonal karakterde ICC hiperplazilerinin varlığı dikkat çekicidir. Bu poliklonal odakların, GİST için prekürsör lezyon olduğu ve tümöre dönüşüm için PDGF ve KIT dışı bir başka mutasyon varlığını öne süren hipotetik görüşler mevcuttur (98). Gastrointestinal stromal tümörlerde KIT ve PDGFRα mutasyonları iki kategoride incelenebilir (95) : 1)Tirozin kinaz (TK) inhibitörleri ile tedaviden önce saptanmış mutasyonlar (primer KIT ve PDGFRα mutasyonları) 2)Tedavi sırasında, TK inhibitörlerine bağlı rezistans gelişmesine neden olan mutasyonlar (sekonder KIT ve PDGFRα mutasyonları) Tüm GİST olgularının %80-92 sinde KIT mutasyonu, %5-14 ünde PDGFRα mutasyonu saptanırken, kalan düşük oranlardaki GİST vakalarında hiçbir mutasyon mevcut değildir (wild tip-wt) (68,90,95,99-101). KIT mutasyonu görülen vakalar JM domaindeki (ekson 11) genetik defektlerdir ve sıklıkla nokta mutasyonu veya delesyon şeklinde görülmektedir. GİST lerde en sık mutasyon KIT ekson 11 de görülmekle birlikte, %5-18 sıklıkta ekson 9 da, % sıklıkta ekson 13 ve 17 de mutasyonlar görülmektedir ( ). Platelet derived growth factor receptor α geninde en sık saptanan mutasyon lokusları sırası ile, ekson 18, 12 ve 14 tür (68, 105). PDGFRα mutasyonuna sahip tümörlerin çoğu, primer olarak midede yerleşim gösterirken, KIT mutasyonu saptanan vakalar Gİ sistemin herhangi bir yerinde gelişebilir (105). Bununla birlikte PDGFRA mutasyonlu tümörler, daha çok epiteloid fenotipte olup, KIT mutant tümörler kadar güçlü CD117 boyanması göstermezler (106,107). Ancak mutasyon içermeyen wild-type genotipindeki vakalar ile PDGFRα mutant vakaları da içeren GİST lerin, yaklaşık %95 inde CD117 ekspresyonu görülür. Bazı vakalarda bu ekspresyon fokal ve zayıf olabilir. Sık karşılaşılan yanlış anlaşılmalara karşın belirtilmelidir ki, GİST lerde mevcut olan KIT mutasyonu, c-kit ekspresyonuna neden olmaz, fakat KIT fonksiyonunu modifiye eder (83). Wild tip GİST olgularında, klinikopatolojik olarak ayırıcı olan karakteristik bir özellik bulunmamakla birlikte, tirozin kinaz inhibitörlerine zayıf yanıt mevcuttur. Ayrıca GİST gelişme riski artmış olan, nörofibromatozis 1 (NF1) hastalarında varolan tümörlerde 21
26 çoğu çalışmada, KIT-WT ve PDGFRα-WT genotipi saptanmıştır (A35). NF1 hastalarında genetik olarak nörofibromin inaktivasyonu görülür. Nörofibromin, Ras-MAP kinaz kaskadını süprese eder. Bu yüzden NF1 hastalarında, Ras-MAP kinaz kaskad hiperaktivasyonu nedeniyle GİST gelişir (108). YENİ GELİŞMELER Gastrointestinal stromal tümörlerin efektif tedavisindeki gelişmeler ve farlılıklar nedeni ile bu tümörlere doğru tanı konabilmesi klinik açıdan oldukça önem arz etmektedir. GİST lerin çoğu, tümör lokalizasyonu, histolojik görünüm ve immünohistokimyasal olarak c- kit pozitifliği kombinasyonu temel alınarak tanımlanabilmektedir. Ancak GİST lerin önemli bir bölümünde (~%4-15), şüpheli veya negatif saptanan c-kit ekspresyonu, tanıda tereddütlere neden olabilir. Mutasyon statülerinin değerlendirilebilmesi ise hem her merkezde mümkün olamamakta, hem de yüksek maliyetlere neden olmaktadır. Bu amaçla tanıda yardımcı olacak, rutin pratikte kullanılabilir, yeni yöntemler araştırılmaktadır (41,109). Günümüzde, DOG1 olarak isimlendirilen, hipotetikal protein kodlayan, yumuşak doku tümörleri çalışmalarında, özellikle GİST lerde spesifik overekspresyonu saptanan, yeni bir gen bulunmuştur ( ). Bu gen, insan kromozomu 11q13, CCND1-EMS lokusunda tariflenmektedir (113,114). DOG1, 26 ekson içererek, yaklaşık 114 Kb boyut ile 960 aminoasitlik bir protein kodlar. Temel DNA sekans analizlerinde, bu proteinin 8 transmembran domaini tespit edilmiştir. Fonksiyonu bilinmemektedir, ancak yüksek sayıdaki transmembran zonları, bir iyon kanalı olduğunu düşündürmektedir (113,115). Daha yeni çalışmalarda ise, ilk hipotezler ile uyumlu olarak, TMEM16A (transmembran protein 16A) ismi ile tariflenen bu genin ürününün, bir kalsiyum bağımlı klor kanal proteini olduğu saptanmış ve ANO1 (anoktamin 1) olarak yeniden isimlendirilmiştir (45,116,117). İnsan DOG1 proteini, fare DOG1 proteini ile yüksek derecede homologdur (%89). 11q13 lokusu, baş-boyun skuamöz hücreli karsinomları, mesane tümörleri ve meme kanserleri gibi bir çok tümörde de amplifiye olmaktadır ( ). Buna ilaveten son çalışmalarda, özellikle papilloma virüs ile ilişkili olmayan, özefagus ve baş-boyun bölgesinin skuamöz hücreli karsinomlarında kötü prognoz göstergesi olduğu bildirilmektedir ( ). Henüz sınırlı sayıdaki yeni birkaç çalışmada, mutasyon statüsü fark etmeksizin, tüm GİST lerde DOG1 in sensitif ve spesifik bir immün belirleyici olduğu savunulmaktadır ( , ). Miwa ve ark. (111) nın bu konuyla ilgili yayınında, çalışılan 10 GİST vakasının tümünde, DOG1 ile pozitif immünreaktivite gösterilirken, olguların 4 üne, 22
27 DOG1 in 26 eksonunun hepsi için genetik analiz uygulanmış, hiçbirinde mutasyon saptanmamıştır. Bu sonuca dayanarak, DOG1 in, füzyon, amplifikasyon, otokrin ve parakrin stümülasyon gibi gen mutasyon yollarından farklı bir mekanizma ile aktive olduğu düşünülmüştür (111). Espinosa ve ark. (112) nın çalışmalarında ise, DOG1 in rutin uygulamada ayırıcı tanı panelinde yer alması, özellikle c-kit negatif olguların doğru tanı almasını sağladığı bildirilmektedir. Aynı zamanda DOG1 in, c-kit pozitif olgularda da tanıyı destekleyen alternatif bir belirleyici olabileceği vurgulanmaktadır (112). Platelet derived growth factor receptor α da c-kit gibi, reseptör tirozin kinaz III ailesindendir (125). KIT mutasyonunda yoksun ama PDGFRα mutasyonuna sahip GİST vakalarının tespiti ile, immünohistokimyasal olarak PDGFRα ile yapılan çalışmalar artmaya başlamıştır (126,127). Ancak bu konuda immünohistokimyasal bilgiler hala kısıtlıdır ve CD117 eksresyonu ile mutasyonel statü arasındaki ilişki henüz net belirlenememiştir (128). Peterson ve ark. (128) nın çalışmalarında, hem PDGFRα, hem de KIT mutant GİST lerde, immünohistokimyasal olarak PDGFRα ile güçlü pozitif reaksiyon saptanmıştır. Aynı çalışmada PDGFRα-pozitif GİST lerde, CD117 ile de pozitif reaksiyon görülmüştür (128). Rossi ve ark. (129) nın yayınlarında da, özellikle CD117 ekspresyonu saptanamayan GİST vakalarının tümünde (8/125), İHK sal PDGFRα pozitifliği saptanmış olup, bu antikorun kullanımının diğer gastrointestinal mezenkimal tümörler ile ayırıcı tanıda yardımcı olabileceği belirtilmiştir. Daha yeni çalışmalarda ise, ticari olarak PDGFRα için sağlanabilen antikorların yoğun zemin boyama yapması ve standartizasyonunun sağlanamaması nedeniyle parafin kesitler için rutin pratikte kullanışlı olmadığı bildirmektedirler (49,121). Hücre proliferasyon, diferansiyasyon ve motilitesinde rol oynayan, bir serin/treonin kinaz molekülü olan, protein kinaz C theta (PKCӨ) ile GİST olgularında yeni çalışmalar son yıllarda dikkati çekmektedir. KIT/SCFR tirozin kinaz aktivitesinin kontrolü ve sellüler yanıtın düzenlenmesinden PKCӨ sorumludur. PKCӨ nın, c-kit-negatif GİST ler de dahil olmak üzere, tüm GİST olgularında aktive olduğu gösterilmiştir (49,130,131). Kim ve ark. (132) nın çalışmalarında, PKCӨ nın, GİST tanısında sensitif ve spesifik bütünleyici bir immünohistokimyasal belirteç olduğu öne sürülmüştür. Lee ve ark. (133) nın makalesinde ise, PKCӨ nın sensitif bir belirteç olduğu, ancak KIT-negatif GİST lerde ekspresyonunun düşük olması ve bazı GİST dışı vakalarda da eksprese edilmesi nedeniyle tanısal değerinin sınırlı olduğu belirtilmiştir. Son yayınlarda da, GİST tanısında İHK sal yöntem ile PKCӨ kullanımının rutin pratikte uygun olmadığı bildirilmiştir (131, ). 23
28 PROGNOZ Bindokuzyüzseksenlerden beri yayınlanan bir çok makalede, GİST lerde klinik davranış ve histolojik özellikler arasında korelasyon kurulmaya çalışılmıştır. Belirlenen bir çok özellik, klinik gidiş ile uyumlu olarak korelasyon göstermekle birlikte, bazı vakalar uygulamada bu korelasyonu bozmaktadır. Nadir özel durumlarda, histolojik olarak benign görünümlü tümörlerin, klinik olarak malign davranış sergileyebildiği görülmüştür. Bazı otörler, histolojik özellikler temel alınarak, bu tümörlerin büyük çoğunluğunun, benign veya malign olarak gruplanabileceğini savunurken, diğer bir grup ise bu tümörlerin hepsinin en azından düşük malign potansiyelli tümörler olarak değerlendirilmesi gerektiğini önermektedir (1). İmatinib mesilat ajanının, GİST olgularının tedavisindeki başarı oranı göz önüne alındığında, bu tümörlerin tam ve doğru tanı alması yönündeki önemi bir kez daha ortaya çıkmaktadır. Bu nedenle National Institutes of Health (NIH), 2001 yılının nisan ayında, tüm GİST ler için morfolojik özellikler esas alınarak, tanı koyma ve prognoz değerlendirmede başvurulabilecek bir konsensus yayınladı (41). Bu GİST çalışma grubunun belirlediği, GİST lerde agresif davranış risk tanımlaması Tablo 4 te özetlenmiştir (41). Tablo 4. National Institutes of Health gastrointestinal stromal tümör çalışma grubu 2001: Agresif davranış risk tanımlaması (41) RİSK BOYUT MİTOZ (50 BBA) Çok düşük risk <2 cm <5 Düşük risk 2-5 cm <5 Orta risk Yüksek risk BBA; Büyük büyütme alanı. <5 cm cm <5 >5 cm >5 >10 cm Herhangi mitotik oran Herhangi boyut >10 Özetle, bu tümörler tümör boyutu (en büyük tek boyut) ve mitoz sayısı (50 BBA nındaki mitoz sayısı) esas alınarak, çok düşük risk, düşük risk, orta risk ve yüksek risk olarak tanımlanmıştır. Şüphesiz ki, relatif olarak basit ve objektif iki parametreden oluşan bu 24
29 yaklaşım geliştirilebilir. Ayrıca bu gruplamada, değişik anatomik bölgelerde yerleşim gösteren GİST ler arasındaki farklılıklar göz önünde bulundurulmamıştır. Daha yeni olarak, Armed Forces Institute of Pathology tarafından yayınlanan daha geniş birkaç klinikopatolojik çalışma, bu tümörlerin biyolojisini anlamada önemli bilgiler sağladı (68,83,90). Bu çalışmalarda, tümör yerleşim yerine göre inceleme esas alınarak, değerlendirmeye tümör lokalizasyonu da eklendi. Değerlendirmede tümör boyutu ve mitotik aktivitenin esas alınmasına devam edilerek, kriterler mide ve ince barsak için değiştirildi. Bu temel çalışmalara dayanarak modifiye edilen prognoza yönelik yeni sınıflama, klasik kitaplarda yerini almıştır (Tablo 5) (1). Tablo 5. Mitotik indeks, boyut ve anatomik bölgeye göre gastrointestinal stromal tümör risk sınıflaması (1) Tümör Parametreleri Progresif Hastalık Riski* (%) Mitoz 5 50 BBA da Mitoz >5 50 BBA da Boyut Mide Duodenum Jejunum/İleum Rektum 2 cm Risk yok (%0) Risk yok (%0) Risk yok (%0) Risk yok (%0) >2 cm ve 5 cm >5cm ve 10 cm Çok düşük risk (%1,9) Düşük risk (%3,6) >10 cm Orta risk (%10) Düşük risk (%8,3) Yetersiz bilgi Yüksek risk (%34) Düşük risk (%4,3) Orta risk (%24) Yüksek risk (%52) Düşük risk (%8,5) Yetersiz bilgi Yüksek risk (%57) 2 cm Risk yok Yetersiz bilgi Yüksek risk Yüksek risk (%54) >2 cm ve 5 cm >5 cm ve 10 cm Orta risk (%16) Yüksek risk (%55) >10 cm Yüksek risk (%86) Yüksek risk (%50) Yetersiz bilgi Yüksek risk (%86) Yüksek risk (%73) Yüksek risk (%85) Yüksek risk (%90) * Metastaz veya tümör nedenli ölüm, Az sayıda vaka, BBA; Büyük büyütme alanı. Yüksek risk (%52) Yetersiz bilgi Yüksek risk (%71) Ancak bazı literatürlerde, tümör boyutu ve mitoz oranının, uzun vadeli ve doğru prognozu belirlemek için yeterli olmadığı savunulmaktadır (136). Bu yayınlara göre, tümör 25
30 davranışını belirlemede sadece tümör boyutu, lokalizasyonu ve mitoz oranına bağlı kalmayıp, daha geniş, kapsamlı verilerin (mukozal invazyon, yaş, nekroz, atipi, hücre tipi vb) kullanılması önerilmektedir (Tablo 6) (2). Tablo 6. Gastrointestinal stromal tümörlerde Prognostik Faktörler (2) Tümör lokalizasyonu Tümör boyutu Metastaz varlığı Mukozal invazyon Hasta yaşı Mitotik indeks (proliferasyon indeksi) Nekroz Sitolojik atipi, sellülarite, nükleer pleomorfizm Atipik mitoz Sitomorfoloji (epitelyal, iğsi vs) Stroma natürü KIT veya Platelet derived growth factor receptor α mutasyon statüsü 1p36 heterozigosite kaybı TEDAVİ Tümörün tümüyle rezeksiyonu ve gerekliyse çevre dokularla birlikte çıkarılmasının hedeflendiği cerrahi prosedür tedavide esastır. Ancak komple cerrahi rezeksiyon sonrasında da, çoğu malign GİST lerde rekürrens görülür. Cerrahi tedavide başarılı olunamayan vakalarda, tümör primer bölgesinde nüks ve yayılım gösterebilir veya periton, omentum, karaciğere ve overe infiltre olabilir (137,138). GİST ler nadiren abdominal kavite dışına metastaz yaparlar. Rekürrens ilk 2 yılda görülmekle birlikte, düşük dereceli tümörlerde uzun yıllarca rekürrens görülmeyebilir (2). Son on yıla kadar diğer tedavilerin (kemoterapi veya radyoterapi gibi) efektif olmadığı biliniyordu. Ancak c-kit ve PDGFRα reseptörlerinin her ikisinde de, tirozin kinaz aktivitesinin inaktivasyonunu hedefleyen tedavi modellerinin kullanıma girmesi hasta prognozunu geliştirmiştir. İmatinib, c-kit in tirozin kinaz aktivitesinin, selektif adenozin trifosfat (ATP) kompetitif inhibitörüdür. Bu ajan proliferasyonu azaltarak, apoptozu indükler (139). U.S. Food and Drug Administration bu ilacın kullanımına rezeksiyon yapılamayan veya metastatik GİST lerde onay vermektedir (1). İmatinib tedavisi alan, metastatik GİST li hastaların %60 ından fazlasında, tümör volümünde %70 ila %90 arasında azalma ile uzun süreli yanıt alınmıştır (140). Bir başka 26
31 literatürde ise, bu ilacın genellikle iyi tolere edildiği ve hastaların %50 den fazlasında en azından parsiyel yanıt alındığı ve kalan %25-30 unda hastalığın stabilleştiği bildirilmiştir (141). İmatinib tedavisine yanıt vermiş ve daha sonra rezeke edilmiş GİST lerde histolojik olarak, yaygın likefaksiyon ve hyalinizasyon alanlarının yanı sıra, miksoid dejenerasyon göstererek, hiposellüler karakter kazandığı bildirilmektedir. Hiposellüler görünüm alan neoplazi CD117 immünreaktivitesini kaybetmez (1). İmatinib efektifliği ve hastalık kontrol süreci mutasyon tipi veya KIT mutasyon lokalizasyonu ile korele olabilir. Exon 11 mutasyonlu tümörlerin %80 i imatinib tedavisine sensitiftir (142). KIT in ATP yi bağlayan bölgesini içeren, ekson 14 de nokta mutasyon içeren tümörler de imatinib sensitivitesi gösterirler (143). Buna karşılık, kinaz katalitik alanını etkileyen, KIT-D816V mutasyonu, imatinib bağlanma bölgesi ile çatışarak, ilaç inefektifliğine neden olur (144). Ekson 9 mutasyonlu tümörlerin sadece %50 si imatinib tedavisine yanıt verirken, mutasyon içermeyen tümörlerin %20 sinde parsiyel yanıt görülür. Kinaz alanı 1, missense mutasyonları ile KIT-Del /T670I veya KIT-Ins /V654A mutasyonu taşıyan hücreler ise imatinib rezistandır (2,145). Platelet derived growth factor receptor α gen mutasyonlarındaki lokalizasyonlar da imatinib sensitivitesini etkiler. Ekson 18 in D842 kodonunu içeren yer değiştirme mutasyonlarının çoğu isoformu (D842V, RD KI ve D M), D842Y hariç tutulursa, ilaç rezistansı gösterirler. Ekson 18 deki diğer mutasyonlar (D846Y, N84K, Y849K ve HDSN P) imatinib sensitiftir (146). Corless ve ark. (146), GİST lerin moleküler klasifikasyonunda tedaviye yönelik yeni bir öneri sunmuştur (Tablo 7). Günümüzde, süregelen tedavi sırasında, bazı GİST hastalarında gelişen imatinib rezistansı aydınlığa kavuşmuştur. Rezistansın iki formu görülebilir; tanı anında rezistan olanlar (primer rezistans) veya öncesinde ilaçtan yarar görürken, sonrasında kazanılmış rezistans (sekonder rezistans). KIT ekson 11 de mutasyonu olup, imatinib tedavisine yanıt alınmış olguların bir kısmında, sonradan ilaca yönelik sekonder rezistans gelişmekte ve bu olguların %46 sında ikinci bir mutasyon varlığı saptanmıştır. Saptanan bu sekonder mutasyonların önemli kısmı ekson 17 de lokalizedir. Daha az oranlarda ekson 13 ve 14 te de mutasyon olabilir (145,147). Agresif seyirli tümörlerde aynı zamanda kazanılmış PDGFRα- D842V mutasyonu gösterilebilir (2). 27
32 Tablo 7. Sporadik gastrointestinal stromal tümörlerde tedaviye yönelik moleküler klasifikasyon (2) GİST mutasyon tipi Yorumlar KIT mutasyon Ekson 11 Ekson 9 Ekson 13 Ekson 17 İmatinibe en iyi yanıt İmatinibe orta dereceli yanıt İmatinibe in vitro sensitif; klinik gözlem devam ediyor İmatinibe in vitro sensitif; klinik gözlem devam ediyor PDGFRα mutasyon Ekson 12 İmatinibe in vitro sensitif; klinik gözlem devam ediyor Wild tip İmatinibe zayıf yanıt GİST; Gastrointestinal stromal tümör, PDGFRα; Platelet derived growth factor receptor α. Klinik açıdan önemli bir nokta ise, KIT veya PDGFRα reseptörlerinin her ikisine de cevapsız, ilaç rezistansı gösteren tümörlerin nasıl tedavi edileceğidir. Son zamanlarda, imatinib insensitivitesi gösteren bazı tümörler için, c-kit i de içeren çeşitli tirozin kinazların ATP bağlanan bölgelerini hedef alan yeni ilaçlar geliştirilmiştir (148). Örneklemek gerekirse, yeni bir kinaz inhibitörü olan SU11248 (sunitinib malate), daha geniş bir aktivite spektrumu göstererek, mutatik KIT veya PDGFRα nın aktivasyonunu inhibe eder. Bununla birlikte bu molekül vasküler endoteliyal büyüme faktör (VEGF) reseptörü inhibisyonunu sağlayan, güçlü bir antianjiogenik ajandır. Bu ilacın klinik denemeleri hala devam etmektedir (148). 28
33 GEREÇ VE YÖNTEMLER Bu çalışmada, Trakya Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı rapor arşivinden, yılları arasında tanı almış, Gastrointestinal Stromal Tümörler tarandı. Buna göre toplam 39 GİST olgusu tespit edildi. İki vaka çalışma dışı bırakıldı. Bu vakalardan biri mideden endoskopik biyopsi olarak gönderilmiş olup, doku yetersiz ve diğer tümör parametrelerinin (boyut, mitoz, hücresellik, nekroz, immünohistokimya gibi) sağlıklı değerlendirilmesi mümkün değildi. Diğer vaka ise konsültasyon amacı ile dış merkezden bölümümüze gönderilmiş ve tanı sonrası blokları iade edilmişti. Sonuç olarak gastrointestinal sistemde lokalize 37 GİST olgusu rezeksiyon materyali immünohistokimyasal profil açısından değerlendirmek amacı ile çalışma kapsamına alındı. Ayrıca GİST ler ile gerek lokalizasyon, gerekse morfolojik karakteristikleri açısından, karışma ihtimali olan, yumuşak doku tümörleri çalışmaya dahil edildi. Bu amaçla sinir, çizgili ve düz kas, yağ, bağ, damar, sinovyum, ganglion ve histiositik kökenli farklı mezenkimal dokulara ait arşivimizdeki, benign ve malign mezenkimal tümörler içinden, demonstratif rastgele 45 olgu seçildi. Bu 45 vakanın dağılımı; 5 i malign periferik sinir kılıfı tümörü, 5 i benign sinir doku tümörü (3 ü schwannom, 2 si nörofibrom), 5 i düz kas doku tümörü (3 ü malign, 2 si malignite potansiyeli belirsiz), 5 i malign çizgili kas doku tümörü (rabdomyosarkom), 5 i adipöz doku tümörü (4 ü liposarkom, 1 i atipik lipomatöz tümör), 5 i malign damar doku tümörü (anjiosarkom), 5 i gangliositik tümör (3 ü ganglionörom, 2 si nöroblastom), 5 i fibrohistiositik tümör, 5 i malign sinovyal doku tümörü (sinovyal sarkom) idi (Tablo 8). Bu vakaların seçiminde, özellikle batın içi lokalizasyonda olan tümörler tercih edilerek, her bir mezenkimal doku tümörü grubu için 5 vaka alındı. Ancak yeterli sayıda batın 29
34 içi lokalizasyonda vaka saptanamayan gruplara, diğer yumuşak doku bölgelerinden olgular da dahil edildi. Tablo 8. Gastrointestinal stromal tümör dışı mezenkimal tümörlerin listesi Malign Sinir Doku Tümörü Benign Sinir Doku Tümörü Düz Kas Tümörü Çizgili Kas Tümörü Adipöz Doku Tümörü Damar Tümörü Gangliositk Tümör Fibrohistiositik Tümör No Yaş/Cins Tanı Lokalizasyon 1 68/E Malign Periferik Sinir Kılıfı Tümörü Retroperiton 2 75/E Malign Periferik Sinir Kılıfı Tümörü Kol 3 55/E Malign Periferik Sinir Kılıfı Tümörü Uyluk 4 71/K Malign Periferik Sinir Kılıfı Tümörü Posterior mediasten 5 80/E Malign Periferik Sinir Kılıfı Tümörü Kruris 6 44/K Schwannom Suprarenal 7 34/K Schwannom Toraks 8 35/K Nörofibrom Mide küçük kurvatur 9 36/K Nörofibrom Omentum 10 37/K Schwannom Safra kesesi komşuluğu 11 58/K Leiomyosarkom İnce barsak mezosu 12 35/K Malignite Potansiyeli Belirsiz Düz Kas Tümörü İntrapelvik 13 60/E Malignite Potansiyeli Belirsiz Düz Kas Tümörü Mezenter 14 35/K Leiomyosarkom M.Rectus abdominis 15 84/E Leiomyosarkom Skrotal bölge 16 5/K Rabdomyosarkom, Embriyonal Tip İntra-abdominal 17 3/E Rabdomyosarkom, Botyroid Tip Mesane 18 11/K Rabdomyosarkom Retroperiton 19 61/E Rabdomyosarkom Jejunum, kolon mezosu 20 16/E Rabdomyosarkom, Embriyonal Tip Paratestiküler doku 21 51/E Miksoid Liposarkom Sol kolon, retroperiton 22 80/K İyi Diferansiye Liposarkom Retroperiton 23 77/K Atipik Lipomatöz Tümör Retroperiton 24 69/E Dediferansiye Liposarkom Aksilla 25 72/E Pleomorfik Liposarkom M.Pectoralis major 26 55/K Anjiosarkom İnce barsak, kolon 27 58/E Anjiosarkom İnce barsak, kolon 28 83/E Anjiosarkom Çekum 29 42/K Anjiosarkom Dalak 30 51/K Anjiosarkom Uterin serviks 31 4/E Nöroblastom Retroperiton 32 14/E Ganglionörom Retroperiton 33 55/K Ganglionörom Retroperiton 34 7/K Nöroblastom Kol 35 41/K Ganglionörom İntratorasik kitle 36 38/K Agresif Fibromatozis Retroperiton 37 51/K İnflamatuar Myofibroblastik Tümör Omentum 38 40/K Desmoid Tip Fibromatozis İnce barsak mezenteri 39 65/E Malign Fibröz Histiositom İnce barsak 40 54/K Dermatofibrosarkoma Protuberans Batın duvarı Sinovyal Doku Tümörü 41 32/E Sinovyal sarkom, monofazik Ayak bileği 42 33/K Sinovyal sarkom, bifazik Omuz 43 30/K Sinovyal sarkom, bifazik Akciğer 44 51/E Sinovyal sarkom, monofazik Akciğer 45 45/E Sinovyal sarkom, monofazik Kol E; Erkek, K; Kadın. 30
35 Otuzyedi GİST ve toplam 45 yumuşak doku tümörüne, standart mezenkimal tümör belirleyicileri olan, vimentin, SMA, desmin, S100 ve CD34, proliferasyon indeksini belirlemek amacıyla ki67, risk kategorizasyonu için bcl2, GİST ler için spesifik belirleyiciler olan CD117 ve PDGFRα, son yıllarda GİST ler için spesifitesi tartışılan popüler belirleyici DOG1 antikorları çalışıldı. Olgular arşivde var olan HE kesitleri ile, retrospektif olarak tekrar incelenerek, Progresif Hastalık Riski (41) temel alınarak risk kategorizasyonuna göre yeniden değerlendirildi ve buna göre revize edildi (Tablo 9). Her olgudan tümörü iyi temsil eden birer parafin blok seçilerek, İHK sal inceleme için 4 μm kalınlığında seri kesitler alındı. Uygun blok seçiminde pozitif ve/veya negatif kontrol amacıyla, tümör çevresinde, normal mezenkimal dokuların bulunmasına özen gösterildi. Çalışmaya alınan toplam 82 olgunun yaş, cins, tümör lokalizasyonu, operasyon şekli, tümör çapı, tümör tanısı ve diğer morfolojik bulguları arşivimizdeki raporlarından temin edildi. Tablo 9. Gastrointestinal stromal tümör vakalarının progresif hastalık risk dağılımı Risk Kategorizasyonu Vaka Sayısı % Risk Yok Çok Düşük Risk Düşük Risk Orta Risk Yüksek Risk Elde edilen kesitlere Avidin-Biotin Peroksidaz yöntem kullanılarak sözü edilen antikorlar uygulandı. Kullanılan antikorların spesifitesi ve özelliklerini gösterir bilgiler Tablo 10 dadır. Çalışmamız 2009/185 protokol numarası ile Trakya Üniversitesi Tıp Fakültesi Dekanlığı Etik Kurul Başkanlığı nın tarih ve 12 sayılı oturumunda görüşülmüş ve onaylanmış olup buna ilişkin yazı ekte sunulmuştur (Ek 1). 31
36 Tablo 10. Kullanılan antikorlar ve özellikleri ANTİKOR CİNS / KLON KAYNAK / KOD SÜRE DİLÜSYON Vimentin MKL-fare / V9 Biocare Medical / CM 048 A, B, C SMA MKL-fare / 1A4 Biocare Medical / CM 001 A, B, C Desmin MKL-fare / D33 Biocare Medikal / CM 036 A, B, C S100 PKL-fare / 4C4.9 CD34 MKL-fare / QBEnd/10 Ki67 MKL-tavşan / SP6 Bcl2 MKL-fare / 100/D5 CD117 PKL-tavşan / C-19 PDGFRα PKL-tavşan / C-20 DOG1 MKL-tavşan / SP31 MKL; monoklonal, PKL; poliklonal. Scy Tek / A00087 Neomarkers / MS-363-P0 Biocare Medical / CRM 325 A, B, C Thermo Scientific / MS-123-P0 Santa Cruz / sc-168 Santa Cruz / sc-338 Thermo Scientific / RM-9132-S0 45 dk 1/ dk 1/ dk 1/25 45 dk Kullanıma hazır 45 dk 1/ dk 1/ dk Kullanıma hazır 45 dk 1/ dk 1/ dk 1/50 İMMUNOHİSTOKİMYASAL YÖNTEM İmmunohistokimya; immunolojik ilkelere dayanarak, varlığı araştırılan antijenlere karşı geliştirilmiş, poliklonal veya monoklonal antikorlar aracılığı ile dokudaki antijeniteyi gösteren bir yöntemdir. Çalışmamızda indirekt immunperoksidaz yöntemi uygulanmıştır. Yöntemin Uygulanışı 1. Tümör ve tümör çevresi doğal dokuları en iyi örnekleyen kesite ait parafin bloklardan 4 μm kalınlığında kesitler yapıldı. Kesitler pozitif şarjlı lamlara alındı. 2. Kesitler 1 gece 37 C etüvde bekletilerek deparafinizasyon işlemine başlandı. 3. Deparafinizasyona ksilen ile devam edildi. Bu işlem 60 C etüvde 3 kez 10 ar dakika ksilende bekletme ve her 10 dakikanın ardından 5 er dakika solüsyon yenilenerek dışarıda soğumaya bırakma şeklinde uygulandı. 32
37 4. Ksilenin giderilmesi için %96 lık alkol muamelesine geçildi. Kesitler alkolde 60 C etüvde 4 defa her seferinde solüsyon yenilenerek, 10 ar dakika tutuldu. 5. Lamlar 3 kez distile sudan geçirildi. 6. Vimentin, SMA, desmin, S100, CD34, ki67, Bcl2, CD117, PDGFRα, DOG1 için antijen geri kazanımı işlemi yapıldı. Bu işlem için 1/10 oranında distile su ile dilue edilen (90 ml distile su + 10 ml EDTA buffer), EDTA buffer 10X ph 8,0 (Kod: 15-M820, Lot.50930) solüsyonu kullanıldı. a) CD117, PDGFRα, DOG1, Bcl2, ki67 antikorları için, kesitler antijen geri kazanım solüsyonunda mikrodalga fırında maksimum watt ta 20 dakika, 600 watt ta 10 dakika kaynatıldı. Vimentin, SMA, desmin, S100, CD34 antikorları için aynı işlem, maksimum watt ta 15 dakika tutulup 5 dakika kaynatma şeklinde uygulandı (bu antikorların datasheet lerinde mikrodalgada antijen retriaval şartı olmamasına rağmen, kullandığımız blokların nispeten büyük olması ve bazı dokuların yıllarının eski olması nedeniyle işlem uygulandı). b) Dışarıda oda sıcaklığına gelene kadar 20 dakika bekletildi. c) Lamlar 3 kez distile sudan geçirildi. 7. Dokularda bulunan endojen peroksiti bloke etmek için 10 dakika 37 0 C etüvde metanolde hazırlanmış %3 lük H 2 O 2 uygulaması yapıldı. 8. Lamlar 3 kez distile sudan geçirildi. 9. Lamlar ph 7,4 olarak hazırlanmış PBS solüsyonunda 10 dakika bekletildi. 10. Reaktiflerin kesit dışına taşmasını engellemek için lamlardaki kesitlerin etrafı Pappen ile çizildi. 11. Her bir lama Large Volume Ultra V Blok (Kod No: TA-125-UB, Neomarkers, Fremont, CA, ABD) damlatıldı ve 7 dakika bekletildi. Sonra solüsyon lamlar üzerinden PBS ile uzaklaştırıldı. 12. Her bir vaka için ayrı ayrı numaralandırılmış lamlara Vimentin, SMA, desmin, S100, CD34, ki67, Bcl2, CD117, PDGFRα, DOG1 (Tablo 10) antikorları damlatılarak oda sıcaklığında, ancak nemli ortamda ( chamber içinde) 45 dakika inkübasyon yapıldı. 13. Lamlar üzerindeki antikorlar distile su ile uzaklaştırılıp PBS solüsyonuna alınarak 5 dakika bekletildi. 14. Zemin boyanmasını engellemek için, Super Block Sensi Tek Anti Polyvalent HRP kitinin (Scy Tek, Kod. SHP 125, Utah, USA) 1 nolu Super Block (Ref: AAA125, lot ) solüsyonu damlatıldı ve 10 dakika bekletildi. 33
38 15. PBS solüsyonu ile 5 dakika yıkanan lamlara, yukarıda tanımlanan kitin 2 nolu biotine bağlanacak olan işaretleyici solüsyonu Anti-Polyvalent Biotinylated antibody, (Ref: ABF125, Lot ) damlatıldı ve 20 dakika daha bekletildi. 16. Tekrar PBS solüsyonu ile 5 dakika yıkanan lamlara, yine aynı kitin 3 nolu solüsyonu, Sensi Tek HRP Streptavidin biotinylated peroxidase-complex, (Ref: ABG125, Lot.18452) damlatıldı ve 20 dakika bekletildi. 17. Lamlar PBS ile 3 dakika yıkandı. 18. Scy Tek AEC chromogen/substrate kit (ref: ACJ 125, Lot ) (1 mililitre AEC substrat buffer + 1 damla AEC chromogen (Ref: ACD 030, Lot.18618)), damlatılarak 10 dakika bekletildi. 19. Lamlar musluk suyunda 5 dakika yıkandıktan sonra, Harris hematoksilen solüsyonunda dakika tutularak zıt boyama yapıldı. 20. Lamlar tekrar musluk suyunda yıkandı. 21. Lamlar %5 lik amonyak solüsyonunda 15 saniye tutularak, morartma işlemine tabi tutuldu. 22. Lamlar musluk suyunda yıkandı. 23. Aqueous-Mount (Ref: AML030, Lot ) kullanılarak lamel ile kapatıldı. İMMUNOHİSTOKİMYASAL DEĞERLENDİRME Çalışmaya alınan vakalar boyanmadan önce, özellikle yeni araştırma antikorlarının çalışıp çalışmadığını kontrol etmek amacıyla, katalogda belirtilen kontrol dokuları arşivden temin edilerek test boyama yapıldı. Bu amaçla, CD117 ve DOG1 için GİST, PDGFRα için ise deri ekleri içeren cilt dokuları kullanıldı. Diğer rutinde kullanılan antikorlar için ise, seçilmiş tümör bloklarının üzerinde pozitif kontrol olabilecek mezenkimal elemanların olmasına özen gösterildi. Bu antikorlardan DOG1, CD117, PDGFRα nın sitoplazmik ve membranöz, vimentin, aktin, desmin, S100, CD34, Bcl2 nin sitoplazmik, ki67 nin ise nükleer boyanma özelliği esas alındı. Çalışmaya alınan vakalar CD117, vimentin, aktin, desmin, S100, CD34, Bcl2, ki67 ile immünohistokimyasal boyanma paternlerinin ölçülmesinde kriter olarak Türk Patoloji Derneği öncülüğünde, Türkiye GİST Çalışma Grubu tarafından 2004 yılında hazırlanmış örnek kitapçık esas alındı. DOG1 ve PDGFRα araştırma antikorları değerlendirilmesi de, CD117 için literatürde kullanılan kriterler esas alınarak benzer şekilde yapıldı. 34
39 Buna göre CD117, DOG1 ve PDGFRα ekspresyonu için değerlendirme; * 0 -% 10 oranında boyanma (negatif) -Boyanma yaygınlığı * % oranında boyanma (fokal) * >% 50 oranında boyanma (diffüz) * + Hafif -Boyanma yoğunluğu * ++ Orta * +++ Kuvvetli Bu boyanma kriterlerine göre antikor pozitifliğinin değerlendirilmesi : Yaygınlık 0 - %10 ve yoğunluk + : Negatif, Yaygınlık < %50 ve yoğunluk + veya ++ : Pozitif. (Bu olgular, ikinci araştırmacı tarafından tekrar değerlendirildi. Şüphede kalınması durumunda immünohistokimyasal işlem tekrarlandı), Yaygınlık > %50 ve yoğunluk ++ veya +++ : Pozitif kabul edildi. Vimentin, aktin, desmin, S100, CD34, Bcl2 için değerlendirme yukarıda CD 117 için belirtilen boyanma yaygınlığı kritelerine benzer şekilde yapıldı. Buna göre %10 un üstü pozitif olgu olarak kabul edildi. Mitozun en yoğun olduğu bloğa ki67 antikoru çalışıldı. Nükleer boyanmanın en yoğun olduğu alanda 1000 hücre sayılarak, % olarak ifade edildi. %10 un üzerindeki değerler yüksek proliferasyon indeksi olarak kabul edildi. İSTATİSTİKSEL YÖNTEM Veriler kodlanarak bilgisayara girildikten sonra, istatistik analizleri Trakya Üniversitesi Tıp Fakültesi Dekanlığı Bilgi İşlem Merkezi nde bulunan Statistica 7.0 (Lisans No: 31N6YUCV38) programı kullanılarak yapıldı. Tanımlayıcı istatistiklerin yanısıra olgu sayısının yeterli olduğu durumlarda değişkenler arasında ilişkilerin önemlilik derecesini belirlemek için Pearson Ki Kare, Fisher Kesin Ki Kare, Spearman korelasyon ve Mann Whitney U testi ile Kruskal Wallis varyans analizi kullanıldı. P değerinin <0.05 olması anlamlı kabul edildi. 35
40 BULGULAR KLİNİK VE PATOLOJİK BULGULAR Çalışma grubunu oluşturan 37 GİST vakamızın tümü Progresif Hastalık Riski (41) temel alınarak risk kategorizasyonuna göre yeniden değerlendirilmiştir. Buna göre, 37 vakanın 1 (%2.70) i risk yok, 3 (%8.11) ü çok düşük risk, 6 (%16.22) sı düşük risk, 7 (%18.92) si orta risk, 20 (%54.05) si yüksek risk olarak sınıflandı (Tablo 9). Gastrointestinal stromal tümör vakalarımızın yaş dağılımı arasında, yaş ortalaması 57,18 olup 22 (%59.5) si kadın, 15 (%40.5) i erkekti. Kadınlardaki yaş dağılımı (ortalama yaş; 58.6), erkeklerdeki yaş dağılımı (ortalama yaş; 55.1) idi. Ayrıca kadın ve erkek olgular, progressif hastalık risk sınıflamasına göre gruplandığında, her iki cinste de sırasıyla %54.5 ve %53.3 oranlar ile yüksek risk grubunda yoğunlaşma görüldü. (Tablo 11). Gastrointestinal stromal tümör vakalarımızın 19 (%51.4) u ince barsak, 11 (%29.7) i mide, 4 (%10.8) ü kalın barsak, 3 (%8.1) ü retroperitoneal yerleşimli idi (Tablo 12). Her iki cinsiyet içinde, yüksek risk predominansı gösteren GİST vakalarında, kadınlarda primer lokalizasyon ince barsak (%63.6), erkeklerde ise 1 vaka fark ile mide (%40) öncelikli yerleşim bölgesiydi. Erkeklerde ince barsak yerleşim yüzdesi %33.3 idi (Tablo 13). 36
41 Tablo 11. Gastrointestinal stromal tümör vakalarının progressif hastalık riski ve demografik özelliklerine göre dağılım Risk G YD OY K/E EY EYO KY KYO N (%) RY / ( 2.70) ÇDR / ( 8.11) DR / (16.22) OR / (18.92) YR / (54.05) TOPLAM / ( 100) Risk G; Risk grupları, RY; Risk yok, ÇDR; Çok düşük risk, DR; Düşük risk, OR; Orta risk, YR; yüksek risk, YD; Yaş dağılımı, OY; Ortalama yaş, K/E; Kadın erkek oranı, EY; Erkek yaş aralığı, EYO; Erkek yaş ortalaması, KY; Kadın yaş aralığı, KYO; Kadın yaş ortalaması, N;Vaka sayı.ve yüzde. Tablo 12. Gastrointestinal stromal tümör vakalarının lokalizasyona göre dağılımı Lokalizasyon Vaka Sayısı % Mide İnce Barsak Kalın Barsak Retroperiton Tablo 13. Gastrointestinal stromal tümör vakalarının cinsiyete göre lokalizasyona dağılımı Lokalizasyon Kadın n(%) Erkek n(%) TOPLAM Mide 5 (45.5) 6 (54.5) 11 İnce Barsak 14 (73.7) 5 (26.3) 19 Kalın Barsak 2 (50) 2 (50) 4 Retroperiton 1 (33.3) 2 (66.7) 3 TOPLAM 22 (59.5) 15 (40.5) 37 37
42 Olgularımızda tümör çapı (ortalama çap 9.3) cm arasında değişmekteydi. Tümör lokalizasyonuna göre çap boyutu istatistiksel olarak incelendiğinde anlamlı bir fark bulunamadı, (Kruskal Wallis Varyans analizi; p>0.05), (Tablo 14) (Şekil 4-6). Tablo 14. Tümör primer lokalizasyonuna göre demografik özellikler, risk sınıflaması ve boyut dağılımı LOKALİZASYON YAŞ K/E RY / ÇDR / DR / OR / YR ÇAP(cm)* Mide (n=11) /6 0 / 3 / 3 / 2 / İnce Barsak (n=19) /5 0 / 0 / 3 / 5 / Kalın Barsak (n=4) /2 1 / 0 / 0 / 0 / Retroperiton (n=3) /2 0 / 0 / 0 / 0 / TOPLAM (n=37) /15 1 / 3 / 6 / 7 / K/E; kadın erkek, RY; Risk yok,çdr; Çok düşük risk,dr; Düşük risk, OR; Orta risk, YR; yüksek risk. *: Kruskal Wallis Varyans analizi; p= Lokalizasyonuna göre risk bakıldığında, olguların gruplara göre dağılımında vaka sayımız düşük olduğu için, yüksek risk grubu kötü prognoz göstergesi olan grup olarak seçilirken, diğer dört risk grubu tek grup halinde istatistiksel incelemeye alınmıştır ve bundan sonraki risk grupları istatistiksel incelemelerinde de bu tablo dikkate alınarak uygulanmıştır. Bu gruplamaya göre, kötü prognoza sahip olguların ağırlıklı olarak ince barsakta lokalize olduğu görüldü, (Tablo 15). Tablo 15 te izlenen grupların bazılarında sayısal değerler çok düşük olduğu için istatistiksel değerlendirme yapılamadı. Tablo 15. Risk sınıflamasına göre gastrointestinal stromal tümörlerin lokalizasyon dağılımı Mide İnce barsak Kalın barsak Retroperiton TOPLAM Yüksek Risk Grubu Diğer Gruplar Gastrointestinal stromal tümör vakalarımızda, mide lokalizasyonu erkek ve kadın olgularda neredeyse eşit sayıda görülürken, yaş dağılımı arasındadır. Mide yerleşimli vakalarımızın çapları 3 ile 16 (ortalama çap 8.7) cm arasındadır. Midedeki olgular risk 38
43 grupları açısından incelendiğinde, herhangi bir grupta yoğunlaşma yoktu. Risk yok grupta olgumuz yok iken diğer gruplara vakalar eşit sayıda dağılmıştı (Tablo 14). En genç olgumuz 23 yaşında olup, tümör lokalizasyonu ince barsaktır. İnce barsak lokalizasyonunda kadın hastaların sayısı erkek hastalara göre 2.8 kat daha fazladır. Bu yerleşim yerinde risk yok ve çok düşük risk grubundan hasta görülmez iken, yüksek risk grubundaki hasta sayısında belirgin yükseklik vardır. Risk belirlerleme parametrelerinden olan tümör çapı ince barsakta (ortalama çap 9.1) cm arasındadır (Tablo 14). Kalın barsak yerleşimindeki 1 olgu risk yok kategorisine girerken, diğer 3 olgu yüksek risk kategorisindedir (Tablo 14). Retroperitoneal alandaki 3 olgunun hepsi yüksek risk kategorisinde olup,bu olgulardan biri en büyük çapa sahip (24 cm) GİST olgumuzu oluşturmaktaydı (Tablo 14). Yüksek risk grubundaki GİST olgularının %60 ının çapı 10 cm den büyük iken, orta risk grubunda vakaların %72 sinin çapı 5 ila 10 cm arasındadır. Düşük risk grubundaki vakaların çapları 2-10 cm arasında dağılım gösterirken, çok düşük risk grubundaki vakaların tümü 2-5 cm arasındadır. Risk negatif grubundaki 1 vakanın boyutu 2 cm den küçüktür. Yüksek risk grubu dışındakileri tek grup halinde incelediğimizde çapı 5 cm üzerinde olan 26 olgunun 17 si yüksek risk grubuna dahiledildi ve yüksek risk grubundaki olguların çap ortalaması, diğerlerinin çap ortalamasından anlamlı düzeyde yüksek bulundu, (Mann Whitney U testi; p= 0.007), (Tablo 16). Tablo 16. Risk sınıflamasına göre gastrointestinal stromal tümör vakalarının çap dağılımı Risk Kategorizasyonu Mann Whitney U testi; p= n Çap (cm) - n (%) 2 >2 ve 5 >5 ve 10 >10 Risk Yok 1 1(%100) 0(%0) 0(%0) 0(%0) Çok Düşük Risk 3 0(%0) 3(%100) 0(%0) 0(%0) Düşük Risk 6 0(%0) 3(%50) 3(%50) 0(%0) Orta Risk 7 0(%0) 1(%14) 5(%72) 1(%14) Yüksek Risk 20 0(%0) 3(%15) 5(%25) 12(%60) 39
44 Progresif hastalık risk sınıflamasına göre yapılan kategorizasyonda, risk yok, çok düşük risk ve düşük risk grubu, 10 GİST vakasının tümünde 50 BBA da 5 ten az mitoz sayılmıştır. Orta risk grubundaki 7 olgunun 1 (%14) inde, yüksek risk grubundaki 20 olgunun ise 18 (%90) inde, 50 BBA da 5 ten fazla mitoz sayılmıştır. Yüksek risk grubu dışındakileri tek grup halinde kabul ederek sınıflama yapıldığında yüksek risk grubunda 50 BBA ndaki ortalama mitoz sayısı 21.9 iken, diğer grupların tümünde bu sayı 3.1 olarak saptanmış ve istatistiksel olarak anlamlı bulunmuştur, (Mann Whitney U testi; p=0.000), (Tablo 17). Tablo 17. Gastrointestinal stromal tümör vakalarında risk sınıflamasına göre mitoz oranları Risk Kategorizasyonu n Mitoz / 50BBA n (%) 5 >5 Risk Yok 1 1 (%100) 0 (%0) Çok Düşük Risk 3 3 (%100) 0 (%0) Düşük Risk 6 6 (%100) 0 (%0) Orta Risk 7 6 (%86) 1 (%14) Yüksek Risk 20 2 (%10) 18 (%90) BBA; Büyük büyütme alanı. Mann Whitney U testi; p=0.000 Risk grupları ile tümör çapı ve mitoz sayısı arasındaki ilişki Spearman korelasyon analizi ile değerlendirildiğinde, risk grubu yükseldikçe, tümör çapı büyümekte (r=0.523, p=0.001) ve mitoz sayısı artmaktadır (r=0.798, p=0.000) ve bu sonuç anlamlı bulunmuştur. Pür iğsi hücreli tümörlerde, 50BBA daki mitoz sayısı, 5 ve >5 mitoz gruplarında eşit oranda dağılım göstermektedir. Pür epiteloid morfolojideki 1 GİST vakasında, mitoz sayısı 50 BBA nda 5 ten fazladır. Hem iğsi hem de epiteloid hücre morfolojisini içeren mikst tümörlerin ise %88 inde 50 BBA nda 5 ten fazla mitoz sayılmıştır (Tablo 18). Pür iğsi hücreli GİST olgularının %55 i ve mikst hücreli GİST olgularının %50 si yüksek risk grubunda idi (Tablo 18). Sitolojik atipinin belirgin olduğu 18 vakanın hepsinde belirgin hücresellik dikkati çekmiştir. Hafif sitolojik atipi içeren vakaların %79 unda da yine belirgin hücresellik mevcuttur. Fischer kesin χ 2 testi uygulamasında bu durum anlamlı bulunmamıştır, (p>0.05), (Tablo 19). 40
45 Tablo 18. Gastrointestinal stromal tümör hücre morfolojisine göre risk sınıflaması ve mitoz oranı HÜCRE TİPİ Risk Yok RİSK KATEGORİZASYONU* n (%) Çok Düşük Orta Düşük Risk Risk Risk Yüksek Risk MİTOZ / 50 BBA n (%) 5 >5 İĞSİ 1 (%5) 1 (%5) 3 (%15) 4(%20) 11 (%55) 10 (%50) 10 (%50) EPİTELOİD 0 (%0) 0 (%0) 0 (%0) 0 (%0) 1 (%100) 0 (%0) 1 (%100) MİKST 0 (%0) 2(%12) 3(%19) 3(%19) 8 (%50) 1 (%12) 7 (%88) BBA; Büyük büyütme alanı. *: Fischer kesin χ 2 ; p=0.765 Sitolojik atipinin belirgin olduğu vakaların %72 si yüksek risk grubuna girerken, çok düşük risk ve risk yok grubunda sitolojik atipi hafiftir. Buna karşın hafif sitolojik atipi içeren vakaların %37 si yüksek risk grubuna dahil olmuştur. Sitolojik atipi ve risk grupları arasındaki ilişki istatistiksel olarak anlamlı bulunmuştur, (Pearson χ 2 =4.659, p=0.031), (Tablo 19). Olgulara ait mikroskopik özellikler Şekil 7-11 de izlenmektedir. Tablo 19. Gastrointestinal stromal tümör vakalarında sitolojik atipiye göre hücresellik ve risk sınıflaması SİTOLOJİK ATİPİ HÜCRESELLİK* RİSK KATEGORİZASYONU** Çok Düşük Risk Düşük Orta Yüksek Az Belirgin Risk Yok Risk Risk Risk HAFİF 4 (%21) 15 (%79) 1 (%5) 3 (%16) 4 (%21) 4 (%21) 7 (%37) BELİRGİN 0 (% 0) 18(%100) 0 (%0) 0 (% 0) 2 (%11) 3 (%17) 13 (%72) *: Fischer kesin χ 2 ; p=0.059, **: Pearson χ 2 =4.659, p= Sitolojik atipi (hafif/belirgin) ile mitoz sayıları ( 5 veya >5) kendi aralarında kıyaslandığında, mitoz sayısı 5 ten fazla olan vakalarda belirgin atipi diğer gruba göre daha fazla bulundu ve bu sonuç istatistiksel olarak anlamlı idi, (Pearson χ 2 =6.112, p=0.013), (Tablo 20). Mukozal invazyon varlığı ile mitoz sayıları kıyaslandığında anlamlı fark mevcut değildi (Pearson χ 2 =1.668, p=0.19). Gastrointestinal stromal tümör olgularında tümörde kanama, düşük risk ve orta risk grubundaki vakaların tümünde mevcuttu. Yüksek risk grubundaki vakaların ise %80 inde tümörde kanama tespit edildi, (Fischer kesin χ 2 ; p>0.05), (Tablo 21). 41
46 Tablo 20. Gastrointestinal stromal tümör olgularında sitolojik atipi ve mitoz sayılarının kıyaslanması Mitoz 5/50BBA Mitoz >5/50BBA Toplam Hafif sitolojik atipi Belirgin sitolojik atipi Toplam BBA; Büyük büyütme alanı, Pearson χ 2 =6.112, p=0.013 Yüksek risk grubundaki GİST vakalarının %40 ında, makroskopik ve mikroskopik incelemede, yüzey mukozasında ülserasyon mevcut iken, düşük ve çok düşük risk grubundaki 1 er vakada ülser saptandı, (Fischer kesin χ 2 ; p>0.05), (Tablo 21). Gastrointestinal stromal tümörlerde yüksek risk grubundaki olgulardan %85 inde (17 vaka) tümörde nekroz gözlenirken, diğer grupların toplamında bu oran %52.9 dur. Aradaki fark istatistiksel olarak anlamlıdır, (Pearson χ 2 =4.521, p=0.033), (Tablo 21). Tablo 21. Risk gruplarına göre, gastrointestinal stromal tümörlerde izlenen morfolojik patolojik parametreler Risk KANAMA n(%)* ÜLSER n(%)** NEKROZ n(%)*** Kategorizasyonu Yok Var Yok Var Yok Var Risk Yok 1(% 100) 0 (% 0) 1 (% 100) 0 (% 0) 1 (%100) 0 (% 0) Çok Düşük Risk 2 (% 67) 1 (% 33) 2 (% 67) 1 (% 33) 2 (% 67) 1 (% 33) Düşük Risk 0 (% 0) 6 (% 100) 5 (% 83) 1 (% 17) 3 (% 50) 3 (% 50) Orta Risk 0 (% 0) 7 (% 100) 7 (%100) 0 (% 0) 2 (% 29) 5 (% 71) Yüksek Risk 4 (% 20) 16 (% 80) 12 (% 60) 8 (% 40) 3 (% 15) 17 (% 85) *: Fischer kesin χ 2 ; p=0.596, **: Fischer kesin χ 2 ; p=0.058, ***: Pearson χ 2 =4.521, p= Gastrointestinal stromal tümörlerin risk gruplarına göre, primer lokalizasyonlarında gösterdikleri duvar invazyonu incelendiğinde, bazı otörlere göre (2) prognostik faktör olarak kabul edilen mukozal invazyon, en çok yüksek risk grubunda (10/20, %50) saptandı. Bununla birlikte, çok düşük ve düşük risk grubunda da 1 er vakada mukozal invazyon görüldü. Tüm risk grupları dikkate alındığında, tümör yoğun olarak submukoza, muskuler tabaka ve serozada invazyon göstermekteydi. Çevre organlara invazyon yine en yüksek oran ile yüksek risk grubunda (8/20, %40) saptanırken, orta risk grubundaki 1 vakada da omentum invazyonu görüldü (Tablo 22). 42
47 Tablo 22. Risk gruplarına göre gastrointestinal stromal tümörlerin invazyon alanları RİSK MUKOZA SUBMUKOZA MUSKULER ÇEVRE SEROZA GRUPLARI TABAKA DOKU RY 0/1 1/1 0/1 0/1 0/1 ÇDR 1/3 3/3 2/3 0/3 0/3 DR 1/6 5/6 6/6 6/6 0/6 OR 0/7 5/7 5/7 6/7 1/7 YR 10/20 15/20 16/20 18/20 8/20 TOPLAM 12/37 29/37 29/37 30/37 9/37 RY; Risk yok, ÇDR; Çok düşük risk, DR; Düşük risk, OR; Orta risk, YR; yüksek risk. Yüksek risk ve diğer risk grupları halinde olgular iki ana grupta değerlendirildiğinde, mukozal invazyon bulunan olguların çoğu anlamlı derecede yüksek risk grubunda yer almaktaydı (Pearson χ 2 =6.130, p=0.013). Aynı şekilde yapılan gruplamada mukozal invazyon ve ülseri birlikte gösteren 10 olgunun 8 i, (Fischer kesin χ 2 ; p>0.05), mukozal ve çevre doku invazyonu beraber gösteren 2 olgu yüksek risk grubunda yer almaktaydı, (Fischer kesin χ 2 ; p>0.05), (Tablo 23). Tablo 23. Gastrointestinal stromal tümör olgularında prognostik kriterlerin risk gruplarına göre dağılımı Yüksek risk grubu Diğer gruplar Mukozal invazyon* 10 2 Mukozal invazyon + Ülser** 8 2 Mukoza + Çevre doku invazyonu*** 2 0 *: Pearson χ 2 =6.130, p=0.013, **: Fischer kesin χ 2 ; p=0.058, ***: Fischer kesin χ 2 ; p= Olgularımızdan 5 inde tanı konulduğu anda batın ve batın içi organlarda birden fazla tümöral kitle (2-19 adet) mevcuttu. Primer yerleşim yeri ince barsak olan 3 olgumuzda ise, ay sonra batın içinde farklı odaklarda nüks saptanmıştır. Nüks gelişen ve hepsi 5 cm den büyük olan bu olguların, 2 si yüksek risk, 1 i orta risk grubunda olup, tümünde çevre organ invazyonu, nekroz, kanama ve hipersellülarite, 2 sinde belirgin sitolojik atipi ve 1 inde mukozal ülserasyon izlendi (Tablo 24). 43
48 Tablo 24. Multipl kitle ve nüks olan gastrointestinal stromal tümör vakalarında histomorfolojik bulguların dökümü Birden fazla kitle Olgu sıra no Biyopsi no Cins/ Yaş RG L Ç S A M N K Ü ÇDİ /03 51/E YR Retroperiton 3cm belirgin belirgin 40 yok var yok var /04 55/E OR İnce barsak 8.5cm belirgin hafif 4 var var yok yok /05 46/K YR İnce barsak 7cm belirgin hafif 14 var yok var yok /09 47/E DR Mide 8cm belirgin belirgin 5 var var var yok Birden fazla kitle ve Nüks /02 54/K YR Nüks /02 57/K YR /08 51/E OR İnce barsak İnce barsak İnce barsak 18cm belirgin belirgin 43 var var yok var 10cm belirgin belirgin 11 var var var var 10cm belirgin hafif 4 var var yok var RG; Risk grupları, L; Lokalizasyon, Ç; En büyük tümör çapı, S; Sellülarite, A; Hücresel atipi, M; mitoz, N; Nekroz, K; Kanama, Ü; ülser, ÇDİ; Çevre doku invazyonu K; kadın, E; Erkek, YR; Yüksek risk, OR; Orta risk, DR; Düşük risk. Gastrointestinal stromal tümör vakalarımızın 3 ünde lenf bezi, 4 ünde karaciğer metastazı mevcuttu. İnce barsak yerleşimli yüksek risk grubundan 1 (20 nolu olgu) ve mide yerleşimli düşük risk grubundan 1 vakada (30 nolu olgu), rezeksiyon materyali serozal yağlı dokudan ayıklanan lenf nodlarından 1 er tanesinde tümör metastazı görüldü. Orta risk grubundan mide yerleşimli bir vakanın (11 nolu olgu) ise ilk tanı tarihinden 6 yıl sonra, sol servikal bölgede lenfadenopati nedeni ile uygulanan eksizyonel biyopsi örneğinde ( protokol nolu), olgunun ilk tanısı ile uyumlu tümör metastazı saptandı. Yüksek risk grubundan 2 si ince barsak 2 si mide yerleşimli olan 4 vakada (16, 20, 23, 30 nolu olgu, Şekil 12), bölümümüze ayrıca gönderilen karaciğer dokularına ait biyopsi örneklerinde, tümör metastazı mevcuttu. Karaciğer metastazı yapmış olgulardan ikisinin tanı anında metastatik olduğu saptanmış iken, diğer iki olguda metastaz 2 ve 18 ay sonra gelişmiştir. İMMÜNOHİSTOKİMYASAL BULGULAR Tüm risk gruplarındaki toplam 37 GİST olgusunun hepsinde vimentin ile diffüz pozitif reaksiyon görülmüştür. SMA ile orta risk ve yüksek risk grubunda 1 er vakada, S100 ile risk yok grubundaki tek vakada pozitiflik saptanmış olup, desmin ile vakaların hiç birinde 44
49 boyanma izlenmemiştir. CD34 ile tüm GİST vakalarının %62.16 (23/37) sında pozitif boyanma saptanmış ve bu oran risk grupları ile kıyaslandığında anlamlı fark bulunmamıştır (Pearson χ 2, p>0.05), (Tablo 25). Tablo 25. Gastrointestinal stromal tümör vakalarında mezenkimal tümör belirleyicileri ile boyanma dağılımları Risk Kategorizasyonu VİMENTİN SMA DESMİN S100 CD34 * Risk Yok 1/1 0/1 0/1 1/1 1/1 Çok Düşük Risk 3/3 0/3 0/3 0/3 3/3 Düşük Risk 6/6 0/6 0/6 0/6 5/6 Orta Risk 7/7 1/7 0/7 0/7 3/7 Yüksek Risk 20/20 1/20 0/20 0/20 11/20 Toplam 37/37 2/37 0/37 1/37 23/37 * ;Pearson χ 2 =0.949, p= Otuzyedi GİST vakasının %100 ünde, hem CD117 hem de PDGFRα ekspresyonu saptanmıştır (Şekil 13,14). CD117 nin tümöral dokudaki boyanma paterni dikkate alınarak vakaların mitoz sayıları kıyaslandığında, fokal ve/veya zayıf CD117 pozitifliği gösteren olgularda ortalama mitoz sayısının, kuvvetli ve diffüz boyanan olgulara göre anlamlı derecede yüksek olduğu izlendi, (Mann Whitney U testi; p=0.038), (Tablo 26). Düşük risk grubundan 1 ve yüksek risk grubundan 3 vaka olmak üzere toplam 4 (%11) vakada, DOG1 ile boyanma izlenmemiştir. Yüksek risk grubu dışındakiler tek grup olarak yapılan değerlendirmede, yüksek risk grubundakilerin %85, diğer risk grubundakilerin %94.1 i DOG1 pozitif bulunmuştur, arada anlamlı bir fark yoktur, (Fischer kesin χ 2 ; p>0.05), (Tablo 27). Tablo 26. Gastrointestinal stromal tümörlerde CD117 ekspresyon paterninin ortalama mitoz sayıları ile kıyaslanması Olgu (n) Ortalama mitoz sayısı CD117; fokal ve/veya zayıf boyanma ±22.07 CD117; diffüz/kuvvetli boyanma ±11.85 Mann Whitney U testi; p=0.038 Otuzüç (%89) DOG1 pozitif GİST vakasında, İHK değerlendirme kriterlerine göre yoğunluk ve yaygınlık sınıflamasında, sırasıyla +++ ve >%50 gruplarında yoğunlaşan DOG1 45
50 pozitifliği saptanmıştır (Şekil 15). Risk durumu yükseldikçe, DOG1 pozitivitesinin hem yoğunluğu, hem de yaygınlığında hafif azalma olmakla beraber, bu fark istatistiksel olarak anlamlı değildi, (Spearman korelasyon; p>0.05), (Tablo 27). Benzer şekilde CD117 ve PDGFRα nın tümöral dokudaki boyanma yoğunluk ve yaygınlık dereceleri risk gruplarına göre kıyaslandı ve istatistiksel olarak anlamlı sonuç bulunmadı, (Spearman korelasyon; p>0.05). Tablo 27. Risk sınıflamasına göre DOG1 ekspresyonu dağılımı Risk G (-) n(%) (+) n(%) Yoğunluk** Yaygınlık*** * <%10 %10-50 >%50 RY 0 (% 0) 1 (%100) ÇDR 0 (% 0) 3 (%100) DR 1 (%17) 5 (% 83) OR 0 (% 0) 7 (%100) YR 3 (%15) 17(% 85) TOPLAM 4 (%11) 33(% 89) Risk G; Risk grupları, RY; Risk yok, ÇDR; Çok düşük risk, DR; Düşük risk, OR; Orta risk, YR; yüksek risk, (-); DOG1 negatif vakalar, (+); DOG1 pozitif vakalar. *: Fischer kesin χ 2 ; p=0,367, **: Spearman korelasyon; p=0.897, ***: Spearman korelasyon; p= Yüksek risk grubundaki vakaların %60 ında, ki67 ile >%10 nükleer pozitiflik görülmüş olup, bu vakalar yüksek proliferasyon indeksi grubunda değerlendirilmiştir. Risk yok ve çok düşük risk grubundaki vakaların hepsi, düşük ve orta risk grubundaki vakaların ise sırasıyla %83.33 ve %85.71 i düşük proliferatif indekse sahipti. Yüksek risk grubu dışındakileri tek grup halinde incelediğimizde, yüksek risk grubunda ki67 proliferasyon indeksinin diğer gruba göre anlamlı derecede yüksek olduğu saptanmıştır, (Pearson χ 2 ; p=0.003), (Tablo 28). Tablo 28. Gastrointestinal stromal tümörlerde risk ve Ki67 korelasyonu Ki67 Risk Kategorizasyonu <%10 >%10 N % N % Risk Yok 1/1 (%100) 0/1 (%0) Çok Düşük Risk 3/3 (%100) 0/3 (%0) Düşük Risk 5/6 (%83) 1/6 (%17) Orta Risk 6/7 (%86) 1/7 (%14) Yüksek Risk 8/20 (%40) 12/20 (%60) Pearson χ 2 ; p=
51 Tüm GİST olgularında, mitoz ile ki67 proliferasyon indeks oranlarının korelayonuna bakıldığında mitoz sayısı 5 in üzeri olan olguların %57.9 unda ki67 proliferasyon indeksi %10 dan büyük olarak saptanmıştır ve gruplar arasındaki fark istatistiksel olarak anlamlı bulunmuştur, (Pearson χ 2 =6.680, p=0.010), (Tablo 29). Tablo 29. Gastrointestinal stromal tümör olgularında mitoz ve ki67 korelasyonu MİTOZ Ki67 <%10 Ki67 >% > Pearson χ 2 =6.680, p= Gastrointestinal stromal tümörlerde %54 (20/37) oranında Bcl2 ekspresyonu saptanmış, en yoğun olarak %86 oranla orta risk grubunda görülmüştür. Yüksek risk grubunda ise bu oran %45 olarak saptanmıştır, (Pearson χ 2 ; p>0.05), (Tablo 30). Tablo 30.Gastrointestinal stromal tümörlerde risk sınıflamasına göre Bcl2 ekspresyonu dağılımı Risk Kategorizasyonu Bcl2 % Risk Yok 0/1 0 Çok Düşük Risk 1/3 33 Düşük Risk 4/6 67 Orta Risk 6/7 86 Yüksek Risk 9/20 45 Pearson χ 2 =1.437, p= Gastrointestinal stromal tümör olgularındaki immün profil sonuçlarını, GİST ile morfolojik olarak karışabilen diğer mezenkimal tümörler ile kıyaslayıp, ayırıcı tanıya olan katkılarını amaçlayarak; bilinen yumuşak doku tümörlerinden, rastgele aldığımız 45 olguya da aynı antikorlar çalışıldı. Gastrointestinal stromal tümör olgularının tümünde CD117 ekspresyonu görülürken, GİST dışı mezenkimal tümörlerin %18 inde bu antikor ile pozitif reaksiyon saptandı ve bu oran anlamlı bulundu, (Pearson χ 2 =55.436, p=0.000), (Tablo 31). Platelet derived growth factor receptor α ile yine tüm GİST vakalarında pozitif boyanma gözlenirken, GİST dışı mezenkimal tümörlerde, diğer araştırma antikorlarına göre nispeten daha yüksek oranda (%47) pozitif reaksiyon izlendi ve oldukça anlamlı sonuç alındı, (Pearson χ 2 =27.899, p=0.000), (Tablo 31). 47
52 Gastrointestinal stromal tümör vakalarında %89 oranında izlenen DOG1 pozitifliğine karşılık, GİST dışı mezenkimal tümörlerde 45 olgunun 3 ünde (%7) pozitif reaksiyon saptandı. Ancak DOG1 pozitifliği gösteren bu vakalardan 2 sinde boyanma fokal ve zayıf nitelikte idi. DOG1 pozitifliği, GİST dışı tümörlere göre, GİST olgularında anlamlı derecede pozitifti, (Pearson χ 2 =56.145, p=0.000), (Tablo 31). Tablo 31. Gastrointestinal stromal tümör ve diğer mezenkimal tümörlerde araştırma antikorları ekspresyonu TANI CD117* PDGFR** DOG1*** GİST 37/37 (%100) 37/37 (%100) 33/37 (%89) GİSTdışı mezankimal tümörler 8/45 (% 18) 21/45 (% 47) 3/45 (% 7) Pearson χ 2 ; *: χ 2 =55.436, p=0.000, **: χ 2 =27.899, p=0.000, ***: χ 2 =56.145, p= Gastrointestinal stromal tümör dışı mezenkimal tümörlerde, CD117 ve DOG1 e kıyasla, daha yoğun ekspresyonu gözlenen PDGFRα, en yoğun olarak düz kas (%80) ve damar tümörlerinde (%80) pozitif bulundu. Diğer mezenkimal tümörlerde PDGFRα pozitifliği çizgili kas, fibrohistiositik ve sinovyal tümörlerde %60, adipöz doku tümörlerinde %40, benign sinir doku ve gangliositik tümörlerde % 20 olarak tespit edildi. PDGFRα nın negatif olduğu tek grup ise malign davranış gösteren sinir tümörleri idi (Tablo 32). Tablo 32. Gastrointestinal stromal tümör dışı mezenkimal tümörlerde Platelet derived growth factor reseptor α ekspresyon dağılımı GİST dışı Mezenkimal Tümörler PDGFRα N (%) Malign Sinir Doku Tümörleri 0/5 (%0) Benign Sinir Doku Tümörleri 1/5 (%20) Düz Kas Tümörleri 4/5 (%80) Çizgili Kas Tümörleri 3/5 (%60) Adipöz Doku Tümörleri 2/5 (%40) Damar Tümörleri 4/5 (%80) Gangliositik Tümörler 1/5 (%20) Fibrohistiositik Tümörler 3/5 (%60) Sinovyal Tümörler 3/5 (%60) Desmin ile, GİST vakalarının hiçbirinde boyanma görülmez iken, çizgili ve düz kas tümörlerinde sırasıyla % 80 ve % 20 oranlarında pozitif reaksiyon izlenmiştir, (Fischer kesin χ 2 ; p=0.045), (Tablo 33). 48
53 SMA ile, 2 GİST vakasında görülen ekspresyon, düz kas tümörlerinin tümünde ve 1 inflamatuar myofibroblastik tümörde saptanmıştır, (Fischer kesin χ 2 ; p>0.05), (Tablo 33). S100 ile 1 GİST vakasında mevcut olan pozitifliğe karşılık, sinir, yağ ve gangliositik orijinli tümör gruplarındaki vakaların hepsinde pozitif boyanma izlenmiştir, (Pearson χ 2 =18.570, p=0.000), (Tablo 33). CD34 ile GİST vakalarının %62 sinde pozitif reaksiyon görülmüş olup, adipöz doku, ve fibrohistiositik tümörlerde %20, damar tümörlerinde %40 oranında CD34 ekspresyonu izlenmiştir, (Pearson χ 2 =26.093, p=0.000), (Tablo 33), (Şekil 16). CD117 ile %100 oranında pozitif boyanma gösteren GİST vakalarına karşılık, GİST dışı mezenkimal tümörlerin %18 i CD117 pozitiftir. Doku gruplarına göre baktığımızda, düz ve çizgili kas, gangliositik, fibrohistiositik, adipöz ve sinovyal doku tümörlerinin hiç birinde boyanma olmaz iken, anjiosarkomların %80 (4/5) i, malign periferik sinir kılıfı tümörlerinin %60 (3/5) ı, benign schwannomların %20 (1/5) si, CD117 ile pozitif reaksiyon vermiştir (Tablo 33). Gastrointestinal stromal tümör vakalarının %89 u DOG1 ekspresyonu gösterir iken, GİST dışı mezenkimal tümörlerde DOG1 pozitifliği %7 olarak bulundu. GİST dışı mezenkimal tümörlerden DOG1 pozitif 3 olgunun 1 i malign periferik sinir kılıfı tümörü, 1 i schwannom, 1 i anjiosarkom idi (Tablo 33), (Şekil 17-19). Tablo 33.Gastrointestinal stromal tümör ve dışı mezenkimal tümör vakalarının immünohistokimyasal boyanma dağılımları Desmin N (%)* SMA N (%)** S-100 N (%)*** 49 CD34 N (%) CD117 N (%) DOG1 N (%) GİST 0(%0) 2/37(%5) 1/37(%3) 23/37(%62) 37/37(%100) 33/37(%89) MSDT 0/5(%0) 0/5(%0) 5/5(%100) 0/5(%0) 3/5(%60) 1/5(%20) BSDT 0/5(%0) 0/5(%0) 5/5(%100) 0/5(%0) 1/5(%20) 1/5(%20) DKT 1/5(%20) 5/5(%100) 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) ÇKT 4/5(%80) 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) ADT 0/5(%0) 0/5(%0) 5/5(%100) 1/5(%20) 0/5(%0) 0/5(%0) DT 0/5(%0) 0/5(%0) 0/5(%0) 2/5(%40) 4/5(%80) 1/5(%20) GT 0/5(%0) 0/5(%0) 5/5(%100) 0/5(%0) 0/5(%0) 0/5(%0) FHT 0/5(%0) 1/5(%20) 0/5(%0) 1/5(%20) 0/5(%0) 0/5(%0) SDT 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) 0/5(%0) GİST; Gastrointestinal stromal tümör, MSDT; Malign sinir doku tümörü, BSDT; Benign sinir doku tümörü, DKT; Düz kas tümörü, ÇKT; Çizgili kas tümörü, ADT; Adipöz doku tümörü, DT; Damar tümörü, GT; Gangliositik tümör, FHT; Fibrohistiositik tümör, SDT; Sinovyal doku tümörü. *: Fischer kesin χ2; p=0.045, **: Fischer kesin χ2; p=0.205,***: Pearson χ2=18.570, p=0.000, : χ2=26.093, p=0.000
54 Çalışmamızda yer alan gastrointestinal stromal tümör olgularının demografik ve histopatolojik özellikleri ile immmünohistokimyasal bulguları Tablo 34 te, gastrointestinal stromal tümör dışı mezenkimal tümör olgularının protokol ve tanı listesi Ek 2 deki Tablo Ek te belirtilmiştir. Ayrıca gastrointestinal stromal tümör olguları için kullandığımız patoloji rapor örneği Ek 3 te mevcuttur. 50
55 Tablo 34. Gastrointestinal stromal tümör tanılı olguların klinik ve histopatolojik bulguları Sıra Biyopsi No Ad Protokol No Operasyon Tipi Yaş / Cins Lokalizasyon Risk Grupları Çap (cm) Mitoz Hücre tipi Ülser Nekroz Kanama Mukozal invazyon Çevre doku invazyonu Selülarite Sitolojik Atipi Metastaz Multipl Kitle-Nüks CD117 PDGFRα DOG1 CD34 Vimentin Aktin Desmin S100 Bcl-2 Ki H S 30 Rez 53/K İb OR 8 4 İğsi B Hafif <% F D 06 Rez 70/K Kolon YR 11 5 İğsi B B >% M A 68 Rez 63/K Mide ÇDR 5 2 Mikst Az Hafif <% S 00 Ç ---- Rez 55/E İb YR 13 6 Mikst B Hafif <% M B 23 Rez 57/K İb YR İğsi B B - Nüks <% S Ç 67 Rez 52/E Kolon YR İğsi B B >% A B 55 Rez 45/K İb OR 7 2 İğsi Az Hafif <% N K 79 Rez 54/K İb YR Mikst B B - MK+Nüks >% O T 71 Rez 53/E kolon YR Mikst B B >% E M 02 Eks 66/E Mide ÇDR 5 0 Mikst B Hafif <% İ A 702 Eks 53/E Mide OR 16 3 Mikst B B LN <% H Y 96 Eks 51/E Rp YR 3 40 Epiteloid B B - MK >% F K 618 Eks 69/E Mide OR 4 7 Mikst B B <% N K 91 Rez 57/K Kolon RY İğsi Az Hafif <%10 15 A İ A Rez 55/E İb OR İğsi B Hafif - MK <% A S 150 Rez 41/E İb YR İğsi B B KC <%10 Rez; Rezeksiyon, Eks; Eksizyon, K; Kadın, E; Erkek, İb; İncebarsak, Rp; Retroperiton, OR; Orta risk, YR; Yüksek risk, ÇDR; Çok düşük risk, RY; Risk yok, DR; Düşük risk, B; Belirgin, KC; Karaciğer, LN; Lenf nodu, MK; Multipl kitle 51
56 Tablo 34 (devam). Gastrointestinal stromal tümör tanılı olguların klinik ve histopatolojik bulguları Sıra Biyopsi No Ad Protokol No Operasyon Tipi Yaş / Cins Lokalizasyon Risk Grupları Çap (cm) Mitoz Hücre tipi Ülser Nekroz Kanama Mukozal invazyon Çevre doku invazyonu Selülarite Sitolojik Atipi Metastaz Multipl Kitle-Nüks CD117 PDGFRα DOG1 CD34 Vimentin Aktin Desmin S100 Bcl-2 Ki H T R Ç H Ö K K G T H Ş E K F C H F A G A K N R Z D H A Rez 66/K İb DR İğsi B Hafif <%10 Rez 23/K İb YR 16 2 Mikst B Hafif <%10 Rez 66/K İb YR Mikst B Hafif >%10 Rez 46/K İb YR 7 14 İğsi B Hafif 52 LN, KC MK >%10 Rez 59/K İb DR 5 5 İğsi B Hafif <%10 Eks 58/K Mide YR 7 8 İğsi B Hafif >%10 Eks 43/E Mide YR İğsi B B KC >%10 Eks 71/K Rp YR Mikst B B >%10 Eks 68/K Mide YR Mikst B Hafif <%10 Rez 70/K İb OR 9 5 İğsi B B <%10 Rez 51/E İb OR 10 4 Mikst B Hafif - Nüks >%10 Rez 60/K İb YR 9 28 Mikst B B >%10 Eks 51/E Mide DR Mikst B B <%10 Rez 47/E Mide DR 8 5 Mikst B B LN, KC MK >%10 Rez; Rezeksiyon, Eks; Eksizyon, K; Kadın, E; Erkek, İb; İncebarsak, Rp; Retroperiton, OR; Orta risk, YR; Yüksek risk, ÇDR; Çok düşük risk, RY; Risk yok, DR; Düşük risk, B; Belirgin, KC; Karaciğer, LN; Lenf nodu, MK; Multipl kitle
57 Tablo 34 (devam). Gastrointestinal stromal tümör tanılı olguların klinik ve histopatolojik bulguları Sıra Biyopsi No Ad Protokol No Operasyon Tipi Yaş / Cins Lokalizasyon Risk Grupları Çap (cm) Mitoz Hücre tipi Ülser Nekroz Kanama Mukozal invazyon Çevre doku invazyonu Selülarite Sitolojik Atipi Metastaz Multipl Kitle- Nüks CD117 PDGFRα DOG1 CD34 Vimentin Aktin Desmin S100 Bcl-2 Ki A Ç E E K Y N O F E H G E A Rez 66/E İb YR İğsi B B >%10 Rez 61/K İb YR 5 9 İğsi B B <%10 Rez 36/K İb YR 6 9 iğsi B B <%10 Eks 67/K Mide DR 9 3 Mikst B Hafif <%10 Rez 70/K İb DR 4 1 İğsi Az Hafif <%10 Eks 74/E Rp YR İğsi B Hafif <%10 Rez 69/K Mide ÇDR 3 5 İğsi B Hafif <%10 Rez; Rezeksiyon, Eks; Eksizyon, K; Kadın, E; Erkek, İb; İncebarsak, Rp; Retroperiton, OR; Orta risk, YR; Yüksek risk, ÇDR; Çok düşük risk, RY; Risk yok, DR; Düşük risk, B; Belirgin, KC; Karaciğer, LN; Lenf nodu, MK; Multipl kitle 53
58 A B C D E F Şekil 4. Gastrointestinal stromal tümör olgularından makroskopik örnekler; A) Mide duvarında 8cm çapta lobüle kitle (Düşük risk, 30 nolu olgu, B ), B) Mide duvarında 13 cm lik, fibroz bantlar ile ayrılmış lobüller içeren tümöral kitle (Yüksek riskte, 25 nolu olgu, B ), C) İnce barsak duvarında 7cm çapta nekrotik kitle (Yüksek riskte, 20 nolu olgu), D) İleum duvarında 18 cm çapta kitle (Yüksek riskte, 16 nolu olgu, B ), E) D deki olgunun barsak mukozası ile F) D deki olgunun barsak serozası ile ilişkisi 54
59 A B C D Şekil 5. A-B-C-D) Mide duvarında GİST olgusu; 4cm çapta kanamalı ve nekrotik tümöral kitlenin farklı seviyelerde kesit yüzü (Orta riskte,13 nolu olgu, B ) 55
60 A B C D Şekil 6. Gastrointestinal stromal tümör olgularından makroskopik örnekler; A) Mide duvarında 9.5 cm lik solid kitlede kanama odakları (Düşük riskte, 29 nolu olgu, B ), B) Jejunumda 4.5 cm çapta solid kitle (Düşük riskte,17 nolu olgu, B ), C) Mide duvarında 13 cm lik kitlenin kesit yüzünde geniş nekroz ve kanama (Yüksek riskte, 25 nolu olgu, B ), D) Karaciğerde GİST metastazı (Primer tümör midede, yüksek risk, 30 nolu olgu, B ) 56
61 A B Şekil 7. Mide submukozasında gastrointestinal stromal tümöre ait ekspansif, nodüler kitle, olgu 13, (A: HEx12.5, B: HEx50) A B Şekil 8. Gastrointestinal stromal tümör; A) İğsi tip, olgu 33, (HEx50), B) Epiteloid tip, olgu 27, (HEx100) A B Şekil 9. Gastrointestinal stromal tümörde hipersellülarite ve hücresel atipi; A) İğsi tip, olgu 33, (HEx200), B) Epiteloid tip, olgu 8, (HEx200) 57
62 A B Şekil 10. İğsi hücreli gastrointestinal stromal tümörde subnükleer vakuoller, olgu 37; A: (HEx100), B: (HEx200). A B Şekil 11. Mikst tip gastrointestinal stromal tümörün epiteloid odağında;a) Kanama alanları, olgu 27, (HEx100), B) Mikzoid değişiklikler, olgu 13, (HEx50) 58
63 A B t k C D Şekil 12. Midede 8cm çapta düşük riskli gastrointestinal stromal tümörü olan hastada (30.olgu) 18 ay sonra karaciğerde saptanan metastatik tümör; A) Sol altta karaciğer (k) ve üstte metastatik tümör (t), HEx12.5, B) Karaciğerde tümörün portal alanı (ok) infiltre edişi, HEx100, C) Tümörde belirgin sitolojik atipi ve hipersellülarite, HE x100, D) Tümörde kuvvetli membranöz CD117 pozitifliği, İmmünohistokimya x100 59
64 A B C D E Şekil 13. Gastrointestinal stromal tümörde CD117 ekspresyonu; A) Kuvvetli diffüz(+++), x12.5, B) İnkomplet membranöz (+++), x50, C) Sitoplazmik (++), x100, D) Sitoplazmik (++), x50, E) Komplet ve inkomplet membranoz, sitoplazmik, (+++) x200, (İmmünohistokimya) A B C Şekil 14. Gastrointestinal stromal tümörde PDGFRA ekspresyonu; A) Kuvvetli diffüz (+++), x50, B) Diffüz (++), x50, C) Kuvvetli diffüz (+++), x100, (İmmünohistokimya) 60
65 A B C Şekil 15. Gastrointestinal stromal tümörde DOG1 ekspresyonu; A, B ve C) Kuvvetli, diffüz (+++), x100, D) Membranöz (+++), x200, E) Diffüz (++), x100, (İmmünohistokimya) D E A B Şekil 16. Gastrointestinal stromal tümörde CD34 ekspresyonu; A) Kuvvetli membranöz boyanma, x100, B) Kuvvetli sitoplazmik boyanma, x100, (İmmünohistokimya) 61
66 A B C D Şekil 17. Anjiosarkom olgusu (B ): A) Tipik histolojik görünüm,hex100, B) CD31 ile kuvvetli pozitiflik, x100, C) CD117 ekspresyonu, x100, D) DOG1 antikoru ile ++ boyanma, x100 A B C D Şekil 18. Schwannom olgusu (B ) : A) Tipik histolojik görünüm,hex50, B) S- 100 ile kuvvetli pozitiflik, x100, C) Kuvvetli CD117 ekspresyonu, x100, D) DOG1 antikoru ile (+++) boyanma, x100 62
67 A B C D Şekil 19. Malign periferik sinir kılıfı tümörü (B ); A) Tipik histolojik görünüm, HEx50, B) S-100 ile kuvvetli pozitiflik, x12.5, C) CD117 ekspresyonu (++), x50, D) DOG1 antikoru ile ++ boyanma, x50 63
68 TARTIŞMA Gastrointestinal stromal tümörler, önceleri orijini iyi tanımlanamayan, klasik tedaviye cevap vermeyen, gastrointestinal sistemin mezenkimal karakterli tümörleri olarak isimlendirilir iken, günümüzde bu tümörlerin tanımlanması ve gelişimi algılanabilmiş, bu sayede de biyolojilerine bağlı olarak, hedefe yönelik yeni ve moleküler tıbba model olabilecek tedavi rejimlerinin geliştirilebileceği ümidini doğurmuştur (49,99). Günümüzde GİST ler, GİS de gelişim gösteren mezenkimal tümörlerin yaklaşık %80 ini oluşturmaktadır (149). Tüm Gİ tümörlerin ise %1 inden azdır (150). Yıllık insidans, 11/10 6 ile 14.5/10 6 arasında iken, beklenen prevelans 129/10 6 dur (39,43). Nilsson ve ark. (44) nın 2005 yılında yayınladıkları çalışmalarında, Fletcher kriterleri (41) esas alınarak risk gruplarına ayrılmış vakaların prevalans oranları ise, çok düşük risk grubu için 22.2/10 6, düşük risk grubu için 51.9/10 6, orta risk grubu için 24.2/10 6 ve yüksek risk grubu için 22.2/10 6 olarak bildirilmiştir. Ancak yetersiz sınıflama ve tanımlama yüzünden gerçek insidans ve prevelans tam belirlenememektedir (151). Literatürde GİST lerin yaklaşık %10-50 sinin malign davranış gösterdiği bildirilmektedir (44,50,89,90,152,153). Trakya Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı nda, yılları arasında Gastrointestinal Stromal Tümör tanısı almış 37 olgu çalışmamıza dahil edildi. Günümüzde kullanılan risk gruplarına göre (1,4,41) sınıflandığında, 20 olgu (%54.05) malign davranış gösteren gruba (yüksek risk grubu) girmekte idi. 20. Avrupa Patoloji Kongresi nde sunulan, Türkiye deki 28 merkezden toplanan 1008 GİST olgusunu içeren çalışmada olguların %54 ü yüksek, %19 u orta, %21 i düşük ve %6 sı çok düşük risk grubuna dahildi. Olgularımızın risk gruplarına göre dağılımı, sözü edilen ülkemiz genelini yansıtan çok merkezli çalışma ile uyumluydu (154), (Tablo 9). 64
69 Klinik olarak GİST lerin çoğu orta yaştaki bireylerde görülmekte ve yaş aralığı 40-98, median yaş ise yaklaşık 60 tır (3,49,152,154,155). Bununla birlikte nadiren çocuklar ve yeni doğanlarda dahil tüm yaş gruplarında bildirilen vakalar mevcuttur (156). Çalışmamızda yaş aralığımız arasında, median yaş ise 57 idi. Literatürde GİST lerin görülme sıklığı ile cinsiyet arasında istatiksel olarak anlamlı fark bulunmadığı, ancak birkaç yayında erkeklerde biraz daha sık görüldüğü belirtilmiştir (43,49,154,157). Çalışmamızda ise aksine olguların %59,5 i kadın, %40,5 i erkekti. Gastrointestinal stromal tümörler Gİ kanal boyunca tüm organlarda ve farklı biyolojik davranışlarda saptanabilmekle birlikte, en sık mide (%50-70) ve ince barsakta (%20-40) görülmektedir (3,51,52,154). Bunun yanı sıra GİST ler, rektum, özefagus, omentum ve mezenterde yaklaşık %5-10 ve Gİ kanal dışı alanlarda ise <%5 lik oran ile daha nadir görülürler (3,158,159). Çalışmamızdaki vakaların primer yerleşim bölgeleri en sık ince barsak(%51.35), daha sonra midedir (%29.72). Kalın barsak yerleşimli tümörlerin oranı %10.8, Gİ kanal dışı ise %8.10 dur. Bir çok çalışmada, GİST lerde anatomik lokalizasyonunun bağımsız prognostik faktör olduğu konusunda fikir birliğine varılmıştır (5,41,68,70,90,152,160,161). İnce barsak yerleşimli GİST ler, benzer çap ve mitotik aktiviteye sahip mide yerleşimli tümörlere göre daha kötü prognoza sahiptirler (146,162). İntestinal GİST lerin %40-50 si, gastrik GİST lerin ise yaklaşık %20-25 i, klinik açıdan malign davranıştadır (45). Yakın oranlarla, çalışmamızda agresif davranış göstergesi olan yüksek risk grubu, ince barsak yerleşimli vakaların %58 ini, mide yerleşimli vakaların ise %27 sini oluşturmaktadır. Gastrointestinal stromal tümörlerde, benign-malign davranışın önceden saptanabilmesine yönelik çok sayıda çalışma yapılarak, farklı klinik ve morfolojik parametreler incelenmiş ve bazı sonuçlar öne sürülmüştür. Ancak prognoz tayininde, bu parametrelerden tümör boyutu ve mitoz oranının en güvenilir parametre olduğu birçok otör tarafından kabul edilmiştir (41,43,45). Miettinen ve ark. (70) nın 2002 yılındaki çalışmasında, multivarite analizlerine dayanarak, tümör çapı bağımsız prognostik belirteç olarak tanımlanmıştır. Aynı yazarın (68,90) daha yakın tarihte yayınlanan makalelerinde, lokalizasyona göre sınıflanmış, oldukça geniş serilerin incelendiği GİST vakalarında, ince barsak yerleşimli tümörlerde 5 cm, gastrik yerleşimli tümörlerde ise 10 cm den büyük tümör çapının kötü prognostik belirteç olduğu bildirilmiştir. Literatürde GİST olgularının boyut aralığı oldukça geniştir ( cm) (5,43,68,154). Çalışmamızda olguların çapları cm arasında ve ortalama çap 9.31 cm dir. Yüksek risk grubundaki olgularımızın %60 ının çapı 10 65
70 cm den büyüktür. İnce barsak yerleşimli, yüksek risk grubundan 11 vakamızın 10 u 5 cm den büyük çapa sahiptir. Gastrik yerleşimli, yüksek risk grubundan 3 vakamızın ise 2 si 10 cm den, 1 i 5 cm den büyük çaptadır. Karaciğer metastazı görülen 4 olgumuzda, en büyük tümör çapı 7, 8, 16 ve 18 cm dir. Batında multiple nodüller saptanan olgumuzda tümör çapı 18 cm, omental nüks gelişen bir vakamızda ise tümör çapı 10 cm idi. Kalın barsak yerleşimli GİST ler tanı anında genellikle ilerlemiş büyük kitleler halinde saptanmaktadır (70). Vakalarımız içerisindeki kalın barsak yerleşimli 4 GİST olgusunun 3 ü, >10 cm çapa sahip (11-13 cm) olup yüksek risk grubundandır. Diğer vaka ise, insidental olarak erken tanı almış bir olgu idi. Gastrointestinal stromal tümörlerde mitoz sayısının, malignite tanımlanmasında ve prognoz öngörülmesinde en değerli parametre olduğu ve tümörde aktif büyümeye işaret ettiği belirtilmektedir (163). Wong ve ark. (164) nın prognoz tayinine yönelik çalışmalarında, uni ve multivarite analizleri kullanılarak, 50 BBA nında 5 in üzerinde mitoz varlığının, tek ve en önemli kriter olduğu saptanmıştır. Miettinen ve ark. (90) da benzer olarak 906 vakalık GİST serilerinde, tümör boyutuna bakılmaksızın, tümör mortalite oranını en yüksek olarak, mitozun 50 BBA nda 5 in üzerinde olduğu vakalarda (%84) saptamıştır. Huang ve ark. (161) da, 50 BBA da 10 dan fazla mitoz varlığının güçlü malignite göstergesi olduğunu bildirmiştir. Bununla birlikte 10 dan az mitoz gösteren ancak diğer malignite kriterlerine sahip tümörlerin de, malign davranış gösterebileceği özellikle vurgulanmaktadır (163). Olgularımızdan yüksek risk grubundaki vakaların %90 ınında 50 BBA nda 5 ten fazla mitoz saptanmıştır. Karaciğer metastazı saptanan 4 vakamızda 50 BBA nda mitoz sayısı ortalama ( mitoz) dir. Batında multiple nodüllerin mevcut olduğu vakada ise mitoz sayısı 50BBA da 43 sayılmıştır. Literatür bilgilerinden farklı olarak omental nüks gelişen vakada 50 BBA da 4 mitoz sayılmıştır. Ancak ince barsak yerleşimli bu vakada, nekroz ve çevre dokulara invazyon görülmüş olup, çapı 10 cm dir. Gastrik GİST lerde vakaların %50 sinde iğsi hücre morfolojisi izlenir iken, %30 unda epiteloid, %20 sinde de mikst hücre popülasyonu hakimdir (68). Çalışmamızdaki mide yerleşimli GİST vakalarının %64 (7/11) ü mikst, %36 (4/11) sı iğsi hücreli tipe sahiptir. İnce barsak yerleşimli GİST vakalarında da daha yüksek oranda iğsi hücre tip izlenmektedir (41,73,165). İnce barsak yerleşimli olgularımızın %68 (13/19) i iğsi, %32 si mikst hücre tipinden oluşmaktadır. Fletcher ve ark. (41) nın bir çalışmasında, hücre tipinin prognostik öneminin sınırlılığından bahsedilmiş, ancak daha önceki çalışmalarda malignite kriteri olan mitotik 66
71 indeksin, iğsi hücreli tiplerde, epiteloid hücrelilere göre daha yüksek olduğu belirtilmiştir (41). Çalışmamızda mikst ve epiteloid hücre morfolojisi gözlenen GİST lerin 8 (8/16) inde, iğsi hücrelilerin 10 (10/20) unda 5 ten fazla mitoz görülmüştür. Daha yeni yayınlarda da, baskın hücre tipi, risk grupları ve prognoz arasında istatiksel anlamlı ilişki bulunmadığı vurgulanmıştır (164). Çalışmamızda hücre tipine göre risk grupları karşılaştırıldığında literatürle uyumlu olarak anlamlı fark saptanmamıştır (p>0.05). İğsi hücreli GİST ler genellikle sellüler nitelikli, hafif atipi içeren tümörlerdir. Epiteloid GİST lerde de genellikle hafif atipi izlenebilmektedir. Her iki grupta da belirgin pleomorfizm görülme oranı oldukça düşüktür (49,52,99). Çalışmamızdaki iğsi hücreli GİST lerin %85 inde belirgin sellülarite mevcuttur. Tüm vakaların ise %51 (19/37) inde atipi hafif derecelidir. Bazı yayınlarda hafif sellülarite olumlu prognostik faktör kabul edilirken, bazı yayınlarda bu parametrenin standartizasyon güçlüğünden ve klinik davranış açısından öneminin net olmayışından bahsedilmiştir (43,73). Miettinen ve ark. (68) nın çalışmasında diffüz orta ve yüksek dereceli atipi prognostik kriter olarak öngörülmüş olup, fokal ve hafif dereceli atipinin önemli olmadığı rapor edilmiştir. Sitolojik atipinin belirgin olduğu vakalarımızdan %72 (13/18) si, sitolojik atipinin hafif olduğu vakalarımızdan ise %37 (7/19) si yüksek risk grubundandır (p<0.05). Bununla birlikte tüm otörlerce, kötü prognostik faktör olarak kabul edilen mitoz sayısı da, sitolojik belirgin atipinin izlendiği vakalarda anlamlı olarak daha yüksek saptanmıştır (p<0.05). Gastrointestinal stromal tümörlerde, zengin ince cidarlı vasküler yapılar nedeniyle tümörde kanama sık görülen bir bulgudur (52). Fujimoto ve ark. (157) nın makalesinde, univarite analizlerleri ile tümörde kanama varlığı kötü prognostik faktör olarak değerlendirilmiştir. Bununla birlikte prognoz değerlendirilmesinde güvenilir bir parametre olmadığını belirten çalışmada vardır (166). Çalışma grubumuzdaki vakalarda da, kanama ile risk grupları arasında anlamlı fark bulunmamaktadır (p>0.05). Miettinen ve ark. (70) nın 2002 yılındaki GİST lerde prognoz çalışmasında, gastrik ve intestinal GİST lerde sık karşılaşılan ülserasyonun, hem benign hem de malign davranış gösteren tümörlerde görülebileceği ve tümör nedenli Gİ kanamaya sebep olabileceği belirtilmiştir. Bununla birlikte yapılan diğer çalışmalarda ülser varlığının, tümör boyutu ile ilişkili olabileceği ancak prognostik önemi olmadığı raporlanmıştır (73,76). Miettinen ve ark. (68) nın 2005 yılındaki çalışmasında ise, ülserasyonun progresif hastalı için istatistiksel öneminden bahsedilmiş olup, tümör boyutu ve mitotik orana sekonder, prognostik belirleyici olarak kabul edilmesi önerilmiştir (68). Çalışmamızdaki olgularda ülser oranı, yüksek risk 67
72 grubundaki vakaların %40 (8/20) ında, diğer risk gruplarının ise %12 (2/17) sinde saptanmıştır (p>0.05). Çok düşük risk grubunda mide yerleşimli, ülser saptanan bir vakada (10 nolu olgu) tümör primer olarak submukozal yerleşimli, 5 cm çapta ve sınırlı alanlarda nekroz bulunup, bu alanlarda lamina propriayı infiltre ederek yüzeyel ülser oluşturmaktadır. Düşük risk grubunda, ülser saptanan mide yerleşimli tek vaka ise 8 cm çaptadır ve yine submukozal yerleşim göstermekte, nekroz alanları içermektedir. Dolayısıyla, bu iki vakada saptanan yüzeyel ülserlerin nedeni, yüksek risk faktörlerini içermesinden ziyade tümör boyutuna ve mide duvarında lümene yakın bir bölgeden köken almasına bağlı olabilir. Miettinen ve ark. (68) nın oldukça geniş serilerinde prognostik histolojik prediktif parametre olarak belirtilen, muhtemel tümör infarktının bir göstergesi olan, koagülatif nekroz GİST lerde malign tümör davranışı ile ilintili bulunmuştur. Ancak bu bulgunun benign tümörlerde de görülebileceği belirtilmiştir. Aynı çalışmada, mikrokistik yapıların oluşmasına neden olan likefaksiyon nekrozunun ise yine benign GİST lerde de saptanabilen, sık karşılaşılan bir özellik olduğu, bununla birlikte kötü prognoz göstergesi olarak önemi olmadığı raporlanmıştır (68). Tetikkurt ve ark. (160) nın çalışmasında, GİST lerde nekroz ve artan risk derecesi ile önemli korelasyon saptanmıştır. Fujimoto ve ark. (157), 140 olgu içeren klinikopatolojik çalışmalarının univarite analizlerinde, tümör nekrozunun prognoz tahmininde önemli olduğunu belirtirken, multivarite analizlerinde aynı sonuca ulaşamamışlardır. Wong ve ark. (164) ile Muro-Cacho ve ark. (167) nın yayınlarında da tümörde nekroz varlığının, malign davranışın belirlenmesinde önemli bir bulgu olduğu vurgulanmıştır. Çalışmamızda da, artan risk derecesi ile nekroz varlığı gösteren vakalar korelasyon göstermektedir (p<0.05). Mukozal invazyon, neoplastik hücrelerin glandüler elemanlar arasından lenfomabenzeri paternde diffüz infiltrasyonudur (70). Sık görülmemekle birlikte [çalışmalardan birine göre GİST lerin %3 ünde (68)], kötü prognozu işaret eder (73,90). Klinik davranış açısından mukozal invazyonun önemi konusunda net fikir birliğine varılamamıştır, ülserasyon ile ayrımının yapılmasının önemli olduğu vurgulanmaktadır (5). Miettinen ve ark. (70) nın çalışmalarına göre mukozal invazyon sadece malign GİST lerde görülmektedir. Wong ve ark. (164) nın çalışmasında, progresyon değerlendirme kriterleri (çap, mitoz, nekroz, ki67 indeksi, p53 immün pozitivite) multivarite analizleri ile anlamlı bulunmuş, mukozal invazyon ise anlamlı bulunmamıştır. Çalışmamızdaki vakaların %32 sinde (12 olgu) mukozal invazyon, %27 sinde (10 olgu) ise mukozal invazyon yanı sıra ülserasyon da mevcuttur. Mukozal invazyon gösteren olguların %83 ü (p<0.05), mukozal invazyon ve ülserasyon beraber gözlenen olguların %80 i (p>0.05) yüksek risk grubuna dahildir. İlginç olarak düşük risk 68
73 grubunda, mukozal invazyon görülen 1 vakamızda (30. olgu) lenf bezi metastazının da olması Miettinen in hipotezini desteklemektedir. Miettinen ve ark. (90) nın bir başka makalesinde de mukozal invazyon gösteren vakalarda mitotik aktivitenin yüksek olduğu saptanmıştır. Mukozal invazyon saptanan 12 olgumuzda sayılan mitoz ortalaması 16 dır. Mukozal invazyon mitoz sayısı ile beraber değerlendirildiğinde, istatistiksel olarak anlamlı sonuç bulunmuştur (p<0.05). Kas invazyonu GİST lerde sık karşılaşılan (%60-69) bir bulgudur (68,90). Özellikle küçük GİST lerde düz kas lif ve demetleri arasında tümör invazyonunun görülmesi karakteristik büyüme paternidir. Bu gelişim şekli, GİST lerin köken aldığı düşünülen Cajal hücreleri veya kök hücrelerinin muskularis propria tabakaları arasında yerleşim göstermesi ile açıklanmaktadır (67,84,94). Bu yüzden düz kas invazyonunun prognostik önemi olmadığı belirtilmektedir (70). Çalışmamızda literatüre kıyasla daha yüksek oranda (%78) kas invazyonu görülmüştür. Özellikle ekstramural tümörler başta olmak üzere, ekilme yoluyla yayılmaya eğilimi olan GİST ler, rekürrens ve uzak metastazlarını, çevre dokulara direkt invazyon ile gerçekleştirirler. Bir çok çalışmada serozal invazyon ile progresif hastalık arasında korelasyon tespit edilmiştir (5,68,90,161,168). Agaimy ve ark. (168) nın çalışmasında, ekstramural yerleşimli tümöral kitlenin serozal penetrasyon ve peritoneal yayılımın, serozal yüzde bulunan ince fibröz dokunun kısmi veya tam yokluğu ile gerçekleştiği tanımlanmıştır. Olgularımızdan 9 unda çevre dokulara invazyon görülmüş olup, bu vakaların 8 i yüksek risk grubundandır. Orta risk grubundan çevre doku invazyonu gösteren 1 vakada da omental nüks gelişmiştir. Literatürde, tanı anında birden fazla kitle halinde saptanan olguların, metastatik mi yoksa multisentrik GİST mi olduğu önemli bir tartışma konusudur. Klinik davranış ve tedavi protokolünün belirlenmesi açısından oldukça önemli olan bu kararın verilmesi bazen güç olmaktadır. Metastatik olan vakalar gerçek malign davranışta kabul edilirken, multipl GİST tanısı almış vakalar multipl primer tümör olarak değerlendirilmelidir. KIT mutasyon statülerine göre multipl GİST ler üç gruba ayrılmaktadır; 1) Sporadik multipl GİST somatik KIT mutant, 2) Ailesel multipl GİST germline KIT mutant, 3) Wild tip (mutasyon içermeyen) multipl GİST nörofibromatozis 1 ilişkili. Nadir saptanan multipl GİST vakaları, genellikle ailesel kalıtım ya da nörofibromatozis 1 ile ilişkili bulunur iken, sporadik multifokal GİST ler çok daha nadirdir (88, ). Ailesel GİST sendromu otozomal dominant geçiş gösteren, ailenin iki veya daha fazla mensubunu etkileyen, bir veya daha çok kitlenin saptanabildiği hastalık olarak tanımlanmıştır. Genellikle orta yaşlı bireylerde benign 69
74 tümöral kitleler olarak izlenen GİST lere, hiperpigmentasyon, ürtikeriya pigmentoza ve disfaji gibi bulgular eşlik edebilir (172). Orta yaş veya yaşlı bireylerde görülen Nörofibromatozis 1 ilişkili GİST ler, genellikle ince barsak (ileum ve jejunum) yerleşimli olup, tümöral kitleler sıklıkla çok sayıdadır. Ayrıca bu vakalarda tümör dışı barsak alanlarında ICC hiperplazisi izlenmektedir. Multipl sporadik GİST ler, genellikle daha ileri yaş grubundaki hastalarda görülen, iki veya üç senkron kitle şeklinde prezente olan, çoğunlukla mide yerleşimli ve iğsi hücreli tümörlerdir. CD117 ve CD34 pozitifliği gösteren bu tümöral kitlelerin her birinde farklı genlerin (KIT veya PDGFRα), farklı lokuslarında değişik tipte genetik mutasyonlar saptanabilir (172). Agaimy ve ark. (171) nın bir çalışmasında, moleküler analiz yapılmasının mümkün olmadığı durumlarda multipl kitlelerin gelişim şeklini açıklayabilmek için, rutin pratikte uygulanabilir histolojik kriterler önerilmiştir. Bu önerilere göre, muskularis propria invazyonu göstermeyen, peritoneal yerleşimli, benzer histolojik görünüm ve immünprofile sahip, yüksek risk özellikleri taşıyan kitleler metastatik hastalık olarak değerlendirilmelidir. GİST olgularımızın 5 inde tanı anında batın ve batın içi organlarda birden fazla kitle saptanmıştır. Bu olguların 3 ünde ana kitle (en büyük çapa sahip kitle) ince barsak duvarında ve mezosunda, 1 inde retroperitonda, 1 inde midede yer almaktaydı. İnce barsakta yer alan olguların hepsinde tümör çapı 5 cm nin üzerinde idi. Ayrıca, bu olguların tümünde nekroz ve hipersellülarite mevcut iken, 2 sinde kanama, 1 inde belirgin sitolojik atipi, 1 inde serozal invazyon, 1 inde ise karaciğer metastazı izlendi. Multipl kitle içeren vakalardan retroperitoneal yerleşimli olan olgumuz, yüksek risk grubunda, çevre organ yayılımı göstermekte, kanama, belirgin sitolojik atipi ve hücresellik içerip, mitoz oranı 40 iken, en büyük kitle çapı 3 cm idi. Midede multipl kitleleri olan son olgumuzda lenf bezi metastazı saptanmış ve mukozal ülserasyon, nekroz, kanama, serozal invazyon, belirgin sitolojik atipi ve hipersellülarite mevcut olmasına karşın, tümör çapı 10 cm den küçük (8 cm) ve mitoz oranı 5 idi. Vakaların mutasyonel analiz ile değerlendirilmediği çalışmamızda, literatür bilgilerine dayanılarak, histomorfolojik kriterlere göre, gerçek malign davranış gösteren, birden fazla kitle saptanan 5 olgumuz, implantasyon yoluyla metastatik hastalık olarak değerlendirilmiştir. Benzer morfolojik görünüm ve lokalizasyonlarda yerleşim gösteren, ancak tedavi ve prognozu diğer mezenkimal tümörlerden tamamen farklı olan bu özel tümörlerin doğru tanı alabilmesi için, ESMO ( European Society for Medical Oncology ), NCCN ( National Comprehensive Cancer Network ) ve Canadian Advisory Committee on GISTs tarafından yayınlanan yönergelere göre, rutin HE incelemelere ek olarak, İHK sal çalışmalara 70
75 gereksinim vardır (130). İHK sal açıdan, c-kit (CD117) pozitif tümörler olarak tanımlanan GİST lerin, tanı basamaklarında bu belirtecin ekspresyonu anahtar rol oynamaktadır (67,173). Ancak, İHK sal olarak CD117 pozitifliği, tümörde c-kit mutasyon varlığı anlamına gelmemektedir. Mutasyon analizi çalışmaları ile saptanmış, PDGFRα-mutant ve wild tip GİST lerde CD117 ekspresyonu görülebildiği gibi, c-kit-mutant GİST lerde CD117 negatif olabilir (45,52,68,99,152). Çeşitli yayınlarda GİST lerde CD117 ile pozitif reaksiyon oranı % olarak raporlanmış, boyanma niteliğinin genellikle diffüz ve kuvvetli olduğu belirtilmiştir (Tablo 35) (1,25,49,89,90,95,99,121,130,161). Bununla birlikte daha spesifik olarak, CD117 ile dot-like (Golgi-pattern) pozitiflik veya membranöz boyanma görülebilir (45,49,52,68,152). Literatür ile uyumlu olarak, çalışmamızdaki vakaların tümünde CD117 ile pozitif reaksiyon görülmüş, %86 sında diffüz ve kuvvetli boyanma saptanmıştır. Boyanma paterni genellikle sitoplazmik olmakla birlikte, bir vakada membranöz boyanma da tespit edilmiştir. Literatürde CD117 boyanma yaygınlığı veya paterni, c-kit mutasyonu ve imatinib yanıtı ile korele olmadığı belirtilmiştir. Ancak fokal veya zayıf CD117 ekspresyonu gösteren GİST ler ile tamamen negatif olgular muhtemel olarak wild tip ya da PDGFRα-mutant (özellikle gastrik yerleşimli, epiteloid morfolojiye sahip olgular) vakalar olarak yorumlanabilir (49,68). Miettinen ve ark. (174) nın çalışmasında CD117 pozitifliğinin lokalizasyon ile korele olmadığı rapor edilmiştir. Zayıf ve/veya fokal boyanma gözlenen 5 olgumuzdan 2 si kolon yerleşimli iken (bu lokalizasyondaki olguların %50 si), diğerleri ince barsak, retroperiton ve mide yerleşimlidir. Hücre morfolojileri heterojen dağılım gösteren bu vakaların 4 ü yüksek risk grubundandır. İlginç olarak bu vakalardaki mitoz oranı oldukça yüksek saptanmıştır (ortalama 31.4), (p<0.05). Ancak bu bulgu ile ilgili literatürde örnek bilgiye rastlanmamıştır. Bununla birlikte risk gruplarına göre yapılan, CD117 boyanma paterni karşılaştırmalarında anlamlı fark görülmemiştir (p>0.05). GİST olgularımızın %100 ünde CD117 pozitif iken, GİST dışı mezenkimal tümör olgularımızın %18 (8/45) inde pozitiftir (p<0.05). CD117 antikorunun tanımlanmasından önce, hematopoetik progenitör hücre antijeni olan CD34 GİST tanısında en değerli kabul edilen belirteç idi (45,82). Literatürde GİST lerde CD34 ile pozitiflik oranı %40-82 arasında değişmektedir (5,25,41,43,52,68,87-90). Literatürle uyumlu olarak vakalarımızın %62 sinde CD34 ile pozitif reaksiyon izlendi. Çeşitli çalışmalarda CD34 pozitifliğinin özefagus ve rektum yerleşimli tümörlerde daha yüksek oranlarda olduğu belirtilmiştir (41,45,175). Başka bir çalışmada ise, gastrik GİST lerin (%82), ince barsak yerleşimli GİST lere (%40) oranla, daha fazla CD34 ekspresyonu gösterdiği 71
76 raporlanmıştır (83). Rektum ve özefagus yerleşimli vakamız bulunmamakla birlikte, mide yerleşimli vakalarımızda CD34 pozitiflik oranı (%81.9) literatüre uyumlu olarak ince barsaktakilere kıyasla, nispeten daha yüksek bulunmuştur. Lina ve ark. (176) tarafından yayınlanan bir çalışmada, benign GİST in tümünde CD34 ile boyanma gözlenirken, malign formlarda boyanma oranının düşük olduğu belirtilmiştir. Bu bulgu yazarlar tarafından, benign GİST lerin ICC lere diferansiye olan, CD34 pozitif kök hücrelerden kaynak almasına, malign GİST lerin ise dediferansiye ICC lerden meydana gelmesine bağlanmıştır (176). Daha yakın tarihli çalışmalarda ise bu antikor ekspresyonunun prognostik önem taşımadığı vurgulanmıştır (45,70,90). Çalışmamızda yüksek risk grubuna dahil olguların %55 inde (11 olgu), diğer risk gruplarının ise %71 inde (12 olgu) CD34 pozitifliği saptanmıştır (p>0.05). GİST ler yüksek lokal rekürrens oranlarının görüldüğü tümörlerdir (110). Ancak KİT ve PDGFRα yı hedefleyen, tip III tirozin kinaz inhibitörleri ile tümör büyümesi kontrol altına alınabilir. Böylece progresyonsuz sağ kalım sağlanarak, klasik tedavi rejimlerinin komplikasyonlarından korunan hastanın yaşam kalitesi arttırılabilir (110,177). Yukarıda da bahsedildiği gibi, yakın tarihlere kadar GİST tanısının verifikasyonunda altın standart immünohistokimyasal c-kit pozitifliği olup, CD34 ekspresyonu tanı destekleyici marker olarak kabul edilirdi (121,134). Ancak özellikle PDGFRα mutant vakalar olmak üzere, GİST lerin önemli bir kısmında (~%4-15) saptanan, negatif veya şüpheli CD117 ekspresyonu tanıda soru işaretlerinin oluşmasına neden olabilmektedir (112,121,134). Bununla birlikte, c-kit in İHK sal uygulama optimizasyonundaki güçlükler, c-kit belirtecinde, yanlış pozitif ve negatif sonuçlara neden olabilmektedir (134). Tanı sıkıntısı yaşanan bu vakaların tanımlanabilmesinde, tümörde KIT veya PDGFRα mutasyon statüleri moleküler yöntemler ile saptanabilmektedir. Ancak bu yöntem, tanı sürecinin uzamasına ve maliyetinin artmasına neden olmakla birlikte, hem yurtiçi hem de yurtdışında sınırlı sayıda merkezde uygulanabilmektedir ( ,122,123). Bu sebepler ile rutin uygulamada kullanılabilecek, tanıya yardımcı çeşitli İHK sal belirteçler üzerinde çalışmalar yapılmaktadır. İlk defa 2004 yılında, West ve ark. (110) ı tarafından hipotetikal proteini kodlayan, FLJ10261 geninin GİST lerde spesifik olarak eksprese edildiği saptanmış ve DOG1 olarak isimlendirilmiştir. Tanımlandığı ilk yıllarda fonksiyonu henüz bilinmeyen DOG1 geni ve bunun ürünü protein, daha sonra transmembran protein 16A (TMEM16A) adı ile yeniden adlandırılmıştır. Son yayınlarda ise, bu genin eksprese ettiği proteinin, bir kalsiyum bağımlı klor kanal proteini olduğu saptanarak ANO1 (anoctamin 1, calcium-activated chloride channel) adı verilmiştir. Ancak her üç sinonimde günümüzde değişik yayınlarda kullanılabilmektedir 72
77 (45,116,117,134). Bu konuda ilk çalışma olan West ve ark. (110) nın araştırmasında, mutasyon statüsünden bağımsız olarak, hem immünohistokimya hem de in situ hibridizasyon yöntemleri ile, GİST olgularının %97.8 inde DOG1 (poliklonal) ekspresyon varlığı gösterilmiştir. Aynı şekilde DOG1 antikoru ile, daha sonra yapılan çeşitli çalışmalarda da GİST lerde % oranlarında boyanma tespit edilmiştir (Tablo 35) (9,110,111,122,124). Son günlerde ise, bu yeni ve popüler antikorun poliklonal formu yerine, daha spesifik olduğu saptanan, K9, DOG1.1 ve DOG1.3 olarak adlandırılan, monoklonal subtipleri üretilmiş ve çalışmalar bu belirteçlerle süldürülmektedir (112,121,123,134,178). Tablo 35. Gastrointestinal stromal tümörlerde Discovered on GIST ve CD117 pozitifliğini araştıran çalışma sonuçlarının kıyaslanması Total GİST (n) Total N-GİST (n) DOG Klon GİST DOG(+) (n %) GİST CD117(+) (n %) DOG(+), CD117(-) GİST (n%) N-GİST DOG(+) (n %) N-GİST CD117(+) (n %) Miettinen 2009 (134) K9, m 1103 (94.4) 1106 (94.7) 14/62 (22.6) 15 (2.6) BY Espinosa 2008 (112) DOG1.1, m 370/425 (87) 317/428 (74) BY 3 (0.3) 20 (2.1) West 2004 (110) p 136/139 (97.8) 134/144 (93) BY 4 (0.9) BY Ardeleanu 2009 (124) 14 Ø p 14 (100) 14 (100) Vaka yok Ø Ø Liegl 2009 (121) 81 Ø DOG1.1, m 61/81 (75.3) 53 (65.4) 10/28 (36) Ø Ø Lopes 2010 (123) DOG1.1, m K9, m 538 (80.5) 642 (96.1) 643 (96.3) 5/25 (20) 19/25 (76) 3 (0.4) 7 (1) 8/686 (1.2) Novelli 2010 (178) K9, m 184/186 (99) 176/182 (97) 7/182 (3.8) 0/28 (0) 0/28 (0) Güler SP31, m 33 (89) 37 (100) Vaka yok 3 (6.7) 8 (18) DOG; Discovered on GIST, GİST; Gastrointestinal stromal tümör, N-GİST; GİST dışı mezenkimal tümör, m; monoklonal, p; poliklonal, Ø; Çalışılmamış, BY; Bilgi yok 73
78 Çalışmamız kapsamındaki GİST olgularının %89 (33/37) unda monoklonal DOG1 (klon SP31) antikoru ile pozitif reaksiyon mevcuttur. Kontrol grubu olarak çalışmamıza seçilen GİST dışı mezenkimal tümörlerin ise sadece %7 (3/45) sinde DOG1 ekspresyonu izlenmiştir, (Tablo 31, p<0.05). GİST vakalarında DOG1 boyanma paterni çoğunlukla kuvvetli ve diffüz iken, GİST dışı mezenkimal tümör grubundaki DOG1 pozitif 3 vakadan birinde fokal, diğer ikisinde nispeten zayıf boyanma izledik. İstatistiksel analiz uygulayabilmek için, çalışmamızdaki GİST olguları yüksek risk grubu ve diğerleri şeklinde sınıflandırıldığında, yüksek risk grubunda DOG1 pozitifliği %85, diğer risk gruplarında ise %94 olarak saptanmıştır. DOG1 pozitivitesinin yoğunluk ve yaygınlığında, risk durumu yükseldikçe hafif bir azalma dikkat çekmekle birlikte, bu durum anlamlı bulunmamıştır (Tablo 27, p>0.05). Literatürde DOG1 antikoru ile yapılmış GİST çalışmalarında, DOG1 pozitifliği tümörün değişik parametreleri (mutasyon tipi, tümör derecesi, tümör boyutu, hasta yaşı, primer lokalizasyon, mitoz, pleomorfizm) ile kıyaslanmış ancak hiçbir parametre ile anlamlı sonuç olmadığı bildirilmiştir (121,122,134). Bununla birlikte Miettinen ve ark. (134) nın oldukça geniş bir seriyi kapsayan çalışmalarında, intestinal yerleşimli GİST lerde (1168 olgu) c-kit antikorunun DOG1 den daha sensitif olduğu vurgulanmıştır. Lee ve ark. (122) nın çalışmalarında da, DOG1 in gastrik orijinli, epiteloid morfolojideki, PDGFRα mutasyonu gösteren GİST lerde daha sensitif olduğu belirtilirken, iğsi hücreli tiplerde ise c-kit in daha sensitif olduğu raporlanmıştır. Sözü edilen tümör parametrelerinin çalışmamızda DOG1 pozitifliği ile kıyaslanması planlandı ancak total tümör sayımızın düşük olmasına bağlı olarak, gruplardaki tümör sayılarının da az olması nedeniyle, istatistiksel analiz için uygun bulunmadı. Miettinen ve ark. (134) DOG1 i konu alan son yayınlarında, çalışma kapsamına 1168 GİST vakası yanı sıra, diğer tümör grupları ve normal dokulardan 672 vakayı dahil etmişlerdir. GİST olguları dışındaki mezenkimal tümörlerin (562 olgu) 15 inde (uterin tip retroperitoneal leiomyom, peritoneal leiomyomatozis, sinovyal sarkom) DOG1(monoklonal, klon K9) pozitif bulunmuştur. Lopes ve ark. (123) nın çalışmalarında da 686 mezenkimal tümörden 7 sinde (yumuşak doku leiomyosarkomu, sinovyal sarkom, anjiosarkom) DOG1 (monoklonal, klon K9) antikor ekspresyonu gösterilmiştir. West ve ark. (110) nın makalesinde, 438 GİST dışı mezenkimal tümörün 4 ünde (sinovyal sarkom, leiomyosarkom, fibrosarkom, Ewing sarkom) DOG1 (poliklonal) pozitifliği saptanmıştır (Tablo 35). Kontrol 74
79 grubu olarak aldığımız GİST dışı mezenkimal tümörlerin 3 ünde (malign periferik sinir kılıfı tümörü, anjiosarkom, schwannom) DOG1 (monoklonal, SP31) pozitif bulundu. Literatürde DOG1 ile yapılmış yayınların neredeyse tümünde, CD117 ile ekspreyon oranları karşılaştırılarak tanı algoritmasında en spesifik immünohistokimyasal panel belirlenmeye çalışılmıştır. West ve ark. (110) nın çalışmasında bu konudaki ilk yayınlarında KIT veya PDGFRα mutant toplam 9 c-kit negatif GİST vakasında, DOG1 pozitifliği saptanmıştır. Diğer çalışmalarda da CD117 negatif GİST vakalarında DOG1 pozitiflik oranı %6-36 olarak bildirilmiştir (112,121,122). Espinosa ve ark. (112) çalışmalarında, PDGFRα mutant vakalarda c-kit ekspresyonunu %9, DOG1 ekspresyonunu ise %78 olarak saptamışlardır. Miettinen ve ark. (134) ise çalışma gruplarındaki GİST lerde, DOG1 ile %94.4 ve CD117 ile %94.7 oranında ekspresyon saptamış ve tanı basamaklarında DOG1 in de İHK sal panele eklenmesi gerektiğini belirtmişlerdir. Bununla birlikte aynı çalışmada, GİST olgularının %2.6 sında (27 olgu) her iki antikorla negatif reaksiyon izlenmiş ve böyle çıkmaz oluşturan vakalarda, doğru tanı için mutasyon analizlerinin gerekliliğinden bahsedilmiştir. Çalışmamızda ise c-kit negatif olgu mevcut olmadığı için bu konuda yorum yapılamadı. Klasik c-kit mutasyonu saptanmayan GİST lerde, PDGFRα gen mutasyonu iyi tanımlanmış alternatif bir onkojenik mekanizmadır. GİST leri konu alan çoğu yayında, bu tümörlerin PDGFRα mutasyon statüleri araştırılmıştır. Ancak PDGFRα immün belirleyicisinin tanı basamaklarındaki önemi, ticari antikorlarun güç ulaşılaşılabilir olması nedeniyle, sınırlı sayıda makalede değerlendirilmiş ve farklı sonuçlar elde edilmiştir (49,121,128,129,179). Peterson ve ark. (128) çalışmalarında, GİST lerin mutasyon statülerinden bağımsız olarak %89.7 (35/39) sinde, GİST dışı mezenkimal tümörlerin ise %25 (5/20) inde PDGFRα ekspresyonunu İHK sal olarak saptamışlardır. Bu yayında GİST dışı vakalarda görülen pozitifliğin, zayıf veya orta şiddette olduğu belirtilmiş, kuvvetli sitoplazmik boyanmanın sadece GİST vakalarında mevcut olduğu vurgulanmıştır. Rossi ve ark. (129) nın çalışmalarında da, c-kit ekspresyonu saptanmayan GİST vakalarının tümünde PDGFRα ile pozitif reaksiyon görüldüğü bildirilmiştir. Daha yeni yayınlarda ise, özellikle ticari olarak sağlanabilen PDGFRα antikorunun uygulanmasındaki optimizasyon problemleri ve yoğun zemin boyanmasının engellenememesi nedeni ile, PDGFRα nın rutin İHK sal kullanımında yaranının sınırlı olduğu belirtilmektedir (49,121). Çalışmamızdaki GİST olgularının hepsinde PDGFRα ile pozitif reaksiyon izlenmiştir. GİST dışı mezenkimal tümör grubundaki vakalarımızın ise %47 (21/45) sinde PDGFRα ekspresyonu mevcuttur (p<0.05). Ayrıca GİST 75
80 olgularımızda, boyanma paterni risk grupları ile korele olmayan (p>0.05) PDGFRα pozitivitesi genellikle şiddetli ve diffüzdür. Gastrointestinal stromal tümörler mezenkimal hücre belirleyicisi olan vimentin ile % oranında pozitif reaksiyon gösterirler (25,45,153,157). Literatürle uyumlu olarak, çalışmamızdaki GİST olgularının tümünde vimentin ile boyanma mevcuttur. Cajal hücrelerinin ultrastrüktürel incelenmesinde, karakteristik yapı olarak hem düz kas, hem de nöral diferansiyasyona ait özellikler taşıdığı görülmüştür. Öncül multipotansiyel hücreler olarak kabul edilen Cajal hücrelerinin neoplastik formunun bu nedenle myoid ve nöral antijenleri eksprese edebildiği düşünülmektedir (89,157). Gastrointestinal stromal tümörlerde düz kas hücre kökeni belirteci olan SMA ile boyanma oranı değişik yayınlarda %5,5-40 olarak raporlanmış olup, reaksiyonun fokal nitelikli olduğu belirtilmiştir (5,41,43,45,52,90,99,157). Bununla birlikte SMA ekspresyonu gösteren olguların daha çok ince barsak yerleşimli olduğu ve nispeten daha iyi prognoza sahip olduğu bildirilmiştir (41,45,68,90,164). Olgularımızdan %5.4 (2/37) ünde SMA ile boyanma saptanmış olup, vakalardan biri ince barsak (orta risk grubu), diğeri kalın barsak (yüksek risk grubu) yerleşimlidir. Literatürde gerçek c-kit pozitif GİST lerde desmin pozitifliği oldukça nadirdir. Yayınların çoğunda desmin pozitivite oranı %1-2 dir (5,41,52,87,155,180). Bazı tümörlerde ise, tedavi öncesi ve sonrası yapılan seri biyopsiler ile imatinib tedavisinin desmin ekspresyonunu arttırdığı bildirilmiştir (45). Çalışmamızdaki vakaların hiç birinde desmin ekspresyonu saptanmamıştır. Gastrointestinal stromal tümörlerde, nöronal bir belirteç olan, S100 ile boyanma oranı (%0-10) düşüktür (5,41,43,52,87,89,153,180,181). Bazı yayınlarda S100 ile boyanma oranının ince barsak lokalizasyonundaki tümörlerde daha yüksek olduğu bildirilmiş, bazı yayınlarda da gastrik yerleşimlilerde saptanan ekspresyonun kötü prognoz göstergesi olduğu belirtilmiştir (89,181). Wong ve ark. (164) nın çalışmasında, S100 ekspresyonu gösteren GİST lerin daha yüksek sağ kalıma sahip olduğu, Miettinen ve ark. (90) nın çalışmasında ise bu özelliğin prognostik önem taşımadığı vurgulanmıştır. Çalışmamızda S100 pozitif GİST olgusu saptanmamıştır. Gastrointestinal stromal tümörlerde prognoz öngörüsü için birçok kriter test edilmiş ancak çoğunun yeterince yardımcı olmadığı görülmüştür. Küçük çaplara (hatta 2 cm den küçük) ve çok düşük mitoz oranlarına sahip lezyonların dahi metastaz yapabildiği bildirilmiştir. Bu nedenle çoğu otör, malign davranışın belirlenebilmesi için, daha objektif olması amacıyla, İHK sal olarak hücre proliferasyon belirteçleri ile çalışmalar yapmışlardır 76
81 (41). Çalışmalarda saptanmıştır ki, bu prognostik belirteçlerden en önemlisi ki67 dir ve çoğu çalışmada %10 dan fazla nükleer ki67 antijen pozitifliği, yüksek proliferasyon indeksi olarak kabul edilmiştir (157,164). Wong ve ark. (164) nın pür gastrik GİST lerden oluşan geniş serilik bir çalışmasında, yüksek ki67 indeksinin bağımsız kötü prognoz prediktörü olduğu raporlanmıştır. Ancak yine aynı çalışmada, hücre proliferasyonunu belirlemede resmileşmiş en tutarlı bulgunun mitoz sayımı olduğu belirtilerek, İHK sal sonuçlara üstünlüğü vurgulanmıştır. Benzer bulgular başka çalışmalarca da desteklenmiştir (41,45,70,160,164). Farklı olarak Meara ve ark. (181) çalışmalarında agresif ve agresif olmayan GİST ler arasında istatistiksel anlamlı ki67 indeks farkı bulunmadığını bildirmişlerdir. Çalışmamızda GİST olgularının %37.8 inde ki67 proliferasyon indeksi >%10 idi. Risk gruplarına göre baktığımızda da yüksek risk grubuna ait vakaların %60 ında yüksek proliferasyon indeksi saptanırken, diğer risk gruplarında ise bu oran %11.8 idi ve aradaki fark anlamlı bulundu (p<0.05). Ki67 indeksi ile mitoz sayısı kıyaslandığında, mitoz oranı 50 BBA da >5 olan 19 vakanın 11 (%58) inde yüksek ki67 proliferayon indeksi mevcuttu. Mitoz sayısı 50 BBA da 5 olan olguların %83 ünde ki67 oranı %10 dan küçük bulundu (p<0.05). Hücre proliferasyon belirteçlerinden başka, GİST lerde klinik davranışı öngörebilmek için, farlı İHK sal belirteçlerde denenmiştir. Bu belirteçlerden biri de antiapoptotik molekül olan Bcl-2 dir (164). Stem cell factor ile aktive olan KIT in Bcl-2 ekspresyonuna öncülük ettiği bilinmektedir. Bu nedenle, GİST lerde sıklıkla saptanan bu antikorun yüksek ekspresyonu, KIT aktivasyonunun karakteristiğine bağlı olabilir. Diğer taraftan yüksek Bcl-2 ekspresyon oranı farklı tedavi rejimleri gerekliliğinin göstergesi olabilir (182). İmmünohistokimyasal olarak Bcl-2 nin artmış ekspresyonunun GİS dışındaki mezenkimal tümörlerde (uterin ve ekstrauterin leiomyosarkom ve yumuşak doku sarkomları gibi) prognostik önem taşıdığı gösterilmiştir (164). Küçük hasta gruplarında çalışılmış Bcl-2 ekspresyon varlığının GİST lerde de prognostik önem taşıdığını savunan çalışmalarla birlikte, aksi sonuçların raporlandığı çalışmalar da bulunmaktadır (164,182). Bernadette ve ark. (49) nın makalesinde de, Bcl-2 ve benzeri belirteçlerin GİST lerde öneminin net olmadığı vurgulanmıştır. Çalışmamızda GİST olgularının %54 (20/37) ünde Bcl-2 pozitifliği saptandı. Yüksek risk grubunda Bcl-2 pozitifliği %45 (9/20) iken, diğer grupların toplamında %65 (11/17) olarak tespit edilmiştir (p>0.05). Karaciğere metastaz yapmış olguların 3 ünde, lenf bezi metastazı olan 3 olgunun tümünde ve nüks saptanan olguların 2 sinde Bcl-2 pozitifliği mevcuttu. 77
82 SONUÇLAR Çalışmamızda Trakya Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı nda GİST tanısı almış 37 olgu ve kontrol grubu olarak seçilen 45 mezenkimal tümör birlikte yeniden değerlendirilip, immunohistokimyasal belirleyiciler eşliğinde, GİST lerde tümör davranışının öngörüsü ile spesifik ve sensitif ayırıcı tanı basamaklarının tespiti amaçlanmıştır. 1. Progressif hastalık risk gruplarına göre yeniden sınıflandırılan GİST olgularımızın %54.05 i yüksek, %18.92 si orta, %16.22 si düşük, %8.11 i çok düşük risk ve %2.70 i risk yok grubuna dahildi. 2. GİST olgularımızın yaş aralığı olup, %59.5 i kadın, %40.5 i erkekti. En sık primer tümör yerleşim bölgesi ince barsak (%51.4), daha sonra sırasıyla mide (%29.7), kalın barsak (%10.8), retroperiton (%8.1) du. Lokalizasyon ve risk grupları arasındaki ilişki, gruplardaki olgu sayıları az olduğu için istatistiksel olarak değerlendirilemedi ancak, yüksek risk grubundaki hastaların %55 inin ince barsak yerleşimli olduğu saptandı. 3. Tümör çapı cm arasında değişen GİST olgularımızda, boyut ve lokalizasyon arasında anlamlı fark izlenmedi (p>0.05). Tümör çapı ve risk grupları arasındaki ilişki ise istatistiksel olarak anlamlı bulundu (p<0.05). Yüksek risk grubunda çap ortalaması cm, diğer risk gruplarında ise 6.82 cm olarak saptandı. 4. Yüksek risk grubuna dahil GİST olgularının %90 ında, 50 BBA da 5 ten fazla mitoz sayılmış olup, bu grupta mitoz ortalaması 21.9, diğer risk gruplarında ise 3.1 olarak saptandı. Mitoz sayısı ile risk grupları arasındaki ilişki istatistiksel olarak anlamlı bulundu (p<0.05). 5. GİST hücre tipi ile risk grupları arasında anlamlı fark saptanmadı (p>0.05). 78
83 6. GİST olgularımızın çoğunda belirgin pleomorfizm görülmemesine karşın, sitolojik atipinin nispeten belirgin olduğu vakaların %72 si yüksek risk grubunda idi (p<0.05). Sitolojik belirgin atipi ile mitoz sayısının >5/50 BBA olması arasındaki ilişki anlamlı bulundu (p<0.05). Sitolojik atipi ile hücresellik arasında ise istatistiksel anlamlı ilişki saptanmadı (p>0.05). 7. GİST lerde sık görülen bir bulgu olan tümörde kanama varlığı vakalarımızın 30 (%81.1) unda izlendi, ancak risk grupları ile ilişkili bulunmadı (p>0.05). 8. Tümör kitle çapının büyüklüğü ve tümör yerleşim yerine ya da tümöral infiltrasyona bağlı olarak oluşan mukozal ülserasyon, GİST vakalarımızın 10 (%27) unda saptandı ancak bu oran risk grupları ile ilişkili bulunmadı (p>0.05). 9. Tümör nekrozu, yüksek risk grubundaki vakaların %85 inde, diğer risk grubundaki vakaların ise %52.9 unda saptanmıştır (p<0.05). 10. Prognostik faktör olarak kabul edilen mukozal invazyon 12, çevre organ invazyonu ise 9 olguda mevcuttu ve bunların çoğunluğu yüksek risk grubuna dahildi. Mukozal invazyon gösteren olguların ağırlıklı olarak yüksek risk grubunda toplanması istatistiksel olarak anlamlı idi (p<0.05). 11. GİST olgularımızın 5 inde, tanı anında batın içinde farklı lokalizasyonlarda birden fazla kitle mevcut iken, 3 ünde lenf bezi, 4 ünde karaciğer metastazı saptanmıştır. Vakaların 3 ünde ilk operasyondan 3-9 ay sonra nüks görülmüştür. 12. DOG1 ile GİST vakalarımızın %89 unda, GİST dışı mezenkimal tümör grubumuzdaki vakaların %7 sinde pozitif reaksiyon saptandı (p<0.05). DOG1 ekspresyonu ile GİST risk grupları arasında istatistiksel anlamlı fark bulunmadı (p>0.05). GİST olgularında izlenen DOG1 pozitifliği genellikle diffüz ve kuvvetli nitelikte idi. Risk durumu yükseldikçe, DOG1 pozitivitesinin hem yoğunluğu, hem de yaygınlığında hafif azalma mevcuttu (p>0.05). 13. Otuzyedi GİST olgumuzun tümünde (%100) CD117 ile pozitif reaksiyon saptandı. GİST dışı diğer mezenkimal tümörlerde ise CD117 pozitiflik oranı %18 di (p<0.05). CD117 boyanma özelliğine göre, zayıf ve/veya fokal pozitifliğin izlendiği olgularda mitoz sayısı ortalaması 31.40, kuvvetli ve diffüz pozitiflerde ise saptandı ve aradaki fark anlamlı bulundu (p<0.05). 14. GİST olgularımızın hepsinde PDGFRα ekspresyonu saptandı. GİST dışı mezenkimal tümörlerin ise %47 sinde pozitiflik mevcuttu (p<0.05). 79
84 15. CD34 ile GİST vakalarının %62 (23/37) sinde boyanma izlendi ve CD34 pozitivitesi ile risk grupları arasında anlamlı fark saptanmadı (p>0.05). 16. GİST olgularımızın hepsinde vimentin ile diffüz pozitif reaksiyon görüldü. SMA ile 2, S100 ile 1 GİST olgusunda pozitiflik izlendi. Desmin tüm GİST olgularında negatif idi. 17. Yüksek risk grubundaki GİST olgularında, ki67 proliferasyon indeksi diğer gruplara göre anlamlı derecede yüksek saptandı (p<0.05). Yüksek mitoz sayısına sahip GİST olgularında (>5/50 BBA), ki67 proliferasyon indeksi de yüksek (>%10) bulundu (p<0.05). 18. GİST olgularının %54 (20/37) ünde Bcl2 ekspresyonu mevcuttu ve Bcl2 pozitifliği ile risk grupları arasında anlamlı fark izlenmedi (p>0.05). 19. Bu çalışmanın sonucunda, tümör yerleşim yeri ve histomorfolojik özellikleri açısından GİST tanısı ile uyumlu olgularda, destekleyici bulgu olarak immünohistokimyasal CD117 pozitifliğinin gösterilmesinin hala altın standart olduğunu düşünmekteyiz. Ancak özellikle CD117 pozitifliği saptanamayan ya da şüpheli boyanmanın izlendiği tümörlerde, DOG1 antikoru immünohistokimyasal tanı panelinde alternatif sensitif ve spesifik belirteç olarak kullanılabilir. Çalışmamızda PDGFRα ekspresyon spesifitesinin nispeten düşük bulunmasına rağmen, GİST lerde sensitivite oranı yüksek olan bu antikor, diğer antikorlar ile beraber çalışılabilecek yardımcı belirteç olarak sınıflandırılabilir. 20. Literatürde progresif hastalık kriterleri olarak kabul görmüş histopatolojik bulgular olan tümör çapı, mitoz, hücresel atipi, nekroz, mukozal invazyon ve ki67 indeksi, bu çalışmadaki olgularda da yüksek risk ile ilişkili bulundu. Bu nedenle, GİST olgu raporlamalarında, hastalık seyrinin öngörüsünde klinisyenlere de yol gösterici olarak, tümörün histolojik tüm parametrelerinin bildirilmesinin önemli olduğunu düşünmekteyiz. 80
85 ÖZET Gastrointestinal stromal tümörler, gastrointestinal sistemin en sık görülen mezenkimal tümörleridir. Çoğu zaman immünohistokimyasal c-kit pozitifliği ile tanımlanan, interstisyel Cajal hücrelerinden orijin alan bu tümörler, reseptör tirozin kinaz aktivitesini etkileyen KIT veya Platelet derived growth factor receptor α (PDGFRα) mutasyonlarına sahiptir ve klasik tedavi rejimlerinden fayda görmezler. Benzer morfolojik görünüme ve lokalizasyona sahip, ancak tedavi ve prognozu diğer mezenkimal tümörlerden tamamen farklı olan gastrointestinal stromal tümörlerin doğru tanı alabilmesi oldukça önemlidir. Çalışmamızda yıllarında tanı almış 37 gastrointestinal stromal tümör olgusunun, histolojik ve immünohistokimyasal parametreleri yeniden değerlendirildi. Ayrıca gastrointestinal stromal tümörler ile gerek lokalizasyon, gerekse morfolojik karakteristikleri açısından karışma ihtimali olan, 45 mezenkimal tümör de çalışmaya dahil edildi. Olguların tümüne immünohistokimyasal olarak, standart gastrointestinal stromal tümörler tanı ve ayırıcı tanı panel antikorları yanı sıra, son yıllarda gastrointestinal stromal tümörler için sensitivitesi kabul edilmiş popüler belirleyici Discovered on GIST 1 (DOG1) antikoru ile rutin pratikteki yararı tartışılan PDGFRα immün belirteçleri uygulandı. Çalışma kapsamımızdaki gastrointestinal stromal tümörlerin, progresif hastalık risk gruplarına göre sınıflandırılarak histomorfolojik parametrelerin araştırılması sonucunda tümör çapı, mitoz, atipi, nekroz ve ki67 indeksinin tümör risk grubu ile ilişkili olduğu saptandı (p>0.05). Gastrointestinal stromal tümör olgularımızın tümünde (%100) CD117 ve PDGFRα ile pozitif reaksiyon izlendi. CD117 ve PDGFRα pozitivite oranları, gastrointestinal stromal tümörler ile gastrointestinal stromal tümörler dışı mezenkimal tümörler arasında anlamlı 81
86 olarak farklılık göstermekte idi (p<0.05). DOG1 antikoru, gastrointestinal stromal tümörler vakalarının 33 (%89) ünde, diğer mezenkimal tümörlerin ise 3 (%7) ünde pozitif saptandı (p<0.05). DOG1 ekspresyon oranları ile gastrointestinal stromal tümörlerin çeşitli parametreleri arasında (risk grupları, boyut, lokalizasyon, mitoz) farklılık izlenmedi. Sonuç olarak, gastrointestinal stromal tümörler tanı algoritmasında lokalizasyon ve histomorfolojik bulgulara ek olarak, ayırıcı tanıya yönelik, tümör hücre kökenini belirleyebilmek için immünohistokimyasal yöntemlere gereksinim duyulmaktadır. CD117 antikoru günümüzde hala gastrointestinal stromal tümör tanısında anahtar rol oynamaktadır. Ancak, özellikle PDGFRα mutant vakalar başta olmak üzere, CD117 ekspresyonu saptanamayan olgularda yardımcı başka antikorlara ihtiyaç vardır. DOG1 ve PDGFRα antikorlarının sensitif belirteçler olarak, CD117 ile kombine edilerek kullanılmasının tanıda yarar sağlayabileceği düşünülmüştür. Anahtar kelimeler: Gastrointestinal stromal tümör, DOG1, CD117, PDGFRα, immünohistokimya. 82
87 DIFFERENTIAL DIAGNOSIS OF GASTROINTESTINAL STROMAL TUMORS SUMMARY Gastrointestinal stromal tumors are the most common mesenchymal tumors of the gastrointestinal tract. They have been generally described as immunohistochemical c-kit positive spindle or epiteloid tumors. Because of the phenotypic similarities with the interstitial cells of Cajal, a histogenetic origin from these cells has been suggested. Gastrointestinal stromal tumors commonly have activating KIT or Platelet derived growth factor receptor α (PDGFRα) mutations and the conventional treatments are not benefit for these tumors. In this study, we investigated 37 gastrointestinal stromal tumor and 45 other mesenchymal tumor cases and examined their morphological characteristic again. All cases were screened for immunoreactivity for classic diagnostic antibody panel and recently described populer markers Discovered on GIST 1 (DOG1) and PDGFRα. Based on these study, according to the gastrointestinal stromal tumor progressive disease classifying, tumor size, mitotic rate, necrosis and ki67 index were found to be associated with high risk groups. All gastrointestinal stromal tumor cases were positive with CD117 and PDGFRα. This result showed significant different from other mesenchymal tumor group (p<0.05). Thirty three gastrointestinal stromal tumors and 3 other mesenchymal tumors were positive with DOG1 antibody (p<0.05). There was no difference of DOG1 expression rate between gastrointestinal morphologic parameters (risk group, size, location, mitotic count). 83
88 In conclusion, CD117 antibody still play a key role in the diagnosis of gastrointestinal stromal tumor. However, CD117 expression negative patients, especially PDGFRα mutant cases need different markers. DOG1 and PDGFRα combination is a useful adjunct in the diagnosis of gastrointestinal stromal tumor. Key words: Gastrointestinal stromal tumor, DOG1, CD117, PDGFRα, immunohistochemistry. 84
89 KAYNAKLAR 1. Goldblum JR. Mesenchymal tumors of the GI tract. In: Odze RD, Goldblum JR (Eds.).Surgical pathology of the GI tract, liver, biliary tract and pancreas, 2nd ed. Philadelphia: Saunders Elsevier; Ch 26, p Cecilia M. Fenoglio-Preiser C, Noffsinger A, Stemmermann GN, Lantz PE, Isaacson PG. Mesenchymal tumors. In: Fenoglio-Preiser C (Ed.). Gastrointestinal pathology: An atlas and text. 3th ed. Virginia: Lippincott Williams&Wilkins; Ch 19, p Miettinen M, Blay JY, Sobin LH. Mesenchymal tumours of the stomach. In: Hamilton SR, Aaltonen LA(Eds.). World health organization classification of tumours: Pathology and genetics of tumours of the digestive system. Lyon, France: IARC Press; P Rubin BP. Gastrointestinal Stromal tumor. In: Folpe AL, Inwards CY (Eds.). Bone and soft tissue pathology, Philadelphia: Saunders Elsevier; Ch 8, p Rubin BP. Gastrointestinal stromal tumours: an update [review]. Histopathology 2006;48(1): Greenson JK. Gastrointestinal stromal tumors and other mesenchymal lesions of the gut. Mod Pathol. 2003;16(4): Herrera GA, Cerezo L, Jones JE, Sack J, Grizzle WE, Pollack WJ et al. Gastrointestinal autonomic nerve tumors, 'Plexosarcomas'. Arch Pathol Lab Med. 1989;113(8): Lauwers GY, Erlandson RA, Casper ES, Brennan MF, Woodruff JM. Gastrointestinal autonomic nerve tumors; a clinicopathological, immunohistochemical, and ultrastructural study of 12 cases. Am J Surg Pathol. 1993;17(9): Tornillo L, Terracciano LM. An update on molecular genetics of gastrointestinal stromal tumours [review]. J Clin Pathol. 2006;59(6):
90 10. Garcia-Lopez P, Garcia-Marin V, Martínez-Murillo R, Freire M. Updating old ideas and recent advances regarding the Interstitial Cells of Cajal. Brain Res Rev. 2009;61(2): Maeda H, Yamagata A, Nishikawa S, Yoshinaga K, Kobayashi S, Nishi K et al. Requirement of c-kit for development of intestinal pacemaker system. Development 1992;116(2): Lecoin L, Gabella G, Le Douarin N. Origin of the c-kit-positive interstitial cells in the avian bowel. Development 1996;122(3): Ward SM, Sanders KM. Interstitial cells of Cajal: primary targets of enteric motor innervation [review]. Anat Rec. 2001;262(1): Young HM, Ciampoli D, Southwell BR, Newgreen DF. Origin of interstitial cells of Cajal in the mouse intestine. Dev Biol. 1996;180(1): Torihashi S, Ward SM, Sanders KM. Development of c-kit-positive cells and the onset of electrical rhythmicity in murine small intestine. Gastroenterology 1997 Jan;112(1): Klüppel M, Huizinga JD, Malysz J, Bernstein A. Developmental origin and kit-dependent development of the interstitial cells of cajal in the mammalian small intestine. Dev Dyn. 1998;211(1): Sohal GS, Ali MM, Farooqui FA. A second source of precursor cells for the developing enteric nervous system and interstitial cells of Cajal. Int J Dev Neurosci. 2002;20(8): Torihashi S, Horisawa M, Watanabe Y. C-Kit immunoreactive interstitial cells in the human gastrointestinal tract. J Auton Nerv Syst. 1999;75(1): Wang XY, Paterson C, Huizinga JD. Cholinergic and nitrergic innervation of ICC-DMP and ICC-IM in the human small intestine. Neurogastroenterol Motil. 2003;15(5): Zhang SC, Fedoroff S. Cellular localization of stem cell factor and c-kit receptor in the mouse nervous system. J Neurosci Res. 1997;47(1): Faussone-Pellegrini MS, Thuneberg L. Guide to the identification of interstitial cells of Cajal [review]. Microsc Res Tech. 1999;47(4): Komuro T, Seki K, Horiguchi K. Ultrastructural characterization of the interstitial cells of Cajal [review]. Arch Histol Cytol. 1999;62(4): Huizinga JD, Thuneberg L, Vanderwinden JM, Rumessen JJ. Interstitial cells of Cajal as targets for pharmacological intervention in gastrointestinal motor disorders. Trends Pharmacol Sci. 1997;18(10):
91 24. Jain D. Neuromucular Disorders of the GI Tract. In: Odze RD, Goldblum JR (Eds.).Surgical pathology of the GI tract, liver, biliary tract and pancreas, 2nd ed. Philadelphia: Saunders Elsevier; Ch 7, p Badalamenti G, Rodolico V, Fulfaro F, Cascio S, Cipolla C, Cicero G et al. Gastrointestinal stromal tumors (GISTs): focus on histopathological diagnosis and biomolecular features. Ann Oncol. 2007;18(6): Cecilia M. Fenoglio-Preiser C, Noffsinger A, Stemmermann GN, Lantz PE, Isaacson PG. Motility disorders. In: Fenoglio-Preiser C (Ed.). Gastrointestinal pathology: An atlas and text. 3th ed. Virginia: Lippincott Williams&Wilkins; Ch 10, p Lang RJ, Klemm MF. Interstitial cell of Cajal-like cells in the upper urinary tract. J Cell Mol Med. 2005;9(3): Sergeant GP, Thornbury KD, McHale NG, Hollywood MA. Interstitial cells of Cajal in the urethra. J Cell Mol Med. 2006;10(2): Ciontea SM, Radu E, Regalia T, Ceafalan L, Cretoiu D, Gherghiceanu M et al. C-kit immunopositive interstitial cells (Cajal-type) in human myometrium. J Cell Mol Med. 2005;9(2): Popescu LM, Ciontea SM, Cretoiu D. Interstitial Cajal-like cells in human uterus and fallopian tube. Ann N Y Acad Sci. 2007;1101: Suciu L, Popescu LM, Gherghiceanu M. Human placenta: de visu demonstration of interstitial Cajal-like cells. J Cell Mol Med. 2007;11(3): Chakder S, Bandyopadhyay A, Rattan S. Neuronal NOS gene expression in gastrointestinal myenteric neurons and smooth muscle cells. Am J Physiol. 1997;273(6 Pt 1):C Jeng YM, Mao TL, Hsu WM, Huang SF, Hsu HC. Congenital interstitial cell of cajal hyperplasia with neuronal intestinal dysplasia. Am J Surg Pathol. 2000;24(11): Jain D, Moussa K, Tandon M, Culpepper-Morgan J, Proctor DD. Role of interstitial cells of Cajal in motility disorders of the bowel [abstract]. Am J Gastroenterol 2003; 98(3): Isozaki K, Hirota S, Miyagawa J, Taniguchi M, Shinomura Y, Matsuzawa Y. Deficiency of c-kit+ cells in patients with a myopathic form of chronic idiopathic intestinal pseudoobstruction [abstract]. Am J Gastroenterol 1997; 92(2): Yamataka A, Ohshiro K, Kobayashi H, Lane GJ, Yamataka T, Fujiwara T et al. Abnormal distribution of intestinal pacemaker (C-KIT-positive) cells in an infant with chronic idiopathic intestinal pseudoobstruction. J Pediatr Surg 1998; 33(6):
92 37. Kenny SE, Vanderwinden JM, Rintala RJ, Connell MG, Lloyd DA, Vanderhaegen JJ et al. Delayed maturation of the interstitial cells of Cajal: a new diagnosis for transient neonatal pseudoobstruction, report of two cases. J Pediatr Surg 1998; 33(1): Torihashi S, Ward SM, Nishikawa S, Nishi K, Kobayashi S, Sanders KM. C-kitdependent development of interstitial cells and electrical activity in the murine gastrointestinal tract. Cell Tissue Res 1995; 280(1): Giebel LB, Spritz RA. Mutation of the KIT (mast/stem cell growth factor receptor) protooncogene in human piebaldism. Proc Natl Acad Sci U S A 1991; 88(19): Fleischman RA, Saltman DL, Stastny V, Zneimer S. Deletion of the c-kit protooncogene in the human developmental defect piebald trait. Proc Natl Acad Sci USA 1991;88(23): Fletcher CD, Berman JJ, Corless C, Gorstein F, Lasota J, Longley BJ et al. Diagnosis of gastrointestinal stromal tumors: a concensus approach [review]. Hum Pathol. 2002;33(5): Montgomery E, Fisher C. Gastrointestinal mesenchymal tumors. In: Iacobuzio-Donahue AC, Montgomery EA (Eds). Gastrointestinal and liver pathology, Philadelphia: Churchill Livingstone Elsevier; Ch 7, p Tryggvason G, Gíslason HG, Magnússon MK, Jónasson JG. Gastrointestinal stromal tumors in Iceland, : the icelandic GIST study, a population-based incidence and pathologic risk stratification study. Int J Cancer 2005;117(2): Nilsson B, Bümming P, Meis-Kindblom JM, Odén A, Dortok A, Gustavsson B et al. Gastrointestinal stromal tumors: The incidence, prevalence, clinical course, and prognostication in the preimatinib mesylate era, a population-based study in western Sweden. Cancer 2005; 103(4): Miettinen M, Lasota J. Gastrointestinal stromal tumors: review on morphology, molecular pathology, prognosis, and differential diagnosis [review]. Arch Pathol Lab Med. 2006;130(10): Levy AD, Remotti HE, Thompson WM, Sobin LH, Miettinen M. Gastrointestinal stromal tumors: radiologic features with pathologic correlation. Radiographics 2003;23(2): Bates AW, Feakins RM, Scheimberg I. Congenital gastrointestinal stromal tumour is morphologically indistinguishable from the adult form, but does not express CD117 and carries a favourable prognosis. Histopathology 2000;37(4): DeMatteo RP, Lewis JJ, Leung D, Mudan SS, Woodruff JM, Brennan MF. Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival. Ann Surg. 2000;231(1):
93 49. Liegl-Atzwanger B, Fletcher JA, Fletcher CD. Gastrointestinal stromal tumors [review]. Virchows Arch. 2010;456(2): Miettinen M, Sarlomo-Rikala M, Lasota J. Gastrointestinal stromal tumors: recent advances in understanding of their biology. Hum Pathol. 1999;30(10): Biasco G, Velo D, Angriman I, Astorino M, Baldan A, Baseggio M et al. Gastrointestinal stromal tumors: report of an audit and review of the literature. Eur J Cancer Prev. 2009;18(2): Parfitt JR, Streutker CJ, Riddell RH, Driman DK. Gastrointestinal stromal tumors: a contemporary review [review]. Pathology-Research and Practice 2006;202(12): Daum O, Klecka J, Ferda J, Treska V, Vanecek T, Sima R et al. Gastrointestinal stromal tumor of the pancreas: case report with documentation of KIT gene mutation. Virchows Arch. 2005;446(4): Ortiz-Hidalgo C, de Leon Bojorge B, Albores-Saavedra J. Stromal tumor of the gallbladder with phenotype of interstitial cells of Cajal: a previously unrecognized neoplasm. Am J Pathol 2000;24(10): Miettinen M, Sobin LH. Gastrointestinal stromal tumors in the appendix: a clinicopathologic and immunohistochemical study of four cases. Am J Surg Pathol. 2001;25(11): Miettinen M, Monihan JM, Sarlomo-Rikala M, Kovatich AJ, Carr NJ, Emory TS et al. Gastrointestinal stromal tumors/smooth muscle tumors (GISTs) primary in the omentum and mesentery: clinicopathologic and immunohistochemical study of 26 cases. Am J Surg Pathol 1999; 23(9): Reith JD, Goldblum JR, Lyles RH, Weiss SW. Extragastrointestinal (soft tissue) stromal tumors: an analysis of 48 cases with emphasis on histologic predictors of outcome. Mod Pathol 2000;13(5): Wingen CB, Pauwels PA, Debiec-Rychter M, van Gemert WG, Vos MC. Uterine gastrointestinal stromal tumour (GIST). Gynecol Oncol. 2005;97(3): Lam MM, Corless CL, Goldblum JR, Heinrich MC, Downs-Kelly E, Rubin BP. Extragastrointestinal stromal tumors presenting as vulvovaginal/rectovaginal septal masses: a diagnostic pitfall. Int J Gynecol Pathol. 2006;25(3): van der Zwan SM, DeMatteo RP. Gastrointestinal stromal tumor: 5 years later. Cancer 2005;104(9): Kim HC, Lee JM, Choi SH, Kim KW, Kim SH, Lee JY et al. Imaging of gastrointestinal stromal tumors. J Comput Assist Tomogr. 2004;28(5):
94 62. Ji F, Wang ZW, Wang LJ, Ning JW, Xu GQ. Clinicopathological characteristics of gastrointestinal mesenchymal tumors and diagnostic value of endoscopic ultrasonography. J Gastroenterol Hepatol. 2008;23(8 Pt 2): Belloni M, De Fiori E, Mazzarol G, Curti A, Crosta C. Endoscopic ultrasound and Computed Tomography in gastric stromal tumours [abstract]. Radiol Med. 2002; 103(1-2): Jeon SW, Park YD, Chung YJ, Cho CM, Tak WY, Kweon YO et al. Gastrointestinal stromal tumors of the stomach: endosonographic differentiation in relation to histological risk. J Gastroenterol Hepatol. 2007;22(12): Gomes AL, Bardales RH, Milanezi F, Reis RM, Schmitt F. Molecular analysis of c-kit and PDGFRA in GISTs diagnosed by EUS. Am J Clin Pathol 2007;127(1): Stamatakos M, Douzinas E, Stefanaki C, Safioleas P, Polyzou E, Levidou G et al. Gastrointestinal stromal tumor [review]. World J Surg Oncol. 2009;7(61): Miettinen M, Lasota J. Gastrointestinal stromal tumors-definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnosis. Virchows Arch. 2001;438(1): Miettinen M, Sobin LH, Lasota J. Gastrointestinal stromal tumors of the stomach: a clinicopathologic, immunohistochemical, and molecular genetic study of 1765 cases with long-term follow-up. Am J Surg Pathol. 2005;29(1): Miettinen M, Sarlomo-Rikala M, Sobin LH, Lasota J. Esophageal stromal tumors: a clinicopathologic, immunohistochemical, and molecular genetic study of 17 cases and comparison with esophageal leiomyomas and leiomyosarcomas. Am J Surg Pathol. 2000;24(2): Miettinen M, El-Rifai W, H L Sobin L, Lasota J. Evaluation of malignancy and prognosis of gastrointestinal stromal tumors: a review. Hum Pathol. 2002;33(5): Trupiano JK, Stewart RE, Misick C, Appelman HD, Goldblum JR. Gastric stromal tumors: a clinicopathologic study of 77 cases with correlation of features with nonaggressive and aggressive clinical behaviors. Am J Surg Pathol. 2002;26(6): Miettinen M, Kopczynski J, Makhlouf HR, Sarlomo-Rikala M, Gyorffy H, Burke A et al. Gastrointestinal stromal tumors, intramural leiomyomas, and leiomyosarcomas in the duodenum: A clinicopathologic, immunohistochemical, and molecular genetic study of 167 cases. Am J Surg Pathol 2003;27(5): Brainard JA, Goldblum JR. Stromal tumors of the jejunum and ileum: a clinicopathologic study of 39 cases. Am J Surg Pathol 1997; 21(4):
95 74. Tworek JA, Goldblum JR, Weiss SW, Greenson JK, Appelman HD. Stromal tumors of the abdominal colon: a clinicopathologic study of 20 cases. Am J Surg Pathol 1999;23(8): Miettinen M, Sarlomo-Rikala M, Sobin LH. Mesenchymal tumors of muscularis mucosae of colon and rectum are benign leiomyomas that should be separated from gastrointestinal stromal tumors: a clinicopathologic and immunohistochemical study of eighty-eight cases. Mod Pathol 2001;14(10): Miettinen M, Furlong M, Sarlomo-Rikala M, Burke A, Sobin LH, Lasota J. Gastrointestinal stromal tumors, intramural leiomyomas, and leiomyosarcomas in the rectum and anus: a clinicopathologic, immunohistochemical, and molecular genetic study of 144 cases. Am J Surg Pathol 2001;25(9): Walsh NM, Bodurtha A. Auerbach's myenteric plexus: A possible site of origin for gastrointestinal stromal tumors in von Recklinghausen's neurofibromatosis. Arch Pathol Lab Med 1990;114(5): Tworek JA, Goldblum JR, Weiss SW, Greenson JK, Appelman HD. Stromal tumors of the anorectum: a clinicopathologic study of 22 cases. Am J Surg Pathol 1999;23(8): Haque S, Dean PJ. Stromal neoplasms of the rectum and anal canal. Hum Pathol 1992;23(7): van de Rijn M, Hendrickson MR, Rouse RV. CD34 expression by gastrointestinal tract stromal tumors [abstract]. Hum Pathol 1994;25(8): Monihan JM, Carr NJ, Sobin LH. CD34 immunoexpression in stromal tumours of the gastrointestinal tract and in mesenteric fibromatoses [abstract]. Histopathology 1994;25(5): Miettinen M, Virolainen M, Maarit-Sarlomo-Rikala. Gastrointestinal stromal tumors: value of CD34 antigen in their identification and separation from true leiomyomas and schwannomas [abstract]. Am J Surg Pathol 1995;19(2): Miettinen M, Lasota J. Gastrointestinal stromal tumors: pathology and prognosis at different sites. Semin Diagn Pathol 2006;23(2): Kindblom LG, Remotti HE, Aldenborg F, Meis-Kindblom JM. Gastrointestinal pacemaker cell tumor (GIPACT): gastrointestinal stromal tumors show phenotypic characteristics of the interstitial cells of Cajal. Am J Pathol 1998;152(5): Antonescu CR. Targeted therapy of cancer: new roles for pathologists in identifying GISTs and other sarcomas. Mod Pathol. 2008;21(2):
96 86. Pauwels P, Debiec-Rychter M, Stul M, De Wever I, Van Oosterom AT, Sciot R. Changing phenotype of gastrointestinal stromal tumours under imatinib mesylate treatment: a potential diagnostic pitfall. Histopathology 2005;47(1): Wasag B, Debiec-Rychter M, Pauwels P, Stul M, Vranckx H, Oosterom AV et al. Differential expression of KIT/PDGFRA mutant isoforms in epithelioid and mixed variants of gastrointestinal stromal tumors depends predominantly on the tumor site. Mod Pathol. 2004;17(8): Lasota J, Corless CL, Heinrich MC, Debiec-Rychter M, Sciot R, Wardelmann E et al. Clinicopathologic profile of gastrointestinal stromal tumors (GISTs) with primary KIT exon 13 or exon 17 mutations: a multicenter study on 54 cases. Mod Pathol. 2008;21(4): Doğanavşargil B, Akalın T, Sezak M, Alkanat BM, Kandiloğlu G, Tunçyürek M. Gastrointestinal stromal tümörlerde histopatolojik değerlendirme Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı nın yılları arasındaki deneyimi. Ege Journal of Medicine 2008;47(3): Miettinen M, Makhlouf H, Sobin LH, Lasota J. Gastrointestinal stromal tumors of the jejunum and ileum: a clinicopathologic, immunohistochemical, and molecular genetic study of 906 cases before imatinib with long-term follow-up. Am J Surg Pathol. 2006;30(4): Wang L, Vargas H, French SW. Cellular origin of gastrointestinal stromal tumors: a study of 27 cases. Arch Pathol Lab Med. 2000;124(10): Sarlomo-Rikala M, Tsujimura T, Lendahl U, Miettinen M. Patterns of nestin and other intermediate filament expression distinguish between gastrointestinal stromal tumors, leiomyomas and schwannomas. APMIS 2002;110(6): Yantiss RK, Spiro IJ, Compton CC, Rosenberg AE. Gastrointestinal stromal tumor versus intra-abdominal fibromatosis of the bowel wall: a clinically important differential diagnosis. Am J Surg Pathol 2000;24(7): Hirota S, Isozaki K, Moriyama Y, Hashimoto K, Nishida T, Ishiguro S et al. Gain-offunction mutations of c-kit in human gastrointestinal stromal tumors. Science 1998;279(5350): Lasota J, Miettinen M. Clinical significance of oncogenic KIT and PDGFRA mutations in gastrointestinal stromal tumours [review]. Histopathology 2008;53(3): Pawson T. Regulation and targets of receptor tyrosine kinases. Eur J Cancer 2002;38(5):
97 97. Mol CD, Dougan DR, Schneider TR, Skene RJ, Kraus ML, Scheibe DN et al. Structural basis for the autoinhibition and STI-571 inhibition of c-kit tyrosine kinase. J Biol Chem. 2004;279(30): Chen H, Hirota S, Isozaki K, Sun H, Ohashi A, Kinoshita K et al. Polyclonal nature of diffuse proliferation of interstitial cells of Cajal in patients with familial and multiple gastrointestinal stromal tumours. Gut 2002;51(6): Steigen SE, Eide TJ. Gastrointestinal stromal tumors (GISTs): a review. Apmis 2009;117(2): Rubin BP, Singer S, Tsao C, Duensing A, Lux ML, Ruiz R et al. KIT activation is a ubiquitous feature of gastrointestinal stromal tumors. Cancer Res. 2001;61(22): Heinrich MC, Corless CL, Demetri GD, Blanke CD, von Mehren M, Joensuu H et al. Kinase mutations and imatinib response in patients with metastatic gastrointestinal stromal tumor. J Clin Oncol. 2003;21(23): Lasota J, Wozniak A, Sarlomo-Rikala M, Rys J, Kordek R, Nassar A et al. Mutations in exons 9 and 13 of KIT gene are rare events in gastrointestinal stromal tumors. A study of 200 cases. Am J Pathol 2000;157(4): Perrone F, Tamborini E, Dagrada GP, Colombo F, Bonadiman L, Albertini V et al. 9p21 locus analysis in high-risk gastrointestinal stromal tumors characterized for c-kit and platelet-derived growth factor receptor alpha gene alterations. Cancer 2005;104(1): Lasota J, Corless CL, Heinrich MC, Debiec-Rychter M, Sciot R, Wardelmann E et al. Clinicopathologic profile of gastrointestinal stromal tumors (GISTs) with primary KIT exon 13 or exon 17 mutations: a multicenter study on 54 cases. Mod Pathol. 2008;21(4): Corless CL, Schroeder A, Griffith D, Town A, McGreevey L, Harrell P et al. PDGFRA mutations in gastrointestinal stromal tumors: frequency, spectrum and in vitro sensitivity to imatinib. J Clin Oncol. 2005;23(23): Penzel R, Aulmann S, Moock M, Schwarzbach M, Rieker RJ, Mechtersheimer G. The location of KIT and PDGFRA gene mutations in gastrointestinal stromal tumours is site and phenotype associated. J Clin Pathol. 2005;58(6): Steigen SE, Eide TJ, Wasag B, Lasota J, Miettinen M. Mutations in gastrointestinal stromal tumors-a population-based study from Northern Norway. APMIS 2007;115(4): Maertens O, Prenen H, Debiec-Rychter M, Wozniak A, Sciot R, Pauwels P et al. Molecular pathogenesis of multiple gastrointestinal stromal tumors in NF1 patients. Hum Mol Genet. 2006;15(6):
98 109. Sarlomo-Rikala M, Kovatich AJ, Barusevicius A, Miettinen M. CD117: a sensitive marker for gastrointestinal stromal tumors that is more specific than CD34. Mod Pathol. 1998;11(8): West RB, Corless CL, Chen X, Rubin BP, Subramanian S, Montgomery K et al. The novel marker, DOG1, is expressed ubiquitously in gastrointestinal stromal tumors ırrespective of KIT or PDGFRA mutation status. American Journal of Pathology 2004;165(1): Miwa S, Nakajima T, Murai Y, Takano Y, Sugiyama T. Mutation assay of the novel gene DOG1 in gastrointestinal stromal tumors (GISTs). J Gastroenterol 2008;43(7): Espinosa I, Lee CH, Kim MK, Rouse BT, Subramanian S, Montgomery K et al. A novel monoclonal antibody against DOG1 is a sensitive and specific marker for gastrointestinal stromal tumors. Am J Surg Pathol 2008;32(2): Katoh M, Katoh M. FLJ10261 gene, located within the CCND1-EMS1 locus on human chromosome 11q13, encodes the eight-transmembrane protein homologous to C12orf3, C11orf25 and FLJ34272 gene products. Int J Oncol. 2003;22(6): Galindo BE, Vacquier VD. Phylogeny of the TMEM16 protein family: some members are overexpressed in cancer. Int J Mol Med. 2005;16(5): Carles A, Millon R, Cromer A, Ganguli G, Lemaire F, Young J et al. Head and neck squamous cell carcinoma transcriptome analysis by comprehensive validated differential display. Oncogene 2006;25(12): Caputo A, Caci E, Ferrera L, Pedemonte N, Barsanti C, Sondo E et al. TMEM16A, a membrane protein associated with calcium-dependent chloride channel activity. Science 2008;322(5901): Yang YD, Cho H, Koo JY, Tak MH, Cho Y, Shim WS et al. TMEM16A confers receptor-activated calcium-dependent chloride conductance. Nature 2008;455(7217): Wreesmann VB, Shi W, Thaler HT, Poluri A, Kraus DH, Pfister D et al. Identification of novel prognosticators of outcome in squamous cell carcinoma of the head and neck. J Clin Oncol. 2004;22(19): Rodrigo JP, García-Carracedo D, García LA, Menéndez S, Allonca E, González MV et al. Distinctive clinicopathological associations of amplification of the cortactin gene at 11q13 in head and neck squamous cell carcinomas. J Pathol. 2009;217(4): Clark ES, Brown B, Whigham AS, Kochaishvili A, Yarbrough WG, Weaver AM. Aggressiveness of HNSCC tumors depends on expression levels of cortactin, a gene in the 11q13 amplicon. Oncogene 2009;28(3):
99 121. Liegl B, Hornick JL, Corless CL, Fletcher CD. Monoclonal antibody DOG1.1 shows higher sensitivity than KIT in the diagnosis of gastrointestinal stromal tumors, including unusual subtypes. Am J Surg Pathol. 2009;33(3): Lee CH, Liang CW, Espinosa I. The utility of discovered on gastrointestinal stromal tumor 1 (DOG1) antibody in surgical pathology-the GIST of it [review]. Adv Anat Pathol. 2010;17(3): Lopes LF, West RB, Bacchi LM, van de Rijn M, Bacchi CE. DOG1 for the diagnosis of gastrointestinal stromal tumor (GIST): Comparison between 2 different antibodies. Appl Immunohistochem Mol Morphol 2010;18(4): Ardeleanu C, Arsene D, Hinescu M, Andrei F, Gutu D, Luca L et al. Pancreatic expression of DOG1 A novel gastrointestinal stromal tumor (GIST) biomaker. Appl Immunohistochem Mol Morphol 2009;17(5): Kang HJ, Nam SW, Kim H, Rhee H, Kim NG, Kim H et al. Correlation of KIT and platelet-derived growth factor receptor alpha mutations with gene activation and expression profiles in gastrointestinal stromal tumors. Oncogene 2005;24(6): Heinrich MC, Corless CL, Duensing A, McGreevey L, Chen CJ, Joseph N et al. PDGFRA activating mutations in gastrointestinal stromal tumors. Science 2003;299(5607): Hirota S, Ohashi A, Nishida T, Isozaki K, Kinoshita K, Shinomura Y et al. Gain-offunction mutations of platelet-derived growth factor receptor alpha gene in gastrointestinal stromal tumors. Gastroenterology 2003;125(3): Peterson MR, Piao Z, Weidner N, Yi ES. Strong PDGFRA positivity is seen in GISTs but not in other intra-abdominal mesenchymal tumors: Immunohistochemical and mutational analyses. Appl Immunohistochem Mol Morphol. 2006;14(4): Rossi G, Valli R, Bertolini F, Marchioni A, Cavazza A, Mucciarini C. PDGFR expression in differential diagnosis between KIT-negative gastrointestinal stromal tumours and other primary soft-tissue tumours of the gastrointestinal tract. Histopathology 2005;46(5): Blay JY, von Mehren M, Blackstein ME. Perspective on updated treatment guidelines for patients with gastrointestinal stromal tumors [review]. Cancer 2010 Jul 26: Duensing A, Joseph NE, Medeiros F, Smith F, Hornick JL, Heinrich MC et al. Protein Kinase C theta (PKCtheta) expression and constitutive activation in gastrointestinal stromal tumors (GISTs). Cancer Res. 2004;64(15): Kim KM, Kang DW, Moon WS, Park JB, Park CK, Sohn JH et al. PKCtheta expression in gastrointestinal stromal tumor. Mod Pathol. 2006;19(11):
100 133. Lee HE, Kim MA, Lee HS, Lee BL, Kim WH. Characteristics of KIT-negative gastrointestinal stromal tumours and diagnostic utility of protein kinase C theta immunostaining. J Clin Pathol. 2008;61(6): Miettinen M, Wang ZF, Lasota J. DOG1 antibody in the differential diagnosis of gastrointestinal stromal tumors: a study of 1840 cases. Am J Surg Pathol. 2009;33(9): Blay P, Astudillo A, Buesa JM, Campo E, Abad M, García-García J et al. Protein kinase C theta is highly expressed in gastrointestinal stromal tumors but not in other mesenchymal neoplasias. Clin Cancer Res. 2004;10(12 Pt 1): Emory TS, Sobin LH, Lukes L, Lee DH, O'Leary TJ. Prognosis of gastrointestinal smooth-muscle (stromal) tumors: dependence on anatomic site. Am J Surg Pathol. 1999;23(1): DeMatteo RP, Lewis JJ, Leung D, Mudan SS, Woodruff JM, Brennan MF. Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival. Ann Surg 2000;231(1): Irving JA, Lerwill MF, Young RH. Gastrointestinal stromal tumors metastatic to the ovary: a report of five cases. Am J Surg Pathol. 2005;29(7): Tuveson DA, Willis NA, Jacks T, Griffin JD, Singer S, Fletcher CD et al. STI571 inactivation of the gastrointestinal stromal tumor c-kit oncoprotein: biological and clinical implications. Oncogene 2001;20(36): Joensuu H, Fletcher C, Dimitrijevic S, Silberman S, Roberts P, Demetri G. Management of malignant gastrointestinal stromal tumours [review]. Lancet Oncol. 2002;3(11): Demetri GD, von Mehren M, Blanke CD, Van den Abbeele AD, Eisenberg B, Roberts PJ et al. Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med 2002; 347(7): Debiec-Rychter M, Cools J, Dumez H, Sciot R, Stul M, Mentens N et al. Mechanisms of resistance to imatinib mesylate in gastrointestinal stromal tumors and activity of the PKC412 inhibitor against imatinib-resistant mutants. Gastroenterology 2005;128(2): Tamborini E, Bonadiman L, Greco A, Albertini V, Negri T, Gronchi A et al. A new mutation in the KIT ATP pocket causes acquired resistance to imatinib in a gastrointestinal stromal tumor patient. Gastroenterology 2004;127(1): Frost MJ, Ferrao PT, Hughes TP, Ashman LK. Juxtamembrane mutant V560GKit is more sensitive to Imatinib (STI571) compared with wild-type c-kit whereas the kinase domain mutant D816VKit is resistant. Mol Cancer Ther. 2002;1(12):
101 145. Chen LL, Trent JC, Wu EF, Fuller GN, Ramdas L, Zhang W et al. A missense mutation in KIT kinase domain 1 correlates with imatinib resistance in gastrointestinal stromal tumors. Cancer Res. 2004;64(17): Corless CL, Fletcher JA, Heinrich MC. Biology of gastrointestinal stromal tumors. J Clin Oncol. 2004;22(18): Antonescu CR, Sommer G, Sarran L, Tschernyavsky SJ, Riedel E, Woodruff JM et al. Association of KIT exon 9 mutations with nongastric primary site and aggressive behavior: KIT mutation analysis and clinical correlates of 120 gastrointestinal stromal tumors. Clin Cancer Res. 2003;9(9): Andrejauskas-Buchdunger E, Regenass U. Differential inhibition of the epidermal growth factor-, platelet-derived growth factor-, and protein kinase C-mediated signal transduction pathways by the staurosporine derivative CGP Cancer Res. 1992;52(19): Nishida T, Hirota S. Biological and clinical review of stromal tumors in the gastrointestinal tract [review]. Histol Histopathol. 2000;15(4): Joensuu H. Gastrointestinal stromal tumor (GIST) [review]. Ann Oncol. 2006;17(10): Tran T, Davila JA, El-Serag HB. The epidemiology of malignant gastrointestinal stromal tumors: an analysis of 1,458 cases from 1992 to Am J Gastroenterol. 2005;100(1): Stamatakos M, Douzinas E, Stefanaki C, Safioleas P, Polyzou E, Levidou G et al. Gastrointestinal stromal tumor [review]. World J Surg Oncol. 2009;7(61): Dorn J, Spatz H, Schmieder M, Barth TF, Blatz A, Henne-Bruns D et al. Cyclin H expression is increased in GIST with very-high risk of malignancy. BMC Cancer 2010; 350(10): Kaygusuz G, Cekin N, Sahin F, Bozdayi M, Erhan A, Kapran Y et al. Clinicopathologic and molecular characteristics of 523 Turkish gastrointestinal stromal tumor cases: a multicenter study; 21 st European Congress of Pathology. Final Program Book, p.76 (Oral Presentation 25-10), İstanbul, Rubin BP, Heinrich MC, Corless CL. Gastrointestinal stromal tumor. The Lancet 2007;vol.369: Rosai J. Gastrointestinal tract.in: Houstom M (Ed.), Rosai and Ackerman s surgical pathology. Ninth edition. New york: Mosby; Fujimoto Y, Nakanishi Y, Yoshimura K, Shimoda T. Clinicopathologic study of primary malignant gastrointestinal stromal tumor of the stomach, with special reference to prognostic factors: analysis of results in 140 surgically resected patients. Gastric Cancer 2003;6(1):
102 158. Kitamura Y. Gastrointestinal stromal tumors: past, present, and future. J Gastroenterol. 2008;43(7): Miettinen M, Lasota J. Gastrointestinal stromal tumors (GISTs): definition, occurrence, pathology, differential diagnosis and [review]. Pol J Pathol. 2003;54(1): Tetikkurt US, Ozaydin IY, Ceylan S, Gurbuz Y, Erdogan N, Oz F. Predicting malignant potential of gastrointestinal stromal tumors: Role of p16 and E2F1 expression. Appl Immunohistochem Mol Morphol. 2010;18(4): Huang H, Liu YX, Zhan ZL, Liang H, Wang P, Ren XB. Different sites and prognoses of gastrointestinal stromal tumors of the stomach: report of 187 cases. World J Surg. 2010;34(7): Ueyama T, Guo KJ, Hashimoto H, Daimaru Y, Enjoji M. A clinicopathologic and immunohistochemical study of gastrointestinal stromal tumors. Cancer. 1992;69(4): Hou YY, Lu SH, Zhou Y, Xu JF, Ji Y, Hou J et al. Predictive values of clinical and pathological parameters for malignancy of gastrointestinal stromal tumors. Histol Histopathol. 2009;24(6): Wong NA, Young R, Malcomson RD, Nayar AG, Jamieson LA, Save VE et al. Prognostic indicators for gastrointestinal stromal tumours: a clinicopathological and immunohistochemical study of 108 resected cases of the stomach. Histopathology. 2003;43(2): Goldblum JR, Appelman HD. Stromal tumors of the duodenum. A histologic and immunohistochemical study of 20 cases. Am J Surg Pathol. 1995;19(1): Suster S. Gastrointestinal stromal tumors [review]. Semin Diagn Pathol. 1996;13(4): Muro-Cacho CA, Cantor AB, Morgan M. Prognostic factors in malignant gastrointestinal stromal tumors [abstrct]. Ann Clin Lab Sci. 2000;30(3): Agaimy A. Gastrointestinal stromal tumors (GIST) from risk stratification systems to the new TNM proposal: more questions than answers? A review emphasizing the need for a standardized GIST reporting [review]. Int J Clin Exp Pathol. 2010;3(5): Kang DY, Park CK, Choi JS, Jin SY, Kim HJ, Joo M et al. Multiple gastrointestinal stromal tumors: Clinicopathologic and genetic analysis of 12 patients. Am J Surg Pathol 2007;31(2): Kleist B, Lasota J, Miettinen M. Gastrointestinal stromal tumor and gastric adenocarcinoma collision tumors. Human pathology 2010;41(7):
103 171. Agaimy A, Märkl B, Arnholdt H, Wünsch PH, Terracciano LM, Dirnhofer S et al. Multiple sporadic gastrointestinal stromal tumours arising at different gastrointestinal sites: pattern of involvement of the muscularis propria as a clue to independent primary GISTs. Virchows Arch 2009;455(2): Díaz-Delgado M, Hernández-Amate A, Sánchez-León M, Pereira-Gallardo S, Prieto- Sánchez E, Jiménez-Sáenz M et al. Multiple non-metastatic gastrointestinal stromal tumors. Differential features. Rev Esp Enferm Dig 2010;102(8): Price ND, Trent J, El-Naggar AK, Cogdell D, Taylor E, Hunt KK et al. Highly accurate two-gene classifier for differentiating gastrointestinal stromal tumors and leiomyosarcomas. Proc Natl Acad Sci USA 2007;104(9): Miettinen M, Lasota J. KIT (CD117): a review on expression in normal and neoplastic tissues, and mutations and their clinicopathologic correlation. Appl Immunohistochem Mol Morphol. 2005;13(3): Narasimhamurthy MS, Vallachira GP, Mahadev PS. Synchronous adenocarcinoma and gastrointestinal stromal tumor in the stomach. Saudi J Gastroenterology 2010;16(3): Wang L, Vargas H, French SW. Cellular origin of gastrointestinal stromal tumors: a study of 27 cases. Arch Pathol Lab Med. 2000;124(10): van Oosterom AT, Judson I, Verweij J, Stroobants S, Donato di Paola E, Dimitrijevic S et al. Safety and efficacy of imatinib (STI571) in metastatic gastrointestinal stromal tumours: a phase I study. Lancet. 2001;358(9291): Novelli R, Rossi S, Rodriguez-Justo M, Taniere P, Seddon B, Toffolatti L. et al. DOG1 and CD117 are the antibodies of choice in the diagnosis of gastrointestinal stromal tumours. Histopathol 2010; 57: Pauls K, Merkelbach-Bruse S, Thal D, Büttner R, Wardelmann E. PDGFRalpha- and c- kit-mutated gastrointestinal stromal tumours (GISTs) are characterized by distinctive histological and immunohistochemical features. Histopathology. 2005;46(2): Terada T. Gastrointestinal stromal tumor of the digestive organs: a histopathologic study of 31 cases in a single Japanese institute. Int J Clin Exp Pathol. 2010;3(2): Meara RS, Cangiarella J, Simsir A, Horton D, Eltoum I, Chhieng DC. Prediction of aggressiveness of gastrointestinal stromal tumours based on immunostaining with bcl-2, Ki-67 and p53. Cytopathology. 2007;18(5): Romeo S, Debiec-Rychter M, Van Glabbeke M, Van Paassen H, Comite P, Van Eijk R et al. Cell cycle/apoptosis molecule expression correlates with imatinib response in patients with advanced gastrointestinal stromal tumors. Clin Cancer Res. 2009;15(12):
104 EKLER 100
105 Ek 1 101
106 Ek 2 Tablo Ek. Gastrointestinal stromal tümör dışı mezenkimal tümör olgu listesi Olgu No Biyopsi No Protokol No Tanı Malign Periferik Sinir Kılıfı Tümörü Malign Periferik Sinir Kılıfı Tümörü Malign Periferik Sinir Kılıfı Tümörü Malign Periferik Sinir Kılıfı Tümörü Malign Periferik Sinir Kılıfı Tümörü Schwannom Schwannom Nörofibrom Nörofibrom Schwannom Leiomyosarkom Malignite Potansiyeli Belirsiz Düz Kas Tümörü Malignite Potansiyeli Belirsiz Düz Kas Tümörü Leiomyosarkom Leiomyosarkom Rabdomyosarkom, Embriyonal Tip Rabdomyosarkom, Botyroid Tip Rabdomyosarkom Rabdomyosarkom Rabdomyosarkom, Embriyonal Tip Miksoid Liposarkom İyi Diferansiye Liposarkom Atipik Lipomatöz Tümör Dediferansiye Liposarkom Pleomorfik Liposarkom Anjiosarkom Anjiosarkom Anjiosarkom Anjiosarkom Anjiosarkom Nöroblastom Ganglionörom Ganglionörom Nöroblastom Ganglionörom Agresif Fibromatozis İnflamatuar Myofibroblastik Tümör Desmoid Tip Fibromatozis Malign Fibröz Histiositom Dermatofibrosarkoma Protuberans Sinovyal sarkom, monofazik Sinovyal sarkom, bifazik Sinovyal sarkom, bifazik Sinovyal sarkom, monofazik Sinovyal sarkom, monofazik 102
107 EK 3 GASTROİNTESTİNAL STROMAL TÜMÖR RAPOR ÖRNEĞİ * : Biyopsi No: Tarih: Hasta Adı / Soyadı : Yaş / Cins :... Biyopsi Yeri:.. Biyopsi şekli:.. Klinik Bulgular:. Ön Tanı:. Makroskopik Tarif:... Makroskopik Bulgular: Yer:. (mide, ince barsak, kalın barsak, özefagus, omentum-periton) Çap:... x.x.cm..(mümkünse 3 boyut verilmeli) Tümör Sınırları:.. (ekspansif, infiltratif) Ülser:... (yok, var) Nekroz:... (yok, var) Kanama:... (yok, var) İnvazyon: (mukoza, submukoza, muskuler tabaka, seroza, çevre organ) Mikroskopik Bulgular: Mitoz: /50 BBA.. Hücre Tipi: (iğsi, epiteloid, mikst) Hücresellik:...(az, belirgin) Sitolojik Atipi:..(hafif, belirgin) Büyüme Paterni: (ekspansif, infiltratif) Ülserasyon: (yok, var) Nekroz:..(yok, var) Kanama: (yok, var) İnvazyon Derinliği: (mukoza, submukoza, muskuler tabaka, seroza, çevre organ) Lenf Düğümü Tutulumu : (yok, var), (Sayısı: ) Uzak Metastaz : (yok, var), (Yeri:.) İmmünohistokimya Sonuçları: CD117: Negatif, Pozitif Yaygınlık:.. ( <%10 %10-50 >%50 ) Yoğunluk: ( + / ++ / +++ ) CD34: Negatif / Pozitif Yaygınlık:.. ( <%10 %10-50 >%50 ) 103
108 SMA: Negatif / Pozitif Yaygınlık:. ( <%10 %10-50 >%50 ) Desmin: Negatif / Pozitif Yaygınlık:. ( <%10 %10-50 >%50 ) S100: Negatif / Pozitif Yaygınlık:...( <%10 %10-50 >%50 ) Ki67: ( <%10 >%10 ) Diğer :.. ( DOG1, PDGFRα vb ) TANI : Risk Grubu:... (Risk Yok, Çok Düşük Risk, Düşük Risk, Orta Risk, Yüksek Risk ) * : Türk Patoloji Derneği - GİST Çalışma Grubu tarafından 2004 yılında hazırlanmış örnek kitapçıktan uyarlanmıştır. 104
Tiroid bezinde ender bir mezenkimal tümör. Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı
 Tiroid bezinde ender bir mezenkimal tümör Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 10-10 - 2015 ANKARA Ülkemizin başı sağ olsun Değerli Hocamızı saygıyla anıyoruz Prof.
Tiroid bezinde ender bir mezenkimal tümör Dr. Ersin TUNCER Cumhuriyet Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 10-10 - 2015 ANKARA Ülkemizin başı sağ olsun Değerli Hocamızı saygıyla anıyoruz Prof.
Endometrial stromal tümörler
 Endometrial stromal tümörler WHO-2014 sınıflamasında neler değişti? Dr. Şennur İlvan İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji AD Endometrial stromal tümör (1966) Endometrial stromal nodül Low grade endometrial
Endometrial stromal tümörler WHO-2014 sınıflamasında neler değişti? Dr. Şennur İlvan İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji AD Endometrial stromal tümör (1966) Endometrial stromal nodül Low grade endometrial
Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D
 Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D 03.11.2016 Olgu 22 yaşında, kadın hasta Bacakta nodüler lezyon Son 1 yıl içinde farkediyor. Özgeçmiş: Özellik yok. Klinik ön tanı: Yumuşak doku sarkomu?
Dr. Merih Tepeoğlu Başkent Üniversitesi Patoloji A.B.D 03.11.2016 Olgu 22 yaşında, kadın hasta Bacakta nodüler lezyon Son 1 yıl içinde farkediyor. Özgeçmiş: Özellik yok. Klinik ön tanı: Yumuşak doku sarkomu?
Pleomorfik mezankimal tümörler ve taklitçileri. Dr. Bahar Müezzinoğlu
 Pleomorfik mezankimal tümörler ve taklitçileri Dr. Bahar Müezzinoğlu Pleomorfik lezyon yaş yerleşim hikaye Pleomorfik lezyon neoplastik Neoplastik değil benign malign sarkom Karsinom Lenfoma melanom Pleomorfizm
Pleomorfik mezankimal tümörler ve taklitçileri Dr. Bahar Müezzinoğlu Pleomorfik lezyon yaş yerleşim hikaye Pleomorfik lezyon neoplastik Neoplastik değil benign malign sarkom Karsinom Lenfoma melanom Pleomorfizm
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER
 MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 25. Ulusal Patoloji Kongresi 14-17
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Osman ZEKİOĞLU - Dr. Gülnur GÜLER OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 25. Ulusal Patoloji Kongresi 14-17
Dev Karaciğer Metastazlı Gastrointestinal Stromal Tümör Olgusu ve Cerrahi Tedavi Serüveni
 Dev Karaciğer Metastazlı Gastrointestinal Stromal Tümör Olgusu ve Cerrahi Tedavi Serüveni Dr. Koray TOPGÜL Medical Park Samsun Hastanesi Genel Cerrahi Bölümü/ SAMSUN 35 yaşında erkek hasta, İlk kez 2007
Dev Karaciğer Metastazlı Gastrointestinal Stromal Tümör Olgusu ve Cerrahi Tedavi Serüveni Dr. Koray TOPGÜL Medical Park Samsun Hastanesi Genel Cerrahi Bölümü/ SAMSUN 35 yaşında erkek hasta, İlk kez 2007
Akciğer Karsinomlarının Histopatolojisi
 Akciğer Karsinomlarının Histopatolojisi Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Akciğer karsinomlarının gelişiminde preinvaziv epitelyal lezyonlar; Akciğer karsinomlarının gelişiminde
Akciğer Karsinomlarının Histopatolojisi Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Akciğer karsinomlarının gelişiminde preinvaziv epitelyal lezyonlar; Akciğer karsinomlarının gelişiminde
Çocukluk çağı yuvarlak hücreli tümörleri 21.Ulusal Patoloji Kongresi İzmir. Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji AD
 Çocukluk çağı yuvarlak hücreli tümörleri 21.Ulusal Patoloji Kongresi İzmir Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji AD 15 yaşında kız 1 yıldır farkettiği giderek büyüyen karın şişliği
Çocukluk çağı yuvarlak hücreli tümörleri 21.Ulusal Patoloji Kongresi İzmir Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Tıbbi Patoloji AD 15 yaşında kız 1 yıldır farkettiği giderek büyüyen karın şişliği
Böbrek kistleri olan hastaya yaklaşım
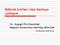 Böbrek kistleri olan hastaya yaklaşım Dr. Ayşegül Örs Zümrütdal Başkent Üniversitesi-Nefroloji Bilim Dalı 20/05/2011-ANTALYA Böbrek kistleri Genetik ya da genetik olmayan nedenlere bağlı olarak, Değişik
Böbrek kistleri olan hastaya yaklaşım Dr. Ayşegül Örs Zümrütdal Başkent Üniversitesi-Nefroloji Bilim Dalı 20/05/2011-ANTALYA Böbrek kistleri Genetik ya da genetik olmayan nedenlere bağlı olarak, Değişik
BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ. Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi
 BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi 61 y/ K Sol parotiste kitle Makroskopi: 2.3x2.2x0.7 cm ölçülerinde kirli beyaz-kahverengi, kesitinde
BAŞ BOYUN PATOLOJİSİ SLAYT SEMİNERİ Dr. Sezer Kulaçoğlu Ankara Numune Eğitim ve Araştırma Hastanesi 61 y/ K Sol parotiste kitle Makroskopi: 2.3x2.2x0.7 cm ölçülerinde kirli beyaz-kahverengi, kesitinde
MEME PATOLOJİSİ SLAYT SEMİNERİ
 MEME PATOLOJİSİ SLAYT SEMİNERİ Prof. Dr. Şahsine Tolunay Uludağ Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 17.10.2015 OLGU 43 yaşında kadın 2 çocuğu var Sol memede ağrı ve kitle yakınması mevcut
MEME PATOLOJİSİ SLAYT SEMİNERİ Prof. Dr. Şahsine Tolunay Uludağ Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 17.10.2015 OLGU 43 yaşında kadın 2 çocuğu var Sol memede ağrı ve kitle yakınması mevcut
Adrenalde sık ve nadir görülen lezyonlar. Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD
 Adrenalde sık ve nadir görülen lezyonlar Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD Feokromositoma Kromafin hücrelerden köken alır 2 tip hücre içerir:kromafin hücreler ve sustentaküler
Adrenalde sık ve nadir görülen lezyonlar Dr.Aylar Poyraz Gazi Üniversitesi Tıp Fakültesi Patoloji AD Feokromositoma Kromafin hücrelerden köken alır 2 tip hücre içerir:kromafin hücreler ve sustentaküler
Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm
 BAZAL HÜCRELİ KARSİNOM Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm Nadiren met. yapar fakat tedavisiz bırakıldığında invazif davranış göstermesi,lokal invazyon,
BAZAL HÜCRELİ KARSİNOM Epidermal bazal hücrelerden veya kıl folikülünün dış kök kılıfından köken alan malin deri tm Nadiren met. yapar fakat tedavisiz bırakıldığında invazif davranış göstermesi,lokal invazyon,
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ
 MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
MİDE KANSERİNDE APOPİTOZİSİN BİYOLOJİK BELİRTEÇLERİNİN PROGNOSTİK ÖNEMİ Cem Sezer 1, Mustafa Yıldırım 2, Mustafa Yıldız 2, Arsenal Sezgin Alikanoğlu 1,Utku Dönem Dilli 1, Sevil Göktaş 1, Nurullah Bülbüller
ADENOKARSİNOMLARDA HİSTOLOJİK ALT TİPLER. Prof. Dr. Ali VERAL Ege ÜTF Patoloji A.D. 21. Ulusal Patoloji Kongresi İzmir
 ADENOKARSİNOMLARDA HİSTOLOJİK ALT TİPLER Prof. Dr. Ali VERAL Ege ÜTF Patoloji A.D. 21. Ulusal Patoloji Kongresi 17.11.2011 İzmir Adenokarsinom WHO 1967 1981 Bronkojenik o Asiner o Papiller Bronkiolo-alveoler
ADENOKARSİNOMLARDA HİSTOLOJİK ALT TİPLER Prof. Dr. Ali VERAL Ege ÜTF Patoloji A.D. 21. Ulusal Patoloji Kongresi 17.11.2011 İzmir Adenokarsinom WHO 1967 1981 Bronkojenik o Asiner o Papiller Bronkiolo-alveoler
Göğüs Cerrahisi Alkın Yazıcıoğlu. Journal of Clinical and Analytical Medicine Göğüs Cerrahisi
 Mediastenin Nadir Görülen Tümörleri Tüm mediastinal kitlelerin %10 dan azını meydana getiren bu lezyonlar mezenkimal veya epitelyal kökenli tümörlerden oluşmaktadır. Journal of linical and nalytical Medicine
Mediastenin Nadir Görülen Tümörleri Tüm mediastinal kitlelerin %10 dan azını meydana getiren bu lezyonlar mezenkimal veya epitelyal kökenli tümörlerden oluşmaktadır. Journal of linical and nalytical Medicine
Tanı: Metastatik hastalık için patognomonik bir radyolojik. Tek veya muitipl nodüller iyi sınırlı veya difüz. Göğüs Cerrahisi Hasan Çaylak
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Hasan Çaylak Göğüs Cerrahisi Metastatik Akciğer Tümörleri Giriş İzole akciğer metastazlarına tedavi edilemez gözüyle bakılmamalıdır Tümör tipine
Deri Tümörleri Pratik Ders İçeriği
 Deri Tümörleri Pratik Ders İçeriği Deri Tümörleri DSÖ(2006) sınıflaması Yassı Hücreli Karsinom Bazal Hücreli Karsinom Bazoskuamoz Karsinom Melanositik Dermal Nevus Melanom DSÖ DERİ TÜMÖRLERİ SINIFLAMASI
Deri Tümörleri Pratik Ders İçeriği Deri Tümörleri DSÖ(2006) sınıflaması Yassı Hücreli Karsinom Bazal Hücreli Karsinom Bazoskuamoz Karsinom Melanositik Dermal Nevus Melanom DSÖ DERİ TÜMÖRLERİ SINIFLAMASI
DİFÜZ GLİAL TÜMÖRLER
 DİFÜZ GLİAL TÜMÖRLER DSÖ 2016 da erişkin glial tümörler açısından sizce en önemli değişiklik ne olmuştur? Curr Opin Oncol 2016 Nov;28(6):494-501. Diffuz astrositik ve oligodentroglial tümörler aynı grup
DİFÜZ GLİAL TÜMÖRLER DSÖ 2016 da erişkin glial tümörler açısından sizce en önemli değişiklik ne olmuştur? Curr Opin Oncol 2016 Nov;28(6):494-501. Diffuz astrositik ve oligodentroglial tümörler aynı grup
MEME KARSİNOMLARINDA GATA 3 EKSPRESYONU VE KLİNİKOPATOLOJİK PARAMETRELER İLE İLİŞKİSİ
 MEME KARSİNOMLARINDA GATA 3 EKSPRESYONU VE KLİNİKOPATOLOJİK PARAMETRELER İLE İLİŞKİSİ Aslı ÇAKIR 1, Özgür EKİNCİ 2, İpek IŞIK GÖNÜL 2, Bülent ÇETİN 3, Mustafa BENEKLİ 3, Ömer ULUOĞLU 2 1 Çorlu Devlet Hastanesi
MEME KARSİNOMLARINDA GATA 3 EKSPRESYONU VE KLİNİKOPATOLOJİK PARAMETRELER İLE İLİŞKİSİ Aslı ÇAKIR 1, Özgür EKİNCİ 2, İpek IŞIK GÖNÜL 2, Bülent ÇETİN 3, Mustafa BENEKLİ 3, Ömer ULUOĞLU 2 1 Çorlu Devlet Hastanesi
Polipte Kanser. Dr.Cem Terzi. Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi
 Polipte Kanser Dr.Cem Terzi Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi Polip ve polipoid karsinoma POLİP Epitelyal yüzeyden kaynaklanan çıkıntı HİSTOLOJİK POLİP TİPLERİ
Polipte Kanser Dr.Cem Terzi Dokuz Eylül Üniversitesi Genel Cerrahi Anabilim Dalı Kolorektal Cerrahi Birimi Polip ve polipoid karsinoma POLİP Epitelyal yüzeyden kaynaklanan çıkıntı HİSTOLOJİK POLİP TİPLERİ
DFSP, Klinik 14.10.2015. DERMATOFİBROSARKOMA PROTUBERANS (Morfolojik spektrum ve ayırıcı tanı) DFSP, Histopatoloji
 Dermatofibrosarkoma protuberans (DFSP) DERMATOFİBROSARKOMA PROTUBERANS (Morfolojik spektrum ve ayırıcı tanı) Prof Dr Taner Akalın Ege ÜTF Patoloji AD 25. Ulusal Patoloji Kongresi, 14-17 Ekim 2015, Bursa
Dermatofibrosarkoma protuberans (DFSP) DERMATOFİBROSARKOMA PROTUBERANS (Morfolojik spektrum ve ayırıcı tanı) Prof Dr Taner Akalın Ege ÜTF Patoloji AD 25. Ulusal Patoloji Kongresi, 14-17 Ekim 2015, Bursa
SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU
 SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU Ezgi Işıl Turhan 1, Nesrin Uğraş 1, Ömer Yerci 1, Seçil Ak 2, Berrin Tunca 2, Ersin Öztürk
SAĞ VE SOL KOLON YERLEŞİMLİ TÜMÖRLER: AYNI ORGANDA FARKLI PATOLOJİK BULGULAR VE MİKROSATELLİT İNSTABİLİTE DURUMU Ezgi Işıl Turhan 1, Nesrin Uğraş 1, Ömer Yerci 1, Seçil Ak 2, Berrin Tunca 2, Ersin Öztürk
İNTERAKTİF VAKA TARTIŞMASI
 İNTERAKTİF VAKA TARTIŞMASI Olgu 1: Yaşlı mide kanserli olgu OLGU 1: 77 yaşında, erkek hasta, 2 yıl önce antrum lokalizasyonunda mide kanseri tanısıyla opere edildi subtotal gastrektomi- D1 lenfadenektomi
İNTERAKTİF VAKA TARTIŞMASI Olgu 1: Yaşlı mide kanserli olgu OLGU 1: 77 yaşında, erkek hasta, 2 yıl önce antrum lokalizasyonunda mide kanseri tanısıyla opere edildi subtotal gastrektomi- D1 lenfadenektomi
21.Ulusal Patoloji Kongresi Yumuşak Doku Kursu Lipomatöz Tümörler. Dr. Burçin Tuna DEÜTF Patoloji AD 16-20 Kasım 2011-İZMİR
 21.Ulusal Patoloji Kongresi Yumuşak Doku Kursu Lipomatöz Tümörler Dr. Burçin Tuna DEÜTF Patoloji AD 16-20 Kasım 2011-İZMİR Sunum planı Lipomatöz tümör nedir? ve sınıflama Sorun yaratan lipomlar Liposarkomlarda
21.Ulusal Patoloji Kongresi Yumuşak Doku Kursu Lipomatöz Tümörler Dr. Burçin Tuna DEÜTF Patoloji AD 16-20 Kasım 2011-İZMİR Sunum planı Lipomatöz tümör nedir? ve sınıflama Sorun yaratan lipomlar Liposarkomlarda
NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ
 NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ Dinç Süren 1, Mustafa Yıldırım 2, Vildan Kaya 3, Ruksan Elal 1, Ömer Tarık Selçuk 4, Üstün Osma 4, Mustafa Yıldız 5, Cem
NAZOFARENKS KARSİNOMUNDA CLAUDIN 1, 4 VE 7 EKSPRESYON PATERNİ VE PROGNOSTİK ÖNEMİ Dinç Süren 1, Mustafa Yıldırım 2, Vildan Kaya 3, Ruksan Elal 1, Ömer Tarık Selçuk 4, Üstün Osma 4, Mustafa Yıldız 5, Cem
OLGU. 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle
 OLGU 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle Meme USG; Sağ memeyi bütünüyle dolduran, düzgün sınırlı, içerisinde yer yer kistik alanların ve kalsifikasyonların izlendiği, yoğun vasküler sinyal
OLGU 57 yaşında Sağ memede son 10 ayda hızla büyüyen kitle Meme USG; Sağ memeyi bütünüyle dolduran, düzgün sınırlı, içerisinde yer yer kistik alanların ve kalsifikasyonların izlendiği, yoğun vasküler sinyal
Meme Olgu Sunumu. Gürdeniz Serin. Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı. 3 Kasım Antalya
 Meme Olgu Sunumu 3 Kasım 2016 Antalya Gürdeniz Serin Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Olgu 35 yaşında kadın Sağ meme de kitle Özgeçmişinde: SLE - Renal Tx Radyoloji Mamografi: Sağ
Meme Olgu Sunumu 3 Kasım 2016 Antalya Gürdeniz Serin Ege Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Olgu 35 yaşında kadın Sağ meme de kitle Özgeçmişinde: SLE - Renal Tx Radyoloji Mamografi: Sağ
PROSTAT İĞNE BİYOPSİSİNDE TÜMÖR TANISI. Dr. Duygu Kankaya Ankara Üniversitesi Tıp Fakültesi
 PROSTAT İĞNE BİYOPSİSİNDE TÜMÖR TANISI Dr. Duygu Kankaya Ankara Üniversitesi Tıp Fakültesi Prostat İğne Biyopsisi Anormal digital rektal inceleme- Endurasyon, asimetri, sert nodülasyon Serum PSA 4mg/dl
PROSTAT İĞNE BİYOPSİSİNDE TÜMÖR TANISI Dr. Duygu Kankaya Ankara Üniversitesi Tıp Fakültesi Prostat İğne Biyopsisi Anormal digital rektal inceleme- Endurasyon, asimetri, sert nodülasyon Serum PSA 4mg/dl
AZ DİFERANSİYE TİROİD KANSERLERİ. Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM
 AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
AZ DİFERANSİYE TİROİD KANSERLERİ Prof. Dr. Müfide Nuran AKÇAY Atatürk Üniversitesi Tıp Fakültesi Genel Cerrahi Anabilim Dalı ERZURUM Tanım Az diferansiye tiroid karsinomları, iyi diferansiye ve anaplastik
Karsinoid Tümörler Giriş Sınıflandırma: Göğüs Cer rahisi rahisi Göğüs Cer Klinik:
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Karsinoid Tümörler Giriş Ender görülen akciğer tümörleridirler Rezeksiyon uygulanan akciğer tümörlerinin %0,4- %3 ünü oluştururlar Benign-malign
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Karsinoid Tümörler Giriş Ender görülen akciğer tümörleridirler Rezeksiyon uygulanan akciğer tümörlerinin %0,4- %3 ünü oluştururlar Benign-malign
İTF
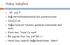 Vaka takdimi 65 yaş, E Sağ sternoklaidomastoid kas posteriorunda 3,5x2,5 cm Yoğun kontrast tutulumu gösteren metastatik lenf nodu Klinik tanı: Tiroid Ca met? İİA yapıldı Prot. No. 24738-11 Hasta başı yeterlik
Vaka takdimi 65 yaş, E Sağ sternoklaidomastoid kas posteriorunda 3,5x2,5 cm Yoğun kontrast tutulumu gösteren metastatik lenf nodu Klinik tanı: Tiroid Ca met? İİA yapıldı Prot. No. 24738-11 Hasta başı yeterlik
Göğüs Cerrahisi Sedat Gürkok. Göğüs Cerrahisi. Journal of Clinical and Analytical Medicine
 Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Soliter Pulmoner Nodül Tanım: Genel bir tanımı olmasa da 3 cm den küçük, akciğer parankimi ile çevrili, beraberinde herhangi patolojinin eşlik
Journal of Clinical and Analytical Medicine Göğüs Cerrahisi Soliter Pulmoner Nodül Tanım: Genel bir tanımı olmasa da 3 cm den küçük, akciğer parankimi ile çevrili, beraberinde herhangi patolojinin eşlik
AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ. Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi
 AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi Nöroendokrin tümörlerde 2004 WHO sınıflaması Tümör Tipi Tipik Karsinoid Atipik Karsinoid Büyük Hücreli nöroendokrin
AKCİĞERİN NÖROENDOKRİN TÜMÖRLERİ Doç. Dr. Mutlu DEMİRAY Bursa Medical Park Hastanesi Nöroendokrin tümörlerde 2004 WHO sınıflaması Tümör Tipi Tipik Karsinoid Atipik Karsinoid Büyük Hücreli nöroendokrin
Dr. A. Nimet Karadayı. Hastanesi, Patoloji Kliniği
 Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
Dr. A. Nimet Karadayı Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, Patoloji Kliniği MEME TÜMÖRLERİNDE PATOLOJİ RAPORLARINDA STANDARDİZASYON Amaç, hasta
Küçük Hücreli Dışı Akciğer Karsinomlarının EGFR Mutasyon Analizinde Real-Time PCR Yöntemi ile Mutasyona Spesifik İmmünohistokimyanın Karşılaştırılması
 Küçük Hücreli Dışı Akciğer Karsinomlarının EGFR Mutasyon Analizinde Real-Time PCR Yöntemi ile Mutasyona Spesifik nın Karşılaştırılması Dr.M.Çisel Aydın, Doç.Dr.Sevgen Önder, Prof.Dr.Gaye Güler Tezel Hacettepe
Küçük Hücreli Dışı Akciğer Karsinomlarının EGFR Mutasyon Analizinde Real-Time PCR Yöntemi ile Mutasyona Spesifik nın Karşılaştırılması Dr.M.Çisel Aydın, Doç.Dr.Sevgen Önder, Prof.Dr.Gaye Güler Tezel Hacettepe
MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR?
 MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR? Dr. Nebil BAL Başkent Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Adana Arş ve Uyg Mrk 1 Malign Melanoma Deri Mukozal 2 Malign Melanoma Biyopsi
MELANOMA PATOLOJİSİ KLİNİSYEN PATOLOGTAN NE BEKLEMELİDİR? Dr. Nebil BAL Başkent Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Adana Arş ve Uyg Mrk 1 Malign Melanoma Deri Mukozal 2 Malign Melanoma Biyopsi
PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ
 PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ Dr. Nimet Karadayı Dr.Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi Patoloji Kliniği Lenf nodları metastatik malignitelerde en
PRİMERİ BİLİNMEYEN AKSİLLER METASTAZ AYIRICI TANISINDA PATOLOJİNİN YERİ Dr. Nimet Karadayı Dr.Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi Patoloji Kliniği Lenf nodları metastatik malignitelerde en
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ. Dr. Derin KÖSEBAY
 ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
ERKEN EVRE OVER KANSERİ VE BORDERLİNE OVER TÜMÖRLERİ Dr. Derin KÖSEBAY OVER KANSERİ Over kanseri tanısı koyulduktan sonra ortalama 5 yıllık yaşam oranı %35 civarındadır. Evre I olgularında 5 yıllık yaşam
DERMATOFİBROSARKOM PROTUBERANS. Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği
 DERMATOFİBROSARKOM PROTUBERANS Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği Dermatofibrosarkom Protuberans Dermatofibrosarkom Protuberans (DFSP), dermal
DERMATOFİBROSARKOM PROTUBERANS Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği Dermatofibrosarkom Protuberans Dermatofibrosarkom Protuberans (DFSP), dermal
İNVAZİF ASPERGİLLOZ Radyolojik Tanı. Dr. Recep SAVAŞ Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir
 İNVAZİF ASPERGİLLOZ Radyolojik Tanı Dr. Recep SAVAŞ Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir AMAÇ Radyolojik olarak algoritm Tanı ve bulgular Tedavi sonrası takip İnvazif Asperjilloz Akciğer
İNVAZİF ASPERGİLLOZ Radyolojik Tanı Dr. Recep SAVAŞ Ege Üniversitesi Tıp Fakültesi Radyoloji AD, İzmir AMAÇ Radyolojik olarak algoritm Tanı ve bulgular Tedavi sonrası takip İnvazif Asperjilloz Akciğer
Özofagus Tümörleri. Doç. Dr. Halil Kıyıcı 2016
 Özofagus Tümörleri Doç. Dr. Halil Kıyıcı 2016 Özofagus tümörleri Benign / iyi huylu tümörler Malign / kötü huylu tümörler daha fazla! Skuamöz /yassı hücreli karsinom (SCC) Dünyada en çok görülen özofagus
Özofagus Tümörleri Doç. Dr. Halil Kıyıcı 2016 Özofagus tümörleri Benign / iyi huylu tümörler Malign / kötü huylu tümörler daha fazla! Skuamöz /yassı hücreli karsinom (SCC) Dünyada en çok görülen özofagus
Lafora hastalığı, Unverricht Lundborg hastalığı, Nöronal Seroid Lipofuksinoz ve Sialidozlar en sık izlenen PME'lerdir. Progresif miyoklonik
 LAFORA HASTALIĞI Progressif Myoklonik Epilepsiler (PME) nadir olarak görülen, sıklıkla otozomal resessif olarak geçiş gösteren heterojen bir hastalık grubudur. Klinik olarak değişik tipte nöbetler ve progressif
LAFORA HASTALIĞI Progressif Myoklonik Epilepsiler (PME) nadir olarak görülen, sıklıkla otozomal resessif olarak geçiş gösteren heterojen bir hastalık grubudur. Klinik olarak değişik tipte nöbetler ve progressif
KOLOREKTAL POLİPLER. Prof. Dr. Mustafa Taşkın
 KOLOREKTAL POLİPLER Prof. Dr. Mustafa Taşkın -Polip,mukozal örtülerden lümene doğru gelişen oluşumlara verilen genel isimdir. -Makroskopik ve radyolojik görünümü tanımlar. -Sindirim sisteminde en çok kolonda
KOLOREKTAL POLİPLER Prof. Dr. Mustafa Taşkın -Polip,mukozal örtülerden lümene doğru gelişen oluşumlara verilen genel isimdir. -Makroskopik ve radyolojik görünümü tanımlar. -Sindirim sisteminde en çok kolonda
KOLOREKTAL KARSİNOMLARDA HPV NİN ROLÜ VE KARSİNOGENEZ AÇISINDAN P53 VE BCL-2 İLE İLİŞKİSİ
 KOLOREKTAL KARSİNOMLARDA HPV NİN ROLÜ VE KARSİNOGENEZ AÇISINDAN P53 VE BCL-2 İLE İLİŞKİSİ Ruksan ELAL 1, Arsenal SEZGİN ALİKANOĞLU 2, Dinç SÜREN 2, Mustafa YILDIRIM 3, Nurullah BÜLBÜLLER 4, Cem SEZER 2
KOLOREKTAL KARSİNOMLARDA HPV NİN ROLÜ VE KARSİNOGENEZ AÇISINDAN P53 VE BCL-2 İLE İLİŞKİSİ Ruksan ELAL 1, Arsenal SEZGİN ALİKANOĞLU 2, Dinç SÜREN 2, Mustafa YILDIRIM 3, Nurullah BÜLBÜLLER 4, Cem SEZER 2
BAŞ-BOYUN PATOLOJİSİ SLAYT SEMİNERİ-TÜKRÜK BEZİ TÜMÖRLERİ OLGU SUNUMU. Dr. Özlem Saraydaroğlu
 BAŞ-BOYUN PATOLOJİSİ SLAYT SEMİNERİ-TÜKRÜK BEZİ TÜMÖRLERİ OLGU SUNUMU Dr. Özlem Saraydaroğlu 63 yaşında, erkek hasta İki yıldır boyun sol tarafında, kulak altında şişlik yakınması Dış merkezli USG sonucu;
BAŞ-BOYUN PATOLOJİSİ SLAYT SEMİNERİ-TÜKRÜK BEZİ TÜMÖRLERİ OLGU SUNUMU Dr. Özlem Saraydaroğlu 63 yaşında, erkek hasta İki yıldır boyun sol tarafında, kulak altında şişlik yakınması Dış merkezli USG sonucu;
OLGU SUNUMU. Prof. Dr. Yeşim Gürbüz
 OLGU SUNUMU Prof. Dr. Yeşim Gürbüz HİKAYE 48 yaşında bayan hasta, 2 senedir nefes darlığı olan hasta dahiliyeye başvurmuş, Tiroit palpasyonunda sol lopta 3x2 cm boyutunda kitle ele gelmiş, MNG tanısı
OLGU SUNUMU Prof. Dr. Yeşim Gürbüz HİKAYE 48 yaşında bayan hasta, 2 senedir nefes darlığı olan hasta dahiliyeye başvurmuş, Tiroit palpasyonunda sol lopta 3x2 cm boyutunda kitle ele gelmiş, MNG tanısı
İNVAZİV MESANE TÜMÖRLERİ. -Patoloji- Dilek Ertoy Baydar Hacettepe Ün. Patoloji AD
 İNVAZİV MESANE TÜMÖRLERİ -Patoloji- Dilek Ertoy Baydar Hacettepe Ün. Patoloji AD İnvaziv Mesane Karsinomları Mesane karsinomlarının %30 u Papiller tümörün tabanında veya içinde Karsinoma in-situ beraberinde
İNVAZİV MESANE TÜMÖRLERİ -Patoloji- Dilek Ertoy Baydar Hacettepe Ün. Patoloji AD İnvaziv Mesane Karsinomları Mesane karsinomlarının %30 u Papiller tümörün tabanında veya içinde Karsinoma in-situ beraberinde
Pediatrik Over Tümörleri Slayt Semineri
 Pediatrik Over Tümörleri Slayt Semineri Dr. H. Serap Toru Akdeniz Üniversitesi Tıp Fakültesi Patoloji A.D. Antalya /Türkiye Takip 4 yıl, hastalıksız takipte Östradiol ve inhibin düzeyleri Pelvik USG 13
Pediatrik Over Tümörleri Slayt Semineri Dr. H. Serap Toru Akdeniz Üniversitesi Tıp Fakültesi Patoloji A.D. Antalya /Türkiye Takip 4 yıl, hastalıksız takipte Östradiol ve inhibin düzeyleri Pelvik USG 13
Cerrahi Dışı Tedaviler
 KÖTÜ HUYLU YUMUŞAK DOKU TÜMÖRLERİ Cerrahi Dışı Tedaviler Dr.Selami ÇAKMAK GATA Haydarpaşa Eğitim Hastanesi 50 den fazla yumuşak doku sarkomu tipi Kaynaklandığı doku, Klinik gidişat, Görülme yaşı, Agresifliği,
KÖTÜ HUYLU YUMUŞAK DOKU TÜMÖRLERİ Cerrahi Dışı Tedaviler Dr.Selami ÇAKMAK GATA Haydarpaşa Eğitim Hastanesi 50 den fazla yumuşak doku sarkomu tipi Kaynaklandığı doku, Klinik gidişat, Görülme yaşı, Agresifliği,
Gastrointestinal stromal tümörler (GIST) gastrointestinal
 güncel gastroenteroloji 13/2 Gastrointestinal Stromal Tümörlerde MDBT ve MR Görüntüleme Nazan ÇİLEDAĞ, Kemal ARDA, Pelin Demir GÜMÜŞDAĞ Ankara Onkoloji Eğitim ve Araştırma Hastanesi, Radyoloji Bölümü,
güncel gastroenteroloji 13/2 Gastrointestinal Stromal Tümörlerde MDBT ve MR Görüntüleme Nazan ÇİLEDAĞ, Kemal ARDA, Pelin Demir GÜMÜŞDAĞ Ankara Onkoloji Eğitim ve Araştırma Hastanesi, Radyoloji Bölümü,
Amiloidozis Patolojisi. Dr. Yıldırım Karslıoğlu GATA Patoloji Anabilim Dalı
 Amiloidozis Patolojisi Dr. Yıldırım Karslıoğlu GATA Patoloji Anabilim Dalı Tanım Amiloid = Latince amylum (nişasta, amiloz) benzeri Anormal ekstrasellüler protein depozisyonu Fizyolojik eliminasyon mekanizmaları
Amiloidozis Patolojisi Dr. Yıldırım Karslıoğlu GATA Patoloji Anabilim Dalı Tanım Amiloid = Latince amylum (nişasta, amiloz) benzeri Anormal ekstrasellüler protein depozisyonu Fizyolojik eliminasyon mekanizmaları
Endometrium Karsinomları
 Endometrium Karsinomları Prof. Dr. Türkan KÜÇÜKALİ Hacettepe Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Ankara Endometrium Adenokarsinomlarının Histolojik Tipleri Endometrioid adenokarsinom Silli
Endometrium Karsinomları Prof. Dr. Türkan KÜÇÜKALİ Hacettepe Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı Ankara Endometrium Adenokarsinomlarının Histolojik Tipleri Endometrioid adenokarsinom Silli
Prostat Tümörlerinde WHO 2016 Sınıflandırması DR. BORA GÜREL KOCAELİ ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI
 Prostat Tümörlerinde WHO 2016 Sınıflandırması DR. BORA GÜREL KOCAELİ ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI Giriş En son WHO sınıflandırması 2004 yılında Son 12 yılda hatırı sayılır yenilikler
Prostat Tümörlerinde WHO 2016 Sınıflandırması DR. BORA GÜREL KOCAELİ ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI Giriş En son WHO sınıflandırması 2004 yılında Son 12 yılda hatırı sayılır yenilikler
Adrenal lezyonların görüntüleme bulguları. Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul
 Adrenal lezyonların görüntüleme bulguları Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul Öğrenme hedefleri Adrenal bez kitlelerinin BT ile değerlendirilmesinde temel prensip ve bulguları öğrenmek
Adrenal lezyonların görüntüleme bulguları Dr. Ercan KOCAKOÇ Bezmialem Vakıf Üniversitesi İstanbul Öğrenme hedefleri Adrenal bez kitlelerinin BT ile değerlendirilmesinde temel prensip ve bulguları öğrenmek
AYIRICI TANIDA ZORLUK YARATAN LEZYONLAR
 AYIRICI TANIDA ZORLUK YARATAN LEZYONLAR Dr. D. Sema ARICI Bezmialem Vakıf Üniversitesi 26.ULUSAL PATOLOJİ/7. SİTOPATOLOJİ KONGRESİ 2-6 KASIM 2016,ANTALYA OLGU 1 51 y Myom nedeniyle TAH +BSO Makroskopi:
AYIRICI TANIDA ZORLUK YARATAN LEZYONLAR Dr. D. Sema ARICI Bezmialem Vakıf Üniversitesi 26.ULUSAL PATOLOJİ/7. SİTOPATOLOJİ KONGRESİ 2-6 KASIM 2016,ANTALYA OLGU 1 51 y Myom nedeniyle TAH +BSO Makroskopi:
Multipl Endokrin Neoplaziler. Dr. Tuba T. Duman-2012
 Multipl Endokrin Neoplaziler Dr. Tuba T. Duman-2012 Multipl Endokrin Neoplaziler Klinik gözlemlerle, endokrin bezleri içeren neoplastik sendromlar tanımlanmıştır. Paratiroid, hipofiz, adrenal,tiroid ve
Multipl Endokrin Neoplaziler Dr. Tuba T. Duman-2012 Multipl Endokrin Neoplaziler Klinik gözlemlerle, endokrin bezleri içeren neoplastik sendromlar tanımlanmıştır. Paratiroid, hipofiz, adrenal,tiroid ve
TANISAL SİTOLOJİDE ALGORİTMİK YAKLAŞIM. Doç. Dr. Özlem AYDIN, F.I.A.C. Acıbadem Üniv. Tıp Fakültesi Patoloji AD - İstanbul
 TANISAL SİTOLOJİDE ALGORİTMİK YAKLAŞIM Doç. Dr. Özlem AYDIN, F.I.A.C. Acıbadem Üniv. Tıp Fakültesi Patoloji AD - İstanbul Sağ meme Hipersellüler, tek dağınık dissosiye hücre patterni Sol meme ??? Hipersellüler,
TANISAL SİTOLOJİDE ALGORİTMİK YAKLAŞIM Doç. Dr. Özlem AYDIN, F.I.A.C. Acıbadem Üniv. Tıp Fakültesi Patoloji AD - İstanbul Sağ meme Hipersellüler, tek dağınık dissosiye hücre patterni Sol meme ??? Hipersellüler,
56Y, erkek hasta Generalize LAP ( servikal, inguinal, aksiller, toraks ve abdomende ) Ateş Gece terlemesi Lenfopeni IgG, IgA, IgM yüksek
 56Y, erkek hasta Generalize LAP ( servikal, inguinal, aksiller, toraks ve abdomende ) Ateş Gece terlemesi Lenfopeni IgG, IgA, IgM yüksek Sedimantasyon (77mm/saat) CRP 7.67(N:0-0.8mg/dl) Servikal lenf nodu
56Y, erkek hasta Generalize LAP ( servikal, inguinal, aksiller, toraks ve abdomende ) Ateş Gece terlemesi Lenfopeni IgG, IgA, IgM yüksek Sedimantasyon (77mm/saat) CRP 7.67(N:0-0.8mg/dl) Servikal lenf nodu
TÜM MİDE BİYOPSİLERİNE RUTİN OLARAK GIEMSA VE ALCIAN BLUE UYGULAMALI MIYIZ?
 TÜM MİDE BİYOPSİLERİNE RUTİN OLARAK GIEMSA VE ALCIAN BLUE UYGULAMALI MIYIZ? PROF. DR. SÜLEN SARIOĞLU¹, DR. EVREN UZUN¹, DOÇ. DR. MEHTAT ÜNLܹ, PROF. DR. HÜLYA ELLİDOKUZ² DOKUZ EYLÜL ÜNİVERSİTESİ TIBBİ
TÜM MİDE BİYOPSİLERİNE RUTİN OLARAK GIEMSA VE ALCIAN BLUE UYGULAMALI MIYIZ? PROF. DR. SÜLEN SARIOĞLU¹, DR. EVREN UZUN¹, DOÇ. DR. MEHTAT ÜNLܹ, PROF. DR. HÜLYA ELLİDOKUZ² DOKUZ EYLÜL ÜNİVERSİTESİ TIBBİ
KOLOREKTAL KARSİNOMA VE ÖNCÜ LEZYONLARINDA MİKROSATELLİT İNSTABİLİTESİNİN İMMÜNHİSTOKİMYASAL OLARAK DEĞERLENDİRİLMESİ
 KOLOREKTAL KARSİNOMA VE ÖNCÜ LEZYONLARINDA MİKROSATELLİT İNSTABİLİTESİNİN İMMÜNHİSTOKİMYASAL OLARAK DEĞERLENDİRİLMESİ Seher YÜKSEL 1, Berna SAVAŞ 2, Elçin KADAN 3, Arzu ENSARİ 2, Nazmiye KURŞUN 4 1 Gümüşhane
KOLOREKTAL KARSİNOMA VE ÖNCÜ LEZYONLARINDA MİKROSATELLİT İNSTABİLİTESİNİN İMMÜNHİSTOKİMYASAL OLARAK DEĞERLENDİRİLMESİ Seher YÜKSEL 1, Berna SAVAŞ 2, Elçin KADAN 3, Arzu ENSARİ 2, Nazmiye KURŞUN 4 1 Gümüşhane
TAKD olgu sunumları- 21 Kasım Dr Şebnem Batur Dr Büge ÖZ İÜ Cerrahpaşa Tıp Fakültesi Patoloji AD
 TAKD olgu sunumları- 21 Kasım 2012 Dr Şebnem Batur Dr Büge ÖZ İÜ Cerrahpaşa Tıp Fakültesi Patoloji AD Konuşma akışı; ALK mutasyonu değerlendirmedeki sorunlar ROS-1 mutasyonu Avrupa pulmoner patoloji çalışma
TAKD olgu sunumları- 21 Kasım 2012 Dr Şebnem Batur Dr Büge ÖZ İÜ Cerrahpaşa Tıp Fakültesi Patoloji AD Konuşma akışı; ALK mutasyonu değerlendirmedeki sorunlar ROS-1 mutasyonu Avrupa pulmoner patoloji çalışma
Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi
 Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Testis tümörleri Erkeklerdeki kanserlerin %1 i Yıllık %3-6 artış Avrupa da her yıl 24.000 yeni vak a Testis Tümör Epidemiyolojisi İnsidans dünya genelinde
Dr. Yaşar BEDÜK Ankara Üniversitesi Tıp Fakültesi Testis tümörleri Erkeklerdeki kanserlerin %1 i Yıllık %3-6 artış Avrupa da her yıl 24.000 yeni vak a Testis Tümör Epidemiyolojisi İnsidans dünya genelinde
Gülay Aydoğdu, Pınar Fırat, Yasemin Özlük, Dilek Yılmazbayhan
 "ÖNEMİ BELİRSİZ ATİPİ/ÖNEMİ BELİRSİZ FOLİKÜLER LEZYON" "FOLİKÜLER NEOPLAZİ/FOLİKÜLER NEOPLAZİ KUŞKUSU" "MALİGNİTE KUŞKUSU" TANILI TİROİD İNCE İĞNE ASPİRASYON MATERYALLERİNDE MORFOLOJİK DEĞERLENDİRME VE
"ÖNEMİ BELİRSİZ ATİPİ/ÖNEMİ BELİRSİZ FOLİKÜLER LEZYON" "FOLİKÜLER NEOPLAZİ/FOLİKÜLER NEOPLAZİ KUŞKUSU" "MALİGNİTE KUŞKUSU" TANILI TİROİD İNCE İĞNE ASPİRASYON MATERYALLERİNDE MORFOLOJİK DEĞERLENDİRME VE
Merkel Hücreli Karsinom
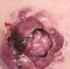 Merkel Hücreli Karsinom Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği IV. DOD Dermatoloji Gündemi, 3-6 Eylül 2015, Eskişehir Merkel Hücreli Karsinom
Merkel Hücreli Karsinom Doç. Dr. Filiz Canpolat Dışkapı Yıldırım Beyazıt Eğitim ve Araştırma Hastanesi Dermatoloji Kliniği IV. DOD Dermatoloji Gündemi, 3-6 Eylül 2015, Eskişehir Merkel Hücreli Karsinom
OVERİN YÜZEY EPİTELİNDEN KAYNAKLANAN TÜMÖRLERİ. Prof.Dr. Nafi Oruç İ.Ü. Cerrahpaşa Tıp Fakültesi
 OVERİN YÜZEY EPİTELİNDEN KAYNAKLANAN TÜMÖRLERİ Prof.Dr. Nafi Oruç İ.Ü. Cerrahpaşa Tıp Fakültesi Seröz Tümörler Seröz Tümörler Sıklık Tüm over tümörlerinin %30 u Benign over tümörlerinin %22 si Malign over
OVERİN YÜZEY EPİTELİNDEN KAYNAKLANAN TÜMÖRLERİ Prof.Dr. Nafi Oruç İ.Ü. Cerrahpaşa Tıp Fakültesi Seröz Tümörler Seröz Tümörler Sıklık Tüm over tümörlerinin %30 u Benign over tümörlerinin %22 si Malign over
TİROİD NODÜLLERİNİN SIVI BAZLI (SurePath) SİTOLOJİSİ: 3 Yıllık Histopatolojik Korelasyon
 TİROİD NODÜLLERİNİN SIVI BAZLI (SurePath) SİTOLOJİSİ: 3 Yıllık Histopatolojik Korelasyon Dr. M. Salih Deveci GATA Gülhane Askeri Tıp Fakültesi Patoloji AD, Ankara Patoloji & Sitopatoloji Kongresi Bursa
TİROİD NODÜLLERİNİN SIVI BAZLI (SurePath) SİTOLOJİSİ: 3 Yıllık Histopatolojik Korelasyon Dr. M. Salih Deveci GATA Gülhane Askeri Tıp Fakültesi Patoloji AD, Ankara Patoloji & Sitopatoloji Kongresi Bursa
Savaş Baba, Sabri Özden, Barış Saylam, Umut Fırat Turan Ankara Numune EAH. Meme Endokrin Cerrahi Kliniği
 Savaş Baba, Sabri Özden, Barış Saylam, Umut Fırat Turan Ankara Numune EAH. Meme Endokrin Cerrahi Kliniği Tiroid kanserleri bütün kanserler içinde yaklaşık % 1 oranında görülmekte olup, özellikle kadınlarda
Savaş Baba, Sabri Özden, Barış Saylam, Umut Fırat Turan Ankara Numune EAH. Meme Endokrin Cerrahi Kliniği Tiroid kanserleri bütün kanserler içinde yaklaşık % 1 oranında görülmekte olup, özellikle kadınlarda
Mide Rezeksiyon Materyallerine Yaklaşım, Evreleme ve Raporlama
 Mide Rezeksiyon Materyallerine Yaklaşım, Evreleme ve Raporlama Banu Bilezikçi Güven Hastanesi Patoloji Bölümü, Ankara 25. Ulusal Patoloji Kongresi 6. Sitopatoloji Kongresi 14-17 Ekim 2015, Bursa 2014
Mide Rezeksiyon Materyallerine Yaklaşım, Evreleme ve Raporlama Banu Bilezikçi Güven Hastanesi Patoloji Bölümü, Ankara 25. Ulusal Patoloji Kongresi 6. Sitopatoloji Kongresi 14-17 Ekim 2015, Bursa 2014
Malignite ve Transplantasyon. Doç. Dr. Halil Yazıcı İstanbul Tıp Fakültesi Nefroloji Bilim Dalı
 Malignite ve Transplantasyon Doç. Dr. Halil Yazıcı İstanbul Tıp Fakültesi Nefroloji Bilim Dalı Sunum Planı -Pretransplant malignitesi olan alıcı -Pretransplant malignitesi olan donör -Posttransplant de
Malignite ve Transplantasyon Doç. Dr. Halil Yazıcı İstanbul Tıp Fakültesi Nefroloji Bilim Dalı Sunum Planı -Pretransplant malignitesi olan alıcı -Pretransplant malignitesi olan donör -Posttransplant de
Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım. Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi
 Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi okült (gizli, saklı, bilinmeyen, anlaşılmaz) okült + kanser primeri bilinmeyen
Primeri Bilinmeyen Aksiller Metastazda Cerrahi Yaklaşım Dr. Ali İlker Filiz GATA Haydarpaşa Eğitim Hastanesi Genel Cerrahi Servisi okült (gizli, saklı, bilinmeyen, anlaşılmaz) okült + kanser primeri bilinmeyen
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Zerrin CALAY- Dr. Ekrem YAVUZ OLGU SUNUMU
 MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Zerrin CALAY- Dr. Ekrem YAVUZ OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 26. Ulusal Patoloji Kongresi 2-6 Kasım
MEME PATOLOJİSİ Slayt Semineri Oturum Başkanları: Dr. Zerrin CALAY- Dr. Ekrem YAVUZ OLGU SUNUMU Dr Tülin Öztürk İ.Ü. Cerrahpaşa Tıp Fakültesi Patoloji Anabilim Dalı 26. Ulusal Patoloji Kongresi 2-6 Kasım
HIV & CMV Gastrointestinal ve Solunum Sistemi
 Uzm. Dr. Sinem AKKAYA IŞIK Sultan Abdülhamid Han Eğitim ve Araştırma Hastanesi HIV & CMV Gastrointestinal ve Solunum Sistemi AIDS CMV; nadir ölümcül İlk vaka 1983 Etkili ART sıklık azalmakta, tedavi şansı
Uzm. Dr. Sinem AKKAYA IŞIK Sultan Abdülhamid Han Eğitim ve Araştırma Hastanesi HIV & CMV Gastrointestinal ve Solunum Sistemi AIDS CMV; nadir ölümcül İlk vaka 1983 Etkili ART sıklık azalmakta, tedavi şansı
MEME KANSERİ KÖK HÜCRELERİNİN GEN EKSPRESYON PROFİLİ
 MEME KANSERİ KÖK HÜCRELERİNİN GEN EKSPRESYON PROFİLİ Sait Murat Doğan, A. Pınar Erçetin, Zekiye Altun, Duygu Dursun, Safiye Aktaş Dokuz Eylül Üniversitesi Onkoloji Enstitüsü, İzmir Slayt 1 / 14 Meme Kanseri
MEME KANSERİ KÖK HÜCRELERİNİN GEN EKSPRESYON PROFİLİ Sait Murat Doğan, A. Pınar Erçetin, Zekiye Altun, Duygu Dursun, Safiye Aktaş Dokuz Eylül Üniversitesi Onkoloji Enstitüsü, İzmir Slayt 1 / 14 Meme Kanseri
OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI. Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı
 OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı Malign mikst müllerian tümör Diğer isimleri Malign mikst mezodermal
OVER KAYNAKLI MALİGN MİKST MÜLLERİAN TÜMÖRLERDE TEDAVİ YAKLAŞIMI Mustafa ÖZGÜROĞLU Cerrahpaşa Tıp Fakültesi Tıbbi Onkoloji Bilim Dalı Malign mikst müllerian tümör Diğer isimleri Malign mikst mezodermal
SERT DOKUNUN SULU (KĠSTĠK) LEZYONU. Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011
 SERT DOKUNUN SULU (KĠSTĠK) LEZYONU Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011 OLGU 9 Y, K Sağ humerus proksimali 2 yıl önce kırık Doğal iyileşmeye bırakılmış
SERT DOKUNUN SULU (KĠSTĠK) LEZYONU Dr Arzu AVCI ATATÜRK EĞİTİM VE ARAŞTIRMA HASTANESİ TIBBİ PATOLOJİ KLİNİĞİ 17 Kasım 2011 OLGU 9 Y, K Sağ humerus proksimali 2 yıl önce kırık Doğal iyileşmeye bırakılmış
KOLON VE İNCE BAĞIRSAĞIN NONTÜMÖRAL REZEKSİYON MATERYALLERİNDE TANIYA YAKLAŞIM. Dr. Armağan GÜNAL GATA Tıbbi Patoloji AD - Ankara
 KOLON VE İNCE BAĞIRSAĞIN NONTÜMÖRAL REZEKSİYON MATERYALLERİNDE TANIYA YAKLAŞIM Dr. Armağan GÜNAL GATA Tıbbi Patoloji AD - Ankara Konuşmanın başlığı üzerine GİS patolojisinde Kolon ve ince bağırsağın Nontümöral
KOLON VE İNCE BAĞIRSAĞIN NONTÜMÖRAL REZEKSİYON MATERYALLERİNDE TANIYA YAKLAŞIM Dr. Armağan GÜNAL GATA Tıbbi Patoloji AD - Ankara Konuşmanın başlığı üzerine GİS patolojisinde Kolon ve ince bağırsağın Nontümöral
MESANE TÜMÖRLERİNİN DOĞAL SEYRİ
 MESANE TÜMÖRLERİNİN DOĞAL SEYRİ ve MOLEKÜLER PROGNOSTİK FAKTÖRLER Prof. Dr. Levent Türkeri Üroloji Anabilim Dalı Marmara Üniversitesi Tıp Fakültesi Mesane Tümörü (Transizyonel Hücreli Karsinom) Yüzeyel
MESANE TÜMÖRLERİNİN DOĞAL SEYRİ ve MOLEKÜLER PROGNOSTİK FAKTÖRLER Prof. Dr. Levent Türkeri Üroloji Anabilim Dalı Marmara Üniversitesi Tıp Fakültesi Mesane Tümörü (Transizyonel Hücreli Karsinom) Yüzeyel
MALİGN VE BENİGN GRANÜLER HÜCRELİ TÜMÖR KARŞILAŞMALI İKİ OLGU SUNUMU. e-mail: [email protected]
 IAAOJ, Health Sciences, 2013,1(2), 45-51 MALİGN VE BENİGN GRANÜLER HÜCRELİ TÜMÖR KARŞILAŞMALI İKİ OLGU SUNUMU Meltem Öznur 1, Gamze Erfan 2, Kemal Behzatoğlu 3, Pelin Yıldız 4, Mustafa KULAÇ 2 e-mail:
IAAOJ, Health Sciences, 2013,1(2), 45-51 MALİGN VE BENİGN GRANÜLER HÜCRELİ TÜMÖR KARŞILAŞMALI İKİ OLGU SUNUMU Meltem Öznur 1, Gamze Erfan 2, Kemal Behzatoğlu 3, Pelin Yıldız 4, Mustafa KULAÇ 2 e-mail:
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri. Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı
 Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
Aksillanın Görüntülenmesi ve Biyopsi Teknikleri Prof. Dr. Meltem Gülsün Akpınar Hacettepe Üniversitesi Radyoloji Anabilim Dalı Meme kanserli hastalarda ana prognostik faktörler: Primer tümörün büyüklüğü
KOLOREKTAL KANSERLERİN MOLEKÜLER SINIFLAMASI. Doç.Dr.Aytekin AKYOL Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı 23 Mart 2014
 KOLOREKTAL KANSERLERİN MOLEKÜLER SINIFLAMASI Doç.Dr.Aytekin AKYOL Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı 23 Mart 2014 Kolorektal Kanserler; Sunum Planı Genel bilgiler Moleküler
KOLOREKTAL KANSERLERİN MOLEKÜLER SINIFLAMASI Doç.Dr.Aytekin AKYOL Hacettepe Üniversitesi Tıp Fakültesi Tıbbi Patoloji Anabilim Dalı 23 Mart 2014 Kolorektal Kanserler; Sunum Planı Genel bilgiler Moleküler
Tiroid nodüllerinin değerlendirilmesinde tru-cut biyopsi yöntemi kullanılmalı mı?
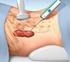 Tiroid nodüllerinin değerlendirilmesinde tru-cut biyopsi yöntemi kullanılmalı mı? Beril Güler, Tuğçe Kıran, Dilek Sema Arıcı, Erhan Ayşan, Fatma Cavide Sönmez Tiroid nodülü nedir? Çevre tiroid parankiminden
Tiroid nodüllerinin değerlendirilmesinde tru-cut biyopsi yöntemi kullanılmalı mı? Beril Güler, Tuğçe Kıran, Dilek Sema Arıcı, Erhan Ayşan, Fatma Cavide Sönmez Tiroid nodülü nedir? Çevre tiroid parankiminden
ERKEK GENİTAL SİSTEMİ. Webmaster tarafından yazıldı. Pazartesi, 12 Ocak 2009 11:39 - Son Güncelleme Perşembe, 15 Ocak 2009 09:19
 1) Çocuklarda en sık görülen testis tümörü aşağıdakilerden hangisidir? (1998 NİSAN) a) Klasik seminom b) Teratom c) Yolk sak tümörü d) Kariokarsinom e) Spermatositik seminom Testisde en sık görülen tümör
1) Çocuklarda en sık görülen testis tümörü aşağıdakilerden hangisidir? (1998 NİSAN) a) Klasik seminom b) Teratom c) Yolk sak tümörü d) Kariokarsinom e) Spermatositik seminom Testisde en sık görülen tümör
NEOPLAZİ D R. Y A S E M İ N S E Z G İ N. yasemin sezgin
 NEOPLAZİ D R. Y A S E M İ N S E Z G İ N yasemin sezgin Neoplazi Yeni bir doku oluşmasını ifade eder. Oluşan bu kitleye neoplazm denir. Aslen şişlik anlamına gelen tümör deyimi de neoplazm anlamında kullanılmaktadır.
NEOPLAZİ D R. Y A S E M İ N S E Z G İ N yasemin sezgin Neoplazi Yeni bir doku oluşmasını ifade eder. Oluşan bu kitleye neoplazm denir. Aslen şişlik anlamına gelen tümör deyimi de neoplazm anlamında kullanılmaktadır.
KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI
 KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI AMAÇ Kanser ön ya da kesin tanılı hastalarda radyolojik algoritmayı belirlemek ÖĞRENİM HEDEFLERİ Kanser riski olan hastalara doğru radyolojik tetkik
KANSERDE RADYOLOJİK GÖRÜNTÜLEME DOÇ. DR.İSMAİL MİHMANLI AMAÇ Kanser ön ya da kesin tanılı hastalarda radyolojik algoritmayı belirlemek ÖĞRENİM HEDEFLERİ Kanser riski olan hastalara doğru radyolojik tetkik
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi
 Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
Meme ve Over Kanserlerinde Laboratuvar: Klinisyenin Laboratuvardan Beklentisi Dr. Handan Onur XXI. Düzen Klinik Laboratuvar Günleri, Ankara, 23 Ekim 2011 MEME KANSERİ Meme Kanseri Sıklıkla meme başına
ENDOMETRİAL KARSİNOM SPORADİK Mİ? HEREDİTER Mİ? Dr Ş.Funda Tanay Eren Marmara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı
 ENDOMETRİAL KARSİNOM SPORADİK Mİ? HEREDİTER Mİ? Dr Ş.Funda Tanay Eren Marmara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 26.ULUSALPATOLOJİ KONGRESİ ANTALYA 2016 Kalıtsal kanser sendromlarının tespit
ENDOMETRİAL KARSİNOM SPORADİK Mİ? HEREDİTER Mİ? Dr Ş.Funda Tanay Eren Marmara Üniversitesi Tıp Fakültesi Patoloji Anabilim Dalı 26.ULUSALPATOLOJİ KONGRESİ ANTALYA 2016 Kalıtsal kanser sendromlarının tespit
HER2 POZİTİF HASTALIĞA YAKLAŞIM
 HER2 POZİTİF HASTALIĞA YAKLAŞIM Dr.Merih Güray Durak DEÜTF Patoloji ABD 9.Ekim.2014 İzmir Meme Hastalıkları Derneği Bilimsel Toplantısı Meme Kanserinde HER2 HER2 (human epidermal growth factor receptor
HER2 POZİTİF HASTALIĞA YAKLAŞIM Dr.Merih Güray Durak DEÜTF Patoloji ABD 9.Ekim.2014 İzmir Meme Hastalıkları Derneği Bilimsel Toplantısı Meme Kanserinde HER2 HER2 (human epidermal growth factor receptor
Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi
 Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi 1 Öğrenme hedefleri Metastazların genel özellikleri Görüntüleme Teknikleri Tedavi sonrası metastaz takibi Ayırıcı tanı 2 Metastatik Hastalık Total
Dr Ercan KARAARSLAN Acıbadem Üniversitesi Maslak Hastanesi 1 Öğrenme hedefleri Metastazların genel özellikleri Görüntüleme Teknikleri Tedavi sonrası metastaz takibi Ayırıcı tanı 2 Metastatik Hastalık Total
Gastrointestinal stromal tümörler (GİST), gastrointestinal sistemin en sık görülen
 DERLEME Hacettepe Tıp Dergisi 2004; 35:87-91 Gastrointestinal stromal tümörler ve imatinib (Glivec ) tedavisi Ömer Dizdar 1, ilüfer Güler 2 1Araştırma Görevlisi, Hacettepe Üniversitesi Tıp Fakültesi İç
DERLEME Hacettepe Tıp Dergisi 2004; 35:87-91 Gastrointestinal stromal tümörler ve imatinib (Glivec ) tedavisi Ömer Dizdar 1, ilüfer Güler 2 1Araştırma Görevlisi, Hacettepe Üniversitesi Tıp Fakültesi İç
Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları ABD, Medikal Onkoloji BD Güldal Esendağlı
 Sağlık Bakanlığından Muaf Hekimin Ünvanı - Adı Soyadı Aydın Aytekin Bildiriyi Sunacak Kişi Ünvanı - Adı Soyadı Rafiye Çiftçiler Bildiriyi Sunacak Kişi Kurumu Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları
Sağlık Bakanlığından Muaf Hekimin Ünvanı - Adı Soyadı Aydın Aytekin Bildiriyi Sunacak Kişi Ünvanı - Adı Soyadı Rafiye Çiftçiler Bildiriyi Sunacak Kişi Kurumu Gazi Üniversitesi Tıp Fakültesi, İç Hastalıkları
MEDÜLLER TİROİD KANSERİ VE EŞ ZAMANLI AİLESEL OLGULAR
 MEDÜLLER TİROİD KANSERİ VE EŞ ZAMANLI AİLESEL OLGULAR PROF DR TÜLAY CANDA DOKUZ EYLÜL ÜNİVERSİTESİ TIP FAKÜLTESİ 21. Ulusal Patoloji Kongresi, 16-20 Kasım 2011, İZMİR Kongre Düzenleme Kuruluna Kongreye
MEDÜLLER TİROİD KANSERİ VE EŞ ZAMANLI AİLESEL OLGULAR PROF DR TÜLAY CANDA DOKUZ EYLÜL ÜNİVERSİTESİ TIP FAKÜLTESİ 21. Ulusal Patoloji Kongresi, 16-20 Kasım 2011, İZMİR Kongre Düzenleme Kuruluna Kongreye
GASTROİNTESTİNAL STROMAL TÜMÖRLERDE HİSTOPATOLOJİK,TANISAL VE PROGNOSTİK BULGULARIN DEĞERLENDİRİLMESİ
 T.C. ÇUKUROVA ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI GASTROİNTESTİNAL STROMAL TÜMÖRLERDE HİSTOPATOLOJİK,TANISAL VE PROGNOSTİK BULGULARIN DEĞERLENDİRİLMESİ DR. FİLİZ ÇEVLİK UZMANLIK TEZİ TEZ
T.C. ÇUKUROVA ÜNİVERSİTESİ TIP FAKÜLTESİ PATOLOJİ ANABİLİM DALI GASTROİNTESTİNAL STROMAL TÜMÖRLERDE HİSTOPATOLOJİK,TANISAL VE PROGNOSTİK BULGULARIN DEĞERLENDİRİLMESİ DR. FİLİZ ÇEVLİK UZMANLIK TEZİ TEZ
En Etkili Kemoterapi İlacı Seçimine Yardımcı Olan Moleküler Genetik Test
 En Etkili Kemoterapi İlacı Seçimine Yardımcı Olan Moleküler Genetik Test Yeni Nesil DNA Dizileme (NGS), İmmünHistoKimya (IHC) ile Hastanızın Kanser Tipinin ve Kemoterapi İlacının Belirlenmesi Kanser Tanı
En Etkili Kemoterapi İlacı Seçimine Yardımcı Olan Moleküler Genetik Test Yeni Nesil DNA Dizileme (NGS), İmmünHistoKimya (IHC) ile Hastanızın Kanser Tipinin ve Kemoterapi İlacının Belirlenmesi Kanser Tanı
SERVİKAL PREKANSER VE KANSERLERİN TESPİTİNDE P16/Kİ 67 DUAL BOYAMA YÖNTEMİNİN DEĞERLENDİRİLMESİ VE TARAMA TRİAGE KULLANIMI PROF. DR. M.
 SERVİKAL PREKANSER VE KANSERLERİN TESPİTİNDE P16/Kİ 67 DUAL BOYAMA YÖNTEMİNİN DEĞERLENDİRİLMESİ VE TARAMA TRİAGE KULLANIMI PROF. DR. M.YAVUZ SALİHOGLU İ.Ü. İSTANBUL TIP FAKÜLTESİ KADIN HASTALIKLARI VE
SERVİKAL PREKANSER VE KANSERLERİN TESPİTİNDE P16/Kİ 67 DUAL BOYAMA YÖNTEMİNİN DEĞERLENDİRİLMESİ VE TARAMA TRİAGE KULLANIMI PROF. DR. M.YAVUZ SALİHOGLU İ.Ü. İSTANBUL TIP FAKÜLTESİ KADIN HASTALIKLARI VE
Tiroidin en sık görülen benign tümörleri foliküler adenomlardır.
 GİRİŞ: Tiroidin en sık görülen benign tümörleri foliküler adenomlardır. Foliküler adenomlar iyi sınırlı tek lezyon şeklinde olup, genellikle adenomu normal tiroid dokusundan ayıran kapsülleri vardır. Sıklıkla
GİRİŞ: Tiroidin en sık görülen benign tümörleri foliküler adenomlardır. Foliküler adenomlar iyi sınırlı tek lezyon şeklinde olup, genellikle adenomu normal tiroid dokusundan ayıran kapsülleri vardır. Sıklıkla
AORT ANEVRİZMASI YAKIN DOĞU ÜNİVERSİTESİ SHMYO İLK VE ACİL YARDIM BÖLÜMÜ YRD DOÇ DR SEMRA ASLAY 2015
 AORT ANEVRİZMASI YAKIN DOĞU ÜNİVERSİTESİ SHMYO İLK VE ACİL YARDIM BÖLÜMÜ YRD DOÇ DR SEMRA ASLAY 2015 Ani ölümün önemli bir nedenidir Sıklığı yaşla birlikte artar 50 yaş altında nadir rastlanır E>K Aile
AORT ANEVRİZMASI YAKIN DOĞU ÜNİVERSİTESİ SHMYO İLK VE ACİL YARDIM BÖLÜMÜ YRD DOÇ DR SEMRA ASLAY 2015 Ani ölümün önemli bir nedenidir Sıklığı yaşla birlikte artar 50 yaş altında nadir rastlanır E>K Aile
KANSER EPİDEMİYOLOJİSİ VE KARSİNOGENEZ
 KANSER EPİDEMİYOLOJİSİ VE KARSİNOGENEZ Gökhan Erdem GATA Tıbbi Onkoloji BD 19 Mart 2014 5. Türk Tıbbi Onkoloji Kongresi, 19-23 Mart 2014, Antalya EPİDEMİYOLOJİ Epidemiyoloji, sağlık olaylarının görünme
KANSER EPİDEMİYOLOJİSİ VE KARSİNOGENEZ Gökhan Erdem GATA Tıbbi Onkoloji BD 19 Mart 2014 5. Türk Tıbbi Onkoloji Kongresi, 19-23 Mart 2014, Antalya EPİDEMİYOLOJİ Epidemiyoloji, sağlık olaylarının görünme
TÜLAY AKSARAY TECİMER 4 MAYIS 2013
 TÜLAY AKSARAY TECİMER 4 MAYIS 2013 Langerhans hücreli histiyositoz(lhh) Castleman Hastalığı (CH) Kimura Hastalığı Kikuchi Fujimoto -Histiyositik nekrotizan lenfadenit Rosai-Dorfman hastalığı Tanım Langerhans
TÜLAY AKSARAY TECİMER 4 MAYIS 2013 Langerhans hücreli histiyositoz(lhh) Castleman Hastalığı (CH) Kimura Hastalığı Kikuchi Fujimoto -Histiyositik nekrotizan lenfadenit Rosai-Dorfman hastalığı Tanım Langerhans
Klasik Hodgkin Lenfoma Vakalarında PD-L1 Ekspresyonunun Sıklığı, EBV ile İlişkisi, Klinik ve Prognostik Önemi
 Klasik Hodgkin Lenfoma Vakalarında PD-L1 Ekspresyonunun Sıklığı, EBV ile İlişkisi, Klinik ve Prognostik Önemi Dr. Süleyman ÖZDEMİR, Uzm. Dr Özlem TON, Prof Dr. Fevziye KABUKÇUOĞLU Sağlık Bilimleri Üniversitesi
Klasik Hodgkin Lenfoma Vakalarında PD-L1 Ekspresyonunun Sıklığı, EBV ile İlişkisi, Klinik ve Prognostik Önemi Dr. Süleyman ÖZDEMİR, Uzm. Dr Özlem TON, Prof Dr. Fevziye KABUKÇUOĞLU Sağlık Bilimleri Üniversitesi
